JP5159788B2 - 1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶形 - Google Patents
1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶形 Download PDFInfo
- Publication number
- JP5159788B2 JP5159788B2 JP2009538905A JP2009538905A JP5159788B2 JP 5159788 B2 JP5159788 B2 JP 5159788B2 JP 2009538905 A JP2009538905 A JP 2009538905A JP 2009538905 A JP2009538905 A JP 2009538905A JP 5159788 B2 JP5159788 B2 JP 5159788B2
- Authority
- JP
- Japan
- Prior art keywords
- methyl
- fluorophenyl
- glucopyranosyl
- thienylmethyl
- hemihydrate
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H7/00—Compounds containing non-saccharide radicals linked to saccharide radicals by a carbon-to-carbon bond
- C07H7/04—Carbocyclic radicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7034—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/12—Drugs for disorders of the metabolism for electrolyte homeostasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/48—Drugs for disorders of the endocrine system of the pancreatic hormones
- A61P5/50—Drugs for disorders of the endocrine system of the pancreatic hormones for increasing or potentiating the activity of insulin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Diabetes (AREA)
- Molecular Biology (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Endocrinology (AREA)
- Epidemiology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Urology & Nephrology (AREA)
- Emergency Medicine (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Dermatology (AREA)
- Child & Adolescent Psychology (AREA)
- Vascular Medicine (AREA)
- Hospice & Palliative Care (AREA)
- Psychiatry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Saccharide Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Plural Heterocyclic Compounds (AREA)
Description
で示される1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼンが記載されている。
1. 1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶;
2. CuKα放射を用いて測定された粉末X線回折パターンが、以下の2θ値を含む、1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶:4.36 ± 0.2, 13.54 ± 0.2, 16.00 ± 0.2, 19.32 ± 0.2, 20.80 ± 0.2;
3. X線粉末回折パターンが図1に示されたものと実質的に同一である、1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶;
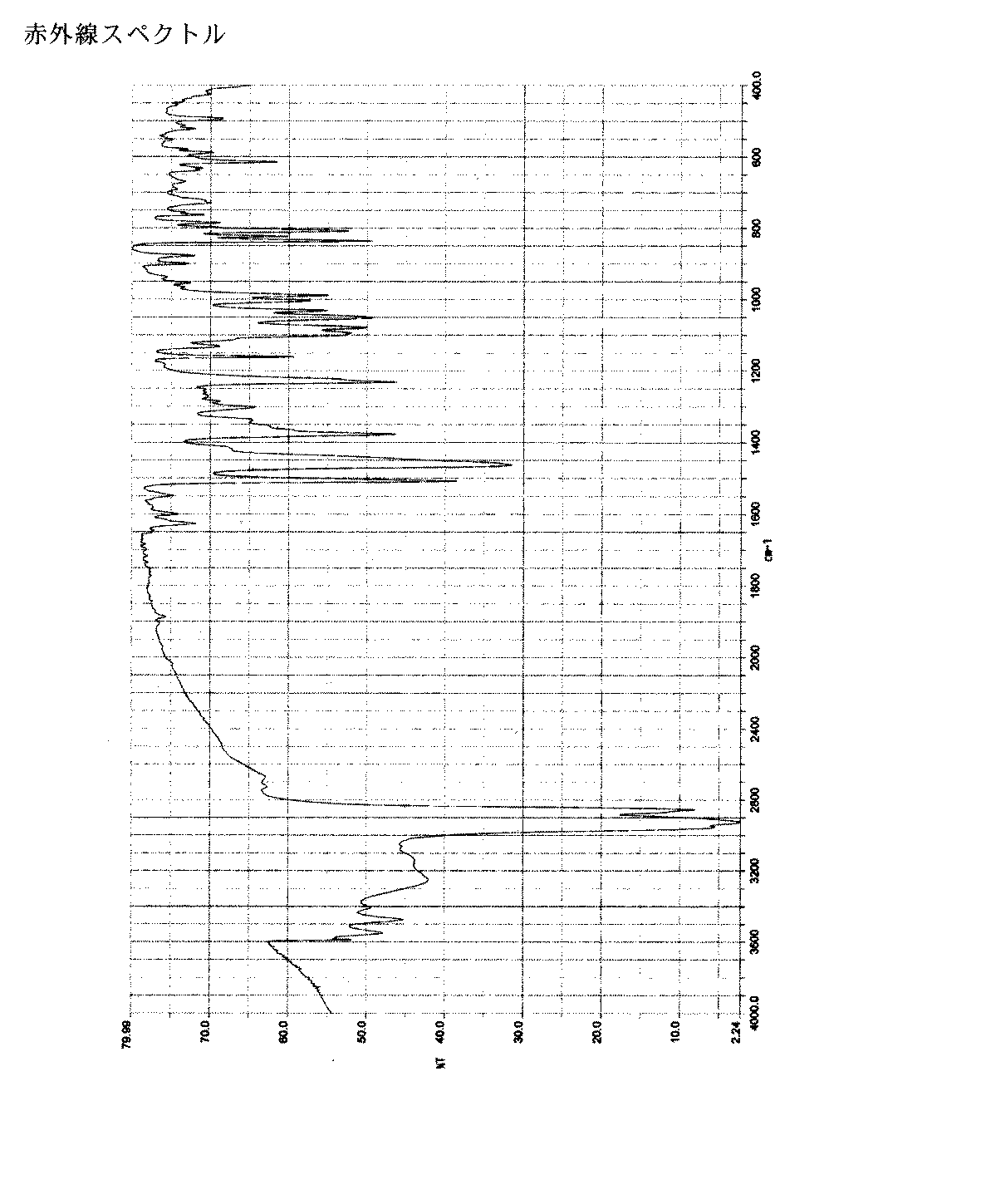
4. IRスペクトルが図2に示されたものと実質的に同一である、1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶;
5. 1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼンの溶液を形成し、そして該溶液から沈殿または再結晶によりその1/2水和物を結晶化することからなる、1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶の製造方法;
6. 有効量の1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶および薬理的に許容しうる担体を含む医薬組成物;
7. 糖尿病、糖尿病性網膜症、糖尿病性神経障害、糖尿病性腎症、遅延創傷治癒、インスリン抵抗性、高血糖症、高インスリン血症、高脂肪酸血症、高グリセロール血症、高脂血症、肥満症、高トリグリセリド血症、X症候群、糖尿病性合併症、アテローム硬化症または高血圧症の処置または進行もしくは発症を遅延させる方法であって、治療有効量の1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶を投与することを含む方法。
本発明の化合物(I)の結晶形は、X線粉末回折パターンにより特徴付けられる。化合物(I)の1/2水和物の結晶のX線回折パターンは、CuKα放射を用いて測定するX線回折計(RINT-TTR III、リガク、東京、日本)で測定した。X線粉末回折の方法は、以下の通りである:
走査速度: 2.00度/分。
ターゲット: CuKα。
電圧: 50kV。
電流: 300mA。
走査範囲: 3〜40.0度
サンプリング幅: 0.0200度。
鉱物油における本発明の結晶形の赤外線スペクトルは、以下の主なピークを含む:1626,1600,1549,および1507cm−1。
本発明の結晶形は、1/2水和物の形態で存在することが観察された。本発明の結晶形の理論的含水量は、1.98%である。本発明の結晶の熱重量分析は、1.705%の質量損失を示す。
WO2005/012326に記載されたのと同様の方法で、1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼンを調製した。
1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン(1.62g)のアモルファス粉末を、アセトン(15ml)に溶解し、そこにH2O(30ml)および種結晶を加えた。混合物を室温で18時間攪拌し、沈殿物を収集し、アセトン−H2O(1:4、30ml)で洗浄し、減圧下、室温で乾燥させ、1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物(1.52g)を無色の結晶として得た。mp 97-100℃.
Claims (4)
- X線粉末回折パターンが図1に示されたものと実質的に同一である、1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶。
- 鉱物油における結晶形の赤外線スペクトルが以下のピークを含む、1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶:1626,1600,1549,および1507cm −1 。
- IRスペクトルが図2に示されたものと実質的に同一である、1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶。
- 含水溶媒を用いて1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼンの溶液を形成し、そしてその溶液から沈殿または再結晶により該化合物の1/2水和物を結晶化することからなる、請求項1、2又は3に記載された1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009538905A JP5159788B2 (ja) | 2006-12-04 | 2007-12-03 | 1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶形 |
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US86842606P | 2006-12-04 | 2006-12-04 | |
| US60/868,426 | 2006-12-04 | ||
| JP2006327019 | 2006-12-04 | ||
| JP2006327019 | 2006-12-04 | ||
| JP2009538905A JP5159788B2 (ja) | 2006-12-04 | 2007-12-03 | 1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶形 |
| PCT/JP2007/073729 WO2008069327A1 (en) | 2006-12-04 | 2007-12-03 | CRYSTALLINE FORM OF 1- (β-D-GLUCOPYRANOSYL) -4 -METHYL- 3- [5- (4 -FLUOROPHENYL) -2-THIENYLMETHYL] BENZENE HEMIHYDRATE |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010511602A JP2010511602A (ja) | 2010-04-15 |
| JP5159788B2 true JP5159788B2 (ja) | 2013-03-13 |
Family
ID=38973167
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009538905A Active JP5159788B2 (ja) | 2006-12-04 | 2007-12-03 | 1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶形 |
Country Status (34)
| Country | Link |
|---|---|
| US (2) | US7943582B2 (ja) |
| EP (1) | EP2102224B2 (ja) |
| JP (1) | JP5159788B2 (ja) |
| KR (1) | KR101146095B1 (ja) |
| CN (3) | CN102675299A (ja) |
| AR (3) | AR064099A1 (ja) |
| AU (1) | AU2007329895C1 (ja) |
| BR (1) | BRPI0718882B8 (ja) |
| CA (1) | CA2671357C (ja) |
| CL (1) | CL2007003487A1 (ja) |
| CO (1) | CO6210719A2 (ja) |
| CR (1) | CR10861A (ja) |
| DK (1) | DK2102224T4 (ja) |
| EA (1) | EA017103B1 (ja) |
| EC (1) | ECSP099489A (ja) |
| ES (1) | ES2456640T5 (ja) |
| GT (1) | GT200900151A (ja) |
| IL (1) | IL199032A (ja) |
| ME (1) | ME01829B (ja) |
| MX (1) | MX2009005857A (ja) |
| MY (1) | MY153702A (ja) |
| NO (1) | NO344354B1 (ja) |
| NZ (1) | NZ577545A (ja) |
| PA (1) | PA8759401A1 (ja) |
| PE (3) | PE20081201A1 (ja) |
| PL (1) | PL2102224T5 (ja) |
| PT (1) | PT2102224E (ja) |
| RS (1) | RS53274B2 (ja) |
| SI (1) | SI2102224T2 (ja) |
| SV (1) | SV2009003285A (ja) |
| TW (1) | TWI403325B (ja) |
| UY (1) | UY30730A1 (ja) |
| WO (1) | WO2008069327A1 (ja) |
| ZA (1) | ZA200903941B (ja) |
Families Citing this family (100)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| UY30730A1 (es) * | 2006-12-04 | 2008-07-03 | Mitsubishi Tanabe Pharma Corp | Forma cristalina del hemihidrato de 1-(b (beta)-d-glucopiranosil) -4-metil-3-[5-(4-fluorofenil) -2-tienilmetil]benceno |
| DK2200606T3 (en) | 2007-09-10 | 2017-12-04 | Janssen Pharmaceutica Nv | PROCEDURE FOR THE PREPARATION OF RELATIONSHIP USED AS INHIBITORS OF SGLT |
| NZ604897A (en) | 2008-08-22 | 2014-03-28 | Theracos Sub Llc | Processes for the preparation of sglt2 inhibitors |
| US9056850B2 (en) * | 2008-10-17 | 2015-06-16 | Janssen Pharmaceutica N.V. | Process for the preparation of compounds useful as inhibitors of SGLT |
| JP5685550B2 (ja) | 2009-02-13 | 2015-03-18 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | Sglt2阻害剤、dpp−iv阻害剤、更に必要により抗糖尿病薬を含む医薬組成物及びその使用 |
| US20110009347A1 (en) * | 2009-07-08 | 2011-01-13 | Yin Liang | Combination therapy for the treatment of diabetes |
| CN102482250B (zh) * | 2009-07-10 | 2014-11-19 | 詹森药业有限公司 | 1-(β-D-吡喃葡糖基)-4-甲基-3-[5-(4-氟苯基)-2-噻吩基甲基]苯的结晶方法 |
| US8869918B2 (en) | 2009-10-07 | 2014-10-28 | Longyear Tm, Inc. | Core drilling tools with external fluid pathways |
| EP2488515B1 (en) * | 2009-10-14 | 2017-01-04 | Janssen Pharmaceutica NV | Process for the preparation of compounds useful as inhibitors of sglt2 |
| WO2011070592A2 (en) | 2009-12-09 | 2011-06-16 | Panacea Biotec Ltd. | Novel sugar derivatives |
| CN102115468B (zh) * | 2009-12-31 | 2014-06-11 | 上海特化医药科技有限公司 | 一种2,5-二取代噻吩化合物的合成方法 |
| WO2011107494A1 (de) | 2010-03-03 | 2011-09-09 | Sanofi | Neue aromatische glykosidderivate, diese verbindungen enthaltende arzneimittel und deren verwendung |
| WO2011120923A1 (en) | 2010-03-30 | 2011-10-06 | Boehringer Ingelheim International Gmbh | Pharmaceutical composition comprising an sglt2 inhibitor and a ppar- gamma agonist and uses thereof |
| US20120115799A1 (en) * | 2010-05-11 | 2012-05-10 | Wenhua Wang | Pharmaceutical formulations |
| WO2011142478A1 (en) | 2010-05-11 | 2011-11-17 | Mitsubishi Tanabe Pharma Corporation | Canagliflozin containing tablets |
| WO2011153712A1 (en) | 2010-06-12 | 2011-12-15 | Theracos, Inc. | Crystalline form of benzylbenzene sglt2 inhibitor |
| EP2582709B1 (de) | 2010-06-18 | 2018-01-24 | Sanofi | Azolopyridin-3-on-derivate als inhibitoren von lipasen und phospholipasen |
| US8530413B2 (en) | 2010-06-21 | 2013-09-10 | Sanofi | Heterocyclically substituted methoxyphenyl derivatives with an oxo group, processes for preparation thereof and use thereof as medicaments |
| TW201221505A (en) | 2010-07-05 | 2012-06-01 | Sanofi Sa | Aryloxyalkylene-substituted hydroxyphenylhexynoic acids, process for preparation thereof and use thereof as a medicament |
| TW201215387A (en) | 2010-07-05 | 2012-04-16 | Sanofi Aventis | Spirocyclically substituted 1,3-propane dioxide derivatives, processes for preparation thereof and use thereof as a medicament |
| TW201215388A (en) | 2010-07-05 | 2012-04-16 | Sanofi Sa | (2-aryloxyacetylamino)phenylpropionic acid derivatives, processes for preparation thereof and use thereof as medicaments |
| ES2609791T3 (es) | 2010-07-06 | 2017-04-24 | Janssen Pharmaceutica, N.V. | Fórmula para tratamientos de co-terapia de diabetes |
| WO2012041898A1 (en) | 2010-09-29 | 2012-04-05 | Celon Pharma Sp. Z O.O. | Combination of sglt2 inhibitor and a sugar compound for the treatment of diabetes |
| US20120283169A1 (en) | 2010-11-08 | 2012-11-08 | Boehringer Ingelheim International Gmbh | Pharmaceutical composition, methods for treating and uses thereof |
| US20130035281A1 (en) | 2011-02-09 | 2013-02-07 | Boehringer Ingelheim International Gmbh | Pharmaceutical composition, methods for treating and uses thereof |
| EA028946B1 (ru) * | 2011-04-13 | 2018-01-31 | Янссен Фармацевтика Нв | Способ получения соединений для применения в качестве ингибиторов sglt2 |
| US9035044B2 (en) * | 2011-05-09 | 2015-05-19 | Janssen Pharmaceutica Nv | L-proline and citric acid co-crystals of (2S, 3R, 4R, 5S,6R)-2-(3-((5-(4-fluorophenyl)thiopen-2-yl)methyl)4-methylphenyl)-6-(hydroxymethyl)tetrahydro-2H-pyran-3,4,5-triol |
| BR112013031032A2 (pt) | 2011-06-03 | 2016-11-29 | Boehringer Ingelheim Int | inibidores de sglt-2 para o tratamento de distúrbios metabólicos em pacientes tratados com agentes neurolépticos |
| WO2013037390A1 (en) | 2011-09-12 | 2013-03-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-styryl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| US9018249B2 (en) | 2011-09-13 | 2015-04-28 | Panacea Biotec Limited | SGLT inhibitors |
| EP2760862B1 (en) | 2011-09-27 | 2015-10-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-alkyl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| CN103889429B (zh) * | 2011-10-31 | 2016-10-19 | 台湾神隆股份有限公司 | Sglt2抑制剂的结晶和非结晶形式 |
| US9193751B2 (en) | 2012-04-10 | 2015-11-24 | Theracos, Inc. | Process for the preparation of benzylbenzene SGLT2 inhibitors |
| CN103965267A (zh) * | 2013-01-24 | 2014-08-06 | 江苏豪森医药集团连云港宏创医药有限公司 | 1-(β-D-吡喃葡糖基)-4-甲基-3-[5-(4-氟苯基)-2-噻吩基甲基]苯与L-苯丙氨酸共晶物及其制备方法 |
| EP2968375B1 (en) | 2013-03-14 | 2019-06-12 | MSD International GmbH | Methods for preparing sglt2 inhibitors |
| ES2647526T3 (es) | 2013-03-15 | 2017-12-22 | Janssen Pharmaceutica Nv | Combinación de canagliflozina y probenecid para el tratamiento de la hiperuricemia |
| EP4245765A3 (en) | 2013-04-04 | 2024-03-20 | Boehringer Ingelheim Vetmedica GmbH | Treatment of metabolic disorders in equine animals |
| CA2911261A1 (en) | 2013-05-08 | 2014-11-13 | Lek Pharmaceuticals D.D. | Novel crystalline hydrates of 1-(.beta.-d-glucopyranosyl)-4-methyl-3-[5-(4-fluorophenyl)-2-thienylmethyl]benzene |
| WO2014195966A2 (en) | 2013-05-30 | 2014-12-11 | Cadila Healthcare Limited | Amorphous form of canagliflozin and process for preparing thereof |
| WO2015051484A1 (en) | 2013-10-12 | 2015-04-16 | Theracos, Inc. | Preparation of hydroxy-benzylbenzene derivatives |
| CN103641822B (zh) * | 2013-10-21 | 2016-06-08 | 江苏奥赛康药业股份有限公司 | 一种卡格列净化合物及其药物组合物 |
| WO2015071761A2 (en) * | 2013-11-11 | 2015-05-21 | Crystal Pharmatech Co., Ltd. | Crystalline forms b, c, and d of canagliflozin |
| CN103588762A (zh) * | 2013-11-27 | 2014-02-19 | 苏州晶云药物科技有限公司 | 坎格列净的新晶型及其制备方法 |
| CN105828815B (zh) | 2013-12-17 | 2020-03-27 | 勃林格殷格翰动物保健有限公司 | 猫科动物中代谢紊乱的治疗 |
| PL3485890T3 (pl) * | 2014-01-23 | 2023-08-28 | Boehringer Ingelheim Vetmedica Gmbh | Inhibitory SGLT2 do leczenia zaburzeń metabolicznych u zwierząt psowatych |
| MX2016010011A (es) * | 2014-01-31 | 2016-10-07 | Janssen Pharmaceutica Nv | Metodos para tratar y prevenir trastornos renales y trastornos del higado graso. |
| US10174010B2 (en) * | 2014-03-19 | 2019-01-08 | Hangzhou Pushai Pharmaceutical Technology Co., Ltd. | Canagliflozin monohydrate and its crystalline forms, preparation methods and uses thereof |
| CN103980261B (zh) * | 2014-04-01 | 2016-06-29 | 天津大学 | 卡格列净的a晶型及其结晶制备方法 |
| CN103980262B (zh) * | 2014-04-01 | 2016-06-22 | 天津大学 | 卡格列净的b晶型及其结晶制备方法 |
| DK3125882T3 (da) | 2014-04-01 | 2020-06-29 | Boehringer Ingelheim Vetmedica Gmbh | Behandling af metabolske lidelser i hestedyr |
| CN103896930B (zh) * | 2014-04-02 | 2016-08-17 | 安徽联创生物医药股份有限公司 | 卡格列净半水合物药用晶型的制备方法 |
| EP2933255A1 (en) | 2014-04-17 | 2015-10-21 | LEK Pharmaceuticals d.d. | Novel crystalline form of 1-(beta-D-glucopyranosyl)-4- methyl-3-[5-(4-fluorophenyl)-2-thienylmethyl]benzene |
| CN103936726B (zh) * | 2014-04-18 | 2016-06-15 | 王军 | 晶体、制备方法及其用途 |
| CN103936800A (zh) * | 2014-05-08 | 2014-07-23 | 安徽联创药物化学有限公司 | 1-(1-甲氧基吡喃葡糖基)-4-甲基-3-[5-(4-氟苯基)-2-噻吩基甲基]苯的制备方法 |
| EP2947077A1 (en) | 2014-05-19 | 2015-11-25 | LEK Pharmaceuticals d.d. | Stereoselective synthesis of intermediates in the preparation of ß-C-arylglucosides |
| CN105330706B (zh) * | 2014-06-05 | 2019-04-16 | 江苏豪森药业集团有限公司 | 卡格列净中间体的制备方法 |
| CN105319294B (zh) * | 2014-06-20 | 2021-03-30 | 重庆医药工业研究院有限责任公司 | 一种分离测定卡格列净及其有关物质的方法 |
| CN104761546A (zh) * | 2014-06-21 | 2015-07-08 | 山东富创医药科技有限公司 | 一种新颖的 (1s)-1,5-脱氢-1-[3-[[5-(4-氟苯基)-2-噻吩基]甲基]-4-甲基苯基]-d-葡萄糖醇晶型及其制备方法 |
| WO2016016774A1 (en) * | 2014-07-31 | 2016-02-04 | Sun Pharmaceutical Industries Limited | Crystalline forms of canagliflozin |
| EP2990029A1 (en) * | 2014-08-29 | 2016-03-02 | Sandoz Ag | Pharmaceutical compositions comprising Canagliflozin |
| US20170247359A1 (en) | 2014-09-05 | 2017-08-31 | Mylan Laboratories Ltd. | Process for the preparation of canagliflozin |
| CZ2014634A3 (cs) | 2014-09-16 | 2016-03-23 | Zentiva, K.S. | Komplexy canagliflozinu a cyklodextrinů |
| CN104402946B (zh) * | 2014-11-17 | 2018-01-02 | 连云港恒运药业有限公司 | 卡格列净中间体及其无定形的制备方法 |
| CN105753910A (zh) * | 2014-12-16 | 2016-07-13 | 康普药业股份有限公司 | 一种卡格列净中间体的制备方法 |
| CN104530023A (zh) * | 2014-12-25 | 2015-04-22 | 重庆医药工业研究院有限责任公司 | 一种卡格列净晶型i及其制备方法 |
| CN104945392A (zh) * | 2015-01-27 | 2015-09-30 | 江苏嘉逸医药有限公司 | 结晶型卡格列净一水合物、制备方法及其应用 |
| CN104530024B (zh) | 2015-02-04 | 2017-08-08 | 上海迪赛诺药业有限公司 | 1‑(β‑D‑吡喃葡糖基)‑4‑甲基‑3‑[5‑(4‑氟苯基)‑2‑噻吩基甲基]苯的晶型及其制备方法 |
| US10633372B2 (en) * | 2015-02-27 | 2020-04-28 | Msn Laboratories Private Limited | Process for the preparation of amorphous (1S)-1,5-anhydro-1-[3-[[5-(4 fluorophenyl)-2-thienyl]-4-methylphenyl]-D-glucitol and its polymorphs thereof |
| JP2018087140A (ja) * | 2015-02-27 | 2018-06-07 | 田辺三菱製薬株式会社 | 1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼンの新規結晶 |
| WO2016142950A1 (en) * | 2015-03-11 | 2016-09-15 | Harman Finochem Limited | A novel process for preparing (2s,3r,4r,5s,6r)-2-{3-[5-[4-fluoro-phenyl)- thiophen-2-ylmethyl]-4-methyl-phenyl}-6-hydroxymethyl-tetrahydro-pyran-3,4,5- triol and its stable amorphous hemihydrate form |
| EP3298007B1 (en) * | 2015-05-22 | 2020-07-22 | Janssen Pharmaceutica NV | Anhydrous crystalline form of (1s)-1,5-anhydro-1-[3-[[5-(4-fluorophenyl)-2-thienyl]methyl]-4-methylphenyl]-d-glucitol |
| CN106279134A (zh) * | 2015-06-23 | 2017-01-04 | 中美华世通生物医药科技(武汉)有限公司 | 卡格列净单晶及其制备方法和用途 |
| CZ2015435A3 (cs) | 2015-06-25 | 2017-01-04 | Zentiva, K.S. | Pevné formy amorfního canagliflozinu |
| US20170071970A1 (en) | 2015-09-15 | 2017-03-16 | Janssen Pharmaceutica Nv | Co-therapy comprising canagliflozin and phentermine for the treatment of obesity and obesity related disorders |
| US10428053B2 (en) | 2015-09-15 | 2019-10-01 | Laurus Labs Limited | Co-crystals of SGLT2 inhibitors, process for their preparation and pharmaceutical compositions thereof |
| WO2017064679A1 (en) * | 2015-10-15 | 2017-04-20 | Lupin Limited | Process for the preparation of amorphous canagliflozin |
| WO2017071813A1 (en) * | 2015-10-30 | 2017-05-04 | Zaklady Farmaceutyczne Polpharma Sa | Process for the preparation of a pharmaceutical agent |
| CZ2015824A3 (cs) * | 2015-11-20 | 2017-05-31 | Zentiva, K.S. | Krystalická forma Canagliflozinu a způsob její přípravy |
| AU2016376653B2 (en) | 2015-12-21 | 2020-07-30 | Janssen Pharmaceutica Nv | Crystallization procedure for obtaining canagliflozin hemihydrate crystals |
| CN105541818A (zh) * | 2016-03-04 | 2016-05-04 | 浙江华海药业股份有限公司 | 一种卡格列净水合物新晶型及其制备方法 |
| CN107540706A (zh) * | 2016-06-28 | 2018-01-05 | 山东诚创医药技术开发有限公司 | 伊格列净中间体的制备方法 |
| WO2018020506A1 (en) | 2016-07-25 | 2018-02-01 | Natco Pharma Ltd | Process for the preparation of amorphous form of canagliflozin |
| EA201990951A1 (ru) | 2016-10-19 | 2019-11-29 | Комбинации, содержащие ssao/vap-1 ингибитор и sglt2-ингибитор, и их применение | |
| CN108017626A (zh) * | 2016-11-04 | 2018-05-11 | 上海奥博生物医药技术有限公司 | 一种坎格列净半水合物新晶型 |
| CN106588898A (zh) | 2017-02-20 | 2017-04-26 | 浙江华海药业股份有限公司 | 一种卡格列净无定型的制备方法 |
| KR20200014406A (ko) | 2017-06-12 | 2020-02-10 | 얀센 파마슈티카 엔.브이. | Ii형 진성 당뇨병을 갖는 환자에서 심혈관 사건을 감소시키거나 예방하는 방법 |
| CN109553649B (zh) * | 2017-09-26 | 2020-12-04 | 北大方正集团有限公司 | 一种卡格列净中间体的制备方法 |
| EP3781166A1 (en) | 2018-04-17 | 2021-02-24 | Boehringer Ingelheim International GmbH | Pharmaceutical composition, methods for treating and uses thereof |
| WO2020039394A1 (en) | 2018-08-24 | 2020-02-27 | Novartis Ag | New drug combinations |
| TW202103709A (zh) | 2019-03-26 | 2021-02-01 | 比利時商健生藥品公司 | 用於治療患有慢性腎臟病之對象的方法 |
| WO2021105152A1 (en) | 2019-11-28 | 2021-06-03 | Boehringer Ingelheim Vetmedica Gmbh | Use of sglt-2 inhibitors in the drying-off of non-human mammals |
| JP7423800B2 (ja) | 2020-02-17 | 2024-01-29 | ベーリンガー インゲルハイム フェトメディカ ゲーエムベーハー | ネコにおける心臓疾患の予防および/または治療のためのsglt-2阻害剤の使用 |
| EP4138826A1 (en) | 2020-04-22 | 2023-03-01 | Bayer Aktiengesellschaft | Combination of finerenone and a sglt2 inhibitor for the treatment and/or prevention of cardiovascular and/or renal diseases |
| CN113943329A (zh) * | 2020-07-16 | 2022-01-18 | 尚科生物医药(上海)有限公司 | 一种坎格列净中间体的非对映异构体的制备方法 |
| WO2022067724A1 (zh) | 2020-09-30 | 2022-04-07 | 北京睿创康泰医药研究院有限公司 | 一种sglt-2抑制剂·肌氨酸共晶体及其制备方法和应用 |
| KR20240041966A (ko) | 2021-07-28 | 2024-04-01 | 베링거잉겔하임베트메디카게엠베하 | 고양이를 제외한 비인간 포유류, 특히 개에서 심장 질환의 예방 및/또는 치료를 위한 sglt-2 억제제의 용도 |
| WO2023006745A1 (en) | 2021-07-28 | 2023-02-02 | Boehringer Ingelheim Vetmedica Gmbh | Use of sglt-2 inhibitors for the prevention and/or treatment of hypertension in non-human mammals |
| AU2022318037A1 (en) | 2021-07-28 | 2024-02-22 | Boehringer Ingelheim Vetmedica Gmbh | Use of sglt-2 inhibitors for the prevention and/or treatment of renal diseases in non-human mammals |
| WO2023129595A1 (en) | 2021-12-30 | 2023-07-06 | Newamsterdam Pharma B.V. | Obicetrapib and sglt2 inhibitor combination |
| US20230381101A1 (en) | 2022-05-25 | 2023-11-30 | Boehringer Ingelheim Vetmedica Gmbh | Aqueous pharmaceutical compositions comprising sglt-2 inhibitors |
Family Cites Families (76)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4160861A (en) * | 1977-10-03 | 1979-07-10 | Merck & Co., Inc. | Method for the separation of antibiotic macrolides |
| US4584369A (en) * | 1981-07-31 | 1986-04-22 | Sloan-Kettering Institute For Cancer Research | Anti-leukemic beta-glycosyl C-nucleosides |
| JP2544609B2 (ja) | 1986-10-07 | 1996-10-16 | 和光純薬工業株式会社 | Tcnq錯体 |
| DE68920798T2 (de) | 1988-08-19 | 1995-05-18 | Warner Lambert Co | Substituierte Dihydroisochinolinone und verwandte Verbindungen als Verstärker der letalen Effekte von Bestrahlung und bestimmten Chemotherapeutika; ausgewählte Verbindungen, Analoga und Verfahren. |
| JPH04253974A (ja) | 1991-02-05 | 1992-09-09 | Ishihara Sangyo Kaisha Ltd | スルホニル尿素系化合物、それらの製造方法及びそれらを含有する除草剤 |
| US5149838A (en) * | 1991-09-20 | 1992-09-22 | Merck & Co., Inc. | Intermediates for substituted azetidinones useful as anti-inflammatory and antidegenerative agents |
| GB9208161D0 (en) | 1992-04-14 | 1992-05-27 | Pfizer Ltd | Indoles |
| US5334225A (en) | 1992-07-15 | 1994-08-02 | Kao Corporation | Keratinous fiber dye composition containing a 2-substituted amino-5-alkylphenol derivative coupler |
| CA2102591C (en) * | 1992-11-12 | 2000-12-26 | Kenji Tsujihara | Hypoglycemic agent |
| US5731292A (en) * | 1992-11-12 | 1998-03-24 | Tanabe Seiyaku Co., Ltd. | Dihydrochalcone derivatives which are hypoglycemic agents |
| US6297363B1 (en) * | 1993-02-12 | 2001-10-02 | Nomura Co., Ltd. | Glycoside indoles |
| US5830873A (en) * | 1994-05-11 | 1998-11-03 | Tanabe Seiyaku Co., Ltd. | Propiophenone derivative and a process for preparing the same |
| US5780483A (en) * | 1995-02-17 | 1998-07-14 | Smithkline Beecham Corporation | IL-8 receptor antagonists |
| JP2002500618A (ja) | 1995-10-31 | 2002-01-08 | イーライ・リリー・アンド・カンパニー | 抗血栓性ジアミン |
| JP3059088B2 (ja) * | 1995-11-07 | 2000-07-04 | 田辺製薬株式会社 | プロピオフェノン誘導体およびその製法 |
| JPH09263549A (ja) | 1996-01-25 | 1997-10-07 | Fujisawa Pharmaceut Co Ltd | ベンゼン誘導体の製造法 |
| PT850948E (pt) * | 1996-12-26 | 2002-08-30 | Tanabe Seiyaku Co | Derivados propiofenona e processo para a preparacao dos mesmos |
| US6153632A (en) * | 1997-02-24 | 2000-11-28 | Rieveley; Robert B. | Method and composition for the treatment of diabetes |
| JPH10324632A (ja) | 1997-03-25 | 1998-12-08 | Takeda Chem Ind Ltd | 医薬組成物 |
| JP2000034239A (ja) | 1998-07-16 | 2000-02-02 | Asahi Glass Co Ltd | トリフルオロメチル化芳香族化合物の製造方法 |
| JP3857429B2 (ja) | 1998-07-17 | 2006-12-13 | ポーラ化成工業株式会社 | 含硫黄抗真菌剤 |
| US20020032164A1 (en) * | 1998-12-30 | 2002-03-14 | Dale Roderic M. K. | Antimicrobial compounds and methods for their use |
| GB9912961D0 (en) | 1999-06-03 | 1999-08-04 | Pfizer Ltd | Metalloprotease inhibitors |
| US6515117B2 (en) | 1999-10-12 | 2003-02-04 | Bristol-Myers Squibb Company | C-aryl glucoside SGLT2 inhibitors and method |
| PH12000002657B1 (en) | 1999-10-12 | 2006-02-21 | Bristol Myers Squibb Co | C-aryl glucoside SGLT2 inhibitors |
| JP4456768B2 (ja) | 2000-02-02 | 2010-04-28 | 壽製薬株式会社 | C−配糖体を含有する薬剤 |
| US6627611B2 (en) | 2000-02-02 | 2003-09-30 | Kotobuki Pharmaceutical Co Ltd | C-glycosides and preparation of thereof as antidiabetic agents |
| AU2001232175B2 (en) | 2000-03-03 | 2005-07-07 | Pfizer Products Inc. | Pyrazole ether derivatives as anti-inflammatory/analgesic agents |
| NZ521369A (en) | 2000-03-17 | 2004-07-30 | Kissei Pharmaceutical | Glucopyranosyloxybenzylbenzene derivatives, medicinal compositions containing the same and intermediates for the preparation of the derivatives |
| US6555519B2 (en) | 2000-03-30 | 2003-04-29 | Bristol-Myers Squibb Company | O-glucosylated benzamide SGLT2 inhibitors and method |
| US6683056B2 (en) | 2000-03-30 | 2004-01-27 | Bristol-Myers Squibb Company | O-aryl glucoside SGLT2 inhibitors and method |
| AU2002210990A1 (en) | 2000-11-02 | 2002-05-15 | Ajinomoto Co. Inc. | Novel pyrazole derivatives and diabetes remedies containing the same |
| US6476352B2 (en) * | 2000-12-18 | 2002-11-05 | General Electric Company | Laser beam stop sensor and method for automatically detecting the presence of laser beam stop material using a laser beam stop sensor |
| PL209375B1 (pl) | 2000-12-28 | 2011-08-31 | Kissei Pharmaceutical | Pochodne glukopiranozyloksypirazolu, kompozycja farmaceutyczna zawierająca takie pochodne i zastosowanie tych pochodnych do wytwarzania kompozycji farmaceutycznej |
| EP1364957B1 (en) | 2001-02-26 | 2008-12-31 | Kissei Pharmaceutical Co., Ltd. | Glycopyranosyloxypyrazole derivatives and medicinal use thereof |
| US7294618B2 (en) * | 2001-02-27 | 2007-11-13 | Kissei Pharmaceutical Co., Ltd. | Glucopyranosyloxypyrazole derivatives and medicinal use thereof |
| JP4190290B2 (ja) | 2001-03-02 | 2008-12-03 | ユニバーシティー オブ ウエスタン オンタリオ | 放射能標識された化合物のポリマー前駆体、ならびにその作製および使用法 |
| US6936590B2 (en) * | 2001-03-13 | 2005-08-30 | Bristol Myers Squibb Company | C-aryl glucoside SGLT2 inhibitors and method |
| ATE318272T1 (de) * | 2001-04-11 | 2006-03-15 | Bristol Myers Squibb Co | Aminosäurekomplexe von c-arylglycosiden zur behandlung von diabetes und verfahren |
| EP1389621A4 (en) | 2001-04-27 | 2005-05-11 | Ajinomoto Kk | N-SUBSTITUTED PYRAZOLYL-O-GLYCOSIDE DERIVATIVES AND DIABETES CONTAINING THEREOF |
| GB0112122D0 (en) | 2001-05-18 | 2001-07-11 | Lilly Co Eli | Heteroaryloxy 3-substituted propanamines |
| EP1405859A4 (en) | 2001-06-20 | 2008-01-23 | Kissei Pharmaceutical | NITROGENIC HETEROCYCLIC DERIVATIVE, MEDICAL COMPOSITION, MEDICAL USE AND INTERMEDIATE PRODUCTS CONTAINING THEREOF |
| JP4115105B2 (ja) | 2001-07-02 | 2008-07-09 | 協和醗酵工業株式会社 | ピラゾール誘導体 |
| WO2003011880A1 (fr) | 2001-07-31 | 2003-02-13 | Kissei Pharmaceutical Co., Ltd. | Derive de glucopyranosyloxybenzylbenzene, composition medicinale contenant ce derive, usage medicinal de cette composition et produit intermediaire pour produire cette composition |
| WO2003020737A1 (en) | 2001-09-05 | 2003-03-13 | Bristol-Myers Squibb Company | O-pyrazole glucoside sglt2 inhibitors and method of use |
| EP1436411B1 (en) * | 2001-10-24 | 2005-12-14 | Michael Burton | Chromogenic enzyme substrates and method for detecting beta-d-ribofuranosidase activity |
| NZ552216A (en) | 2001-11-16 | 2008-07-31 | Bioform Medical Inc | Pharmaceutical and cosmetic compositions containing oxy group-bearing aromatic aldehydes |
| US6617313B1 (en) * | 2002-03-13 | 2003-09-09 | Council Of Scientific And Industrial Research | Glucopyranoside and process of isolation thereof from pterocarpus marsupium pharmaceutical composition containing the same and use thereof |
| US6562791B1 (en) * | 2002-03-29 | 2003-05-13 | Council Of Scientific And Industrial Research | Glucopyranoside, process for isolation thereof, pharmaceutical composition containing same and use thereof |
| DE60328010D1 (de) | 2002-04-18 | 2009-07-30 | Astrazeneca Ab | Heterocyclische verbindungen |
| DE10231370B4 (de) * | 2002-07-11 | 2006-04-06 | Sanofi-Aventis Deutschland Gmbh | Thiophenglycosidderivate, diese Verbindungen enthaltende Arzneimittel und Verfahren zur Herstellung dieser Arzneimittel |
| TWI254635B (en) | 2002-08-05 | 2006-05-11 | Yamanouchi Pharma Co Ltd | Azulene derivative and salt thereof |
| AU2003254904A1 (en) | 2002-08-09 | 2004-02-25 | Taisho Pharmaceutical Co., Ltd. | Aryl 5-thio-beta-d-glucopyranoside derivatives and therapeutic agents for diabetes containing the same |
| AU2003260078A1 (en) | 2002-08-23 | 2004-03-11 | Dr. Reddy's Laboratories Limited | Crystalline and amorphous forms of (s) -repaglinide and the processes for preparation thereof |
| AU2003262262A1 (en) | 2002-08-27 | 2004-03-19 | Kissei Pharmaceutical Co., Ltd. | Pyrazole derivatives, medicinal composition containing the same, and medicinal use thereof |
| DE10258007B4 (de) * | 2002-12-12 | 2006-02-09 | Sanofi-Aventis Deutschland Gmbh | Aromatische Fluorglycosidderivate, diese Verbindungen enthaltende Arzneimittel und Verfahren zur Herstellung dieser Arzneimittel |
| DE10258008B4 (de) | 2002-12-12 | 2006-02-02 | Sanofi-Aventis Deutschland Gmbh | Heterocyclische Fluorglycosidderivate, diese Verbindungen enthaltende Arzneimittel und Verfahren zur Herstellung dieser Arzneimittel |
| CN101260130A (zh) | 2003-01-03 | 2008-09-10 | 布里斯托尔-迈尔斯斯奎布公司 | 制备c-芳基葡糖苷sglt2抑制剂的方法 |
| MXPA05009356A (es) | 2003-03-14 | 2005-12-05 | Astellas Pharma Inc | Derivados de c-glicosido y sales de los mismos. |
| JP2004300102A (ja) | 2003-03-31 | 2004-10-28 | Kissei Pharmaceut Co Ltd | 縮合複素環誘導体、それを含有する医薬組成物およびその医薬用途 |
| AU2003902263A0 (en) | 2003-05-12 | 2003-05-29 | Fujisawa Pharmaceutical Co., Ltd. | Monosaccharide compounds |
| EP1637539B1 (en) | 2003-06-20 | 2012-01-18 | Kissei Pharmaceutical Co., Ltd. | Pyrazole derivative, drug composition containing the same and production intermediate therefor |
| AR048377A1 (es) * | 2003-08-01 | 2006-04-26 | Janssen Pharmaceutica Nv | Benzoimidazol-, benzotriazol- y benzoimidazolona - o- glucosidos sustituidos |
| SG130189A1 (en) * | 2003-08-01 | 2007-03-20 | Janssen Pharmaceutica Nv | Substituted indole-o-glucosides |
| RS20060320A (en) * | 2003-08-01 | 2008-08-07 | Janssen Pharmaceutica N.V., | Substituted indazole-o-glucosides |
| EA009768B1 (ru) * | 2003-08-01 | 2008-04-28 | Янссен Фармацевтика Нв | Замещенные конденсированные гетероциклические с-гликозиды |
| UA86042C2 (en) * | 2003-08-01 | 2009-03-25 | Янссен Фармацевтика Н.В. | Substituted indazole-o-glucosides |
| EA015104B1 (ru) | 2003-08-01 | 2011-06-30 | Мицубиси Танабе Фарма Корпорейшн | Новые соединения, обладающие ингибирующей активностью в отношении натрийзависимого транспортера |
| WO2005030127A2 (en) | 2003-09-23 | 2005-04-07 | Merck & Co., Inc. | Novel crystalline form of a phosphoric acid salt of a dipeptidyl peptidase-iv inhibitor |
| WO2006108842A1 (en) | 2005-04-15 | 2006-10-19 | Boehringer Ingelheim International Gmbh | Glucopyranosyl-substituted (heteroaryloxy-benzyl)-benzene derivatives as sglt inhibitors |
| US7772191B2 (en) | 2005-05-10 | 2010-08-10 | Boehringer Ingelheim International Gmbh | Processes for preparing of glucopyranosyl-substituted benzyl-benzene derivatives and intermediates therein |
| US20090221592A1 (en) | 2005-07-25 | 2009-09-03 | Ellison Martha E | Dodecylsulfate Salt Of A Dipeptidyl Peptidase-Iv Inhibitor |
| WO2007054978A2 (en) | 2005-11-10 | 2007-05-18 | Jubilant Organosys Limited | Process for preparing paroxetine hydrochloride hemihydrate |
| EP1842850A1 (en) | 2006-03-23 | 2007-10-10 | Sandoz AG | Rosiglitazone hydrochloride hemihydrate |
| UY30730A1 (es) * | 2006-12-04 | 2008-07-03 | Mitsubishi Tanabe Pharma Corp | Forma cristalina del hemihidrato de 1-(b (beta)-d-glucopiranosil) -4-metil-3-[5-(4-fluorofenil) -2-tienilmetil]benceno |
| DK2200606T3 (en) † | 2007-09-10 | 2017-12-04 | Janssen Pharmaceutica Nv | PROCEDURE FOR THE PREPARATION OF RELATIONSHIP USED AS INHIBITORS OF SGLT |
-
2007
- 2007-11-20 UY UY30730A patent/UY30730A1/es not_active Application Discontinuation
- 2007-12-03 MY MYPI20092200A patent/MY153702A/en unknown
- 2007-12-03 CN CN2012100910385A patent/CN102675299A/zh active Pending
- 2007-12-03 EP EP07850306.7A patent/EP2102224B2/en active Active
- 2007-12-03 ZA ZA200903941A patent/ZA200903941B/xx unknown
- 2007-12-03 JP JP2009538905A patent/JP5159788B2/ja active Active
- 2007-12-03 SI SI200731417T patent/SI2102224T2/sl unknown
- 2007-12-03 KR KR1020097013946A patent/KR101146095B1/ko active IP Right Review Request
- 2007-12-03 CN CN2007800431547A patent/CN101573368B/zh active Active
- 2007-12-03 BR BRPI0718882A patent/BRPI0718882B8/pt active IP Right Grant
- 2007-12-03 ES ES07850306T patent/ES2456640T5/es active Active
- 2007-12-03 AU AU2007329895A patent/AU2007329895C1/en active Active
- 2007-12-03 DK DK07850306.7T patent/DK2102224T4/da active
- 2007-12-03 PA PA20078759401A patent/PA8759401A1/es unknown
- 2007-12-03 PT PT78503067T patent/PT2102224E/pt unknown
- 2007-12-03 CA CA2671357A patent/CA2671357C/en active Active
- 2007-12-03 CN CN2012101116538A patent/CN102675380A/zh active Pending
- 2007-12-03 NZ NZ577545A patent/NZ577545A/en unknown
- 2007-12-03 PL PL07850306T patent/PL2102224T5/pl unknown
- 2007-12-03 RS RS20140194A patent/RS53274B2/sr unknown
- 2007-12-03 MX MX2009005857A patent/MX2009005857A/es active IP Right Grant
- 2007-12-03 AR ARP070105383A patent/AR064099A1/es not_active Application Discontinuation
- 2007-12-03 EA EA200970540A patent/EA017103B1/ru active Protection Beyond IP Right Term
- 2007-12-03 ME MEP-2014-45A patent/ME01829B/me unknown
- 2007-12-03 US US11/987,670 patent/US7943582B2/en active Active
- 2007-12-03 WO PCT/JP2007/073729 patent/WO2008069327A1/en active Application Filing
- 2007-12-04 PE PE2007001714A patent/PE20081201A1/es not_active Application Discontinuation
- 2007-12-04 TW TW096146015A patent/TWI403325B/zh active
- 2007-12-04 PE PE2011001164A patent/PE20110841A1/es not_active Application Discontinuation
- 2007-12-04 CL CL200703487A patent/CL2007003487A1/es unknown
- 2007-12-04 PE PE2013000220A patent/PE20130591A1/es active IP Right Grant
-
2009
- 2009-05-06 NO NO20091778A patent/NO344354B1/no unknown
- 2009-05-31 IL IL199032A patent/IL199032A/en active IP Right Grant
- 2009-06-04 SV SV2009003285A patent/SV2009003285A/es unknown
- 2009-06-04 GT GT200900151A patent/GT200900151A/es unknown
- 2009-06-11 CR CR10861A patent/CR10861A/es unknown
- 2009-07-02 CO CO09068422A patent/CO6210719A2/es not_active Application Discontinuation
- 2009-07-03 EC EC2009009489A patent/ECSP099489A/es unknown
-
2011
- 2011-05-09 US US13/103,557 patent/US8513202B2/en active Active
-
2017
- 2017-02-01 AR ARP170100253A patent/AR107510A2/es unknown
-
2020
- 2020-03-19 AR ARP200100781A patent/AR118450A2/es unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5159788B2 (ja) | 1−(β−D−グルコピラノシル)−4−メチル−3−[5−(4−フルオロフェニル)−2−チエニルメチル]ベンゼン1/2水和物の結晶形 | |
| JP6538556B2 (ja) | 1−シアノ−2−(4−シクロプロピル−ベンジル)−4−(β−D−グルコピラノース−1−イル)−ベンゼンの結晶性錯体、その調製方法及び薬物を調製するためのその使用 | |
| KR20160003899A (ko) | 마크롤리드 고체상 형태 | |
| WO2003037881A1 (fr) | Cristal a forme $g(a) ou $g(b) d'un derive acetanilinide | |
| US20090298947A1 (en) | Polymorphic and amorphous forms of lacosamide and amorphous compositions | |
| KR20070007196A (ko) | 펙소페나딘 히드로클로라이드의 결정형 및 이의 제조 방법 | |
| TW201837033A (zh) | 一種阿片樣物質受體(mor)激動劑的鹽、其富馬酸鹽i晶型及製備方法 | |
| KR20040012747A (ko) | 펙소페나딘 염산염의 다형체 | |
| WO2008090565A1 (en) | Novel thermodynamically stable polymorphic form-l of letrozole | |
| JP6294665B2 (ja) | スピロケタール誘導体の結晶 | |
| WO2017206827A1 (zh) | 钠-葡萄糖协同转运蛋白2抑制剂的晶型 | |
| WO2019200502A1 (zh) | 玻玛西尼甲磺酸盐晶型及其制备方法和药物组合物 | |
| TW202014188A (zh) | 一種鴉片類物質受體激動劑的結晶形式及製備方法 | |
| WO2016136830A1 (ja) | 1-(β-D-グルコピラノシル)-4-メチル-3-[5-(4-フルオロフェニル)-2-チエニルメチル]ベンゼンの新規結晶 | |
| KR102659846B1 (ko) | 치환된-퀴녹살린-유형 브리지된-피페리딘 화합물의 다형체 형태 | |
| WO2006054456A1 (ja) | 二環式へテロ環含有スルホンアミド化合物の結晶 | |
| WO2021121270A1 (zh) | 一种SGLTs抑制剂的纯化方法及其应用 | |
| WO2020225783A1 (ko) | Pi3k 저해제의 결정다형 및 이의 제조방법 | |
| KR20140045550A (ko) | 6-(피페리딘-4-일옥시)-2h-이소퀴놀린-1-온 하이드로클로라이드의 결정성 용매화물 | |
| KR20200003645A (ko) | 신규한 결정형 및 그의 제조방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120605 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120615 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120717 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20121120 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20121211 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5159788 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20151221 Year of fee payment: 3 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |