【발명의 명칭】 [Name of invention]
리간드 화합물, 유기 크름 화합물, 을레핀 올리고머화용 촉매 시스템, 및 이를 이용한 을레핀의 올리고머화 방법 Ligand compound, organic crum compound, catalyst system for ollepin oligomerization, and oligomerization method of ollepin using the same
【관련 출원 (들)과의 상호 인용】 [Cross Citation with Related Application (s)]
본 출원은 2015년 6월 12일자 한국 특허 출원 제 10-2015-0083650호 및 2015년 12월 18일자 한국 특허 출원 제 10-2015-0182257호에 기초한 우선권의 이익을 주장하며, 해당 한국 특허 출원들의 문헌에 개시된 모든 내용은 본 명세서의 일부로서 포함된다. This application claims the benefit of priority based on Korean Patent Application No. 10-2015-0083650 dated June 12, 2015 and Korean Patent Application No. 10-2015-0182257 dated December 18, 2015. All content disclosed in the literature is included as part of this specification.
【기술분야】 Technical Field
본 발명은 리간드 화합물, 유기 크롬 화합물, 상기 리간드 화합물 또는 유기 크롬 화합물을 포함하는 을레핀 올리고머화용 촉매 시스템, 및 이를 이용한 을레핀의 을리고머화 방법에 관한 것이다. The present invention relates to a ligand compound, an organic chromium compound, a catalyst system for urepin oligomerization comprising the ligand compound or an organic chromium compound, and a method for oligomerization of urepin using the same.
【배경기술】 Background Art
1-핵센, 1-옥텐 등과 같은 선형 알파-을레핀 (Linear alpha-olefin)은 세정제, 윤활제, 가소제 둥으로 사용되며, 히 선형 저밀도 폴리에틸렌 (LLDPE)의 제조시 폴리머의 밀도 조절을 위한 공단량체로 많이 사용된다. Linear alpha-olefins, such as 1-nuxene and 1-octene, are used as detergents, lubricants, and plasticizers, and as comonomers for controlling the density of polymers in the production of high linear density polyethylene (LLDPE). It is used a lot.
이러한 선형 알파-올레핀은 Shell Higher Olefin Process 를 통해 주로 생산되었다. 그러나, 상기 방법은 Schultz-Flory 분포에 따라 다양한 길이의 알파-을레핀이 동시에 합성되기 때문에, 특정 알파-을레핀을 얻기 위해서는 별도의 분리 공정을 거쳐야 하는 번거로움이 있었다. These linear alpha-olefins were produced primarily through the Shell Higher Olefin Process. However, since the method synthesizes alpha-le-lephins of various lengths according to the Schultz-Flory distribution at the same time, it is cumbersome to undergo a separate separation process to obtain a specific alpha-le-lepine.
' 이러한 문제점을 해결하기 위해, 에틸렌의 삼량화 반웅을 통해 1-핵센을 선택적으로 합성하거나, 에틸렌의 사량화 반웅을 통해 1-옥텐을 선택적으로 합성하는 방법이 제안되었다. 그리고, 이러한 선택적인 에틸렌의 을리고머화를 가능케 하는 촉매 시스템에 대한 많은 연구가 이루어지고 있다. In order to solve this problem, a method of selectively synthesizing 1-nuxene through trimerization reaction of ethylene or selectively synthesizing 1-octene through tetramerization reaction of ethylene has been proposed. And, much research has been made on catalyst systems that enable the selective limerization of such selective ethylene.
【발명의 내용】 [Content of invention]
【해결하려는 과제】
본 발명은 올레핀의 을리고머화 반웅에 있어서 높은 촉매 활성과 선택도의 발현을 가능케 하는 신규한 리간드 화합물을 제공하기 위한 것이다. 또한, 본 발명은 올레핀의 을리고머화 반웅에 있어서 높은 촉매 활성과 선택도의 발현을 가능케 하는 신규한 유기 크롬 화합물을 제공하기 위한 것이다. [Problem to solve] The present invention is to provide a novel ligand compound that enables the expression of high catalytic activity and selectivity in the reaction of oligomerization of olefins. The present invention also provides a novel organic chromium compound which enables the expression of high catalytic activity and selectivity in the oligomerization reaction of olefins.
또한, 본 발명은 상기 리간드 화합물 또는 유기 크롬 화합물을 포함하는 올레핀 을리고머화용 촉매 시스템을 제공하기 위한 것이다. In addition, the present invention is to provide a catalyst system for olefin oligomerization comprising the ligand compound or an organic chromium compound.
또한, 본 발명은 상기 촉매 시스템을 이용한 을레핀의 을리고머화 방법을 제공하기 위한 것이다. In addition, the present invention is to provide a method for the oligomerization of urepin using the catalyst system.
【과제의 해결 수단】 [Measures of problem]
본 발명은 분자 내에 하기 화학식 1로 표시되는 그룹을 하나 이상 포함하는 리간드 화합물을 제공한다. The present invention provides a ligand compound comprising at least one group represented by the following formula (1) in the molecule.
[화학식 1] [Formula 1]
상기 화학식 1에서, In Chemical Formula 1,
*은 상기 화학식 1로 표시되는 그룹이 라디칼임을 의미하고, * Means that the group represented by the formula (1) is a radical,
A는 붕소 (B), 질소 (N), 인 (P) 또는 안티몬 (Sb)이고 A is boron (B), nitrogen (N), phosphorus (P) or antimony (Sb)
X는 각각 독립적으로 인 (P), 비소 (As), 또는 안티몬 (Sb)이고, Each X is independently phosphorus (P), arsenic (As), or antimony (Sb),
R1 내지 R4는, 각각 독립적으로; R1 to R4 are each independently;
메타 또는 파라 위치에 선택적으로, 알킬기, 알콕시, 알킬설파닐기, 및 알킬실릴기로 이루어진 군에서 선택된 1종 이상의 치환기가 치환되거나 결합된, 탄소수 6 내지 20의 아릴기이다. Optionally in the meta or para position, an aryl group having 6 to 20 carbon atoms, wherein one or more substituents selected from the group consisting of an alkyl group, an alkoxy, an alkylsulfanyl group, and an alkylsilyl group are substituted or bonded.
또한, 본 발명은 상기 리간드 화합물 및 크롬 (Cr)을 포함하는, 유기 크름 화합물을 제공한다. The present invention also provides an organic crumb compound comprising the ligand compound and chromium (Cr).
또한, 본 발명은 상기 리간드 화합물, 크롬 소스, 및 조촉매를 포함하는 올레핀 을리고머화용 촉매 시스템을 제공한다.
또한, 본 발명은 상술한 촉매 시스템의 존재 하에 , 을레핀의 을리고머화 반웅을 진행하여, 알파-을레핀을 형성하는 단계를 포함하는, 을레핀의 을리고머화 방법을 제공한다. The present invention also provides a catalyst system for olefin oligomerization comprising the ligand compound, chromium source, and cocatalyst. The present invention also provides a method for the oligomerization of olephine, which comprises the step of undergoing the oligomerization reaction of olephine in the presence of the above-described catalyst system to form alpha- olephine.
【발명의 효과】 【Effects of the Invention】
본 발명에 따른 올레핀 올리고머화 촉매 시스템은 우수한 촉매 활성을 가지면서도 1-핵센 또는 1-옥텐에 대한 높은 선택도를 나타내어, 보다 효율적인 알파-올레핀의 제조를 가능케 한다. 【발명을 실시하기 위한 구체적인 내용】 The olefin oligomerization catalyst system according to the invention exhibits high selectivity for 1-nuxene or 1-octene while having good catalytic activity, allowing the production of more efficient alpha-olefins. [Specific contents to carry out invention]
이하, 본 발명의 구현 예들에 따른 리간드 화합물, 유기 크름 화합물, 올레핀 을리고머화 용 촉매 시스템, 및 이를 이용한 을레핀의 을리고머화 방법에 대하여, 보다 상세하게 설명한다. Hereinafter, a ligand compound, an organic cream compound, an olefin oligomerization catalyst system, and a oligomerization method of urepin using the same according to embodiments of the present invention will be described in more detail.
그에 앞서, 본 명세서에서 사용되는 용어는 단지 예시적인 실시예들을 설명하기 위해 사용된 것으로, 본 발명을 한정하려는 의도는 아니다. 단수의 표현은 문맥상 명백하게 다르게 뜻하지 않는 한, 복수의 표현을 포함한다. 본 명세서에서, "포함하다" "구비하다" 또는 "가지다" 등의 용어는 실시된 특징, 숫자, 단계, 구성 요소 또는 이들을 조합한 것이 존재함을 지정하려는 것이지, 하나 또는 그 이상의 다른 특징들이나 숫자, 단계, 구성 요소, 또는 이들을 조합한 것들의 존재 또는 부가 가능성을 미리 배제하지 않는 것으로 이해되어야 한다. Prior to this, the terminology used herein is for the purpose of describing exemplary embodiments only and is not intended to be limiting of the invention. Singular expressions include plural expressions unless the context clearly indicates otherwise. As used herein, the terms "comprise", "comprise" or "have" are intended to indicate that there is a feature, number, step, component, or combination thereof, that is, one or more other features or numbers. It is to be understood that the present invention does not exclude the possibility of the presence or the addition of steps, components, or combinations thereof.
본 발명은 다양한 변경을 가할 수 있고 여러 가지 형태를 가질 수 있는 바, 특정 실시예들을 예시하고 하기에서 상세하게 설명하고자 한다. 그러 이는 본 발명을 특정한 개시 형태에 대해 한정하려는 것이 아니며 본 발명의 사상 및 기술 범위에 포함되는 모든 변경 균등물 내지 대체물을 포함하는 것으로 이해되어야 한다. As the invention allows for various changes and numerous modifications, particular embodiments will be illustrated and described in detail below. As such, it is to be understood that the present invention is not intended to be limited to the particular disclosed forms and includes all modification equivalents and substitutes included in the spirit and scope of the present invention.
또한, 본 명세서 전체에서 '촉매 시스템 '이라 함은 크롬 소스, 리간드 화합물 및 조촉매를 포함하는 3 성분, 또는 대안적으로, 유기 크롬 화합물 및 조촉매의 2 성분이 동시에 또는 임의의 순서로 첨가되어 활성이 있는 촉매 조성물로 수득될 수 있는 상태의 것을 의미한다. 상기 촉매 시스템의 3 성분
또는 2 성분은 용매 및 단량체의 존재 또는 부존재 하에 첨가될 수 있으며, 담지 또는 비담지 상태로 사용될 수 있다. In addition, throughout this specification, the term "catalyst system" means a three component comprising a chromium source, a ligand compound and a promoter, or alternatively, two components of an organic chromium compound and a promoter are added simultaneously or in any order. It means the state which can be obtained with an active catalyst composition. Three components of the catalyst system Or the two components may be added in the presence or absence of a solvent and a monomer, and may be used in a supported or unsupported state.
본 발명의 일 측면에 따르면, 분자 내에 하기 화학식 1로 표시되는 그룹을 하나 이상 포함하는 리간드 화합물이 제공된다. According to one aspect of the invention, there is provided a ligand compound comprising at least one group represented by the formula (1) in the molecule.
[화학식 1] [Formula 1]
X X X X
R2 R3 R2 R3
상기 화학식 1에서, In Chemical Formula 1,
*은 상기 화학식 1로 표시되는 그룹이 라디칼임을 의미하고, * Means that the group represented by the formula (1) is a radical,
A는 붕소 (B), 질소 (N), 인 (P) 또는 안티몬 (Sb)이고, A is boron (B), nitrogen (N), phosphorus (P) or antimony (Sb),
X는 각각 독립적으로 인 (P), 비소 (As), 또는 안티몬 (Sb)이고, Each X is independently phosphorus (P), arsenic (As), or antimony (Sb),
R1 내지 R4는, 각각 독립적으로; R1 to R4 are each independently;
메타 또는 파라 위치에 선택적으로, 알킬기, 알콕시, 알킬설파닐기, 및 알킬실릴기로 이루어진 군에서 선택된 1종 이상의 치환기가 치환되거나 결합된, 탄소수 6 내지 20의 아릴기이다. Or an aryl group having 6 to 20 carbon atoms, optionally substituted at the meta or para position, with one or more substituents selected from the group consisting of alkyl groups, alkoxy, alkylsulfanyl groups, and alkylsilyl groups.
본 발명자들의 계속적인 실험 결과, 상기 리간드 화합물을 을레핀의 올리고머화용 촉매 시스템에 적용할 경우, 우수한 촉매 활성을 나타내면서도 As a result of continuous experiments of the present inventors, when the ligand compound is applied to the catalyst system for oligomerization of olepin, it shows excellent catalytic activity.
1-핵센 또는 1-옥텐에 대한 높은 선택도를 나타내어 보다 효율적인 알파- 을레핀의 제조를 가능케 함이 확인되었다. It has been shown that high selectivity for 1-nuxene or 1-octene allows for the preparation of more efficient alpha-urepin.
발명의 일 구현 예에 따르면, 상기 리간드 화합물은 분자 내에 상기 화학식 1로 표시되는 그룹 (특히, 디포스피노 아미닐 잔기 (diphosphino aminyl moiety))을 포함하고, 디포스피노 아미닐 잔기의 말단에, 특정 치환기를 가지는 아릴 그룹과 연결되에 그 자체로 강한 전자 공여 그룹의 역할을 할 수 있는 형태를 가질 수 있다. According to one embodiment of the invention, the ligand compound comprises a group represented by the formula (1) in the molecule (particularly, diphosphino aminyl moiety), at the end of the diphosphino aminyl moiety, a specific substituent It may have a form that can be connected to an aryl group having and serve as a strong electron donating group by itself.
이러한 구조적 특징에 기인하여, 상기 리간드 화합물은 을레핀의 을리고머화 촉매 시스템에 적용되어 높은 을리고머화 반웅 활성을 나타낼 수
있고, 특히 1-헥센, 1-옥텐 등에 대한 높은 선택도를 나타낼 수 있다. 이는 각각의 인접한 크름 활성점 사이의 상호 작용에 의한 것으로 볼 수 있으며, 특히, 디포스피노 아미닐 기의 인 (P) 원자에 특정 치환기가 치환 또는 연결된 아릴이 연결되는 경우, 디포스피노 아미닐 기에 포함된 인 (P) 원자 및 질소 (N) 원자에서 전자 밀도가 증가하게 되며, 전체 리간드 화합물의 전기적, 입체적 성질이 변화할 수 있다. Due to this structural feature, the ligand compound can be applied to the lyremerization catalyst system of leupin to exhibit high lygomerization reaction activity. In particular, it can exhibit high selectivity for 1-hexene, 1-octene and the like. This can be considered to be due to the interaction between adjacent adjacent active points of activity, in particular in the diphosphino aminyl group, when an aryl is substituted or substituted by a specific substituent to the phosphorus (P) atom of the diphosphino aminyl group. The electron density increases at the phosphorus (P) atom and the nitrogen (N) atom, and the electrical and steric properties of the entire ligand compound may change.
이에 따라, 리간드와 크롬 원자 사이의 결합에 변화가 생기게 되어, 촉매의 구조가 더 안정해질 수 있으며, 기존의 metallacycloheptane, 또는 metallacyclononane 형태에 비해 전이상태의 에너지, 즉 반웅의 활성화 에너지를 변화시켜, 보다 높은 활성과 선택도로 알파-을레핀을 형성할 수 있게 되고, PE Wax와 같은 분자량이 큰 고형 알파-을레핀 등의 부산물의 양을 더욱 감소시킬 수 있게 된다. As a result, the bond between the ligand and the chromium atom may be changed, the structure of the catalyst may be more stable, and the energy of the transition state, that is, the activation energy of reaction reaction, may be changed, compared to the conventional metallacycloheptane or metallacyclononane form. It is possible to form alpha-olepin with high activity and selectivity, and to further reduce the amount of by-products such as high molecular weight solid alpha-olepin such as PE Wax.
나아가, 올리고머화 반웅에서 적은 양으로도 생성물에 큰 영향을 끼치는 1-핵센 이성질체의 양을 크게 줄일 수 있으며, 부수적으로는 1-핵센의 증가 및 1-핵센 이성질체의 감소에 따라 분리가 불필요할 수 있음에 따른 에너지 절감의 효과도 가져올 수 있다. Furthermore, a small amount in the oligomerization reaction can significantly reduce the amount of 1-nucleene isomers that have a great effect on the product, and concomitantly, separation may not be necessary due to an increase in 1-nucleene and a decrease in 1-nucenne isomers. It can also bring about energy savings.
한편, 발명의 일 구현 예에 따르면, 상기 화학식 1에서 X는 각각 독립적으로 인 (P), 비소 (As) 또는 안티몬 (Sb)일 수 있다. 바람직하게는, 상기 화학식 1로 표시되는 그룹은 각각의 X가 인 (P)인 디포스피노 아미닐 잔기 (diphosphino aminyl moiety)일 수 있다. Meanwhile, according to one embodiment of the present invention, X in Chemical Formula 1 may be each independently phosphorus (P), arsenic (As), or antimony (Sb). Preferably, the group represented by Formula 1 may be a diphosphino aminyl moiety in which each X is phosphorus (P).
그리고, 상기 화학식 1에서 R1 내지 R4는, R1 내지 R4는, 각각 독립적으로; And, in Formula 1, R1 to R4, R1 to R4, each independently;
알킬기, 알콕시, 알킬설파닐기, 및 알킬실릴기로 이루어진 군에서 선택된 1종 이상의 치환기가 치환되거나 결합된, 탄소수 6 내지 20의 아릴기이다. 상기 화학식 1의 R1 내지 R4를 더 구체적으로 설명하면, R1 내지 R4 각각 독립적으로; 탄소수 1 내지 10의 알킬기, 탄소수 1 내지 10의 알콕시기, 탄소수 1 내지 10의 알킬설파닐기, 및 탄소수 1 내지 10의 알킬실릴기로 이루어진 군에서 선택된 1종 이상의 치환기가 치환되거나 결합된, 탄소수 6
내지 20의 아릴기일 수 있다. An aryl group having 6 to 20 carbon atoms, in which one or more substituents selected from the group consisting of an alkyl group, an alkoxy, an alkylsulfanyl group, and an alkylsilyl group is substituted or bonded. When explaining R1 to R4 of the formula (1) in more detail, each of R1 to R4 independently; 6 or more carbon atoms, in which one or more substituents selected from the group consisting of an alkyl group having 1 to 10 carbon atoms, an alkoxy group having 1 to 10 carbon atoms, an alkylsulfanyl group having 1 to 10 carbon atoms, and an alkylsilyl group having 1 to 10 carbon atoms are substituted or bonded. It may be an aryl group of 20 to.
R1 내지 R4의 치환 형태는, 구체적으로 예를 들어, R1 내지 R4는 각각 독립적으로, 총 탄소수 6 내지 20의 페닐기의 형태로; X 연결 부위에 대해 메타 (meta) 위치 중 어느 하나만이, 탄소수 1 내지 10의 알킬기, 탄소수 1 내지 10의 알콕시기, 탄소수 1 내지 10의 알킬설파닐기, 및 탄소수 1 내지 10의 알킬실릴기로 이루어진 군에서 선택된 1종의 치환기로 치환되거나 결합된 것일 수 있다. Substituted forms of R1 to R4, specifically, for example, R1 to R4 are each independently in the form of a phenyl group having 6 to 20 carbon atoms in total; Only one of the meta positions relative to the X linking site is a group consisting of an alkyl group having 1 to 10 carbon atoms, an alkoxy group having 1 to 10 carbon atoms, an alkylsulfanyl group having 1 to 10 carbon atoms, and an alkylsilyl group having 1 to 10 carbon atoms It may be substituted or combined with one substituent selected from.
아니면, R1 내지 R4는, 각각 독립적으로, 총 탄소수 6 내지 20의 페닐기이며; X 연결 부위에 대해 메타 (meta) 및 파라 (para) 위치 중 둘 이상이, 탄소수 1 내지 10의 알킬기, 탄소수 1 내지 10의 알콕시기, 탄소수 1 내지 10의 알킬설파닐기, 및 탄소수 1 내지 10의 알킬실릴기로 이루어진 군에서 선택된 1종 이상의 치환기로 치환되거나 결합된 것일 수도 있다. 발명의 일 실시예에 따르면, 상기 화학식 1의 X는 인 (P)이고, 상기 화학식 1의 (R1)(R2)X- 및 (R3)(R4)X-로 표시되는 잔기 (Moiety)는 각각 하기 구조식들로 표시될 수 있으나, 반드시 이에 한정되는 것은 아니다. Or R1 to R4 are each independently a phenyl group having 6 to 20 carbon atoms in total; At least two of the meta and para positions with respect to the X linking site may be an alkyl group having 1 to 10 carbon atoms, an alkoxy group having 1 to 10 carbon atoms, an alkylsulfanyl group having 1 to 10 carbon atoms, and a carbon group having 1 to 10 carbon atoms. It may be substituted or bonded with one or more substituents selected from the group consisting of alkylsilyl groups. According to an embodiment of the present invention, X in formula 1 is phosphorus (P), and the residues represented by (R 1 ) (R 2 ) X- and (R 3 ) (R 4 ) X- of formula 1 ( Moiety) may be represented by the following structural formula, respectively, but is not necessarily limited thereto.
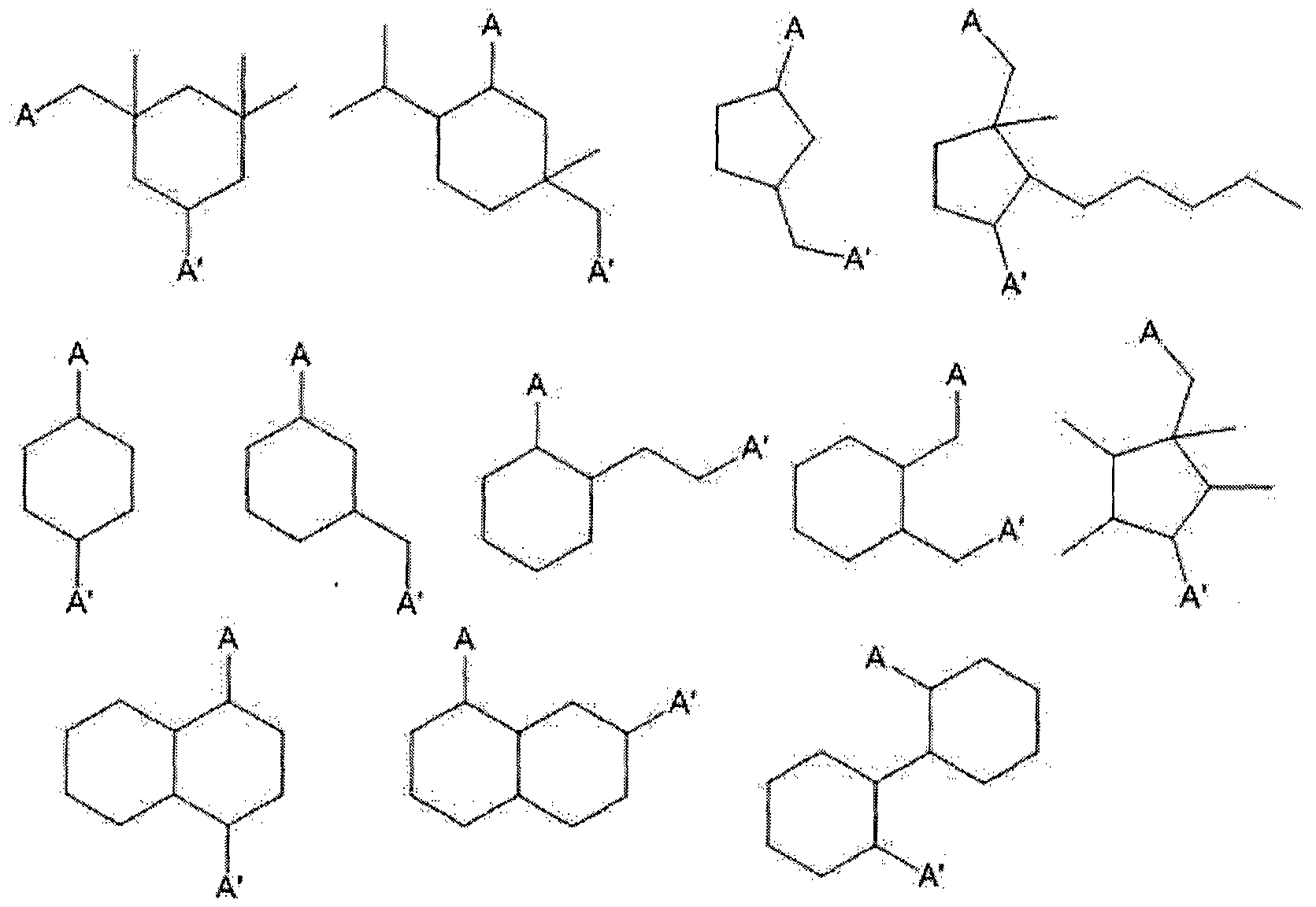
또한, 상기 화학식 1로 표시되는 그룹은 한 화합물 내에 2 이상 포함될 수도 있으며, 이 경우, 두 그룹을 연결하는 링커는 탄소수 2 내지 20의 지방족 그룹, 탄소수 2 내지 20의 헤테로 지방족 그룹, 탄소수 2 내지 20의 지환족 그룹, 탄소수 2 내지 20의 헤테로 지환족 그룹, 또는 상기 지방족 그룹, 헤테로 지방족 그룹, 지환족 그룹, 및 헤테로 지환족 그룹을 포함할 수 있으며, 더욱 구체적으로 예를 들면, 비제한적인 예로, 상기 링커는 상기 화학식 1로 표시되는 둘 이상의 그룹 사이를 각각 2 내지 8 개의 탄소 원자로 연결하는 탄소수 2 내지 20의 지방족 그룹 (예를 들어, 알킬렌 그룹, 알케닐렌 그룹, 알키닐렌 그룹, 또는 상기 지방족 그룹에 헤테로 원자가 포함된 헤테로 지방족 그룹), 탄소수 2 내지 20의 지환족 그룹 (예를 들어, 사이클로알킬렌 그룹, 사이클로알케닐렌 그룹, 사이클로알키닐렌 그룹, 또는 상기 지환족 그룹에 헤테로 원자가 포함된■헤테로 지환족 그룹), 또는 상기 지방족 (또는 헤테로 지방족) 그룹과 지환족 (또는 해테로 지환족) 그룹이 결합된 형태일 수 있다. 상술한 리간드 화합물의 비제한적인 예로, 다음과 같은 구조를 갖는 화합물을 들 수 있다. 아래의 예시에서 상기 화학식 1로 표시되는 그룹은 편의상 [A], [Α'] 또는 [Α"]로 표시되었으며, [Α], [Α'] 및 [Α"] 는 같거나 다를 수 있다. In addition, two or more groups represented by Formula 1 may be included in one compound. In this case, the linker connecting the two groups may be an aliphatic group having 2 to 20 carbon atoms, a heteroaliphatic group having 2 to 20 carbon atoms, and 2 to 20 carbon atoms. It may include an alicyclic group of, a heteroalicyclic group of 2 to 20 carbon atoms, or the aliphatic group, heteroaliphatic group, alicyclic group, and heteroalicyclic group, more specifically, for example, non-limiting examples The linker may be an aliphatic group having 2 to 20 carbon atoms (for example, an alkylene group, an alkenylene group, an alkynylene group, or Heteroaliphatic group containing a hetero atom in the aliphatic group, alicyclic group having 2 to 20 carbon atoms (for example, cycloalkylene group , A cycloalkyl alkenylene group, cyclo alkynylene group, or wherein the alicyclic group contains a hetero atom ■ heterocyclic aliphatic group), or the aliphatic (or heterocyclic aliphatic) group and the alicyclic (or by interrogating alicyclic) groups combined It may be in the form. As a non-limiting example of the above-mentioned ligand compound, the compound which has a structure as follows is mentioned. In the following example, the group represented by Formula 1 is represented by [A], [Α ′] or [Α ″] for convenience, and [Α], [Α ′] and [Α ″] may be the same or different.
(i) 복수의 Α사이를 2 또는 3 개의 탄소 원자로 연결하는 그룹을 갖는 화합물:
(i) a compound having a group connecting two or three carbon atoms between a plurality of A:
(iii) 복수의 A 사이를 5 개 이상의 탄소 원자로 연결하는 그룹을 갖는 화합물:
(iii) a compound having a group connecting a plurality of As with at least 5 carbon atoms:
본 발명에 따른 리간드 화합물은 상기 예들 이외에도 전술한 조건을 만족하는 범위에서 다양한 조합으로 구현될 수 있다. 그리고, 상기 리간드 화합물은 공지의 반웅들을 응용하여 합성될 수 있으며, 보다 상세한 합성 방법은 실시예 부분에서 상술한다. 한편, 본 발명의 다른 일 측면에 따르면, 상술한 리간드 화합물 및 크롬 (Cr)을 포함하는, 유기 크름 화합물이 제공된다. Ligand compounds according to the present invention can be implemented in various combinations in the range satisfying the above conditions in addition to the above examples. In addition, the ligand compound may be synthesized by applying known reactions, and a more detailed synthesis method is described in the Examples section. On the other hand, according to another aspect of the present invention, there is provided an organic cream compound, including the above-described ligand compound and chromium (Cr).
상기 유기 크름 화합물은, 배위자로 하고, 크롬 원자를 중심 금속으로 하여, 상술한 리간드 화합물이 배위된 형태의 화합물일 수 있으며, 예를 들면, 하기 화학식 1-1로 표시되는 그룹을 포함할 수 있다. The organic cream compound may be a compound in which the ligand compound is coordinated with a ligand, and a chromium atom as a center metal, and may include, for example, a group represented by the following Chemical Formula 1-1. .
[화학식 1-1] [Formula 1-1]
상기 화학식 1-1에서, In Chemical Formula 1-1,
*은 상기 화학식 1-1로 표시되는 그룹이 라디칼임을 의미하고
A는 붕소 (B), 질소 (N), 인 (P) 또는 안티몬 (Sb)이고, * Means that the group represented by the formula 1-1 is a radical A is boron (B), nitrogen (N), phosphorus (P) or antimony (Sb),
χ는 각각 독립적으로 인 (p), 비소 (As), 또는 안티몬 (Sb)이고, χ is each independently phosphorus (p), arsenic (As), or antimony (Sb),
R1 내지 R4는, 각각 독립적으로; R1 to R4 are each independently;
메타 또는 파라 위치에 선택적으로, 알킬기, 알콕시, 알킬설파닐기, 및 알킬실릴기로 이루어진 군에서 선택된 1종 이상의 치환기가 치환되거나 결합된, 탄소수 6 내지 20의 아릴기이고; An aryl group having 6 to 20 carbon atoms, optionally substituted at the meta or para position, with one or more substituents selected from the group consisting of an alkyl group, an alkoxy, an alkylsulfanyl group, and an alkylsilyl group;
Cr은 크롬이고, Cr is chromium ,
Y1 내지 Y3는 각각 독립적으로, 할로겐, 수소, 탄소수 1 내지 10의 하이드로카빌, 또는 탄소수 1 내지 10의 헤테로하이드로카빌이다. Y 1 to Y 3 are each independently halogen, hydrogen, hydrocarbyl having 1 to 10 carbon atoms, or heterohydrocarbyl having 1 to 10 carbon atoms.
상기 유기 크롬 화합물은 상술한 리간드 화합물의 크롬 착화합물 (complex compound)로서, 크름 소스의 크롬이 상기 화학식 1로 표시되는 그룹의 X 부분에 배위 결합을 이룬 형태를 가질 수 있다. 이러한 유기 크름 화합물은 올레핀의 을리고머화 반웅용 촉매 시스템에 적용되어 우수한 촉매 활성과 1-핵센 또는 1-옥텐에 대한 높은 선택도를 나타낼 수 있다. 그리고, 상기 화학식 1-1에서, X와 R1 내지 R4에 대한 설명과 구체적인 예들은 상기 화학식 1의 리간드 화합물에서 설명한 바와 같다. 한편, 본 발명의 또 다른 일 측면에 따르면,!) 크롬 소스, 상술한 리간드 화합물, 및 조촉매를 포함하거나; 또는 ii) 하기 화학식 1-1로 표시되는 그룹을 포함하는 유기 크름 화합물, 및 조촉매를 포함하는, 올레핀 을리고머화 용 촉매 시스템이 제공된다. The organic chromium compound may be a chromium complex compound of the above-described ligand compound, and may have a form in which chromium of a creme source forms a coordinative bond to the X portion of the group represented by Formula 1. These organic kink compounds can be applied to the catalyst system for the oligomerization reaction mixture of olefins to exhibit good catalytic activity and high selectivity for 1-nuxene or 1-octene. In Formula 1-1, descriptions and specific examples of X and R1 to R4 are the same as those described for the ligand compound of Formula 1. On the other hand, according to another aspect of the invention,!) comprises a chromium source, the above-described ligand compound, and a promoter; Or ii) an organic cream compound comprising a group represented by the following Chemical Formula 1-1, and a promoter, and a catalyst system for olefin oligomerization is provided.
[화학식 1-1] [Formula 1-1]
상기 화학식 1-1에서,
*은 상기 화학식 1-1로 표시되는 그룹이 라디칼임을 의미하고, In Chemical Formula 1-1, * Means that the group represented by the formula 1-1 is a radical,
A는 붕소 (B), 질소 (N), 인 (P) 또는 안티몬 (Sb)이고, A is boron (B), nitrogen (N), phosphorus (P) or antimony (Sb),
X는 각각 독립적으로 인 (P), 비소 (As), 또는 안티몬 (Sb)이고 Each X is independently phosphorus (P), arsenic (As), or antimony (Sb)
R1 내지 R4는, 각각 독립적으로; R1 to R4 are each independently;
메타 또는 파라 위치에 선택적으로, 알킬기, 알콕시, 알킬설파닐기, 및 알킬실릴기로 이루어진 군에서 선택된 1종 이상의 치환기가 치환되거나 결합된, 탄소수 6 내지 20의 아릴기이고; An aryl group having 6 to 20 carbon atoms optionally substituted in the meta or para position, at least one substituent selected from the group consisting of an alkyl group, an alkoxy, an alkylsulfanyl group, and an alkylsilyl group;
Cr은 크롬이고, Cr is chromium,
Y1 내지 Y3는 각각 독립적으로, 할로겐, 수소, 탄소수 1 내지 10의 하이드로카빌, 또는 탄소수 1 내지 10의 헤테로하이드로카빌이다. Y1 to Y3 are each independently halogen, hydrogen, hydrocarbyl having 1 to 10 carbon atoms, or heterohydrocarbyl having 1 to 10 carbon atoms.
여기서, 상기 리간드 화합물 및 유기 크름 화합물에 대한 설명과 구체적인 예들은 전술한 내용으로 갈음한다. Here, the description and specific examples of the ligand compound and the organic crum compound will be replaced with the above description.
발명의 일 구현 예에 따르면, 상기 올레핀 올리고머화용 촉매 시스템은 i) 크롬 소스, 상술한 리간드 화합물 및 조촉매를 포함하는 3 성분계 촉매 시스템, 또는 ii) 상술한 유기 크름 화합물 및 조촉매를 포함하는 2 성분계 촉매 시스템일 수 있다. According to one embodiment of the invention, the catalyst system for olefin oligomerization comprises: i) a three-component catalyst system comprising a chromium source, a ligand compound, and a promoter as described above, or ii) a two-component catalyst comprising an organic crum compound and a promoter as described above. It may be a component catalyst system.
상기 촉매 시스템에 있어서, 상기 크롬 소스는 크름의 산화 상태가 0 내지 6인 유기 또는 무기 크름 화합물로서, 예를 들어 크롬 금속이거나, 또는 임의의 유기 또는 무기 라디칼이 크름에 결합된 화합물일 수 있다. 여기서, 상기 유기 라디칼은 라디칼당 1 내지 20의 탄소 원자를 갖는 알킬, 알콕시, 에스테르, 케톤, 아미도, 카르복실레이트 라디칼 등일 수 있고, 상기 무기 라디칼은 할라이드, 황산염, 산화물 등일 수 있다. In the catalyst system, the chromium source is an organic or inorganic crescent compound in which the oxidation state of the crack is 0 to 6, for example chromium metal, or a compound in which any organic or inorganic radical is bonded to the crack. Here, the organic radical may be an alkyl, alkoxy, ester, ketone, amido, carboxylate radical, etc. having 1 to 20 carbon atoms per radical, and the inorganic radical may be a halide, sulfate, oxide, or the like.
바람직하게는, 상기 크롬 소스는 을레핀의 올리고머화에 높은 활성을 나타낼 수 있고 사용 및 입수가 용이한 화합물로서, 크로뮴 (III) 아세틸아세토네이트, 크로뮴 (ᅵᅵᅵ) 클로라이드 테트라하이드로퓨란, 크로뮴 (III) 2- 에틸핵사노에이트 크로뮴 (III) 아세테이트, 크로뮴 (III) 부티레이트, 크로뮴 (III) 펜타노에이트, 크로뮴 (ᅵᅵᅵ) 라우레이트, 크로뮴 (ᅵᅵᅵ) 트리스 (2,2,6,6-테트라메틸 -3.5- 헵테인디오네이트), 및 크로뮴 (III) 스테아레이트로 이루어진 군에서 선택된 1종 이상의 화합물일 수 있다. Preferably, the chromium source is a compound that may exhibit high activity in oligomerization of olepin and is easy to use and obtain, such as chromium (III) acetylacetonate, chromium chloride, tetrahydrofuran, chromium ( III) 2-Ethylnucleoate chromium (III) acetate, chromium (III) butyrate, chromium (III) pentanoate, chromium (ᅵ) laurate, chromium (ᅵ) Tris (2,2,6) , 6-tetramethyl-3.5-heptanedionate), and chromium (III) stearate.
바람직하게는, 상기 조촉매는 13족 금속을 포함하는 유기 금속
화합물로서, 일반적으로 전이금속 화합물의 촉매 하에 올레핀을 중합할 때 이용될 수 있는 것이라면 특별히 한정되지 않고 적용될 수 있다. Preferably, the promoter is an organic metal comprising a Group 13 metal As the compound, as long as it can be used when polymerizing the olefin under the catalyst of the transition metal compound, it can be applied without particular limitation.
예를 들어, 상기 조촉매는 하기 화학식 4 내지 6으로 표시되는 화합물로 이루어진 군에서 선택된 1종 이상의 화합물일 수 있다: For example, the promoter may be at least one compound selected from the group consisting of compounds represented by Formulas 4 to 6 below:
[화학식 4] [Formula 4]
-[AI(Rx)-O]c- 상기 화학식 4에서, Rx는 서로 동일하거나 상이하고, 각각 독립적으로 할로겐 라디칼, 탄소수 1 내지 20의 하이드로카빌 라디칼, 또는 할로겐으로 치환된 탄소수 1 내지 20의 하이드로카빌 라디칼이고, c는 2 이상의 정수이고, [화학식 5] -[AI (Rx) -O] c -In Formula 4, Rx is the same or different from each other, and each independently a halogen radical, a hydrocarbyl radical of 1 to 20 carbon atoms, or a hydro of 1 to 20 carbon atoms substituted with halogen A carbyl radical, c is an integer of 2 or more, and [Formula 5]
D(Ry)3 D (Ry) 3
상기 화학식 5에서, D는 알루미늄 또는 보론이고, Ry는 탄소수 1 내지 In Formula 5, D is aluminum or boron, Ry is 1 to carbon atoms
20의 하이드로카빌 또는 할로겐으로 치환된 탄소수 1 내지 20의 하이」 로카빌이고, 20 '' hydrocarbyl or halogen substituted by high '' rocabil,
[화학식 6] [Formula 6]
[L-H]+[Q(E)4]' [LH] + [Q (E) 4 ] '
상기 화학식 6에서, In Chemical Formula 6,
L은 중성 루이스 염기이고, [L-H]+는 브뢴스테드 산이며, Q는 +3 형식 산화 상태의 붕소 또는 알루미늄이고, E는 각각 독립적으로 1 이상의 수소 원자가 할로겐, 탄소수 1 내지 20의 하이드로카빌, 알콕시 작용기 또는 페녹시 작용기로 치환 또는 비치환된 탄소수 6 내지 20의 아릴기 또는 탄소수 1 내지 20의 알킬기이다. L is a neutral Lewis base, [LH] + is Bronsted acid, Q is boron or aluminum in the +3 type oxidation state, each E is independently at least one hydrogen atom is halogen, a hydrocarbyl having 1 to 20 carbon atoms, An aryl group having 6 to 20 carbon atoms or an alkyl group having 1 to 20 carbon atoms which is unsubstituted or substituted with an alkoxy functional group or a phenoxy functional group.
일 구현 예에 따르면, 상기 화학식 4로 표시되는 화합물은 메틸알루미녹산, 에틸알루미녹산, 이소부틸알루미녹산, 부틸알루미녹산 등의 알킬알루미녹산일 수 있다. According to one embodiment, the compound represented by Formula 4 may be alkyl aluminoxane, such as methyl aluminoxane, ethyl aluminoxane, isobutyl aluminoxane, butyl aluminoxane.
그리고, 일 구현 예에 따르면, 상기 화학식 5로 표시되는 화합물은 트리메틸알루미늄, 트리에틸알루미늄, 트리이소부틸알루미늄, 트리프로필알루미늄, 트리부틸알루미늄, 디메틸클로로알루미늄, 디메틸이소부틸알루미늄, 디메틸에틸알루미늄, 디에틸클로로알루미늄, 트리이소프로필알루미늄, 트리 -S-부틸알루미늄, 트리씨클로펜틸알루미늄,
트리펜틸알루미늄, 트리이소펜틸알루미늄, 트리핵실알루미늄, 에틸디메틸알루미늄, 메틸디에틸알루미늄 트리페닐알루미늄, 트리 -P- 를릴알루미늄, 디메틸알루미늄메록시드, 디메틸알루미늄에톡시드, 트리메틸보론, 트리에틸보론, 트리이소부틸보론, 트리프로필보론, 트리부틸보론 등일 수 있다. 또한, 일 구현 예에 따르면, 상기 화학식 6으로 표시되는 화합물은 트리에틸암모니움테트라페닐보론, 트리부틸암모니움테트라페닐보론, 트리메틸암모니움테트라페닐보론, 트리프로필암모니움테트라페닐보론, 트리메틸암모니움테트라 (P-를릴)보론, 트리프로필암모니움테트라 (P-를릴 )보론ᅳ 트리에틸암모니움테트라 (ο,ρ-디메틸페닐)보론, 트리메틸암모니움테트라 (ο,ρ- 디메틸페닐)보론, 트리부틸암모니움테트라 (Ρ-트리플루오로메틸페닐)보론, 트리메틸암모니움테트라 (Ρ-트리풀로로메틸페닐)보론, According to one embodiment, the compound represented by Chemical Formula 5 is trimethylaluminum, triethylaluminum, triisobutylaluminum, tripropylaluminum, tributylaluminum, dimethylchloroaluminum, dimethylisobutylaluminum, dimethylethylaluminum, di Ethylchloroaluminum , triisopropylaluminum , tri-S-butylaluminum , tricyclopentylaluminum, Tripentyl aluminum, triisopentyl aluminum, trinuclear sil aluminum, ethyl dimethyl aluminum, methyl diethyl aluminum triphenyl aluminum, tri-P- ryl aluminum, dimethyl aluminum hydroxide, dimethyl aluminum ethoxide, trimethyl boron, triethyl boron, Triisobutyl boron, tripropyl boron, tributyl boron and the like. In addition, according to one embodiment, the compound represented by Formula 6 is triethylammonium tetraphenylboron, tributylammonium tetraphenylboron, trimethylammonium tetraphenylboron, tripropylammonium tetraphenylboron, trimethylammonium Tetra (P-Lyl) boron, tripropyl ammonium tetra (P-lryl) boron ᅳ triethyl ammonium tetra (ο, ρ-dimethylphenyl) boron, trimethyl ammonium tetra (ο, ρ-dimethylphenyl) boron, tri Butyl ammonium tetra (Ρ-trifluoromethylphenyl) boron, trimethyl ammonium tetra (Ρ-trifluoro methylphenyl) boron,
트리부틸암모니움테트라펜타풀루오로페닐보론, Ν,Ν- 디에틸아닐리니움테트라페닐 보론, Ν,Ν-디에틸아닐리니움테트라페닐보론, Ν,Ν- 디에틸아닐리니움테트라펜타플루오로페닐보론, Tributylammonium tetrapentapulophenylphenyl, Ν, Ν- diethylanilinium tetraphenyl boron, Ν, Ν-diethylanilinium tetraphenylboron, Ν, Ν- diethylanilinium tetrapentafluoro Rophenylboron,
디에틸암모니움테트라펜타플투오로페닐보론, 트리페닐포스포늄테트라페닐보론, 트리메틸포스포늄테트라페닐보론, 트리에틸암모니움테트라페닐알루미늄, 트리부틸암모니움테트라페닐알루미늄, 트리메틸암모니움테트라페닐알루미늄, 트리프로필암모니움테트라페닐알루미늄, 트리메틸암모니움테트라 (Ρ- 를릴)알루미늄, 트리프로필암모니움테트라 (Ρ-를릴)알루미늄, 트리에틸암모니움테트라 (ο,ρ-디메틸페닐)알루미늄, 트리부틸암모니움테트라 (Ρ- 트리플루오로메틸페닐)알루미늄, 트리메틸암모니움테트라 (Ρ- 트리플루오로메틸페닐)알루미늄,트리부틸암모니움테트라펜타플루오로페닐알루 미늄, Ν,Ν-디에틸아닐리니움테트라페닐알루미늄 Ν,Ν- 디에틸아닐리니움테트라페닐알루미늄, Ν,Ν- 디에틸아닐리니움테트라펜타플로로페닐알루미늄, Diethyl ammonium tetrapentaplefluorophenyl boron, triphenyl phosphonium tetraphenyl boron, trimethyl phosphonium tetraphenyl boron, triethyl ammonium tetraphenyl aluminum, tributyl ammonium tetraphenyl aluminum, trimethyl ammonium tetraphenyl aluminum, tree Propyl Ammonium Tetraphenyl Aluminum, Trimethyl Ammonium Tetra (Ρ-rylryl) Aluminum, Tripropyl Ammonium Tetra (Ρ-rylryl) Aluminum, Triethyl Ammonium Tetra (ο, ρ-dimethylphenyl) Aluminum, Tributyl Ammonium Tetra (Ρ-trifluoromethylphenyl) aluminum, trimethylammonium tetra (Ρ- trifluoromethylphenyl) aluminum, tributylammonium tetrapentafluorophenylaluminum, Ν, Ν-diethylanilinium tetraphenylaluminum Ν, Ν- diethylanilinium tetraphenylaluminum, Ν, Ν- diethylanilinium tetrapentafluorophenyl Aluminum,
디에틸암모니움테트라펜타플루오로페닐알루미늄, Diethylammonium tetrapentafluorophenylaluminum,
트리페닐포스포늄테트라페닐알루미늄, 트리메틸포스포늄테트라페닐알루미늄, 트리페닐카보니움테트라페닐보론, 트리페닐카보니움테트라페닐알루미늄, 트리페닐카보니움테트라 (ρᅳ트리플로로메틸페닐)보론, Triphenylphosphonium tetraphenylaluminum, trimethylphosphonium tetraphenylaluminum, triphenylcarbonium tetraphenylboron, triphenylcarbonium tetraphenylaluminum, triphenylcarbonium tetra (ρ ᅳ trifluoromethylphenyl) boron,
트리페닐카보니움테트라펜타플루오로페닐보론 등 일 수 있다.
또한, 비제한적인 예로, 상기 조촉매는 유기알루미늄 화합물, 유기붕소 화합물, 유기마그네슴 화합물, 유기아연 화합물, 유기리튬 화합물, 또는 이들의 흔합물일 수 있다. 일 실시예에 따르면, 상기 조촉매는 유기알루미늄 화합물인 것이 바람직하며, 보다 바람직하게는 트리메틸 알루미늄 (trimethyl aluminium), 트리에틸 알루미늄 (triethyl aluminium), 트리이소프로필 알루미늄 (triisopropyl aluminium), 트리이소부틸 알루미늄 (triisobutyl aluminum), 에틸알루미늄 세스퀴클로라이드 (ethylaluminum sesquichloride), 디에틸알루미늄 클로라이드 (diethylaluminum chloride), 에틸 알루미늄 디클로라이드 (ethyl aluminium dichloride), 메틸알루미녹산 (methylaluminoxane), 및 개질된 메틸알루미녹산 (modified methylaluminoxane)으로 이루어진 군에서 선택된 1종 이상의 화합물일 수 있다. Triphenylcarbonium tetrapentafluorophenylboron and the like. In addition, as a non-limiting example, the promoter may be an organoaluminum compound, an organoboron compound, an organomagnesium compound, an organozinc compound, an organolithium compound, or a combination thereof. According to one embodiment, the promoter is preferably an organoaluminum compound, more preferably trimethyl aluminum, triethyl aluminum, triisopropyl aluminum, triisobutyl aluminum (triisobutyl aluminum), ethylaluminum sesquichloride, diethylaluminum chloride, ethyl aluminum dichloride, methylaluminoxane, and modified methylaluminoxane It may be one or more compounds selected from the group consisting of
한편, 상기 촉매 시스템을 구성하는 성분들의 함량비는 촉매 활성과 선형 알파-을레핀에 대한 선택도 등을 고려하여 결정될 수 있다. 일 구현 예에 따르면, 상기 3 성분계 촉매 시스템인 경우, 상기 리간드 화합물의 디포스피노 아미닐 잔기: 크롬 소스: 조촉매의 몰비는 약 1 :1 :1 내지 10:1 :10,000, 또는 약 1 :1 :100 내지 5:1 :3,000으로 조절되는 것이 유리하다. 그리고, 상기 2 성분계 촉매 시스템인 경우, 상기 유기 크름 화합물의 디포스피노 아미닐 잔기: 조촉매의 몰비는 1 :1 내지 1 :10,000, 또는 1 :1 내지 1 :5,000, 또는 1 :1 내지 1 :3,000으로 조절되는 것이 유리하다. On the other hand, the content ratio of the components constituting the catalyst system may be determined in consideration of the catalytic activity and the selectivity to the linear alpha-lefin. According to one embodiment, in the three-component catalyst system, the molar ratio of diphosphino aminyl residue: chromium source: cocatalyst of the ligand compound is about 1: 1: 1 to 10: 1: 10,000, or about 1: 1: 1 It is advantageous to adjust from: 100 to 5: 1: 3,000. And, in the case of the two-component catalyst system, the molar ratio of diphosphino aminyl moiety: cocatalyst of the organic kneading compound is 1: 1 to 1: 10,000, or 1: 1 to 1: 5,000, or 1: 1 to 1: 1. It is advantageous to adjust to 3,000.
그리고, 상기 촉매 시스템을 구성하는 성분들은 동시에 또는 임의 순서로, 적절한 용매 및 단량체의 존재 또는 부재 하에 첨가되어 활성이 있는 촉매 시스템으로 작용할 수 있다. 이때, 적합한 용매로는 헵탄, 를루엔, 사이클로핵산, 메틸사이클로핵산, 1-핵센 1-옥텐, 디에틸에테르, 테트라히드로푸란, 아세토니트릴, 디클로로메탄, 클로로포름, 클로로벤젠, 메탄올, 아세톤 등이 사용될 수 있다. The components constituting the catalyst system can then be added simultaneously or in any order in the presence or absence of suitable solvents and monomers to act as an active catalyst system. At this time, suitable solvents include heptane, toluene, cyclonucleic acid, methylcyclonucleic acid, 1-nuxene 1-octene, diethyl ether, tetrahydrofuran, acetonitrile, dichloromethane, chloroform, chlorobenzene, methanol, acetone, and the like. Can be.
또한, 발명의 일 구현 예에 따르면, 상기 촉매 시스템은 담체를 더욱 포함할 수 있다. 즉, 상기 화학식 1의 리간드 화합물은 담체에 담지된 형태로 에틸렌 올리고머화에 적용될 수 있다. 상기 담체는 통상의 담지 촉매에 적용되는 금속, 금속 염 또는 금속 산화물 등일 수 있다. 비제한적인 예로, 상기 담체는 실리카, 실리카 -알루미나, 실리카 -마그네시아 등일 수 있으며,
Na20, K2CO3, BaS04, Mg(N03)2 등과 같은 금속의 산화물, 탄산염, 황산염, 질산염 성분을 포함할 수 있다. In addition, according to one embodiment of the invention, the catalyst system may further comprise a carrier. That is, the ligand compound of Formula 1 may be applied to ethylene oligomerization in a form supported on a carrier. The carrier may be a metal, a metal salt, a metal oxide, or the like applied to a conventional supported catalyst. As a non-limiting example, the carrier may be silica, silica-alumina, silica-magnesia, and the like, Oxides, carbonates, sulfates, nitrates of metals such as Na 2 O, K 2 CO 3, BaS0 4 , Mg (N0 3 ) 2, and the like.
이러한 촉매 시스템은 바람직하게는, 에틸렌의 4량화 반응용으로 사용될 수 있으며, 상술한 바에 의해 높은 선택도로, 1-옥텐을 제조할 수 있게 된다. 한편, 본 발명의 또 다른 일 측면에 따르면, 상술한 촉매 시스템의 존재 하에, 을레핀의 올리고머화 반웅을 진행하여, 알파-을레핀을 형성하는 단계;를 포함하는, 을레핀의 을리고머화 방법이 제공된다. Such a catalyst system can preferably be used for the quaternization reaction of ethylene, allowing the production of 1-octene with high selectivity as described above. On the other hand, according to another aspect of the present invention, in the presence of the above-described catalyst system, proceeding the oligomerization reaction of the olepin, to form the alpha- olepin; comprising; This is provided.
바람직하게는, 상기 올레핀의 올리고머화 반웅은, 에틸렌의 4량화 반응일 수 있고, 반응 결과물로 1-옥텐을 형성하는 것일 수 있다. 본 발명에 따론 을레핀의 을리고머화 방법은 을레핀 (예를 들어, 에틸렌)을 원료로 전술한 촉매 시스템과 통상적인 장치 및 접촉 기술을 적용하여 수행될 수 있다. 비제한적인 예로, 상기 을레핀의 을리고머화 반응은 불활성 용매의 존재 또는 부재 하에서의 균질 액상 반웅, 또는 상기 촉매 시스템이 일부 용해되지 않거나 전부 용해되지 않은 형태인 슬러리 반웅, 또는 생성물인 알파-올레핀이 주 매질로 작용하는 벌크상 반옹, 또는 가스상 반웅으로 수행될 수 있다. Preferably, the oligomerization reaction of the olefin may be a quaternization reaction of ethylene, and may form 1-octene as a reaction product. According to the present invention, the method for the ligomerization of leupine can be carried out by applying the above-described catalyst system with conventional elepine (for example, ethylene) as a raw material and conventional apparatus and contacting techniques. By way of non-limiting example, the ligomerization reaction of leulevine may be a homogeneous liquid reaction in the presence or absence of an inert solvent, or a slurry reaction in which the catalyst system is partially or completely undissolved, or a product of alpha-olefin. It may be carried out as a bulk reaction, or as a gas reaction, acting as the main medium.
그리고, 상기 을레핀의 올리고머화 반웅은 불활성 용매 하에서 수행될 수 있다. 비제한적인 예로, 상기 불활성 용매는 벤젠, 를루엔, 크실렌, 큐멘, 클로로벤젠, 디클로로벤젠, 헵탄, 사이클로핵산, 메틸사이클로핵산, 메틸사이클로펜탄, n-핵산, 1-핵센, 1-옥텐 등일 수 있다. And, the oligomerization reaction of the olepin can be performed under an inert solvent. As a non-limiting example, the inert solvent may be benzene, toluene, xylene, cumene, chlorobenzene, dichlorobenzene, heptane, cyclonucleic acid, methylcyclonucleic acid, methylcyclopentane, n-nucleic acid, 1-nuxene, 1-octene, etc. have.
그리고, 상기 올레핀의 을리고머화 반웅은 약 0 내지 약 200°C , 또는 약 0 내지 약 150°C , 또는 약 30 내지 약 100°C , 또는 약 50 내지 약 100 °C의 온도 하에서 수행될 수 있다. 또한, 상기 반웅은 약 15 내지 약 3000 psig, 또는 약 15 내지 약 1500 psig, 또는 약 15 내지 약 1000 psig의 압력 하에서 수행될 수 있다. And, the oligomerization reaction of the olefin can be carried out at a temperature of about 0 to about 200 ° C, or about 0 to about 150 ° C, or about 30 to about 100 ° C, or about 50 to about 100 ° C. have. In addition, the reaction may be performed under a pressure of about 15 to about 3000 psig, or about 15 to about 1500 psig, or about 15 to about 1000 psig.
이하, 발명의 구체적인 실시예를 통해, 발명의 작용 및 효과를 보다
상술하기로 한다. 다만, 이러한 실시예는 발명의 예시로 제시된 것에 불과하며, 이에 의해 발명의 권리범위가 정해지는 것은 아니다. Hereinafter, through the specific examples of the invention, the operation and effects of the invention It will be described in detail. However, these embodiments are only presented as an example of the invention, whereby the scope of the invention is not determined.
<실시^ l> <Implementation ^ l>
모든 반웅은 Schlenk technique 또는 gloN ebox¾ 이용하여 아르곤 하에서 진행되었다. 합성된 리간드는 Varian 500 MHz spectrometer를 이용하여 1H (500 MHz)와 31 P (202 MHz) NMR spectra를 찍어 분석하였다. Shift는 residual solvent peak를 reference로 하여 TMS로부터 downfield에서 ppm으로 나타내었다. Phosphorous probe는 aqueous H3PC 로 calibration하였다. All reactions were performed under argon using the Schlenk technique or gloN ebox¾. The synthesized ligand was analyzed by 1H (500 MHz) and 31 P (202 MHz) NMR spectra using a Varian 500 MHz spectrometer. Shift is expressed in ppm in the downfield from TMS with the residual solvent peak as a reference. Phosphorous probes were calibrated with aqueous H3PC.
리간드화합물합성 Ligand Compound Synthesis
아르곤 하에서 2-ethyl-6-methylaniline (10 mmol) 과 triethylamine (3 equiv. to amine)을 dichloromethane (80 mL)에 녹였다. 플라스크를 water bath에 담근 상태에서, chlorobis(3, 5-dimethylphenyl)phosphine (20 mmol)을 천천히 넣고, 밤새 교반하였다. 진공상태에서 용매를 제거한 후, 다른 용매인 diethyl ether, tetrahydrofuran 또는 hexane를 넣어 충분히 교반하여, air-free glass filter로 triethylammonium chloride salt을 제거하였다. 여과액에서 용매를 제거하여 생성물을 얻었다. Under argon, 2-ethyl-6-methylaniline (10 mmol) and triethylamine (3 equiv. To amine) were dissolved in dichloromethane (80 mL). While the flask was immersed in a water bath, chlorobis (3, 5-dimethylphenyl) phosphine (20 mmol) was slowly added thereto and stirred overnight. After the solvent was removed in vacuo, other solvents such as diethyl ether, tetrahydrofuran or hexane were added and sufficiently stirred to remove triethylammonium chloride salt with an air-free glass filter. The solvent was removed from the filtrate to give the product.
31P NMR (202 MHz, CDCI3): 49.6 (br m), 53.8 (br m), 61.8 (br s) 3 1 P NMR (202 MHz, CDCI 3 ): 49.6 (br m), 53.8 (br m), 61.8 (br s)
아르곤 하에서 2-ethyl-6-methylaniline (10 mmol) 과 triethylamine (3
equiv. to amine)을 dichbromethane (80 ml_)에 녹였다. 폴라스크를 water bath에 담근 상태에서, chlorobis(3-methylphenyl)phosphine (20 mmol)을 천천히 넣고, 밤새 교반하였다. 진공상태에서 용매를 제거한 후, 다른 용매인 diethyl ether, tetrahydrofuran 또는 hexane를 넣어 층분히 교반하여, air-free glass filter로 ' triethylammonium chloride salt을 제거하였다. 여과액에서 용매를 제거하여 생성물을 얻었다. 2-ethyl-6-methylaniline (10 mmol) and triethylamine under argon (3 equiv. to amine) was dissolved in dichbromethane (80 ml_). Chlorobis (3-methylphenyl) phosphine (20 mmol) was slowly added while the polar flask was soaked in a water bath and stirred overnight. After the solvent was removed in vacuo, another solvent, diethyl ether, tetrahydrofuran or hexane, was added to the mixture and stirred. The triethylammonium chloride salt was removed using an air-free glass filter. The solvent was removed from the filtrate to give the product.
31 P NMR (202 MHz, CDCI3): 56.2 (br s) 31 P NMR (202 MHz, CDCI 3 ): 56.2 (br s)
아르곤 하에서 2-ethyl-6-methylaniline (10 mmol) 과 triethylamine (3 equiv. to amine)을 dichloromethane (80 mL)에 녹였다. 플라스크를 water bath에 담근 상태에서, chlorobis(3, 4-dimethylphenyl)phosphine (20 mmol)을 천천히 넣고ᅳ 밤새 교반하였다. 진공상태에서 용매를 제거한 후, 다른 용매인 diethyl ether, tetrahydrofuran 또는 hexane를 넣어 층분히 교반하여, air-free glass filter로 triethylammonium chloride salt을 제거하였다. 여과액에서 용매를 제거하여 생성물을 얻었다. Under argon, 2-ethyl-6-methylaniline (10 mmol) and triethylamine (3 equiv. To amine) were dissolved in dichloromethane (80 mL). While the flask was immersed in a water bath, chlorobis (3, 4-dimethylphenyl) phosphine (20 mmol) was slowly added thereto and stirred overnight. After the solvent was removed in vacuo, another solvent, diethyl ether, tetrahydrofuran or hexane, was added to the mixture and stirred. The triethylammonium chloride salt was removed using an air-free glass filter. The solvent was removed from the filtrate to give the product.
31P NMR (202 MHz, CDCI3): 50.0 (m) 31 P NMR (202 MHz, CDCI 3 ): 50.0 (m)
아르곤 하에서 2-isopropylcyclohexan-1 -amine (10 mmol) 과 triethylamine (3 equiv. to amine)을 dichloromethane (80 mL)에 녹였다 - 풀라스크를 water bath에 담근 상태에서, chlorabis(3, 5-
dimethylphenyl)phosphine (20 mmol)을 천천히 넣고, 밤새 교반하였다. 진공상태에서 용매를 제거한 후, 다른 용매인 diethyl ether, tetrahydrafuran 또는 hexane를 넣어 층분히 교반하여, air-free glass filter로 triethylammonium chloride salt을 제거하였다. 여과액에서 용매를 제거하여 생성물을 얻었다. Under argon, 2-isopropylcyclohexan-1 -amine (10 mmol) and triethylamine (3 equiv. To amine) were dissolved in dichloromethane (80 mL)-chlorabis (3, 5- with a full-laser in a water bath). Dimethylphenyl) phosphine (20 mmol) was slowly added and stirred overnight. After the solvent was removed in vacuo, another solvent, diethyl ether, tetrahydrafuran or hexane, was added to the mixture and stirred. The triethylammonium chloride salt was removed using an air-free glass filter. The solvent was removed from the filtrate to give the product.
31P NMR (202 MHz, CDCI3): 52.3 (s) 3 1 P NMR (202 MHz, CDCI 3 ): 52.3 (s)
아르곤 하에서 2-isopropylcyclohexan-1 -amine (10 mmol) 과 triethylamine (3 equiv. to amine)을 dichloromethane (80 mL)에 녹였다 · 플라스크를 water bath에 담근 상태에서, cNorobis(3-methylphenyl)phosphine (20 mmol)을 천천히 넣고, 밤새 교반하였다. 진공상태에서 용매를 제거한 후, 다른 용매인 diethyl ether, tetrahydrofuran 또는 hexane를 넣어 층분히 교반하여, air- free glass filter로 triethylammonium chloride salt을 제거하였다. 여과액에서 용매를 제거하여 생성물을 얻었다. Under argon, 2-isopropylcyclohexan-1 -amine (10 mmol) and triethylamine (3 equiv. To amine) were dissolved in dichloromethane (80 mL). · CNOrobis (3-methylphenyl) phosphine (20 mmol) while the flask was immersed in a water bath. ) Was slowly added and stirred overnight. After the solvent was removed in vacuo, another solvent, diethyl ether, tetrahydrofuran or hexane, was added to the mixture and stirred. The triethylammonium chloride salt was removed using an air-free glass filter. The solvent was removed from the filtrate to give the product.
31P NMR (202 MHz, CDCI3): 51.8 (br s) 31 P NMR (202 MHz, CDCI 3 ): 51.8 (br s)
아르곤 하에서 2-isopropylcyclohexan-1 -amine (10 mmol) 과 triethylamine (3 equiv. to amine)을 dichloromethane (80 mL)에 녹였다 . 플라스크를 water bath에 담근 상태에서, chbrobis(3, 4- dimethylphenyl)phosphine (20 mmol)을 천천히 넣고, 밤새 교반하였다. 진공상태에서 용매를 제거한 후, 다른 용매인 diethyl ether, tetrahydrofuran 또는
hexane를 넣어 충분히 교반하여, air-free glass filter로 triethylammonium chloride salt을 제거하였다. 여과액에서 용매를 제거하여 생성물을 얻었다. Under argon, 2-isopropylcyclohexan-1 -amine (10 mmol) and triethylamine (3 equiv. To amine) were dissolved in dichloromethane (80 mL). While the flask was immersed in a water bath, chbrobis (3,4-dimethylphenyl) phosphine (20 mmol) was slowly added thereto and stirred overnight. After removing the solvent under vacuum, other solvents such as diethyl ether, tetrahydrofuran or Hexane was added sufficiently to remove hexane and triethylammonium chloride salt was removed using an air-free glass filter. The solvent was removed from the filtrate to give the product.
3 P NMR (202 MHz, CDCI3): 54.5 (br s) 3 P NMR (202 MHz, CDCI 3 ): 54.5 (br s)
[비교 h2
Ph2 의 합성 아르곤 하에서 2-aminopropane (10 mmol)과 triethylamine (3 내지 10 equiv. to amine)을 dichloromethane (80 ml)어 l 녹였다 . 폴라스크를 water bath에 담근 상태에서, chloradiphenylphosphine (20 mmol)을 천천히 넣고 밤새 교반하였다. 진공 상태에서 용매를 제거한 후, 테트라하이드로퓨란을 넣어 충분히 교반하여 air-free glass filter로 triethylammonium chloride salt¾- 제거하였다. 여과액에서 용매를 제거하여 상기 화합물을 얻었다. [Comparative h 2 Dichloromethane (80 ml) was dissolved in 2-aminopropane (10 mmol) and triethylamine (3 to 10 equiv. To amine) under synthetic argon of Ph 2 . In a state in which the polar flask was soaked in a water bath, chloradiphenylphosphine (20 mmol) was slowly added thereto and stirred overnight. After removing the solvent in vacuo, tetrahydrofuran was added to the mixture was sufficiently stirred to remove triethylammonium chloride salt¾- with an air-free glass filter. The solvent was removed from the filtrate to obtain the compound.
31P NMR (202 MHz, CDCI3): 48.4 (br s) 31 P NMR (202 MHz, CDCI 3 ): 48.4 (br s)
[비교합성예 2] Comparative Example 2
0르곤 하에서 3-(aminomethyl)-3,5,5-trimethylcyclohexanamine (5 mmol)과 triethylamine (3 내지 10 equiv. to amine)을 dichloromethane (80 ml)에 녹였다. 플라스크를 water bath에 담근 상태에서, chloradiphenylphosphine (20 mmol)을 천천히 넣고 밤새 교반하였다. 진공 상태에서 용매를 제거한 후, 테트라하이드로퓨란을 넣어 층분히 교반하여 air-free glass filter로 triethylammonium chloride salt를 제거하였다. 여과액에서 용매를 제거하여 상기 화합물을 얻었다. Under 0 rgon, 3- (aminomethyl) -3,5,5-trimethylcyclohexanamine (5 mmol) and triethylamine (3 to 10 equiv. To amine) were dissolved in dichloromethane (80 ml). While the flask was immersed in a water bath, chloradiphenylphosphine (20 mmol) was slowly added thereto and stirred overnight. After removing the solvent in vacuo, tetrahydrofuran was added and stirred thoroughly to remove triethylammonium chloride salt with an air-free glass filter. The solvent was removed from the filtrate to obtain the compound.
31P NMR (202 MHz, CDC!3): 45.6 (br s), 56.2 (br s)
촉매 시스템의 제조 및 에틸렌 을리고머화반웅진행 31 P NMR (202 MHz, CDC! 3 ): 45.6 (br s), 56.2 (br s) Preparation of catalyst system and progress of ethylene oligomerization reaction
[실시예 1 내지 6 및 비교예 1 내지 2] [Examples 1 to 6 and Comparative Examples 1 to 2]
아르곤 가스 분위기 하에서, 크로뮴 (III) 아세틸아세토네이트 (17.5 mg, 0.05 mmol)와 상기 합성예 및 비교합성예에 따른 리간드 화합물 (0.025 mmol)를 플라스크에 담은 후, 여기에 10 ml의 사이클로핵산을 넣고 교반하여 5 mM (Cr기준)의 촉매 용액을 준비하였다. In an argon gas atmosphere, chromium (III) acetylacetonate (17.5 mg, 0.05 mmol) and a ligand compound (0.025 mmol) according to the above synthesis and comparative synthesis examples were put in a flask, and 10 ml of cyclonucleic acid was added thereto. By stirring, 5 mM (based on Cr) of the catalyst solution was prepared.
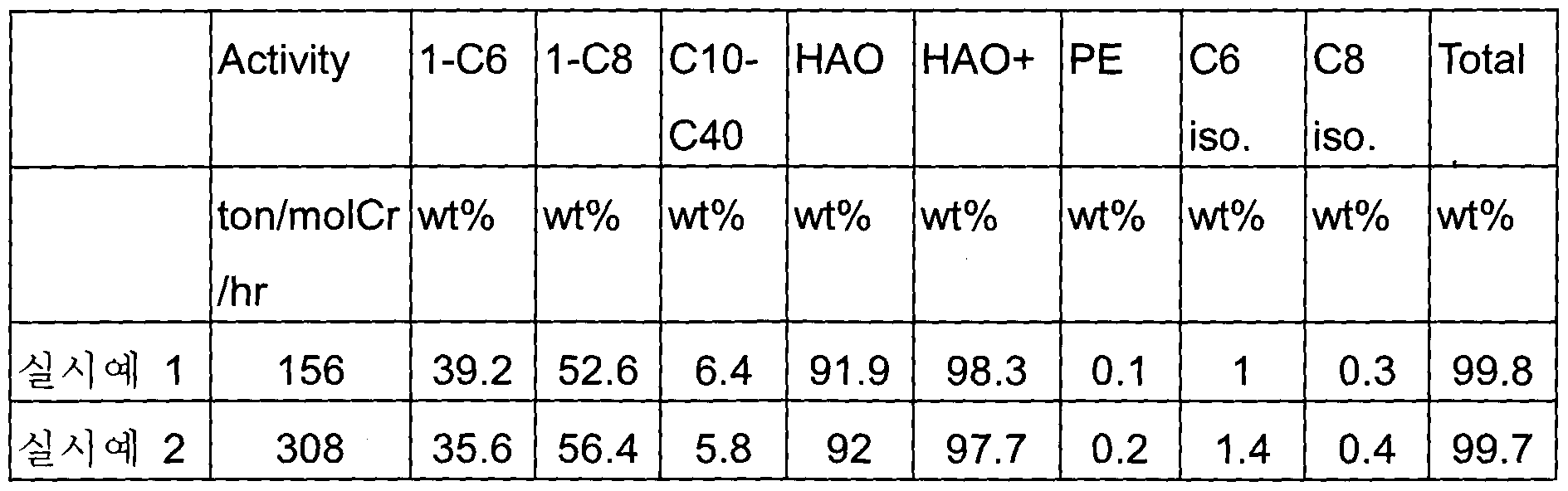
600 ml 용량의 Parr 반웅기를 준비하여 120 °C로 2 시간 동안 진공을 잡은 후, 내부를 아르곤으로 치환하고 은도를 60 °C로 내렸다. 그 후, 180 ml의 사이클로핵산 및 2ml의 MMAO (isoheptane solution, Al/Cr=1200)를 주입하고, 상기 촉매 용액 0.5 ml (2.5 마이크로 몰 Cr)를 주입하였다. 2 분 동안 500 rpm으로 교반 후, 60 bar로 맞춰진 에틸렌 라인의 벨브를 열어 반웅기 안을 에틸렌으로 채운 다음, 45 °C로 제열되도록 조절하여 500 rpm으로 15 분 동안 교반하였다. 에틸렌 라인 벨브를 잠그고, 반옹기를 드라이 아이스 / 아세톤 bath를 이용하여 0°C로 식힌 후, 미반응 에틸렌을 천천히 vent한 후 0.5 ml의 노네인 (GC internal standard)을 넣어주었다. 10 초 동안 교반한 다음, 반웅기의 액체 부분을 2ml 취하여 물로 quench하고, 얻어진 유기 부분을 PTFE syringe filter로 필터하여 GC-FID 샘플을 만들었다. 그리고 liquid product의 distribution을 GC로 분석하였다. 또한 남은 반응액에 ethanol/HCI (10 vol% of aqueous 12M HCI solution) 400 ml를 넣어 교반하고 필터하여 고체의 양을 분석하였다. 수득한 폴리머는 65 °C vacuum oven 에서 밤새 건조하였다. 상기 실시예 및 비교예의 결과를 아래 표에 정리하였다. Parr reaction vessels of 600 ml capacity were prepared and vacuumed at 120 ° C for 2 hours, after which the interior was replaced with argon and the silver was lowered to 60 ° C. Thereafter, 180 ml of cyclonucleic acid and 2 ml of MMAO (isoheptane solution, Al / Cr = 1200) were injected, and 0.5 ml (2.5 micromol Cr) of the catalyst solution was injected. After stirring at 500 rpm for 2 minutes, the valve of the ethylene line set to 60 bar was opened to fill the reaction vessel with ethylene, and then adjusted to be defrosted at 45 ° C. and stirred at 500 rpm for 15 minutes. After closing the ethylene line valve, the reactor was cooled to 0 ° C using a dry ice / acetone bath, slowly unvented ethylene was vented, and 0.5 ml of nonane (GC internal standard) was added thereto. After stirring for 10 seconds, 2 ml of the liquid portion of the reaction mixture was quenched with water, and the obtained organic portion was filtered with a PTFE syringe filter to make a GC-FID sample. And the distribution of the liquid product was analyzed by GC. In addition, 400 ml of ethanol / HCI (10 vol% of aqueous 12M HCI solution) was added to the remaining reaction solution, followed by stirring and filtering to analyze the amount of solids. The obtained polymer was dried overnight in a 65 ° C vacuum oven. The results of the Examples and Comparative Examples are summarized in the table below.
【표 11 Table 11
상기 표 1을 참조하면, 본원 발명의 실시예의 경우, 비교예에 비해, HAO(higher alpha 이 efin)의 선택도가 향상된 것을 확인할 수 있으며, 또한, 고형 알파-올레핀인 PE Wax의 함량이 감소한 것을 확인할 수 있다. Referring to Table 1, in the case of the embodiment of the present invention, compared to the comparative example, it can be seen that the selectivity of HAO (higher alpha is efin) is improved, and also, the content of PE Wax, which is a solid alpha-olefin, is reduced. You can check it.
즉, 본원 발명에서와 같이, 특정 구조를 가진 리간드 화합물의 다이포스핀 그룹에 별도의 치환기로 치환된 아릴기를 포함시킬 경우에는 을리고머화 반응에서 알파-올레핀 (1-핵센 및 1-옥텐)에 대한 선택도를 향상시킬 수 있고, 바람직하지 않은 이성질체 형태의 알파-을레핀 및 고형 알파-올레핀인 PE Wax의 양을 저감시킬 수 있는 것을 확인할 수 있다.
That is, as in the present invention, when the diphosphine group of the ligand compound having a specific structure includes an aryl group substituted with a separate substituent, alpha-olefins (1-nuxene and 1-octene) in the ligomerization reaction are included. It can be seen that the selectivity can be improved, and the amount of PE Wax, which is alpha-olepin and solid alpha-olefin in the form of undesirable isomers, can be reduced.