WO2009141458A1 - Antibody specific for propionylated/butyrylated lysine, method for obtaining same and uses thereof - Google Patents
Antibody specific for propionylated/butyrylated lysine, method for obtaining same and uses thereof Download PDFInfo
- Publication number
- WO2009141458A1 WO2009141458A1 PCT/EP2009/056334 EP2009056334W WO2009141458A1 WO 2009141458 A1 WO2009141458 A1 WO 2009141458A1 EP 2009056334 W EP2009056334 W EP 2009056334W WO 2009141458 A1 WO2009141458 A1 WO 2009141458A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- antibodies
- formula
- epitope
- dilution
- equal
- Prior art date
Links
- 0 *C(C(CNC(*)=O)N(*)*)=O Chemical compound *C(C(CNC(*)=O)N(*)*)=O 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/44—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material not provided for elsewhere, e.g. haptens, metals, DNA, RNA, amino acids
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6803—General methods of protein analysis not limited to specific proteins or families of proteins
- G01N33/6806—Determination of free amino acids
- G01N33/6812—Assays for specific amino acids
Definitions
- PROPIONYLE / BUTYRYLEE LYSINE-SPECIFIC ANTIBODY METHOD FOR PRODUCING THE SAME, AND APPLICATIONS THEREOF
- the present invention relates to the field of protein modifications called post-translational modifications and in particular the domain of acyl radical-bearing proteins. More specifically, the invention relates to novel antibodies specific for these acyl radical-bearing proteins (in particular propionyl and butyryl radicals) as well as to their method of production and their applications.
- acyl radical-bearing proteins in particular propionyl and butyryl radicals
- the main objective of the invention is to provide means and methods for detecting said post-translational modifications that are more appropriate, faster and more reliable than the means used in the prior art, and consequently to make it possible to elucidate the mechanisms and to improve the diagnosis, treatment, monitoring and prognosis of diseases induced by these two post-translational modifications (propionylation and / or butyrylation of lysines).
- Another object of the present invention is to provide compositions comprising this more appropriate detection means for use in diagnosis, therapy and research.
- Another objective of the present invention is to provide economical, high-performance, reliable and feasible diagnostic methods simply in vitro or in vivo thanks to, on the one hand, a method and a kit for detecting, in a biological sample, molecules comprising said post-translational modifications (propionylation and / or butyrylation) and secondly a method and a kit for detecting, in a biological sample, autoantibodies directed against said post-translational modifications, in vitro or in vivo.
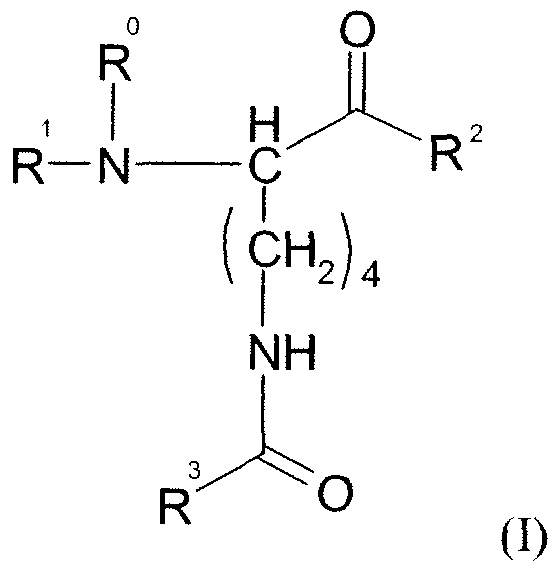
- R is H, alkyl, aryl, alkylaryl or aralkyl
- R 1 is H, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide or an entity consisting of at least one amino acid unit, said amino acid unit being attached to the lysyl unit by a peptide bond
- R 2 is OH, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide, an entity consisting of at least one amino acid unit, said amino acid unit being attached to the lysyl unit by a peptide bond, or OR where R 4 is an alkyl, an aryl, a sugar, a lipid,
- R 3 is equivalent to - (CHi) n -CH 3 where n is 1 or 2.
- These antibodies are not specific for an epitope containing at least one lysyl unit of formula (I) in which R 0, R 1 , R 2 are as defined above and R 3 is equivalent to -CH 3 .
- the present invention also relates to a process for the production of said antibodies or of one of their functional fragments consisting, in the first place, of manufacturing a synthon of formula (I) above, and then to using this synthon as an epitope antigenic to allow the production of antibodies by at least one injection of at least this epitope to an appropriate animal.
- the present invention also relates to a composition
- a composition comprising antibodies or functional fragments of the antibodies according to the present invention, said composition being able to be used in at least one of the following applications: research, diagnosis, analysis, prognosis of pathology, therapeutic, test of efficacy or toxicity of a drug.
- the present invention also relates to a method and a kit for detecting molecules containing at least the epitope of formula (I), in a biological sample, in vitro or in vivo.
- the present invention also relates to a method and a kit for detecting autoantibodies against the epitope of formula (I) in a biological sample or in vivo.
- R 0 is H, alkyl, aryl, alkylaryl or aralkyl
- R 1 is H, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide or an entity consisting of at least one amino acid unit, said amino acid unit being attached to the lysyl unit by a peptide bond,
- R is OH, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide, an entity consisting of at least one amino acid unit, said amino acid unit being attached to the lysyl unit through a linkage peptide, or OR 4 where R 4 is an alkyl, an aryl, a sugar, a lipid,
- R 3 is equivalent to - (CH 2 ) U -CH 3 where n is 1 or 2.
- the invention also relates to isolated antibodies or at least one of their functional fragments, as defined above, characterized in that they are little or not specific for an epitope containing at least one lysyl unit of formula ( I) wherein R 0 , R, R 2 are as defined above and R 3 is equivalent to -CH 3 .
- the term "antibody” designates, for example, immunoglobulins (Ig) for example of the gamma (IgG) or Mu (IgM) type, preferably IgG.
- IgG immunoglobulins
- IgM immunoglobulins
- These antibodies may be polyclonal or monoclonal. They are derived from immunization of animals such as the rabbit, the mouse and all the animals that can be immunized and known to those skilled in the art, but they can be produced by genetic engineering.
- the antibodies according to the invention may be naturally occurring or humanized animal (preferably murine) antibodies.
- the antibodies according to the present invention may be functional and specific fragments of said antibodies such as the Fab fragment which contains the antigen-specific recognition site or the F (ab ') 2 fragment which contains at least the two sites of the antigen-specific recognition site.
- specific antigen recognition By “specific” is meant for example that the antibodies are capable of recognizing and binding to a given epitope, namely the epitope comprising at least one lysyl unit of formula (I), via their paratope according to the known principles of immunology.
- the antibodies according to the present invention are, for example, capable of recognizing and binding to an epitope comprising at least one lysylpropionyl or butyrylated unit but are not suitable, for example, for recognizing and binding specifically to an epitope comprising at least one minus an acetylated lysyl motif.
- the recognized antigen is defined by its particular epitope and this according to the structure or the conformation thereof.
- the term "epitope" designates for example a molecule or a region thereof which can be recognized by the specific recognition part of an antibody (the paratope).
- An antigen is characterized by its epitopes.
- peptide forming the epitope for the generation of specific antibodies according to the invention, is meant for example a peptide comprising at least one lysyl unit substituted by a propionyl and / or butyryl radical, and more specifically a peptide sequence comprising between 2 and 50 amino acids, at least one of the amino acids being a lysyl unit substituted with a propionyl and / or butyryl radical.
- a peptide sequence of 2 to 25 amino acids and most preferably 2 to 15 amino acids will be preferred.
- protein forming the epitope for the generation of specific antibodies according to the present invention is meant for example an immunogenic protein comprising at least one lysyl unit substituted with a propionyl and / or butyryl radical, and more specifically a higher peptide sequence. at least 50 amino acids, at least one of said amino acids being a lysyl unit substituted with a propionyl and / or butyryl radical.
- said protein has a molecular weight of 5 kDaltons to 100 kDaltons and more particularly a molecular weight between 5 to 20 kDa.
- proteins such as p53 or histones, and more particularly histones H3, H4, H2A and H2B, may be mentioned.
- the human H3 histone with a molecular weight of approximately 15 kDa, may be propionylated and / or butyrylated on the lysines at the 4, 9, 14, 18, 23, and generally on at least one lysine (represented by K).
- Mention may also be made of human H4 histone with a molecular weight of about 11 kDa, of which at least one lysine at position 5, 8, 12, 16, 20 may be propionylated and / or butyrylated.
- human H2B histone of molecular weight of about 14 kDa can be propionylated and / or butyrylated on lysines at position 5, 1 1, 12, 15, 16, .. as well as human histone H2A of weight molecular weight of about 14 kDa can be propionylated and / or butyrylated on lysines 5, 9, 13, 15, ..
- propionylated and / or butyrylated lysines correspond to the formula (I) above and may thus represent antigens inducing the formation and specific recognition of the antibodies according to the invention.
- the radical R 0 of the epitope recognized by the antibody is an H.
- R 0 is an alkyl chosen from linear, branched or cyclic alkyls, substituted or not by a heteroatom and having from 1 to 20 carbon atoms.
- R 0 is an aryl chosen from aryls which may or may not be substituted by a heteroatom and which has 3 to 20 carbon atoms.
- R 0 may also be an aralkyl substituted or not with a heteroatom and having 4 to 20 carbon atoms, an alkylaryl substituted or not with a heteroatom and having 4 to 20 carbon atoms.
- the radical R 1 of the epitope recognized by the antibody is an H.
- R 1 is an alkyl chosen from linear, branched or cyclic alkyls, substituted or unsubstituted by a heteroatom and comprising from 1 to 20 carbon atoms.
- R 1 is an aryl selected from aryls substituted or not with a heteroatom and having 3 to 20 carbon atoms.
- R 1 may also be an aralkyl substituted or not with a heteroatom and having 4 to 20 carbon atoms, an alkylaryl substituted or not with a heteroatom and having 4 to 20 carbon atoms.
- R 1 is a sugar chosen from the saccharide, monosaccharide, disaccharide (sucrose, maltose eg) or hydrogenated polysaccharide or not, and their mixtures.
- R 1 is a lipid chosen from fatty acids, their derivatives and their esters.
- R 1 may be a nucleotide selected from known nucleotides.
- R 1 is an entity consisting of at least one amino acid which, via its C-terminal end, forms a peptide bond with the lysyl motif. It may thus be, for example, a simple amino acid, a peptide, preferably a peptide contained in the sequence of a histone and more particularly the histones H3, H4 or H2A, of a protein, preferably a histone protein and more particularly the histones H3, H4 or H2A, a glycoprotein, a lipoprotein ...
- the amino acid involved in the peptide bond with the lysyl motif is any amino acid selected from the 22 known amino acids. At least one amino acid is a natural or unnatural amino acid, D or L.
- the radical R 2 of the epitope recognized by the antibody is an OH.
- R is an alkyl chosen from linear, branched or cyclic alkyls, substituted or not by a heteroatom and having from 1 to 1 to 20 carbon atoms.
- R is an aryl chosen from heteroatom-substituted and non-substituted aryls having 3 to 20 carbon atoms.
- R 2 may also be an aralkyl substituted or not with a heteroatom and having 4 to 20 carbon atoms, an alkylaryl substituted or not with a heteroatom and having 4 to 20 carbon atoms.
- R is a sugar chosen from the saccharide, monosaccharide, disaccharide (sucrose, maltose e.g.) or hydrogenated polysaccharide or not, and their mixtures.
- R is a lipid chosen from fatty acids, their derivatives and their esters.
- R may be a nucleotide selected from known nucleotides.
- R is an entity consisting of at least one amino acid which, via its N-terminus, forms a peptide bond with the lysyl motif. It may thus be, for example, a simple amino acid, a peptide, preferably a peptide contained in the sequence of a histone and more particularly the histones H3, H4, H2A or H2B, of a protein, preferably a histone protein and more particularly the histones H3, H4, H2A or H2B, of a glycoprotein ....
- the amino acid involved in the peptide bond with the lysyl unit is any amino acid selected from the 22 known amino acids of which at least one amino acid is a natural or non-natural amino acid, D or L.
- R is equivalent to OR 4 where R 4 is an alkyl, an aryl, a sugar, a lipid as defined and / or exemplified above.
- the epitope contains at least one propionyl or butyrylated site.
- the radical R 3 of the epitope recognized by the antibody according to the invention is a - (CH 2 ) H -CH 3 radical where n is 1 or 2.
- n 1, the lysyl unit is substituted with a propionic acid.
- the epitope of formula (I) according to the present invention contains a lysyl propionyl unit.
- n corresponds to 2
- the lysyl unit is substituted by a butyric acid (or, by convention, a butyryl) thus forming an epitope of formula (I) containing a lysyl butyryl unit.
- the epitope may consist of a molecule made of at least two amino acids, one of which is a propionylated or butyrylated lysine, a peptide such as the N-terminal sequence of histones, a protein such as a histone, a glycoprotein or any other molecule containing at least one lysyl motif substituted with R 3 as defined above.
- These proteins can be natural, cellular, tissue or plasma proteins, or artificially produced proteins, recombinant proteins produced by genetic engineering. They are preferably histone proteins and especially histones H3, H4, H2A and H2B.
- the epitope of formula (I) corresponds to a polypeptide of one hundred amino acids.
- R 0 is H and R 1 and R 2 are any of the same or different amino acids.
- R 3 is other than - (CH 1 ) n -CH 3 where n is 1 or 2, the antibodies according to the invention do not bind to the molecule specifically. This is particularly the case when R is acetyl.
- lysine-rich peptides are used to generate the antibody.
- an antigenic site generally contains 5 to 20 amino acids, but according to a preferred embodiment of the invention, the specific antigenic epitope recognized by the antibody may contain a lower number of acids. amino, that is to say a single amino acid, lysine substituted by a propionyl or butyryl itself, at 5 amino acids without being limited to this number. Indeed, the epitope may contain up to 10 amino acids and preferably 5 amino acids.
- the lysyl unit substituted with a propionyl or butyryl radical is placed as centrally as possible within said antigenic site generating the antibody according to the invention.
- the peptide or protein comprising an epitope of formula (I) contains several propionylated and / or butyrylated lysines. These peptides are made by conventional peptide synthesis methods known to those skilled in the art.
- the antibody tool according to the present invention allows a qualitative but also quantitative detection of molecules bearing the epitope of formula (I) in biological samples, in vitro and in vivo.
- the antibodies according to the present invention may be present in vivo and generated either: - naturally in the body, during pathological processes, it is then the autoantibodies exposed below, - artificially, that is to say by activation of the immune system of a given organism via the introduction of an antigen comprising said epitope of formula (I).
- the organism produces antibodies specific for the epitope, recognized as non-self.
- this immunoreactivity is reflected by a T test for measuring the immunoreactivity of sera containing the epitopes (i) and / or (ii) and / or (iii).
- This test T is defined eg as follows: adsorbing, on a 96-well polystyrene plate (EIA / RIA, High Binding, Corning Costar), 100 ⁇ l per well of an antigen solution (BSA-propionylated, butyrylated BSA, acetylated BSA) at 10 ⁇ g / ml in buffer 0.1 M bicarbonate pH 9.5,
- the T test is an ELISA test.
- the present invention also covers the antibodies or at least one of their functional fragments specific for an epitope containing at least one lysyl unit of formula (I) as defined above, characterized in that their immunoreactivity for BSA antigens -propionylated or BSA-butyrylated, measured in a test T defined above, is such that it meets at least one of the following characteristics: for a dilution of the serum containing said antibodies to 1/500, the OD at 450 nm is > 1, preferably is> 1.5; for dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is> 0.5, preferably is> 0.9; for a dilution of the serum containing said antibodies at 1/2000, the OD at 450 nm is
- 0.5 preferably is> 0.6;
- the OD at 450 nm is> 0.2, preferably is>0.3; for dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is> 0.2, preferably> 0.25.
- the present invention also relates to antibodies or at least one of their functional fragments as defined above, characterized
- the OD at 450 nm is greater than or equal to, in ascending order preferably 0.6; 0.8; 1.0; 1.5; 2.0;
- the OD at 450 nm is greater than or equal to, in increasing order of preference: 0.3; 0.6; 0.8; 1.0; 1.5; 2.0; 2.2;
- the OD at 450 nm is greater than or equal to, in ascending order preferably: 0.25; 0.4; 0.6; 1.0; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is greater than or equal to, in ascending order preferably: 0.2; 0.4; 0.6; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is greater than or equal to, in ascending order preferably: 0.2; 0.4; 0.6; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is greater than or equal to, in ascending order
- the OD at 450 nm is less than or equal to, in ascending order preferably: 1.2; 1.0; 0.9; 0.8; 0.5;
- the OD at 450 nm is less than or equal to, in increasing order of preference: 1.0; 0.8; 0.6; 0.5; 0.4;
- the OD at 450 nm is less than or equal to, in increasing order of preference: 0.8; 0.6; 0.7; 0.5; 0.3; 0.2; for dilution of the serum containing said antibodies to 1/8000, the OD at 450 nm is less than or equal to, in ascending order preferably: 0.7, 0.6; 0.5; 0.4; 0.25;
- the present invention relates to antibodies or at least one of their functional fragments as defined above, characterized
- the OD at 450 nm is greater than or equal to, in increasing order of preference: 0.2; 0.4; 0.6; 1.0; 1.5; for dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.16; 0.4; 0.6; 0.9; for a dilution of the serum containing said antibodies at 1/2000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.14; 0.3; 0.5; 0.6; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.1; 0.15; 0.2; 0.3; for dilution of the
- the OD at 450 nm is less than or equal to, in ascending order preferably 0.6; 0.5; 0.4; 0.3; 0.15; 0.1.
- the present invention relates to an antibody as defined above, characterized in that in a T test, its immunoreactivity with respect to the BSA-acetylated (BA) or the propionylated BSA (BP) is such that the measurement of OD at 450 nm corresponds to one of the following characteristics:
- the present invention relates to an antibody as defined above, characterized in that in a T test, its immunoreactivity with BSA-acetylated (BA) or butyrylated BSA (BB) is such that the measurement of the OD at 450 nm corresponds to one of the following characteristics:
- residues of the epitope of the formula (I), namely R 0 , R 1 , R 2 and R 3 , are grafted to the lysyl residue either naturally, for example in vivo, or artificially in vitro by simple reaction of the residues or molecules together or by forced reactions known to those skilled in the art.
- the present invention thus relates to a method of manufacturing the antibodies or their functional fragments as defined above, characterized in that it consists in: a) implementing a synthon of formula (I), b) coupling said synthon to a carrier molecule, c) recovering plasma / serum from said animal to which the synthon-carrier molecule cut has been previously injected, d) selecting the specific antibodies of said synthon used in step a) using one or more epitopes of formula (I) as defined above, e) optionally purifying the antibodies by the known methods of skilled in the art.
- the synthon corresponds to the formula (I). More precisely, said synthon corresponds to at least one substituted amino acid: a propionylated lysine or a butyrylated lysine.
- the synthon according to the present invention and as defined above is made by the method described by M. Bashir Uddin Surfraz et al in J. Med. Chem. 2007, 50, 1418-1422 and by Takeshi M. et al in Biomacromolecules, 2007, 8, 318-321.
- Such a synthon is particularly interesting in the production of the antibodies according to the invention and particularly in the production of the antigen constituted by said synthon or comprising it.
- the synthon produced and is coupled directly to a carrier protein, or inserted into a peptide sequence it can be used in the manufacture of specific antibodies directed against it or stored, preferably frozen at -20 ° C. for later use.
- the term “coupled” is meant for example bound or conjugated. This binding or conjugation can be done chemically, for example by a covalent bond, adsorption or another method of attachment known to those skilled in the art.
- the coupling is done by a coupling agent such as cardodiimide or glutaraldehyde.
- the carrier molecule to which the synthon is coupled is a molecule of molecular weight large enough to induce an immune reaction and the production of circulating antibodies.
- This molecule can be a protein, a polypeptide, a natural or synthetic polymer. It is preferably a protein and in particular a protein of molecular weight greater than or equal to 5 kDaltons such as albumin or keyhole limpet hemocyanin (KLH for Keyhole Limpet Haemocyanin). In a preferred form of the invention, KLH is used as the carrier protein.
- the synthon-carrier molecule pair is injected into an animal to be immunized. It is preferably in suspension and mixed with a solution of Freund's adjuvant (complete or incomplete).
- the animal to which is injected said synthon-carrier molecule in suspension can be the rabbit, the mouse, the rat, the goat, the sheep, the horse or the guinea pig, preferably the rabbit, the rat and the mouse.
- the injection of said pair can be done in one or more times according to conventional and known methods of immunization.
- the main routes of administration are subcutaneous, intradermal, or intramuscular injections; intravenous and intraperitoneal injections are only used in special cases.
- the types of antibodies produced, specific to the synthon are different. Indeed, it may be type G or M immunoglobulins.
- approximately 1 ml of said antigenic couple is injected intramuscularly into a rabbit and about 100 ⁇ l into a mouse.
- the concentration of synthon in the injection mixture is about 50 ⁇ g / ml.
- the blood of the animal containing, among others, said antibodies specific for the injected synthon is recovered by sampling or by exsanguination.
- plasma or serum also containing, inter alia, antibodies specific for the synthon as defined above.
- the serum containing the desired antibodies, directed against said synthon normally contains several different antibody species directed against several epitopes of the same antigen, this polyclonal preparation is called.
- Techniques can also be employed to isolate and clone lymphocytes that produce only one molecular species (i.e. clonotype) of antibodies: antibodies that recognize only a single epitope of the antigen.
- the step of selecting antibodies specific for said synthon as defined above is done using the ELISA (Enzyme-Linked Immuno Sorbent Assay) technique.
- This selection technique is widely described in the literature. To summarize, this principle known to those skilled in the art, is carried out as follows: the synthon described above or an epitope of formula (I) is attached to a carrier conventionally used in ELISA techniques at least a washing is carried out, the plasma or serum of the animal which has been immunized is added to the support, at least one washing is carried out, a solution containing antibodies, preferably of goat or sheep, specifically antibodies derived from the animal having been immunized, preferably rabbit, rat or mouse, said added antibodies being coupled to a molecule useful for their detection, preferably a substrate-degrading enzyme such as TMB degrading peroxidase or DAB at least one wash is carried out, the substrate of the molecule useful for detection (TMB or DAB) is added, the optical density is read, indicating the presence of the desired antibodies, and selected
- the propionylated and / or butyrylated BSA as defined in the present application is preferably used but the synthon as defined above coupled to a carrier protein or a peptide containing at least one lysylpropionylated unit and / or butyryl coupled to a carrier protein may also be used.
- the latter may be made in the liquid or solid phase and in different ways namely affinity chromatography using either separation columns, magnetic beads or resins bearing said synthon in as a ligand.
- a solid support such as a sepharose column on which the synthons have been attached is preferably preferred, preferably by covalent bonding.
- the present invention also relates to isolated antibodies or at least one of the functional fragments thereof, characterized in that they are obtained from an antigen consisting of a synthon of formula (I) in which R 0 equals at H, alkyl, aryl, alkylaryl or aralkyl, R 1 is H, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide, R is OH, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide or OR 4 wherein R 4 is alkyl, aryl, sugar, lipid, R is - (CH 2 ) H -CH 3 where n is 1 or 2.
- R 0 equals at H, alkyl, aryl, alkylaryl or aralkyl
- R 1 is H, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide
- R is OH,
- the antibodies according to the present invention are specific for their epitope directly after their production, without requiring the use of other techniques such as the depletion of polyclonal antibodies to obtain their high specificity vis- with respect to propionylated or butyrylated lysines. This presents a major advantage.
- the invention also relates to a method for manufacturing the antibodies or a functional fragment thereof as defined above, characterized in that it consists of: a) reacting a molecule of formula CH 3 - (CH 2) n -CO-O-CO- (CH 2 ) n -CH 3 where n is 1 or 2 with a carrier molecule in order to substitute the lysyl units of said carrier molecule, bl) recovering plasma / serum said animal to which said carrier molecule thus substituted has been injected beforehand; cl) selecting the antibodies specific for the substituted lysyl units produced in step a1) using one or more epitopes of formula (I) as defined above; above, dl) optionally purify the antibodies according to conventional methods.
- Step a1 is carried out as follows:
- the carrier molecule preferably BSA or KLH, is reacted with propionic or butyric anhydride, of formula CH 3 - (CH 2 ) H -CO-O-CO- (CHi) n -CH 3 where n is 1 or 2 respectively, so that the lysines of the carrier molecule react to form a molecule containing substituted lysines and more specifically propionylées lysines and / or butyrylées.
- This carrier molecule, the lysines of which are substituted, is used as an immunogen comprising the epitopes of formula (I) described above.
- Steps b1) to d1) are identical to steps c) to e) of the method of manufacturing antibodies or a functional fragment thereof described above.
- the present invention also relates to a method for manufacturing the antibodies, or a functional fragment thereof, as defined above, characterized in that it consists in: a2) implementing an epitope of formula (I) in which at least one of the residues R 0 , R 1 is different from H or R 2 is different from OH, b2) couple said epitope to a carrier molecule, c2) recovering plasma / serum from said animal to which said epitope-carrier molecule pair has has been previously injected, d2) select the specific antibodies of said epitope used in step a) using one or more epitopes as defined in claim 1, e2) optionally purify the antibodies according to conventional methods.
- Steps b2) to e2) are identical to steps b) to e) described above in the method of making antibodies specific to the synthon itself and will therefore not be recalled.
- the implementation of an epitope as defined above is carried out by the production, the extemporaneous manufacture of said epitope or by the use of an epitope corresponding to the formula (I) already synthesized according to known conventional synthetic methods. preferably peptide or protein syntheses.
- the present invention also relates to a composition
- a composition comprising antibodies, or at least one of their functional fragments, as defined above, or obtained according to the process as defined above.
- Said composition may advantageously comprise reagents such as labeled or non-labeled secondary antibodies and revealing or visualization solutions making it possible to demonstrate the antibody-antigen reactions.
- Said composition may also comprise excipients of different types of type conventionally used in compositions containing antibodies.
- composition just like the antibodies according to the invention, can advantageously be used in the field of research, to explain biological phenomena and to test the efficacy of said antibodies or of the composition as defined above.
- this composition comprising at least antibodies specific for the epitope of formula (I) exposed above, can be used in at least one of the following applications: research, diagnosis, analysis, prognosis of pathology, therapeutic, test for efficacy or toxicity of a drug.
- pathologies related to the propionylation and / or butyrylation of lysine residues there may be mentioned, for example, cancer, neurodegenerative diseases, diabetes and inflammatory pathologies.
- the present invention relates to a method for detecting, in a biological sample, in vitro or in vivo, the epitope of formula (I) as defined above, characterized in that it comprises the steps following: A) optionally fix on a suitable support the antibodies or at least one of their functional fragments as defined above or included in a composition as defined above,
- the antibodies according to the present invention are fixed on a substantially solid support or any reaction support making it possible to carry out an immunological test.
- the attachment to the support is preferably carried out by adsorption or covalent bonding.
- a possible washing step makes it possible to eliminate, after said fixation, the antibodies not fixed to said support, if appropriate.
- the biological sample concerned, to be used with the antibodies according to the invention may be any substance capable of containing said epitope in question of formula (I) such as a solid or liquid substance, such as for example an animal, a complete organ or not, tissue cells, nuclear extracts of given cells, cytoplasmic extracts of given cells, blood, plasma, serum, lymph, urine, saliva.
- serum is used.
- the sample contains molecules containing at least one substituted lysyl unit corresponding to formula (I) and constituting an epitope
- these molecules via this epitope will bind specifically to the antibodies previously fixed on a suitable support.
- a possible wash will eliminate non-fixed antibodies to the support and non-specific antibody-molecule complexes.
- the specific antibody may be used in the liquid phase, in solution.
- the immunological reaction supports used may be of a different nature and are chosen from: slides, microplates, fluorescent latices, and latices. Magnetic membranes, immuno-filtration membranes or immuno-migration membranes, biochips, beads, fins, tubes but also liposomes, lipid vesicles, biological microparticles or obtained from polymers, emulsions ....
- step D) can be divided into several technologies such as ELISA, immunoturbidimetry, slide agglutination, nephelometry, turbidimetry, turbidimetry or latex particle amplified nephelometry, immunofluorescence (on slide, microplate, fluorescent latex, magnetic latex, test, on membrane, biochips etc .. and in general can be used any method for identifying and / or quantifying a reaction between an antigen and more particularly an epitope and an antibody, whatever the isotype.
- technologies such as ELISA, immunoturbidimetry, slide agglutination, nephelometry, turbidimetry, turbidimetry or latex particle amplified nephelometry, immunofluorescence (on slide, microplate, fluorescent latex, magnetic latex, test, on membrane, biochips etc .. and in general can be used any method for identifying and / or quantifying a reaction between an antigen and more particularly
- the immunological reaction namely the recognition of the antibody or at least one of its functional fragments according to the invention with the epitope of formula (I)
- an indicator reaction which allows the photometric detection of the enzymatic activity linked to the antibody-epitope complex of formula (I).
- the present invention also relates to a detection kit, in a biological sample in vitro or in vivo, of a molecule containing at least the epitope of formula (I) as defined above, characterized in that it comprises: at least an antibody or at least one of its functional fragments as defined above, preferably fixed on a support and the appropriate material and necessary to detect the antibody-epitope complexes of formula (I).
- This kit makes it possible to quickly and reliably detect the presence or absence of a molecule comprising at least one epitope of formula (I)
- the present invention is an antibody directed against an epitope of formula (I) as defined above.
- These autoantibodies thus induce autoimmune pathologies and it may prove to be very important to be able to rapidly diagnose the presence or absence of autoantibodies in vivo in a patient, to be able to perform an analysis, preferably a serological follow-up. and a prognosis for pathologies.
- the invention therefore also relates to a method for detecting specific autoantibodies of the epitopes of formula (I) as defined above, in a biological sample in vitro or in vivo, preferably a plasma or a serum, characterized in that what it includes the following steps:
- the support is solid but it may be any reaction support for performing an immunological test.
- the epitope of formula (I) is attached to a suitable support. As stated above, preferably the attachment is by adsorption but it can also be performed by co val valent bond on a suitable support. It will be ensured that the amount of fixed epitope of formula (I) is not a limiting factor so that all the autoantibodies of the sample to be tested can thus be specifically attached thereto.
- the biological sample to be tested may be any biological substance capable of containing said epitope-specific autoantibodies (I) such as cells of the tissues, blood, plasma, serum, urine and saliva.
- the sample to be tested is plasma or serum, diluted or not, of a patient potentially containing autoantibodies directed against the epitope of formula (I).
- the possible washes are intended to eliminate on the one hand the epitopes not fixed on the support, but also and especially to eliminate the free autoantibodies or non-specifically fixed to their specific epitope.
- the different detection methods used are qualitative and / or quantitative. These methods for detecting autoantibody-epitope complexes are known to those skilled in the art. They can be broken down into several technologies such as those set out above for the process and the kit for detecting epitopes of formula (1).
- the present invention also relates to a kit for detecting autoantibodies specific for the epitopes of formula (I) as defined above, in a biological sample in vitro or in vivo, preferably a plasma or a serum, characterized in that that he understands:
- said auto-antibody detection kit it is thus simpler, easier and faster to establish a diagnosis of possible pathologies induced by lysines substituted with a propionyl or butyryl residue, to carry out monitoring and analysis of the pathology and especially the serology of the patient to monitor, evaluate the efficacy and toxicity of a drug or a composition targeting for example these autoantibodies or use these autoantibodies in research.
- FIG. 1 shows two titration curves of rabbit anti-lysine propionylated serum.
- Figure 2 shows two titration curves of rabbit anti-lysine butyrylated serum.
- FIG. 3 represents a photograph of a Western blot analysis of the acetylation reaction of histones H3 and H4 revealed by means of anti-acetyl antibodies.
- FIG. 4 represents a photograph of a western blot analysis of the propionylation reaction of the H3 and H4 histones revealed by the antibodies that are the subject of the invention.
- FIG. 5 represents a photograph of a western blot analysis of the propionylation reaction of histones H3 and H4 in the presence or absence of various co-factors and revealed by means of the antibodies which are the subject of the invention.
- FIG. 6 represents a photograph of a Western blot analysis of the detection of the natural propionylation of H2A histones revealed by the antibodies that are the subject of the invention.
- step a1 Preparation of epitopes of formula (I) (step a1) for the production of immunogens and antigens.
- propionylated KLH and butyrylated KLH antigens were prepared as follows:
- Propionylated KLH 2 mg of KLH solubilized in 1 ml of 0.1 M bicarbonate buffer pH 9.5 were brought into contact with 0.7 mmol of propionic anhydride (CH 3 - (CHa) -CO-O-
- propionylated BSA protein BP
- propionylated KHL propionylated KHL
- butyrylated BSA protein BB
- Table 1 Degree of acylation of proteins by spectrophotometric assay of primary amines.
- Table 1 shows that for the 2 synthesized antigens (propionylated BSA and butyrylated BSA), the acylation is almost complete, it follows that almost all of the accessible ⁇ NH 2 groups of lysine present on the BSA are acylated.
- the antibodies specific for the substituted lysyl units were selected in the serum with the epitope of formula (I) produced above by determining the immunoreactivity of the rabbit serum by the ELISA technique (step c1).
- BP or BB antigens are adsorbed on 96-well polystyrene plates.
- 100 ⁇ l of a solution 10 ⁇ g / ml of each antigen in 0.1 M bicarbonate buffer pH 9.5 are distributed per well.
- the wells are emptied and a deposit of 150 ⁇ l / well of a 0.5% BSA solution in PBS buffer is prepared in order to saturate the excess adsorption sites on the surface. plastic.
- This saturation step requires an incubation of one hour at 37 ° C. At this stage, the plates are ready for the deposition of the sera.
- the sera are used starting from the 1/500 dilution in PBS buffer containing 0.1% tween-20. These solutions are deposited and then diluted two by two directly on the plate (1/500, 1/1000, 1/2000 ...) so as to obtain 100 ⁇ l / well of final volume.
- the immuno-purification steps of the antibodies are carried out according to the protocols described in the publication Thomas V et al in J. Immunol Methods. 2004 Sep; 292 (1-2): 83-95.
- Table 2 Optical density measurements according to the dilutions of the sera. Table 2 reflects the immunoreactivity of rabbit sera containing antibodies specific for propionylated and / or butyrylated lysines, vis-à-vis acetylated BSA and propionylated BSA. Propionylated BSA forms a complex with antibodies specific for propionylated lysine (high absorbance).
- Figure 1 illustrates the immunoreactivity of sera against two antigens: acetylated BSA and propionylated BSA.
- the ordinate axis represents optical density values measured at 450 nm and the x-axis represents the different dilutions of the serum.
- This figure 1 illustrates that the sera contain antibodies specific for propionylated lysines.
- the antibodies obtained and contained in the serum react strongly with the lysylpropionyl unit contained in the BP antigen (absorbance of 1.647 at the 1/2000 dilution of the serum), whereas they do not react or very little with the motif.
- acetylated lysyl contained in BA antigen (absorbance of 0.250 at 1/2000 dilution of serum).
- Table 3 Optical density measurements according to the dilutions of the sera. Table 3 reflects the immunoreactivity of rabbit sera containing antibodies specific for propionylated and / or butyrylated lysines against acetylated BSA and butyrylated BSA. Butyrylated BSA forms a complex with antibodies specific for butyrylated lysine (high absorbance).
- Figure 2 illustrates the immunoreactivity of sera against two antigens: acetylated BSA and butyrylated BSA.
- the ordinate axis represents optical density values measured at 450 nm and the x-axis represents the different dilutions of the serum.
- This figure 2 illustrates that the sera contain antibodies specific for butyrylated lysines.
- the antibodies obtained and contained in the serum react with the lysyl butyryl unit contained in the BB antigen (absorbance of 1.558 at the 1/500 dilution of the serum) whereas they do not react with the acetylated lysyl motif contained in BA antigen (absorbance of 0.158 at 1/500 dilution of serum).
- These antibodies make it possible to differentiate N- ⁇ -butyryl-L-Lysine from N- ⁇ -acetyl-L-lysine and are therefore highly specific for butyrylated lysines.
- the synthon is obtained according to the methods described by M. Bashir Uddin Surfraz et al in J. Med. Chem. 2007, 50, 1418-1422 and by Takeshi M. et al in Biomacromolecules, 2007, 8, 318-321.
- HL60 cells were incubated with 1.5 ⁇ M Trichostatin A (TSA) a histone deacetylase inhibitor for 5 hours. The cells are then washed 3 times with PBS buffer and centrifuged at 13,000 g. The cell pellet is then resuspended in IPH buffer (50mM Tris pH 8, 15OmM NaCl, 5mM EDTA, 5% NP-40, 1.5uM TSA) and the suspension is left for 15 min at 4 ° C. The tubes are then centrifuged at 13,000 g for 10 min. The chromatin pellet is then taken up in the electrophoresis buffer as described previously to carry out the western blot.
- TSA Trichostatin A
- FIG. 3 illustrates the acetylation reaction of the histones H3 and H4 of the HL60 cells by the Histone Acetyl Transferases HATs (P / CAF & CBP) in the presence (+) or not (-) of the TSA inhibitor.
- the revelation is carried out with the anti-acetyl lysine monoclonal antibody (mab0019).
- the control reaction to verify the model of posttranslational histone modification in vitro clearly shows significant acetylation of H3 and H4 histones.
- the addition of TSA exerts an inhibitory effect on the HDAC enzyme since the intensity of labeling is greater.
- FIG. 4 illustrates the propionylation reaction of the histones H3 and H4 of the HL60 cells by the histones acetyl transferases HATs (P / CAF & CBP) in the presence (+) or not (-) of the TSA inhibitor.
- HATs P / CAF & CBP
- the revelation is carried out with the polyclonal rabbit anti-lysine propionylated antibody (object of the invention).
- HATs P / CAF & CBP
- acetyl-CoA Ac
- propionyl-CoA Pr
- butyryl-CoA Bu
- cofactor -
- the revelation is carried out with the polyclonal rabbit anti-lysine propionylated antibody (object of the invention).
- Anti-lysine propionylated polyclonal antibodies specifically recognize H3 and H4 histone propionylated by the action of HATs (P / CAF and CBP). There is no cross reaction of anti-lysine propionylated antibodies with acetylated or butyrylated histones.
- FIG. 6 illustrates the detection of naturally propionylated H2A histones of HL60 cells in the (+) or non (-) presence of the TSA inhibitor. The revelation is carried out with the polyclonal rabbit anti-lysine propionylated antibody (object of the invention).
- the polyclonal rabbit anti-lysine propionylated antibody detects a natural propionylation of histone H2A in HL60 cells. Propionylation is slightly affected by the action of HDAC as shown by the result obtained with the addition of TSA.
- the antibodies of the invention can also be used in immunohistochemistry or immunocytology for the detection of epitopes of formula (I) according to the technique described in Roch et al. 1991 May 10; 48 (2): 215-20.
- Example 1.3 The same method described in Example 1.3 above is used to detect autoantibodies in a sample and in particular in a serum.
- BP or BB antigens are adsorbed on 96-well polystyrene plates.
- 100 ⁇ l of a solution 10 ⁇ g / ml of each antigen in 0.1 M bicarbonate buffer pH 9.5 are distributed per well.
- the wells are emptied and a deposit of 150 ⁇ l / well of a solution of 0.5% BSA in PBS buffer is prepared in order to saturate the excess adsorption sites on the surface. plastic. This saturation step requires an incubation of one hour at 37 ° C.
- the plates are ready for depositing the serum to be tested.
- the serum to be tested is a human serum taken and then used at different dilutions in PBS tween 0.1%. This solution is deposited and then diluted two by two directly on the plate (1 / 50.1 / 100, 1/200,) so as to obtain 100 .mu.l / well of final volume. After one hour of incubation at 37 ° C., the plates are washed 3 times with PBS containing 0.1% tween-20. An anti-human IgG (H + L) sheep antibody labeled with peroxidase and deposited at a rate of 100 ⁇ l / well and left for 30 min. at 37 ° C.
- the plates are then washed with 3 successive washes to remove the excess reagent (sheep antibody). Said possible epitope-autoantibody complexes are revealed thanks to the substrate of peroxidase.
- the peroxidase activity is revealed using the hydrogen peroxide / tetramethylbenzidine (TMB) reagent (Covalab).
- TMB hydrogen peroxide / tetramethylbenzidine
- the reaction is stopped with 100 ⁇ l of H 2 SO 4 (2N). The absorbance is measured on a plate reader at 450 nm.
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Genetics & Genomics (AREA)
- Physics & Mathematics (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Cell Biology (AREA)
- Bioinformatics & Computational Biology (AREA)
- Microbiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Food Science & Technology (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
The invention relates to a novel antibody or at least one functional fragment thereof, which is specific, comprising at least one lysyl unit of formula (I), in which R0 is H, an alkyl, an aryl, an alkylaryl or an aralkyl, R1 is H, an alkyl, an aryl, an alkylaryl, an aralkyl, a sugar, a lipid, a nucleotide or an entity comprising at least one amino acid unit, wherein said amino acid unit is linked to the lysyl unit by a peptide bond, R2 is OH, an alkyl, an aryl, an alkylaryl, an aralkyl, a sugar, a lipid, a nucleotide or an entity comprising at least one amino acid unit, wherein said amino acid unit is linked to the lysyl unit by a peptide bond, or OR4 where R4 is an alkyl, an aryl, a sugar or a lipid, and R3 is (CH2)n‑CH3 where n is 1 or 2.
The invention also relates to a method for producing this novel antibody and to a composition containing same. In addition, for uses in research, diagnosis and therapeutics, the invention relates to methods and kits for detection of the epitopes of formula (I) and of autoantibodies which recognize said epitopes of formula (I).
Description
ANTICORPS SPECIFIQUE DE LA LYSINE PROPIONYLEE/BUTYRYLEE, SON PROCEDE D'OBTENTION ET SES APPLICATIONS PROPIONYLE / BUTYRYLEE LYSINE-SPECIFIC ANTIBODY, METHOD FOR PRODUCING THE SAME, AND APPLICATIONS THEREOF
Domaine technique de l'invention :Technical Field of the Invention
La présente invention concerne le domaine des modifications des protéines appelées modifications post-traductionnelles et en particulier, le domaine des protéines portant des radicaux acyles. Plus précisément, l'invention porte sur de nouveaux anticorps spécifiques à ces protéines portant des radicaux acyles (en particulier des radicaux propionyle et butyryle) ainsi que sur leur procédé d'obtention et leurs applications.The present invention relates to the field of protein modifications called post-translational modifications and in particular the domain of acyl radical-bearing proteins. More specifically, the invention relates to novel antibodies specific for these acyl radical-bearing proteins (in particular propionyl and butyryl radicals) as well as to their method of production and their applications.
Art antérieur et problème technique :Prior art and technical problem:
Transcription et traduction sont des mécanismes piliers pour les cellules et les modifications post-transcriptionnelles et post-traductionnelles ont des impacts fondamentaux dans le fonctionnement cellulaire. Les protéines restant à leur état natif et les protéines ayant subi ces modifications chimiques post-traductionnelles montrent de grandes différences tant au niveau de leurs localisations cellulaires, de leurs demi- vies, de leurs propriétés physico-chimiques ainsi que de leurs actions intra ou intercellulaires. Ainsi, la connaissance et la compréhension des mécanismes régulant ces modifications peuvent s'avérer fort intéressantes dans les domaines non seulement de la recherche fondamentale mais aussi et surtout le domaine thérapeutique. Il est donc indispensable pour cela de disposer d'outils maitrisés pour identifier, détecter, localiser voire quantifier et induire ou éviter ces modifications. La demande de brevet US 2008/0241862 (Zhao et al.) décrit des moyens d'identifier les lysines propionylées et butyrylées dans les protéines. Ces moyens d'identification sont des anticorps polyclonaux qui reconnaissent spécifiquement des lysines acétylées et reconnaissent par réaction croisée, des lysines propionylées et des lysines butyrylées du fait de leur structure proche. Des anticorps spécifiques des lysines propionylées ou butyrylées sont obtenus par purification en utilisant des techniques longues et coûteuses d'épuisement. .Transcription and translation are pillar mechanisms for cells and post-transcriptional and post-translational modifications have fundamental impacts in cellular functioning. The proteins remaining in their native state and the proteins having undergone these post-translational chemical modifications show great differences as regards their cell localizations, their half lives, their physico-chemical properties as well as their intra or intercellular actions. . Thus, the knowledge and understanding of the mechanisms regulating these changes can be very interesting in the areas not only of basic research but also and especially the therapeutic field. It is therefore essential for this to have mastered tools to identify, detect, locate and even quantify and induce or avoid these changes. US patent application 2008/0241862 (Zhao et al.) Discloses means for identifying propionylated and butyrylated lysines in proteins. These means of identification are polyclonal antibodies which specifically recognize acetylated lysines and recognize, by cross-reaction, propionylated lysines and butyrylated lysines because of their close structure. Antibodies specific for propionylated or butyrylated lysines are obtained by purification using long and expensive techniques of exhaustion. .
Aussi, il apparait donc nécessaire de fournir des moyens et méthodes de détection mis en œuvre plus facilement et directement, fiables, sensibles, reproductibles et de trouver des outils d'identification/ localisation de ces modifications (propionylation et/ou butyrylation de motif lysyls) permettant également d'améliorer la recherche, le diagnostic, le suivi, le pronostic et le traitement des pathologies y étant associées. Aussi, l'inventeur a-t-il développé des anticorps monoclonaux capables de reconnaître et de se lier spécifiquement
à ces nouvelles modifications protéiques sans avoir à utiliser des techniques de purification (par ex. épuisement) pour obtenir leur spécificité.Also, it therefore appears necessary to provide detection means and methods implemented more easily and directly, reliable, sensitive, reproducible and to find tools for identifying / locating these modifications (propionylation and / or butyrylation of lysyl motif). also improving the research, diagnosis, monitoring, prognosis and treatment of pathologies associated with it. Also, has the inventor developed monoclonal antibodies capable of recognizing and binding specifically to these new protein modifications without having to use purification techniques (eg depletion) to obtain their specificity.
Objectifs principaux de l'invention :Main objectives of the invention:
L'objectif principal de l'invention est de fournir des moyens et des méthodes de détection desdites modifications post-traductionnelles plus appropriés, plus rapides et fiables que les moyens utilisés dans l'art antérieur, et par conséquent de permettre d'élucider les mécanismes biologiques et d'améliorer le diagnostic, le traitement, le suivi et le pronostic de maladies induites par ces deux modifications post-traductionnelles (propionylation et/ou butyrylation des lysines).The main objective of the invention is to provide means and methods for detecting said post-translational modifications that are more appropriate, faster and more reliable than the means used in the prior art, and consequently to make it possible to elucidate the mechanisms and to improve the diagnosis, treatment, monitoring and prognosis of diseases induced by these two post-translational modifications (propionylation and / or butyrylation of lysines).
Un autre objectif de la présente invention est de fournir des compositions comportant ce moyen de détection plus approprié utilisables en diagnostic, thérapie et recherche.Another object of the present invention is to provide compositions comprising this more appropriate detection means for use in diagnosis, therapy and research.
Un autre objectif de la présente invention est de fournir des méthodes de diagnostic économiques, performantes, fiables et réalisables simplement in vitro ou in vivo grâce à, d'une part, un procédé et un nécessaire de détection, dans un échantillon biologique, de molécules comportant lesdites modifications post-traductionnelles (propionylation et/ou butyrylation) et d'autre part un procédé et un nécessaire de détection, dans un échantillon biologique, d'auto-anticorps dirigés contre lesdites modifications post-traductionnelles, in vitro ou in vivo.Another objective of the present invention is to provide economical, high-performance, reliable and feasible diagnostic methods simply in vitro or in vivo thanks to, on the one hand, a method and a kit for detecting, in a biological sample, molecules comprising said post-translational modifications (propionylation and / or butyrylation) and secondly a method and a kit for detecting, in a biological sample, autoantibodies directed against said post-translational modifications, in vitro or in vivo.
Description succincte de l'invention :Brief description of the invention
Ces objectifs, parmi d'autres sont atteints par la présente invention qui concerne tout d'abord de nouveaux anticorps ou au moins l'un de leurs fragments fonctionnels spécifiques d'un épitope contenant au moins un motif lysyl de formule (I) suivante :These objectives, among others, are achieved by the present invention which firstly relates to new antibodies or at least one of their functional fragments specific for an epitope containing at least one lysyl unit of formula (I) below:
dans laquelle R équivaut à H, un alkyle, un aryle, un alkylaryle ou un aralkyle,
R1 équivaut à H, un alkyle, un aryle, un alkylaryle, un aralkyle, un sucre, un lipide, un nucléotide ou une entité constituée d'au moins un motif acide aminé, ledit motif acide aminé étant relié au motif lysyl par une liaison peptidique, in which R is H, alkyl, aryl, alkylaryl or aralkyl, R 1 is H, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide or an entity consisting of at least one amino acid unit, said amino acid unit being attached to the lysyl unit by a peptide bond,
R2 équivaut à OH, un alkyle, un aryle, un alkylaryle, un aralkyle, un sucre, un lipide, un nucléotide, une entité constituée d'au moins un motif acide aminé, ledit motif acide aminé étant relié au motif lysyl par une liaison peptidique, ou OR où R4 est un alkyle, un aryle, un sucre, un lipide,R 2 is OH, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide, an entity consisting of at least one amino acid unit, said amino acid unit being attached to the lysyl unit by a peptide bond, or OR where R 4 is an alkyl, an aryl, a sugar, a lipid,
R3 équivaut à -(CHi)n-CH3 où n vaut 1 ou 2.R 3 is equivalent to - (CHi) n -CH 3 where n is 1 or 2.
Ces anticorps ne sont pas spécifiques d'un épitope contenant au moins un motif lysyl de formule (I) dans laquelle R°, R1, R2 sont tels que définis ci-dessus et R3 équivaut à -CH3.These antibodies are not specific for an epitope containing at least one lysyl unit of formula (I) in which R 0, R 1 , R 2 are as defined above and R 3 is equivalent to -CH 3 .
La présente invention concerne également un procédé de fabrication desdits anticorps ou de l'un de leurs fragments fonctionnels consistant, en premier lieu, à fabriquer un synthon de formule (I) ci-dessus, puis à utiliser ce synthon, en tant qu'épitope antigénique pour permettre la production des anticorps grâce à au moins une injection d'au moins cet épitope à un animal approprié.The present invention also relates to a process for the production of said antibodies or of one of their functional fragments consisting, in the first place, of manufacturing a synthon of formula (I) above, and then to using this synthon as an epitope antigenic to allow the production of antibodies by at least one injection of at least this epitope to an appropriate animal.
La présente invention concerne également une composition comportant des anticorps ou des fragments fonctionnels des anticorps selon la présente invention, ladite composition pouvant être utilisée dans au moins l'une des applications suivantes : recherche, diagnostic, analyse, pronostic de pathologie, thérapeutique, test d'efficacité ou de toxicité d'un médicament.The present invention also relates to a composition comprising antibodies or functional fragments of the antibodies according to the present invention, said composition being able to be used in at least one of the following applications: research, diagnosis, analysis, prognosis of pathology, therapeutic, test of efficacy or toxicity of a drug.
La présente invention concerne également un procédé et un nécessaire de détection des molécules contenant au moins l'épitope de formule (I), dans un échantillon biologique, in vitro ou in vivo.The present invention also relates to a method and a kit for detecting molecules containing at least the epitope of formula (I), in a biological sample, in vitro or in vivo.
La présente invention concerne également un procédé et un nécessaire de détection des autoanticorps dirigés contre l'épitope de formule (I) dans un échantillon biologique ou in vivo.The present invention also relates to a method and a kit for detecting autoantibodies against the epitope of formula (I) in a biological sample or in vivo.
Description détaillée de l'invention :Detailed description of the invention
L'anticorpsantibody
Pour détecter des modifications moléculaires comme les modifications post-traductionnelles in vitro et in vivo, comprendre leurs implications cellulaires et éventuellement avoir un effet sur elles particulièrement dans le cadre thérapeutique de pathologies induites par ces modifications, il est particulièrement intéressant de disposer d'outils spécifiques, aptes à reconnaitre des cibles précises directement. C'est pourquoi, il est du mérite de l'inventeur d'avoir développé des anticorps isolés ou au moins des fragments fonctionnels de ceux-ci,
caractérisés en ce qu'ils sont spécifiques d'un épitope comprenant au moins un motif lysyl de formule (I) suivante :To detect molecular modifications such as post-translational modifications in vitro and in vivo, to understand their cellular implications and possibly to have an effect on them particularly in the therapeutic context of pathologies induced by these modifications, it is particularly interesting to have specific tools , able to recognize specific targets directly. Therefore, it is the merit of the inventor to have developed isolated antibodies or at least functional fragments thereof, characterized in that they are specific for an epitope comprising at least one lysyl unit of the following formula (I):
dans laquelle R0 équivaut à H, un alkyle, un aryle, un alkylaryle ou un aralkyle, wherein R 0 is H, alkyl, aryl, alkylaryl or aralkyl,
R1 équivaut à H, un alkyle, un aryle, un alkylaryle, un aralkyle, un sucre, un lipide, un nucléotide ou une entité constituée d'au moins un motif acide aminé, ledit motif acide aminé étant relié au motif lysyl par une liaison peptidique,R 1 is H, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide or an entity consisting of at least one amino acid unit, said amino acid unit being attached to the lysyl unit by a peptide bond,
R équivaut à OH, un alkyle, un aryle, un alkylaryle, un aralkyle, un sucre, un lipide, un nucléotide, une entité constituée d'au moins un motif acide aminé, ledit motif acide aminé étant relié au motif lysyl par une liaison peptidique, ou OR4 où R4 est un alkyle, un aryle, un sucre, un lipide,R is OH, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide, an entity consisting of at least one amino acid unit, said amino acid unit being attached to the lysyl unit through a linkage peptide, or OR 4 where R 4 is an alkyl, an aryl, a sugar, a lipid,
R3 équivaut à -(CH2)U-CH3 où n vaut 1 ou 2.R 3 is equivalent to - (CH 2 ) U -CH 3 where n is 1 or 2.
L'invention concerne également des anticorps isolés ou au moins l'un de leurs fragments fonctionnels, tel que défini ci-dessus, caractérisés en ce qu'ils sont peu ou pas spécifiques d'un épitope contenant au moins un motif lysyl de formule (I) dans laquelle R0, R , R2 sont tels que définis ci-dessus et R3 équivaut à -CH3.The invention also relates to isolated antibodies or at least one of their functional fragments, as defined above, characterized in that they are little or not specific for an epitope containing at least one lysyl unit of formula ( I) wherein R 0 , R, R 2 are as defined above and R 3 is equivalent to -CH 3 .
Dans la présente demande, le terme «anticorps» désigne par exemple des immunoglobulines (Ig) par exemple de type Gamma (Ig G) ou Mu (Ig M), de préférence IgG. Ces anticorps peuvent être polyclonaux ou monoclonaux. Ils sont issus d'immunisation d'animaux tels que le lapin, la souris et tous les animaux que l'on peut immuniser et connus de l'homme de l'art mais ils peuvent être produits par génie génétique. Par ailleurs, les anticorps selon l'invention peuvent être des anticorps d'origine animale (de préférence murine) naturels ou humanisés. Par extension, les anticorps selon la présente invention peuvent être des fragments fonctionnels et spécifiques desdits anticorps comme le fragment Fab qui contient le site de reconnaissance spécifique à l'antigène ou le fragment F(ab')2 qui contient au moins les deux sites de reconnaissance spécifique à l'antigène.
Par « spécifique », on entend par exemple que les anticorps sont aptes à reconnaitre et à se lier à un épitope donné, à savoir l'épitope comprenant au moins un motif lysyl de formule (I), via leur paratope selon les principes connus de l'immunologie. En particulier, les anticorps selon la présente invention sont par exemple aptes à reconnaitre et se lier à un épitope comprenant au moins un motif lysyl propionylé ou butyrylé mais ne sont pas aptes par exemple à reconnaitre et se lier de manière spécifique à un épitope comprenant au moins un motif lysyl acétylé. En effet, l'antigène reconnu est défini par son épitope particulier et ceci selon la structure ou la conformation de celui-ci. Dans la présente demande, le terme «épitope» désigne par exemple une molécule ou une région de celle-ci qui peut être reconnue par la partie de reconnaissance spécifique d'un anticorps (le paratope). Un antigène est caractérisé par ses épitopes. Il s'agit donc dans la présente demande d'une molécule contenant au moins un motif lysyl de formule (I) tel que défini ci-dessus. Par « peptide » formant l'épitope pour la génération d'anticorps spécifiques selon l'invention, on entend par exemple un peptide comprenant au moins un motif lysyl substitué par un radical propionyl et/ou butyryl, et plus précisément une séquence peptidique comprenant entre 2 et 50 acides aminés, au moins l'un des acides aminés étant un motif lysyl substitué par un radical propionyl et/ou butyryl. On préférera une séquence peptidique de 2 à 25 acides aminés et tout particulièrement de 2 à 15 acides aminés. Par « protéine » formant l'épitope pour la génération d'anticorps spécifiques selon la présente invention, on entend par exemple une protéine immunogène comprenant au moins un motif lysyl substitué par un radical propionyl et/ou butyryl, et plus précisément une séquence peptidique supérieure à 50 acides aminés, au moins l'un desdits acides aminés étant un motif lysyl substitué par un radical propionyl et/ou butyryl. De préférence, ladite protéine a un poids moléculaire de 5 kDaltons à 100 kDaltons et plus particulièrement un poids moléculaire entre 5 à 20 kDa.In the present application, the term "antibody" designates, for example, immunoglobulins (Ig) for example of the gamma (IgG) or Mu (IgM) type, preferably IgG. These antibodies may be polyclonal or monoclonal. They are derived from immunization of animals such as the rabbit, the mouse and all the animals that can be immunized and known to those skilled in the art, but they can be produced by genetic engineering. Moreover, the antibodies according to the invention may be naturally occurring or humanized animal (preferably murine) antibodies. By extension, the antibodies according to the present invention may be functional and specific fragments of said antibodies such as the Fab fragment which contains the antigen-specific recognition site or the F (ab ') 2 fragment which contains at least the two sites of the antigen-specific recognition site. specific antigen recognition. By "specific" is meant for example that the antibodies are capable of recognizing and binding to a given epitope, namely the epitope comprising at least one lysyl unit of formula (I), via their paratope according to the known principles of immunology. In particular, the antibodies according to the present invention are, for example, capable of recognizing and binding to an epitope comprising at least one lysylpropionyl or butyrylated unit but are not suitable, for example, for recognizing and binding specifically to an epitope comprising at least one minus an acetylated lysyl motif. Indeed, the recognized antigen is defined by its particular epitope and this according to the structure or the conformation thereof. In the present application, the term "epitope" designates for example a molecule or a region thereof which can be recognized by the specific recognition part of an antibody (the paratope). An antigen is characterized by its epitopes. It is therefore in the present application a molecule containing at least one lysyl unit of formula (I) as defined above. By "peptide" forming the epitope for the generation of specific antibodies according to the invention, is meant for example a peptide comprising at least one lysyl unit substituted by a propionyl and / or butyryl radical, and more specifically a peptide sequence comprising between 2 and 50 amino acids, at least one of the amino acids being a lysyl unit substituted with a propionyl and / or butyryl radical. A peptide sequence of 2 to 25 amino acids and most preferably 2 to 15 amino acids will be preferred. By "protein" forming the epitope for the generation of specific antibodies according to the present invention is meant for example an immunogenic protein comprising at least one lysyl unit substituted with a propionyl and / or butyryl radical, and more specifically a higher peptide sequence. at least 50 amino acids, at least one of said amino acids being a lysyl unit substituted with a propionyl and / or butyryl radical. Preferably, said protein has a molecular weight of 5 kDaltons to 100 kDaltons and more particularly a molecular weight between 5 to 20 kDa.
On peut citer par exemple les protéines comme p53 ou les histones et plus particulièrement les histones H3, H4, H2A et H2B. Plus particulièrement, l'histone H3 humaine, de poids moléculaire d'environ 15kDa, peut être propionylée et/ou butyrylée sur les lysines en position 4, 9, 14, 18, 23,... et en général sur au moins une lysine (représentée par K). On peut citer également l'histone H4 humaine de poids moléculaire d'environ 11 kDa dont au moins une lysine en position 5, 8, 12, 16, 20,.. peut être propionylée et/ou butyrylée. De même pour l'histone H2B humaine de poids moléculaire d'environ 14 kDa peut être propionylée et/ou butyrylée sur les lysines en position 5, 1 1, 12, 15, 16,.. ainsi que l'histone H2A humaine de poids moléculaire d'environ 14 kDa peut être propionylée et/ou butyrylée sur les lysines 5, 9, 13, 15,..
Ces lysines propionylées et/ou butyrylées répondent à la formule (I) ci-dessus et peuvent représenter ainsi des antigènes induisant la formation et la reconnaissance spécifique des anticorps selon l'invention.For example, proteins such as p53 or histones, and more particularly histones H3, H4, H2A and H2B, may be mentioned. More particularly, the human H3 histone, with a molecular weight of approximately 15 kDa, may be propionylated and / or butyrylated on the lysines at the 4, 9, 14, 18, 23, and generally on at least one lysine (represented by K). Mention may also be made of human H4 histone with a molecular weight of about 11 kDa, of which at least one lysine at position 5, 8, 12, 16, 20 may be propionylated and / or butyrylated. Similarly for human H2B histone of molecular weight of about 14 kDa can be propionylated and / or butyrylated on lysines at position 5, 1 1, 12, 15, 16, .. as well as human histone H2A of weight molecular weight of about 14 kDa can be propionylated and / or butyrylated on lysines 5, 9, 13, 15, .. These propionylated and / or butyrylated lysines correspond to the formula (I) above and may thus represent antigens inducing the formation and specific recognition of the antibodies according to the invention.
Selon un mode particulier de réalisation de la présente invention, dans la formule (1) ci- dessus, le radical R0 de l'épitope reconnu par l'anticorps est un H.According to a particular embodiment of the present invention, in the formula (1) above, the radical R 0 of the epitope recognized by the antibody is an H.
Selon un autre mode particulier de réalisation de la présente invention, R0 est un alkyle choisi parmi les alkyles linéaires, ramifiés ou cycliques, substitués ou non par un hétéroatome et comportant de 1 à 20 atomes de carbone. Selon encore un autre mode particulier de réalisation de la présente invention, R0 est un aryle choisi parmi les aryles substitués ou non par un hétéroatome et comportant 3 à 20 atomes de carbone.According to another particular embodiment of the present invention, R 0 is an alkyl chosen from linear, branched or cyclic alkyls, substituted or not by a heteroatom and having from 1 to 20 carbon atoms. According to yet another particular embodiment of the present invention, R 0 is an aryl chosen from aryls which may or may not be substituted by a heteroatom and which has 3 to 20 carbon atoms.
R0 peut également être un aralkyle substitué ou non par un hétéroatome et comportant 4 à 20 atomes de carbone, un alkylaryle substitué ou non par un hétéroatome et comportant 4 à 20 atomes de carbone.R 0 may also be an aralkyl substituted or not with a heteroatom and having 4 to 20 carbon atoms, an alkylaryl substituted or not with a heteroatom and having 4 to 20 carbon atoms.
Selon un mode particulier de réalisation de la présente invention, le radical R1 de l'épitope reconnu par l'anticorps est un H.According to a particular embodiment of the present invention, the radical R 1 of the epitope recognized by the antibody is an H.
Selon un autre mode particulier de réalisation de la présente invention, R1 est un alkyle choisi parmi les alkyles linéaires, ramifiés ou cycliques, substitués ou non par un hétéroatome et comportant de 1 à 20 atomes de carbone.According to another particular embodiment of the present invention, R 1 is an alkyl chosen from linear, branched or cyclic alkyls, substituted or unsubstituted by a heteroatom and comprising from 1 to 20 carbon atoms.
R1 est un aryle choisi parmi les aryles substitués ou non par un hétéroatome et comportant 3 à 20 atomes de carbone.R 1 is an aryl selected from aryls substituted or not with a heteroatom and having 3 to 20 carbon atoms.
R1 peut également être un aralkyle substitué ou non par un hétéroatome et comportant 4 à 20 atomes de carbone, un alkylaryle substitué ou non par un hétéroatome et comportant 4 à 20 atomes de carbone.R 1 may also be an aralkyl substituted or not with a heteroatom and having 4 to 20 carbon atoms, an alkylaryl substituted or not with a heteroatom and having 4 to 20 carbon atoms.
Dans un autre mode particulier de l'invention, R1 est un sucre choisi parmi les restes saccharide, monosaccharide, disaccharide (saccharose, maltose e.g.) ou polysaccharide hydrogéné ou non, et leurs mélanges. Dans un autre mode particulier de l'invention, R1 est un lipide choisi parmi les acides gras, leurs dérivés et leurs esters.In another particular embodiment of the invention, R 1 is a sugar chosen from the saccharide, monosaccharide, disaccharide (sucrose, maltose eg) or hydrogenated polysaccharide or not, and their mixtures. In another particular embodiment of the invention, R 1 is a lipid chosen from fatty acids, their derivatives and their esters.
Dans un mode particulier de réalisation de l'invention, R1 peut être un nucléotide choisi parmi les nucléotides connus.In a particular embodiment of the invention, R 1 may be a nucleotide selected from known nucleotides.
Dans un autre mode particulier de réalisation de l'invention, R1 est une entité constituée d'au moins un acide aminé lequel forme, via son extrémité C terminale, une liaison peptidique avec le motif lysyl. Il peut ainsi s'agir par exemple d'un acide aminé simple, d'un peptide, de préférence un peptide contenu dans la séquence d'une histone et plus particulièrement les histones H3, H4 ou H2A, d'une protéine, de préférence une protéine histone et plus particulièrement les histones H3, H4 ou H2A, d'une glycoprotéine, d'une lipoprotéine...
L'acide aminé impliqué dans la liaison peptidique avec le motif lysyl est peut être n'importe quel acide aminé choisi parmi les 22 acides aminés connus. Au moins un acide aminé est un acide aminé naturel ou non naturel, D ou L.In another particular embodiment of the invention, R 1 is an entity consisting of at least one amino acid which, via its C-terminal end, forms a peptide bond with the lysyl motif. It may thus be, for example, a simple amino acid, a peptide, preferably a peptide contained in the sequence of a histone and more particularly the histones H3, H4 or H2A, of a protein, preferably a histone protein and more particularly the histones H3, H4 or H2A, a glycoprotein, a lipoprotein ... The amino acid involved in the peptide bond with the lysyl motif is any amino acid selected from the 22 known amino acids. At least one amino acid is a natural or unnatural amino acid, D or L.
Selon un mode particulier de réalisation de la présente invention, le radical R2 de l'épitope reconnu par l'anticorps est un OH.According to a particular embodiment of the present invention, the radical R 2 of the epitope recognized by the antibody is an OH.
Selon un autre mode particulier de réalisation de la présente invention, R est un alkyle choisi parmi les alkyles linéaires, ramifiés ou cycliques, substitués ou non par un hétéroatome et comportant de 1 à de 1 à 20 atomes de carbone. Selon encore un autre mode particulier de réalisation de la présente invention, R est un aryle choisi parmi les aryles substitués ou non par un hétéroatome et comportant 3 à 20 atomes de carboneAccording to another particular embodiment of the present invention, R is an alkyl chosen from linear, branched or cyclic alkyls, substituted or not by a heteroatom and having from 1 to 1 to 20 carbon atoms. According to yet another particular embodiment of the present invention, R is an aryl chosen from heteroatom-substituted and non-substituted aryls having 3 to 20 carbon atoms.
R2 peut également être un aralkyle substitué ou non par un hétéroatome et comportant 4 à 20 atomes de carbone, un alkylaryle substitué ou non par un hétéroatome et comportant 4 à 20 atomes de carbone.R 2 may also be an aralkyl substituted or not with a heteroatom and having 4 to 20 carbon atoms, an alkylaryl substituted or not with a heteroatom and having 4 to 20 carbon atoms.
Dans un autre mode particulier de l'invention, R est un sucre choisi parmi les restes saccharide, monosaccharide, disaccharide (saccharose, maltose e.g.) ou polysaccharide hydrogéné ou non, et leurs mélanges.In another particular embodiment of the invention, R is a sugar chosen from the saccharide, monosaccharide, disaccharide (sucrose, maltose e.g.) or hydrogenated polysaccharide or not, and their mixtures.
Dans un autre mode particulier de l'invention, R est un lipide choisi parmi les acides gras, leurs dérivés et leurs esters.In another particular embodiment of the invention, R is a lipid chosen from fatty acids, their derivatives and their esters.
Dans un mode particulier de réalisation de l'invention, R peut être un nucléotide choisi parmi les nucléotides connus.In a particular embodiment of the invention, R may be a nucleotide selected from known nucleotides.
Dans un autre mode particulier de réalisation de l'invention, R est une entité constituée d'au moins un acide aminé lequel forme, via son extrémité N terminale, une liaison peptidique avec le motif lysyl. 11 peut ainsi s'agir par exemple d'un acide aminé simple, d'un peptide, de préférence un peptide contenu dans la séquence d'une histone et plus particulièrement les histones H3, H4, H2A ou H2B, d'une protéine, de préférence une protéine histone et plus particulièrement les histones H3, H4, H2A ou H2B, d'une glycoprotéine.... L'acide aminé impliqué dans la liaison peptidique avec le motif lysyl est peut être n'importe quel acide aminé choisi parmi les 22 acides aminés connus dont au moins un acide aminé est un acide aminé naturel ou non naturel, D ou L.In another particular embodiment of the invention, R is an entity consisting of at least one amino acid which, via its N-terminus, forms a peptide bond with the lysyl motif. It may thus be, for example, a simple amino acid, a peptide, preferably a peptide contained in the sequence of a histone and more particularly the histones H3, H4, H2A or H2B, of a protein, preferably a histone protein and more particularly the histones H3, H4, H2A or H2B, of a glycoprotein .... The amino acid involved in the peptide bond with the lysyl unit is any amino acid selected from the 22 known amino acids of which at least one amino acid is a natural or non-natural amino acid, D or L.
Dans un mode particulier de réalisation de l'invention, R équivaut à OR4 où R4 est un alkyle, un aryle, un sucre, un lipide tel que défini et/ou exemplifié ci-dessus.In a particular embodiment of the invention, R is equivalent to OR 4 where R 4 is an alkyl, an aryl, a sugar, a lipid as defined and / or exemplified above.
L'épitope contient au moins un site propionylé ou butyrylé. En effet, selon un mode particulier de réalisation de la présente invention, le radical R3 de l'épitope reconnu par l'anticorps selon l'invention est un radical -(CH2)H-CH3 où n vaut 1 ou 2. Lorsque n correspond à 1, l'unité lysyl est substituée par un acide propionique. Par convention dans la
présente demande, on pourra parler alors de résidu propionyl lié au motif lysyl, ainsi l'épitope de formule (I) selon la présente invention contient un motif lysyl propionylé. Lorsque n correspond à 2, l'unité lysyl est substituée par un acide butyrique (ou par convention un butyryl) formant ainsi un épitope de formule (I) contenant un motif lysyl butyrylé.The epitope contains at least one propionyl or butyrylated site. Indeed, according to a particular embodiment of the present invention, the radical R 3 of the epitope recognized by the antibody according to the invention is a - (CH 2 ) H -CH 3 radical where n is 1 or 2. When n is 1, the lysyl unit is substituted with a propionic acid. By convention in the In the present application, it will be possible to speak of a propionyl residue bonded to the lysyl unit, so that the epitope of formula (I) according to the present invention contains a lysyl propionyl unit. When n corresponds to 2, the lysyl unit is substituted by a butyric acid (or, by convention, a butyryl) thus forming an epitope of formula (I) containing a lysyl butyryl unit.
Comme on le comprend de la présente formule (I) et de l'exposé ci -dessus, l'épitope reconnu spécifiquement par les anticorps, ou au moins l'un de leurs fragments fonctionnels, selon la présente invention, peut être constitué d'un simple acide aminé substitué, à savoir la lysine substituée par un radical propionyl (n=l) ou un radical butyryl (n^), c'est le cas où R0, R1 sont des H et R2 est un OH mais R0, R1 et R2 de cet épitope peuvent être identiques ou différents. Ainsi, l'épitope peut être constitué d'une molécule faite d'au moins deux acides aminés dont l'un est une lysine propionylée ou butyrylée, d'un peptide tel que la séquence N terminale des histones, d'une protéine telle qu'une histone, une glycoprotéine ou toute autre molécule contenant au moins un motif lysyl substituée par R3 tel que défini ci-dessus. Ces protéines peuvent être des protéines naturelles, cellulaires, tissulaires ou plasmatiques, ou des protéines réalisées artificiellement, des protéines recombinantes produites par génie génétique. Elles sont de préférence des protéines histones et tout particulièrement les histones H3, H4, H2A et H2B. De façon préférentielle, l'épitope de formule (I) correspond à un polypeptide d'une centaine d'acides aminés. Dans la forme de réalisation préférée de l'invention, R0 correspond à H et R1 et R2 correspondent à des acides aminés quelconques identiques ou différents. Lorsque R3 est différent de -(CHi)n-CH3 où n vaut 1 ou 2, les anticorps selon l'invention ne se lient pas à la molécule de façon spécifique. Ceci est particulièrement le cas, lorsque R est un acétyl.As understood from the present formula (I) and from the discussion above, the epitope specifically recognized by the antibodies, or at least one of their functional fragments, according to the present invention, may consist of a simple substituted amino acid, namely lysine substituted with a propionyl radical (n = 1) or a butyryl radical (n 1), this is the case where R 0 , R 1 are H and R 2 is an OH but R 0 , R 1 and R 2 of this epitope may be the same or different. Thus, the epitope may consist of a molecule made of at least two amino acids, one of which is a propionylated or butyrylated lysine, a peptide such as the N-terminal sequence of histones, a protein such as a histone, a glycoprotein or any other molecule containing at least one lysyl motif substituted with R 3 as defined above. These proteins can be natural, cellular, tissue or plasma proteins, or artificially produced proteins, recombinant proteins produced by genetic engineering. They are preferably histone proteins and especially histones H3, H4, H2A and H2B. Preferably, the epitope of formula (I) corresponds to a polypeptide of one hundred amino acids. In the preferred embodiment of the invention, R 0 is H and R 1 and R 2 are any of the same or different amino acids. When R 3 is other than - (CH 1 ) n -CH 3 where n is 1 or 2, the antibodies according to the invention do not bind to the molecule specifically. This is particularly the case when R is acetyl.
Dans un mode préféré de l'invention, on utilise des peptides riches en lysine pour générer l'anticorps. Il est connu de l'homme de l'art qu'un site antigénique contient généralement 5 à 20 acides aminés mais selon un mode préféré de l'invention l'épitope antigénique spécifique reconnu par l'anticorps peut contenir un nombre inférieur d'acides aminés, c'est-à-dire de un seul acide aminé, la lysine substituée par un radical propionyl ou butyryl elle-même, à 5 acides aminés sans se limiter à ce nombre. En effet, l'épitope peut contenir jusqu'à 10 acides aminés et de préférence 5 acides aminés.In a preferred embodiment of the invention, lysine-rich peptides are used to generate the antibody. It is known to one skilled in the art that an antigenic site generally contains 5 to 20 amino acids, but according to a preferred embodiment of the invention, the specific antigenic epitope recognized by the antibody may contain a lower number of acids. amino, that is to say a single amino acid, lysine substituted by a propionyl or butyryl itself, at 5 amino acids without being limited to this number. Indeed, the epitope may contain up to 10 amino acids and preferably 5 amino acids.
Dans sa forme préférée, le motif lysyl substitué par un radical propionyl ou butyryl est placé de façon la plus centrale possible au sein dudit site antigénique générant l'anticorps selon l'invention.In its preferred form, the lysyl unit substituted with a propionyl or butyryl radical is placed as centrally as possible within said antigenic site generating the antibody according to the invention.
Dans un mode de réalisation particulièrement préféré, le peptide ou la protéine comprenant un épitope de formule (I), contient plusieurs lysines propionylées et/ou butyrylées. Ces
peptides sont réalisés par des méthodes classiques de synthèse peptidiques connues de l'homme de l'art.In a particularly preferred embodiment, the peptide or protein comprising an epitope of formula (I), contains several propionylated and / or butyrylated lysines. These peptides are made by conventional peptide synthesis methods known to those skilled in the art.
Ainsi, par le biais de ces anticorps, l'état de la propionylation et/ou butyrylation des protéines cellulaires impliquées dans les métabolismes et les fonctions cellulaires peut être déterminé, caractérisé et quantifié. En effet, l'outil anticorps selon la présent invention permet une détection qualitative mais également quantitative des molécules portant l'épitope de formule (I) dans des échantillons biologiques, in vitro et in vivo. De plus, on peut obtenir une localisation cellulaire des molécules, de préférence les protéines contenant ledit épitope de formule (I) reconnu de façon spécifique par les anticorps selon la présente invention ainsi qu'une localisation de cet épitope de formule (I) lui-même dans une molécule particulière, de préférence une protéine. Ceci est particulièrement important dans la compréhension de mécanismes cellulaires et par conséquent dans le traitement de pathologies impliquant la propionylation/butyrylation des molécules, de préférence protéines et particulièrement la propionylation de la lysine, telles que le cancer, les maladies neurodégénératives, le diabète et l'inflammation.Thus, through these antibodies, the state of the propionylation and / or butyrylation of cellular proteins involved in metabolisms and cellular functions can be determined, characterized and quantified. Indeed, the antibody tool according to the present invention allows a qualitative but also quantitative detection of molecules bearing the epitope of formula (I) in biological samples, in vitro and in vivo. In addition, it is possible to obtain a cellular localization of the molecules, preferably the proteins containing said epitope of formula (I) specifically recognized by the antibodies according to the present invention, as well as a location of this epitope of formula (I) itself. even in a particular molecule, preferably a protein. This is particularly important in the understanding of cellular mechanisms and consequently in the treatment of pathologies involving the propionylation / butyrylation of molecules, preferably proteins, and particularly the propionylation of lysine, such as cancer, neurodegenerative diseases, diabetes and diabetes. 'inflammation.
Les anticorps selon la présente invention peuvent être présents in vivo et générés soit : - naturellement dans l'organisme, lors de processus pathologiques, il s'agit alors des autoanticorps exposés plus bas, - artificiellement, c'est-à-dire par activation volontaire du système immunitaire d'un organisme donné via l'introduction d'un antigène comportant ledit épitope de formule (I). Ainsi l'organisme concerné produit des anticorps spécifiques de l'épitope, reconnu comme non-soi.The antibodies according to the present invention may be present in vivo and generated either: - naturally in the body, during pathological processes, it is then the autoantibodies exposed below, - artificially, that is to say by activation of the immune system of a given organism via the introduction of an antigen comprising said epitope of formula (I). Thus the organism produces antibodies specific for the epitope, recognized as non-self.
Les anticorps selon la présente invention peuvent être définis par leur immunoréactivité vis-à- vis d'épitopes choisi dans le groupe comprenant : i. les épitopes comprenant au moins un résidu lysyl acétylé (n=0 dans la définition deR3 de la formule (I)); n. les épitopes comprenant au moins un résidu lysyl proprionylé (n=l dans la définition deR3 de la formule (I)); m. les épitopes comprenant au moins un résidu lysyl butyrylé (n=2 dans la définition deR de la formule (I)).The antibodies according to the present invention may be defined by their immunoreactivity against epitopes selected from the group consisting of: i. epitopes comprising at least one acetylated lysyl residue (n = 0 in the definition of R 3 of formula (I)); not. epitopes comprising at least one lysyl propionyl residue (n = 1 in the definition of R 3 of formula (I)); m. epitopes comprising at least one lysyl butyrylated residue (n = 2 in the definition of R of formula (I)).
Conformément à la présente invention cette immunoréactivité est reflétée par un test T de mesure de l'immuno-réactivité de sérums contenant les épitopes (i) et/ou (ii) et/ou (iii). Ce test T est défini e.g. comme suit :
- adsorber, sur une plaque 96 puits en polystyrène (EIA/RIA, High Binding, Corning Costar), 100 μl par puits d'une solution d'antigènes (BSA-propionylée, BSA butyrylée, BSA acétylée) à lOμg/ml en tampon bicarbonate 0,1 M pH 9,5,According to the present invention this immunoreactivity is reflected by a T test for measuring the immunoreactivity of sera containing the epitopes (i) and / or (ii) and / or (iii). This test T is defined eg as follows: adsorbing, on a 96-well polystyrene plate (EIA / RIA, High Binding, Corning Costar), 100 μl per well of an antigen solution (BSA-propionylated, butyrylated BSA, acetylated BSA) at 10 μg / ml in buffer 0.1 M bicarbonate pH 9.5,
- incuber pendant 2 heures à 37°C, - vider les puits et déposer 150 μl/puits d'une solution de BSA 0.5% dans du tampon PBS pour saturer les sites d'adsorption excédentaires sur le plastique, et laisser incuber une heure à 37°C,incubate for 2 hours at 37 ° C., empty the wells and deposit 150 μl / well of a 0.5% BSA solution in PBS buffer to saturate the excess adsorption sites on the plastic, and incubate for one hour at 37 ° C,
- déposer les sérums aux dilutions indiquées en tampon PBS contenant du tween-20 à 0.1%. Ces solutions sont déposées puis dilués de deux en deux directement sur la plaque (1/500, 1/1000, 1/2000 ...) de façon à obtenir 100 μl/ puits de volume final,deposit the sera at the indicated dilutions in PBS buffer containing 0.1% tween-20. These solutions are deposited and diluted two by two directly on the plate (1/500, 1/1000, 1/2000 ...) so as to obtain 100 μl / well of final volume,
- incuber une heure à 37°C, puis laver 3 fois avec du PBS tween,- Incubate for one hour at 37 ° C, then wash 3 times with PBS tween,
- ajouter lOOμl/puits d'un anticorps de mouton anti IgG (H+L) de lapin marqué à la peroxydase et laisser 30 min. à 37°C,add 100 μl / well of a peroxidase-labeled rabbit anti-IgG (H + L) sheep antibody and leave for 30 min. at 37 ° C,
- laver 3 fois successivement pour éliminer l'excédent de réactif, -révéler l'activité peroxydase en utilisant le réactif eau oxygénée/tetraméthylbenzidine (TMB) (Covalab),washing 3 times successively to eliminate the excess of reagent, -release the peroxidase activity using the reagent oxygenated water / tetramethylbenzidine (TMB) (Covalab),
- stopper la réaction avec lOOμl de H2 SO4 (2N),stopping the reaction with 100 μl of H 2 SO 4 (2N),
- mesurer à 450 nm l'absorbance sur lecteur de plaque (Multiskan Ascent, Labsystems). Le test T est un test ELISA.- measure at 450 nm absorbance on plate reader (Multiskan Ascent, Labsystems). The T test is an ELISA test.
La présente invention couvre également les anticorps ou au moins l'un de leurs fragments fonctionnels spécifiques d'un épitope contenant au moins un motif lysyl de formule (I) telle que définie précédemment, caractérisés en ce que leur immuno-réactivité pour les antigènes BSA-propionylée ou BSA-butyrylée, mesurée dans un test T défini précédemment, est telle qu'elle répond à au moins l'une des caractéristiques suivantes : pour une dilution du sérum contenant lesdits anticorps à 1/500, la DO à 450 nm est > 1, de préférence est > 1,5 ; pour une dilution du sérum contenant lesdits anticorps à 1/1000, la DO à 450 nm est > 0,5, de préférence est > 0,9 ; - pour une dilution du sérum contenant lesdits anticorps à 1/2000, la DO à 450 nm est >The present invention also covers the antibodies or at least one of their functional fragments specific for an epitope containing at least one lysyl unit of formula (I) as defined above, characterized in that their immunoreactivity for BSA antigens -propionylated or BSA-butyrylated, measured in a test T defined above, is such that it meets at least one of the following characteristics: for a dilution of the serum containing said antibodies to 1/500, the OD at 450 nm is > 1, preferably is> 1.5; for dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is> 0.5, preferably is> 0.9; for a dilution of the serum containing said antibodies at 1/2000, the OD at 450 nm is
0,5, de préférence est > 0,6 ;0.5, preferably is> 0.6;
- pour une dilution du sérum contenant lesdits anticorps à 1/4000, la DO à 450 nm est > 0,2, de préférence est > 0,3 ; pour une dilution du sérum contenant lesdits anticorps à 1/8000, la DO à 450 nm est > 0,2, de préférence est > 0,25.
La présente invention concerne également des anticorps ou au moins l'un de leurs fragments fonctionnels tels que définis ci-dessus, caractérisésfor a dilution of the serum containing said antibodies at 1/4000, the OD at 450 nm is> 0.2, preferably is>0.3; for dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is> 0.2, preferably> 0.25. The present invention also relates to antibodies or at least one of their functional fragments as defined above, characterized
• en ce que leur immuno-réactivité pour les antigènes BSA-propionylée, mesurée dans un test T, est telle qu'elle répond à au moins l'une des caractéristiques suivantes : - pour une dilution du sérum contenant lesdits anticorps à 1/500, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,6; 0,8; 1,0; 1,5; 2,0; 2 5- 2 7 - pour une dilution du sérum contenant lesdits anticorps à 1/1000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,3; 0,6 ; 0,8 ; 1,0 ; 1,5 ; 2,0 ; 2,2 ; pour une dilution du sérum contenant lesdits anticorps à 1/2000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,25 ; 0,4 ; 0,6 ; 1,0 ; pour une dilution du sérum contenant lesdits anticorps à 1/4000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,2 ; 0,4 ; 0,6 ; - pour une dilution du sérum contenant lesdits anticorps à 1/8000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,2 ; 0,4 ;In that their immunoreactivity for BSA-propionylated antigens, measured in a T test, is such that it meets at least one of the following characteristics: for a dilution of the serum containing said antibodies at 1/500 the OD at 450 nm is greater than or equal to, in ascending order preferably 0.6; 0.8; 1.0; 1.5; 2.0; For a dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is greater than or equal to, in increasing order of preference: 0.3; 0.6; 0.8; 1.0; 1.5; 2.0; 2.2; for dilution of the serum containing said antibodies to 1/2000, the OD at 450 nm is greater than or equal to, in ascending order preferably: 0.25; 0.4; 0.6; 1.0; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is greater than or equal to, in ascending order preferably: 0.2; 0.4; 0.6; for a dilution of the serum containing said antibodies at 1/8000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.2; 0.4;
• et en ce que leur immuno-réactivité pour les antigènes BSA-acétylés, mesurée dans un test T, est telle qu'elle répond à au moins l'une des caractéristiques suivantes : pour une dilution du sérum contenant lesdits anticorps à 1/500, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 1,5; 1,0; 0,9; 0,8; 0,7;And in that their immunoreactivity for BSA-acetylated antigens, measured in a T-test, is such that it meets at least one of the following characteristics: for a dilution of the serum containing said antibodies at 1/500 the OD at 450 nm is less than or equal to, in increasing order preferably: 1.5; 1.0; 0.9; 0.8; 0.7;
0,6 ; pour une dilution du sérum contenant lesdits anticorps à 1/1000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 1,2; 1,0; 0,9; 0,8; 0,5;0.6; for dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is less than or equal to, in ascending order preferably: 1.2; 1.0; 0.9; 0.8; 0.5;
0,4 ; - pour une dilution du sérum contenant lesdits anticorps à 1/2000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 1,0; 0,8; 0,6; 0,5; 0,4;0.4; for dilution of the serum containing said antibodies to 1/2000, the OD at 450 nm is less than or equal to, in increasing order of preference: 1.0; 0.8; 0.6; 0.5; 0.4;
0,3 ; - pour une dilution du sérum contenant lesdits anticorps à 1/4000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,8; 0,6; 0,7; 0,5; 0,3; 0,2 ; pour une dilution du sérum contenant lesdits anticorps à 1/8000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,7, 0,6; 0,5; 0,4; 0,25;0.3; for a dilution of the serum containing said antibodies at 1/4000, the OD at 450 nm is less than or equal to, in increasing order of preference: 0.8; 0.6; 0.7; 0.5; 0.3; 0.2; for dilution of the serum containing said antibodies to 1/8000, the OD at 450 nm is less than or equal to, in ascending order preferably: 0.7, 0.6; 0.5; 0.4; 0.25;
0,15.0.15.
La présente invention concerne des anticorps ou au moins l'un de leurs fragments fonctionnels tels que définis ci-dessus, caractérisésThe present invention relates to antibodies or at least one of their functional fragments as defined above, characterized
• en ce que leur immuno-réactivité pour les antigènes BSA-butyrylée, mesurée dans un
test T, est telle qu'elle répond à au moins l'une des caractéristiques suivantes : pour une dilution du sérum contenant lesdits anticorps à 1/500, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,2 ; 0,4 ; 0,6 ; 1 ,0 ; 1,5 ; - pour une dilution du sérum contenant lesdits anticorps à 1/1000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,16 ; 0,4 ; 0,6 ; 0,9 ; - pour une dilution du sérum contenant lesdits anticorps à 1/2000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,14 ; 0,3 ; 0,5 ; 0,6 ; pour une dilution du sérum contenant lesdits anticorps à 1/4000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,1 ; 0,15 ; 0,2 ; 0,3 ; pour une dilution du sérum contenant lesdits anticorps à 1/8000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,1 ; 0,15 ; 0,2 ; 0,25 ; • et en ce que leur immuno-réactivité pour les antigènes BSA-acétylés, mesurée dans un test T, est telle qu'elle répond à au moins l'une des caractéristiques suivantes : - pour une dilution du sérum contenant lesdits anticorps à 1/500, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,8; 0,7 ; 0,6 ; 0,4 ; 0,3; 0,2 ; pour une dilution du sérum contenant lesdits anticorps à 1/1000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,7; 0,6; 0,5; 0,3; 0,20; 0,15 ; pour une dilution du sérum contenant lesdits anticorps à 1/2000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,6; 0,5; 0,4; 0,3; 0,15; 0,1 ; pour une dilution du sérum contenant lesdits anticorps à 1/4000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,6; 0,5; 0,4; 0,3; 0,15;In that their immunoreactivity for BSA-butyrylated antigens, measured in a T test, is such that it meets at least one of the following characteristics: for a dilution of the serum containing said antibodies to 1/500, the OD at 450 nm is greater than or equal to, in increasing order of preference: 0.2; 0.4; 0.6; 1.0; 1.5; for dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.16; 0.4; 0.6; 0.9; for a dilution of the serum containing said antibodies at 1/2000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.14; 0.3; 0.5; 0.6; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.1; 0.15; 0.2; 0.3; for dilution of the serum containing said antibodies to 1/8000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.1; 0.15; 0.2; 0.25; And in that their immunoreactivity for the BSA-acetylated antigens, measured in a T test, is such that it meets at least one of the following characteristics: for a dilution of the serum containing said antibodies at 1 / 500, the OD at 450 nm is less than or equal to, in increasing order preferably: 0.8; 0.7; 0.6; 0.4; 0.3; 0.2; for a dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is less than or equal to, in ascending order preferably: 0.7; 0.6; 0.5; 0.3; 0.20; 0.15; for a dilution of the serum containing said antibodies to 1/2000, the OD at 450 nm is less than or equal to, in ascending order preferably: 0.6; 0.5; 0.4; 0.3; 0.15; 0.1; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is less than or equal to, in ascending order preferably: 0.6; 0.5; 0.4; 0.3; 0.15;
0,1 ; pour une dilution du sérum contenant lesdits anticorps à 1/8000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,6; 0,5; 0,4; 0,3; 0,15; 0,1.0.1; for dilution of the serum containing said antibodies to 1/8000, the OD at 450 nm is less than or equal to, in ascending order preferably 0.6; 0.5; 0.4; 0.3; 0.15; 0.1.
La présente invention concerne un anticorps tel que défini ci-dessus, caractérisé en ce que dans un test T, son immuno-réactivité vis-à-vis des la BSA-acétylée (BA) ou la BSA propionylée (BP) est telle que la mesure de la DO à 450 nm correspond à l'une des caractéristiques suivantes :
The present invention relates to an antibody as defined above, characterized in that in a T test, its immunoreactivity with respect to the BSA-acetylated (BA) or the propionylated BSA (BP) is such that the measurement of OD at 450 nm corresponds to one of the following characteristics:
La présente invention concerne un anticorps tel que défini ci-dessus, caractérisé en ce que dans un test T, son immunoréactivité vis-à-vis des la BSA-acétylée (BA) ou la BSA butyrylée (BB) est telle que la mesure de la DO à 450 nm correspond à l'une des caractéristiques suivantes :The present invention relates to an antibody as defined above, characterized in that in a T test, its immunoreactivity with BSA-acetylated (BA) or butyrylated BSA (BB) is such that the measurement of the OD at 450 nm corresponds to one of the following characteristics:
Procédé de fabrication de l'anticorpsMethod of making the antibody
Les résidus de l'épitope de la formule (I), à savoir R0, R1, R2 et R3, sont greffés au résidu lysyl soit naturellement, par exemple in vivo, soit artificiellement in vitro par simple réaction des résidus ou molécules entre elles ou bien par des réactions forcées connues de l'homme du métier. Ainsi, il est possible de produire des anticorps grâce à des antigènes endogènes portant l'épitope de formule (I) ou par la synthèse de ces antigènes. La présente invention concerne ainsi un procédé de fabrication des anticorps ou de leurs fragments fonctionnels tels que définis ci-dessus, caractérisé en ce qu'il consiste à : a) mettre en œuvre un synthon de formule (I), b) coupler ledit synthon à une molécule porteuse, c) récupérer du plasma/sérum dudit animal auquel le coupe synthon - molécule porteuse a été préalablement injecté,
d) sélectionner les anticorps spécifiques dudit synthon utilisé à l'étape a) à l'aide d'un ou plusieurs épitopes de formule (I) telle que définie ci-dessus, e) éventuellement purifier les anticorps par les méthodes connues de l'homme de l'art.The residues of the epitope of the formula (I), namely R 0 , R 1 , R 2 and R 3 , are grafted to the lysyl residue either naturally, for example in vivo, or artificially in vitro by simple reaction of the residues or molecules together or by forced reactions known to those skilled in the art. Thus, it is possible to produce antibodies by endogenous antigens carrying the epitope of formula (I) or by the synthesis of these antigens. The present invention thus relates to a method of manufacturing the antibodies or their functional fragments as defined above, characterized in that it consists in: a) implementing a synthon of formula (I), b) coupling said synthon to a carrier molecule, c) recovering plasma / serum from said animal to which the synthon-carrier molecule cut has been previously injected, d) selecting the specific antibodies of said synthon used in step a) using one or more epitopes of formula (I) as defined above, e) optionally purifying the antibodies by the known methods of skilled in the art.
Le synthon correspond à la formule (I). Plus précisément, ledit synthon correspond au moins à un acide aminé substitué : une lysine propionylée ou une lysine butyrylée. Le synthon selon la présente invention et tel que défini ci-dessus est réalisé par le procédé décrit par M. Bashir Uddin Surfraz et al dans J. Med. Chem. 2007, 50, 1418-1422 et par Takeshi M.et al dans Biomacromolecules, 2007, 8, 318-321.The synthon corresponds to the formula (I). More precisely, said synthon corresponds to at least one substituted amino acid: a propionylated lysine or a butyrylated lysine. The synthon according to the present invention and as defined above is made by the method described by M. Bashir Uddin Surfraz et al in J. Med. Chem. 2007, 50, 1418-1422 and by Takeshi M. et al in Biomacromolecules, 2007, 8, 318-321.
Un tel synthon est particulièrement intéressant dans la production des anticorps selon l'invention et particulièrement dans la réalisation de l'antigène constitué par ledit synthon ou le comportant. Une fois le synthon produit et soit couplé directement à une protéine porteuse, soit inséré dans une séquence peptidique, il peut être utilisé dans la fabrication des anticorps spécifiques dirigés contre lui ou être stocké, de préférence congelé à -200C pour être utilisé ultérieurement. Par le terme « couplé », on entend par exemple lié ou conjugué. Cette liaison ou conjugaison peut se faire chimiquement, par exemple par une liaison covalente, adsorption ou un autre mode de fixation connu de l'homme de l'art. De préférence, le couplage se fait par un agent de couplage comme par exemple le cardodiimide ou la glutaraldéhyde. La molécule porteuse à laquelle est couplé le synthon est une molécule de poids moléculaire suffisamment important pour induire une réaction immunitaire et la production d'anticorps circulants. Cette molécule peut être une protéine, un polypeptide, un polymère naturel ou synthétique. Elle est de préférence une protéine et en particulier une protéine de poids moléculaire supérieur ou égal à 5 kDaltons telle que l'albumine ou l'hémocyanine de patelle (KLH pour Keyhole Limpet Haemocyanin). Dans une forme préférée de l'invention, on utilise la KLH en tant que protéine porteuse. Le couple synthon-molécule porteuse est injecté à un animal à immuniser. Il est de préférence en suspension et mélangé avec une solution d'adjuvant de Freund (complet ou incomplet). L'animal auquel est injecté ledit couple synthon-molécule porteuse en suspension peut être le lapin, la souris, le rat, la chèvre, le mouton, le cheval ou le cobaye, de préférence le lapin, le rat et la souris. L'injection dudit couple peut se faire en une ou plusieurs fois selon les méthodes classiques et connues d'immunisation. Les principales voies d'administration sont des injections sous-cutanées, intradermiques, ou intramusculaires; les injections intraveineuses et intrapéritonéales ne sont employées que dans des cas particuliers. S'il y a plusieurs injections du couple synthon-molécule porteuse, les types d'anticorps produits,
spécifiques du synthon, sont différents. En effet, il peut s'agir d'immunoglobulines de type G ou M. Ainsi, on injecte de préférence en intramusculaire environ 1 ml dudit couple antigénique à un lapin et environ lOOμl à une souris. La concentration en synthon dans le mélange d'injection est d'environ 50μg/ml.Such a synthon is particularly interesting in the production of the antibodies according to the invention and particularly in the production of the antigen constituted by said synthon or comprising it. Once the synthon produced and is coupled directly to a carrier protein, or inserted into a peptide sequence, it can be used in the manufacture of specific antibodies directed against it or stored, preferably frozen at -20 ° C. for later use. . By the term "coupled" is meant for example bound or conjugated. This binding or conjugation can be done chemically, for example by a covalent bond, adsorption or another method of attachment known to those skilled in the art. Preferably, the coupling is done by a coupling agent such as cardodiimide or glutaraldehyde. The carrier molecule to which the synthon is coupled is a molecule of molecular weight large enough to induce an immune reaction and the production of circulating antibodies. This molecule can be a protein, a polypeptide, a natural or synthetic polymer. It is preferably a protein and in particular a protein of molecular weight greater than or equal to 5 kDaltons such as albumin or keyhole limpet hemocyanin (KLH for Keyhole Limpet Haemocyanin). In a preferred form of the invention, KLH is used as the carrier protein. The synthon-carrier molecule pair is injected into an animal to be immunized. It is preferably in suspension and mixed with a solution of Freund's adjuvant (complete or incomplete). The animal to which is injected said synthon-carrier molecule in suspension can be the rabbit, the mouse, the rat, the goat, the sheep, the horse or the guinea pig, preferably the rabbit, the rat and the mouse. The injection of said pair can be done in one or more times according to conventional and known methods of immunization. The main routes of administration are subcutaneous, intradermal, or intramuscular injections; intravenous and intraperitoneal injections are only used in special cases. If there are several injections of the synthon-carrier molecule pair, the types of antibodies produced, specific to the synthon, are different. Indeed, it may be type G or M immunoglobulins. Thus, approximately 1 ml of said antigenic couple is injected intramuscularly into a rabbit and about 100 μl into a mouse. The concentration of synthon in the injection mixture is about 50 μg / ml.
Le sang de l'animal contenant, entre autres, lesdits anticorps spécifiques du synthon injecté est récupéré par prélèvement ou par exsanguination. De préférence, on prélève du plasma ou du sérum contenant également, entre autres, les anticorps spécifiques du synthon tel que défini ci-dessus. Le sérum contenant les anticorps recherchés, dirigés contre ledit synthon, contient normalement plusieurs espèces d'anticorps différents dirigés contre plusieurs épitopes du même antigène, on appelle cette préparation polyclonale. On peut également mettre en œuvre des techniques permettant d'isoler et de cloner des lymphocytes ne produisant qu'une espèce moléculaire (i.e. clonotype) d'anticorps : les anticorps qui ne reconnaissent qu'un seul épitope de l'antigène.The blood of the animal containing, among others, said antibodies specific for the injected synthon is recovered by sampling or by exsanguination. Preferably, plasma or serum also containing, inter alia, antibodies specific for the synthon as defined above. The serum containing the desired antibodies, directed against said synthon, normally contains several different antibody species directed against several epitopes of the same antigen, this polyclonal preparation is called. Techniques can also be employed to isolate and clone lymphocytes that produce only one molecular species (i.e. clonotype) of antibodies: antibodies that recognize only a single epitope of the antigen.
L'étape de sélection des anticorps spécifiques dudit synthon tel que défini ci-dessus se fait à l'aide de la technique ELISA (Enzyme- Linked Immuno Sorbent Assay). Cette technique de sélection est largement décrite dans la littérature. Pour résumer, ce principe connu de l'homme de l'art, on procède comme suit : - le synthon décrit ci-dessus ou un épitope de formule (I) est fixé à un support classiquement utilisé dans les techniques d'ELISA au moins un lavage est effectué, on ajoute sur le support le plasma ou le sérum de l'animal ayant été immunisé, au moins un lavage est effectué, - on ajoute une solution contenant des anticorps, de préférence de chèvre ou de mouton, reconnaissant spécifiquement les anticorps issus de l'animal ayant été immunisé, de préférence le lapin, le rat ou la souris, lesdits anticorps ajoutés étant couplés à une molécule utiles pour leur détection, de préférence une enzyme dégradant un substrat comme la peroxydase dégradant le TMB ou la DAB, - au moins un lavage est effectué, on ajoute le substrat de la molécule utile à la détection (le TMB ou la DAB), on effectue une lecture de la densité optique révélatrice de la présence des anticorps souhaités et ainsi sélectionnés. Dans cette technique de sélection, on utilise de préférence la BSA propionylée et/ou butyrylée telle que définie dans la présente demande mais le synthon tel que défini ci-dessus couplé à une protéine porteuse ou un peptide contenant au moins un motif lysyl propionylé et/ou butyrylé couplé à une protéine porteuse peuvent également être utilisés.
Lorsqu'une étape de purification des anticorps est réalisée, cette dernière peut être faite en phase liquide ou solide et de différentes façons à savoir la chromatographie d'affinité en utilisant soit des colonnes de séparation, des billes magnétiques ou des résines portant ledit synthon en tant que ligand. On préfère un support solide tel qu'une colonne de sépharose sur laquelle les synthons ont été fixés, de préférence par liaison covalente.The step of selecting antibodies specific for said synthon as defined above is done using the ELISA (Enzyme-Linked Immuno Sorbent Assay) technique. This selection technique is widely described in the literature. To summarize, this principle known to those skilled in the art, is carried out as follows: the synthon described above or an epitope of formula (I) is attached to a carrier conventionally used in ELISA techniques at least a washing is carried out, the plasma or serum of the animal which has been immunized is added to the support, at least one washing is carried out, a solution containing antibodies, preferably of goat or sheep, specifically antibodies derived from the animal having been immunized, preferably rabbit, rat or mouse, said added antibodies being coupled to a molecule useful for their detection, preferably a substrate-degrading enzyme such as TMB degrading peroxidase or DAB at least one wash is carried out, the substrate of the molecule useful for detection (TMB or DAB) is added, the optical density is read, indicating the presence of the desired antibodies, and selected insi. In this selection technique, the propionylated and / or butyrylated BSA as defined in the present application is preferably used but the synthon as defined above coupled to a carrier protein or a peptide containing at least one lysylpropionylated unit and / or butyryl coupled to a carrier protein may also be used. When a step of purification of the antibodies is carried out, the latter may be made in the liquid or solid phase and in different ways namely affinity chromatography using either separation columns, magnetic beads or resins bearing said synthon in as a ligand. A solid support such as a sepharose column on which the synthons have been attached is preferably preferred, preferably by covalent bonding.
La présente invention vise également des anticorps isolés ou au moins l'un des fragments fonctionnels de ceux-ci, caractérisés en ce qu'il sont obtenus à partir d'un antigène consistant en un synthon de formule (I) dans laquelle R0 équivaut à H, un alkyle, un aryle, un alkylaryle ou un aralkyle, R1 équivaut à H, un alkyle, un aryle, un alkylaryle, un aralkyle, un sucre, un lipide, un nucléotide, R équivaut à OH, un alkyle, un aryle, un alkylaryle, un aralkyle, un sucre, un lipide, un nucléotide ou OR4 où R4 est un alkyle, un aryle, un sucre, un lipide, R équivaut à -(CH2)H-CH3 où n vaut 1 ou 2.The present invention also relates to isolated antibodies or at least one of the functional fragments thereof, characterized in that they are obtained from an antigen consisting of a synthon of formula (I) in which R 0 equals at H, alkyl, aryl, alkylaryl or aralkyl, R 1 is H, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide, R is OH, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide or OR 4 wherein R 4 is alkyl, aryl, sugar, lipid, R is - (CH 2 ) H -CH 3 where n is 1 or 2.
Ainsi, les anticorps selon la présente invention, obtenus à partir dudit synthon, sont spécifiques de leur épitope directement après leur production, sans nécessiter l'utilisation d'autres techniques telles que l'épuisement d'anticorps polyclonaux pour obtenir leur haute spécificité vis-à-vis des lysines propionylées ou butyrylées. Ceci présente un avantage majeur. Dans une variante de réalisation, l'invention concerne également un procédé de fabrication des anticorps ou de l'un de leurs fragments fonctionnels tels que définis ci-dessus, caractérisé en ce qu'il consiste à : al ) faire réagir une molécule de formule CH3-(CH2)n-CO-O-CO-(CH2)n-CH3 où n vaut 1 ou 2 avec une molécule porteuse afin de substituer les motifs lysyl de ladite molécule porteuse, bl) récupérer du plasma/sérum dudit animal auquel ladite molécule porteuse ainsi substituée a été préalablement injecté, cl) sélectionner les anticorps spécifiques des motifs lysyl substitués réalisés à l'étape al) à l'aide d'un ou plusieurs épitopes de formule (I) tels que définis ci-dessus, dl) éventuellement purifier les anticorps selon les méthodes classiques.Thus, the antibodies according to the present invention, obtained from said synthon, are specific for their epitope directly after their production, without requiring the use of other techniques such as the depletion of polyclonal antibodies to obtain their high specificity vis- with respect to propionylated or butyrylated lysines. This presents a major advantage. In an alternative embodiment, the invention also relates to a method for manufacturing the antibodies or a functional fragment thereof as defined above, characterized in that it consists of: a) reacting a molecule of formula CH 3 - (CH 2) n -CO-O-CO- (CH 2 ) n -CH 3 where n is 1 or 2 with a carrier molecule in order to substitute the lysyl units of said carrier molecule, bl) recovering plasma / serum said animal to which said carrier molecule thus substituted has been injected beforehand; cl) selecting the antibodies specific for the substituted lysyl units produced in step a1) using one or more epitopes of formula (I) as defined above; above, dl) optionally purify the antibodies according to conventional methods.
L'étape al est réalisée comme suit : La molécule porteuse, de préférence BSA ou KLH est mise à réagir avec l'anhydride propionique ou butyrique, de formule CH3-(CH2)H-CO-O-CO-(CHi)n-CH3 où n vaut respectivement 1 ou 2, afin que les lysines de cette molécule porteuse réagissent pour former une molécule contenant des lysines substituées et plus précisément des lysines propionylées et/ou butyrylées. Cette molécule porteuse dont les lysines sont substituées est utilisée comme immunogène comportant les épitopes de formule (I) décrite ci-dessus.Step a1 is carried out as follows: The carrier molecule, preferably BSA or KLH, is reacted with propionic or butyric anhydride, of formula CH 3 - (CH 2 ) H -CO-O-CO- (CHi) n -CH 3 where n is 1 or 2 respectively, so that the lysines of the carrier molecule react to form a molecule containing substituted lysines and more specifically propionylées lysines and / or butyrylées. This carrier molecule, the lysines of which are substituted, is used as an immunogen comprising the epitopes of formula (I) described above.
Les étapes bl) à dl) sont identiques aux étapes c) à e) du procédé de fabrication d'anticorps ou de l'un de leurs fragments fonctionnels décrit ci-dessus.
La présente invention concerne également un procédé de fabrication des anticorps, ou d'un de leurs fragments fonctionnels, tels que définis ci-dessus, caractérisé en ce qu'il consiste à : a2) mettre en oeuvre un épitope de formule (I) dans laquelle au moins un des résidus R0 , R1 est différent de H ou R2 est différent de OH, b2) coupler ledit épitope à une molécule porteuse, c2) récupérer du plasma/sérum dudit animal auquel ledit couple épitope-molécule porteuse a été préalablement injecté, d2) sélectionner les anticorps spécifiques dudit épitope utilisé à l'étape a) à l'aide d'un ou plusieurs épitopes tels que définis dans la revendication 1, e2) éventuellement purifier les anticorps selon les méthodes classiques.Steps b1) to d1) are identical to steps c) to e) of the method of manufacturing antibodies or a functional fragment thereof described above. The present invention also relates to a method for manufacturing the antibodies, or a functional fragment thereof, as defined above, characterized in that it consists in: a2) implementing an epitope of formula (I) in which at least one of the residues R 0 , R 1 is different from H or R 2 is different from OH, b2) couple said epitope to a carrier molecule, c2) recovering plasma / serum from said animal to which said epitope-carrier molecule pair has has been previously injected, d2) select the specific antibodies of said epitope used in step a) using one or more epitopes as defined in claim 1, e2) optionally purify the antibodies according to conventional methods.
Les étapes b2) à e2) sont identiques aux étapes b) à e) décrites ci-dessus dans le procédé de réalisation des anticorps spécifiques du synthon lui-même et ne seront donc pas rappelées. La mise en œuvre d'un épitope tel que défini ci-dessus se fait par la réalisation, la fabrication extemporanée dudit épitope ou par l'utilisation d'un épitope répondant à la formule (I) déjà synthétisé selon les méthodes classiques de synthèse connues, de préférence les synthèses peptidiques ou protéiques.Steps b2) to e2) are identical to steps b) to e) described above in the method of making antibodies specific to the synthon itself and will therefore not be recalled. The implementation of an epitope as defined above is carried out by the production, the extemporaneous manufacture of said epitope or by the use of an epitope corresponding to the formula (I) already synthesized according to known conventional synthetic methods. preferably peptide or protein syntheses.
CompositionComposition
La présente invention concerne également une composition comprenant des anticorps, ou au moins l'un de leurs fragments fonctionnels, tels que définis ci-dessus, ou obtenus selon le procédé tel que défini précédemment.The present invention also relates to a composition comprising antibodies, or at least one of their functional fragments, as defined above, or obtained according to the process as defined above.
Ladite composition peut avantageusement comprendre des réactifs tels que des anticorps secondaires marqués ou non et des solutions de révélation ou de visualisation permettant de mettre en évidence les réactions anticorps-antigènes. Ladite composition peut également comprendre des excipients de différentes natures de type de ceux classiquement utilisés dans des compositions contenant des anticorps.Said composition may advantageously comprise reagents such as labeled or non-labeled secondary antibodies and revealing or visualization solutions making it possible to demonstrate the antibody-antigen reactions. Said composition may also comprise excipients of different types of type conventionally used in compositions containing antibodies.
Ladite composition, tout comme les anticorps selon l'invention, peuvent avantageusement être utilisés dans le domaine de la recherche, pour expliquer des phénomènes biologiques et tester l'efficacité desdits anticorps ou de la composition telle que définie ci-dessus. Par ailleurs, cette composition comprenant au moins des anticorps spécifiques de l'épitope de formule (I) exposée ci -dessus, peut être utilisée dans au moins l'une des applications suivantes : recherche, diagnostic, analyse, pronostic de pathologie, thérapeutique, test d'efficacité ou de toxicité d'un médicament. Parmi les pathologies liées à la propionylation et/ou la butyrylation de résidus lysine, on peut citer par exemple le cancer, les maladies neurodégénératives, le diabète et les pathologies inflammatoires.
Procédé et nécessaire de détection des épitopesSaid composition, just like the antibodies according to the invention, can advantageously be used in the field of research, to explain biological phenomena and to test the efficacy of said antibodies or of the composition as defined above. Moreover, this composition comprising at least antibodies specific for the epitope of formula (I) exposed above, can be used in at least one of the following applications: research, diagnosis, analysis, prognosis of pathology, therapeutic, test for efficacy or toxicity of a drug. Among the pathologies related to the propionylation and / or butyrylation of lysine residues, there may be mentioned, for example, cancer, neurodegenerative diseases, diabetes and inflammatory pathologies. Method and device for detecting epitopes
Selon un autre mode de réalisation, la présente invention concerne un procédé de détection, dans un échantillon biologique, in vitro ou in vivo, de l'épitope de formule (I) tel que défini précédemment, caractérisé en ce qu'il comprend les étapes suivantes : A) éventuellement fixer sur un support approprié les anticorps ou au moins l'un de leurs fragments fonctionnels tels que définis ci-dessus ou compris dans une composition telle que définie ci-dessus,According to another embodiment, the present invention relates to a method for detecting, in a biological sample, in vitro or in vivo, the epitope of formula (I) as defined above, characterized in that it comprises the steps following: A) optionally fix on a suitable support the antibodies or at least one of their functional fragments as defined above or included in a composition as defined above,
B) mettre en contact un échantillon biologique contenant potentiellement ledit épitope de formule (I) avec les anticorps ou au moins l'un de leurs fragments fonctionnels tels que définis précédemment ou tels que compris dans une composition telle que définie ci-dessus,B) contacting a biological sample potentially containing said epitope of formula (I) with the antibodies or at least one of their functional fragments as defined above or as included in a composition as defined above,
C) éventuellement effectuer au moins un lavage,C) optionally perform at least one wash,
D) détecter/révéler les complexes anticorps-épitope(s) de formule (I).D) detecting / revealing the antibody-epitope complexes of formula (I).
De préférence, au préalable, les anticorps selon la présente invention sont fixés sur un support essentiellement solide ou tout support réactionnel permettant de réaliser un test immunologique. La fixation au support est réalisée, de préférence, par adsorption ou liaison covalente. Une éventuelle étape de lavage permet de supprimer après ladite fixation les anticorps non fixés audit support le cas échéant. L'échantillon biologique concerné, à mettre en œuvre avec les anticorps selon l'invention, peut être toute substance susceptible de contenir ledit épitope en question de formule (I) telle qu'une substance solide ou liquide, comme par exemple un animal, un organe complet ou non, des cellules de tissus, des extraits nucléaires de cellules données, des extraits cytoplasmiques de cellules données, du sang, du plasma, du sérum, de la lymphe, de l'urine, de la salive. De préférence, on utilise du sérum. Lorsque l'échantillon contient des molécules contenant au moins un motif lysyl substitué répondant à la formule (I) et constituant un épitope, ces molécules via cet épitope vont se lier spécifiquement aux anticorps préalablement fixés sur support adapté. Un éventuel lavage permettra d'éliminer les anticorps non fixés au support et les complexes molécules-anticorps non spécifiques. Selon des méthodes connues de l'homme de l'art, l'anticorps spécifique peut être utilisé en phase liquide, en solution.Preferably, beforehand, the antibodies according to the present invention are fixed on a substantially solid support or any reaction support making it possible to carry out an immunological test. The attachment to the support is preferably carried out by adsorption or covalent bonding. A possible washing step makes it possible to eliminate, after said fixation, the antibodies not fixed to said support, if appropriate. The biological sample concerned, to be used with the antibodies according to the invention, may be any substance capable of containing said epitope in question of formula (I) such as a solid or liquid substance, such as for example an animal, a complete organ or not, tissue cells, nuclear extracts of given cells, cytoplasmic extracts of given cells, blood, plasma, serum, lymph, urine, saliva. Preferably, serum is used. When the sample contains molecules containing at least one substituted lysyl unit corresponding to formula (I) and constituting an epitope, these molecules via this epitope will bind specifically to the antibodies previously fixed on a suitable support. A possible wash will eliminate non-fixed antibodies to the support and non-specific antibody-molecule complexes. According to methods known to those skilled in the art, the specific antibody may be used in the liquid phase, in solution.
Dans le cadre du procédé et du nécessaire de détection des épitopes de formule (I) de la présente demande, les supports de réactions immunologiques utilisés peuvent être de nature différentes et sont choisis parmi : les lames, les microplaques, les latex fluorescents, les latex magnétiques, les membranes d'immuno-filtration ou les membranes d'immuno- migration, les biochips, les billes, les ailettes, les tubes mais également les liposomes, les vésicules lipidiques, les microparticules biologiques ou obtenues à partir de polymères, les émulsions.... et la méthode de détection de l'étape D) peut être déclinée en plusieurs
technologies telles que les tests ELISA, l'immunoturbidimétrie, l'agglutination de latex sur lame, la néphélométrie, la turbidimétrie, la turbidimétrie ou néphélométrie amplifiée par particules de latex, immunofluorescence (sur lame, microplaque, latex fluorescent, latex magnétique, test, sur membrane, biochips etc .. et de façon générale peut être utilisé tout procédé permettant d'identifier et/ou de quantifier une réaction entre un antigène et plus particulièrement un épitope et un anticorps, quelque soit l'isotype.In the context of the method and the kit for detecting the epitopes of formula (I) of the present application, the immunological reaction supports used may be of a different nature and are chosen from: slides, microplates, fluorescent latices, and latices. Magnetic membranes, immuno-filtration membranes or immuno-migration membranes, biochips, beads, fins, tubes but also liposomes, lipid vesicles, biological microparticles or obtained from polymers, emulsions .... and the detection method of step D) can be divided into several technologies such as ELISA, immunoturbidimetry, slide agglutination, nephelometry, turbidimetry, turbidimetry or latex particle amplified nephelometry, immunofluorescence (on slide, microplate, fluorescent latex, magnetic latex, test, on membrane, biochips etc .. and in general can be used any method for identifying and / or quantifying a reaction between an antigen and more particularly an epitope and an antibody, whatever the isotype.
Dans une variante, on peut utiliser des techniques permettant la détection directe des anticorps en tant que complexes anticorps-épitope telle que la réfractométrie, la diffraction de rayons lumineux par la surface réactionnelle, des méthodes de modification de la conductivité électrique ou du champ magnétique, etc...Alternatively, techniques for the direct detection of antibodies as antibody-epitope complexes such as refractometry, diffraction of light rays by the reaction surface, methods for modifying electric conductivity or magnetic field can be used. etc ...
De préférence, la réaction immunologique, à savoir la reconnaissance de l'anticorps ou d'au moins l'un de ses fragments fonctionnels selon l'invention avec l' épitope de formule (I), est suivie par une réaction indicatrice qui permet la détection photométrique de l'activité enzymatique liée au complexe anticorps-épitope de formule (I).Preferably, the immunological reaction, namely the recognition of the antibody or at least one of its functional fragments according to the invention with the epitope of formula (I), is followed by an indicator reaction which allows the photometric detection of the enzymatic activity linked to the antibody-epitope complex of formula (I).
Ces méthodes de détection du complexe anticorps-épitope de formule (I) permettent non seulement de détecter les épitopes de formule (I) présents dans un échantillon biologique donné in vitro ou in vivo mais elles permettent aussi de localiser et/ou quantifier ledit épitope au niveau subcellulaire ou moléculaire ainsi que d'estimer lesrôles biologiques potentiels de ces modifications post-traductionnelles détectées.These methods for detecting the antibody-epitope complex of formula (I) make it possible not only to detect the epitopes of formula (I) present in a given biological sample in vitro or in vivo, but they also make it possible to locate and / or quantify said epitope at subcellular or molecular level as well as to estimate the potential biological roles of these detected post-translational modifications.
La présente invention concerne également un nécessaire de détection, dans un échantillon biologique in vitro ou in vivo, de molécule contenant au moins l'épitope de formule (I) tel que défini ci-dessus, caractérisé en ce qu'il comprend : au moins un anticorps ou au moins l'un de ses fragments fonctionnels tels que définis ci-dessus, de préférence fixé sur un support et le matériel approprié et nécessaire pour détecter les complexes anticorps-épitopes de formule (I). Ce nécessaire permet de détecter de façon rapide et fiable la présence ou non de molécule comprenant au moins un épitope de formule (I)The present invention also relates to a detection kit, in a biological sample in vitro or in vivo, of a molecule containing at least the epitope of formula (I) as defined above, characterized in that it comprises: at least an antibody or at least one of its functional fragments as defined above, preferably fixed on a support and the appropriate material and necessary to detect the antibody-epitope complexes of formula (I). This kit makes it possible to quickly and reliably detect the presence or absence of a molecule comprising at least one epitope of formula (I)
Procédé et nécessaire de détection des auto-anticorpsMethod and kit for detecting autoantibodies
Ces modifications post-traductionnelles de propionylation et/ou butyrylation des lysines ont pu être observées in vitro. Grâce à la présente invention, il est désormais possible d'observer ces modifications in vivo. Elles peuvent engendrer des pathologies comme les pathologies inflammatoires, le cancer, des maladies neurodégénératives et le diabète. Une propionylation/butyrylation inadaptée d'un résidu lysine peut devenir un antigène in vivo et
donc induire une réaction immunitaire, la protéine défectueuse étant identifiée comme du non-soi. L'organisme développe alors des anticorps contre son propre organisme appelés auto-anticorps. En effet, dans la présente demande, le terme «auto-anticorps» désigne par exemple une immunoglobuline dirigée contre un constituant de l'organisme qui produit l'immunoglobuline (ou anticorps) en question. Selon la présente invention, il s'agit d'un anticorps dirigé contre un épitope de formule (I) telle que définie précédemment. Ces auto-anticorps produits induisent donc des pathologies auto-immunes et il peut s'avérer être très important de pouvoir diagnostiquer rapidement la présence ou non d'auto-anticorps in vivo chez un patient, pouvoir réaliser une analyse, un suivi de préférence sérologique et un pronostic vis-à-vis de pathologies. L'invention porte donc également sur un procédé de détection des auto-anticorps spécifiques des épitopes de formule (I) tels que définis ci-dessus, dans un échantillon biologique in vitro ou in vivo, de préférence un plasma ou un sérum, caractérisé en ce qu'il comprend les étapes suivantes :These post-translational modifications of propionylation and / or butyrylation of lysines could be observed in vitro. Thanks to the present invention, it is now possible to observe these modifications in vivo. They can cause pathologies such as inflammatory diseases, cancer, neurodegenerative diseases and diabetes. Inadequate propionylation / butyrylation of a lysine residue can become an antigen in vivo and therefore induce an immune reaction, the defective protein being identified as non-self. The body then develops antibodies against its own body called autoantibodies. Indeed, in the present application, the term "autoantibody" means for example an immunoglobulin directed against a constituent of the body that produces the immunoglobulin (or antibody) in question. According to the present invention, it is an antibody directed against an epitope of formula (I) as defined above. These autoantibodies thus induce autoimmune pathologies and it may prove to be very important to be able to rapidly diagnose the presence or absence of autoantibodies in vivo in a patient, to be able to perform an analysis, preferably a serological follow-up. and a prognosis for pathologies. The invention therefore also relates to a method for detecting specific autoantibodies of the epitopes of formula (I) as defined above, in a biological sample in vitro or in vivo, preferably a plasma or a serum, characterized in that what it includes the following steps:
Al) éventuellement fixer sur un support approprié au moins un épitope de formule (I),Al) optionally fixing on a suitable support at least one epitope of formula (I),
Bl) mettre en contact ledit épitope de formule (I), de préférence fixé sur un support approprié avec un échantillon biologique,B1) contacting said epitope of formula (I), preferably fixed on a suitable support with a biological sample,
Cl) éventuellement effectuer au moins un lavage,Cl) optionally carry out at least one wash,
Dl) détecter/révéler lesdits (éventuels) complexes auto-anticorps-épitopes de formule (I) par des moyens de détections appropriés.D1) detecting / revealing said (optional) autoantibody-epitope complexes of formula (I) by appropriate detection means.
De préférence, le support est solide mais il peut s'agir de tout support réactionnel permettant de réaliser un test immunologique. L'épitope de formule (I) est fixé sur un support adapté. Comme exposé plus haut, de préférence la fixation se fait par adsorbtion mais elle peut également être réalisée par liaison co val ente sur un support adapté. On veillera à ce que la quantité d' épitope de formule (I) fixée ne soit pas un facteur limitant afin que tous les auto-anticorps de l'échantillon à tester puissent ainsi s'y fixer spécifiquement.Preferably, the support is solid but it may be any reaction support for performing an immunological test. The epitope of formula (I) is attached to a suitable support. As stated above, preferably the attachment is by adsorption but it can also be performed by co val valent bond on a suitable support. It will be ensured that the amount of fixed epitope of formula (I) is not a limiting factor so that all the autoantibodies of the sample to be tested can thus be specifically attached thereto.
Les différents supports utilisables sont identiques à ceux utilisables et détaillés ci-dessus pour la mise en œuvre du procédé et du nécessaire de détection des épitopes de formule (I).The different supports that can be used are identical to those usable and detailed above for implementing the method and the kit for detecting epitopes of formula (I).
L'échantillon biologique à tester peut être toute substance biologique susceptible de contenir cesdits auto-anticorps spécifiques de l'épitope (I) comme des cellules des tissus, du sang, plasma, du sérum, de l'urine, de la salive .... De préférence, l'échantillon à tester est du plasma ou du sérum, dilué ou non, d'un patient contenant potentiellement des autoanticorps dirigés contre l'épitope de formule (I).
Les éventuels lavages ont pour but d'éliminer d'une part les épitopes non fixés sur le support, mais également et surtout d'éliminer les auto-anticorps libres ou fixés de façon non spécifique à leur épitope spécifique. Selon la présente invention, les différentes méthodes de détections utilisées sont qualitatives et/ou quantitatives. Ces méthodes de détection des complexes auto-anticorps-épitopes sont connues de l'homme du métier. Elles peuvent être déclinées en plusieurs technologies telles que celles exposées précédemment pour le procédé et le nécessaire de détection des épitopes de formule (1).The biological sample to be tested may be any biological substance capable of containing said epitope-specific autoantibodies (I) such as cells of the tissues, blood, plasma, serum, urine and saliva. Preferably, the sample to be tested is plasma or serum, diluted or not, of a patient potentially containing autoantibodies directed against the epitope of formula (I). The possible washes are intended to eliminate on the one hand the epitopes not fixed on the support, but also and especially to eliminate the free autoantibodies or non-specifically fixed to their specific epitope. According to the present invention, the different detection methods used are qualitative and / or quantitative. These methods for detecting autoantibody-epitope complexes are known to those skilled in the art. They can be broken down into several technologies such as those set out above for the process and the kit for detecting epitopes of formula (1).
La présente invention porte également sur un nécessaire de détection des auto-anticorps spécifiques des épitopes de formule (I) tels que définis ci-dessus, dans un échantillon biologique in vitro ou in vivo, de préférence un plasma ou un sérum, caractérisé en ce qu'il comprend :The present invention also relates to a kit for detecting autoantibodies specific for the epitopes of formula (I) as defined above, in a biological sample in vitro or in vivo, preferably a plasma or a serum, characterized in that that he understands:
- au moins un épitope de formule (I) tel que défini ci-dessus et - le matériel approprié et nécessaire pour détecter/révéler les complexes anticorps- épitopes de formule (I).at least one epitope of formula (I) as defined above and the appropriate material necessary to detect / reveal the antibody-epitope complexes of formula (I).
Dans le cadre de la mise en œuvre du procédé et du nécessaire de détection des autoanticorps selon l'invention, est utilisée l'une des différentes méthodes de détection citées ci-dessus dans le cadre de la mise en œuvre du procédé ou du nécessaire de détection des épitopes de formule (I).In the context of the implementation of the method and the autoantibody detection kit according to the invention, one of the different detection methods mentioned above is used in the context of the implementation of the method or kit of detection of epitopes of formula (I).
Grâce audit nécessaire de détection des auto-anticorps, il est ainsi plus simple, plus facile et plus rapide d'établir un diagnostic d'éventuelles pathologies induites par les lysines substituées par un résidu propionyl ou butyryl, de réaliser un suivi et une analyse de la pathologie et surtout de la sérologie du patient à surveiller, d'évaluer l'efficacité et la toxicité d'un médicament ou d'une composition ciblant par exemple ces auto-anticorps ou d'utiliser ces auto-anticorps en recherche.Thanks to said auto-antibody detection kit, it is thus simpler, easier and faster to establish a diagnosis of possible pathologies induced by lysines substituted with a propionyl or butyryl residue, to carry out monitoring and analysis of the pathology and especially the serology of the patient to monitor, evaluate the efficacy and toxicity of a drug or a composition targeting for example these autoantibodies or use these autoantibodies in research.
ExemplesExamples
Les exemples qui suivent illustrent la présente demande.The following examples illustrate the present application.
L'invention sera mieux comprise si l'on se réfère aux figures annexées dans lesquels : la figure 1 représente deux courbes de titration de sérum de lapin anti-lysine propionylée. la figure 2 représente deux courbes de titration de sérum de lapin anti-lysine butyrylée.
la figure 3 représente une photographie d'une analyse en western blot de la réaction d'acétylation des histones H3 et H4 révélée grâce à des anticorps anti-acétyl. la figure 4 représente une photographie d'une analyse en western blot de la réaction de propionylation des histones H3 et H4 révélée grâce aux anticorps objet de l'invention.The invention will be better understood with reference to the accompanying figures in which: Figure 1 shows two titration curves of rabbit anti-lysine propionylated serum. Figure 2 shows two titration curves of rabbit anti-lysine butyrylated serum. FIG. 3 represents a photograph of a Western blot analysis of the acetylation reaction of histones H3 and H4 revealed by means of anti-acetyl antibodies. FIG. 4 represents a photograph of a western blot analysis of the propionylation reaction of the H3 and H4 histones revealed by the antibodies that are the subject of the invention.
La figure 5 représente une photographie d'une analyse en western blot de la réaction de propionylation des histones H3 et H4 en présence ou non de différents co facteurs et révélée grâce aux anticorps objet de l'invention.FIG. 5 represents a photograph of a western blot analysis of the propionylation reaction of histones H3 and H4 in the presence or absence of various co-factors and revealed by means of the antibodies which are the subject of the invention.
La figure 6 représente une photographie d'une analyse en western blot de la détection de la propionylation naturelle des histones H2A révélée grâce aux anticorps objet de l'invention.FIG. 6 represents a photograph of a Western blot analysis of the detection of the natural propionylation of H2A histones revealed by the antibodies that are the subject of the invention.
Exemple 1 : Procédé de préparation des anticorps polyclonaux spécifiques de l'épitope de formule (I)Example 1 Process for the Preparation of Polyclonal Antibodies Specific for the Epitope of Formula (I)
1.1 Préparation des épitopes de formule (I) (étape al) pour la production des immunogènes et des antigènes.1.1 Preparation of epitopes of formula (I) (step a1) for the production of immunogens and antigens.
1.1. a/ Préparation des immunogènes (KLH) contenant les motifs lysyl acylés (propionylés et/ou butyrylés) pour l'immunisation des animaux.1.1. a / Preparation of immunogens (KLH) containing lysyl acylated units (propionyl and / or butyrylated) for the immunization of animals.
Cette préparation a été décrite dans l'article suivant :Thomas V et al, dans J ImmunolThis preparation has been described in the following article: Thomas V et al, in J Immunol
Methods. 2004 Sep;292(l-2):83-95.Methods. 2004 Sep; 292 (1-2): 83-95.
Brièvement, les antigènes KLH propionylé et KLH butyrylé ont été préparés comme suit :Briefly, the propionylated KLH and butyrylated KLH antigens were prepared as follows:
KLH propionylée : 2mg de KLH solubilisée dans 1 ml de tampon bicarbonate 0.1 M pH 9,5 ont été mis en contact avec 0,7 mmoles d'anhydride propionique (CH3-(CHa)-CO-O-Propionylated KLH: 2 mg of KLH solubilized in 1 ml of 0.1 M bicarbonate buffer pH 9.5 were brought into contact with 0.7 mmol of propionic anhydride (CH 3 - (CHa) -CO-O-
CO-(CHo)-CH3). Après une incubation de 2 heures à 22°C, la protéine modifiée, substituée par des radicaux propionyl sur les motifs lysyl est dialysée 3 fois contre 2 litres de tamponCO- (CHo) -CH 3 ). After incubation for 2 hours at 22 ° C., the modified protein, substituted with propionyl radicals on the lysyl units, is dialysed 3 times against 2 liters of buffer.
PBS.PBS.
KLH butyrylée .'2mg de KLH solubilisée dans 1 ml tampon bicarbonate 0.1 M pH 9,5 ont été mis en contact avec 0,7 mmoles d'anhydride butyrique (CH3-(CHa)a-CO-O-CO-(CHa)2- CH3). Après une incubation de 2 heures à 22°C, la protéine modifiée, substituée par des radicaux butyryl sur les motifs lysyl est dialysée 3 fois contre 2 litres de PBS.KLH butyrylated .2 mg of KLH solubilized in 1 ml of 0.1 M bicarbonate buffer pH 9.5 were brought into contact with 0.7 mmol of butyric anhydride (CH 3 - (CH 2 ) a-CO-O-CO- (CH 3 ) ) 2 - CH 3 ). After incubation for 2 hours at 22 ° C., the modified protein substituted with butyryl radicals on the lysyl units is dialyzed 3 times against 2 liters of PBS.
1.1. b/ Préparation des antigènes (BSA) contenant les motifs lysyl acylés (propionylés et/ou butyrylés) pour le test ELISA.1.1. b / Preparation of antigens (BSA) containing lysyl acylated units (propionyl and / or butyrylated) for the ELISA test.
Pour obtenir la protéine BSA propionylée (BP), la même procédure et les mêmes proportions que pour KHL propionylée ci-dessus sont utilisées.
Pour obtenir la protéine BSA butyrylée (BB), la même procédure et les mêmes proportions que pour KLH butyrylée ci-dessus sont utilisées.To obtain the propionylated BSA protein (BP), the same procedure and the same proportions as for propionylated KHL above are used. To obtain the butyrylated BSA protein (BB), the same procedure and the same proportions as for butyrylated KLH above are used.
Pour obtenir la protéine BSA acétylée (BA), la même procédure et les mêmes proportions que décrite dans Thomas V. et al dans J Immunol Methods. 2004 Sep;292(l-2):83-95 sont utilisées.To obtain the acetylated BSA protein (BA), the same procedure and the same proportions as described in Thomas V. et al in J Immunol Methods. 2004 Sep; 292 (1-2): 83-95 are used.
1.1. c/ Contrôle du degré d'acylation par dosage spectrophotométrique des aminés primaires.1.1. c / Control of the degree of acylation by spectrophotometric assay of the primary amines.
A 50 μl des solutions de BSA native et de BSA acylée (BP, BB) (2mg/ml) sont ajoutés 50 μl d'une solution de tétraborate de sodium saturée et 50 μl d'acide 2, 4, 6-trinitrobenzène sulfonique (0.ImM). L'acide 2, 4, 6-trinitrobenzène sulfonique est un réactif qui permet le dosage colorimétrique des aminés primaires. L'acylation consiste à former sur les aminés primaires et notamment sur les résidus εNH2 de la lysine de la BSA des liaisons amides. Les résidus amidés ne sont pas réactifs avec l'acide 2, 4, 6-trinitrobenzène sulfonique, il s'ensuit qu'une diminution d'absorbance est proportionnelle au degré d'acylation, cette technique de dosage permet donc de calculer le pourcentage d'aminés acylées. Après 30 minutes de réaction, l'absorbance à 420 nm est mesurée par spectrophotométrie. La diminution d'absorbance par rapport à celle obtenue avec la BSA native est exprimée en pourcentage.To 50 μl of solutions of native BSA and of acylated BSA (BP, BB) (2 mg / ml) are added 50 μl of a solution of saturated sodium tetraborate and 50 μl of 2,4,6-trinitrobenzene sulphonic acid ( 0.ImM). 2,4,6-trinitrobenzene sulphonic acid is a reagent that allows the colorimetric assay of primary amines. The acylation consists of forming amide bonds on the primary amines and in particular on the εNH 2 residues of the lysine of the BSA. The amidated residues are not reactive with 2,4,6-trinitrobenzene sulphonic acid, it follows that a decrease in absorbance is proportional to the degree of acylation, this assay technique therefore makes it possible to calculate the percentage of acylated amines. After 30 minutes of reaction, the absorbance at 420 nm is measured spectrophotometrically. The decrease in absorbance compared to that obtained with the native BSA is expressed as a percentage.
Tableau 1 : Degré d'acylation des protéines par dosage spectro-photométrique des aminés primaires.Table 1: Degree of acylation of proteins by spectrophotometric assay of primary amines.
Le tableau 1 montre que pour les 2 antigènes synthétisés (BSA propionylée et BSA butyrylée), l'acylation est pratiquement totale, il en résulte que la quasi totalité des groupements εNH2 accessibles de la lysine présents sur la BSA sont acylés.Table 1 shows that for the 2 synthesized antigens (propionylated BSA and butyrylated BSA), the acylation is almost complete, it follows that almost all of the accessible εNH 2 groups of lysine present on the BSA are acylated.
1.2 Immunisation des animaux 4 lapins femelles New Zealand de 2,5 Kg ont reçu 4 injections par voies intra-dermique et sous-cutanée aux jours JO, J 14, J28 et J74 de ImI d'un mélange (50%/50%) d'une solution contenant lOOμg de l'immunogène KLH-propionylé (2 lapins) et KLH-butyrylé (2 lapins) et de l'adjuvant de Freund selon le protocole d'immunisation dans le tableau ci-dessous.
Des prélèvements réguliers (à J53, J74 et J90) de sang ont été effectués pour contrôler la réponse immunitaire (étape cl). Ce sang est laissé à coaguler pendant 30 minutes puis est centrifugé pendant 10 minutes à 2500 tours par min afin de récupérer le sérum et tester l'immuno-réactivié des anticorps (étape bl).1.2 Immunization of Animals 4 New Zealand female rabbits weighing 2.5 kg received 4 injections intradermally and subcutaneously on days JO, D14, D28 and J74 of ImI of a mixture (50% / 50%). a solution containing 100 μg of the immunogen KLH-propionyl (2 rabbits) and KLH-butyryl (2 rabbits) and Freund's adjuvant according to the immunization protocol in the table below. Regular blood samples (at days 53, 74 and 90) were taken to control the immune response (step c1). This blood is allowed to coagulate for 30 minutes and then is centrifuged for 10 minutes at 2500 rpm to recover the serum and test the immuno-reactivated antibodies (step b1).
1.3- Sélection des anticorps spécifiques de l'épitope dans les sérums (étape cl)1.3- Selection of antibodies specific for the epitope in the sera (step c)
Les anticorps spécifiques des motifs lysyl substitués ont été sélectionnés dans le sérum avec l'épitope de formule (I) produits ci-dessus grâce à la détermination de l'immunoréactivité du sérum de lapin par la technique ELISA (étape cl).The antibodies specific for the substituted lysyl units were selected in the serum with the epitope of formula (I) produced above by determining the immunoreactivity of the rabbit serum by the ELISA technique (step c1).
Les antigènes BP ou BB sont adsorbés sur des plaques 96 puits en polystyrène. Pour ce faire, lOOμl d'une solution lOμg/ml de chaque antigène en tampon bicarbonate 0.1 M pH 9,5 sont distribués par puits. Après une incubation de 2 heures à 37°C, les puits sont vidés et un dépôt de 150 μl/puits d'une solution de BSA 0.5% dans du tampon PBS est réalisé dans le but de saturer les sites d'adsorption excédentaires sur le plastique. Cette étape de saturation nécessite une incubation d'une heure à 37°C. A ce stade, les plaques sont prêtes pour le dépôt des sérums. Pour ce test, les sérums sont utilisés à partir de la dilution de 1/500 en tampon PBS contenant du tween-20 à 0.1%. Ces solutions sont déposées puis dilués de deux en deux directement sur la plaque (1/500, 1/1000, 1/2000 ...) de façon à obtenir 100 μl/ puits de volume final.BP or BB antigens are adsorbed on 96-well polystyrene plates. To do this, 100 μl of a solution 10 μg / ml of each antigen in 0.1 M bicarbonate buffer pH 9.5 are distributed per well. After incubation for 2 hours at 37 ° C., the wells are emptied and a deposit of 150 μl / well of a 0.5% BSA solution in PBS buffer is prepared in order to saturate the excess adsorption sites on the surface. plastic. This saturation step requires an incubation of one hour at 37 ° C. At this stage, the plates are ready for the deposition of the sera. For this test, the sera are used starting from the 1/500 dilution in PBS buffer containing 0.1% tween-20. These solutions are deposited and then diluted two by two directly on the plate (1/500, 1/1000, 1/2000 ...) so as to obtain 100 μl / well of final volume.
Après une heure d'incubation à 37°C, les plaques sont lavées 3 fois avec du PBS tween. Un anticorps de mouton anti IgG (H+L) de lapin marqué à la peroxydase et déposé à raison de 100 μl/puits et laissé 30 min. à 370C. Les plaques sont alors lavées comme précédemment par 3 lavages successifs pour éliminer l'excédent de réactif. L'activité peroxydase est révélée en utilisant le réactif eau oxygénée/tetraméthylbenzidine (TMB) (Covalab). La réaction est stoppée avec lOOμl de H2 SO4 (2N). L'absorbance est mesurée sur lecteur de plaque à 450 nm.
1.4-purification des anticorps (étape el)After one hour of incubation at 37 ° C., the plates are washed 3 times with PBS tween. An anti-rabbit IgG (H + L) sheep antibody labeled with peroxidase and deposited at a rate of 100 μl / well and left for 30 min. at 37 ° C. The plates are then washed as previously by 3 successive washes to remove the excess reagent. The peroxidase activity is revealed using the hydrogen peroxide / tetramethylbenzidine (TMB) reagent (Covalab). The reaction is stopped with 100 μl of H 2 SO 4 (2N). The absorbance is measured on a plate reader at 450 nm. 1.4-purification of the antibodies (step el)
Les étapes d'immuno-purification des anticorps sont réalisées suivant les protocoles décrits dans la publication Thomas V et al dans J Immunol Methods. 2004 Sep;292 (l-2):83-95.The immuno-purification steps of the antibodies are carried out according to the protocols described in the publication Thomas V et al in J. Immunol Methods. 2004 Sep; 292 (1-2): 83-95.
1.5- Résultats : Détermination de l'immunoréactivité des sérums de lapin par ELISA1.5- Results: Determination of the immunoreactivity of rabbit sera by ELISA
5 .1- Sélection des anticorps de lapin anti N-ε-propionyl-L-Lysine avec la BSA acétylée (BA) ou la BSA propionylée (BP).5 .1- Selection of anti-N-ε-propionyl-L-Lysine rabbit antibodies with acetylated BSA (BA) or propionylated BSA (BP).
Tableau 2 : Mesures de densité optique suivant les dilutions des sérums. Le tableau 2 reflète l'immunoréactivité des sérums de lapin contenant les anticorps spécifiques des lysines propionylées et/ou butyrylées, vis-à-vis de la BSA acétylée et de la BSA propionylée. La BSA propionylée forme un complexe avec les anticorps spécifiques de la lysine propionylée (absorbance élevée).Table 2: Optical density measurements according to the dilutions of the sera. Table 2 reflects the immunoreactivity of rabbit sera containing antibodies specific for propionylated and / or butyrylated lysines, vis-à-vis acetylated BSA and propionylated BSA. Propionylated BSA forms a complex with antibodies specific for propionylated lysine (high absorbance).
La figure 1 illustre l'immunoréactivité des sérums vis-à-vis de deux antigènes : BSA acétylée et BSA propionylée. L'axe des ordonnées représente les valeurs de densités optiques mesurées à 450 nm et l'axe des abscisses représente les différentes dilutions du sérum. Cette figure 1 illustre le fait que les sérums contiennent des anticorps spécifiques des lysines propionylées. En effet, les anticorps obtenus et contenus dans le sérum réagissent fortement avec le motif lysyl propionylé contenu dans l'antigène BP (absorbance de 1.647 à la dilution 1/2000 du sérum) alors qu'ils ne réagissent pas ou très peu avec le motif lysyl acétylé contenu dans l'antigène BA (absorbance de 0.250 à la dilution 1/2000 du sérum). Ces anticorps permettent de différencier la N-ε-propionyl-L- lysine de la N-ε-acétyl-L-lysine et sont donc hautement spécifiques des lysines propionylées.
5.2-Sélection des anticorps de lapin anti N-ε-butyryl-L-lysine avec la BSA acétylée (BA) ou la BSA butyrylée (BB).Figure 1 illustrates the immunoreactivity of sera against two antigens: acetylated BSA and propionylated BSA. The ordinate axis represents optical density values measured at 450 nm and the x-axis represents the different dilutions of the serum. This figure 1 illustrates that the sera contain antibodies specific for propionylated lysines. In fact, the antibodies obtained and contained in the serum react strongly with the lysylpropionyl unit contained in the BP antigen (absorbance of 1.647 at the 1/2000 dilution of the serum), whereas they do not react or very little with the motif. acetylated lysyl contained in BA antigen (absorbance of 0.250 at 1/2000 dilution of serum). These antibodies make it possible to differentiate N-ε-propionyl-L-lysine from N-ε-acetyl-L-lysine and are therefore highly specific for propionylated lysines. 5.2-Selection of anti-N-ε-butyryl-L-lysine rabbit antibodies with acetylated BSA (BA) or butyrylated BSA (BB).
Tableau 3 : Mesures de densité optique suivant les dilutions des sérums. Le tableau 3 reflète l'immunoréactivité des sérums de lapin contenant les anticorps spécifiques des lysines propionylées et/ou butyrylées, vis-à-vis de la BSA acétylée et de la BSA butyrylée. La BSA butyrylée forme un complexe avec les anticorps spécifiques de la lysine butyrylée (absorbance élevée).Table 3: Optical density measurements according to the dilutions of the sera. Table 3 reflects the immunoreactivity of rabbit sera containing antibodies specific for propionylated and / or butyrylated lysines against acetylated BSA and butyrylated BSA. Butyrylated BSA forms a complex with antibodies specific for butyrylated lysine (high absorbance).
La figure 2 illustre l'immunoréactivité des sérums vis-à-vis de deux antigènes : BSA acétylée et BSA butyrylée. L'axe des ordonnées représente les valeurs de densités optiques mesurées à 450 nm et l'axe des abscisses représente les différentes dilutions du sérum. Cette figure 2 illustre le fait que les sérums contiennent des anticorps spécifiques des lysines butyrylées. En effet, les anticorps obtenus et contenus dans le sérum réagissent avec le motif lysyl butyrylé contenu dans l'antigène BB (absorbance de 1.558 à la dilution 1/500 du sérum) alors qu'ils ne réagissent pas avec le motif lysyl acétylé contenu dans l'antigène BA (absorbance de 0.158 à la dilution 1/500 du sérum). Ces anticorps permettent de différentier la N-ε-butyryl-L-Lysine de la N-ε-acétyl-L-lysine et sont donc hautement spécifiques des lysines butyrylées.Figure 2 illustrates the immunoreactivity of sera against two antigens: acetylated BSA and butyrylated BSA. The ordinate axis represents optical density values measured at 450 nm and the x-axis represents the different dilutions of the serum. This figure 2 illustrates that the sera contain antibodies specific for butyrylated lysines. In fact, the antibodies obtained and contained in the serum react with the lysyl butyryl unit contained in the BB antigen (absorbance of 1.558 at the 1/500 dilution of the serum) whereas they do not react with the acetylated lysyl motif contained in BA antigen (absorbance of 0.158 at 1/500 dilution of serum). These antibodies make it possible to differentiate N-ε-butyryl-L-Lysine from N-ε-acetyl-L-lysine and are therefore highly specific for butyrylated lysines.
Exemple 2. Procédé de production des anticorpsExample 2. Method of producing the antibodies
Le synthon est obtenu selon les méthodes décrites par M. Bashir Uddin Surfraz et al dans J. Med. Chem. 2007, 50, 1418-1422 et par Takeshi M.et al dans Biomacromolecules, 2007, 8, 318-321.The synthon is obtained according to the methods described by M. Bashir Uddin Surfraz et al in J. Med. Chem. 2007, 50, 1418-1422 and by Takeshi M. et al in Biomacromolecules, 2007, 8, 318-321.
5 mg de synthon lysyl propionylée et/ou butyrylée est couplé à 2 mg de BSA ou KLH en utilisant le carbodiimide comme agent de couplage pour conjuguer les synthons par les domaines alpha acide carboxylique laissés libres pour la réalisation dudit couplage selon la technique décrite par Thomas V et al dans J Immunol Methods. 2004 Sep;292 (l-2):83-95.
L'immunogène ainsi préparé est injecté aux animaux dans les mêmes conditions et modes opératoires décrits dans l'exemple 1.5 mg of lysylpropionylated and / or butyrylated synthon is coupled to 2 mg of BSA or KLH using carbodiimide as coupling agent to conjugate the synthons by the alpha carboxylic acid domains left free for carrying out said coupling according to the technique described by Thomas V et al in J Immunol Methods. 2004 Sep; 292 (1-2): 83-95. The immunogen thus prepared is injected into the animals under the same conditions and procedures described in Example 1.
Exemple 3. Etude de la spécificité des anticorps anti propionyl et anti butyryl sur les histones modifiés in vitro et in vivo et procédé de détection de l'épitope de formule (I)Example 3 Study of the Specificity of the Anti-Propionyl and Anti-Butyryl Antibodies on the In Vitro and In Vivo Modified Histones and the Method for Detecting the Epitope of the Formula (I)
La préparation des histones, les électrophorèses en gel de polyacrylamide et les western- blots ont été réalisés selon la méthode référencée dans Bannister AJ et Kouzarides T, Nature. 1996 Dec 19-26;384 (6610):641-3. Les anticorps appropriés utilisés sont l'anticorps monoclonal anti acétyl lysine (clone HAl mab0019-Covalab) et les anticorps polyclonaux de lapin anti priopionyl et anti butyryl (objet de l'invention). Les réactions enzymatiques des histones acétyl tranférases P/CAF et PCB ont été réalisées selon la méthode décrite par Bannister AJ et Kouzarides T dans Nature. 1996 Dec 19- 26;384 (6610):641-3 en ajoutant dans le milieu réactionnel les cofacteurs acétyl CoA, propionyl CoA ou le butyryl-CoA à la concentration finales de lOOμM.Preparation of histones, polyacrylamide gel electrophoresis and western blots were carried out according to the method referenced in Bannister AJ and Kouzarides T, Nature. 1996 Dec 19-26; 384 (6610): 641-3. The appropriate antibodies used are the anti-acetyl lysine monoclonal antibody (HA1 clone mab0019-Covalab) and the anti-priopionyl and anti-butyryl rabbit polyclonal antibodies (object of the invention). The enzymatic reactions of the histones acetyl tranferases P / CAF and PCB were carried out according to the method described by Bannister AJ and Kouzarides T in Nature. 1996 Dec 19-26; 384 (6610): 641-3 by adding to the reaction medium the acetyl CoA, propionyl CoA or final butyryl-CoA cofactors of 100 μM.
Traitement des cellules HL60: Les cellules HL60 ont été incubées avec 1.5μM de Trichostatin A (TSA) un inhibiteur des histones désacétylase, pendant 5 heures. Les cellules sont ensuite lavées 3 fois avec du tampon PBS et centrifugées à 13 000g. Le culot cellulaire est ensuite resuspendu dans le tampon IPH (5OmM Tris pH 8, 15OmM Nacl, 5mM EDTA, 5% NP-40, 1.5uM TSA) puis la suspension est laissée pendant 15 min à 4°C. Les tubes sont ensuite centrifugés à 13 000g pendant 10min. Le culot chromatinien est ensuite repris dans le tampon d'électrophorèse comme décrit précédemment pour réaliser les western blot.Treatment of HL60 cells: HL60 cells were incubated with 1.5 μM Trichostatin A (TSA) a histone deacetylase inhibitor for 5 hours. The cells are then washed 3 times with PBS buffer and centrifuged at 13,000 g. The cell pellet is then resuspended in IPH buffer (50mM Tris pH 8, 15OmM NaCl, 5mM EDTA, 5% NP-40, 1.5uM TSA) and the suspension is left for 15 min at 4 ° C. The tubes are then centrifuged at 13,000 g for 10 min. The chromatin pellet is then taken up in the electrophoresis buffer as described previously to carry out the western blot.
Résultats:Results:
- la figure 3 illustre la réaction d'acétylation des histones H3 et H4 des cellules HL60 par les Histone AcétylTransférases HATs (P/CAF & CBP) en présence (+) ou non (-) de l'inhibiteur TSA. La révélation est réalisée avec l'anticorps monoclonal anti acétyl lysine (mab0019). Conclusion : La réaction de contrôle pour vérifier le modèle de modification post- traductiormelle des histones in vitro montre clairement une acétylation importante des histones H3 et H4. L'addition du TSA exerce un effet inhibiteur de l'enzyme HDAC puisque l'intensité du marquage est plus importante. Ces résultats sont en parfaite concordance avec la littérature et valide bien le système utilisé. - la figure 4 illustre la réaction de propionyl ation des histones H3 et H4 des cellules HL60 par les Histones AcétylTransférases HATs (P/CAF & CBP) en présence (+) ou non (-) de l'inhibiteur TSA. La révélation est réalisée avec l'anticorps polyclonal de lapin anti lysine propionylée (objet de l'invention).
Conclusion : Dans les conditions de modification post-traductionnelles des cellules HL60 démontrées sur la figure 3, ces résultats montrent bien une propionylation des histones H3 et H4. L'addition de TSA montre que l'enzyme HDCA exerce un effet sur la propionylation, à savoir une dépropionylation des lysines des histones. - la figure 5 illustre la réaction de propionylation des histones H3 et H4 des cellules HL60 par les Histones AcétylTransférases HATs (P/CAF & CBP) en présence de : acétyl-CoA (Ac), propionyl-CoA (Pr), butyryl-CoA (Bu) ou sans cofacteur (-). La révélation est réalisée avec l'anticorps polyclonal de lapin anti lysine propionylé (objet de l'invention). Conclusion : Les anticorps polyclonaux anti lysine propionylée reconnaissent spécifiquement les histones H3 et H4 propionylées par l'action des HATs (P/CAF et CBP). Il n'y a pas de réaction croisée des anticorps anti-lysine propionylée avec les histones acétylées ou butyrylées.FIG. 3 illustrates the acetylation reaction of the histones H3 and H4 of the HL60 cells by the Histone Acetyl Transferases HATs (P / CAF & CBP) in the presence (+) or not (-) of the TSA inhibitor. The revelation is carried out with the anti-acetyl lysine monoclonal antibody (mab0019). Conclusion: The control reaction to verify the model of posttranslational histone modification in vitro clearly shows significant acetylation of H3 and H4 histones. The addition of TSA exerts an inhibitory effect on the HDAC enzyme since the intensity of labeling is greater. These results are in perfect agreement with the literature and validate the system used. FIG. 4 illustrates the propionylation reaction of the histones H3 and H4 of the HL60 cells by the histones acetyl transferases HATs (P / CAF & CBP) in the presence (+) or not (-) of the TSA inhibitor. The revelation is carried out with the polyclonal rabbit anti-lysine propionylated antibody (object of the invention). Conclusion: In the post-translational modification conditions of the HL60 cells demonstrated in FIG. 3, these results clearly show a propionylation of the histones H3 and H4. The addition of TSA shows that the HDCA enzyme has an effect on propionylation, namely a depropionylation of histone lysines. FIG. 5 illustrates the propionylation reaction of the histones H3 and H4 of the HL60 cells by the histones acetyl transferases HATs (P / CAF & CBP) in the presence of: acetyl-CoA (Ac), propionyl-CoA (Pr), butyryl-CoA (Bu) or without cofactor (-). The revelation is carried out with the polyclonal rabbit anti-lysine propionylated antibody (object of the invention). Conclusion: Anti-lysine propionylated polyclonal antibodies specifically recognize H3 and H4 histone propionylated by the action of HATs (P / CAF and CBP). There is no cross reaction of anti-lysine propionylated antibodies with acetylated or butyrylated histones.
- la figure 6 illustre la détection des histones H2A naturellement propionylées des cellules HL60 en présence (+) ou non (-) de l'inhibiteur TSA. La révélation est réalisée avec l'anticorps polyclonal de lapin anti lysine propionylée (objet de l'invention).FIG. 6 illustrates the detection of naturally propionylated H2A histones of HL60 cells in the (+) or non (-) presence of the TSA inhibitor. The revelation is carried out with the polyclonal rabbit anti-lysine propionylated antibody (object of the invention).
Conclusion : L'anticorps polyclonal de lapin anti lysine propionylée permet de détecter une propionylation naturelle de l'histone H2A dans les cellules HL60. La propionylation est légèrement affectée par l'action de l'HDAC comme le montre le résultat obtenu avec l'addition du TSA. Les anticorps de l'invention peuvent également être utilisés en immunohistochimie ou immunocytologie pour la détection des épitopes de formule (I) selon la technique décrite dans Roch et al Int J Cancer. 1991 May 10;48(2):215-20.Conclusion: The polyclonal rabbit anti-lysine propionylated antibody detects a natural propionylation of histone H2A in HL60 cells. Propionylation is slightly affected by the action of HDAC as shown by the result obtained with the addition of TSA. The antibodies of the invention can also be used in immunohistochemistry or immunocytology for the detection of epitopes of formula (I) according to the technique described in Roch et al. 1991 May 10; 48 (2): 215-20.
Exemple 4 : Procédé de détection des auto-anticorps spécifiques des épitopes de formule (I)Example 4 Method for Detecting Specific Autoantibodies of the Epitopes of Formula (I)
Le même procédé décrit dans l'exemple 1.3 ci-dessus est utilisé pour détecter les autoanticorps dans un échantillon et en particulier dans un sérum. Les antigènes BP ou BB sont adsorbés sur des plaques 96 puits en polystyrène. Pour ce faire, lOOμl d'une solution lOμg/ml de chaque antigène en tampon bicarbonate 0.1 M pH 9,5 sont distribués par puits. Après une incubation de 2 heures à 370C, les puits sont vidés et un dépôt de 150 μl/puits d'une solution de BSA 0.5% dans du tampon PBS est réalisé dans le but de saturer les sites d'adsorption excédentaires sur le plastique. Cette étape de saturation nécessite une incubation d'une heure à 37°C. A ce stade, les plaques sont prêtes pour le dépôt du sérum à tester. Pour ce test, le sérum à tester est un sérum humain prélevé puis utilisé à différentes dilutions en PBS tween 20 0.1%. Cette solution est déposée puis diluée de deux en deux directement sur la plaque (1/50,1/100, 1/200, ) de façon à obtenir 100 μl/ puits de volume final. Après une heure d'incubation à 37°C, les plaques
sont lavées 3 fois avec du PBS contenant du tween-20 à 0.1%. Un anticorps de mouton anti IgG (H+L) humaine marqué à la peroxydase et déposé à raison de 100 μl/puits et laissé 30 min. à 37°C. Les plaques sont alors lavées par 3 lavages successifs pour éliminer l'excédent de réactif (anticorps de mouton).Lesdits éventuels complexes épitopes-auto- anticorps sont révélés grâce au substrat de la peroxydase. L'activité peroxydase est révélée en utilisant le réactif eau oxygénée/tetraméthylbenzidine (TMB) (Covalab). La réaction est stoppée avec lOOμl de H2 SO4 (2N). L'absorbance est mesurée sur lecteur de plaque à 450 nm.
The same method described in Example 1.3 above is used to detect autoantibodies in a sample and in particular in a serum. BP or BB antigens are adsorbed on 96-well polystyrene plates. To do this, 100 μl of a solution 10 μg / ml of each antigen in 0.1 M bicarbonate buffer pH 9.5 are distributed per well. After incubation for 2 hours at 37 ° C., the wells are emptied and a deposit of 150 μl / well of a solution of 0.5% BSA in PBS buffer is prepared in order to saturate the excess adsorption sites on the surface. plastic. This saturation step requires an incubation of one hour at 37 ° C. At this stage, the plates are ready for depositing the serum to be tested. For this test, the serum to be tested is a human serum taken and then used at different dilutions in PBS tween 0.1%. This solution is deposited and then diluted two by two directly on the plate (1 / 50.1 / 100, 1/200,) so as to obtain 100 .mu.l / well of final volume. After one hour of incubation at 37 ° C., the plates are washed 3 times with PBS containing 0.1% tween-20. An anti-human IgG (H + L) sheep antibody labeled with peroxidase and deposited at a rate of 100 μl / well and left for 30 min. at 37 ° C. The plates are then washed with 3 successive washes to remove the excess reagent (sheep antibody). Said possible epitope-autoantibody complexes are revealed thanks to the substrate of peroxidase. The peroxidase activity is revealed using the hydrogen peroxide / tetramethylbenzidine (TMB) reagent (Covalab). The reaction is stopped with 100 μl of H 2 SO 4 (2N). The absorbance is measured on a plate reader at 450 nm.
Claims
1. Anticorps isolés ou au moins l'un de leurs fragments fonctionnels, caractérisés en ce qu'ils sont spécifiques d'un épitope comprenant au moins un motif lysyl de formule (I) suivante :1. Isolated antibodies or at least one of their functional fragments, characterized in that they are specific for an epitope comprising at least one lysyl unit of formula (I) below:
dans laquelle R0 équivaut à H, un alkyle, un aryle, un alkylaryle ou un aralkyle, wherein R 0 is H, alkyl, aryl, alkylaryl or aralkyl,
R1 équivaut à H, un alkyle, un aryle, un alkylaryle, un aralkyle, un sucre, un lipide, un nucléotide ou une entité constituée d'au moins un motif acide aminé, ledit motif acide aminé étant relié au motif lysyl par une liaison peptidique,R 1 is H, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide or an entity consisting of at least one amino acid unit, said amino acid unit being attached to the lysyl unit by a peptide bond,
R équivaut à OH, un alkyle, un aryle, un alkylaryle, un aralkyle, un sucre, un lipide, un nucléotide, une entité constituée d'au moins un motif acide aminé, ledit motif acide aminé étant relié au motif lysyl par une liaison peptidique, ou OR4 où R4 est un alkyle, un aryle, un sucre, un lipide,R is OH, alkyl, aryl, alkylaryl, aralkyl, sugar, lipid, nucleotide, an entity consisting of at least one amino acid unit, said amino acid unit being attached to the lysyl unit through a linkage peptide, or OR 4 where R 4 is an alkyl, an aryl, a sugar, a lipid,
R3 équivaut à -(CH2)O-CH3 où n vaut 1 ou 2.R 3 is equivalent to - (CH 2 ) O -CH 3 where n is 1 or 2.
2. Anticorps isolés ou au moins l'un de leurs fragments fonctionnels, selon la revendication 1 caractérisés en ce qu'ils sont peu ou pas spécifiques d'un épitope contenant au moins un motif lysyl de formule (I) dans laquelle R0, R1, R2 sont tels que définis ci-dessus et R3 équivaut à -CH3.2. Isolated antibodies or at least one of their functional fragments, according to claim 1 characterized in that they are little or not specific for an epitope containing at least one lysyl unit of formula (I) in which R 0 , R 1 , R 2 are as defined above and R 3 is equivalent to -CH 3 .
3. Anticorps ou au moins l'un de leurs fragments fonctionnels selon la revendication 1 ou 2, caractérisés • en ce que leur immuno-réactivité pour les antigènes BSA-propionylée, mesurée dans un test T, est telle qu'elle répond à au moins l'une des caractéristiques suivantes : pour une dilution du sérum contenant lesdits anticorps à 1/500, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,6; 0,8; 1,0; 1,5; 2,0; 2 5' 2 7 - pour une dilution du sérum contenant lesdits anticorps à 1/1000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,3; 0,6 ; 0,8 ; 1,0 ;3. Antibody or at least one of their functional fragments according to claim 1 or 2, characterized in that their immunoreactivity for BSA-propionylated antigens, measured in a T test, is such that it responds to least one of the following characteristics: for a dilution of the serum containing said antibodies to 1/500, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.6; 0.8; 1.0; 1.5; 2.0; 2 5 '2 7 - for dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is greater than or equal to, in increasing order of preference: 0.3; 0.6; 0.8; 1.0;
1,5 ; 2,0 ; 2,2 ; pour une dilution du sérum contenant lesdits anticorps à 1/2000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,25 ; 0,4 ; 0,6 ; 1,0 ; pour une dilution du sérum contenant lesdits anticorps à 1/4000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,2 ; 0,4 ; 0,6 ; pour une dilution du sérum contenant lesdits anticorps à 1/8000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,2 ; 0,4 ; • et en ce que leur immuno-réactivité pour les antigènes BSA-acétylés, mesurée dans un test T, est telle qu'elle répond à au moins l'une des caractéristiques suivantes : pour une dilution du sérum contenant lesdits anticorps à 1/500, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 1,5; 1,0; 0,9; 0,8; 0,7;1.5; 2.0; 2.2; for dilution of the serum containing said antibodies to 1/2000, the OD at 450 nm is greater than or equal to, in ascending order preferably: 0.25; 0.4; 0.6; 1.0; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is greater than or equal to, in ascending order preferably: 0.2; 0.4; 0.6; for a dilution of the serum containing said antibodies at 1 / 8,000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.2; 0.4; And in that their immunoreactivity for BSA-acetylated antigens, measured in a T-test, is such that it meets at least one of the following characteristics: for a dilution of the serum containing said antibodies at 1/500 the OD at 450 nm is less than or equal to, in increasing order preferably: 1.5; 1.0; 0.9; 0.8; 0.7;
0,6 ; - pour une dilution du sérum contenant lesdits anticorps à 1/1000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 1,2; 1,0; 0,9; 0,8; 0,5;0.6; for a dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is less than or equal to, in increasing order preferably: 1.2; 1.0; 0.9; 0.8; 0.5;
0,4 ; pour une dilution du sérum contenant lesdits anticorps à 1/2000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 1,0; 0,8; 0,6; 0,5; 0,4; 0,3 ; pour une dilution du sérum contenant lesdits anticorps à 1/4000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,8; 0,6; 0,7; 0,5; 0,3;0.4; for a dilution of the serum containing said antibodies to 1/2000, the OD at 450 nm is less than or equal to, in ascending order preferably: 1.0; 0.8; 0.6; 0.5; 0.4; 0.3; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is less than or equal to, in ascending order preferably: 0.8; 0.6; 0.7; 0.5; 0.3;
0,2 ; pour une dilution du sérum contenant lesdits anticorps à 1/8000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,7, 0,6; 0,5; 0,4; 0,25;0.2; for dilution of the serum containing said antibodies to 1/8000, the OD at 450 nm is less than or equal to, in ascending order preferably: 0.7, 0.6; 0.5; 0.4; 0.25;
0,15.0.15.
4. Anticorps ou au moins l'un de leurs fragments fonctionnels selon l'une quelconque des revendications 1 à 3, caractérisés • en ce que leur immuno-réactivité pour les antigènes BSA-butyrylée, mesurée dans un test T, est telle qu'elle répond à au moins l'une des caractéristiques suivantes : pour une dilution du sérum contenant lesdits anticorps à 1/500, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,2 ; 0,4 ; 0,6 ; 1 ,0 ; 1,5 ; - pour une dilution du sérum contenant lesdits anticorps à 1/1000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,16 ; 0,4 ; 0,6 ; 0,9 ; pour une dilution du sérum contenant lesdits anticorps à 1/2000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,14 ; 0,3 ; 0,5 ; 0,6 ; pour une dilution du sérum contenant lesdits anticorps à 1/4000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,1 ; 0,15 ; 0,2 ; 0,3 ; pour une dilution du sérum contenant lesdits anticorps à 1/8000, la DO à 450 nm est supérieure ou égale à, dans un ordre croissant de préférence : 0,1 ; 0,15 ; 0,2 ; 0,25 ; • et en ce que leur immuno-réactivité pour les antigènes BSA-acétylés, mesurée dans un test T, est telle qu'elle répond à au moins l'une des caractéristiques suivantes : pour une dilution du sérum contenant lesdits anticorps à 1/500, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,8; 0,7 ; 0,6 ; 0,4 ; 0,3;4. Antibody or at least one of their functional fragments according to any one of Claims 1 to 3, characterized in that their immunoreactivity for BSA-butyrylated antigens, measured in a T test, is such that it corresponds to at least one of the following characteristics: for a dilution of the serum containing said antibodies at 1/500, the OD at 450 nm is greater than or equal to, in increasing order of preference: 0.2; 0.4; 0.6; 1.0; 1.5; for dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.16; 0.4; 0.6; 0.9; for a dilution of the serum containing said antibodies to 1/2000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.14; 0.3; 0.5; 0.6; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.1; 0.15; 0.2; 0.3; for dilution of the serum containing said antibodies to 1/8000, the OD at 450 nm is greater than or equal to, in increasing order preferably: 0.1; 0.15; 0.2; 0.25; And in that their immunoreactivity for BSA-acetylated antigens, measured in a T-test, is such that it meets at least one of the following characteristics: for a dilution of the serum containing said antibodies at 1/500 the OD at 450 nm is less than or equal to, in ascending order preferably 0.8; 0.7; 0.6; 0.4; 0.3;
0,2 ; - pour une dilution du sérum contenant lesdits anticorps à 1/1000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,7; 0,6; 0,5; 0,3; 0,20;0.2; for a dilution of the serum containing said antibodies to 1/1000, the OD at 450 nm is less than or equal to, in increasing order of preference: 0.7; 0.6; 0.5; 0.3; 0.20;
0,15 ; pour une dilution du sérum contenant lesdits anticorps à 1/2000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,6; 0,5; 0,4; 0,3; 0,15; 0,1 ; pour une dilution du sérum contenant lesdits anticorps à 1/4000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,6; 0,5; 0,4; 0,3; 0,15;0.15; for a dilution of the serum containing said antibodies to 1/2000, the OD at 450 nm is less than or equal to, in ascending order preferably: 0.6; 0.5; 0.4; 0.3; 0.15; 0.1; for a dilution of the serum containing said antibodies to 1/4000, the OD at 450 nm is less than or equal to, in ascending order preferably: 0.6; 0.5; 0.4; 0.3; 0.15;
0,1 ; pour une dilution du sérum contenant lesdits anticorps à 1/8000, la DO à 450 nm est inférieure ou égale à, dans un ordre croissant de préférence : 0,6; 0,5; 0,4; 0,3; 0,15;0.1; for dilution of the serum containing said antibodies to 1/8000, the OD at 450 nm is less than or equal to, in ascending order preferably 0.6; 0.5; 0.4; 0.3; 0.15;
0,1.0.1.
5. Procédé de fabrication des anticorps ou de au moins l'un de leurs fragments fonctionnels tels que définis dans l'une des revendications 1 à 4, caractérisé en ce qu'il consiste à : a) mettre en oeuvre un synthon de formule (I), b) coupler ledit synthon à une molécule porteuse, c) récupérer du plasma/sérum dudit animal auquel ledit couple synthon-molécule porteuse a été préalablement injecté, d) sélectionner les anticorps spécifiques dudit synthon utilisé à l'étape a) à l'aide d'un ou plusieurs épitopes de formule (I) tels que définis dans la revendication I, e) éventuellement purifier les anticorps selon les méthodes classiques.5. A process for producing the antibodies or at least one of their functional fragments as defined in one of claims 1 to 4, characterized in that it consists in: a) implementing a synthon of formula ( I), b) coupling said synthon to a carrier molecule, c) recovering plasma / serum from said animal to which said synthon-carrier molecule pair has been previously injected, d) selecting antibodies specific for said synthon used in step a) to using one or more epitopes of formula (I) as defined in claim I, e) optionally purify the antibodies according to conventional methods.
6. Procédé de fabrication des anticorps ou de au moins l'un de leurs fragments fonctionnels tels que définis dans l'une des revendications 1 à 4, caractérisé en ce qu'il consiste à : al) faire réagir une molécule de formule CH3-(CH2)n-CO-O-CO-(CH2)n-CH3 où n vaut 1 ou 2 avec une molécule porteuse afin de substituer les motifs lysyl de la molécule porteuse, bl) récupérer du plasma/sérum dudit animal auquel ladite molécule porteuse ainsi substituée a été préalablement injectée, cl) sélectionner les anticorps spécifiques des motifs lysyl substitués réalisés à l'étape al) à l'aide d'un ou plusieurs épitopes de formule (I) tels que définis dans la revendication 1 , dl) éventuellement purifier les anticorps selon les méthodes classiques.6. A process for producing the antibodies or at least one of their functional fragments as defined in one of claims 1 to 4, characterized in that consists of: a) reacting a molecule of the formula CH 3 - (CH 2 ) n -CO-O-CO- (CH 2 ) n -CH 3 where n is 1 or 2 with a carrier molecule in order to substitute the lysyl units of the carrier molecule, bl) recovering the plasma / serum of said animal to which said carrier molecule thus substituted has been previously injected, cl) selecting the antibodies specific for the substituted lysyl units carried out in step a1) using one or several epitopes of formula (I) as defined in claim 1, dl) optionally purify the antibodies according to conventional methods.
7. Procédé de fabrication des anticorps ou de au moins l'un de leurs fragments fonctionnels tels que définis dans l'une des revendications 1 à 4, caractérisé en ce qu'il consiste à : a2) mettre en œuvre un épitope de formule (I) dans laquelle au moins un des résidus R0 R1 est différent de H ou R2 est différent de OH, b2) coupler ledit épitope à une molécule porteuse, c2) récupérer du plasma/sérum dudit animal auquel ledit couple épitope-molécule porteuse a été préalablement injecté, d2) sélectionner les anticorps spécifiques dudit épitope utilisé à l'étape a2) à l'aide d'un ou plusieurs épitopes de formule (I) tels que définis dans la revendication 1, e2) éventuellement purifier les anticorps selon les méthodes classiques.7. Process for the manufacture of antibodies or at least one of their functional fragments as defined in one of Claims 1 to 4, characterized in that it consists in: a2) implementing an epitope of formula ( I) wherein at least one of the residues R 0 R 1 is different from H or R 2 is different from OH, b2) coupling said epitope to a carrier molecule, c2) recovering plasma / serum from said animal to which said epitope-molecule pair carrier has been previously injected, d2) select the specific antibodies of said epitope used in step a2) using one or more epitopes of formula (I) as defined in claim 1, e2) optionally purify the antibodies according to classical methods.
8. Composition comprenant des anticorps ou d'au moins l'un de leurs fragments fonctionnels tels que définis dans l'une des revendications 1 à 4, ou obtenus selon le procédé tel que défini dans l'une des revendications 5 à 7.8. Composition comprising antibodies or at least one of their functional fragments as defined in one of Claims 1 to 4, or obtained according to the process as defined in one of Claims 5 to 7.
9. Composition selon la revendication 8, caractérisée en ce qu'elle est utilisée dans au moins l'une des applications suivantes : recherche, diagnostic, analyse, pronostic de pathologie, thérapeutique, test d'efficacité ou de toxicité d'un médicament.9. Composition according to claim 8, characterized in that it is used in at least one of the following applications: research, diagnosis, analysis, prognosis of pathology, therapeutic, test of efficacy or toxicity of a drug.
10. Procédé de détection, dans un échantillon biologique, de l'épitope de formule (I) tel que défini dans la revendication 1 , caractérisé en ce qu'il comprend les étapes suivantes : A) éventuellement fixer sur un support approprié les anticorps ou l'un de leurs fragments fonctionnels tels que définis dans l'une des revendications 1 à 4 ou compris dans une composition telle que définie dans la revendication 8, B) mettre en contact un échantillon contenant potentiellement ledit épitope de formule (I) avec les anticorps ou au moins l'un de leurs fragments fonctionnels tels que définis dans l'une des revendications 1 à 4 ou compris dans une composition telle que définie dans la revendication 8, C) éventuellement effectuer au moins un lavage,10. A method for detecting, in a biological sample, the epitope of formula (I) as defined in claim 1, characterized in that it comprises the following steps: A) optionally fixing on an appropriate support the antibodies or one of their functional fragments as defined in one of claims 1 to 4 or included in a composition as defined in claim 8, B) contacting a sample potentially containing said epitope of formula (I) with the antibodies or at least one of their functional fragments as defined in one of claims 1 to 4 or included in a composition as defined in claim 8, C) optionally performing at least one wash,
D) détecter/révéler les complexes anticorps-épitope(s) de formule (I).D) detecting / revealing the antibody-epitope complexes of formula (I).
11. Nécessaire de détection, dans un échantillon biologique, de molécule contenant au moins l' épitope de formule (I) tel que défini dans la revendication 1, caractérisé en ce qu'il comprend : au moins un anticorps tel que défini dans la revendication 1 , de préférence fixé sur un support et le matériel approprié et nécessaire pour détecter les complexes anticorps-épitopes de formule (I).11. A kit for detecting, in a biological sample, a molecule containing at least the epitope of formula (I) as defined in claim 1, characterized in that it comprises: at least one antibody as defined in the claim 1, preferably attached to a support and the appropriate material and necessary to detect antibody-epitope complexes of formula (I).
12. Procédé de détection des auto-anticorps spécifiques des épitopes de formule (I) tels que définis dans la revendication 1, dans un échantillon biologique, de préférence un plasma ou un sérum, caractérisé en ce qu'il comprend les étapes suivantes : Al) éventuellement fixer sur un support approprié au moins un épitope de formule12. A method for detecting specific autoantibodies of the epitopes of formula (I) as defined in claim 1, in a biological sample, preferably a plasma or a serum, characterized in that it comprises the following steps: ) optionally fixing on a suitable support at least one epitope of formula
(I),(I)
Bl) mettre en contact ledit épitope de formule (I), de préférence fixé sur un support approprié, avec un échantillon,B1) contacting said epitope of formula (I), preferably fixed on a suitable support, with a sample,
C 1 ) éventuellement effectuer au moins un lavage, Dl) détecter/révéler lesdits (éventuels) complexes auto-anticorps-épitopes de formule (I) par des moyens de détections appropriés.C 1) optionally carry out at least one washing, Dl) detecting / revealing said (optional) autoantibody-epitope complexes of formula (I) by appropriate detecting means.
13. Nécessaire de détection des auto-anticorps spécifiques des épitopes de formule (I) tels que définis dans la revendication 1, dans un échantillon biologique, de préférence un plasma ou un sérum, caractérisé en ce qu'il comprend :13. A kit for detecting specific autoantibodies of the epitopes of formula (I) as defined in claim 1, in a biological sample, preferably a plasma or a serum, characterized in that it comprises:
- au moins un épitope de formule (I) tel que défini dans la revendication 1 etat least one epitope of formula (I) as defined in claim 1 and
- le matériel approprié et nécessaire pour détecter/révéler les complexes anticorps- épitopes de formule (I). the appropriate and necessary material for detecting / revealing the antibody-epitope complexes of formula (I).
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP09749948A EP2297201A1 (en) | 2008-05-23 | 2009-05-25 | Antibody specific for propionylated/butyrylated lysine, method for obtaining same and uses thereof |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0853362 | 2008-05-23 | ||
| FR0853362A FR2931481B1 (en) | 2008-05-23 | 2008-05-23 | PROPIONYLE / BUTYRYLEE LYSINE-SPECIFIC ANTIBODY, METHOD FOR PRODUCING THE SAME, AND APPLICATIONS THEREOF |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2009141458A1 true WO2009141458A1 (en) | 2009-11-26 |
Family
ID=40456970
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2009/056334 WO2009141458A1 (en) | 2008-05-23 | 2009-05-25 | Antibody specific for propionylated/butyrylated lysine, method for obtaining same and uses thereof |
Country Status (3)
| Country | Link |
|---|---|
| EP (1) | EP2297201A1 (en) |
| FR (1) | FR2931481B1 (en) |
| WO (1) | WO2009141458A1 (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10647780B2 (en) | 2016-05-25 | 2020-05-12 | Novartis Ag | Reversal binding agents for anti-factor XI/XIa antibodies and uses thereof |
| US11168147B2 (en) | 2016-12-23 | 2021-11-09 | Novartis Ag | Factor XI antibodies and methods of use |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JOP20200312A1 (en) | 2015-06-26 | 2017-06-16 | Novartis Ag | Factor xi antibodies and methods of use |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0785432B1 (en) * | 1996-01-18 | 2000-09-13 | Société Anonyme dite: IMMUNOTECH S.A. | Method for the immunological identification or determination of polypeptide antigens |
| US20080241862A1 (en) * | 2007-01-29 | 2008-10-02 | Yingming Zhao | Propionyl and butyryl lysine modifications in proteins |
-
2008
- 2008-05-23 FR FR0853362A patent/FR2931481B1/en not_active Expired - Fee Related
-
2009
- 2009-05-25 WO PCT/EP2009/056334 patent/WO2009141458A1/en active Application Filing
- 2009-05-25 EP EP09749948A patent/EP2297201A1/en not_active Withdrawn
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0785432B1 (en) * | 1996-01-18 | 2000-09-13 | Société Anonyme dite: IMMUNOTECH S.A. | Method for the immunological identification or determination of polypeptide antigens |
| US20080241862A1 (en) * | 2007-01-29 | 2008-10-02 | Yingming Zhao | Propionyl and butyryl lysine modifications in proteins |
Non-Patent Citations (6)
| Title |
|---|
| BARTON MA ET AL: "Synthetic polypeptides antigens of defined geometry", JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 99, no. 26, 1977, pages 8491 - 8498, XP008104608 * |
| CHEN YUE ET AL: "Lysine propionylation and butyrylation are novel post-translational modifications in histones.", MOLECULAR & CELLULAR PROTEOMICS : MCP MAY 2007, vol. 6, no. 5, May 2007 (2007-05-01), pages 812 - 819, XP002522297, ISSN: 1535-9476 * |
| EL ALAOUI S ET AL: "Transglutaminase activity and N epsilon (gamma glutamyl) lysine isopeptide levels during cell growth: an enzymic and immunological study.", 10 May 1991, INTERNATIONAL JOURNAL OF CANCER. JOURNAL INTERNATIONAL DU CANCER 10 MAY 1991, VOL. 48, NR. 2, PAGE(S) 221 - 226, ISSN: 0020-7136, XP008104787 * |
| IWABATA HISAKO ET AL: "Proteomic analysis of organ-specific post-translational lysine-acetylation and -methylation in mice by use of anti-acetyllysine and -methyllysine mouse monoclonal antibodies.", PROTEOMICS DEC 2005, vol. 5, no. 18, December 2005 (2005-12-01), pages 4653 - 4664, XP002522296, ISSN: 1615-9853 * |
| THOMAS V ET AL: "Definition of the fine specificity of the monoclonal antibody 81D4: its reactivity with lysine and polyamine isopeptide cross-links", JOURNAL OF IMMUNOLOGICAL METHODS, ELSEVIER SCIENCE PUBLISHERS B.V.,AMSTERDAM, NL, vol. 292, no. 1-2, 1 September 2004 (2004-09-01), pages 83 - 95, XP004550502, ISSN: 0022-1759 * |
| VILLAR-GAREA ANA ET AL: "The analysis of histone modifications.", December 2006, BIOCHIMICA ET BIOPHYSICA ACTA DEC 2006, VOL. 1764, NR. 12, PAGE(S) 1932 - 1939, ISSN: 0006-3002, XP002522298 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10647780B2 (en) | 2016-05-25 | 2020-05-12 | Novartis Ag | Reversal binding agents for anti-factor XI/XIa antibodies and uses thereof |
| US11168147B2 (en) | 2016-12-23 | 2021-11-09 | Novartis Ag | Factor XI antibodies and methods of use |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2297201A1 (en) | 2011-03-23 |
| FR2931481A1 (en) | 2009-11-27 |
| FR2931481B1 (en) | 2013-05-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2018214104A1 (en) | Pathway specific assays for predicting irritable bowel syndrome diagnosis | |
| EP0423301A1 (en) | Synthetic peptides of the conjugate of ubiquitine and histone h2a. | |
| FR2841249A1 (en) | COMPOSITIONS AND METHODS FOR THE ASSAY OF APO B48 AND APO B100 | |
| EP1907861A2 (en) | Method for detecting aggregate-forming circulating protein forms and agent for capturing formed aggregates | |
| Al-Abed et al. | [11] Advanced glycation end products: Detection and reversal | |
| Campos-Pinto et al. | Epitope mapping and characterization of 4-hydroxy-2-nonenal modified-human serum albumin using two different polyclonal antibodies | |
| WO2009141458A1 (en) | Antibody specific for propionylated/butyrylated lysine, method for obtaining same and uses thereof | |
| EP2446038A1 (en) | Sequences, antibodies, methods and kits for detection and in vitro assay of periostin, in order to provide a diagnosis, follow-up or prognosis of diseases and biological phenomena involving periostin | |
| Ashraf et al. | Prevalence of autoantibodies against 3-DG-glycated H2A protein in type 2 diabetes | |
| EP0667897B1 (en) | Method for specific immunoassay of human plasmatic glutathione peroxidase | |
| EP0736770A2 (en) | An immunoreactive conjugate, method for its preparation, antibodies to said conjugate and a pharmaceutical composition and diagnostic device containing them | |
| EP2649452A1 (en) | Method and case for the in vitro diagnosis of prostate cancer | |
| EP0495971B1 (en) | Thrombocytopenia determination | |
| BE1000850A3 (en) | METHOD FOR DETERMINATION OF ANTIBODY antisporozoite FALCIPARUM IN THE HUMAN BLOOD. | |
| FR3007763A1 (en) | ANTIBODIES AGAINST THE HUMAN NAV1.9 SODIUM CHANNEL AND THEIR USES IN DIAGNOSIS | |
| FR2663034A1 (en) | Peptides of the antigen Sm-D and their use especially for the diagnosis of systemic lupus erythematosus | |
| BE1006974A3 (en) | Detection method and / or different class quantitation immunoglobulins specific disease with an auto-immune response. | |
| FR2682113A1 (en) | Peptides derived from the protein A of the ribonucleoprotein snRNP-U1 and their use for the diagnosis of mixed connective tissue disease | |
| FR2718849A1 (en) | Method for immunoassay of glycosaminoglycan-activated antithrombin III, corresponding monoclonal antibodies and their method of production | |
| WO2010134506A1 (en) | Immunosensor for detecting explosive material and method for producing same | |
| FR3035971A1 (en) | ENRICHED COMPOSITION IN ANTI-A AND / OR ANTI-B POLYCLONAL IMMUNOGLOBULINS | |
| Golubović et al. | Human carcinoma-associated and salivary mucins detected by anti-bovine submaxillary mucin antibodies | |
| BE1009917A6 (en) | Immunoreactive conjugate, method to obtain said conjugate, antibodies directed against said conjugate and diagnostic device comprising same | |
| FR2908413A1 (en) | SPECIFIC MARKER FOR OXIDATIVE DEGRADATION OF TISSUES CONTAINING TYPE III COLLAGEN, MEANS AND METHODS, DIAGNOSTIC KITS FOR MONITORING OR PROGNOSIS OF THE PATHOLOGIES TARGETED BY THIS MARKER. | |
| FR2945290A1 (en) | BIOMARKER ANTIBODY AND DIAGNOSTIC DEVICE FOR THE DETECTION OF CERTAIN AUTOIMMUNE DISEASES |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 09749948 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2009749948 Country of ref document: EP |