RU2806175C2 - Универсальная тест-полоска для выборочного определения микотоксинов методом иммунохроматографии - Google Patents
Универсальная тест-полоска для выборочного определения микотоксинов методом иммунохроматографии Download PDFInfo
- Publication number
- RU2806175C2 RU2806175C2 RU2022105036A RU2022105036A RU2806175C2 RU 2806175 C2 RU2806175 C2 RU 2806175C2 RU 2022105036 A RU2022105036 A RU 2022105036A RU 2022105036 A RU2022105036 A RU 2022105036A RU 2806175 C2 RU2806175 C2 RU 2806175C2
- Authority
- RU
- Russia
- Prior art keywords
- antibodies
- mycotoxins
- test strip
- sample
- mycotoxin
- Prior art date
Links
- 239000002636 mycotoxin Substances 0.000 title claims abstract description 38
- 238000012360 testing method Methods 0.000 title claims abstract description 37
- 231100000678 Mycotoxin Toxicity 0.000 title claims abstract description 36
- 238000003317 immunochromatography Methods 0.000 title claims abstract description 4
- 239000012528 membrane Substances 0.000 claims abstract description 32
- 239000000872 buffer Substances 0.000 claims abstract description 9
- 239000003550 marker Substances 0.000 claims abstract description 8
- 239000003153 chemical reaction reagent Substances 0.000 claims abstract description 7
- 238000007865 diluting Methods 0.000 claims description 6
- 239000011152 fibreglass Substances 0.000 claims description 2
- 239000003053 toxin Substances 0.000 abstract description 4
- 230000000694 effects Effects 0.000 abstract description 3
- 239000012898 sample dilution Substances 0.000 abstract description 3
- 239000007853 buffer solution Substances 0.000 abstract description 2
- 239000003365 glass fiber Substances 0.000 abstract 1
- 239000000126 substance Substances 0.000 abstract 1
- 238000004458 analytical method Methods 0.000 description 22
- BXFOFFBJRFZBQZ-QYWOHJEZSA-N T-2 toxin Chemical compound C([C@@]12[C@]3(C)[C@H](OC(C)=O)[C@@H](O)[C@H]1O[C@H]1[C@]3(COC(C)=O)C[C@@H](C(=C1)C)OC(=O)CC(C)C)O2 BXFOFFBJRFZBQZ-QYWOHJEZSA-N 0.000 description 16
- 239000000243 solution Substances 0.000 description 16
- BXFOFFBJRFZBQZ-UHFFFAOYSA-N T2 Toxin Natural products C1=C(C)C(OC(=O)CC(C)C)CC2(COC(C)=O)C1OC1C(O)C(OC(C)=O)C2(C)C11CO1 BXFOFFBJRFZBQZ-UHFFFAOYSA-N 0.000 description 14
- VYLQGYLYRQKMFU-UHFFFAOYSA-N Ochratoxin A Natural products CC1Cc2c(Cl)cc(CNC(Cc3ccccc3)C(=O)O)cc2C(=O)O1 VYLQGYLYRQKMFU-UHFFFAOYSA-N 0.000 description 11
- DAEYIVCTQUFNTM-UHFFFAOYSA-N ochratoxin B Natural products OC1=C2C(=O)OC(C)CC2=CC=C1C(=O)NC(C(O)=O)CC1=CC=CC=C1 DAEYIVCTQUFNTM-UHFFFAOYSA-N 0.000 description 11
- RWQKHEORZBHNRI-BMIGLBTASA-N ochratoxin A Chemical compound C([C@H](NC(=O)C1=CC(Cl)=C2C[C@H](OC(=O)C2=C1O)C)C(O)=O)C1=CC=CC=C1 RWQKHEORZBHNRI-BMIGLBTASA-N 0.000 description 10
- MBMQEIFVQACCCH-UHFFFAOYSA-N trans-Zearalenon Natural products O=C1OC(C)CCCC(=O)CCCC=CC2=CC(O)=CC(O)=C21 MBMQEIFVQACCCH-UHFFFAOYSA-N 0.000 description 10
- MBMQEIFVQACCCH-QBODLPLBSA-N zearalenone Chemical compound O=C1O[C@@H](C)CCCC(=O)CCC\C=C\C2=CC(O)=CC(O)=C21 MBMQEIFVQACCCH-QBODLPLBSA-N 0.000 description 10
- 240000008042 Zea mays Species 0.000 description 9
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 9
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 9
- 235000005822 corn Nutrition 0.000 description 9
- LINOMUASTDIRTM-QGRHZQQGSA-N deoxynivalenol Chemical compound C([C@@]12[C@@]3(C[C@@H](O)[C@H]1O[C@@H]1C=C(C([C@@H](O)[C@@]13CO)=O)C)C)O2 LINOMUASTDIRTM-QGRHZQQGSA-N 0.000 description 9
- 229930002954 deoxynivalenol Natural products 0.000 description 9
- LINOMUASTDIRTM-UHFFFAOYSA-N vomitoxin hydrate Natural products OCC12C(O)C(=O)C(C)=CC1OC1C(O)CC2(C)C11CO1 LINOMUASTDIRTM-UHFFFAOYSA-N 0.000 description 9
- 235000013339 cereals Nutrition 0.000 description 7
- 238000001514 detection method Methods 0.000 description 7
- 239000000284 extract Substances 0.000 description 7
- 239000002115 aflatoxin B1 Substances 0.000 description 6
- 229930020125 aflatoxin-B1 Natural products 0.000 description 6
- 239000003008 fumonisin Substances 0.000 description 6
- 240000007594 Oryza sativa Species 0.000 description 5
- 235000007164 Oryza sativa Nutrition 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 235000009566 rice Nutrition 0.000 description 5
- 108010078791 Carrier Proteins Proteins 0.000 description 4
- 102000014914 Carrier Proteins Human genes 0.000 description 4
- 235000021307 Triticum Nutrition 0.000 description 4
- 241000209140 Triticum Species 0.000 description 4
- OQIQSTLJSLGHID-WNWIJWBNSA-N aflatoxin B1 Chemical compound C=1([C@@H]2C=CO[C@@H]2OC=1C=C(C1=2)OC)C=2OC(=O)C2=C1CCC2=O OQIQSTLJSLGHID-WNWIJWBNSA-N 0.000 description 4
- 235000013305 food Nutrition 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 238000000034 method Methods 0.000 description 4
- 235000007340 Hordeum vulgare Nutrition 0.000 description 3
- 240000005979 Hordeum vulgare Species 0.000 description 3
- 108060003951 Immunoglobulin Proteins 0.000 description 3
- 241000209056 Secale Species 0.000 description 3
- 235000007238 Secale cereale Nutrition 0.000 description 3
- 239000000427 antigen Substances 0.000 description 3
- 108091007433 antigens Proteins 0.000 description 3
- 102000036639 antigens Human genes 0.000 description 3
- 102000018358 immunoglobulin Human genes 0.000 description 3
- 229940072221 immunoglobulins Drugs 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 238000012545 processing Methods 0.000 description 3
- 238000010186 staining Methods 0.000 description 3
- 235000007319 Avena orientalis Nutrition 0.000 description 2
- 244000075850 Avena orientalis Species 0.000 description 2
- 241000196324 Embryophyta Species 0.000 description 2
- 240000008620 Fagopyrum esculentum Species 0.000 description 2
- 235000009419 Fagopyrum esculentum Nutrition 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 239000003463 adsorbent Substances 0.000 description 2
- 239000012491 analyte Substances 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical compound C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 2
- 238000011088 calibration curve Methods 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- 238000011109 contamination Methods 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 235000011868 grain product Nutrition 0.000 description 2
- 235000014571 nuts Nutrition 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 231100000765 toxin Toxicity 0.000 description 2
- 108700012359 toxins Proteins 0.000 description 2
- 244000105624 Arachis hypogaea Species 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 206010029155 Nephropathy toxic Diseases 0.000 description 1
- 240000006711 Pistacia vera Species 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000000711 cancerogenic effect Effects 0.000 description 1
- 231100000315 carcinogenic Toxicity 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 235000013312 flour Nutrition 0.000 description 1
- 231100000025 genetic toxicology Toxicity 0.000 description 1
- 230000001738 genotoxic effect Effects 0.000 description 1
- 231100000086 high toxicity Toxicity 0.000 description 1
- 230000008073 immune recognition Effects 0.000 description 1
- 238000003018 immunoassay Methods 0.000 description 1
- 230000001506 immunosuppresive effect Effects 0.000 description 1
- 239000002596 immunotoxin Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 1
- 231100000219 mutagenic Toxicity 0.000 description 1
- 230000003505 mutagenic effect Effects 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 230000007694 nephrotoxicity Effects 0.000 description 1
- 231100000417 nephrotoxicity Toxicity 0.000 description 1
- 235000020232 peanut Nutrition 0.000 description 1
- 238000011197 physicochemical method Methods 0.000 description 1
- 235000020233 pistachio Nutrition 0.000 description 1
- 239000000419 plant extract Substances 0.000 description 1
- 230000005070 ripening Effects 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 229930000044 secondary metabolite Natural products 0.000 description 1
- 231100000378 teratogenic Toxicity 0.000 description 1
- 230000003390 teratogenic effect Effects 0.000 description 1
- 238000010200 validation analysis Methods 0.000 description 1
Images
Abstract
Изобретение относится к определению группы токсичных метаболитов. Раскрыта аналитическая система для определения микотоксинов методом иммунохроматографии, представляющая собой тест-полоску - комплекс мембран с предварительно нанесенными реагентами, включающими контрольную зону с антивидовыми антителами, ряд аналитических зон с конъюгатами белок-микотоксин на 6 или более микотоксинов, стекловолоконную мембрану под конъюгат антивидовых антител с окрашенным маркером, при этом специфические к определяемому микотоксину антитела не входят в состав тест-полоски, а представлены раздельно, где каждый вид специфических к определяемому микотоксину антител находится в отдельном флаконе с буфером для разбавления проб. Изобретение обеспечивает сокращение вариантов изделия с шести отдельных тест-полосок до одного варианта универсальной тест-полоски и набора буферных растворов с разными антителами. 4 ил., 2 пр.
Description
Изобретение относится к определению группы токсичных метаболитов - афлатоксин В1, охратоксин А, фумонизин, зеараленон, Т2 токсин и дезоксиниваленол, и может быть использовано как быстрый и удобный инструмент внелабораторного скрининга продуктов питания, кормов и сельскохозяйственной продукции.
Микотоксины - низкомолекулярные вторичные метаболиты плесневых грибов. На сегодняшний день известно более 300 микотоксинов (Trucksess and Diaz-Amigo, 2011), но, к счастью, только 20 из них обнаружены в пищевых продуктах в количествах, достаточных для негативного воздействия на человека или животных. Микотоксинам свойственна высокая токсичность, они обладают мутагенными, тератогенными, канцерогенными, иммунодепрессивными свойствами (Sharma 1993; Zinedine, Soriano et al. 2007), а также гено- и нефротоксичностью (Wang, Quan et al. 2006; Xu, Xie et al. 2009). Поражение растительных культур может происходить как при вызревании, так и при хранении (особенно при нарушении его условий). Наиболее часто встречающиеся микотоксины - афлатоксин В1 (преимущественно в арахисе, фисташках, орехах, семенах масличных культур), охратоксин А (в рисе, ржи, пшенице, гречихе, ячмене), фумонизины (в хлебных злаках, кукурузе, рисе), зеараленон (в пшенице, хлебных злаках, рисе, ячмене, овсе), Т2 токсин (в рисе, ржи, пшенице, ячмене, овсе), дезоксиниваленол (в кукурузе, рисе, ржи, пшенице, гречихе). Приоритетным загрязнителем для зерновых продуктов является дезоксиниваленол; для орехов и семян масличных - афлатоксин В1; для продовольственного зерна и мукомольно-крупяных изделий - охратоксин А, для кукурузы и продуктов ее переработки - фумонизин.
Большинство микотоксинов не разрушается в процессе обычной обработки пищевого сырья, поэтому, попав в него на начальном этапе, микотоксины сохраняются при прохождении продукции по технологической цепочке, попадая в конечный продукт. Отсюда следует необходимость тщательного мониторинга микотоксинов на всех этапах производства - от хранения и транспортировки сырья до конечного товара.
Традиционно для решения этой задачи используются физико-химические методы анализа, сочетающие низкий предел обнаружения и высокую воспроизводимость результатов. Однако для применения этих методов необходимо дорогостоящее оборудование и квалифицированный персонал, а стоимость анализа одной пробы довольно высока. Необходимость тщательной очистки проб делает невозможным проведение анализа напрямую и требует продолжительных стадий очистки проб и концентрирования аналита.
Активно развиваются альтернативные методы, основанные на селективном иммунном распознавании микотоксинов антителами. Среди них особе место занимает иммунохроматография, подход, сочетающий высокие аналитические характеристики, малое время анализа и простоту выполнения. Однако из-за необходимости контроля различных видов микотоксинов важно сокращение затрат при производстве тест-систем. Нами вместо разработки тест-систем на каждое соединение предлагается использовать одну тест-полоску, способную детектировать любой из целевых аналитов. Изготовление тест-системы в предлагаемом варианте упрощается и удешевляется по сравнению с обычной мультипараметрической тест-системой, в которой на одной полоске происходит одновременное определение всех аналитов. Мультипараметрическая тест-система требует использования более дорогих компонентов, более сложных условий сборки и валидации теста.
Наиболее близкими аналогами изобретения являются иммунохроматографические тест-системы с непрямым введением маркера и детекцией микотоксинов в различных средах:
1. тест-система для непрямого иммунохроматографического определения деоксиниваленола и Т-2 токсина, в которой антитела помещены в буфера для нанесения пробы, описанная в публикации Петраковой и соавторов «Lateral flow immunoassay for bisphenol A: "External" antibodies as the simplest tool for sensitive immunochromatographic tests («Внешние» антитела как простой инструмент для высокочувствительного анализа): Talanta, 2017, v. 175, p.77-81. DOI: 10.1016/j.talanta.2017.07.027;
2. иммунохроматографическая тест-система для непрямого определения Т2 токсина, в которой маркер и специфические антитела предварительно нанесены и высушены на мембране, описанная в публикации Урусова и соавторов «Immunochromatographic assay of Т-2 toxin using labeled anti-species antibodies)) (Иммунохроматографический анализ T2 токсина с использованием меченых антивидовых антител), Applied Biochemistry and Microbiology, 2017, v. 53, N 5, p.594-599. DOI: 10.1134/S0003683817050167.
Описанная в первой публикации тест-система представляет собой мембранный композит, в состав которого входит:
1. рабочая мембрана с иммобилизованными конъюгатами Т2 токсина и диоксиниваленола с белками-носителями в аналитической зоне и с иммобилизованными антивидовыми антителами в контрольной зоне;
2. мембраны под конъюгат с нанесенными и высушенным конъюгатом антивидовых антител против иммуноглобулинов мыши;
3. мембраны для впитывания и сепарации тестируемой пробы;
4. конечная адсорбирующая мембрана для впитывания компонентов пробы после прохождения реакции;
5. флакон с буфером для разбавления пробы, в который одновременно внесены мышиные моноклональные антитела против Т2 токсина и деоксиниваленола.
Анализ проводят следующим образом:
1. Экстракты растительного сырья смешивают с буфером для разведения пробы, в который добавлены антитела одновременно к двум антигенам;
2. 100 мкл полученного раствора наносят на нижнюю часть тест-полоски (мембраны для нанесения пробы);
3. После нанесения инкубируют 15 минут;
4. Результат анализа фиксируют визуально или с использованием детектора.
Результат анализа интерпретируют следующим образом:
1. Если на рабочей мембране проявляется одна окрашенная контрольная линия, то в пробе отсутствуют и Т2 токсин, и деоксиниваленол;
2. Если окрашивается контрольная линии и одна из аналитических, то в пробе присутствует только один определяемый токсин;
3. Если окрашенных линий не наблюдается, анализ признается недействительным и повторяется.
Представленная во второй публикации тест-система представляет собой мембранный композит, в состав которого входит:
1. рабочая мембрана с иммобилизованными конъюгатом Т2 токсина с белком-носителем в аналитической зоне и иммобилизованными антивидовыми антителами в контрольной зоне;
2. мембраны под конъюгат с нанесенными и высушенными конъюгатом антивидовых антител против иммуноглобулинов мыши и специфическими антителами против Т2 токсина;
3. мембраны для впитывания и сепарации тестируемой пробы;
4. конечная адсорбирующая мембрана для впитывания компонентов пробы после прохождения реакции;
5. флакон с буфером для разбавления пробы. Анализ проводят следующим образом:
1. Экстракты растительного сырья смешивают с буфером для разведения пробы;
2. 100 мкл полученного раствора наносят на нижнюю часть тест-полоски (мембраны для нанесения образца);
3. После нанесения инкубируют 15 минут;
4. Результат анализа фиксируют визуально или с использованием детектора.
Результат анализа интерпретируют следующим образом:
4. Если на рабочей мембране проявляется одна окрашенная контрольная линия, то в пробе присутствует Т2 токсин.
5. Если окрашиваются и контрольная, и аналитическая линии, то в пробе отсутствует Т2 токсин.
6. Если окрашенных линий не наблюдается, анализ признается недействительным и повторяется.
В первом варианте хоть и происходит одновременная детекция двух микотоксинов, но она осложнена взаимным влиянием образующихся комплексов «окрашенный маркер-антивидовые антитела-специфические антитела к различным микотоксинам». Расширение до большего количества одновременно определяемых микотоксинов потребует значительного роста концентрации конъюгата антивидовых антител с окрашенным маркером (чтобы их количество было достаточным для покрытия всех свободных антител, вносимых в систему с буфером для разведения пробы) и в то же время - неоправданных расходов специфических антител. Такой перерасход особенно критичен при анализе проб, которые не могут быть контаминированы одновременно различными токсинами, или если нужно подтверждение контаминации, выявленной по внешним признакам.
Во втором варианте и специфические антитела, и конъюгаты антивидовых антител с маркером наносятся одновременно на одну мембрану, что требует значительного расхода реагентов для обеспечения мультипараметрической детекции и зачастую вызывает негативные эффекты при хранении. При этом для каждого микотоксина требуется создание отдельной тест-полоски со своим протоколом нанесения реагентов и последующей обработки мембран.
Задачей заявленного изобретения является сокращение стадий производства и упрощение технологического процесса. Результат заявленного изобретения заключается в сокращении вариантов изделия: с шести отдельных тест-полосок (с нанесенными реагентами разной специфичности) до одного варианта универсальной тест-полоски и набора буферных растворов с разными антителами. Таким образом, определение одного выбранного микотоксина потребует только выбора флакона со специфическими к определяемому микотоксину антителами.
Указанный результат достигается тем, что:
- на рабочую мембрану нанесены сразу 6 и более аналитических зон (сорбированы конъюгаты микотоксинов с белками-носителями);
- на стекловолоконную мембрану нанесен конъюгат антивидовых антител против иммуноглобулинов мыши с окрашенными наночастицами;
- специфические антитела к определяемым микотоксинам исключены из комплектации самой тест-полоски и помещены в буфер для разведения пробы, при этом антитела разной специфичности не смешиваются друг с другом;
- для проведения анализа берется универсальная тест-полоска и выбирается необходимый раствор специфических антител.
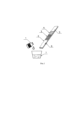
Для проведения анализа, как показано на рис. 1:
1. Готовятся универсальные тест-полоски, на которые уже нанесены конъюгат окрашенного маркера с антивидовыми антителами, аналитические зоны - конъюгаты микотоксинов с белками-носителями - и реагенты контрольной зоны.
2. В зависимости от задачи (контролируемого аналита) выбирается раствор специфических антител, который смешивается с анализируемой пробой в отношении 1 к 1 и инкубируется в течение 1 минуты (контролируемый микотоксин определяется исходя из наибольшей вероятности контаминации им данной серии проб на основе информации о виде продукции, условиях выращивания и хранения).
3. На мембрану для пробы наносится 100-150 мкл полученного раствора и инкубируется 15 минут.
4. По образованию окрашенных линий проводится интерпретация результата.
Описанный анализ включает следующие процессы:
Анализируемая проба смешивается с тестируемой пробой. Находящиеся в растворе антитела связываются с определяемым микотоксином. После этого проба наносится на мембраны для пробы и начинает движение вдоль тест-полоски. Доходя до мембраны с конъюгатом, антитела связываются с ним, образуя комплекс антиген-специфическое антитело-антивидовые антитело-окрашенный маркер. Комплексы продолжают движение вдоль тест-полоски и доходят до аналитических зон. Если в пробе присутствует микотоксин, то комплексы не связываются в аналитической зоне (все центры связывания антител уже заняты) и продолжают свое движение. Если в пробе нет микотоксина или его количество ниже заявленного предела детекции, то свободные антитела в составе комплекса метка-антивидовые антитела-специфические антитела связываются с поверхностью мембраны и образуют окрашенную линию. Избыток комплексов доходит до контрольной линии, где связывается с иммобилизованными антивидовыми антителами независимо от наличия антигена в пробе, образуя окрашенную линию контрольной зоны.
Интерпретация результатов анализа производится в соответствие со схемой, представленной на рис. 2: при использовании раствора антител против афлатоксина В1 проводят идентификацию первой аналитической зоны (рис 2 А). Ее появление свидетельствует об отсутствии микотоксина в пробе. Если же линия не проявляется (на тесте присутствует только одна контрольная зона), делается вывод о наличии микотоксина в пробе (превышение порогового значения концентрации). Полное отсутствие какой-либо из окрашенных линий или проявление иных аналитических зон толкуется как недействительный результат анализа. Аналогично анализ с использованием антител против охратоксина А интерпретируется по окрашиванию второй аналитической зоны (рис 2 Б), антител против фумонизина - по окрашиванию третьей аналитической зоны (рис 2 В), антител против зеараленона - четвертой аналитической зоны (рис 2 Г), антител против Т2 токсина - пятой аналитической зоны (рис 2 Д), антител против дезоксиниваленола - шестой аналитической зоны (рис 2 Е).
Эффективность данного подхода подтверждается следующими представленными ниже примерами:
Пример 1 (определение концентрации охратоксина А)
С использованием заявляемого устройства проводят анализ экстрактов зерен кукурузы. Пробы с разной концентрацией охратоксина А смешивают с раствором специфических антител и инкубируют 1 минуту. После этого на поверхность мембраны для пробы вносят 150 мкл полученной смеси. Через 15 минут проводят документирование результатов анализа и их последующую цифровую обработку.
На рисунке 3 представлен график полученной зависимости интенсивности окрашивания аналитической зоны (результат цифровой обработки изображений тест-полосок) от концентрации охратоксина А в пробе. Из полученных данных видно, что созданный тест способен проводить идентификацию микотоксина охратоксина А в с экстрактах зерен кукурузы с пределом обнаружения 5 мкг/кг (начало роста интенсивности окрашивания, т.е. появления линии в аналитической зоне).
Пример 2 (определение концентрации зеараленона)
С использованием заявляемого устройства проводят анализ экстрактов зерен кукурузы. Пробы с разной концентрацией зеараленона смешивают с раствором специфических антител и инкубируют 1 минуту. После этого на поверхность мембраны для пробы вносят 150 мкл полученной смеси. Через 15 минут проводят документирование результатов анализа и их последующую цифровую обработку.
На рисунке 4 представлен график полученной зависимости интенсивности окрашивания аналитической зоны от концентрации зеараленона в пробе. Из полученных данных видно, что созданный тест способен проводить идентификацию зеараленона в экстрактах зерен кукурузы с пределом обнаружения 200 нг/г.
Краткое описание чертежей
На рис. 1 изображена схема аналитической системы. 1 - раствор со специфическими антителами для разведения пробы, 2 - мембрана под пробу, 3 - аналитические зоны, 4 - контрольная зона, 5 - впитывающая мембрана, 6 - мембрана для нанесения конъюгата, 7 - анализируемая проба.
На рис. 2 изображены результаты использования устройства при выборе реагентов для анализа соответствующих микотоксинов
А: 8 - раствор антител на афлатоксин В1, 9 - аналитическая линия на афлатоксин В1,
Б: 10 - раствор антител на охратоксин А, 11 - аналитическая линия на охратоксин А,
В: 12 - раствор антител на фумонизин, 13 - аналитическая линия на фумонизин,
Г: 14 - раствор антител на зеараленон, 15 - аналитическая линия на зеараленон,
Д: 16 - раствор антител на Т2 токсин, 17 - аналитическая линия на Т2 токсин,
Е: 18 - раствор антител на дезоксиниваленонл, 19 - аналитическая линия на дезоксиниваленол).
На рис. 3 изображена калибровочная кривая иммунохроматографического определения охратоксина А в экстрактах кукурузы.
На рис. 4 изображена калибровочная кривая иммунохроматографического определения зеараленона в экстрактах кукурузы.
Claims (1)
- Аналитическая система для определения микотоксинов методом иммунохроматографии, представляющая собой тест-полоску - комплекс мембран с предварительно нанесенными реагентами, включающими контрольную зону с антивидовыми антителами, ряд аналитических зон с конъюгатами белок-микотоксин на 6 или более микотоксинов, стекловолоконную мембрану под конъюгат антивидовых антител с окрашенным маркером, отличающаяся тем, что специфические к определяемому микотоксину антитела не входят в состав тест-полоски, а представлены раздельно, где каждый вид специфических к определяемому микотоксину антител находится в отдельном флаконе с буфером для разбавления проб.
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2022105036A RU2022105036A (ru) | 2023-02-06 |
| RU2806175C2 true RU2806175C2 (ru) | 2023-10-27 |
Family
ID=
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20140256588A1 (en) * | 2013-03-11 | 2014-09-11 | Meso Scale Technologies, Llc. | Methods for conducting multiplexed assays |
| CN111474359A (zh) * | 2020-04-22 | 2020-07-31 | 北京倍肯恒业科技发展股份有限公司 | 一种多联检测胶体金免疫层析试纸条的制备方法及应用 |
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20140256588A1 (en) * | 2013-03-11 | 2014-09-11 | Meso Scale Technologies, Llc. | Methods for conducting multiplexed assays |
| CN111474359A (zh) * | 2020-04-22 | 2020-07-31 | 北京倍肯恒业科技发展股份有限公司 | 一种多联检测胶体金免疫层析试纸条的制备方法及应用 |
Non-Patent Citations (2)
| Title |
|---|
| ZHANG W. et al. Multiplex SERS-based lateral flow immunosensor for the detection of major mycotoxins in maize utilizing dual Raman labels and triple test lines // Journal of Hazardous Materials, 2020, V.393, pp.1-9. * |
| ГУБАЙДУЛЛИНА М.К. и др. Иммунохроматографические тест-системы с использованием конъюгата антивидовые антитела - коллоидное золото: особенности и преимущества на примере определения охратоксина А // ВЕСТН. МОСК. УН-ТА. СЕР. 2. ХИМИЯ, 2018, т.59, N.2, стр.144-150. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Tripathi et al. | Recent advancements in lateral flow immunoassays: A journey for toxin detection in food | |
| Raeisossadati et al. | Lateral flow based immunobiosensors for detection of food contaminants | |
| Krska et al. | Rapid test strips for analysis of mycotoxins in food and feed | |
| Schneider et al. | Rapid methods for deoxynivalenol and other trichothecenes | |
| Sapsford et al. | Indirect competitive immunoassay for detection of aflatoxin B1 in corn and nut products using the array biosensor | |
| Kolosova et al. | Lateral-flow colloidal gold-based immunoassay for the rapid detection of deoxynivalenol with two indicator ranges | |
| Stave | Detection of new or modified proteins in novel foods derived from GMO–future needs | |
| Lattanzio et al. | Current analytical methods for trichothecene mycotoxins in cereals | |
| Zhang et al. | Development of multianalyte flow-through and lateral-flow assays using gold particles and horseradish peroxidase as tracers for the rapid determination of carbaryl and endosulfan in agricultural products | |
| Meneely et al. | A rapid optical immunoassay for the screening of T-2 and HT-2 toxin in cereals and maize-based baby food | |
| De Saeger et al. | A collaborative study to validate novel field immunoassay kits for rapid mycotoxin detection | |
| Maragos | Emerging technologies for mycotoxin detection | |
| Oswald et al. | Automated regenerable microarray-based immunoassay for rapid parallel quantification of mycotoxins in cereals | |
| Koch et al. | Optical flow-cell multichannel immunosensor for the detection of biological warfare agents | |
| Ngundi et al. | Detection of deoxynivalenol in foods and indoor air using an array biosensor | |
| CN110488016A (zh) | 一种玉米赤霉烯酮-呕吐毒素双通道免疫定量试纸条 | |
| Hossain et al. | Immunoassay utilizing imaging surface plasmon resonance for the detection of cyclopiazonic acid (CPA) in maize and cheese | |
| Badran et al. | Simultaneous determination of four food allergens using compact disc immunoassaying technology | |
| Thongrussamee et al. | Monoclonal-based enzyme-linked immunosorbent assay for the detection of zearalenone in cereals | |
| US20220326209A1 (en) | Paper-Based Microfluidic Don-Chip for Rapid and Low-Cost Deoxynivalenol Quantification in Foods, Feeds and Feed Ingredients | |
| CN101738479A (zh) | 多种霉菌毒素定量检测蛋白芯片及其试剂盒 | |
| Guo et al. | Europium nanosphere-based fluorescence strip sensor for ultrasensitive and quantitative determination of fumonisin B 1 | |
| Kim et al. | Development of a simultaneous lateral flow strip test for the rapid and simple detection of deoxynivalenol and zearalenone | |
| Vidal et al. | Rapid simultaneous extraction and magnetic particle-based enzyme immunoassay for the parallel determination of ochratoxin A, fumonisin B1 and deoxynivalenol mycotoxins in cereal samples | |
| Porricelli et al. | Optimization and validation of a fluorescence polarization immunoassay for rapid detection of T-2 and HT-2 toxins in cereals and cereal-based products |