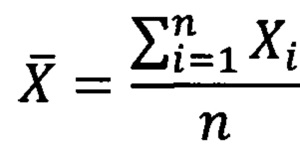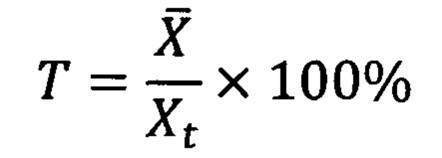RU2763178C2 - Антитела для лабораторной диагностики концентрации интерлейкина-11 - Google Patents
Антитела для лабораторной диагностики концентрации интерлейкина-11 Download PDFInfo
- Publication number
- RU2763178C2 RU2763178C2 RU2020111785A RU2020111785A RU2763178C2 RU 2763178 C2 RU2763178 C2 RU 2763178C2 RU 2020111785 A RU2020111785 A RU 2020111785A RU 2020111785 A RU2020111785 A RU 2020111785A RU 2763178 C2 RU2763178 C2 RU 2763178C2
- Authority
- RU
- Russia
- Prior art keywords
- antibodies
- seq
- antibody
- antigen
- concentration
- Prior art date
Links
- 102000003815 Interleukin-11 Human genes 0.000 title claims abstract description 52
- 108090000177 Interleukin-11 Proteins 0.000 title claims abstract description 52
- 229940074383 interleukin-11 Drugs 0.000 title description 46
- 239000000427 antigen Substances 0.000 claims abstract description 31
- 108091007433 antigens Proteins 0.000 claims abstract description 31
- 102000036639 antigens Human genes 0.000 claims abstract description 31
- 230000027455 binding Effects 0.000 claims abstract description 25
- 239000012634 fragment Substances 0.000 claims abstract description 23
- 101001010568 Homo sapiens Interleukin-11 Proteins 0.000 claims abstract description 20
- 102000049885 human IL11 Human genes 0.000 claims abstract description 20
- 241000282567 Macaca fascicularis Species 0.000 claims abstract description 16
- 241001465754 Metazoa Species 0.000 claims abstract description 15
- 238000000034 method Methods 0.000 claims description 28
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 claims description 18
- 229960002685 biotin Drugs 0.000 claims description 9
- 235000020958 biotin Nutrition 0.000 claims description 9
- 239000011616 biotin Substances 0.000 claims description 9
- 241000282553 Macaca Species 0.000 claims description 5
- 238000012360 testing method Methods 0.000 claims description 4
- 108091007491 NSP3 Papain-like protease domains Proteins 0.000 claims description 2
- 125000003275 alpha amino acid group Chemical group 0.000 claims 1
- 238000010171 animal model Methods 0.000 claims 1
- 230000000694 effects Effects 0.000 abstract description 2
- 239000000126 substance Substances 0.000 abstract description 2
- 108090000623 proteins and genes Proteins 0.000 description 16
- 239000012491 analyte Substances 0.000 description 13
- 239000000872 buffer Substances 0.000 description 13
- 210000004027 cell Anatomy 0.000 description 12
- 102000004169 proteins and genes Human genes 0.000 description 12
- 239000000243 solution Substances 0.000 description 10
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 9
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 9
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 9
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 9
- 238000005516 engineering process Methods 0.000 description 9
- 150000001413 amino acids Chemical group 0.000 description 8
- 201000010099 disease Diseases 0.000 description 8
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 8
- 239000007790 solid phase Substances 0.000 description 8
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 8
- 238000002965 ELISA Methods 0.000 description 7
- 238000003018 immunoassay Methods 0.000 description 7
- 239000003446 ligand Substances 0.000 description 7
- 238000005259 measurement Methods 0.000 description 7
- 239000000523 sample Substances 0.000 description 7
- 239000013060 biological fluid Substances 0.000 description 6
- 230000014509 gene expression Effects 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- 230000003287 optical effect Effects 0.000 description 6
- 102000004190 Enzymes Human genes 0.000 description 5
- 108090000790 Enzymes Proteins 0.000 description 5
- 239000012482 calibration solution Substances 0.000 description 5
- 238000010790 dilution Methods 0.000 description 5
- 239000012895 dilution Substances 0.000 description 5
- 238000010494 dissociation reaction Methods 0.000 description 5
- 230000005593 dissociations Effects 0.000 description 5
- 229940088598 enzyme Drugs 0.000 description 5
- 238000002823 phage display Methods 0.000 description 5
- 102000004127 Cytokines Human genes 0.000 description 4
- 108090000695 Cytokines Proteins 0.000 description 4
- 102000004889 Interleukin-6 Human genes 0.000 description 4
- 108090001005 Interleukin-6 Proteins 0.000 description 4
- 238000001514 detection method Methods 0.000 description 4
- 229940100601 interleukin-6 Drugs 0.000 description 4
- 239000002245 particle Substances 0.000 description 4
- 102000004196 processed proteins & peptides Human genes 0.000 description 4
- 108090000765 processed proteins & peptides Proteins 0.000 description 4
- 239000000758 substrate Substances 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 3
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 3
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 3
- 108010058846 Ovalbumin Proteins 0.000 description 3
- 229920001213 Polysorbate 20 Polymers 0.000 description 3
- 108020004511 Recombinant DNA Proteins 0.000 description 3
- 125000003277 amino group Chemical group 0.000 description 3
- RIIWUGSYXOBDMC-UHFFFAOYSA-N benzene-1,2-diamine;hydron;dichloride Chemical compound Cl.Cl.NC1=CC=CC=C1N RIIWUGSYXOBDMC-UHFFFAOYSA-N 0.000 description 3
- 229940098773 bovine serum albumin Drugs 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 238000007796 conventional method Methods 0.000 description 3
- 239000012228 culture supernatant Substances 0.000 description 3
- 239000013604 expression vector Substances 0.000 description 3
- 239000001963 growth medium Substances 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 230000009871 nonspecific binding Effects 0.000 description 3
- 229940092253 ovalbumin Drugs 0.000 description 3
- 210000002381 plasma Anatomy 0.000 description 3
- 239000004033 plastic Substances 0.000 description 3
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 3
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 3
- 229920001184 polypeptide Polymers 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 230000035945 sensitivity Effects 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 210000001519 tissue Anatomy 0.000 description 3
- 239000013598 vector Substances 0.000 description 3
- GPUBPSKTFNYPHI-AYGRAXKESA-N 3-[5-[(3as,4s,6ar)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoyl]-1-hydroxypyrrolidine-2,5-dione Chemical compound O=C1N(O)C(=O)CC1C(=O)CCCC[C@H]1[C@H]2NC(=O)N[C@H]2CS1 GPUBPSKTFNYPHI-AYGRAXKESA-N 0.000 description 2
- 108090001008 Avidin Proteins 0.000 description 2
- AMRLSQGGERHDHJ-FXQIFTODSA-N Cys-Ala-Arg Chemical compound [H]N[C@@H](CS)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O AMRLSQGGERHDHJ-FXQIFTODSA-N 0.000 description 2
- BPHKULHWEIUDOB-FXQIFTODSA-N Cys-Gln-Gln Chemical compound SC[C@H](N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(O)=O BPHKULHWEIUDOB-FXQIFTODSA-N 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- 108060003951 Immunoglobulin Proteins 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- 108091028043 Nucleic acid sequence Proteins 0.000 description 2
- 229920002873 Polyethylenimine Polymers 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 108010090804 Streptavidin Proteins 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 108010013835 arginine glutamate Proteins 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 230000006287 biotinylation Effects 0.000 description 2
- 238000007413 biotinylation Methods 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 230000037182 bone density Effects 0.000 description 2
- 239000007853 buffer solution Substances 0.000 description 2
- 238000007385 chemical modification Methods 0.000 description 2
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 2
- 238000007405 data analysis Methods 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 235000013601 eggs Nutrition 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 235000013861 fat-free Nutrition 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- 108010010147 glycylglutamine Proteins 0.000 description 2
- 210000004408 hybridoma Anatomy 0.000 description 2
- 102000018358 immunoglobulin Human genes 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 238000003771 laboratory diagnosis Methods 0.000 description 2
- 235000013336 milk Nutrition 0.000 description 2
- 239000008267 milk Substances 0.000 description 2
- 210000004080 milk Anatomy 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 2
- 230000003472 neutralizing effect Effects 0.000 description 2
- 230000000771 oncological effect Effects 0.000 description 2
- 230000001575 pathological effect Effects 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 239000013612 plasmid Substances 0.000 description 2
- 229940068977 polysorbate 20 Drugs 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 230000019491 signal transduction Effects 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 230000010474 transient expression Effects 0.000 description 2
- 102000010400 1-phosphatidylinositol-3-kinase activity proteins Human genes 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- 102000011767 Acute-Phase Proteins Human genes 0.000 description 1
- 108010062271 Acute-Phase Proteins Proteins 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- HTSSXFASOUSJQG-IHPCNDPISA-N Asp-Tyr-Trp Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CC1=CNC2=C1C=CC=C2)C(O)=O HTSSXFASOUSJQG-IHPCNDPISA-N 0.000 description 1
- 239000010755 BS 2869 Class G Substances 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 101710132601 Capsid protein Proteins 0.000 description 1
- 206010008111 Cerebral haemorrhage Diseases 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 101710091045 Envelope protein Proteins 0.000 description 1
- 241001198387 Escherichia coli BL21(DE3) Species 0.000 description 1
- 241000724791 Filamentous phage Species 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- OTQSTOXRUBVWAP-NRPADANISA-N Gln-Ser-Val Chemical compound [H]N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](C(C)C)C(O)=O OTQSTOXRUBVWAP-NRPADANISA-N 0.000 description 1
- IDEODOAVGCMUQV-GUBZILKMSA-N Glu-Ser-Leu Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(O)=O IDEODOAVGCMUQV-GUBZILKMSA-N 0.000 description 1
- TZXOPHFCAATANZ-QEJZJMRPSA-N Glu-Ser-Trp Chemical compound C1=CC=C2C(=C1)C(=CN2)C[C@@H](C(=O)O)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(=O)O)N TZXOPHFCAATANZ-QEJZJMRPSA-N 0.000 description 1
- LJPIRKICOISLKN-WHFBIAKZSA-N Gly-Ala-Ser Chemical compound NCC(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(O)=O LJPIRKICOISLKN-WHFBIAKZSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- VHHYJBSXXMPQGZ-AVGNSLFASA-N His-Gln-Leu Chemical compound CC(C)C[C@@H](C(=O)O)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H](CC1=CN=CN1)N VHHYJBSXXMPQGZ-AVGNSLFASA-N 0.000 description 1
- WXLYNEHOGRYNFU-URLPEUOOSA-N Ile-Thr-Phe Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC1=CC=CC=C1)C(=O)O)N WXLYNEHOGRYNFU-URLPEUOOSA-N 0.000 description 1
- 108010058683 Immobilized Proteins Proteins 0.000 description 1
- 102100034349 Integrase Human genes 0.000 description 1
- 102000004553 Interleukin-11 Receptors Human genes 0.000 description 1
- 108010017521 Interleukin-11 Receptors Proteins 0.000 description 1
- 102000042838 JAK family Human genes 0.000 description 1
- 108091082332 JAK family Proteins 0.000 description 1
- KFKWRHQBZQICHA-STQMWFEESA-N L-leucyl-L-phenylalanine Natural products CC(C)C[C@H](N)C(=O)N[C@H](C(O)=O)CC1=CC=CC=C1 KFKWRHQBZQICHA-STQMWFEESA-N 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 210000002361 Megakaryocyte Progenitor Cell Anatomy 0.000 description 1
- 101150097381 Mtor gene Proteins 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- AJHCSUXXECOXOY-UHFFFAOYSA-N N-glycyl-L-tryptophan Natural products C1=CC=C2C(CC(NC(=O)CN)C(O)=O)=CNC2=C1 AJHCSUXXECOXOY-UHFFFAOYSA-N 0.000 description 1
- 108091007960 PI3Ks Proteins 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 206010033645 Pancreatitis Diseases 0.000 description 1
- 206010033647 Pancreatitis acute Diseases 0.000 description 1
- 108090000526 Papain Proteins 0.000 description 1
- 102000057297 Pepsin A Human genes 0.000 description 1
- 108090000284 Pepsin A Proteins 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- CUMXHKAOHNWRFQ-BZSNNMDCSA-N Phe-Asp-Tyr Chemical compound C([C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(O)=O)C1=CC=CC=C1 CUMXHKAOHNWRFQ-BZSNNMDCSA-N 0.000 description 1
- 108010004729 Phycoerythrin Proteins 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- 101710193132 Pre-hexon-linking protein VIII Proteins 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 108010076504 Protein Sorting Signals Proteins 0.000 description 1
- 101710188315 Protein X Proteins 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- GXXTUIUYTWGPMV-FXQIFTODSA-N Ser-Arg-Ala Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(O)=O GXXTUIUYTWGPMV-FXQIFTODSA-N 0.000 description 1
- YRBGKVIWMNEVCZ-WDSKDSINSA-N Ser-Glu-Gly Chemical compound OC[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(O)=O YRBGKVIWMNEVCZ-WDSKDSINSA-N 0.000 description 1
- JFWDJFULOLKQFY-QWRGUYRKSA-N Ser-Gly-Phe Chemical compound [H]N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC1=CC=CC=C1)C(O)=O JFWDJFULOLKQFY-QWRGUYRKSA-N 0.000 description 1
- GZGFSPWOMUKKCV-NAKRPEOUSA-N Ser-Pro-Ile Chemical compound CC[C@H](C)[C@@H](C(O)=O)NC(=O)[C@@H]1CCCN1C(=O)[C@@H](N)CO GZGFSPWOMUKKCV-NAKRPEOUSA-N 0.000 description 1
- XQJCEKXQUJQNNK-ZLUOBGJFSA-N Ser-Ser-Ser Chemical compound OC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O XQJCEKXQUJQNNK-ZLUOBGJFSA-N 0.000 description 1
- VVKVHAOOUGNDPJ-SRVKXCTJSA-N Ser-Tyr-Ser Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CO)C(O)=O VVKVHAOOUGNDPJ-SRVKXCTJSA-N 0.000 description 1
- 238000000692 Student's t-test Methods 0.000 description 1
- -1 Thermo Fisher Chemical compound 0.000 description 1
- BIBYEFRASCNLAA-CDMKHQONSA-N Thr-Phe-Gly Chemical compound C[C@@H](O)[C@H](N)C(=O)N[C@H](C(=O)NCC(O)=O)CC1=CC=CC=C1 BIBYEFRASCNLAA-CDMKHQONSA-N 0.000 description 1
- SVGAWGVHFIYAEE-JSGCOSHPSA-N Trp-Gly-Gln Chemical compound C1=CC=C2C(C[C@H](N)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(O)=O)=CNC2=C1 SVGAWGVHFIYAEE-JSGCOSHPSA-N 0.000 description 1
- CDEZPHVWBQFJQQ-NKKJXINNSA-N Trp-Trp-Pro Chemical compound C1C[C@@H](N(C1)C(=O)[C@H](CC2=CNC3=CC=CC=C32)NC(=O)[C@H](CC4=CNC5=CC=CC=C54)N)C(=O)O CDEZPHVWBQFJQQ-NKKJXINNSA-N 0.000 description 1
- OOEUVMFKKZYSRX-LEWSCRJBSA-N Tyr-Ala-Pro Chemical compound C[C@@H](C(=O)N1CCC[C@@H]1C(=O)O)NC(=O)[C@H](CC2=CC=C(C=C2)O)N OOEUVMFKKZYSRX-LEWSCRJBSA-N 0.000 description 1
- KOVXHANYYYMBRF-IRIUXVKKSA-N Tyr-Glu-Thr Chemical compound C[C@H]([C@@H](C(=O)O)NC(=O)[C@H](CCC(=O)O)NC(=O)[C@H](CC1=CC=C(C=C1)O)N)O KOVXHANYYYMBRF-IRIUXVKKSA-N 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 201000003229 acute pancreatitis Diseases 0.000 description 1
- 101150063416 add gene Proteins 0.000 description 1
- 230000011759 adipose tissue development Effects 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 230000030741 antigen processing and presentation Effects 0.000 description 1
- 239000012472 biological sample Substances 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- 108700021042 biotin binding protein Proteins 0.000 description 1
- 102000043871 biotin binding protein Human genes 0.000 description 1
- 150000001615 biotins Chemical class 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 238000011088 calibration curve Methods 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 210000000234 capsid Anatomy 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000013522 chelant Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 210000000038 chest Anatomy 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 239000003593 chromogenic compound Substances 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 230000010437 erythropoiesis Effects 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 108010084389 glycyltryptophan Proteins 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 210000003494 hepatocyte Anatomy 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 238000003119 immunoblot Methods 0.000 description 1
- 238000010185 immunofluorescence analysis Methods 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 238000003364 immunohistochemistry Methods 0.000 description 1
- 238000009169 immunotherapy Methods 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 108010044056 leucyl-phenylalanine Proteins 0.000 description 1
- HWYHZTIRURJOHG-UHFFFAOYSA-N luminol Chemical compound O=C1NNC(=O)C2=C1C(N)=CC=C2 HWYHZTIRURJOHG-UHFFFAOYSA-N 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 210000003593 megakaryocyte Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 201000000050 myeloid neoplasm Diseases 0.000 description 1
- 210000002997 osteoclast Anatomy 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 229940055729 papain Drugs 0.000 description 1
- 235000019834 papain Nutrition 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 229940111202 pepsin Drugs 0.000 description 1
- 102000013415 peroxidase activity proteins Human genes 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 238000012503 pharmacopoeial method Methods 0.000 description 1
- 239000002953 phosphate buffered saline Substances 0.000 description 1
- 230000004983 pleiotropic effect Effects 0.000 description 1
- 230000008488 polyadenylation Effects 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000017854 proteolysis Effects 0.000 description 1
- 229940024999 proteolytic enzymes for treatment of wounds and ulcers Drugs 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 238000003127 radioimmunoassay Methods 0.000 description 1
- 238000003259 recombinant expression Methods 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 230000001850 reproductive effect Effects 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 210000000582 semen Anatomy 0.000 description 1
- 235000020183 skimmed milk Nutrition 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000002594 sorbent Substances 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 238000002798 spectrophotometry method Methods 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000012085 test solution Substances 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 108010038745 tryptophylglycine Proteins 0.000 description 1
- 241001515965 unidentified phage Species 0.000 description 1
- 210000000689 upper leg Anatomy 0.000 description 1
- 210000002845 virion Anatomy 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Biomedical Technology (AREA)
- Urology & Nephrology (AREA)
- Genetics & Genomics (AREA)
- Hematology (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Food Science & Technology (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Biotechnology (AREA)
- Peptides Or Proteins (AREA)
Abstract
Изобретение относится к области биотехнологии, в частности к антителу, специфичному к ИЛ-11 человека и модельных животных, таких как яванская макака, или его антигенсвязывающему фрагменту, а также к содержащему его конъюгату. Изобретение эффективно для определения в пробах концентрации ИЛ-11 человека и модельных животных, таких как яванская макака. 3 н.п. ф-лы, 2 ил., 3 пр.
Description
Область техники, к которой относится изобретение
Настоящее изобретение относится к области биотехнологии, иммунологии и медицины и может найти применение для лабораторной диагностики концентрации интерлейкина-11 в биологических жидкостях.
Уровень техники
Интерлейкин-11 (ИЛ-11) является плейотропным цитокином, относящимся к семейству интерлейкина-6 (ИЛ-6). Зрелый белок состоит из 178 аминокислотных остатков и имеет небольшую молекулярную массу (около 19 кДа). Гомология последовательности аминокислот ИЛ 11 человека и яванской макаки (Macacafascicularis) составляет 93,8% (Sokolov A.S. et al., Molecules 2016, 21, 1632). Рецепторами ИЛ-11 выступают мультисубъединичные мембранные комплексы, состоящие из a- (IL-11RA) и β-субъединиц (glycoprotein 130, gp 130). Специфическое связывание лиганда с субъединицей IL-11RA вызывает конформационное изменение последней, приводящее к увеличению ее сродства к gp 130. Гомодимеризация молекул gp 130 в составе мультимерного комплекса запускает передачу сигнала внутрь клетки посредством активации сигнальных каскадов JAKs/STAT 1,3, ERK/RAS и mTor/PI3K (Negahdaripour М. et al., Cytokine Growth Factor Rev. 2016;32:41-61).
ИЛ-11 непосредственно стимулирует пролиферацию клеток-предшественников мегакариоцитов и индуцирует созревание мегакариоцитов, что приводит к увеличению продукции тромбоцитов. Кроме этого он стимулирует эритропоэз, миелопоэз, лимфопоэз и развитие остеокластов, активирует синтез белков острой фазы гепатоцитами и ингибирует адипогенез.
Помимо участия ИЛ-11 в физиологически важных процессах, он вовлечен в патогенез ряда заболеваний, в том числе онкологических. Необходимость поиска новых маркеров для проведения диагностики заболеваний на возможно более ранних сроках, особенно это касается онкологических заболеваний, не вызывает сомнений.
Показано, что в плазме больных раком поджелудочной железы достоверно наблюдается повышенный уровень ИЛ-11 (Ren C.L. et al., Tumor Biol. 2014,35:11467-11472).
ИЛ-11 появляется в бронхоальвеолярной лаважной жидкости у больных раком легких, в том числе на фоне хронической обструктивной болезни легких (Pastor M.D. et al., J Thorac Oncol. 2016 Dec; 11 (12):2183-2192).
Спонтанные внутримозговые кровоизлияния сопровождаются повышением содержания ИЛ-11 в плазме крови и спинномозговой жидкости, более того уровень данного цитокина коррелирует со смертностью от данного заболевания (Fang H.Y. et al., Surg Neurol. 2005;64(6):511-7; Tu C.J. et al., J Int Med Res. 2011;39(4): 1265-74).
Концентрация ИЛ-11 сыворотке крови повышается у больных с приступами острого панкреатита и находится в прямой зависимости от их тяжести (Chen С.С. et al., Gut 1999;45:895-899).
Исходя из вышеизложенного ИЛ-11 может рассматриваться в качестве нового независимого маркера, мониторинг уровня которого в биологических жидкостях позволит диагностировать и следить за течением заболеваний, ассоциированных с экспрессией данного цитокина.
Повышенный уровень ИЛ-11 в семенной жидкости увеличивает оплодотворяющую способность сперматозоидов, поэтому содержание ИЛ-11 может быть одним из контрольных параметров качества эякулята при проведении вспомогательных репродуктивных технологий (Seshadri S. et al., Andrologia. 2011 Dec;43(6):378-86).
Из патента РФ RU 2318829 С2 известны нейтрализующие химерные или гуманизированные анти-ИЛ-6-антитела, содержащие не менее одного гипервариабельного участка тяжелой или легкой цепи мышиного моноклонального антитела CLB-8. Предпочтительными антителами согласно изобретению являются антитела, которые связываются с участком молекулы ИЛ-6, отвечающим за связывание с gp 130 (сайт 1). Описаны последовательности ДНК, кодирующие гипервариабельные участки 1-3 легкой и тяжелой цепей мышиного моноклонального антитела CLB-8, а также их аминокислотные последовательности. Раскрыт состав лекарственных препаратов на основе указанных антител и их применение для лечения онкологических или иных заболеваний, опосредуемых ИЛ-6. Однако описанные в данном патенте антитела не являются специфичными к интерлейкину-11, и, следовательно, не могут использоваться для диагностики или лечения заболеваний, ассоциированных с ИЛ-11.
В патенте США US 6998123 (В1) описан способ лечения или облегчения симптомов патологических состояний, при которых наблюдается снижение плотности костной ткани, при помощи введения пациенту эффективного количества анти-ИЛ-11 антител, которые блокируют образование мультимерного лиганд-рецепторного комплекса на поверхности клеток. Термин «анти- ИЛ-11 антитело» в данном патенте применяется для определения нейтрализующих химерных, гуманизированных или гибридных моноклональных антител, а также фрагментов антител, способных связываться с антигеном. В патенте приводятся результаты использования только одного типа молекул анти-ИЛ-11 антител на мышиной модели: у мышей с удаленными обоими яичниками после внутрибрюшинного введения афинно очищенных поликлональных антител козы против ИЛ-11 мыши наблюдается больший объем губчатой костной ткани в бедренной кости по сравнению с контрольной группой животных. В документе не приведено описание строения используемых антител, в том числе аминокислотной последовательности, а также деталей их получения. Указанный способ применения анти-ИЛ-11 антител относится к терапии заболеваний, при этом отсутствует информация о потенциальном использовании данных анти-ИЛ-11 антител в диагностике патологических состояний, при которых наблюдается снижение плотности костной ткани.
Раскрытие изобретения
Целью настоящего изобретения является устранение вышеуказанных недостатков аналогов анти-ИЛ-11 антител путем создания настоящего изобретения.
Изобретение представляет собой антитела, специфичные к ИЛ-11 человека и модельных животных, таких как яванская макака, или их производные, или антигенсвязывающие фрагменты антител, в которых вариабельные домены тяжелой и легкой цепей содержат одну из следующих комбинаций аминокислотных последовательностей гипервариабельных участков:
Антитела, соответствующие изобретению, могут быть полной длины или могут содержать только антиген-связывающий фрагмент (например, фрагмент Fab, F(ab')2).
Антитела могут быть моноклональными химерными, гуманизированными или гибридными, различных классов и подклассов, наиболее предпочтительно IgG1 или IgG4.
Термин «антитело», используемый здесь, предназначен для определения полноразмерных молекул иммуноглобулина, состоящих из четырех полипептидных цепей (две тяжелые (Н) цепи и две легкие (L) цепи), связанных дисульфидными связями. Каждая тяжелая цепь содержит вариабельный участок (сокращенный здесь как VH) и константный участок, содержащий три домена CH1, СН2 и СН3. Каждая легкая цепь содержит вариабельный участок (сокращенный здесь как VL) и константный участок, содержащий один домен CL. Участки VH и VL состоят из трех гипервариабельных участков, которые окружены четырьмя более консервативными каркасными участками. Гипервариабельные участки называют также участками, определяющими комплементарность, и обозначают как CDR (complementarity determining regions), поскольку именно они образуют антигенсвязывающие центры молекулы антитела. Каркасные участки (FR, framework regions) обычно не принимают участия в связывании антигена, но имеют существенное значение для укладки V-домена, которая обеспечивает адекватную конформацию антигенсвязывающего центра.
Термин «антиген-связывающий фрагмент» антитела (или просто «фрагмент антитела»), используемый здесь, относится к одному или более фрагментам антитела, которые сохраняют способность специфически связывать антиген ИЛ-11 человека и модельных животных. Примеры связывающих фрагментов, охватываемые термином "антиген-связывающий фрагмент" антитела, включают (i) фрагмент Fab, моновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; (ii) фрагмент F(ab')2, бивалентный фрагмент, содержащий два фрагмента Fab, связанные дисульфидным мостиком в районе петли. Далее, антитело или его антиген-связывающий фрагмент могут быть частью более крупных молекул иммуноадгезии, образованных ковалентной или нековалентной связью антитела или фрагмента антитела с одним или более белком или пептидом.
В одном варианте осуществления изобретение представляет собой полноразмерное антитело подкласса IgG1, обозначаемое U13, у которого аминокислотные последовательности гипервариабельных участков вариабельных доменов тяжелой и легкой цепей соответствуют комбинации # 1.
В другом варианте осуществления изобретение представляет собой полноразмерное антитело подкласса IgG1, обозначаемое L1, у которого аминокислотные последовательности гипервариабельных участков вариабельных доменов тяжелой и легкой цепей соответствуют комбинации # 2.
В еще одном варианте осуществления изобретение представляет собой Fab фрагмент, обозначаемый Fab3, у которого аминокислотные последовательности гипервариабельных участков вариабельных доменов тяжелой и легкой цепей соответствуют комбинации # 1.
В другом варианте осуществления изобретение представляет собой Fab фрагмент, обозначаемый Fab11, у которого аминокислотные последовательности гипервариабельных участков вариабельных доменов тяжелой и легкой цепей соответствуют комбинации # 2.
Еще одним объектом настоящего изобретения являются производные антител или их фрагментов, например, гибридные белки. В качестве молекул слияния могут выступать другие полипептиды, например, биотин и белки с ферментативной активностью, такие как пероксидаза хрена и щелочная фосфатаза, а также органические или неорганические молекулы, например, флуоресцентные метки (например, флуоресцеин, изотиоцианат флуоресцеина, родамин, хлорид 5-диметиламин-1-нафталинсульфонила, фикоэритрин и т.п.), радиоактивные метки (например, изотопы Р-32 и I-125) или хемилюминесцентные метки (например, люминол и его производные).
В еще одном варианте осуществления изобретение представляет собой антитело U13, конъюгированное с молекулой биотина, обозначаемое U13-bio.
В еще одном варианте осуществления изобретение представляет собой антитело L1, конъюгированное с молекулой биотина, обозначаемое L1-bio.
Антитела, или их антигенсвязывающие фрагменты, или их производные, соответствующие изобретению, обладают хотя бы одним из следующих свойств:
1) способны специфически связываться с ИЛ-11 человека и модельных животных, таких как яванская макака;
2) способны связываться с ИЛ-11 с высокой аффинностью: равновесная константа диссоциации (Kd) равна 1×10-8 М или меньше, и кинетическая константа диссоциации (Koff) 1×10-4c-1 или меньше, определенные, например, с помощью метода поверхностного плазмонного резонанса;
3) величина равновесной константы диссоциации при связывании ИЛ-11 человека отличается от величины Kd связывания ИЛ-11 модельных животных, таких как яванская макака, не более 10 раз;
4) молекулы с разным набором гипервариабельных участков не конкурируют между собой за связывание с ИЛ-11
Антитела U13 и L1 имеют следующие параметры связывания ИЛ-11 человека:
1) Kd, равная 1,0×10-11 М и 5,0×10-10 М, соответственно;
2) Koff, равная 2,0×10-6 с-1 и 8,0×10-5 с-1, соответственно.
Антитела U13 и L1 имеют следующие параметры связывания ИЛ-11 яванской макаки:
3) Kd, равная 7,0×10-11 М и 2,0×10-10 М, соответственно;
4) Koff, равная 7,0×10-6 с-1 и 2,0×10-5 с-1, соответственно.
Антитела могут быть получены общепринятыми методами, например, иммунизацией соответствующим антигеном животных, или гибридомной технологией, или при помощи технологии генной инженерии. Методы получения антител описаны в литературе: Zola, Н. (CRC Press, 1987). Monoclonal Antibodies: A Manual of Techniques; John G.R. Hurrell (CRC Press, 1982). Monoclonal Hybridoma Antibodies: Techniques and Applications.
Фрагменты антител получают расщеплением антител соответствующими протеолитическими ферментами, например, папаином и пепсином, а также при помощи технологии рекомбинантной ДНК.
Для отбора рекомбинантных антител требуемой специфичности используют такие технологии, как фаговый дисплей. Чаще всего для фагового дисплея используют нитчатые фаги Ff семейства (М13, fd, f1). Нуклеотидные последовательности, кодирующие фрагменты антител, например, Fab или scFv, объединяют в составе фагового генома или фагмид с частью гена одного из пяти белков оболочки бактериофагов, наиболее часто используют рШ и pVIII. В результате фаговые частицы экспрессируют в составе капсида копии корового белка с пришитой к ним полипептидной последовательностью фрагмента антител. Отбор как правило осуществляют в виде нескольких последовательных раундов, каждый из которых включает сорбцию фаговых частиц, экспрессирующих соответствующие фрагменты антител, на носителях с иммобилизованным антигеном, отмывку несвязавшихся частиц, элюирование оставшихся связанными и размножение полученных фагов в бактериальных клетках. Выделяют и секвенируют фаговую ДНК или фагмиды. Фаговый дисплей широко описан в литературе: Bradbury A.R., Marks J.D. Antibodies from phage antibody libraries. J. Immunol. Methods 2004, 290, 29-49; Ledsgaard, L. et al. Basics of Antibody Phage Display Technology. Toxins 2018, 10, 236; John M. Walker. The Protein Protocols Handbook. Springer, 2007.
Технология рекомбинантной ДНК подразумевает получение экспрессионных генетических конструкций, кодирующих цепи антитела под контролем соответствующих регуляторных элементов в одном или разных несущих векторах. Регуляторные элементы представляют собой промоторные последовательности и сигнальные последовательности, например, сигналы полиаденилирования, которые контролируют транскрипцию или трансляцию генов цепи антитела. Такие регуляторные последовательности описаны, например, в работе Gene Expression Technology: Methods in Enzymology, vol. 185, Edited by David V. Goeddel, Academic Press, San Diego, CA (1990).
Экспрессионные конструкции одну или более переносят общепринятыми методами в клетки, пригодные для экспрессии и предпочтительно секреции антител в культуральную среду. Клетками продуцентами полноразмерных антител предпочтительно являются клетки млекопитающих линий СНО (клетки яичников китайского хомячка), SP2/0 (клетки мышиной миеломы) или HEK293 (клетки человеческой эмбриональной почки). Данные клеточные линии пригодны как для получения линий, стабильно экспрессирующих целевое антитело, так и для наработки антител лишь некоторое время (транзиентная экспрессия). Фрагменты антител, например, Fab, производят в бактериях, дрожжах, нитчатых грибах и линиях клеток насекомых. Трансформированные клетки культивируют общепринятыми методами и выделяют антитела, их фрагменты из культуральной среды. Стандартные способы с применением рекомбинантной ДНК используются для получения генов тяжелой и легкой цепей, включения этих генов в рекомбинантные экспрессионные векторы и введения векторов в клетки-хозяина так, как описано Sambrook, J., Fritsch Е. F., and Т. Maniatis. Molecular cloning: A laboratory manual, Second Edition, Cold Spring Harbor, N.Y. (1989); Ausubel F., Brent R. et al. Current Protocols in Molecular Biology, John Wiley & Sons (2003).
Производные антител и их фрагментов получают в том числе в результате химической модификации с использованием активированных производных молекул слияния. Например, самым распространенным и универсальным методом биотинилирования является химическая модификация с использованием активированных производных биотина, таких как биотинил-N-гидроксисукцинимид (BNHS), при этом биотин присоединяется по ε - аминогруппам остатков лизина в молекуле антител и их фрагментов. Подробное описание биотинилирования приведено в литературе, например, Diamandis Е. Р and Christopoulos Т K (1991) The biotin-(strept)avidin system principles and applications in biotechnology Chn Chem 37, 625-636.
Следующий аспект изобретения касается способа определения в пробах наличия и концентрации ИЛ-11 человека и модельных животных, таких как яванская макака, заключающийся в том, что 1) исследуемый образец, содержащей ИЛ-11, приводят в контакт с антителами, или их фрагментами, или производными, являющимися объектами настоящего изобретения, и 2) оценивают наличие и концентрацию иммунных комплексов антител, или их фрагментов, или производных с антигеном (ИЛ-11).
В качестве проб, в которых необходимо определить наличие или концентрацию ИЛ-11, могут быть образцы биологических жидкостей (например, кровь, плазма, сыворотка) и кусочки ткани, полученные в результате биопсии, организма человека и модельных животных, например, яванской макаки, а также образцы супернатантов клеточных культур, растворы очищенных рекомбинантных ИЛ-11 человека и животных, например, яванской макаки.
Для лабораторной диагностики наличия и концентрации ИЛ-11 в образцах биологических жидкостей, супернатантах клеточных культур и растворах очищенного ИЛ-11 может быть использован широкий круг методов иммуноанализа, среди которых иммуноблоттинг, иммуноферментный, радиоиммунный и иммунофлуоресцентный анализ, иммунотурбодиметрия. В образцах тканей для определения наличия ИЛ-11 используют метод иммуногистохимии.
В зависимости от дизайна эксперимента антитела, их производные или фрагменты, соответствующие настоящему изобретению, могут использоваться по отдельности или попарно друг с другом.
В еще одном варианте осуществления изобретение представляет собой сэндвич-вариант иммуноанализа с использованием пар антител U13 и L1, а также их конъюгатов, например, U13-bio или L1-bio. Антитела U13 и L1 и их конъюгаты специфически распознают разные неперекрывающиеся участки молекулы ИЛ-11 (эпитопы), благодаря чему между ними отсутствует конкуренция за связывание с антигеном. Данный способ анализа позволяет добиться высокой чувствительности, точности и специфичности при определении антигена даже в гетерогенных образцах, таких как биологические жидкости и ткани, супернатанты клеточных культур.
Биологический образец может быть подвергнут предварительной обработке или же непосредственно приведен в контакт, по меньшей мере, с одним захватывающим антителом в условиях, способствующих контакту с эпитопом.
В соответствии с предпочтительным способом реализации захватывающие антитела подвергают иммобилизации на твердой фазе. В качестве неограничивающих примеров твердой фазы можно использовать микропланшеты, в особенности микропланшеты из полистирола типа тех, что выпускают фирмы Thermo scientific NUNC (Дания) и Corning-Costar (CIIIA). Использование твердой фазы позволяет увеличить чувствительность метода благодаря удалению веществ, не участвующих в реакции, за счет иммобилизации на твердой фазе одного из компонентов реакционной смеси.
В качестве детектирующего антитела, как правило, используют конъюгированные антитела, направленные против другого эпитопа ИЛ-11.
Предлагаемый способ ИФА включает в себя фиксацию на поверхности лунок пластикового планшета захватывающих антител против ИЛ-11; блокирование неспецифических мест связывания; внесение в лунки исследуемого материала и инкубирование планшета; отмывку буферным раствором от молекул антигена, несвязавшихся с захватывающими антителами; внесение в лунки детектирующих антител и инкубирование планшета; отмывку буферным раствором от молекул детектирующих антител, несвязавшихся с комплексом антиген-антитело на поверхности твердой фазы; определение концентрации иммунных комплексов.
Если детектирующие антитела представляют собой конъюгат с ферментом, то концентрацию иммунных комплексов определяют по активности ферментной метки: вносят в реакционную смесь соответствующий хромогенный субстрат и определяют содержание окрашенных продуктов ферментативных реакций по изменению оптической плотности раствора при определенной длине волны. Благодаря способности одной молекулы фермента катализировать превращение большого числа молекул субстрата достигается высокая чувствительность метода.
Если детектирующие антитела представляют собой конъюгат с биотином, то иммунные комплексы детектируют, например, при помощи биотинсвязывающих белков, например, авидина яичного белка или стрептавидина, сшитых с флуоресцентной, хемилюминесцентной или ферментной меткой.
Экспериментальные данные иммуноанализа сэндвич-типа преимущественно представляют в виде графика зависимости величины сигнала от концентрации антигена (ИЛ-11) в пробе, построенному при помощи калибровочных растворов с известной концентрацией антигена. Для изготовления калибровочных растворов может быть использован раствор высокоочищенного рекомбинантного ИЛ-11 человека или модельных животных, или референсный препарат ИЛ-11 NIBSC 92/788, рекомендованный ВОЗ в качестве стандарта. При отсутствии лимитирующих факторов в рабочем диапазоне метода должна существовать прямая линейная зависимость между величиной сигнала и концентрацией антигена. Однако реальные кривые сэндвич-анализов могут иметь в разной степени искаженный вид, поэтому проводят линеаризующие преобразования, например, используют логарифмический масштаб величин по оси абсцисс и/или ординат.
Концентрацию антигена в исследуемой пробе определяют по калибровочному графику, исходя из измеренной величины сигнала.
Нижеследующие рисунки и примеры раскрывают изобретение, не ограничивая его.
Краткое описание рисунков
На Рис. 1А представлен график зависимости среднего значения оптической плотности при длине волны 492 нм от логарифма по основанию 2 концентрации ИЛ-11 человека в калибровочных растворах (в нг/мл) для определения концентрации ИЛ-11 человека в пробах методом твердофазного иммуноферментного анализа с использованием сэндвич-пары анти-ИЛ-11: захватывающих антител U13, адсорбированных на пластике в лунках 96-луночного микропланшета, и детектирующих антител L1-bio, конъюгированных с биотином.
На Рис. 1Б представлен график зависимости среднего значения оптической плотности при длине волны 492 нм от логарифма по основанию 2 концентрации ИЛ-11 человека в калибровочных растворах (в нг/мл) для определения концентрации ИЛ-11 человека в пробах методом твердофазного иммуноферментного анализа с использованием сэндвич-пары анти-ИЛ-11: захватывающих антител L1, адсорбированных на пластике в лунках 96-луночного микропланшета, и детектирующих антител U13-bio, конъюгированных с биотином.
На Рис. 2А представлен сенсограммы и теоретические кривые взаимодействия антитела U13 с ИЛ-11 человека (верхняя панель) и яванской макаки (нижняя панель), согласно данным метода поверхностного плазмонного резонанса (НИР). Лиганды ковалентно пришиты на поверхности сенсорного чипа за аминогруппы. Концентрации нанесения антител в рабочем буфере: 15, 12.9, 8.57 нМ. Анализ данных проведен в программе ProteOn Manager 3.0 в рамках схемы бивалентного аналита.
На Рис. 2Б представлен сенсограммы и теоретические кривые взаимодействия антитела L1 с ИЛ-11 человека (верхняя панель) и яванской макаки (нижняя панель), согласно данным метода поверхностного плазмонного резонанса (ППР). Лиганды ковалентно пришиты на поверхности сенсорного чипа за аминогруппы. Концентрации нанесения антител в рабочем буфере: 10, 8.57, 2.58 нМ. Анализ данных проведен в программе ProteOn Manager 3.0 в рамках схемы бивалентного аналита.
Пример 1
Определение концентрации ИЛ-11 человека методом иммуноферментного анализа с использованием сэндвич-пары антител L1 и U13-bio, или U13 и L1-bio
I. Сорбция захватывающих антител на твердой фазе В лунки 96-луночного планшета из полистерола помещают по 100 мкл фосфатно-солевого буфера рН 7,2-7,4 (1xPBS), содержащего 1-2 мкг антител L1 или U13. Закрытый крышкой планшет выдерживают в течение 16-18 часов при температуре +(5±3)°С или в течение 2-6 часов при температуре +(37±2)°С при постоянном встряхивании/перемешивании. Содержимое лунок удаляют без промывания или лунки промывают от несвязавшихся молекул антител 1-3 раза буфером 1xPBS, содержащим 0,05-0,1% полисорбата 20 (1xPBST), по 250-300 мкл.
II. Блокировка мест неспецифичного связывания на твердой фазе В лунки планшета помещают по 250 мкл буфера 1xPBST, содержащего 0,5-1,0% бычьего сывороточного альбумина или яичного овальбумина, или обезжиренного молока. Закрытый крышкой планшет выдерживают в течение 1-2 часов при температуре +(37±2)°С или при комнатной температуре при постоянном встряхивании/перемешивании.
Содержимое лунок удаляют и лунки промывают 1-3 раза буфером 1xPBST по 250-300 мкл.
III. Инкубация с антигеном
В лунки планшета помещают по 100 мкл проб биологических жидкостей, либо двукратных разведений стандарта ИЛ-11 человека. Разведения антигена должны быть приготовлены на основе 1xPBST, содержащего 0,1% бычьего сывороточного альбумина или яичного овальбумина, или нежирного молока, поскольку полисорбат 20 снижает неспецифичное связывание белковых молекул друг с другом и с поверхностью планшета, а белок препятствует протеолизу антигена. Исследуемый раствор и стандартные разведения антигена вносят по 2-3 повторности, используя по две (три) лунки на каждое разведение белка. Закрытый крышкой планшет выдерживают в течение 0,5-2 часов при температуре +(37±2)°С или при комнатной температуре при постоянном встряхивании/перемешивании. Содержимое лунок удаляют и лунки промывают 3-5 раза буфером 1xPBST по 250-300 мкл.
IV. Инкубация с детектирующими антителами
В лунки планшета помещают по 100 мкл буфера 1xPBST, содержащего 0,1% бычьего сывороточного альбумина или яичного овальбумина, или нежирного молока, и не менее 2 мкг/мл антител U13-bio или L1-bio, конъюгированных с биотином (в паре с адсорбированными антителами L1 используют антитела U13-bio, а с антителами U13 - антитела L1-bio). Закрытый крышкой планшет выдерживают в течение 30-60 мин при температуре +(37±2)°С или при комнатной температуре при постоянном встряхивании/перемешивании. Содержимое лунок удаляют и лунки промывают 3-5 раз буфером 1xPBST по 250-300 мкл.
V. Детектирование иммунных комплексов на твердой фазе
В лунки планшета помещают по 100 мкл буфера 1xPBST, содержащего конъюгат стрептавидина с пероксидазой хрена (например, Thermo Fisher, кат. № N100). Оптимальная концентрация конъюгированного стрептавидина как правило указывается производителем данного реагента (обычно составляет не менее 1/4 000). Закрытый крышкой планшет выдерживают в течение 30-45 мин при температуре +(37±2)°С или при комнатной температуре при постоянном встряхивании/перемешивании. Содержимое лунок удаляют и лунки промывают 3-5 раз буфером 1xPBST по 250-300 мкл.
В лунки вносят по 100 мкл раствора субстрата пероксидазы хрена и инкубируют при комнатной температуре и постоянном перемешивании 5-15 мин в защищенном от света месте. В качестве субстрата пероксидазы хрена может быть использован OPD (o-phenylenediamine dihydrochloride), например, Thermo Fisher, кат. №34006, в буфере, содержащем пероксид водорода, например, Thermo Fisher, кат. №34062.
Проводят остановку реакции внесением в каждую лунку по 50 мкл 10% раствора серной кислоты. После этого сразу приступают к измерению оптической плотности раствора при соответствующей длине волны (для субстрата OPD 492 нм) с использованием планшетного спектрофотометра.
Интерпретацию результатов проводят следующим образом. Строится график зависимости средних значений оптической плотности калибровочных растворов, рассчитанных по нескольким повторным измерениям, от логарифма концентрации ИЛ-11. Определяется формула области линейного участка (формула линии тренда), с помощью которой определяется численное значение концентрации ИЛ-11 в исследуемых пробах в зависимости от значений их оптической плотности.
Полученные результаты приведены на Рис. 1, где на Рис. 1А представлены результаты, полученные с использованием сэндвич-пары антител U13 и L1-bio, а на Рис. 1Б - с использованием сэндвич-пары антител L1 и U13-bio.
Под «правильностью» методики понимают степень близости среднего значения концентрации ИЛ-11 в исследуемых пробах, полученного на основании серии результатов измерений, к принятому опорному значению. В качестве опорного значения используют действительное значение концентрации аналита (ИЛ-11) в пробе, рассчитанное с учетом концентрации аналита в исходном растворе, измеренной одним из фармакопейных методов определения концентрации белка (например, спектрофотометрическим анализом) или указанной в паспорте, и степени разведения исходного раствора в процессе приготовления пробы.
где Xi - результат i-го измерения концентрации,
n - количество измерений концентрации аналита в пробах одного и того же однородного образца.
Правильность (Т) выражают в процентах среднего значения концентрации ИЛ-11 в пробах от опорного значения, для расчета используют формулу:
где Xt - действительное значение концентрации аналита (ИЛ-11) в пробах одного и того же однородного образца.
Истинное значение величины правильности методики иммуноферментного анализа, описанной в Примере 1, с вероятностью 95% лежит в промежутке от 80 до 115%) с использованием сэндвич-пары антител U13 и L1-bio, и в промежутке от 90 до 110%. с использованием сэндвич-пары антител L1 и U13-bio.
Для расчета доверительного интервала, в который попадают величины правильности, рассчитанные для концентраций аналита в рабочем диапазоне конкретной методики иммуноанализа, используют методы математической статистики, например, через критическое значение критерий Стьюдента.
Пример 2
Измерение величин кинетических и равновесных констант ассоциации/диссоциации комплекса ИЛ-11 человека или модельных животных с антителами U13 и L1 методом поверхностного плазмонного резонанса
Измерение проводят при температуре +(25±1)°С, используя спектрометр Bio-Rad ProteOn™ XPR36. Для этого лиганд (ИЛ-11 человека или яванской макаки) иммобилизуют на поверхности чипа ProteOn™ GLH #176-5013 через аминогруппы. Контроль степени завершенности фазы иммобилизации лиганда на чипе проводят по кинетике сигнала ППР.
В перпендикулярном направлении наносят на чип раствор аналита (антител U13 или L1) в рабочем буфере (10 мМ HEPES, 150 мМ NaCl, 0,05% Tween 20, рН 7.4) в пяти различных концентрациях белка от 2,0 нМ до 20 нМ, а на одну дорожку - рабочий буфер в качестве контроля. Контроль степени завершенности фазы диссоциации комплекса проводят по величине снижения сигнала ППР.
Поверхность чипа регенерируют после цикла связывания с аналитом пропусканием через чип 10 мМ глицин рН 2.0 в течение 300 сек.
Расчет констант взаимодействия лиганда с аналитом проводят в стандартной программе Bio-Rad ProteOn Manager 3.0 с использованием простейшей схемы бивалентного аналита для не менее трех концентраций аналита.
Полученные результаты приведены на Рис. 2.
Пример 3
Получение полноразмерных антител
Получение Fab-фрагментов антител проводили с использованием технологии на основе трех фаговых библиотек компании ООО «Антерикс», г. Пущино: Fab2h-library, Fab5h-library, Fab7h-library.
Технология фагового дисплея описана в литературе, например, Bazan, J., I. Calkosinski, and A. Gamian, Phage display-a powerful technique for immunotherapy: 1. Introduction and potential of therapeutic applications. Hum Vaccin Immunother, 2012. 8(12): p. 1817-28.
Из исходного разнообразия фаговых библиотек в ходе трех раундов селекции были отобраны фаговые частицы, содержащие на своей поверхности Fab-фрагменты антител, специфически связывающихся с ИЛ-11 человека и макаки. Использованы две схемы селекции, отличающиеся порядком презентации антигенов (ИЛ-11 человека - ИЛ-11 макаки - ИЛ-11 человека и ИЛ-11 макаки - ИЛ-11 человека - ИЛ-11 человека).
Фагмиды из бактериальных клеток, инфицированных отобранными вирионами, выделяли при помощи набора QIAprep Spin Miniprep kit (Qiagen, #27106) и секвенировали.
Последовательности, кодирующие домены VL, VH, CL и СН1 антител, из отобранных фагмид были переклонированы в вектор pLL4 (Addgene plasmid #107208) для экспрессии в клетках Е. coli штамма BL-21(DE3) Fab-фрагментов, несущих 8XHis метку на С-конце. Выделение и очистку фрагментов антител из клеточного лизата проводили с помощью металл-хелатной хроматографии. Скрининг Fab-фрагментов на предмет их специфичности к ИЛ-11 человека и макаки проводили при помощи ИФА.
Для создания полноразмерных антител последовательность, кодирующую VH домен, клонировали в экспрессионный вектор рТТ5, содержащий последовательности, кодирующие константные области IgG1 человека (CH1, СН2, СН3), в то время, как последовательность, кодирующую VL домен, клонировали в экспрессионный вектор рТТ5, содержащий последовательности, кодирующие константные области k-легкой цепи человека (CL).
Наработку антител проводили в системе транзиентной экспрессии в эукариотических клетках линии СНО-3Е7 (RRID:CVCL_JY74), адаптированных для продукции белков млекопитающих. Клетки СНО-3Е7 котрансфицировали полученными плазмидами с использованием полиэтиленимина (PEI, polyethylenimine). Выделение и очистку антител из культуральной среды проводили с помощью аффинной хроматографии с использованием сорбента с иммобилизованным белком A (HiTrap rProtein A FF, GE Healthcare Life Sciences), имеющим высокое сродство к иммуноглобулинам класса G. Полученные антитела были диализованы и стерилизованы фильтрацией через 0,22 мкм фильтр. Сродство полученных антител к ИЛ-11 было проверено с помощью ИФА и спектроскопии поверхностного плазмонного резонанса.
Использованные в работе рутинные методы широко описаны в литературе (Barbas CF, Wagner J (1995). Synthetic Human Antibodies: Selecting and Evolving Functional Proteins. Methods. 8 (2): 94-103. doi: 1.0.1006/meth. 1995.9997; Barbas CF (1995). Synthetic human antibodies. Nat. Med. 1 (8): 837-839. doi:10.1038/nm0895-837. PMID 7585190; Wild D. The Immunoassay Handbook (4th edition). Theory and applications of ligand binding, ELISA and related techniques. 2013; Greenfield E.A., Antibodies. A laboratory manual. Second edition. 2014).
Последовательность тяжелой цепи HCDR1
SEQ ID № 1:Phe Thr Phe Thr Gly Tyr Trp Met Asn Trp Val Arg;
Последовательность тяжелой цепи HCDR2
SEQ ID № 2:Val Ser Ser Ile Ser Ser Tyr Gly Gly Gly Thr Tyr Tyr Ala Asp Ser;
Последовательность тяжелой цепи HCDR3
SEQ ID № 3:Cys Ala Arg Glu Ser Leu His Gln Leu Phe Asp Tyr Trp Gly Gln;
Последовательность легкой цепи LCDR1
SEQ ID № 4:Gln Ser Val Ser Ser Ser;
Последовательность легкой цепи LCDR2
SEQ ID № 5:Gly Ala Ser Ser Arg Ala Thr;
Последовательность легкой цепи LCDR3
SEQ ID № 6:Cys Gln Gln Ser Tyr Ser Tyr Ala Pro Ile Thr Phe Gly Gln;
Последовательность тяжелой цепи HCDR1
SEQ ID № 7:Phe Thr Phe Thr Asp Tyr Trp Met Asn Trp Val Arg;
Последовательность тяжелой цепи HCDR2
SEQ ID № 8:Val Ser Thr Ile Ala Ser Ser Asn Ser Tyr Thr Asp Tyr Ala Asp Ser;
Последовательность тяжелой цепи HCDR3
SEQ ID № 9:Cys Ala Arg Glu Ser Trp Ser Glu Gly Trp Trp Pro Ser Gly Phe Asp Tyr Trp Gly Gln;
Последовательность легкой цепи LCDR3
SEQ ID № 10:Cys Gln Gln Tyr Glu Thr Ser Pro Ile Thr Phe Gly Gln.
Claims (20)
1. Антитело, специфичное к ИЛ-11 человека и модельных животных, таких как яванская макака, или его антигенсвязывающий фрагмент, в которых вариабельные домены тяжелой и легкой цепей содержат одну из следующих комбинаций аминокислотных последовательностей гипервариабельных участков:
# 1:
HCDR1: SEQ ID №1,
HCDR2: SEQ ID №2,
HCDR3: SEQ ID №3,
LCDR1: SEQ ID №4,
LCDR2: SEQ ID №5,
LCDR3: SEQ ID №6,
и/или
#2:
HCDR1: SEQ ID №7,
HCDR2: SEQ ID №8,
HCDR3: SEQ ID №9,
LCDR1: SEQ ID №4,
LCDR2: SEQ ID №5,
LCDR3: SEQ ID №10.
2. Конъюгат для определения в пробах концентрации ИЛ-11 человека и модельных животных, таких как яванская макака, содержащий антитело или его антигенсвязывающий фрагмент по п. 1, конъюгированный с биотином.
3. Способ определения в пробах концентрации ИЛ-11 человека и модельных животных, таких как яванская макака, заключающийся в том, что:
1) исследуемый образец, содержащей ИЛ-11, приводят в контакт с антителом или его антигенсвязывающим фрагментом по п. 1,
2) оценивают концентрацию иммунных комплексов антитела или его антигенсвязывающего фрагмента по п. 1 с антигеном ИЛ-11.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2020111785A RU2763178C2 (ru) | 2020-03-23 | 2020-03-23 | Антитела для лабораторной диагностики концентрации интерлейкина-11 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2020111785A RU2763178C2 (ru) | 2020-03-23 | 2020-03-23 | Антитела для лабораторной диагностики концентрации интерлейкина-11 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2016151730A Previously-Filed-Application RU2016151730A (ru) | 2016-12-28 | 2016-12-28 | Антитела для лабораторной диагностики концентрации интерлейкина-11 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2020111785A RU2020111785A (ru) | 2021-09-23 |
| RU2020111785A3 RU2020111785A3 (ru) | 2021-09-23 |
| RU2763178C2 true RU2763178C2 (ru) | 2021-12-28 |
Family
ID=77836461
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2020111785A RU2763178C2 (ru) | 2020-03-23 | 2020-03-23 | Антитела для лабораторной диагностики концентрации интерлейкина-11 |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2763178C2 (ru) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN119080927B (zh) * | 2023-06-05 | 2025-06-24 | 北京东方百泰生物科技股份有限公司 | 一种结合il-11的抗体、其抗原结合片段及应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6407218B1 (en) * | 1997-11-10 | 2002-06-18 | Cytimmune Sciences, Inc. | Method and compositions for enhancing immune response and for the production of in vitro mabs |
| US7094402B2 (en) * | 1994-12-22 | 2006-08-22 | Genetics Institute, Llc | Antibodies to human interleukin-11 receptor |
| RU2515108C2 (ru) * | 2005-08-19 | 2014-05-10 | Эббви Инк | Иммуноглобулин с двойными вариабельными доменами и его применения |
-
2020
- 2020-03-23 RU RU2020111785A patent/RU2763178C2/ru active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7094402B2 (en) * | 1994-12-22 | 2006-08-22 | Genetics Institute, Llc | Antibodies to human interleukin-11 receptor |
| US6407218B1 (en) * | 1997-11-10 | 2002-06-18 | Cytimmune Sciences, Inc. | Method and compositions for enhancing immune response and for the production of in vitro mabs |
| RU2515108C2 (ru) * | 2005-08-19 | 2014-05-10 | Эббви Инк | Иммуноглобулин с двойными вариабельными доменами и его применения |
Non-Patent Citations (1)
| Title |
|---|
| HAM et al., Critical role of interleukin-11 in isoflurane-mediated protection against ischemic acute kidney injury in mice, Anesthesiology, 2013, Vol. 119, N. 6, pp. 1389-1401. * |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2020111785A (ru) | 2021-09-23 |
| RU2020111785A3 (ru) | 2021-09-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN110167967B (zh) | 针对抗pd-l1抗体的独特型抗体及其用途 | |
| CN102112489B (zh) | 抗-hepcidin-25选择性抗体及其用途 | |
| US6998241B2 (en) | Antibody pair screening methods | |
| AU2010309931B2 (en) | Non-cross-reactive anti IgG antibodies | |
| KR20150041801A (ko) | 복합체-특이적 항체 및 항체 단편 및 그의 용도 | |
| US9766251B2 (en) | Anti-human IgG1 antibody | |
| CN113156134B (zh) | 用于检测人白介素23的elisa试剂盒及检测方法 | |
| RU2763178C2 (ru) | Антитела для лабораторной диагностики концентрации интерлейкина-11 | |
| CN117624367B (zh) | 抗人cd141蛋白的兔单克隆抗体及其应用 | |
| CN117264072B (zh) | 一种抗sn38单抗及其应用 | |
| CN115947844B (zh) | 一种新的抗人il-33单克隆抗体、包含其的试剂盒及其检测方法 | |
| CN119350501B (zh) | 一种抗reg3a蛋白的抗体或其抗原结合片段及其用途 | |
| US7517663B2 (en) | Rabbit monoclonal antibody against Id1 protein | |
| CN118852448B (zh) | 蒜氨酸单克隆抗体及其制备方法与应用 | |
| US20250263505A1 (en) | Antibody against kynurenine | |
| CN110579610A (zh) | 用于检测t细胞活化的v域免疫抑制因子的试剂盒 | |
| CN112724253B (zh) | 抗人穹窿体蛋白的抗体及其应用 | |
| CN111208307B (zh) | 一种与参照分子具有相同或不同的靶蛋白结合的分子的筛选方法 | |
| EP4194054A1 (en) | Camelid antibodies for use in therapy and diagnosis | |
| CN108727493B (zh) | 抗Stathmin单克隆抗体及其用途 | |
| CN116143929A (zh) | 抗重组人凝血因子VIIa-Fc融合蛋白的抗体及其应用 | |
| CN116333139A (zh) | 一种抗fda0128抗体、其制备方法和应用 | |
| HK40013368A (en) | Idiotypic antibodies against anti-pd-l1 antibodies and uses thereof | |
| HK40024539A (en) | Method for determining anti-drug antibodies in a minipig sample |