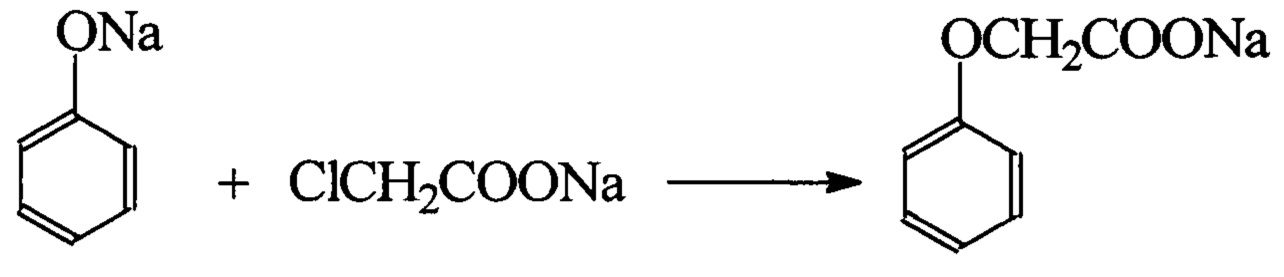RU2757739C1 - Method for synthesising 2,4-dichlorophenoxyacetic acid - Google Patents
Method for synthesising 2,4-dichlorophenoxyacetic acid Download PDFInfo
- Publication number
- RU2757739C1 RU2757739C1 RU2020116391A RU2020116391A RU2757739C1 RU 2757739 C1 RU2757739 C1 RU 2757739C1 RU 2020116391 A RU2020116391 A RU 2020116391A RU 2020116391 A RU2020116391 A RU 2020116391A RU 2757739 C1 RU2757739 C1 RU 2757739C1
- Authority
- RU
- Russia
- Prior art keywords
- acid
- sodium
- phenoxyacetic acid
- temperature
- phenoxyacetic
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C51/00—Preparation of carboxylic acids or their salts, halides or anhydrides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C51/00—Preparation of carboxylic acids or their salts, halides or anhydrides
- C07C51/347—Preparation of carboxylic acids or their salts, halides or anhydrides by reactions not involving formation of carboxyl groups
- C07C51/363—Preparation of carboxylic acids or their salts, halides or anhydrides by reactions not involving formation of carboxyl groups by introduction of halogen; by substitution of halogen atoms by other halogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C59/00—Compounds having carboxyl groups bound to acyclic carbon atoms and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups
- C07C59/40—Unsaturated compounds
- C07C59/58—Unsaturated compounds containing ether groups, groups, groups, or groups
- C07C59/64—Unsaturated compounds containing ether groups, groups, groups, or groups containing six-membered aromatic rings
- C07C59/66—Unsaturated compounds containing ether groups, groups, groups, or groups containing six-membered aromatic rings the non-carboxylic part of the ether containing six-membered aromatic rings
- C07C59/68—Unsaturated compounds containing ether groups, groups, groups, or groups containing six-membered aromatic rings the non-carboxylic part of the ether containing six-membered aromatic rings the oxygen atom of the ether group being bound to a non-condensed six-membered aromatic ring
- C07C59/70—Ethers of hydroxy-acetic acid, e.g. substitutes on the ring
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
Изобретение относится к области органической химии, конкретно к синтезу химического соединения 2,4-дихлорфеноксиуксусной кислоты (2,4-Д), хорошо известному гербициду, который в виде органических и неорганических солей, сложных эфиров и смесевых препаратов широко применяется для борьбы с двудольными и широколистными сорными растениями в посевах злаковых культур.The invention relates to the field of organic chemistry, specifically to the synthesis of the
Из большого числа известных методов получения 2,4-дихлорфеноксиуксусной кислоты практическое значение для промышленного производства имеют лишь два. Первый метод основан на конденсации натриевых солей монохлоруксусной кислоты с 2,4-дихлорфенолятами в водном растворе или безводных средах:Of the large number of known methods for the preparation of 2,4-dichlorophenoxyacetic acid, only two are of practical importance for industrial production. The first method is based on the condensation of sodium salts of monochloroacetic acid with 2,4-dichlorophenolates in an aqueous solution or anhydrous media:
В свою очередь 2,4-дихлорфенолят натрия получается прямым хлорированием фенола хлором в органических растворителях или в расплаве с последующим взаимодействием с гидроксидом натрия:In turn,
2,4-Дихлорфеноксиуксусная кислота, полученная по указанному методу, практически всегда содержит некоторое количество 2,4-дихлорфенола, который придает специфический неприятный запах. Кроме того, в щелочной среде, особенно при повышенной температуре, в качестве примесей из 2,4-дихлорфенола образуются высокотоксичные соединения - хлорзамещенные диоксины.2,4-Dichlorophenoxyacetic acid obtained by this method almost always contains a certain amount of 2,4-dichlorophenol, which gives a specific unpleasant odor. In addition, in an alkaline environment, especially at elevated temperatures, highly toxic compounds - chlorine-substituted dioxins - are formed from 2,4-dichlorophenol as impurities.
Второй метод получения 2,4-дихлорфеноксиуксусной кислоты основан на хлорировании феноксиуксусной кислоты:The second method for the preparation of 2,4-dichlorophenoxyacetic acid is based on the chlorination of phenoxyacetic acid:
Феноксиуксусную кислоту получают реакцией фенолята натрия с монохлорацетатом в водном растворе при температуре 105-107°С:Phenoxyacetic acid is obtained by the reaction of sodium phenolate with monochloroacetate in an aqueous solution at a temperature of 105-107 ° C:
При реакции конденсации происходит щелочной гидролиз монохлоруксусной кислоты с образованием значительного количества гликолевой кислоты, что снижает выход феноксиуксусной кислоты и повышает количество непрореагировавшего фенолята натрия в целевом продукте. (Н.Н. Мельников «Пестициды» Химия, технология и применение, Москва, Химия, 1987, стр. 229-232).During the condensation reaction, alkaline hydrolysis of monochloroacetic acid occurs with the formation of a significant amount of glycolic acid, which reduces the yield of phenoxyacetic acid and increases the amount of unreacted sodium phenolate in the target product. (NN Melnikov "Pesticides" Chemistry, technology and application, Moscow, Chemistry, 1987, pp. 229-232).
Известен способ получения феноксиуксусной кислоты и ее замещенных (Авторское свидетельство СССР №84982, С07С 59/70, заявлено 1949 г.) при конденсации, под давлением и без давления фенолята щелочного металла с щелочной солью хлоруксусной кислоты, взятых в эквимолекулярных количествах, с добавлением в реакционную смесь поваренной соли для получения ее концентрации в 10% и выше с последующим выделением продукта реакции известным образом. Для получения 2,4-дихлорфеноксиуксусной кислоты в растворе едкого натра растворяют 2,4-дихлор-фенол и добавляют поваренную соль. К смеси при размешивании быстро приливают раствор хлоруксуснокислого натрия. Реакционную смесь нагревают в течение 2 часов при температуре 150-155°С и давлении 3,4-3,7 атм. После этого смесь охлаждают до температуры 15-20°С и выпавшие кристаллы 2,4-дихлорфеноксиуксуснокислого натрия отфильтровывают, отжимают и промывают спиртом. При нейтрализации реакционной массы минеральной кислотой получают свободную кислоту с выходом 86-89% от теоретически возможного.A known method of producing phenoxyacetic acid and its substituted (USSR Inventor's Certificate No. 84982, С07С 59/70, declared in 1949) by condensation, under pressure and without pressure of an alkali metal phenolate with an alkaline salt of chloroacetic acid, taken in equimolecular amounts, with the addition of the reaction mixture of sodium chloride to obtain its concentration of 10% and higher, followed by the isolation of the reaction product in a known manner. To obtain 2,4-dichlorophenoxyacetic acid, 2,4-dichlorophenol is dissolved in sodium hydroxide solution and sodium chloride is added. A solution of sodium chloroacetic acid is quickly added to the mixture with stirring. The reaction mixture is heated for 2 hours at a temperature of 150-155 ° C and a pressure of 3.4-3.7 atm. After that, the mixture is cooled to a temperature of 15-20 ° C and the precipitated crystals of
Недостатками способа являются:The disadvantages of this method are:
- низкий выход целевого продукта (86-89%);- low yield of the target product (86-89%);
- необходимость эффективного разделения хлорида натрия и целевого продукта;- the need for effective separation of sodium chloride and the target product;
- большое количество образующихся сточных вод, вызывающих загрязнение окружающей среды.- a large amount of generated wastewater, causing environmental pollution.
Известен способ получения 2,4-дихлорфеноксиуксусной кислоты (Авторское свидетельство СССР №97724, С07С 59/70, 1954 г.) конденсацией 2,4-дихлорфенолята натрия с водным раствором натриевой соли монохлоруксусной кислоты в конденсаторе прямоточного действия при температуре 150-180°С под давлением 10-15 атм. После конденсации реакционную массу направляют для сушки в распылительную сушилку. Выход целевого продукта составляет 88-92%.A known method of producing 2,4-dichlorophenoxyacetic acid (USSR author's certificate No. 97724, С07С 59/70, 1954) by condensation of
Недостатками способа являются:The disadvantages of this method are:
- недостаточно высокий выход целевого продукта (88-92%);- insufficiently high yield of the target product (88-92%);
высокая температура конденсации (150-180°С) способствует образованию высокотоксичных соединений - хлорзамещенных диоксинов;high condensation temperature (150-180 ° C) promotes the formation of highly toxic compounds - chlorine-substituted dioxins;
- высокое давление 10-15 атм., что усложняет технологию производства.- high pressure 10-15 atm., which complicates the production technology.
Известен способ получения 2,4-дихлорфеноксиуксусной кислоты (Авторское свидетельство СССР №118508, С07С 59/70, 1959 г.) действием 40%-ного раствора едкого натра на сплав 2,4-дихлорфенола с хлоруксусной кислотой при температуре реакционной смеси 40-60°С, после чего продолжают нагревание при 60-65°С в течение 2 часов и для окончания реакции смесь нагревают еще в течение 3-4 часов при температуре 100°С.A known method of producing 2,4-dichlorophenoxyacetic acid (USSR author's certificate No. 118508, С07С 59/70, 1959) by the action of a 40% sodium hydroxide solution on an alloy of 2,4-dichlorophenol with chloroacetic acid at a reaction mixture temperature of 40-60 ° C, after which heating is continued at 60-65 ° C for 2 hours, and to complete the reaction, the mixture is heated for another 3-4 hours at a temperature of 100 ° C.
К горячей полутвердой массе прибавляют горячую воду и смесь тщательно перемешивают при нагревании на водяной бане в течение 1 часа. После охлаждения до комнатной температуре реакционную массу отфильтровывают и для окончательной отмывки от 2,4-дихлорфенола промывают разбавленной щелочью, фильтруют, дважды промывают на фильтре небольшим количеством воды. Полученную натриевую соль 2,4-дихлорфеноксиуксусной кислоты высушивают в паровой сушилке.Hot water is added to the hot semi-solid mass and the mixture is thoroughly stirred while heating in a water bath for 1 hour. After cooling to room temperature, the reaction mass is filtered off and for final washing from 2,4-dichlorophenol, washed with dilute alkali, filtered, washed twice on the filter with a small amount of water. The obtained sodium salt of 2,4-dichlorophenoxyacetic acid is dried in a steam dryer.
Далее соль растворяют в кипящей воде (на 1 весовую часть соли 15 весовых частей воды), фильтруют, к фильтрату, нагретому до 50-60°С, прибавляют постепенно при перемешивании 15%-ную соляную кислоту до кислой реакции. После выпадения осадка смесь охлаждают до комнатной температуры, осадок тщательно промывают водой до удаления соляной кислоты и высушивают в паровой сушилке (70-90°С). Получают целевой продукт с выходом 78% (считая на 2,4-дихлорфенол). Для окончательной очистки продукт перекристаллизовывают из 35%-ной уксусной кислоты.Next, the salt is dissolved in boiling water (for 1 weight part of the
Недостатками способа являются:The disadvantages of this method are:
- низкий выход целевого продукта (78%);- low yield of the target product (78%);
- большие объемы сточных вод;- large volumes of waste water;
- довольно много физических стадий для выделения и очистки целевого продукта: охлаждение, фильтрация, промывка, отстаивание, сушка, перекристаллизация, что увеличивает расходы на содержание оборудования и усложняет процесс.- quite a lot of physical stages for the isolation and purification of the target product: cooling, filtration, washing, settling, drying, recrystallization, which increases the cost of maintaining equipment and complicates the process.
Известен способ получения арилоксиалкилкарбоновых кислот (Авторское свидетельство СССР №187766, С07С 59/70, 1966 г.) конденсацией фенола или ортокрезола или их производных с хлоралкилкарбоновыми кислотами в соотношениях от 1,2:1 до 2:1 в среде этиленгликоля при рН 8-11 и температуре 105-120°С.A known method of producing aryloxyalkyl carboxylic acids (USSR Inventor's Certificate No. 187766, С07С 59/70, 1966) by condensation of phenol or orthocresol or their derivatives with chloralkyl carboxylic acids in ratios from 1.2: 1 to 2: 1 in ethylene glycol at pH 8- 11 and a temperature of 105-120 ° C.
Для получения 2,4-дихлорфеноксиуксусной кислоты к расплавленному дихлорфенолу загружают кристаллическую монохлоруксусную кислоту (мольное соотношение 1,2:1), этиленгликоль, едкий натр в виде 42%-ного раствора, поддерживая при этом температуру не выше 20°С и тщательно перемешивая; рН среды 10. Массу нагревают, проводя реакцию конденсации при 110°С в течение 4 часов. Конденсированную массу подкисляют до рн 6-6,5 и подвергают вакуумной отгонке этиленгликоля с непрореагировавшим дихлорфенолом (остаточное давление 30-40 мм рт.ст.). Продукт подкисляют, выделяют свободную кислоту и сушат. Выход 2,4-дихлорфеноксиуксусной кислоты составляет 90,5-96%, содержание основного вещества 96-96,5%), дихлорфенола 0,9-1%, поваренной соли 1,1%, влаги 1,9%.To obtain 2,4-dichlorophenoxyacetic acid, crystalline monochloroacetic acid (molar ratio 1.2: 1), ethylene glycol, sodium hydroxide in the form of a 42% solution are loaded to molten dichlorophenol, while maintaining the temperature not higher than 20 ° C and stirring thoroughly; The pH of the medium is 10. The mass is heated by conducting a condensation reaction at 110 ° C for 4 hours. The condensed mass is acidified to pH 6-6.5 and subjected to vacuum distillation of ethylene glycol with unreacted dichlorophenol (residual pressure 30-40 mm Hg). The product is acidified, the free acid is isolated and dried. The yield of 2,4-dichlorophenoxyacetic acid is 90.5-96%, the content of the basic substance is 96-96.5%), dichlorophenol 0.9-1%, sodium chloride 1.1%, moisture 1.9%.
Недостатками способа являются:The disadvantages of this method are:
- недостаточно высокие выход и качество целевого продукта;- insufficiently high yield and quality of the target product;
- значительное загрязнение целевого продукта дихлорфенолом (до 1%);- significant contamination of the target product with dichlorophenol (up to 1%);
- необходимость в дополнительных технологических операциях по отделению непрореагировавшего дихлорфенола и этиленгликоля.- the need for additional technological operations to separate unreacted dichlorophenol and ethylene glycol.
Известен способ получения 2,4-дихлорфеноксиуксусной кислоты (Авторское свидетельство СССР №220978, С07С 59/70, 1968 г.) путем хлорирования тонкой суспензии феноксиуксусной кислоты хлором при температуре 60-65°С в водной или солянокислой среде в течение 3 часов и давлении от нормального до 5-10 мм вод. ст. Реакционную массу перемешивают, охлаждают до комнатной температуры, фильтруют на барабанном вакуум-фильтре и промывают водой. Получают целевой продукт в виде пасты с выходом до 80%.A known method of producing 2,4-dichlorophenoxyacetic acid (USSR author's certificate No. 220978, S07C 59/70, 1968) by chlorination of a thin suspension of phenoxyacetic acid with chlorine at a temperature of 60-65 ° C in an aqueous or hydrochloric acid medium for 3 hours and pressure from normal to 5-10 mm of water. Art. The reaction mixture is stirred, cooled to room temperature, filtered on a drum vacuum filter and washed with water. The target product is obtained in the form of a paste with a yield of up to 80%.
Недостатками способа являются:The disadvantages of this method are:
- низкий выход целевого продукта (до 80%);- low yield of the target product (up to 80%);
- продукт в виде пасты неудобен при дальнейшей работе с ним.- the product in the form of a paste is inconvenient for further work with it.
Известен способ получения хлорзамещенных арилоксиалкилкарбоновых кислот (Авторское свидетельство СССР №256750, С07С 59/70, 1970 г.). Для получения 2,4-дихлорфеноксиуксусной кислоты проводят конденсацию фенола с монохлоруксусной кислотой, взятых в соотношении 1,2:1, в среде гексахлорбутадиена в присутствии 30-42%-ного водного раствора едкого натра при температуре 110-115°С в течение 2 часов. После чего реакционную массу охлаждают до 80°С, подкисляют концентрированной соляной кислотой до рН 2-2,5, добавляют горячую воду, перемешивают, отстаивают и разделяют слои. Органический (нижний) слой упаривают (давление 30 мм рт. ст.) приблизительно до половины первоначального объема и получают суспензию, содержащую феноксиуксусную кислоту, находящуюся в остатке гексахлорбутадиена. Через полученную суспензию при температуре 125-130°С и энергичном перемешивании пропускают хлор. Выход 2,4-дихлорфеноксиуксусной кислоты составляет 89,5%.A known method of producing chlorine-substituted aryloxyalkylcarboxylic acids (USSR author's certificate No. 256750, S07C 59/70, 1970). To obtain 2,4-dichlorophenoxyacetic acid, phenol is condensed with monochloroacetic acid, taken in a ratio of 1.2: 1, in a hexachlorobutadiene medium in the presence of a 30-42% aqueous solution of sodium hydroxide at a temperature of 110-115 ° C for 2 hours ... Then the reaction mass is cooled to 80 ° C, acidified with concentrated hydrochloric acid to pH 2-2.5, hot water is added, stirred, settled and the layers are separated. The organic (lower) layer is evaporated (
Недостатками способа являются:The disadvantages of this method are:
- низкий выход целевого продукта;- low yield of the target product;
- использование хлорорганического растворителя, высокие температуры хлорирования, необходимость применения вакуума усложняют технологию процесса.- the use of an organochlorine solvent, high chlorination temperatures, the need to use a vacuum complicate the process technology.
Известен способ получения 4-хлорфеноксиуксусной или 2,4-дихлорфеноксиуксусной кислот (RU 2082711, С07С 59/70, С07С 51/363, 1997 г.) хлорированием феноксиуксусной кислоты газообразным хлором в среде ледяной уксусной кислоты и уксусного ангидрида или смеси уксусного ангидрида и хлорированного углерода (метилхлороформ, тетрахлорэтан, перхлорэтилен, четыреххлористый углерод) в присутствии хлорида натрия при температуре 60-65°С. Выделение проводят кристаллизацией при 8-13°С. Выход целевого продукта составляет 85-89%; содержание основного вещества 97-99%, содержание дихлорфенола 0,08-0,2%.A known method of producing 4-chlorophenoxyacetic or 2,4-dichlorophenoxyacetic acids (RU 2082711, С07С 59/70, С07С 51/363, 1997) by chlorination of phenoxyacetic acid with gaseous chlorine in an environment of glacial acetic acid and acetic anhydride or a mixture of acetic anhydride carbon (methyl chloroform, tetrachloroethane, perchlorethylene, carbon tetrachloride) in the presence of sodium chloride at a temperature of 60-65 ° C. Isolation is carried out by crystallization at 8-13 ° C. The yield of the target product is 85-89%; the content of the basic substance is 97-99%, the content of dichlorophenol is 0.08-0.2%.
Недостатками способа являются:The disadvantages of this method are:
- низкий выход целевого продукта (85-89%);- low yield of the target product (85-89%);
- наличие в продукте токсичного дихлорфенола, склонного к образованию диоксинов;- the presence of toxic dichlorophenol in the product, which is prone to the formation of dioxins;
- использование хлорорганического растворителя приводит к коррозионному растрескиванию, что предъявляет повышенные требования к конструкционным материалам и удорожает процесс.- the use of an organochlorine solvent leads to stress corrosion cracking, which imposes increased requirements on structural materials and increases the cost of the process.
Известен способ получения очищенной 2,4-дихлорфеноксиуксусной кислоты (RU 2149157, С07С 59/70, С07С 51/347, 2000 г.) конденсацией технического 2,4-дихлорфенола с монохлоруксусной кислотой в щелочной среде при 100-110°С с последующим подкислением реакционной массы до рН 1-2 в присутствии органического растворителя, такого, как перхлорэтилен или толуол и выделением целевого продукта кристаллизацией из органического растворителя при охлаждении до 5-30°С, фильтрацией и сушкой полученного продукта. В результате получают сухую 2,4-дихлор-феноксиуксусную кислоту с выходом 80-87% и содержанием 2,4-Д изомера 96,28-99,8%.A known method of producing purified 2,4-dichlorophenoxyacetic acid (RU 2149157, С07С 59/70, С07С 51/347, 2000) by condensation of technical 2,4-dichlorophenol with monochloroacetic acid in an alkaline medium at 100-110 ° С, followed by acidification the reaction mass to pH 1-2 in the presence of an organic solvent such as perchlorethylene or toluene and the isolation of the target product by crystallization from the organic solvent with cooling to 5-30 ° C, filtration and drying of the resulting product. As a result, dry 2,4-dichloro-phenoxyacetic acid is obtained with a yield of 80-87% and a content of the 2,4-D isomer of 96.28-99.8%.
Недостатками способа являются:The disadvantages of this method are:
- низкий выход целевого продукта (80-87%);- low yield of the target product (80-87%);
- наличие в продукте 0,02-0,41% хлорфенола, 0,15-0,82% трихлор-замещенной феноксиуксусной кислоты;- the presence of 0.02-0.41% chlorophenol, 0.15-0.82% trichloro-substituted phenoxyacetic acid in the product;
- использование большого количества растворителя.- the use of a large amount of solvent.
Известен способ получения арилоксикарбоновых кислот (RU 2345978, С07С 51/02, С07С 59/70, 2009 г.), включающий стадию получения фенолятов щелочных металлов взаимодействием фенола с гидроксидом щелочного металла; стадию получения солей арилоксикарбоновых кислот взаимодействием соли монохлоруксусной кислоты с полученными на первой стадии фенолятами щелочных металлов при нагревании, причем указанные процессы осуществляют в твердой фазе при одновременном тонком измельчении и интенсивном перемешивании с последующим подкислением соли и выделением конечного продукта.A known method of producing aryloxycarboxylic acids (RU 2345978, S07C 51/02, S07C 59/70, 2009), including the stage of obtaining phenolates of alkali metals by the interaction of phenol with an alkali metal hydroxide; the stage of obtaining salts of aryloxycarboxylic acids by the interaction of the salt of monochloroacetic acid with the phenolates of alkali metals obtained in the first stage upon heating, and these processes are carried out in the solid phase with simultaneous fine grinding and vigorous stirring, followed by acidification of the salt and the isolation of the final product.
Для получения натриевой соли феноксиуксусной кислоты 1,01-1,04 моля твердой щелочи NaOH измельчают до получения тонкоизмельченного порошка, добавляют 1 моль фенола и при температуре не выше температуры плавления реакционной смеси перемешивают и измельчают до получения тонкоизмельченной порошкообразной массы. Затем к феноляту натрия (1 моль) добавляют порошкообразной натриевой соли монохлоруксусной кислоты (1,05-1,15 моль) и интенсивно перемешивают в течение 0,5-2 час. при температуре 80-95°С и получают натриевую соль феноксиуксусной кислоты, которая может быть переработана в кислоту известным способом, например, подкислением с последующей экстракцией.To obtain the sodium salt of phenoxyacetic acid, 1.01-1.04 mol of solid alkali NaOH is ground to obtain a finely ground powder, 1 mol of phenol is added and at a temperature not exceeding the melting point of the reaction mixture, the mixture is stirred and ground to obtain a finely ground powdery mass. Then to sodium phenate (1 mol) add powdered sodium salt of monochloroacetic acid (1.05-1.15 mol) and stir vigorously for 0.5-2 hours. at a temperature of 80-95 ° C and the sodium salt of phenoxyacetic acid is obtained, which can be processed into an acid by a known method, for example, acidification followed by extraction.
Конверсия фенола в фенолят натрия составляет 99,1-99,5; конверсия фенолята натрия в натриевую соль феноксиуксусной кислоты составляет 99,3-99,6%; содержание свободного фенола в реакционной массе 0,4-0,8%.The conversion of phenol to sodium phenolate is 99.1-99.5; conversion of sodium phenolate to sodium salt of phenoxyacetic acid is 99.3-99.6%; the content of free phenol in the reaction mass is 0.4-0.8%.
Для образования фенолята 2,4-дихлорфенола берут твердую щелочь NaOH, измельчают и перемешивают в смесителе с 2,4-дихлорфенолом. Полученный продукт, содержащий 0,5 моля 2,4-дихлорфенолята натрия, в смесителе контактирует с порошкообразной Na-солью монохлор-уксусной кислоты в условиях, аналогичных примеру 1, и при температуре 95°С, в течение 2 час.For the formation of
Конверсия 2,4-дихлорфенола в 2,4-дихлорфенолят натрия - 99,9%; конверсия 2,4-дихлорфенолята натрия в натриевую соль 2,4-дихлорфеноксиуксусной кислоты - 99,7%; содержание свободного 2,4-дихлор-фенола в реакционной массе 0,3%.Conversion of 2,4-dichlorophenol to
Недостатками способа являются:The disadvantages of this method are:
- гидроксид натрия весьма гигроскопичен и поэтому его сложно получить в виде тонкоизмельченной порошкообразной массы;- sodium hydroxide is very hygroscopic and therefore it is difficult to obtain it in the form of a finely ground powdery mass;
- реакция взаимодействия 2,4-дихлорфенола и натриевой соли монохлоруксусной кислоты в присутствии гидроксида натрия протекает с большим выделением тепла. Поэтому при крупномасштабном производстве весьма затруднительно поддерживать стабильную температуру ниже плавления реакционной смеси в условиях плохой теплопередачи порошков. Кроме того, необходима дополнительная стадия синтеза натриевой соли монохлоруксусной кислоты и ее сушки;- the reaction of interaction of 2,4-dichlorophenol and sodium salt of monochloroacetic acid in the presence of sodium hydroxide proceeds with a large evolution of heat. Therefore, in large-scale production, it is very difficult to maintain a stable temperature below the melting point of the reaction mixture under conditions of poor heat transfer of the powders. In addition, an additional step is required for the synthesis of the sodium salt of monochloroacetic acid and its drying;
- требуется дополнительная стадия получения 2,4-дихлорфенола;- an additional stage of obtaining 2,4-dichlorophenol is required;
- наличие свободного фенола (0,4-0,8%) и высокотоксичного 2,4-дихлорфенола (0,3%) ухудшает потребительские характеристики продукта.- the presence of free phenol (0.4-0.8%) and highly toxic 2,4-dichlorophenol (0.3%) impairs the consumer characteristics of the product.
Известен способ получения хлорзамещенных арилоксикарбоновых кислот (RU 2380350, С07С 51/363, С07С 51/02, С07С 59/68, С07С 59/70, 2010 г.) путем твердофазного хлорирования кислот общей формулыA known method for producing chlorine-substituted aryloxycarboxylic acids (RU 2380350, С07С 51/363, С07С 51/02, С07С 59/68, С07С 59/70, 2010) by solid-phase chlorination of acids of the general formula
где R1 - водород, галоид, С1-С4-алкил, n - целое число от 1 до 3, или их солей гипохлоритом кальция в отсутствии растворителей с активацией процесса механическим воздействием в виде ударной или ударно-сдвиговой нагрузки на смесь твердых реагентов в присутствии катализатора, в качестве которого используют кислоты Льюиса, в течение 10-30 минут при температуре окружающей среды и атмосферном давлении. Механическое воздействие осуществляют с помощью шаровой, виброшаровой или планетарной мельницы. Для получения 2,4-дихлор-феноксиуксусной кислоты смесь натриевой соли феноксиуксусной кислоты, гипохлорита кальция в виде двутретиосновной соли гипохлорита кальция с содержанием активного хлора 60% и железа хлорного гексагидрата механически обрабатывают в течение 10 минут до получения тонко измельченного порошка. Полученную массу растворяют при интенсивном перемешивании в 15% хлористоводородной кислоте и выдерживают 15 минут. Выпавший осадок отфильтровывают, промывают и сушат. Осадок содержит 98,1% 2,4-дихлорфеноксиуксусной кислоты.where R 1 is hydrogen, halogen, C 1 -C 4 -alkyl, n is an integer from 1 to 3, or their salts with calcium hypochlorite in the absence of solvents with the activation of the process by mechanical action in the form of shock or shock-shear load on a mixture of solid reagents in the presence of a catalyst, which is Lewis acid, for 10-30 minutes at ambient temperature and atmospheric pressure. Mechanical action is carried out using a ball, vibroball or planetary mill. To obtain 2,4-dichloro-phenoxyacetic acid, a mixture of sodium salt of phenoxyacetic acid, calcium hypochlorite in the form of a dibasic salt of calcium hypochlorite with an active chlorine content of 60% and ferric chloride hexahydrate is mechanically processed for 10 minutes to obtain a finely ground powder. The resulting mass is dissolved with vigorous stirring in 15% hydrochloric acid and incubated for 15 minutes. The formed precipitate is filtered off, washed and dried. The precipitate contains 98.1% 2,4-dichlorophenoxyacetic acid.
Недостатком способа является использование в процессе дополнительного оборудования (мельницы) и катализатора, что при промышленном производстве приведет к дополнительным материальным затратам. Кроме того, образуется значительное количество трудноутилизируемых сточных вод.The disadvantage of this method is the use in the process of additional equipment (mill) and catalyst, which in industrial production will lead to additional material costs. In addition, a significant amount of difficult-to-use wastewater is generated.
Известен твердофазный синтез феноксиуксусной кислоты в условиях механохимической активации. (Башкирский химический журнал, 2008. Том 15. №1. С. 11-13. Ю.Е. Сапожников, В.В. Масленникова, Л.И. Буслаева, З.Б. Галиева, Н.А. Сапожникова, Р.Б. Валитов Твердофазный синтез феноксиуксусной кислоты в условиях механохимической активации).Known solid-phase synthesis of phenoxyacetic acid under conditions of mechanochemical activation. (Bashkir Chemical Journal, 2008.
Синтез натриевой соли феноксиуксусной кислоты проводят в две стадии. Первоначально получают моногидрат фенолята натрия дозированием фенола в течение 30-60 минут в мелкодисперсный (модальный размер Х50=3 мкм) гидроксид натрия, обеспечивая интенсивное перемешивание и температуру 20-50°С. Авторы отмечают, что скорость процесса существенно зависит от степени измельчения гидроксида натрия и интенсивности перемешивания и слабо зависит от температуры. После завершения процесса реакционная масса представляет собой сыпучий порошок. На первой стадии удается достичь остаточной концентрации фенола, не вступившего в реакцию, менее 0,4%.The synthesis of the sodium salt of phenoxyacetic acid is carried out in two stages. Initially, sodium phenolate monohydrate is obtained by dosing phenol for 30-60 minutes into finely dispersed (modal size X50 = 3 microns) sodium hydroxide, providing intensive stirring and a temperature of 20-50 ° C. The authors note that the rate of the process depends significantly on the degree of grinding of sodium hydroxide and the intensity of stirring and depends only slightly on temperature. After the completion of the process, the reaction mass is a free-flowing powder. At the first stage, it is possible to achieve a residual concentration of unreacted phenol of less than 0.4%.
На второй стадии после добавления в реакционную массу монохлорацетата натрия измельченная смесь подвергается предварительной механической активации в вибро- или планетарной мельнице и последующему нагреву до 60-95°С в условиях механического воздействия или без него, давая целевой продукт - натриевую соль феноксиуксусной кислоты.At the second stage, after adding sodium monochloroacetate to the reaction mass, the crushed mixture is subjected to preliminary mechanical activation in a vibratory or planetary mill and subsequent heating to 60-95 ° C with or without mechanical action, giving the target product - sodium salt of phenoxyacetic acid.
Поскольку в некоторых экспериментах исследовалось влияние содержания воды на стадии конденсации, исходные реагенты предварительно высушивались в вакуум-сушильном шкафу при температуре 90°С и остаточном давлении 10 мм рт.ст. в течение 10-12 ч.Since in some experiments the effect of water content at the condensation stage was investigated, the initial reagents were preliminarily dried in a vacuum drying oven at a temperature of 90 ° C and a residual pressure of 10 mm Hg. within 10-12 hours.
Недостатки способа следующие:The disadvantages of this method are as follows:
- в целевом продукте содержится исходный фенол в количестве до 0,4% и его присутствие скажется на потребительских характеристиках продукта, так как при хлорировании данного продукта с целью получения 2,4-дихлорфеноксиуксусной кислоты, фенол также будет хлорироваться с образованием хлорфенолов - источников супертоксикантов - диоксинов. Но даже если продукт подвергнуть очистке, образуются токсичные сточные воды (ПДК в воде водоемов хлорфенолов должно быть не более 0, 0001 мг/л);- the target product contains initial phenol in an amount of up to 0.4% and its presence will affect the consumer characteristics of the product, since when this product is chlorinated to obtain 2,4-dichlorophenoxyacetic acid, phenol will also be chlorinated to form chlorophenols - sources of supertoxicants - dioxins. But even if the product is purified, toxic waste water is formed (MPC in the water of chlorophenols should be no more than 0, 0001 mg / l);
- вследствие высокой гигроскопичности гидроксида натрия весьма сложно получать его в мелкодисперсном виде до размера 3 мкм. При промышленном производстве очень трудно будет удерживать температуру в интервале 20-50°С ввиду большой экзотермичности процесса и плохой теплопроводности дисперсных порошков;- due to the high hygroscopicity of sodium hydroxide, it is very difficult to obtain it in a finely dispersed form up to a size of 3 microns. In industrial production, it will be very difficult to keep the temperature in the range of 20-50 ° C due to the high exothermicity of the process and poor thermal conductivity of dispersed powders;
- в синтезе используют готовую натриевую соль монохлоруксусной кислоты (хлорацетат натрия). Требуется дополнительная стадия для ее получения и очистки, так как монохлоруксусная кислота склонна к гидролизу;- ready-made sodium salt of monochloroacetic acid (sodium chloroacetate) is used in the synthesis. An additional stage is required for its preparation and purification, since monochloroacetic acid is prone to hydrolysis;
- в синтезе используют моногидрат фенолята натрия. Это еще одна дополнительная технологическая операция для его получения из фенола и воды;- sodium phenolate monohydrate is used in the synthesis. This is one more additional technological operation for its production from phenol and water;
- необходимость предварительного продолжительного высушивания (10-12 часов) исходных реагентов при глубоком вакууме (10 мм.рт.ст.), который очень трудно создать в промышленных условиях.- the need for preliminary long-term drying (10-12 hours) of the initial reagents under high vacuum (10 mm Hg), which is very difficult to create in industrial conditions.
В патентной заявке CN 106397176 (А) (С07С 51/367, С07С 59/70, 2017 г.) предложен способ получения феноксиацетата натрия, включающий следующие этапы: 1) хлоруксусную кислоту растворяют в воде и охлаждают до 0°С; 2) насыщенный раствор карбоната натрия добавляют к раствору хлоруксусной кислоты при перемешивании при 0°С до тех пор, пока значение рН раствора не будет 7-8; 3) к смешанному раствору добавляют фенол, воду, 35%-ный раствор гидроксида натрия до значения рН 12 и нагревают реакционную смесь до 92°С, подвергая реакции в течение 0,5 час; 4) реакционную массу фильтруют, твердое вещество, полученное путем фильтрации, промывают, сушат и получают феноксиацетат натрия с выходом 80-85%. Недостатками способа являются:In patent application CN 106397176 (A) (C07C 51/367, C07C 59/70, 2017), a method for producing sodium phenoxyacetate is proposed, including the following steps: 1) chloroacetic acid is dissolved in water and cooled to 0 ° C; 2) a saturated sodium carbonate solution is added to the chloroacetic acid solution with stirring at 0 ° C until the pH of the solution is 7-8; 3) phenol, water, 35% sodium hydroxide solution are added to the mixed solution to
- низкий выход целевого продукта;- low yield of the target product;
- образование значительных количеств загрязняющих сточных вод, так как натриевая соль феноксиацетата достаточно хорошо растворима в воде.- the formation of significant amounts of polluting wastewater, since the sodium salt of phenoxyacetate is quite well soluble in water.
В патентной заявке CN 106397177 (А) (С07С 51/41, С07С 51/47, С07С 59/70, 2017 г.) предложен полноциклический способ получения феноксиацетата натрия, включающий следующие стадии: 1) синтез хлорацетата натрия взаимодействием хлоруксусной кислоты с карбонатом натрия в водном растворе при температуре не выше 35°С и перемешивании; 2) синтез феноксиацетата натрия взаимодействием насыщенного раствора хлорацетата натрия, полученного на стадии 1), фенола и 40%-ного гидроксида натрия при весовом отношении компонентов 1:1,2:1,2, значении рН 12, температуре 92°С и перемешивании в течение 0,5 часов, добавлением концентрированной соляной кислоты до рН 7 и охлаждением до комнатной температуры; 3) очистка феноксиацетата натрия; 4) обработка органической фазы и повторное использование; 5) обработка водной фазы и повторное использование.In patent application CN 106397177 (A) (C07C 51/41, C07C 51/47, C07C 59/70, 2017), a full-cycle method for the preparation of sodium phenoxyacetate is proposed, including the following steps: 1) synthesis of sodium chloroacetate by the interaction of chloroacetic acid with sodium carbonate in an aqueous solution at a temperature not higher than 35 ° C and stirring; 2) synthesis of sodium phenoxyacetate by the interaction of a saturated solution of sodium chloroacetate obtained in stage 1), phenol and 40% sodium hydroxide at a weight ratio of components 1: 1.2: 1.2,
В описании заявки примеров получения натриевой соли феноксиуксусной кислоты, количественных и качественных показателей целевого продукта не приводится.In the description of the application examples of obtaining sodium salt of phenoxyacetic acid, quantitative and qualitative indicators of the target product are not given.
Недостатками способа являются:The disadvantages of this method are:
- многостадийность процесса;- multistage process;
- необходимость использования двух видов щелочи: карбоната натрия и гидроксида натрия;- the need to use two types of alkali: sodium carbonate and sodium hydroxide;
- образование значительных количеств загрязняющих сточных вод, так как натриевая соль феноксиацетата достаточно хорошо растворима в воде.- the formation of significant amounts of polluting wastewater, since the sodium salt of phenoxyacetate is quite well soluble in water.
В патентной заявке CN 104151152 (А) (С07С 51/02, С07С 51/367, С07С 51/42, С07С 59/70, 2014 г.) предложен циклический способ получения феноксиуксусной кислоты, который включает следующие стадии: 1) конденсация фенолята натрия с хлорацетатом натрия с образованием феноксиацетата натрия при температуре 90-95°С в присутствии катализатора (хлорид железа, ЭДТА, иодид натрия при соотношении 1:1:1); 2) растворение избыточного фенола в растворителе (хлорбензол, дихлорбензол, толуол, ксилол, дихлорэтан или тетрахлорэтилен) для возврата в цикл; 3) промывание феноксиацетата натрия в растворителе для удаления фенола; 4) подкисление феноксиацетата натрия, охлаждение и кристаллизация для выделения феноксиуксусной кислоты.In patent application CN 104151152 (A) (C07C 51/02, C07C 51/367, C07C 51/42, C07C 59/70, 2014), a cyclic method for producing phenoxyacetic acid is proposed, which includes the following stages: 1) condensation of sodium phenolate with sodium chloroacetate to form sodium phenoxyacetate at a temperature of 90-95 ° C in the presence of a catalyst (ferric chloride, EDTA, sodium iodide at a ratio of 1: 1: 1); 2) dissolving excess phenol in a solvent (chlorobenzene, dichlorobenzene, toluene, xylene, dichloroethane or tetrachlorethylene) to return to the cycle; 3) washing sodium phenoxyacetate in a solvent to remove phenol; 4) acidification of sodium phenoxyacetate, cooling and crystallization to isolate phenoxyacetic acid.
Получают продукт с выходом 95-98% и чистотой 98%.The product is obtained with a yield of 95-98% and a purity of 98%.
Недостатками способа являются:The disadvantages of this method are:
- многостадийность процесса;- multistage process;
- применение катализатора сложного состава, само приготовление которого требует дополнительного технологического оборудования;- the use of a catalyst of complex composition, the preparation of which itself requires additional technological equipment;
- использование хлорорганического растворителя усложняет технологию процесса.- the use of an organochlorine solvent complicates the process technology.
В патентной заявке CN 101921188 (А) (С07С 51/363, С07С 59/70, 2010 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты хлорированием феноксиуксусной кислоты хлором при 10-100°С в смешанном растворителе в присутствии катализаторов фенотиазана и диметиламинопиридина. Смешанный растворитель состоит из двух или более растворителей, таких как вода, диоксан, тетрагидрофуран, диметиловый или диэтиловый эфир этиленгликоля, диметиловый или диэтиловый эфир диэтиленгликоля, ацетон, бутанон, уксусная кислота, ацетонитрил, диметилформамид, диметилсульфоксид, одноатомный С1-С7-спирт. Массовое отношении феноксиуксусной кислоты к смешанному растворителю = 1:1-100, молярное отношение феноксиуксусной кислоты к общему количеству вводимого хлорирующего газа = 1:2-2,2. Выход 2,4-дихлорфеноксиуксусной кислоты 95,0-95,3% в пересчете на феноксиуксусную кислоту, содержание активного ингредиента составляет 97,8-98,4%).Patent application CN 101921188 (A) (C07C 51/363, C07C 59/70, 2010) proposes a method for producing 2,4-dichlorophenoxyacetic acid by chlorination of phenoxyacetic acid with chlorine at 10-100 ° C in a mixed solvent in the presence of phenothiazan catalysts and dimethylaminopyridine. A mixed solvent composed of two or more solvents such as water, dioxane, tetrahydrofuran, dimethyl or diethyl ether, diethylene glycol dimethyl or diethyl ether, acetone, butanone, acetic acid, acetonitrile, dimethylformamide, dimethylsulfoxide, monohydric C 1 -C 7 -alcohol ... The mass ratio of phenoxyacetic acid to the mixed solvent = 1: 1-100, the molar ratio of phenoxyacetic acid to the total amount of introduced chlorinating gas = 1: 2-2.2. The yield of 2,4-dichlorophenoxyacetic acid is 95.0-95.3% in terms of phenoxyacetic acid, the content of the active ingredient is 97.8-98.4%).
Недостатками способа являются:The disadvantages of this method are:
- использование смешанных растворителей в процессе приведет к потерям целевого продукта при отделении растворителей;- the use of mixed solvents in the process will lead to the loss of the target product during the separation of solvents;
- очистка и регенерация растворителей и катализаторов потребует дополнительных материальных и энергетических затрат;- cleaning and regeneration of solvents and catalysts will require additional material and energy costs;
- требуется дополнительная стадия получения феноксиуксусной кислоты и общий выход 2,4-дихлорфеноксиуксусной кислоты в пересчете на фенол будет меньше.- an additional stage of obtaining phenoxyacetic acid is required and the total yield of 2,4-dichlorophenoxyacetic acid in terms of phenol will be lower.
В патентной заявке CN 102336654 (А) (С07С 51/363, С07С 59/70, 2012 г.) предложен способ хлорирования феноксиуксусной кислоты и ее производных хлорирующим агентом (газообразный хлор, гипохлорит натрия, гипохлорит кальция, сульфурилхлорид) при температуре 40-100°С в течение 1-10 часов в органических растворителях (дихлорметан, дихлорэтан, трихлорметан, четыреххлористый углерод, муравьиная кислота, этилацетат, бензол, толуол, диметилбензол, хлорбензол, о-дихлорбензол) в присутствии катализаторов (хлорид железа, хлорид олова, хлорид алюминия, трифторбром, трифторметилсульфонат, концентрированная серная кислота, надсерная кислота, сульфуроновая кислота). Выход 2,4-дихлорфеноксиуксусной кислоты составляет 90,5% с чистотой 98,05%.In patent application CN 102336654 (A) (C07C 51/363, C07C 59/70, 2012), a method is proposed for the chlorination of phenoxyacetic acid and its derivatives with a chlorinating agent (chlorine gas, sodium hypochlorite, calcium hypochlorite, sulfuryl chloride) at a temperature of 40-100 ° C for 1-10 hours in organic solvents (dichloromethane, dichloroethane, trichloromethane, carbon tetrachloride, formic acid, ethyl acetate, benzene, toluene, dimethylbenzene, chlorobenzene, o-dichlorobenzene) in the presence of catalysts (ferric chloride, tin chloride, aluminum chloride , trifluorobromo, trifluoromethylsulfonate, concentrated sulfuric acid, persulfuric acid, sulfuronic acid). The yield of 2,4-dichlorophenoxyacetic acid is 90.5% with a purity of 98.05%.
Недостатками способа являются:The disadvantages of this method are:
- недостаточный выход целевого продукта;- insufficient yield of the target product;
- использование хлорорганического растворителя усложняет технологию процесса;- the use of an organochlorine solvent complicates the process technology;
- использование растворителей в процессе приведет к потерям целевого продукта при отделении растворителя;- the use of solvents in the process will lead to the loss of the target product during the separation of the solvent;
- требуется дополнительная стадия получения феноксиуксусной кислоты и общий выход 2,4-дихлорфеноксиуксусной кислоты в пересчете на фенол будет меньше;- an additional stage of obtaining phenoxyacetic acid is required and the total yield of 2,4-dichlorophenoxyacetic acid in terms of phenol will be less;
- очистка и регенерация растворителей и катализаторов потребует дополнительных материальных и энергетических затрат.- cleaning and regeneration of solvents and catalysts will require additional material and energy costs.
В патентной заявке CN 103058855 (А) (С07С 51/363, С07С 59/70, 2013 г.) предложен способ синтеза производного феноксиуксусной кислоты. Способ включает следующие стадии: 1) смешивание соли фенола или метил фенола (натриевой, калиевой, метиламинной, этиламинной) с солью хлоруксусной кислоты (натриевой, калиевой, метиламинной, этиламинной) при нагревании (50-150°С) в среде растворителя (вода, метиловый спирт, этиловый спирт, пропиловый спирт, диметилформамид, диметилацетамид, диметилсульф-оксид); 2) подкисление реакционной смеси неорганической кислотой (соляной, серной, азотной, фосфорной) до рН 0-3 для получения феноксиуксусной кислоты; 3) хлорирование феноксиуксусной кислоты хлором для получения 2-хлорфеноксиуксусной или 4-хлорфеноксиуксусной кислоты при нагревании (10-100°С, преимущественно 30-80°С) в течение 1 минуты - 10 часов в среде растворителя (дихлорметан, хлороформ, дихлорэтан, тетрахлорэтилен, хлорбензол, дихлорбензол, уксусная кислота, пропионовая кислота, бутановая кислота, диметиловый эфир этиленгликоля, диоксан, тетрагидрофуран) с добавлением катализатора (оксид или хлорид железа, хрома); охлаждение и кристаллизация с получением хлорированного производного феноксиуксусной кислоты. Выход феноксиуксусной кислоты составляет 95-96%, содержание более 98%.In patent application CN 103058855 (A) (C07C 51/363, C07C 59/70, 2013), a method for the synthesis of a phenoxyacetic acid derivative is proposed. The method includes the following stages: 1) mixing a salt of phenol or methyl phenol (sodium, potassium, methylamino, ethylamino) with a salt of chloroacetic acid (sodium, potassium, methylamino, ethylamino) when heated (50-150 ° C) in a solvent medium (water, methyl alcohol, ethyl alcohol, propyl alcohol, dimethylformamide, dimethylacetamide, dimethylsulfide oxide); 2) acidification of the reaction mixture with inorganic acid (hydrochloric, sulfuric, nitric, phosphoric) to pH 0-3 to obtain phenoxyacetic acid; 3) chlorination of phenoxyacetic acid with chlorine to obtain 2-chlorophenoxyacetic or 4-chlorophenoxyacetic acid by heating (10-100 ° C, mainly 30-80 ° C) for 1 minute - 10 hours in a solvent (dichloromethane, chloroform, dichloroethane, tetrachlorethylene , chlorobenzene, dichlorobenzene, acetic acid, propionic acid, butanoic acid, ethylene glycol dimethyl ether, dioxane, tetrahydrofuran) with the addition of a catalyst (oxide or chloride of iron, chromium); cooling and crystallization to obtain a chlorinated phenoxyacetic acid derivative. The yield of phenoxyacetic acid is 95-96%, the content is more than 98%.
Недостатками способа являются:The disadvantages of this method are:
- использование хлорорганического растворителя усложняет технологию процесса;- the use of an organochlorine solvent complicates the process technology;
- использование растворителей в процессе приведет к потерям целевого продукта при отделении растворителя;- the use of solvents in the process will lead to the loss of the target product during the separation of the solvent;
- очистка и регенерация растворителей и катализаторов потребует дополнительных материальных и энергетических затрат.- cleaning and regeneration of solvents and catalysts will require additional material and energy costs.
В патентной заявке CN 103145549 (А) (С07С 51/363, С07С 59/70, 2013 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты конденсацией о-хлорфенола с хлоруксусной кислотой при температуре 95-110°С в течение 3-5 часов в щелочной (NaOH, KOH) или водной среде, подкислением соляной или серной кислотой, охлаждением и кристаллизацией полученной о-хлорфеноксиуксусной кислоты (выход 97,1-97,23%, содержание 98,6-98,4%); затем взаимодействием о-хлорфеноксиуксусной кислоты с хлором при температуре 10-60°С (преимущественно 30-50°С) в смешанном растворителе, который представляет собой смесь диметилформамида, воды и дихлорэтана. Получают целевой продукт с содержанием 97,1-98,1% и выходом 96,8-97,9%) в пересчете на о-хлорфеноксиуксусную кислоту.In patent application CN 103145549 (A) (C07C 51/363, C07C 59/70, 2013), a method for preparing 2,4-dichlorophenoxyacetic acid by condensation of o-chlorophenol with chloroacetic acid at a temperature of 95-110 ° C for 3- 5 hours in an alkaline (NaOH, KOH) or aqueous medium, acidification with hydrochloric or sulfuric acid, cooling and crystallization of the obtained o-chlorophenoxyacetic acid (yield 97.1-97.23%, content 98.6-98.4%); then the interaction of o-chlorophenoxyacetic acid with chlorine at a temperature of 10-60 ° C (mainly 30-50 ° C) in a mixed solvent, which is a mixture of dimethylformamide, water and dichloroethane. The target product is obtained with a content of 97.1-98.1% and a yield of 96.8-97.9%) in terms of o-chlorophenoxyacetic acid.
Недостатками способа являются:The disadvantages of this method are:
- о-хлорфенол более дорогостоящий реагент по сравнению с фенолом, используемым в подобных способах получения 2,4-дихлорфеноксиуксусной кислоты;- o-chlorophenol is a more expensive reagent in comparison with phenol used in similar methods for producing 2,4-dichlorophenoxyacetic acid;
- требуются две стадии хлорирования: стадия получения о-хлорфенола и стадия хлорирования о-хлорфеноксиуксусной кислоты;- two stages of chlorination are required: the stage of obtaining o-chlorophenol and the stage of chlorination of o-chlorophenoxyacetic acid;
- выход 2,4-дихлорфеноксиуксусной кислоты в пересчете на о-хлорфенол будет меньше;- the yield of 2,4-dichlorophenoxyacetic acid in terms of o-chlorophenol will be less;
- использование смешанного растворителя усложняет технологию процесса;- the use of a mixed solvent complicates the process technology;
- использование растворителей в процессе приведет к потерям целевого продукта при отделении растворителя;- the use of solvents in the process will lead to the loss of the target product during the separation of the solvent;
- регенерация и очистка растворителей потребует дополнительных материальных и энергетических затрат.- regeneration and purification of solvents will require additional material and energy costs.
В патентной заявке CN 103274925 (А) (С07С 51/363, С07С 59/70, 2013 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты, который включает следующие стадии: растворение феноксиуксусной кислоты в органическом растворителе (тетрахлорэтилен, дихлорэтан, четыреххлористый углерод); проведение реакции хлорирования феноксиуксусной кислоты хлором при температуре 25-100°С в присутствии катализатора; удаление образовавшегося хлористого водорода и остаточного хлора после завершения реакции; восстановление катализатора при высокой температуре; фильтрация, охлаждение, кристаллизация фильтрата, сушка готового продукта. Весовое соотношение феноксиуксусной кислоты и органического растворителя составляет 1:2-100, молярное соотношение феноксиуксусной кислоты и хлора-1:2-2,3. Выход 2,4-дихлорфеноксиуксусной кислоты составляет 91,6-96,0%, содержание 96,7-98,7%.In patent application CN 103274925 (A) (C07C 51/363, C07C 59/70, 2013), a method for preparing 2,4-dichlorophenoxyacetic acid is proposed, which includes the following stages: dissolving phenoxyacetic acid in an organic solvent (tetrachlorethylene, dichloroethane, tetrachloride carbon); carrying out the chlorination reaction of phenoxyacetic acid with chlorine at a temperature of 25-100 ° C in the presence of a catalyst; removing the generated hydrogen chloride and residual chlorine after completion of the reaction; catalyst recovery at high temperature; filtration, cooling, crystallization of the filtrate, drying of the finished product. The weight ratio of phenoxyacetic acid and organic solvent is 1: 2-100, the molar ratio of phenoxyacetic acid and chlorine is 1: 2-2.3. The yield of 2,4-dichlorophenoxyacetic acid is 91.6-96.0%, the content is 96.7-98.7%.
Недостатками способа являются:The disadvantages of this method are:
- использование хлорорганического растворителя усложняет технологию процесса;- the use of an organochlorine solvent complicates the process technology;
- при использовании в качестве растворителей легкокипящих дихлорэтана (tкип.=83,47°С) и четыреххлористого углерода (tкип.=76,75°С) для поддержания температуры реакции 100°С потребуется давление, что усложняет технологию процесса;- when using low-boiling dichloroethane ( boiling point = 83.47 ° C) and carbon tetrachloride ( boiling point = 76.75 ° C) as solvents, pressure is required to maintain the reaction temperature of 100 ° C, which complicates the process technology;
- требуется стадия синтеза феноксиуксусной кислоты;- a stage of synthesis of phenoxyacetic acid is required;
- использование растворителей в процессе приведет к потерям целевого продукта при отделении растворителя;- the use of solvents in the process will lead to the loss of the target product during the separation of the solvent;
- очистка и регенерация растворителей и катализаторов потребует дополнительных материальных и энергетических затрат.- cleaning and regeneration of solvents and catalysts will require additional material and energy costs.
В патентной заявке CN 104447290 (А) (С07С 51/363, С07С 59/70, 2015 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты, который включает следующие стадии: получение хлорацетата натрия добавлением хлоруксусной кислоты в раствор гидроксида натрия при перемешивании в течение 15-20 минут; получение феноксиацетата натрия взаимодействием хлорацетата натрия с фенолом при температуре 100°С в течение 40 минут при регулировании до рН=11 бикарбонатом натрия; получение феноксиуксусной кислоты добавлением соляной кислоты до рН=4, охлаждением в ледяной бане, промыванием полученного твердого вещества и сушкой; получение 2,4-дихлорфеноксиуксусной кислоты хлорированием феноксиуксусной кислоты хлором при температуре 75°С в растворе уксусной кислоты и воды в присутствии катализатора фталоцианина железа при перемешивании в течение 35-50 минут, охлаждением до 18°С и фильтрованием реакционной смеси, сушкой твердого вещества при 60°С. Получают целевой продукт с выходом 97,0-98,9% и содержанием 97,9-99,8%). Недостатками способа являются:In patent application CN 104447290 (A) (C07C 51/363, C07C 59/70, 2015), a method for producing 2,4-dichlorophenoxyacetic acid is proposed, which includes the following stages: obtaining sodium chloroacetate by adding chloroacetic acid to a sodium hydroxide solution with stirring within 15-20 minutes; obtaining sodium phenoxyacetate by reacting sodium chloroacetate with phenol at a temperature of 100 ° C for 40 minutes while adjusting to pH = 11 with sodium bicarbonate; obtaining phenoxyacetic acid by adding hydrochloric acid to pH = 4, cooling in an ice bath, washing the resulting solid and drying; obtaining 2,4-dichlorophenoxyacetic acid by chlorination of phenoxyacetic acid with chlorine at a temperature of 75 ° C in a solution of acetic acid and water in the presence of an iron phthalocyanine catalyst with stirring for 35-50 minutes, cooling to 18 ° C and filtering the reaction mixture, drying the solid at 60 ° C. The target product is obtained with a yield of 97.0-98.9% and a content of 97.9-99.8%). The disadvantages of this method are:
- многостадийность процесса;- multistage process;
- охлаждение до низких температур (ледяная баня) в промышленных масштабах потребует использования холодильных установок, что существенно усложняет и удорожает процесс;- cooling to low temperatures (ice bath) on an industrial scale will require the use of refrigeration units, which significantly complicates and increases the cost of the process;
- использование растворителя в процессе приведет к потерям целевого продукта при отделении растворителя;- the use of a solvent in the process will lead to the loss of the target product during the separation of the solvent;
- регенерация катализатора потребует дополнительных материальных и энергетических затрат.- catalyst regeneration will require additional material and energy costs.
Подобный способ получения 2,4-дихлорфеноксиуксусной кислоты предложен в патентной заявке CN 104402707 (А) (С07С 51/363, С07С 59/70, 2015 г.) за исключением того, что хлорирование феноксиуксусной кислоты проводят при температуре 65°С и в качестве катализатора используют композиционный оксид Ni-Al-Mg. Получают целевой продукт с выходом 97,9-99,1%) в пересчете на феноксиуксусную кислоту и содержанием 97,2-99,9%.A similar method for the preparation of 2,4-dichlorophenoxyacetic acid is proposed in patent application CN 104402707 (A) (C07C 51/363, C07C 59/70, 2015), except that the chlorination of phenoxyacetic acid is carried out at a temperature of 65 ° C and as the catalyst uses a composite oxide Ni-Al-Mg. The target product is obtained with a yield of 97.9-99.1%) in terms of phenoxyacetic acid and a content of 97.2-99.9%.
Недостатками способа являются:The disadvantages of this method are:
- многостадийность процесса;- multistage process;
- охлаждение до низких температур (ледяная баня) в промышленных масштабах потребует использования холодильных установок, что существенно усложняет и удорожает процесс;- cooling to low temperatures (ice bath) on an industrial scale will require the use of refrigeration units, which significantly complicates and increases the cost of the process;
- использование растворителя в процессе приведет к потерям целевого продукта при отделении растворителя;- the use of a solvent in the process will lead to the loss of the target product during the separation of the solvent;
- регенерация катализатора потребует дополнительных материальных и энергетических затрат;- catalyst regeneration will require additional material and energy costs;
- выход продукта в пересчете на исходный фенол будет меньше.- the product yield in terms of the initial phenol will be less.
В патентной заявке CN 105001079 (А) (С07С 51/363, С07С 59/70, 2015 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты, включающий следующие стадии: 1) получение феноксиуксусной кислоты реакцией хлоруксусной кислоты с фенолом и 32%-ным гидроксидом натрия в среде насыщенной поваренной соли при температуре 106°С и перемешивании в течение 30 минут; затем реакционную массу охлаждают до 80°С, подкисляют соляной кислотой, охлаждают до 20°С, фильтруют и получают порошок феноксиуксусной кислоты с содержанием 90,2%; 2) хлорирование феноксиуксусной кислоты хлором в растворе низшей карбоновой кислоты и воды при температуре 45-85°С (преимущественно 55-65°С) и перемешивании в течение 0,5-1 час; затем реакционную массу охлаждают до 18°С, фильтруют, полученный осадок сушат при 80°С. В качестве низшей карбоновой кислоты предложена уксусная, пропионовая, бутановая, изобутановая кислоты. Массовое отношение низшей карбоновой кислоты к воде = (1:9)-(9:1), отношение феноксиуксусная кислота : низшая карбоновая кислота : вода = (0,9-1) моль : 560 г : 240 г.In patent application CN 105001079 (A) (C07C 51/363, C07C 59/70, 2015), a method for preparing 2,4-dichlorophenoxyacetic acid is proposed, including the following steps: 1) obtaining phenoxyacetic acid by the reaction of chloroacetic acid with phenol and 32% sodium hydroxide in saturated sodium chloride at a temperature of 106 ° C and stirring for 30 minutes; then the reaction mass is cooled to 80 ° C, acidified with hydrochloric acid, cooled to 20 ° C, filtered to obtain a powder of phenoxyacetic acid with a content of 90.2%; 2) chlorination of phenoxyacetic acid with chlorine in a solution of lower carboxylic acid and water at a temperature of 45-85 ° C (mainly 55-65 ° C) and stirring for 0.5-1 hour; then the reaction mass is cooled to 18 ° C, filtered, the resulting precipitate is dried at 80 ° C. Acetic, propionic, butanoic, isobutanoic acids are proposed as the lower carboxylic acid. Mass ratio of lower carboxylic acid to water = (1: 9) - (9: 1), ratio of phenoxyacetic acid: lower carboxylic acid: water = (0.9-1) mol: 560 g: 240 g.
Выход целевого продукта составляет 84,1-98,5% в пересчете на феноксиуксусную кислоту, содержание 96,4-99,1%).The yield of the target product is 84.1-98.5% in terms of phenoxyacetic acid, the content is 96.4-99.1%).
Недостатками способа являются:The disadvantages of this method are:
- выход рассчитан на промежуточно образующуюся феноксиуксусную кислоту, в расчете на исходную хлоруксусную кислоту выход будет значительно меньше;- the yield is calculated for the intermediate formed phenoxyacetic acid, based on the initial chloroacetic acid, the yield will be much less;
- необходимость разделения хлорида натрия и целевого продукта;- the need to separate sodium chloride and the target product;
- большое количество образующихся сточных вод, вызывающих загрязнение окружающей среды.- a large amount of generated wastewater, causing environmental pollution.
В патентной заявке CN 102180788 (А) (С07С 51/363, С07С 59/70, 2011 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты, включающий стадии: получение феноксиуксусной кислоты из фенола и эпоксиэтана этерификацией, дегидрированием при температуре 65-70°С и перемешивании в течение 2-3 часов в присутствии катализатора окисления CuO/ZrO2; растворение феноксиуксусной кислоты в смешанном растворителе (вода, бензол, толуол, С1-С7-алканол или композиция из двух или более растворителей в диэтиловом эфире); реагирование раствора феноксиуксусной кислоты с хлором при температуре 75-80°С в присутствии катализатора хлорирования (серная/бензолсульфоновая кислота, серная/парахлор-бензолсульфоновая кислота, серная/паратолуолсульфоновая кислота, серная/ортотолуолсульфоновая кислота); охлаждение, кристаллизация, фильтрация и сушка. Получают целевой продукт с выходом 97,6-98,5% и содержанием активного ингредиента 98,7-99,3%.In patent application CN 102180788 (A) (C07C 51/363, C07C 59/70, 2011), a method for producing 2,4-dichlorophenoxyacetic acid is proposed, including the steps: obtaining phenoxyacetic acid from phenol and epoxyethane by esterification, dehydrogenation at a temperature of 65- 70 ° C and stirring for 2-3 hours in the presence of an oxidation catalyst CuO / ZrO 2 ; dissolving phenoxyacetic acid in a mixed solvent (water, benzene, toluene, C 1 -C 7 -alkanol or a composition of two or more solvents in diethyl ether); the reaction of a solution of phenoxyacetic acid with chlorine at a temperature of 75-80 ° C in the presence of a chlorination catalyst (sulfuric / benzenesulfonic acid, sulfuric / parachlorobenzenesulfonic acid, sulfuric / paratoluenesulfonic acid, sulfuric / orthotoluenesulfonic acid); cooling, crystallization, filtration and drying. The target product is obtained with a yield of 97.6-98.5% and an active ingredient content of 98.7-99.3%.
Недостатками способа являются:The disadvantages of this method are:
- использование смешанных растворителей в процессе приведет к потерям целевого продукта при отделении растворителя;- the use of mixed solvents in the process will lead to the loss of the target product during the separation of the solvent;
- необходимость применения катализатора окисления и катализатора хлорирования на разных стадиях процесса;- the need to use an oxidation catalyst and a chlorination catalyst at different stages of the process;
- очистка и регенерация смешанных растворителей и катализаторов потребует значительных дополнительных материальных и энергетических затрат.- purification and regeneration of mixed solvents and catalysts will require significant additional material and energy costs.
В патентной заявке CN105622396 (А) (С07С 51/363, С07С 59/70, 2016 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты, включающий следующие стадии: 1) получение феноксиуксусной кислоты реакцией фенола с хлоруксусной кислотой и жидким основанием в водной среде при значении рН 12 в присутствии катализатора этерификации (четвертичные аммониевые соли, полиэфир, циклический разветвленный эфир и четвертичные фосфониевые соли) при температуре 35-120°С и перемешивании в течение 3-5 часов; добавлением хлоруксусной кислоты до рН 2, охлаждением до 10-30°С, кристаллизацией в течение 1-3 часов, фильтрацией, промывкой и сушкой при 90°С в течение 2 часов; 2) хлорирование полученной феноксиуксусной кислоты хлорирующим агентом (30% соляная кислота и 30% перекись водорода, 36% соляная кислота и кислород, 33% соляная кислота и озон) в растворителе (этилацетат, ацетонитрил) в присутствии катализатора хлорирования (кислота Льюиса (один или более хлорид железа, цинка, олова, алюминия, титана, магния и бария) и/или твердая кислота) при температуре 40-70°С и перемешивании в течение 2-6 часов, охлаждение до комнатной температуры, кристаллизация в течение 3 часов, фильтрация, промывка (вода, метанол) и сушка при 130°С в течение 2 часов. Получают 2,4-дихлорфеноксиуксусную кислоту с чистотой 92,0-98,6%) и выходом 73,38-95,2% в пересчете на фенол.In patent application CN105622396 (A) (C07C 51/363, C07C 59/70, 2016), a method for preparing 2,4-dichlorophenoxyacetic acid is proposed, including the following steps: 1) obtaining phenoxyacetic acid by the reaction of phenol with chloroacetic acid and a liquid base in aqueous medium at pH 12 in the presence of an esterification catalyst (quaternary ammonium salts, polyester, cyclic branched ether and quaternary phosphonium salts) at a temperature of 35-120 ° C and stirring for 3-5 hours; adding chloroacetic acid to pH 2, cooling to 10-30 ° C, crystallization for 1-3 hours, filtration, washing and drying at 90 ° C for 2 hours; 2) chlorination of the obtained phenoxyacetic acid with a chlorinating agent (30% hydrochloric acid and 30% hydrogen peroxide, 36% hydrochloric acid and oxygen, 33% hydrochloric acid and ozone) in a solvent (ethyl acetate, acetonitrile) in the presence of a chlorination catalyst (Lewis acid (one or more chloride of iron, zinc, tin, aluminum, titanium, magnesium and barium) and / or solid acid) at a temperature of 40-70 ° C and stirring for 2-6 hours, cooling to room temperature, crystallization within 3 hours, filtration , washing (water, methanol) and drying at 130 ° C for 2 hours.
Недостатками способа являются:The disadvantages of this method are:
- многостадийность процесса;- multistage process;
- использование органических растворителей в процессе приведет к потерям целевого продукта при отделении растворителя;- the use of organic solvents in the process will lead to the loss of the target product during the separation of the solvent;
- очистка и регенерация растворителей и очистка целевого продукта от катализаторов потребует дополнительных материальных и энергетических затрат.- purification and regeneration of solvents and purification of the target product from catalysts will require additional material and energy costs.
В патентной заявке CN 106892808(A) (С07С 51/02, С07С 59/70, 2017 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты, включающий следующие стадии: 1) получение галогенацетата натрия реакцией галогенуксусной кислоты (хлоруксусная, бромуксусная, йодуксусная) с алкоксидом щелочного металла (метоксид натрия, этоксид натрия) в спиртовом растворе; 2) получение фенолята реакцией фенола с 10-80%-ным (наиболее предпочтительно 20-50%-ным) водным раствором основания (NaOH, KOH, Са(ОН)2, Mg(OH)2, Al(ОН)3, Na2CO3, K2CO3, NaHCO3, KHCO3) при перемешивании с последующим повышением температуры до 110°С для отгонки воды и получения сухого фенолята; 3) получение феноксиацетата натрия добавлением полученного сухого фенолята в спиртовой раствор галогенацетата (хлорацетата натрия) при температуре 50-200°С (наиболее предпочтительно 100°С) и активном перемешивании в течение 2-6 часов (наиболее предпочтительно 4-5 часов); 4) получение 2,4-дихлорфеноксиацетата натрия хлорированием феноксиацетата натрия газообразным хлором или сульфурилхлоридом в спиртовом растворе при перемешивании в присутствии катализатора хлорида металла (титан, алюминий, железо) при температуре 10-80°С (наиболее предпочтительно 20-70°С) в течение 2-10 часов (наиболее предпочтительно 5 час); 5) получение 2,4-дихлорфеноксиуксусной кислоты подкислением 2,4-дихлорфеноксиацетата натрия 10-60%-ной минеральной кислотой (предпочтительнее соляной) и ее кристаллизацией при 5-20°С в течение 1-1,5 часа. Получают целевой продукт с выходом 99,0-99,2% и чистотой 99,2-99,6%).In patent application CN 106892808 (A) (C07C 51/02, C07C 59/70, 2017), a method for producing 2,4-dichlorophenoxyacetic acid is proposed, including the following steps: 1) obtaining sodium haloacetate by the reaction of haloacetic acid (chloroacetic, bromoacetic, iodoacetic) with an alkali metal alkoxide (sodium methoxide, sodium ethoxide) in an alcohol solution; 2) obtaining phenolate by reaction of phenol with 10-80% (most preferably 20-50%) aqueous base solution (NaOH, KOH, Ca (OH) 2 , Mg (OH) 2 , Al (OH) 3 , Na 2 CO 3 , K 2 CO 3 , NaHCO 3 , KHCO 3 ) with stirring, followed by an increase in temperature to 110 ° C to distill off water and obtain dry phenolate; 3) obtaining sodium phenoxyacetate by adding the obtained dry phenolate to an alcoholic solution of haloacetate (sodium chloroacetate) at a temperature of 50-200 ° C (most preferably 100 ° C) and vigorous stirring for 2-6 hours (most preferably 4-5 hours); 4) obtaining 2,4-dichlorophenoxyacetate sodium by chlorination of sodium phenoxyacetate with gaseous chlorine or sulfuryl chloride in an alcohol solution with stirring in the presence of a metal chloride catalyst (titanium, aluminum, iron) at a temperature of 10-80 ° C (most preferably 20-70 ° C) in within 2-10 hours (most preferably 5 hours); 5) obtaining 2,4-dichlorophenoxyacetic acid by acidification of sodium 2,4-dichlorophenoxyacetate with 10-60% mineral acid (preferably hydrochloric acid) and its crystallization at 5-20 ° C for 1-1.5 hours. The target product is obtained with a yield of 99.0-99.2% and a purity of 99.2-99.6%).
Недостатки способа следующие:The disadvantages of this method are as follows:
1) Многостадийность процесса (5 стадий).1) Multi-stage process (5 stages).
2) Сложность технологии 1 стадии процесса:2) The complexity of the technology of the 1st stage of the process:
Метилат натрия образуется при действии металлического натрия на метиловый спирт:Sodium methylate is formed by the action of sodium metal on methyl alcohol:
2СН3ОН+2Na → 2CH3ONa+Н2 2CH 3 OH + 2Na → 2CH 3 ONa + H 2
Кроме того, указанная наиболее предпочтительная температура (100°С) осуществления реакции требует ведения процесса под давлением, так как температура кипения метанола 64,7°С. Это существенно усложняет технологию.In addition, the specified most preferred temperature (100 ° C) for carrying out the reaction requires conducting the process under pressure, since the boiling point of methanol is 64.7 ° C. This significantly complicates the technology.
Алкоголяты натрия и калия устойчивы в безводном спирте, но гидролизуются водой:Sodium and potassium alcoholates are stable in anhydrous alcohol, but hydrolyzed with water:
(Л. Физер, М. Физер «Органическая химия», изд. «Химия», М. 1969, с. 336).(L. Fizer, M. Fizer "Organic Chemistry", ed. "Chemistry", M. 1969, p. 336).
3) Образование побочных продуктов - хлорпроизводных эфиров и альдегидов на стадии хлорирования.3) Formation of by-products - chlorinated ethers and aldehydes at the chlorination stage.
При хлорировании феноксиацетата натрия в спиртовой среде образуются побочные продукты. Так хлорирование в среде метанола приводит к получению побочного продукта - дихлорметилового эфира:When sodium phenoxyacetate is chlorinated in an alcoholic medium, by-products are formed. So chlorination in methanol leads to the receipt of a by-product - dichloromethyl ether:
(«Краткая химическая энциклопедия», Москва, 1961, т. 1, с. 1181), а хлорирование в среде этанола приводит к образованию побочного продукта - хлораля и хлористого водорода:("Brief Chemical Encyclopedia", Moscow, 1961, vol. 1, p. 1181), and chlorination in ethanol leads to the formation of a by-product - chloral and hydrogen chloride:
(П. Каррер «Курс органической химии», Госхимиздат, 1963, с. 313.).(P. Carrer "Course of organic chemistry", Goskhimizdat, 1963, p. 313.).
4) Высокая взрывопожароопасность процесса при использовании метилового и этилового спирта в качестве растворителя.4) High explosion and fire hazard of the process when using methyl and ethyl alcohol as a solvent.
5) Использование токсичного метилового спирта в качестве растворителя.5) Using toxic methyl alcohol as a solvent.
6) Использование катализатора хлорида металла (железа, алюминия, титана) на стадии хлорирования, очистка целевого продукта от которого представляет определенные трудности.6) The use of a metal chloride catalyst (iron, aluminum, titanium) at the chlorination stage, the purification of the target product from which presents certain difficulties.
7) Хлорид железа с фенолами дает окрашивание реакционной массы, что отрицательно скажется на потребительских характеристиках продукта.7) Ferric chloride with phenols gives color to the reaction mass, which will negatively affect the consumer characteristics of the product.
8) Для подкисления реакционной массы минеральной кислотой необходимо дополнительное оборудование (мерники, насосы), что усложняет технологию процесса.8) To acidify the reaction mass with mineral acid, additional equipment (measuring tanks, pumps) is required, which complicates the process technology.
9) Сложность в утилизации сточных вод, содержащих растворы хлористого натрия.9) Difficulty in the disposal of wastewater containing sodium chloride solutions.
В данной заявке промежуточный продукт - соль феноксиуксусной кислоты - получают реакцией фенолята с хлорацетатом натрия в спиртовом растворе, причем в качестве фенолята может быть использован фенолят натрия, калия, кальция, магния, цинка и алюминия. В результате такой реакции, независимо от того какой фенолят взят, образуется щелочная соль феноксиуксусной кислоты.In this application, an intermediate product - a salt of phenoxyacetic acid - is obtained by the reaction of a phenolate with sodium chloroacetate in an alcohol solution, and the phenolate of sodium, potassium, calcium, magnesium, zinc and aluminum can be used as the phenolate. As a result of such a reaction, regardless of which phenolate is taken, an alkaline salt of phenoxyacetic acid is formed.
Известно, что растворимость солей в воде (гидратация) и неводных растворителях (сольватация) определяется разностью энергий кристаллической решетки и энергией гидратации (сольватации).It is known that the solubility of salts in water (hydration) and non-aqueous solvents (solvation) is determined by the difference between the energies of the crystal lattice and the energy of hydration (solvation).
Это согласуется с растворимостью указанных солей в воде, метаноле и этаноле.This is consistent with the solubility of these salts in water, methanol and ethanol.
Растворимость хлоридовSolubility of chlorides
Согласно описанию заявки CN 106892808 в качестве солей могут образовываться NaCl, KCl, CaCl2, MgCl2, ZnCl2, AlCl3. Поэтому очевидно, что в растворе будут преобладать соли Са+2, Mg+2, Zn+2, Al+3, тогда как феноксиуксусная кислота, которая в дальнейшем будет хлорироваться, находится только в виде натриевой соли, что и подтверждается примерами описания.According to the description of CN 106892808, NaCl, KCl, CaCl 2 , MgCl 2 , ZnCl 2 , AlCl 3 can be formed as salts. Therefore, it is obvious that Ca +2 , Mg +2 , Zn +2 , Al +3 salts will prevail in the solution, while phenoxyacetic acid, which will subsequently be chlorinated, is only in the form of a sodium salt, which is confirmed by the examples of the description.
В патентной заявке CN 108947838 (А) (С07С 51/09, 2018 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты и ее соли, где способ получения включает следующие стадии: 1) проведение реакции фенола со сложным эфиром хлоруксусной кислоты в щелочной среде (NaOH, KOH, NaHCO3, KHCO3, Na2CO3, K2CO3, NH(CH3)2) в присутствии органического растворителя (бензол, толуол, ксилол или их смеси) при температуре 60-120°С в течение 0,2-1 часа с получением сложного эфира феноксиуксусной кислоты; 2) проведение реакции селективного хлорирования сложного эфира феноксиуксусной кислоты хлорирующим агентом (газообразный хлор, тионилхлорид, сульфурилхлорид) под действием катализатора А (кислота Льюиса) и катализатора В (С5-С22-тиоэфиры, тиазолы, изотиазолы и тиофены или их галогенированные производные) при температуре 20-100°С в течение 0,2-1 часа с получением 2,4-дихлорфеноксиуксусного эфира; 3) проведение реакции гидролиза сложного эфира 2,4-дихлорфеноксиуксусной кислоты в кислых условиях при температуре 60-120°С в течение 2-4 часов с получением 2,4-дихлорфеноксиуксусной кислоты; или после получения 2,4-дихлорфеноксиуксусного эфира, осуществляя реакцию щелочного гидролиза со щелочным соединением с получением 2,4-дихлорфеноксиацетата.In patent application CN 108947838 (A) (C07C 51/09, 2018), a method for preparing 2,4-dichlorophenoxyacetic acid and its salt is proposed, where the method of preparation includes the following steps: 1) carrying out the reaction of phenol with an ester of chloroacetic acid in an alkaline medium (NaOH, KOH, NaHCO 3 , KHCO 3 , Na 2 CO 3 , K 2 CO 3 , NH (CH 3 ) 2 ) in the presence of an organic solvent (benzene, toluene, xylene or their mixtures) at a temperature of 60-120 ° C within 0.2-1 hours to obtain a phenoxyacetic acid ester; 2) carrying out the reaction of selective chlorination of phenoxyacetic acid ester with a chlorinating agent (chlorine gas, thionyl chloride, sulfuryl chloride) under the action of catalyst A (Lewis acid) and catalyst B (C 5 -C 22 thioesters, thiazoles, isothiazoles and thiophenes or their halogenated derivatives) at a temperature of 20-100 ° C for 0.2-1 hours to obtain 2,4-dichlorophenoxyacetic ether; 3) carrying out the hydrolysis reaction of the ester of 2,4-dichlorophenoxyacetic acid in acidic conditions at a temperature of 60-120 ° C for 2-4 hours to obtain 2,4-dichlorophenoxyacetic acid; or after obtaining 2,4-dichlorophenoxyacetic ester, carrying out an alkaline hydrolysis reaction with an alkaline compound to give 2,4-dichlorophenoxyacetate.
Выход 2,4-дихлорфеноксиуксусной кислоты в пересчете на исходный фенол составляет 98,07-98,62% и содержанием 98,5-98,9%.The yield of 2,4-dichlorophenoxyacetic acid in terms of the starting phenol is 98.07-98.62% and the content is 98.5-98.9%.
Недостатками способа являются:The disadvantages of this method are:
- многостадийность процесса;- multistage process;
- требуется дополнительная стадия синтеза эфира монохлоруксусной кислоты;- an additional stage of synthesis of monochloroacetic acid ester is required;
- использование органических растворителей в процессе приведет к потерям целевого продукта при отделении растворителя и усиливает огнеопасные и токсичные характеристики процесса;- the use of organic solvents in the process will lead to losses of the target product during the separation of the solvent and enhance the flammable and toxic characteristics of the process;
- использование сложных катализаторов на стадии хлорирования;- the use of complex catalysts at the chlorination stage;
- очистка и регенерация растворителей и катализаторов потребует значительных дополнительных материальных и энергетических затрат.- cleaning and regeneration of solvents and catalysts will require significant additional material and energy costs.
В патентной заявке CN 108424366 (А) (С07С 51/363, С07С 59/70, 2018 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты, включающий следующие стадии: 1) получение галогенированного ацетата взаимодействием галогенированной (хлор, бром, йод) уксусной кислоты со спиртом (С2-С10) в присутствии концентрированной серной кислоты при температуре 50-200°С в течение 4-5 часов; 2) получение раствора фенолята взаимодействием фенола со щелочью (NaOH, KOH, Са(ОН)2, Mg(OH)2, Zn(OH)2) при температуре 50-120°С; 3) получение феноксиацетата взаимодействием галогенированного ацетата с фенолятом при температуре 50-200°С в течение 0,5-1 час; 4) получение феноксиуксусной кислоты гидролизом феноксиацетата в щелочной среде минеральной кислотой (серной, соляной, азотной) при температуре 70-200°С в течение 2-4 час; 5) кристаллизация феноксиуксусной кислоты при температуре 10-20°С в течение 1-1,5 час; 6) получение 2,4-дихлорфеноксиуксусной кислоты хлорированием феноксиуксусной кислоты в среде растворителя в присутствии катализатора при температуре 0-100°С в течение 3-7 час. Хлорирующим агентом является газообразный хлор, сульфонилхлорид. В качестве растворителя используют диметилдисульфид, четыреххлористый углерод, дихлорэтан. Катализатором является одно или несколько соединений, состоящих из трихлорида железа, трихлорида алюминия, трифторида бора, пентахлорида ниобия, трифторметансульфоната алюминия, глинозема, оксида железа, триоксида бора, пятиоксида ниобия, дифенилового эфира, дифенилсульфида, дифенилдисульфида, диметилсульфида и диметилдисульфида.In patent application CN 108424366 (A) (C07C 51/363, C07C 59/70, 2018), a method for producing 2,4-dichlorophenoxyacetic acid is proposed, including the following steps: 1) obtaining halogenated acetate by the interaction of halogenated (chlorine, bromine, iodine ) acetic acid with alcohol (C 2 -C 10 ) in the presence of concentrated sulfuric acid at a temperature of 50-200 ° C for 4-5 hours; 2) obtaining a phenolate solution by the interaction of phenol with alkali (NaOH, KOH, Ca (OH) 2 , Mg (OH) 2 , Zn (OH) 2 ) at a temperature of 50-120 ° C; 3) obtaining phenoxyacetate by the interaction of halogenated acetate with phenolate at a temperature of 50-200 ° C for 0.5-1 hour; 4) obtaining phenoxyacetic acid by hydrolysis of phenoxyacetate in an alkaline medium with mineral acid (sulfuric, hydrochloric, nitric) at a temperature of 70-200 ° C for 2-4 hours; 5) crystallization of phenoxyacetic acid at a temperature of 10-20 ° C for 1-1.5 hours; 6) obtaining 2,4-dichlorophenoxyacetic acid by chlorination of phenoxyacetic acid in a solvent medium in the presence of a catalyst at a temperature of 0-100 ° C for 3-7 hours. The chlorinating agent is chlorine gas, sulfonyl chloride. The solvent used is dimethyl disulfide, carbon tetrachloride, dichloroethane. The catalyst is one or more compounds consisting of iron trichloride, aluminum trichloride, boron trifluoride, niobium pentachloride, aluminum trifluoromethanesulfonate, alumina, iron oxide, boron trioxide, niobium pentoxide, diphenyl ether, diphenyl sulfide, diphenyl disulfide and dimethyl sulfide, dimethyl sulfide.
По завершении реакции растворитель отгоняют, продукт кристаллизуют при температуре 10-20°С в течение 1-1,5 час, фильтруют, сушат. Получают 2,4-дихлорфеноксиуксусную кислоту с выходом 99,0-99,4% и чистотой 99,3-99,4%Upon completion of the reaction, the solvent is distilled off, the product is crystallized at a temperature of 10-20 ° C for 1-1.5 hours, filtered, dried.
Недостатками способа являются:The disadvantages of this method are:
- многостадийность процесса;- multistage process;
- использование в процессе 2-х стадий галогенирования;- use in the process of 2 stages of halogenation;
- утилизация галогенированных (бромистых, йодистых) отходов;- utilization of halogenated (bromide, iodide) waste;
- использование органических растворителей в процессе, что при отгонки растворителя приводит к потерям целевого продукта;- the use of organic solvents in the process, which, when the solvent is distilled off, leads to the loss of the target product;
- очистка и регенерация растворителей и катализаторов потребует значительных дополнительных материальных и энергетических затрат.- cleaning and regeneration of solvents and catalysts will require significant additional material and energy costs.
В патентной заявке CN 108947822 (А) (С07С 51/09, С07С 59/68, С07С 59/70, 2018 г.) предложен способ получения феноксикарбоновой кислоты, включающий следующие стадии: 1) получение эфира феноксикарбоновой кислоты конденсацией фенола или орто-крезола с эфиром хлоркарбоновой кислоты общей формулы ClR1COOR, где R1 выбран из алкиленовой группы, имеющей 1-3 атома углерода, R выбран из алкильной группы, имеющей 1-10 атомов углерода, или С3-С10-циклоалкил, в присутствии основания (NaOH, KOH, Са(ОН)2, Mg(OH)2, Na2CO3, K2CO3, NaHCO3, KHCO3) в среде органического растворителя, такого как бензол, толуол, ксилол, при температуре 60-120°С в течение 1-5 час. Полученный жидкий конденсат фильтруется при температуре 30-50°С, промывается водой и сушится до получения твердого продукта; 2) получение эфира хлорфеноксикарбоновой кислоты селективным хлорированием эфира феноксикарбоновой кислоты хлорирующим агентом (газообразный хлор, тионилхлорид, сульфурилхлорид) в присутствии одного или двух катализаторов, выбранных из кислоты Льюиса, С5-С22-тиоэфира, С5-С22-тиазола, С5-С22-изотиазола, С5-С22-тиофена, при температуре от -20°С до 100°С; 3) получение хлорфеноксикарбоновой кислоты реакцией кислотного гидролиза эфира хлорфеноксикарбоновой кислоты при температуре 60-120°С, в течение 2-4 часов. Для гидролиза используют сульфоновую, соляную, фосфорную, серную кислоты. По окончании реакции образовавшийся спирт отделяют, реакционную массу охлаждают до комнатной температуры, фильтруют, осадок промывают водой и сушат. Получают 2,4-дихлорфеноксиуксусную кислоту с содержанием 98,8% и выходом 98,0-98,12% в пересчете на фенол.In patent application CN 108947822 (A) (C07C 51/09, C07C 59/68, C07C 59/70, 2018), a method for producing phenoxycarboxylic acid is proposed, including the following steps: 1) obtaining an ester of phenoxycarboxylic acid by condensation of phenol or ortho-cresol with a chlorocarboxylic acid ester of the general formula ClR 1 COOR, where R 1 is selected from an alkylene group having 1-3 carbon atoms, R is selected from an alkyl group having 1-10 carbon atoms, or C 3 -C 10 -cycloalkyl, in the presence of a base (NaOH, KOH, Ca (OH) 2 , Mg (OH) 2 , Na 2 CO 3 , K 2 CO 3 , NaHCO 3 , KHCO 3 ) in an organic solvent such as benzene, toluene, xylene, at a temperature of 60- 120 ° C for 1-5 hours. The resulting liquid condensate is filtered at a temperature of 30-50 ° C, washed with water and dried until a solid product is obtained; 2) obtaining chlorophenoxycarboxylic acid ester by selective chlorination of phenoxycarboxylic acid ester with a chlorinating agent (chlorine gas, thionyl chloride, sulfuryl chloride) in the presence of one or two catalysts selected from Lewis acid, C 5 -C 22 thioester, C 5 -C 22 thiazole, C 5 -C 22 -isothiazole, C 5 -C 22 -thiophene, at a temperature from -20 ° C to 100 ° C; 3) obtaining chlorophenoxycarboxylic acid by the reaction of acid hydrolysis of chlorophenoxycarboxylic acid ester at a temperature of 60-120 ° C, for 2-4 hours. For hydrolysis, sulfonic, hydrochloric, phosphoric, sulfuric acids are used. At the end of the reaction, the formed alcohol is separated, the reaction mass is cooled to room temperature, filtered, the precipitate is washed with water and dried.
Недостатками способа являются:The disadvantages of this method are:
- стадия получения эфира хлоркарбоновой кислоты в среде органического растворителя;- the stage of obtaining an ester of chlorocarboxylic acid in an organic solvent;
- сушка полученного эфира хлорфенокисуксусной кислоты до твердого состояния, что существенно усложняет дальнейшие технологические операции;- drying of the obtained chlorophenoisacetic acid ester to a solid state, which significantly complicates further technological operations;
- использование органического растворителя на стадии конденсации;- the use of an organic solvent at the condensation stage;
- использование катализаторов на стадии хлорирования и необходимость их регенерации;- the use of catalysts at the chlorination stage and the need for their regeneration;
- очистка и регенерация растворителей и катализаторов потребует значительных дополнительных материальных и энергетических затрат.- cleaning and regeneration of solvents and catalysts will require significant additional material and energy costs.
В патентной заявке CN 108424360 (А) (С07С 51/09, С07С 59/70, 2018 г.) предложен способ получения 2,4-дихлорфеноксиуксусной кислоты, включающий следующие стадии: 1) получение галогенированного ацетата взаимодействием галогенированной (Cl, Br, J) уксусной кислоты со спиртом, имеющим от 2 до 20 атомов углерода, в присутствии катализатора (концентрированная сульфоновая кислота, толуол, бутилтитанат) при температуре 50-200°С и перемешивании в течение 1-10 час; 2) получение фенолята взаимодействием фенола со щелочью (NaOH, KOH, Са(ОН)2, Mg(OH)2, Zn(OH)2) при температуре 50-120°C; 3) получение феноксиацетата взаимодействием галогенированного ацетата с фенолятом при температуре 50-200°С и перемешивании в течение 0,5-1 час; 4) получение 2,4-дихлорфеноксиацетата хлорированием феноксиацетата газообразным хлором или сульфонилхлоридом в среде растворителя (диметилдисульфид, четыреххлористый углерод, дихлорэтан) при температуре 0-100°С в течение 3-7 часов под действием одного или нескольких катализаторов. Катализатор выбран из группы, состоящей из трихлорида железа, трихлорида алюминия, трифторида бора, пентахлорида ниобия, трифторметансульфоната, оксида алюминия, оксида железа, триоксида бора, пятиокиси ниобия, дифенилового эфира, дифенилсульфида, дифенилдисульфида, диметилсульфида и диметилдисульфида; 5) получение 2,4-дихлорфеноксиуксусной кислоты гидролизом 2,4-дихлорфеноксиацетата действием щелочного раствора (NaOH или KOH) при температуре 70-200°С в течение 2-4 часов, а затем раствором кислоты (серная, соляная, азотная, пара-толуолсульфоновая, муравьиная, уксусная) при температуре 70-200°С в течение 2-4 час. После этого растворитель отгоняют, фильтруют, кристаллизуют при температуре 10-20°С в течение 1-1,5 час, сушат и получают 2,4-дихлорфеноксиуксусную кислоту с выходом 99,3-99,5% и чистотой 99,3-99,5%).In patent application CN 108424360 (A) (C07C 51/09, C07C 59/70, 2018), a method for preparing 2,4-dichlorophenoxyacetic acid is proposed, including the following steps: 1) obtaining a halogenated acetate by the reaction of halogenated (Cl, Br, J ) acetic acid with alcohol having from 2 to 20 carbon atoms, in the presence of a catalyst (concentrated sulfonic acid, toluene, butyl titanate) at a temperature of 50-200 ° C and stirring for 1-10 hours; 2) obtaining phenolate by the interaction of phenol with alkali (NaOH, KOH, Ca (OH) 2 , Mg (OH) 2 , Zn (OH) 2 ) at a temperature of 50-120 ° C; 3) obtaining phenoxyacetate by the interaction of halogenated acetate with phenolate at a temperature of 50-200 ° C and stirring for 0.5-1 hour; 4) obtaining 2,4-dichlorophenoxyacetate by chlorination of phenoxyacetate with gaseous chlorine or sulfonyl chloride in a solvent medium (dimethyl disulfide, carbon tetrachloride, dichloroethane) at a temperature of 0-100 ° C for 3-7 hours under the action of one or more catalysts. The catalyst is selected from the group consisting of iron trichloride, aluminum trichloride, boron trifluoride, niobium pentachloride, trifluoromethanesulfonate, alumina, iron oxide, boron trioxide, niobium pentoxide, diphenyl ether, diphenyl sulfide, diphenyl disulfide and dimethyl disulfide; 5) obtaining 2,4-dichlorophenoxyacetic acid by hydrolysis of 2,4-dichlorophenoxyacetate by the action of an alkaline solution (NaOH or KOH) at a temperature of 70-200 ° C for 2-4 hours, and then with an acid solution (sulfuric, hydrochloric, nitric, para- toluenesulfonic, formic, acetic) at a temperature of 70-200 ° C for 2-4 hours. After that, the solvent is distilled off, filtered, crystallized at a temperature of 10-20 ° C for 1-1.5 hours, dried and 2,4-dichlorophenoxyacetic acid is obtained with a yield of 99.3-99.5% and a purity of 99.3-99 ,5%).
Недостатками процесса являются:The disadvantages of the process are:
- многостадийность процесса (5 стадий);- multistage process (5 stages);
- дополнительная стадия получения галогенированной (Cl, Br, J) уксусной кислоты;- additional stage of obtaining halogenated (Cl, Br, J) acetic acid;
- необходимость утилизации бром- и йодсодержащих отходов;- the need to dispose of bromine and iodine-containing waste;
- сложность технологии: вначале получают эфир галогенированного ацетата, который после хлорирования подвергают гидролизу. Это приводит к необходимости регенерации спирта и его очистки. Хлорирование при повышенных температурах вплоть до 100°С потребует работы под давлением, так как предложенные растворители кипят при более низкой температуре (температура кипения четыреххлористого углерода 76,7°С, температура кипения дихлорэтана 83,47°С, температура кипения диметилсульфида 37,34°С);- the complexity of the technology: first, a halogenated acetate ester is obtained, which, after chlorination, is subjected to hydrolysis. This leads to the need for alcohol recovery and purification. Chlorination at elevated temperatures up to 100 ° C will require work under pressure, since the proposed solvents boil at a lower temperature (boiling point of carbon tetrachloride 76.7 ° C, boiling point of dichloroethane 83.47 ° C, boiling point of dimethyl sulfide 37.34 ° WITH);
- необходимость регенерации используемых катализаторов на стадии хлорирования;- the need to regenerate the catalysts used at the chlorination stage;
- очистка растворителей и регенерация катализаторов потребует значительных дополнительных материальных и энергетических затрат.- cleaning of solvents and regeneration of catalysts will require significant additional material and energy costs.
Известен способ получения 2,4-дихлорфеноксиуксусной кислоты (RU 2684114, С07С 59/70, 2019 г.), включающий стадию синтеза щелочноземельной соли феноксиуксусной кислоты конденсацией фенола с монохлоруксусной кислотой и оксидом щелочноземельного металла в водной среде при температуре 90-100°С и перемешивании, стадию хлорирования щелочноземельной соли феноксиуксусной кислоты хлорирующим агентом и выделение целевого продукта известным способом.There is a known method of producing 2,4-dichlorophenoxyacetic acid (RU 2684114, С07С 59/70, 2019), including the stage of synthesis of an alkaline earth salt of phenoxyacetic acid by condensation of phenol with monochloroacetic acid and alkaline earth metal oxide in an aqueous medium at a temperature of 90-100 ° C and stirring, the stage of chlorination of the alkaline earth salt of phenoxyacetic acid with a chlorinating agent and the isolation of the target product in a known manner.
Синтез щелочноземельной соли феноксиуксусной кислоты проводят в три цикла для более полного извлечения продукта.The synthesis of the alkaline earth salt of phenoxyacetic acid is carried out in three cycles for a more complete extraction of the product.
Готовят суспензию щелочноземельного металла в воде перемешиванием в течение 0,5-1,5 часа при комнатной температуре. К полученной суспензии дозируют фенол, затем монохлоруксусную кислоту, поддерживая температуру 20-25°С. По окончании дозирования поднимают температуру в реакционной зоне до 90-100°С и выдерживают при указанной температуре 0,5-1 час. при постоянном перемешивании. Реакционную массу охлаждают до комнатной температуры, отфильтровывают соль феноксиуксусной кислоты (осадок), фильтрат возвращают в следующий цикл синтеза соли феноксиуксусной кислоты, используя вместо воды. Полученные в результате 3-х циклического синтеза осадки объединяют, промывают водой, отфильтровывают и высушивают.A suspension of alkaline earth metal in water is prepared by stirring for 0.5-1.5 hours at room temperature. Phenol is dosed to the resulting suspension, then monochloroacetic acid, maintaining the temperature at 20-25 ° C. At the end of dosing, the temperature in the reaction zone is raised to 90-100 ° C and kept at the specified temperature for 0.5-1 hour. with constant stirring. The reaction mass is cooled to room temperature, the phenoxyacetic acid salt (precipitate) is filtered off, the filtrate is returned to the next synthesis cycle of the phenoxyacetic acid salt, using instead of water. The precipitates obtained as a result of 3-cycle synthesis are combined, washed with water, filtered off and dried.
Три цикла синтеза соли феноксиуксусной кислоты на возвратном фильтрате обусловлено тем, чтобы избежать потерь продукта с фильтратом и дополнительных операций при более полном выделении продукта, то есть выпаривания, захолаживания.Three cycles of synthesis of the salt of phenoxyacetic acid on the return filtrate is due to the avoidance of product losses with the filtrate and additional operations with a more complete product recovery, that is, evaporation, cooling.
Хлорирование щелочноземельной соли феноксиуксусной кислоты газообразным хлором проводят в водной среде при температуре 20-25°С и перемешивании в течение 2-3 часов. По завершении реакции хлор отдувают воздухом или инертным газом. Осадок отфильтровывают, промывают водой, высушивают. Сухой продукт при необходимости промывают толуолом, сушат.Chlorination of the alkaline earth salt of phenoxyacetic acid with gaseous chlorine is carried out in an aqueous medium at a temperature of 20-25 ° C and stirring for 2-3 hours. Upon completion of the reaction, chlorine is purged with air or an inert gas. The precipitate is filtered off, washed with water, and dried. The dry product, if necessary, is washed with toluene and dried.
В случае использования в качестве хлорирующих агентов гипохлоритов натрия и кальция, а также хлористого водорода в присутствии перекиси водорода или соляной кислоты и перекиси водорода хлорирование проводят в водной среде при температуре 90-100°С и перемешивании в течение 3-3,5 часов. Целевой продукт выделяют известными приемами: реакционную массу охлаждают, отфильтровывают, промывают, высушивают.In the case of using sodium and calcium hypochlorites as chlorinating agents, as well as hydrogen chloride in the presence of hydrogen peroxide or hydrochloric acid and hydrogen peroxide, chlorination is carried out in an aqueous medium at a temperature of 90-100 ° C and stirring for 3-3.5 hours. The target product is isolated by known methods: the reaction mass is cooled, filtered, washed, dried.
Данное техническое решение выбрано в качестве прототипа, недостатками которого являются:This technical solution was chosen as a prototype, the disadvantages of which are:
- для осуществления стадии конденсации фенола с монохлоруксусной кислотой и оксидом щелочноземельного металла необходимо нагревать водный раствор реакционной смеси до температуры 90-100°С, что требует больших энергетических затрат;- to carry out the stage of condensation of phenol with monochloroacetic acid and alkaline earth metal oxide, it is necessary to heat the aqueous solution of the reaction mixture to a temperature of 90-100 ° C, which requires high energy costs;
- для более полного выделения промежуточного продукта из фильтрата проводят 3-х циклический синтез, что усложняет технологический процесс и увеличивает его продолжительность;- for a more complete separation of the intermediate product from the filtrate, a 3-cycle synthesis is carried out, which complicates the technological process and increases its duration;
- предусмотренная утилизация раствора хлористого кальция в обычно образующийся сульфат кальция требует дополнительной стадии взаимодействия с серной кислотой и высокотемпературного (более 1200°С) обжига сульфата кальция, чтобы его можно было использовать в качестве строительного материала. Такая высокая температура требуется для термодеструкции диоксинов, неизбежно образующихся при сжигании хлорорганических соединений. Энергетические затраты на обжиг весьма существенно удорожат стоимость целевого продукта.- the intended disposal of the calcium chloride solution into the usually formed calcium sulfate requires an additional stage of interaction with sulfuric acid and high-temperature (more than 1200 ° C) calcination of calcium sulfate, so that it can be used as a building material. Such a high temperature is required for the thermal destruction of dioxins, which are inevitably formed during the combustion of organochlorine compounds. Energy costs for firing will significantly increase the cost of the target product.
В приведенных патентных источниках авторы разрабатывали технологию получения целевого продукта с минимальным содержанием в нем хлорфенолов, так как их присутствие в гербицидном препарате снижает биологическое действие, ухудшает стабильность препарата при его хранении, придает неприятный устойчивый запах товарному продукту. Кроме того, из хлорфенолов могут образовываться высокотоксичные опасные соединения - диоксины.In the cited patent sources, the authors developed a technology for obtaining the target product with a minimum content of chlorophenols in it, since their presence in the herbicidal preparation reduces the biological effect, worsens the stability of the preparation during storage, and imparts an unpleasant persistent odor to the commercial product. In addition, highly toxic hazardous compounds, dioxins, can be formed from chlorophenols.
Диоксины и диоксиноподобные полихлорированные бифенилы (ПХБ) - это вещества, загрязняющие окружающую среду, стойкие органические загрязнители. Они являются побочными продуктами промышленного производства, которые образуются, например, при производстве пестицидов и сжигании отходов. Из-за высокой химической стабильности и хорошей растворимости в животных жирах они накапливаются в окружающей среде, растениях и живых организмах. Человек может быть подвержен действию диоксинов в результате употребления мясных, молочных и рыбных продуктов. Диоксины обладают нейротоксическим действием, могут вызывать поражение иммунной системы, гормональные нарушения, онкологические заболевания, проблемы в области репродуктивного здоровья и т.д. Поэтому во многих странах на государственном уровне запрещено использовать сырье, а также готовые продукты и корма с их повышенным содержанием.Dioxins and dioxin-like polychlorinated biphenyls (PCBs) are environmental pollutants, persistent organic pollutants. They are industrial by-products that are generated, for example, from the production of pesticides and waste incineration. Due to their high chemical stability and good solubility in animal fats, they accumulate in the environment, plants and living organisms. A person can be exposed to dioxins as a result of eating meat, dairy and fish products. Dioxins are neurotoxic, can cause damage to the immune system, hormonal disorders, cancer, reproductive health problems, etc. Therefore, in many countries at the state level, it is prohibited to use raw materials, as well as finished products and feeds with their increased content.
Технической задачей изобретения является упрощение и увеличение производительности технологического процесса получения 2,4-дихлорфеноксиуксусной кислоты, при котором не образуются хлорзамещенные фенолы и, как следствие, токсиканты - диоксины.The technical objective of the invention is to simplify and increase the productivity of the technological process for producing 2,4-dichlorophenoxyacetic acid, which does not form chlorine-substituted phenols and, as a consequence, toxicants - dioxins.
Поставленная задача решена разработанным способом получения 2,4-дихлорфеноксиуксусной кислоты, который состоит в том, что промежуточный продукт - кальциевую соль феноксиуксусной кислоты - получают конденсацией фенола с монохлоруксусной кислотой и оксидом или гидроксидом кальция в расплаве. Синтез проходит в условиях саморазогревания реакционной массы и температуру в зоне реакции удерживают в интервале 80-160°С в течение 10-30 минут при постоянном перемешивании. В результате получают моногидрат кальциевой соли феноксиуксусной кислоты.The problem is solved by the developed method for producing 2,4-dichlorophenoxyacetic acid, which consists in the fact that the intermediate product - the calcium salt of phenoxyacetic acid - is obtained by condensation of phenol with monochloroacetic acid and calcium oxide or hydroxide in the melt. The synthesis takes place under conditions of self-heating of the reaction mass and the temperature in the reaction zone is kept in the range of 80-160 ° C for 10-30 minutes with constant stirring. As a result, the monohydrate of the calcium salt of phenoxyacetic acid is obtained.
Для получения моногидрата кальциевой соли феноксиуксусной кислоты предложено три варианта.To obtain monohydrate of calcium salt of phenoxyacetic acid, three options have been proposed.
Вариант 1. В расплав фенола дозируют оксид кальция (СаО) или гидроксид кальция (СаОН)2, затем монохлоруксусную кислоту.
Вариант 2. В расплав монохлоруксусной кислоты дозируют оксид кальция (СаО) или гидроксид кальция (СаОН)2, затем дозируют фенол.
Вариант 3. В расплав фенола с монохлоруксусной кислотой дозируют оксид кальция (СаО) или гидроксид кальция (СаОН)2.
Полученный моногидрат кальциевой соли феноксиуксусной кислоты хлорируют газообразным хлором в водной среде при температуре 20-25°С и перемешивании в течение 1,5-2,5 часов. По завершении реакции хлор отдувают воздухом или азотом. Осадок отфильтровывают, промывают водой, высушивают. Сухой продукт при необходимости промывают толуолом, сушат.The obtained monohydrate of the calcium salt of phenoxyacetic acid is chlorinated with gaseous chlorine in an aqueous medium at a temperature of 20-25 ° C and stirring for 1.5-2.5 hours. Upon completion of the reaction, chlorine is purged with air or nitrogen. The precipitate is filtered off, washed with water, and dried. The dry product, if necessary, is washed with toluene and dried.
Известно, что при нормальном давлении хлора 1 атм. при температуре ниже 9,5°С в воде образуются кристаллы газового гидрата хлора приблизительного состава С12 ⋅ 6H2O и С12 ⋅ 8H2O. Поэтому хлорирование водного раствора соли феноксиуксусной кислоты хлором при температуре ниже 20°С нежелательно, так как при повышенном давлении твердые гидраты хлора существуют при более высоких температурах.It is known that at a normal chlorine pressure of 1 atm. at temperatures below 9.5 ° C, crystals of chlorine gas hydrate with an approximate composition of C1 2 ⋅ 6H 2 O and C1 2 ⋅ 8H 2 O are formed in water. Therefore, chlorination of an aqueous solution of a salt of phenoxyacetic acid with chlorine at temperatures below 20 ° C is undesirable, since at At elevated pressures, solid chlorine hydrates exist at higher temperatures.
Повышение температуры при хлорировании газообразным хлором водного раствора соли феноксиуксусной кислоты выше 30°С нецелесообразно. Это приводит к уменьшению растворимости хлора в воде, что неблагоприятно сказывается на скорости реакции хлорирования и возрастают энергетические затраты на нагрев реакционной массы. Кроме того, при растворении хлора в воде образуется хлорноватистая кислотаIncreasing the temperature during chlorination with gaseous chlorine of an aqueous solution of a salt of phenoxyacetic acid above 30 ° C is impractical. This leads to a decrease in the solubility of chlorine in water, which adversely affects the rate of the chlorination reaction and increases the energy consumption for heating the reaction mass. In addition, when chlorine is dissolved in water, hypochlorous acid is formed.
Cl2+H2O → HClO+HCl,Cl 2 + H 2 O → HClO + HCl,
которая при нагревании распадается до хлорноватой кислотыwhich, when heated, decomposes to chloric acid
6HClO → 4HCl+2HClO3.6HClO → 4HCl + 2HClO 3 .
Хлорноватая кислота является сильным окислителем и может приводить к нежелательным окислительным процессам, снижающим выход 2,4-дихлорфеноксиуксусной кислоты и загрязняющую ее продуктами окисления.Chloric acid is a strong oxidizing agent and can lead to undesirable oxidative processes that reduce the yield of 2,4-dichlorophenoxyacetic acid and contaminate it with oxidation products.
Хлорирование не ограничивается газообразным хлором или любым хлорсодержащим газом. Хлорирование может осуществляться хлором, образующимся в химических или электрохимических процессах, например, при взаимодействии пероксидов с водными растворами хлористого водорода. Хлорирование также может осуществляться другими реагентами, содержащими активный хлор, например, гипохлоритами, но не ограничивается ими. Все гипохлориты весьма неустойчивы и являются хорошими окислителями (Ф. Коттон, Дж. Уилкинсон «Современная неорганическая химия». Изд. «Мир», М., 1969, с. 430). Во избежание протекания окислительных процессов при хлорировании кальциевой соли феноксиуксусной кислоты в некоторых случаях целесообразно вводить в реакционную зону добавки, нейтрализующие действие гипохлорит-ионов.Chlorination is not limited to chlorine gas or any chlorine gas. Chlorination can be carried out with chlorine formed in chemical or electrochemical processes, for example, when peroxides react with aqueous solutions of hydrogen chloride. Chlorination can also be carried out by other reagents containing active chlorine, for example, but not limited to hypochlorites. All hypochlorites are very unstable and are good oxidizing agents (F. Cotton, J. Wilkinson "Modern inorganic chemistry". Publishing house "Mir", Moscow, 1969, p. 430). In order to avoid the occurrence of oxidative processes during the chlorination of the calcium salt of phenoxyacetic acid, in some cases it is advisable to introduce additives into the reaction zone that neutralize the effect of hypochlorite ions.
Отличительным признаком предлагаемого способа является то, что синтез кальциевой соли феноксиуксусной кислоты осуществляют не в водном растворе, а в расплаве фенола, монохлоруксусной кислоты или их смеси с оксидом или гидроксидом кальция.A distinctive feature of the proposed method is that the synthesis of the calcium salt of phenoxyacetic acid is carried out not in an aqueous solution, but in a melt of phenol, monochloroacetic acid or their mixture with oxide or calcium hydroxide.
Неожиданным оказалось то, что реакция конденсации может идти в расплаве реагентов без участия растворителя при температуре до 170°С с образованием моногидрата кальциевой соли феноксиуксусной кислоты, что заранее предугадать было невозможно.It turned out unexpectedly that the condensation reaction can proceed in the melt of the reagents without the participation of a solvent at temperatures up to 170 ° C with the formation of monohydrate of the calcium salt of phenoxyacetic acid, which was impossible to predict in advance.
Сущность изобретения заключается в следующем.The essence of the invention is as follows.
Химизм образования кальциевой соли феноксиуксусной кислоты:The chemistry of the formation of the calcium salt of phenoxyacetic acid:
Суммарный процесс выглядит следующим образом:The overall process looks like this:
В случае использования гидроксида кальция суммарный химизм процесса описывается следующим образом:In the case of using calcium hydroxide, the total chemistry of the process is described as follows:
Химизм хлорирования кальциевой соли феноксиуксусной кислоты:The chlorination chemistry of the calcium salt of phenoxyacetic acid:
Преимуществами предложенного технического решения являются:The advantages of the proposed technical solution are:
- при дозировании в расплавы исходных компонентов оксида кальция или гидроксида кальция идет саморазогрев реакционной массы, что в промышленных масштабах экономит электроэнергию, позволяет резко уменьшить габариты реакторов, что снижает материальные затраты;- when dosing the initial components of calcium oxide or calcium hydroxide into the melts, the reaction mass self-heating occurs, which saves electricity on an industrial scale, allows to drastically reduce the dimensions of the reactors, which reduces material costs;
- проведение реакции конденсации в расплаве исходных реагентов увеличивает скорость химического процесса, что положительно скажется на производительности реакторного оборудования синтеза кальциевой соли феноксиуксусной кислоты и приведет к удешевлению процесса;- carrying out the condensation reaction in the melt of the initial reagents increases the rate of the chemical process, which will have a positive effect on the productivity of the reactor equipment for the synthesis of the calcium salt of phenoxyacetic acid and will lead to a reduction in the cost of the process;
- процесс является безотходным, проведение реакции конденсации в расплаве устраняет образование сточных вод, благодаря системе обратного осмоса чистая вода возвращается в производственный цикл, что улучшает экологичность процесса.- the process is waste-free, carrying out the condensation reaction in the melt eliminates the formation of waste water, thanks to the reverse osmosis system, clean water is returned to the production cycle, which improves the environmental friendliness of the process.
Краткое описание чертежей.Brief description of the drawings.
Фиг. 1 представляет собой дериватаграмму кальциевой, соли феноксиуксусной кислоты, полученной согласно настоящего изобретения.FIG. 1 is a derivative of the calcium phenoxyacetic acid salt prepared according to the present invention.
Фиг. 2 представляет собой 1H-спектр ядерного магнитного резонанса феноксиуксусной кислоты, полученной согласно настоящего изобретения.FIG. 2 is a 1 H nuclear magnetic resonance spectrum of phenoxyacetic acid prepared according to the present invention.
Фиг. 3 представляет собой 1Н-спектр ядерного магнитного резонанса 2,4-дихлорфеноксиуксусной кислоты, полученной согласно настоящего изобретения.FIG. 3 is a 1 H nuclear magnetic resonance spectrum of 2,4-dichlorophenoxyacetic acid prepared according to the present invention.
Фиг. 4 представляет собой блок-схему безотходного технологического процесса получения 2,4-дихлорфеноксиуксусной кислоты согласно настоящего изобретения, в производственный процесс которого включены:FIG. 4 is a block diagram of a waste-free process for producing 2,4-dichlorophenoxyacetic acid according to the present invention, the production process of which includes:
1. Действующее производство хлора.1. Operating chlorine production.
2. Реактор синтеза кальциевой соли феноксиуксусной кислоты (ФУК).2. Reactor for the synthesis of calcium salt of phenoxyacetic acid (FCA).
3. Узел фильтрации и промывки кальциевой соли феноксиуксусной кислоты (ФУК).3. Unit of filtration and washing of calcium salt of phenoxyacetic acid (FUA).
4. Реактор хлорирования кальциевой соли феноксиуксусной кислоты (ФУК).4. Reactor for chlorination of calcium salt of phenoxyacetic acid (FUA).
5. Узел фильтрации 2,4-Д.5.
6. Реактор гидролиза хлористого кальция.6. Reactor for hydrolysis of calcium chloride.
7. Узел фильтрации гидроксида кальция.7. Unit for filtration of calcium hydroxide.
8. Сушилка хлористого кальция.8. Dryer for calcium chloride.
9. Реактор фотолитической очистки фильтратов.9. Reactor for photolytic filtrate purification.
10. Газораспределитель.10. Gas distributor.
11. Блок термокаталитической фильтрации озона газовой фазы.11. Block of thermocatalytic filtration of ozone in the gas phase.
12. Блок каталитической деструкции озона жидкой фазы.12. Unit for catalytic destruction of liquid phase ozone.
13. Аппарат обратного осмоса.13. Reverse osmosis apparatus.
Обозначение потоков:Threads designation:
А - Фенол.A - Phenol.
В - Монохлоруксусная кислота.B - Monochloroacetic acid.
С - Оксид или гидроксид кальция.C - Calcium oxide or hydroxide.
D1 - Вода на промывку кальциевой соли феноксиуксусной кислоты.D1 - Water for washing the calcium salt of phenoxyacetic acid.
D2 - Вода на промывку 2,4-Д.D2 - Water for rinsing 2,4-D.
Е - Хлор.E - Chlorine.
G - Гидроксид натрия.G - Sodium hydroxide.
Н - Озон.H - Ozone.
F1 - Фильтрат после промывки кальциевой соли феноксиуксусной кислоты.F1 - Filtrate after washing with calcium salt of phenoxyacetic acid.
F2 - Фильтрат после промывки 2,4-Д. F3 - Осадок гидроксида кальция.F2 - Filtrate after washing with 2,4-D. F3 - Calcium hydroxide precipitate.
F4 (D) - Вода (пермеат) после осмотической обработки водного раствора хлористого натрия.F4 (D) - Water (permeate) after osmotic treatment of an aqueous solution of sodium chloride.
F5 (в 1) - Раствор хлористого натрия, возврат в производство хлора.F5 (in 1) - Sodium chloride solution, return to chlorine production.
F6 (С) (в 2) - Гидроксид или оксид кальция, возврат в реактор (2) синтеза кальциевой соли феноксиуксусной кислоты.F6 (C) (in 2) - Calcium hydroxide or oxide, return to the reactor (2) for the synthesis of the calcium salt of phenoxyacetic acid.
Изобретение иллюстрируется следующими примерами.The invention is illustrated by the following examples.
Пример 1.Example 1.
В подходящий реактор загружают 18,82 г (0,20 моль) фенола, 18,90 г (0,20 моль) монохлоруксусной кислоты, разогревают смесь до плавления и при интенсивном перемешивании дозируют 11,21 г (0,20 моль) оксида кальция СаО. При этом наблюдается самопроизвольный разогрев реакционной массы. При температуре 95-100°С реакционную массу выдерживают в течение 10 минут и после охлаждения дозируют 76 мл воды для отмывки образовавшейся кальциевой соли феноксиуксусной кислоты от хлористого кальция. Реакционную массу отфильтровывают. Затем реакционную массу охлаждают до комнатной температуры и дополнительно отфильтровывают 2,01 г твердого продукта. Осадок высушивают и получают 35,03 г продукта, являющегося моногидратом кальциевой соли феноксиуксусной кислоты:A suitable reactor is charged with 18.82 g (0.20 mol) of phenol, 18.90 g (0.20 mol) of monochloroacetic acid, the mixture is heated to melting and 11.21 g (0.20 mol) of calcium oxide are dosed with vigorous stirring CaO. In this case, spontaneous heating of the reaction mass is observed. At a temperature of 95-100 ° C, the reaction mass is kept for 10 minutes and after cooling, 76 ml of water is dosed to wash the formed calcium salt of phenoxyacetic acid from calcium chloride. The reaction mass is filtered off. Then the reaction mass is cooled to room temperature and additionally filtered off 2.01 g of solid product. The precipitate is dried and 35.03 g of the product is obtained, which is the monohydrate of the calcium salt of phenoxyacetic acid:
На фиг. 1 представлена дериватаграмма кальциевой соли феноксиуксусной кислоты. Дериватографические измерения проводили с помощью Q-дериватографа со скоростью нагрева 57 мин.FIG. 1 shows the derivatogram of the calcium salt of phenoxyacetic acid. Derivatographic measurements were performed using a Q-derivatograph with a heating rate of 57 min.
На кривой DTA обнаружен эндотермический пик с максимальной температурой процесса 150°С, при котором наблюдается потеря массы образца, соответствующее удалению 1 молекулы кристаллогидратной воды.The DTA curve exhibits an endothermic peak with a maximum process temperature of 150 ° C, at which a loss of sample mass is observed, corresponding to the removal of 1 molecule of crystalline hydrate water.
С помощью ЯМР 1Н-спектроскопии раствора кальциевой соли феноксиуксусной кислоты обнаружены сигналы химических сдвигов и констант спин-спинового взаимодействия, характерные для феноксиуксусной кислоты.Using 1 H-NMR spectroscopy of the solution of the calcium salt of phenoxyacetic acid chemical shifts detected signals and constants of spin-spin interaction characteristic of phenoxyacetic acid.
Спектр 1Н ядерного магнитного резонанса, снятый на ЯМР-спектрометре Avance-400 фирмы «Брукер», приведенный на фиг. 2, подтверждает образование феноксиуксусной кислоты.The 1 H nuclear magnetic resonance spectrum recorded on a Brooker Avance-400 NMR spectrometer, shown in FIG. 2, confirms the formation of phenoxyacetic acid.
Спектр характеризует структуру, содержащую феноксигруппу с химическими сдвигами δ, м.д.: 6.91-6.93 (2Н, d, С2Н, С6Н), 6,998 (1Н, t, С4Н), 7,302 (2Н, t, С3Н, С5Н) и карбоксиметильный фрагмент δ=4,664 м.д. (2Н, О-CH 2 -COOH), что однозначно идентифицирует соединение как феноксиуксусную кислоту.The spectrum characterizes the structure containing a phenoxy group with chemical shifts δ, ppm: 6.91-6.93 (2H, d, C 2 H, C 6 H), 6.998 (1H, t, C 4 H), 7.302 (2H, t, C 3 H, C 5 H) and carboxymethyl fragment δ = 4.664 ppm. (2H, O-C H 2 -COOH), which uniquely identifies the compound as phenoxyacetic acid.
Таким образом, получен продукт в количестве 35,03 г в виде моногидрата кальциевой соли феноксиуксусной кислоты с выходом 97,2% в пересчете на фенол.Thus, the product was obtained in the amount of 35.03 g in the form of monohydrate of the calcium salt of phenoxyacetic acid with a yield of 97.2% in terms of phenol.
Пример 2.Example 2.
В реакционное устройство, снабженное подходящим перемешивающим устройством, системой для охлаждения, заливают расплав фенола в количестве 47,06 г (0,50 моль). Через дозирующее устройство загружают 28,60 г (0,51 моль) оксида кальция (СаО) и расплав 48,19 г (0,51 моль) монохлоруксусной кислоты. Реакционная смесь саморазогревается и температуру в зоне реакции удерживают в интервале 80-100°С в течение 30 минут при постоянном перемешивании. Для удаления образовавшегося хлорида кальция в реакционную массу добавляют 120 мл воды и перемешивают для полноты удаления хлорида кальция. После фильтрации реакционной массы и высушивания осадка получают 86,59 г моногидрата кальциевой соли феноксиуксусной кислоты с выходом 96,1%) в пересчете на фенол.A phenol melt in the amount of 47.06 g (0.50 mol) is poured into a reaction device equipped with a suitable stirring device, a cooling system. Through a dosing device load 28.60 g (0.51 mol) of calcium oxide (CaO) and a melt of 48.19 g (0.51 mol) of monochloroacetic acid. The reaction mixture is self-heating and the temperature in the reaction zone is kept in the range of 80-100 ° C for 30 minutes with constant stirring. To remove the formed calcium chloride, 120 ml of water are added to the reaction mass and stirred to complete the removal of calcium chloride. After filtration of the reaction mixture and drying of the precipitate, 86.59 g of monohydrate of the calcium salt of phenoxyacetic acid are obtained with a yield of 96.1% in terms of phenol.
Пример 3.Example 3.
В реактор с перемешивающим и дозирующим устройством, оборудованный системой охлаждения, загружают расплав монохлоруксусной кислоты в количестве 48,19 г (0,51 моль). Затем в расплав при интенсивном перемешивании загружают 28,60 г (0,51 моль) оксида кальция СаО. После этого дозируют фенол в количестве 47,06 г (0,5 моль). При дозировании температура реакционной смеси самопроизвольно повышается до 150°С. Перемешивают реакционную массу 10-20 минут и после охлаждения добавляют 140 мл воды для очистки образовавшейся кальциевой соли феноксиуксусной кислоты. Осадок отфильтровывают и после сушки получают 87,49 г моногидрата кальциевой соли феноксиуксусной кислоты с выходом 97,1% в пересчете на фенол.In a reactor with a stirring and dosing device, equipped with a cooling system, the monochloroacetic acid melt is charged in an amount of 48.19 g (0.51 mol). Then, 28.60 g (0.51 mol) of calcium oxide CaO are charged into the melt with vigorous stirring. Thereafter, phenol is metered in in the amount of 47.06 g (0.5 mol). When dosing, the temperature of the reaction mixture spontaneously rises to 150 ° C. The reaction mass is stirred for 10-20 minutes and after cooling, 140 ml of water is added to purify the formed calcium salt of phenoxyacetic acid. The precipitate is filtered off and after drying, 87.49 g of monohydrate of the calcium salt of phenoxyacetic acid are obtained with a yield of 97.1% in terms of phenol.
Пример 4.Example 4.
В подходящий реактор загружают 68,04 г (0,72 моль) монохлоруксусной кислоты, 65,88 г (0,70 моль) фенола, разогревают смесь до плавления и при интенсивном перемешивании дозируют 53,35 г (0,72 моль) гидроксида кальция Са(ОН)2. При этом наблюдается самопроизвольный разогрев реакционной массы. При температуре 95°С реакционную массу выдерживают в течение 30 минут и после охлаждения дозируют 200 мл воды для отмывки образовавшейся кальциевой соли феноксиуксусной кислоты от хлористого кальция. Реакционную массу отфильтровывают. Затем реакционную массу охлаждают до комнатной температуры и дополнительно отфильтровывают. Осадок высушивают и получают 121,09 г моногидрата кальциевой соли феноксиуксусной кислоты с выходом 96,0% в пересчете на фенол.A suitable reactor is charged with 68.04 g (0.72 mol) of monochloroacetic acid, 65.88 g (0.70 mol) of phenol, the mixture is heated to melting and 53.35 g (0.72 mol) of calcium hydroxide is dosed with vigorous stirring Ca (OH) 2 . In this case, spontaneous heating of the reaction mass is observed. At a temperature of 95 ° C, the reaction mass is kept for 30 minutes and after cooling, 200 ml of water is dosed to wash the formed calcium salt of phenoxyacetic acid from calcium chloride. The reaction mass is filtered off. Then the reaction mass is cooled to room temperature and additionally filtered. The precipitate is dried to obtain 121.09 g of monohydrate of the calcium salt of phenoxyacetic acid with a yield of 96.0% in terms of phenol.
Пример 5.Example 5.
В реактор с перемешивающим и дозирующим устройством, оборудованный системой охлаждения, загружают расплав монохлоруксусной кислоты в количестве 95,44 г (1,01 моль). Затем в расплав при интенсивном перемешивании загружают 74,83 г (1,01 моль) гидроксида кальция Са(ОН)2. После этого дозируют фенол в количестве 94,11 г (1,00 моль). При дозировании температура реакционной смеси самопроизвольно повышается до 160°С. Перемешивают реакционную массу 10-20 минут и после охлаждения добавляют 290 мл воды для очистки образовавшейся кальциевой соли феноксиуксусной кислоты. Осадок отфильтровывают и после сушки получают 174,06 г моногидрата кальциевой соли феноксиуксусной кислоты с выходом 96,6% в пересчете на фенол.In a reactor with a stirring and dosing device, equipped with a cooling system, the monochloroacetic acid melt is charged in the amount of 95.44 g (1.01 mol). Then, 74.83 g (1.01 mol) of calcium hydroxide Ca (OH) 2 is loaded into the melt with vigorous stirring. Thereafter, phenol is dosed in an amount of 94.11 g (1.00 mol). When dosing, the temperature of the reaction mixture spontaneously rises to 160 ° C. The reaction mixture is stirred for 10-20 minutes and after cooling, 290 ml of water is added to purify the formed calcium salt of phenoxyacetic acid. The precipitate is filtered off and after drying, 174.06 g of monohydrate of the calcium salt of phenoxyacetic acid are obtained with a yield of 96.6% in terms of phenol.
Водный фильтрат после очистки кальциевой соли феноксиуксусной кислоты направляют на стадию гидролиза хлористого кальция, а затем, после его отделения, осветленный фильтрат - на стадию фотохимического озонирования.After purification of the calcium salt of phenoxyacetic acid, the aqueous filtrate is directed to the stage of hydrolysis of calcium chloride, and then, after its separation, the clarified filtrate is directed to the stage of photochemical ozonation.
Полностью минерализованный фильтрат после фотохимического озонирования поступает в узел очистки рассола действующего производства электрохимического получения хлора.Completely mineralized filtrate, after photochemical ozonation, enters the brine purification unit of the existing production of electrochemical chlorine production.
Данный способ получения 2,4-дихлорфеноксиуксусной кислоты наиболее целесообразно совместить с производством хлора либо в непосредственной близости действующего производства хлора. В этом случае технологический процесс может быть организован как безотходный.This method of obtaining 2,4-dichlorophenoxyacetic acid is most expediently combined with the production of chlorine or in the immediate vicinity of the existing chlorine production. In this case, the technological process can be organized as waste-free.
Пример 6.Example 6.
Синтез 2,4-дихлорфеноксиуксусной кислоты из моногидрата кальциевой соли феноксиуксусной кислоты.Synthesis of 2,4-dichlorophenoxyacetic acid from monohydrate of calcium salt of phenoxyacetic acid.
В круглодонную колбу, оборудованную перемешивающим устройством, барботером и термостатом, загружают 330 мл воды и 28,83 г (0,08 моль) моногидрата кальциевой соли феноксиуксусной кислоты, полученного по примерам 1-5. При включенной мешалке через барботер подают газообразный хлор. С учетом того, что в водной среде кальциевая соль феноксиуксусной кислоты существует не в виде гидрата, реакция протекает следующим образом:In a round bottom flask equipped with a stirrer, bubbler and thermostat, load 330 ml of water and 28.83 g (0.08 mol) of monohydrate of calcium salt of phenoxyacetic acid obtained in examples 1-5. With the stirrer turned on, chlorine gas is fed through the bubbler. Taking into account the fact that the calcium salt of phenoxyacetic acid does not exist in the form of a hydrate in an aqueous medium, the reaction proceeds as follows:
Температуру в зоне реакции поддерживают в интервале 20-25°С. Хлорирование осуществляют в течение 1,5 час. После завершения реакции растворенный в реакционной массе хлор отдувают током воздуха.The temperature in the reaction zone is maintained in the range of 20-25 ° C. Chlorination is carried out for 1.5 hours. After the completion of the reaction, chlorine dissolved in the reaction mass is blown off with a stream of air.
Выпавший осадок отфильтровывают и промывают 65 мл воды и высушивают. После сушки получают 35,63 г сухого продукта, который при необходимости промывают 60 мл органического растворителя, преимущественно толуолом, и после сушки получают 33,94 г продукта, содержащего 99,4% 2,4-дихлорфеноксиуксусной кислоты и 0,6% монохлор-феноксиуксусной кислоты. Выход 2,4-дихлорфеноксиуксусной кислоты составляет 95,4% от теоретического в пересчете на моногидрат кальциевой соли феноксиуксусной кислоты.The formed precipitate is filtered off and washed with 65 ml of water and dried. After drying, 35.63 g of dry product is obtained, which, if necessary, is washed with 60 ml of an organic solvent, mainly toluene, and after drying, 33.94 g of a product is obtained containing 99.4% of 2,4-dichlorophenoxyacetic acid and 0.6% of monochloro- phenoxyacetic acid. The yield of 2,4-dichlorophenoxyacetic acid is 95.4% of theoretical in terms of monohydrate of the calcium salt of phenoxyacetic acid.
Спектр 1Н ядерного магнитного резонанса 2,4-дихлорфеноксиуксусной кислоты, снятый на ЯМР-спектрометре Avance-400 фирмы «Брукер», приведен на фиг. 3.The 1 H nuclear magnetic resonance spectrum of 2,4-dichlorophenoxyacetic acid, recorded on a Bruker Avance-400 NMR spectrometer, is shown in FIG. 3.
Спектр соответствует 2,4-дихлорфеноксиуксусной кислоте с резонансными сигналами δ, м.д.: 6.869-6.886 (1Н, dm, Ar(С6Н)), 6.7227-7.245 (1H, dd, Ar(С5Н)), 7.461 (1H, d, Ar(C3H)), 4.633-4.641 (2Н, d, О-CH 2 -СООН).The spectrum corresponds to 2,4-dichlorophenoxyacetic acid with resonance signals δ, ppm: 6.869-6.886 (1H, dm, Ar (C 6 H)), 6.7227-7.245 (1H, dd, Ar (C 5 H)), 7.461 (1H, d, Ar (C 3 H)), 4.633-4.641 (2H, d, O — C H 2 —COOH).
Приведенный спектр однозначно доказывает образование 2,4-дихлорфеноксиуксусной кислоты.The spectrum presented unambiguously proves the formation of 2,4-dichlorophenoxyacetic acid.
Пример 7.Example 7.
Синтез 2,4-дихлорфеноксиуксусной кислоты из кальциевой соли феноксиуксусной кислоты.Synthesis of 2,4-dichlorophenoxyacetic acid from the calcium salt of phenoxyacetic acid.
При необходимости хлорировать можно не моногидрат кальциевой соли феноксиуксусной кислоты, а кальциевую соль феноксиуксусной кислоты.If necessary, it is possible to chlorinate not the monohydrate of the calcium salt of phenoxyacetic acid, but the calcium salt of phenoxyacetic acid.
Высушенный при 160°С моногидрат кальциевой соли феноксиуксусной кислоты теряет молекулу воды и становится кальциевой солью феноксиуксусной кислоты.Dried at 160 ° C monohydrate of the calcium salt of phenoxyacetic acid loses the water molecule and becomes the calcium salt of phenoxyacetic acid.
В круглодонную колбу, оборудованную перемешивающим устройством, барботером и термостатом, загружают 1000 мл воды и 205,42 г (0,60 моль) кальциевой соли феноксиуксусной кислоты. При включенной мешалке через барботер подают газообразный хлор при 20-25°С в течение 2,5 часа.A round bottom flask equipped with a stirrer, bubbler and thermostat is charged with 1000 ml of water and 205.42 g (0.60 mol) of the calcium salt of phenoxyacetic acid. With the stirrer turned on, chlorine gas is fed through the bubbler at 20-25 ° C for 2.5 hours.
После завершения реакции растворенный в реакционной массе хлор отдувают током азота.After the completion of the reaction, chlorine dissolved in the reaction mass is blown off with a stream of nitrogen.
Выпавший осадок центрифугируют и промывают 120 мл воды, и после сушки получают 258,05 г продукта, содержащего 99,5% 2,4-дихлорфеноксиуксусной кислоты и 0,5% монохлорфеноксиуксусных кислот. Выход 2,4-дихлорфеноксиуксусной кислоты составляет 96,8% от теоретического в пересчете на кальциевую соль феноксиуксусной кислоты.The precipitate formed is centrifuged and washed with 120 ml of water, and after drying, 258.05 g of a product containing 99.5% 2,4-dichlorophenoxyacetic acid and 0.5% monochlorophenoxyacetic acids are obtained. The yield of 2,4-dichlorophenoxyacetic acid is 96.8% of theoretical in terms of the calcium salt of phenoxyacetic acid.
С целью утилизации отходов производства образовавшийся в результате реакции хлористый кальций может быть возвращен в технологический процесс. Для этого после фильтрации моногидрата кальциевой соли феноксиуксусной кислоты, фильтрат подщелачивают гидроксидом натрия. При этом образуется гидроксид кальция и хлористый натрий:In order to dispose of production wastes, the calcium chloride formed as a result of the reaction can be returned to the technological process. For this, after filtration of the monohydrate of the calcium salt of phenoxyacetic acid, the filtrate is made alkaline with sodium hydroxide. This forms calcium hydroxide and sodium chloride:
СаС12+2NaOH → Са(ОН)2+2NaClCaCl 2 + 2NaOH → Ca (OH) 2 + 2NaCl
Однако фильтрат после синтеза кальциевой соли феноксиуксусной кислоты содержит органические примеси - кальциевые соли феноксиуксусной кислоты, фенола, оксиуксусной кислоты.However, the filtrate after the synthesis of the calcium salt of phenoxyacetic acid contains organic impurities - calcium salts of phenoxyacetic acid, phenol, oxyacetic acid.
При обработке фильтрата со стадии синтеза кальциевой соли феноксиуксусной кислоты гидроксидом натрия образуется натриевая соль фенолаWhen processing the filtrate from the stage of synthesis of the calcium salt of phenoxyacetic acid with sodium hydroxide, the sodium salt of phenol is formed
и натриевая соль феноксиуксусной кислотыand sodium salt of phenoxyacetic acid
СаС12+2NaOH → Са(ОН)2+2NaClCaCl 2 + 2NaOH → Ca (OH) 2 + 2NaCl
Образовавшийся гидроксид кальция отфильтровывают и возвращают на стадию синтеза кальциевой соли феноксиуксусной кислоты, а фильтрат подвергают фотохимическому озонированию в подходящем фотохимическом реакторе.The formed calcium hydroxide is filtered off and returned to the stage of synthesis of the calcium salt of phenoxyacetic acid, and the filtrate is subjected to photochemical ozonation in a suitable photochemical reactor.
После фильтрации гидроксида кальция в концентрате остается некоторое количество непрореагировавшего хлористого кальция, который может быть направлен в существующую систему очистки рассола, который возвращается в цех производства хлора. Очистку от ионов кальция проводят обычным способом - в рассол вводят раствор кальцинированной соды:After filtration of calcium hydroxide, a certain amount of unreacted calcium chloride remains in the concentrate, which can be sent to the existing brine purification system, which is returned to the chlorine production plant. Calcium ions are removed in the usual way - a solution of soda ash is introduced into the brine:
CaCl2+Na2CO3 → СаСО3+2NaClCaCl 2 + Na 2 CO 3 → CaCO 3 + 2NaCl
При этом растворимость СаСО3 при 40-50°С около 4-5 мг/л, что соответствует требованиям, предъявляемым к рассолам в производстве хлора диафрагменным способом.At the same time, the solubility of CaCO 3 at 40-50 ° C is about 4-5 mg / l, which meets the requirements for brines in the production of chlorine by the diaphragm method.
(https://chem21.info/page/177210234199166151151213102198236065169123199134).(https://chem21.info/page/177210234199166151151213102198236065169123199134).
В результате взаимного усиления озона и ультрафиолетового света происходит полная минерализация органики.. Протекающие химические реакции:As a result of mutual amplification of ozone and ultraviolet light, a complete mineralization of organic matter occurs. Proceeding chemical reactions:
Фильтрат после хлорирования кальциевой соли феноксиуксусной кислоты, содержащий некоторое количество 2,4-дихлорфеноксиуксусной кислоты, также обрабатывают гидроксидом натрия и подвергают фотохимическому озонированию.The filtrate after chlorination of the calcium salt of phenoxyacetic acid, containing some 2,4-dichlorophenoxyacetic acid, is also treated with sodium hydroxide and subjected to photochemical ozonation.
Требования к рассолу, направляемому на производство хлора при диафрагменном способе производства:Requirements for brine sent to chlorine production using diaphragm production:
(https://chem21.info/page/101128055038148249171089085009219147148076209048/).(https://chem21.info/page/101128055038148249171089085009219147148076209048/).
Образующиеся при синтезе кальциевой соли феноксиуксусной кислоты и хлорировании кальциевой соли феноксиуксусной кислоты водные растворы после отделения гидроксида кальция направляются в реактор фотолитического озонирования. Могут быть использованы реакторы, выпускаемые промышленностью, работающие на озоно-кислородной или озоно-воздушной смеси с УФ-облучением с длиной волны в диапазоне 170-280 мм. Озон под действием УФ-облучения образует активные ОН• радикалы, разрушающие органические соединения. Время прохождения обрабатываемого раствора через зону облучения должно быть достаточным для полной минерализации органических соединений (Rein Munter «Advanced Oxidution Processe-Current Status and Prospects» - Proc. Estonian Acid. Sci. Chem., 2001, 50, 2, 59-80).The aqueous solutions formed during the synthesis of the calcium salt of phenoxyacetic acid and the chlorination of the calcium salt of phenoxyacetic acid are sent to the photolytic ozonation reactor after separation of calcium hydroxide. Reactors produced by the industry, operating on an ozone-oxygen or ozone-air mixture with UV irradiation with a wavelength in the range of 170-280 mm, can be used. Ozone under the action of UV irradiation forms active OH • radicals that destroy organic compounds. The time of passage of the treated solution through the irradiation zone should be sufficient for the complete mineralization of organic compounds (Rein Munter "Advanced Oxidution Processe-Current Status and Prospects" - Proc. Estonian Acid. Sci. Chem., 2001, 50, 2, 59-80).
После фотокаталитического озонирования раствор поступает в газоотделительную систему. Газовая фаза, в составе которой имеется непрореагировавший озон, поступает в термокаталитический блок разложения озона для его деструкции до уровня предельно-допустимых значений при сбросе в атмосферу. Роль катализатора может выполнять, например, Гопталюм, или другой подходящий катализатор. Жидкая фаза проходит через каталитический фильтр, например, на основе гидроксида марганца, но не ограничивается им, для удаления растворенного озона.After photocatalytic ozonation, the solution enters the gas separation system. The gas phase, which contains unreacted ozone, enters the thermocatalytic ozone decomposition unit for its destruction to the level of maximum permissible values when discharged into the atmosphere. The role of the catalyst can be played, for example, by Goptalum, or another suitable catalyst. The liquid phase passes through a catalytic filter, such as but not limited to manganese hydroxide, to remove dissolved ozone.
После фотокаталитического озонирования в водном растворе хлорида натрия в небольших количествах образуется перекись водородаAfter photocatalytic ozonation in an aqueous solution of sodium chloride, hydrogen peroxide is formed in small amounts
О3+Н2О → Н2О2+О2 О 3 + Н 2 О → Н 2 О 2 + О 2
(М. Tozihi, М. Vahedpouz, F. Nazan, Journal of the Iranian Chemical Society, 7, 3, 585-596 (2010).(M. Tozihi, M. Vahedpouz, F. Nazan, Journal of the Iranian Chemical Society, 7, 3, 585-596 (2010).
Перекись разлагается достаточно медленно. Поэтому перед подачей водного раствора хлористого натрия в систему обратного осмоса, перекись водорода каталитически разрушаютPeroxide decomposes rather slowly. Therefore, before feeding an aqueous solution of sodium chloride to the reverse osmosis system, hydrogen peroxide is catalytically destroyed
2H2O2 → 2H2O+O2 2H 2 O 2 → 2H 2 O + O 2
в контактном аппарате, содержащем, например, гидроксид марганца или другой подходящий катализатор.in a contact apparatus containing, for example, manganese hydroxide or other suitable catalyst.
При озонировании происходит полное окисление органических молекул, а с хлористым натрием озон не реагирует.(Доклады Академии наук, 2010, том 434, №4, с. 493-495. Физическая химия).During ozonation, organic molecules are completely oxidized, and ozone does not react with sodium chloride (Doklady Akademii Nauk, 2010, vol. 434, no. 4, pp. 493-495. Physical chemistry).
При анализе сточной воды после фотохимического озонирования с помощью ВЭЖХ HITACHI "Chromaster" на хроматографической колонке с обращенной фазой и УФ-детектором органических веществ не обнаружено.When analyzing waste water after photochemical ozonation using HPLC HITACHI "Chromaster" on a chromatographic column with a reversed phase and a UV detector, organic substances were not detected.
Образовавшийся водный раствор хлористого натрия, имеющий соответствующее осмотическое давление, подвергают обратному осмосу при давлении, необходимом для получения раствора хлористого натрия с концентрацией около 100 г/литр.The resulting aqueous solution of sodium chloride, having a corresponding osmotic pressure, is subjected to reverse osmosis at the pressure required to obtain a solution of sodium chloride with a concentration of about 100 g / liter.
После системы обратного осмоса пермеат (чистая вода) возвращается в технологический процесс на стадию отмывки кальциевой соли феноксиуксусной кислоты или промывки 2,4-дихлорфеноксиуксусной кислоты, а концентрат (10%-ный водный раствор хлористого натрия) возвращается в отделение приготовления водного раствора хлористого натрия необходимой концентрации и далее в цех производства хлора:After the reverse osmosis system, the permeate (pure water) returns to the technological process to the stage of washing the calcium salt of phenoxyacetic acid or
Для системы обратного осмоса могут быть применены любые подходящие агрегаты и устройства, например, плунжерные насосы высокого давления, например, PRATISSOLI, но не ограниченные ими.For a reverse osmosis system, any suitable units and devices can be used, for example, high pressure plunger pumps, for example, PRATISSOLI, but not limited to them.
При промышленном производстве хлора основными статьями затрат являются электроэнергия и сырье - хлористый натрий.In the industrial production of chlorine, the main cost items are electricity and raw materials - sodium chloride.
Кроме того, в процессе электролиза расход воды также значителен, что обусловлено ее электролитическим разложением, а также получением раствора гидроксида натрия. Поэтому для ресурсосбережения важное значение имеет возврат раствора хлористого натрия в производство хлора.In addition, in the process of electrolysis, the consumption of water is also significant, which is due to its electrolytic decomposition, as well as the production of a sodium hydroxide solution. Therefore, for resource conservation, it is important to return the sodium chloride solution to the chlorine production.
Водный раствор хлористого натрия после фотолитического озонирования и блока обратного осмоса может быть возвращен в существующую систему очистки питающего рассола хлорного производства.The aqueous solution of sodium chloride after photolytic ozonation and the reverse osmosis unit can be returned to the existing system of purification of the feed brine of the chlorine production.
Согласно закону Вант-Гоффа осмотическое давление, кПа:According to Van't Hoff's law, osmotic pressure, kPa:
гдеwhere
i - коэффициент Вант-Гоффа (для хлористого натрия = 2)i - Van't Hoff coefficient (for sodium chloride = 2)
R - универсальная газовая постоянная, равная 8,31 дж/моль ⋅ КR - universal gas constant equal to 8.31 J / mol ⋅ K
Т - температура растворенного вещества, КT is the temperature of the solute, K
С - концентрация растворенного вещества, г/дм3 С - concentration of solute, g / dm 3
М - масса одного моля растворенного веществаM is the mass of one mole of a solute
(для хлористого натрия = 58,5)(for sodium chloride = 58.5)
Для получения концентрации водного раствора хлористого натрия 100 г/дм3 To obtain a concentration of an aqueous solution of sodium chloride 100 g / dm 3
В этом случае могут применяться подходящие высоконапорные мембраны, например FILMTECCW30XLE - 440С с рабочим давлением до 83 бар и степени селективности 99,7% по хлористому натрию.In this case, suitable high-pressure diaphragms can be used, for example FILMTECCW30XLE - 440C with an operating pressure of up to 83 bar and a selectivity of 99.7% for sodium chloride.
Схема наиболее энергоэффективной установки обратного осмоса может быть оснащена любыми подходящими водяными насосами, например, PRATISSOLI серии КТ с рабочим давлением от 80 бар и выше.The scheme of the most energy efficient reverse osmosis plant can be equipped with any suitable water pump, for example, PRATISSOLI KT series with operating pressures of 80 bar and above.
Основным методом определения содержания органических примесей в сточных водах является химическое потребление кислорода (ХПК) с помощью бихромата калия в качестве окислителя.The main method for determining the content of organic impurities in wastewater is chemical oxygen demand (COD) using potassium dichromate as an oxidizing agent.
Однако, присутствующий в водном растворе хлористый натрий во время анализа с участием серной кислоты (ГОСТ 31859-2012) будет выделять хлористый водород, окисляющийся под действием бихромата калия:However, sodium chloride present in the aqueous solution during the analysis with the participation of sulfuric acid (GOST 31859-2012) will release hydrogen chloride, which is oxidized under the action of potassium dichromate:
14HCl+K2Cr2O7 → 3Cl2+2CrCl3+2KCl+7H2O14HCl + K 2 Cr 2 O 7 → 3Cl 2 + 2CrCl 3 + 2KCl + 7H 2 O
При этом будет ложно-положительный анализ даже в отсутствии органических примесей.In this case, there will be a false-positive analysis even in the absence of organic impurities.
Анализ содержания органических примесей в воде после фотолитического озонирования фильтратов и каталитического разрушения озона проводили с помощью ВЭЖХ HITACHI "Chromaster" на хроматографической колонке с обращенной фазой и УФ-детектором. Остаточное содержание органических примесей в обработанной воде составило 420-630 мкГ/литр в пересчете на фенол.The analysis of the content of organic impurities in water after photolytic ozonation of filtrates and catalytic destruction of ozone was carried out using HPLC HITACHI "Chromaster" on a chromatographic column with a reversed phase and UV detector. The residual content of organic impurities in the treated water was 420-630 μG / liter in terms of phenol.
Таким образом, технологический процесс получения 2,4-дихлорфеноксиуксусной кислоты является безотходным.Thus, the technological process for producing 2,4-dichlorophenoxyacetic acid is waste-free.
Безотходный технологический процесс получения 2,4-дихлорфеноксиуксусной кислоты поясняется блок-схемой, представленной на фиг. 4.The waste-free technological process for producing 2,4-dichlorophenoxyacetic acid is illustrated by the block diagram shown in FIG. 4.
Claims (1)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2020116391A RU2757739C1 (en) | 2020-04-28 | 2020-04-28 | Method for synthesising 2,4-dichlorophenoxyacetic acid |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2020116391A RU2757739C1 (en) | 2020-04-28 | 2020-04-28 | Method for synthesising 2,4-dichlorophenoxyacetic acid |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2757739C1 true RU2757739C1 (en) | 2021-10-21 |
Family
ID=78289496
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2020116391A RU2757739C1 (en) | 2020-04-28 | 2020-04-28 | Method for synthesising 2,4-dichlorophenoxyacetic acid |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2757739C1 (en) |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2107061C1 (en) * | 1996-04-18 | 1998-03-20 | Уфимское государственное производственное предприятие "Химпром" | Method for production of 2,4-dichlorophenoxyacetic acid |
| CN105622396A (en) * | 2014-10-27 | 2016-06-01 | 浙江新安化工集团股份有限公司 | 2,4-dichlorophenoxyacetic acid preparation method |
| RU2684114C1 (en) * | 2018-10-16 | 2019-04-04 | Борис Павлович Струнин | Method for producing 2,4-dichlorophenoxyacetic acid |
-
2020
- 2020-04-28 RU RU2020116391A patent/RU2757739C1/en active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2107061C1 (en) * | 1996-04-18 | 1998-03-20 | Уфимское государственное производственное предприятие "Химпром" | Method for production of 2,4-dichlorophenoxyacetic acid |
| CN105622396A (en) * | 2014-10-27 | 2016-06-01 | 浙江新安化工集团股份有限公司 | 2,4-dichlorophenoxyacetic acid preparation method |
| RU2684114C1 (en) * | 2018-10-16 | 2019-04-04 | Борис Павлович Струнин | Method for producing 2,4-dichlorophenoxyacetic acid |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Adimurthy et al. | Eco-friendly and versatile brominating reagent prepared from a liquid bromine precursor | |
| CN112299983B (en) | 3, 6-Dichloro salicylic acid compounds and related methods of synthesis | |
| US3658921A (en) | Process for production of halonitro alcohols | |
| RU2757739C1 (en) | Method for synthesising 2,4-dichlorophenoxyacetic acid | |
| RU2684114C1 (en) | Method for producing 2,4-dichlorophenoxyacetic acid | |
| CN104926661A (en) | Synthetic method for bronopol | |
| HU193589B (en) | Process for preparing fluorinated phtaloyl- and terephtaloyl compounds | |
| JPS6312855B2 (en) | ||
| JPS58116435A (en) | Preparation of 4-hydroxy-2,4,6-trimethylcyclohexa-2, 5-dien-1-one | |
| EP0202838B1 (en) | Process for production of m-phenoxybenzyl alcohol | |
| US3624157A (en) | Process for preparing ortho-chlorobenzaldehyde | |
| EP0713856A1 (en) | Process for preparing brominated or chlorinated aromatic carboxylic acids | |
| EP0002373A1 (en) | A method of making 2,4,5-trichlorophenol | |
| CN101200430A (en) | Improved method for synthesizing bronopol | |
| US4242523A (en) | Process for the preparation of para-nitroso-diphenyl-hydroxylamines | |
| JP2514368B2 (en) | Method for producing hexafluoroacetone or its hydrate | |
| KR900003299B1 (en) | Process for the preparation of perfluoro alkane carboxylic acids | |
| WO1990009979A1 (en) | Methods for the preparation of brominated intermediates | |
| EP0321857B1 (en) | Process for preparing aromatic hydroxycarboxylic acids | |
| JPH0549654B2 (en) | ||
| CN109081826B (en) | Preparation method of oxidant IBX | |
| US20050182274A1 (en) | Method for the production of 2,4,5-trimethylphenyl acetic acid | |
| KR0124964B1 (en) | Process for carboxybenzaldehyde from residue of dimethylterephthalate | |
| RU2082711C1 (en) | Method of synthesis of 4-chlorophenoxyacetic or 2,4-dichlorophenoxyacetic acid | |
| JPS61118333A (en) | Production of perfluoroallyl chloride |