RU2659032C1 - Способ модификации гентамицина сополимером винилпирролидона с диацеталем акролеина - Google Patents
Способ модификации гентамицина сополимером винилпирролидона с диацеталем акролеина Download PDFInfo
- Publication number
- RU2659032C1 RU2659032C1 RU2017114890A RU2017114890A RU2659032C1 RU 2659032 C1 RU2659032 C1 RU 2659032C1 RU 2017114890 A RU2017114890 A RU 2017114890A RU 2017114890 A RU2017114890 A RU 2017114890A RU 2659032 C1 RU2659032 C1 RU 2659032C1
- Authority
- RU
- Russia
- Prior art keywords
- gentamicin
- sovial
- bonds
- copolymer
- azomethine
- Prior art date
Links
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 title claims abstract description 71
- 229930182566 Gentamicin Natural products 0.000 title claims abstract description 69
- 238000000034 method Methods 0.000 title claims abstract description 32
- 229920001577 copolymer Polymers 0.000 title claims abstract description 29
- 230000004048 modification Effects 0.000 title claims description 5
- 238000012986 modification Methods 0.000 title claims description 5
- 229960002518 gentamicin Drugs 0.000 claims abstract description 68
- HGINCPLSRVDWNT-UHFFFAOYSA-N Acrolein Chemical group C=CC=O HGINCPLSRVDWNT-UHFFFAOYSA-N 0.000 claims abstract description 27
- 125000003172 aldehyde group Chemical group 0.000 claims abstract description 13
- 230000015572 biosynthetic process Effects 0.000 claims abstract description 13
- 239000000126 substance Substances 0.000 claims abstract description 10
- 230000000845 anti-microbial effect Effects 0.000 claims abstract description 9
- 238000005903 acid hydrolysis reaction Methods 0.000 claims abstract description 4
- 230000006698 induction Effects 0.000 claims abstract 2
- 230000003115 biocidal effect Effects 0.000 claims description 15
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 claims description 10
- 239000011780 sodium chloride Substances 0.000 claims description 5
- 230000000844 anti-bacterial effect Effects 0.000 claims description 4
- 239000012535 impurity Substances 0.000 claims description 4
- 241000283973 Oryctolagus cuniculus Species 0.000 claims description 3
- 229920005654 Sephadex Polymers 0.000 claims description 3
- 239000012507 Sephadex™ Substances 0.000 claims description 3
- 229910052739 hydrogen Inorganic materials 0.000 claims description 3
- 239000001257 hydrogen Substances 0.000 claims description 3
- 238000002523 gelfiltration Methods 0.000 claims description 2
- 238000003786 synthesis reaction Methods 0.000 claims description 2
- 238000012546 transfer Methods 0.000 claims description 2
- 238000011026 diafiltration Methods 0.000 claims 1
- 238000000746 purification Methods 0.000 claims 1
- 239000002699 waste material Substances 0.000 claims 1
- 239000000203 mixture Substances 0.000 abstract description 13
- 239000003814 drug Substances 0.000 abstract description 11
- 238000004519 manufacturing process Methods 0.000 abstract description 11
- 125000003277 amino group Chemical group 0.000 abstract description 8
- 230000000694 effects Effects 0.000 abstract description 6
- 230000008569 process Effects 0.000 abstract description 4
- 230000002035 prolonged effect Effects 0.000 abstract description 2
- 239000000243 solution Substances 0.000 description 23
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 13
- 238000011534 incubation Methods 0.000 description 12
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 10
- 229940079593 drug Drugs 0.000 description 10
- RDEIXVOBVLKYNT-VQBXQJRRSA-N (2r,3r,4r,5r)-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,6s)-3-amino-6-(1-aminoethyl)oxan-2-yl]oxy-2-hydroxycyclohexyl]oxy-5-methyl-4-(methylamino)oxane-3,5-diol;(2r,3r,4r,5r)-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,6s)-3-amino-6-(aminomethyl)oxan-2-yl]o Chemical compound OS(O)(=O)=O.O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC[C@@H](CN)O2)N)[C@@H](N)C[C@H]1N.O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC[C@H](O2)C(C)N)N)[C@@H](N)C[C@H]1N.O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N RDEIXVOBVLKYNT-VQBXQJRRSA-N 0.000 description 7
- 239000003242 anti bacterial agent Substances 0.000 description 7
- 229940088710 antibiotic agent Drugs 0.000 description 7
- 230000003993 interaction Effects 0.000 description 7
- 229920000642 polymer Polymers 0.000 description 7
- 238000001228 spectrum Methods 0.000 description 7
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- ZETHHMPKDUSZQQ-UHFFFAOYSA-N Betulafolienepentol Natural products C1C=C(C)CCC(C(C)CCC=C(C)C)C2C(OC)OC(OC)C2=C1 ZETHHMPKDUSZQQ-UHFFFAOYSA-N 0.000 description 5
- HEOKFDGOFROELJ-UHFFFAOYSA-N diacetal Natural products COc1ccc(C=C/c2cc(O)cc(OC3OC(COC(=O)c4cc(O)c(O)c(O)c4)C(O)C(O)C3O)c2)cc1O HEOKFDGOFROELJ-UHFFFAOYSA-N 0.000 description 5
- 238000005516 engineering process Methods 0.000 description 5
- 229910000033 sodium borohydride Inorganic materials 0.000 description 5
- 239000012279 sodium borohydride Substances 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- 231100000419 toxicity Toxicity 0.000 description 5
- 230000001988 toxicity Effects 0.000 description 5
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 4
- PCSMJKASWLYICJ-UHFFFAOYSA-N Succinic aldehyde Chemical compound O=CCCC=O PCSMJKASWLYICJ-UHFFFAOYSA-N 0.000 description 4
- 238000004364 calculation method Methods 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- LDHQCZJRKDOVOX-NSCUHMNNSA-N crotonic acid Chemical compound C\C=C\C(O)=O LDHQCZJRKDOVOX-NSCUHMNNSA-N 0.000 description 4
- 239000000499 gel Substances 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- LDHQCZJRKDOVOX-UHFFFAOYSA-N trans-crotonic acid Natural products CC=CC(O)=O LDHQCZJRKDOVOX-UHFFFAOYSA-N 0.000 description 4
- 229920001817 Agar Polymers 0.000 description 3
- 230000004913 activation Effects 0.000 description 3
- 239000008272 agar Substances 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- 239000000969 carrier Substances 0.000 description 3
- 238000007385 chemical modification Methods 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 238000010668 complexation reaction Methods 0.000 description 3
- 238000011084 recovery Methods 0.000 description 3
- 238000000108 ultra-filtration Methods 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- 238000004566 IR spectroscopy Methods 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- DDTDNCYHLGRFBM-YZEKDTGTSA-N chembl2367892 Chemical compound CC(=O)N[C@H]1[C@@H](O)[C@H](O)[C@H](CO)O[C@H]1O[C@@H]([C@H]1C(N[C@@H](C2=CC(O)=CC(O[C@@H]3[C@H]([C@H](O)[C@H](O)[C@@H](CO)O3)O)=C2C=2C(O)=CC=C(C=2)[C@@H](NC(=O)[C@@H]2NC(=O)[C@@H]3C=4C=C(O)C=C(C=4)OC=4C(O)=CC=C(C=4)[C@@H](N)C(=O)N[C@H](CC=4C=C(Cl)C(O5)=CC=4)C(=O)N3)C(=O)N1)C(O)=O)=O)C(C=C1Cl)=CC=C1OC1=C(O[C@H]3[C@H]([C@@H](O)[C@H](O)[C@H](CO)O3)NC(C)=O)C5=CC2=C1 DDTDNCYHLGRFBM-YZEKDTGTSA-N 0.000 description 2
- 238000002512 chemotherapy Methods 0.000 description 2
- 238000010494 dissociation reaction Methods 0.000 description 2
- 230000005593 dissociations Effects 0.000 description 2
- 239000003657 drainage water Substances 0.000 description 2
- 238000002329 infrared spectrum Methods 0.000 description 2
- 208000004396 mastitis Diseases 0.000 description 2
- OKPYIWASQZGASP-UHFFFAOYSA-N n-(2-hydroxypropyl)-2-methylprop-2-enamide Chemical compound CC(O)CNC(=O)C(C)=C OKPYIWASQZGASP-UHFFFAOYSA-N 0.000 description 2
- 235000015097 nutrients Nutrition 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 239000000377 silicon dioxide Substances 0.000 description 2
- 235000012239 silicon dioxide Nutrition 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- 238000013519 translation Methods 0.000 description 2
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- VUOPFFVAZTUEGW-SRXUPNLNSA-N 32p08cbb99 Chemical compound C=1C([C@@H]2C(=O)N[C@@H]([C@@H](C3=CC=C(C=C3)OC=3C=C4C=C(C=3O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@@H](CO[C@H]5[C@@H]([C@H](O)[C@@H](O)[C@H](C)O5)O)O3)O[C@@H]3[C@H]([C@@H](O)[C@H](O)[C@@H](CO)O3)O[C@H]3[C@H]([C@H](O)[C@H](O)CO3)O)OC3=CC=C(C=C3)[C@@H](O)[C@@H]3C(=O)N[C@@H](C=5C=C(C(=C(O)C=5)C)OC=5C(O)=CC=C(C=5)[C@@H](N)C(=O)N3)C(=O)N[C@H]4C(=O)N2)O[C@@H]2O[C@@H](C)[C@H](O)[C@H](N)C2)C(=O)N[C@@H](C2=CC(O)=C3)C(=O)OC)=CC=C(O)C=1C2=C3O[C@@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@@H]1O VUOPFFVAZTUEGW-SRXUPNLNSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 229930186147 Cephalosporin Natural products 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 1
- 102000015636 Oligopeptides Human genes 0.000 description 1
- 108010038807 Oligopeptides Proteins 0.000 description 1
- 108010053950 Teicoplanin Proteins 0.000 description 1
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- -1 acrolein diacetal Chemical class 0.000 description 1
- 238000007792 addition Methods 0.000 description 1
- 230000009435 amidation Effects 0.000 description 1
- 238000007112 amidation reaction Methods 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 229940126574 aminoglycoside antibiotic Drugs 0.000 description 1
- 239000002647 aminoglycoside antibiotic agent Substances 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- RHRAMPXHWHSKQB-GGEUKFTFSA-N betamicin Chemical class O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CN)O2)O)[C@@H](N)C[C@H]1N RHRAMPXHWHSKQB-GGEUKFTFSA-N 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- 210000002421 cell wall Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 229940124587 cephalosporin Drugs 0.000 description 1
- 150000001780 cephalosporins Chemical class 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000005595 deprotonation Effects 0.000 description 1
- 238000010537 deprotonation reaction Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 229960000633 dextran sulfate Drugs 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- IUNMPGNGSSIWFP-UHFFFAOYSA-N dimethylaminopropylamine Chemical compound CN(C)CCCN IUNMPGNGSSIWFP-UHFFFAOYSA-N 0.000 description 1
- 239000002158 endotoxin Substances 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000009036 growth inhibition Effects 0.000 description 1
- 229920001480 hydrophilic copolymer Polymers 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 229920006008 lipopolysaccharide Polymers 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 238000002715 modification method Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 239000005543 nano-size silicon particle Substances 0.000 description 1
- 230000017066 negative regulation of growth Effects 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 150000003961 organosilicon compounds Chemical group 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229920000447 polyanionic polymer Polymers 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- KJASTBCNGFYKSR-UHFFFAOYSA-N prop-2-enehydrazide Chemical compound NNC(=O)C=C KJASTBCNGFYKSR-UHFFFAOYSA-N 0.000 description 1
- 239000012429 reaction media Substances 0.000 description 1
- 238000012827 research and development Methods 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 108010062729 ristocetin A Proteins 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical class CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 1
- 230000035322 succinylation Effects 0.000 description 1
- 238000010613 succinylation reaction Methods 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 229960001608 teicoplanin Drugs 0.000 description 1
- 231100000048 toxicity data Toxicity 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7034—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin
- A61K31/7036—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin having at least one amino group directly attached to the carbocyclic ring, e.g. streptomycin, gentamycin, amikacin, validamycin, fortimicins
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Molecular Biology (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Изобретение относится к применимому в биологической и медицинской промышленности способу изготовления гентамицина, модифицированного совиалем. Предложенный способ основан на индукции альдегидных групп в составе совиаля за счет кислотного гидролиза акролеинового звена и формировании азометиновых связей между альдегидными группами сополимера и депротонированными аминогруппами гентамицина. Предложенный способ позволяет получить стабильный обладающий пролонгированным антимикробным действием конъюгат гентамицина и совиаля, сформированный за счет азометиновых связей, способный диссоциировать на исходные компоненты. 6 з.п. ф-лы, 8 табл., 4 ил., 1 пр.
Description
Изобретение относится к биотехнологической или медицинской промышленности, в частности, к способу синтеза совиаля (сополимера винилпирролидона с диацеталем акролеина), модифицированного гентамицином (аминогликозидный антибиотик) за счет формирования азометиновых или одинарных ковалентных связей.
Известные научно-технические решения направлены на: (1) преодоление антибиотико-резистентности микроорганизмов; (2) повышение специфической активности и увеличение спектра противомикробного действия; (3) снижение токсичности действующего начала и увеличение периода его полувыведения из организма реципиента.
На современном этапе развития науки и техники возможно выделить два основных направления исследований и разработок, ориентированных на решение указанных выше задач:
- во-первых, создание комплексов антибиотик-носитель на основе нековалентных связей без изменения структуры действующего начала;
- во-вторых, модификация антибиотика с изменением его структуры и на основе формирования прочных ковалентных связей в составе химерного конъюгата, сохранившего противомикробную активность.
Известен способ повышения фармакологической активности и снижения уровня побочных эффектов, если в качестве носителя используется диоксид кремния, а технология изготовления лекарственного средства основана на принципах механохимии для обеспечения супрамолекулярного состояния. Способ апробирован для изготовления супрамолекулярных систем на основе антибиотиков из группы цефалоспоринов [1. Душкин А.В. // Фундаментальные исследования. 2012. №4 (часть 1). С. 47-52]. Механохимическая технология с использованием диоксида кремния рассматривается как перспективный технологический подход, позволяющий увеличить антибактериальную активность и снизить токсический эффект, поскольку бактерицидный эффект достигается за счет многократного увеличения площади адсорбционного взаимодействия, занимаемой наночастицами кремния, нагруженными антибиотиком.
Известен способ изготовления препарата диеномаст, в состав которого входит гентамицин, диоксидин и масляная основа, обеспечивающая пролонгирующий эффект за счет постепенного всасывания антибиотика [2. Инструкция по применению ДиеномастаАФ для лечения мастита у коров, регистрационный номер ПВР-2-0.2/01043, ЗАО НПП Агрофарм].
Известен способ изготовления препарата гентам на основе гентамицина и амоксициклина, выпускаемый в форме суспензии [3. Инструкция по применению препарата ГЕНТАМ, регистрационный номер ПВР-3-2.1/02697, ООО НПО «АПИ-САН»].
Известен способ изготовления препарата гентоксан, представляющего собой комплекс гентамицина сульфата, производных цинка и триптофана на основе координационных связей в составе кремнийорганического соединения [4. Инструкция по медицинскому применению лекарственного средства ГентаСЕПТ, регистрационный номер UA/1279/01/01, ПАО НПЦ «Борщаговский химико-фармацевтический завод»].
Перечисленные выше технические решения направлены на создание пролонгированного лекарственного средства, предназначенного в основном для наружного применения. Технологические нововведения на основе указанных решений в принципе не предназначены для производства инъекционных форм антибиотиков. В частности, комплексообразование во всех перечисленных формах гентамицинсодержащих препаратов реализуется за счет слабых нековалентных взаимодействий.
Заслуживают особого внимания результаты прикладных исследований, нацеленных на создание комплексов антибиотиков на основе синтетических (со)полимеров.
Опубликован способ модификации гентамицина и канамицина путем ковалентного присоединения их к сополимеру N-(2-гидроксипропил) метакриламида с N-метакроильным производным олигопептидов с помощью биорасщепляющего спейсера, имеющего структуру - Гли-Лей-Гли. При этом полученные производные обладают высоким уровнем антимикробной активности in vitro [5. Назарова О.В. // Прикладная химия. 1993. №3. С. 193-197]. Однако, нет данных о токсичности и биосовместимости полимера-носителя. Собственно способ модификации трудоемок и требует дорогостоящих реагентов, в частности аминокислот и пептидов. Способ может быть реализован только в лабораторном масштабе.
Опубликован способ ковалентного присоединения гентамицина с помощью азометиновой связи к диальдегиддекстрану [6. Хомяков К.П. и соавт. // Известия вузов. Химия и химическая технология. 1979. №10. С. 1267-1271]. Производное сохраняло высокий уровень антибиотической активности, хотя в состав конъюгата гентамицин-носитель вошло не более 34,8 масс % антибиотика. Также не приводятся данные о токсичности синтезированного комплекса и токсичности полимера-носителя, содержащего высокую концентрацию альдегидных групп.
Наиболее перспективными искусственными носителями являются сополимеры N-винил-2-пирролидона (ВП), благодаря их амфифильности и способности к комплексообразованию в качестве носителей и пролонгаторов лекарственных средств [7. Панарин Е.Ф., Лавров Н.А., Соловский М.В., Шальнова Л.И. Полимеры-носители биологически активных веществ. СПб: Профессия. 2014. 304 с].
Известны способы нековалентного и ковалентного связывания лекарственных средств с гидрофильными сополимерами ВП [8. Соловский М.В., Никольская Н.В. // Химико-фармацевтический журнал. 2000. Т. 34. №11. С. 21-24].
При инкубировании гентамицина с сополимерами ВП и кротоновой кислоты (или n-кротонил-аминофенилуксусной кислоты) нековалентное связывание достигается за счет ионного взаимодействия карбоксильных групп в составе полимерных цепей с положительно заряженными аминогруппами антибиотика [9. Соловский М.В., Еропкин М.Ю., Еропкина Е.М., Киселев О.И., Панарин Е.Ф., Гаврилова И.И., Шульцева Е.Л. Патент РФ №2335510. БИ №28. 2008]. По-видимому, наивысший уровень связывания гентамицина с сополимерами ВП достигается также за счет формирования водородных связей, о чем свидетельствуют результаты равновесного диализа сополимернопроизводных форм гентамицина в воде и в физиологическом растворе.
Недостатком известного метода является стадия перевода гентамицин-сульфата в гентамицин-основание. Из-за процесса диссоциации комплекса гентамицин-сополимер ВП на исходные компоненты реакционную среду подвергают лиофильной сушке.
Описан способ связывания гентамицина с сополимерами N-винилпирролидона и кротоновой кислоты или n-кротоноиламино-феноксиуксусной кислоты [10. Соловский М.В. // Антибиотики и химиотерапия. 2000. №6. с. 10-12]. Конечные продукты сохраняют высокий уровень антимикробной активности. Их токсичность по величине LD50 снижалась по сравнению с таковой у нативной формы гентамицина [10].
Известны исследовательские подходы по созданию комплексов гентамицина с полимерными сульфосодержащими анионами. На основе сополимеров акриламида с 2-акриламид-2-метилсульфоновой кислотой и N-2-гидроксипропилметакриламида с акриловой кислотой и декстрансульфатом были получены комплексы с гентамицином. Гентамицин в составе полианионов сохраняет высокую антибактериальную активность, в т.ч. конъюгат проявляет вироцидный эффект.
Известен способ получения модифицированных водорастворимых сополимеров [11. Панарин Е.Ф. и соавт. // авт. свид. СССР №431185. БИ №28]. В соответствии с данным способом получено азометиновое производное стрептомицина и сополимера N-винилпирролидона с виниламидом или с гидразидом акриловой кислоты. Установлено, что синтезированные комплексы обладают высоким уровнем антимикробной активности. Однако данные о токсичности конечных продуктов не приводятся. Полагают, что наличие аминогрупп в составе сополимерных носителей будет содействовать увеличению токсического эффекта синтезированного комплекса.
Известны способы химической модификации антибиотиков за счет изменения химической структуры действующего начала.
Из тейкопланина получены антибиотики MDL 62708 и MDL 62766 за счет амидирования концевой карбоксильной группировки диметиламинопропиламином. Установлено, что производное тейкопланина способно преодолевать природную резистентность грамотрицательных бактерий за счет увеличения проницаемости наружных липополисахаридных слоев клеточной стенки [12. Смирнова И.Г. и соавт. // Вестник Московского университета. Т. 41 (Серия 2). 2000].
Известны методы химической модификации антибиотиков пептидной группы. При сохранении циклической структуры действующего начала объектами модификации могут быть сложноэфирные связи, α-аминогруппы, гидрофобное ядро и аминокислотные остатки. За счет сукцинилирования ристомицина А удалось снизить нежелательные действия антибиотика [12].
Известен способ изготовления изепамицина - производного гентамицина В - химической модификацией природного антибиотика за счет ацилирования аминогруппы, находящейся в первом положении остатка дезоксистрептомицина. Изепамицин оказался более устойчив к действию аминогликозидмодифицирующих ферментов [13. Ч.Х. Танн и др. Способ получения изепамицина и промежуточные соединения // авт. свид. №2120444].
К обобщенным недостаткам известных методов относится или невозможность на их основе изготовить инъекционную форму антибиотика или необходимость дополнительного синтеза сополимерного носителя с надлежащими сорбционными свойствами, или нестабильность изготовленного комплекса на основе слабых физических связей, или химическая модификация антибиотика, не позволяющая обсуждать пролонгирующие свойства нового продукта, т.к. химическая модификация достигается за счет связывания действующего начала антибиотика с низкомолекулярными носителями (амидирование, сукцинилирование, карбоксилирование и т.д.).
Наиболее близким техническим решением является способ нековалентной модификации гентамицина сополимерами N-винил-2-пирролидона [10], которые как носители обладают необходимыми физико-химическими и физиологическими свойствами. За счет карбоксилсодержащих сополимеров N-винилпирролидона с кротоновой кислотой удалось создать комплекс с гентамицином на основе нековалентного связывания и формирования ионной сшивки, включая водородные связи. Вместе с тем нековалентное комплексообразование для технологически ориентированных решений не позволяет в объективных количественных критериях оценивать показатели качества перспективной субстанции гентамицина в составе сополимерного носителя на основе поливинилпирролидона и кротоновой кислоты. Опубликованное научно-техническое решение требует дополнительных стадий, касающихся перевода гентамицина сульфата в основание гентамицина и модификации комплекса гентамицина и сополимера из-за его диссоциации на исходные компоненты.
Задача изобретения состоит в создании комплексов с различными уровнями стабильности на основе гентамицина и сополимера винилпирролидона за счет формирования азометиновых или ковалентных связей между антибиотиком и сополимерным носителем с молекулярной массой 33 кДа.
Поставленная задача решается за счет использования сополимера винилпирролидона с диацеталем акролеина (коммерческое название Совиаль), имеющего средневзвешенную молекулярную массу в пределах 30 кДа, в составе которого акролеиновое звено занимает около 14 или 16% [14. Панарин Е.Ф., Гаврилова И.И. // авт. свид. №560425. БИ №47; 15. Аникина Т.Б., Панарин Е.Ф. // авт. свид. №522198. БИ №27]. Индукцию альдегидных групп в составе совиаля осуществляли кислотным гидролизом в 0,1 моль/л растворе соляной кислоты в течение двух часов на кипящей водяной бане. Взаимодействие активированного кислотным гидролизом совиаля и гентамицина осуществляли за счет формирования азометиновых связей и перевода их в прочные ковалентные -CH-N- с помощью боргидрида натрия в условиях депротонирования реакционно-способных аминогрупп антибиотика.
Изложенный подход апробирован с использованием серийно выпускаемых инъекционных форм гентамицина сульфата и образцов совиаля.
Из анализа современного уровня научно-технических решений следует, что в реакциях белок-белок или белок-полимер достаточно часто используется принцип формирования азометиновых связей и последующий их перевод в прочные ковалентные. Для синтеза таких полимерных структур выбираются соразмерные по конформации и массе макромолекулы, а их соотношение подчиняется требованиям эквимолярности с учетом сохранения целевой функциональной активности в составе сформировавшегося производного.
Техническое решение изобретения взаимовложено в действующие регламенты на производство гентамицина. Дополнения и изменения, предусмотренные техническим решением, касаются конечных стадий производства гентамицина и не требуют существенных затрат.
Пример реализации предлагаемого способа
Стадия 1. Кислотный гидролиз акролеинового звена совиаля. Готовят раствор совиаля в 0,1 моль/л растворе соляной кислоты. Для этого в лабораторном варианте в стеклянную пробирку объемом 25 мл вносят 8 мл 0,1 моль/л раствора соляной кислоты и добавляют 400 мг порошка совиаля. После растворения навески раствор совиаля в соляной кислоте выдерживают в течение 2 часов на кипящей водяной бане.
Стадия 2. Формирование инкубационной среды. Раствор совиаля в соляной кислоте охлаждают до комнатной температуры (18±4)°С и добавляют 2,2 мл 4% раствора гентамицина, серийное производство которого в форме инъекционного лекарственного средства осуществляет Борисовский завод медицинских препаратов (Беларусь). Полученный раствор, содержащий совиаль и гентамицин, при кислом значении рН перемешивают на магнитной мешалке в течение 10-15 минут.
Расчет необходимого количества антибиотика проводили на основе следующих допущений:
а) при активации все акролеиновые звенья образуют альдегидную группу (следовательно, количество акролеиновых звеньев равно количеству альдегидных групп в молекуле совиаля после активации);
б) количество реакционноспособных аминогрупп на молекуле гентамицина может быть от 1 до 3.
Мольные соотношения гентамицин/совиаль в инкубационной среде могут быть представлены из расчета:
a) мольных соотношений соответственно n молей гентамицина на m молей совиаля;
b) мольных соотношений n молей гентамицина на 1 моль альдегидных групп в составе 1 моля активированного совиаля.
Взаимодействие аминогрупп гентамицина и альдегидных групп совиаля описывается схемой:
-NH2+O=СН-→-N=CH-+Н2O
Коммерческий препарат сополимера винилпирролидона с диацеталем акролеина (совиаль) характеризуется средневзвешенной молекулярной массой и величиной мольного процента акролеиновых звеньев. Совиаль, используемый в работе, имеет молекулярную массу 33 кДа и мольный процент акролеиновых звеньев 16%. Препарат гентамицина сульфата представляет собой 4% раствор для внутримышечного введения со средней молекулярной массой 477 Да.
Мольный процент представляет собой величину, которая выражает долю данной функциональной группы (ф.гр.) в сополимере (Σ гр), выраженную в процентах:
моль %=(N ф.гр/NΣгр)*100%,
где моль % - величина мольного процента, Nф.гр - количество мономеров данной группы в сополимере, NΣгр - общее количество всех звеньев в сополимере.
Совиаль представляет собой сополимер винилпирролидона с диацеталем акролеина. Молекулярная масса диацеталя акролеина (далее акролеиновое звено) в молекуле совиаля равна 130 Да, а винилпирролидона - 111 Да. Мольный процент акролеинового звена равен 16%, значит, мольный процент винилпирролидона равен 84%. Исходя из этого, можно разбить молекулу совиаля на элементарное звено, в котором на одну молекулу акролеина приходится 5,25 (0,84/0,16) звеньев винилпирролидона. Молекулярный вес такого звена равен 712, 75 Да. Зная, что молекулярная масса совиаля равна 33000 Да, определяем количество таких элементарных звеньев в одной молекуле совиаля: 33000 Да/ 712,75 Да=46. Следовательно, одна молекула совиаля содержит 46 акролеиновых звеньев, т.к. одно элементарное звено содержит одно акролеиновое.
Приведем расчет количеств совиаля и гентамицина для взаимодействия с учетом того, что 1 молекула гентамицина будет связываться с каждой альдегидной группой совиаля. Из приведенного выше расчета очевидно, что мольное соотношение n(гент)/n(сов)=46. При этом массовые соотношения получим:
Гентамицин содержит 3 аминогруппы, однако одновременное взаимодействие двух групп, а тем более 3, с альдегидными группами совиаля представляется маловероятным из-за стерических препятствий.
Стадия 3. Формирование азометиновых связей между гентамицином и совиалем. С помощью 1 моль/л раствора натрия гидроксида рН инкубационной среды доводят до 11,0±0,02. Указанное значение рН с помощью 0,1 моль/л гидроксида натрия поддерживают в течение более 2 часов. Окончание реакции контролируют по отсутствию снижения рН от исходного (11,0±0,02) в течение 30 минут дополнительного инкубирования. Затем с помощью 1 моль/л раствора соляной кислоты рН инкубационной среды снижают до 7,0±0,1. В состав комплекса входят 88 мг гентамицина на 400 мг совиаля. Формирование комплекса контролируют методом инфракрасной спектроскопии (фиг. 1-2, табл. 1-2, фиг. 3, табл. 3). На фиг. 1 представлен эталонный спектр гентамицина, на фиг. 2 - эталонный спектр активированного совиаля, фиг.3 - спектр модифицированного гентамицина до восстановления.
Из расшифровки инфракрасного спектра модифицированного гентамицина до восстановления (табл. 3) видно, что в области 1680-1630 см-1 он имеет характерные для азометиновых связей полосы поглощения со средней интенсивностью, которые отсутствуют в спектре активированного совиаля и гентамицина (фиг. 1, 2, табл. 1, 2). Продукт нестабилен при хранении его в 0,15 моль/л растворе хлорида натрия при температуре (5±3)°С. В течение 1 месяца (80±10)% конъюгата распадается на свободные исходные компоненты - гентамицин и совиаль (табл. 4).
Стадия 4. Перевод азометиновых связей в прочные ковалентные. Выполняется в соответствии с алгоритмом предыдущей стадии вплоть до операции доведения рН до (7,0±0,1). При рН (11,0±0,02) вносят 21 мг натрия боргидрида и выдерживают инкубационную среду с боргидридом натрия в течение 2-12 часов при комнатной температуре.
Расчет необходимого количества боргидрида натрия проводили на основе эквимолярных соотношений:
и следующих допущений:
а) при активации все акролеиновые звенья образуют альдегидную группу, количество альдегидных групп равно 46;
б) количество азометиновых связей в конъюгате равно количеству активированных альдегидных групп.
m(NaBH4)=M(NaBH4)*n(NaBH4)=M(NaBH4)*n(coв)*46= =-46M(NaBH4)/M(coв)*m(coв)
Масса совиаля, используемая в эксперименте - 400 мг (0,4 г). Тогда необходимая для восстановления масса боргидрида натрия:
m(NaBH4)=46*38/33000*0,4=21,2 мг
Формирование комплекса контролируют методом инфракрасной спектроскопии (фиг. 1-2, табл. 1-2, фиг. 4, табл. 5). Спектр модифицированного гентамицина после восстановления представлен на фиг. 4. В состав комплекса входит 88 мг гентамицина и 400 мг совиаля.
Из расшифровки инфракрасного спектра модифицированного гентамицина после восстановления (табл. 5) видно, что в области 3300-3500 см-1 он имеет характерные для вторичных аминов полосы пропускания с большой интенсивностью, которые отсутствуют в спектре активированного совиаля и гентамицина (фиг. 1, 2, табл. 1, 2). Продукт стабилен при хранении его в 0,15 моль/л растворе хлорида натрия и температуре (5±3)°С. В течение 8 месяцев (10±5)% комплекса распадается на исходные реагенты реакции - гентамицин и совиаль (табл. 6).
Стадия 5. Удаление технологических примесей из состава инкубационной среды. Удаляли технологические примеси, включая несвязавшийся с совиалем гентамицин, из состава комплекса, сформированного за счет азометиновых связей (стадия 3) или из состава комплекса, образованного за счет перевода азометиновых связей в прочные ковалентные (стадия 4). Процедуру изменения состава инкубационной среды на физиологически приемлемый 0,15 моль/л натрия хлорид осуществляют либо колоночной хроматографией в режиме гель-фильтрации с использованием сефадекса G-25, либо ультрадиафильтрацией в тангенциальном потоке с помощью установки типа Vivaflow (ООО «Сартогосм»). Хроматографию проводят на колонке (Sосн - 5 см2, h=25 см), упакованной гелем Сефадекса G-25 до объема 125 мл. Объем образца составлял 25% от объема колонки. В хроматографических фракциях контролируют наличие совиаля йодным реактивом и наличие гентамицина - методом ИФА. Собирают пробирочные подфракции, содержащие совиаль, обобщенная фракция совиаля выходит первым пиком в объеме 16±2% от общего объема геля. В пробирочных подфракциях, соответствующих общему объему геля, измеряют концентрацию гентамицина с помощью ИФА. В конечных продуктах - комплексах, образованных за счет азометиновых или прочных ковалентных связей, определяют концентрацию совиаля и гентамицина вышеуказанными методами. Концентрацию гентамицина уточняют с помощью баланса с учетом количества гентамицина, внесенного в инкубационную среду, и количества несвязавшегося гентамицина, объем выхода которого соответствует общему объему геля. Для этих целей возможно также использовать установку для ультрадиафильтрации с пределом эксклюзии мембранных фильтров 10 кДа. Контроль процесса удаления технологических примесей осуществляют по содержанию гентамицина в сливных водах и возвратной фракции. Процесс ультрадиафильтрации, т.е. перевода раствора инкубационной среды в физиологически приемлемый 0,15 моль/л раствор натрия хлорида останавливают, когда концентрация гентамицина в сливных водах снижается до 0,5 нг/мл. Концентрацию гентамицина и совиаля определяют в возвратной фракции в соответствии с вышеуказанными методами. При расчете % гентамицина в составе комплексов учитывают количество несвязавшегося антибиотика по результату определения его концентрации в сливных водах. Доля связанного гентамицина в % в зависимости от мольного соотношения реагирующих компонентов представлена в таблице 7.
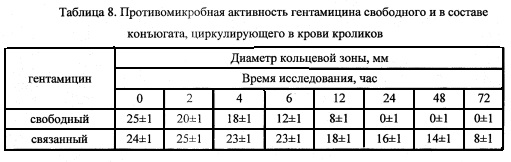
Стадия 6. Определение в кровеносном русле комплекса, образованного за счет перевода азометиновых связей в прочные ковалентные (стадия 4), и свободного гентамицина сульфата проводили на основе их противомикробной активности методом диффузии в агар [16. Государственная фармакопея Российской Федерации: в 5-и частях / Научный центр экспертизы средств медицинского применения. Изд. 12-е. Москва. 2008. Ч. 1. 704 с] на плотной питательной среде путем сравнения размеров зон угнетения роста тест-микробов. В чашки, установленные на горизонтальном столике, наливали 20 мл расплавленной питательной среды определенного состава, зараженной тест-культурой Е. Coli (количество клеток около 106, ОП550=0,7-1,4). На застывшей поверхности агара по трафарету, подложенному под дно чашки Петри, вырезали лунки диаметром 8 мм в толще агара стерильным сверлом. В лунки вносили растворы исследуемых образцов в объеме 0,1 мл. В качестве исследуемых образцов использовали сыворотку, полученную путем центрифугирования при 3000 об/мин крови кролика, взятой через 0, 2, 4, 6, 12, 24, 48, 72 часа после введения либо комплекса, образованного за счет перевода азометиновых связей в прочные ковалентные (стадия 4), либо гентамицина сульфата.
После инкубации в термостате при 36-38°С в течение 16-18 ч измеряли диаметры зон задержки роста тест-микроба, отчетливо видных вокруг лунок. Результаты представлены в таблице 8.
Анализ полученных результатов показал, что модифицированный гентамицином совиаль в течение трех дней идентифицируют в кровеносном русле подопытных кроликов на основе противомикробной активности гентамицина (табл. 8).
Источники информации
1. Душкин А.В. // Фундаментальные исследования. 2012. №4 (часть 1). С. 47-52
2. Инструкция по применению ДиеномастаАФ для лечения мастита у коров. Регистрационный номер ПВР-2-0.2/01043, ЗАО НПП Агрофарм.
3. Инструкция по применению препарата ГЕНТАМ. Регистрационный номер ПВР-3-2.1/02697, ООО НПО «АПИ-САН».
4. Инструкция по медицинскому применению лекарственного средства ГентаСЕПТ. Регистрационный номер UA/1279/01/01, ПАО НПЦ «Борщаговский химико-фармацевтический завод».
5. Назарова О.В. // Прикладная химия. 1993. №3. С. 193-197.
6. Хомяков К.П. и соавт. // Известия вузов. Химия и химическая технология. 1979. №10. С. 1267-1271.
7. Панарин Е.Ф., Лавров Н.А., Соловский М.В., Шальнова Л.И. Полимеры-носители биологически активных веществ. СПб.: Профессия. 2014. 304 с.
8. Соловский М.В., Никольская Н.В. // Химико-фармацевтический журнал. 2000. Т. 34. №11. С. 21-24.
9. Соловский М.В., Еропкин М.Ю., Еропкина Е.М., Киселев О.И., Панарин Е.Ф., Гаврилова И.И., Шульцева Е.Л. Патент РФ №2335510. БИ №28. 2008
10. Соловский М. В. //Антибиотики и химиотерапия. 2000. №6. с. 10-12.
11. Панарин Е.Ф. и соавт. // авт. свид. СССР №431185. БИ №28.
12. Смирнова И.Г. и соавт. // Вестник Московского университета. Т. 41 (Серия 2). 2000.
13. Танн Ч.Х. и др. Способ получения изепамицина и промежуточные соединения // авт. свид. №2120444. 1998
14. Панарин Е.Ф., Гаврилова И.И. // авт. свид. №560425. БИ №47.
15. Аникина Т.Б., Панарин Е.Ф. // авт. свид. №522198. БИ №27.
16. Государственная фармакопея Российской Федерации: в 5-и частях / Научный центр экспертизы средств медицинского применения. Изд. 12-е. Москва. 2008. Ч. 1. 704 с.
Claims (7)
1. Способ получения гентамицина в комплексе с совиалем путем индукции альдегидных групп за счет кислотного гидролиза акролеинового звена, отличающийся тем, что позволяет получать промежуточный нестабильный продукт за счет непрочных азометиновых связей между антибиотиком и сополимером, который, в зависимости от целей конструирования, можно использовать для кинетических исследований либо переводить азометиновые связи в одинарные ковалентные для получения стабильного продукта, в котором доля гентамицина составляет 14 моль на 1 моль совиаля.
2. Способ по п. 1, отличающийся тем, что прототипное научно-техническое решение основано на формировании комплекса гентамицина с сополимерами винилпирролидона за счет кулоновских сил и водородных связей и, как следствие этого, диссоциирующего на исходные составляющие - сополимер винилпирролидона и гентамицин.
3. Способ по п. 1, отличающийся тем, что конъюгат, сформированный за счет азометиновых связей, обратимо диссоциирует на исходные компоненты в течение 30 дней.
4. Способ по п. 1, отличающийся тем, что конъюгат, сформированный за счет ковалентных связей, сохраняет 90% антибактериальной активности при хранении в 0,15 моль/л растворе натрия хлорида при температуре (5-25)°C в течение 8 месяцев.
5. Способ по п. 1, отличающийся тем, что в синтез ковалентного конъюгата на основе гентамицина и совиаля базируется на заводской субстанции, не требующей дополнительной очистки либо перевода в основание гентамицина.
6. Способ по п. 1, отличающийся тем, что стадия удаления низкомолекулярных примесей, представленная гельфильтрацией на сефадексе G-25 или ультрадиафильтрацией, позволяет либо в общем объеме упакованной гелем колонки, либо в составе бросовой фракции определять несвязавшийся гентамицин и, тем самым, контролировать технологическую дисциплину способа (или стадии) модификации гентамицина совиалем.
7. Способ по п. 1, отличающийся тем, что модифицированный гентамицином совиаль в течение трех дней идентифицируют в кровеносном русле подопытных кроликов на основе противомикробной активности гентамицина.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2017114890A RU2659032C1 (ru) | 2017-04-26 | 2017-04-26 | Способ модификации гентамицина сополимером винилпирролидона с диацеталем акролеина |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2017114890A RU2659032C1 (ru) | 2017-04-26 | 2017-04-26 | Способ модификации гентамицина сополимером винилпирролидона с диацеталем акролеина |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2659032C1 true RU2659032C1 (ru) | 2018-06-27 |
Family
ID=62713539
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2017114890A RU2659032C1 (ru) | 2017-04-26 | 2017-04-26 | Способ модификации гентамицина сополимером винилпирролидона с диацеталем акролеина |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2659032C1 (ru) |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2120444C1 (ru) * | 1989-06-21 | 1998-10-20 | Шеринг Корпорейшн | Способ получения изепамицина и промежуточные соединения |
| RU2335510C2 (ru) * | 2006-02-22 | 2008-10-10 | Институт высокомолекулярных соединений РАН | Водорастворимые полимерные комплексы антибиотиков-аминогликозидов |
| RU2414237C2 (ru) * | 2008-04-30 | 2011-03-20 | Государственное образовательное учреждение высшего профессионального образования "Удмуртский государственный университет" | Модификация альбумина совиалем как способ повышения его стабильности для производства фармацевтического биопрепарата альбумина в комплексе с гентамицином или стимаденом |
-
2017
- 2017-04-26 RU RU2017114890A patent/RU2659032C1/ru not_active IP Right Cessation
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2120444C1 (ru) * | 1989-06-21 | 1998-10-20 | Шеринг Корпорейшн | Способ получения изепамицина и промежуточные соединения |
| RU2335510C2 (ru) * | 2006-02-22 | 2008-10-10 | Институт высокомолекулярных соединений РАН | Водорастворимые полимерные комплексы антибиотиков-аминогликозидов |
| RU2414237C2 (ru) * | 2008-04-30 | 2011-03-20 | Государственное образовательное учреждение высшего профессионального образования "Удмуртский государственный университет" | Модификация альбумина совиалем как способ повышения его стабильности для производства фармацевтического биопрепарата альбумина в комплексе с гентамицином или стимаденом |
Non-Patent Citations (1)
| Title |
|---|
| Соловский М.В. и др. АНТИБИОТИКИ И ХИМИОТЕРАПИЯ, 2000, N6, стр. 10-12. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ehrbar et al. | Drug-sensing hydrogels for the inducible release of biopharmaceuticals | |
| CN108329467B (zh) | 一种超支化抗菌肽聚合物的制备方法 | |
| CN110437374B (zh) | 一种季铵盐类两亲性阳离子聚合物及其应用 | |
| CN110393725B (zh) | 具有革兰氏选择性的苯硼酸及其衍生物修饰的金纳米颗粒、其制备方法及应用 | |
| Barrios-Gumiel et al. | PEGylated AgNP covered with cationic carbosilane dendrons to enhance antibacterial and inhibition of biofilm properties | |
| CN104628829A (zh) | 抗菌肽wy-21及其应用 | |
| JP2001037472A (ja) | 三次元細胞培養基材及びそれを用いた細胞培養方法 | |
| Liu et al. | Efficient synthesis and excellent antimicrobial activity of star-shaped cationic polypeptides with improved biocompatibility | |
| CN106750262A (zh) | 两亲性嵌段抗菌肽的合成及其组装体的制备方法和应用 | |
| CN116617220B (zh) | 抗青霉素类耐药菌的绿原酸-小檗碱纳米药物、药物组合物及其制备方法 | |
| WO2018162009A2 (de) | Verfahren und material zur differenzierten sequestrierung von stoffen verschiedener stoffgruppen mit hilfe von sulfatierte oder sulfonierte komponenten enthaltenden hydrogelen | |
| CN115105624B (zh) | 一种海洋多糖基高效抗菌膜敷料及其制备方法 | |
| CN114478834A (zh) | 一种胍基透明质酸抗菌聚合物及其制备方法和应用 | |
| RU2659032C1 (ru) | Способ модификации гентамицина сополимером винилпирролидона с диацеталем акролеина | |
| Palantoken et al. | Synthesis and characterization of a ROMP-based polycationic antimicrobial hydrogel | |
| CN110755638A (zh) | 一种具有骨靶向性的药物载体及其制备方法与应用 | |
| CN109364256B (zh) | 一种琼脂糖胶束药物载体 | |
| CN111548388B (zh) | 一种pH响应的非螺旋-螺旋转变抗菌聚肽及其制备方法 | |
| CN111116717B (zh) | 含有n-甲基-d-葡糖胺单元的糖肽水凝胶、制备方法及其应用 | |
| RU2541103C1 (ru) | Углеродный сорбент с антибактериальными и антимикотическими свойствами и способ его получения | |
| US12049543B2 (en) | Copolymer containing cyclic nitroxide radical and trialkoxysilyl in side chain, and use thereof | |
| CN108524945B (zh) | 一种庆大霉素改性壳聚糖的制备方法 | |
| Solovskij et al. | Polymer water-soluble derivatives of polypeptide antibiotic, gramicidin-S based on reactive copolymers of N-(2-hydroxypropyl) methacrylamide | |
| RU2623877C1 (ru) | Способ получения полимерных комплексов рифампицина с пониженной токсичностью и высокой противотуберкулёзной активностью | |
| Gergova et al. | Comparative investigation of the feasibility of bacterial biofilms formation on the surface of the hybrid material UREASIL |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20190427 |