RU2643329C1 - Synthetic immunogen for protection and treatment of psychoactive substances addiction - Google Patents
Synthetic immunogen for protection and treatment of psychoactive substances addiction Download PDFInfo
- Publication number
- RU2643329C1 RU2643329C1 RU2016136844A RU2016136844A RU2643329C1 RU 2643329 C1 RU2643329 C1 RU 2643329C1 RU 2016136844 A RU2016136844 A RU 2016136844A RU 2016136844 A RU2016136844 A RU 2016136844A RU 2643329 C1 RU2643329 C1 RU 2643329C1
- Authority
- RU
- Russia
- Prior art keywords
- conjugate
- vinylpyridine
- immunogen
- synthetic polymer
- synthetic
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/385—Haptens or antigens, bound to carriers
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Medicinal Chemistry (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
Abstract
Description
Изобретение относится к медицине, в частности к иммунологии, и может применяться для лечения наркоманий, отравлений различными ядами в промышленности и быту, при техногенных катастрофах и т.п.The invention relates to medicine, in particular to immunology, and can be used for the treatment of drug addiction, poisoning with various poisons in industry and everyday life, in industrial accidents, etc.
Изобретение представляет собой синтетический иммуноген для защиты от токсического действия наркотических и психоактивных веществ. Иммуноген выполнен в виде конъюгата макромолекулярного носителя, выбранного из ряда: природный или искусственный белок, олиго- и полипептид, углевод, липид или нуклеотид, и гаптена - наркотического или психотропного соединения, связанного с синтетическим полимером, отличающийся тем, что в качестве синтетического полимера используют сополимер 2-метил-5-винилпиридина и N-винилпирролидона общей формулы IThe invention is a synthetic immunogen for protection against the toxic effects of narcotic and psychoactive substances. The immunogen is made in the form of a conjugate of a macromolecular carrier selected from the series: natural or artificial protein, oligo - and polypeptide, carbohydrate, lipid or nucleotide, and hapten - a narcotic or psychotropic compound associated with a synthetic polymer, characterized in that it is used as a synthetic polymer copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone of the general formula I
где n равно 25-50 мол. %, а средневязкостная молекулярная масса Мη равна 15-45 кДа, или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона общей формулы IIwhere n is equal to 25-50 mol. %, and the average viscosity molecular weight Mη is 15-45 kDa, or a copolymer of 4-vinylpyridine, 2-methyl-5-vinylpyridine and N-vinylpyrrolidone of the general formula II
где (m+k) составляет 20-90 мол. %, при этом доля мономерных звеньев 4-винилпиридина составляет от 0,05(m+k) до 0,30(m+k), а средневязкостная молекулярная масса Мη равна 15-250 кДа. Из уровня техники известен синтетический иммуноген для терапии и профилактики злоупотреблений наркотическими веществами (в частности, опиатной зависимости), представляющий собой конъюгат в виде носителя - природного или искусственного белка и гаптена - наркотического или психотропного соединения. Причем в качестве носителя он содержит бычий сывороточный альбумин или синтетические полипептиды и гликопротеины, а в качестве гаптена - морфин, или кодеин, или героин, или метадон, или т.п. (см. Ковалев И.Е., Полевая О.Ю. Биохимические основы иммунитета к низкомолекулярным химическим соединениям. М.: Наука, 1985).where (m + k) is 20-90 mol. %, while the proportion of monomer units of 4-vinylpyridine is from 0.05 (m + k) to 0.30 (m + k), and the average viscosity molecular weight Mη is 15-250 kDa. A synthetic immunogen is known from the prior art for the treatment and prevention of drug abuse (in particular, opiate addiction), which is a conjugate in the form of a carrier - a natural or artificial protein and hapten - a narcotic or psychotropic compound. Moreover, it contains bovine serum albumin or synthetic polypeptides and glycoproteins as a carrier, and morphine, or codeine, or heroin, or methadone, or the like as a hapten. (see Kovalev I.E., Polevaya O.Yu. Biochemical basis of immunity to low molecular weight chemical compounds. M: Nauka, 1985).
Однако этот иммуноген имеет балластные примеси, снижающие его терапевтическую (иммуностимулирующую) активность и требует применения больших доз (до 20 мг/кг). Кроме того, продолжительность иммунизации доходит до 6 месяцев, а достижение стабильного и/или пролонгированного иммунитета не всегда возможно.However, this immunogen has ballast impurities that reduce its therapeutic (immunostimulating) activity and requires the use of large doses (up to 20 mg / kg). In addition, the duration of immunization reaches 6 months, and the achievement of stable and / or prolonged immunity is not always possible.
Известен иммуноген, представляющий собой конъюгаты производных морфина (6-гемисукцинильного и 3-О-карбоксиметильного) с белком-носителем (столбнячный анатоксин), способный, по результатам доклинических испытаний на грызунах, запускать синтез поликлональных антител к опиатам - морфину и его структурному аналогу героину - в результате повторного введения этих препаратов при активной иммунизации (ЕР 1767221 А2, 28.03.2007; US 20080241183 А1, 10.02.2008; US 008,008,457 В2, 30.08.2011). При введении такого иммуногена в крови появляются в высоких титрах антитела к этим опиатам, способные связать поступающие в организм извне наркотики в кровяном русле и воспрепятствовать тем самым их проникновению в мозг через гематоэнцефалический барьер. В результате снижения положительного подкрепления угасает влечение к опиатам (морфину и его производным, в частности, героину), что было показано на модели внутривенного самовведения этих наркотиков грызунами.An immunogen is known, which is a conjugate of morphine derivatives (6-hemisuccinyl and 3-O-carboxymethyl) with a carrier protein (tetanus toxoid), capable of, according to the results of preclinical tests in rodents, trigger the synthesis of polyclonal antibodies to opiates - morphine and its structural analogue of heroin - as a result of repeated administration of these drugs during active immunization (EP 1767221 A2, 03/28/2007; US 20080241183 A1, 02/10/2008; US 008,008,457 B2, 08/30/2011). With the introduction of such an immunogen in the blood, antibodies to these opiates appear in high titers, which can bind drugs that enter the body from the outside in the bloodstream and thereby prevent their entry into the brain through the blood-brain barrier. As a result of a decrease in positive reinforcement, the attraction to opiates (morphine and its derivatives, in particular heroin) is dying away, which was shown on the model of intravenous self-administration of these drugs by rodents.
Недостатком этого иммуногена является нестабильность такого соединения, приводящая к самопроизвольному распаду на исходные составляющие, пусть даже в незначительных количествах.The disadvantage of this immunogen is the instability of such a compound, leading to spontaneous decomposition into the original components, even in small quantities.
Известен синтетический иммуноген для терапии и профилактики злоупотреблений наркотическими и психоактивными веществами (патент RU 2236257 С1, 15.09.2003), который представляет собой конъюгат в виде носителя - природного или искусственного белка (яичный альбумин, человеческий гаммаглобулин, микробные токсины) и наркотического или психотропного соединения из следующих групп низкомолекулярных соединений: ароматические пропанамины, или изохинолины, или дифенилметаны, или индоламины, или производные барбитуровой кислоты, или производные замещенных пиперидинов. Конъюгат модифицирован иммунокомпетентным полиэлектролитом - полиоксидонием.A synthetic immunogen is known for the treatment and prevention of drug and psychoactive substance abuse (patent RU 2236257 C1, September 15, 2003), which is a conjugate in the form of a carrier - natural or artificial protein (egg albumin, human gammaglobulin, microbial toxins) and narcotic or psychotropic compounds of the following groups of low molecular weight compounds: aromatic propanamines, or isoquinolines, or diphenylmethanes, or indolamines, or derivatives of barbituric acid, or derivatives substituted x piperidines. The conjugate is modified by an immunocompetent polyelectrolyte - polyoxidonium.
К недостаткам этого иммуногена можно отнести то, что получение предлагаемого конъюгата требует использования либо высокотоксичного и канцерогенного бензидина, либо сукцинилдихлорида, обладающего лакриматорными свойствами, высокой токсичностью и коррозионной активностью.The disadvantages of this immunogen can be attributed to the fact that obtaining the proposed conjugate requires the use of either highly toxic and carcinogenic benzidine, or succinyl dichloride, which has lacrimator properties, high toxicity, and corrosive activity.
Известно также средство для профилактики и лечения опийной наркомании (патент RU 2264228, 20.11.2005), представляющее собой иммуноген - первичные моноклональные антитела к опиатам, в частности к конъюгату морфин-3БСА, при иммунизации которыми в организме животного или человека должны образовываться антиидиотипические (вторичные) антитела. Механизм действия такого средства, по мнению автора, связан с модификацией образуемыми антиидиотипическими антителами периферических опиоидных рецепторов, что отраженным образом может влиять на опиоидную систему мозга.There is also known a tool for the prevention and treatment of opium addiction (patent RU 2264228, 11/20/2005), which is an immunogen - primary monoclonal antibodies to opiates, in particular to the morphine-3BSA conjugate, when immunized with which anti-idiotypic (secondary ) antibodies. The mechanism of action of such a tool, according to the author, is associated with the modification of peripheral opioid receptors by the formed anti-idiotypic antibodies, which in a reflected manner can affect the brain's opioid system.
Недостатком этого средства является достаточно сложная и дорогая технология получения моноклональных антител (получение поликлональных антител проще и дешевле), а также тот факт, что эффект от иммунизации будет наблюдаться только в случае присутствия в крови определенного уровня вторичных (антиидиотипических) антител к опиатам (морфину). Употребление опиатов, которое может иметь место, несмотря на иммунизацию, не будет дополнительно стимулировать выработку вторичных (антиидиотипических) антител к опиатам (морфину).The disadvantage of this tool is the rather complicated and expensive technology for producing monoclonal antibodies (obtaining polyclonal antibodies is simpler and cheaper), as well as the fact that the effect of immunization will be observed only if a certain level of secondary (anti-idiotypic) antibodies to opiates (morphine) is present in the blood . The use of opiates, which may occur despite immunization, will not further stimulate the production of secondary (anti-idiotypic) antibodies to opiates (morphine).
В качестве ближайшего аналога настоящего изобретения авторы рассматривают конъюгат гаптен-носитель, который способен вызывать выработку антител против гаптена для лечения от зависимости от психоактивных веществ, представляющий собой конъюгат макромолекулярного носителя, гаптена, который выполнен в виде сополимерных частиц, нековалентно связанный с конъюгатом (европейский патент ЕР 1329226 А2, 23.07.2003).As the closest analogue of the present invention, the authors consider the hapten-carrier conjugate, which is capable of producing anti-hapten antibodies for treatment of dependence on psychoactive substances, which is a conjugate of a macromolecular carrier, a hapten, which is made in the form of copolymer particles, non-covalently bound to the conjugate (European patent EP 1329226 A2, 07/23/2003).
Задачей настоящего изобретения является создание иммуногена, который не требует для своего получения использования поли(4-нитрофенил)акрилата, трудноудаляемых и огнеопасных органических растворителей и при этом позволяет вызвать в организме стабильный иммунный ответ и уменьшает токсическое действие наркотиков и психоактивных веществ за счет стойкого повышения титра специфических антител к ним.The objective of the present invention is to provide an immunogen that does not require the use of poly (4-nitrophenyl) acrylate, hard-to-remove and flammable organic solvents, and at the same time it can cause a stable immune response in the body and reduces the toxic effect of drugs and psychoactive substances due to a steady increase in titer specific antibodies to them.
Поставленная задача решается тем, что в известном синтетическом иммуногене для защиты от токсического действия наркотических и психоактивных веществ, представляющем собой конъюгат макромолекулярного носителя, выбранного из природного или искусственного белка, олиго- и полипептида, углевода, липида или нуклеотида, и гаптена - наркотического или психотропного соединения, новым является то, что в качестве синтетического полимера используют сополимер 2-метил-5-винилпиридина и N-винилпирролидона или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона.The problem is solved in that in the known synthetic immunogen for protection against the toxic effects of narcotic and psychoactive substances, which is a conjugate of a macromolecular carrier selected from a natural or artificial protein, oligo - and polypeptide, carbohydrate, lipid or nucleotide, and hapten - narcotic or psychotropic of the compound, it is new that a copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone or a copolymer of 4-vinylpyridine, 2-methyl-5-vinyl is used as a synthetic polymer iridina and N-vinylpyrrolidone.
Таким образом, изобретение представляет синтетический иммуноген вызывающий выработку антител специфичных по отношению к психоактивным веществам, представляющий собой конъюгат макромолекулярного носителя, выбранного из ряда: природный или искусственный белок, олиго- или полипептид, углевод, липид или нуклеотид, и гаптена - наркотического или психотропного соединения, и связанного с коньюгатом синтетического полимера, отличающийся тем, что в качестве синтетического полимера используют сополимер 2-метил-5-винилпиридина и N-винилпирролидона общей формулы IThus, the invention provides a synthetic immunogen that induces the production of antibodies specific for psychoactive substances, which is a conjugate of a macromolecular carrier selected from the range: natural or artificial protein, oligo- or polypeptide, carbohydrate, lipid or nucleotide, and hapten - a narcotic or psychotropic compound , and associated with the conjugate synthetic polymer, characterized in that as a synthetic polymer using a copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolide she is of general formula I
где n равно 25-50 мол. %, а средневязкостная молекулярная масса Mη равна 15-45 кДа, или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона общей формулы IIwhere n is equal to 25-50 mol. %, and the average viscosity molecular weight Mη is 15-45 kDa, or a copolymer of 4-vinylpyridine, 2-methyl-5-vinylpyridine and N-vinylpyrrolidone of the general formula II
где (m+k) составляет 20-90 мол. %, при этом доля мономерных звеньев 4-винилпиридина составляет от 0,05(m+k) до 0,30(m+k), а средневязкостная молекулярная масса Мη равна 15-250 кДа.where (m + k) is 20-90 mol. %, while the proportion of monomer units of 4-vinylpyridine is from 0.05 (m + k) to 0.30 (m + k), and the average viscosity molecular weight Mη is 15-250 kDa.
Предпочтительно в качестве макромолекулярного носителя, выбранного из группы природных белков иммуноген содержит человеческий гамма-глобулин или альбумин.Preferably, as the macromolecular carrier selected from the group of natural proteins, the immunogen contains human gamma globulin or albumin.
В качестве гаптена он может содержать наркотическое или психотропное соединение, выбранное из опиатов, например морфин, героин, кодеин; антагонистов опиоидных рецепторов, например, налтрексон налоксон; каннабиноидов, например дельта-9-тетрагидроканнабинол; амфетаминов, например амфетамин, метамфетамин, экстази; бензоилэкгонина и его производных, например кокаин; барбитуратов, например барбамил, фенобарбитал; бензодиазепинов, например гидезепам; метадона, фенциклидина, трициклических антидепрессантов, котинина и их производных и метаболитов.As a hapten, it may contain a narcotic or psychotropic compound selected from opiates, for example morphine, heroin, codeine; opioid receptor antagonists, for example, naltrexone naloxone; cannabinoids, for example, delta-9-tetrahydrocannabinol; amphetamines, for example amphetamine, methamphetamine, ecstasy; benzoylegonin and its derivatives, for example cocaine; barbiturates, for example barbamyl, phenobarbital; benzodiazepines, for example gidezepam; methadone, phencyclidine, tricyclic antidepressants, cotinine and their derivatives and metabolites.
Предпочтительно в качестве гаптена иммуноген содержит налтрексон.Preferably, the immunogen contains naltrexone as a hapten.
Техническим результатом изобретения является более эффективная по сравнению с ближайшим аналогом иммунная реакция, которую заявляемый синтетический иммуноген обеспечивает за счет добавления к конъюгату синтетического полимера, в качестве которого применяют сополимер 2-метил-5-винилпиридина и N-винилпирролидона общей формулы I или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона общей формулы II. Таким образом, в стандартных условиях без применения трудноудаляемых и огнеопасных веществ возможно воспроизводить структуру иммуногена в заданном диапазоне соотношений компонентов, добиваясь увеличения длительности стойкого гуморального иммунитета и повышенного содержания специфических антител. Кроме того, в результате использования изобретения наблюдается снижение токсичности иммуногена, что связано с составом применяемых при его получении химических соединений.The technical result of the invention is a more effective immune reaction than the closest analogue, which the claimed synthetic immunogen provides by adding to the conjugate a synthetic polymer, which is used as a copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone of the general formula I or copolymer 4- vinylpyridine, 2-methyl-5-vinylpyridine and N-vinylpyrrolidone of the general formula II. Thus, under standard conditions without the use of difficult to remove and flammable substances, it is possible to reproduce the structure of the immunogen in a given range of component ratios, achieving an increase in the duration of persistent humoral immunity and an increased content of specific antibodies. In addition, as a result of using the invention, a decrease in the toxicity of the immunogen is observed, which is associated with the composition of the chemical compounds used in its preparation.
Диапазон соотношений от 2 до 20 молей конъюгата на моль синтетического полимера обеспечивает стандартизацию и контроль фармакологического эффекта в заданных соотношениях при формировании и укрупнении структуры иммуногена. Предпочтительным является отношение 10:1 моль/моль, которое дает максимально возможную воспроизводимость и стабильность синтетического иммуногена.The range of ratios from 2 to 20 moles of conjugate per mole of synthetic polymer provides standardization and control of the pharmacological effect in predetermined proportions during the formation and enlargement of the structure of the immunogen. A ratio of 10: 1 mol / mol is preferred, which gives the highest possible reproducibility and stability of the synthetic immunogen.
Использование в предлагаемом синтетическом иммуногене конкретных носителей и гаптенов защищает организм человека от действия широкого спектра психоактивных и наркотических веществ.The use of specific carriers and haptens in the proposed synthetic immunogen protects the human body from the effects of a wide range of psychoactive and narcotic substances.
Анализ известных технических решений позволяет сделать вывод о том, что предлагаемое изобретение не известно из уровня техники, что свидетельствует о его соответствии условию патентоспособности «новизна».Analysis of the known technical solutions allows us to conclude that the invention is not known from the prior art, which indicates its compliance with the condition of patentability "novelty".
По мнению авторов, специалист не способен прийти к техническому решению, предлагаемому в соответствии с настоящим изобретением, исключительно на основании общих знаний и анализа известного уровня техники, что позволяет сделать вывод о его соответствии условию патентоспособности «изобретательский уровень».According to the authors, the specialist is not able to come to a technical solution proposed in accordance with the present invention solely on the basis of general knowledge and analysis of the prior art, which allows us to conclude that it meets the patentability condition of "inventive step".
Возможность приготовления синтетического иммуногена из доступных промышленно выпускаемых компонентов на традиционном оборудовании с помощью известных методик с достижением технических результатов свидетельствует о соответствии изобретения критерию «промышленная применимость».The possibility of preparing a synthetic immunogen from available commercially available components on traditional equipment using well-known techniques with the achievement of technical results indicates the compliance of the invention with the criterion of "industrial applicability".
Далее приведены примеры осуществления изобретения, способствующие более точному и полному пониманию его сути. Специалисту в данной области очевидны возможные модификации и замены, например, относящиеся к протоколам исследований, которые не выходят за рамки объема изобретения, определяемые его формулой.The following are examples of the invention, contributing to a more accurate and complete understanding of its essence. Possible modifications and replacements are obvious to those skilled in the art, for example, those related to research protocols, which do not fall outside the scope of the invention as defined by its claims.
Приведенные примеры подтверждают, но не ограничивают объем заявленных притязаний по настоящему изобретению.These examples confirm, but do not limit the scope of the claimed claims of the present invention.
1. Краткое описание таблиц и терминов1. Brief description of tables and terms
В Таблице 1 представлены данные по специфичности и доступности эпитопов иммуногена связывания с антителами в ИФА.Table 1 presents data on the specificity and accessibility of epitopes of the immunogen binding to antibodies in ELISA.
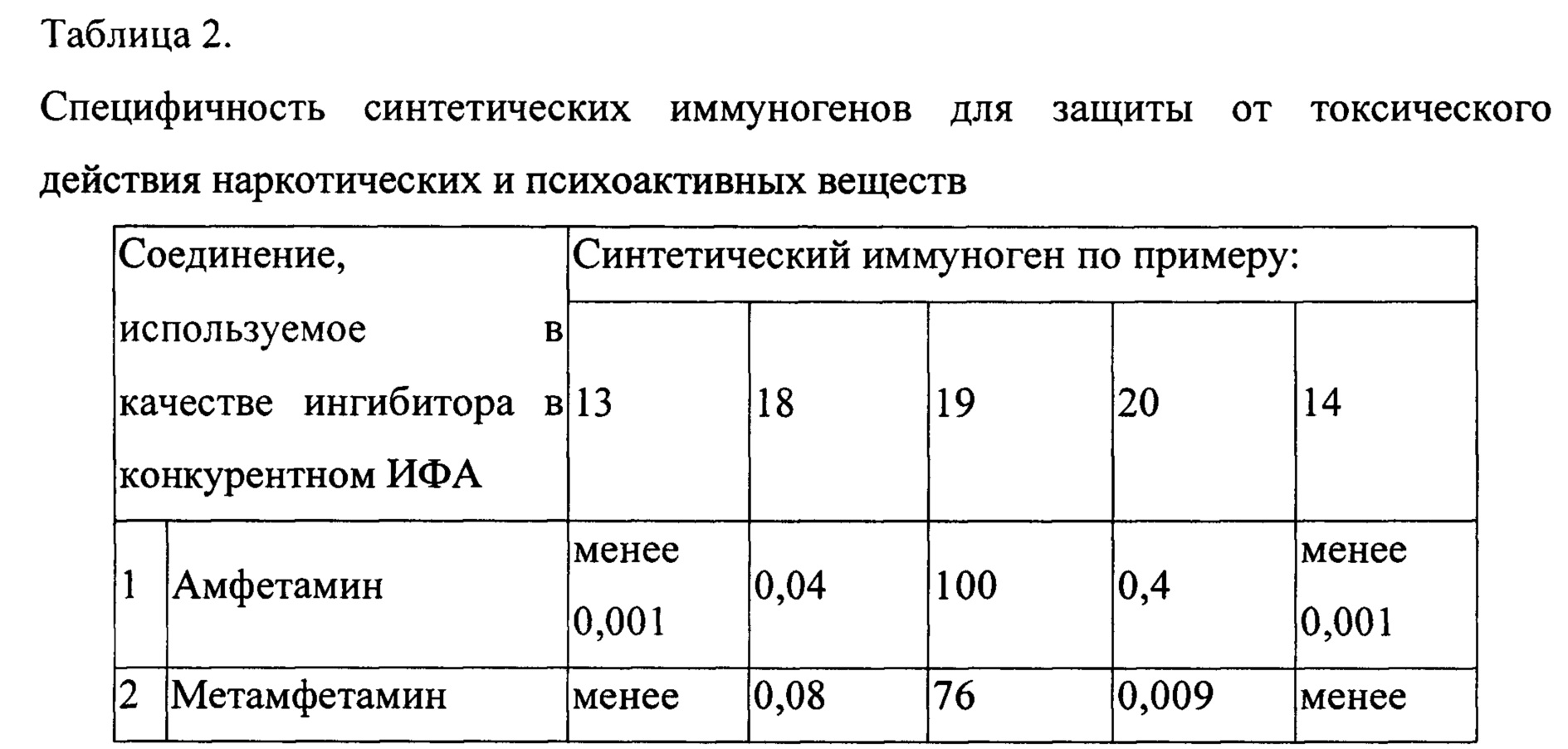
В Таблице 2 представлены обобщенные данные по изучению специфичности антител, полученных при иммунизации кроликов синтетическими иммуногенами.Table 2 summarizes the data on the specificity of antibodies obtained by immunizing rabbits with synthetic immunogens.
В Таблице 3 представлены составы предлагаемого синтетического иммуногена и известного, взятого за прототип, а также данные по определению иммунологической активности и их фармакологического действия.Table 3 presents the compositions of the proposed synthetic immunogen and known, taken as a prototype, as well as data on the determination of immunological activity and their pharmacological action.
В настоящем изобретении под термином «ингибитор» понимается вещество, которое используют в процедуре конкурентного иммуноферментного анализа (ИФА) для оценки специфичности и аффинности антител. В качестве ингибиторов применяют соединения, структурно родственные гаптену, входящему в состав заявленного иммуногена, а также наркотические вещества и ряд психотропных лекарственных препаратов другой химической природы: это метадон, псевдоэфедрин, норэфедрин, барбамил, канабинол, морфин, героин, кодеин и др.In the present invention, the term "inhibitor" refers to a substance that is used in a competitive enzyme-linked immunosorbent assay (ELISA) to assess the specificity and affinity of antibodies. As inhibitors, compounds are used that are structurally related to the hapten that is part of the claimed immunogen, as well as narcotic substances and a number of psychotropic drugs of a different chemical nature: methadone, pseudoephedrine, norephedrine, barbamil, canabinol, morphine, heroin, codeine, etc.
2. Синтез конъюгатов макромолекулярных носителей с гаптенами2. Synthesis of conjugates of macromolecular carriers with haptens
Введение карбоксилсодержащих производных, способствующих проведению реакции связывания гаптена с макромолекулярным носителем, для опиатов, кокаина, барбитуратов, бензодиазепинов осуществляют их взаимодействием с ангидридом янтарной кислоты в абсолютированном растворителе.The introduction of carboxyl-containing derivatives that contribute to the hapten binding reaction with a macromolecular carrier for opiates, cocaine, barbiturates, benzodiazepines is carried out by their interaction with succinic acid anhydride in an absolute solvent.
Синтез карбоксилсодержащих производных каннабиноидов, амфетамина, метадона, фенциклидина, трициклических антидепрессантов, котинина проводят по реакции азосочетания с диазотированной 4-аминобензойной кислотой.The synthesis of carboxyl-containing derivatives of cannabinoids, amphetamine, methadone, phencyclidine, tricyclic antidepressants, cotinine is carried out by the azo coupling reaction with diazotized 4-aminobenzoic acid.
На основе модифицированных наркотических и психотропных веществ готовят конъюгаты, в которых эти вещества нековалентно связанны с макромолекулярными носителями.Conjugates are prepared on the basis of modified narcotic and psychotropic substances in which these substances are non-covalently bound to macromolecular carriers.
Реакции конденсации карбоксилсодержащих производных гаптенов с макромолекулярным носителем осуществляют с использованием водорастворимого карбодиимида, глутарового альдегида или изобутилхлорформиата. Макромолекулярные носители содержат перечисленные выше гаптены.Condensation reactions of carboxyl-containing hapten derivatives with a macromolecular carrier are carried out using water-soluble carbodiimide, glutaraldehyde or isobutyl chloroformate. Macromolecular carriers contain the haptens listed above.
Полученный конъюгат выделяли гель-хроматографией на колонке (2×50 см) с сефадексом G-25, уравновешенным в 0.05 М фосфатном буфере (pH 7.2). Скорость элюирования составляла 50 мл/ч, при этом отбирали белковую фракцию конъюгата, выходящую в свободном объеме колонки (250 мл). Контроль хроматографического процесса осуществляли с помощью проточной кварцевой ячейки Uvicord II фирмы «Pharmacia» (Швеция) при длине волны 280 нм с использованием регистрирующегося устройства и коллектора фракций той же фирмы. Концентрацию белка, присутствующего в элюированной фракции, определяли при длине волны 280 нм в спектрофотометре Genesys 10UV (Thermo Fisher Scientific, США).The resulting conjugate was isolated by gel chromatography on a column (2 × 50 cm) with Sephadex G-25, equilibrated in 0.05 M phosphate buffer (pH 7.2). The elution rate was 50 ml / h, and the protein fraction of the conjugate was withdrawn in the free volume of the column (250 ml). The chromatographic process was monitored using a Uvicord II flowing quartz cell from Pharmacia (Sweden) at a wavelength of 280 nm using a recording device and a fraction collector of the same company. The concentration of the protein present in the eluted fraction was determined at a wavelength of 280 nm in a Genesys 10UV spectrophotometer (Thermo Fisher Scientific, USA).
Количество молей гаптена, связавшихся с макромолекулярным белковым носителем, определяют с помощью сравнительного спектрального анализа в ультрафиолетовой и видимой областях.The number of moles of hapten bound to a macromolecular protein carrier is determined by comparative spectral analysis in the ultraviolet and visible regions.
Пример 1. Синтез конъюгата морфина с человеческим сывороточным альбумином (М-ЧСА)Example 1. The synthesis of the conjugate of morphine with human serum albumin (M-HSA)
Раствор 65 мг (0,001 ммоль) человеческого сывороточного альбумина (ЧСА) в 5,0 мл дистиллированной воды смешивают с 3,0 мл 0,1М фосфатного буфера содержащего 15,0 мг (0,039 ммоль) 6-(3-(аминогексиламинокарбонил)-пропионат)морфина и при охлаждении по каплям прибавляют раствор 15 мг (0,055 ммоль) водорастворимого карбодиимида в 3 мл дистиллированной воды. Реакционную смесь инкубируют в течение 5 часов при 4°С. Полученный конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.A solution of 65 mg (0.001 mmol) of human serum albumin (HSA) in 5.0 ml of distilled water is mixed with 3.0 ml of 0.1 M phosphate buffer containing 15.0 mg (0.039 mmol) of 6- (3- (aminohexylaminocarbonyl) propionate ) of morphine and upon cooling, a solution of 15 mg (0.055 mmol) of water-soluble carbodiimide in 3 ml of distilled water is added dropwise. The reaction mixture was incubated for 5 hours at 4 ° C. The resulting conjugate was isolated by column gel chromatography (Sephadex G-25) and freeze-dried.
Получают 25 мг конъюгата морфина с ЧСА (М-ЧСА), содержащего 5 молей морфина на моль белка.Get 25 mg of the conjugate of morphine with HSA (M-HSA) containing 5 moles of morphine per mole of protein.
Пример 2. Синтез конъюгатов амфетамина с человеческим сывороточным альбумином (А-ЧСА).Example 2. The synthesis of conjugates of amphetamine with human serum albumin (A-HSA).
D,L-1-фенил-2-аминопропан (5 мг; 0,0369 ммоль) и (14 мг; 0,00022 ммоль) ЧСА растворяют в 3,0 мл 0,1 М фосфатного буфера. По каплям при комнатной температуре и перемешивании к реакционной смеси добавляют 50 мкл (0,4 ммоль) раствора глутарового альдегида. Постепенно реакционная смесь приобретает характерную желтую окраску, свидетельствующую об окончании реакции. Для остановки реакции к смеси добавляют 40 мкл 1М раствора лизина и инкубируют в течение 1 часа.D, L-1-phenyl-2-aminopropane (5 mg; 0.0369 mmol) and (14 mg; 0.00022 mmol) HSA was dissolved in 3.0 ml of 0.1 M phosphate buffer. 50 μl (0.4 mmol) of glutaraldehyde solution are added dropwise at room temperature with stirring. Gradually, the reaction mixture acquires a characteristic yellow color, indicating the end of the reaction. To stop the reaction, 40 μl of a 1M lysine solution was added to the mixture and incubated for 1 hour.
Полученный конъюгат диализируют против фосфатного буфера в течение ночи при температуре 4°С. Выделение конъюгата проводят колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.The resulting conjugate was dialyzed against phosphate buffer overnight at 4 ° C. The conjugate is isolated by column gel chromatography (Sephadex G-25) and freeze-dried.
Получают 5 мг конъюгата (А-ЧСА), содержащего 12 молей амфетамина на моль белка.Get 5 mg of conjugate (A-HSA) containing 12 moles of amphetamine per mole of protein.
Пример 3. Синтез конъюгата кокаина с сывороточным альбумином человека (Кок-ЧСА)Example 3. Synthesis of a conjugate of cocaine with human serum albumin (Kok-HSA)
Конъюгат кокаина с сывороточным альбумином человека (Кок-ЧСА) получают по методике примера 1 из 65 мг (0,001 ммоль) ЧСА и 4,55 мг (0,015 ммоль) бензоилэкгонина.The conjugate of cocaine with human serum albumin (Kok-HSA) is obtained according to the method of example 1 from 65 mg (0.001 mmol) of HSA and 4.55 mg (0.015 mmol) of benzoylegonin.
Выделяют 29 мг конъюгата Кок-ЧСА, содержащего 14 молей кокаина на моль белка.Allocate 29 mg of the Kok-HSA conjugate containing 14 moles of cocaine per mole of protein.
Пример 4. Синтез конъюгата тетрагидроканнабинола с человеческим сывороточным альбумином (Δ9-ТГК-ЧСА).Example 4. Synthesis of a conjugate of tetrahydrocannabinol with human serum albumin (Δ 9 -THC-HSA).
К раствору 21 мг (3,3×10-3 ммоль) ЧСА в 3 мл дистиллированной воды прибавляют раствор 16,6 мг (0,05 ммоль) дельта-9-тетрагидроканнабинола, модифицированного реакцией азосочетания с диазотированной 4-аминобензойной кислотой в 2,0 мл 0,1 М фосфатного буфера, реакционную смесь охлаждают до 0°С и при перемешивании прибавляют 5 мг водорастворимого карбодиимида. Реакционную смесь выдерживают в течение 12 часов в холодильнике, отделяют выпавший осадок мочевины, а полученный конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25).To a solution of 21 mg (3.3 × 10 -3 mmol) of HSA in 3 ml of distilled water, a solution of 16.6 mg (0.05 mmol) of delta-9-tetrahydrocannabinol, modified by the reaction of azo coupling with diazotized 4-aminobenzoic acid in 2, is added. 0 ml of 0.1 M phosphate buffer, the reaction mixture is cooled to 0 ° C and 5 mg of water-soluble carbodiimide are added with stirring. The reaction mixture was kept in the refrigerator for 12 hours, the precipitated urea precipitate was separated, and the resulting conjugate was isolated by column gel chromatography (Sephadex G-25).
Получают 10 мг конъюгата тетрагидроканнабинола с ЧСА (Δ9-ТГК-ЧСА), содержащего 15 молей гаптена на моль белка.10 mg of tetrahydrocannabinol conjugate with HSA (Δ 9 -THC-HSA) containing 15 moles of hapten per mole of protein are obtained.
Пример 5. Синтез конъюгата налтрексона с человеческим сывороточным альбумином (Н-ЧСА).Example 5. Synthesis of conjugate of naltrexone with human serum albumin (N-HSA).
Раствор 65 мг (0,001 ммоль) ЧСА в 17,0 мл дистиллированной воды смешивают с 4,0 мл 0,1 М фосфатного буфера, содержащего 12 мг (0,03 ммоль) сукцинилналтрексона, и при охлаждении по каплям прибавляют раствор 13 мг (0,04 ммоль) водорастворимого карбодиимида в 3 мл дистиллированной воды. Реакционную смесь инкубируют в течение 5 часов при 4°С. Полученный конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.A solution of 65 mg (0.001 mmol) of HSA in 17.0 ml of distilled water is mixed with 4.0 ml of 0.1 M phosphate buffer containing 12 mg (0.03 mmol) of succinylnaltrexone, and a solution of 13 mg (0) is added dropwise. , 04 mmol) of water-soluble carbodiimide in 3 ml of distilled water. The reaction mixture was incubated for 5 hours at 4 ° C. The resulting conjugate was isolated by column gel chromatography (Sephadex G-25) and freeze-dried.
Получают 27 мг конъюгата налтрексона с человеческим сывороточным альбумином (Н-ЧСА), содержащего 17 молей налтрексона на моль белка.Obtain 27 mg of naltrexone conjugate with human serum albumin (H-HSA) containing 17 moles of naltrexone per mole of protein.
Пример 6. Получение конъюгата морфина с лизоцимом (М-Лиз).Example 6. Obtaining a conjugate of morphine with lysozyme (M-Lys).
К раствору 50 мг (3,33×10-3 ммоль) лизоцима в 2,5 мл 0,3 М раствора NaHCO3 прибавляют при охлаждении 0,3 мл раствора смешанного ангидрида 6-сукцинилморфина, полученного из 19,2 мг (0,05 ммоль) 6-сукцинилморфина и 6,0 мкл изобутилхлорформиата. Реакционную смесь инкубируют в течение 18 часов. При 4°С образовавшийся конъюгат морфина с лизоцимом выделяют гель-фильтрацией на колонке с Сефадексом G-25 и лиофильно высушивают.To a solution of 50 mg (3.33 × 10 -3 mmol) of lysozyme in 2.5 ml of a 0.3 M solution of NaHCO 3, 0.3 ml of a solution of mixed 6-succinylmorphine anhydride obtained from 19.2 mg (0, 05 mmol) of 6-succinylmorphine and 6.0 μl of isobutyl chloroformate. The reaction mixture was incubated for 18 hours. At 4 ° C, the resulting morphine-lysozyme conjugate was isolated by gel filtration on a Sephadex G-25 column and freeze-dried.
Получают 30 мг конъюгата морфина с лизоцимом (М-Лиз). Количество присоединенного морфина вычисляют на основе УФ-спектров исходного белка и полученного конъюгата по изменению поглощения при 280 нм. В полученном конъюгате содержится 12 молей морфина на моль белка.30 mg of morphine conjugate with lysozyme (M-Lys) are obtained. The amount of attached morphine is calculated based on the UV spectra of the starting protein and the resulting conjugate from the change in absorbance at 280 nm. The resulting conjugate contains 12 moles of morphine per mole of protein.
Пример 7. Получение конъюгатов морфина с полилизином (М-ПолиЛиз)Example 7. Obtaining conjugates of morphine with polylysine (M-PolyLys)
Раствор 50 мг (0,001 ммоль) полилизина (полиструктура пептидов) в 5,0 мл дистиллированной воды смешивают с 2,0 мл 0,1 М фосфатного буфера, содержащего 15,0 мг (0,039 ммоль) 6-сукцинилморфина, и при охлаждении по каплям прибавляют раствор 15 мг (0,055 ммоль) водорастворимого в 3 мл дистиллированной воды. Реакционную смесь инкубируют в течение 5 часов при 4°С. Полученный конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.A solution of 50 mg (0.001 mmol) of polylysine (peptide polystructure) in 5.0 ml of distilled water is mixed with 2.0 ml of 0.1 M phosphate buffer containing 15.0 mg (0.039 mmol) of 6-succinylmorphine, and dropwise upon cooling a solution of 15 mg (0.055 mmol) of water-soluble in 3 ml of distilled water is added. The reaction mixture was incubated for 5 hours at 4 ° C. The resulting conjugate was isolated by column gel chromatography (Sephadex G-25) and freeze-dried.
Получают 25 мг конъюгата морфина с полилизином (М-ПолиЛиз), содержащего 10 молей морфина на моль белка.Get 25 mg of the conjugate of morphine with polylysine (M-PolyLys) containing 10 moles of morphine per mole of protein.
Пример 8. Получение конъюгатов морфина с полилизином (М-ПолиЛиз)Example 8. Obtaining conjugates of morphine with polylysine (M-PolyLys)
Раствор 27 мг (0,0005 ммоль) полилизина в 30 мл 0,25 М раствора NaHCO3 добавляют к раствору смешанного ангидрида, содержащего 1,0 мг (0,003 ммоль) 3-О-карбоксиметилморфина. Смесь выдерживают при 0°С в течение ночи. Конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.A solution of 27 mg (0.0005 mmol) of polylysine in 30 ml of a 0.25 M NaHCO 3 solution is added to a mixed anhydride solution containing 1.0 mg (0.003 mmol) of 3-O-carboxymethylmorphine. The mixture was kept at 0 ° C. overnight. The conjugate was isolated by column gel chromatography (Sephadex G-25) and freeze-dried.
Получают 20 мг конъюгата морфина с полилизином (М-ПолиЛиз), содержащего 2 моля морфина на моль белка.Get 20 mg of a conjugate of morphine with polylysine (M-PolyLys) containing 2 mol of morphine per mole of protein.
Пример 9. Получение конъюгата Δ9-тетрагидроканнабинола с гамма-глобулином (Δ9-ТГК-гамма-глобулин)Example 9. Obtaining a conjugate of Δ 9 -tetrahydrocannabinol with gamma globulin (Δ 9 -THC-gamma-globulin)
К раствору 15 мг (0,1×10-3 ммоль) гамма-глобулина в 3 мл дистиллированной воды прибавляют раствор 2,0 мг (0,006 ммоль) производного 4-карбосифенил-азо Δ9-тетрагидроканнабинола (каннабиноид) в 1,0 мл 0,1 М фосфатного буфера, охлаждают реакционную смесь до 0°С и при перемешивании добавляют 5 мг водорастворимого карбодиимида. Реакционную смесь выдерживают в течение 12 часов в холодильнике, удаляют выпавший осадок мочевины, конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.To a solution of 15 mg (0.1 × 10 -3 mmol) of gamma globulin in 3 ml of distilled water, a solution of 2.0 mg (0.006 mmol) of 4-carbosiphenyl-azo Δ 9 -tetrahydrocannabinol derivative (cannabinoid) in 1.0 ml is added. 0.1 M phosphate buffer, cool the reaction mixture to 0 ° C and add 5 mg of water-soluble carbodiimide with stirring. The reaction mixture was kept in a refrigerator for 12 hours, the precipitated urea precipitate was removed, the conjugate was isolated by column gel chromatography (Sephadex G-25), and lyophilized.
Получают 12 мг конъюгата Δ9-тетрагидроканнабинола с гамма-глобулином (Δ9-ТГК-гамма-глобулин), содержащего 5 молей Δ9-тетрагидроканнабинола на моль белка.12 mg of Δ 9 -tetrahydrocannabinol conjugate with gamma-globulin (Δ 9 -THC-gamma-globulin) containing 5 moles of Δ 9 -tetrahydrocannabinol per mole of protein are obtained.
Пример 10. Синтез конъюгированных антигенов амфетамина с дифтерийным токсином (А-Дт)Example 10. Synthesis of conjugated amphetamine antigens with diphtheria toxin (A-Dt)
Аналогично примеру 2 используют D,L-1-фенил-2-аминопропан (2 мг; 0,014 ммоль) и 10 мг (0,00016 ммоль) белка дифтерийного токсина, которые растворяют в 2,0 мл 0,1 М фосфатного буфера.Analogously to example 2, D, L-1-phenyl-2-aminopropane (2 mg; 0.014 mmol) and 10 mg (0.00016 mmol) of diphtheria toxin protein are used, which are dissolved in 2.0 ml of 0.1 M phosphate buffer.
Получают 7 мг конъюгата, содержащего 6 молей амфетамина на моль белка.Get 7 mg of conjugate containing 6 moles of amphetamine per mole of protein.
Пример 11. Получение конъюгата барбамила с гамма-глобулином человека (Б-ГГЧ)Example 11. Obtaining a conjugate of barbamil with human gamma globulin (B-hCG)
Аналогично примеру 9 из раствора 15 мг (0,1×10-3 ммоль) гамма-глобулина в 3 мл дистиллированной воды, к которому прибавляют при охлаждении и перемешивании раствор 1,0 мл 0,1 М фосфатного буфера, содержащего 5,2 мг (0,02 ммоль) барбамила (производного барбитуровой кислоты) и 5 мг водорастворимого карбодиимида, получают 10 мг конъюгата барбамила с гамма-глобулином (Б-ГГЧ), содержащего 6 молей барбамила на моль белка.Analogously to example 9, from a solution of 15 mg (0.1 × 10 -3 mmol) of gamma globulin in 3 ml of distilled water, to which a solution of 1.0 ml of 0.1 M phosphate buffer containing 5.2 mg is added with cooling and stirring (0.02 mmol) of barbamyl (a derivative of barbituric acid) and 5 mg of water-soluble carbodiimide, 10 mg of a conjugate of barbamil with gamma globulin (B-hCG) containing 6 moles of barbamil per mole of protein are obtained.
Пример 12. Получение конъюгата налтрексона с гамма-глобулином человека (Н-ГГЧ)Example 12. Obtaining a conjugate of naltrexone with human gamma globulin (N-hCG)
Раствор 50 мг (0,0003 ммоль) гамма-глобулина в 40 мл дистиллированной воды смешивают с 15,0 мл 0,1 М фосфатного буфера, содержащего 30,0 мг (0,07 ммоль) сукцинилналтрексона, и при охлаждении по каплям прибавляют раствор 45 мг (0,16 ммоль) водорастворимого карбодиимида в 10 мл дистиллированной воды. Реакционную смесь инкубируют в течение 5 часов при 4°С. Конъюгат выделяют колоночной гель-хроматографией (Сефадекс G-25) и лиофильно высушивают.A solution of 50 mg (0.0003 mmol) of gamma globulin in 40 ml of distilled water is mixed with 15.0 ml of 0.1 M phosphate buffer containing 30.0 mg (0.07 mmol) of succinylnaltrexone, and the solution is added dropwise with cooling 45 mg (0.16 mmol) of water-soluble carbodiimide in 10 ml of distilled water. The reaction mixture was incubated for 5 hours at 4 ° C. The conjugate was isolated by column gel chromatography (Sephadex G-25) and freeze-dried.
Получают 35 мг конъюгата налтрексона с гамма-глобулином, содержащего 43 моля налтрексона на моль белка (Н-ГГЧ).35 mg of gamma globulin-naltrexone conjugate is obtained containing 43 moles of naltrexone per mole of protein (N-hCG).
3. Получение синтетического иммуногена3. Obtaining a synthetic immunogen
Для получения синтетического иммуногена - комплекса, состоящего из конъюгата макромолекулярного носителя в виде природного или искусственного белка и гаптена - наркотического или психотропного соединения, нековалентно связанного с полимерной матрицей в качестве которой используют сополимер 2-метил-5-винилпиридина и N-винилпирролидона или сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона необходимо соблюдать соотношение гаптена и макромолекулярного носителя в соответствии с предлагаемым изобретением. Коньюгат содержит указанные выше макромолекулярные носители и гаптены в различных соотношениях (Примеры 1-12).To obtain a synthetic immunogen, a complex consisting of a conjugate of a macromolecular carrier in the form of a natural or artificial protein and a hapten, a narcotic or psychotropic compound non-covalently linked to a polymer matrix, a copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone or copolymer 4 is used -vinylpyridine, 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, it is necessary to observe the ratio of hapten and macromolecular carrier in accordance with the invention. The conjugate contains the above macromolecular carriers and haptens in various ratios (Examples 1-12).
Пример 13. Получение иммуногена, состоящего из конъюгата налтрексона с ЧСА (Н-ЧСА), связанного с синтетическим полимером (сополимер 2-метил-5-винилпиридина и N-винилпирролидона, где n=50 мол. % и Мη=15 кДа).Example 13. Obtaining an immunogen consisting of a naltrexone conjugate with HSA (N-HSA) bound to a synthetic polymer (copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, where n = 50 mol% and Mη = 15 kDa).
К раствору 180 мг конъюгата (Н-ЧСА), полученного в примере №5, в 30 мл 0,1 М фосфатного буфера (pH 7,2) добавляют 1600 мг синтетического полимера, представляющего сополимер 2-метил-5-винилпиридина и N-винилпирролидона, с n=50 мол. % и Mη=15 кДа. Смесь выдерживают в течение суток при 20°С. Полученный иммуноген лиофильно высушивают, в результате получают иммуноген, содержащий конъюгат гаптен/Н-ЧСА (12:1) и синтетический полимер в соотношении 1:10, структуру которого характеризуют с помощью ИФА, определяя доступность эпитопов гаптена налтрексона для связывания с антителами к опиатам (Таблица 1, №2).To a solution of 180 mg of the conjugate (H-HSA) obtained in Example No. 5 in 30 ml of 0.1 M phosphate buffer (pH 7.2), 1600 mg of a synthetic polymer representing a copolymer of 2-methyl-5-vinylpyridine and N- vinylpyrrolidone, with n = 50 mol. % and Mη = 15 kDa. The mixture is incubated for 24 hours at 20 ° C. The resulting immunogen is freeze-dried, as a result, an immunogen is obtained containing the hapten / H-HSA conjugate (12: 1) and a synthetic polymer in a ratio of 1:10, the structure of which is characterized by ELISA, determining the availability of hapten naltrexone epitopes for binding to opiate antibodies ( Table 1, No. 2).
Пример 14. Получение иммуногена, состоящего из конъюгата налтрексона с ГГЧ (Н-ГГЧ), связанного с синтетическим полимером (сополимер 2-метил-5-винилпиридина и N-винилпирролидона)Example 14. Obtaining an immunogen consisting of a naltrexone conjugate with hCG (N-hCG) bound to a synthetic polymer (copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone)
К раствору 300 мг конъюгата (Н-ГГЧ), полученного в примере 12, в 80 мл 0,1 М фосфатного буфера (pH 7,2) добавляют 2500 мг синтетического полимера, представляющего собой сополимер 2-метил-5-винил пиридина и N-винилпирролидона, с n=25 мол. % и Мη=45 кДа. Смесь выдерживают в течение суток при 20°С. Очистку иммуногена и его характеризацию осуществляют, как описано в примере 13.To a solution of 300 mg of the conjugate (N-hCG) obtained in Example 12 in 80 ml of 0.1 M phosphate buffer (pH 7.2) was added 2500 mg of a synthetic polymer, a copolymer of 2-methyl-5-vinyl pyridine and N -vinylpyrrolidone, with n = 25 mol. % and Mη = 45 kDa. The mixture is incubated for 24 hours at 20 ° C. Purification of the immunogen and its characterization is carried out as described in example 13.
Получают иммуноген, содержащий конъюгат налтрексон/Н-ГГЧ (43:1) и синтетический полимер в соотношении 1:10. Структуру иммуногена и доступность эпитопов гаптена характеризуют с помощью ИФА (Таблица 1, №1).An immunogen is obtained containing the naltrexone / N-hCG conjugate (43: 1) and a synthetic polymer in a ratio of 1:10. The structure of the immunogen and the availability of hapten epitopes are characterized by ELISA (Table 1, No. 1).
Пример 15. Получение иммуногена, состоящего из конъюгата ЧСА с морфином (М-ЧСА), и связанного с ним синтетическим полимером (сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона, (m+k)=20 мол. %, доля мономерных звеньев 4-винилпиридина составляет 0,05(m+k), Мη=250 кДа).Example 15. Obtaining an immunogen consisting of a conjugate of HSA with morphine (M-HSA) and a synthetic polymer bound thereto (copolymer of 4-vinylpyridine, 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, (m + k) = 20 mol %, the proportion of monomer units of 4-vinylpyridine is 0.05 (m + k), Mη = 250 kDa).
К раствору 13,5 мг синтетического полимера в 2 мл воды апирогенной добавляют 38 мг М-ЧСА, полученного в примере 1, содержащего в качестве гаптена 6-(3-(аминогексиламинокарбонил)-пропионат)морфина, в соотношении 5:1 выдерживают смесь в течение суток при 20°С. Полученный иммуноген характеризуют, как описано в примере 13.To a solution of 13.5 mg of a synthetic polymer in 2 ml of pyrogen-free water, 38 mg of M-HSA obtained in Example 1 containing 6- (3- (aminohexylaminocarbonyl) propionate) morphine as a hapten is added, in a ratio of 5: 1 the mixture is kept in during the day at 20 ° C. The resulting immunogen is characterized as described in example 13.
Получают иммуноген, содержащий конъюгат налтрексон / М-ЧСА (5:1) и синтетический полимер в соотношении 1:10. Структуру иммуногена и доступность эпитопов гаптена характеризуют с помощью ИФА (Таблица 1, №3).An immunogen is obtained containing the naltrexone / M-HSA conjugate (5: 1) and a synthetic polymer in a ratio of 1:10. The structure of the immunogen and the availability of hapten epitopes are characterized by ELISA (Table 1, No. 3).
Пример 16. Получение иммуногена, состоящего из конъюгата ЧСА (М-ЧСА) с морфином, и связанного с ним синтетического полимера (сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона, (m+k)=90 мол. %, доля мономерных звеньев 4-винилпиридина составляет 0,3(m+k), Mη=15 кДа), при соотношении 10 молей синтетического полимера на моль конъюгата.Example 16. Obtaining an immunogen consisting of a conjugate of HSA (M-HSA) with morphine, and the associated synthetic polymer (copolymer of 4-vinylpyridine, 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, (m + k) = 90 mol %, the proportion of monomer units of 4-vinylpyridine is 0.3 (m + k), Mη = 15 kDa), with a ratio of 10 moles of synthetic polymer per mole of conjugate.
Получение проводят аналогично примеру 14, только в качестве исходного соединения берут 6 мг синтетического полимера (сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона, (m+k)=90 мол. %, доля мономерных звеньев 4-винилпиридина составляет 0,3(m+k), Мη=15 кДа) в 2 мл воды апирогенной и 2 мг М-ЧСА, полученного в примере 1, содержащего в качестве гаптена (6-(3-(аминогексиламинокарбонил)-пропионат)морфина.The preparation is carried out analogously to example 14, only 6 mg of a synthetic polymer (copolymer of 4-vinylpyridine, 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, (m + k) = 90 mol.%, The proportion of monomer units 4- vinylpyridine is 0.3 (m + k), Mη = 15 kDa) in 2 ml of pyrogen-free water and 2 mg of M-HSA obtained in Example 1 containing (6- (3- (aminohexylaminocarbonyl) propionate) morphine as a hapten .
Получают иммуноген, содержащий конъюгат морфин/М-ЧСА (5:1) и синтетический полимер в соотношении 1:10. Структуру иммуногена и доступность эпитопов гаптена характеризуют с помощью ИФА (Таблица 1, №4).An immunogen is obtained containing the morphine / M-HSA conjugate (5: 1) and a synthetic polymer in a ratio of 1:10. The structure of the immunogen and the availability of hapten epitopes are characterized by ELISA (Table 1, No. 4).
Пример 17. Получение иммуногена, состоящего из конъюгата полилизин (М-ПолиЛиз) с морфином, связанного с синтетическим полимером (сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона, (m+k)=90 мол. %, доля мономерных звеньев 4-винилпиридина составляет 0,3 (m+k), Мη=15 кДа), при соотношении 1 моль конъюгата на 3 моля полимера.Example 17. Obtaining an immunogen consisting of a conjugate of polylysine (M-PolyLys) with morphine bound to a synthetic polymer (copolymer of 4-vinylpyridine, 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, (m + k) = 90 mol% , the proportion of monomer units of 4-vinylpyridine is 0.3 (m + k), Mη = 15 kDa), with a ratio of 1 mol of conjugate per 3 mol of polymer.
Получение проводят аналогично примеру 14, только в качестве исходных соединений берут 5 мг синтетического полимера (сополимер 4-винилпиридина, 2-метил-5-винилпиридина и N-винилпирролидона, (m+k)=90 мол. %, доля мономерных звеньев 4-винилпиридина составляет 0,3(m+k), Мη=15 кДа), в 2 мл фосфатного буфера и 1,4 мг конъюгата М-ПолиЛиз, полученного в примере 7.The preparation is carried out analogously to example 14, only 5 mg of a synthetic polymer (copolymer of 4-vinylpyridine, 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, (m + k) = 90 mol.%, The proportion of monomer units 4- vinylpyridine is 0.3 (m + k), Mη = 15 kDa) in 2 ml of phosphate buffer and 1.4 mg of the M-PolyLys conjugate obtained in example 7.
Получаемый комплекс имеет 3:1 замещение полимерной матрицы конъюгатом полилизина со спейсером (3-О-карбоксиметилморфина) по 3-му положению молекулы морфина.The resulting complex has a 3: 1 replacement of the polymer matrix with a conjugate of polylysine with a spacer (3-O-carboxymethylmorphine) at the 3rd position of the morphine molecule.
Пример 18. Получение иммуногена, состоящего из конъюгата гамма-глобулина с Δ9-тетрагидроканнабинолом (Δ9-ТГК-гамма-глобулин), связанного с синтетическим полимером (сополимер 2-метил-5-винилпиридина и N-винилпирролидона, где n=25 мол. % и Мη=25 кДа) при соотношении 1 моль конъюгата на 2 моля полимера.Example 18. The preparation of an immunogen consisting of a conjugate of gamma globulin with Δ 9 -tetrahydrocannabinol (Δ 9 -THC-gamma-globulin) bound to a synthetic polymer (copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, where n = 25 mol.% and Mη = 25 kDa) with a ratio of 1 mol of conjugate to 2 mol of polymer.
Получение проводят аналогично примеру 14, только в качестве исходного соединения берут 3,5 мг сополимера 2-метил-5-винилпиридина и N-винилпирролидона, где n=25 мол. % и Мη=25 кДа, в 1 мл фосфатного буфера и 1,2 мг конъюгата Δ9-ТГК-гамма-глобулин, полученного в примере 9. Получаемый комплекс имеет 2:1 замещение полимерной матрицы конъюгатом Δ9-ТГК-гамма-глобулин.The preparation is carried out analogously to example 14, only 3.5 mg of a copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, where n = 25 mol. % and Mη = 25 kDa in 1 ml of phosphate buffer and 1.2 mg of the Δ 9 -THC-gamma-globulin conjugate obtained in Example 9. The resulting complex has a 2: 1 substitution of the polymer matrix with the Δ 9 -THC-gamma-globulin conjugate .
Пример 19. Получение иммуногена, состоящего из конъюгата дифтерийного токсина с амфетамином, связанного с синтетическим полимером (сополимер 2-метил-5-винилпиридина и N-винилпирролидона, где n=23 мол. % и Мη=45 кДа) при соотношении 1 моль конъюгата на 4 моля полимера.Example 19. Obtaining an immunogen consisting of a diphtheria toxin conjugate with amphetamine bound to a synthetic polymer (copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, where n = 23 mol% and Mη = 45 kDa) at a ratio of 1 mol of conjugate for 4 moles of polymer.
Получение проводят аналогично примеру 14, только в качестве исходного соединения берут 3,5 мг сополимера 2-метил-5-винилпиридина и N-винилпирролидона, где n=23 мол. % и Mη=45 кДа в 1 мл фосфатного буфера и 0,9 мг конъюгата амфетамин-дифтерийный токсин, полученного в примере 10.The preparation is carried out analogously to example 14, only 3.5 mg of a copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, where n = 23 mol. % and Mη = 45 kDa in 1 ml of phosphate buffer and 0.9 mg of the amphetamine-diphtheria toxin conjugate obtained in Example 10.
Получаемый комплекс имеет 4:1 замещение полимерной матрицы конъюгатом амфетамин-дифтерийный токсин.The resulting complex has a 4: 1 substitution of the polymer matrix with the amphetamine-diphtheria toxin conjugate.
Пример 20. Получение иммуногена, состоящего из конъюгата гамма-глобулина с барбамилом, связанного с синтетическим полимером (сополимер 2-метил-5-винилпиридина и N-винилпирролидона, где n=20 мол. % и Мη=35 кДа) при соотношении 1 моль конъюгата на 6 молей полимерной матрицыExample 20. Obtaining an immunogen consisting of a conjugate of gamma globulin with barbamil bound to a synthetic polymer (copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, where n = 20 mol% and Mη = 35 kDa) at a ratio of 1 mol conjugate per 6 moles of polymer matrix
Получение проводят аналогично примеру 14, только в качестве исходного соединения берут 3,5 мг сополимера 2-метил-5-винилпиридина и N-винилпирролидона, где n=20 мол. % и Мη=35 кДа в 3 мл фосфатного буфера и 0,5 мг конъюгата барбамил-гамма-глобулин, полученного в примере 11.The preparation is carried out analogously to example 14, only 3.5 mg of a copolymer of 2-methyl-5-vinylpyridine and N-vinylpyrrolidone, where n = 20 mol. % and Mη = 35 kDa in 3 ml of phosphate buffer and 0.5 mg of the conjugate of barbamyl-gamma-globulin obtained in example 11.
Получаемый комплекс имеет 6:1 замещение полимерной матрицы конъюгатом барбамил-гамма-глобулин.The resulting complex has a 6: 1 substitution of the polymer matrix with the conjugate barbamyl-gamma-globulin.
4. Эксперименты in vivo4. In vivo experiments
В экспериментах на животных показано, что полученные синтетические иммуногены способны индуцировать иммунные ответы с появлением антител, специфически взаимодействующих с гаптеном и нейтрализующие их активность в организме. В серии опытов была выяснена возможность нейтрализации токсического действия морфина на животных.In animal experiments, it was shown that the obtained synthetic immunogens are able to induce immune responses with the appearance of antibodies that specifically interact with haptens and neutralize their activity in the body. In a series of experiments, the possibility of neutralizing the toxic effects of morphine on animals was clarified.
Пример 21. Кроличья модель интоксикации морфиномExample 21. Rabbit model of intoxication with morphine
Кроликов распределяют на две группы с учетом возраста и массы тела так, чтобы средние показатели были сопоставимы. Группа контрольных животных состоит из восьми неиммунизированных кроликов, а опытная группа включает восемь кроликов, предварительно иммунизированных синтетическим иммуногеном морфин-ЧСА-синтетический полимер, полученным в примере 13. Для этого в течение месяца с интервалом 7 дней, делают инъекции по 0,2 мл в 4 точки вблизи позвоночника - в области лопаток и в области крестца из расчета в 200 мкг/кг на кролика.Rabbits are divided into two groups based on age and body weight so that the average values are comparable. The control group of animals consists of eight non-immunized rabbits, and the experimental group includes eight rabbits previously immunized with the synthetic immunogen morphine-HSA-synthetic polymer obtained in example 13. To do this, for a month with an interval of 7 days, injections of 0.2 ml per 4 points near the spine - in the area of the scapula and in the sacral region at the rate of 200 μg / kg per rabbit.
Всем животным внутривенно вводят летальную дозу морфина (LD100). Все восемь кроликов контрольной группы погибают от указанной летальной дозы. Среди иммунизированных кроликов гибели не зарегистрировано ни в одном из восьми случаев, т.е. наблюдается высокая иммунологическая защита образовавшимися в процессе иммунизации специфическими антителами.A lethal dose of morphine (LD100) is administered intravenously to all animals. All eight control rabbits die from the indicated lethal dose. Among the immunized rabbits, death was not recorded in any of eight cases, i.e. high immunological protection is observed for specific antibodies formed during the immunization process.
Пример 22. Крысиная модель интоксикации первитиномExample 22. Rat model of pervitin intoxication
Аналогично примеру 21 проводят исследования в двух группах по шесть половозрелых беспородных крыс обоего пола. Животных из опытной группы иммунизируют синтетическим иммуногеном амфетамин-дифтерийный токсин-синтетический полимер из расчета 400 мкг/кг. Всем крысам вводят летальную дозу психоактивного вещества первитина.Analogously to example 21, studies are carried out in two groups of six sexually mature outbred rats of both sexes. Animals from the experimental group are immunized with a synthetic immunogen amphetamine-diphtheria toxin-synthetic polymer at a rate of 400 μg / kg All rats are given a lethal dose of the psychoactive substance Pervitin.
Все животные контрольной группы, не получавшие иммуноген, погибли. Среди иммунизированных крыс гибели не зарегистрировано ни в одном из шести случаев, т.е. наблюдается высокая иммунологическая защита образовавшимися в процессе иммунизации специфическими антителами.All animals of the control group that did not receive the immunogen died. Among the immunized rats, deaths were not recorded in any of the six cases, i.e. high immunological protection is observed for specific antibodies formed during the immunization process.
Пример 23. Крысиная модель интоксикации барбитуратомExample 23. Rat model of barbiturate intoxication
Аналогично примеру 21 шесть половозрелых беспородных крыс обоего пола иммунизируют синтетическим иммуногеном барбамил-гамма-глобулин-синтетический полимер (гаптен из группы производных барбитуровой кислоты) из расчета 200 мкг/кг. Вводят летальную дозу снотворного - барбитурата.Analogously to example 21, six sexually mature outbred rats of both sexes were immunized with a synthetic immunogen barbamyl-gamma-globulin-synthetic polymer (hapten from the group of derivatives of barbituric acid) at a rate of 200 μg / kg. A lethal dose of sleeping pills is introduced - barbiturate.
В контрольной группе погибают все животные. Среди иммунизированных крыс гибели не зарегистрировано ни в одном из шести случаев, т.е. наблюдается полная иммунологическая защита образовавшимися в процессе иммунизации специфическими антителами.In the control group, all animals die. Among the immunized rats, deaths were not recorded in any of the six cases, i.e. complete immunological protection is observed for specific antibodies formed during the immunization process.
Исследования по указанной выше схеме, выполненные для гаптенов, входящих в заявленный состав иммуногена, показали аналогичные результаты.Studies according to the above scheme, performed for haptens included in the claimed composition of the immunogen, showed similar results.
Пример 24. Определение специфичности антител, образующихся при иммунизации синтетическим иммуногеномExample 24. Determination of the specificity of antibodies generated by immunization with a synthetic immunogen
Специфичность определяют в тесте конкуренции ИФА. Для этого в твердофазном ИФА в качестве ингибиторов используют соединения, структурно родственные гаптену, входящему в состав заявленного иммуногена, а также наркотические вещества и ряд психотропных лекарственных препаратов другой химической природы.Specificity is determined in the ELISA competition test. For this, in solid-phase ELISA, as inhibitors, compounds are used that are structurally related to the hapten that is part of the claimed immunogen, as well as narcotic substances and a number of psychotropic drugs of a different chemical nature.
Для каждого из этих соединений определяют концентрацию, при которой происходит 50% торможение взаимодействия антигаптеновых антител, с антигеном на твердой фазе. Специфичность вычисляют как отношение молярных концентраций исследуемого вещества и исходного гаптена и выражают в процентах. Данные о специфичности антител (в %) представлены в таблице 2.For each of these compounds, the concentration is determined at which 50% inhibition of the interaction of antigapten antibodies with the antigen in the solid phase occurs. Specificity is calculated as the ratio of molar concentrations of the test substance to the starting hapten and expressed as a percentage. Data on the specificity of antibodies (in%) are presented in table 2.
По данным таблицы 2 видно, что только иммунные кроличьи антитела к гаптенам, входящим в состав заявляемого иммуногена, не давали перекрестных реакций с соединениями других классов и в значительной степени реагировали со структурно родственными веществами. Так, для иммуногена, состоящего из конъюгата альбумина с налтрексоном (Н-ЧСА), связанного с синтетическим полимером (пример 13), образуются антитела, специфически реагирующие с морфином, героином и в чуть меньшей степени с кодеином. Перекрестные реакции отсутствуют с метадоном, амфетамином, каннабиноидами, кокаином и др. веществами, не относящимися к классу опиатов.According to table 2, it is seen that only immune rabbit antibodies to haptens that are part of the inventive immunogen did not cross-react with compounds of other classes and largely reacted with structurally related substances. So, for an immunogen consisting of an albumin conjugate with naltrexone (N-HSA) bound to a synthetic polymer (Example 13), antibodies are formed that specifically react with morphine, heroin and, to a slightly lesser extent, with codeine. Cross-reactions are absent with methadone, amphetamine, cannabinoids, cocaine and other substances that are not classified as opiates.
Аналогичные результаты получены и для иммуногена, состоящего из конъюгата гамма-глобулина (Н-ГГЧ) с налтрексоном, связанного с синтетическим полимером (пример 14).Similar results were obtained for an immunogen consisting of a gamma globulin conjugate (N-hCG) with naltrexone bound to a synthetic polymer (Example 14).
Для иммуногена, состоящего из конъюгата гамма-глобулина с Δ9-тетрагидроканнабинолом (Δ9-ТГК-ГГЧ), связанного с синтетическим полимером, специфическая реакция антител наблюдается только для каннабиноидов (пример 18). Для иммуногена, состоящего из конъюгата альбумина с амфетамином (пример 19), связанного с синтетическим полимером антитела реагируют с амфетамином и в меньшей степени с метамфетамином при отсутствии реакции со структурами эфедрина, а также с соединениями других классов.For an immunogen consisting of a conjugate of gamma globulin with Δ 9 -tetrahydrocannabinol (Δ 9 -THC-hCG) bound to a synthetic polymer, a specific antibody reaction is observed only for cannabinoids (Example 18). For an immunogen consisting of an albumin conjugate with amphetamine (Example 19) bound to a synthetic polymer, the antibodies react with amphetamine and to a lesser extent with methamphetamine in the absence of reaction with ephedrine structures, as well as with compounds of other classes.
Для иммуногена, состоящего из конъюгата гамма-глобулина с барбамилом Б-ГГЧ), связанного с синтетическим полимером, полученные антитела взаимодействуют с барбамилом и в меньшей степени с фенобарбиталом, не давая перекрестных реакций с соединениями других классов (пример 20).For an immunogen consisting of a conjugate of gamma globulin with barbamil B-hCG) bound to a synthetic polymer, the resulting antibodies interact with barbamil and to a lesser extent phenobarbital, without giving cross-reactions with compounds of other classes (Example 20).
Таким образом, антитела, полученные иммунизацией животных искусственными синтетическими иммуногенами, могут быть использованы для нейтрализации вредного воздействия психоактивного вещества, что в свою очередь может быть использовано для защиты от токсического действия при злоупотреблениях наркотическими и психоактивными веществами.Thus, antibodies obtained by immunizing animals with artificial synthetic immunogens can be used to neutralize the harmful effects of a psychoactive substance, which in turn can be used to protect against toxic effects in the abuse of narcotic and psychoactive substances.
Для подтверждения полученных данных в таблице 3 приведены дополнительные сведения об иммуногенах.To confirm the data obtained, table 3 shows additional information about the immunogens.
СП - синтетический полимерSP - synthetic polymer
КМНГ - конъюгат макромолекулярного носителя с гаптеном.KMNG is a conjugate of a macromolecular carrier with a hapten.
6. Иммунный ответ в крысиной модели6. The immune response in the rat model
Пример 25. Интоксикация первитиномExample 25. Intoxication with Pervitinum
Шесть половозрелых крыс обоего пола иммунизируют синтетическим иммуногеном комплекс с конъюгатом : дифтерийный токсин : амфетамин и синтетическим полимером, полученным в примере 19, из расчета 400 мкг/кг.Six sexually mature rats of both sexes are immunized with a synthetic immunogen complex with a conjugate: diphtheria toxin: amphetamine and the synthetic polymer obtained in Example 19, at a rate of 400 μg / kg.
Лабораторные данные: ИФА 1 мл - 75000 пмоль (через 5 недель после начала иммунизации). Вводили летальную дозу психоактивного вещества первитина.Laboratory data: ELISA 1 ml - 75000 pmol (5 weeks after the start of immunization). A lethal dose of the psychoactive substance Pervitin was administered.
Контрольные лабораторные данные: ИФА 1 мл - 54000 пмоль. Синтез антител, отсутствие аллергических реакций.Control laboratory data: ELISA 1 ml - 54000 pmol. Antibody synthesis, lack of allergic reactions.
Пример 26. Интоксикация барбитуратомExample 26. Intoxication with barbiturate
Шесть половозрелых крыс обоего пола иммунизируют синтетическим иммуногеном комплекса с конъюгатом гамма-глобулин : барбамил : синтетическим полимером, полученным в примере 20, из расчета 500 мкг/кг.Six sexually mature rats of both sexes are immunized with a synthetic immunogen complex with a gamma-globulin: barbamyl conjugate: the synthetic polymer obtained in Example 20, at a rate of 500 μg / kg.
Лабораторные данные: ИФА 1 мл - 76000 пмоль (через 5 недель после начала иммунизации). Вводили летальную дозу снотворного - барбитурата.Laboratory data: ELISA 1 ml - 76000 pmol (5 weeks after the start of immunization). A lethal dose of sleeping pills, barbiturate, was administered.
Контрольные лабораторные данные: ИФА 1 мл - 57000 пмоль. Синтез антител; отсутствие аллергических реакций.Control laboratory data: ELISA 1 ml - 57000 pmol. Synthesis of antibodies; lack of allergic reactions.
Пример 27. Интоксикация героиномExample 27. Heroin Intoxication
Шесть половозрелых крыс обоего пола иммунизируют синтетическим иммуногеном комплекс с конъюгатом овальбумин : морфин : синтетическим полимером, полученным в примере 15, из расчета 300 мкг/кг.Six sexually mature rats of both sexes were immunized with a synthetic immunogen complex with an ovalbumin: morphine conjugate: the synthetic polymer obtained in Example 15, at a rate of 300 μg / kg.
Лабораторные данные: ИФА 1 мл - 85000 пмоль специфических антител к героину (через 4 недели после начала иммунизации). Вводили летальную дозу наркотического вещества героина 100 мг/кг.Laboratory data: ELISA 1 ml - 85000 pmol of specific antibodies to heroin (4 weeks after the start of immunization). A lethal dose of a heroin narcotic of 100 mg / kg was administered.
Контрольные лабораторные данные: ИФА 1 мл - 60000 пмоль. Синтез антител; отсутствие аллергических реакций.Control laboratory data: ELISA 1 ml - 60,000 pmol. Synthesis of antibodies; lack of allergic reactions.
Как видно из приведенных примеров и данных таблицы 3, введение заявляемого синтетического иммуногена позволяет вызывать образование в организме антител и стабильный иммунный ответ, что приводит к детоксикации организма в отношении соответствующих психоактивных и наркотических веществ.As can be seen from the above examples and the data of table 3, the introduction of the inventive synthetic immunogen can cause the formation of antibodies in the body and a stable immune response, which leads to detoxification of the body in relation to the corresponding psychoactive and narcotic substances.
Claims (8)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2016136844A RU2643329C1 (en) | 2016-09-14 | 2016-09-14 | Synthetic immunogen for protection and treatment of psychoactive substances addiction |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2016136844A RU2643329C1 (en) | 2016-09-14 | 2016-09-14 | Synthetic immunogen for protection and treatment of psychoactive substances addiction |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2643329C1 true RU2643329C1 (en) | 2018-01-31 |
Family
ID=61173442
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2016136844A RU2643329C1 (en) | 2016-09-14 | 2016-09-14 | Synthetic immunogen for protection and treatment of psychoactive substances addiction |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2643329C1 (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2703494C1 (en) * | 2018-11-12 | 2019-10-18 | Федеральное государственное унитарное предприятие "Государственный научно-исследовательский институт особо чистых биопрепаратов" Федерального медико-биологического агентства | Monoclonal antibody 6g1 to morphine derivatives |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2000004C1 (en) * | 1992-07-16 | 1993-02-15 | Фармацевтическая фирма "Ковидон" | Copolymers of 2-methyl-5-vinylpyridine and n-vinylpyrrolidone showing immunostimulation effect |
| EP1329226A2 (en) * | 1995-03-31 | 2003-07-23 | Xenova Research Limited | Hapten-Carrier Conjugates for use in Drug Abuse Therapy |
| RU2459838C1 (en) * | 2011-10-05 | 2012-08-27 | Станислав Анатольевич Кедик | Copolymer containing n-vinyl pyrrolidone, 2-methyl-5-vinyl pyridine and 4-vinyl pyridine links |
| RU2471478C1 (en) * | 2011-12-08 | 2013-01-10 | Станислав Анатольевич Кедик | Pharmaceutical composition for treating alcoholism, drug addiction and chemical abuse with improved naltrexone release profile |
-
2016
- 2016-09-14 RU RU2016136844A patent/RU2643329C1/en active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2000004C1 (en) * | 1992-07-16 | 1993-02-15 | Фармацевтическая фирма "Ковидон" | Copolymers of 2-methyl-5-vinylpyridine and n-vinylpyrrolidone showing immunostimulation effect |
| EP1329226A2 (en) * | 1995-03-31 | 2003-07-23 | Xenova Research Limited | Hapten-Carrier Conjugates for use in Drug Abuse Therapy |
| RU2459838C1 (en) * | 2011-10-05 | 2012-08-27 | Станислав Анатольевич Кедик | Copolymer containing n-vinyl pyrrolidone, 2-methyl-5-vinyl pyridine and 4-vinyl pyridine links |
| RU2471478C1 (en) * | 2011-12-08 | 2013-01-10 | Станислав Анатольевич Кедик | Pharmaceutical composition for treating alcoholism, drug addiction and chemical abuse with improved naltrexone release profile |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2703494C1 (en) * | 2018-11-12 | 2019-10-18 | Федеральное государственное унитарное предприятие "Государственный научно-исследовательский институт особо чистых биопрепаратов" Федерального медико-биологического агентства | Monoclonal antibody 6g1 to morphine derivatives |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8357375B2 (en) | Process for the preparation and use of a bivalent vaccine against morphine-heroine addiction | |
| Jalah et al. | Efficacy, but not antibody titer or affinity, of a heroin hapten conjugate vaccine correlates with increasing hapten densities on tetanus toxoid, but not on CRM197 carriers | |
| RU2236257C1 (en) | Synthetic immunogen for therapy and prophylaxis of addiction with narcotic and psychoactive substances | |
| De Weck et al. | The Role of Penicilloylated Protein Impurities, Penicillin Polymers and Dimers in Penicillin Allergy (Part 1 of 2) | |
| WO1993012145A1 (en) | Pva or peg conjugates of peptides for epitope-specific immunosuppression | |
| AU7050091A (en) | Vaccine and immunoserum against drugs of abuse | |
| US20190240306A1 (en) | Anti-opioid vaccines | |
| RU2643329C1 (en) | Synthetic immunogen for protection and treatment of psychoactive substances addiction | |
| RU2635517C1 (en) | Synthetic immunogen for protection and treatment of psychoactive substances addiction | |
| JP2007537972A (en) | Monoclonal antibodies specific for buprenorphine and its metabolites | |
| CA2211385C (en) | N-1-carboxyalkyl derivatives of lsd | |
| Liu et al. | Preparation of anti‐danofloxacin antibody and development of an indirect competitive enzyme‐linked immunosorbent assay for detection of danofloxacin residue in chicken liver | |
| RU2526807C2 (en) | Synthetic immunogen for protection against toxic action of narcotic and psychoactive substances | |
| JP2008523011A (en) | Saquinavir derivatives useful in immunoassays | |
| WO2013147586A1 (en) | A method for preparing an immunogen and a use thereof | |
| JP2004514655A (en) | Vaccine immunogen containing disulfide-bridged cyclized peptide and its use in treating allergy | |
| US4835258A (en) | Conjugation of aromatic amines or nitro-containing compounds with proteins or polypeptides by photoirradiation of the azide derivatives with ultraviolet light in order to produce antibodies against the haptens | |
| EP2716659B1 (en) | Immunoassays for meperidine and metabolites | |
| De Weck | Immunochemical particularities of anaphylactic reactions to compounds used in anaesthesia | |
| RU2548802C1 (en) | Immunogen for treating and preventing opiate addiction | |
| EP2698383A1 (en) | Detection of synthetic Cannabinoids | |
| EP3185015A1 (en) | Opioid detection | |
| Sahui‐Gnassi et al. | Selective antibodies to propranolol enantiomers produced from a new conjugate | |
| JPH01269485A (en) | Cell line capable of producing monoclonal antibody and monoclonal antibody | |
| SU1573427A1 (en) | Method of determining theophylline in blood serum |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PD4A | Correction of name of patent owner |