RU2625754C1 - Combined drug of anxiolithic, stress-protector, nootropic and antioxidant action - Google Patents
Combined drug of anxiolithic, stress-protector, nootropic and antioxidant action Download PDFInfo
- Publication number
- RU2625754C1 RU2625754C1 RU2016123907A RU2016123907A RU2625754C1 RU 2625754 C1 RU2625754 C1 RU 2625754C1 RU 2016123907 A RU2016123907 A RU 2016123907A RU 2016123907 A RU2016123907 A RU 2016123907A RU 2625754 C1 RU2625754 C1 RU 2625754C1
- Authority
- RU
- Russia
- Prior art keywords
- tryptophan
- stress
- nootropic
- thiotriazoline
- anxiolytic
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/095—Sulfur, selenium, or tellurium compounds, e.g. thiols
- A61K31/10—Sulfides; Sulfoxides; Sulfones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/405—Indole-alkanecarboxylic acids; Derivatives thereof, e.g. tryptophan, indomethacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4196—1,2,4-Triazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2121/00—Preparations for use in therapy
Abstract
Description
Изобретение относится к фармации и медицине, и может быть использовано в фармацевтической промышленности при изготовлении медикаментозных средств с комбинированным составом активных компонентов, которые применяются для лечения и профилактики заболеваний центральной нервной системы, сопровождающихся такими состояниями организма, как тревога, беспокойство, страх, эмоциональное напряжение, в основе которых лежит стресс. Также действие предлагаемого средства будет направлено на устранение психосоматических расстройств при неврозах, неврозоподобных состояниях, абстиненции, алкоголизме, наркомании.The invention relates to pharmacy and medicine, and can be used in the pharmaceutical industry in the manufacture of medicines with a combined composition of active ingredients that are used to treat and prevent diseases of the central nervous system, accompanied by such conditions of the body as anxiety, anxiety, fear, emotional stress, based on stress. Also, the action of the proposed tool will be aimed at eliminating psychosomatic disorders in case of neurosis, neurosis-like conditions, withdrawal symptoms, alcoholism, and drug addiction.
Уменьшение длительности, а также ухудшение качества жизни прямо связано с увеличением количества больных с заболеваниями ЦНС, в этногенезе которых лежит стресс [10]. В этой связи, разработка мер фармакологической коррекции эмоционального стресса является одной из актуальных задач современной медицины. Известно [1, 2, 10, 11], что одним из звеньев патогенеза эмоционального стресса является гиперпродукция активных форм кислорода (АФК) биоэнергетическими и нейрохимическими системами головного мозга. Избыток АФК в условиях антиоксидантной недостаточности приводит к окислительной модификации липидов, нуклеиновых кислот и белков. Окислительная модификация белковых фрагментов рецепторов, ионных каналов, синаптических структур нейрона приводит к нарушению генерации, образования, проводимости нервного импульса, нарушает синаптическую передачу и, как следствие, приводит к ухудшению когнитивно-мнестических функций головного мозга [1, 2, 13]. Известно также, что под действием АФК в клетке происходит активация экспрессии редокс-чувствительных генов, одни из которых необходимы для защиты клеток от токсических эффектов окислительного стресса, а другие, при избытке АФК, инициируют апоптоз [1, 15]. В связи с вышеизложенным, перспективным направлением фармакокоррекции стресса и его последствий является применение антиоксидантов, ноотропов, анксиолитиков [2, 3]. Широкое применение в клинической практике в качестве стресспротекторов и анксиолитиков нашли структурные аналоги нейротрансмиттеров - ноофен, глицин, ГАМК, триптофан [2].A decrease in duration, as well as a deterioration in the quality of life, is directly related to an increase in the number of patients with central nervous system diseases whose ethnogenesis is stress [10]. In this regard, the development of measures for pharmacological correction of emotional stress is one of the urgent tasks of modern medicine. It is known [1, 2, 10, 11] that one of the links in the pathogenesis of emotional stress is the overproduction of reactive oxygen species (ROS) by the bioenergetic and neurochemical systems of the brain. Excess ROS in conditions of antioxidant deficiency leads to oxidative modification of lipids, nucleic acids and proteins. Oxidative modification of protein fragments of receptors, ion channels, synaptic structures of a neuron leads to impaired generation, formation, conduction of a nerve impulse, disrupts synaptic transmission and, as a result, leads to a deterioration in the cognitive-mnemonic functions of the brain [1, 2, 13]. It is also known that, under the influence of ROS, the expression of redox-sensitive genes is activated in the cell, some of which are necessary to protect cells from the toxic effects of oxidative stress, while others, with an excess of ROS, initiate apoptosis [1, 15]. In connection with the above, a promising direction of pharmacocorrection of stress and its consequences is the use of antioxidants, nootropics, anxiolytics [2, 3]. Structural analogues of neurotransmitters, such as noofen, glycine, GABA, and tryptophan, have found widespread use in clinical practice as stress protectors and anxiolytics [2].
В последнее время также прослеживается тенденция создания комбинированных лекарственных средств с ноотропным действием, способных восстанавливать нарушенные мнестические и мыслительные функции, снижать неврологические дефициты, а также защищать мозг и повышать резистентность организма к экстремальным воздействиям.Recently, there has also been a tendency to create combined drugs with a nootropic effect that can restore impaired mental and mental functions, reduce neurological deficits, and also protect the brain and increase the body's resistance to extreme influences.
Однако современный арсенал анксиолитических, ноотропных, стресспротекторных, антиоксидантных средств не всегда отвечает всем требованиям клиницистов. Чаще всего такие препараты назначаются в виде отдельных лекарственных форм, что приводит к полипрагмазии, снижает комплайенс пациентов. Иногда препараты бывают недостаточно эффективными. Все это обусловливает необходимость создания новых комбинированных высокоэффективных и малотоксичных препаратов, которые бы совмещали в себе позитивные эффекты активных действующих веществ или же даже усиливали бы их терапевтический эффект.However, the modern arsenal of anxiolytic, nootropic, stress-protective, antioxidant agents does not always meet all the requirements of clinicians. Most often, such drugs are prescribed in the form of separate dosage forms, which leads to polypharmacy, reduces the compliance of patients. Sometimes drugs are not effective enough. All this necessitates the creation of new combined highly effective and low-toxic drugs that would combine the positive effects of active active substances or even enhance their therapeutic effect.
Известен комбинированный препарат Тиоцетам, который в своем составе содержит тиотриазолин и пирацетам (0,05 г тиотриазолина и 0,2 г пирацетама). Препарат обладает выраженным антиоксидантным, противоишемическим, ноотропным и церебропротективным действием [2, 6, 8, 9]. Однако Тиоцетам не обладает анксиолитическими свойствами и у него недостаточно выражена стресс-протекторная активность.Known combination drug Thiocetam, which in its composition contains thiotriazolin and piracetam (0.05 g of thiotriazolin and 0.2 g of piracetam). The drug has a pronounced antioxidant, anti-ischemic, nootropic and cerebroprotective effect [2, 6, 8, 9]. However, Thiocetam does not have anxiolytic properties and it does not have enough pronounced stress-protective activity.
Известно также средство Ноофен (активное вещество - фенибут, (γ-амино-β-фенилмасляная кислота) для перорального применения (Компендиум - лекарственные препараты online http://compendium.com.ua/info/262/olajnfarm/noofen-sup-sup-500-mg-i-poroshok-i-), которое обладает антигипоксическим, антиамнестическим и анксиолитическим (транквилизирующим) действием. Ноофен стимулирует процессы обучения, улучшает память, повышает физическую и умственную деятельность. Также Ноофен обладает транквилизирующими особенностями: устраняет психоэмоциональное напряжение, тревожность, страх, эмоциональную лабильность, раздражительность, улучшает сон; удлиняет и усиливает действие снотворных, наркотических, нейролептических и противосудорожных средств. Под влиянием Ноофена улучшаются показатели высшей нервной деятельности (внимание, память, скорость и точность сенсорно-моторных реакций). Препарат удлиняет латентный период и сокращает продолжительность и выраженность нистагма, обладает противоэпилептическим эффектом. Не влияет на холино- и адренорецепторы. Ноофен заметно уменьшает проявления астении и вазовегетативные симптомы, в том числе головную боль, ощущение тяжести в голове. У больных с астенией и у эмоционально лабильных пациентов уже с первых дней терапии препаратом улучшается самочувствие, повышается интерес и инициативность, мотивация к активной деятельности без седативного эффекта или возбуждения. Установлено, что при приеме Ноофена при черепно-мозговой травме увеличивается количество митохондрий в клетках перифокальных тканей и улучшаются биоэнергетические процессы в мозгу. При наличии нарушений деятельности сердца и желудка нормализует процессы пероксидации липидов.Noofen is also known (the active substance is phenibut, (γ-amino-β-phenylbutyric acid) for oral use (Compendium - drugs online http://compendium.com.ua/info/262/olajnfarm/noofen-sup-sup -500-mg-i-poroshok-i-), which has antihypoxic, antiamnestic and anxiolytic (tranquilizing) effects.Noofen stimulates learning processes, improves memory, increases physical and mental activity.Noofen also has tranquilizing features: eliminates psychoemotional stress, anxiety , fear, emotions onal lability, irritability, improves sleep; prolongs and enhances the effect of sleeping pills, drugs, antipsychotics and anticonvulsants. Under the influence of Noofen, higher nervous activity indicators (attention, memory, speed and accuracy of sensory-motor reactions) improve. The drug lengthens the latent period and reduces the duration and the severity of nystagmus, has an antiepileptic effect. Does not affect choline and adrenoreceptors. Noofen significantly reduces the manifestations of asthenia and vasovegetative symptoms, including headache, a feeling of heaviness in the head. In patients with asthenia and in emotionally labile patients, from the first days of treatment with the drug, their health improves, interest and initiative increase, motivation for active work without a sedative effect or arousal. It has been established that when taking Noofen during traumatic brain injury, the number of mitochondria in the cells of perifocal tissues increases and bioenergetic processes in the brain improve. In the presence of disturbances in the activity of the heart and stomach, it normalizes the processes of lipid peroxidation.
Однако спектр ноотропного действия Ноофена весьма узок - препарат проявляет только антиамнестическое действие (влияя на кратковременную память), не влияя на долговременную память, на уровень суждений, кортикальный контроль (http://gomelpsyhosp.by/?p=1080). Ноофен проявляет ряд побочных эффектов, что ограничивает его применение в клинической практике, особенно педиатрической и геронтологической. Препарат может вызывать зависимость, имеет синдром отмены (http://otravleniya.net/ximicheskie-otravleniya/fenibut-privykanie.html). Имеются данные, что Ноофен при длительном применении может оказывать на печень негативное влияние.However, the spectrum of nootropic action of Noofen is very narrow - the drug exhibits only an antiamnestic effect (affecting short-term memory), without affecting long-term memory, level of judgment, cortical control (http://gomelpsyhosp.by/?p=1080). Noofen has a number of side effects, which limits its use in clinical practice, especially pediatric and gerontological. The drug can be addictive, has withdrawal syndrome (http://otravleniya.net/ximicheskie-otravleniya/fenibut-privykanie.html). There is evidence that Noofen with prolonged use may have a negative effect on the liver.
Известно средство Триптофан (http://www.likar.info/lekarstva/Triptofan/), которое является предшественником нейротрансмиттера серотонина. Триптофан способствует повышению настроения, снятию тревожности, гиперактивности, навязчивых состояний и синдрома хронической усталости, устраняет чувство страха и напряжения, способствует хорошему засыпанию и нормальному сну.Tryptophan is known (http://www.likar.info/lekarstva/Triptofan/), which is a precursor to the neurotransmitter serotonin. Tryptophan helps to improve mood, relieve anxiety, hyperactivity, obsessive states and chronic fatigue syndrome, eliminates feelings of fear and tension, and contributes to good sleep and normal sleep.
Однако триптофан не имеет выраженного самостоятельного ноотропного, стресс-протективного и антиоксидантного действия.However, tryptophan does not have a pronounced independent nootropic, stress-protective and antioxidant effect.
Бесспорный интерес представляет поиск возможностей усиления протекторных свойств триптофана за счет комбинирования с веществами, способными улучшать энергообеспечение головного мозга, проявлять антиоксидантное действие и тормозить оксидативный стресс и тем самым восстанавливать чувствительность рецепторов нейрона. К таким веществам относят тиотриазолин. Тиотриазолин способен усилить анксиолитическое действие триптофана, регулируя Red/Oxi - зависимые механизмы повышения аффинности к серотониновым рецепторам. Триптофан, в свою очередь, может усилить антиоксидантное действие тиотриазолина. Так, триптофан, посредством превращения в организме в мелатонин, сможет образовать с тиотриазолином своеобразный тандем по утилизации таких зловещих кислородных радикалов, как гидроксил-радикал и пероксинитрит. Триптофан совместно с тиотриазолином способны оказывать влияние на механизмы памяти как кратковременной - за счет подавления амнезии, вызванной избытком свободных радикалов, так и долговременной - за счет совместного влияния на АТФ-зависимые механизмы синтеза белков памяти.Of undoubted interest is the search for ways to enhance the protective properties of tryptophan by combining with substances that can improve the energy supply of the brain, exhibit antioxidant effects and inhibit oxidative stress, and thereby restore the sensitivity of neuron receptors. These substances include thiotriazolin. Thiotriazolin is able to enhance the anxiolytic effect of tryptophan by regulating Red / Oxi-dependent mechanisms for increasing affinity for serotonin receptors. Tryptophan, in turn, can enhance the antioxidant effect of thiotriazoline. So, tryptophan, by converting it to melatonin in the body, can form a kind of tandem with thiotriazoline to utilize such ominous oxygen radicals as hydroxyl radical and peroxynitrite. Tryptophan together with thiotriazolin can affect the memory mechanisms both short-term - by suppressing amnesia caused by an excess of free radicals, and long-term - due to the joint effect on ATP-dependent mechanisms of the synthesis of memory proteins.
Подобное совместное действие триптофана и тиотриазолина, направленное на регуляцию Red/Oxi - зависимых механизмов аффинности серотониновых рецепторов, восстановление функции этой системы (снижение тревоги, страха, нарушения сна, беспокойства), а также на усиление антиоксидатного и энерготропного действия (процессы памяти), можно использовать в профилактике и лечении заболеваний, важным звеном патогенеза которых является стресс, а это - заболевания центральной нервной и сердечно-сосудистой системы.A similar combined effect of tryptophan and thiotriazolin, aimed at regulating Red / Oxi - dependent mechanisms of the affinity of serotonin receptors, restoring the function of this system (reducing anxiety, fear, sleep disturbance, anxiety), as well as enhancing the antioxidant and energetic effects (memory processes), can use in the prevention and treatment of diseases whose important pathogenesis is stress, and these are diseases of the central nervous and cardiovascular system.
В основу изобретения поставлена задача разработки комбинированного лекарственного средства, которое будет обладать более высокой анксиолитической и антиоксидантной активностью по сравнению с известными средствами, и дополнительно будет оказывать ноотропное и стресс-протективное действие.The basis of the invention is the task of developing a combined drug that will have a higher anxiolytic and antioxidant activity compared to known means, and will additionally have a nootropic and stress-protective effect.
Поставленная задача решается тем, что в комбинированном лекарственном средстве анксиолитического, стресс-протективного, ноотропного и антиоксидантного действия, содержащем триптофан, новым является то, что он дополнительно содержит тиотриазолин.The problem is solved in that in the combined drug anxiolytic, stress-protective, nootropic and antioxidant effects containing tryptophan, the new is that it additionally contains thiotriazoline.
Новым также является то, что комбинированное лекарственное средство анксиолитического, стресс-протективного, ноотропного и антиоксидантного действия содержит триптофан и тиотриазолин в следующем соотношении: триптофан - в пределах от 1 до 7 массовых долей, тиотриазолин - 1 массовая доля.Also new is the fact that the combined drug of anxiolytic, stress-protective, nootropic and antioxidant action contains tryptophan and thiotriazoline in the following ratio: tryptophan - in the range from 1 to 7 mass fractions, thiotriazoline - 1 mass fraction.
Новым также является то, что комбинированное лекарственное средство анксиолитического, стресс-протективного, ноотропного и антиоксидантного действия имеет форму таблеток, капсул, инъекционных и инфузионных растворов.Also new is the fact that the combined drug of anxiolytic, stress-protective, nootropic and antioxidant action takes the form of tablets, capsules, injection and infusion solutions.
Исходя из изученных механизмов действия обоих компонентов предлагаемого комбинированного средства, содержащего триптофан и тиотриазолин, и предположив возможность того, что предлагаемое комбинированное средство может иметь более эффективное анксиолитическое и антиоксидантное действие, было проведено экспериментальное исследование в этом направлении.Based on the studied mechanisms of action of both components of the proposed combination agent containing tryptophan and thiotriazoline, and suggesting the possibility that the proposed combination agent may have a more effective anxiolytic and antioxidant effect, an experimental study was conducted in this direction.
При проведении экспериментальных исследований, которые подтвердили предположение, было обнаружено дополнительное неочевидное свойство комбинации триптофана с тиотриазолином - ее ноотропное и стресс-протективное действие, а также усиление анксиолитического и антиоксидантного эффекта.When conducting experimental studies that confirmed the hypothesis, an additional non-obvious property of the combination of tryptophan with thiotriazoline was discovered - its nootropic and stress-protective effect, as well as an increase in the anxiolytic and antioxidant effect.
Были изучены разные комбинации тиотриазолина с триптофаном - 1:1; 1:2; 1:4; 1:5; 1:7 соответственно, в условиях теста «подвешивания за хвост». Была выявлена оптимальная комбинация тиотриазолина с триптофаном - 1:4. Ниже в таблице 1 приводятсяч данные, которые это подтверждают.Various combinations of thiotriazolin with tryptophan - 1: 1 were studied; 1: 2; 1: 4; 1: 5; 1: 7, respectively, in the conditions of the test "hanging by the tail." The optimal combination of thiotriazoline with tryptophan - 1: 4 was revealed. Table 1 below provides data that confirms this.
Анксиолитическое действие комбинированного препарата с разным соотношением активных компонентов (тиотриазолина с триптофаном) изучали на 50 белых нелинейных крысах обоего пола массой 170-230 г. Блиц-тестом, применение которого возможно для определения уровня тревожности и выяснения анксиопрофиля препаратов, является подвешивание животного за хвост. Метод основан на наблюдении, что животные, при их подвешивании за хвост, будут демонстрировать соответствующий период иммобильности, по продолжительности которого можно судить об уровне тревожности, страха и отчаяния. Комбинации тиотриазолина с триптофаном вводили в дозе 250 мг/кг внутрижелудочно в виде водного раствора с помощью металлического зонда за 60 мин до тестирования. После введения исследуемых комбинаций животное вытаскивалось из клетки и придерживалось за хвост возле туловища в висячем положении головой вниз. Регистрировалось время, в течение которого животное будет оставаться иммобильным (т.е. до того момента, пока морда животного не достигнет основания хвоста) [10, 14].The anxiolytic effect of the combined preparation with a different ratio of active components (thiotriazoline with tryptophan) was studied in 50 nonlinear white rats of both sexes weighing 170-230 g. A blitz test, the use of which is possible to determine the level of anxiety and ascertain the anxioprofile of drugs, is by hanging the animal by the tail. The method is based on the observation that animals, when suspended by the tail, will demonstrate an appropriate period of immobility, the duration of which can be used to judge the level of anxiety, fear and despair. Combinations of thiotriazolin with tryptophan were administered at a dose of 250 mg / kg intragastrically as an aqueous solution using a metal probe 60 minutes before testing. After the introduction of the studied combinations, the animal was pulled out of the cage and held by the tail near the body in a hanging position, head down. The time was recorded during which the animal would remain immobilized (that is, until the animal's muzzle reached the base of the tail) [10, 14].
В результате проведенных исследований было установлено, что наиболее активной оказалась комбинация тиотриазолина и триптофана в соотношении 1:4 соответственно, но при этом комбинации с соотношением 1:1; 1:2; 1:5 и 1:7 также являются терапевтически эффективными.As a result of the studies, it was found that the combination of thiotriazoline and tryptophan in the ratio of 1: 4, respectively, but the combination with the ratio of 1: 1, turned out to be the most active; 1: 2; 1: 5 and 1: 7 are also therapeutically effective.
Как известно (Кукес В.Г. Клиническая фармакология, 4 издание, Москва, «ГЕОТАР-медиа», 2008, с. 164-169; Гилман А.Г. Клиническая фармакология по Гудману и Гилману, Москва, «Практика», 2006, с. 57), фармакодинамическое взаимодействие лекарственных средств может быть направлено как в сторону усиления их фармакологических эффектов, так и на их ослабление. Поэтому, хотя тиотриазолин и триптофан оказывают каждый в отдельности широкий спектр положительных фармакологических эффектов, для специалиста не является очевидной возможность использовать тиотриазолин или триптофан в сочетании с любыми другими лекарственными средствами.As is known (Kukes V.G. Clinical Pharmacology, 4th edition, Moscow, “GEOTAR-Media”, 2008, pp. 164-169; Gilman A.G. Clinical Pharmacology according to Goodman and Gilman, Moscow, “Practice”, 2006, p. 57), the pharmacodynamic interaction of drugs can be directed both towards enhancing their pharmacological effects, and to weaken them. Therefore, although thiotriazoline and tryptophan each have a wide range of positive pharmacological effects, it is not obvious to a specialist that thiotriazoline or tryptophan can be used in combination with any other drugs.
Также лекарственные средства могут иметь физическую несовместимость. Она обусловлена физическими свойствами ингредиентов, которые входят в состав лекарств, и может вызываться нерастворимостью, отволаживанием ингредиентов, другими процессами.Also, drugs may have physical incompatibility. It is due to the physical properties of the ingredients that make up the drug, and can be caused by insolubility, smoothing of the ingredients, and other processes.
Компоненты предлагаемого комбинированного лекарственного средства могут быть также химически несовместимыми, что обусловлено их химическим взаимодействием. Это приводит, как правило, к снижению или полной потере терапевтической активности лекарственного средства.The components of the proposed combined drug may also be chemically incompatible, due to their chemical interaction. This usually leads to a decrease or complete loss of therapeutic activity of the drug.
Лекарственные вещества могут действовать антагонистично или взаимно усиливать побочное или токсическое действие друг друга, и, таким образом, иметь фармакологическую несовместимость. Фармакологическая несовместимость лекарственных веществ во многих случаях исключает возможность их одновременного применения. Несовместимые сочетания компонентов делают фиксированную лекарственную комбинацию неполноценной в терапевтическом отношении, а в некоторых случаях даже опасной для жизни пациента.Medicinal substances can act antagonistically or mutually reinforce each other's side or toxic effects, and thus have pharmacological incompatibility. The pharmacological incompatibility of drugs in many cases precludes the possibility of their simultaneous use. Incompatible combinations of components make the fixed drug combination therapeutic inferior, and in some cases even life-threatening to the patient.
Также не является очевидным то, что, если назначать в схеме лечения лекарственные средства с разными действующими веществами в разных лекарственных формах, и назначить средство, которое содержит эти же действующие вещества, скомбинированные в одной лекарственной форме, то эффект будет одинаковым.It is also not obvious that if you prescribe drugs with different active substances in different dosage forms in the treatment regimen and prescribe a drug that contains the same active substances combined in one dosage form, the effect will be the same.
Таким образом, возможность создания определенного комбинированного лекарственного средства может подтвердить или опровергнуть лишь экспериментальное исследование. В нашем случае - это сочетание триптофана с тиотриазолином.Thus, the possibility of creating a specific combination drug can only confirm or refute an experimental study. In our case, this is a combination of tryptophan with thiotriazolin.
Говорить о положительном результате взаимодействия упомянутых компонентов комбинированного лекарственного средства можно только на основании проведенных экспериментальных исследований. Без изучения результатов таких исследований мысль о возможном высоком терапевтическом эффекте комбинированного средства является лишь теоретической предпосылкой.Talking about the positive result of the interaction of the above components of the combined drug can only be based on experimental studies. Without studying the results of such studies, the idea of a possible high therapeutic effect of the combined agent is only a theoretical premise.
В данной заявке приведены результаты оригинальных исследований предложенной комбинации, которые подтверждают высокую анксиолитическую, стресс-протекторную, ноотропную и антиоксидантную активность комбинированного препарата, содержащего в своем составе тиотриазолин и триптофан.This application presents the results of original studies of the proposed combination, which confirm the high anxiolytic, stress-protective, nootropic and antioxidant activity of the combined preparation containing thiotriazoline and tryptophan in its composition.
Пример 1. Антитревожное (анксиолитическое) действиеExample 1. Anti-anxiety (anxiolytic) action
Анксиолитическое действие препаратов и их комбинаций изучали на 50 белых нелинейных крысах обоего пола массой 170-230 г. Использовался блиц-тест для определения уровня тревожности и выяснения анксиопрофиля препаратов (подвешивание животного за хвост). Комбинированное средство тиотриазолина с триптофаном (1:4) вводили в дозе 250 мг/кг, таблетки Ноофен - в дозе 250 мг/кг, в этой серии исследований также изучали в качестве референс-препарата триптофан, который вводили в дозе 250 мг/кг. После введения препаратов (за 60 мин до тестирования) животное вытаскивалось из клетки и придерживалось за хвост возле туловища в висячем положении головой вниз. Регистрировалось время, в течение которого животное будет оставаться иммобильным (т.е. до того момента, пока морда животного не достигнет основания хвоста) [10, 14].The anxiolytic effect of drugs and their combinations was studied on 50 white non-linear rats of both sexes weighing 170-230 g. A blitz test was used to determine the level of anxiety and ascertain the anxioprofile of drugs (hanging the animal by the tail). The combined thiotriazoline with tryptophan (1: 4) was administered at a dose of 250 mg / kg, Noofen tablets at a dose of 250 mg / kg, tryptophan, which was administered at a dose of 250 mg / kg, was also studied as a reference drug in this series of studies. After drug administration (60 minutes before testing), the animal was pulled out of the cage and held by the tail near the body in a hanging position, head down. The time was recorded during which the animal would remain immobilized (that is, until the animal's muzzle reached the base of the tail) [10, 14].
В результате проведенных исследований было установлено, что при введении комбинированного средства тиотриазолина и триптофана (1:4) животные дольше находились при проведении эксперимента в иммобильном состоянии на 48,7% (р<0,05), что можно расценивать как снижение тревожности и страха (табл.2).As a result of the studies, it was found that with the introduction of the combined agent of thiotriazolin and tryptophan (1: 4), the animals were 48.7% longer (p <0.05) during the experiment, which can be regarded as a decrease in anxiety and fear (table 2).
Менее выраженные изменения продолжительности периода иммобильности отмечались при введении Ноофена и триптофана. Так, введение Ноофена приводило к увеличению времени иммобильности на 35,5% по сравнению с контролем (р<0,05). Введение триптофана приводило к увеличению времени иммобильности на 30,5% по сравнению с контролем 0X0,05).Less pronounced changes in the duration of the period of immobility were noted with the introduction of Noofen and tryptophan. So, the introduction of Noofen led to an increase in immobility time by 35.5% compared with the control (p <0.05). Administration of tryptophan led to an increase in immobility time by 30.5% compared with the control 0X0.05).
Таким образом, исследуемый препарат - комбинированное средство тиотриазолина и триптофана (1:4) снижает уровень тревожности, страха и отчаяния более значительно, чем препараты сравнения - анксиолитик и ноотроп Ноофен и анксиолитик триптофан.Thus, the studied drug - a combined agent of thiotriazolin and tryptophan (1: 4) reduces the level of anxiety, fear and despair more significantly than the comparison drugs - anxiolytic and nootropic Noofen and anxiolytic tryptophan.
Пример 2. Изучение стресс-протективного, ноотропного, анксиолитического и антиоксидантного действияExample 2. The study of stress-protective, nootropic, anxiolytic and antioxidant effects
Эксперименты были проведены на 40 крысах-самцах линии Вистар массой 210-230 г в возрасте 6 мес. Хронический иммобилизационный стресс (ХИС) моделировали жестокой двухчасовой иммобилизацией на спине на протяжении 10 дней [3, 10, 12]. Комбинированное средство тиотриазолина и триптофана (1:4) (НПО «Фарматрон», Украина), эталонный препарат ноотропного, стресс-протективного и анксиолитического действия - Ноофен («Олайнфарм», Латвия), а также комбинированный препарат, содержащий эквивалентное количество тиотриазолина - Тиоцетам, вводили в дозе 250 мг/кг перорально с помощью металлического зонда на 0,5 мл воды в течение 10 дней, раз в сутки за 30 мин до иммобилизации. На первые сутки эксперимента, за 30 мин до стрессирования у животных вырабатывали условную реакцию пассивного избегания (УРПИ) в двухчелночной камере. Через 10 сут, спустя 2 ч после последнего стрессирования, у крыс проводили тест «открытое поле». В течение 3 мин регистрировали количество вертикальных, горизонтальных движений, а также количество заглядываний в «норку», груминг (акты) и количество дефекаций. В эти же сроки оценивали сохранность УРПИ по латентному периоду захода в темный отсек двухчелночной камеры [10, 14]. Затем животные выводились из эксперимента под нембуталовым наркозом (40 мг/кг). Для биохимических иследований мозг промывали в охлажденном изотоническом растворе KCl (+5°С), затем гомогенизировали в гомогенизаторе Поттера (1500 об/мин) в течение 3 мин в 5 объемах буфера, содержащего 50 мМ Трис-HCL, 2 мМ ЭДТА и 2 мМ дитиотрейтол (рН 7,4). Аликвоты этих гомогенатов центифугировали 10 мин при 11000 g [4].The experiments were conducted on 40 male Wistar rats weighing 210-230 g at the age of 6 months. Chronic immobilization stress (CHI) was modeled by brutal two-hour immobilization on the back for 10 days [3, 10, 12]. The combined agent of thiotriazolin and tryptophan (1: 4) (NPO Farmatron, Ukraine), the reference drug of nootropic, stress-protective and anxiolytic action is Noofen (Olainfarm, Latvia), as well as the combined drug containing an equivalent amount of thiotriazoline - Thiocetam , was administered at a dose of 250 mg / kg orally with a metal probe in 0.5 ml of water for 10 days, once a day 30 minutes before immobilization. On the first day of the experiment, 30 minutes before stressing, the animals developed a conditioned passive avoidance reaction (passive avoidance reaction) in a two-shuttle chamber. 10 days later, 2 hours after the last stress, an open field test was performed in rats. Within 3 minutes, the number of vertical and horizontal movements was recorded, as well as the number of peeps into the “mink”, grooming (acts) and the number of bowel movements. At the same time, the safety of passive avoidance reaction was evaluated by the latent period of entry into the dark compartment of the two-shuttle chamber [10, 14]. Then the animals were withdrawn from the experiment under nembutal anesthesia (40 mg / kg). For biochemical studies, the brain was washed in a chilled isotonic KCl solution (+ 5 ° C), then homogenized in a Potter homogenizer (1500 rpm) for 3 min in 5 volumes of buffer containing 50 mM Tris-HCL, 2 mM EDTA and 2 mM dithiothreitol (pH 7.4). Aliquots of these homogenates were centrifuged for 10 min at 11000 g [4].
В супернатанте (5 мг/мл) определяли продукты окислительной модификации белка (ОМБ) по уровню альдегидфенилгидразонов (АФГ) и кетонфенилгидразонов (КФГ) по реакции взаимодействия окисленных аминокислотных остатков с 2,4-динитрофенилгидразином [4]. Также определяли стабильные метаболиты NO по уровню нитратов в реакции Грисса [4] и активность NO-синтазы (NOS). Активность NOS определяли по разности между скоростью окисления NADPH, регистрируемой флюорометрически, в двух параллельных образцах как не содержащих, так и содержащих ингибитор NOS - N-нитро-L-аргинин [4]. Концентрацию белка оценивали по методу Бредфорда. Степень окислительной модификации ДНК определяли по суточной экскреции 8-гидроксигуанина (8- OHG) в моче [4].In the supernatant (5 mg / ml), the products of oxidative modification of the protein (OMB) were determined by the level of aldehyde phenylhydrazone (APH) and ketonphenylhydrazone (CPH) by the reaction of the interaction of oxidized amino acid residues with 2,4-dinitrophenylhydrazine [4]. Stable NO metabolites were also determined by the level of nitrates in the Griss reaction [4] and the activity of NO synthase (NOS). NOS activity was determined by the difference between the NADPH oxidation rate, recorded fluorometrically, in two parallel samples, both not containing and containing a NOS inhibitor, N-nitro-L-arginine [4]. Protein concentration was evaluated according to the Bradford method. The degree of oxidative DNA modification was determined by daily excretion of 8-hydroxyguanine (8-OHG) in urine [4].
Результаты проведенных исследований показали, что ХИС характеризуется изменением двигательной активности, что выражается в снижении горизонтальной активности на 82,3%, вертикальной - на 77%, угнетением исследовательской активности (количество заглядываний) на 90%, а также повышением тревожности, о чем свидетельствовало снижение актов груминга на 43% и повышение актов дефекации на 112,5%. Также установлено, что перенесенный ХИС угнетает когнитивно-мнестические функции ЦНС, о чем свидетельствовало уменьшение латентного периода УРПИ на 79% и снижение на 70% количество обученных животных. Введение крысам с ХИС комбинированного средства тиотриазолина с триптофаном (1:4) статистически достоверно по отношению к контрольной группе животных (р<0,05) повышало ориентировочно-исследовательскую активность. Так, в этой группе животных увеличилось количество горизонтальных движений в 2,54 раза, вертикальных - в 2,57 раза, что свидетельствовало о повышении двигательной активности. Под действием комбинированного препарата увеличилось количество заглядываний в «норку» в 5,75 раз. Результаты введения Ноофена уступали изучаемому препарату по степени влияния на исследуемые показатели ориентировочно-исследовательской активности у животных с ХИС. Также введение комбинированного средства тиотриазолина и триптофана (1:4) приводило к увеличению актов груминга на 57% и количества дефекаций на 47%, что свидетельствовало о снижении тревожности после стресса. Воспроизведение УРПИ, проведенное через 10 суток ежедневного стрессирования, показало, что у контрольных животных нарушено воспроизводство памятного следа, о чем свидетельствовало уменьшение времени УРПИ на 79%. Почти все крысы этой группы быстро заходили в темную «опасную» камеру. Введение животным комбинированного средства тиотриазолина и триптофана (1:4) ослабляло амнезию УРПИ, вызванную ХИС, статистически достоверно увеличивая латентное время рефлекса при воспроизведении (табл. 3). Так, введение комбинированного средства тиотриазолина и триптофана (1:4) увеличивало латентный период УРПИ в 2,38 раз, а введение Ноофена - в 1,44 раза. Стоит отметить, что введение комбинированного средства тиотриазолина и триптофана (1:4) достоверно увеличивало количество обученных крыс в группе до 90%, а введение Ноофена до 60%. Приведенные данные подтверждают ноотропную и стресс-протективную активность предлагаемого комбинированного средства.The results of the studies showed that ChIS is characterized by a change in motor activity, which is expressed in a decrease in horizontal activity by 82.3%, vertical - by 77%, inhibition of research activity (number of peeks) by 90%, as well as an increase in anxiety, as evidenced by a decrease grooming acts by 43% and an increase in bowel movements by 112.5%. It was also found that the transferred HIS depresses the cognitive-mnestic functions of the central nervous system, as evidenced by a 79% decrease in the latent period of passive avoidance reaction and a 70% decrease in the number of trained animals. The introduction of a combination agent of thiotriazoline with tryptophan (1: 4) into rats with chis is statistically significant in relation to the control group of animals (p <0.05) increased the tentative research activity. So, in this group of animals the number of horizontal movements increased by 2.54 times, vertical - by 2.57 times, which indicated an increase in motor activity. Under the influence of the combined preparation, the number of peeks into the “mink” increased by 5.75 times. The results of the introduction of Noofen were inferior to the study drug in terms of the degree of influence on the studied indicators of orientational research activity in animals with HIS. Also, the introduction of a combined agent of thiotriazoline and tryptophan (1: 4) led to an increase in grooming by 57% and the number of bowel movements by 47%, indicating a decrease in anxiety after stress. Reproduction of passive avoidance reaction, conducted after 10 days of daily stress, showed that in the control animals reproduction of the commemorative trace was impaired, as evidenced by a decrease in passive avoidance reaction by 79%. Almost all rats in this group quickly entered the dark “dangerous” chamber. The administration of a combination of thiotriazoline and tryptophan (1: 4) to animals weakened the passive avoidance reaction amnesia caused by ChIS, statistically significantly increasing the latent time of the reflex during reproduction (Table 3). Thus, the introduction of a combined agent of thiotriazoline and tryptophan (1: 4) increased the latent period of passive avoidance reaction by 2.38 times, and the introduction of Noofen by 1.44 times. It is worth noting that the introduction of a combined agent of thiotriazolin and tryptophan (1: 4) significantly increased the number of trained rats in the group to 90%, and the introduction of Noofen to 60%. The data presented confirm the nootropic and stress-protective activity of the proposed combination agent.
Моделирование ХИС в течение 10 суток приводило к развитию оксидативного стресса в головном мозге экспериментальных животных, о чем свидетельствовало повышение уровня маркерных продуктов окислительной модификации белка. Так, концентрация АФГ и КФГ в контрольной группе животных на 120% и на 134% соответственно превышала таковые показатели интактной группы. Введение комбинированного средства тиотриазолина и триптофана (1:4) достоверно (р<0,05) снижало концентрацию маркеров ОМБ - АФГ на 46%, КФГ на 36%. По степени снижения маркеров оксидативного стресса - АФГ и КФГ - изучаемое комбинированное средство достоверно превосходило эффективность референс-препарата Ноофена, а по степени снижения АФГ - и Тиоцетама. Окислительная модификация белков приводит к снижению функции белков в цепи переносчиков электронов, активности АТФ-азы, избирательности действия транспортных пор. Изменение Red/Ox - потенциала митохондриальной мембраны может влиять на дисфункцию каскада дыхательной цепи нейрональной клетки. Вышеперечисленные изменения, в конечном итоге, приводят к нарушению секреторной, инкреторной, транспортной функции нейрона, и, как следствие, к развитию когнитивного дефицита [1, 2, 10].Simulation of ChIS for 10 days led to the development of oxidative stress in the brain of experimental animals, as evidenced by an increase in the level of marker products of oxidative protein modification. Thus, the concentration of APH and CPG in the control group of animals was 120% and 134% respectively higher than those of the intact group. The introduction of the combined agent of thiotriazoline and tryptophan (1: 4) significantly (p <0.05) reduced the concentration of OMB - AFH markers by 46%, and CFG by 36%. In terms of the degree of reduction of oxidative stress markers - AFH and KFG - the studied combination drug significantly exceeded the effectiveness of the reference drug Noofen, and in terms of the degree of decrease in AFH - and Tiocetam. Oxidative modification of proteins leads to a decrease in the function of proteins in the chain of electron carriers, the activity of ATPase, and the selectivity of the action of transport pores. Changes in the Red / Ox potential of the mitochondrial membrane can affect the dysfunction of the neuronal cell respiratory chain cascade. The above changes, ultimately, lead to a violation of the secretory, incretory, transport function of the neuron, and, as a consequence, to the development of cognitive deficit [1, 2, 10].
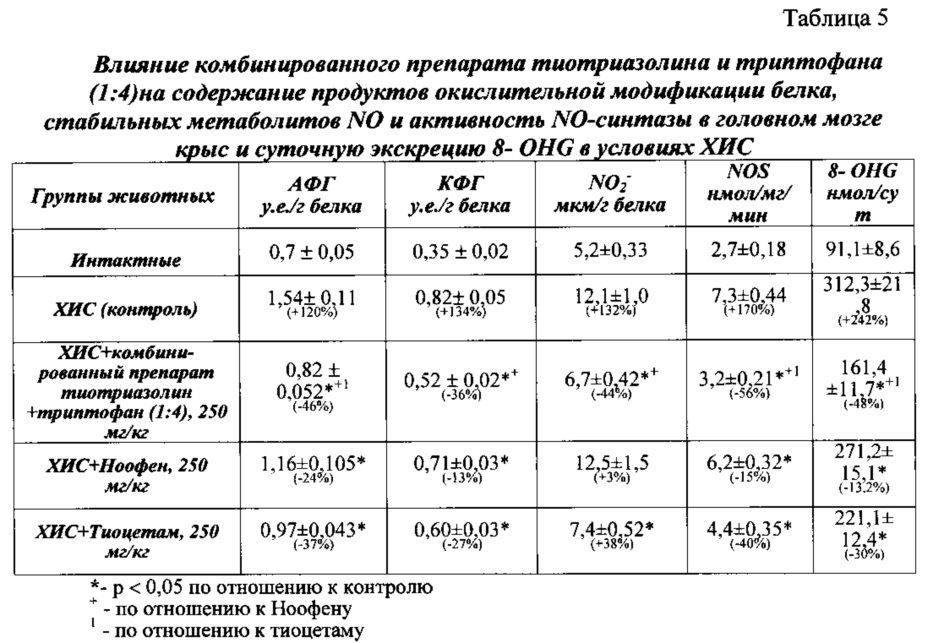
Гиперпродукция NO и ОН. при некоторых патологических состояниях (ишемия, стресс, нейродегенеративные заболевания и т.д.) играет ключевую роль в молекулярных механизмах окислительного стресса и является пусковым механизмом в окислительной деструкции ДНК клетки [1, 2, 13]. Окислительная модификация ДНК приводит к образованию 8-гидроксигуанина (8-OHG), который оказывает выраженное цито- и геномотоксическое действие, важнейшими последствиями которого является искажение молекулярно-биологических процессов в клетке - репликации и транскрипции. Из таблицы 5 видно, что ХИС сопровождается значительным повышением концентрации 8-OHG (в 2,42 раза) в суточной моче крыс.Hyperproduction of NO and OH . in some pathological conditions (ischemia, stress, neurodegenerative diseases, etc.) plays a key role in the molecular mechanisms of oxidative stress and is a trigger in the oxidative destruction of cell DNA [1, 2, 13]. Oxidative modification of DNA leads to the formation of 8-hydroxyguanine (8-OHG), which has a pronounced cyto- and genomotoxic effect, the most important consequences of which are the distortion of molecular biological processes in the cell - replication and transcription. From table 5 it is seen that CI is accompanied by a significant increase in the concentration of 8-OHG (2.42 times) in the daily urine of rats.
Введение экспериментальным животным комбинированного средства тиотриазолина и триптофана (1:4) оказывало протективное действие в отношении нуклеиновых кислот при оксидативном стрессе, о чем свидетельствовало снижение суточной экскреции 8- OHG на 48% (р<0,05). Введение Ноофена приводило к снижению 8-OHG на 13,2% (р<0,05) в суточной моче. Введение комбинированного препарата, содержащего тиотриазолин - Тиоцетама - снижало 8-OHG на 30% (р<0,05) в суточной моче. Стоит отметить, что по данному тесту предлагаемое комбинированное средство достоверно превосходило эффект Ноофена и Тиоцетама, что свидетельствует о более выраженном антиоксидантном и геномопротективном действии комбинированного препарата тиотриазолина и триптофана.The introduction of a combination of thiotriazoline and tryptophan (1: 4) into experimental animals had a protective effect on nucleic acids under oxidative stress, as evidenced by a 48% decrease in daily excretion of 8-OHG (p <0.05). The introduction of Noofen led to a decrease in 8-OHG by 13.2% (p <0.05) in daily urine. The introduction of a combination drug containing thiotriazolin - Thiocetam - reduced 8-OHG by 30% (p <0.05) in daily urine. It is worth noting that in this test the proposed combination agent significantly exceeded the effect of Noofen and Thiocetam, which indicates a more pronounced antioxidant and genomoprotective effect of the combined preparation of thiotriazoline and tryptophan.
Существенную роль в гиперпродукции NO принадлежит индуцибельной NO-синтазе, которая экспрессируется под действием факторов транскрипции-JunB; c-Fos; AP-1 [1, 2]. Данными исследованиями было установлено, что ХИС приводил к активации NO-синтазы на 132% и гиперпродукции NO, о чем свидетельствовало повышение на 170% в головном мозге крыс его стабильных метаболитов. Назначение экспериментальным животным комбинированного средства тиотриазолина и триптофана (1:4) приводило к снижению активности NO-синтазы на 56% и гиперпродукции NO на 44%. Введение Ноофена не оказывало достоверного влияния на содержание нитритов и достоверно уступало по степени влияния на активность NO-синтазы. Введение Тиоцетама снижало активность NO-синтазы на 40% и гиперпродукции NO на 38%. По степени снижения активности NO-синтазы комбинированный препарат тиотриазолина и триптофана (1:4) достоверно превосходит Тиоцетам (табл. 5).An essential role in the overproduction of NO belongs to inducible NO synthase, which is expressed under the influence of transcription factors-JunB; c-fos; AP-1 [1, 2]. These studies found that ChIS led to the activation of NO synthase by 132% and overproduction of NO, as evidenced by an increase of 170% in the brain of rats of its stable metabolites. The use of the combination agent thiotriazolin and tryptophan (1: 4) in experimental animals reduced the activity of NO synthase by 56% and overproduction of NO by 44%. The introduction of Noofen did not have a significant effect on the nitrite content and was significantly inferior in degree of influence on the activity of NO synthase. The introduction of Thiocetam reduced the activity of NO synthase by 40% and overproduction of NO by 38%. The combination of thiotriazolin and tryptophan (1: 4) significantly exceeds Thiocetam in the degree of decrease in the activity of NO synthase (Table 5).
Подобный эффект комбинированного средства тиотриазолина и триптофана (1:4) является одним из ключевых механизмов его нейропротективного действия, так как от соотношения внутриклеточных концентраций NO и АФК зависит характер действия этих соединений на процессы, связанные с регуляцией апоптоза в нейрональной клетке [1, 2].A similar effect of the combined agent of thiotriazoline and tryptophan (1: 4) is one of the key mechanisms of its neuroprotective effect, since the nature of the action of these compounds on the processes associated with the regulation of apoptosis in a neuronal cell depends on the ratio of intracellular concentrations of NO and ROS [1, 2] .
Таким образом, исследуемый препарат - комбинированное средство тиотриазолина и триптофана (1:4) обладает выраженными стресс-протективными, ноотропными, анксиолитическими и антиоксидантными свойствами, и по силе этих фармакологических эффектов достоверно превосходит референс-препарат Ноофен, а по силе антиоксидатного действия - Тиоцетам.Thus, the studied drug, a combined agent of thiotriazolin and tryptophan (1: 4), has pronounced stress-protective, nootropic, anxiolytic and antioxidant properties, and it significantly exceeds the reference drug Noofen in the strength of these pharmacological effects, and Thiocetam in the strength of the antioxidant effect.
Проанализировав результаты проведенных исследований, можно сделать вывод, что предлагаемое комбинированное средство тиотриазолина и триптофана обеспечивает более высокую анксиолитическую и антиоксидантную активность по сравнению с препаратами сравнения. Кроме того, предлагаемое средство проявило новые виды активности - ноотропное и стресс-протективное действия, которыми в отдельности компоненты комбинированного средства -триптофан и тиотриазолин - не обладали.After analyzing the results of the studies, we can conclude that the proposed combination agent of thiotriazoline and tryptophan provides a higher anxiolytic and antioxidant activity compared with the comparison drugs. In addition, the proposed tool showed new types of activity - nootropic and stress-protective actions, which separately the components of the combined means - tryptophan and thiotriazoline - did not have.
Таблетки, содержащие триптофан и тиотриазолин, изготавливают покрытыми оболочкой или без оболочки. Ядро таблеток изготавливают различными способами, например, путем получения порошкообразной смеси этих активных ингредиентов с добавлением достаточного количества вспомогательных веществ и последующего прессования. В состав таблеток входят различные вспомогательные вещества, которые влияют на физико-химические свойства, например, полифункциональные вспомогательные вещества, наполнители, разрыхлители, антифрикционные вещества и т.д.Tablets containing tryptophan and thiotriazolin are made coated or uncoated. The tablet core is made in various ways, for example, by obtaining a powdery mixture of these active ingredients with the addition of a sufficient amount of auxiliary substances and subsequent pressing. The composition of the tablets includes various excipients that affect the physicochemical properties, for example, multifunctional excipients, fillers, disintegrants, antifriction substances, etc.
Капсулы изготавливают путем дозирования смеси активных компонентов триптофана и тиотриазолина и вспомогательных веществ в капсулы, которые могут содержать разовую или высшую терапевтическую дозу предлагаемого средства.Capsules are made by dosing a mixture of the active components of tryptophan and thiotriazolin and excipients into capsules, which may contain a single or higher therapeutic dose of the proposed agent.
Раствор для инъекций, содержащий как активные вещества триптофан и тиотриазолин, готовят как с использованием стабилизатора, так и без него. Возможно использование веществ, которые позволяют достичь изотоничности раствора. Раствор изготавливают различных концентраций, которые содержат терапевтическую дозу предлагаемого комбинированного лекарственного средства.An injection solution containing both the active substances tryptophan and thiotriazoline is prepared with or without a stabilizer. It is possible to use substances that make it possible to achieve isotonicity of the solution. The solution is prepared in various concentrations, which contain a therapeutic dose of the proposed combination drug.
Для изготовления инфузионных растворов комбинированного препарата триптофана с тиотриазолином могут использоваться физиологические растворы различного состава.For the preparation of infusion solutions of the combined preparation of tryptophan with thiotriazoline, physiological solutions of various compositions can be used.
Таким образом, использование предлагаемого средства позволит расширить отечественный арсенал лекарственных средств, которые можно применять в неврологии, и которые являются безопасными и обладают высокой эффективностью.Thus, the use of the proposed tool will expand the domestic arsenal of drugs that can be used in neurology, and which are safe and highly effective.
ЛитератураLiterature
1. Беленичев И.Ф., Губский Ю.И, Павлов С.В. Токсические последствия окислительной модификации белков при различных патологических состояниях // Совр. пробл. токсикол. - 2005. - №3. - С. 20-26.1. Belenichev I.F., Gubsky Yu.I., Pavlov S.V. Toxic effects of oxidative protein modification in various pathological conditions // Sovr. prob. toxicol. - 2005. - No. 3. - S. 20-26.
2. Беленичев И.Ф., Черний В.И., Павлов С.В., Кучеренко Л.И. Нейропротекция и нейропластичность. - К.: Логос, 2015. - 512 с.2. Belenichev I.F., Cherniy V.I., Pavlov S.V., Kucherenko L.I. Neuroprotection and neuroplasticity. - K .: Logos, 2015 .-- 512 s.
3. Гойкова Л.А., Зорян Е.В., Анисимова Е.Н. // Фармакологические методы коррекции стресса // Вопр. биол. мед. и фарм. химии. - 2004. - №3. - С. 3-5.3. Goikova L.A., Zoryan E.V., Anisimova E.N. // Pharmacological methods of stress correction // Vopr. biol. honey. and farm. chemistry. - 2004. - No. 3. - S. 3-5.
4. Доклиническое изучение специфической активности потенциальных нейропротективных препаратов / И.С. Чекман, И.Ф. Беленичев, Л.А. Громов и др. - Методические рекомендации Государственного Фармакологического Центра МЗ Украины, Киев. - 2010. - 81 с.4. Preclinical study of the specific activity of potential neuroprotective drugs / I.S. Chekman, I.F. Belenichev, L.A. Gromov et al. - Methodological recommendations of the State Pharmacological Center of the Ministry of Health of Ukraine, Kiev. - 2010 .-- 81 s.
5. Дьюсбери Р. Изучение поведения животных. М.: Наука, 1980. - 376 с.5. Dewsbury R. Studying the behavior of animals. M .: Nauka, 1980 .-- 376 p.
6. Експериментальне дослiдження активностi таблеток "Тiоцетам" Мазур I.A., I.Ф., Стець В.Р. // Експер.фiзiол.та бioxiм. - 2002. - №1. - С. 7-11.6. Experimentation the activity of the tablets "Tiocetam" Mazur IA, I.F., Stets V.R. // Expert.physiol.ta bioxim. - 2002. - No. 1. - S. 7-11.
7. Турпаев К.Т. Активные формы кислорода и регуляция экспрессии генов // Биохимия. - 2002. - Т. 67, №3. - С. 339-352.7. Turpaev K.T. Active forms of oxygen and regulation of gene expression // Biochemistry. - 2002. - T. 67, No. 3. - S. 339-352.
8. Мазур И.А., Беленичев И.Ф. К вопросу создания препаратов нейропротективного действия // Вiсник та . - 2006. - №4. - С. 28-36.8. Mazur I.A., Belenichev I.F. To the question of the creation of neuroprotective drugs // News that . - 2006. - No. 4. - S. 28-36.
9. Мазур И.А., Зименковский Б.С., Волошин Н.А., Чекман И.С., Стец В.Р. Тиотриазолин. - Львов: Наутилус, 2005. - 230 с.9. Mazur I.A., Zimenkovsky B.S., Voloshin N.A., Chekman I.S., Stets V.R. Thiotriazolinum. - Lviv: Nautilus, 2005 .-- 230 p.
10. Калуев А.В. Стресс, тревожность и поведение. Актуальные проблемы моделирования тревожного поведения у животных. - Киев, 1998. - 95 с.10. Kaluev A.V. Stress, anxiety and behavior. Actual problems of modeling anxiety behavior in animals. - Kiev, 1998 .-- 95 s.
11. Коплик Е.В., Мещеряков А.Ф., Перцов С.С. и др. Влияние дипептида вилона на устойчивость крыс к эмоциональному стрессу // Рос. физиол. журн. - 2002. - Т. 88, №11. - С. 1440-1452.11. Koplik E.V., Meshcheryakov A.F., Pertsov S.S. et al. Effect of Vilon dipeptide on the resistance of rats to emotional stress // Ros. fiziol. journal - 2002. - T. 88, No. 11. - S. 1440-1452.
12. Стефанов А.В. Доклинические исследования лекарственных веществ. - Киев: ГФЦ МЗ Украины, 2000. - 540 с.12. Stefanov A.V. Preclinical studies of drugs. - Kiev: State Pharmacological Center of the Ministry of Health of Ukraine, 2000 .-- 540 p.
13. Aruoma О., Halliwell В. Molecular Biology of Free Radicals in Human Diseases - St. Lucia, London: OCIA Int., 1999. - 345 p.13. Aruoma O., Halliwell B. Molecular Biology of Free Radicals in Human Diseases - St. Lucia, London: OCIA Int., 1999 .-- 345 p.
14. Bures J. Cortical spreading depression as a memory disturbing factor / J. Bures, O. Buresude // J. соmр. and phisiol. - 1963. - Vol. 56, №2. - P. 268-272.14. Bures J. Cortical spreading depression as a memory disturbing factor / J. Bures, O. Buresude // J. comp. and phisiol. - 1963. - Vol. 56, No. 2. - P. 268-272.
15. Mikava S., Kinouchi H., Kami H. et al. Attenuation of acute and chronic damage fllowing traumatic brain injuri in copper, zinc- superoxide dismutsse transgenic mice // J. Neurosurg. - 1996. - V. 85. - P. 885-891.15. Mikava S., Kinouchi H., Kami H. et al. Attenuation of acute and chronic damage fllowing traumatic brain injuri in copper, zinc-superoxide dismutsse transgenic mice // J. Neurosurg. - 1996. - V. 85. - P. 885-891.
Claims (3)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2016123907A RU2625754C1 (en) | 2016-06-15 | 2016-06-15 | Combined drug of anxiolithic, stress-protector, nootropic and antioxidant action |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2016123907A RU2625754C1 (en) | 2016-06-15 | 2016-06-15 | Combined drug of anxiolithic, stress-protector, nootropic and antioxidant action |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2625754C1 true RU2625754C1 (en) | 2017-07-18 |
Family
ID=59495326
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2016123907A RU2625754C1 (en) | 2016-06-15 | 2016-06-15 | Combined drug of anxiolithic, stress-protector, nootropic and antioxidant action |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2625754C1 (en) |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2248203C2 (en) * | 2003-02-14 | 2005-03-20 | Общество С Ограниченной Ответственностью "Научно-Производственное Объединение "Фарматрон" | Cerebroprotective and nootropic medicinal agent "nootril" in envelope-covered tablet |
| US20130064803A1 (en) * | 2011-09-14 | 2013-03-14 | Naidu Lp | BIO-REPLENISHMENT (BioRep) FOR COGNITIVE HEALTH |
| US20130156872A1 (en) * | 2012-10-04 | 2013-06-20 | Invivo Beverages Llc | Integrated Neuromodulation System for Mood Enhancement of a Living Human Subject |
-
2016
- 2016-06-15 RU RU2016123907A patent/RU2625754C1/en active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2248203C2 (en) * | 2003-02-14 | 2005-03-20 | Общество С Ограниченной Ответственностью "Научно-Производственное Объединение "Фарматрон" | Cerebroprotective and nootropic medicinal agent "nootril" in envelope-covered tablet |
| US20130064803A1 (en) * | 2011-09-14 | 2013-03-14 | Naidu Lp | BIO-REPLENISHMENT (BioRep) FOR COGNITIVE HEALTH |
| US20130156872A1 (en) * | 2012-10-04 | 2013-06-20 | Invivo Beverages Llc | Integrated Neuromodulation System for Mood Enhancement of a Living Human Subject |
Non-Patent Citations (2)
| Title |
|---|
| V. I. Sapegin, et al. L-lysine escinat, thiotriazolin, gordox and mydocalm influence on oxygen tension in the intestinal wall and acid-base balance and limited proteolysis in intestinal venous blood in terms of intraabdominal hypertension modeling // Medical Perspectives. - 2014. - V.19, N4. - P. 4-12. * |
| С. В. Павлов. ВЛИЯНИЕ АНТИОКСИДАНТОВ НА СИСТЕМУ ОКСИДА АЗОТА В ГОЛОВНОМ МОЗГЕ КРЫС ПРИ ОСТРОЙ ЦЕРЕБРАЛЬНОЙ ИШЕМИИ // Одеський медичний журнал. -2014. -N1. - С. 21-26. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ionescu-Tucker et al. | Emerging roles of oxidative stress in brain aging and Alzheimer's disease | |
| Krishnan et al. | The epigenetic landscape of alcoholism | |
| Cornelius et al. | Traumatic brain injury: oxidative stress and neuroprotection | |
| Pasyukova et al. | HDAC inhibitors: A new promising drug class in anti-aging research | |
| Hannan | Environmental enrichment and brain repair: harnessing the therapeutic effects of cognitive stimulation and physical activity to enhance experience‐dependent plasticity | |
| Zhang et al. | Hydrogen sulfide: a neuromodulator and neuroprotectant in the central nervous system | |
| de Diego-Otero et al. | α-tocopherol protects against oxidative stress in the fragile X knockout mouse: an experimental therapeutic approach for the Fmr1 deficiency | |
| Rosa et al. | Oxidative stress induced by intense and exhaustive exercise impairs murine cognitive function | |
| Peterson et al. | Dose-dependent effects of wheel running on cocaine-seeking and prefrontal cortex Bdnf exon IV expression in rats | |
| Zhou et al. | PQQ ameliorates D-galactose induced cognitive impairments by reducing glutamate neurotoxicity via the GSK-3β/Akt signaling pathway in mouse | |
| Ke et al. | Post-translational modifications in MeHg-induced neurotoxicity | |
| Bennion et al. | Neuroprotection by post‐stroke administration of an oral formulation of angiotensin‐(1–7) in ischaemic stroke | |
| Trivedi et al. | Redox-based epigenetic status in drug addiction: a potential contributor to gene priming and a mechanistic rationale for metabolic intervention | |
| Leikas et al. | Brief isoflurane anesthesia regulates striatal AKT‐GSK3β signaling and ameliorates motor deficits in a rat model of early‐stage Parkinson′ s disease | |
| Paul et al. | The potential physiological crosstalk and interrelationship between two sovereign endogenous amines, melatonin and homocysteine | |
| Sajja et al. | In vitro modulation of redox and metabolism interplay at the brain vascular endothelium: genomic and proteomic profiles of sulforaphane activity | |
| Pogun et al. | Nicotine modulates nitric oxide in rat brain | |
| Coppedè | Epigenetic regulation in Alzheimer’s disease: is it a potential therapeutic target? | |
| Hrnčić et al. | The role of nitric oxide in convulsions induced by lindane in rats | |
| KV et al. | Cognitive improvement by vorinostat through modulation of endoplasmic reticulum stress in a corticosterone-induced chronic stress model in mice | |
| Mendez et al. | Long-lasting sensitization of reward-directed behavior by amphetamine | |
| Jeremic et al. | Targeting epigenetics: a novel promise for Alzheimer’s disease treatment | |
| Mehta et al. | REM sleep and its loss-associated epigenetic regulation with reference to noradrenaline in particular | |
| RU2625754C1 (en) | Combined drug of anxiolithic, stress-protector, nootropic and antioxidant action | |
| Gladkova et al. | Epidrugs in the Therapy of Central Nervous System Disorders: A Way to Drive on? |