RU2546111C2 - Method of phenacetin obtaining - Google Patents
Method of phenacetin obtaining Download PDFInfo
- Publication number
- RU2546111C2 RU2546111C2 RU2012130826/04A RU2012130826A RU2546111C2 RU 2546111 C2 RU2546111 C2 RU 2546111C2 RU 2012130826/04 A RU2012130826/04 A RU 2012130826/04A RU 2012130826 A RU2012130826 A RU 2012130826A RU 2546111 C2 RU2546111 C2 RU 2546111C2
- Authority
- RU
- Russia
- Prior art keywords
- phenacetin
- target product
- ethoxyaniline
- ethoxynitrobenzene
- separation
- Prior art date
Links
- CPJSUEIXXCENMM-UHFFFAOYSA-N phenacetin Chemical compound CCOC1=CC=C(NC(C)=O)C=C1 CPJSUEIXXCENMM-UHFFFAOYSA-N 0.000 title claims abstract description 51
- 229960003893 phenacetin Drugs 0.000 title claims abstract description 26
- 238000000034 method Methods 0.000 title claims abstract description 17
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 claims abstract description 22
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 claims abstract description 21
- NWPKEYHUZKMWKJ-UHFFFAOYSA-N 1-ethoxy-4-nitrobenzene Chemical compound CCOC1=CC=C([N+]([O-])=O)C=C1 NWPKEYHUZKMWKJ-UHFFFAOYSA-N 0.000 claims abstract description 11
- IMPPGHMHELILKG-UHFFFAOYSA-N 4-ethoxyaniline Chemical compound CCOC1=CC=C(N)C=C1 IMPPGHMHELILKG-UHFFFAOYSA-N 0.000 claims abstract description 11
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims abstract description 7
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 7
- 239000001257 hydrogen Substances 0.000 claims abstract description 7
- 239000007868 Raney catalyst Substances 0.000 claims description 5
- 238000011946 reduction process Methods 0.000 claims description 2
- 230000015572 biosynthetic process Effects 0.000 abstract description 7
- 239000003054 catalyst Substances 0.000 abstract description 6
- 230000009467 reduction Effects 0.000 abstract description 5
- 239000000126 substance Substances 0.000 abstract description 5
- 238000003786 synthesis reaction Methods 0.000 abstract description 4
- 230000010933 acylation Effects 0.000 abstract description 3
- 238000005917 acylation reaction Methods 0.000 abstract description 3
- 238000002156 mixing Methods 0.000 abstract description 3
- 230000008569 process Effects 0.000 abstract description 3
- 238000000746 purification Methods 0.000 abstract description 3
- 239000003638 chemical reducing agent Substances 0.000 abstract description 2
- 238000005516 engineering process Methods 0.000 abstract description 2
- 238000000926 separation method Methods 0.000 abstract 3
- NPXOKRUENSOPAO-UHFFFAOYSA-N Raney nickel Chemical compound [Al].[Ni] NPXOKRUENSOPAO-UHFFFAOYSA-N 0.000 abstract 1
- 230000036571 hydration Effects 0.000 abstract 1
- 238000006703 hydration reaction Methods 0.000 abstract 1
- 238000004519 manufacturing process Methods 0.000 description 13
- 239000000047 product Substances 0.000 description 10
- 238000005984 hydrogenation reaction Methods 0.000 description 8
- 239000002904 solvent Substances 0.000 description 7
- 230000003197 catalytic effect Effects 0.000 description 6
- 238000006722 reduction reaction Methods 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 5
- 239000003153 chemical reaction reagent Substances 0.000 description 5
- 239000011541 reaction mixture Substances 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 230000021736 acetylation Effects 0.000 description 3
- 238000006640 acetylation reaction Methods 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 235000014413 iron hydroxide Nutrition 0.000 description 3
- NCNCGGDMXMBVIA-UHFFFAOYSA-L iron(ii) hydroxide Chemical compound [OH-].[OH-].[Fe+2] NCNCGGDMXMBVIA-UHFFFAOYSA-L 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 3
- LXEFYWWNLGZTQB-UHFFFAOYSA-N 2-ethoxy-n-phenylacetamide Chemical compound CCOCC(=O)NC1=CC=CC=C1 LXEFYWWNLGZTQB-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- 239000006227 byproduct Substances 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- URAYPUMNDPQOKB-UHFFFAOYSA-N triacetin Chemical compound CC(=O)OCC(OC(C)=O)COC(C)=O URAYPUMNDPQOKB-UHFFFAOYSA-N 0.000 description 2
- 239000002699 waste material Substances 0.000 description 2
- YJFNFQHMQJCPRG-UHFFFAOYSA-N 1-(4-ethoxyphenyl)ethanone Chemical compound CCOC1=CC=C(C(C)=O)C=C1 YJFNFQHMQJCPRG-UHFFFAOYSA-N 0.000 description 1
- JTXMVXSTHSMVQF-UHFFFAOYSA-N 2-acetyloxyethyl acetate Chemical compound CC(=O)OCCOC(C)=O JTXMVXSTHSMVQF-UHFFFAOYSA-N 0.000 description 1
- XVMSFILGAMDHEY-UHFFFAOYSA-N 6-(4-aminophenyl)sulfonylpyridin-3-amine Chemical compound C1=CC(N)=CC=C1S(=O)(=O)C1=CC=C(N)C=N1 XVMSFILGAMDHEY-UHFFFAOYSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 230000000202 analgesic effect Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 150000001448 anilines Chemical class 0.000 description 1
- 230000001754 anti-pyretic effect Effects 0.000 description 1
- 239000002221 antipyretic Substances 0.000 description 1
- RDHPKYGYEGBMSE-UHFFFAOYSA-N bromoethane Chemical compound CCBr RDHPKYGYEGBMSE-UHFFFAOYSA-N 0.000 description 1
- 238000010531 catalytic reduction reaction Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000006203 ethylation Effects 0.000 description 1
- 238000006200 ethylation reaction Methods 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000001087 glyceryl triacetate Substances 0.000 description 1
- 235000013773 glyceryl triacetate Nutrition 0.000 description 1
- 239000005457 ice water Substances 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000002828 nitro derivatives Chemical class 0.000 description 1
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- JVBXVOWTABLYPX-UHFFFAOYSA-L sodium dithionite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])=O JVBXVOWTABLYPX-UHFFFAOYSA-L 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 238000004809 thin layer chromatography Methods 0.000 description 1
- 239000012485 toluene extract Substances 0.000 description 1
- 239000010891 toxic waste Substances 0.000 description 1
- 229960002622 triacetin Drugs 0.000 description 1
Landscapes
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
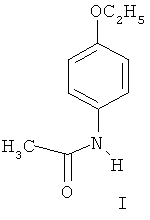
Изобретение относится к области органической химии, а именно к способу получения фенацетина (п-этоксиацетиламинобензол) I [1], который обладает жаропонижающим, анальгезирующим действием и является составной частью ряда лекарственных препаратов.The invention relates to the field of organic chemistry, and in particular to a method for producing phenacetin (p-ethoxyacetylaminobenzene) I [1], which has an antipyretic, analgesic effect and is an integral part of a number of drugs.
Известны защищенные патентами, способы получения фенацетина из различных производных фенола или анилина. Так, 4-этоксиацетофенон превращается в фенацетин при нагревании с гидроокисью аммония в пиридине в присутствии серы с выходом 62% [2]. При нагревании п-фенетидина (п-этоксианилин) с этилацетатом, этиленгликольдиацетатом или триацетином в присутствии метилата натрия получают фенацетин с выходом 59-79% [3].Patent-protected methods for producing phenacetin from various phenol or aniline derivatives are known. So, 4-ethoxyacetophenone is converted to phenacetin when heated with ammonium hydroxide in pyridine in the presence of sulfur with a yield of 62% [2]. By heating p-phenethidine (p-ethoxyaniline) with ethyl acetate, ethylene glycol diacetate or triacetin in the presence of sodium methylate, phenacetin is obtained in a yield of 59-79% [3].
К недостаткам указанных способов следует отнести использование дорогостоящих химических реагентов, невысокие выходы целевого продукта, сложные процессы выделения и очистки, наличие большого количества отходов.The disadvantages of these methods include the use of expensive chemicals, low yields of the target product, complex processes of isolation and purification, the presence of a large amount of waste.
Наиболее близким к заявляемому способу по исходному сырью и его химическим превращениям является классический синтез фенацетина из побочного продукта в производстве красителей - п-нитрофенола II, заключающийся в этилировании последнего этилбромидом под давлением с последующим восстановлением образовавшегося п-этоксинитробензола III в п-этоксианилин (п-фенетидин) IV, ацетилирование которого приводит к получению фенацетина (схема 1) [4].Closest to the claimed method according to the feedstock and its chemical transformations is the classical synthesis of phenacetin from a by-product in the production of dyes - p-nitrophenol II, which consists in the ethylation of the latter with ethyl bromide under pressure, followed by reduction of the resulting p-ethoxynitrobenzene III into p-ethoxyaniline (p-ethoxyaniline phenethidine) IV, acetylation of which leads to phenacetin production (Scheme 1) [4].
Схема 1Scheme 1
Восстановление п-этоксинитробензола (п-фенетол) III п-этоксианилин (п-фенетидин) IV, осуществляемое железом в присутствии соляной кислоты и каталитических количеств платины, сопровождается образованием большого количества гидроокиси железа, загрязняющей амин IV. Гидроокись железа отфильтровывают, жидкий фильтрат и твердую гидроокись железа раздельно экстрагируют толуолом. Толуольные экстракты объединяют, сушат и перегоняют. Перегнанный п-фенетидин IV обрабатывают уксусной кислотой и получают целевой фенацетин I.The reduction of p-ethoxynitrobenzene (p-phenethol) III p-ethoxyaniline (p-phenethidine) IV, carried out by iron in the presence of hydrochloric acid and catalytic amounts of platinum, is accompanied by the formation of a large amount of iron hydroxide, polluting amine IV. Iron hydroxide is filtered off, the liquid filtrate and solid iron hydroxide are separately extracted with toluene. Toluene extracts are combined, dried and distilled. Distilled p-phenethidine IV is treated with acetic acid and the desired phenacetin I is obtained.
Очевидно, что синтез фенацетина I из п-фенетола II через стадию восстановления его реагентными методами сопряжен с необходимостью выделения и очистки промежуточного фенетидина IV и обуславливает появление большого количества токсичных отходов.Obviously, the synthesis of phenacetin I from p-phenethol II through the stage of reduction by reagent methods is associated with the need to isolate and purify intermediate phenetidine IV and causes the appearance of a large amount of toxic waste.
Более чистыми, экологичными и экономически эффективными по сравнению с реагентными являются каталитические способы восстановления. При этом выбор оптимальной каталитической системы для промышленного осуществления реакции восстановления является сложной задачей, т.к. варьирование типа катализатора, растворителя, температуры и других параметров могут изменить механизм и направление реакции. С другой стороны выбор оптимального катализатора определяется с точки зрения внедрения в производство его доступностью и стоимостью. Наиболее широко распространенными, промышленно используемыми и существенно более дешевыми, чем катализаторы платиновой группы являются катализаторы Ni-Ренея.Catalytic reduction methods are cleaner, more environmentally friendly, and cost-effective compared to reagents. In this case, the selection of the optimal catalytic system for the industrial implementation of the reduction reaction is a difficult task, because varying the type of catalyst, solvent, temperature and other parameters can change the mechanism and direction of the reaction. On the other hand, the choice of the optimal catalyst is determined from the point of view of introducing it into production by its availability and cost. The most widely used, industrially used and substantially cheaper than the platinum group catalysts are Ni-Raney catalysts.
Однако в технической литературе отсутствуют сведения о гидрировании п-этоксинитробензола с использованием катализаторов Ni-Ренея.However, in the technical literature there is no information on the hydrogenation of p-ethoxynitrobenzene using Ni-Raney catalysts.
Таким образом, разработка практически реализуемого способа получения фенацетина восстановлением п-этоксинитробензола с использованием катализаторов Ni-Ренея является сложной задачей со многими неизвестными параметрами (растворитель, температура реакции) и далеко неочевидными перспективами ее решения.Thus, the development of a practically feasible method for producing phenacetin by reduction of p-ethoxynitrobenzene using Ni-Raney catalysts is a difficult task with many unknown parameters (solvent, reaction temperature) and far from obvious prospects for its solution.
В связи с этим задачей настоящего изобретения являлась разработка простого? экономически эффективного, экологичного способа получения фенацетина.In this regard, the objective of the present invention was to develop a simple? cost-effective, environmentally friendly method for producing phenacetin.
Поставленная задача решается предлагаемым способом получения фенацетина I, который заключается в том, что п-этоксинитробензол II перемешивают при температуре 60-70°С в растворе изопропилового спирта в присутствии Ni-Ренея и уксусного ангидрида при давлении водорода 2.0-4.0 атм.The problem is solved by the proposed method for producing phenacetin I, which consists in the fact that p-ethoxynitrobenzene II is stirred at a temperature of 60-70 ° C in a solution of isopropyl alcohol in the presence of Ni-Raney and acetic anhydride at a hydrogen pressure of 2.0-4.0 atm.
Окончание реакции восстановления определяют с помощью тонкослойной хроматографии по отсутствию в реакционной смеси исходного нитросоединения II.The end of the reduction reaction is determined by thin-layer chromatography by the absence of the initial nitro compound II in the reaction mixture.
Целевой продукт - п-этоксиацетиламинобензол (фенацетин) выделяют известными методами, в том числе фильтрацией от катализатора, отгонкой под вакуумом растворителя, обработкой остатка водой и последующим фильтрованием.The target product, p-ethoxyacetylaminobenzene (phenacetin), is isolated by known methods, including filtration from a catalyst, distillation of a solvent under vacuum, treatment of the residue with water and subsequent filtration.
Идентичность образцов целевого продукта полученного предлагаемым способом, и ацилированием заведомого п-фенетидина подтверждена совпадением температуры плавления соответствующих образцов и отсутствием температурной депрессии, для пробы смешения. ПМР спектры сравниваемых образцов полностью идентичны.The identity of the samples of the target product obtained by the proposed method, and the acylation of the known p-phenethidine is confirmed by the coincidence of the melting point of the corresponding samples and the absence of temperature depression, for sample mixing. The NMR spectra of the compared samples are completely identical.
Величина избытка используемого для ацетилирования, образующегося в ходе гидрирования п-этоксианилина, уксусного ангидрида определялась экспериментально. Для полного эффективного связывания образующегося п-фенетидина достаточно добавления 2-кратного избытка уксусного ангидрида по отношению к исходному п-этоксинитробензолу.The amount of excess used for acetylation formed during the hydrogenation of p-ethoxyaniline, acetic anhydride was determined experimentally. For complete effective binding of the resulting p-phenethidine, it is sufficient to add a 2-fold excess of acetic anhydride with respect to the starting p-ethoxynitrobenzene.
В качестве растворителя для проведения реакции гидрирования предлагается использовать доступный дешевый растворитель - изопропиловый спирт. Изопропиловый спирт легко может быть регенерирован и многократно использован.As a solvent for the hydrogenation reaction, it is proposed to use an affordable low-cost solvent - isopropyl alcohol. Isopropyl alcohol can be easily regenerated and reused.
Экспериментально установлено, что оптимальными температурами для проведения гидрирования для предлагаемой каталитической системы (Ni-Ренея, изопропиловый спирт) является интервал температур 60-70°C. Следует отметить, что понижение температуры приводит к замедлению скорости образования целевого продукта и появлению большого количества побочных продуктов и практической невозможности выделения обычными методами целевого фенацетина. С другой стороны, при проведении реакции гидрирования в спиртовом растворе при высоких температурах имеет место образование окрашенных продуктов, которые ухудшают показатели цветности целевого продукта. Для предотвращения ухудшения качества целевого продукта оказалось эффективным проводить процесс восстановления в присутствии уксусного ангидрида. При этом удается стабилизировать образующийся п-фенетидин, переводя его в устойчивый целевой продукт - фенацетин.It was experimentally established that the optimum temperature for hydrogenation for the proposed catalytic system (Ni-Raney, isopropyl alcohol) is a temperature range of 60-70 ° C. It should be noted that lowering the temperature slows down the rate of formation of the target product and the appearance of a large number of by-products and the practical impossibility of isolating the target phenacetin by conventional methods. On the other hand, when carrying out the hydrogenation reaction in an alcohol solution at high temperatures, the formation of colored products occurs, which impair the color performance of the target product. To prevent deterioration in the quality of the target product, it was found to be effective to carry out the reduction process in the presence of acetic anhydride. At the same time, it is possible to stabilize the resulting p-phenetidine, translating it into a stable target product - phenacetin.
Длительность реакции гидрирования зависит от интенсивности перемешивания реакционной массы. На используемой пилотной установке экспериментально установлено, что для полного превращения п-этоксинитробензола в фенацетин при температуре 60-70°C достаточно 1.5-2 часового перемешивания реакционной массы.The duration of the hydrogenation reaction depends on the intensity of mixing of the reaction mass. Using the pilot plant used, it was experimentally established that for the complete conversion of p-ethoxynitrobenzene to phenacetin at a temperature of 60-70 ° C, 1.5-2 hours stirring of the reaction mixture is sufficient.
Описываемый способ получения фенацетина по сравнению с известными имеет следующие преимущества:The described method for producing phenacetin in comparison with the known has the following advantages:
1. Для реализации каталитического способа получения фенацетина не требуются химические регенты-восстановители и соответствующие меры по очистке и утилизации отходов.1. For the implementation of the catalytic method for the production of phenacetin does not require chemical reagents, reducing agents and appropriate measures for the treatment and disposal of waste.
2. Предлагаемый способ предполагает использовать дешевый промышленно доступный катализатор Ni-Ренея.2. The proposed method involves the use of a cheap commercially available Ni-Raney catalyst.
3. Применяемый для гидрирования растворитель - изопропиловый спирт может быть легко регенерирован и многократно использован.3. The solvent used for hydrogenation - isopropyl alcohol can be easily regenerated and reused.
4. Заявляемый каталитический способ получения фенацетина позволяет осуществить в одном реакторе одновременно процессы гидрирования п-этоксинитробензола и ацетилирование промежуточно образующегося п-фенетидина без его выделения, что уменьшает расход реагентов и существенно упрощает технологическую схему.4. The inventive catalytic method for producing phenacetin allows the simultaneous hydrogenation of p-ethoxynitrobenzene and acetylation of the intermediate p-phenethidine without its isolation, which reduces the consumption of reagents and greatly simplifies the process flow diagram.
Технический результат, получаемый по предлагаемому способу, заключается в совершенствовании технологии синтеза, в том числе: использовании в производственном процессе вместо химических реагентных восстановителей водорода и, как следствие, упрощении выделения, очистке и повышении качества целевого продукта.The technical result obtained by the proposed method is to improve the synthesis technology, including: using hydrogen instead of chemical reagents in the production process and, as a result, simplifying the isolation, purification and improving the quality of the target product.
Пример 1. В металлический реактор емкостью 1 л, снабженный перемешивающим устройством, гильзой для термометра, манометром, газоподводящими трубками и рубашкой, подключенной к водяному термостату для нагрева и охлаждения реакционной массы, загружают 3.34 г (20.0 ммоль) п-этоксинитробензола II в 100 мл изопропилового спирта, 4.12 г (40.0 ммоль) уксусного ангидрида, 0.5 г Ni-Ренея. Реакционную смесь перемешивают под давлением водорода 2.0-4.0 атм водорода при температуре 60-70°C в течение 1,5-2 часов. При отсутствии в отобранной пробе (ТСХ) исходного п-фенетола II, реакционную массу фильтруют от катализатора, растворитель отгоняют под вакуумом. Остаток разбавляют 10-15 мл холодной воды, охлаждают до 5-10°C и перемешивают при этой температуре 0.5-1.0 час. Выпавший осадок фенацетина отфильтровывают, промывают 10-15 мл ледяной воды. После высушивания получают 3.30 г (92% от теории). Т.пл. 135-137°C (Т.пл. лит. [3] 136-137°C). Для получения фармакопейного фенацетина полученный продукт может быть перекристаллизован из дистиллированной воды с добавлением активированного угля. В случае отрицательного анализа кристаллов на цветность, проводят дополнительную кристаллизацию с добавлением гидросульфита натрия для осветления из расчета 0.01 г на 1 г фенацетина.Example 1. In a metal reactor with a capacity of 1 l, equipped with a stirrer, a thermometer sleeve, a manometer, gas pipes and a jacket connected to a water thermostat for heating and cooling the reaction mixture, 3.34 g (20.0 mmol) of p-ethoxynitrobenzene II in 100 ml are charged isopropyl alcohol, 4.12 g (40.0 mmol) of acetic anhydride, 0.5 g of Ni-Raney. The reaction mixture is stirred under a hydrogen pressure of 2.0-4.0 atm hydrogen at a temperature of 60-70 ° C for 1.5-2 hours. In the absence of the initial p-phenethol II in the selected sample (TLC), the reaction mixture is filtered from the catalyst, the solvent is distilled off under vacuum. The residue is diluted with 10-15 ml of cold water, cooled to 5-10 ° C and stirred at this temperature for 0.5-1.0 hours. The precipitated phenacetin precipitate is filtered off, washed with 10-15 ml of ice water. After drying, 3.30 g (92% of theory) are obtained. Mp 135-137 ° C (mp. Lit. [3] 136-137 ° C). To obtain pharmacopoeial phenacetin, the resulting product can be recrystallized from distilled water with the addition of activated carbon. In the case of a negative analysis of the crystals for color, additional crystallization is carried out with the addition of sodium hydrosulfite to clarify at the rate of 0.01 g per 1 g of phenacetin.
Предлагаемый каталитический способ получения позволяет синтезировать на предприятиях отечественной химико-фармацевтической промышленности субстанцию фенацетина для получения лекарственных препаратов.The proposed catalytic production method allows you to synthesize phenacetin substance at the enterprises of the domestic chemical and pharmaceutical industry for the production of medicines.
Источники информацииInformation sources
1. М.Д.Машковский, Лекарственные средства. Ч.1. Москва. Медицина. 1993. Стр. 202.1. M.D. Mashkovsky, Medicines. Part 1. Moscow. The medicine. 1993. p. 202.
2. Патент US 5932075, A1, 1999.2. Patent US 5932075, A1, 1999.
3. Патент US 2005/27120, A1.3. Patent US 2005/27120, A1.
4. Г.Дайсон, П.Мей. Химия синтетических лекарственных веществ. Мир. Москва, 1964. Стр. 124.4. G. Dyson, P. May. Chemistry of synthetic medicinal substances. Peace. Moscow, 1964. Page 124.
Claims (1)
путем восстановления п-этоксинитробензола, ацилирования образующегося п-этоксианилина и выделением целевого продукта, отличающийся тем, что процесс восстановления ведут в изопропиловом спирте в присутствии уксусного ангидрида и катализатора Ni-Ренея при давлении водорода 2,0-4,0 атм при температуре 60-70°C. The method of obtaining phenacetin formula I
by reducing p-ethoxynitrobenzene, acylating the resulting p-ethoxyaniline and isolating the target product, characterized in that the reduction process is carried out in isopropyl alcohol in the presence of acetic anhydride and Ni-Raney catalyst at a hydrogen pressure of 2.0-4.0 atm at a temperature of 60- 70 ° C.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2012130826/04A RU2546111C2 (en) | 2012-07-18 | 2012-07-18 | Method of phenacetin obtaining |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2012130826/04A RU2546111C2 (en) | 2012-07-18 | 2012-07-18 | Method of phenacetin obtaining |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2012130826A RU2012130826A (en) | 2014-01-27 |
| RU2546111C2 true RU2546111C2 (en) | 2015-04-10 |
Family
ID=49956897
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2012130826/04A RU2546111C2 (en) | 2012-07-18 | 2012-07-18 | Method of phenacetin obtaining |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2546111C2 (en) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002105037A (en) * | 2000-09-29 | 2002-04-10 | Sumitomo Chem Co Ltd | Method for producing acetylamine |
| CN101823979A (en) * | 2010-05-17 | 2010-09-08 | 无锡宏瑞生物医药科技有限公司 | Clean production process for paraacetamino phenetole by reactor coupled simulated moving bed |
-
2012
- 2012-07-18 RU RU2012130826/04A patent/RU2546111C2/en not_active IP Right Cessation
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002105037A (en) * | 2000-09-29 | 2002-04-10 | Sumitomo Chem Co Ltd | Method for producing acetylamine |
| CN101823979A (en) * | 2010-05-17 | 2010-09-08 | 无锡宏瑞生物医药科技有限公司 | Clean production process for paraacetamino phenetole by reactor coupled simulated moving bed |
Non-Patent Citations (2)
| Title |
|---|
| DWPI * |
| Е. KUO et al., Facile reduction of aromatic nitro compounds to anilines with 2-propanol and Raney nickel, SYNTHETIC COMMUNICATIONS, 1985, 15(7), pp.599-602. АБДУЛЛАЕВ М. Г., Получение 4-этоксиацетанилида восстановительным ацетилированием п-этоксинитробензола на палладиевых катализаторах, ХИМИКО-ФАРМАЦЕВТИЧЕСКИЙ ЖУРНАЛ, 2002, 6, с.40-41. Г. ДАЙСОН, П. МЕЙ, Химия синтетических лекарственных веществ, Москва, Мир, 1964, с.124-125. * |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2012130826A (en) | 2014-01-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN110590635A (en) | Preparation method of levetiracetam and intermediate thereof | |
| Melis et al. | Synthesis of functionalized tryptamines by Brønsted acid catalysed cascade reactions | |
| CN107200705B (en) | A kind of preparation method of 3-nitro-2-indolinone derivative | |
| Hajjami et al. | Incredible role of glycerol in multicomponent synthesis of 2, 3-dihydroquinazoline-4 (1H)-ones and 1-amidoalkyl-2-naphthols | |
| CN109678840A (en) | The preparation method of pomalidomide | |
| CN108558692A (en) | A kind of preparation method of amides compound | |
| CN102351777B (en) | Preparation method for chiral 3-hydroxyl-3-methylene nitro indole-2-ketone derivative | |
| RU2546111C2 (en) | Method of phenacetin obtaining | |
| RU2461543C1 (en) | Method for producing paracetamol | |
| WO2021047603A1 (en) | Synthesis method applied to kras inhibitor drug heterocyclic intermediate | |
| CN116041203B (en) | Among the octenib Synthesis method of intermediate | |
| RU2495865C1 (en) | METHOD OF PRODUCING n-ACETYLAMINOPHENOL | |
| CN113024411B (en) | Preparation method of tralkoxydim | |
| JP6028606B2 (en) | Method for producing amine compound | |
| CN105418613A (en) | Environment-friendly preparation method of adenine | |
| CN103467356B (en) | Tetrahydroindole compound, and preparation method and application thereof | |
| Valizadeh et al. | A facile and efficient [bmim] N 3 catalyzed direct oxidative esterification of arylaldehydes with alcohols | |
| RU2574733C1 (en) | Method for producing paracetamol | |
| RU2505526C1 (en) | Method of obtaining anesthesinum | |
| CN104450851B (en) | A kind of preparation method for removing acetyl cefathiamidine | |
| JP2018525376A (en) | Novel process for producing chromanol derivatives | |
| RU2615760C1 (en) | Method for n-(4-methyl-3-chlorophenyl)-2-acetoxy-3,5-dichlorobenzamide preparation | |
| CN108929226B (en) | A kind of method for preparing benzoylformate derivatives | |
| CN113004161B (en) | Preparation method of (2R, 3R) -3-methyl-3-phenylalanine | |
| Wan et al. | High stereoselective mannich reaction catalyzed by starch sulfonic acid in water |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20150719 |