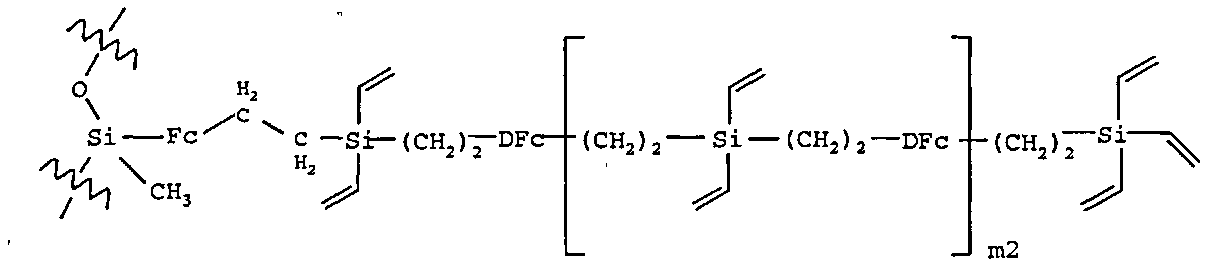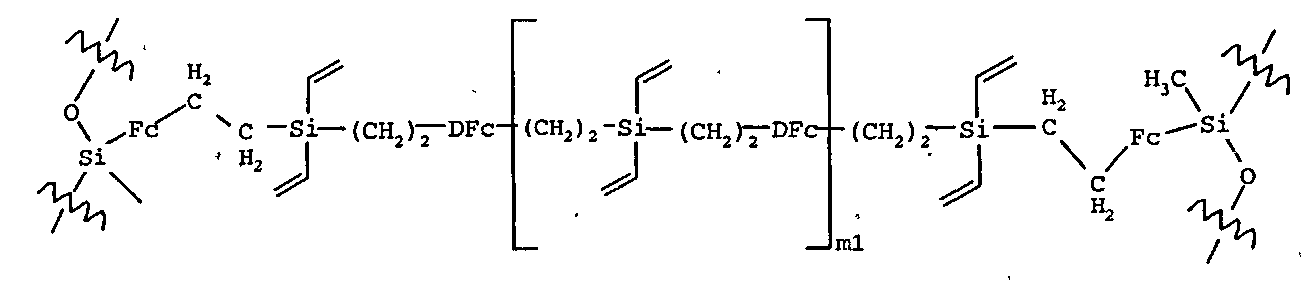RU2441874C1 - Polymer on the base of poly(ferrocenyl)sylane, method of its production and the film including the polymer the base of poly(ferrocenyl)sylane - Google Patents
Polymer on the base of poly(ferrocenyl)sylane, method of its production and the film including the polymer the base of poly(ferrocenyl)sylane Download PDFInfo
- Publication number
- RU2441874C1 RU2441874C1 RU2010125697/04A RU2010125697A RU2441874C1 RU 2441874 C1 RU2441874 C1 RU 2441874C1 RU 2010125697/04 A RU2010125697/04 A RU 2010125697/04A RU 2010125697 A RU2010125697 A RU 2010125697A RU 2441874 C1 RU2441874 C1 RU 2441874C1
- Authority
- RU
- Russia
- Prior art keywords
- formula
- group
- substituted
- represented
- range
- Prior art date
Links
- 0 CC(C1[C@]23*(C)C2C3)N1N Chemical compound CC(C1[C@]23*(C)C2C3)N1N 0.000 description 7
- BWWLCYLGZIWOHK-UHFFFAOYSA-N CCN(C)C(C)(C)C Chemical compound CCN(C)C(C)(C)C BWWLCYLGZIWOHK-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/22—Polysiloxanes containing silicon bound to organic groups containing atoms other than carbon, hydrogen and oxygen
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/06—Preparatory processes
- C08G77/08—Preparatory processes characterised by the catalysts used
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/48—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule in which at least two but not all the silicon atoms are connected by linkages other than oxygen atoms
- C08G77/58—Metal-containing linkages
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/60—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule in which all the silicon atoms are connected by linkages other than oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J5/00—Manufacture of articles or shaped materials containing macromolecular substances
- C08J5/18—Manufacture of films or sheets
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/0009—Materials therefor
- G02F1/0072—Mechanical, acoustic, electro-elastic, magneto-elastic properties
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/0128—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on electro-mechanical, magneto-mechanical, elasto-optic effects
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/19—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on variable-reflection or variable-refraction elements not provided for in groups G02F1/015 - G02F1/169
Landscapes
- Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Nonlinear Science (AREA)
- Optics & Photonics (AREA)
- General Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Materials Engineering (AREA)
- Acoustics & Sound (AREA)
- Silicon Polymers (AREA)
Abstract
Description
Настоящее изобретение относится к полимерам на основе поли(ферроценил)силана (в аббревиатуре - PFS), к способам их получения и пленкам на основе поли(ферроценил)силановых полимеров. Предлагается упрощенный способ получения полимеров на основе PFS, реализация которого в промышленности обеспечит снижение производственных затрат. Кроме того, полимеры на основе PFS используются в фотонных полупроводниковых матрицах.The present invention relates to polymers based on poly (ferrocenyl) silane (abbreviated as PFS), to methods for their preparation and films based on poly (ferrocenyl) silane polymers. A simplified method for producing PFS-based polymers is proposed, the implementation of which in industry will ensure a reduction in production costs. In addition, PFS-based polymers are used in photonic semiconductor arrays.
Электроактивные полимеры (Electroactive Polymers - ЕАР) являются полимерами, которые способны преобразовывать электрическую энергию в механическую энергию, или наоборот. ЕАР могут быть разделены на категорию ионных ЕАР и категорию электрических ЕАР. К категории ионных ЕАР относятся композиты из металлов и ионных полимеров, а также токопроводящие полимеры. К категории электрических ЕАР относятся диэлектрические эластомеры и электрострикционные полимеры. Эти полимеры имеют разные назначения из-за их особенностей. Среди таких полимеров ионные металл-полимерные композиты являются наиболее подходящими для использования в дисплеях из-за их низкого рабочего напряжения и относительно короткого времени отклика. Однако использование ионных металл-полимерных композитов в фотонной кристаллической матрице затруднено.Electroactive Polymers (EAP) are polymers that can convert electrical energy into mechanical energy, or vice versa. EAP can be divided into the category of ionic EAP and the category of electrical EAP. Compounds of metals and ionic polymers, as well as conductive polymers, belong to the category of ionic EAPs. Electrical EAPs include dielectric elastomers and electrostrictive polymers. These polymers have different purposes because of their characteristics. Among these polymers, ionic metal-polymer composites are most suitable for use in displays because of their low operating voltage and relatively short response time. However, the use of ionic metal-polymer composites in a photonic crystal matrix is difficult.
При изучении существующего уровня техники был проведен анализ способов изготовления ЕАР полимеров с поперечными связями, содержащих способные к окислению и восстановлению металлоорганические фрагменты. В этом отношении мономеры, содержащие представителей ферроценовой группы, являются очень перспективными для получения ЕАР с отличными рабочими параметрами, поскольку они устойчивы по отношению к кислороду и воде, и способны обратимо электрохимически окисляться и восстанавливаться в различных растворителях.When studying the current level of technology, an analysis was made of the methods for the manufacture of crosslinked EAP polymers containing organometallic fragments capable of oxidation and reduction. In this regard, monomers containing representatives of the ferrocene group are very promising for obtaining EAP with excellent operating parameters, since they are resistant to oxygen and water, and are capable of reversibly electrochemically oxidizing and reducing in various solvents.
Такие мономеры (сила[1]ферроценофаны - SFP) полимеризируются посредством полимеризации с раскрытием цикла (ring-opening polymerization - ROP), такой как тепловая полимеризация (TP) или полимеризация с использованием металлокомплексного катализатора (МСР). Однако тепловая полимеризация требует высокой температуры 130-280 градусов и атмосферы из инертного газа, и, кроме того, она не дает возможности управлять молекулярным весом полимера (см. Bellas, V.; Rehahn, М. Angewandte Chemie International Edition, 2007, 46, 5082. (2) Manners, I. Organometallics 1996, 15, 1972) [1].Such monomers (strength [1] ferrocenophanes - SFP) are polymerized by ring-opening polymerization (ROP), such as thermal polymerization (TP) or polymerization using a metal complex catalyst (MCP). However, thermal polymerization requires a high temperature of 130-280 degrees and an atmosphere of inert gas, and, in addition, it does not make it possible to control the molecular weight of the polymer (see Bellas, V .; Rehahn, M. Angewandte Chemie International Edition, 2007, 46, 5082. (2) Manners, I. Organometallics 1996, 15, 1972) [1].
Анионная (АР) полимеризация SFP выполняется в относительно мягких условиях, давая полимеры с высокой степенью полимеризации. Она дает возможность управления молекулярным весом полимера, но в то же время требует чрезвычайно чистых мономеров, полученных путем многочисленных процессов очистки. В то же время полимеризация МСР с использованием соединений платины в качестве катализатора не требует высокой температуры и мономеров высокой чистоты, которые необходимы для тепловой полимеризации и анионной полимеризации, однако данный метод не эффективен для контролирования молекулярного веса полимера.Anionic (AP) SFP polymerization is performed under relatively mild conditions, giving polymers with a high degree of polymerization. It makes it possible to control the molecular weight of the polymer, but at the same time requires extremely pure monomers obtained through numerous purification processes. At the same time, the polymerization of MCP using platinum compounds as a catalyst does not require high temperature and high purity monomers, which are necessary for thermal polymerization and anionic polymerization, however, this method is not effective for controlling the molecular weight of the polymer.
На данный момент в качестве электроактивных полимерных материалов для использования в создании образцов полноцветного пиксела на основе опаловых структур широко используются полимеры, получаемые при сшивании линейных поли(ферроценилметилвинил)силанов (PFMVS) и поли(ферроценилдивинил)силанов (PFDVS) с помощью органических кросс-линкеров (связующих компонентов) в результате радикальной полимеризации (см., например, Ozin, G.A. Angewandte Chemie International Edition, 2009, 48, 943) [2]. В этом случае линейные полимеры PFMVS и PFDVS предварительно синтезируются методом анионной полимеризации AnROP (см., например, J. Am. Chem. Soc. 1996, 118, 4102) [3] из соответствующих винил-замещенных сила[1]ферроценофанов в результате отдельной синтетической стадии. В качестве сшивающего агента используются различные органические α,ω-дитиолы, например 1,4-бутандитиол в количестве 5-10 мольных % от количества линейного полимера. Реакция сшивки инициируется радикальным катализатором Igracure под действием интенсивного УФ-излучения в течение 10-14 часов. Образец сшитого полимера, полученного при использовании 10 мольных % кросс-линкера, показывает механическую стабильность, достаточную для использования его в качестве рабочего материала в образцах полноцветных пикселов. Несмотря на то что известный способ [2] получения сшитого электроактивного PFS полимера является относительно простым и уже зарекомендовал себя эффективным для приготовления полимерных матриц типа "инвертированного опала", этот метод имеет ряд недостатков. В частности:Currently, polymers obtained by crosslinking linear poly (ferrocenylmethylvinyl) silanes (PFMVS) and poly (ferrocenyldivinyl) silanes (PFDVS) using organic cross-linkers are widely used as electroactive polymer materials for use in creating samples of a full-color pixel based on opal structures. (binding components) as a result of radical polymerization (see, for example, Ozin, GA Angewandte Chemie International Edition, 2009, 48, 943) [2]. In this case, linear polymers PFMVS and PFDVS are pre-synthesized by AnROP anionic polymerization (see, for example, J. Am. Chem. Soc. 1996, 118, 4102) [3] from the corresponding vinyl-substituted force [1] ferrocenophanes as a result of a separate synthetic stage. Various organic α, ω-dithiols, for example 1,4-butanedithiol, are used as a crosslinking agent in an amount of 5-10 mol% of the amount of a linear polymer. The crosslinking reaction is initiated by the radical Igracure catalyst under the influence of intense UV radiation for 10-14 hours. A crosslinked polymer sample obtained using 10 mol% cross-linker shows mechanical stability sufficient to be used as a working material in samples of full-color pixels. Despite the fact that the known method [2] for producing a crosslinked electroactive PFS polymer is relatively simple and has already proven effective for the preparation of polymer matrices of the “inverted opal” type, this method has several disadvantages. In particular:
а) получение линейного полимера PFMVS или PFDVS методом AnROP является отдельной синтетической стадией, требующей использования исходногоa) the preparation of the linear polymer PFMVS or PFDVS by AnROP is a separate synthetic step, requiring the use of the original
сила[1]ферроценофана особо высокой чистоты, прошедшего специальную многостадийную очистку (10-15 стадий), и выделения продукта из реакционной смеси, - все это усложняет технологическую реализацию метода в промышленности;the strength [1] of ferrocenophane of especially high purity, which underwent a special multi-stage purification (10-15 stages), and the isolation of the product from the reaction mixture — all this complicates the technological implementation of the method in industry;
б) использование 10 мольных % органического сшивающего агента снижает на такую же величину количество электроактивных фрагментов в конечном сшитом полимере и, соответственно, величину его отклика (например, степень набухания) под действием электрического тока;b) the use of 10 mol% of an organic crosslinking agent reduces by the same amount the number of electroactive fragments in the final crosslinked polymer and, accordingly, the magnitude of its response (for example, the degree of swelling) under the influence of an electric current;
в) метод сшивки, основанный на радикальной тиоленовой реакции, требующей постоянного воздействия мощного УФ-излучения для ее протекания, является серьезным ограничением метода, поскольку не позволяет использовать его для получения сшитого PFS полимера при приготовлении композитных материалов, непрозрачных для УФ-излучения. Кроме того, в случае достаточно чувствительных к кислороду воздуха PFS-полимеров желательным (особенно для тонких PFS-пленок) является использование инертной атмосферы во время процесса сшивки, что также является технологически неудобным при применении постоянного облучения образца УФ-светом.c) the crosslinking method based on the radical thiolene reaction, which requires constant exposure to powerful UV radiation to proceed, is a serious limitation of the method because it does not allow using it to obtain a crosslinked PFS polymer in the preparation of composite materials that are opaque to UV radiation. In addition, in the case of PFS polymers that are sufficiently sensitive to air oxygen, it is desirable (especially for thin PFS films) to use an inert atmosphere during the crosslinking process, which is also technologically inconvenient when continuous exposure of the sample to UV light is applied.
В целом известный на данный момент метод приготовления сетчатых PFS-полимеров страдает как от технологических недостатков (необходимость специальной доочистки исходных сила[1]ферроценофанов, использование специального кварцевого оборудования для УФ-облучения), так и от невозможности достичь некоторых технических характеристик (максимальное количество электроактивных ферроценовых фрагментов в сшитом полимере), а в ряде случаев он просто непригоден (для непрозрачных для УФ-диапазона материалов, предназначенных для пропитки PFS-полимером).In general, the currently known method for the preparation of cross-linked PFS polymers suffers both from technological shortcomings (the need for special post-treatment of the initial strength [1] of ferrocenophanes, the use of special quartz equipment for UV irradiation), and the inability to achieve some technical characteristics (maximum number of electroactive ferrocene fragments in a crosslinked polymer), and in some cases it is simply unsuitable (for materials opaque to the UV range intended for impregnation of PFS-polymer ).
Задачей, на решение которой направлено заявляемое изобретение, является разработка технологически простого способа получения сшитого PFS-полимера, лишенного недостатков известных аналогов, в частности не требующего специальных многостадийных методов очистки исходных реагентов (сила[1]ферроценофанов); состоящего практически полностью из электроактивных ферроценилсилановых звеньев и пригодного для получения сшитого PFS-полимера на/в любых (прозрачных и непрозрачных) материалах.The problem to which the invention is directed is the development of a technologically simple way to obtain a cross-linked PFS-polymer, devoid of the disadvantages of known analogues, in particular not requiring special multi-stage methods for purification of the starting reagents (strength [1] of ferrocenophanes); consisting almost entirely of electroactive ferrocenylsilane units and suitable for producing a crosslinked PFS polymer on / in any (transparent and opaque) materials.
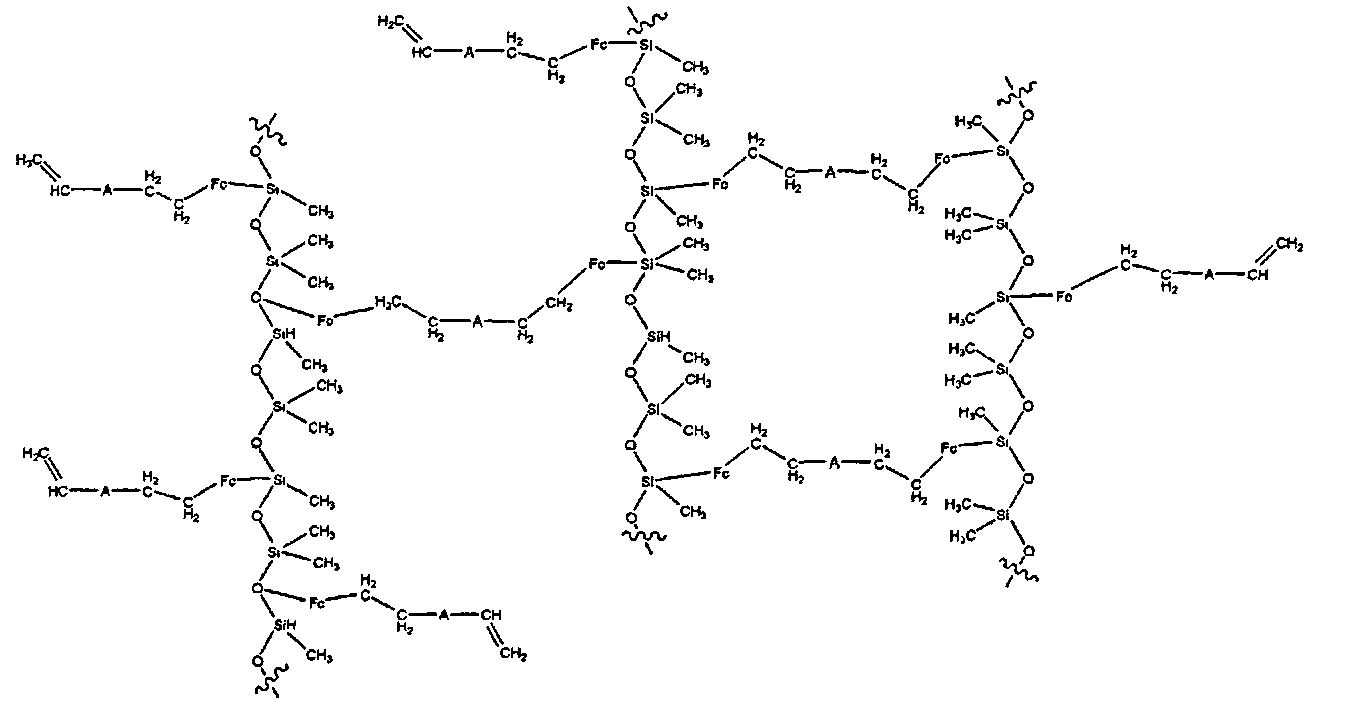
Технический результат достигается за счет разработки новой формулы ячеистых полимеров на основе PFS, которые изготовляют с применением упрощенного процесса и используют для производства пленки, включающей в себя ячеистые полимеры на основе PFS. При этом заявляемый ячеистый полимер на основе поли(ферроценил)силана включает в себя повторяющийся блок, представленный Формулой 1, повторяющийся блок, представленный Формулой 2, и повторяющийся блок, представленный Формулой 3:The technical result is achieved through the development of a new formula of cellular polymers based on PFS, which are manufactured using a simplified process and are used for the production of films, including cellular polymers based on PFS. In this case, the inventive cellular polymer based on poly (ferrocenyl) silane includes a repeating unit represented by Formula 1, a repeating unit represented by Formula 2, and a repeating unit represented by Formula 3:
<Формула 1><Formula 1>
<Формула 2><Formula 2>
<Формула 3><Formula 3>
где Fc представляет собой группу ферроценилена, представленную Формулой 4а, DFc является связующей группой на основе диферроценилсилана, представленной Формулой 4b, a m1 и m2 - каждый по отдельности является числом 0 или 1;where Fc is a ferrocene group represented by Formula 4a, DFc is a linker group based on diferrocenylsilane represented by Formula 4b, am 1 and m 2 - each individually is a number 0 or 1;
<Формула 4а><Formula 4a>
где m4 является числом из диапазона от 1 до 10;where m4 is a number from the range from 1 to 10;
<Формула 4b><Formula 4b>
где n1 и n2 являются каждый по отдельности числом из диапазона от 5 до 95, X1 - этоwhere n 1 and n 2 are each individually a number from the range from 5 to 95, X 1 is
или or
где R1 и R2 - каждый по отдельности представляет собой замещенную или незамещенную в диапазоне от С6 до С20 алкильную группу или замещенную или незамещенную в диапазоне от С6 до С30 арильную группу, а Х2 - представляет собойwhere R 1 and R 2 each individually represents a substituted or unsubstituted alkyl group in the range from C6 to C20 or a substituted or unsubstituted aryl group in the range from C6 to C30, and X 2 represents
-О-, -S-, в диапазоне от С6 до С20 замещенную или незамещенную алкиленовую группу, или в диапазоне от С6 до С30 замещенную или незамещенную ариленовую группу. При этом возможны различные описанные ниже варианты химической формулы заявляемого полимера на основе PFS.-O-, -S-, in the range from C6 to C20 a substituted or unsubstituted alkylene group, or in the range from C6 to C30 a substituted or unsubstituted arylene group. In this case, the various options described below for the chemical formula of the inventive polymer based on PFS are possible.
Предложен также способ получения ячеистого полимера на основе поли(ферроценил)силана, включающий в себя выполнение следующих операций: пространственно сшивают базовый полимер, представленный Формулой 5, и связующий компонент, представленный Формулой 6:A method for producing a cellular polymer based on poly (ferrocenyl) silane is also proposed, which includes the following operations: the base polymer represented by Formula 5 and the binder component represented by Formula 6 are spatially crosslinked:
<Формула 5><Formula 5>
где n1 и n2 каждый по отдельности является числом из диапазона от 5 до 95, m3 - это 0 или 1,where n 1 and n 2 each individually is a number from the range from 5 to 95, m3 is 0 or 1,
или or
где R1 и R2 - каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 - представляет собой -О-, -S-, С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу;where R 1 and R 2 - each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 - represents-O-, -S-, C6 to C20 substituted or an unsubstituted alkylene group, or from C6 to C30 a substituted or unsubstituted arylene group;
<Формула 6><Formula 6>
где n3 представляет собой число от 10 до 25, и R3 обозначает метальную группу и ферроценильную группу, представленную Формулой 13, и когда метальная группа и ферроценильная группа сосуществуют как R3, отношение количества метильных групп к сумме метальных групп и ферроценильных групп находится в диапазоне от 0,1 до 0,9:where n 3 is a number from 10 to 25, and R 3 denotes a methyl group and a ferrocenyl group represented by Formula 13, and when the methyl group and the ferrocenyl group coexist as R 3 , the ratio of the number of methyl groups to the sum of methyl groups and ferrocenyl groups is range from 0.1 to 0.9:
<Формула 13><Formula 13>
где m4 - это число от 1 до 10.where m4 is a number from 1 to 10.
И, наконец, предложена структура полимерной пленки, включающей в себя: подложку; и ячеистый полимер на основе поли(ферроценил)силана, полученного любым из заявляемых способов, отличающейся тем, что ячеистый полимер на основе поли(ферроценил)силана связан с этой подложкой.And finally, the proposed structure of a polymer film, including: a substrate; and a cellular polymer based on poly (ferrocenyl) silane obtained by any of the claimed methods, characterized in that the cellular polymer based on poly (ferrocenyl) silane is bonded to this substrate.
Дополнительные аспекты данного комплекса связанных единым замыслом изобретений поясняются далее по тексту описания на примерах реализации со ссылками на графические материалы. При этом предложенные варианты воплощения могут принимать различные формы и не должны рассматриваться как ограничивающиеся настоящим описанием. Поэтому такие варианты реализации описаны далее со ссылкой на чертежи всего лишь с целью пояснения отдельных аспектов технического решения.Additional aspects of this complex of inventions related by a single concept are explained further in the text of the description using examples of implementation with reference to graphic materials. Moreover, the proposed embodiments may take various forms and should not be construed as being limited by the present description. Therefore, such embodiments are described below with reference to the drawings merely for the purpose of explaining certain aspects of the technical solution.
Ячеистый полимер на основе PFS, получаемый согласно заявляемому изобретению, является электроактивным и поперечно связанным, при этом он включает в себя повторяющийся блок, представленный Формулой 1, повторяющийся блок, представленный Формулой 2, и повторяющийся блок, представленный Формулой 3:The PFS-based cellular polymer obtained according to the claimed invention is electroactive and cross-linked, while it includes a repeating unit represented by Formula 1, a repeating unit represented by Formula 2, and a repeating unit represented by Formula 3:
<Формула 1><Formula 1>
<Формула 2><Formula 2>
<Формула 3><Formula 3>
где Fc - группа ферроценилена, представленная Формулой 4а, DFc - связующая группа на основе диферроценилсилана, представленная Формулой 4b, a m1 и m2 - каждый по отдельности равен 0 или 1;where Fc is the ferrocene group represented by Formula 4a, DFc is the linker group based on diferrocenylsilane represented by Formula 4b, and m1 and m2 are each individually 0 or 1;
<Формула 4а><Formula 4a>
где m4 - число из диапазона от 1 до 10;where m4 is a number from the range from 1 to 10;
<Формула 4b><Formula 4b>
где n1 и n2 - каждый в отдельности является числом из диапазона от 5 до 95, X1 - этоwhere n 1 and n 2 - each individually is a number from the range from 5 to 95, X 1 is
или or
где R1 и R2 - каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 - представляет собой -О-, -S-, С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу.where R 1 and R 2 - each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 - represents-O-, -S-, C6 to C20 substituted or an unsubstituted alkylene group, or from C6 to C30 a substituted or unsubstituted arylene group.
Согласно заявляемому изобретению в ячеистом полимере повторяющийся блок Формулы 1 может иметь степень полимеризации, например, от близкой к 5 до близкой к ста, повторяющийся блок Формулы 2 может иметь степень полимеризации, например, от близкой к пяти до близкой к ста, а повторяющийся блок Формулы 3 может иметь степень полимеризации, например, от близкой к десяти до близкой к двадцати пяти.According to the claimed invention, in a cellular polymer, the repeating unit of Formula 1 may have a degree of polymerization, for example, from close to 5 to close to one hundred, the repeating unit of Formula 2 may have a polymerization degree, for example, from close to five to close to one hundred, and the repeating unit of Formula 3 may have a degree of polymerization, for example, from close to ten to close to twenty-five.
Согласно заявляемому изобретению, если повторяющийся блок Формулы 1 повторился, то, по крайней мере, один из повторяющихся блоков Формулы 2 и повторяющийся блок Формулы 3 могут быть вставлены между повторяющимися блоками Формулы 1.According to the claimed invention, if the repeating block of Formula 1 is repeated, then at least one of the repeating blocks of Formula 2 and the repeating block of Formula 3 can be inserted between the repeating blocks of Formula 1.
Ячеистый полимер на основе PFS, включающий повторяющийся блок, представленный Формулой 1, повторяющийся блок, представленный Формулой 2, и повторяющийся блок, представленный Формулой 3, может быть получен путем полимеризации базового полимера, представленного Формулой 5, и связующего компонента, представленного Формулой 6:A PFS-based cellular polymer including a repeating unit represented by Formula 1, a repeating unit represented by Formula 2, and a repeating unit represented by Formula 3 can be obtained by polymerizing a base polymer represented by Formula 5 and a binder component represented by Formula 6:
<Формула 5><Formula 5>
где n1 и n2 каждый в отдельности является числом из диапазона от 5 до 95, m3 - это 0 или 1, X1 - этоwhere n 1 and n 2 each individually is a number from the range from 5 to 95, m3 is 0 or 1, X 1 is
или or
где R1 и R2 - каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 - представляет собой -О-, -S-, С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу;where R 1 and R 2 - each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 - represents-O-, -S-, C6 to C20 substituted or an unsubstituted alkylene group, or from C6 to C30 a substituted or unsubstituted arylene group;
<Формула 6><Formula 6>
где n3 представляет число от 10 до 25, и R3 может обозначать метальную и ферроценильную группу, представленную Формулой 13, и когда R3 представлен смесью метальной и ферроценильной групп, мольное соотношение метальной к сумме метальной и ферроценильной групп находится в диапазоне от 0,1 до 0,9:where n 3 is a number from 10 to 25, and R 3 can denote a methyl and ferrocenyl group represented by Formula 13, and when R 3 is a mixture of methyl and ferrocenyl groups, the molar ratio of metal to total methyl and ferrocenyl groups is in the range from 0, 1 to 0.9:
<Формула 13><Formula 13>
где m4 - это число от 1 до 10.where m4 is a number from 1 to 10.
Полимеры, полученные согласно заявляемым примерам реализации, могут включать различные повторяющиеся блоки в своем каркасе, и хотя эти повторяющиеся блоки описываются как отдельное образование в составе полимеров, такие полимеры могут также являться блок-сополимерами или статистическими сополимерами.The polymers obtained according to the claimed implementation examples may include various repeating blocks in their framework, and although these repeating blocks are described as a separate formation in the composition of the polymers, such polymers can also be block copolymers or random copolymers.
Что касается базового полимера по Формуле 5, когда m3 является 0, базовый полимер может представлять собой базовый полимер, представленный Формулой 7:As for the base polymer according to Formula 5, when m3 is 0, the base polymer may be a base polymer represented by Formula 7:
<Формула 7><Formula 7>
где n1 и n2 являются каждый в отдельности числом из диапазона от 5 до 95, X1 - этоwhere n 1 and n 2 are each individually a number from the range from 5 to 95, X 1 is
или or
где R1 и R2 - каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 - представляет собой -О-, -S-, С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу.where R 1 and R 2 - each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 - represents-O-, -S-, C6 to C20 substituted or an unsubstituted alkylene group, or from C6 to C30 a substituted or unsubstituted arylene group.
- Получение базового полимера- Getting the base polymer
Базовый полимер, представленный Формулой 7, может быть получен согласно Схеме Реакции 1:The base polymer represented by Formula 7 can be obtained according to Reaction Scheme 1:
<Схема Реакции 1><Reaction Scheme 1>
где X1 - это или where X 1 is or
где R1 и R2 - каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 - представляет собой -О-, -S-, С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу; n1 и n2 - каждый по отдельности представлен числом от 5 до 95, и n представляет собой n1+n2.where R 1 and R 2 - each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 - represents-O-, -S-, C6 to C20 substituted or an unsubstituted alkylene group, or from C6 to C30 a substituted or unsubstituted arylene group; n 1 and n 2 are each individually represented by a number from 5 to 95, and n represents n 1 + n 2 .
Способ получения согласно Схеме Реакции 1 - это способ получения линейного базового PFS. Согласно Схеме Реакции 1 компонент на основе дигидросилана по Формуле 8 вступает в реакцию с диметилсила[1]ферроценофаном по Формуле 9, образуя в результате раскрытия цикла (ROP) линейный олигоферроценилсилан с Формулой 10, имеющей Si-H на обоих концах цепи; и затем к нему добавляют избыточный тетравинилсилан для образования в результате гидросилилирования олигоферроценилсилана по Формуле 7, несущего тривинилсилильные группы на концах цепи. Что касается базового полимера по Формуле 7, то величина суммы n1 и n2 может лежать в диапазоне значений от близких к десяти до близких к ста.The production method according to Reaction Scheme 1 is a method for producing a linear base PFS. According to Reaction Scheme 1, the dihydrosilane-based component of Formula 8 reacts with dimethylsil [1] by ferrocenophane of Formula 9 to form a linear oligoferrocenylsilane with
Полимеризация с раскрытием цикла и гидросилилирование по Схеме Реакции 1 могут проходить в присутствии катализатора на основе соединений платины (Pt), например, катализатора Карстеда Pt[(СН2=СН-SiMe2)2O]1.5 и димера соли Цейзе Pt[(С2Н4)Cl2]2. Количество такого платинового катализатора может лежать в диапазоне от близкого к 0,01 мольного % до близкого к 1 мольного %, из расчета на 1 моль реагента.Cycle opening polymerization and hydrosilylation according to the Scheme of Reaction 1 can take place in the presence of a catalyst based on platinum (Pt) compounds, for example, Carsted catalyst Pt [(СН 2 = СН-SiMe 2 ) 2 O] 1.5 and Zeiss salt dimer Pt [(С 2 H 4 ) Cl 2 ] 2 . The amount of such a platinum catalyst may range from close to 0.01 mol% to close to 1 mol%, based on 1 mol of reagent.
Гидросилилирование может быть выполнено от 2 до 10 раз быстрее, если Si(vinyl)4 взят в избытке, при этом избыточное количество непрореагировавшего Si(vinyl)4 может быть удалено с помощью вакуума.Hydrosilylation can be performed 2 to 10 times faster if Si (vinyl) 4 is taken in excess, while an excess of unreacted Si (vinyl) 4 can be removed by vacuum.
Что касается Схемы Реакции 1, то в качестве органического растворителя может быть использован бензол, толуол, или ксилол, и реакция может быть выполнена, например, в течение 1-48 часов при температуре от 10 до 50°С.As for Reaction Scheme 1, benzene, toluene, or xylene can be used as the organic solvent, and the reaction can be performed, for example, within 1-48 hours at a temperature of from 10 to 50 ° C.
Далее, базовый полимер по Формуле 7 может вступать в реакцию с линейным олигоферроценилсиланом по Формуле 10 в присутствии катализатора на основе соединений платины, образуя в результате базовый полимер по Формуле 11, приведенной ниже, то есть базовый полимер, представленный Формулой 5 при m3 равной единице.Further, the base polymer according to Formula 7 can react with a linear oligoferrocenylsilane according to
<Формула 11><Formula 11>
где X1 - этоwhere X 1 is
или or
где R1 и R2 - каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 - представляет собой -О-, -S-, С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу; n1 и n2 - каждый по отдельности представлен числом от 5 до 95.where R 1 and R 2 - each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 - represents-O-, -S-, C6 to C20 substituted or an unsubstituted alkylene group, or from C6 to C30 a substituted or unsubstituted arylene group; n 1 and n 2 - each individually represented by a number from 5 to 95.
- Получение связующего компонента- Obtaining a binder component
Связующий компонент по Формуле 6, который должен вступать в реакцию с базовым полимером с Формулой 5, может быть получен согласно Схеме Реакции 2:The binder component according to Formula 6, which should react with the base polymer with Formula 5, can be obtained according to Reaction Scheme 2:
<Схема Реакции 2><Reaction Scheme 2>
где в качестве R4 может применяться смесь из метальной группы и водорода, в качестве R3 может применяться смесь из метальной группы и ферроценильной группы с Формулой 13, причем n3 принимает значение из диапазона от десяти до двадцати пяти,wherein as R 4 may apply a mixture of hydrogen and a methyl group as R 3 can be a mixture of methyl group and ferrocenyl group of Formula 13, wherein n assumes the value 3 in the range of ten to twenty-five,
<Формула 13><Formula 13>
где m4 принимает значение из диапазона от единицы до десяти.where m4 takes a value from a range of one to ten.
Схема Реакции 2 - это процесс получения связующего компонента с Формулой 6. В Схеме Реакции 2 поли(диметилсилокеан) с Формулой 12, который является линейным олигомером, вступает в реацию с диметилсила[1]ферроценофаном с Формулой 9 в присутствии катализатора на основе Pt, получая таким образом связующий компонент с Формулой 7.Reaction Scheme 2 is a process for preparing a binder component with Formula 6. In Reaction Scheme 2, poly (dimethylsiloxane) with Formula 12, which is a linear oligomer, enters into reaction with dimethylsil [1] ferrocenophane with Formula 9 in the presence of a Pt-based catalyst, to obtain thus a binder component with Formula 7.
При использовании поли(диметилсилоксана) с Формулой 12 в качестве исходного материала некоторые метальные группы в нем замещены водородом, и необходимо заместить эти атомы водорода на ферроценильные группы с Формулой 13. Иными словами, в поли(диметилсилоксане) с Формулой 12, R4 может означать смесь из метильной группы и водорода, а содержание гидридных групп к метальным, то есть H/(H+methyl), может лежать в диапазоне значений от 0,1 до 0,9, например около 0,1-0,5, и если это значение составляет 0,5, то это означает, что гидридная и метальная группы в R4 присутствуют в соотношении 1:1.When using poly (dimethylsiloxane) with Formula 12 as starting material, some methyl groups in it are replaced by hydrogen, and it is necessary to replace these hydrogen atoms with ferrocenyl groups with Formula 13. In other words, in poly (dimethylsiloxane) with Formula 12, R 4 may mean a mixture of a methyl group and hydrogen, and the content of hydride groups to metal, that is, H / (H + methyl), can lie in the range from 0.1 to 0.9, for example, about 0.1-0.5, and if this value is 0.5, it means that the hydride and the methyl group in the R 4 pres tvuyut in the ratio of 1: 1.
R4 может быть представлена смесью из атомов водорода и метильной группы, и водород в R4 замещается ферроценильным фрагментом с Формулой 13, согласно Схеме Реакции 2. То есть в связующем компоненте с Формулой 6 R3 может быть представлен смесью водорода и ферроценильной группы с Формулой 13, и доля ферроценильной группы может быть такой же, как и содержание водорода в R4. То есть, когда R4 представлен водородом и группой метила в соотношении 1:1, в R3 соотношение между метильной группой и ферроценильной группой может быть близким к 1:1.R 4 can be represented by a mixture of hydrogen atoms and a methyl group, and the hydrogen in R 4 is replaced by a ferrocene fragment with Formula 13 according to Reaction Scheme 2. That is, in the binder component of Formula 6, R 3 can be represented by a mixture of hydrogen and a ferrocene group with Formula 13, and the proportion of the ferrocenyl group may be the same as the hydrogen content in R 4 . That is, when R 4 is represented by hydrogen and a methyl group in a ratio of 1: 1, in R 3 the ratio between the methyl group and the ferrocenyl group can be close to 1: 1.
Схема Реакции 3 является частным примером Схемы Реакции 2, когда R4 представлен смесью водорода и метильной группы в соотношении 1:1.Reaction Scheme 3 is a particular example of Reaction Scheme 2 when R 4 is a 1: 1 mixture of hydrogen and methyl group.
<Схема Реакции 3><Reaction Scheme 3>
где R4 включает метальной группу и водород в соотношении 1:1, а n3 является числом из диапазона от 10 до 25, и каждый элемент m4 является числом из диапазона от 1 до 10.where R 4 includes a methyl group and hydrogen in a ratio of 1: 1, and n 3 is a number from the range from 10 to 25, and each element m 4 is a number from the range from 1 to 10.
В вышеприведенной Схеме Реакции 3 R4 включает метальной группу или водород в соотношении 1:1, и диметилсила[1]ферроценофан с Формулой 9 замещают водородом для получения связующего компонента с Формулой 14, содержащего метальную группу и ферроценильную группу в соотношении 1:1.In the above Reaction Scheme 3, R 4 includes a methyl group or hydrogen in a 1: 1 ratio, and dimethylsil [1] ferrocenophan with Formula 9 is replaced with hydrogen to produce a binder component with Formula 14 containing a methyl group and a ferrocenyl group in a 1: 1 ratio.
Что касается Схемы Реакции 2, то используемый органический растворитель может быть представлен бензолом, толуолом, или ксилолом, и реакция может выполняться в течение 1-48 часов при температуре 10-50°С.As for Reaction Scheme 2, the organic solvent used may be benzene, toluene, or xylene, and the reaction may be carried out for 1-48 hours at a temperature of 10-50 ° C.
Схема Реакции 2 может выполняться в присутствии катализатора на основе соединений платины, и такой катализатор может представлять собой, например, катализатор Карстеда Pt[(CH2=CH-SiMe2)2O]1.5 или димер соли Цейзе Pt[(C2H4)Cl2]2. Количество катализатора на платиновой основе может лежать в диапазоне значений от близких к 0,01 мольному % до близких к 1 мольному % из расчета на 1 моль реагента.Reaction Scheme 2 can be carried out in the presence of a platinum-based catalyst, and such a catalyst can be, for example, a Carsted catalyst Pt [(CH 2 = CH-SiMe 2 ) 2 O] 1.5 or a Zeiss salt dimer Pt [(C 2 H 4 ) Cl 2 ] 2 . The amount of platinum-based catalyst may range from close to 0.01 mol% to close to 1 mol% based on 1 mol of reagent.
- Получение ячеистого полимера на основе PFS- Obtaining a cellular polymer based on PFS
После того как базовый полимер и связующий компонент получен вышеуказанным способом, они вступают в реакцию один с другим по приведенной ниже Схеме Реакции 4 в присутствии катализатора на основе соединений платины, образуя ячеистый полимер на основе PFS:After the base polymer and the binder component are obtained by the above method, they react with each other according to the Reaction Scheme 4 below in the presence of a catalyst based on platinum compounds, forming a cellular polymer based on PFS:
<Схема Реакции 4><Reaction Scheme 4>
где X1 - этоwhere X 1 is
или or
где R1 и R2 - каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 - представляет собой -О-, -S-, С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу;where R 1 and R 2 - each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 - represents-O-, -S-, C6 to C20 substituted or an unsubstituted alkylene group, or from C6 to C30 a substituted or unsubstituted arylene group;
n1 и n2 - каждый по отдельности многие 5-95, иn 1 and n 2 are each individually many 5-95, and
m3 - число 0 или 1.m3 is the number 0 or 1.
В Схеме Реакции 4 метальная группа и ферроценильная группа с Формулой 13, приведенной ниже, могут одновременно присутствовать в R3, а n3 является числом из диапазона от десяти до двадцати пяти:In Reaction Scheme 4, a methyl group and a ferrocenyl group with Formula 13 below can be simultaneously present in R 3 , and n 3 is a number in the range of ten to twenty-five:
<Формула 13><Formula 13>
где m4 является числом из диапазона от единицы до десяти.where m4 is a number in the range from one to ten.
В Схеме Реакции 4 одна из винильных групп на одном конце цепи базового полимера с Формулой 5 поперечно связана с атомом водорода на конце цепи ферроценильной группы у связующего компонента с Формулой 6. То есть базовый полимер с Формулой 5 не сшит пространственно с R3, который связан с атомом кремния в связующем компоненте с Формулой 6, когда R3 является метальной группой, и сшит с R3, когда R3 является ферроценильной группой.In Reaction Scheme 4, one of the vinyl groups at one end of the chain of the base polymer with Formula 5 is cross-linked to the hydrogen atom at the end of the chain of the ferrocenyl group of the binder with Formula 6. That is, the base polymer with Formula 5 is not spatially crosslinked with R 3 , which is bound with a silicon atom in the binder component of Formula 6 when R 3 is a methyl group, and is crosslinked with R 3 when R 3 is a ferrocenyl group.
Ячеистый полимер на основе PFS, полученный в результате реакции пространственного сшивания, описанной выше, включает повторяющийся блок с Формулой 1, повторяющийся блок с Формулой 2, и повторяющийся блок с Формулой 3:The PFS-based cellular polymer obtained by the spatial crosslinking reaction described above includes a repeating unit with Formula 1, a repeating unit with Formula 2, and a repeating unit with Formula 3:
<Формула 1><Formula 1>
<Формула 2><Formula 2>
<Формула 3><Formula 3>
где Fc представляет собой группу ферроценилена с Формулой 4а, приведенной ниже, DFc является связующей группой на основе диферроценилсилана с Формулой 4b, приведенной ниже, a m1 и m2 - каждый по отдельности является числом 0 или 1;where Fc is a ferrocenyl group with Formula 4a below, DFc is a linker group based on diferrocenylsilane with Formula 4b below, a m1 and m2 are each individually a number 0 or 1;
<Формула 4а><Formula 4a>
где m4 является числом из диапазона от 1 до 10;where m4 is a number from the range from 1 to 10;
<Формула 4b><Formula 4b>
где n1 и n2 являются каждый в отдельности числом из диапазона от 5 до 95, Х1 - этоwhere n 1 and n 2 are each individually a number from the range from 5 to 95, X 1 is
или or
где R1 и R2 - каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 - представляет собой -О-, -S-, С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу.where R 1 and R 2 - each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 - represents-O-, -S-, C6 to C20 substituted or an unsubstituted alkylene group, or from C6 to C30 a substituted or unsubstituted arylene group.
Повторяющийся блок с Формулой 1 относится к случаю, когда винильные группы, все расположенные на концах цепи основного полимера с Формулой 5, связаны со связующим компонентом с Формулой 6, повторяющийся блок с Формулой 2 относится к случаю, когда только винильная группа на конце цепи полимера с Формулой 5 связана со связующим компонентом с Формулой 6, а повторяющийся блок с Формулой 3 относится к той части связующего компонента, которая не связана с базовым полимером.The repeating unit with Formula 1 refers to the case when the vinyl groups, all located at the ends of the main polymer chain with Formula 5, are connected to the binder component with Formula 6, the repeating unit with Formula 2 refers to the case when only the vinyl group at the end of the polymer chain with Formula 5 is associated with a binder component with Formula 6, and the repeating unit with Formula 3 refers to that part of the binder component that is not associated with the base polymer.
Что касается Схемы Реакции 4, то используемый органический растворитель может быть представлен бензолом, толуолом, или ксилолом, и реакция может быть осуществлена, например, в течение 1-48 часов при температуре 30-80°С.As for Reaction Scheme 4, the organic solvent used may be benzene, toluene, or xylene, and the reaction may be carried out, for example, within 1-48 hours at a temperature of 30-80 ° C.
Схема Реакции 4 может быть осуществлена в присутствии катализатора на основе соединений платины, причем в качестве такого катализатора может выступать, например, катализатор Карстеда Pt(CH2=CH-SiMe2)2O]1.5 или димер соли Цейзе Pt[(C2H4)Cl2]2. Количество катализатора на основе платины может лежать в диапазоне от близкого к 0,01 мольного % до близкого к 1 мольного %, из расчета на 1 моль реагента.The reaction scheme 4 can be carried out in the presence of a catalyst based on platinum compounds, and such a catalyst can be, for example, a Carsted catalyst Pt (CH 2 = CH-SiMe 2 ) 2 O] 1.5 or a dimer of the Zeise salt Pt [(C 2 H 4 ) Cl 2 ] 2 . The amount of platinum-based catalyst may range from close to 0.01 mol% to close to 1 mol%, based on 1 mol of reagent.
Ячеистый полимер на основе PFS, согласно заявляемому изобретению, представляет собой ячеистую структуру, включающую повторяющиеся блоки с Формулами 1, 2 и 3, причем ячеистая структура не является линейной, а имеет пространственный характер, и в ней базовый полимер объемно сцеплен со связующим компонентом.The PFS-based cellular polymer according to the claimed invention is a cellular structure including repeating blocks with Formulas 1, 2 and 3, wherein the cellular structure is not linear, but has a spatial character, and in it the base polymer is voluminously bonded to the binder component.
Например, повторяющийся блок с Формулой 1 может повторяться в форме лестницы, образуя полимер в форме лестницы, а повторяющиеся блоки с Формулами 2 и 3 вставляют в промежутки между ними.For example, a repeating block with Formula 1 can be repeated in the form of a ladder, forming a polymer in the form of a ladder, and repeating blocks with Formulas 2 and 3 are inserted into the spaces between them.
Пример ячеистого полимера на основе PFS, включающего повторяющиеся блоки с Формулами 1, 2 и 3, представлен Формулой 15:An example of a cellular polymer based on PFS, including repeating blocks with Formulas 1, 2 and 3, is represented by Formula 15:
<Формула 15><Formula 15>
где А - этоwhere A is
Как показано в Формуле 15, ячеистый полимер на основе PFS имеет не простое линейное строение, а характеризуется пространственной (трехмерной) структурой, и базовый полимер с Формулой 5 сцеплен со связующим компонентом с Формулой 6 по моно- или би-дентатному типу.As shown in Formula 15, the PFS-based cellular polymer is not a simple linear structure, but is characterized by a spatial (three-dimensional) structure, and the base polymer with Formula 5 is bonded to the binder component with Formula 6 in a mono- or bententate type.
Повторяющиеся блоки с Формулами 1, 2 и 3 в Формуле 15 выделены рамками на нижеприведенной Формуле 16:Repeating blocks with Formulas 1, 2, and 3 in Formula 15 are outlined in the Formula 16 below:
<Формула 16><Formula 16>
где А - этоwhere A is
Что касается Формулы 16, то а является примером повторяющегося блока с Формулой 1, b является примером повторяющегося блока с Формулой 2, и с - пример повторяющегося блока с Формулой 3.With regard to Formula 16, and is an example of the recurring unit of Formula 1, b is an example of the repeating unit of Formula 2, and - an example of a repeating unit of Formula 3.
- Изготовление полимерной пленки на основе PFS- PFS based polymer film manufacturing
Вышеописанный ячеистый полимер на основе PFS может использоваться для изготовления пленок различными методами, например нанесением в центробежном поле (spin-coating), погружением (dip-coating), или помощью растворителя (sovent-casting) на различные подложки, например на стеклянные подложки, на подложки из оксидов индия и олова (ITO), или пластиковые подложки.The above-described PFS-based cellular polymer can be used to make films by various methods, for example, spin-coating, dip-coating, or sovent-casting on various substrates, for example glass substrates, substrates from indium and tin oxides (ITO), or plastic substrates.
Этот ячеистый полимер на основе поли(ферроценил)силана может быть синтезирован путем использования в качестве исходного материала всего лишь одного типа сила[1]ферроценофана вместо нескольких различныхThis cellular polymer based on poly (ferrocenyl) silane can be synthesized by using only one type of force [1] ferrocenophane as starting material instead of several different
сила[1]ферроценофанов, при этом производственные процессы не требовательны к высокой степени очистки, и поэтому желаемый уровень очистки легко достигается путем использования всего лишь трех-четырех процессов перекристаллизации. Кроме того, такие свойства базового полимера, как длина цепи и количество способных к связыванию винилсилильных функциональных групп, могут легко регулироваться за счет используемого соотношения исходных компонентов сила[1]ферроценофана, дигидросилана и тетравинилсилана. Кроме того, связующий компонент легко насыщается ферроценовой группой, таким образом, позволяя повысить число электрохимически активных фрагментов в конечном трехмерном ячеистом полимере на основе PFS.the strength [1] of ferrocenophanes, while the production processes are not demanding for a high degree of purification, and therefore the desired level of purification is easily achieved by using only three to four recrystallization processes. In addition, properties of the base polymer, such as chain length and the number of vinylsilyl functional groups capable of binding, can be easily controlled by using the ratio of the initial components of the strength [1] of ferrocenophan, dihydrosilane and tetravinyl silane. In addition, the binder component is easily saturated with the ferrocene group, thus, allowing to increase the number of electrochemically active fragments in the final three-dimensional cellular polymer based on PFS.
Кроме того, базовый полимер и связующий компонент могут быть использованы без выделения из реакционной смеси (in situ). Поскольку платиновый катализатор (катализатор на основе соединений Pt) в количестве от 0,02 до 0,5 мольных % из расчета на одну группу Si-H используется во всех процессах и сохраняет свою активность с момента введения его на начальной стадии, то нет необходимости многократного добавления платинового катализатора на последующих этапах.In addition, the base polymer and the binder component can be used without isolation from the reaction mixture (in situ). Since the platinum catalyst (a catalyst based on Pt compounds) in an amount of 0.02 to 0.5 mol% based on one Si-H group is used in all processes and retains its activity from the moment it is introduced at the initial stage, there is no need for multiple adding a platinum catalyst in subsequent steps.
Кроме того, процесс отвердевания для получения конечного продукта не требует облучения ультрафиолетом и наличия инертной атмосферы и может быть полностью выполнен при температуре 50-70°С в течение всего лишь нескольких часов.In addition, the curing process to obtain the final product does not require ultraviolet irradiation and an inert atmosphere and can be completely performed at a temperature of 50-70 ° C in just a few hours.
Так как базовый полимер и связующий компонент, необходимые для получения ячеистого полимера, используются по мере необходимости, даже когда базовый полимер и связующий компонент готовятся заранее и складируются, их можно сохранять без снижения качества.Since the base polymer and the binder component necessary to obtain a cellular polymer are used as needed, even when the base polymer and binder component are prepared in advance and stored, they can be stored without compromising on quality.
Как описано выше, ячеистый полимер на основе PES легко изготовлять в больших количествах (в массовом производстве) и использовать в качестве активного компонента управляемого фотонного полупроводника. Кроме того, ячеистый полимер на основе PES может использоваться в прозрачном исполнительном устройстве или биодатчике, или как антиокислительный материал прозрачного электрода.As described above, a PES-based cellular polymer is easy to manufacture in large quantities (in mass production) and used as an active component of a controlled photonic semiconductor. In addition, a PES-based cellular polymer can be used in a transparent actuator or biosensor, or as an antioxidant material of a transparent electrode.
Поскольку содержание электроактивных ферроценовых групп, способных к обратимому окислению и восстановлению, а также плотность поперечной сшивки в ячеистом PFS легко контролируются в широких пределах в процессе приготовления полимера и могут достигать высоких значений, появляется возможность изготовления устройств отображения на основе фотонных кристаллов с высокой скоростью срабатывания (малым временем отклика), широким цветовым диапазоном и высокой износостойкостью, что отвечает запросам потребителей.Since the content of electroactive ferrocene groups capable of reversible oxidation and reduction, as well as the cross-linking density in cellular PFS are easily controlled over a wide range during polymer preparation and can reach high values, it becomes possible to manufacture display devices based on photonic crystals with a high response speed ( short response time), a wide color range and high wear resistance, which meets the needs of consumers.
Далее заявляемое изобретение описывается в деталях для вариантов его реализации. Однако заявляемое изобретение не ограничивается описанными вариантами.Further, the claimed invention is described in detail for options for its implementation. However, the claimed invention is not limited to the described options.
Пример 1Example 1
a) Получение связующего компонентаa) Obtaining a binder component
Гидрогенизированный поли(диметилсилоксан) Me[(HSiMeO)(SiMe2O)]6SiMe3 (65 мг, 0,4 mmol, Si-H) и [Pt(C2H4)Cl2]2 (10 мг, 0,8 мл, 1 мол.%) были добавлены в раствор FcSiMe2 (200 мг, 0,8 mmol) в 1,2 мл бензола при температуре 25°С, и перемешивались в течение 3-5 часов. Молекулярный весHydrogenated Poly (dimethylsiloxane) Me [(HSiMeO) (SiMe 2 O)] 6 SiMe 3 (65 mg, 0.4 mmol, Si-H) and [Pt (C 2 H 4 ) Cl 2 ] 2 (10 mg, 0 , 8 ml, 1 mol.%) Were added to a solution of FcSiMe 2 (200 mg, 0.8 mmol) in 1.2 ml of benzene at a temperature of 25 ° C, and stirred for 3-5 hours. Molecular weight
Me[(RSiMeO)(SiMe2O)]6SiMe3 (R=-(FcSiMe2)2H) в качестве связующего компонента составлял приблизительно 3800, и содержание ферроценовых групп составляло приблизительно 75% (содержание = ферроценильная группа/(метильная группа+ферроценильная группа) · 100).Me [(RSiMeO) (SiMe 2 O)] 6 SiMe 3 (R = - (FcSiMe 2 ) 2 H) as a binder component was approximately 3800, and the content of ferrocene groups was approximately 75% (content = ferrocenyl group / (methyl group + ferrocenyl group) 100).
b) Получение базового полимера: поли(ферроценил)силан с тривинилсилильными концевыми группамиb) Preparation of base polymer: poly (ferrocenyl) silane with trivinylsilyl end groups
Катализатор Карстеда (Aldrich, 2% Pt в ксилоле, 5 µl%, 0,43 мол.% к Ph2SiH2) был добавлен к раствору диметилсила[1]ферроценофана (0,24 г, 1,00 mmol) и дифенилсилана Ph2SiH2 (19 µl, 0,10 mmol) в 3 мл бензола при температуре 25°С при перемешивании, реакция проводилась в течение 1-3 часов. Полученный в результате реакции продукт был идентифицирован с применением ядерного магнитного резонанса (NMR).Carstead's catalyst (Aldrich, 2% Pt in xylene, 5 μl%, 0.43 mol% for Ph 2 SiH 2 ) was added to a solution of dimethylsil [1] ferrocenophan (0.24 g, 1.00 mmol) and diphenylsilane Ph 2 SiH 2 (19 μl, 0.10 mmol) in 3 ml of benzene at a temperature of 25 ° C with stirring, the reaction was carried out for 1-3 hours. The resulting product was identified using nuclear magnetic resonance (NMR).
1Н NMR (δ, CDCl3): 7.57-7.64 (о-Н, Ph, 4Н); 7.35-7.41 (m-Н и р-Н, Ph, 6Н); 3.9-4.3 (С5Н4, Fc, 77Н), 0.25-0.55 (SiMe2, 58Н); 5.44 (Ph2Si-H, 0.20.7Н); 4.42 (Me2Si-H, 1.31.8H).1 H NMR (δ, CDCl 3 ): 7.57-7.64 (o-H, Ph, 4H); 7.35-7.41 (m-H and p-H, Ph, 6H); 3.9-4.3 (C 5 H 4 , Fc, 77H), 0.25-0.55 (SiMe2, 58H); 5.44 (Ph2Si-H, 0.20.7H); 4.42 (Me2Si-H, 1.31.8H).
Тетравинилсилан (340 µl, 2 mmol, 10-кратный избыток) был добавлен к готовому раствору, и реакционная смесь перемешивалась в течение 3 дней, затем растворитель был удален, и остаток был высушен в вакууме.Tetravinyl silane (340 μl, 2 mmol, 10-fold excess) was added to the prepared solution, and the reaction mixture was stirred for 3 days, then the solvent was removed and the residue was dried in vacuo.
1H NMR (δ, CDCl3): 7.50-7.62 (о-Н, Ph, 4Н); 7.32-7.40 (m-Н и р-Н, Ph, 6Н); 3.8-4.3 (С5Н4, Fc, 77Н), 0.25-0.55 (SiMe2+СН2, 64Н); 5.7-5.8 (Винил, 5Н); 6.0-6.2 (Винил, 10Н).1H NMR (δ, CDCl 3 ): 7.50-7.62 (o-H, Ph, 4H); 7.32-7.40 (m-H and p-H, Ph, 6H); 3.8-4.3 (C 5 H 4 , Fc, 77H), 0.25-0.55 (SiMe 2 + CH 2 , 64H); 5.7-5.8 (Vinyl, 5H); 6.0-6.2 (Vinyl, 10H).
с) Получение трехмерного полигидроферроценилсиланаc) Preparation of three-dimensional polyhydroferrocenylsilane
Катализатор Карстеда (Aldrich, 2% Pt в ксилоле, 3 µl, 0.26 µmol Pt, 0.25 мол.% на Si-H) был добавлен к 0.26 г (1.1 mmol) диметилсила[1]ферроценофана и 0.087 г (0.09 mmol) полигидросилоксана (Me3Si-[(OSiMeH)(OSiMe2)6]3-H), растворенных в 3 мл бензола, реакционная смесь перемешивалась в течение 3 часов, затем растворитель был удален, и остаток высушен в вакууме.Carstead's catalyst (Aldrich, 2% Pt in xylene, 3 μl, 0.26 μmol Pt, 0.25 mol% on Si-H) was added to 0.26 g (1.1 mmol) of dimethylsil [1] ferrocenophan and 0.087 g (0.09 mmol) of polyhydrosiloxane ( Me 3 Si - [(OSiMeH) (OSiMe 2 ) 6 ] 3 -H) dissolved in 3 ml of benzene, the reaction mixture was stirred for 3 hours, then the solvent was removed and the residue was dried in vacuo.
1H NMR (δ, CDCl3): 4.7 (синглет, FcSiMe2H, 5Н), 4.0-4.2 (С5Н4, Fc, 8Н), 0.3-0.7 (Me, OSiMe2+OSiMeFc+SiMe2Fc+SiMe3, 11Н).1H NMR (δ, CDCl 3 ): 4.7 (singlet, FcSiMe 2 H, 5H), 4.0-4.2 (C 5 H 4 , Fc, 8H), 0.3-0.7 (Me, OSiMe 2 + OSiMeFc + SiMe 2 Fc + SiMe 3 , 11H).
d) Получение пленки PFSd) Obtaining a PFS film
Продукты реакций, полученные согласно b) и с), были смешаны и затем выдерживались при комнатной температуре в течение одного дня. Затем смесь была нанесена методом центрифугирования (spin-coating) на стеклянную подложку, после чего нагревалась в течение 3-12 часов при температуре 70°С, образуя, таким образом, прозрачное желто-оранжевое стекловидное покрытие.The reaction products obtained according to b) and c) were mixed and then kept at room temperature for one day. Then the mixture was spin-coated on a glass substrate, and then heated for 3-12 hours at a temperature of 70 ° C, thus forming a transparent yellow-orange glassy coating.
Характеристики полученной в приведенном Примере 1 пленки в части электрических свойств в ходе экспериментальной проверки были определены методом циклической вольтометрии, и результаты представлены на Фиг.1, где можно убедиться, что процессы окисления и восстановления являются обратимыми.The characteristics of the film obtained in Example 1 in terms of electrical properties during the experimental verification were determined by the method of cyclic voltometry, and the results are presented in Figure 1, where it can be verified that the oxidation and reduction processes are reversible.
Как описано выше, согласно одному или более вариантам реализации заявляемого изобретения, получение ячеистого полимера на основе поли(ферроценил)силана с помощью упрощенного процесса, использование катализатора на основе соединений платины при получении базового полимера, связующего компонента и ячеистого полимера на основе PFS путем сшивания базового полимера и связующего компонента позволяют осуществлять реакцию in situ, при этом промежуточные продукты не нуждаются в очистке, и процесс сшивания, который является заключительной операцией, выполняется в мягких условиях, а именно нагревании.As described above, according to one or more embodiments of the claimed invention, the production of a cellular polymer based on poly (ferrocenyl) silane using a simplified process, the use of a catalyst based on platinum compounds in the preparation of a base polymer, a binder component and a PFS based cellular polymer by crosslinking the base polymer and a binder component allow the reaction to be carried out in situ, while the intermediate products do not need to be purified, and the crosslinking process, which is the final step it is carried out under mild conditions, namely heat.
Кроме того, в случае когда ячеистый полимер используется для формирования пленки трехмерного полимера, подложку, на которую предполагается наносить пленку, можно функционализировать соединениями с виниловыми группами, к которым затем можно присоединить связующий компонент. С помощью такой операции обеспечивается отсутствие использования излишков PFS, достигается минимальное снижение оптических характеристик, в то время как основные параметры пленки улучшаются.In addition, in the case where the cellular polymer is used to form a three-dimensional polymer film, the substrate on which the film is to be applied can be functionalized with compounds with vinyl groups, to which a binder component can then be attached. Using this operation ensures the absence of the use of excess PFS, a minimal decrease in optical characteristics is achieved, while the basic parameters of the film are improved.
Необходимо отметить, что приведенные в описании примеры реализации следует рассматривать лишь в качестве иллюстрации, но они не носят ограничительного характера. Описания характеристик или особенностей каждого варианта воплощения изобретения следует, как правило, рассматривать в качестве основы для других сходных модификаций признаков и аспектов в различных вариантах реализации изобретений.It should be noted that the examples of implementation described in the description should be considered only as an illustration, but they are not restrictive. Descriptions of the characteristics or features of each embodiment of the invention should, as a rule, be considered as the basis for other similar modifications of features and aspects in various embodiments of the inventions.
Claims (12)
<Формула 1>
<Формула 2>
<Формула 3>
где Fc представляет собой группу ферроценилена, представленную Формулой 4а, DFc является связующей группой на основе диферроценилсилана, представленной Формулой 4b, a m1 и m2 каждый по отдельности является числом 0 или 1;
<формула 4а>
где m4 является числом из диапазона от 1 до 10;
<Формула 4b>
где n1 и n2 являются каждый по отдельности числом из диапазона от 5 до 95, X1 - это
или
где R1 и R2 каждый по отдельности представляет собой замещенную или незамещенную в диапазоне от С6 до С20 алкильную группу или замещенную или незамещенную в диапазоне от С6 до С30 арильную группу, а Х2 представляет собой О-, -S-, в диапазоне от С6 до С20 замещенную или незамещенную алкиленовую группу, или в диапазоне от С6 до С30 замещенную или незамещенную ариленовую группу.1. A cellular polymer based on poly (ferrocenyl) silane, including a repeating unit represented by Formula 1, a repeating unit represented by Formula 2, and a repeating unit represented by Formula 3:
<Formula 1>
<Formula 2>
<Formula 3>
where Fc is a ferrocene group represented by Formula 4a, DFc is a linker group based on diferrocenylsilane represented by Formula 4b, a m1 and m2 each individually is a number 0 or 1;
<formula 4a>
where m4 is a number from the range from 1 to 10;
<Formula 4b>
where n 1 and n 2 are each individually a number from the range from 5 to 95, X 1 is
or
where R 1 and R 2 each individually represents a substituted or unsubstituted in the range from C6 to C20 alkyl group or substituted or unsubstituted in the range from C6 to C30 an aryl group, and X 2 represents O-, -S-, in the range from C6 to C20 substituted or unsubstituted alkylene group, or in the range from C6 to C30 substituted or unsubstituted arylene group.
<Формула 5>
где n1 и n2 каждый по отдельности является числом из диапазона от 5 до 95, m3 - это 0 или 1, X1 - это
или
где R1 и R2 каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 представляет собой -О-, -S-, от С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу;
<Формула 6>
где n3 представляет собой число от 10 до 25, и R3 обозначает метильную группу и ферроценильную группу, представленную Формулой 13, и, когда метильная группа и ферроценильная группа сосуществуют как R3, отношение количества метильных групп к сумме метильных групп и ферроценильных групп находится в диапазоне от 0,1 до 0,9:
<Формула 13>
где m4 - это число от 1 до 10.4. The method of producing a cellular polymer based on poly (ferrocenyl) silane according to claim 1, which includes performing the following operations: spatially crosslink the base polymer represented by Formula 5 and the binder component represented by Formula 6:
<Formula 5>
where n 1 and n 2 each individually is a number from the range from 5 to 95, m3 is 0 or 1, X 1 is
or
where R 1 and R 2 each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 represents —O—, —S—, from C6 to C20 substituted or an unsubstituted alkylene group, or from C6 to C30 a substituted or unsubstituted arylene group;
<Formula 6>
where n 3 represents a number from 10 to 25, and R 3 denotes a methyl group and a ferrocenyl group represented by Formula 13, and when the methyl group and the ferrocenyl group coexist as R 3 , the ratio of the number of methyl groups to the sum of methyl groups and ferrocenyl groups is in the range from 0.1 to 0.9:
<Formula 13>
where m4 is a number from 1 to 10.
<Формула 7>
где n1 и n2 являются каждый по отдельности числом из диапазона от 5 до 95, X1 - это
или
где R1 и R2 каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 представляет собой -О-, -S-, от С6 до С20 замещенную или незамещенную алкиленовую группу или от С6 до С30 замещенную или незамещенную ариленовую группу.5. The method according to claim 4, characterized in that in the base polymer represented by Formula 5, m3 has a value of 0, and it is a base polymer represented by Formula 7:
<Formula 7>
where n 1 and n 2 are each individually a number from the range from 5 to 95, X 1 is
or
where R 1 and R 2 each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 represents —O—, —S—, from C6 to C20 substituted or unsubstituted alkylene group; or from C6 to C30 substituted or unsubstituted arylene group.
- проведение реакции дигидросилана, представленного Формулой 8, с диметилсила[1]ферроценофаном, представленным Формулой 9, в присутствии катализатора на основе соединений платины, образуя в результате линейный олигоферроценилсилан, представленный Формулой 10, имеющей Si-H на обоих концах цепи, и
- проведение реакции линейного олигоферроценилсилана с тетравинилсиланом до получения базового полимера с Формулой 7:
где X1 - это
или
где R1 и R2 каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 представляет собой -О-, -S-, от С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу; n1 и n2 каждый по отдельности представлен числом от 5 до 95, и n представляет собой n1+n2.6. The method according to claim 5, characterized in that the method further includes:
- carrying out the reaction of dihydrosilane represented by Formula 8 with dimethylsil [1] ferrocenophan represented by Formula 9 in the presence of a catalyst based on platinum compounds, resulting in a linear oligoferrocenylsilane represented by Formula 10 having Si-H at both ends of the chain, and
- the reaction of linear oligoferrocenylsilane with tetravinylsilane to obtain a base polymer with Formula 7:
where X 1 is
or
where R 1 and R 2 each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 represents —O—, —S—, from C6 to C20 substituted or unsubstituted alkylene group, or from C6 to C30 substituted or unsubstituted arylene group; n 1 and n 2 are each individually represented by a number from 5 to 95, and n represents n 1 + n 2 .
- проведение реакции базового полимера, представленного Формулой 7, с линейным олигоферроценилсиланом, представленным Формулой 10, в присутствии катализатора на основе соединений платины до получения базового полимера, представленного нижеприведенной Формулой 11:
<Формула 11>
где X1 - это
или
где R1 и R2 каждый по отдельности представляет собой замещенную или незамещенную от С6 до С20 алкильную группу или замещенную или незамещенную от С6 до С30 арильную группу, а Х2 - представляет собой -О-, -S-, от С6 до С20 замещенную или незамещенную алкиленовую группу, или от С6 до С30 замещенную или незамещенную ариленовую группу; n1 и n2 каждый по отдельности представлен числом от 5 до 95.7. The method according to claim 6, characterized in that the method further comprises the following steps:
- carrying out the reaction of the base polymer represented by Formula 7 with a linear oligoferrocenylsilane represented by Formula 10 in the presence of a catalyst based on platinum compounds to obtain the base polymer represented by the following Formula 11:
<Formula 11>
where X 1 is
or
where R 1 and R 2 each individually represents a substituted or unsubstituted from C6 to C20 alkyl group or a substituted or unsubstituted from C6 to C30 aryl group, and X 2 - represents-O-, -S-, from C6 to C20 substituted or an unsubstituted alkylene group, or from C6 to C30 a substituted or unsubstituted arylene group; n 1 and n 2 are each individually represented by a number from 5 to 95.
где в качестве R4 применяют смесь из метильной группы и водорода, в качестве R3 применяют смесь из метильной группы и ферроценильной группы с Формулой 13, причем n3 принимает значение из диапазона от десяти до двадцати пяти,
<Формула 13>
где m4 принимает значение из диапазона от единицы до десяти.8. The method according to claim 4, characterized in that the binder component with Formula 6 is obtained by reacting the poly (dimethylsiloxane) represented by Formula 12 below as a linear oligomer with dimethylsil [1] ferrocenophane represented by Formula 9 in the presence of a catalyst on based platinum compounds:
wherein as R 4, a mixture of hydrogen and a methyl group as R 3, a mixture of a methyl group and ferrocenyl group of Formula 13, wherein n assumes the value 3 in the range of ten to twenty-five,
<Formula 13>
where m4 takes a value from a range of one to ten.
<Формула 1>
<Формула 2>
<Формула 3>
где Fc представляет собой группу ферроценилена, представленную Формулой 4а, DFc является связующей группой на основе диферроценилсилана, представленной Формулой 4b, a m1 и m2 каждый по отдельности является числом 0 или 1;
<Формула 4а>
где m4 является числом из диапазона от 1 до 10;
<Формула 4b>
где n1 и n2 являются каждый по отдельности числом из диапазона от 5 до 95, X1 - это
или
где R1 и R2 каждый по отдельности представляет собой замещенную или незамещенную в диапазоне от С6 до С20 алкильную группу или замещенную или незамещенную в диапазоне от С6 до С30 арильную группу, а Х2 представляет собой -О-, -S-, в диапазоне от С6 до С20 замещенную или незамещенную алкиленовую группу, или в диапазоне от С6 до С30 замещенную или незамещенную ариленовую группу.11. The method according to claim 4, characterized in that the cellular polymer based on poly (ferrocenyl) silane includes a repeating unit represented by Formula 1, a repeating unit represented by Formula 2, and a repeating unit represented by Formula 3:
<Formula 1>
<Formula 2>
<Formula 3>
where Fc is a ferrocene group represented by Formula 4a, DFc is a linker group based on diferrocenylsilane represented by Formula 4b, and m1 and m2 are each individually a number 0 or 1;
<Formula 4a>
where m4 is a number from the range from 1 to 10;
<Formula 4b>
where n 1 and n 2 are each individually a number from the range from 5 to 95, X 1 is
or
where R 1 and R 2 each individually represents a substituted or unsubstituted alkyl group in the range from C6 to C20 or a substituted or unsubstituted aryl group in the range from C6 to C30, and X 2 represents —O—, —S—, in the range from C6 to C20 a substituted or unsubstituted alkylene group, or in the range from C6 to C30 a substituted or unsubstituted arylene group.
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2010125697/04A RU2441874C1 (en) | 2010-06-23 | 2010-06-23 | Polymer on the base of poly(ferrocenyl)sylane, method of its production and the film including the polymer the base of poly(ferrocenyl)sylane |
| KR1020100101034A KR101750399B1 (en) | 2010-06-23 | 2010-10-15 | Poly(ferrocenyl)silane based polymer, process for preparing the same and film comprising the polymer |
| US13/165,221 US8592534B2 (en) | 2010-06-23 | 2011-06-21 | Poly(ferrocenyl)silane based polymer, method of preparing the same, and film including the poly(ferrocenyl)silane based polymer |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2010125697/04A RU2441874C1 (en) | 2010-06-23 | 2010-06-23 | Polymer on the base of poly(ferrocenyl)sylane, method of its production and the film including the polymer the base of poly(ferrocenyl)sylane |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2010125697A RU2010125697A (en) | 2011-12-27 |
| RU2441874C1 true RU2441874C1 (en) | 2012-02-10 |
Family
ID=45505091
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2010125697/04A RU2441874C1 (en) | 2010-06-23 | 2010-06-23 | Polymer on the base of poly(ferrocenyl)sylane, method of its production and the film including the polymer the base of poly(ferrocenyl)sylane |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR101750399B1 (en) |
| RU (1) | RU2441874C1 (en) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115304770B (en) * | 2022-09-05 | 2023-09-29 | 山东省科原石油科技有限责任公司 | Environment-friendly petroleum auxiliary agent and preparation method thereof |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5844052A (en) | 1997-03-14 | 1998-12-01 | The United States Of America As Represented By The Secretary Of The Navy | Linear metallocene polymers containing acetylenic and inorganic units and thermosets and ceramics therefrom |
| US6495483B1 (en) | 1997-03-14 | 2002-12-17 | The United States Of America As Represented By The Secretary Of The Navy | Linear metallocene polymers containing acetylenic and inorganic units and thermosets and ceramics therefrom |
| JP5442941B2 (en) | 2007-07-12 | 2014-03-19 | 株式会社カネカ | Curable composition |
-
2010
- 2010-06-23 RU RU2010125697/04A patent/RU2441874C1/en active
- 2010-10-15 KR KR1020100101034A patent/KR101750399B1/en active IP Right Grant
Non-Patent Citations (2)
| Title |
|---|
| Daniel P.Puzzo et al. Electroactive Inverse Opal: A Single Material for All Colors. Angewandte Chemie International Edition, 2009, vol.48, pp.943-947. David L. Zechel et al. Thermal and Transition-Metal-Catalyzed Ring-Opening Polymerization (ROP) of [l]Silaferrocenophanes with Chlorine Substituents at Silicon: A Route to Tunable Poly(ferrocenylsilanes). Organometallics, 1996, vol.15, pp.1972-1978. * |
| Yizeng Ni et al. Transition Metal-Based Polymers with Controlled Architectures: Well-Defined Poly(ferrocenylsilane) Homopolymers and Multiblock Copolymers via the Living Anionic Ring-Opening Polymerization of Silicon-Bridged [1]Ferrocenophanes. Journal of American Chemical Society, 1996, vol.118, p.4102-4114. * |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20110139635A (en) | 2011-12-29 |
| RU2010125697A (en) | 2011-12-27 |
| KR101750399B1 (en) | 2017-06-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Dudziec et al. | Double-decker silsesquioxanes: current chemistry and applications | |
| KR100969496B1 (en) | Polysiloxane film and process for producing the same | |
| US5902863A (en) | Dendrimer-based networks containing lyophilic organosilicon and hydrophilic polyamidoamine nanoscopic domains | |
| CN106866722B (en) | Benzocyclobutene-containing functionalized organosilicon compound and preparation method thereof | |
| KR20000063142A (en) | Starting materials for manufacturing polyorganosilsesquioxanes, polyorganosilsesquioxanes and method for manufacturing polyorganosilsesquioxanes | |
| Kumar et al. | Properties and applications of polysilanes | |
| KR20120087120A (en) | Silicon-containing curable composition and cured product thereof | |
| CN102408565B (en) | Preparation method for phenyl hydrogen-containing silicone oil | |
| JP2979145B1 (en) | New silsesquioxane-containing polymer and method for producing the same | |
| Pohl et al. | Thermoplastic silsesquioxane hybrid polymers with a local ladder-type structure | |
| RU2441874C1 (en) | Polymer on the base of poly(ferrocenyl)sylane, method of its production and the film including the polymer the base of poly(ferrocenyl)sylane | |
| Briesenick et al. | High-refractive-index polysiloxanes containing naphthyl and phenanthrenyl groups and their thermally cross-linked resins | |
| KR20170030563A (en) | Method for producing cyclic silane using concentration method | |
| US5229481A (en) | High-molecular weight, silicon-containing polymers and methods for the preparation and use thereof | |
| CN107759791B (en) | Organosilicon polymer containing silicon-oxygen eight-membered ring, crosslinked body and preparation method | |
| González-García et al. | Hexacoordinated oligosilanes from a hexacoordinated silicon (IV) complex containing an O, N, N, O salen-type and thiocyanato-N ligands | |
| JP5296961B2 (en) | Copolysilane and resin composition containing this copolysilane | |
| US5290897A (en) | Low temperature vulcanizing carborane siloxane adhesive | |
| Gates | Inorganic and organometallic polymers | |
| JPS60188429A (en) | Manufacture of polyhydridesilane and pyropolymer of same | |
| Huaijun et al. | Effects of phenyl hydrogen polysiloxane molecular structure on the performance of LED packaging silicone rubber | |
| JP6652488B2 (en) | High molecular weight polysilane and method for producing the same | |
| Maeda et al. | Preparation of a soluble polysilsesquioxane containing a macrocyclic structure and capture of palladium ions | |
| JP3636940B2 (en) | Flame-retardant carborane-containing silicon-based resin composition and method for producing cured product thereof | |
| US8592534B2 (en) | Poly(ferrocenyl)silane based polymer, method of preparing the same, and film including the poly(ferrocenyl)silane based polymer |