RU2436802C2 - Method of producing polybutadiene - Google Patents
Method of producing polybutadiene Download PDFInfo
- Publication number
- RU2436802C2 RU2436802C2 RU2008150488/04A RU2008150488A RU2436802C2 RU 2436802 C2 RU2436802 C2 RU 2436802C2 RU 2008150488/04 A RU2008150488/04 A RU 2008150488/04A RU 2008150488 A RU2008150488 A RU 2008150488A RU 2436802 C2 RU2436802 C2 RU 2436802C2
- Authority
- RU
- Russia
- Prior art keywords
- compound
- group
- polymerization
- atom
- cis
- Prior art date
Links
Abstract
Description
Область техники, к которой относится изобретениеFIELD OF THE INVENTION
Настоящее изобретение относится к способу получения путем полимеризации 1,3-бутадиена армированного полибутадиена с уменьшенным запахом (здесь и далее в этом документе обозначаемого как полимер VCR), включающего цис-1,4-полимер и синдиотактический 1,2-полимер.The present invention relates to a method for producing, by polymerization of 1,3-butadiene, a reinforced polybutadiene with reduced odor (hereinafter referred to as VCR polymer), comprising a cis-1,4 polymer and a syndiotactic 1,2 polymer.
Предшествующий уровень техникиState of the art
В патенте JP-B-1974-17666 (патентная литература 1) и патенте JP-B-1974-17667 (патентная литература 2) в качестве способа получения полимера VCR описан способ, который заключается в проведении цис-1,4-полимеризации 1,3-бутадиена в инертном органическом растворителе с помощью катализатора, получаемого из воды, растворимого соединения кобальта и хлорида алюминийорганического соединения с общей формулой AlRnX3-n, и затем проведения в полимеризационной системе синдиотактической 1,2-полимеризации 1,3-бутадиена в присутствии катализатора синдиотактической 1,2-полимеризации, получаемого из растворимого соединения кобальта, алюминийорганического соединения с общей формулой AlR3 и дисульфида углерода.JP-B-1974-17666 (Patent Literature 1) and JP-B-1974-17667 (Patent Literature 2) describe, as a method for producing a VCR polymer, a method which involves cis-1,4 polymerization 1, 3-butadiene in an inert organic solvent using a catalyst obtained from water, a soluble compound of cobalt and chloride of an organoaluminum compound with the general formula AlR n X 3-n , and then carrying out in the polymerization system the syndiotactic 1,2-polymerization of 1,3-butadiene in the presence of a syndiotactic 1,2-poly a sterilization process obtained from a soluble cobalt compound, an organoaluminum compound with the general formula AlR 3 and carbon disulfide.
Кроме того, в качестве способа получения полимера VCR в патентах JP-B-1987-171 (патентная литература 3), JP-B-1988-36324 (патентная литература 4), JP-B-1990-37927 (патентная литература 5), JP-B-1990-38081 (патентная литература 6) и JP-B-1991-63566 (патентная литература 7) описан, например, способ, который заключается в проведении для получения полимера VCR цис-1,4-полимеризации 1,3-бутадиена в присутствии или в отсутствие дисульфида углерода или после получения полимера VCR в отделении 1,3-бутадиена от дисульфида углерода для повторного использования и циркуляции в отделении 1,3-бутадиена, не содержащего, по существу, дисульфида углерода и инертного органического растворителя. Более того, в патенте JP-B-1992-48815 (патентная литература 8) описан полимер VCR, который обладает низкой степенью разбухания экструдируемого расплава при превращении в компаунд, а при вулканизации компаунда является отличным в отношении величины напряжения при растяжении и сопротивления разрушению при многократном изгибе и является подходящим для производства боковых поверхностей шин.In addition, as a method of producing a VCR polymer in patents JP-B-1987-171 (patent literature 3), JP-B-1988-36324 (patent literature 4), JP-B-1990-37927 (patent literature 5), JP-B-1990-38081 (Patent Literature 6) and JP-B-1991-63566 (Patent Literature 7) describe, for example, a method that involves 1,3- cis-1,4 polymerization of VCR polymer butadiene in the presence or absence of carbon disulfide or after receiving the VCR polymer in the separation of 1,3-butadiene from carbon disulfide for reuse and circulation in the separation of 1,3-butadiene , essentially free of carbon disulfide and an inert organic solvent. Moreover, JP-B-1992-48815 (Patent Literature 8) describes a VCR polymer which exhibits a low degree of swelling of the extrudable melt upon conversion to compound, and upon vulcanization of the compound is excellent in terms of tensile stress and multiple fracture resistance bending and is suitable for the production of tire side surfaces.
В патенте JP-A-2000-44633 (патентная литература 9) предоставлен способ получения нового полимера VCR, который заключается в проведении цис-1,4-полимеризации 1,3-бутадиена в инертном органическом растворителе, состоящем, в основном, из фракции С4, с использованием каталитической системы, включающей галогенсодержащее алюминийорганическое соединение, растворимое соединение кобальта и воду, и в проведении в получающейся в ходе полимеризации реакционной смеси синдиотактической 1,2-полимеризации 1,3-бутадиена в присутствии катализатора синдиотактической 1,2-полимеризации, получаемого из растворимого соединения кобальта, соединения триалкилалюминия и дисульфида углерода. Более того, раскрыто, что полученный полимер VCR представляет собой композицию VCR, содержащую от 3 до 30 мас.% нерастворимого в кипящем н-гексане вещества, которое является синдиотактическим 1,2-полибутадиеном, в виде диспергированных коротких волокнистых кристаллов, и от 97 до 70 мас.% растворимого в кипящем н-гексане вещества, которое обладает цис-структурой, содержащей 90% или более цис-1,4-полибутадиена.JP-A-2000-44633 (Patent Literature 9) provides a method for producing a new VCR polymer, which consists in cis-1,4-polymerizing 1,3-butadiene in an inert organic solvent, consisting mainly of fraction C4 using a catalytic system comprising a halogen-containing organoaluminum compound, a soluble cobalt compound and water, and in the resulting polymerization reaction mixture the syndiotactic 1,2-polymerization of 1,3-butadiene in the presence of a syndiotactically catalyst and 1,2-polymerization obtained from a soluble cobalt compound, a trialkylaluminum compound and carbon disulfide. Moreover, it is disclosed that the obtained VCR polymer is a VCR composition containing from 3 to 30 wt.% A substance insoluble in boiling n-hexane, which is syndiotactic 1,2-polybutadiene, in the form of dispersed short fibrous crystals, and from 97 to 70 wt.% Soluble in boiling n-hexane substance, which has a cis structure containing 90% or more cis-1,4-polybutadiene.
В патентах JP-A-2000-154215 (патентная литература 10) и JP-A-2000-159836 (патентная литература 11) предоставлен способ получения нового полимера VCR, который заключается в проведении цис-1,4-полимеризации 1,3-бутадиена с использованием катализатора, получаемого из (А) комплексного соединения переходного металла металлоценового типа, и (В) ионного соединения, образованного не образующими координационные связи анионом и катионом и/или алюмоксана, и в проведении в получающейся в ходе полимеризации реакционной смеси синдиотактической 1,2-полимеризации 1,3-бутадиена в присутствии катализатора, получаемого, по меньшей мере, из одного соединения, выбираемого из (E) соединения кобальта, (F) соединения изоциановой кислоты и дисульфида углерода.Patents JP-A-2000-154215 (Patent Literature 10) and JP-A-2000-159836 (Patent Literature 11) provide a method for producing a new VCR polymer, which involves the cis-1,4 polymerization of 1,3-butadiene using a catalyst obtained from (A) a complex compound of a transition metal of the metallocene type, and (B) an ionic compound formed by not forming coordination bonds with the anion and cation and / or alumoxane, and in carrying out the syndiotactic 1,2 reaction mixture resulting from polymerization polymerization of 1,3-butadiene and in the presence of a catalyst obtained by at least one compound selected from (E) a cobalt compound, (F) an isocyanic acid compound and carbon disulfide.
Однако при синдиотактической 1,2-полимеризации 1,3-бутадиена отмечают в зависимости от используемых условий полимеризации случаи возникновения неприятного запаха от применяемого соединения серы, что требует улучшения.However, when syndiotactic 1,2-polymerization of 1,3-butadiene is observed, depending on the polymerization conditions used, there are cases of unpleasant odor from the sulfur compound used, which requires improvement.
В патенте US 6956093 (патентная литература 12) раскрыт способ получения каучуковой композиции с уменьшенным запахом, который включает обработку пероксидом водорода синдиотактического 1,2-полибутадиена, получаемого с использованием катализатора, содержащего дисульфид углерода в качестве каталитического компонента. Однако такой способ не является предпочтительным, поскольку пероксид водорода может окислять двойную связь полибутадиена или оставшийся бутадиеновый мономер.US Pat. No. 6,956,093 (Patent Literature 12) discloses a method for producing a rubber composition with a reduced odor, which comprises treating with hydrogen peroxide the syndiotactic 1,2-polybutadiene obtained using a catalyst containing carbon disulfide as a catalytic component. However, this method is not preferred since hydrogen peroxide can oxidize the polybutadiene double bond or the remaining butadiene monomer.
Патентная литература 1: JP-B-1974-17666Patent Literature 1: JP-B-1974-17666
Патентная литература 2: JP-B-1974-17667Patent Literature 2: JP-B-1974-17667
Патентная литература 3: JP-B-1987-171Patent Literature 3: JP-B-1987-171
Патентная литература 4: JP-B-1988-36324Patent Literature 4: JP-B-1988-36324
Патентная литература 5: JP-B-1990-37927Patent Literature 5: JP-B-1990-37927
Патентная литература 6: JP-B-1990-38081Patent Literature 6: JP-B-1990-38081
Патентная литература 7: JP-B-1991-63566Patent Literature 7: JP-B-1991-63566
Патентная литература 8: JP-B-1992-48815Patent Literature 8: JP-B-1992-48815
Патентная литература 9: JP-A-2000-44633Patent Literature 9: JP-A-2000-44633
Патентная литература 10: JP-A-2000-154215Patent Literature 10: JP-A-2000-154215
Патентная литература 11: JP-B-2000-159836Patent Literature 11: JP-B-2000-159836
Патентная литература 12: патент US 6956093Patent literature 12: patent US 6956093
Раскрытие изобретенияDisclosure of invention
Задача, на решение которой направлено настоящее изобретение, заключается в предоставлении способа получения полимеризацией 1,3-бутадиена армированного полибутадиена с уменьшенным запахом (здесь и далее в данном документе часто обозначаемого как полимер VCR), включающего цис-1,4-полимер и синдиотактический 1,2-полимер.The problem to which the present invention is directed, is to provide a method for the polymerization of 1,3-butadiene-reinforced polybutadiene with reduced odor (hereinafter, often referred to as the polymer VCR), including cis-1,4-polymer and syndiotactic 1 , 2 polymer.
Настоящее изобретение относится к способу получения полибутадиена с уменьшенным запахом, который заключается в проведении цис-1,4-полимеризации 1,3-бутадиена, а затем осуществлении синдиотактической 1,2-полимеризации продукта реакции в получающейся в ходе полимеризации системе, причем способ отличается тем, что после проведения полимеризации вводят галогенсодержащую кислоту или соль галогенсодержащей кислоты, обе представлены нижеследующей общей формулой (I):The present invention relates to a method for producing polybutadiene with a reduced odor, which consists in cis-1,4-polymerizing 1,3-butadiene, and then carrying out syndiotactic 1,2-polymerization of the reaction product in the resulting polymerization system, the method being characterized in that that after polymerization, a halogen-containing acid or a salt of a halogen-containing acid is introduced, both are represented by the following general formula (I):
М'(X'Oq)rZ's (I)M '(X'O q ) r Z' s (I)
(где М' является атомом металла или атомом водорода, Х' является атомом галогена, выбираемым из хлора, брома и йода, О является атомом кислорода, q представляет собой целое число от 1 до 4, Z' является анионом, способным к образованию связи с атомом M', r представляет собой целое число, равное 1 или более, а сумма r+s является степенью окисления M').(where M 'is a metal atom or a hydrogen atom, X' is a halogen atom selected from chlorine, bromine and iodine, O is an oxygen atom, q is an integer from 1 to 4, Z 'is an anion capable of forming a bond with atom M ', r is an integer of 1 or more, and the sum r + s is the oxidation state of M').
Предпочтительно, чтобы в настоящем изобретении атом X' в соединении, представляемом общей формулой (I), являлся хлором.Preferably, in the present invention, the X 'atom in the compound represented by general formula (I) is chlorine.
Предпочтительно, чтобы в настоящем изобретении соединение, представленное общей формулой (I), являлось хлорноватистой кислотой или солью хлорноватистой кислоты.Preferably, in the present invention, the compound represented by general formula (I) is hypochlorous acid or a hypochlorous acid salt.
Настоящее изобретение можно использовать как способ получения армированного полибутадиенового каучука с уменьшенным запахом, используя полибутадиен, полученный нижеследующим способом. А именно, во-первых, армированный полибутадиеновый каучук с уменьшенным запахом можно получить, используя полибутадиен, полученный с применением в качестве катализатора цис-1,4-полимеризации катализатора, включающего соединение кобальта, алюминийорганическое соединение и воду. Во-вторых, армированный полибутадиеновый каучук с уменьшенным запахом можно получить, используя полибутадиен, полученный цис-1,4-полимеризацией 1,3-бутадиена с применением катализатора, получаемого из комплексного соединения переходного металла металлоценового типа и ионного соединения, образованного не образующими координационные связи анионом и катионом и/или алюмоксана. В-третьих, армированный полибутадиеновый каучук с уменьшенным запахом можно получить, используя полибутадиен, полученный с применением в качестве катализатора цис-1,4-полимеризации катализатора, полученного из (А) соединения иттрия, (Б) ионного соединения, образованного не образующими координационные связи анионом и катионом и (В) металлоорганического соединения элемента, выбираемого из 2-й группы, 12-й группы и 13-й группы Периодической таблицы.The present invention can be used as a method for producing a reduced odor reinforced polybutadiene rubber using the polybutadiene obtained by the following method. Namely, firstly, a reinforced polybutadiene rubber with a reduced odor can be obtained using polybutadiene obtained using a cis-1,4 polymerization catalyst as a catalyst, including a cobalt compound, an organoaluminum compound and water. Secondly, a reduced odor reinforced polybutadiene rubber can be obtained using polybutadiene obtained by cis-1,4 polymerization of 1,3-butadiene using a catalyst obtained from a metallocene-type transition metal complex and an ionic compound formed without coordination bonds anion and cation and / or alumoxane. Thirdly, a reduced odor reinforced polybutadiene rubber can be obtained using polybutadiene obtained using cis-1,4 polymerization as a catalyst obtained from (A) a yttrium compound, (B) an ionic compound formed not forming coordination bonds anion and cation; and (B) an organometallic compound of an element selected from the 2nd group, the 12th group and the 13th group of the Periodic table.
Во-первых, для способа по настоящему изобретению при использовании полибутадиена, полученного с применением в качестве катализатора цис-1,4-полимеризации катализатора, включающего соединение кобальта, алюминийорганическое соединение и воду, предпочтительно, чтобы алюминийорганическое соединение являлось соединением триалкилалюминия с формулой R1 3Al (где группа R1 является углеводородной группой, имеющей от 1 до 10 атомов углерода) и галогенсодержащим соединением алюминия с формулой R2 3-nAlXn (где группа R2 является углеводородной группой, имеющей от 1 до 10 атомов углерода, Х является атомом галогена, а n является числом от 1 до 2).First, for the method of the present invention, when using polybutadiene obtained using a cis-1,4 polymerization catalyst as a catalyst comprising a cobalt compound, an organoaluminum compound and water, it is preferable that the organoaluminum compound is a trialkylaluminum compound of the formula R 1 3 Al (where the R 1 group is a hydrocarbon group having from 1 to 10 carbon atoms) and a halogen-containing aluminum compound of the formula R 2 3-n AlX n (where the R 2 group is a hydrocarbon group, having from 1 to 10 carbon atoms, X is a halogen atom, and n is a number from 1 to 2).
Также предпочтительно, чтобы катализатор цис-1,4-полимеризации представлял собой катализатор, полученный выдержкой компонентов, выбираемых из соединения металлов 3-й группы Периодической таблицы, соединения, представляющего собой гидрид алкилалюминия, бутадиена, метилалюмоксана и хлорсодержащего соединения.It is also preferred that the cis-1,4 polymerization catalyst be a catalyst obtained by extracting components selected from a metal compound of the 3rd group of the Periodic Table, a compound consisting of an aluminum hydride of aluminum, butadiene, methylaluminoxane and a chlorine-containing compound.
Во-вторых, также предпочтительно, чтобы катализатор цис-1,4-полимеризации представлял собой катализатор, полученный из комплексного соединения переходного металла металлоценового типа, ионного соединения, образованного не образующими координационные связи анионом и катионом, металлоорганического соединения элемента групп с 1-й по 3-ю Периодической таблицы и воды [(металлоорганическое соединение элемента групп с 1-ой по 3-ю периодической таблицы)/(вода) = от 0,66 до 5 (мольное отношение)].Secondly, it is also preferable that the cis-1,4 polymerization catalyst be a catalyst obtained from a metallocene-type transition metal complex compound, an ionic compound formed by anion and cation not forming coordination bonds, an organometallic compound of an element of groups 1 to Of the 3rd Periodic Table and water [(organometallic compound of the element of groups 1 through 3 of the periodic table) / (water) = from 0.66 to 5 (molar ratio)].
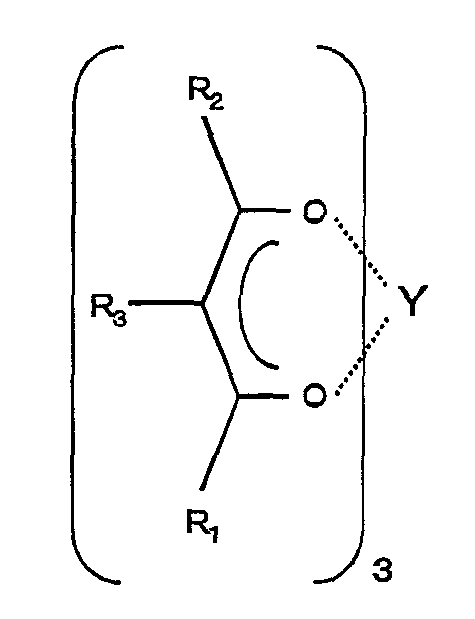
Предпочтительно, когда при использовании катализатора, содержащего соединение иттрия, можно использовать соединение иттрия с объемным лигандом, представленное нижеследующей общей формулой:Preferably, when using a catalyst containing a yttrium compound, a yttrium compound with a bulky ligand represented by the following general formula can be used:
[формула 1][Formula 1]
(где каждая из групп R1, R2 и R3 является атомом водорода или углеводородной группой с числом атомов углерода от 1 до 12, О является атомом кислорода, а Y является атомом иттрия).(where each of the groups R 1 , R 2 and R 3 is a hydrogen atom or a hydrocarbon group with the number of carbon atoms from 1 to 12, O is an oxygen atom, and Y is a yttrium atom).
В данном случае предпочтительно, чтобы катализатор синдиотактической 1,2-полимеризации состоял из соединения кобальта, соединения алкилалюминия и соединения серы.In this case, it is preferable that the syndiotactic 1,2-polymerization catalyst consist of a cobalt compound, an alkyl aluminum compound, and a sulfur compound.
Настоящее изобретение также относится к способу получения армированного полибутадиена с уменьшенным запахом, где полибутадиен представляет собой армированный полибутадиен, содержащий (1) от 3 до 30 мас.% нерастворимого в кипящем н-гексане вещества и (2) от 97 до 70 мас.% растворимого в кипящем н-гексане вещества.The present invention also relates to a method for producing a reduced odor reinforced polybutadiene, wherein the polybutadiene is a reinforced polybutadiene containing (1) from 3 to 30 wt.% Insoluble in boiling n-hexane and (2) from 97 to 70 wt.% Soluble in boiling n-hexane substance.
Настоящее изобретение предоставляет способ получения армированного полибутадиенового каучука с уменьшенным запахом, включающего цис-1,4-полимер и синдиотактический 1,2-полимер, посредством введения после проведения полимеризации 1,3-бутадиена галогенсодержащей кислоты или соли галогенсодержащей кислоты.The present invention provides a method for producing a reduced odor reinforced polybutadiene rubber comprising a cis-1,4 polymer and a syndiotactic 1,2 polymer by introducing after polymerization a 1,3-butadiene of a halogen-containing acid or a salt of a halogen-containing acid.
Наилучший способ осуществления изобретенияBEST MODE FOR CARRYING OUT THE INVENTION
Настоящее изобретение предоставляет способ получения полибутадиена, который заключается в проведении цис-1,4-полимеризации 1,3-бутадиена, а затем осуществления синдиотактической 1,2-полимеризации продукта реакции в получающейся в ходе полимеризации системе, вещество, вводимое после проведения полимеризации для уменьшения запаха представляет собой галогенсодержащую кислоту или соль галогенсодержащей кислоты, обе представлены нижеследующей общей формулой (I):The present invention provides a method for producing polybutadiene, which involves the cis-1,4 polymerization of 1,3-butadiene, and then the syndiotactic 1,2-polymerization of the reaction product in the resulting polymerization system, the substance introduced after polymerization to reduce the odor is a halogen-containing acid or a salt of a halogen-containing acid, both represented by the following general formula (I):
M'(X'Oq)rZ's (I)M '(X'O q ) r Z' s (I)
(где М' является атомом металла или атомом водорода, Х' является атомом галогена, выбираемым из хлора, брома и йода, О является атомом кислорода, q представляет собой целое число от 1 до 4, Z' является анионом, способным к образованию связи с атомом М', r представляет собой целое число, равное 1 или более, а сумма r+s представляет собой степень окисления М'). В качестве атома М' можно упомянуть атомы водорода, лития, натрия, калия, магния, кальция, стронция, бария, иттрия, ванадия, железа, кобальта, никеля, меди, цинка, бора, алюминия и т.д. Предпочтительно, М' представляет собой атом водорода, лития, натрия, калия, магния, кальция или алюминия, особенно желательными являются атомы водорода, натрия, калия, магния или кальция, а еще более предпочтительно, когда он представляет собой атом натрия или кальция.(where M 'is a metal atom or a hydrogen atom, X' is a halogen atom selected from chlorine, bromine and iodine, O is an oxygen atom, q is an integer from 1 to 4, Z 'is an anion capable of forming a bond with atom M ', r represents an integer equal to 1 or more, and the sum of r + s represents the oxidation state of M'). As the atom M ', atoms of hydrogen, lithium, sodium, potassium, magnesium, calcium, strontium, barium, yttrium, vanadium, iron, cobalt, nickel, copper, zinc, boron, aluminum, etc. can be mentioned. Preferably, M ′ is a hydrogen, lithium, sodium, potassium, magnesium, calcium or aluminum atom, hydrogen, sodium, potassium, magnesium or calcium atoms are particularly desirable, and even more preferably when it is a sodium or calcium atom.
В качестве атома Х' можно упомянуть атомы хлора, брома и йода. Среди них атом хлора является предпочтительным.As the X 'atom, chlorine, bromine and iodine atoms can be mentioned. Among them, a chlorine atom is preferred.
q представляет собой целое число от 1 до 4, предпочтительно 1 или 2, особенно желательно 1.q is an integer from 1 to 4, preferably 1 or 2, particularly preferably 1.
Анион Z' является анионом, отличающимся от иона галогенсодержащей кислоты, и в отношении него не существует особенных ограничений при условии, что он может связываться, компенсируя положительный заряд М', остающийся без достаточной компенсации ионом галогенсодержащей кислоты. Можно упомянуть, например, ионы таких галогенов, как хлор, бром, йод и им подобные, гидроксид-ион, оксид-ион, ион азотной кислоты, ион азотистой кислоты, ион серной кислоты, ион фосфорной кислоты, ион фосфористой кислоты, ион борной кислоты, ион карбоновой кислоты, и алкокси-ион. Среди них особенно предпочтительными являются ион хлора и гидроксид-ион.The anion Z 'is an anion different from the halogen-containing acid ion, and there are no particular restrictions on it, provided that it can bind, compensating for the positive charge M', remaining without sufficient compensation by the halogen-containing acid ion. Mention may be made, for example, of halogen ions such as chlorine, bromine, iodine and the like, hydroxide ion, oxide ion, nitric acid ion, nitrous acid ion, sulfuric acid ion, phosphoric acid ion, phosphoric acid ion, boric acid ion , a carboxylic acid ion, and an alkoxy ion. Among them, chlorine ion and hydroxide ion are particularly preferred.
r является числом ионов галогенсодержащей кислоты, связанных с атомом М', и представляет собой положительную сумму, не превышающую степень окисления M'.r is the number of halogen-containing acid ions bonded to the atom M 'and represents a positive amount not exceeding the oxidation state M'.
s является числом анионов Z', связанных с атомом М'. Поэтому сумма r+s представляет собой степень окисления М'.s is the number of anions Z 'bonded to the atom M'. Therefore, the sum r + s represents the oxidation state of M '.
В качестве конкретных примеров галогенсодержащей кислоты или соли галогенсодержащей кислоты можно упомянуть хлорноватистую кислоту, хлористую кислоту, хлорноватую кислоту, перхлорную кислоту, бромноватистую кислоту, бромистую кислоту, бромноватую кислоту, пербромную кислоту, йодноватистую кислоту, йодистую кислоту, йодноватую кислоту, перйодную кислоту, гипохлорит лития, гипохлорит натрия, гипохлорит магния, гипохлорит кальция, гипохлорит хлорид кальция, а также гипохлорит гидроксид кальция. Предпочтительными являются гипохлорит натрия, гипохлорит кальция, гипохлорит хлорид кальция и гипохлорит гидроксид кальция, а особенно желательным является гипохлорит натрия.As specific examples of the halogen-containing acid or salt of the halogen-containing acid, mention may be made of hypochlorous acid, perchloric acid, hypochlorous acid, perchloric acid, hydrobromic acid, bromic acid, hydrobromic acid, perbromic acid, hypochlorous acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodic acid, iodide acid , sodium hypochlorite, magnesium hypochlorite, calcium hypochlorite, calcium chloride hypochlorite, and calcium hypochlorite. Preferred are sodium hypochlorite, calcium hypochlorite, calcium chloride hypochlorite and calcium hydroxide hypochlorite, and sodium hypochlorite is particularly desirable.
В качестве растворителя используемого при получении полибутадиена по настоящему изобретению, можно упомянуть углеводородные растворители, такие как неразветвленный алифатический углеводород, такой как н-гексан, бутан, гептан или пентан, циклический алифатический углеводород, такой как циклопентан или циклогексан, олефиновый углеводород ряда С4, такой как 1-бутен, цис-2-бутен или транс-2-бутен, уайт-спирит, сольвент-нафта, керосин и им подобные, галогенированные углеводородные растворители, такие как метиленхлорид и ему подобные, и так далее. Их можно использовать сами по себе или в виде смеси. Среди них предпочтительно используют содержащий циклогексан растворитель. Смесь циклогексана и углеводорода ряда С4 (например, цис-2-бутена или транс-2-бутена) используют особенно предпочтительно.As the solvent used in the preparation of the polybutadiene of the present invention, mention may be made of hydrocarbon solvents such as a straight chain aliphatic hydrocarbon such as n-hexane, butane, heptane or pentane, a cyclic aliphatic hydrocarbon such as cyclopentane or cyclohexane, a C4 series olefinic hydrocarbon such like 1-butene, cis-2-butene or trans-2-butene, white spirit, solvent naphtha, kerosene and the like, halogenated hydrocarbon solvents such as methylene chloride and the like, and so on e. They can be used alone or as a mixture. Among them, a cyclohexane-containing solvent is preferably used. A mixture of cyclohexane and a C4 hydrocarbon (e.g. cis-2-butene or trans-2-butene) is used particularly preferably.
В качестве первого катализатора цис-1,4-полимеризации можно использовать катализатор, включающий соединение кобальта, алюминийорганическое соединение и воду. В качестве алюминийорганического соединения можно использовать смесь соединения триалкилалюминия с формулой R1 3Al (где группа R1 является углеводородной группой, имеющей от 1 до 10 атомов углерода) и галогенсодержащего соединения алюминия с формулой R2 3-nAlXn (где группа R2 является углеводородной группой, имеющей от 1 до 10 атомов углерода, Х является атомом галогена, а n представляет собой число от 1 до 2).As the first cis-1,4 polymerization catalyst, a catalyst comprising a cobalt compound, an organoaluminum compound and water can be used. As the organoaluminum compound, a mixture of a trialkylaluminum compound with the formula R 1 3 Al (where the R 1 group is a hydrocarbon group having from 1 to 10 carbon atoms) and a halogen-containing aluminum compound with the formula R 2 3-n AlX n (where the group R 2 is a hydrocarbon group having from 1 to 10 carbon atoms, X is a halogen atom, and n is a number from 1 to 2).
В качестве соединения кобальта в катализаторе цис-1,4-полимеризации предпочтительно используют соль или комплекс кобальта. В качестве особенно предпочтительных соединений кобальта можно упомянуть соли кобальта, такие как хлорид кобальта, бромид кобальта, нитрат кобальта, октилат кобальта, нафтенат кобальта, ацетат кобальта, малонат кобальта и им подобные, бисацетилацетонат кобальта и трисацетилацетонат кобальта, этилацетоацетат кобальта, галогенидтриарилфосфиновый комплекс кобальта, его триалкилфосфиновый комплекс, его комплекс с органическим основанием, такой как его комплекс с пиридином или его комплекс с пиколином, или его комплекс с этиловым спиртом, и т.д.As the cobalt compound in the cis-1,4 polymerization catalyst, a salt or cobalt complex is preferably used. Particularly preferred cobalt compounds include cobalt salts, such as cobalt chloride, cobalt bromide, cobalt nitrate, cobalt octylate, cobalt naphthenate, cobalt acetate, cobalt malonate and the like, cobalt bisacetylacetone cobalt acetate, triacetalacetate acetate, triacetalacetate acetate its trialkylphosphine complex, its complex with an organic base, such as its complex with pyridine or its complex with picoline, or its complex with ethyl alcohol, etc.
В качестве соединения триалкилалюминия с формулой R1 3Al (где группа R1 является углеводородной группой, имеющей от 1 до 10 атомов углерода, предпочтительно, имеющей от 2 до 8 атомов углерода) можно упомянуть триэтилалюминий, триметилалюминий, триизобутилалюминий, тригексилалюминий, триоктилалюминий и т.д. Среди них триэтилалюминий является предпочтительным.As the trialkylaluminum compound of the formula R 1 3 Al (where the R 1 group is a hydrocarbon group having from 1 to 10 carbon atoms, preferably having from 2 to 8 carbon atoms), mention may be made of triethylaluminum, trimethylaluminum, triisobutylaluminum, trihexylaluminum, trioctylaluminum and so on .d. Among them, triethylaluminum is preferred.
В качестве галогенсодержащего соединения алюминия с формулой R2 3-nAlXn (где группа R2 является углеводородной группой, имеющей от 1 до 10 атомов углерода, предпочтительно, имеющей от 2 до 8 атомов углерода, атом Х является атомом галогена, а n представляет собой число от 1 до 2) можно упомянуть галогениды диалкилалюминия, такие как хлорид диалкилалюминия, бромид диалкилалюминия и им подобные, полуторагалогениды алкилалюминия, такие как полуторахлорид алкилалюминия, полуторабромид алкилалюминия и им подобные, дигалогениды алкилалюминия, такие как дихлорид алкилалюминия, дибромид алкилалюминия и им подобные, и т.д. В качестве конкретных соединений можно упомянуть монохлорид диэтилалюминия, монобромид диэтилалюминия, монохлорид дибутилалюминия, полуторахлорид этилалюминия, дихлорид этилалюминия, монохлорид дициклогексилалюминия, монохлорид дифенилалюминия и т.д. Среди них монохлорид диэтилалюминия является предпочтительным.As a halogen-containing aluminum compound of the formula R 2 3-n AlX n (where the R 2 group is a hydrocarbon group having from 1 to 10 carbon atoms, preferably having from 2 to 8 carbon atoms, the X atom is a halogen atom, and n represents a number from 1 to 2) mention may be made of dialkyl aluminum halides such as dialkyl aluminum chloride, dialkyl aluminum bromide and the like, alkyl aluminum sesquichalides such as alkyl aluminum sesquichloride, alkyl aluminum sesquioxides and the like, alkyl aluminum dihalides, such such as alkylaluminum dichloride, alkylaluminum dibromide and the like, etc. As specific compounds, diethylaluminum monochloride, diethylaluminum monobromide, dibutylaluminum monochloride, ethylaluminum sesquichloride, ethylaluminum dichloride, dicyclohexylaluminum monochloride, diphenylaluminum monochloride, etc. can be mentioned. Among them, diethylaluminum monochloride is preferred.
Количество используемого соединения кобальта обычно составляет от 1×10-7 до 1×10-4 моль, предпочтительно от 1×10-6 до 1×10-5 моль, на 1 моль используемого бутадиена.The amount of cobalt compound used is usually from 1 × 10 -7 to 1 × 10 -4 mol, preferably from 1 × 10 -6 to 1 × 10 -5 mol, per 1 mol of butadiene used.
Количество используемого триалкилалюминия обычно составляет от 10 до 5000 моль, предпочтительно от 50 до 1000 моль, на 1 моль используемого соединения кобальта.The amount of trialkyl aluminum used is usually from 10 to 5000 mol, preferably from 50 to 1000 mol, per 1 mol of cobalt compound used.
Количество используемого галогенсодержащего соединения алюминия составляет от 0 до 1, предпочтительно от 0,1 до 0,9, особенно желательно от 0,25 до 0,75, в терминах отношения (X/Al) количества атома Х в галогенсодержащем соединении алюминия к количеству атома Al в триалкилалюминии и галогенсодержащем соединении алюминия.The amount of halogen-containing aluminum compound used is from 0 to 1, preferably from 0.1 to 0.9, particularly preferably from 0.25 to 0.75, in terms of the ratio (X / Al) of the amount of X atom in the halogen-containing aluminum compound to the amount of atom Al in trialkylaluminium and a halogen-containing aluminum compound.
Количество используемой воды составляет от 0,1 до 1,45 моль, предпочтительно от 0,2 до 1,2 моль, на 1 моль соединения алюминия.The amount of water used is from 0.1 to 1.45 mol, preferably from 0.2 to 1.2 mol, per 1 mol of aluminum compound.
В отношении порядка введения каталитических компонентов не существует конкретных ограничений. Однако предпочтительно, когда триалкилалюминий и галогенсодержащее соединение алюминия смешивают и выдерживают в инертном растворителе, а затем используют. Желательно, чтобы время выдерживания составляло от 0,1 часа до 24 часов, и предпочтительно, чтобы температура выдерживания находилась в диапазоне от 0 до 80°С.With regard to the order of introduction of the catalytic components, there are no particular restrictions. However, it is preferred that the trialkylaluminum and the halogen-containing aluminum compound are mixed and incubated in an inert solvent and then used. It is desirable that the holding time is from 0.1 hours to 24 hours, and it is preferable that the holding temperature is in the range from 0 to 80 ° C.
Желательно, чтобы воду добавляли в смесь после выдержки с последующей дальнейшей выдержкой. Предпочтительно, когда время выдержки составляет от 0,1 часа до 24 часов, и желательно, чтобы температура выдержки находилась в диапазоне от 0 до 80°С.Preferably, water is added to the mixture after exposure followed by further exposure. Preferably, the holding time is from 0.1 hours to 24 hours, and it is desirable that the holding temperature is in the range from 0 to 80 ° C.
В качестве катализатора цис-1,4-полимеризации можно также использовать катализаторы, получаемые выдержкой компонентов, выбираемых из соединения металла 3-й группы Периодической таблицы, соединения, представляющего собой галогенид алкилалюминия, бутадиена, метилалюмоксана и хлорсодержащего соединения.As a catalyst for cis-1,4 polymerization, you can also use catalysts obtained by extracting components selected from a metal compound of the 3rd group of the Periodic Table, a compound consisting of an aluminum alkyl halide, butadiene, methylaluminoxane and a chlorine-containing compound.
Атом металла, входящий в состав соединения металла 3-й группы Периодической таблицы, которое является компонентом вышеупомянутой каталитической системы, представляет собой атом 3-й группы Периодической таблицы и включает элементы ряда лантанидов, элементы ряда актинидов и т.д. Атом редкоземельного металла является предпочтительным. Конкретно, можно упомянуть неодим, празеодим, церий, лантан, гадолиний или их смеси. Атом неодима является особенно предпочтительным.A metal atom that is part of a metal compound of the 3rd group of the Periodic Table, which is a component of the above catalyst system, is an atom of the 3rd group of the Periodic Table and includes elements of a number of lanthanides, elements of a number of actinides, etc. A rare earth metal atom is preferred. Specifically, mention may be made of neodymium, praseodymium, cerium, lanthanum, gadolinium, or mixtures thereof. A neodymium atom is particularly preferred.
В качестве соединения металла 3-й группы Периодической таблицы можно упомянуть карбоксилат металла 3-й группы Периодической таблицы, его алкоксид, его комплекс с β-дикетоном, его фосфат или его фосфит и т.д. Среди них карбоксилат и фосфат являются предпочтительными, а особенно желательным является карбоксилат.As a metal compound of the 3rd group of the Periodic Table, mention may be made of a metal carboxylate of the 3rd group of the Periodic table, its alkoxide, its complex with β-diketone, its phosphate or its phosphite, etc. Among them, carboxylate and phosphate are preferred, and carboxylate is particularly desirable.
Карбоксилат металла 3-й группы Периодической таблицы представляет собой соединение с общей формулой (RCO2)3M (где атом М является атомом металла 3-й группы Периодической таблицы, а группа R представляет собой углеводородную группу с числом атомов углерода от 1 до 20).The metal carboxylate of the 3rd group of the Periodic Table is a compound with the general formula (RCO 2 ) 3 M (where the M atom is a metal atom of the 3rd group of the Periodic Table and the R group is a hydrocarbon group with the number of carbon atoms from 1 to 20) .
Группа R является насыщенной или ненасыщенной алкильной группой, которая представляет собой неразветвленную цепь, разветвленную цепь или является циклической. Карбоксильная группа СО2 связана с первичным, вторичным или третичным атомом углерода. Конкретно можно упомянуть соли октановой кислоты, 2-этилгексановой кислоты, олеиновой кислоты, стеариновой кислоты, бензойной кислоты, нафтеновой кислоты, кислоты «Версатик» (торговая марка фирмы Shell Chemical; карбоновая кислота, в которой карбоксильная группа связана с третичным атомом углерода) и т.д. Среди них 2-этилгексановая кислота и кислота «Версатик» являются предпочтительными.The group R is a saturated or unsaturated alkyl group, which is a straight chain, branched chain or is cyclic. The carboxyl group of CO 2 is bound to a primary, secondary or tertiary carbon atom. Specifically, mention may be made of salts of octanoic acid, 2-ethylhexanoic acid, oleic acid, stearic acid, benzoic acid, naphthenic acid, Versatic acid (a trademark of Shell Chemical; a carboxylic acid in which a carboxyl group is attached to a tertiary carbon atom) and t .d. Among them, 2-ethylhexanoic acid and Versatic acid are preferred.
Алкоксид металла 3-й группы Периодической таблицы является соединением с общей формулой (RO)3M (где группа R и атом М определены таким же образом, как указано выше). В качестве примеров алкоксигруппы, представляемой в виде RO, можно упомянуть 2-этилгексилоксигруппу, олеилоксигруппу, стеарилоксигруппу, феноксигруппу и бензилоксигруппу. Среди них 2-этилгексилоксигруппа и бензилоксигруппа являются предпочтительными.The metal alkoxide of the 3rd group of the Periodic Table is a compound with the general formula (RO) 3 M (wherein the R group and the M atom are defined in the same manner as described above). As examples of an alkoxy group represented as RO, mention may be made of a 2-ethylhexyloxy group, an oleyloxy group, a stearyloxy group, a phenoxy group, and a benzyloxy group. Among them, a 2-ethylhexyloxy group and a benzyloxy group are preferred.
В качестве комплекса металла 3-ей группы Периодической таблицы с β-дикетоном можно упомянуть, например, комплекс металла 3-й группы Периодической таблицы с ацетилацетоном, бензоилацетоном, пропионитрилацетоном, валерилацетоном или этилацетоацетоном. Среди них комплекс с ацетилацетоном и комплекс с этилацетоацетоном являются предпочтительными.As the metal complex of the 3rd group of the Periodic Table with β-diketone, mention may be made, for example, of the metal complex of the 3rd group of the Periodic Table with acetylacetone, benzoylacetone, propionitrile acetone, valeryl acetone or ethyl acetoacetone. Among them, a complex with acetylacetone and a complex with ethyl acetoacetone are preferred.
В качестве фосфата или фосфита металла 3-й группы Периодической таблицы можно упомянуть бис(2-этилгексил)фосфат металла 3-й группы Периодической таблицы, его бис(1-метилгептилфосфат), его бис(пара-нонилфенил)фосфат, бис(полиэтиленгликоль-пара-нонилфенил)фосфат, его (1-метилгептил)(2-этилгексил)фосфат, его (2-этилгексил)(пара-нонилфенил)фосфат, его моно-2-этилгексил-2-этилгексилфосфонат, его моно-2-нонилфенил-2-этилгексилфосфонат, его бис(2-этилгексил)фосфинат, его бис(1-метилгептил)фосфинат, его бис(пара-нонилфенил)фосфинат, его (1-метилгептил)(2-этилгексил)фосфинат, его (2-этилгексил)(пара-нонилфенил)фосфинат и т.д. Среди них предпочтительными являются бис(2-этилгексил)фосфат металла 3-й группы Периодической таблицы, его бис(1-метилгептил)фосфат, его моно-2-этилгексил-2-этилгексилфосфонат, его бис(2-этилгексил)фосфинат и т.д.As the phosphate or phosphite of the metal of the 3rd group of the Periodic Table, mention may be made of bis (2-ethylhexyl) phosphate of the metal of the 3rd group of the Periodic table, its bis (1-methylheptylphosphate), its bis (paranylphenyl) phosphate, bis (polyethylene glycol- para-nonylphenyl) phosphate, its (1-methylheptyl) (2-ethylhexyl) phosphate, its (2-ethylhexyl) (paranylphenyl) phosphate, its mono-2-ethylhexyl-2-ethylhexylphosphonate, its mono-2-nonylphenyl- 2-ethylhexylphosphonate, its bis (2-ethylhexyl) phosphinate, its bis (1-methylheptyl) phosphinate, its bis (paranylphenyl) phosphinate, its (1-methylheptyl) (2-these hexyl) phosphinate, its (2-ethylhexyl) (p-nonylphenyl) phosphinate, etc. Among them, preferred are metal bis (2-ethylhexyl) phosphate of the 3rd group of the Periodic Table, its bis (1-methylheptyl) phosphate, its mono-2-ethylhexyl-2-ethylhexylphosphonate, its bis (2-ethylhexyl) phosphinate, etc. d.
Из вышеуказанных соединений особенно желательными являются фосфат неодима или карбоксилат неодима, а наиболее предпочтительными являются соли карбоновых кислот, например неодимовая соль 2-этилгексановой кислоты и неодимовая соль кислоты «Версатик».Of the above compounds, neodymium phosphate or neodymium carboxylate is particularly desirable, and carboxylic acid salts, for example 2-ethylhexanoic acid neodymium salt and Versatic acid neodymium salt, are most preferred.
В качестве представляющего собой гидрид алкилалюминия соединения вышеуказанной каталитической системы можно упомянуть гидрид диэтилалюминия, гидрид дипропилалюминия, гидрид ди-н-бутилэтилалюминия, гидрид диизобутилалюминия, гидрид дифенилалюминия и т.д.As the alkyl aluminum hydride compound of the above catalyst system, diethyl aluminum hydride, dipropyl aluminum hydride, di-n-butyl ethyl aluminum hydride, diisobutyl aluminum hydride, diphenyl aluminum hydride, etc. can be mentioned.
В качестве хлорсодержащего соединения вышеуказанной каталитической системы можно упомянуть хлорид алкилалюминия. В особенности, можно упомянуть галогенид диалкилалюминия, такой как хлорид диалкилалюминия, бромид диалкилалюминия или им подобные, полуторный галогенид алкилалюминия, такой как полуторный хлорид алкилалюминия, полуторный бромид алкилалюминия или им подобные, дигалогенид алкилалюминия, такой как дихлорид алкилалюминия, дибромид алкилалюминя или им подобные, и т.д. В качестве конкретных соединений можно упомянуть монохлорид диэтилалюминия, монобромид диэтилалюминия, монохлорид дибутилалюминия, полуторахлорид этилалюминия, дихлорид этилалюминия, монохлорид дихлоргексилалюминия, монохлорид дифенилалюминия и т.д.As the chlorine-containing compound of the above catalyst system, mention may be made of alkyl aluminum chloride. In particular, mention may be made of a dialkylaluminum halide such as dialkylaluminum chloride, dialkylaluminum bromide or the like, one-and-a-half alkylaluminum halide, one-and-a-half alkylaluminum chloride or the like, an alkylaluminum dihalide, such as etc. As specific compounds, diethylaluminum monochloride, diethylaluminum monobromide, dibutylaluminum monochloride, ethylaluminum sesquichloride, ethylaluminum dichloride, dichlorohexylaluminum monochloride, diphenylaluminum monochloride, etc. can be mentioned.
Предпочтительно, чтобы относительные содержания индивидуальных компонентов вышеуказанной каталитической системы были такими, как приведено ниже:It is preferred that the relative contents of the individual components of the above catalyst system are as follows:
(соединение, представляющее собой гидрид алкилалюминия): (соединение металла 3-й группы Периодической таблицы) = от 1:1 до 100:1 (мольное соотношение);(compound representing alkyl aluminum hydride): (metal compound of the 3rd group of the Periodic Table) = from 1: 1 to 100: 1 (molar ratio);
(бутадиен):(соединение металла 3-й группы Периодической таблицы) = от 0,5:1 до 200:1 (мольное соотношение);(butadiene) :( metal compound of the 3rd group of the Periodic table) = from 0.5: 1 to 200: 1 (molar ratio);
(метилалюмоксан):(соединение металла 3-й группы Периодической таблицы) = от 1:1 до 1000:1 (мольное соотношение);(methylaluminoxane) :( metal compound of the 3rd group of the Periodic table) = from 1: 1 to 1000: 1 (molar ratio);
(хлорсодержащее соединение):(соединение металла 3-й группы Периодической таблицы) = от 1:1 до 10:1 (мольное соотношение).(chlorine-containing compound) :( metal compound of the 3rd group of the Periodic table) = from 1: 1 to 10: 1 (molar ratio).
Предпочтительно, чтобы вышеуказанную каталитическую систему использовали после выдержки. Желательно, чтобы время выдержки составляло от 1 минуты до 150 минут. Предпочтительно, чтобы температура выдержки находилась в диапазоне от - 10°С до 60°С.Preferably, the above catalyst system is used after exposure. It is desirable that the exposure time was from 1 minute to 150 minutes. Preferably, the holding temperature is in the range from −10 ° C. to 60 ° C.
В качестве второго катализатора цис-1,4-полимеризации можно использовать катализатор, полученный из (а) комплексного соединения переходного металла металлоценового типа и (b) ионного соединения, образованного не образующими координационные связи анионом и катионом и/или алюмоксана, или катализатор, полученный из (а) комплексного соединения переходного металла металлоценового типа, (b) ионного соединения, образованного не образующими координационные связи анионом и катионом, (c) металлоорганического соединения элемента с 1-й по 3-ю группы Периодической таблицы и (d) воды [(c)/(d) = от 0,65 до 5 (мольное соотношение)].As a second cis-1,4 polymerization catalyst, a catalyst obtained from (a) a metallocene-type transition metal complex compound and (b) an ionic compound formed by non-coordinating anion and cation and / or alumoxane compounds, or a catalyst prepared from (a) a complex compound of a transition metal of a metallocene type, (b) an ionic compound formed by anion and cation not forming coordination bonds, (c) an organometallic compound of an element of groups 1 through 3 of Pe the periodic table and (d) water [(c) / (d) = 0.65 to 5 (molar ratio)].
В качестве комплексного соединения переходного металла металлоценового типа, который представляет собой компонент (а), можно упомянуть комплекс соединения переходного металла групп с 4-й по 8-ю Периодической таблицы металлоценового типа.As the complex compound of the transition metal of the metallocene type, which is component (a), we can mention the complex of the compound of the transition metal of groups 4 through 8 of the Periodic table of the metallocene type.
Можно упомянуть, например, комплекс переходного металла 4-ой группы Периодической таблицы, такого как титан или цирконий, металлоценового типа (например, CpTiCl3), комплекс переходного металла 5-ой группы Периодической таблицы, такого как ванадий, ниобий или тантал, металлоценового типа, комплекс переходного металла 6-ой группы Периодической таблицы, такого как хром, металлоценового типа, а также комплекс переходного металла 8-ой группы Периодической таблицы, такого как кобальт или никель, металлоценового типа.Mention may be made, for example, of a transition metal complex of the 4th group of the Periodic Table, such as titanium or zirconium, of a metallocene type (e.g. CpTiCl 3 ), of a transition metal complex of the 5th group of the Periodic Table, such as vanadium, niobium or tantalum, of a metallocene type , a transition metal complex of the 6th group of the Periodic table, such as chromium, metallocene type, as well as a transition metal complex of the 8th group of the Periodic table, such as cobalt or nickel, metallocene type.
Среди них предпочтительно используют комплекс переходного металла 5-ой группы Периодической таблицы металлоценового типа.Among them, a transition metal complex of the 5th group of the metallocene type periodic table is preferably used.
В качестве комплекса переходного металла 5-й группы Периодической таблицы металлоценового типа можно упомянуть соединения с нижеследующими общими формулами:As a transition metal complex of the 5th group of the periodic table of the metallocene type, mention may be made of compounds with the following general formulas:
(1) RM·La (1) RM · L a
(2) RnMX2-n·La (2) R n MX 2-nL L a
(3) RnMX3-n·La (3) R n MX 3-nL L a
(4) RMX3·La (4) RMX 3 · L a
(5) RM(O)X2·La (5) RM (O) X 2 · L a
(6) RnMX3-n(NR')La (6) R n MX 3-n (NR ') L a
(где n равно 1 или 2, и а равно 0, 1 или 2).(where n is 1 or 2, and a is 0, 1 or 2).
Среди них можно предпочтительно упомянуть RM·La, RMX3·La, RM(O)X2·La и т.д.Among them, it is preferable to mention RM · L a , RMX 3 · L a , RM (O) X 2 · L a , etc.
Желательно, чтобы М являлось соединением переходного металла 5-й группы Периодической таблицы. В частности, М представляет собой ванадий (V), ниобий (Nb) или тантал (Та), причем ванадий является предпочтительным.Preferably, M is a transition metal compound of the 5th group of the Periodic Table. In particular, M is vanadium (V), niobium (Nb) or tantalum (Ta), with vanadium being preferred.
Группа R представляет собой циклопентадиенильную группу, замещенную циклопентадиенильную группу, инденильную группу, замещенную инденильную группу, флуоренильную группу или замещенную флуоренильную группу.The R group is a cyclopentadienyl group, a substituted cyclopentadienyl group, an indenyl group, a substituted indenyl group, a fluorenyl group or a substituted fluorenyl group.
В качестве заместителя в замещенной циклопентадиенильной группе, замещенной инденильной группе или замещенной флуоренильной группе можно, например, упомянуть неразветвленные или разветвленные алифатические углеводородные группы, такие как метильная, этильная, пропильная, изопропильная, н-бутильная, изобутильная, втор-бутильная, трет-бутильная, гексильная и им подобные, ароматические углеводородные группы, такие как фенильная, толильная, нафтильная, бензильная и им подобные, а также содержащие атом кремния углеводородные группы, такие как триметилсилильная и ей подобные. Кроме того, в число таких групп включают группы, в которых циклопентадиенильное кольцо связано с группой Х посредством связующей группировки, такой как диметилсилильная, диметилметиленовая, метилфенилметиленовая, дифенилметиленовая, этиленовая, замещенная этиленовая и им подобные.As a substituent in a substituted cyclopentadienyl group, a substituted indenyl group or a substituted fluorenyl group, for example, straight or branched aliphatic hydrocarbon groups such as methyl, ethyl, propyl, isopropyl, n-butyl, isobutyl, sec-butyl, tert-butyl can be mentioned , hexyl and the like, aromatic hydrocarbon groups such as phenyl, tolyl, naphthyl, benzyl and the like, as well as silicon atoms containing hydrocarbon groups, such like trimethylsilyl and the like. In addition, such groups include groups in which the cyclopentadienyl ring is bonded to group X via a linking group such as dimethylsilyl, dimethylmethylene, methylphenylmethylene, diphenylmethylene, ethylene, substituted ethylene and the like.
В качестве конкретных примеров замещенной циклопентадиенильной группы можно упомянуть метилциклопентадиенильную группу, 1,2-диметилциклопентадиенильную группу, 1,3-диметилциклопентадиенильную группу, 1,3-ди(трет-бутил)циклопентадиенильную группу и 1,2,3-триметилциклопентадиенильную группу.As specific examples of the substituted cyclopentadienyl group, mention may be made of a methylcyclopentadienyl group, a 1,2-dimethylcyclopentadienyl group, a 1,3-dimethylcyclopentadienyl group, a 1,3-di (tert-butyl) cyclopentadienyl group, and a 1,2,3-trimethylcyclopentadienyl group.
Группа Х представляет собой атом водорода, атом галогена, углеводородную группу с числом атомов углерода от 1 до 20, алкоксигруппу или аминогруппу. Все группы Х могут быть одинаковыми или отличаться друг от друга.Group X represents a hydrogen atom, a halogen atom, a hydrocarbon group with the number of carbon atoms from 1 to 20, an alkoxy group or an amino group. All groups X may be the same or different from each other.
В качестве группы Х предпочтительными являются атом водорода, атом фтора, атом хлора, атом брома, метильная, этильная, бутильная, метокси-, этокси-, диметиламино-, диэтиламино- и т.д.As a group X, a hydrogen atom, a fluorine atom, a chlorine atom, a bromine atom, methyl, ethyl, butyl, methoxy, ethoxy, dimethylamino, diethylamino, etc. are preferred.
Соединение L представляет собой основание Льюиса и является обычным неорганическим или органическим соединением типа основания Льюиса, которое может образовывать координационную связь с металлом. Особенно предпочтительным является соединение, не обладающее активным атомом водорода. В качестве конкретных примеров можно упомянуть простой эфир, сложный эфир, кетон, амин, фосфин, силилоксисоединение, олефин, диен, ароматическое соединение, а также алкин.Compound L is a Lewis base and is a common inorganic or organic compound such as a Lewis base that can form a coordination bond with a metal. Particularly preferred is a compound that does not have an active hydrogen atom. As specific examples, mention may be made of ether, ester, ketone, amine, phosphine, silyloxy compound, olefin, diene, aromatic compound, as well as alkine.
NR' представляет собой имидную группу. R' является углеводородной группой с числом атомов углерода от 1 до 25.NR 'is an imide group. R 'is a hydrocarbon group with the number of carbon atoms from 1 to 25.
В качестве компонента (а), то есть комплексного соединения переходного металла 5-ой группы Периодической таблицы металлоценового типа, предпочтительным является тот, в котором М является ванадием, то есть соединение ванадия. Например, желательными являются соединения RV·La, RVX·La, R2V·La, RVX2·La, R2VX·La, RVX3·La и RV(O)X2·La. Соединения RV·La и RVX3·La особенно предпочтительны.As component (a), i.e. a complex compound of a transition metal of the 5th group of the periodic table of the metallocene type, it is preferable in which M is vanadium, that is, a vanadium compound. For example, RV · L a , RVX · L a , R 2 V · L a , RVX 2 · L a , R 2 VX · L a , RVX 3 · L a and RV (O) X 2 · L a are desirable . Compounds RV · L a and RVX 3 · L a are particularly preferred.
В качестве RМ·La, то есть соединения переходного металла 5-ой группы Периодической таблицы со степенью окисления +1 с одной циклоалкадиенильной группой в качестве лиганда, можно упомянуть циклопентадиенил(бензол)ванадия, циклопентадиенил(толуол)ванадия, циклопентадиенил(ксилол)ванадия, циклопентадиенил(триметилбензол)ванадия, циклопентадиенил(гексаметилбензол)ванадия, циклопентадиенил(ферроцен)ванадия, метилциклопентадиенил(бензол)ванадия и т.д.As RM · L a , i.e., compounds of a transition metal of the 5th group of the Periodic Table with an oxidation state of +1 with one cycloalkadienyl group as a ligand, mention may be made of cyclopentadienyl (benzene) vanadium, cyclopentadienyl (toluene) vanadium, cyclopentadienyl (xylene) vanadium , cyclopentadienyl (trimethylbenzene) vanadium, cyclopentadienyl (hexamethylbenzene) vanadium, cyclopentadienyl (ferrocene) vanadium, methylcyclopentadienyl (benzene) vanadium, etc.
Соединение, представленное формулой RnMX2-n·La, где n равно 1, то есть данное соединение обладает одной циклоалкадиенильной группой в качестве лиганда, может включать в качестве других лигандов лиганд, образующий σ-связь, атом водорода, атом галогена, такой как атом хлора, атом брома, атом йода или им подобные, углеводородную группу, такую как метильная группа, фенильная группа, бензильная группа, неопентильная группа, триметилсилильная группа, бистриметилсилилметильная группа или им подобные, углеводородоксигруппу, такую как метоксигруппа, этоксигруппа, изопропоксигруппа или им подобные, а также углеводородаминогруппу, такую как диметиламиногруппа, диэтиламиногруппа, диизопропиламиногруппа, диоктиламиногруппа или им подобные.The compound represented by the formula R n MX 2-n · L a , where n is 1, that is, this compound has one cycloalkadienyl group as a ligand, may include, as other ligands, a ligand forming a σ-bond, a hydrogen atom, a halogen atom, such as a chlorine atom, a bromine atom, an iodine atom or the like, a hydrocarbon group such as a methyl group, a phenyl group, a benzyl group, a nonopentyl group, a trimethylsilyl group, a bistrimethylsilylmethyl group or the like, a hydrocarbonoxy group such as a methoxy group , an ethoxy group, an isopropoxy group or the like, and a hydrocarbonamino group such as a dimethylamino group, a diethylamino group, a diisopropylamino group, a dioctylamino group or the like.
Кроме того, в качестве другого лиганда соединение может включать не обладающее зарядом основание Льюиса, такое как амин, амид, фосфин, простой эфир, кетон, сложный эфир, олефин, диен, ароматический углеводород, алкин или им подобные. Основание Льюиса, которое не содержит активный атом водорода, является предпочтительным.In addition, as another ligand, the compound may include a non-charge Lewis base such as an amine, amide, phosphine, ether, ketone, ester, olefin, diene, aromatic hydrocarbon, alkine or the like. A Lewis base that does not contain an active hydrogen atom is preferred.
Соединение, представленное формулой RnMX2-n·La, где n равно 2, то есть данное соединение обладает двумя циклоалкадиенильными группами в качестве лиганда, включает те соединения, в которых два циклоалкадиенильных кольца связаны друг с другом через мостиковую группировку, такую как Me2Si-группа, диметилэтиленовая группа, метилфенилметиленовая группа, дифенилметиленовая группа, этиленовая группа, замещенная этиленовая группа или им подобные.The compound represented by the formula R n MX 2-n · L a , where n is 2, that is, this compound has two cycloalkadienyl groups as a ligand, includes those compounds in which two cycloalkadienyl rings are linked to each other via a bridging group, such as Me 2 Si group, dimethylethylene group, methylphenylmethylene group, diphenylmethylene group, ethylene group, substituted ethylene group or the like.
В качестве конкретных примеров соединения, представленного формулой RnMX2-n·La, в котором n=1, то есть соединения переходного металла 5-ой группы Периодической таблицы со степенью окисления +2 с одной циклоалкадиенильной группой в качестве лиганда, можно упомянуть хлорциклопентадиенил(тетрагидрофуран)ванадия, хлорциклопентадиенил(триметилфосфин)ванадия и хлорциклопентадиенилбис(триметилфосфин)ванадия.As specific examples of the compound represented by the formula R n MX 2-n · L a in which n = 1, that is, a transition metal compound of the 5th group of the Periodic table with an oxidation state of +2 with one cycloalkadienyl group as a ligand, mention may be made of Chlorocyclopentadienyl (tetrahydrofuran) vanadium, Chlorocyclopentadienyl (trimethylphosphine) vanadium and Chlorocyclopentadienylbis (trimethylphosphine) vanadium.
В качестве конкретных примеров соединения, представленного формулой RnMX2-n·La, в котором n=2, то есть соединения переходного металла 5-ой группы Периодической таблицы со степенью окисления +2 с двумя циклоалкадиенильными группами в качестве лиганда, можно упомянуть бисциклопентадиенилванадия, бис(метилциклопентадиенил)ванадия, бис(1,2-диметилциклопентадиенил)ванадия и бис(1,3-диметилциклопентадиенил)ванадия.As specific examples of the compound represented by the formula R n MX 2-n · L a in which n = 2, that is, a transition metal compound of the 5th group of the Periodic table with an oxidation state of +2 with two cycloalkadienyl groups as a ligand, mention may be made of biscyclopentadienyl vanadium, bis (methylcyclopentadienyl) vanadium, bis (1,2-dimethylcyclopentadienyl) vanadium and bis (1,3-dimethylcyclopentadienyl) vanadium.
В качестве конкретных примеров соединения, представленного формулой RnMX3-n·La, в котором n=1, можно упомянуть дихлорид циклопентадиенилванадия, дихлорид метилциклопентадиенилванадия, дихлорид(1,3-диметилциклопентадиенил)ванадия и дихлорид(1-бутил-3-метилциклопентадиенил)ванадия. В качестве конкретных примеров соединения, представленного формулой RnMX3-n·La, в котором n=2, можно упомянуть хлорид дициклопентадиенилванадия и хлорид бис(метилциклопентадиенил)ванадия.As specific examples of the compound represented by the formula R n MX 3-n · L a , in which n = 1, mention may be made of cyclopentadienyl vanadium dichloride, methyl cyclopentadienyl vanadium dichloride, (1,3-dimethyl cyclopentadienyl) vanadium dichloride and (1-butyl-3- dichloride methylcyclopentadienyl) vanadium. As specific examples of the compound represented by the formula R n MX 3-n · L a , in which n = 2, mention may be made of dicyclopentadienyl vanadium chloride and bis (methylcyclopentadienyl) vanadium chloride.
В качестве конкретных примеров соединения, представленного формулой RMX3, можно упомянуть нижеследующие соединения.As specific examples of the compound represented by the formula RMX 3 , the following compounds may be mentioned.
(i) Можно упомянуть трихлорид циклопентадиенилванадия. Можно упомянуть однозамещенные трихлориды циклопентадиенилванадия, например трихлорид метилциклопентадиенилванадия, трихлорид этилциклопентадиенилванадия и трихлорид пропилциклопентадиенилванадия.(i) Mention may be made of cyclopentadienyl vanadium trichloride. Mention may be made of monosubstituted cyclopentadienyl vanadium trichlorides, for example methyl cyclopentadienyl vanadium trichloride, ethyl cyclopentadienyl vanadium trichloride and propyl cyclopentadienyl vanadium trichloride.
(ii) Можно упомянуть трихлориды 1,2-двухзамещенного циклопентадиенилванадия, например трихлорид(1,2-диметилциклопентадиенил)ванадия, трихлорид(1-этил-2-метилциклопентадиенил)ванадия, трихлорид(1-метил-2-пропилциклопентадиенил)ванадия, трихлорид(1-бутил-2-метилциклопентадиенил)ванадия и трихлорид(1-метил-2-бис(триметилсилил)метилциклопентадиенил)ванадия.(ii) Mention may be made of 1,2-dibasic cyclopentadienyl vanadium trichlorides, for example (1,2-dimethylcyclopentadienyl) vanadium trichloride, (1-ethyl-2-methylcyclopentadienyl) vanadium trichloride, (1-methyl-2-propylcyclopentadienyl) vanadium trichloride 1-butyl-2-methylcyclopentadienyl) vanadium and (1-methyl-2-bis (trimethylsilyl) methylcyclopentadienyl) vanadium trichloride.
(iii) Можно упомянуть трихлориды 1,2,3-трехзамещенного циклопентадиенилванадия, например трихлорид(1,2,3-триметилциклопентадиенил)ванадия.(iii) Mention may be made of 1,2,3-trisubstituted cyclopentadienyl vanadium trichlorides, for example (1,2,3-trimethylcyclopentadienyl) vanadium trichloride.
В качестве конкретных примеров соединения, представленного формулой RM(O)X2, можно упомянуть дихлорид циклопентадиенилоксованадия и дихлорид метилциклопентадиенилоксованадия. Помимо этого можно упомянуть метилзамещенные соединения, получаемые замещением атома хлора в каждом из вышеуказанных соединений на метильную группу.As specific examples of the compound represented by the formula RM (O) X 2 , mention may be made of cyclopentadieniloxovanadium dichloride and methylcyclopentadieniloxovanadium dichloride. In addition, methyl substituted compounds obtained by replacing the chlorine atom in each of the above compounds with a methyl group can be mentioned.
Можно упомянуть диметоксид циклопентадиенилоксованадия, диизопропоксид циклопентадиенилоксованадия, ди-трет-бутоксид циклопентадиенилоксованадия, дифеноксид циклопентадиенилоксованадия, метоксихлорид циклопентадиенилоксованадия, изопропоксихлорид циклопентадиенилоксованадия, трет-бутоксихлорид циклопентадиенилоксованадия, феноксихлорид циклопентадиенилоксованадия и т.д. Помимо этого можно упомянуть метилзамещенные соединения, получаемые замещением атома хлора в каждом из вышеупомянутых соединений на метильную группу.Mention may be made of cyclopentadienyl oxovanadium dimethoxide, cyclopentadienyl oxovanadium diisopropoxide, cyclopentadienyl oxovanadium di-tert-butoxide, cyclopentadienyl oxovanadium diphenoxide, cyclopentadieniloxovanadium methoxychloride cyclopentadienyl oxo-phenyl butadiene-phenyl butadiene-phenyl butadiene-phenyl butadiene-phenyl butadiene-phenyl butadiene-phenyl butadiene-phenyl butadiene-phenyl-butoxy-phenyl-butadiene-phenyl-butoxy-phenyl-butyl-cyclo-cyclo-pentadienyl-phenyl-cyclo-cyclo-pentadienyl-cyclo-cyclohexylanediophenyl-cycloheated In addition, methyl substituted compounds obtained by replacing the chlorine atom in each of the above compounds with a methyl group can be mentioned.
В качестве конкретного примера соединения, представленного формулой RnMX3-n(NR') можно упомянуть дихлорид циклопентадиенил(метилимид)ванадия.As a specific example of the compound represented by the formula R n MX 3-n (NR ′), mention may be made of vanadium cyclopentadienyl (methylimide) dichloride.
В качестве не образующего координационные связи аниона, который входит в состав компонента (b), то есть ионного соединения, образованного не образующими координационные связи анионом и катионом, можно упомянуть, например, тетра(фенил)борат, тетра(фторфенил)борат, тетракис(дифторфенил)борат, тетракис(трифторфенил)борат, тетракис(тетрафторфенил)борат, тетракис(пентафторфенил)борат и тетракис(3,5-бистрифторметилфенил)борат.As the anion that does not form coordination bonds, which is part of component (b), i.e., the ionic compound formed by the anion and cation not forming coordination bonds, we can mention, for example, tetra (phenyl) borate, tetra (fluorophenyl) borate, tetrakis ( difluorophenyl) borate, tetrakis (trifluorophenyl) borate, tetrakis (tetrafluorophenyl) borate, tetrakis (pentafluorophenyl) borate and tetrakis (3,5-bistrifluoromethylphenyl) borate.
При этом в качестве катиона можно упомянуть катион карбония, катион оксония, катион аммония, катион фосфония, катион циклогептатриенила, содержащий атом переходного металла катион, такой как ферроцений, и т.д.Moreover, as a cation, mention may be made of a carbonium cation, an oxonium cation, an ammonium cation, a phosphonium cation, a cycloheptatrienyl cation containing a transition metal atom, a cation such as ferrocenium, etc.
В качестве конкретных примеров катиона карбония можно упомянуть трехзамещенные катионы карбония, такие как катион трифенилкарбония, катион трис(замещенный фенил)карбония и им подобные. В качестве конкретных примеров катиона трис(замещенный фенил)карбония можно упомянуть катион три(метилфенил)карбония и катион трис(диметилфенил)карбония.As specific examples of the carbonium cation, trisubstituted carbonium cations such as triphenylcarbonium cation, tris (substituted phenyl) carbonium cation and the like can be mentioned. As specific examples of the tris (substituted phenyl) carbonium cation, the tri (methylphenyl) carbonium cation and the tris (dimethylphenyl) carbonium cation may be mentioned.
В качестве конкретных примеров катиона аммония можно упомянуть катионы триалкиламмония, такие как катион триметиламмония, катион триэтиламмония, катион трипропиламмония, катион трибутиламмония, катион три-н-бутиламмония и им подобные, а также катион N,N-диметиланилиния.As specific examples of the ammonium cation, mention may be made of trialkylammonium cations such as trimethylammonium cation, triethylammonium cation, tripropylammonium cation, tributylammonium cation, tri-n-butylammonium cation and the like, as well as N, N-dimethylanilinium cation.
В качестве конкретных примеров катиона фосфония можно упомянуть катионы триарилфосфония, такие как катион трифенилфосфония, катион три(метилфенил)фосфония, катион три(диметилфенил)фосфония и им подобные.As specific examples of the phosphonium cation, triarylphosphonium cations such as triphenylphosphonium cation, tri (methylphenyl) phosphonium cation, tri (dimethylphenyl) phosphonium cation and the like can be mentioned.
Предпочтительно, чтобы в качестве ионного соединения можно было использовать любую комбинацию одного из вышеуказанных не образующих координационные связи анионов и одного из вышеуказанных катионов.Preferably, any combination of one of the above non-coordinating anions and one of the above cations can be used as the ionic compound.
Предпочтительными в качестве ионных соединений являются тетракис(пентафторфенил)борат трифенилкарбония, тетракис(фторфенил)борат трифенилкарбония, тетракис(пентафторфенил)борат N,N-диметиланилиния, тетракис(пентафторфенил)борат 1,1'-диметилферроцения и т.д.Preferred as ionic compounds are tetrakis (pentafluorophenyl) triphenylcarbonium borate, tetrakis (fluorophenyl) triphenylcarbonium borate, tetrakis (pentafluorophenyl) borate N, N-dimethylanilinium, tetrakis (pentafluorophenyl) borate 1,1'-dimerfen etc.
Ионное соединение можно использовать само по себе или в виде комбинации двух или более типов.The ionic compound can be used alone or as a combination of two or more types.
В качестве компонента (b) можно выбрать алюмоксан. Алюмоксан получают взаимодействием алюминийорганического соединения с реагентом, вызывающим конденсацию. Можно упомянуть алюмоксан линейного типа или циклический алюмоксан, оба представлены общей формулой (-Al(R')O-)n, где группа R' является углеводородной группой, имеющей от 1 до 10 атомов углерода и может являться частично замещенной атомом галогена и/или алкоксигруппой, n представляет собой степень полимеризации и составляет 5 или более, предпочтительно 10 или более. В качестве группы R' можно упомянуть метильную группу, этильную группу, пропильную группу и изобутильную группу, причем метильная группа этильная группа являются предпочтительными. В качестве алюминийорганического соединения, используемого как исходное вещество для получения алюмоксана, можно упомянуть, например, соединения триалкилалюминия, такие как триметилалюминий, триэтилалюминий, триизобутилалюминий и им подобные, а также их смеси.As component (b), alumoxane can be selected. Alumoxane is prepared by reacting an organoaluminum compound with a condensation reagent. Mention may be made of a linear type aluminoxane or cyclic aluminoxane, both represented by the general formula (-Al (R ') O-) n , where the R' group is a hydrocarbon group having from 1 to 10 carbon atoms and may be partially substituted by a halogen atom and / or alkoxygroup, n represents the degree of polymerization and is 5 or more, preferably 10 or more. As the group R ′, mention may be made of a methyl group, an ethyl group, a propyl group and an isobutyl group, with a methyl group being an ethyl group being preferred. As the organoaluminum compound used as the starting material for the production of aluminoxane, mention may be made, for example, of trialkylaluminum compounds such as trimethylaluminum, triethylaluminum, triisobutylaluminum and the like, as well as mixtures thereof.
Предпочтительно, когда можно использовать алюмоксан, полученный с использованием в качестве исходного вещества смеси триметилалюминия с трибутилалюминием.Preferably, when you can use alumoxane obtained using a mixture of trimethylaluminum with tributylaluminum as the starting material.
В отношении реагента, вызывающего конденсацию, в качестве типичного вызывающего конденсацию реагента можно упомянуть воду. Кроме того, можно упомянуть любой вызывающий конденсацию реагент, в присутствии которого триалкилалюминий может вступать в реакцию конденсации, например, адсорбированную неорганическим соединением воду и ей подобные, а также диол.With respect to a condensation inducing reagent, water may be mentioned as a typical condensation inducing reagent. In addition, any condensation-causing reagent in the presence of which trialkylaluminum can undergo a condensation reaction, for example, water and the like adsorbed by an inorganic compound, as well as a diol, can be mentioned.
В качестве компонента (c) можно вводить металлоорганическое соединение элемента группы с 1-й по 3-ю Периодической таблицы. Можно упомянуть, например, алюминийорганическое соединение, литийорганическое соединение, магнийорганическое соединение, цинкорганическое соединение и борорганическое соединение.As component (c), an organometallic compound of an element of a group from the 1st to the 3rd periodic table can be introduced. Mention may be made, for example, of an organoaluminum compound, an organolithium compound, an organomagnesium compound, an organozinc compound and an organoboron compound.
В качестве конкретных соединений можно упомянуть метиллитий, бутиллитий, фениллитий, бензиллитий, неопентиллитий, бистриметилсилилметиллитий, дибутилмагний, дигексилмагний, диэтилцинк, триметилалюминий и т.д.As specific compounds, mention may be made of methyl lithium, butyllithium, phenyl lithium, benzyl lithium, neopentyl lithium, bistrimethylsilylmethyl lithium, dibutyl magnesium, dihexyl magnesium, diethyl zinc, trimethyl aluminum, etc.
Кроме того, компонент (c) охватывает галогениды металлоорганических соединений, такие как хлорид этилмагния, хлорид бутилмагния, хлорид диметилалюминия, хлорид диэтилалюминия, хлорид полутораэтилалюминия, дихлорид этилалюминия и им подобные, гидриды металлоорганических соединений, такие как гидрид диэтилалюминия, гидрид полутораэтилалюминия и им подобные.In addition, component (c) encompasses organometallic halides such as ethylmagnesium chloride, butylmagnesium chloride, diethylaluminium chloride, diethylaluminium chloride, ethylaluminum dichloride, and the like, organometallic hydrides such as diethylaminoethyl aluminum hydrides and the like.
В качестве компонента (c) алюминийорганическое соединение, то есть металлоорганическое соединение элемента с 1-ой по 3-ю группу Периодической таблицы, является предпочтительным. Конкретные примеры алюминийорганического соединения были упомянуты выше и охватывают соединения триалкилалюминия, такие как триметилалюминий, триэтилалюминий, триизобутилалюминий и им подобные, галогениды алюминийорганических соединений, такие как хлорид диметилалюминия, хлорид диэтилалюминия, хлорид полутораэтилалюминия, дихлорид этилалюминия и им подобные, гидриды алюминийорганических соединений, такие как гидрид диэтилалюминия, гидрид полутораэтилалюминия и им подобные. Можно использовать вышеупомянутый алюмоксан. Вышеуказанное металлоорганическое соединение можно использовать в виде комбинации двух или более типов.As component (c), an organoaluminum compound, that is, an organometallic compound of an element of the 1st to 3rd group of the Periodic Table, is preferred. Specific examples of the organoaluminum compound have been mentioned above and encompass trialkylaluminum compounds such as trimethylaluminum, triethylaluminum, triisobutylaluminum and the like, organoaluminum halides such as dimethylaluminum chloride, diethylaluminium chloride, dichloride such as aluminum diethylaluminum hydride, sesquiolumine hydride and the like. The aforementioned alumoxane may be used. The above organometallic compound may be used as a combination of two or more types.
Предпочтительно, чтобы мольное отношение количества компонента (а), то есть комплекса металлоценового типа, к количеству компонента (b), то есть ионного соединения, составляло от 1:0,1 до 1:10, более желательно от 1:0,2 до 1:5.Preferably, the molar ratio of the amount of component (a), i.e. the metallocene type complex, to the amount of component (b), i.e. the ionic compound, is from 1: 0.1 to 1:10, more preferably from 1: 0.2 to 1: 5.
Предпочтительно, чтобы мольное отношение количества компонента (а), то есть комплекса металлоценового типа, к количеству компонента (c), то есть металлоорганического соединения, составляло от 1:0,1 до 1:1000, более желательно от 1:10 до 1:1000, еще более предпочтительно от 1:10 до 1:500.Preferably, the molar ratio of the amount of component (a), i.e. the metallocene type complex, to the amount of component (c), i.e. the organometallic compound, is from 1: 0.1 to 1: 1000, more preferably from 1:10 to 1: 1000, even more preferably from 1:10 to 1: 500.
Предпочтительно, чтобы к вышеупомянутым каталитическим компонентам добавляли воду в качестве компонента (d). Желательно, чтобы мольное отношение количества компонента (c), то есть металлоорганического соединения, к количеству компонента (d), то есть воды, составляло 0,66:5, более предпочтительно от 0,7 до 1,5, еще более желательно от 0,8 до 1,5.Preferably, water is added to the aforementioned catalyst components as component (d). It is desirable that the molar ratio of the amount of component (c), i.e., the organometallic compound, to the amount of component (d), i.e. water, is 0.66: 5, more preferably from 0.7 to 1.5, even more preferably from 0 , 8 to 1.5.
В отношении порядка введения вышеуказанных каталитических компонентов не существует конкретных ограничений. Однако введение можно осуществлять, например, в следующем порядке. Компонент (d) добавляют к представляющему собой сопряженное диеновое соединение мономеру, который следует полимеризовать, или к смеси этого мономера с растворителем, вводят компонент (c), затем в желаемом порядке вводят компонент (а) и компонент (b). Или иначе, компонент (d) и компонент (c) добавляют к представляющему собой сопряженное диеновое соединение мономеру, который следует полимеризовать, или к смеси этого мономера с растворителем, затем в желаемом порядке вводят компонент (а) и компонент (b).With regard to the order of introduction of the above catalyst components, there are no particular restrictions. However, the introduction can be carried out, for example, in the following order. Component (d) is added to the monomer to be polymerized, or to a mixture of this monomer with a solvent, component (c) is added, then component (a) and component (b) are introduced in the desired order. Alternatively, component (d) and component (c) are added to the monomer to be polymerized as a conjugated diene compound, or to a mixture of this monomer with a solvent, then component (a) and component (b) are introduced in the desired order.
В данном документе представляющий собой сопряженное диеновое соединение мономер, который следует полимеризовать, может составлять все количество мономера или часть такового. В том случае, когда он составляет часть мономера, вышеуказанную каталитическую смесь можно смешивать с остающимся мономером или остающимися раствором мономера.In this document, the monomer to be polymerized as a conjugated diene compound may comprise all or part of the monomer. When it forms part of the monomer, the above catalytic mixture can be mixed with the remaining monomer or the remaining monomer solution.
При полимеризации на первой стадии молекулярную массу получающегося в результате полимера контролируют, полимеризуя представляющее собой сопряженный диен соединение с применением вышеуказанного катализатора предпочтительно в присутствии водорода.In the polymerization in the first step, the molecular weight of the resulting polymer is controlled by polymerizing a conjugated diene compound using the above catalyst, preferably in the presence of hydrogen.
Предпочтительно, чтобы количество присутствующего водорода составляло 500 ммоль или менее либо 12 литров или менее при температуре 20°С и давлении 1 атмосфера на 1 моль сопряженного диена, более предпочтительно 50 ммоль или менее либо 1,2 литра или менее при температуре 20°С и давлении 1 атмосфера, еще более желательно от 0,005 ммоль до 20 ммоль либо от 0,00001 до 0,48 литра при температуре 20°С и давлении 1 атмосфера. Или иначе, водород можно вводить в полимеризационный реактор непрерывно.Preferably, the amount of hydrogen present is 500 mmol or less or 12 liters or less at a temperature of 20 ° C and a pressure of 1 atmosphere per 1 mol of conjugated diene, more preferably 50 mmol or less or 1.2 liters or less at a temperature of 20 ° C and a pressure of 1 atmosphere, even more preferably from 0.005 mmol to 20 mmol or from 0.00001 to 0.48 liters at a temperature of 20 ° C and a pressure of 1 atmosphere. Or else, hydrogen can be introduced continuously into the polymerization reactor.
Предпочтительно, чтобы температура полимеризации составляла от -100 до 120°С, особенно желательно от -50 до 100°С. Продолжительность полимеризации составляет от 10 минут до 12 часов, особенно предпочтительно от 30 минут до 6 часов. Для дополнительного подавления гелеобразования в ходе полимеризации можно использовать известный ингибитор гелеобразования.Preferably, the polymerization temperature is from -100 to 120 ° C., Particularly preferably from -50 to 100 ° C. The duration of the polymerization is from 10 minutes to 12 hours, particularly preferably from 30 minutes to 6 hours. To further inhibit gelling during polymerization, a known gelling inhibitor can be used.
Использование второй каталитической системы позволяет получать полибутадиен с характеристической вязкостью от 0,1 до 20, измеряемой при температуре 30°С в толуоле. В этом случае можно получить матричный полибутадиен, который обладает средневесовой молекулярной массой от 10000 до 4000000, определяемой с помощью метода гель-проникающей хроматографии с использованием полистирола в качестве вещества-стандарта, и вязкостью по Муни (ML1+4, 100°С, здесь и далее обозначаемой как ML) от 10 до 130, предпочтительно от 15 до 80, и который не обладает значительным содержанием гелеобразной фракции.Using the second catalytic system allows to obtain polybutadiene with a characteristic viscosity of from 0.1 to 20, measured at a temperature of 30 ° C in toluene. In this case, it is possible to obtain matrix polybutadiene, which has a weight average molecular weight of 10,000 to 4,000,000, determined by gel permeation chromatography using polystyrene as a standard substance, and a Mooney viscosity (ML1 + 4, 100 ° C, here and hereinafter referred to as ML) from 10 to 130, preferably from 15 to 80, and which does not have a significant gel fraction.
В качестве третьего катализатора цис-1,4-полимеризации можно использовать катализатор, полученный из (А) соединения иттрия, (В) ионного соединения, образованного не образующими координационные связи анионом и катионом и (В) металлоорганического соединения элемента, выбираемого из 2-ой группы, 12-й группы и 13-й группы Периодической таблицы.As the third cis-1,4 polymerization catalyst, a catalyst obtained from (A) yttrium compounds, (B) an ionic compound formed by non-coordinating anion and cation compounds, and (B) an organometallic compound of an element selected from the 2nd can be used group, 12th group and 13th group of the Periodic table.
Предпочтительно, чтобы в качестве компонента (А), то есть соединения иттрия вышеуказанной каталитической системы, использовали соль иттрия или комплекс иттрия. В качестве особенно предпочтительных соединений можно упомянуть соли иттрия, такие как трихлорид иттрия, трибромид иттрия, трийодид иттрия, нитрат иттрия, сульфат иттрия, трифторметансульфонат иттрия, ацетат иттрия, трифторацетат иттрия, малонат иттрия, октилат (этилгексаноат) иттрия, нафтенат иттрия, Версатат иттрия, неодеканоат иттрия и им подобные, алкоксиды, такие как триметоксид иттрия, триэтоксид иттрия, триизопропоксид иттрия, трибутоксид иттрия, трифеноксид иттрия и им подобные, иттрийорганические соединения, такие как трисацетилацетанатоиттрий, трис(гександионато)иттрий, трис(гептандионато)иттрий, трис(диметилгептандионато)иттрий, трис(тетраметилгептандионато)иттрий, трисацетоацетатоиттрий, дихлорид циклопентадиенилиттрия, хлорид дициклопентадиенилиттрия, трициклопентадиенил иттрия и им подобные, комплексы органических оснований, такие как пиридиниевый комплекс иттриевой соли, пиколиновый комплекс иттриевой соли и им подобные, гидраты иттриевых солей, спиртовые комплексы иттриевых солей и т.д.Preferably, as component (A), i.e., a yttrium compound of the above catalyst system, a yttrium salt or a yttrium complex is used. Particularly preferred compounds include yttrium salts such as yttrium trichloride, yttrium tribromide, yttrium triiodide, yttrium nitrate, yttrium sulfate, yttrium trifluoromethanesulfonate, yttrium acetate, yttrium trifluoroacetate, yttrium malonate, yttrium nitrate, yttrium, yttrium neodecanoate and the like, alkoxides such as yttrium trimethoxide, yttrium triethoxide, yttrium triisopropoxide, yttrium tributoxide, yttrium triphenoxide and the like, organo yttrium compounds lacetanatoyttrium, tris (hexanedionato) yttrium, tris (heptanedionato) yttrium, tris (dimethylheptanedionato) yttrium, tris (tetramethylheptanedionato) yttrium, trisacetoacetatoitrium, dichloride dichloride, cyclotentadienyltrityl dichloride , the picolinic complex of yttrium salt and the like, yttrium salt hydrates, alcohol complexes of yttrium salts, etc.
Кроме того, можно использовать нижеследующее соединение иттрия.In addition, the following yttrium compound may be used.
[Формула 2][Formula 2]
(В вышеуказанной формуле каждая из групп R1, R2 и R3 является атомом водорода или углеводородной группой с числом атомов углерода от 1 до 12, О представляет собой атом кислорода, а Y является атомом иттрия.)(In the above formula, each of the groups R 1 , R 2, and R 3 is a hydrogen atom or a hydrocarbon group with the number of carbon atoms from 1 to 12, O represents an oxygen atom, and Y represents a yttrium atom.)
В качестве конкретных примеров групп R1, R2 и R3 можно упомянуть атом водорода, метильную группу, этильную группу, винильную группу, н-пропильную группу, изопропильную группу, 1-пропенильную группу, аллильную группу, н-бутильную группу, втор-бутильную группу, изобутильную группу, трет-бутильную группу, н-пентильную группу, 1-метилбутильную группу, 2-метилбутильную группу, 3-метилбутильную группу, 1,1-диметилпропильную группу, 1,2-диметилпропильную группу, 2,2-диметилпропильную группу, гексильную группу, гептильную группу, октильную группу, нонильную группу, децильную группу, ундецильную группу, додецильную группу, циклогексильную группу, метилциклогексильную группу, этилциклогексильную группу, фенильную группу, бензильную группу, толуильную группу и этоксифенильную группу. Кроме того, включают те группы, в которых любая из вышеупомянутых групп является замещенной в любом положении гидроксильной группой, карбоксильной группой, карбометоксигруппой, карбоэтоксигруппой, амидной группой, аминогруппой, алкоксигруппой, феноксигруппой или им подобными.As specific examples of the groups R 1 , R 2 and R 3 , mention may be made of a hydrogen atom, methyl group, ethyl group, vinyl group, n-propyl group, isopropyl group, 1-propenyl group, allyl group, n-butyl group, sec- butyl group, isobutyl group, tert-butyl group, n-pentyl group, 1-methylbutyl group, 2-methylbutyl group, 3-methylbutyl group, 1,1-dimethylpropyl group, 1,2-dimethylpropyl group, 2,2-dimethylpropyl group, hexyl group, heptyl group, octyl group, nonyl th group, decyl group, undecyl group, dodecyl group, cyclohexyl group, methylcyclohexyl group, ethylcyclohexyl group, phenyl group, benzyl group, toluilnuyu group and ethoxyphenyl group. In addition, those groups are included in which any of the above groups is substituted at any position by a hydroxyl group, a carboxy group, a carbomethoxy group, a carbethoxy group, an amide group, an amino group, an alkoxy group, a phenoxy group or the like.
Предпочтительно, чтобы в качестве соединения иттрия использовали соль иттрия или комплекс иттрия. Особенно предпочтительными соединениями иттрия являются трис(ацетилацетонато)иттрий, трис(гександионато)иттрий, трис(гептандионато)иттрий, трис(диметилгептандионато)иттрий, трис(триметилгептандионато)иттрий, трис(тетраметилгептандионато)иттрий, трис(пентаметилгептандионато)иттрий, трис(гексаметилгептандионато)иттрий, трисацетоацетатоиттрий и т.д.Preferably, the yttrium salt or yttrium complex is used as the yttrium compound. Particularly preferred yttrium compounds are tris (acetylacetonato) yttrium, tris (hexanedionato) yttrium, tris (heptanedionato) yttrium, tris (dimethylheptanedionato) yttrium, tris (trimethylheptanedionato) yttrium, tris (tetramethylheptanedtanthanthato ) yttrium, trisacetoaceto-yttrium, etc.
В компоненте (В) вышеуказанной каталитической системы, то есть ионном соединении между не образующим координационные связи анионом и катионом, в качестве не образующего координационные связи аниона можно упомянуть, например, тетра(фенил)борат, тетра(фторфенил)борат, тетракис(дифторфенил)борат, тетракис(трифторфенил)борат, тетракис(тетрафторфенил)борат, тетракис(пентафторфенил)борат, тетракис(3,5-бистрифторметилфенил)борат, тетракис(тетрафторметилфенил)борат, тетра(толуил)борат, тетра(ксилил)борат, трифенил(пентафторфенил)борат, трис(пентафторфенил)(фенил)борат, тридекагидрид-7,8-дикарбундекаборат, тетрафторборат и гексафторфосфат.In component (B) of the aforementioned catalyst system, i.e., the ionic compound between a non-coordination bond anion and a cation, mention may be made, for example, of a tetra (phenyl) borate, tetra (fluorophenyl) borate, tetrakis (difluorophenyl) borate, tetrakis (trifluorophenyl) borate, tetrakis (tetrafluorophenyl) borate, tetrakis (pentafluorophenyl) borate, tetrakis (3,5-bistrifluoromethylphenyl) borate, tetrakis (tetrafluoromethylphenyl) borate, tetra (toluyl tetra boron, borate, borate pentafluorophenyl) borate, tris (ne taftorfenil) (phenyl) borate, tridekagidrid-7,8-dikarbundekaborat, tetrafluoroborate and hexafluorophosphate.
Помимо этого в качестве катиона можно упомянуть катион карбония, катион оксония, катион аммония, катион фосфония, катион циклогептатриенила, катион ферроцения и т.д.In addition, the cation can include carbonium cation, oxonium cation, ammonium cation, phosphonium cation, cycloheptatrienyl cation, ferrocenium cation, etc.
В качестве конкретных примеров катиона карбония можно упомянуть трехзамещенные катионы карбония, такие как катион трифенилкарбония, катион три(замещенный фенил)карбония и им подобные. В качестве конкретных примеров катиона три(замещенный фенил)карбония можно упомянуть катион три(метилфенил)карбония и катион три(диметилфенил)карбония.As specific examples of the carbonium cation, trisubstituted carbonium cations such as triphenylcarbonium cation, tri (substituted phenyl) carbonium cation and the like can be mentioned. As specific examples of a tri (substituted phenyl) carbonium cation, a tri (methylphenyl) carbonium cation and a tri (dimethylphenyl) carbonium cation may be mentioned.
В качестве конкретных примеров катиона аммония можно упомянуть катионы триалкиламмония, такие как катион триметиламмония, катион триэтиламмония, катион трипропиламмония, катион трибутиламмония, катион три(н-бутил)аммония и им подобные, катионы N,N-диалкиланилиния, такие как катион N,N-диметиланилиния, катион N,N-диэтиланилиния, катион N,N-2,4,6-пентаметиланилиния и им подобные, а также катионы диалкиламмония, такие как катион ди(изопропил)аммония и ему подобные.As specific examples of the ammonium cation, mention may be made of trialkylammonium cations such as trimethylammonium cation, triethylammonium cation, tripropylammonium cation, tributylammonium cation, tri (n-butyl) ammonium cation and the like, N, N-dialkylanilinium cations, such as N cation, dimethylanilinium, an N, N-diethylanilinium cation, an N, N-2,4,6-pentamethylanilinium cation and the like, and dialkylammonium cations such as di (isopropyl) ammonium cation and the like.
В качестве конкретных примеров катиона фосфония можно упомянуть катионы арилфосфония, такие как катион трифенилфосфония, катион тетрафенилфосфония, катион три(метилфенил)фосфония, катион тетра(метилфенил)фосфония, катион три(диметилфенил)фосфония, катион тетра(диметилфенил)фосфония и им подобные.As specific examples of the phosphonium cation, mention may be made of arylphosphonium cations, such as triphenylphosphonium cation, tetraphenylphosphonium cation, tri (methylphenyl) phosphonium cation, tetra (methylphenyl) phosphonium cation, tri (dimethylphenyl) phosphonium cation, tetra (im) phenylphosphonium.
Предпочтительно, чтобы в качестве ионного соединения можно было использовать любую комбинацию одного из вышеуказанных не образующих координационные связи анионов и одного из вышеуказанных катионов.Preferably, any combination of one of the above non-coordinating anions and one of the above cations can be used as the ionic compound.
В качестве ионного соединения предпочтительными являются тетракис(пентафторфенил)борат трифенилкарбония, тетракис(фторфенил)борат трифенилкарбония, тетракис(пентафторфенил)борат N,N-диметиланилиния, тетракис(пентафторфенил)борат 1,1'-диметилферроцения и т.д. Ионное соединение можно использовать само по себе либо в виде комбинации двух или более типов.As the ionic compound, tetrakis (pentafluorophenyl) triphenylcarbonium borate, tetrakis (fluorophenyl) triphenylcarbonium borate, tetrakis (pentafluorophenyl) borate N, N-dimethylanilinium, tetrakis (pentafluorophenyl) borate 1,1'-dimerfer etc. are preferred. The ionic compound can be used alone or as a combination of two or more types.
В качестве компонента (В) можно выбрать алюмоксан. Алюмоксан получают взаимодействием алюминийорганического соединения с реагентом, вызывающим конденсацию. Можно упомянуть алюмоксан линейного типа и циклический алюмоксан, оба представлены общей формулой (-Al(R')O-)n, где группа R' является углеводородной группой, имеющей от 1 до 10 атомов углерода и может являться частично замещенной атомом галогена и/или алкоксигруппой, n представляет собой степень полимеризации и составляет 5 или более, предпочтительно 10 или более. В качестве группы R' можно упомянуть метильную группу, этильную группу, пропильную группу и изобутильную группу, причем метильная группа является предпочтительной. В качестве алюминийорганического соединения, используемого как исходное вещество для получения алюмоксана, можно упомянуть, например, соединения триалкилалюминия, такие как триметилалюминий, триэтилалюминий, триизобутилалюминий и им подобные, а также их смеси.As component (B), alumoxane can be selected. Alumoxane is prepared by reacting an organoaluminum compound with a condensation reagent. Mention may be made of the linear type aluminoxane and cyclic aluminoxane, both represented by the general formula (-Al (R ') O-) n , where the R' group is a hydrocarbon group having from 1 to 10 carbon atoms and may be partially substituted by a halogen atom and / or alkoxygroup, n represents the degree of polymerization and is 5 or more, preferably 10 or more. As the group R ′, mention may be made of a methyl group, an ethyl group, a propyl group and an isobutyl group, with a methyl group being preferred. As the organoaluminum compound used as the starting material for the production of aluminoxane, mention may be made, for example, of trialkylaluminum compounds such as trimethylaluminum, triethylaluminum, triisobutylaluminum and the like, as well as mixtures thereof.
Предпочтительно, когда можно использовать алюмоксан, полученный с использованием как исходного вещества смеси триметилалюминия с трибутилалюминием.Preferably, when aluminoxane obtained using a mixture of trimethylaluminum with tributylaluminum as the starting material can be used.
Что касается вызывающего конденсацию реагента, в качестве типичного реагента, вызывающего конденсацию, можно упомянуть воду. Кроме того, можно упомянуть любой реагент, вызывающий конденсацию, в присутствии которого триалкилалюминий может вступать в реакцию конденсации, например, адсорбированную неорганическим соединением воду и ей подобные, а также диол.As for the condensation causing reagent, water may be mentioned as a typical condensation causing reagent. In addition, any condensation-causing reagent in the presence of which trialkylaluminum can undergo a condensation reaction, for example, water and the like adsorbed by an inorganic compound, as well as a diol, can be mentioned.
В качестве компонента (В) вышеуказанной каталитической системы, то есть металлоорганического соединения элемента 2-й, 12-й или 13-й групп Периодической таблицы, можно использовать, например, магнийорганическое, цинкорганическое или алюминийорганическое соединение. Среди этих соединений диалкилмагний, хлорид алкилмагния, бромид алкилмагния, диалкилцинк, триалкилалюминий, хлорид диалкилалюминия, бромид диалкилалюминия, полуторахлорид алкилалюминия, полуторабромид алкилалюминия, дихлорид алкилалюминия, гидрид диалкилалюминия и т.д. являются предпочтительными.As component (B) of the above catalytic system, i.e., an organometallic compound of an element of the 2nd, 12th or 13th groups of the Periodic Table, for example, an organomagnesium, organozinc or organoaluminum compound can be used. Among these compounds are dialkyl magnesium, alkyl magnesium chloride, alkyl magnesium bromide, dialkyl zinc, trialkyl aluminum, dialkyl aluminum chloride, dialkyl aluminum bromide, alkyl aluminum sesquichloride, alkyl aluminum sesquichromide, alkyl aluminum dichloride, dialkyl hydride etc. are preferred.
В качестве конкретных соединений можно упомянуть галогениды алкилмагния, такие как хлорид метилмагния, хлорид этилмагния, хлорид бутилмагния, хлорид гексилмагния, хлорид октилмагния, бромид этилмагния, бромид бутилмагния, йодид бутилмагния, йодид гексилмагния и им подобные.As specific compounds, alkyl magnesium halides such as methyl magnesium chloride, ethyl magnesium chloride, butyl magnesium chloride, hexyl magnesium chloride, octyl magnesium chloride, ethyl magnesium bromide, butyl magnesium bromide, butyl magnesium iodide and hexyl iodide can be mentioned.
Кроме того, можно упомянуть соединения диалкилмагния, такие как диметилмагний, диэтилмагний, дибутилмагний, дигексилмагний, диоктилмагний, этилбутилмагний, этилгексилмагний и им подобные.In addition, dialkyl magnesium compounds such as dimethyl magnesium, diethyl magnesium, dibutyl magnesium, dihexyl magnesium, dioctyl magnesium, ethyl butyl magnesium, ethyl hexyl magnesium and the like can be mentioned.
Кроме того, можно упомянуть соединения диалкилцинка, такие как диметилцинк, диэтилцинк, диизобутилцинк, дигексилцинк, диоктилцинк, дидецилцинк и им подобные.In addition, dialkylzinc compounds such as dimethylzinc, diethylzinc, diisobutylzinc, dihexylzinc, dioctylzinc, didecylzinc and the like can be mentioned.
Кроме того, можно упомянуть соединения триалкилалюминия, такие как триметилалюминий, триэтилалюминий, триизобутилалюминий, тригексилалюминий, триоктилалюминий, тридецилалюминий и им подобные.In addition, trialkylaluminum compounds such as trimethylaluminum, triethylaluminum, triisobutylaluminum, trihexylaluminum, trioctylaluminum, tridecylaluminum and the like can be mentioned.
Кроме того, можно упомянуть галогениды алюминийорганических соединений, такие как хлориды диалкилалюминия, такие как хлорид диметилалюминия или хлорид диэтилалюминия, полуторахлорид этилалюминия, дихлорид этилалюминия и им подобные, гидриды алюминийорганических соединений, такие как гидрид диэтилалюминия, гидрид диизобутилалюминия, полуторагидрид этилалюминия и им подобные.In addition, mention may be made of organoaluminum halides, such as dialkylaluminum chlorides, such as dimethylaluminum chloride or diethylaluminum chloride, ethylaluminum sesquichloride, ethylaluminum dichloride and the like, organoaluminum hydrides such as diethylaluminium aluminum hydride, diisobutyl hydride and diisobutyl hydride.
Такие металлоорганические соединения элементов 2-й, 12-й и 13-й группы Периодической таблицы можно использовать сами по себе или в виде комбинации двух или более типов.Such organometallic compounds of elements of the 2nd, 12th and 13th groups of the Periodic Table can be used on their own or as a combination of two or more types.
При третьем способе в качестве регулятора молекулярной массы получаемого полибутадиена можно использовать соединение, выбираемое из (1) водорода, (2) соединения, представляющего собой гидрид металла, и (3) гидрида металлоорганического соединения.In the third method, as a molecular weight regulator of the obtained polybutadiene, a compound selected from (1) hydrogen, (2) a metal hydride compound, and (3) an organometallic hydride can be used.
В качестве представляющего собой гидрид металла соединения (2), используемого в качестве регулятора молекулярной массы, можно упомянуть гидрид лития, гидрид натрия, гидрид калия, гидрид магния, гидрид кальция, гидрид бора, гидрид алюминия, гидрид галлия, гидрид германия, литийборгидрид, натрийборгидрид, литийалюминийгидрид, натрийалюминийгидрид и т.д.As the metal hydride of compound (2) used as a molecular weight regulator, mention may be made of lithium hydride, sodium hydride, potassium hydride, magnesium hydride, calcium hydride, boron hydride, aluminum hydride, gallium hydride, germanium hydride, lithium borohydride, sodium borohydride lithium aluminum hydride, sodium aluminum hydride, etc.
В качестве гидрида металлоорганического соединения (3), используемого в качестве регулятора молекулярной массы, можно упомянуть, например, алкилбораны, такие как метилборан, этилборан, пропилборан, бутилборан, фенилборан и им подобные, диалкилбораны, такие как диметилборан, диэтилборан, дипропилборан, дибутилборан, дифенилборан и им подобные, дигидриды алкилалюминия, такие как дигидрид метилалюминия, дигидрид этилалюминия, дигидрид пропилалюминия, дигидрид бутилалюминия, дигидрид фенилалюминия и им подобные, гидриды диалкилалюминия, такие как гидрид диметилалюминия, гидрид диэтилалюминия, гидрид дипропилалюминия, гидрид дибутилалюминия, гидрид дифенилалюминия и им подобные, силаны, такие как метилсилан, этилсилан, пропилсилан, бутилсилан, фенилсилан, диметилсилан, диэтилсилан, дипропилсилан, дибутилсилан, дифенилсилан, триметилсилан, триэтилсилан, трипропилсилан, трибутилсилан, трифенилсилан и им подобные, а также германы, такие как метилгерман, этилгерман, пропилгерман, бутилгерман, фенилгерман, диметилгерман, диэтилгерман, дипропилгерман, дибутилгерман, дифенилгерман, триметилгерман, триэтилгерман, трипропилгерман, трибутилгерман, трифенилгерман и им подобные.As the hydride of the organometallic compound (3) used as a molecular weight regulator, mention may be made, for example, of alkyl borans such as methyl borane, ethyl borane, propyl borane, butyl borane, phenyl borane and the like, dialkyl boranes such as dimethyl borane, diethyl borane, dipropyl borane, dibutyl borane diphenylborane and the like, alkylaluminum dihydrides such as methylaluminum dihydride, ethylaluminum dihydride, propylaluminum dihydride, butylaluminum dihydride, phenylaluminum dihydride and the like, dialkylaluminum hydrides, and such as dimethylaluminum hydride, diethylaluminum hydride, dipropylaluminum hydride, dibutylaluminum hydride, diphenylaluminum hydride and the like, silanes such as methylsilane, ethylsilane, propylsilane, butylsilane, phenylsilane sillyl, diphenylsilane, dimethylsilane, diphenyl, silane, tri tributylsilane, triphenylsilane and the like, as well as germans such as methylgerman, ethylgerman, propylgerman, butylgerman, phenylgerman, dimethylgerman, diethylgerman, dipropylgerman, dibutylgerman, diphenylge Man, trimetilgerman, trietilgerman, tripropilgerman, tributilgerman, trifenilgerman and the like.
Среди них гидрид диизобутилалюминия и гидрид диэтилалюминия являются предпочтительными, а особенно желательным является гидрид диэтилалюминия.Among them, diisobutylaluminum hydride and diethylaluminum hydride are preferred, and diethylaluminum hydride is particularly desirable.
В отношении порядка введения каталитических компонентов не существует конкретных ограничений, однако введение можно осуществлять согласно нижеследующему порядку.With respect to the order of introduction of the catalytic components, there are no particular restrictions, however, the introduction can be carried out according to the following order.
(1) Компонент (В) вводят в инертном органическом растворителе при отсутствии или в присутствии бутадиенового мономера, который следует полимеризовать, а компонент (А) и компонент (В) вводят в любом желаемом порядке.(1) Component (B) is introduced in an inert organic solvent in the absence or presence of butadiene monomer to be polymerized, and component (A) and component (B) are introduced in any desired order.
(2) Компонент (В) вводят в инертном органическом растворителе при отсутствии или в присутствии бутадиенового мономера, который следует полимеризовать, добавляют вышеуказанный регулятор молекулярной массы, а затем вводят в любом желаемом порядке компонент (А) и компонент (В).(2) Component (B) is introduced in an inert organic solvent in the absence or presence of a butadiene monomer to be polymerized, the above molecular weight regulator is added, and then component (A) and component (B) are added in any desired order.
(3) Компонент (А) вводят в инертном органическом растворителе при отсутствии или в присутствии бутадиенового мономера, который следует полимеризовать, компонент (В) и вышеуказанный регулятор молекулярной массы добавляют в любом желаемом порядке, а затем вводят компонент (В).(3) Component (A) is introduced in an inert organic solvent in the absence or presence of the butadiene monomer to be polymerized, component (B) and the above molecular weight regulator are added in any desired order, and then component (B) is introduced.
(4) Компонент (В) вводят в инертном органическом растворителе при отсутствии или в присутствии бутадиенового мономера, который следует полимеризовать, компонент (В) и вышеуказанный регулятор молекулярной массы добавляют в любом желаемом порядке, а затем вводят компонент (А).(4) Component (B) is introduced in an inert organic solvent in the absence or presence of the butadiene monomer to be polymerized, component (B) and the above molecular weight regulator are added in any desired order, and then component (A) is introduced.
(5) Компонент (В) вводят в инертном органическом растворителе при отсутствии или в присутствии бутадиенового мономера, который следует полимеризовать, компонент (А) и компонент (В) добавляют в любом желаемом порядке, а затем вводят вышеуказанный регулятор молекулярной массы.(5) Component (B) is introduced in an inert organic solvent in the absence or presence of the butadiene monomer to be polymerized, component (A) and component (B) are added in any desired order, and then the above molecular weight regulator is introduced.
Перед использованием индивидуальные компоненты можно подвергать выдержке. В частности, предпочтительно, чтобы компонент (А) и компонент (В) подвергали выдержке.Before use, individual components can be aged. In particular, it is preferred that component (A) and component (B) be aged.
Что касается условий выдержки, то компонент (А) и компонент (В) смешивают в инертном растворителе в присутствии или при отсутствии бутадиенового мономера, который следует полимеризовать. Температура выдержки составляет от -50 до 80°С, предпочтительно от -10 до 50°С, а продолжительность выдержки составляет от 0,01 часа до 24 часов, желательно от 0,05 часа до 5 часов, особенно предпочтительно от 0,1 часа до 1 часа.Regarding the exposure conditions, component (A) and component (B) are mixed in an inert solvent in the presence or absence of butadiene monomer to be polymerized. The holding temperature is from -50 to 80 ° C, preferably from -10 to 50 ° C, and the holding time is from 0.01 hours to 24 hours, preferably from 0.05 hours to 5 hours, particularly preferably from 0.1 hour up to 1 hour.
В настоящем изобретении индивидуальные каталитические компоненты можно применять, помещая их на неорганическое соединение или органическое полимерное соединение.In the present invention, individual catalytic components can be used by placing them on an inorganic compound or an organic polymer compound.
При производстве полибутадиена с использованием первого или также второго катализатора можно использовать известный регулятор молекулярной массы, например водород, несопряженный диен, такой как циклооктадиен или аллен, или α-олефин, такой как этилен, пропилен или бутен-1.In the manufacture of polybutadiene using the first or second catalyst, a known molecular weight regulator, for example hydrogen, a non-conjugated diene, such as cyclooctadiene or allen, or an α-olefin, such as ethylene, propylene or butene-1, can be used.
При полимеризации полибутадиена с использованием первого катализатора предпочтительно, чтобы температура полимеризации составляла от -30 до 100°С, особенно желательно от 30 до 80ºС. Предпочтительно, чтобы продолжительность полимеризации составляла от 10 минут до 12 часов, особенно желательно от 30 минут до 6 часов. Полимеризацию проводят при нормальном давлении или при повышенном давлении примерно вплоть до 10 атмосфер (избыточное давление). Предпочтительно, когда цис-1,4-полимеризацию проводят так, чтобы концентрация полимера после цис-1,4-полимеризации составляла от 5 до 26 мас.%. Что касается полимеризационного реактора, то используют одиночный реактор либо два или более соединенных реактора. Полимеризацию проводят, перемешивая раствор в полимеризационном реакторе (полимеризационной установке). В качестве полимеризационного реактора можно использовать полимеризационный реактор с устройством для перемешивания раствора высокой вязкости, например установку, описанную в JP-B-1965-2645.In the polymerization of polybutadiene using the first catalyst, it is preferable that the polymerization temperature is from -30 to 100 ° C, particularly preferably from 30 to 80 ° C. Preferably, the polymerization time is from 10 minutes to 12 hours, particularly preferably from 30 minutes to 6 hours. The polymerization is carried out at normal pressure or at elevated pressure up to about 10 atmospheres (gauge pressure). Preferably, the cis-1,4 polymerization is carried out so that the polymer concentration after cis-1,4 polymerization is from 5 to 26% by weight. As for the polymerization reactor, a single reactor or two or more connected reactors is used. The polymerization is carried out by mixing the solution in a polymerization reactor (polymerization unit). As the polymerization reactor, you can use a polymerization reactor with a device for mixing a solution of high viscosity, for example, the installation described in JP-B-1965-2645.
Для дополнительного подавления гелеобразования в ходе полимеризации можно использовать известный ингибитор гелеобразования. Полученный полибутадиен обычно обладает содержанием цис-1,4-звеньев 90% или более, в частности 95% или более, вязкостью по Муни (ML1+4, 100°C, здесь и далее в данном документе обозначаемой как ML) от 10 до 130, предпочтительно от 15 до 80, и, по существу, не содержит гелеобразной фракции.To further inhibit gelling during polymerization, a known gelling inhibitor can be used. The obtained polybutadiene usually has a cis-1,4-unit content of 90% or more, in particular 95% or more, Mooney viscosity (ML1 + 4, 100 ° C, hereinafter referred to as ML) from 10 to 130 , preferably from 15 to 80, and essentially does not contain a gel fraction.
1,3-Бутадиен можно вводить в полученную, как указано выше, реакционную смесь для цис-1,4-полимеризации или его можно не вводить в нее. После этого в этой полимеризационной системе проводят синдиотактическую 1,2-полимеризацию.1,3-Butadiene can be added to the cis-1,4-polymerization reaction mixture obtained as described above, or it can be omitted. After that, syndiotactic 1,2-polymerization is carried out in this polymerization system.
Что касается способа полимеризации с применением третьего катализатора, то в отношении его также не существует конкретных ограничений. Можно проводить полимеризацию в массе, используя в качестве растворителя для полимеризации 1,3-бутадиен сам по себе, полимеризацию в растворе и т.д. В качестве растворителя при проведении полимеризации в растворе можно упомянуть алифатические углеводороды, такие как бутан, пентан, гексан, гептан и им подобные, алициклические углеводороды, такие как циклопентан, циклогексан и им подобные, ароматические углеводороды, такие как бензол, толуол, ксилол, этилбензол и им подобные, олефиновые углеводороды, такие как вышеупомянутые олефиновые соединения, цис-2-бутен, транс-2-бутен и им подобные, и так далее.As for the polymerization process using a third catalyst, there are also no particular restrictions on it. It is possible to carry out bulk polymerization using 1,3-butadiene per se as a solvent for polymerization, solution polymerization, etc. As a solvent in the polymerization in solution, mention may be made of aliphatic hydrocarbons such as butane, pentane, hexane, heptane and the like, alicyclic hydrocarbons such as cyclopentane, cyclohexane and the like, aromatic hydrocarbons such as benzene, toluene, xylene, ethylbenzene and the like, olefinic hydrocarbons such as the aforementioned olefinic compounds, cis-2-butene, trans-2-butene and the like, and so on.
Среди них предпочтительно используемыми являются бензол, толуол, циклогексан, смесь цис-2-бутена с транс-2-бутеном и т.д.Among them, benzene, toluene, cyclohexane, a mixture of cis-2-butene with trans-2-butene, etc., are preferably used.
Предпочтительно, чтобы температура полимеризации составляла от -30 до 150°С, особенно желательно от 30 до 100°С. Предпочтительно, чтобы продолжительность полимеризации составляла от 1 минуты до 12 часов, особенно желательно от 5 минут до 5 часов.Preferably, the polymerization temperature is from -30 to 150 ° C., Particularly preferably from 30 to 100 ° C. Preferably, the polymerization time is from 1 minute to 12 hours, particularly preferably from 5 minutes to 5 hours.
После проведения полимеризации в течение заданного промежутка времени внутреннее давление в полимеризационном реакторе сбрасывают по мере необходимости и осуществляют действия по пост-обработке, такие как промывание, сушка и им подобные.After the polymerization is carried out for a predetermined period of time, the internal pressure in the polymerization reactor is relieved as necessary and post-processing actions such as washing, drying and the like are carried out.
В качестве получаемого таким способом полибутадиена можно упомянуть цис-1,4-полибутадиен с содержанием цис-1,4-звеньев желательно 90% или выше, более предпочтительно 92% или выше, особенно желательно 96% или выше. Величину [η] полимера на основе сопряженного диена можно регулировать до значения предпочтительно от 0,1 до 10, более желательно от 1 до 7, особенно предпочтительно от 1,5 до 5.As the polybutadiene obtained in this way, cis-1,4-polybutadiene with a content of cis-1,4-units, preferably 90% or higher, more preferably 92% or higher, especially 96% or higher, can be mentioned. The value [η] of the conjugated diene polymer can be adjusted to a value of preferably from 0.1 to 10, more preferably from 1 to 7, particularly preferably from 1.5 to 5.
Желательно, когда цис-1,4-полимеризацию проводят так, чтобы концентрация полимера после осуществления цис-1,4-полимеризации составляла от 5 до 26 мас.%. Что касается полимеризационного реактора, то используют одиночный реактор либо два или более соединенных реактора. Полимеризацию проводят, перемешивая раствор в полимеризационном реакторе (полимеризационной установке). В качестве полимеризационного реактора можно использовать полимеризационный реактор с устройством для перемешивания раствора высокой вязкостью, например установку, описанную в патенте JP-B-1965-2645.Preferably, when the cis-1,4 polymerization is carried out so that the polymer concentration after the cis-1,4 polymerization is carried out is from 5 to 26% by weight. As for the polymerization reactor, a single reactor or two or more connected reactors is used. The polymerization is carried out by mixing the solution in a polymerization reactor (polymerization unit). As the polymerization reactor, you can use a polymerization reactor with a device for mixing a solution of high viscosity, for example, the installation described in patent JP-B-1965-2645.
Для дополнительного подавления гелеобразования в ходе полимеризации можно использовать известный ингибитор гелеобразования. Обычно полученный полибутадиен обладает содержанием цис-1,4-звеньев 90% или более, в частности 95% или более, и вязкостью по Муни (ML) от 10 до 130, желательно от 15 до 80, и предпочтительно, по существу, не содержит гелеобразной фракции.To further inhibit gelling during polymerization, a known gelling inhibitor can be used. Typically, the resulting polybutadiene has a cis-1,4-unit content of 90% or more, in particular 95% or more, and a Mooney viscosity (ML) of 10 to 130, preferably 15 to 80, and preferably substantially free gel fraction.
В качестве катализатора синдиотактической 1,2-полимеризации можно использовать каталитическую систему, включающую соединение триалкилалюминия с формулой R1 3Al (для которого группа R1 является углеводородной группой, имеющей от 1 до 10 атомов углерода), соединение серы и, при необходимости, соединение кобальта.As a syndiotactic 1,2-polymerization catalyst, a catalytic system comprising a trialkylaluminum compound of the formula R 1 3 Al (for which the R 1 group is a hydrocarbon group having from 1 to 10 carbon atoms), a sulfur compound and, if necessary, a compound can be used cobalt.
В качестве соединения серы можно упомянуть дисульфид углерода, фенилизотиоцианат, соединение ксантогеновой кислоты и т.д. Среди них дисульфид углерода является предпочтительным. В качестве соединения триалкилалюминия с формулой R1 3Al (для которого группа R1 является углеводородной группой, имеющей от 1 до 10 атомов углерода) и соединения кобальта можно упомянуть вышеупомянутые соединения, используемые при цис-1,4-полимеризации.As the sulfur compound, carbon disulfide, phenyl isothiocyanate, xanthogen acid compound, etc. can be mentioned. Among them, carbon disulfide is preferred. As the trialkylaluminum compound of the formula R 1 3 Al (for which the R 1 group is a hydrocarbon group having from 1 to 10 carbon atoms) and cobalt compounds, the aforementioned compounds used in cis-1,4 polymerization can be mentioned.
Соединение триалкилалюминия используют в количестве 0,1 ммоль или более, в частности от 0,5 ммоль до 50 ммоль или более, на 1 моль 1,3-бутадиена. В отношении соединения серы не существует конкретных ограничений, но предпочтительно, чтобы оно не содержало воды. Концентрация соединения серы составляет 20 ммоль/л или менее, особенно предпочтительно, когда она находится в диапазоне от 0,01 до 10 ммоль/л.The trialkylaluminum compound is used in an amount of 0.1 mmol or more, in particular from 0.5 mmol to 50 mmol or more, per 1 mol of 1,3-butadiene. There are no particular restrictions on the sulfur compound, but it is preferred that it does not contain water. The concentration of the sulfur compound is 20 mmol / L or less, particularly preferably when it is in the range of 0.01 to 10 mmol / L.
Температура 1,2-полимеризации 1,3-бутадиена составляет от 0°С до 100°С, предпочтительно, чтобы она находилась в диапазоне от 10 до 100°С, более желательно от 20 до 100°С. В полимеризационную систему, в которой следует проводить 1,2-полимеризацию, 1,3-бутадиен можно вводить в количестве от 1 весовой части до 50 масссовых частей, предпочтительно от 1 массовой части до 20 массовых частей, на 100 массовых частей смеси, в которой провoдят цис-полимеризацию, обуславливая тем самым возможность повышения выхода 1,2-полибутадиена в ходе 1,2-полимеризации. Предпочтительно, чтобы продолжительность полимеризации (среднее время пребывания) составляла от 10 минут до 2 часов. Желательно, когда 1,2-полимеризацию проводят так, чтобы концентрация полимера после осуществления 1,2-полимеризации составляла от 9 до 29 мас.%. Что касается полимеризационного реактора, то используют одиночный реактор либо два или более соединенных реактора. Полимеризацию проводят, перемешивая полимеризационный раствор в полимеризационном реакторе (полимеризационная установка). В качестве полимеризационного реактора, используемого для осуществления 1,2-полимеризации, можно использовать полимеризационный реактор с устройством для перемешивания раствора высокой вязкости, например, установку, описанную в патенте JP-B-1965-2645, поскольку вязкость раствора в ходе 1,2-полимеризации становится более высокой и проявляется тенденция полимера к адгезии.The 1,2-polymerization temperature of 1,3-butadiene is from 0 ° C to 100 ° C, preferably it is in the range from 10 to 100 ° C, more preferably from 20 to 100 ° C. In the polymerization system in which 1,2-polymerization is to be carried out, 1,3-butadiene can be introduced in an amount of from 1 weight part to 50 mass parts, preferably from 1 mass part to 20 mass parts, per 100 mass parts of a mixture in which cis polymerization is carried out, thereby causing the possibility of increasing the yield of 1,2-polybutadiene during 1,2-polymerization. Preferably, the polymerization time (average residence time) is from 10 minutes to 2 hours. Preferably, when the 1,2-polymerization is carried out so that the concentration of the polymer after the 1,2-polymerization is from 9 to 29 wt.%. As for the polymerization reactor, a single reactor or two or more connected reactors is used. The polymerization is carried out by mixing the polymerization solution in a polymerization reactor (polymerization unit). As the polymerization reactor used for the implementation of 1,2-polymerization, you can use a polymerization reactor with a device for mixing a solution of high viscosity, for example, the installation described in patent JP-B-1965-2645, since the viscosity of the solution during 1.2- polymerization becomes higher and the polymer shows a tendency to adhesion.
Когда в ходе реакции полимеризации достигают желаемой конверсии, для прекращения полимеризации вводят вышеупомянутую галогенсодержащую кислоту или соль галогенсодержащей кислоты. Предпочтительно, чтобы галогенсодержащую кислоту или соль галогенсодержащей кислоты водили в виде раствора, особенно водного раствора или спиртового раствора, такого как метанольного или этанольного раствора. Кроме того, для улучшения степени диспергирования в полимерном растворе можно допустить присутствие поверхностно-активного вещества.When the desired conversion is achieved during the polymerization reaction, the aforementioned halogen-containing acid or a salt of the halogen-containing acid is introduced to terminate the polymerization. Preferably, the halogen-containing acid or salt of the halogen-containing acid is administered as a solution, especially an aqueous solution or an alcohol solution, such as a methanol or ethanol solution. In addition, to improve the degree of dispersion in the polymer solution, the presence of a surfactant can be allowed.
Количество вводимой галогенсодержащей кислоты или соли галогенсодержащей кислоты составляет от 0,001 моль до 10 моль, предпочтительно от 0,002 моль до 5 моль, более желательно от 0,005 моль до 2 моль, на 1 моль соединения серы. Продолжительность смешения после введения составляет от 5 секунд до 1 часа, предпочтительно от 10 секунд до 30 минут, более желательно от 20 секунд до 10 минут.The amount of halogen-containing acid or salt of halogen-containing acid added is from 0.001 mol to 10 mol, preferably from 0.002 mol to 5 mol, more preferably from 0.005 mol to 2 mol, per 1 mol of sulfur compound. The duration of mixing after administration is from 5 seconds to 1 hour, preferably from 10 seconds to 30 minutes, more preferably from 20 seconds to 10 minutes.
Кроме того, можно вводить известный антиоксидант согласно обычному способу. В качестве антиоксиданта можно упомянуть 2,6-ди-трет-бутил-пара-крезол (ВНТ) как соединение фенольного типа, тринонилфенилфосфит (TNP) как соединение фосфорсодержащего типа, дилаурил-3,3'-тиодипропионат (TPL) как соединение серосодержащего типа и т.д. Антиоксидант можно использовать индивидуально или в виде комбинации двух или более типов. Количество вводимого антиоксиданта составляет от 0,001 весовой части до 5 весовых частей на 100 весовых частей полимера VCR. Затем в полимеризационную систему для прекращения полимеризации вводят реагент, тормозящий реакцию. Введение осуществляют согласно самому по себе известному способу, например способу подачи полимеризационного раствора в реактор для прекращения полимеризации после проведения реакции полимеризации и введения туда большого количества полярного растворителя, такого как спирт, например метанол или этанол, вода или им подобные, либо способу введения в полимеризационный раствор неорганической кислоты, такой как соляная кислота или серная кислота, органической кислоты, такой как уксусная кислота или бензойная кислота, или газообразного хлороводорода. Затем образовавшийся полимер VCR отделяют, промывают и сушат согласно обычным способам.In addition, a known antioxidant may be administered according to a conventional method. As an antioxidant, mention may be made of 2,6-di-tert-butyl-para-cresol (BHT) as a phenolic compound, trinonyl phenyl phosphite (TNP) as a phosphorus-containing compound, dilauryl-3,3'-thiodipropionate (TPL) as a sulfur-containing compound etc. An antioxidant can be used individually or as a combination of two or more types. The amount of antioxidant administered is from 0.001 parts by weight to 5 parts by weight per 100 parts by weight of VCR polymer. Then, a reagent inhibiting the reaction is introduced into the polymerization system to stop the polymerization. The introduction is carried out according to a known method per se, for example, a method for feeding a polymerization solution into a reactor to terminate the polymerization after the polymerization reaction is carried out and a large amount of a polar solvent is introduced therein, such as alcohol, for example methanol or ethanol, water or the like, or a method for introducing into the polymerization a solution of an inorganic acid such as hydrochloric acid or sulfuric acid, an organic acid such as acetic acid or benzoic acid, or gaseous x orovodoroda. The resulting VCR polymer is then separated, washed and dried according to conventional methods.
В данном случае, когда до отделения и проведения очистки галогенсодержащая кислота или соль галогенсодержащей кислоты остается в реакционной системе, остающуюся галогенсодержащую кислоту или соль галогенсодержащей кислоты деактивируют взаимодействием с водным раствором, содержащим восстанавливающий реагент, такой как сернистая кислота, соль сернистой кислоты, соль тиосерной кислоты, соль азотистой кислоты, щавелевую кислоту, соль щавелевой кислоты и им подобные. Тем самым можно предотвратить окисление полученного полимера VCR.In this case, when a halogen-containing acid or a salt of a halogen-containing acid remains in the reaction system before separation and purification, the remaining halogen-containing acid or a salt of a halogen-containing acid is deactivated by interaction with an aqueous solution containing a reducing reagent, such as sulfurous acid, a sulfuric acid salt, a thiosulfuric acid salt , a salt of nitrous acid, oxalic acid, a salt of oxalic acid and the like. Thereby, oxidation of the obtained VCR polymer can be prevented.
Для предотвращения окисления остающейся галогенсодержащей кислотой или солью галогенсодержащей кислоты полимер VCR можно предохранить от окисления также введением эффективного вспомогательного реагента, например, вспомогательного реагента (например, антиоксиданта), обычно добавляемого к резиновой композиции. В качестве антиоксиданта можно использовать известный антиоксидант, такой как стерически экранированный фенол или ему подобные.To prevent oxidation by the remaining halogen-containing acid or halogen-containing acid salt, the VCR polymer can also be protected from oxidation by the addition of an effective auxiliary reagent, for example, an auxiliary reagent (e.g., an antioxidant), typically added to the rubber composition. As an antioxidant, a known antioxidant such as sterically shielded phenol or the like can be used.
Таким способом полученный полимер VCR содержит (1) от 3 до 30 мас.% нерастворимого в кипящем н-гексане вещества (H.I.) и (2) от 97 до 70 мас.% растворимого в кипящем н-гексане вещества. Растворимое в кипящем н-гексане вещество представляет собой цис-1,4-полибутадиен с микроструктурой, характеризующейся содержанием цис-1,4-звеньев 80% или более. Вещество H.I. представляет собой синдиотактический 1,2-полибутадиен (SPBD) с температурой плавления, находящейся в диапазоне от 180 до 215°С. Полимер VCR обладает значением ML, находящимся в диапазоне от 20 до 150, предпочтительно от 25 до 100, при температуре 100°С. В полимере VCR синдиотактический 1,2-полибутадиен однородно диспергирован в матрице цис-1,4-полибутадиена в виде тонкодисперсных кристаллов. Полимер VCR обладает слабым запахом по сравнению с традиционными полимерами VCR.In this way, the obtained VCR polymer contains (1) from 3 to 30 wt.% Insoluble in boiling n-hexane substance (H.I.) and (2) from 97 to 70 wt.% Soluble in boiling n-hexane. The soluble substance in boiling n-hexane is cis-1,4-polybutadiene with a microstructure characterized by a content of cis-1,4-units of 80% or more. Substance H.I. is a syndiotactic 1,2-polybutadiene (SPBD) with a melting point in the range from 180 to 215 ° C. The VCR polymer has an ML value ranging from 20 to 150, preferably from 25 to 100, at a temperature of 100 ° C. In the VCR polymer, the syndiotactic 1,2-polybutadiene is uniformly dispersed in the cis-1,4-polybutadiene matrix in the form of fine crystals. VCR polymer has a low odor compared to traditional VCR polymers.
Полимер VCR, полученный по настоящему изобретению, компаундируют отдельно или смешением с другим синтетическим каучуком или природным каучуком, при необходимости наполняют технологическим маслом, затем смешивают с наполнителем (например, углеродной сажей), сшивающим реагентом, ускорителем вулканизации и другими обычными компаундирующими реагентами и вулканизируют. Получающийся в результате продукт используют в применениях, связанных с каучуками, при которых требуются необходимые механические свойства и сопротивление истиранию, таких как те, которые связаны с производством шин (например, при производстве протекторов, боковых стенок, элементов жесткости, бортовых прокладок, внутренней футеровки и каркасов) и разнообразных других промышленных продуктов (например, шлангов и ремней). Полимер VCR можно также использовать в качестве модификатора для пластиков.The VCR polymer obtained according to the present invention is separately compounded or mixed with another synthetic rubber or natural rubber, filled with process oil if necessary, then mixed with a filler (e.g. carbon black), a crosslinking agent, a vulcanization accelerator and other conventional compounding agents and vulcanized. The resulting product is used in rubbers-related applications that require the necessary mechanical properties and abrasion resistance, such as those associated with tire manufacturing (for example, in the manufacture of treads, side walls, stiffeners, side gaskets, inner lining and frames) and various other industrial products (e.g. hoses and belts). VCR can also be used as a modifier for plastics.
ПРИМЕРЫEXAMPLES
В нижеследующих примерах и сравнительных примерах измерения для каждого бутадиенового каучука проводили согласно нижеприведенным пунктам как указано ниже.In the following examples and comparative examples, measurements for each butadiene rubber were performed according to the points below as follows.
Приведенная вязкость нерастворимого в н-гексане веществаReduced viscosity of n-hexane insoluble substance
25 г бутадиенового каучука помещали в 1000 мл кипящего н-гексана и смесь кипятили с обратным холодильником, в результате чего полибутадиеновый каучук разделяли на растворимое в кипящем н-гексане вещество и нерастворимое в н-гексане вещество. 0,2 г нерастворимого в кипящем н-гексане вещества растворяли в 100 мл тетралина и измеряли вязкость раствора при температуре 130°С, используя вискозиметр Уббелоде.25 g of butadiene rubber were placed in 1000 ml of boiling n-hexane and the mixture was heated to reflux, whereby the polybutadiene rubber was separated into a substance soluble in boiling n-hexane and insoluble in n-hexane. 0.2 g of a substance insoluble in boiling n-hexane was dissolved in 100 ml of tetralin, and the viscosity of the solution was measured at a temperature of 130 ° C using a Ubbelode viscometer.
Температура плавления нерастворимого в н-гексане веществаMelting point of n-hexane insoluble substance
Определяли по эндотермической кривой, полученной методом дифференциальной сканирующей калориметрии.It was determined by the endothermic curve obtained by differential scanning calorimetry.
Определение средневесовой молекулярной массы растворимого в н-гексане веществаDetermination of the weight average molecular weight of a substance soluble in n-hexane
25 г полибутадиенового каучука помещали в 1000 мл кипящего н-гексана и смесь кипятили с обратным холодильником. Нерастворимое в кипящем н-гексане вещество отделяли фильтрованием для выделения раствора н-гексана. н-Гексан удаляли из раствора н-гексана для получения растворимого в н-гексане вещества. Растворимое в н-гексане вещество растворяли в тетрагидрофуране. Раствор анализировали с помощью метода гель-проникающей хроматографии для определения молекулярной массы, используя полистирол в качестве стандарта, и Mw растворимого в н-гексане вещества рассчитывали из этих данных. Измерения проводили при нижеследующих условиях.25 g of polybutadiene rubber was placed in 1000 ml of boiling n-hexane and the mixture was refluxed. The insoluble in boiling n-hexane substance was separated by filtration to isolate a solution of n-hexane. n-Hexane was removed from the n-hexane solution to obtain a substance soluble in n-hexane. A n-hexane soluble substance was dissolved in tetrahydrofuran. The solution was analyzed using gel permeation chromatography to determine molecular weight using polystyrene as a standard, and M w of a n-hexane-soluble substance was calculated from these data. The measurements were carried out under the following conditions.
Прибор: модель HLC-802A (производство фирмы Tosoh Corporation), колонки: GMH 6000, две параллельно; элюент: тетрагидрофуран; скорость потока элюента: 1,0 мл/мин; температура, при которой проводили измерение: собирательный кожух колонны 40°С, детектор 40°С; концентрация образца: 0,25 г/л, количество введенного образца: 0,5 мл.Device: model HLC-802A (manufactured by Tosoh Corporation), speakers: GMH 6000, two in parallel; eluent: tetrahydrofuran; eluent flow rate: 1.0 ml / min; temperature at which the measurement was carried out: collective casing of the column 40 ° C, detector 40 ° C; sample concentration: 0.25 g / l; amount of sample introduced: 0.5 ml.
Микроструктура растворимого в н-гексане веществаMicrostructure of a substance soluble in n-hexane
Растворимое в кипящем н-гексане вещество, полученное, как указано выше, анализировали с помощью метода инфракрасной спектроскопии, и данные о микроструктуре растворимого в кипящем н-гексане вещества получали из отношения интенсивностей полос поглощения соответствующих цис-1,4-структуре при 740 см-1, транс-1,4-структуре при 967 см-1 и 1,2-структуре (винил) при 911 см-1.The boiling n-hexane-soluble substance obtained as described above was analyzed using infrared spectroscopy, and the microstructure of the boiling n-hexane-soluble substance was obtained from the ratio of the intensities of the absorption bands of the corresponding cis-1,4 structure at 740 cm - 1 , the trans-1,4 structure at 967 cm -1 and the 1,2 structure (vinyl) at 911 cm -1 .
Вязкость раствора растворимого в н-гексане вещества в толуоле (T-cp)The viscosity of a solution of a substance soluble in n-hexane in toluene (T-cp)
Полученное, как указано выше, растворимое в кипящем н-гексане вещество растворяли в толуоле так, чтобы получить раствор с концентрацией 5 мас.%. Вязкость раствора измеряли при 25°С, используя вискозиметр Кэннон-Фенске.The soluble in boiling n-hexane obtained as described above was dissolved in toluene so as to obtain a solution with a concentration of 5 wt.%. The viscosity of the solution was measured at 25 ° C. using a Cannon-Fenske viscometer.
Вязкость по Муни растворимого в н-гексане вещества и компаундаMooney viscosity of n-hexane-soluble substance and compound
Определяли согласно методике, указанной в JIS K 6300.Determined according to the procedure specified in JIS K 6300.
Контроль остаточного запахаResidual odor control
Полученный продукт проверяли для контроля степени остаточного запаха. Кроме того, поскольку предающее запах вещество, в основном присутствует в летучих компонентах продукта, количество летучих компонентов использовали в качестве показателя, отражающего объективное знание уровня запаха. Поэтому количество летучих компонентов определяли при нижеследующих условиях. Это количество сравнивали с уровнем запаха, полученным посредством органолептического контроля, и всесторонне судили об уровне остаточного запаха. В данном случае результат измерения количества летучих компонентов выражали в виде относительного значения от количества летучих компонентов, определенного в сравнительном примере 1, которое принимали равным 100, и он показан в таблице 1, которая приведена ниже.The resulting product was checked to control the degree of residual odor. In addition, since the odor-transmitting substance is mainly present in the volatile components of the product, the amount of volatile components was used as an indicator reflecting an objective knowledge of the level of smell. Therefore, the amount of volatile components was determined under the following conditions. This amount was compared with the level of odor obtained through organoleptic control, and comprehensively judged the level of residual odor. In this case, the result of measuring the amount of volatile components was expressed as a relative value from the number of volatile components defined in comparative example 1, which was assumed to be 100, and it is shown in table 1, which is shown below.
2,5 г каучука, полученного в каждом примере, аккуратно взвешивали в 20 мл емкости для образца и нагревали при температуре 170°С в течение 30 минут. Затем с помощью газового хроматографа с пламенным фотометрическим детектором (FPD) проводили измерение, используя 1 мл парообразной фракции из емкости для образца, при нижеследующих условиях.2.5 g of rubber obtained in each example was carefully weighed in 20 ml of sample container and heated at 170 ° C. for 30 minutes. Then, using a gas chromatograph with a flame photometric detector (FPD), measurements were made using 1 ml of the vapor fraction from the sample container under the following conditions.
FPD газовый хроматограф: модель Agilent 6890FPD gas chromatograph: Agilent 6890 model
Модель колонки: HP-1, 60 м (длина)×0,32 мм (внутренний диаметр)×5,0 мкм (толщина пленки)Column model: HP-1, 60 m (length) × 0.32 mm (inner diameter) × 5.0 μm (film thickness)
Условия в колонке: выдержка при температуре 40°С в течение 5 минут, затем повышение температуры до 250°С со скоростью 15°С в минуту и, наконец, выдержка при температуре 250°С в течение 11 минутConditions in the column: holding at a temperature of 40 ° C for 5 minutes, then raising the temperature to 250 ° C at a speed of 15 ° C per minute, and finally holding at a temperature of 250 ° C for 11 minutes
Продолжительность измерения: 30 минутDuration of measurement: 30 minutes
Пример 1Example 1
Цис-1,4-полимеризацияCis-1,4 polymerization
Объем 2,0 л (объем емкости) автоклава продували азотом. В него вводили 1 л раствора (FB), состоящего из циклогексана (350 мл), цис-2-бутена (340 мл) и 1,3-бутадиена (310 мл), с последующим перемешиванием в течение 30 минут. Затем вводили 19 мг дисульфида углерода и 26 мг воды (Н2О) с последующим перемешиванием в течение 30 минут для растворения. Далее вводили хлорид диэтилалюминия (DEAC) так, чтобы его концентрация составляла 2,9 ммоль/л. По истечении 3 минут вводили 8 мг дилаурилтиодипропионата и 1,45 мл циклооктадиена. Смесь нагревали до температуры 50°С. Затем вводили 0,6 мл октилата кобальта [Co(Oct)2] (раствор в толуоле с концентрацией 30 мг/мл) и проводили матричную полимеризацию при температуре 50°С в течение 20 минут.A volume of 2.0 L (capacity volume) of the autoclave was purged with nitrogen. A 1 L solution (FB) of cyclohexane (350 ml), cis-2-butene (340 ml) and 1,3-butadiene (310 ml) was injected into it, followed by stirring for 30 minutes. Then, 19 mg of carbon disulfide and 26 mg of water (H 2 O) were added, followed by stirring for 30 minutes to dissolve. Diethyl aluminum chloride (DEAC) was then introduced so that its concentration was 2.9 mmol / L. After 3 minutes, 8 mg of dilauryl thiodipropionate and 1.45 ml of cyclooctadiene were administered. The mixture was heated to a temperature of 50 ° C. Then 0.6 ml of cobalt octylate [Co (Oct) 2 ] (a solution in toluene with a concentration of 30 mg / ml) was introduced and matrix polymerization was carried out at a temperature of 50 ° C for 20 minutes.
(Синдиотактическая 1,2-полимеризация)(Syndiotactic 1,2-polymerization)
Далее вводили триэтилалюминий (ТЕА) так, чтобы концентрация составляла 3,5 ммоль/л с последующим перемешиванием в течение 5 минут. Затем вводили 0,6 мл раствора октилата кобальта в толуоле (30 мл/л) и проводили полимеризацию в течение 20 минут.Next, triethylaluminum (TEM) was introduced so that the concentration was 3.5 mmol / L, followed by stirring for 5 minutes. Then 0.6 ml of a solution of cobalt octylate in toluene (30 ml / l) was introduced and polymerization was carried out for 20 minutes.
После осуществления полимеризации для прекращения реакции полимеризации вводили 1,26 мл водного раствора гипохлорита натрия (0,05 моль/л). После этого полимеризационную смесь обрабатывали согласно обычному способу для выделения полибутадиенового каучука.After polymerization was completed, 1.26 ml of an aqueous sodium hypochlorite solution (0.05 mol / L) was added to terminate the polymerization reaction. After that, the polymerization mixture was processed according to the usual method for the isolation of polybutadiene rubber.
Выход полученного полибутадиенового каучука составлял 95,7 г, а его вязкость по Муни составляла 49,4 (ML1+4, 100°C). При органолептическом испытании этот каучук, по существу, не обладал запахом.The yield of polybutadiene rubber obtained was 95.7 g, and its Mooney viscosity was 49.4 (ML1 + 4, 100 ° C). In an organoleptic test, this rubber was essentially odorless.
Данный каучук содержал 13 мас.% нерастворимого в кипящем н-гексане вещества и 87 мас.% растворимого в кипящем н-гексане вещества. Нерастворимое в н-гексане вещество обладало пиком на полученной методом дифференциальной сканирующей калориметрии эндотермической кривой при температуре 201,3°С.This rubber contained 13% by weight of a substance insoluble in boiling n-hexane and 87% by weight of a substance insoluble in boiling n-hexane. The n-hexane insoluble substance had a peak in the endothermic curve obtained by differential scanning calorimetry at a temperature of 201.3 ° C.
Пример 2Example 2
Полимеризацию проводили таким же образом, как и в примере 1, за исключением того, что вводимое количество водного раствора гипохлорита натрия составляло 3,72 мл. Выход полученного полибутадиенового каучука составлял 99,2 г, а его вязкость по Муни составляла 48,9 (ML1+4, 100°C). По существу, этот каучук не обладал запахом.The polymerization was carried out in the same manner as in Example 1, except that the injected amount of an aqueous solution of sodium hypochlorite was 3.72 ml. The yield of polybutadiene rubber obtained was 99.2 g, and its Mooney viscosity was 48.9 (ML1 + 4, 100 ° C). Essentially, this rubber was odorless.
Данный каучук содержал 13,5 мас.% нерастворимого в кипящем н-гексане вещества и 86,5 мас.% растворимого в кипящем н-гексане вещества. Нерастворимое в н-гексане вещество обладало пиком на полученной методом дифференциальной сканирующей калориметрии эндотермической кривой при температуре 201,1°С.This rubber contained 13.5% by weight of a substance insoluble in boiling n-hexane and 86.5% by weight of a substance soluble in boiling n-hexane. The n-hexane insoluble substance had a peak in the endothermic curve obtained by differential scanning calorimetry at a temperature of 201.1 ° C.
Сравнительный пример 1Comparative Example 1
Полимеризацию проводили таким же образом, как и в примере 1, за исключением того, что при прекращении полимеризации вместо водного раствора гипохлорита натрия вводили воду. Выход полученного полибутадиенового каучука составлял 99,7 г, а его вязкость по Муни составляла 48,5 (ML1+4, 100°C). Этот каучук обладал неприятным запахом.The polymerization was carried out in the same manner as in Example 1, except that when the polymerization was stopped, water was introduced instead of the aqueous sodium hypochlorite solution. The yield of polybutadiene rubber obtained was 99.7 g, and its Mooney viscosity was 48.5 (ML1 + 4, 100 ° C). This rubber had an unpleasant odor.
Данный каучук содержал 12,9 мас.% нерастворимого в кипящем н-гексане вещества и 87,1 мас.% растворимого в кипящем н-гексане вещества. Нерастворимое в н-гексане вещество обладало пиком на полученной методом дифференциальной сканирующей калориметрии эндотермической кривой при температуре 201,3°С.This rubber contained 12.9% by weight of a substance insoluble in boiling n-hexane and 87.1% by weight of a substance soluble in boiling n-hexane. The n-hexane insoluble substance had a peak in the endothermic curve obtained by differential scanning calorimetry at a temperature of 201.3 ° C.
(Цис-1,4-полимеризация)(Cis-1,4 polymerization)
Пример 3Example 3
Объем 1,5 л (объем емкости) автоклава продували азотом. В него вводили 700 мл раствора смеси, содержащего 33% (мас.) бутадиена, 16% (мас.) циклогексана и 51% (мас.) 2-бутена. При комнатной температуре вводили воду так, чтобы концентрация составляла 3,7 ммоль/л, а также вводили дисульфид углерода и 1,5-циклооктадиен так, чтобы концентрация первого составляла 30 мг/л, а концентрация последнего составляла 10,2 ммоль/л. Осуществляли интенсивное перемешивание при частоте вращения 700 об/мин в течение 30 минут. Вводили 2,4 мл раствора хлорида диэтилалюминия (DEAC) и триэтилалюминия (ТЕА) в циклогексане [DEAC:TEA=2:1 (мольное отношение), концентрация Al=1 моль/л] с последующим перемешиванием при комнатной температуре в течение 5 минут. Смесь нагревали до температуры 60°С и вводили 1,8 мл раствора октилата кобальта [Co(Oct)2] в толуоле (0,005 моль/л). Инициировали полимеризацию и проводили ее при температуре 70°С в течение 15 минут.A volume of 1.5 L (tank volume) of the autoclave was purged with nitrogen. 700 ml of a mixture solution was introduced into it containing 33% (wt.) Butadiene, 16% (wt.) Cyclohexane and 51% (wt.) 2-butene. At room temperature, water was introduced so that the concentration was 3.7 mmol / L, and carbon disulfide and 1,5-cyclooctadiene were introduced so that the concentration of the former was 30 mg / L and the concentration of the latter was 10.2 mmol / L. Intensive mixing was carried out at a speed of 700 rpm for 30 minutes. 2.4 ml of a solution of diethylaluminum chloride (DEAC) and triethylaluminum (TEA) in cyclohexane [DEAC: TEA = 2: 1 (molar ratio), Al concentration = 1 mol / L] were added, followed by stirring at room temperature for 5 minutes. The mixture was heated to a temperature of 60 ° C and 1.8 ml of a solution of cobalt octylate [Co (Oct) 2 ] in toluene (0.005 mol / L) was added. The polymerization was initiated and carried out at a temperature of 70 ° C for 15 minutes.
(Синдиотактическая 1,2-полимеризация)(Syndiotactic 1,2-polymerization)
Далее туда вводили 4,2 мл раствора триэтилалюминия (ТЕА) в циклогексане (1 моль/л). Один за другим вводили 140 мл 1,3-бутадиена, 36 мг воды и 1,05 мл раствора октилата кобальта [Co(Oct)2] в толуоле (0,05 моль/л). Полимеризацию проводили при температуре 60°С в течение 15 минут.Then, 4.2 ml of a solution of triethylaluminum (TEM) in cyclohexane (1 mol / L) was introduced there. One after another, 140 ml of 1,3-butadiene, 36 mg of water and 1.05 ml of a solution of cobalt octylate [Co (Oct) 2 ] in toluene (0.05 mol / L) were added. The polymerization was carried out at a temperature of 60 ° C for 15 minutes.
Для прекращения реакции полимеризации вводили 2 мл водного раствора гипохлорита натрия (0,2 моль/л) с последующим перемешиванием в течение 5 минут. После этого полимеризационную смесь обрабатывали согласно обычному способу для выделения полибутадиенового каучука.To terminate the polymerization reaction, 2 ml of an aqueous sodium hypochlorite solution (0.2 mol / L) was added, followed by stirring for 5 minutes. After that, the polymerization mixture was processed according to the usual method for the isolation of polybutadiene rubber.
Выход полученного полибутадиенового каучука составлял 113 г, а его вязкость по Муни составляла 72 (ML1+4, 100°C). По существу, этот каучук не обладал запахом.The yield of polybutadiene rubber obtained was 113 g, and its Mooney viscosity was 72 (ML1 + 4, 100 ° C). Essentially, this rubber was odorless.
Данный каучук содержал 16,6 мас.% нерастворимого в кипящем н-гексане вещества и 83,4 мас.% растворимого в кипящем н-гексане вещества. Нерастворимое в кипящем н-гексане вещество обладало приведенной вязкостью 1,4 и пиком на полученной методом дифференциальной сканирующей калориметрии эндотермической кривой при температуре 201,2°С. Растворимое в кипящем н-гексане вещество обладало вязкостью по Муни, равной 32 (ML1+4, 100°C), вязкостью раствора в толуоле, равной 82, средневесовой молекулярной массой, равной 400000 и содержало 98,5% звеньев с цис-1,4-структурой, 0,7% звеньев с транс-1,4-структурой и 0,8% звеньев с 1,2-структурой.This rubber contained 16.6% by weight of a substance insoluble in boiling n-hexane and 83.4% by weight of a substance soluble in boiling n-hexane. The insoluble substance in boiling n-hexane had a reduced viscosity of 1.4 and a peak in the endothermic curve obtained by differential scanning calorimetry at a temperature of 201.2 ° C. The soluble in boiling n-hexane substance had a Mooney viscosity of 32 (ML1 + 4, 100 ° C), a solution viscosity in toluene of 82, a weight average molecular weight of 400,000, and contained 98.5% of cis-1 units. 4-structure, 0.7% of units with trans-1,4-structure and 0.8% of units with 1,2-structure.
Пример 4Example 4
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 3, за исключением того, что при прекращении полимеризации вводили водную 3% (мас.) суспензию порошкообразной хлорной извести [CaCl(OCl)]. По существу, полученный каучук не обладал запахом.Polybutadiene was synthesized in the same manner as described in Example 3, except that upon termination of the polymerization, an aqueous 3% (w / w) suspension of powdered bleach [CaCl (OCl)] was introduced. Essentially, the resulting rubber did not have a smell.
Пример 5Example 5
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 3, за исключением того, что при прекращении полимеризации вводили водную 3% (мас.) суспензию высококачественного гипохлорита (гипохлорита кальция). По существу, полученный каучук не обладал запахом.Polybutadiene was synthesized in the same manner as that described in Example 3, except that upon termination of the polymerization, an aqueous 3% (wt.) Suspension of high-quality hypochlorite (calcium hypochlorite) was introduced. Essentially, the resulting rubber did not have a smell.
Пример 6Example 6
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 3, за исключением того, что при прекращении полимеризации вводили водный 3% (мас.) раствор хлората калия. По существу, полученный каучук не обладал запахом.Polybutadiene was synthesized in the same manner as that described in example 3, except that upon termination of the polymerization was introduced an aqueous 3% (wt.) Solution of potassium chlorate. Essentially, the resulting rubber did not have a smell.
Сравнительный пример 2Reference Example 2
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 3, за исключением того, что при прекращении полимеризации не вводили водный раствор гипохлорита натрия. Полученный каучук обладал неприятным запахом.Polybutadiene was synthesized in the same manner as that described in example 3, except that upon termination of the polymerization was not introduced an aqueous solution of sodium hypochlorite. The resulting rubber had an unpleasant odor.
Пример 7Example 7
Выдержка катализатораCatalyst exposure
Смешивали 5,2 мл циклогексана, 1,5 ммоль гидрида диизобутилалюминия (0,75 мл раствора в циклогексане), 0,31 ммоль бутадиена и 0,05 ммоль NDV3 («Версатата» неодима) (в виде раствора в циклогексане). Смесь выдерживали при температуре 50°С в течение 5 минут. Вводили 0,15 ммоль хлорида диэтилалюминия (в виде раствора в циклогескане) с последующим перемешиванием в течение 25 минут.5.2 ml of cyclohexane, 1.5 mmol of diisobutylaluminum hydride (0.75 ml of solution in cyclohexane), 0.31 mmol of butadiene and 0.05 mmol of NDV 3 (Versatate neodymium) (as a solution in cyclohexane) were mixed. The mixture was kept at a temperature of 50 ° C for 5 minutes. 0.15 mmol of diethylaluminium chloride (as a solution in cyclohexane) was added, followed by stirring for 25 minutes.
(Цис-1,4-полимеризация)(Cis-1,4 polymerization)
В 2-литровый автоклав (объем емкости), объем которого продували газообразным азотом, вводили раствор бутадиена, содержащего 25% (мас.) 1,3-бутадиена и 75% (мас.) циклогексана. В него вводили 2,5 ммоль гидрида диизобутилалюминия (1,25 мл раствора в циклогексане), а также суммарное количество полученного ранее выдержанного раствора катализатора. Полимеризацию проводили при температуре 60°С в течение 30 минут.A solution of butadiene containing 25% (wt.) 1,3-butadiene and 75% (wt.) Cyclohexane was introduced into a 2-liter autoclave (tank volume), the volume of which was purged with nitrogen gas. 2.5 mmol of diisobutylaluminum hydride (1.25 ml of the solution in cyclohexane), as well as the total amount of the previously aged catalyst solution obtained, were introduced into it. The polymerization was carried out at a temperature of 60 ° C for 30 minutes.
(Синдиотактическая 1,2-полимеризация)(Syndiotactic 1,2-polymerization)
К полученной, как указано выше, смеси, в которой осуществляли цис-полимеризацию, вводили 15 мг дисульфида углерода, 3,5 ммоль триэтилалюминия и 35 мг октилата кобальта. Смесь перемешивали при температуре 60°С в течение 15 минут для проведения синдиотактической 1,2-полимеризации оставшегося 1,3-бутадиена.To the mixture obtained, as indicated above, in which cis polymerization was carried out, 15 mg of carbon disulfide, 3.5 mmol of triethyl aluminum and 35 mg of cobalt octylate were introduced. The mixture was stirred at 60 ° C. for 15 minutes to syndiotactically 1,2-polymerize the remaining 1,3-butadiene.
Для прекращения реакции полимеризации вводили 2 мл водного раствора гипохлорита натрия (0,2 моль/л) с последующим перемешиванием в течение 5 минут. После этого полимеризационную смесь обрабатывали согласно обычному способу для выделения полибутадиенового каучука.To terminate the polymerization reaction, 2 ml of an aqueous sodium hypochlorite solution (0.2 mol / L) was added, followed by stirring for 5 minutes. After that, the polymerization mixture was processed according to the usual method for the isolation of polybutadiene rubber.
Выход полученного полибутадиенового каучука составлял 97 г, а его вязкость по Муни составляла 51 (ML1+4, 100°C). По существу, этот каучук не обладал запахом.The yield of polybutadiene rubber obtained was 97 g, and its Mooney viscosity was 51 (ML1 + 4, 100 ° C). Essentially, this rubber was odorless.
Данный каучук содержал 14 мас.% нерастворимого в кипящем н-гексане вещества и 86 мас.% растворимого в кипящем н-гексане вещества. Нерастворимое в кипящем н-гексане вещество обладало приведенной вязкостью 1,6 и пиком на полученной методом дифференциальной сканирующей калориметрии эндотермической кривой при температуре 202,4°С. Растворимое в кипящем н-гексане вещество обладало вязкостью по Муни, равной 23 (ML1+4, 100°C), вязкостью раствора в толуоле, равной 91, средневесовой молекулярной массой, равной 600000 и содержало 98,2% звеньев с цис-1,4-структурой, 0,9% звеньев с транс-1,4-структурой и 0,9% звеньев с 1,2-структурой.This rubber contained 14% by weight of a substance insoluble in boiling n-hexane and 86% by weight of a substance soluble in boiling n-hexane. The insoluble substance in boiling n-hexane had a reduced viscosity of 1.6 and a peak on the endothermic curve obtained by differential scanning calorimetry at a temperature of 202.4 ° C. The soluble in boiling n-hexane substance had a Mooney viscosity of 23 (ML1 + 4, 100 ° C), a solution viscosity in toluene of 91, a weight average molecular weight of 600,000, and 98.2% of cis-1 units 4-structure, 0.9% of the links with trans-1,4-structure and 0.9% of the links with 1,2-structure.
Сравнительный пример 3Reference Example 3
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 7, за исключением того, что при прекращении полимеризации не вводили водный раствор гипохлорита натрия. Полученный каучук обладал неприятным запахом.Polybutadiene was synthesized in the same manner as that described in example 7, except that upon termination of the polymerization was not introduced an aqueous solution of sodium hypochlorite. The resulting rubber had an unpleasant odor.
Пример 8Example 8
Цис-1,4-полимеризацияCis-1,4 polymerization
Объем 5,0 л (объем емкости) автоклава продували азотом. В него вводили 3 л раствора (FB), содержащего циклогексан (900 мл), цис-2-бутен (1200 мл) и 1,3-бутадиен (900 мл) с последующим перемешиванием в течение 30 минут. Затем в смеси регулировали содержание воды с помощью определяющего содержание воды контрольно-измерительного прибора Karl Fischer для получения среднего содержания воды 10 миллионных долей. Повторяли эту же операцию и загружали в автоклав 3 литра раствора FB. В него вводили 340 мл (объем при температуре 20°С и давлении 1 атмосфера) газообразного водорода с помощью интегрирующего массового расходомера. Затем вводили 45 мг дисульфида углерода и 56 мг воды (Н2О) с последующим перемешиванием в течение 30 минут для растворения. Далее вводили 6 мл триэтилалюминия (в виде раствора в толуоле с концентрацией 1 ммоль/л). Спустя 3 минуты вводили 3 мл трихлорида циклопентадиенилванадия (CpVCl3) (в виде раствора в толуоле с концентрацией 0,005 ммоль/мл), а также добавляли 12 мл тетракис(пентафторфенил)бората трифенилкарбения [Ph3CB(C6F5)4] (в виде раствора в толуоле с концентрацией 0,0025 ммоль/мл). Матричную полимеризацию проводили при температуре 40°С в течение 30 минут.A volume of 5.0 l (capacity volume) of the autoclave was purged with nitrogen. A 3 L solution (FB) containing cyclohexane (900 ml), cis-2-butene (1200 ml) and 1,3-butadiene (900 ml) was added thereto, followed by stirring for 30 minutes. Then, the water content in the mixture was controlled using a Karl Fischer water-measuring instrument to obtain an average water content of 10 ppm. The same operation was repeated and 3 liters of FB solution were loaded into the autoclave. 340 ml (volume at a temperature of 20 ° C and a pressure of 1 atmosphere) of hydrogen gas were introduced into it using an integrating mass flow meter. Then, 45 mg of carbon disulfide and 56 mg of water (H 2 O) were added, followed by stirring for 30 minutes to dissolve. Next, 6 ml of triethylaluminium was introduced (as a solution in toluene with a concentration of 1 mmol / L). After 3 minutes, 3 ml of cyclopentadienyl vanadium trichloride (CpVCl 3 ) was added (as a solution in toluene with a concentration of 0.005 mmol / ml), and 12 ml of triphenylcarbenium tetrakis (pentafluorophenyl) borate [Ph 3 CB (C 6 F 5 ) 4 ] ( in the form of a solution in toluene with a concentration of 0.0025 mmol / ml). Matrix polymerization was carried out at a temperature of 40 ° C for 30 minutes.
(Синдиотактическая 1,2-полимеризация)(Syndiotactic 1,2-polymerization)
Далее вводили 1,7 мл октоата кобальта (в виде раствора в толуоле с концентрацией 0,1 ммоль/мл) с последующей полимеризацией в течение 30 минут. После проведения полимеризации для прекращения реакции полимеризации вводили 2 мл водного раствора гипохлорита натрия (0,2 моль/л). Затем продолжали перемешивание в течение 5 минут. Полимеризационную смесь обрабатывали согласно обычному способу для выделения полибутадиенового каучука.Next, 1.7 ml of cobalt octoate (as a solution in toluene with a concentration of 0.1 mmol / ml) was introduced, followed by polymerization for 30 minutes. After polymerization, to terminate the polymerization reaction was introduced 2 ml of an aqueous solution of sodium hypochlorite (0.2 mol / l). Then stirring was continued for 5 minutes. The polymerization mixture was treated according to a conventional method for isolating polybutadiene rubber.
Выход полученного полибутадиенового каучука составлял 190 г, а его вязкость по Муни составляла 38 (ML1+4, 100°C). По существу, этот каучук не обладал запахом.The yield of polybutadiene rubber obtained was 190 g, and its Mooney viscosity was 38 (ML1 + 4, 100 ° C). Essentially, this rubber was odorless.
Данный каучук содержал 6 мас.% нерастворимого в кипящем н-гексане вещества и 94 мас.% растворимого в кипящем н-гексане вещества. Нерастворимое в кипящем н-гексане вещество обладало приведенной вязкостью 1,5 и пиком на полученной методом дифференциальной сканирующей калориметрии эндотермической кривой при температуре 204°С. Растворимое в кипящем н-гексане вещество обладало вязкостью по Муни, равной 27 (ML1+4, 100°C) и вязкостью раствора в толуоле, равной 84, а также содержало 88,9% звеньев с цис-1,4-структурой, 0,8% звеньев с транс-1,4-структурой и 10,5% звеньев с 1,2-структурой.This rubber contained 6% by weight of a substance insoluble in boiling n-hexane and 94% by weight of a substance soluble in boiling n-hexane. The insoluble substance in boiling n-hexane had a reduced viscosity of 1.5 and a peak in the endothermic curve obtained by differential scanning calorimetry at a temperature of 204 ° C. The soluble in boiling n-hexane substance had a Mooney viscosity of 27 (ML1 + 4, 100 ° C) and a solution viscosity in toluene of 84, and also contained 88.9% units with a cis-1,4 structure, 0 , 8% of links with a trans-1,4 structure and 10.5% of links with a 1,2 structure.
Пример 9Example 9
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 8, за исключением того, что при прекращении полимеризации вводили водную 3% (мас.) суспензию порошкообразной хлорной извести [CaCl(OCl)]. По существу, полученный каучук не обладал запахом.Polybutadiene was synthesized in the same manner as that described in example 8, except that upon termination of the polymerization was introduced an aqueous 3% (wt.) Suspension of powdered bleach [CaCl (OCl)]. Essentially, the resulting rubber did not have a smell.
Пример 10Example 10
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 8, за исключением того, что при прекращении полимеризации вводили водную 3% (мас.) суспензию высококачественного гипохлорита (гипохлорита кальция). По существу, полученный каучук не обладал запахом.Polybutadiene was synthesized in the same manner as that described in Example 8, except that upon termination of the polymerization, an aqueous 3% (wt.) Suspension of high-quality hypochlorite (calcium hypochlorite) was introduced. Essentially, the resulting rubber did not have a smell.
Пример 11Example 11
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 8, за исключением того, что при прекращении полимеризации вводили водный 3% (мас.) раствор хлората калия. По существу, полученный каучук не обладал запахом.Polybutadiene was synthesized in the same manner as that described in example 8, except that upon termination of the polymerization was introduced an aqueous 3% (wt.) Solution of potassium chlorate. Essentially, the resulting rubber did not have a smell.
Сравнительный пример 4Reference Example 4
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 8, за исключением того, что при прекращении полимеризации не вводили водный 3% (мас.) раствор гипохлорита натрия. Полученный каучук обладал неприятным запахом.Polybutadiene was synthesized in the same manner as that described in example 8, except that upon termination of the polymerization was not introduced an aqueous 3% (wt.) Solution of sodium hypochlorite. The resulting rubber had an unpleasant odor.
Пример 12Example 12
Цис-1,4-полимеризацияCis-1,4 polymerization
Объем 2 л (объем емкости) автоклава продували азотом. В него вводили раствор, содержащий 390 мл толуола и 210 мл бутадиена. Температуру раствора устанавливали равной 30°С. Затем вводили 0,90 мл раствора гидрида диэтилалюминия (DEAH) в толуоле (2 моль/л) с последующим перемешиванием при частоте вращения 550 об/мин в течение 3 минут. Далее вводили 1,8 мл раствора трис(2,2,6,6-тетраметилгептан-3,5-дионато)иттрия в толуоле (20 ммоль/л). Смесь нагревали до температуры 40°С. Перемешивание осуществляли в течение 4 минут. Затем вводили 0,18 мл раствора тетракиспентафторфенилбората трифенилкарбения в толуоле (0,43 моль/л) и инициировали полимеризацию. Полимеризацию проводили при температуре 40°С в течение 30 минут.A volume of 2 l (capacity volume) of the autoclave was purged with nitrogen. A solution containing 390 ml of toluene and 210 ml of butadiene was introduced into it. The temperature of the solution was set equal to 30 ° C. Then, 0.90 ml of a solution of diethylaluminum hydride (DEAH) in toluene (2 mol / L) was added, followed by stirring at a speed of 550 rpm for 3 minutes. Then 1.8 ml of a solution of tris (2,2,6,6-tetramethylheptane-3,5-dionato) yttrium in toluene (20 mmol / L) was added. The mixture was heated to a temperature of 40 ° C. Stirring was carried out for 4 minutes. Then, 0.18 ml of a solution of triphenylcarbenium tetrakispentafluorophenylborate in toluene (0.43 mol / L) was introduced and polymerization was initiated. The polymerization was carried out at a temperature of 40 ° C for 30 minutes.
(Синдиотактическая 1,2-полимеризация)(Syndiotactic 1,2-polymerization)
Далее вводили 1,8 мл раствора триэтилалюминия (ТЕА) в толуоле (1 моль/л). Затем вводили воду так, чтобы ее содержание составляло 0,5 ммоль/л. Вводили 1,8 мл раствора октилата кобальта [Co(Oct)2] в толуоле (0,05 моль/л) и 0,36 мл раствора дисульфида углерода в толуоле (1 моль/л) с последующей полимеризацией при температуре 40°С в течение 10 минут.Next, 1.8 ml of a solution of triethylaluminum (TEA) in toluene (1 mol / L) was added. Then water was introduced so that its content was 0.5 mmol / L. 1.8 ml of a solution of cobalt octylate [Co (Oct) 2 ] in toluene (0.05 mol / L) and 0.36 ml of a solution of carbon disulfide in toluene (1 mol / L) were added, followed by polymerization at 40 ° C in for 10 minutes.
Для прекращения реакции полимеризации вводили 2 мл водного раствора гипохлорита натрия (0,2 моль/л) с последующим перемешиванием в течение 5 минут. Полимеризационную смесь обрабатывали согласно обычному способу для выделения полибутадиенового каучука.To terminate the polymerization reaction, 2 ml of an aqueous solution of sodium hypochlorite (0.2 mol / L) was added, followed by stirring for 5 minutes. The polymerization mixture was treated according to a conventional method for isolating polybutadiene rubber.
Выход полученного полибутадиенового каучука составлял 100 г, а его вязкость по Муни составляла 82 (ML1+4, 100°C). По существу, этот каучук не обладал запахом.The yield of the obtained polybutadiene rubber was 100 g, and its Mooney viscosity was 82 (ML1 + 4, 100 ° C). Essentially, this rubber was odorless.
Данный каучук содержал 11,2 мас.% нерастворимого в кипящем н-гексане вещества и 88,8 мас.% растворимого в кипящем н-гексане вещества. Нерастворимое в кипящем н-гексане вещество обладало пиком на полученной методом дифференциальной сканирующей калориметрии эндотермической кривой при температуре 203,9°С.This rubber contained 11.2% by weight of a substance insoluble in boiling n-hexane and 88.8% by weight of a substance soluble in boiling n-hexane. The substance insoluble in boiling n-hexane had a peak in the endothermic curve obtained by differential scanning calorimetry at a temperature of 203.9 ° C.
Пример 13Example 13
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 12, за исключением того, что при прекращении полимеризации вводили водную 3% (мас.) суспензию порошкообразной хлорной извести [CaCl(OCl)]. По существу, полученный каучук не обладал запахом.Polybutadiene was synthesized in the same manner as that described in example 12, except that upon termination of the polymerization was introduced an aqueous 3% (wt.) Suspension of powdered bleach [CaCl (OCl)]. Essentially, the resulting rubber did not have a smell.
Пример 14Example 14
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 12, за исключением того, что при прекращении полимеризации вводили водную 3% (мас.) суспензию высококачественного гипохлорита (гипохлорита кальция). По существу, полученный каучук не обладал запахом.Polybutadiene was synthesized in the same manner as described in Example 12, except that upon termination of the polymerization, an aqueous 3% (wt.) Suspension of high-quality hypochlorite (calcium hypochlorite) was introduced. Essentially, the resulting rubber was odorless.
Пример 15Example 15
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 12, за исключением того, что при прекращении полимеризации вводили водный 3% (мас.) раствор хлората калия. По существу, полученный каучук не обладал запахом.Polybutadiene was synthesized in the same manner as that described in example 12, except that upon termination of the polymerization was introduced an aqueous 3% (wt.) Solution of potassium chlorate. Essentially, the resulting rubber did not have a smell.
Сравнительный пример 5Reference Example 5
Полибутадиен синтезировали таким же способом, как и тот, который описан в примере 12, за исключением того, что при прекращении полимеризации не вводили водный раствор гипохлорита натрия. Полученный каучук обладал неприятным запахом.Polybutadiene was synthesized in the same manner as that described in example 12, except that upon termination of the polymerization was not introduced an aqueous solution of sodium hypochlorite. The resulting rubber had an unpleasant odor.
Результаты определения содержания летучих компонентов, показанные в таблице 1, хорошо согласуются с результатами испытания на запах посредством обонятельного ощущения.The results of determining the content of volatile components shown in table 1 are in good agreement with the results of the test for smell through olfactory sensation.
В нижеследующих примерах и сравнительных примерах каждый полибутадиеновый каучук, полученный с добавлением Irganox 1520 после прекращения полимеризации, который известен в качестве антиоксиданта, анализировали на способность к разрушению при окислении и приводили результаты. Определяли продолжительность времени, необходимого для проявления разрушения при окислении, и использовали ее в качестве характеристики способности к разрушению при окислении.In the following examples and comparative examples, each polybutadiene rubber obtained with the addition of Irganox 1520 after termination of the polymerization, which is known as an antioxidant, was analyzed for oxidation degradability and the results were reported. The length of time required for the manifestation of the destruction during oxidation was determined, and used it as a characteristic of the ability to destruction during oxidation.
Определение способности к разрушению при окисленииDetermination of oxidation degradability
Полимер, помещенный в контрольно-измерительный прибор для испытаний методом дифференциальной сканирующей калориметрии, выдерживали при заранее определенной температуре в атмосфере воздуха и определяли промежуток времени до проявления выделения тепла из-за разрушения полимера при окислении. Более длинный промежуток времени до проявления выделения тепла указывает на то, что разрушение при окислении является менее вероятным.The polymer, placed in a control instrument for testing by differential scanning calorimetry, was held at a predetermined temperature in the atmosphere of the air and the time interval until heat evolution manifested due to polymer destruction during oxidation was determined. A longer period of time before the manifestation of heat evolution indicates that degradation during oxidation is less likely.
Сравнительный пример 6Reference Example 6
Полимеризацию проводили таким же способом, как и тот, который использовали в сравнительном примере 1, за исключением того, что к полимеру добавляли 1000 миллионных долей Irganox 1520 (антиоксидант) после прекращения полимеризации. Способность к разрушению при окислении для полученного полибутадиенового каучука анализировали при температуре 140°С, 145°С и 150°С. Результаты измерений приведены в таблице 2.The polymerization was carried out in the same manner as that used in comparative example 1, except that 1000 ppm of Irganox 1520 (antioxidant) was added to the polymer after termination of the polymerization. The oxidation degradability for the obtained polybutadiene rubber was analyzed at a temperature of 140 ° C, 145 ° C and 150 ° C. The measurement results are shown in table 2.
Пример 16Example 16
Полимеризацию проводили таким же способом, как и тот, который использовали в примере 1, за исключением того, что к полимеру добавляли 1000 миллионных долей Irganox 1520 (антиоксидант) после прекращения полимеризации, вызываемого введением водного раствора гипохлорита натрия. Способность к разрушению при окислении для полученного полибутадиенового каучука анализировали при температуре 140°С, 145°С и 150°С. Результаты измерений приведены в таблице 2.The polymerization was carried out in the same manner as that used in Example 1, except that 1000 ppm of Irganox 1520 (antioxidant) was added to the polymer after termination of the polymerization caused by the introduction of an aqueous solution of sodium hypochlorite. The oxidation degradability for the obtained polybutadiene rubber was analyzed at a temperature of 140 ° C, 145 ° C and 150 ° C. The measurement results are shown in table 2.
Пример 17Example 17
Полимеризацию проводили таким же способом, как и тот, который использовали в примере 16, за исключением того, что к полимеру добавляли 1350 миллионных долей Irganox 1520. Способность к разрушению при окислении для полученного полибутадиенового каучука анализировали при температуре 140°С, 145°С и 150°С. Результаты измерений приведены в таблице 2.The polymerization was carried out in the same manner as that used in Example 16, except that 1350 ppm of Irganox 1520 was added to the polymer. The oxidation degradability of the resulting polybutadiene rubber was analyzed at a temperature of 140 ° C., 145 ° C. and 150 ° C. The measurement results are shown in table 2.
Пример 18Example 18
Полимеризацию проводили таким же способом, как и тот, который использовали в примере 16, за исключением того, что к полимеру добавляли 1700 миллионных долей Irganox 1520. Способность к разрушению при окислении для полученного полибутадиенового каучука анализировали при температуре 140°С, 145°С и 150°С. Результаты измерений приведены в таблице 2.The polymerization was carried out in the same manner as that used in Example 16, except that 1700 ppm of Irganox 1520 was added to the polymer. The oxidation degradability of the obtained polybutadiene rubber was analyzed at a temperature of 140 ° C., 145 ° C. and 150 ° C. The measurement results are shown in table 2.
Пример 19Example 19
Полимеризацию проводили таким же способом, как и тот, который использовали в примере 16, за исключением того, что к полимеру добавляли 2000 миллионных долей Irganox 1520. Способность к разрушению при окислении для полученного полибутадиенового каучука анализировали при температуре 140°С, 145°С и 150°С. Результаты измерений приведены в таблице 2.The polymerization was carried out in the same manner as that used in Example 16, except that 2000 ppm of Irganox 1520 was added to the polymer. The oxidation degradability of the resulting polybutadiene rubber was analyzed at a temperature of 140 ° C., 145 ° C. and 150 ° C. The measurement results are shown in table 2.
(миллионные доли)(millionths)
Указанные выше результаты отражают следующее. В случае, когда вводимое количество антиоксиданта является недостаточным, как в примере 16, время, требуемое для проявления разрушения при окислении, являлось примерно таким же или немного меньше такового, полученного в примере 6, в котором антиоксидант вводили в таком же количестве, но не вводили водный раствор гипохлорита натрия; однако когда вводили достаточное количество антиоксиданта, как в примерах с 17-го по 19-й, эффект предотвращения разрушения был очевиден по сравнению со случаем, когда не вводили водный раствор гипохлорита натрия.The above results reflect the following. In the case where the amount of antioxidant administered was insufficient, as in Example 16, the time required for the manifestation of oxidation degradation was approximately the same or slightly less than that obtained in Example 6, in which the antioxidant was administered in the same amount, but was not administered an aqueous solution of sodium hypochlorite; however, when a sufficient amount of antioxidant was introduced, as in the examples from the 17th to the 19th, the effect of preventing the destruction was obvious compared to the case when an aqueous solution of sodium hypochlorite was not introduced.
Промышленная применимостьIndustrial applicability
Полимер VCR, полученный по настоящему изобретению, обладает чрезвычайно низким запахом и поэтому его можно использовать сам по себе или компаундированным с другим каучуком, а также при необходимости с разнообразными добавками, для различных применений, например, применений, связанных с использованием каучуков, при которых требуются необходимые механические свойства и сопротивление истиранию, таких как производство шин и разнообразных других промышленных продуктов (например, шлангов и ремней). Полимер VCR также можно использовать в качестве модификатора для пластиков. Соответственно, настоящее изобретение предоставляет полезный для промышленности способ.The VCR polymer obtained according to the present invention has an extremely low odor and therefore can be used alone or compounded with other rubber, as well as various additives, if necessary, for various applications, for example, rubber related applications that require necessary mechanical properties and abrasion resistance, such as the production of tires and various other industrial products (for example, hoses and belts). VCR can also be used as a modifier for plastics. Accordingly, the present invention provides a method useful to industry.
Claims (10)
М'(X'Oq)rZ's (I)
(где М' представляет собой атом металла или атом водорода, X' представляет собой атом галогена, выбираемый из хлора, брома и йода, О представляет собой атом кислорода, q является целым числом от 1 до 4; Z' представляет собой анион, способный связываться с атомом М', r является целым числом равным 1 или более, и сумма r+s является степенью окисления М').1. The method of producing polybutadiene, including, firstly, the cis-1,4-polymerization of 1,3-butadiene and the subsequent syndiotactic 1,2-polymerization of the obtained product in the resulting polymerization system in the presence of a catalyst containing a cobalt compound, an aluminum alkyl compound and a sulfur compound, characterized in that in order to stop the polymerization, a halogen-containing acid or a salt of a halogen-containing acid is introduced, where both are represented by the following general formula (I):
M '(X'O q ) r Z' s (I)
(where M 'represents a metal atom or a hydrogen atom, X' represents a halogen atom selected from chlorine, bromine and iodine, O represents an oxygen atom, q is an integer from 1 to 4; Z 'represents an anion capable of binding with an atom M ', r is an integer of 1 or more, and the sum r + s is the oxidation state of M').
[формула 1]
(где каждая из групп R1, R2 и R3 представляет собой водород или углеводородную группу, имеющую от 1 до 12 атомов углерода, О представляет собой атом кислорода, a Y представляет собой атом иттрия).9. The method of producing polybutadiene according to claim 8, where the compound of yttrium (A) uses a compound of yttrium with a bulky ligand represented by the following general formula:
[Formula 1]
(where each of the groups R 1 , R 2 and R 3 represents hydrogen or a hydrocarbon group having from 1 to 12 carbon atoms, O represents an oxygen atom, and Y represents a yttrium atom).
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006-141109 | 2006-05-22 | ||
| JP2006141109 | 2006-05-22 | ||
| JP2006166617 | 2006-06-15 | ||
| JP2006-166617 | 2006-06-15 | ||
| JP2006-197862 | 2006-07-20 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2008150488A RU2008150488A (en) | 2010-06-27 |
| RU2436802C2 true RU2436802C2 (en) | 2011-12-20 |
Family
ID=42683144
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2008150488/04A RU2436802C2 (en) | 2006-05-22 | 2007-05-17 | Method of producing polybutadiene |
Country Status (2)
| Country | Link |
|---|---|
| BR (1) | BRPI0713099A2 (en) |
| RU (1) | RU2436802C2 (en) |
-
2007
- 2007-05-17 RU RU2008150488/04A patent/RU2436802C2/en not_active IP Right Cessation
- 2007-05-17 BR BRPI0713099-6A patent/BRPI0713099A2/en not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| RU2008150488A (en) | 2010-06-27 |
| BRPI0713099A2 (en) | 2012-10-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5375092B2 (en) | Method for producing polybutadiene | |
| JP5791607B2 (en) | Method and catalyst system for polydiene production | |
| US20050090383A1 (en) | Metal complex compositions and their use as catalysts to produce polydienes | |
| RU2543376C2 (en) | Method of obtaining copolymer of cyclic and acyclic diene and rubber mixture | |
| KR20110104972A (en) | Process for producing conjugated diene polymer | |
| JP2022020012A (en) | Method for preparing functionalized polymer | |
| JP4736772B2 (en) | Method for producing polybutadiene | |
| RU2627708C2 (en) | Method of polymerization in the mass for obtaining polydienes | |
| JPH1180222A (en) | Catalyst and production of conjugated diene polymer | |
| KR101896136B1 (en) | Processes for the preparation of high-cis polydienes | |
| JP6869333B2 (en) | Preparation of cis-1,4-polydiene with multiple silane functional groups prepared by in-situ hydrosilylation of polymer cements | |
| JP2019031686A (en) | Catalyst for conjugated diene polymerization, method of producing conjugated diene polymer using the same, and conjugated diene polymer | |
| RU2436802C2 (en) | Method of producing polybutadiene | |
| JP5370076B2 (en) | Modified conjugated diene polymer and method for producing the same | |
| JP2011127035A (en) | Modified conjugated diene polymer and method for producing the same | |
| WO2003064484A1 (en) | Metal complex compositions based on cobalt and their use as polymerization catalyst for olefins and dienes | |
| JP2013053212A (en) | Rubber composition | |
| JP5266808B2 (en) | Process for producing conjugated diene polymer | |
| US20230089837A1 (en) | Polymerization processes for the production of cis-1,4-polydienes | |
| JP6418227B2 (en) | Catalyst solution for polymerization of conjugated diene and polymerization method using the same | |
| WO2021133818A1 (en) | Polymerization processes for the production of cis-1,4-polydienes | |
| JP2009215430A (en) | Method for producing conjugated diene polymer |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20160518 |