RU2094373C1 - Method of basic aluminium chloride producing - Google Patents
Method of basic aluminium chloride producing Download PDFInfo
- Publication number
- RU2094373C1 RU2094373C1 RU95121525A RU95121525A RU2094373C1 RU 2094373 C1 RU2094373 C1 RU 2094373C1 RU 95121525 A RU95121525 A RU 95121525A RU 95121525 A RU95121525 A RU 95121525A RU 2094373 C1 RU2094373 C1 RU 2094373C1
- Authority
- RU
- Russia
- Prior art keywords
- aluminum
- hydrochloric acid
- metal
- aluminium chloride
- basic aluminium
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 14
- VSCWAEJMTAWNJL-UHFFFAOYSA-K aluminium trichloride Chemical compound Cl[Al](Cl)Cl VSCWAEJMTAWNJL-UHFFFAOYSA-K 0.000 title claims description 14
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims abstract description 22
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 claims abstract description 18
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims abstract description 10
- 229910052782 aluminium Inorganic materials 0.000 claims abstract description 6
- 239000000203 mixture Substances 0.000 claims abstract description 5
- 238000006243 chemical reaction Methods 0.000 claims description 11
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 claims description 5
- 229910052751 metal Inorganic materials 0.000 claims description 3
- 239000002184 metal Substances 0.000 claims description 3
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 abstract description 5
- 239000000126 substance Substances 0.000 abstract description 4
- 230000000694 effects Effects 0.000 abstract description 2
- 239000004411 aluminium Substances 0.000 abstract 1
- 229910021502 aluminium hydroxide Inorganic materials 0.000 abstract 1
- 230000015572 biosynthetic process Effects 0.000 description 4
- 239000000701 coagulant Substances 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 229910018072 Al 2 O 3 Inorganic materials 0.000 description 2
- -1 aluminum oxychloride Chemical compound 0.000 description 2
- NNCOOIBIVIODKO-UHFFFAOYSA-N aluminum;hypochlorous acid Chemical group [Al].ClO NNCOOIBIVIODKO-UHFFFAOYSA-N 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000003651 drinking water Substances 0.000 description 1
- 235000020188 drinking water Nutrition 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- QWPPOHNGKGFGJK-UHFFFAOYSA-N hypochlorous acid Chemical group ClO QWPPOHNGKGFGJK-UHFFFAOYSA-N 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 238000004065 wastewater treatment Methods 0.000 description 1
Images
Landscapes
- Compounds Of Alkaline-Earth Elements, Aluminum Or Rare-Earth Metals (AREA)
- Separation Of Suspended Particles By Flocculating Agents (AREA)
Abstract
Description
Изобретение относится к способам получения основных хлоридов алюминия, которые могут быть использованы в качестве коагулянтов на станциях подготовки питьевой воды и при очистке сточных вод. The invention relates to methods for producing basic aluminum chlorides, which can be used as coagulants at drinking water treatment plants and in wastewater treatment.
Известен способ получения растворов основного хлорида алюминия (авт.св. СССР N 260624, кл C 01 F 7/50, 1970) путем взаимодействия гидроокиси алюминия с соляной кислотой и последующим введением в раствор металлического алюминия. A known method of obtaining solutions of basic aluminum chloride (ed. St. USSR N 260624, CL C 01 F 7/50, 1970) by reacting aluminum hydroxide with hydrochloric acid and subsequent introduction of aluminum metal into the solution.
В известном способе для образования оксихлорида алюминия заданного состава металлический алюминий вводится в раствор хлористого алюминия, что приводит к значительному расходу дорогостоящего сырья. Относительно дешевая гидроокись алюминия используется только для получения раствора хлористого алюминия. In the known method for the formation of aluminum oxychloride of a given composition, aluminum metal is introduced into a solution of aluminum chloride, which leads to a significant consumption of expensive raw materials. Relatively cheap aluminum hydroxide is used only to obtain a solution of aluminum chloride.
Задача изобретения упрощение процесса. The objective of the invention is the simplification of the process.
Поставленная задача достигается тем, что металлический алюминий вводится в исходную суспензию гидрата окиси алюминия в соляной кислоте в присутствии серной кислоты (соотношение Al2O3 Cl 1 2,5 1 2,7; соотношение Cl SO4 80 1). В результате взаимодействие гидрата окиси алюминия с соляной кислотой происходит не только до получения хлористого алюминия, но и до образования основного хлорида. Это приводит к значительному снижению расхода дорогостоящего металлического алюминия.This object is achieved in that metallic aluminum is introduced into the initial suspension of alumina hydrate in hydrochloric acid in the presence of sulfuric acid (ratio Al 2 O 3 Cl 1 2.5 1 2.7; ratio Cl SO 4 80 1). As a result, the interaction of alumina hydrate with hydrochloric acid occurs not only to obtain aluminum chloride, but also to the formation of basic chloride. This leads to a significant reduction in the consumption of expensive metal aluminum.
Разогрев реакционной массы осуществляется путем введения необходимого количества металлического алюминия за счет тепла, выделяющегося при взаимодействии последнего с соляной кислотой. The reaction mass is heated by introducing the necessary amount of aluminum metal due to the heat released during the interaction of the latter with hydrochloric acid.
Тепловой эффект указанной реакции значителен, поэтому добавка металлического алюминия не будет большой. Кроме того, металлический алюминий может вводиться по ходу процесса, так же как и для коррекции состава гидроксихлорида алюминия с целью повышения его основности. The thermal effect of this reaction is significant, so the addition of aluminum metal will not be large. In addition, metallic aluminum can be introduced during the process, as well as to correct the composition of aluminum hydroxychloride in order to increase its basicity.
За счет выделяющегося тепла реакции металлического алюминия с соляной кислотой реакционная масса разогревается до температуры 100 120oC. При этом протекает параллельная реакция взаимодействия соляной кислоты с гидратом окиси алюминия с образованием основных хлоридов алюминия, которая при атмосферном давлении завершается при температуре 115 120oC.Due to the heat of reaction of aluminum metal with hydrochloric acid, the reaction mass is heated to a temperature of 100 120 o C. In this case, a parallel reaction of the interaction of hydrochloric acid with alumina hydrate takes place with the formation of basic aluminum chlorides, which ends at atmospheric pressure at a temperature of 115 120 o C.
Для разогрева реакционной массы до указанных температур необходимо ввести металлический алюминий в количестве 0,74 0,92 мас. от загрузки реакционной массы. To heat the reaction mass to the indicated temperatures, it is necessary to introduce metallic aluminum in an amount of 0.74 to 0.92 wt. from loading the reaction mass.
Для управления тепловым режимом синтеза или корректировки состава гидроксихлорида алюминий может вводиться по частям. To control the thermal regime of synthesis or adjust the composition of hydroxychloride, aluminum can be introduced in parts.
Пример 1 (сравнительный). В реактор с мешалкой загружают 409,1 г 35%-ной соляной кислоты, 110,8 г гидроокиси алюминия с содержанием основного вещества 92,4% (остальное вода). Example 1 (comparative). 409.1 g of 35% hydrochloric acid, 110.8 g of aluminum hydroxide with a basic substance content of 92.4% (the rest is water) are loaded into a stirred reactor.
Реакционная масса разогревается до температуры 105 106oC и затем дозируется металлический алюминий 17,7 г в течение 3,5 ч.The reaction mass is heated to a temperature of 105 106 o C and then metered metal aluminum 17.7 g for 3.5 hours
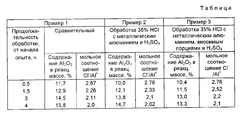
Контроль осуществлялся по содержанию алюминия в растворе (в пересчете на Al2O3) и по мольному соотношению Cl Al. Результаты представлены в таблице.The control was carried out by the aluminum content in the solution (in terms of Al 2 O 3 ) and the molar ratio of Cl Al. The results are presented in the table.
Пример 2. В стеклянный теплоизолированный реактор при работающей мешалке загружают 409,1 г 35%-ной соляной кислоты, 165,7 г гидроокиси алюминия с содержанием основного вещества 92,4% (остальное вода), 3,54 г серной кислоты (50% раствор). После загрузки серной кислоты в реактор загружают металлический алюминий в количестве 0,92% от реакционной массы. Этого количества достаточно, чтобы температура за счет тепла реакции повысилась до 120oC.Example 2. 409.1 g of 35% hydrochloric acid, 165.7 g of aluminum hydroxide with a basic substance content of 92.4% (the rest of the water), 3.54 g of sulfuric acid (50%) are loaded into a thermally insulated glass reactor with a working stirrer solution). After loading sulfuric acid into the reactor, metallic aluminum is charged in an amount of 0.92% of the reaction mass. This amount is enough that the temperature due to the heat of reaction increased to 120 o C.
Пример 3. То же, что и в примере 2, но металлический алюминий вносится порциями по 0,092% от реакционной смеси в течение 2,5 ч. Температура процесса при этом также достигается 120oC.Example 3. The same as in example 2, but aluminum metal is introduced in portions at 0.092% of the reaction mixture for 2.5 hours. The process temperature is also reached 120 o C.
Как следует из таблицы, во всех случаях получается коагулянт гидроксихлорид алюминия, близко соответствующий формуле Al(OH)Cl2, т.е. коагулянту 1/3 оксихлориду алюминия.As follows from the table, in all cases a coagulant of aluminum hydroxychloride is obtained, which closely corresponds to the formula Al (OH) Cl 2 , i.e. coagulant 1/3 aluminum oxychloride.
Claims (4)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU95121525A RU2094373C1 (en) | 1995-12-18 | 1995-12-18 | Method of basic aluminium chloride producing |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU95121525A RU2094373C1 (en) | 1995-12-18 | 1995-12-18 | Method of basic aluminium chloride producing |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU95121525A RU95121525A (en) | 1997-01-10 |
| RU2094373C1 true RU2094373C1 (en) | 1997-10-27 |
Family
ID=20174917
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU95121525A RU2094373C1 (en) | 1995-12-18 | 1995-12-18 | Method of basic aluminium chloride producing |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2094373C1 (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2181694C2 (en) * | 2000-07-20 | 2002-04-27 | Набиуллин Рашит Габдрахманович | METHOD OF PRODUCTION OF COAGULANT (Versions) |
| RU2327643C2 (en) * | 2006-06-13 | 2008-06-27 | Открытое акционерное общество "Аурат" | Method of producing aluminium oxicloride |
-
1995
- 1995-12-18 RU RU95121525A patent/RU2094373C1/en active
Non-Patent Citations (1)
| Title |
|---|
| Авторское свидетельство СССР N 260624, кл. C 01 F 7/50, 1970. * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2181694C2 (en) * | 2000-07-20 | 2002-04-27 | Набиуллин Рашит Габдрахманович | METHOD OF PRODUCTION OF COAGULANT (Versions) |
| RU2327643C2 (en) * | 2006-06-13 | 2008-06-27 | Открытое акционерное общество "Аурат" | Method of producing aluminium oxicloride |
Also Published As
| Publication number | Publication date |
|---|---|
| RU95121525A (en) | 1997-01-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| SU450780A1 (en) | The method of obtaining basic aluminum chlorides | |
| US3989805A (en) | Process for the production of aluminum chlorohydroxides having a controlled chlorine content | |
| JPH0159977B2 (en) | ||
| JPS59116125A (en) | Manufacture of basic aluminum chlorosulfate | |
| US4082685A (en) | Process for the production of aluminum chlorohydroxides | |
| RU2094373C1 (en) | Method of basic aluminium chloride producing | |
| US4034067A (en) | Hydroxychlorides of aluminum and method | |
| CN114084895A (en) | Preparation method of polyaluminum chloride | |
| US4284607A (en) | Chlorination of aluminous materials using preselected solid reducing agents | |
| NL8701037A (en) | METHOD FOR THE PREPARATION OF HYDRATED ALUMINUM OXIDES AND METHOD FOR TREATING ACID WASTE PRODUCTS | |
| US3000703A (en) | Manufacture of zirconium oxide | |
| US4434149A (en) | Acid melt treatment to activate carbon for use as reductant | |
| JPH0891829A (en) | Refining method for magnesium hydroxide | |
| EP1314696B1 (en) | Method for preparing aluminum sulfate | |
| US4292295A (en) | Highly reactive alumina and process for the preparation thereof | |
| JPS61134393A (en) | Manufacture of carboxylic acid trimethylsilyl ester and trimethylsilylcarboxylic acid amide simultaneously | |
| RU2181694C2 (en) | METHOD OF PRODUCTION OF COAGULANT (Versions) | |
| JP3957660B2 (en) | Method for synthesizing reactive oxygen species inclusion materials | |
| US4447351A (en) | Preparation of alumina hydrosol from aluminum sulfate solution | |
| JP4391373B2 (en) | Method for synthesizing reactive oxygen species inclusion material and reactive oxygen species inclusion material | |
| US5021231A (en) | Production of chlorine and sodium sulphate | |
| JPS61286219A (en) | Preparation of aluminium polychloride | |
| SU861301A1 (en) | Method of producing white carbon black | |
| NO137888B (en) | PROCEDURE FOR THE PREPARATION OF ALUMINUM HYDROXYCHLORIDES | |
| JPH08268713A (en) | Refining method of magnesium oxide |