KR20170126689A - Heterocyclic compound and organic solar cell comprising the same - Google Patents
Heterocyclic compound and organic solar cell comprising the same Download PDFInfo
- Publication number
- KR20170126689A KR20170126689A KR1020160057063A KR20160057063A KR20170126689A KR 20170126689 A KR20170126689 A KR 20170126689A KR 1020160057063 A KR1020160057063 A KR 1020160057063A KR 20160057063 A KR20160057063 A KR 20160057063A KR 20170126689 A KR20170126689 A KR 20170126689A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- substituted
- formula
- layer
- unsubstituted
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D285/00—Heterocyclic compounds containing rings having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by groups C07D275/00 - C07D283/00
- C07D285/01—Five-membered rings
- C07D285/02—Thiadiazoles; Hydrogenated thiadiazoles
- C07D285/14—Thiadiazoles; Hydrogenated thiadiazoles condensed with carbocyclic rings or ring systems
-
- H01L51/0068—
-
- H01L51/0069—
-
- H01L51/424—
-
- H01L51/4253—
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K30/00—Organic devices sensitive to infrared radiation, light, electromagnetic radiation of shorter wavelength or corpuscular radiation
- H10K30/20—Organic devices sensitive to infrared radiation, light, electromagnetic radiation of shorter wavelength or corpuscular radiation comprising organic-organic junctions, e.g. donor-acceptor junctions
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K30/00—Organic devices sensitive to infrared radiation, light, electromagnetic radiation of shorter wavelength or corpuscular radiation
- H10K30/30—Organic devices sensitive to infrared radiation, light, electromagnetic radiation of shorter wavelength or corpuscular radiation comprising bulk heterojunctions, e.g. interpenetrating networks of donor and acceptor material domains
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/655—Aromatic compounds comprising a hetero atom comprising only sulfur as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/656—Aromatic compounds comprising a hetero atom comprising two or more different heteroatoms per ring
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Abstract
Description
본 명세서는 헤테로환 화합물 및 이를 포함하는 유기 태양 전지에 관한 것이다.The present invention relates to heterocyclic compounds and organic solar cells comprising the same.
유기 태양전지는 광기전력효과(photovoltaic effect)를 응용함으로써 태양에너지를 직접 전기에너지로 변환할 수 있는 소자이다. 태양전지는 박막을 구성하는 물질에 따라 무기 태양전지와 유기 태양전지로 나뉠 수 있다. 전형적인 태양전지는 무기 반도체인 결정성 실리콘(Si)을 도핑(doping)하여 p-n 접합으로 만든 것이다. 빛을 흡수하여 생기는 전자와 정공은 p-n 접합점까지 확산되고 그 전계에 의하여 가속되어 전극으로 이동한다. 이 과정의 전력변환 효율은 외부 회로에 주어지는 전력과 태양전지에 들어간 태양전력의 비로 정의되며, 현재 표준화된 가상 태양 조사 조건으로 측정 시 24%정도까지 달성되었다. 그러나 종래 무기 태양전지는 이미 경제성과 재료상의 수급에서 한계를 보이고 있기 때문에, 가공이 쉬우며 저렴하고 다양한 기능성을 가지는 유기물 반도체 태양전지가 장기적인 대체 에너지원으로 각광받고 있다.Organic solar cells are devices that can convert solar energy directly into electric energy by applying photovoltaic effect. Solar cells can be divided into inorganic solar cells and organic solar cells depending on the material constituting the thin film. A typical solar cell is made of p-n junction by doping crystalline silicon (Si), which is an inorganic semiconductor. Electrons and holes generated by absorption of light are diffused to the p-n junction, accelerated by the electric field, and moved to the electrode. The power conversion efficiency of this process is defined as the ratio of the power given to the external circuit to the solar power entering the solar cell, and is achieved up to 24% when measured under the current standardized virtual solar irradiation conditions. However, since conventional inorganic solar cells have already been limited in economic efficiency and supply / demand of materials, organic semiconductor solar cells, which are easy to process, have various functions and are inexpensive, are seen as long-term alternative energy sources.
태양전지는 태양 에너지로부터 가능한 많은 전기 에너지를 출력할 수 있도록 효율을 높이는 것이 중요하다. 이러한 태양전지의 효율을 높이기 위해서는 반도체 내부에서 가능한 많은 엑시톤을 생성하는 것도 중요하지만 생성된 전하를 손실됨 없이 외부로 끌어내는 것 또한 중요하다. 전하가 손실되는 원인 중의 하나가 생성된 전자 및 정공이 재결합(recombination)에 의해 소멸하는 것이다. 생성된 전자나 정공이 손실되지 않고 전극에 전달되기 위한 방법으로 다양한 방법이 제시되고 있으나, 대부분 추가 공정이 요구되고 이에 따라 제조 비용이 상승할 수 있다.Solar cells are important to increase efficiency so that they can output as much electrical energy as possible from solar energy. In order to increase the efficiency of such a solar cell, it is also important to generate as much excitons as possible in the semiconductor, but it is also important to draw out generated charges without loss. One of the causes of loss of charge is that the generated electrons and holes are destroyed by recombination. Various methods have been proposed as methods for transferring generated electrons and holes to electrodes without loss, but most of them require additional processing, which may increase the manufacturing cost.
본 명세서는 헤테로환 화합물 및 이를 포함하는 유기 태양 전지를 제공하는 것을 목적으로 한다.It is an object of the present invention to provide a heterocyclic compound and an organic solar cell containing the heterocyclic compound.
본 명세서는 하기 화학식 1로 표시되는 헤테로환 화합물을 제공한다.The present invention provides a heterocyclic compound represented by the following formula (1).
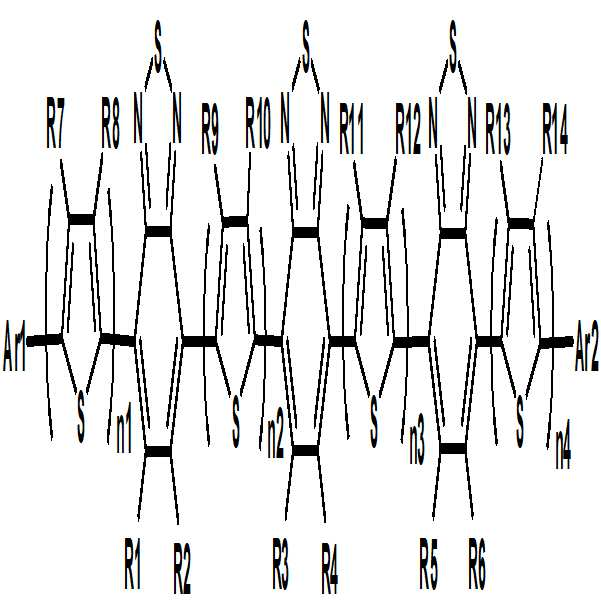
[화학식 1][Chemical Formula 1]
상기 화학식 1에 있어서,In Formula 1,
n1, n2, n3 및 n4는 각각 0 내지 4의 정수이고,n1, n2, n3 and n4 are each an integer of 0 to 4,
n1, n2, n3 및 n4가 각각 2 이상인 경우, 2 이상의 괄호 내의 구조는 서로 같거나 상이하며,When n1, n2, n3 and n4 are each 2 or more, the structures in parentheses of 2 or more are the same or different,
상기 n1+n2+n3+n4≥ 4 이고,N1 + n2 + n3 + n4? 4,
Y1 내지 Y7은 서로 같거나 상이하고, 각각 독립적으로 CRR', NR, O, SiRR', PR, S, GeRR', Se 또는 Te이며,Y1 to Y7 are the same or different from each other and each independently CRR ', NR, O, SiRR', PR, S, GeRR '
X1 내지 X6는 서로 같거나 상이하고, 각각 독립적으로 CR", N, SiR", P 또는 GeR"이고,X1 to X6 are the same or different from each other and are each independently CR ", N, SiR", P or GeR "
L1 내지 L6는 서로 같거나 상이하고, 각각 독립적으로 직접결합; 또는 2가의 연결기이며,L1 to L6 are the same or different from each other, and are each independently a direct bond; Or a divalent linking group,
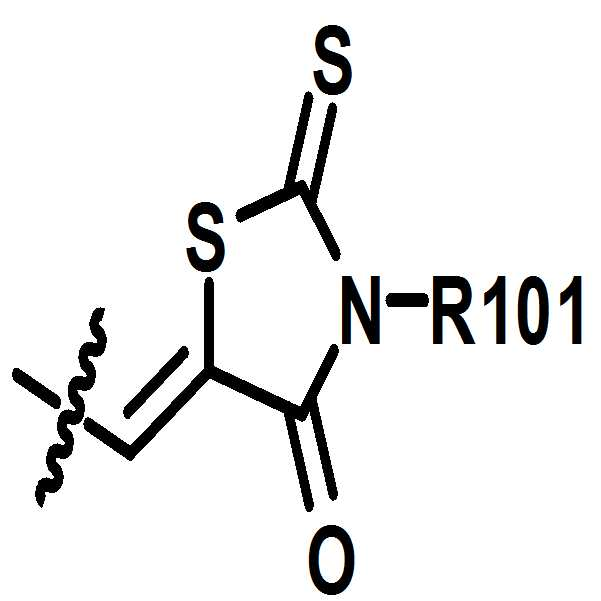
R, R', R", R1 내지 R14, Ar1 및 Ar2는 서로 같거나 상이하고, 각각 독립적으로 수소; 중수소; 할로겐기; 니트릴기; 니트로기; 히드록시기; 카르보닐기; 에스테르기; 이미드기; 아미드기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 아릴포스핀기; 치환 또는 비치환된 포스핀옥사이드기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 헤테로아릴기; 또는 전자 받개로서 작용하는 구조이다.A halogen atom, a nitrile group, a nitro group, a hydroxyl group, a carbonyl group, an ester group, an imide group, an amide group A substituted or unsubstituted alkyl group, a substituted or unsubstituted cycloalkyl group, a substituted or unsubstituted alkoxy group, a substituted or unsubstituted aryloxy group, a substituted or unsubstituted alkylthio group, a substituted or unsubstituted arylthio group A substituted or unsubstituted aryloxy group, a substituted or unsubstituted aryloxy group, a substituted or unsubstituted aryloxy group, a substituted or unsubstituted aryloxy group, a substituted or unsubstituted aryloxy group, a substituted or unsubstituted aryloxy group, A substituted or unsubstituted arylphosphine group, a substituted or unsubstituted phosphine oxide group, a substituted or unsubstituted aryl group, a substituted or unsubstituted heteroaryl group, or an electron acceptor.
또한, 본 명세서는 1 전극; 상기 제1 전극과 대향하여 구비되는 제2 전극; 및 상기 제1 전극과 상기 제2 전극 사이에 구비되고, 광활성층을 포함하는 1층 이상의 유기물층을 포함하고, 상기 유기물층 중 1층 이상은 전술한 헤테로환 화합물을 포함하는 것인 유기 태양 전지를 제공한다.Further, the present specification discloses a plasma display panel comprising a first electrode; A second electrode facing the first electrode; And at least one organic compound layer including a photoactive layer and disposed between the first electrode and the second electrode, wherein at least one of the organic compound layers includes the above-described heterocyclic compound do.
본 명세서의 일 실시상태에 따른 헤테로환 벤조티아디아졸 간의 상호작용으로 분자가 평면의(planar) 성질이 있으며, 전자 주개 성질을 갖는 티오펜과 전자 받개 성질을 갖는 벤조티아디아졸을 포함하는 구조의 코어를 가지므로 낮는 밴드갭 특성을 갖는다.The molecule having planar properties due to the interaction between heterocyclic benzothiadiazoles according to an embodiment of the present invention and the structure comprising thiophene having electron donating property and benzothiadiazole having electron acceptor property And has a low band gap characteristic.
또한, 본 명세서의 일 실시상태에 따른 헤테로환 화합물은 낮은 밴드갭 특성을 가지므로, 유기 태양 전지에 사용되었을 때 높은 전류 값(Isc)을 가질 수 있다.In addition, the heterocyclic compound according to one embodiment of the present invention has a low bandgap characteristic, and thus can have a high current value I sc when used in an organic solar battery.
따라서, 상기 헤테로환 화합물을 유기태양 전지의 유기물층 재료로 사용될 수 있으며, 이를 포함하는 유기 태양 전지는 개방 전압과 단락 전류의 상승, 낮은 밴드갭의 효과 및/또는 효율 증가 등에서 우수한 특성을 나타낼 수 있다. Therefore, the heterocyclic compound can be used as an organic material layer of an organic solar cell, and an organic solar cell including the same can exhibit excellent characteristics in terms of an increase in open-circuit voltage and short-circuit current, a low band gap effect, and / or an increase in efficiency .
본 명세서의 일 실시상태에 따른 헤테로환 화합물은 유기 태양 전지에서 단독 또는 다른 물질과 혼합하여 사용이 가능하고, 효율의 향상, 화합물의 열적 안정성 등의 특성에 의한 소자의 수명 향상 등이 기대될 수 있다.The heterocyclic compound according to one embodiment of the present invention can be used alone or in combination with other materials in an organic solar cell, and the lifetime of the device can be expected to be improved by improving the efficiency and the thermal stability of the compound have.
도 1은 본 명세서의 일 실시상태에 따른 유기 태양 전지를 나타낸 도이다.
도 2는 화합물 A-1의 NMR 데이터를 나타낸 도이다.
도 3은 화합물 1-1의 NMR 데이터를 나타낸 도이다.
도 4는 화합물 1-1의 MS 데이터를 나타낸 도이다.
도 5는 화합물 1-2의 NMR 데이터를 나타낸 도이다.
도 6은 화합물 1-2의 MS 데이터를 나타낸 도이다.
도 7은 화합물 1-3의 MS 데이터를 나타낸 도이다.
도 8은 실험예 1에 따른 유기 태양 전지의 전압에 따른 전류 밀도를 나타낸 도이다.
도 9는 실험예 2에 따른 유기 태양 전지의 전압에 따른 전류 밀도를 나타낸 도이다.1 is a view illustrating an organic solar cell according to an embodiment of the present invention.
2 shows NMR data of Compound A-1.
3 is a view showing NMR data of Compound 1-1.
4 is a diagram showing MS data of the compound 1-1.
5 shows NMR data of Compound 1-2.
6 shows MS data of the compound 1-2.
FIG. 7 shows MS data of the compound 1-3. FIG.
8 is a graph showing a current density according to a voltage of an organic solar cell according to Experimental Example 1. FIG.
9 is a graph showing the current density according to the voltage of the organic solar battery according to Experimental Example 2. FIG.
이하, 본 명세서에 대하여 상세히 설명한다. Hereinafter, the present specification will be described in detail.
본 명세서는 상기 화학식 1로 표시되는 헤테로환 화합물을 제공한다. The present invention provides a heterocyclic compound represented by the above formula (1).
본 명세서의 일 실시상태에 따른 헤테로환 벤조티아디아졸 간의 상호작용으로 분자가 평면의(planar) 성질이 있으며, 전자 주개 성질을 갖는 티오펜과 전자 받개 성질을 갖는 벤조티아디아졸을 포함하는 구조의 코어를 가지므로 낮는 밴드갭 특성을 갖는다.The molecule having planar properties due to the interaction between heterocyclic benzothiadiazoles according to an embodiment of the present invention and the structure comprising thiophene having electron donating property and benzothiadiazole having electron acceptor property And has a low band gap characteristic.
본 명세서에 있어서, 는 다른 치환기에 연결되는 부위를 의미한다.In the present specification, Quot; refers to a moiety that is connected to another substituent.
본 명세서에 있어서, 어떤 부분이 어떤 구성요소를 "포함" 한다고 할 때, 이는 특별히 반대되는 기재가 없는 한 다른 구성요소를 제외하는 것이 아니라 다른 구성 요소를 더 포함할 수 있는 것을 의미한다.In this specification, when a part is referred to as "including " an element, it is to be understood that it may include other elements as well, without departing from the other elements unless specifically stated otherwise.
상기 치환기의 예시들은 아래에서 설명하나, 이에 한정되는 것은 아니다.Examples of such substituents are described below, but are not limited thereto.
상기 "치환"이라는 용어는 화합물의 탄소 원자에 결합된 수소 원자가 다른 치환기로 바뀌는 것을 의미하며, 치환되는 위치는 수소 원자가 치환되는 위치 즉, 치환기가 치환 가능한 위치라면 한정하지 않으며, 2 이상 치환되는 경우, 2 이상의 치환기는 서로 동일하거나 상이할 수 있다.The term "substituted" means that the hydrogen atom bonded to the carbon atom of the compound is replaced with another substituent, and the substituted position is not limited as long as the substituent is a substitutable position, , Two or more substituents may be the same as or different from each other.
본 명세서에서 "치환 또는 비치환된" 이라는 용어는 중수소; 할로겐기; 알킬기; 알케닐기; 알콕시기; 에스터기; 카보닐기; 카복실기; 히드록시기; 시클로알킬기; 실릴기; 아릴알케닐기; 아릴옥시기; 알킬티옥시기; 알킬술폭시기; 아릴술폭시기; 붕소기; 알킬아민기; 아랄킬아민기; 아릴아민기; 아릴아민기; 아릴기; 니트릴기; 니트로기; 히드록시기; 및 N, O, S 원자 중 1개 이상을 포함하는 헤테로고리기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환되었거나 또는 어떠한 치환기도 갖지 않는 것을 의미한다. As used herein, the term " substituted or unsubstituted " A halogen group; An alkyl group; An alkenyl group; An alkoxy group; Ester group; A carbonyl group; A carboxyl group; A hydroxy group; A cycloalkyl group; Silyl group; An arylalkenyl group; An aryloxy group; An alkyloxy group; An alkylsulfoxy group; Arylsulfoxy group; Boron group; An alkylamine group; An aralkylamine group; An arylamine group; An arylamine group; An aryl group; A nitrile group; A nitro group; A hydroxy group; And a heterocyclic group containing at least one of N, O and S atoms, or does not have any substituent (s).
상기 치환기들은 추가의 치환기로 치환 또는 비치환될 수 있다.The substituents may be substituted or unsubstituted with an additional substituent.
본 명세서에 있어서, 할로겐기는 불소, 염소, 브롬 또는 요오드가 될 수 있다.In the present specification, the halogen group may be fluorine, chlorine, bromine or iodine.
본 명세서에 있어서, 이미드기의 탄소수는 특별히 한정되지 않으나, 탄소수 1 내지 25인 것이 바람직하다. 구체적으로 하기와 같은 구조의 화합물이 될 수 있으나, 이에 한정되는 것은 아니다.In the present specification, the number of carbon atoms of the imide group is not particularly limited, but is preferably 1 to 25 carbon atoms. Specifically, it may be a compound having the following structure, but is not limited thereto.
본 명세서에 있어서, 아미드기는 아미드기의 질소가 수소, 탄소수 1 내지 25의 직쇄, 분지쇄 또는 고리쇄 알킬기 또는 탄소수 6 내지 25의 아릴기로 1 또는 2 치환될 수 있다. 구체적으로, 하기 구조식의 화합물이 될 수 있으나, 이에 한정되는 것은 아니다.In the present specification, the amide group may be mono- or di-substituted by nitrogen of the amide group with hydrogen, a straight-chain, branched-chain or cyclic alkyl group having 1 to 25 carbon atoms or an aryl group having 6 to 25 carbon atoms. Specifically, it may be a compound of the following structural formula, but is not limited thereto.
본 명세서에 있어서, 상기 알킬기는 직쇄 또는 분지쇄일 수 있고, 탄소수는 특별히 한정되지 않으나 1 내지 50인 것이 바람직하다. 구체적인 예로는 메틸, 에틸, 프로필, n-프로필, 이소프로필, 부틸, n-부틸, 이소부틸, tert-부틸, sec-부틸, 1-메틸-부틸, 1-에틸-부틸, 펜틸, n-펜틸, 이소펜틸, 네오펜틸, tert-펜틸, 헥실, n-헥실, 1-메틸펜틸, 2-메틸펜틸, 4-메틸-2-펜틸, 3,3-디메틸부틸, 2-에틸부틸, 헵틸, n-헵틸, 1-메틸헥실, 시클로펜틸메틸, 시클로헥틸메틸, 옥틸, n-옥틸, tert-옥틸, 1-메틸헵틸, 2-에틸헥실, 2-프로필펜틸, n-노닐, 2,2-디메틸헵틸, 1-에틸-프로필, 1,1-디메틸-프로필, 이소헥실, 2-메틸펜틸, 4-메틸헥실 및 5-메틸헥실 등이 있으나, 이들에 한정되지 않는다.In the present specification, the alkyl group may be linear or branched, and the number of carbon atoms is not particularly limited, but is preferably 1 to 50. Specific examples include methyl, ethyl, propyl, n-propyl, isopropyl, butyl, n-butyl, isobutyl, tert-butyl, sec- N-pentyl, 3-dimethylbutyl, 2-ethylbutyl, heptyl, n-hexyl, N-octyl, 2-ethylhexyl, 2-propylpentyl, n-nonyl, 2,2-dimethyl Heptyl, 1-ethyl-propyl, 1,1-dimethyl-propyl, isohexyl, 2-methylpentyl, 4-methylhexyl and 5-methylhexyl.
본 명세서에 있어서, 시클로알킬기는 특별히 한정되지 않으나, 탄소수 3 내지 60인 것이 바람직하며, 구체적으로 시클로프로필, 시클로부틸, 시클로펜틸, 3-메틸시클로펜틸, 2,3-디메틸시클로펜틸, 시클로헥실, 3-메틸시클로헥실, 4-메틸시클로헥실, 2,3-디메틸시클로헥실, 3,4,5-트리메틸시클로헥실, 4-tert-부틸시클로헥실, 시클로헵틸 및 시클로옥틸 등이 있으나, 이에 한정되지 않는다. In the present specification, the cycloalkyl group is not particularly limited, but preferably has 3 to 60 carbon atoms. Specific examples thereof include cyclopropyl, cyclobutyl, cyclopentyl, 3-methylcyclopentyl, 2,3-dimethylcyclopentyl, But are not limited to, 3-methylcyclohexyl, 4-methylcyclohexyl, 2,3-dimethylcyclohexyl, 3,4,5-trimethylcyclohexyl, 4-tert- butylcyclohexyl, cycloheptyl and cyclooctyl Do not.
본 명세서에 있어서, 상기 알콕시기는 직쇄, 분지쇄 또는 고리쇄일 수 있다. 알콕시기의 탄소수는 특별히 한정되지 않으나, 탄소수 1 내지 20인 것이 바람직하다. 구체적으로, 메톡시, 에톡시, n-프로폭시, 이소프로폭시, i-프로필옥시, n-부톡시, 이소부톡시, tert-부톡시, sec-부톡시, n-펜틸옥시, 네오펜틸옥시, 이소펜틸옥시, n-헥실옥시, 3,3-디메틸부틸옥시, 2-에틸부틸옥시, n-옥틸옥시, n-노닐옥시, n-데실옥시, 벤질옥시 및 p-메틸벤질옥시 등이 될 수 있으나, 이에 한정되는 것은 아니다.In the present specification, the alkoxy group may be linear, branched or cyclic. The number of carbon atoms of the alkoxy group is not particularly limited, but is preferably 1 to 20 carbon atoms. Specific examples include methoxy, ethoxy, n-propoxy, isopropoxy, i-propyloxy, n-butoxy, isobutoxy, tert-butoxy, sec-butoxy, n-pentyloxy, neopentyloxy, N-hexyloxy, n-hexyloxy, 3,3-dimethylbutyloxy, 2-ethylbutyloxy, n-octyloxy, n-nonyloxy, n-decyloxy, benzyloxy and p- But is not limited thereto.
본 명세서에 있어서, 상기 알케닐기는 직쇄 또는 분지쇄일 수 있고, 탄소수는 특별히 한정되지 않으나, 2 내지 40인 것이 바람직하다. 구체적인 예로는 비닐, 1-프로페닐, 이소프로페닐, 1-부테닐, 2-부테닐, 3-부테닐, 1-펜테닐, 2-펜테닐, 3-펜테닐, 3-메틸-1-부테닐, 1,3-부타디에닐, 알릴, 1-페닐비닐-1-일, 2-페닐비닐-1-일, 2,2-디페닐비닐-1-일, 2-페닐-2-(나프틸-1-일)비닐-1-일, 2,2-비스(디페닐-1-일)비닐-1-일, 스틸베닐기 및 스티레닐기 등이 있으나 이들에 한정되지 않는다.In the present specification, the alkenyl group may be straight-chain or branched, and the number of carbon atoms is not particularly limited, but is preferably 2 to 40. Specific examples include vinyl, 1-propenyl, isopropenyl, 1-butenyl, 2-butenyl, 3-butenyl, 1-pentenyl, Butenyl, allyl, 1-phenylvinyl-1-yl, 2-phenylvinyl-1-yl, (Diphenyl-1-yl) vinyl-1-yl, stilbenyl, and styrenyl groups.
본 명세서에 있어서, 실릴기는 구체적으로 트리메틸실릴기, 트리에틸실릴기, t-부틸디메틸실릴기, 비닐디메틸실릴기, 프로필디메틸실릴기, 트리페닐실릴기, 디페닐실릴기 및 페닐실릴기 등이 있으나 이에 한정되지 않는다. In the present specification, the silyl group specifically includes a trimethylsilyl group, a triethylsilyl group, a t-butyldimethylsilyl group, a vinyldimethylsilyl group, a propyldimethylsilyl group, a triphenylsilyl group, a diphenylsilyl group, But are not limited thereto.
본 명세서에 있어서, 붕소기는 -BR100R101일 수 있으며, 상기 R100 및 R101은 같거나 상이하고, 각각 독립적으로 수소; 중수소; 할로겐; 니트릴기; 치환 또는 비치환된 탄소수 3 내지 30의 단환 또는 다환의 시클로알킬기; 치환 또는 비치환된 탄소수 1 내지 30의 직쇄 또는 분지쇄의 알킬기; 치환 또는 비치환된 탄소수 6 내지 30의 단환 또는 다환의 아릴기; 및 치환 또는 비치환된 탄소수 2 내지 30의 단환 또는 다환의 헤테로아릴기로 이루어진 군으로부터 선택될 수 있다.In the present specification, the boron group may be -BR 100 R 101 , wherein R 100 and R 101 are the same or different and each independently hydrogen; heavy hydrogen; halogen; A nitrile group; A substituted or unsubstituted monocyclic or polycyclic cycloalkyl group having 3 to 30 carbon atoms; A substituted or unsubstituted, straight or branched chain alkyl group having 1 to 30 carbon atoms; A substituted or unsubstituted monocyclic or polycyclic aryl group having 6 to 30 carbon atoms; And a substituted or unsubstituted monocyclic or polycyclic heteroaryl group having 2 to 30 carbon atoms.
본 명세서에 있어서, 포스핀옥사이드기는 구체적으로 디페닐포스핀옥사이드기, 디나프틸포스핀옥사이드 등이 있으나, 이에 한정되는 것은 아니다.In the present specification, the phosphine oxide group specifically includes a diphenylphosphine oxide group, dinaphthylphosphine oxide, and the like, but is not limited thereto.
본 명세서에 있어서, 아릴기는 단환식 아릴기 또는 다환식 아릴기일 수 있으며, 탄소수 1 내지 25의 알킬기 또는 탄소수 1 내지 25의 알콕시기가 치환되는 경우를 포함한다. 또한, 본 명세서 내에서의 아릴기는 방향족고리를 의미할 수 있다.In the present specification, the aryl group may be a monocyclic aryl group or a polycyclic aryl group, and includes a case where an alkyl group having 1 to 25 carbon atoms or an alkoxy group having 1 to 25 carbon atoms is substituted. In addition, an aryl group in the present specification may mean an aromatic ring.
상기 아릴기가 단환식 아릴기인 경우 탄소수는 특별히 한정되지 않으나, 탄소수 6 내지 25인 것이 바람직하다. 구체적으로 단환식 아릴기로는 페닐기, 바이페닐기 및 터페닐기 등이 될 수 있으나, 이에 한정되는 것은 아니다. When the aryl group is a monocyclic aryl group, the number of carbon atoms is not particularly limited, but is preferably 6 to 25 carbon atoms. Specific examples of the monocyclic aryl group include phenyl group, biphenyl group, terphenyl group, and the like, but are not limited thereto.
상기 아릴기가 다환식 아릴기인 경우 탄소수는 특별히 한정되지 않으나. 탄소수 10 내지 24인 것이 바람직하다. 구체적으로 다환식 아릴기로는 나프틸기, 안트라세닐기, 페난트릴기, 파이레닐기, 페릴레닐기, 크라이세닐기 및 플루오레닐기 등이 될 수 있으나, 이에 한정되는 것은 아니다.When the aryl group is a polycyclic aryl group, the number of carbon atoms is not particularly limited. And preferably has 10 to 24 carbon atoms. Specific examples of the polycyclic aryl group include, but are not limited to, a naphthyl group, an anthracenyl group, a phenanthryl group, a pyrenyl group, a perylenyl group, a klycenyl group and a fluorenyl group.
본 명세서에 있어서, 플루오레닐기는 2개의 고리 유기화합물이 1개의 원자를 통하여 연결된 구조이다.In the present specification, a fluorenyl group is a structure in which two cyclic organic compounds are connected through one atom.
본 명세서에 있어서, 상기 플루오레닐기는 치환될 수 있으며, 인접한 치환기들이 서로 결합하여 고리를 형성할 수 있다. In the present specification, the fluorenyl group may be substituted, and adjacent substituents may be bonded to each other to form a ring.
상기 플루오레닐기가 치환되는 경우, , , 및 등이 될 수 있다. 다만, 이에 한정되는 것은 아니다.When the fluorenyl group is substituted, , , And And the like. However, the present invention is not limited thereto.
본 명세서에 있어서, 헤테로아릴기는 이종 원소로 O, N 및 S 중 1개 이상을 포함하는 헤테로아릴기로서, 탄소수는 특별히 한정되지 않으나, 탄소수 2 내지 60인 것이 바람직하다. 헤테로아릴기의 예로는 싸이오펜기, 퓨란기, 피롤기, 이미다졸기, 티아졸기, 옥사졸기, 옥사디아졸기, 피리딜기, 비피리딜기, 피리미딜기, 트리아진기, 트리아졸기, 아크리딜기, 피리다진기, 피라지닐기, 퀴놀리닐기, 퀴나졸린기, 퀴녹살리닐기, 프탈라지닐기, 피리도 피리미디닐기, 피리도 피라지닐기, 피라지노 피라지닐기, 이소퀴놀린기, 인돌기, 카바졸기, 벤조옥사졸기, 벤조이미다졸기, 벤조티아졸기, 벤조카바졸기, 벤조싸이오펜기, 디벤조싸이오펜기, 벤조퓨라닐기, 페난쓰롤린기(phenanthroline), 티아졸릴기, 이소옥사졸릴기, 옥사디아졸릴기, 티아디아졸릴기, 벤조티아디아졸릴기, 벤조티아졸릴기, 페노티아지닐기 및 디벤조퓨라닐기 등이 있으나, 이들에만 한정되는 것은 아니다.In the present specification, the heteroaryl group is a heteroaryl group containing at least one of O, N and S as a hetero atom. The number of carbon atoms is not particularly limited, but is preferably 2 to 60 carbon atoms. Examples of the heteroaryl group include a thiophene group, a furane group, a furyl group, an imidazole group, a thiazole group, an oxazole group, an oxadiazole group, a pyridyl group, a bipyridyl group, a pyrimidyl group, , A pyridazinyl group, a pyrazinyl group, a quinolinyl group, a quinazolinyl group, a quinoxalinyl group, a phthalazinyl group, a pyridopyrimidinyl group, a pyridopyranyl group, a pyrazinopyranyl group, an isoquinoline group, , A carbazole group, a benzoxazole group, a benzoimidazole group, a benzothiazole group, a benzocarbazole group, a benzothiophene group, a dibenzothiophene group, a benzofuranyl group, a phenanthroline, a thiazolyl group, , A thiadiazolyl group, a thiadiazolyl group, a benzothiadiazolyl group, a benzothiazolyl group, a phenothiazinyl group, and a dibenzofuranyl group, but the present invention is not limited thereto.
본 명세서에 있어서, 헤테로고리기는 단환 또는 다환일 수 있으며, 방향족, 지방족 또는 방향족과 지방족의 축합고리일 수 있으며, 상기 헤테로아릴기의 예시 중에서 선택될 수 있다.In the present specification, the heterocyclic group may be monocyclic or polycyclic, and may be an aromatic, aliphatic or aromatic and aliphatic condensed ring, and examples thereof may be selected from the above heteroaryl groups.
본 명세서에 있어서, 아릴아민기의 예로는 치환 또는 비치환된 모노아릴아민기, 치환 또는 비치환된 디아릴아민기, 또는 치환 또는 비치환된 트리아릴아민기가 있다. 상기 아릴아민기 중의 아릴기는 단환식 아릴기일 수 있고, 다환식 아릴기일 수 있다. 상기 아릴기가 2 이상을 포함하는 아릴아민기는 단환식 아릴기, 다환식 아릴기, 또는 단환식아릴기와 다환식 아릴기를 동시에 포함할 수 있다. In the present specification, examples of the arylamine group include a substituted or unsubstituted monoarylamine group, a substituted or unsubstituted diarylamine group, or a substituted or unsubstituted triarylamine group. The aryl group in the arylamine group may be a monocyclic aryl group or a polycyclic aryl group. The arylamine group having at least two aryl groups may contain a monocyclic aryl group, a polycyclic aryl group, or a monocyclic aryl group and a polycyclic aryl group at the same time.
아릴 아민기의 구체적인 예로는 페닐아민, 나프틸아민, 비페닐아민, 안트라세닐아민, 3-메틸-페닐아민, 4-메틸-나프틸아민, 2-메틸-비페닐아민, 9-메틸-안트라세닐아민, 디페닐 아민기, 페닐 나프틸 아민기, 디톨릴 아민기, 페닐 톨릴 아민기, 카바졸 및 트리페닐 아민기 등이 있으나, 이에 한정되는 것은 아니다. Specific examples of the arylamine group include phenylamine, naphthylamine, biphenylamine, anthracenylamine, 3-methylphenylamine, 4-methyl-naphthylamine, 2-methyl- But are not limited to, cenylamine, diphenylamine, phenylnaphthylamine, ditolylamine, phenyltolylamine, carbazole and triphenylamine groups.
본 명세서에 있어서, 헤테로아릴아민기 중의 헤테로 아릴기는 전술한 헤테로고리기의 예시 중에서 선택될 수 있다.In the present specification, the heteroaryl group in the heteroarylamine group can be selected from the examples of the above-mentioned heterocyclic group.
본 명세서에 있어서, 아릴옥시기, 아릴티옥시기, 아릴술폭시기 및 아랄킬아민기 중의 아릴기는 전술한 아릴기의 예시와 같다. 구체적으로 아릴옥시기로는 페녹시, p-토릴옥시, m-토릴옥시, 3,5-디메틸-페녹시, 2,4,6-트리메틸페녹시, p-tert-부틸페녹시, 3-비페닐옥시, 4-비페닐옥시, 1-나프틸옥시, 2-나프틸옥시, 4-메틸-1-나프틸옥시, 5-메틸-2-나프틸옥시, 1-안트릴옥시, 2-안트릴옥시, 9-안트릴옥시, 1-페난트릴옥시, 3-페난트릴옥시, 9-페난트릴옥시 등이 있고, 아릴티옥시기로는 페닐티옥시기, 2-메틸페닐티옥시기, 4-tert-부틸페닐티옥시기 등이 있으며, 아릴술폭시기로는 벤젠술폭시기, p-톨루엔술폭시기 등이 있으나, 이에 한정되지 않는다.In the present specification, the aryl group in the aryloxy group, arylthioxy group, arylsulfoxy group and aralkylamine group is the same as the aforementioned aryl group. Specific examples of the aryloxy group include phenoxy, p-tolyloxy, m-tolyloxy, 3,5-dimethyl-phenoxy, 2,4,6-trimethylphenoxy, Naphthyloxy, 4-methyl-1-naphthyloxy, 5-methyl-2-naphthyloxy, 1-anthryloxy, 2-anthryl Phenanthryloxy, 9-phenanthryloxy and the like. Examples of the arylthioxy group include phenylthio group, 2-methylphenylthio group, 4-tert-butylphenyl And the like. Examples of the aryl sulfoxy group include a benzene sulfoxy group and a p-toluenesulfoxy group, but the present invention is not limited thereto.
본 명세서에 있어서, 알킬티옥시기, 알킬술폭시기 중의 알킬기는 전술한 알킬기의 예시와 같다. 구체적으로 알킬티옥시기로는 메틸티옥시기, 에틸티옥시기, tert-부틸티옥시기, 헥실티옥시기, 옥틸티옥시기 등이 있고, 알킬술폭시기로는 메실, 에틸술폭시기, 프로필술폭시기, 부틸술폭시기 등이 있으나, 이에 한정되지 않는다.In the present specification, the alkyl group in the alkylthio group and the alkylsulfoxy group is the same as the alkyl group described above. Specific examples of the alkyloxy group include a methylthio group, an ethylthio group, a tert-butylthio group, a hexylthio group and an octylthio group. Examples of the alkylsulfoxy group include a mesyl group, an ethylsulfoxy group, a propylsulfoxy group, But are not limited thereto.
본 명세서에 있어서, 2가의 연결기는 치환 또는 비치환된 알킬렌기; 치환 또는 비치환된 아릴렌기; 및 치환 또는 비치환된 헤테로아릴렌기로 이루어진 군에서 1 이상을 포함할 수 있다.In the present specification, the divalent linking group is a substituted or unsubstituted alkylene group; A substituted or unsubstituted arylene group; And a substituted or unsubstituted heteroarylene group.
본 명세서에 있어서, 알킬렌기는 알킬기에 결합 위치가 두 개 있는 것 즉 2가기를 의미한다. 이들은 각각 2가기인 것을 제외하고는 전술한 알킬기의 설명이 적용될 수 있다.In the present specification, an alkylene group means that the alkyl group has two bonding positions, i.e., divalent. The description of the above-mentioned alkyl groups can be applied, except that they are each 2 groups.
본 명세서에 있어서, 아릴렌기는 아릴기에 결합 위치가 두 개 있는 것 즉 2가기를 의미한다. 이들은 각각 2가기인 것을 제외하고는 전술한 아릴기의 설명이 적용될 수 있다.In the present specification, an arylene group means a divalent group having two bonding positions in an aryl group. The description of the aryl group described above can be applied except that each of these is 2 groups.
본 명세서에 있어서, 헤테로아릴렌기는 헤테로아릴기에 결합 위치가 두 개 있는 것 즉 2가기를 의미한다. 이들은 각각 2가기인 것을 제외하고는 전술한 헤테로아릴기의 설명이 적용될 수 있다.In the present specification, the heteroarylene group means that the heteroaryl group has two bonding positions, that is, divalent. The description of the above-mentioned heteroaryl groups can be applied, except that they are each 2 groups.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1은 하기 화학식 1-1로 표시된다.According to one embodiment of the present invention, the formula (1) is represented by the following formula (1-1).
[화학식 1-1][Formula 1-1]
상기 화학식 1-1에 있어서,In Formula 1-1,
n1, n2, n3, n4, X1 내지 X6, Y1 내지 Y7, R1 내지 R14, Ar1 및 Ar2의 정의는 상기 화학식 1과 동일하다.The definitions of n1, n2, n3, n4, X1 to X6, Y1 to Y7, R1 to R14, Ar1 and Ar2 are the same as those in the above formula (1).
본 명세서의 일 실시상태에 따르면, 상기 화학식 1에 있어서, X1 내지 X6은 N이다.According to one embodiment of the present invention, in the general formula (1), X 1 to X 6 are N.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1은 하기 화학식 1-2로 표시된다.According to one embodiment of the present invention, the formula (1) is represented by the following formula (1-2).
[화학식 1-2][Formula 1-2]
상기 화학식 1-2에 있어서,In Formula 1-2,
n1, n2, n3, n4, Y1 내지 Y7, R1 내지 R14, Ar1 및 Ar2의 정의는 상기 화학식 1과 동일하다.The definitions of n1, n2, n3, n4, Y1 to Y7, R1 to R14, Ar1 and Ar2 are the same as those of formula (1).
본 명세서의 일 실시상태에 따르면, 상기 화학식 1에 있어서, Y1 내지 Y4는 S이다.According to one embodiment of the present invention, in the formula (1), Y1 to Y4 are S.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1은 하기 화학식 1-3으로 표시된다.According to one embodiment of the present invention, Formula 1 is represented by Formula 1-3.
[화학식 1-3][Formula 1-3]
상기 화학식 1-3에 있어서,In Formula 1-3,
n1, n2, n3, n4, R1 내지 R14, Ar1 및 Ar2의 정의는 상기 화학식 1과 동일하다.The definitions of n1, n2, n3, n4, R1 to R14, Ar1 and Ar2 are the same as those of formula (1).
본 명세서의 일 실시상태에 따르면, 상기 화학식 1에 있어서, 상기 R1 내지 R14는 서로 같거나 상이하고, 각각 독립적으로 수소; 할로겐기; 치환 또는 비치환된 알킬기; 또는 치환 또는 비치환된 알콕시기이다.According to one embodiment of the present invention, in Formula 1, R1 to R14 are the same or different from each other and each independently hydrogen; A halogen group; A substituted or unsubstituted alkyl group; Or a substituted or unsubstituted alkoxy group.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1에 있어서, 상기 R1 내지 R14는 서로 같거나 상이하고, 각각 독립적으로 수소; 할로겐기; 알킬기; 또는 알콕시기이다.According to one embodiment of the present invention, in Formula 1, R1 to R14 are the same or different from each other and each independently hydrogen; A halogen group; An alkyl group; Or an alkoxy group.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1에 있어서, 상기 R1 내지 R14는 서로 같거나 상이하고, 각각 독립적으로 수소; 불소; 2-옥틸데카닐기; 또는 도데카녹시기이다.According to one embodiment of the present invention, in Formula 1, R1 to R14 are the same or different from each other and each independently hydrogen; Fluorine; 2-octyldecanyl; Or a dodecanoxy group.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1에 있어서, Ar1 및 Ar2는 서로 같거나 상이하고, 각각 독립적으로 수소; 알킬기; 또는 실릴기이다.According to one embodiment of the present invention, in the general formula (1), Ar1 and Ar2 are the same or different and each independently hydrogen; An alkyl group; Or a silyl group.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1에 있어서, Ar1 및 Ar2는 서로 같거나 상이하고, 각각 독립적으로 수소; n-헥실기; 또는 트리메틸실릴기이다.According to one embodiment of the present invention, in the general formula (1), Ar1 and Ar2 are the same or different and each independently hydrogen; n-hexyl group; Or a trimethylsilyl group.
본 명세서의 일 실시상태에 따르면, 상기 화학식 1에 있어서, Ar1 및 Ar2는 서로 같거나 상이하고, 각각 독립적으로 하기 구조 중 어느 하나이다.According to one embodiment of the present invention, in the general formula (1), Ar1 and Ar2 are the same or different and independently of each other are any of the following structures.
상기 구조에 있어서, In the above structure,
a는 1 내지 7의 정수이고, a is an integer of 1 to 7,
b 및 c는 각각 1 내지 4의 정수이며, b and c are each an integer of 1 to 4,
a가 2 이상인 경우, 2 이상의 R102는 서로 동일하거나 상이하고, When a is 2 or more, two or more R102 are the same or different from each other,
b가 2 이상인 경우, 2 이상의 R103은 서로 동일하거나 상이하며, When b is 2 or more, two or more R103 are the same or different from each other,
c가 2 이상인 경우, 2 이상의 R1104는 서로 동일하거나 상이하며, When c is 2 or more, two or more R1104 are the same or different from each other,
R101 내지 R107은 서로 동일하거나 상이하고, 각각 독립적으로 수소; 중수소; 할로겐기; 니트릴기; 니트로기; 이미드기; 아미드기; 히드록시기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 알킬아민기; 치환 또는 비치환된 아랄킬아민기; 치환 또는 비치환된 아릴아민기; 치환 또는 비치환된 헤테로아릴아민기; 치환 또는 비치환된 아릴기; 또는 치환 또는 비치환된 헤테로아릴기이다.R101 to R107 are the same or different from each other, and each independently hydrogen; heavy hydrogen; A halogen group; A nitrile group; A nitro group; Imide; Amide group; A hydroxy group; A substituted or unsubstituted alkyl group; A substituted or unsubstituted cycloalkyl group; A substituted or unsubstituted alkoxy group; A substituted or unsubstituted aryloxy group; A substituted or unsubstituted alkylthio group; A substituted or unsubstituted arylthio group; A substituted or unsubstituted alkylsulfoxy group; A substituted or unsubstituted arylsulfoxy group; A substituted or unsubstituted alkenyl group; A substituted or unsubstituted silyl group; A substituted or unsubstituted boron group; A substituted or unsubstituted alkylamine group; A substituted or unsubstituted aralkylamine group; A substituted or unsubstituted arylamine group; A substituted or unsubstituted heteroarylamine group; A substituted or unsubstituted aryl group; Or a substituted or unsubstituted heteroaryl group.
본 명세서의 일 실시상태에 따르면, 상기 Ar1은 이다.According to one embodiment of the present disclosure, to be.
본 명세서의 일 실시상태에 따르면, 상기 Ar2는 이다.According to one embodiment of the present disclosure, Ar2 is to be.
본 명세서의 일 실시상태에 따르면, 상기 R101는 치환 또는 비치환된 알킬기이다.According to one embodiment of the present invention, R101 is a substituted or unsubstituted alkyl group.
본 명세서의 일 실시상태에 따르면, 상기 R101는 치환 또는 비치환된 탄소수 1 내지 15 직쇄 또는 분지쇄의 알킬기이다.According to one embodiment of the present invention, R101 is a substituted or unsubstituted C1 to C15 linear or branched alkyl group.
본 명세서의 일 실시상태에 따르면, 상기 R101는 치환 또는 비치환된 옥틸기이다.According to one embodiment of the present invention, R101 is a substituted or unsubstituted octyl group.
본 명세서의 일 실시상태에 따르면, 상기 n1은 1이다.According to one embodiment of the present disclosure, n1 is one.
본 명세서의 일 실시상태에 따르면, 상기 n1은 2이다.According to one embodiment of the present disclosure, n1 is 2.
본 명세서의 일 실시상태에 따르면, 상기 n2은 1이다.According to one embodiment of the present disclosure, n2 is one.
본 명세서의 일 실시상태에 따르면, 상기 n2은 2이다.According to one embodiment of the present disclosure, n2 is 2.
본 명세서의 일 실시상태에 따르면, 상기 n3은 1이다.According to one embodiment of the present disclosure, n3 is one.
본 명세서의 일 실시상태에 따르면, 상기 n3은 2이다.According to one embodiment of the present disclosure, n3 is 2.
본 명세서의 일 실시상태에 따르면, 상기 n4은 1이다.According to one embodiment of the present disclosure, n4 is one.
본 명세서의 일 실시상태에 따르면, 상기 n4은 2이다.According to one embodiment of the present disclosure, n4 is 2.
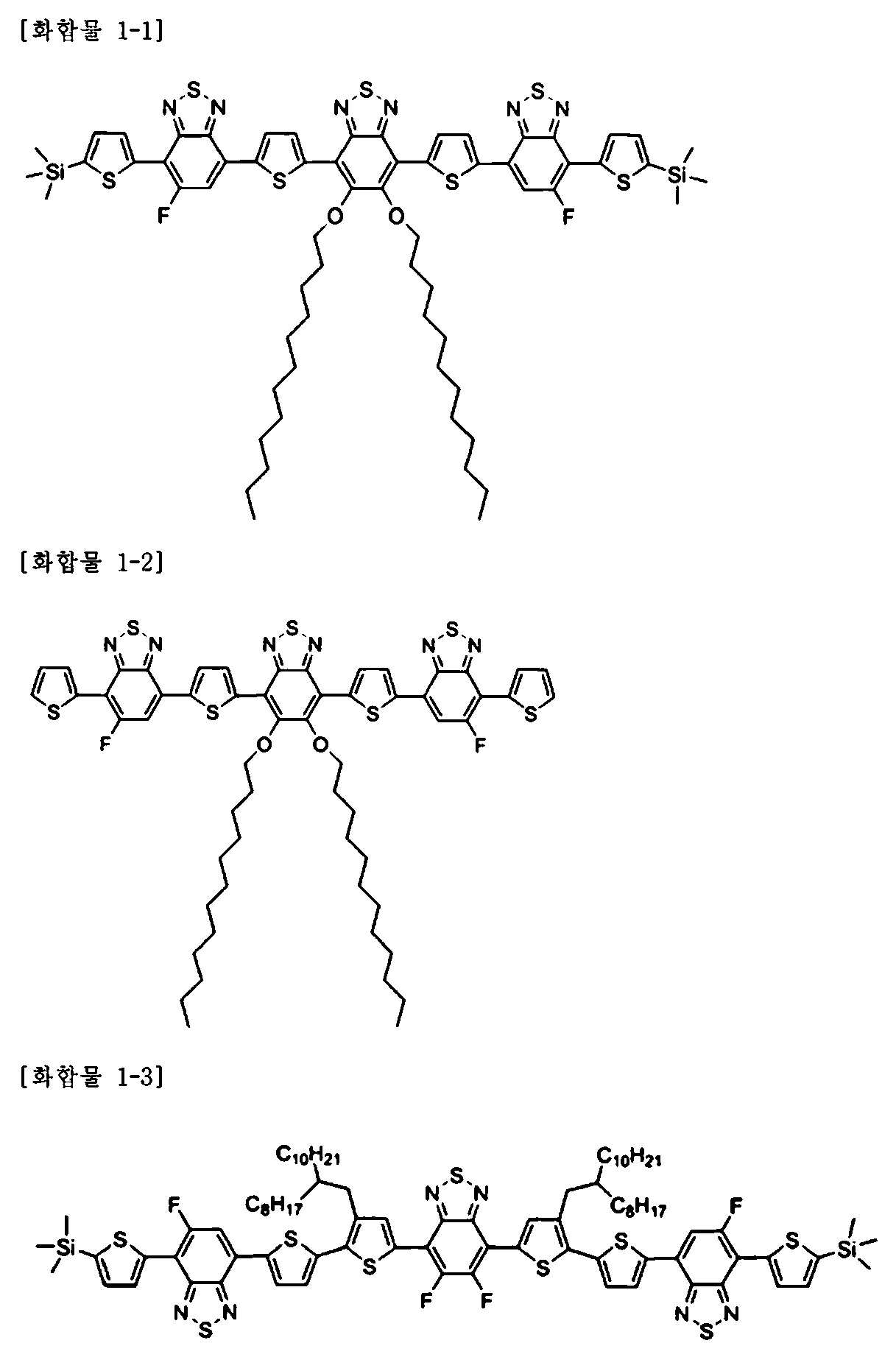
본 명세서의 일 실시상태에 따르면, 상기 화학식 1은 하기 화합물 1-1 내지 1-7 중에서 선택되는 어느 하나이다.According to one embodiment of the present invention, Formula 1 is any one selected from the following Compounds 1-1 to 1-7.
본 명세서의 일 실시상태에 따르면, 제1 전극; 상기 제1 전극과 대향하여 구비되는 제2 전극; 및 상기 제1 전극과 제2 전극 사이에 구비되고, 광활성층을 포함하는 1층 이상의 유기물층을 포함하고, 상기 유기물층 중 1층 이상은 상기 헤테로환 화합물을 포함하는 것인 유기 태양 전지를 제공한다. According to one embodiment of the present disclosure, there is provided a liquid crystal display comprising: a first electrode; A second electrode facing the first electrode; And at least one organic compound layer including a photoactive layer disposed between the first electrode and the second electrode, wherein at least one of the organic compound layers includes the heterocyclic compound.
본 명세서의 일 실시예에 따른 유기 태양 전지는 제1 전극, 광활성층 및 제2 전극을 포함한다. 상기 유기 태양 전지는 기판, 정공수송층 및/또는 전자수송층이 더 포함될 수 있다. An organic solar cell according to an embodiment of the present invention includes a first electrode, a photoactive layer, and a second electrode. The organic solar cell may further include a substrate, a hole transporting layer, and / or an electron transporting layer.
본 명세서의 일 실시상태에 따르면, 상기 유기 태양 전지가 외부 광원으로부터 광자를 받으면 전자 주개와 전자 받개 사이에서 전자와 정공이 발생한다. 발생된 정공은 전자 도너층을 통하여 양극으로 수송된다. According to one embodiment of the present invention, when the organic solar cell receives photons from an external light source, electrons and holes are generated between the electron beams and the electron acceptors. The generated holes are transported to the anode through the electron donor layer.
본 명세서의 일 실시상태에 따르면, 상기 유기물층은 정공 수송층, 정공 주입층 또는 정공 수송과 정공 주입을 동시에 하는 층을 포함하고, 상기 정공 수송층, 정공 주입층 또는 정공 수송과 정공 주입을 동시에 하는 층은 상기 헤테로환 화합물을 포함한다. According to one embodiment of the present invention, the organic material layer includes a hole transporting layer, a hole injecting layer, or a layer simultaneously transporting holes and holes, and the hole transporting layer, the hole injecting layer, or the layer simultaneously transporting holes and injecting holes And the above heterocyclic compound.
또 하나의 일 실시상태에 있어서, 상기 유기물층은 전자주입층, 전자 수송층 또는 전자 주입과 전자 수송을 동시에 하는 층을 포함하고, 상기 전자주입층, 전자 수송층 또는 전자 주입과 전자 수송을 동시에 하는 층은 상기 헤테로환 화합물을 포함한다. In another embodiment, the organic material layer may include an electron injection layer, an electron transport layer, or a layer that simultaneously performs electron injection and electron transport, and the electron injection layer, the electron transport layer, And the above heterocyclic compound.
도 1 본 명세서의 일 실시상태에 따른 유기 태양 전지를 나타낸 도이다.1 illustrates an organic solar cell according to an embodiment of the present invention.
본 명세서의 일 실시상태에 따르면, 상기 유기 태양 전지가 외부 광원으로부터 광자를 받으면 전자 주개와 전자 받개 사이에서 전자와 정공이 발생한다. 발생된 정공은 전자 도너층을 통하여 양극으로 수송된다. According to one embodiment of the present invention, when the organic solar cell receives photons from an external light source, electrons and holes are generated between the electron beams and the electron acceptors. The generated holes are transported to the anode through the electron donor layer.
본 명세서의 일 실시상태에 따르면, 상기 유기 태양 전지는 부가적인 유기물층을 더 포함할 수 있다. 상기 유기 태양 전지는 여러 기능을 동시에 갖는 유기물을 사용하여 유기물층의 수를 감소시킬 수 있다.According to one embodiment of the present disclosure, the organic solar cell may further include an additional organic layer. The organic solar cell can reduce the number of organic layers by using organic materials having various functions at the same time.
본 명세서의 일 실시상태에 따르면, 상기 제1 전극은 애노드이고, 상기 제2 전극은 캐소드이다. 또 하나의 실시상태에 있어서, 상기 제1 전극은 캐소드이고, 상기 제2 전극은 애노드이다. According to one embodiment of the present disclosure, the first electrode is an anode and the second electrode is a cathode. In another embodiment, the first electrode is a cathode and the second electrode is an anode.
본 명세서의 일 실시상태에 따르면, 유기 태양 전지는 캐소드, 광활성층 및 애노드 순으로 배열될 수도 있고, 애노드, 광활성층 및 캐소드 순으로 배열될 수도 있으나, 이에 한정되지 않는다. According to one embodiment of the present disclosure, the organic solar cell may be arranged in the order of the cathode, the photoactive layer, and the anode, and may be arranged in the order of the anode, the photoactive layer, and the cathode.
또 하나의 실시상태에 있어서, 상기 유기 태양 전지는 애노드, 정공수송층, 광활성층, 전자수송층 및 캐소드 순으로 배열될 수도 있고, 캐소드, 전자수송층, 광활성층, 정공수송층 및 애노드 순으로 배열될 수도 있으나, 이에 한정되지 않는다.In another embodiment, the organic solar cell may be arranged in the order of an anode, a hole transporting layer, a photoactive layer, an electron transporting layer and a cathode, and may be arranged in the order of a cathode, an electron transporting layer, a photoactive layer, a hole transporting layer, , But is not limited thereto.
본 명세서의 일 실시상태에 따르면, 상기 유기 태양 전지는 노멀(Normal)구조이다. 상기 노멀구조에서 기판, 애노드, 광활성층을 포함하는 유기물층 및 캐소드의 순서로 적층될 수 있다. According to one embodiment of the present invention, the organic solar cell has a normal structure. In the normal structure, the substrate, the anode, the organic material layer including the photoactive layer, and the cathode may be stacked in this order.
본 명세서의 일 실시상태에 따르면, 상기 유기 태양 전지는 인버티드(Inverted) 구조이다. 상기 인버티드 구조에서는 기판, 캐소드, 광활성층을 포함하는 유기물층 및 애노드의 순서로 적층될 수 있다. According to one embodiment of the present invention, the organic solar cell is an inverted structure. In the inverted structure, the substrate, the cathode, the organic material layer including the photoactive layer, and the anode may be stacked in this order.
본 명세서의 일 실시상태에 따르면, 상기 유기 태양 전지는 탠덤 (tandem) 구조이다. According to one embodiment of the present invention, the organic solar cell is a tandem structure.
본 명세서의 일 실시상태에 따른 유기태양 전지는 광활성층이 1층 또는 2층 이상일 수 있다. 상기 탠덤 구조에서는 광활성층을 2 이상 포함할 수 있다. The organic solar cell according to one embodiment of the present disclosure may have one photoactive layer or two or more layers. In the tandem structure, two or more photoactive layers may be included.
또 하나의 실시상태에 있어서, 버퍼층이 광활성층과 정공수송층 사이 또는 광활성층과 전자수송층 사이에 구비될 수 있다. 이때, 정공 주입층이 애노드와 정공수송층사이에 더 구비될 수 있다. 또한, 전자주입층이 캐소드와 전자수송층 사이에 더 구비될 수 있다. In another embodiment, a buffer layer may be provided between the photoactive layer and the hole transporting layer or between the photoactive layer and the electron transporting layer. At this time, a hole injection layer may be further provided between the anode and the hole transport layer. Further, an electron injecting layer may be further provided between the cathode and the electron transporting layer.
본 명세서의 일 실시상태에 따르면, 상기 광활성층은 전자 주개 및 받개로 이루어진 군에서 선택되는 1 또는 2 이상을 포함하고, 상기 전자 주개물질은 상기 헤테로환 화합물을 포함한다. According to one embodiment of the present invention, the photoactive layer includes one or more selected from the group consisting of an electron donor and a donor, and the electron donor material includes the heterocyclic compound.
본 명세서의 일 실시상태에 따르면, 상기 전자 받개 물질은 플러렌, 플러렌 유도체, 바소쿠프로인, 반도체성 원소, 반도체성 화합물 및 이들의 조합으로 이루어진 군에서 선택될 수 있다. 구체적으로 플러렌(fullerene), 플러렌 유도체(PCBM((6,6)-phenyl-C61-butyric acid-methylester) 또는 PCBCR((6,6)-phenyl-C61-butyric acid-cholesteryl ester), 페릴렌(perylene) PBI(polybenzimidazole), 및 PTCBI(3,4,9,10-perylene-tetracarboxylic bis-benzimidazole)로 이루어진 군에서 선택되는 1 또는 2 이상의 화합물이다. According to one embodiment of the present disclosure, the electron acceptor material may be selected from the group consisting of fullerene, fullerene derivatives, vicocloin, semiconducting elements, semiconducting compounds, and combinations thereof. (6,6) -phenyl-C61-butyric acid-methylester) or PCBCR ((6,6) -phenyl-C61-butyric acid-cholesteryl ester), perylene perylene, polybenzimidazole (PBI), and 3,4,9,10-perylene-tetracarboxylic bis-benzimidazole (PTCBI).
본 명세서의 일 실시상태에 따르면, 상기 전자 주개 및 전자 받개는 벌크 헤테로 정션(BHJ)을 구성한다. According to one embodiment of the present disclosure, the electron donor and the electron acceptor constitute a bulk heterojunction (BHJ).
벌크 헤테로 정션이란 광활성층에서 전자 주개 물질과 전자 받개 물질이 서로 섞여 있는 것을 의미한다.Bulk heterojunction means that the electron donor material and the electron acceptor material are mixed in the photoactive layer.
본 명세서의 일 실시상태에 따르면, 상기 광활성층은 n 형 유기물층 및 p 형 유기물층을 포함하는 이층 박막(bilayer) 구조이며, 상기 p형 유기물층은 상기 헤테로환 화합물을 포함한다. According to an embodiment of the present invention, the photoactive layer is a bilayer structure including an n-type organic layer and a p-type organic layer, and the p-type organic layer includes the heterocyclic compound.
본 명세서에서 상기 기판은 투명성, 표면평활성, 취급용이성 및 방수성이 우수한 유리기판 또는 투명 플라스틱 기판이 될 수 있으나, 이에 한정되지 않으며, 유기 태양 전지에 통상적으로 사용되는 기판이면 제한되지 않는다. 구체적으로 유리 또는 PET(polyethylene terephthalate), PEN(polyethylene naphthalate), PP(polypropylene), PI(polyimide), TAC(triacetyl cellulose) 등이 있으나. 이에 한정되는 것은 아니다. In this specification, the substrate may be a glass substrate or a transparent plastic substrate having excellent transparency, surface smoothness, ease of handling, and waterproofness, but is not limited thereto, and is not limited as long as it is a substrate commonly used in organic solar cells. Specific examples include glass or polyethylene terephthalate, polyethylene naphthalate (PEN), polypropylene (PP), polyimide (PI), and triacetyl cellulose (TAC) But is not limited thereto.
상기 애노드 전극은 투명하고 전도성이 우수한 물질이 될 수 있으나, 이에 한정되지 않는다. 바나듐, 크롬, 구리, 아연, 금과 같은 금속 또는 이들의 합금; 아연 산화물, 인듐 산화물, 인듐주석 산화물(ITO), 인듐아연 산화물(IZO)과 같은 금속 산화물; ZnO:Al 또는 SNO2 : Sb와 같은 금속과 산화물의 조합; 및 폴리(3-메틸싸이오펜), 폴리[3,4-(에틸렌-1,2-디옥시)싸이오펜](PEDOT), 폴리피롤 및 폴리아닐린과 같은 전도성 고분자 등이 있으나, 이들에만 한정되는 것은 아니다.The anode electrode may be a transparent material having excellent conductivity, but is not limited thereto. Metals such as vanadium, chromium, copper, zinc, and gold, or alloys thereof; Metal oxides such as zinc oxide, indium oxide, indium tin oxide (ITO), and indium zinc oxide (IZO); ZnO: Al or SNO 2: a combination of a metal and an oxide such as Sb; And conductive polymers such as poly (3-methylthiophene), poly [3,4- (ethylene-1,2-dioxy) thiophene] (PEDOT), polypyrrole and polyaniline, but are not limited thereto .
상기 애노드 전극의 형성 방법은 특별히 한정되지 않으나, 예컨대 스퍼터링, E-빔, 열증착, 스핀코팅, 스크린 프린팅, 잉크젯 프린팅, 닥터 블레이드 또는 그라비아 프린팅법을 사용하여 기판의 일면에 도포되거나 필름형태로 코팅됨으로써 형성될 수 있다.The method of forming the anode electrode is not particularly limited and may be applied to one surface of the substrate or may be coated in a film form using, for example, sputtering, E-beam, thermal evaporation, spin coating, screen printing, inkjet printing, doctor blade or gravure printing . ≪ / RTI >
상기 애노드 전극을 기판 상에 형성하는 경우, 이는 세정, 수분제거 및 친수성 개질 과정을 거칠 수 있다. When the anode electrode is formed on a substrate, it may undergo cleaning, moisture removal and hydrophilic reforming processes.
예컨대, 패터닝된 ITO 기판을 세정제, 아세톤, 이소프로필 알코올(IPA)로 순차적으로 세정한 다음, 수분 제거를 위해 가열판에서 100 내지150℃에서 1 내지 30분간, 바람직하게는 120℃에서 10분간 건조하고, 기판이 완전히 세정되면 기판 표면을 친수성으로 개질한다.For example, the patterned ITO substrate is sequentially washed with a cleaning agent, acetone, and isopropyl alcohol (IPA), and then dried on a heating plate at 100 to 150 ° C for 1 to 30 minutes, preferably 120 ° C for 10 minutes , And the substrate surface is hydrophilically reformed when the substrate is completely cleaned.
상기와 같은 표면 개질을 통해 접합 표면 전위를 광활성층의 표면 전위에 적합한 수준으로 유지할 수 있다. 또한, 개질 시 애노드 전극 위에 고분자 박막의 형성이 용이해지고, 박막의 품질이 향상될 수도 있다. Through such surface modification, the junction surface potential can be maintained at a level suitable for the surface potential of the photoactive layer. Further, in the modification, the formation of the polymer thin film on the anode electrode is facilitated, and the quality of the thin film may be improved.
애노드 전극의 위한 전처리 기술로는 a) 평행 평판형 방전을 이용한 표면 산화법, b) 진공상태에서 UV 자외선을 이용하여 생성된 오존을 통해 표면을 산화하는 방법, 및 c) 플라즈마에 의해 생성된 산소 라디칼을 이용하여 산화하는 방법 등이 있다.Pretreatment techniques for the anode electrode include a) surface oxidation using a parallel plate discharge, b) a method of oxidizing the surface through ozone generated using UV ultraviolet radiation in vacuum, and c) oxygen radicals generated by the plasma And the like.
애노드 전극 또는 기판의 상태에 따라 상기 방법 중 한가지를 선택할 수 있다. 다만, 어느 방법을 이용하든지 공통적으로 애노드 전극 또는 기판 표면의 산소이탈을 방지하고 수분 및 유기물의 잔류를 최대한 억제하는 것이 바람직하다. 이 때, 전처리의 실질적인 효과를 극대화할 수 있다. One of the above methods can be selected depending on the state of the anode electrode or the substrate. However, whichever method is used, it is preferable to prevent oxygen from escaping from the surface of the anode electrode or the substrate and to suppress the residual of moisture and organic matter as much as possible. At this time, the substantial effect of the pretreatment can be maximized.
구체적인 예로서, UV를 이용하여 생성된 오존을 통해 표면을 산화하는 방법을 사용할 수 있다. 이 때, 초음파 세정 후 패터닝된 ITO 기판을 가열판(hot plate)에서 베이킹(baking)하여 잘 건조시킨 다음, 챔버에 투입하고, UV 램프를 작용시켜 산소 가스가 UV 광과 반응하여 발생하는 오존에 의하여 패터닝된 ITO 기판을 세정할 수 있다. As a specific example, a method of oxidizing the surface through ozone generated using UV can be used. At this time, the ITO substrate patterned after the ultrasonic cleaning is dried by baking on a hot plate, and then put into a chamber. Then, by the action of a UV lamp, ozone generated by reaction of oxygen gas with UV light The patterned ITO substrate can be cleaned.
그러나, 본 명세서에 있어서의 패터닝된 ITO 기판의 표면 개질 방법은 특별히 한정시킬 필요는 없으며, 기판을 산화시키는 방법이라면 어떠한 방법도 무방하다.However, the method of modifying the surface of the patterned ITO substrate in the present specification is not particularly limited, and any method may be used as long as it is a method of oxidizing the substrate.
상기 캐소드 전극은 일함수가 작은 금속이 될 수 있으나, 이에 한정되지 않는다. 구체적으로 마그네슘, 칼슘, 나트륨, 칼륨, 티타늄, 인듐, 이트륨, 리튬, 가돌리늄, 알루미늄, 은, 주석 및 납과 같은 금속 또는 이들의 합금; 또는 LiF/Al, LiO2/Al, LiF/Fe, Al:Li, Al:BaF2, Al:BaF2:Ba와 같은 다층 구조의 물질이 될 수 있으나, 이에 한정되는 것은 아니다. The cathode electrode may be a metal having a small work function, but is not limited thereto. Specifically, metals such as magnesium, calcium, sodium, potassium, titanium, indium, yttrium, lithium, gadolinium, aluminum, silver, tin and lead or alloys thereof; Or a multilayer structure material such as LiF / Al, LiO 2 / Al, LiF / Fe, Al: Li, Al: BaF 2 and Al: BaF 2 : Ba.
상기 캐소드 전극은 5x10- 7torr 이하의 진공도를 보이는 열증착기 내부에서 증착되어 형성될 수 있으나, 이 방법에만 한정되는 것은 아니다.The cathode may be deposited in a thermal evaporator having a degree of vacuum of 5 x 10 < -7 > torr or less, but the method is not limited thereto.
상기 정공수송층 및/또는 전자수송층 물질은 광활성층에서 분리된 전자와 정공을 전극으로 효율적으로 전달시키는 역할을 담당하며, 물질을 특별히 제한하지는 않는다. The hole transporting layer and / or the electron transporting layer material efficiently transfer electrons and holes separated from the photoactive layer to the electrode, and the material is not particularly limited.
상기 정공수송층 물질은 PEDOT:PSS(Poly(3,4-ethylenediocythiophene) doped with poly(styrenesulfonic acid)), 몰리브데늄 산화물(MoOx); 바나듐 산화물(V2O5); 니켈 산화물(NiO); 및 텅스텐 산화물(WOx) 등이 될 수 있으나, 이들에만 한정되는 것은 아니다. The hole transport layer material may include poly (3,4-ethylenediocythiophene) doped with poly (styrenesulfonic acid) (PEDOT: PSS), molybdenum oxide (MoO x ); Vanadium oxide (V 2 O 5 ); Nickel oxide (NiO); And tungsten oxide (WO x ), but the present invention is not limited thereto.
상기 전자수송층 물질은 전자추출금속 산화물(electron-extracting metal oxides)이 될 수 있으며, 구체적으로 8-히드록시퀴놀린의 금속착물; Alq3를 포함한 착물; Liq를 포함한 금속착물; LiF; Ca; 티타늄 산화물(TiOx); 아연 산화물(ZnO); 및 세슘 카보네이트(Cs2CO3) 등이 될 수 있으나, 이들에만 한정되는 것은 아니다.The electron transport layer material may be electron-extracting metal oxides, specifically a metal complex of 8-hydroxyquinoline; Complexes containing Alq 3 ; Metal complexes including Liq; LiF; Ca; Titanium oxide (TiO x ); Zinc oxide (ZnO); And cesium carbonate (Cs 2 CO 3 ), but the present invention is not limited thereto.
광활성층은 전자공여체 및/또는 전자수용체와 같은 광활성 물질을 유기용매에 용해시킨 후 용액을 스핀 코팅, 딥코팅, 스크린 프린팅, 스프레이 코팅, 닥터 블레이드, 브러쉬 페인팅 등의 방법으로 형성할 수 있으나, 이들 방법에만 한정되는 것은 아니다.The photoactive layer can be formed by dissolving a photoactive material such as an electron donor and / or an electron acceptor in an organic solvent, and then applying the solution by spin coating, dip coating, screen printing, spray coating, doctor blade, brush painting, But is not limited to the method.
상기 헤테로환 화합물의 제조 방법 및 이를 포함하는 유기 태양 전지의 제조는 이하 제조예 및 실시예에서 구체적으로 설명한다. 그러나, 하기 실시예는 본 명세서를 예시하기 위한 것이며, 본 명세서의 범위가 이들에 의하여 한정되는 것은 아니다.The production method of the heterocyclic compound and the production of the organic solar cell including the heterocyclic compound will be described in detail in the following Production Examples and Examples. However, the following examples are intended to illustrate the present specification, and the scope of the present specification is not limited thereto.
제조예 1. 화합물 1-1의 제조Production Example 1. Preparation of Compound 1-1
4,7-dibromo-5,6-bis(dodecyloxy)benzo[c][1,2,5]thiadiazole (2.65g, 4mmol), 화합물 A-1 (5.53g, 10mmol), Pd(pph3)4 (0.23g, 0.2mmol), toluene (75 mL)에 디메틸포름아마이드(DMF) 25mL을 더하여 90, 100, 110℃에서 48시간 동안 가열하였다. 이 반응물을 식힌 후, 잔여물을 메탄올에 침전시키고, 여과하였다. 분리된 유기물 층을 물로 세척하였다. 그 후, 감압 증류하여, 메틸렌클로라이드와 클로로포름으로 플래시 크로마토그래피하여 정제하였다. 고체를 다량의 메탄올로 세척하고, 진공 하에 24시간 동안 건조하였다. 어두운 보라색의 파우더 화합물 1-1을 얻었다.(4.3g, 84%)(2.65 g, 4 mmol), Compound A-1 (5.53 g, 10 mmol), Pd (pph 3 ) 4 (0.23 g, 0.2 mmol) and toluene (75 mL) were added 25 mL of dimethylformamide (DMF), and the mixture was heated at 90, 100, and 110 DEG C for 48 hours. After the reaction was cooled, the residue was precipitated in methanol and filtered. The separated organic layer was washed with water. Thereafter, the mixture was subjected to vacuum distillation and purified by flash chromatography with methylene chloride and chloroform. The solid was washed with a large amount of methanol and dried under vacuum for 24 hours. To obtain a dark violet powder compound 1-1 (4.3 g, 84%).
도 2는 화합물 A-1의 NMR 데이터를 나타낸 도이다.2 shows NMR data of Compound A-1.
도 3은 화합물 1-1의 NMR 데이터를 나타낸 도이며, 도 4는 화합물 1-1의 MS 데이터를 나타낸 도이다.FIG. 3 shows NMR data of Compound 1-1, and FIG. 4 shows MS data of Compound 1-1.
제조예 2. 화합물 1-2의 제조Production Example 2. Preparation of Compound 1-2
상온에서 질소하에 etrabutylammonium fluoride (TBAF)의 THF 용액(1.0 M, 4.7 mL, 4.7 mmol, containing ca. 5% H2O)에 화합물 1-1(2g, 1.56mmol)이 녹아 있는 THF 200ml을 적가하면서 교반하였고, 2시간 동안 환류하였다. 그 후, ether 50ml 및 포화 NaHCO3수용액 10ml을 첨가하였고, 10분 동안 교반한 후, 유기층을 분리하여, 포화 NaCl수용액으로 세척하였다. 감압 건조한 후, 클로로포름을 이용하여 플래시 크로마토그래피로 정제하였다. 어두운 보라색 고체를 클로로포름으로 재결정하여 여과하였다. 고체는 충분한 양의 물, 메탄올, 헥산, 에틸아세테이트, 아세톤으로 세척한 후, 24시간 동안 진공 하에 건조하여, 어두운 보라색의 파우더 화합물 1-2를 얻었다. (1.62g, 91%)200 ml of THF in which compound 1-1 (2 g, 1.56 mmol) was dissolved in THF solution (1.0 M, 4.7 mL, 4.7 mmol, containing ca. 5% H 2 O) of etrabutylammonium fluoride (TBAF) Stirred and refluxed for 2 hours. Then 50 ml of ether and 10 ml of a saturated aqueous solution of NaHCO 3 were added and after stirring for 10 min, the organic layer was separated and washed with saturated aqueous NaCl solution. After drying under reduced pressure, the residue was purified by flash chromatography using chloroform. The dark purple solid was recrystallized from chloroform and filtered. The solid was washed with a sufficient amount of water, methanol, hexane, ethyl acetate, acetone, and then dried under vacuum for 24 hours to obtain dark violet powder compound 1-2. (1.62 g, 91%).
도 5는 화합물 1-2의 NMR 데이터를 나타낸 도이며, 도 6은 화합물 1-2의 MS 데이터를 나타낸 도이다.FIG. 5 shows NMR data of the compound 1-2, and FIG. 6 shows MS data of the compound 1-2.
제조예 3. 화합물 1-3의 제조Production Example 3. Preparation of Compound 1-3
4,7-bis(5-bromo-4-(2-octyldodecyl)thiophen-2-yl)-5,6-difluorobenzo[c][1,2,5]thiadiazole(4.22g, 4mmol), 화합물 A-1 (5.53g, 10mmol), Pd(pph3)4 (0.23g, 0.2mmol), toluene (75 mL)에 디메틸포름아마이드(DMF) 25mL을 더하여 90, 100, 110℃에서 48시간 동안 가열하였다. 이 반응물을 식힌 후, 잔여물을 메탄올에 침전시키고, 여과하였다. 분리된 유기물 층을 물로 세척하였다. 그 후, 감압 증류하여, 헥산과 메틸렌클로라이드(hex:MC=1:1)으로 플래시 크로마토그래피하여 정제하였다. 어두운 보라색 고체를 클로로포름과 아세톤으로 재결정하여 여과하였다. 고체는 충분한 양의 메탄올, 아세톤으로 세척한 후, 24시간 동안 진공 하에 건조하여, 어두운 보라색의 파우더 화합물 1-3을 얻었다. (6.45 g, 96.4%)4,7-bis (5-bromo-4- (2-octyldodecyl) thiophen-2-yl) -5,6-difluorobenzo [c] [1,2,5] thiadiazole (4.22 g, 25 mL of dimethylformamide (DMF) was added to 1 (5.53 g, 10 mmol), Pd (pph 3 ) 4 (0.23 g, 0.2 mmol) and toluene (75 mL) and the mixture was heated at 90, 100 and 110 ° C for 48 hours. After the reaction was cooled, the residue was precipitated in methanol and filtered. The separated organic layer was washed with water. Thereafter, the mixture was subjected to vacuum distillation and purified by flash chromatography with hexane and methylene chloride (hex: MC = 1: 1). The dark purple solid was recrystallized from chloroform and acetone and filtered. The solid was washed with a sufficient amount of methanol and acetone, and then dried under vacuum for 24 hours to obtain a dark purple powder compound 1-3. (6.45 g, 96.4%).
실험예 1. 유기 태양 전지의 제조Experimental Example 1. Preparation of Organic Solar Cell
상기 제조예 1로부터 제조된 화합물 1-1과 PC61BM 을 1:2로 클로로벤젠(Chlorobenzene, CB)에 녹여 복합 용액(composit solution)을 제조하였다. 이때, 농도는 4 wt%로 조절하였으며, 유기 태양전지는 ITO/PEDOT:PSS/광활성층/Al 의 구조로 하였다. ITO는 바타입(bar type)으로 1.5 × 1.5 cm2가 코팅된 유리 기판은 증류수, 아세톤, 2-프로판올을 이용하여 초음파 세척하고, ITO 표면을 10 분 동안 오존 처리한 후 45 nm 두께로 PEDOT:PSS(AI4083)를 4000 rpm으로 40초간 스핀코팅하고, 235 에서 10 분 동안 열처리하였다. 광활성층의 코팅을 위해서는 화합물 1-1:PC61BM 복합용액을 158nm 두께로 1,000 rpm으로 20초간 스핀코팅하여, 3x10-8 torr 진공 하에서 열 증발기(thermal evaporator)를 이용하여 100 nm 두께로 1 Å/s 속도로 Al 을 증착하여 유기 태양전지를 제조하였다.Compound 1-1 prepared in Preparation Example 1 and PC 61 BM were dissolved in chlorobenzene (CB) at a ratio of 1: 2 to prepare a composite solution. At this time, the concentration was adjusted to 4 wt%, and the organic solar cell had the structure of ITO / PEDOT: PSS / photoactive layer / Al. The glass substrate coated with 1.5 × 1.5 cm 2 of ITO in a bar type was ultrasonically cleaned using distilled water, acetone, and 2-propanol. The ITO surface was ozone-treated for 10 minutes, and then PEDOT: PSS (AI4083) was spin coated at 4000 rpm for 40 seconds and heat treated at 235 for 10 minutes. For the coating of the photoactive layer, compound 1-1: PC 61 BM complex solution was spin-coated at a thickness of 158 nm at 1,000 rpm for 20 seconds, and then developed with a thermal evaporator under a vacuum of 3 × 10 -8 torr to a thickness of 1 Å / s. < / RTI >
도 8은 실험예 1에 따른 유기 태양 전지의 전압에 따른 전류 밀도를 나타낸 도이다.8 is a graph showing a current density according to a voltage of an organic solar cell according to Experimental Example 1. FIG.
실험예 2. 유기 태양 전지의 제조Experimental Example 2. Preparation of Organic Solar Cell
상기 실험예 1에서 화합물 1-1 대신 상기 제조예 2로부터 제조된 화합물 1-2를 사용하는 것을 제외하고는 동일하게 실험하였다.The same experiment was carried out except that the compound 1-2 prepared in Preparation Example 2 was used instead of the compound 1-1 in Experimental Example 1.
도 9는 실험예 2에 따른 유기 태양 전지의 전압에 따른 전류 밀도를 나타낸 도이다.9 is a graph showing the current density according to the voltage of the organic solar battery according to Experimental Example 2. FIG.
개방전압과 단락전류는 각각 도 8 및 도 9의 전압-전류 밀도 곡선의 4사분면에서 X축과 Y축 절편이며, 이 두 값이 높을수록 태양전지의 효율은 바람직하게 높아진다. 또한 충전율(Fill factor)은 곡선 내부에 그릴 수 있는 직사각형의 넓이를 단락전류와 개방전압의 곱으로 나눈 값이다. 이 세 가지 값을 조사된 빛의 세기로 나누면 에너지 변환 효율을 구할 수 있으며, 높은 값일수록 바람직하다. 상기 도 8 및 도 9의 결과로 본 명세서의 일 실시상태에 따른 유기 태양 전지는 높은 효율을 나타내는 것을 확인할 수 있다.The open-circuit voltage and the short-circuit current are the X-axis and Y-axis intercepts in the fourth quadrant of the voltage-current density curves of FIGS. 8 and 9, respectively, and the higher the two values, the higher the efficiency of the solar cell is. The fill factor is the width of the rectangle that can be drawn inside the curve divided by the product of the short-circuit current and the open-circuit voltage. The energy conversion efficiency can be obtained by dividing these three values by the intensity of the irradiated light, and a higher value is preferable. 8 and 9, the organic solar cell according to one embodiment of the present invention shows high efficiency.
101: 기판
102: 제1 전극
103: 정공수송층
104: 광활성층
105: 제2 전극101: substrate
102: first electrode
103: Hole transport layer
104: photoactive layer
105: second electrode
Claims (12)
[화학식 1]
상기 화학식 1에 있어서,
n1, n2, n3 및 n4는 각각 0 내지 4의 정수이고,
n1, n2, n3 및 n4가 각각 2 이상인 경우, 2 이상의 괄호 내의 구조는 서로 같거나 상이하며,
상기 n1+n2+n3+n4≥ 4 이고,
Y1 내지 Y7은 서로 같거나 상이하고, 각각 독립적으로 CRR', NR, O, SiRR', PR, S, GeRR', Se 또는 Te이며,
X1 내지 X6는 서로 같거나 상이하고, 각각 독립적으로 CR", N, SiR", P 또는 GeR"이고,
L1 내지 L6는 서로 같거나 상이하고, 각각 독립적으로 직접결합; 또는 2가의 연결기이며,
R, R', R", R1 내지 R14, Ar1 및 Ar2는 서로 같거나 상이하고, 각각 독립적으로 수소; 중수소; 할로겐기; 니트릴기; 니트로기; 히드록시기; 카르보닐기; 에스테르기; 이미드기; 아미드기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 아릴옥시기; 치환 또는 비치환된 알킬티옥시기; 치환 또는 비치환된 아릴티옥시기; 치환 또는 비치환된 알킬술폭시기; 치환 또는 비치환된 아릴술폭시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 실릴기; 치환 또는 비치환된 붕소기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 아릴포스핀기; 치환 또는 비치환된 포스핀옥사이드기; 치환 또는 비치환된 아릴기; 치환 또는 비치환된 헤테로아릴기; 또는 전자 받개로서 작용하는 구조이다.A heterocyclic compound represented by the following formula (1):
[Chemical Formula 1]
In Formula 1,
n1, n2, n3 and n4 are each an integer of 0 to 4,
When n1, n2, n3 and n4 are each 2 or more, the structures in parentheses of 2 or more are the same or different,
N1 + n2 + n3 + n4? 4,
Y1 to Y7 are the same or different from each other and each independently CRR ', NR, O, SiRR', PR, S, GeRR '
X1 to X6 are the same or different from each other and are each independently CR ", N, SiR", P or GeR "
L1 to L6 are the same or different from each other, and are each independently a direct bond; Or a divalent linking group,
A halogen atom, a nitrile group, a nitro group, a hydroxyl group, a carbonyl group, an ester group, an imide group, an amide group A substituted or unsubstituted alkyl group, a substituted or unsubstituted cycloalkyl group, a substituted or unsubstituted alkoxy group, a substituted or unsubstituted aryloxy group, a substituted or unsubstituted alkylthio group, a substituted or unsubstituted arylthio group A substituted or unsubstituted aryloxy group, a substituted or unsubstituted aryloxy group, a substituted or unsubstituted aryloxy group, a substituted or unsubstituted aryloxy group, a substituted or unsubstituted aryloxy group, a substituted or unsubstituted aryloxy group, A substituted or unsubstituted arylphosphine group, a substituted or unsubstituted phosphine oxide group, a substituted or unsubstituted aryl group, a substituted or unsubstituted heteroaryl group, or an electron acceptor.
[화학식 1-1]
상기 화학식 1-1에 있어서,
n1, n2, n3, n4, X1 내지 X6, Y1 내지 Y7, R1 내지 R14, Ar1 및 Ar2의 정의는 상기 화학식 1과 동일하다.The heterocyclic compound according to claim 1, wherein the compound represented by Formula 1 is represented by Formula 1-1:
[Formula 1-1]
In Formula 1-1,
The definitions of n1, n2, n3, n4, X1 to X6, Y1 to Y7, R1 to R14, Ar1 and Ar2 are the same as those in the above formula (1).
[화학식 1-2]
상기 화학식 1-1에 있어서,
n1, n2, n3, n4, Y1 내지 Y7, R1 내지 R14, Ar1 및 Ar2의 정의는 상기 화학식 1과 동일하다.The heterocyclic compound according to claim 1, wherein the compound represented by Formula 1 is represented by Formula 1-2:
[Formula 1-2]
In Formula 1-1,
The definitions of n1, n2, n3, n4, Y1 to Y7, R1 to R14, Ar1 and Ar2 are the same as those of the formula (1).
[화학식 1-3]
상기 화학식 1-3에 있어서,
n1, n2, n3, n4, R1 내지 R14, Ar1 및 Ar2의 정의는 상기 화학식 1과 동일하다.The heterocyclic compound according to claim 1, wherein the compound represented by Formula 1 is represented by Formula 1-3:
[Formula 1-3]
In Formula 1-3,
The definitions of n1, n2, n3, n4, R1 to R14, Ar1 and Ar2 are the same as those of formula (1).
The heterocyclic compound according to claim 1, wherein the compound represented by formula (1) is any one selected from the following compounds 1-1 to 1-7:
상기 정공 수송층, 정공 주입층 또는 정공 수송과 정공 주입을 동시에 하는 층은 상기 헤테로환 화합물을 포함하는 유기 태양 전지.[Claim 7] The organic electroluminescent device according to claim 7, wherein the organic material layer comprises a hole transporting layer, a hole injecting layer or a layer simultaneously transporting holes and holes,
Wherein the hole transporting layer, the hole injecting layer, or the layer simultaneously transporting the holes and the hole injecting layer comprises the heterocyclic compound.
상기 유기물층은 전자주입층, 전자 수송층 또는 전자 주입과 전자 수송을 동시에 하는 층을 포함하고,
상기 전자주입층, 전자 수송층 또는 전자 주입과 전자 수송을 동시에 하는 층은 상기 헤테로환 화합물을 포함하는 유기 태양 전지.The method of claim 7,
Wherein the organic material layer includes an electron injection layer, an electron transport layer, or a layer that simultaneously performs electron injection and electron transport,
Wherein the electron injecting layer, the electron transporting layer, or the layer which simultaneously injects electrons and transports electrons comprises the heterocyclic compound.
상기 광활성층은 전자 주개 및 전자 받개로 이루어진 군에서 선택되는 1 또는 2 이상을 포함하고,
상기 전자 주개는 상기 헤테로환 화합물을 포함하는 것인 유기 태양 전지.The method of claim 7,
Wherein the photoactive layer comprises one or more selected from the group consisting of an electron donor and an electron donor,
Wherein the electron donor comprises the heterocyclic compound.
상기 전자 주개 및 전자 받개는 벌크 헤테로 정션(BHJ)을 구성하는 것인 유기 태양 전지.The method of claim 10,
Wherein the electron donor and the electron acceptor constitute bulk heterojunction (BHJ).
상기 광활성층은 n형 유기물층 및 p형 유기물층을 포함하는 이층 박막(bilayer)구조이며,
상기 p형 유기물층은 상기 헤테로환 화합물을 포함하는 것인 유기 태양 전지.The method of claim 7,
The photoactive layer is a bilayer structure including an n-type organic layer and a p-type organic layer,
Wherein the p-type organic compound layer comprises the heterocyclic compound.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020160057063A KR20170126689A (en) | 2016-05-10 | 2016-05-10 | Heterocyclic compound and organic solar cell comprising the same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020160057063A KR20170126689A (en) | 2016-05-10 | 2016-05-10 | Heterocyclic compound and organic solar cell comprising the same |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170126689A true KR20170126689A (en) | 2017-11-20 |
Family
ID=60809053
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020160057063A KR20170126689A (en) | 2016-05-10 | 2016-05-10 | Heterocyclic compound and organic solar cell comprising the same |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR20170126689A (en) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20190029441A (en) * | 2017-09-12 | 2019-03-20 | 주식회사 엘지화학 | Compound and organic electronic device comprising the same |
| KR20190088296A (en) * | 2018-01-18 | 2019-07-26 | 주식회사 엘지화학 | Heterocyclic compound and organic electronic device comprising the same |
| KR20220060905A (en) * | 2020-11-05 | 2022-05-12 | 서울대학교산학협력단 | A novel compound and use thereof as a hole transporting layer |
-
2016
- 2016-05-10 KR KR1020160057063A patent/KR20170126689A/en unknown
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20190029441A (en) * | 2017-09-12 | 2019-03-20 | 주식회사 엘지화학 | Compound and organic electronic device comprising the same |
| KR20190088296A (en) * | 2018-01-18 | 2019-07-26 | 주식회사 엘지화학 | Heterocyclic compound and organic electronic device comprising the same |
| KR20220060905A (en) * | 2020-11-05 | 2022-05-12 | 서울대학교산학협력단 | A novel compound and use thereof as a hole transporting layer |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101677841B1 (en) | Heterocyclic compound and organic solar cell comprising the same | |
| KR101899642B1 (en) | Heterocyclic compound and organic solar cell comprising the same | |
| KR101732220B1 (en) | Heterocyclic compound and organic solar cell comprising the same | |
| KR101725622B1 (en) | Polymer and organic solar cell comprising the same | |
| KR101785200B1 (en) | Heterocyclic compound and organic solar cell comprising the same | |
| KR101713417B1 (en) | Fused ring derivative and organic solar cell comprising the same | |
| KR102176846B1 (en) | Heterocyclic compound and organic solar cell comprising the same | |
| KR20170003234A (en) | Fused ring derivative and organic solar cell comprising the same | |
| KR20180104398A (en) | Heterocyclic compound and organic electronic device comprising the same | |
| KR20180137942A (en) | Compound and organic electronic device comprising the same | |
| KR20170126689A (en) | Heterocyclic compound and organic solar cell comprising the same | |
| KR101863435B1 (en) | Compound and organic solar cell comprising the same | |
| KR20180134151A (en) | Compound and organic solar cell comprising the same | |
| KR102083711B1 (en) | Heterocyclic compound and organic electronic device comprising the same | |
| KR101716035B1 (en) | Fused ring derivative and organic solar cell comprising the same | |
| KR20180127788A (en) | Heterocyclic compound and organic electronic device comprising the same | |
| KR101775758B1 (en) | Metal complexes and organic solar cell comprising the same | |
| KR101676904B1 (en) | Copolymer and organic solar cell comprising the same | |
| KR102605826B1 (en) | Compound and organic electronic device comprising the same | |
| KR102285560B1 (en) | Compound and organic solar cell comprising the same | |
| KR102069409B1 (en) | Copolymer and organic solar cell comprising the same | |
| KR102087474B1 (en) | Compound and organic solar cell comprising the same | |
| KR101732310B1 (en) | Polymer and organic electronic device comprising same | |
| KR101955200B1 (en) | Polymer and organic solar cell comprising the same | |
| KR102601531B1 (en) | Indoline derivative and organic electronic device comprising the same |