JP6879342B2 - Polymers, compositions for organic electroluminescent devices, organic electroluminescent devices, organic EL display devices and organic EL lighting - Google Patents
Polymers, compositions for organic electroluminescent devices, organic electroluminescent devices, organic EL display devices and organic EL lighting Download PDFInfo
- Publication number
- JP6879342B2 JP6879342B2 JP2019141363A JP2019141363A JP6879342B2 JP 6879342 B2 JP6879342 B2 JP 6879342B2 JP 2019141363 A JP2019141363 A JP 2019141363A JP 2019141363 A JP2019141363 A JP 2019141363A JP 6879342 B2 JP6879342 B2 JP 6879342B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- ring
- polymer
- layer
- usually
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 229920000642 polymer Polymers 0.000 title claims description 137
- 239000000203 mixture Substances 0.000 title claims description 79
- 238000002347 injection Methods 0.000 claims description 105
- 239000007924 injection Substances 0.000 claims description 105
- 238000000034 method Methods 0.000 claims description 88
- 230000005525 hole transport Effects 0.000 claims description 74
- 239000002904 solvent Substances 0.000 claims description 66
- 125000001424 substituent group Chemical group 0.000 claims description 56
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 claims description 54
- 125000006615 aromatic heterocyclic group Chemical group 0.000 claims description 46
- 239000000758 substrate Substances 0.000 claims description 24
- 125000000217 alkyl group Chemical group 0.000 claims description 23
- 125000003118 aryl group Chemical group 0.000 claims description 13
- 125000005647 linker group Chemical group 0.000 claims description 13
- 238000004519 manufacturing process Methods 0.000 claims description 11
- 125000002950 monocyclic group Chemical group 0.000 claims description 9
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 8
- 125000000623 heterocyclic group Chemical group 0.000 claims description 5
- UMIVXZPTRXBADB-UHFFFAOYSA-N benzocyclobutene Chemical group C1=CC=C2CCC2=C1 UMIVXZPTRXBADB-UHFFFAOYSA-N 0.000 claims description 4
- 230000005855 radiation Effects 0.000 claims 1
- 239000010410 layer Substances 0.000 description 292
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 132
- 150000001875 compounds Chemical class 0.000 description 123
- 239000010408 film Substances 0.000 description 114
- -1 2-fluorenyl group Chemical group 0.000 description 96
- 239000000243 solution Substances 0.000 description 94
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 68
- 239000000463 material Substances 0.000 description 63
- 229910052757 nitrogen Inorganic materials 0.000 description 42
- 230000015572 biosynthetic process Effects 0.000 description 37
- 238000006243 chemical reaction Methods 0.000 description 34
- 238000000576 coating method Methods 0.000 description 32
- 125000004432 carbon atom Chemical group C* 0.000 description 31
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 30
- 238000007740 vapor deposition Methods 0.000 description 30
- 239000011248 coating agent Substances 0.000 description 28
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 25
- 230000032258 transport Effects 0.000 description 25
- 229910052799 carbon Inorganic materials 0.000 description 24
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 22
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 20
- 238000010438 heat treatment Methods 0.000 description 18
- 230000000903 blocking effect Effects 0.000 description 17
- 229910052751 metal Inorganic materials 0.000 description 17
- 239000002184 metal Substances 0.000 description 17
- 239000012044 organic layer Substances 0.000 description 17
- 238000010992 reflux Methods 0.000 description 17
- 238000004528 spin coating Methods 0.000 description 17
- 125000001140 1,4-phenylene group Chemical group [H]C1=C([H])C([*:2])=C([H])C([H])=C1[*:1] 0.000 description 16
- 239000007788 liquid Substances 0.000 description 16
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 15
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 14
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical group [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 14
- 229910052782 aluminium Inorganic materials 0.000 description 13
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 13
- QARVLSVVCXYDNA-UHFFFAOYSA-N bromobenzene Chemical compound BrC1=CC=CC=C1 QARVLSVVCXYDNA-UHFFFAOYSA-N 0.000 description 12
- HHNHBFLGXIUXCM-GFCCVEGCSA-N cyclohexylbenzene Chemical compound [CH]1CCCC[C@@H]1C1=CC=CC=C1 HHNHBFLGXIUXCM-GFCCVEGCSA-N 0.000 description 12
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 12
- 125000003545 alkoxy group Chemical group 0.000 description 11
- 239000012298 atmosphere Substances 0.000 description 11
- LNAMMBFJMYMQTO-FNEBRGMMSA-N chloroform;(1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].ClC(Cl)Cl.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 LNAMMBFJMYMQTO-FNEBRGMMSA-N 0.000 description 11
- 238000004132 cross linking Methods 0.000 description 11
- 230000000694 effects Effects 0.000 description 11
- 230000001771 impaired effect Effects 0.000 description 11
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 11
- IQTHEAQKKVAXGV-UHFFFAOYSA-N 4-ditert-butylphosphanyl-n,n-dimethylaniline Chemical compound CN(C)C1=CC=C(P(C(C)(C)C)C(C)(C)C)C=C1 IQTHEAQKKVAXGV-UHFFFAOYSA-N 0.000 description 10
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 10
- MTZQAGJQAFMTAQ-UHFFFAOYSA-N ethyl benzoate Chemical compound CCOC(=O)C1=CC=CC=C1 MTZQAGJQAFMTAQ-UHFFFAOYSA-N 0.000 description 10
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 10
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 10
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 9
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 9
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 9
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 9
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 9
- 150000001450 anions Chemical class 0.000 description 9
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 8
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 8
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 8
- 238000004440 column chromatography Methods 0.000 description 8
- 239000004210 ether based solvent Substances 0.000 description 8
- 239000011254 layer-forming composition Substances 0.000 description 8
- 125000001624 naphthyl group Chemical group 0.000 description 8
- 125000004433 nitrogen atom Chemical group N* 0.000 description 8
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 8
- 229910052763 palladium Inorganic materials 0.000 description 8
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 8
- 125000003342 alkenyl group Chemical group 0.000 description 7
- 125000000304 alkynyl group Chemical group 0.000 description 7
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 7
- 239000003759 ester based solvent Substances 0.000 description 7
- 239000003446 ligand Substances 0.000 description 7
- 230000000737 periodic effect Effects 0.000 description 7
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 7
- DPZNOMCNRMUKPS-UHFFFAOYSA-N 1,3-Dimethoxybenzene Chemical compound COC1=CC=CC(OC)=C1 DPZNOMCNRMUKPS-UHFFFAOYSA-N 0.000 description 6
- CHLICZRVGGXEOD-UHFFFAOYSA-N 1-Methoxy-4-methylbenzene Chemical compound COC1=CC=C(C)C=C1 CHLICZRVGGXEOD-UHFFFAOYSA-N 0.000 description 6
- VQGHOUODWALEFC-UHFFFAOYSA-N 2-phenylpyridine Chemical compound C1=CC=CC=C1C1=CC=CC=N1 VQGHOUODWALEFC-UHFFFAOYSA-N 0.000 description 6
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- 125000002252 acyl group Chemical group 0.000 description 6
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 6
- XSIFPSYPOVKYCO-UHFFFAOYSA-N butyl benzoate Chemical compound CCCCOC(=O)C1=CC=CC=C1 XSIFPSYPOVKYCO-UHFFFAOYSA-N 0.000 description 6
- 239000000706 filtrate Substances 0.000 description 6
- 150000002500 ions Chemical class 0.000 description 6
- QPJVMBTYPHYUOC-UHFFFAOYSA-N methyl benzoate Chemical compound COC(=O)C1=CC=CC=C1 QPJVMBTYPHYUOC-UHFFFAOYSA-N 0.000 description 6
- 239000000178 monomer Substances 0.000 description 6
- 230000001590 oxidative effect Effects 0.000 description 6
- 238000006116 polymerization reaction Methods 0.000 description 6
- 229910021642 ultra pure water Inorganic materials 0.000 description 6
- 239000012498 ultrapure water Substances 0.000 description 6
- ABDKAPXRBAPSQN-UHFFFAOYSA-N veratrole Chemical compound COC1=CC=CC=C1OC ABDKAPXRBAPSQN-UHFFFAOYSA-N 0.000 description 6
- HQJQYILBCQPYBI-UHFFFAOYSA-N 1-bromo-4-(4-bromophenyl)benzene Chemical group C1=CC(Br)=CC=C1C1=CC=C(Br)C=C1 HQJQYILBCQPYBI-UHFFFAOYSA-N 0.000 description 5
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 5
- 239000007983 Tris buffer Substances 0.000 description 5
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 5
- 125000001309 chloro group Chemical group Cl* 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 150000004696 coordination complex Chemical class 0.000 description 5
- 125000004093 cyano group Chemical group *C#N 0.000 description 5
- 230000007547 defect Effects 0.000 description 5
- 230000005684 electric field Effects 0.000 description 5
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 5
- 125000001153 fluoro group Chemical group F* 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 238000005259 measurement Methods 0.000 description 5
- 125000000962 organic group Chemical group 0.000 description 5
- 239000003960 organic solvent Substances 0.000 description 5
- 229910000027 potassium carbonate Inorganic materials 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- 239000011541 reaction mixture Substances 0.000 description 5
- 229910052709 silver Inorganic materials 0.000 description 5
- 239000004332 silver Substances 0.000 description 5
- 239000008096 xylene Substances 0.000 description 5
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical group C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 4
- VAIPJQIPFPRJKJ-UHFFFAOYSA-N 1,4-bis(4-bromophenyl)benzene Chemical group C1=CC(Br)=CC=C1C1=CC=C(C=2C=CC(Br)=CC=2)C=C1 VAIPJQIPFPRJKJ-UHFFFAOYSA-N 0.000 description 4
- QPUYECUOLPXSFR-UHFFFAOYSA-N 1-methylnaphthalene Chemical compound C1=CC=C2C(C)=CC=CC2=C1 QPUYECUOLPXSFR-UHFFFAOYSA-N 0.000 description 4
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 4
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 4
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 4
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical group C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 4
- 239000002253 acid Substances 0.000 description 4
- 125000004414 alkyl thio group Chemical group 0.000 description 4
- 150000001408 amides Chemical class 0.000 description 4
- 229910021529 ammonia Inorganic materials 0.000 description 4
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 4
- 125000005110 aryl thio group Chemical group 0.000 description 4
- 125000004104 aryloxy group Chemical group 0.000 description 4
- 230000004888 barrier function Effects 0.000 description 4
- 150000001721 carbon Chemical group 0.000 description 4
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 4
- WDECIBYCCFPHNR-UHFFFAOYSA-N chrysene Chemical group C1=CC=CC2=CC=C3C4=CC=CC=C4C=CC3=C21 WDECIBYCCFPHNR-UHFFFAOYSA-N 0.000 description 4
- 229920001940 conductive polymer Polymers 0.000 description 4
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical compound C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 4
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 4
- 238000000605 extraction Methods 0.000 description 4
- 238000001914 filtration Methods 0.000 description 4
- 125000005843 halogen group Chemical group 0.000 description 4
- 125000005842 heteroatom Chemical group 0.000 description 4
- 229910052740 iodine Inorganic materials 0.000 description 4
- 150000008040 ionic compounds Chemical class 0.000 description 4
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 4
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 4
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 4
- 235000019341 magnesium sulphate Nutrition 0.000 description 4
- 150000002739 metals Chemical class 0.000 description 4
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 4
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 4
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical group C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 4
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 4
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical group C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 4
- 229910052697 platinum Inorganic materials 0.000 description 4
- UOHMMEJUHBCKEE-UHFFFAOYSA-N prehnitene Chemical compound CC1=CC=C(C)C(C)=C1C UOHMMEJUHBCKEE-UHFFFAOYSA-N 0.000 description 4
- 150000003141 primary amines Chemical class 0.000 description 4
- 125000003373 pyrazinyl group Chemical group 0.000 description 4
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 4
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical group C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 4
- 125000000714 pyrimidinyl group Chemical group 0.000 description 4
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 4
- 229920005989 resin Polymers 0.000 description 4
- 239000011347 resin Substances 0.000 description 4
- 150000003839 salts Chemical class 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 238000004506 ultrasonic cleaning Methods 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- CSNIZNHTOVFARY-UHFFFAOYSA-N 1,2-benzothiazole Chemical group C1=CC=C2C=NSC2=C1 CSNIZNHTOVFARY-UHFFFAOYSA-N 0.000 description 3
- KTZQTRPPVKQPFO-UHFFFAOYSA-N 1,2-benzoxazole Chemical group C1=CC=C2C=NOC2=C1 KTZQTRPPVKQPFO-UHFFFAOYSA-N 0.000 description 3
- LZDKZFUFMNSQCJ-UHFFFAOYSA-N 1,2-diethoxyethane Chemical compound CCOCCOCC LZDKZFUFMNSQCJ-UHFFFAOYSA-N 0.000 description 3
- OSIGJGFTADMDOB-UHFFFAOYSA-N 1-Methoxy-3-methylbenzene Chemical compound COC1=CC=CC(C)=C1 OSIGJGFTADMDOB-UHFFFAOYSA-N 0.000 description 3
- IANQTJSKSUMEQM-UHFFFAOYSA-N 1-benzofuran Chemical group C1=CC=C2OC=CC2=C1 IANQTJSKSUMEQM-UHFFFAOYSA-N 0.000 description 3
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical group C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 3
- BLMBNEVGYRXFNA-UHFFFAOYSA-N 1-methoxy-2,3-dimethylbenzene Chemical compound COC1=CC=CC(C)=C1C BLMBNEVGYRXFNA-UHFFFAOYSA-N 0.000 description 3
- AVRPFRMDMNDIDH-UHFFFAOYSA-N 1h-quinazolin-2-one Chemical group C1=CC=CC2=NC(O)=NC=C21 AVRPFRMDMNDIDH-UHFFFAOYSA-N 0.000 description 3
- UJCFZCTTZWHRNL-UHFFFAOYSA-N 2,4-Dimethylanisole Chemical compound COC1=CC=C(C)C=C1C UJCFZCTTZWHRNL-UHFFFAOYSA-N 0.000 description 3
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 3
- SLHKDOGTVUCXKX-UHFFFAOYSA-N 4,4'-biphenyldiboronic acid Chemical compound C1=CC(B(O)O)=CC=C1C1=CC=C(B(O)O)C=C1 SLHKDOGTVUCXKX-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 3
- 0 C[N+](*[N+](C)[O-])[O-] Chemical compound C[N+](*[N+](C)[O-])[O-] 0.000 description 3
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 3
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical group C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 3
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical group CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 3
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 3
- NRCMAYZCPIVABH-UHFFFAOYSA-N Quinacridone Chemical class N1C2=CC=CC=C2C(=O)C2=C1C=C1C(=O)C3=CC=CC=C3NC1=C2 NRCMAYZCPIVABH-UHFFFAOYSA-N 0.000 description 3
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 3
- 125000004062 acenaphthenyl group Chemical group C1(CC2=CC=CC3=CC=CC1=C23)* 0.000 description 3
- IPBVNPXQWQGGJP-UHFFFAOYSA-N acetic acid phenyl ester Natural products CC(=O)OC1=CC=CC=C1 IPBVNPXQWQGGJP-UHFFFAOYSA-N 0.000 description 3
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 3
- 125000004442 acylamino group Chemical group 0.000 description 3
- 125000003282 alkyl amino group Chemical group 0.000 description 3
- 125000004390 alkyl sulfonyl group Chemical group 0.000 description 3
- 125000003277 amino group Chemical group 0.000 description 3
- 125000005577 anthracene group Chemical group 0.000 description 3
- 150000004982 aromatic amines Chemical class 0.000 description 3
- 239000003849 aromatic solvent Substances 0.000 description 3
- 125000001769 aryl amino group Chemical group 0.000 description 3
- 150000008378 aryl ethers Chemical class 0.000 description 3
- 125000004391 aryl sulfonyl group Chemical group 0.000 description 3
- 125000003828 azulenyl group Chemical group 0.000 description 3
- 239000002585 base Substances 0.000 description 3
- TXVHTIQJNYSSKO-UHFFFAOYSA-N benzo[e]pyrene Chemical group C1=CC=C2C3=CC=CC=C3C3=CC=CC4=CC=C1C2=C34 TXVHTIQJNYSSKO-UHFFFAOYSA-N 0.000 description 3
- UDEWPOVQBGFNGE-UHFFFAOYSA-N benzoic acid n-propyl ester Natural products CCCOC(=O)C1=CC=CC=C1 UDEWPOVQBGFNGE-UHFFFAOYSA-N 0.000 description 3
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 3
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 3
- 239000003054 catalyst Substances 0.000 description 3
- 238000010538 cationic polymerization reaction Methods 0.000 description 3
- 239000013626 chemical specie Substances 0.000 description 3
- 229910052801 chlorine Inorganic materials 0.000 description 3
- 125000000259 cinnolinyl group Chemical group N1=NC(=CC2=CC=CC=C12)* 0.000 description 3
- 239000004927 clay Substances 0.000 description 3
- 238000004140 cleaning Methods 0.000 description 3
- 229940126214 compound 3 Drugs 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- 239000010949 copper Substances 0.000 description 3
- 125000006165 cyclic alkyl group Chemical group 0.000 description 3
- 238000000151 deposition Methods 0.000 description 3
- 238000001035 drying Methods 0.000 description 3
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 description 3
- 239000010419 fine particle Substances 0.000 description 3
- 229910052731 fluorine Inorganic materials 0.000 description 3
- 239000007789 gas Substances 0.000 description 3
- 238000007429 general method Methods 0.000 description 3
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 3
- 229910052737 gold Inorganic materials 0.000 description 3
- 239000010931 gold Substances 0.000 description 3
- 238000005286 illumination Methods 0.000 description 3
- 125000002883 imidazolyl group Chemical group 0.000 description 3
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 3
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 238000010030 laminating Methods 0.000 description 3
- 229910001507 metal halide Inorganic materials 0.000 description 3
- 150000005309 metal halides Chemical class 0.000 description 3
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 3
- 229940095102 methyl benzoate Drugs 0.000 description 3
- OLXYLDUSSBULGU-UHFFFAOYSA-N methyl pyridine-4-carboxylate Chemical compound COC(=O)C1=CC=NC=C1 OLXYLDUSSBULGU-UHFFFAOYSA-N 0.000 description 3
- 229910052750 molybdenum Inorganic materials 0.000 description 3
- 239000011733 molybdenum Substances 0.000 description 3
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 150000002894 organic compounds Chemical class 0.000 description 3
- 125000005327 perimidinyl group Chemical group N1C(=NC2=CC=CC3=CC=CC1=C23)* 0.000 description 3
- 150000005041 phenanthrolines Chemical class 0.000 description 3
- 229940049953 phenylacetate Drugs 0.000 description 3
- WLJVXDMOQOGPHL-UHFFFAOYSA-N phenylacetic acid Chemical compound OC(=O)CC1=CC=CC=C1 WLJVXDMOQOGPHL-UHFFFAOYSA-N 0.000 description 3
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 3
- 238000007639 printing Methods 0.000 description 3
- 125000003226 pyrazolyl group Chemical group 0.000 description 3
- 125000005581 pyrene group Chemical group 0.000 description 3
- RQGPLDBZHMVWCH-UHFFFAOYSA-N pyrrolo[3,2-b]pyrrole Chemical group C1=NC2=CC=NC2=C1 RQGPLDBZHMVWCH-UHFFFAOYSA-N 0.000 description 3
- GZTPJDLYPMPRDF-UHFFFAOYSA-N pyrrolo[3,2-c]pyrazole Chemical group N1=NC2=CC=NC2=C1 GZTPJDLYPMPRDF-UHFFFAOYSA-N 0.000 description 3
- 125000000168 pyrrolyl group Chemical group 0.000 description 3
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 3
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical group N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 3
- 238000010898 silica gel chromatography Methods 0.000 description 3
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 3
- 238000001542 size-exclusion chromatography Methods 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 150000003512 tertiary amines Chemical class 0.000 description 3
- 125000005579 tetracene group Chemical group 0.000 description 3
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 3
- VJYJJHQEVLEOFL-UHFFFAOYSA-N thieno[3,2-b]thiophene Chemical group S1C=CC2=C1C=CS2 VJYJJHQEVLEOFL-UHFFFAOYSA-N 0.000 description 3
- 229910052723 transition metal Inorganic materials 0.000 description 3
- 150000003624 transition metals Chemical class 0.000 description 3
- 238000002834 transmittance Methods 0.000 description 3
- 125000005580 triphenylene group Chemical group 0.000 description 3
- 238000001771 vacuum deposition Methods 0.000 description 3
- LWNGJAHMBMVCJR-UHFFFAOYSA-N (2,3,4,5,6-pentafluorophenoxy)boronic acid Chemical compound OB(O)OC1=C(F)C(F)=C(F)C(F)=C1F LWNGJAHMBMVCJR-UHFFFAOYSA-N 0.000 description 2
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 2
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 description 2
- ZMLPKJYZRQZLDA-UHFFFAOYSA-N 1-(2-phenylethenyl)-4-[4-(2-phenylethenyl)phenyl]benzene Chemical group C=1C=CC=CC=1C=CC(C=C1)=CC=C1C(C=C1)=CC=C1C=CC1=CC=CC=C1 ZMLPKJYZRQZLDA-UHFFFAOYSA-N 0.000 description 2
- ARXJGSRGQADJSQ-UHFFFAOYSA-N 1-methoxypropan-2-ol Chemical compound COCC(C)O ARXJGSRGQADJSQ-UHFFFAOYSA-N 0.000 description 2
- UXHUMOFAJUNEEI-UHFFFAOYSA-N 2-(3-iodophenyl)bicyclo[4.2.0]octa-1(6),2,4-triene Chemical compound IC=1C=C(C=CC=1)C1=C2C(CC2)=CC=C1 UXHUMOFAJUNEEI-UHFFFAOYSA-N 0.000 description 2
- DTFKRVXLBCAIOZ-UHFFFAOYSA-N 2-methylanisole Chemical compound COC1=CC=CC=C1C DTFKRVXLBCAIOZ-UHFFFAOYSA-N 0.000 description 2
- KLSJWNVTNUYHDU-UHFFFAOYSA-N Amitrole Chemical group NC1=NC=NN1 KLSJWNVTNUYHDU-UHFFFAOYSA-N 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical group [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 2
- 241000284156 Clerodendrum quadriloculare Species 0.000 description 2
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 239000002841 Lewis acid Substances 0.000 description 2
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 2
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical group C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 description 2
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 2
- 239000003929 acidic solution Substances 0.000 description 2
- 239000005456 alcohol based solvent Substances 0.000 description 2
- 125000002723 alicyclic group Chemical group 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- 125000005196 alkyl carbonyloxy group Chemical group 0.000 description 2
- 229910045601 alloy Inorganic materials 0.000 description 2
- 239000000956 alloy Substances 0.000 description 2
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical class [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 150000004984 aromatic diamines Chemical class 0.000 description 2
- 125000005161 aryl oxy carbonyl group Chemical group 0.000 description 2
- 150000001518 atomic anions Chemical class 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- IPWKHHSGDUIRAH-UHFFFAOYSA-N bis(pinacolato)diboron Chemical compound O1C(C)(C)C(C)(C)OB1B1OC(C)(C)C(C)(C)O1 IPWKHHSGDUIRAH-UHFFFAOYSA-N 0.000 description 2
- 238000006664 bond formation reaction Methods 0.000 description 2
- 150000001638 boron Chemical class 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- DKPFZGUDAPQIHT-UHFFFAOYSA-N butyl acetate Chemical compound CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 2
- 229910052792 caesium Inorganic materials 0.000 description 2
- TVFDJXOCXUVLDH-UHFFFAOYSA-N caesium atom Chemical compound [Cs] TVFDJXOCXUVLDH-UHFFFAOYSA-N 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 238000004364 calculation method Methods 0.000 description 2
- 239000006229 carbon black Substances 0.000 description 2
- 229940125782 compound 2 Drugs 0.000 description 2
- 239000000470 constituent Substances 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- GBRBMTNGQBKBQE-UHFFFAOYSA-L copper;diiodide Chemical compound I[Cu]I GBRBMTNGQBKBQE-UHFFFAOYSA-L 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- NNBZCPXTIHJBJL-UHFFFAOYSA-N decalin Chemical compound C1CCCC2CCCCC21 NNBZCPXTIHJBJL-UHFFFAOYSA-N 0.000 description 2
- DIOQZVSQGTUSAI-UHFFFAOYSA-N decane Chemical compound CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 2
- 230000006866 deterioration Effects 0.000 description 2
- 239000012954 diazonium Substances 0.000 description 2
- 150000001989 diazonium salts Chemical class 0.000 description 2
- 125000001664 diethylamino group Chemical group [H]C([H])([H])C([H])([H])N(*)C([H])([H])C([H])([H])[H] 0.000 description 2
- RXKJFZQQPQGTFL-UHFFFAOYSA-N dihydroxyacetone Chemical compound OCC(=O)CO RXKJFZQQPQGTFL-UHFFFAOYSA-N 0.000 description 2
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 2
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 2
- 125000006575 electron-withdrawing group Chemical group 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- LZCLXQDLBQLTDK-UHFFFAOYSA-N ethyl 2-hydroxypropanoate Chemical compound CCOC(=O)C(C)O LZCLXQDLBQLTDK-UHFFFAOYSA-N 0.000 description 2
- IIEWJVIFRVWJOD-UHFFFAOYSA-N ethylcyclohexane Chemical compound CCC1CCCCC1 IIEWJVIFRVWJOD-UHFFFAOYSA-N 0.000 description 2
- 125000004705 ethylthio group Chemical group C(C)S* 0.000 description 2
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 2
- 238000001704 evaporation Methods 0.000 description 2
- 230000008020 evaporation Effects 0.000 description 2
- 125000003914 fluoranthenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC=C4C1=C23)* 0.000 description 2
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 2
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 2
- 150000004820 halides Chemical class 0.000 description 2
- 125000001188 haloalkyl group Chemical group 0.000 description 2
- ZSIAUFGUXNUGDI-UHFFFAOYSA-N hexan-1-ol Chemical compound CCCCCCO ZSIAUFGUXNUGDI-UHFFFAOYSA-N 0.000 description 2
- 238000004770 highest occupied molecular orbital Methods 0.000 description 2
- 150000007857 hydrazones Chemical class 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- 239000012535 impurity Substances 0.000 description 2
- 229910052738 indium Inorganic materials 0.000 description 2
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 2
- 125000001041 indolyl group Chemical group 0.000 description 2
- 150000007517 lewis acids Chemical class 0.000 description 2
- AUHZEENZYGFFBQ-UHFFFAOYSA-N mesitylene Substances CC1=CC(C)=CC(C)=C1 AUHZEENZYGFFBQ-UHFFFAOYSA-N 0.000 description 2
- 125000001827 mesitylenyl group Chemical group [H]C1=C(C(*)=C(C([H])=C1C([H])([H])[H])C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- 150000004706 metal oxides Chemical class 0.000 description 2
- 125000002816 methylsulfanyl group Chemical group [H]C([H])([H])S[*] 0.000 description 2
- IBHBKWKFFTZAHE-UHFFFAOYSA-N n-[4-[4-(n-naphthalen-1-ylanilino)phenyl]phenyl]-n-phenylnaphthalen-1-amine Chemical group C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 IBHBKWKFFTZAHE-UHFFFAOYSA-N 0.000 description 2
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000005029 naphthylthio group Chemical group C1(=CC=CC2=CC=CC=C12)S* 0.000 description 2
- 229910052759 nickel Inorganic materials 0.000 description 2
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 2
- 125000003566 oxetanyl group Chemical group 0.000 description 2
- VLTRZXGMWDSKGL-UHFFFAOYSA-N perchloric acid Chemical compound OCl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-N 0.000 description 2
- DLRJIFUOBPOJNS-UHFFFAOYSA-N phenetole Chemical compound CCOC1=CC=CC=C1 DLRJIFUOBPOJNS-UHFFFAOYSA-N 0.000 description 2
- 125000006678 phenoxycarbonyl group Chemical group 0.000 description 2
- DYUMLJSJISTVPV-UHFFFAOYSA-N phenyl propanoate Chemical compound CCC(=O)OC1=CC=CC=C1 DYUMLJSJISTVPV-UHFFFAOYSA-N 0.000 description 2
- 125000003356 phenylsulfanyl group Chemical group [*]SC1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 2
- IEQIEDJGQAUEQZ-UHFFFAOYSA-N phthalocyanine Chemical class N1C(N=C2C3=CC=CC=C3C(N=C3C4=CC=CC=C4C(=N4)N3)=N2)=C(C=CC=C2)C2=C1N=C1C2=CC=CC=C2C4=N1 IEQIEDJGQAUEQZ-UHFFFAOYSA-N 0.000 description 2
- 229920000123 polythiophene Chemical class 0.000 description 2
- 235000011056 potassium acetate Nutrition 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 125000005554 pyridyloxy group Chemical group 0.000 description 2
- 125000005030 pyridylthio group Chemical group N1=C(C=CC=C1)S* 0.000 description 2
- MCJGNVYPOGVAJF-UHFFFAOYSA-N quinolin-8-ol Chemical compound C1=CN=C2C(O)=CC=CC2=C1 MCJGNVYPOGVAJF-UHFFFAOYSA-N 0.000 description 2
- 150000003335 secondary amines Chemical class 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- LPXPTNMVRIOKMN-UHFFFAOYSA-M sodium nitrite Chemical compound [Na+].[O-]N=O LPXPTNMVRIOKMN-UHFFFAOYSA-M 0.000 description 2
- 238000005507 spraying Methods 0.000 description 2
- 238000004544 sputter deposition Methods 0.000 description 2
- KZNICNPSHKQLFF-UHFFFAOYSA-N succinimide Chemical compound O=C1CCC(=O)N1 KZNICNPSHKQLFF-UHFFFAOYSA-N 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 229920003002 synthetic resin Polymers 0.000 description 2
- 239000000057 synthetic resin Substances 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- ONCNIMLKGZSAJT-UHFFFAOYSA-N thieno[3,2-b]furan Chemical group S1C=CC2=C1C=CO2 ONCNIMLKGZSAJT-UHFFFAOYSA-N 0.000 description 2
- 125000005031 thiocyano group Chemical group S(C#N)* 0.000 description 2
- 125000002088 tosyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1C([H])([H])[H])S(*)(=O)=O 0.000 description 2
- 230000001052 transient effect Effects 0.000 description 2
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 2
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 2
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 1
- ZSYMVHGRKPBJCQ-UHFFFAOYSA-N 1,1'-biphenyl;9h-carbazole Chemical group C1=CC=CC=C1C1=CC=CC=C1.C1=CC=C2C3=CC=CC=C3NC2=C1 ZSYMVHGRKPBJCQ-UHFFFAOYSA-N 0.000 description 1
- RELMFMZEBKVZJC-UHFFFAOYSA-N 1,2,3-trichlorobenzene Chemical compound ClC1=CC=CC(Cl)=C1Cl RELMFMZEBKVZJC-UHFFFAOYSA-N 0.000 description 1
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 1
- FKASFBLJDCHBNZ-UHFFFAOYSA-N 1,3,4-oxadiazole Chemical compound C1=NN=CO1 FKASFBLJDCHBNZ-UHFFFAOYSA-N 0.000 description 1
- YWDUZLFWHVQCHY-UHFFFAOYSA-N 1,3,5-tribromobenzene Chemical compound BrC1=CC(Br)=CC(Br)=C1 YWDUZLFWHVQCHY-UHFFFAOYSA-N 0.000 description 1
- NKEWBOPVULFSFJ-UHFFFAOYSA-N 1,3-dihydroperimidin-2-one Chemical class C1=CC(NC(O)=N2)=C3C2=CC=CC3=C1 NKEWBOPVULFSFJ-UHFFFAOYSA-N 0.000 description 1
- 125000001989 1,3-phenylene group Chemical group [H]C1=C([H])C([*:1])=C([H])C([*:2])=C1[H] 0.000 description 1
- IJAAWBHHXIWAHM-UHFFFAOYSA-N 1,4-bis(2-phenylethenyl)benzene Chemical compound C=1C=CC=CC=1C=CC(C=C1)=CC=C1C=CC1=CC=CC=C1 IJAAWBHHXIWAHM-UHFFFAOYSA-N 0.000 description 1
- SPPWGCYEYAMHDT-UHFFFAOYSA-N 1,4-di(propan-2-yl)benzene Chemical compound CC(C)C1=CC=C(C(C)C)C=C1 SPPWGCYEYAMHDT-UHFFFAOYSA-N 0.000 description 1
- OCJBOOLMMGQPQU-UHFFFAOYSA-N 1,4-dichlorobenzene Chemical compound ClC1=CC=C(Cl)C=C1 OCJBOOLMMGQPQU-UHFFFAOYSA-N 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- TUXDRFWDZPJPPD-UHFFFAOYSA-N 1-methoxy-2-(trifluoromethoxy)benzene Chemical compound COC1=CC=CC=C1OC(F)(F)F TUXDRFWDZPJPPD-UHFFFAOYSA-N 0.000 description 1
- XHONYVFDZSPELQ-UHFFFAOYSA-N 1-methoxy-3-(trifluoromethyl)benzene Chemical compound COC1=CC=CC(C(F)(F)F)=C1 XHONYVFDZSPELQ-UHFFFAOYSA-N 0.000 description 1
- LIWRTHVZRZXVFX-UHFFFAOYSA-N 1-phenyl-3-propan-2-ylbenzene Chemical group CC(C)C1=CC=CC(C=2C=CC=CC=2)=C1 LIWRTHVZRZXVFX-UHFFFAOYSA-N 0.000 description 1
- YEBQUUKDSJCPIX-UHFFFAOYSA-N 12h-benzo[a]thioxanthene Chemical class C1=CC=CC2=C3CC4=CC=CC=C4SC3=CC=C21 YEBQUUKDSJCPIX-UHFFFAOYSA-N 0.000 description 1
- MQRCTQVBZYBPQE-UHFFFAOYSA-N 189363-47-1 Chemical compound C1=CC=CC=C1N(C=1C=C2C3(C4=CC(=CC=C4C2=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC(=CC=C1C1=CC=C(C=C13)N(C=1C=CC=CC=1)C=1C=CC=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 MQRCTQVBZYBPQE-UHFFFAOYSA-N 0.000 description 1
- DFIGTSPBPXEMAD-UHFFFAOYSA-N 2,5-dinaphthalen-1-yl-3h-oxadiazole Chemical class C1=CC=C2C(C3=CNN(O3)C=3C4=CC=CC=C4C=CC=3)=CC=CC2=C1 DFIGTSPBPXEMAD-UHFFFAOYSA-N 0.000 description 1
- STTGYIUESPWXOW-UHFFFAOYSA-N 2,9-dimethyl-4,7-diphenyl-1,10-phenanthroline Chemical compound C=12C=CC3=C(C=4C=CC=CC=4)C=C(C)N=C3C2=NC(C)=CC=1C1=CC=CC=C1 STTGYIUESPWXOW-UHFFFAOYSA-N 0.000 description 1
- MTUBTKOZCCGPSU-UHFFFAOYSA-N 2-n-naphthalen-1-yl-1-n,1-n,2-n-triphenylbenzene-1,2-diamine Chemical compound C1=CC=CC=C1N(C=1C(=CC=CC=1)N(C=1C=CC=CC=1)C=1C2=CC=CC=C2C=CC=1)C1=CC=CC=C1 MTUBTKOZCCGPSU-UHFFFAOYSA-N 0.000 description 1
- FWPFFKQILIFMAD-UHFFFAOYSA-N 2-phenylpyridine;platinum Chemical compound [Pt].C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1 FWPFFKQILIFMAD-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- GOLORTLGFDVFDW-UHFFFAOYSA-N 3-(1h-benzimidazol-2-yl)-7-(diethylamino)chromen-2-one Chemical compound C1=CC=C2NC(C3=CC4=CC=C(C=C4OC3=O)N(CC)CC)=NC2=C1 GOLORTLGFDVFDW-UHFFFAOYSA-N 0.000 description 1
- DJFCOHRNPCFNJK-UHFFFAOYSA-N 3-(2-bicyclo[4.2.0]octa-1(6),2,4-trienyl)aniline Chemical compound NC=1C=C(C=CC1)C1=C2C(CC2)=CC=C1 DJFCOHRNPCFNJK-UHFFFAOYSA-N 0.000 description 1
- ZVFQEOPUXVPSLB-UHFFFAOYSA-N 3-(4-tert-butylphenyl)-4-phenyl-5-(4-phenylphenyl)-1,2,4-triazole Chemical compound C1=CC(C(C)(C)C)=CC=C1C(N1C=2C=CC=CC=2)=NN=C1C1=CC=C(C=2C=CC=CC=2)C=C1 ZVFQEOPUXVPSLB-UHFFFAOYSA-N 0.000 description 1
- DHDHJYNTEFLIHY-UHFFFAOYSA-N 4,7-diphenyl-1,10-phenanthroline Chemical compound C1=CC=CC=C1C1=CC=NC2=C1C=CC1=C(C=3C=CC=CC=3)C=CN=C21 DHDHJYNTEFLIHY-UHFFFAOYSA-N 0.000 description 1
- ZNSXNNUEMWLJEV-UHFFFAOYSA-N 4-butan-2-yl-n,n-diphenylaniline Chemical compound C1=CC(C(C)CC)=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ZNSXNNUEMWLJEV-UHFFFAOYSA-N 0.000 description 1
- OEDUIFSDODUDRK-UHFFFAOYSA-N 5-phenyl-1h-pyrazole Chemical compound N1N=CC=C1C1=CC=CC=C1 OEDUIFSDODUDRK-UHFFFAOYSA-N 0.000 description 1
- 239000005725 8-Hydroxyquinoline Substances 0.000 description 1
- VFUDMQLBKNMONU-UHFFFAOYSA-N 9-[4-(4-carbazol-9-ylphenyl)phenyl]carbazole Chemical group C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 VFUDMQLBKNMONU-UHFFFAOYSA-N 0.000 description 1
- 229910001316 Ag alloy Inorganic materials 0.000 description 1
- 229910001148 Al-Li alloy Inorganic materials 0.000 description 1
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 1
- KOQWQLVZRCMDJR-UHFFFAOYSA-N Bc(cc1)ccc1-c(cc1)ccc1-c1ccc(B)cc1 Chemical compound Bc(cc1)ccc1-c(cc1)ccc1-c1ccc(B)cc1 KOQWQLVZRCMDJR-UHFFFAOYSA-N 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 1
- 238000006443 Buchwald-Hartwig cross coupling reaction Methods 0.000 description 1
- MRABAEUHTLLEML-UHFFFAOYSA-N Butyl lactate Chemical compound CCCCOC(=O)C(C)O MRABAEUHTLLEML-UHFFFAOYSA-N 0.000 description 1
- XMWRBQBLMFGWIX-UHFFFAOYSA-N C60 fullerene Chemical class C12=C3C(C4=C56)=C7C8=C5C5=C9C%10=C6C6=C4C1=C1C4=C6C6=C%10C%10=C9C9=C%11C5=C8C5=C8C7=C3C3=C7C2=C1C1=C2C4=C6C4=C%10C6=C9C9=C%11C5=C5C8=C3C3=C7C1=C1C2=C4C6=C2C9=C5C3=C12 XMWRBQBLMFGWIX-UHFFFAOYSA-N 0.000 description 1
- XTEGARKTQYYJKE-UHFFFAOYSA-M Chlorate Chemical compound [O-]Cl(=O)=O XTEGARKTQYYJKE-UHFFFAOYSA-M 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- XFXPMWWXUTWYJX-UHFFFAOYSA-N Cyanide Chemical compound N#[C-] XFXPMWWXUTWYJX-UHFFFAOYSA-N 0.000 description 1
- VTLYFUHAOXGGBS-UHFFFAOYSA-N Fe3+ Chemical compound [Fe+3] VTLYFUHAOXGGBS-UHFFFAOYSA-N 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- GYHNNYVSQQEPJS-UHFFFAOYSA-N Gallium Chemical group [Ga] GYHNNYVSQQEPJS-UHFFFAOYSA-N 0.000 description 1
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 1
- 238000003747 Grignard reaction Methods 0.000 description 1
- 229910000846 In alloy Inorganic materials 0.000 description 1
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical group C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 1
- FEXQDZTYJVXMOS-UHFFFAOYSA-N Isopropyl benzoate Chemical compound CC(C)OC(=O)C1=CC=CC=C1 FEXQDZTYJVXMOS-UHFFFAOYSA-N 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- IOVCWXUNBOPUCH-UHFFFAOYSA-M Nitrite anion Chemical compound [O-]N=O IOVCWXUNBOPUCH-UHFFFAOYSA-M 0.000 description 1
- 101150003085 Pdcl gene Proteins 0.000 description 1
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- KJTLSVCANCCWHF-UHFFFAOYSA-N Ruthenium Chemical compound [Ru] KJTLSVCANCCWHF-UHFFFAOYSA-N 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 238000006069 Suzuki reaction reaction Methods 0.000 description 1
- 238000006887 Ullmann reaction Methods 0.000 description 1
- 239000005083 Zinc sulfide Substances 0.000 description 1
- JFBZPFYRPYOZCQ-UHFFFAOYSA-N [Li].[Al] Chemical compound [Li].[Al] JFBZPFYRPYOZCQ-UHFFFAOYSA-N 0.000 description 1
- JHYLKGDXMUDNEO-UHFFFAOYSA-N [Mg].[In] Chemical compound [Mg].[In] JHYLKGDXMUDNEO-UHFFFAOYSA-N 0.000 description 1
- NQMXWGWZHPEURF-UHFFFAOYSA-N [Os].C1(=CC=CC=C1)C1=NC=CC=C1 Chemical compound [Os].C1(=CC=CC=C1)C1=NC=CC=C1 NQMXWGWZHPEURF-UHFFFAOYSA-N 0.000 description 1
- NPRDEIDCAUHOJU-UHFFFAOYSA-N [Pt].N1C(C=C2N=C(C=C3NC(=C4)C=C3)C=C2)=CC=C1C=C1C=CC4=N1 Chemical compound [Pt].N1C(C=C2N=C(C=C3NC(=C4)C=C3)C=C2)=CC=C1C=C1C=CC4=N1 NPRDEIDCAUHOJU-UHFFFAOYSA-N 0.000 description 1
- BWZNMFIGGHVLSV-UHFFFAOYSA-N [Ru].C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1 Chemical compound [Ru].C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1 BWZNMFIGGHVLSV-UHFFFAOYSA-N 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 125000000738 acetamido group Chemical group [H]C([H])([H])C(=O)N([H])[*] 0.000 description 1
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 125000005336 allyloxy group Chemical group 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 description 1
- ROOXNKNUYICQNP-UHFFFAOYSA-N ammonium persulfate Chemical compound [NH4+].[NH4+].[O-]S(=O)(=O)OOS([O-])(=O)=O ROOXNKNUYICQNP-UHFFFAOYSA-N 0.000 description 1
- 239000012935 ammoniumperoxodisulfate Substances 0.000 description 1
- 229910021417 amorphous silicon Inorganic materials 0.000 description 1
- 125000002490 anilino group Chemical group [H]N(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 125000001691 aryl alkyl amino group Chemical group 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 238000007611 bar coating method Methods 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 238000005452 bending Methods 0.000 description 1
- 125000000043 benzamido group Chemical group [H]N([*])C(=O)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 150000001562 benzopyrans Chemical class 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 description 1
- 229920001400 block copolymer Polymers 0.000 description 1
- 229940063013 borate ion Drugs 0.000 description 1
- 229940006460 bromide ion Drugs 0.000 description 1
- 125000004106 butoxy group Chemical group [*]OC([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 1
- 150000001716 carbazoles Chemical class 0.000 description 1
- 125000005708 carbonyloxy group Chemical group [*:2]OC([*:1])=O 0.000 description 1
- 229940005989 chlorate ion Drugs 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- QBWCMBCROVPCKQ-UHFFFAOYSA-M chlorite Chemical compound [O-]Cl=O QBWCMBCROVPCKQ-UHFFFAOYSA-M 0.000 description 1
- 229940005993 chlorite ion Drugs 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 125000005578 chrysene group Chemical group 0.000 description 1
- 239000011247 coating layer Substances 0.000 description 1
- 239000012230 colorless oil Substances 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 239000004020 conductor Substances 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 150000004775 coumarins Chemical class 0.000 description 1
- 150000004292 cyclic ethers Chemical group 0.000 description 1
- IOJUPLGTWVMSFF-UHFFFAOYSA-N cyclobenzothiazole Natural products C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 1
- HPXRVTGHNJAIIH-UHFFFAOYSA-N cyclohexanol Chemical compound OC1CCCCC1 HPXRVTGHNJAIIH-UHFFFAOYSA-N 0.000 description 1
- FHADSMKORVFYOS-UHFFFAOYSA-N cyclooctanol Chemical compound OC1CCCCCCC1 FHADSMKORVFYOS-UHFFFAOYSA-N 0.000 description 1
- IIRFCWANHMSDCG-UHFFFAOYSA-N cyclooctanone Chemical compound O=C1CCCCCCC1 IIRFCWANHMSDCG-UHFFFAOYSA-N 0.000 description 1
- SNRCKKQHDUIRIY-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloromethane;dichloropalladium;iron(2+) Chemical compound [Fe+2].ClCCl.Cl[Pd]Cl.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 SNRCKKQHDUIRIY-UHFFFAOYSA-L 0.000 description 1
- NXQGGXCHGDYOHB-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloropalladium;iron(2+) Chemical compound [Fe+2].Cl[Pd]Cl.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 NXQGGXCHGDYOHB-UHFFFAOYSA-L 0.000 description 1
- 238000006356 dehydrogenation reaction Methods 0.000 description 1
- 239000002274 desiccant Substances 0.000 description 1
- 125000004663 dialkyl amino group Chemical group 0.000 description 1
- 125000004986 diarylamino group Chemical group 0.000 description 1
- RAABOESOVLLHRU-UHFFFAOYSA-N diazene Chemical compound N=N RAABOESOVLLHRU-UHFFFAOYSA-N 0.000 description 1
- 229910000071 diazene Inorganic materials 0.000 description 1
- ZOCHARZZJNPSEU-UHFFFAOYSA-N diboron Chemical compound B#B ZOCHARZZJNPSEU-UHFFFAOYSA-N 0.000 description 1
- 229940117389 dichlorobenzene Drugs 0.000 description 1
- 238000007607 die coating method Methods 0.000 description 1
- HBGGXOJOCNVPFY-UHFFFAOYSA-N diisononyl phthalate Chemical compound CC(C)CCCCCCOC(=O)C1=CC=CC=C1C(=O)OCCCCCCC(C)C HBGGXOJOCNVPFY-UHFFFAOYSA-N 0.000 description 1
- 238000003618 dip coating Methods 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229920000775 emeraldine polymer Polymers 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 125000003700 epoxy group Chemical group 0.000 description 1
- 238000005530 etching Methods 0.000 description 1
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- DFUDMSIRGGTHGI-UHFFFAOYSA-N ethyl 2,3,4,5,6-pentafluorobenzoate Chemical compound CCOC(=O)C1=C(F)C(F)=C(F)C(F)=C1F DFUDMSIRGGTHGI-UHFFFAOYSA-N 0.000 description 1
- 229940116333 ethyl lactate Drugs 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- HAXUFHXMBCWDPM-UHFFFAOYSA-N fluoromethoxybenzene Chemical compound FCOC1=CC=CC=C1 HAXUFHXMBCWDPM-UHFFFAOYSA-N 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 229910052733 gallium Inorganic materials 0.000 description 1
- JVZRCNQLWOELDU-UHFFFAOYSA-N gamma-Phenylpyridine Natural products C1=CC=CC=C1C1=CC=NC=C1 JVZRCNQLWOELDU-UHFFFAOYSA-N 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- 229920000578 graft copolymer Polymers 0.000 description 1
- 238000007646 gravure printing Methods 0.000 description 1
- 238000009499 grossing Methods 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 125000001072 heteroaryl group Chemical group 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 150000004678 hydrides Chemical class 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- RWSOTUBLDIXVET-UHFFFAOYSA-M hydrosulfide Chemical compound [SH-] RWSOTUBLDIXVET-UHFFFAOYSA-M 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- GQZXNSPRSGFJLY-UHFFFAOYSA-N hydroxyphosphanone Chemical compound OP=O GQZXNSPRSGFJLY-UHFFFAOYSA-N 0.000 description 1
- WQYVRQLZKVEZGA-UHFFFAOYSA-N hypochlorite Chemical compound Cl[O-] WQYVRQLZKVEZGA-UHFFFAOYSA-N 0.000 description 1
- 229940005631 hypophosphite ion Drugs 0.000 description 1
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 1
- 150000002484 inorganic compounds Chemical class 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-M iodide Chemical compound [I-] XMBWDFGMSWQBCA-UHFFFAOYSA-M 0.000 description 1
- 229940006461 iodide ion Drugs 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052741 iridium Inorganic materials 0.000 description 1
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 1
- UEEXRMUCXBPYOV-UHFFFAOYSA-N iridium;2-phenylpyridine Chemical compound [Ir].C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1 UEEXRMUCXBPYOV-UHFFFAOYSA-N 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 1
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 239000001989 lithium alloy Substances 0.000 description 1
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- SJCKRGFTWFGHGZ-UHFFFAOYSA-N magnesium silver Chemical compound [Mg].[Ag] SJCKRGFTWFGHGZ-UHFFFAOYSA-N 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 125000005905 mesyloxy group Chemical group 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 description 1
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- DCZNSJVFOQPSRV-UHFFFAOYSA-N n,n-diphenyl-4-[4-(n-phenylanilino)phenyl]aniline Chemical compound C1=CC=CC=C1N(C=1C=CC(=CC=1)C=1C=CC(=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 DCZNSJVFOQPSRV-UHFFFAOYSA-N 0.000 description 1
- 229940017144 n-butyl lactate Drugs 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000003506 n-propoxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 125000005186 naphthyloxy group Chemical group C1(=CC=CC2=CC=CC=C12)O* 0.000 description 1
- 229940005654 nitrite ion Drugs 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- WSGCRAOTEDLMFQ-UHFFFAOYSA-N nonan-5-one Chemical compound CCCCC(=O)CCCC WSGCRAOTEDLMFQ-UHFFFAOYSA-N 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 229910052762 osmium Inorganic materials 0.000 description 1
- SYQBFIAQOQZEGI-UHFFFAOYSA-N osmium atom Chemical compound [Os] SYQBFIAQOQZEGI-UHFFFAOYSA-N 0.000 description 1
- 150000004866 oxadiazoles Chemical class 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 229960003540 oxyquinoline Drugs 0.000 description 1
- 125000006340 pentafluoro ethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 description 1
- 125000000538 pentafluorophenyl group Chemical group FC1=C(F)C(F)=C(*)C(F)=C1F 0.000 description 1
- LLYCMZGLHLKPPU-UHFFFAOYSA-M perbromate Chemical compound [O-]Br(=O)(=O)=O LLYCMZGLHLKPPU-UHFFFAOYSA-M 0.000 description 1
- KHIWWQKSHDUIBK-UHFFFAOYSA-M periodate Chemical compound [O-]I(=O)(=O)=O KHIWWQKSHDUIBK-UHFFFAOYSA-M 0.000 description 1
- 125000005385 peroxodisulfate group Chemical group 0.000 description 1
- CSHWQDPOILHKBI-UHFFFAOYSA-N peryrene Natural products C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 description 1
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 1
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 1
- 150000005359 phenylpyridines Chemical class 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 229940085991 phosphate ion Drugs 0.000 description 1
- AQSJGOWTSHOLKH-UHFFFAOYSA-N phosphite(3-) Chemical compound [O-]P([O-])[O-] AQSJGOWTSHOLKH-UHFFFAOYSA-N 0.000 description 1
- 238000000206 photolithography Methods 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000002985 plastic film Substances 0.000 description 1
- 229920006255 plastic film Polymers 0.000 description 1
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920000767 polyaniline Polymers 0.000 description 1
- 229920000412 polyarylene Polymers 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920002098 polyfluorene Polymers 0.000 description 1
- 229920000193 polymethacrylate Polymers 0.000 description 1
- 229920000128 polypyrrole Polymers 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 150000004032 porphyrins Chemical class 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 150000003151 propanoic acid esters Chemical class 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 229920005604 random copolymer Polymers 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 230000027756 respiratory electron transport chain Effects 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical class [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 229910052703 rhodium Inorganic materials 0.000 description 1
- 239000010948 rhodium Substances 0.000 description 1
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 description 1
- 229910052701 rubidium Inorganic materials 0.000 description 1
- IGLNJRXAVVLDKE-UHFFFAOYSA-N rubidium atom Chemical compound [Rb] IGLNJRXAVVLDKE-UHFFFAOYSA-N 0.000 description 1
- YYMBJDOZVAITBP-UHFFFAOYSA-N rubrene Chemical compound C1=CC=CC=C1C(C1=C(C=2C=CC=CC=2)C2=CC=CC=C2C(C=2C=CC=CC=2)=C11)=C(C=CC=C2)C2=C1C1=CC=CC=C1 YYMBJDOZVAITBP-UHFFFAOYSA-N 0.000 description 1
- 229910052707 ruthenium Inorganic materials 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- SBIBMFFZSBJNJF-UHFFFAOYSA-N selenium;zinc Chemical compound [Se]=[Zn] SBIBMFFZSBJNJF-UHFFFAOYSA-N 0.000 description 1
- HBMJWWWQQXIZIP-UHFFFAOYSA-N silicon carbide Chemical compound [Si+]#[C-] HBMJWWWQQXIZIP-UHFFFAOYSA-N 0.000 description 1
- 229910052814 silicon oxide Inorganic materials 0.000 description 1
- 229920002545 silicone oil Polymers 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 235000010288 sodium nitrite Nutrition 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 150000003413 spiro compounds Chemical class 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 125000005504 styryl group Chemical group 0.000 description 1
- 238000000859 sublimation Methods 0.000 description 1
- 230000008022 sublimation Effects 0.000 description 1
- 229960002317 succinimide Drugs 0.000 description 1
- 150000003457 sulfones Chemical class 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 229940042055 systemic antimycotics triazole derivative Drugs 0.000 description 1
- 125000006836 terphenylene group Chemical group 0.000 description 1
- NLDYACGHTUPAQU-UHFFFAOYSA-N tetracyanoethylene Chemical group N#CC(C#N)=C(C#N)C#N NLDYACGHTUPAQU-UHFFFAOYSA-N 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 125000005297 thienyloxy group Chemical group S1C(=CC=C1)O* 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- 238000007736 thin film deposition technique Methods 0.000 description 1
- 125000003396 thiol group Chemical group [H]S* 0.000 description 1
- 125000005424 tosyloxy group Chemical group S(=O)(=O)(C1=CC=C(C)C=C1)O* 0.000 description 1
- 150000003852 triazoles Chemical group 0.000 description 1
- OBAJXDYVZBHCGT-UHFFFAOYSA-N tris(pentafluorophenyl)borane Chemical compound FC1=C(F)C(F)=C(F)C(F)=C1B(C=1C(=C(F)C(F)=C(F)C=1F)F)C1=C(F)C(F)=C(F)C(F)=C1F OBAJXDYVZBHCGT-UHFFFAOYSA-N 0.000 description 1
- 238000001291 vacuum drying Methods 0.000 description 1
- 238000009834 vaporization Methods 0.000 description 1
- 230000008016 vaporization Effects 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- PXXNTAGJWPJAGM-UHFFFAOYSA-N vertaline Natural products C1C2C=3C=C(OC)C(OC)=CC=3OC(C=C3)=CC=C3CCC(=O)OC1CC1N2CCCC1 PXXNTAGJWPJAGM-UHFFFAOYSA-N 0.000 description 1
- 229910052984 zinc sulfide Inorganic materials 0.000 description 1
- DRDVZXDWVBGGMH-UHFFFAOYSA-N zinc;sulfide Chemical compound [S-2].[Zn+2] DRDVZXDWVBGGMH-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/02—Polyamines
- C08G73/026—Wholly aromatic polyamines
- C08G73/0266—Polyanilines or derivatives thereof
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K71/00—Manufacture or treatment specially adapted for the organic devices covered by this subclass
- H10K71/10—Deposition of organic active material
- H10K71/12—Deposition of organic active material using liquid deposition, e.g. spin coating
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/151—Copolymers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Manufacturing & Machinery (AREA)
- Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
- Devices For Indicating Variable Information By Combining Individual Elements (AREA)
Description
本発明は重合体に関し、特に、有機電界発光素子の正孔注入層及び正孔輸送層として有用な重合体、該重合体を含有する有機電界発光素子用組成物、並びに、この有機電界発光素子を有する有機ELディスプレイ及び有機EL照明に関する。 The present invention relates to a polymer, in particular, a polymer useful as a hole injection layer and a hole transport layer of an organic electroluminescent element, a composition for an organic electroluminescent element containing the polymer, and the organic electroluminescent element. The present invention relates to an organic EL display having an organic EL display and organic EL lighting.
有機電界発光素子における有機層の形成方法としては、真空蒸着法と湿式成膜法が挙げられる。真空蒸着法は積層化が容易であるため、陽極及び/又は陰極からの電荷注入の改善、励起子の発光層封じ込めが容易であるという利点を有する。一方で、湿式成膜法は真空プロセスが要らず、大面積化が容易で、様々な機能をもった複数の材料を混合した塗布液を用いることにより、容易に、様々な機能をもった複数の材料を含有する層を形成できる等の利点がある。
しかしながら、湿式成膜法は積層化が困難であるため、真空蒸着法による素子に比べて駆動安定性に劣り、一部を除いて実用レベルに至っていないのが現状である。
そこで、湿式成膜法による積層化を行うために、架橋性基を有する電荷輸送性ポリマーが所望され、またその開発が行われている。例えば、特許文献1〜5には、特定の繰り返し単位を有する重合体を含有し、湿式成膜法によって、積層化された有機電界発光素子が開示されている。
Examples of the method for forming the organic layer in the organic electroluminescent device include a vacuum vapor deposition method and a wet film deposition method. Since the vacuum vapor deposition method is easy to stack, it has the advantages of improving charge injection from the anode and / or cathode and facilitating containment of excitons in the light emitting layer. On the other hand, the wet film forming method does not require a vacuum process, it is easy to increase the area, and by using a coating liquid in which a plurality of materials having various functions are mixed, a plurality of materials having various functions can be easily obtained. There are advantages such as being able to form a layer containing the above materials.
However, since the wet film formation method is difficult to stack, the drive stability is inferior to that of the device by the vacuum vapor deposition method, and the current situation is that the drive stability has not reached the practical level except for a part.
Therefore, a charge-transporting polymer having a crosslinkable group is desired and is being developed for laminating by a wet film forming method. For example,
しかしながら、特許文献1〜5に記載のこれらの素子は駆動電圧が高く、発光輝度が低く、駆動寿命が短いという問題点があった。そのため、電荷輸送材料の電荷注入輸送能や耐久性の向上が求められていた。
そこで、本発明は、正孔注入輸送能が高く、耐久性の高い重合体及び該重合体を含む有機電界発光素子用組成物を提供することを課題とする。また本発明は、輝度が高く、駆動寿命が長い有機電界発光素子を提供することを課題とする。
However, these elements described in
Therefore, it is an object of the present invention to provide a polymer having high hole injection and transport ability and high durability, and a composition for an organic electroluminescent device containing the polymer. Another object of the present invention is to provide an organic electroluminescent device having high brightness and long drive life.
本発明者らは、鋭意検討した結果、特定の繰り返し単位を有する重合体を用いることで、上記課題を解決することを見出し、本発明を完成するに至った。
即ち、本発明は、以下に関する。
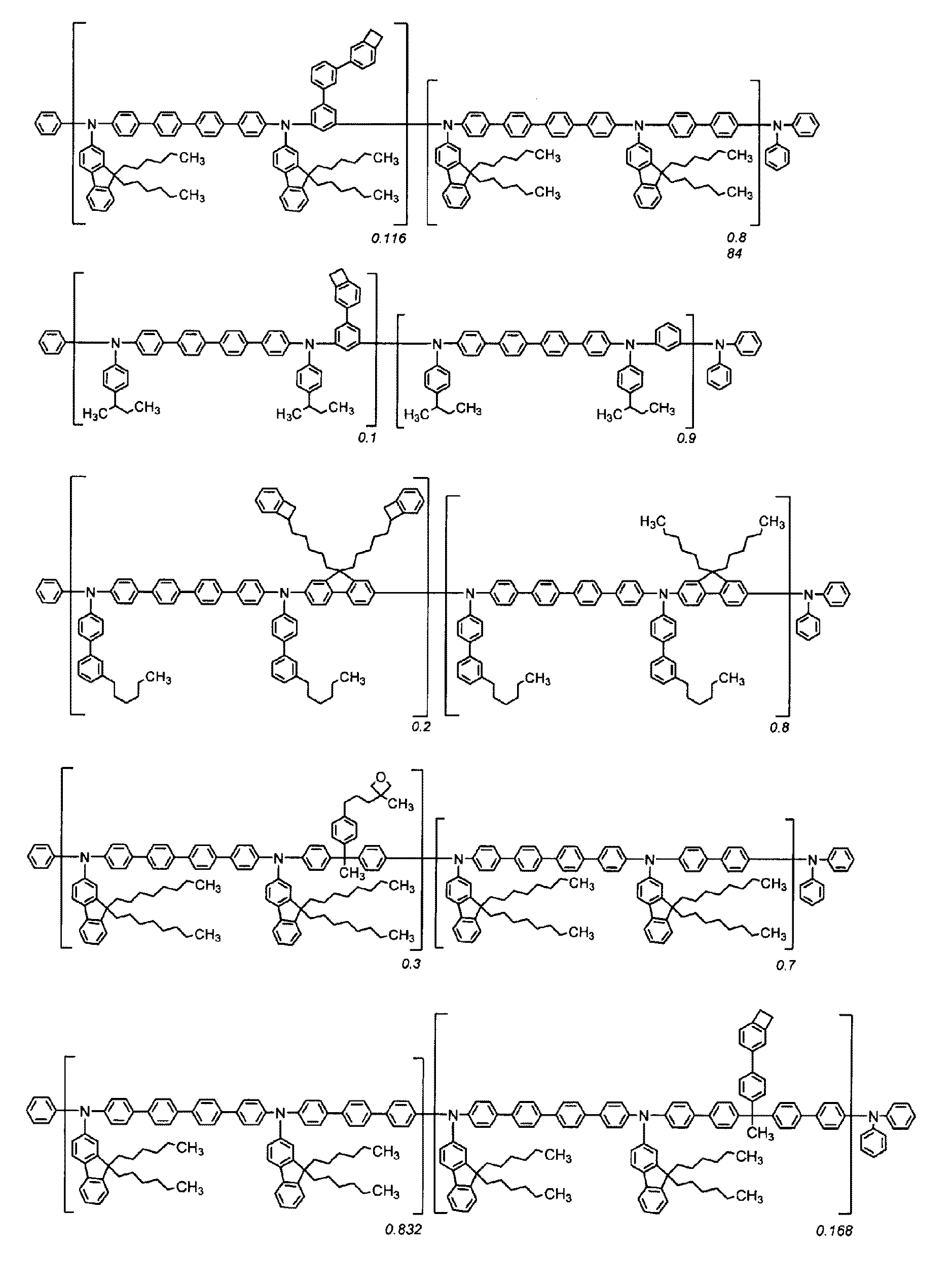
〔1〕下記式(1)で表される繰り返し単位を有する重合体。
As a result of diligent studies, the present inventors have found that the above problems can be solved by using a polymer having a specific repeating unit, and have completed the present invention.
That is, the present invention relates to the following.
[1] A polymer having a repeating unit represented by the following formula (1).
(式中、Ar1、Ar2及びAr3は、各々独立して、置換基を有していても良い、芳香族炭化水素基又は芳香族複素環基を表し、nは4以上の整数を表す。前記芳香族炭化水素基及び芳香族複素環基は、直接又は連結基を介して、複数個連結したものでも良い。)
〔2〕
Ar1、Ar2及びAr3の少なくとも1つ以上に置換基として架橋性基を有する〔1〕に記載の重合体。
〔3〕
架橋性基が、ベンゾシクロブテン環を含む基である〔2〕に記載の重合体。
〔4〕
上記式(1)で表される繰り返し単位を2種以上有し、少なくとも1種の繰り返し単位には架橋性基を含み、少なくとも1種の繰り返し単位には架橋性基を含まない、〔2〕または〔3〕に記載の重合体。
〔5〕
Ar1およびAr2のうち少なくとも一方が、置換基を有しても良い2−フルオレニル基である〔1〕〜〔4〕いずれか一項に記載の重合体。
〔6〕
Ar3が、下記式(2)で表される基である〔1〕〜〔5〕いずれか一項に記載の重合体。
(In the formula, Ar 1 , Ar 2 and Ar 3 each independently represent an aromatic hydrocarbon group or an aromatic heterocyclic group which may have a substituent, and n is an integer of 4 or more. It represents. The aromatic hydrocarbon group and the aromatic heterocyclic group may be linked in plurality directly or via a linking group.)
[2]
The polymer according to [1], which has a crosslinkable group as a substituent at at least one or more of Ar 1 , Ar 2 and Ar 3.
[3]
The polymer according to [2], wherein the crosslinkable group is a group containing a benzocyclobutene ring.
[4]
It has two or more kinds of repeating units represented by the above formula (1), at least one kind of repeating unit contains a crosslinkable group, and at least one kind of repeating unit does not contain a crosslinkable group [2]. Alternatively, the polymer according to [3].
[5]
The polymer according to any one of [1] to [4], wherein at least one of Ar 1 and Ar 2 is a 2-fluorenyl group which may have a substituent.
[6]
The polymer according to any one of [1] to [5], wherein Ar 3 is a group represented by the following formula (2).
(式中、mは1〜3の整数を表す。)
〔7〕
Ar3が、下記式(3)で表される連結基を介して複数個連結された芳香族炭化水素基または芳香族複素環基である〔1〕〜〔5〕いずれか一項に記載の重合体。
(In the formula, m represents an integer from 1 to 3).
[7]
The item according to any one of [1] to [5], wherein Ar 3 is an aromatic hydrocarbon group or an aromatic heterocyclic group in which a plurality of Ar 3 are linked via a linking group represented by the following formula (3). Polymer.
(式中、pは1〜10の整数を表す。R1、R2は、各々独立して、水素原子又は置換基を有していてもよい、アルキル基、芳香族炭化水素基、又は芳香族複素環基を表す。R1、R2が複数個存在する場合、同じであっても異なっていても良い。)
〔8〕
重量平均分子量(Mw)が20,000以上であり、分散度(Mw/Mn)が2.5以下である〔1〕〜〔7〕いずれか一項に記載の重合体。
〔9〕
〔1〕〜〔8〕のいずれか一項に記載の重合体を含有する、有機電界発光素子用組成物。
〔10〕
基板上に、陽極、陰極、及び該陽極と該陰極の間に有機層を有する有機電界発光素子であって、
該有機層が、〔9〕に記載の有機電界発光素子用組成物を用いて、湿式成膜法で形成された層を含む、有機電界発光素子。
〔11〕
前記湿式成膜法で形成された層が、正孔注入層及び正孔輸送層のうちの少なくとも一つである、〔10〕に記載の有機電界発光素子。
〔12〕
陽極と陰極の間に正孔注入層、正孔輸送層及び発光層を含み、前記正孔注入層、正孔輸送層及び発光層は、全て湿式成膜法により形成されたものである、〔10〕又は〔11〕に記載の有機電界発光素子。
〔13〕
〔10〕〜〔12〕のいずれか一項に記載の有機電界発光素子を有する有機EL表示装置。
〔14〕
〔10〕〜〔12〕のいずれか一項に記載の有機電界発光素子を有する有機EL照明。
(In the formula, p represents an integer of 1 to 10. R 1 and R 2 may each independently have a hydrogen atom or a substituent, an alkyl group, an aromatic hydrocarbon group, or an aromatic group. Represents a group heterocyclic group. When a plurality of R 1 and R 2 are present, they may be the same or different.)
[8]
The polymer according to any one of [1] to [7], wherein the weight average molecular weight (Mw) is 20,000 or more and the dispersity (Mw / Mn) is 2.5 or less.
[9]
A composition for an organic electroluminescent device containing the polymer according to any one of [1] to [8].
[10]
An organic electroluminescent device having an anode, a cathode, and an organic layer between the anode and the cathode on a substrate.
An organic electroluminescent device including a layer formed by a wet film forming method using the composition for an organic electroluminescent device according to [9].
[11]
The organic electroluminescent device according to [10], wherein the layer formed by the wet film forming method is at least one of a hole injection layer and a hole transport layer.
[12]
A hole injection layer, a hole transport layer and a light emitting layer are included between the anode and the cathode, and the hole injection layer, the hole transport layer and the light emitting layer are all formed by a wet film forming method. 10] or the organic electroluminescent device according to [11].
[13]
An organic EL display device having the organic electroluminescent device according to any one of [10] to [12].
[14]
Organic EL lighting having the organic electroluminescent device according to any one of [10] to [12].
本発明の重合体は、非共有電子対をもつ窒素原子と窒素原子の間に、4つ以上の連続したp−フェニレン基を有し、HOMOが十分に広く非局在化するため、正孔輸送能に優れる。p−フェニレン基に置換基を有すると、立体障害によって各p−フェニレン基間の2面角が大きくなり、軌道の非局在化が妨げられため、高い正孔輸送能は得られないが、本発明の重合体中のp−フェニレン基は置換基を有さないため、十分に軌道が非局在化し、高い正孔輸送能を有する。 The polymer of the present invention has four or more consecutive p-phenylene groups between nitrogen atoms having unshared electron pairs, and HOMO is sufficiently widely delocalized, so that holes are formed. Excellent transport capacity. If the p-phenylene group has a substituent, the two-plane angle between each p-phenylene group becomes large due to steric hindrance and delocalization of the orbital is hindered, so that high hole transport capacity cannot be obtained. Since the p-phenylene group in the polymer of the present invention does not have a substituent, the orbital is sufficiently delocalized and has a high hole transporting ability.
さらに、本発明の重合体は、2つの窒素原子の間にp−フェニレン基を4つ以上有するため、p−フェニレン基が3つ以下に比べて、窒素原子間の相互作用が小さく、イオン化ポテンシャルが大きくなり、発光層への正孔注入に優れる。正孔輸送層から発光層への正孔注入が向上すると、正孔輸送層、発光層間の正孔の蓄積が抑えられるため、有機電界発光素子の耐久性が向上する。 Furthermore, since the polymer of the present invention has four or more p-phenylene groups between two nitrogen atoms, the interaction between nitrogen atoms is smaller than that of three or less p-phenylene groups, and the ionization potential is small. Is large, and it is excellent in injecting holes into the light emitting layer. When the hole injection from the hole transport layer to the light emitting layer is improved, the accumulation of holes between the hole transport layer and the light emitting layer is suppressed, so that the durability of the organic electroluminescent device is improved.
また、本発明の重合体は、4つ以上の連続したp−フェニレン基を有し、LUMOが十分に広く非局在化するため、電子や励起子に対する耐久性に優れる。4つ以上の連続したp−フェニレン基のうち、2つの窒素原子から遠い位置にある2つ以上の連続したp−フェニレン基にLUMOが分布することにより、電子や励起子に弱い窒素原子周辺には相対的にLUMOが分布しなくなるために耐久性に優れる。p−フェニレン基に置換基を有すると、立体障害によって各p−フェニレン基間の2面角が大きくなり、軌道の非局在化が妨げられるため、高い耐久性は得られないが、本発明の重合体中のp−フェニレン基は置換基を有さないため、十分に軌道が非局在化し、高い耐久性を有する。 In addition, the polymer of the present invention has four or more consecutive p-phenylene groups, and LUMO is sufficiently widely delocalized, so that it has excellent durability against electrons and excitons. Among four or more consecutive p-phenylene groups, LUMO is distributed in two or more consecutive p-phenylene groups located far from two nitrogen atoms, so that they are around nitrogen atoms that are vulnerable to electrons and excitons. Is excellent in durability because LUMO is relatively undistributed. If the p-phenylene group has a substituent, the two-plane angle between each p-phenylene group becomes large due to steric hindrance, and delocalization of the orbital hinders, so that high durability cannot be obtained. Since the p-phenylene group in the polymer of No. 1 has no substituent, the orbital is sufficiently delocalized and has high durability.
また、本発明の重合体を含有する有機電界発光素子用組成物を用いて湿式成膜することにより得られる層は、クラックなどが生じることがなく、平坦である。本発明における有機電界発光素子によれば、輝度が高く、駆動寿命が長い。 Further, the layer obtained by wet film formation using the composition for an organic electroluminescent device containing the polymer of the present invention is flat without cracks or the like. According to the organic electroluminescent device in the present invention, the brightness is high and the drive life is long.
また、本発明の重合体は、電気化学的安定性に優れる為、該重合体を用いて形成された層を含む素子は、フラットパネル・ディスプレイ(例えばOAコンピュータ用や壁掛けテレビ)、車載表示素子、携帯電話表示や面発光体としての特徴を生かした光源(例えば、複写機の光源、液晶ディスプレイや計器類のバックライト光源)、表示板、標識灯への応用が考えられ、その技術的価値は大きいものである。 Further, since the polymer of the present invention is excellent in electrochemical stability, the element including the layer formed by using the polymer is a flat panel display (for example, for an OA computer or a wall-mounted television), an in-vehicle display element. , Light sources that make use of the characteristics of mobile phone displays and surface emitters (for example, light sources for copying machines, backlight sources for liquid crystal displays and instruments), display boards, indicator lights, and their technical value Is a big one.
以下に本発明の実施の形態を詳細に説明するが、以下に記載する構成要件の説明は、本発明の実施態様の一例(代表例)であり、本発明はその要旨を超えない限り、これらの内容に特定されない。
本明細書において“質量%”と“重量%”とは同義である。
本発明の重合体は、下記式(1)で表される繰り返し単位を有する重合体である。
Hereinafter, embodiments of the present invention will be described in detail, but the description of the constituent elements described below is an example (representative example) of the embodiments of the present invention, and the present invention is described as long as the gist of the present invention is not exceeded. Not specified in the content of.
In the present specification, "mass%" and "weight%" are synonymous.
The polymer of the present invention is a polymer having a repeating unit represented by the following formula (1).
(式中、Ar1、Ar2及びAr3は、各々独立して、置換基を有していても良い、芳香族炭化水素基又は芳香族複素環基を表し、nは4以上の整数を表す。前記芳香族炭化水素基及び芳香族複素環基は、直接又は連結基を介して、複数個連結したものでも良い。) (In the formula, Ar 1 , Ar 2 and Ar 3 each independently represent an aromatic hydrocarbon group or an aromatic heterocyclic group which may have a substituent, and n is an integer of 4 or more. It represents. The aromatic hydrocarbon group and the aromatic heterocyclic group may be linked in plurality directly or via a linking group.)
[Ar1、Ar2について]
Ar1、Ar2は、置換基を有していても良い、1価の芳香族炭化水素基又は芳香族複素環基を表す。
芳香族炭化水素基としては、例えば、ベンゼン環、ナフタレン環、アントラセン環、フェナントレン環、ペリレン環、テトラセン環、ピレン環、ベンズピレン環、クリセン環、トリフェニレン環、アセナフテン環、フルオランテン環、フルオレン環などの、6員環の単環又は2〜5縮合環の1価の基が挙げられる。
[About Ar 1 and Ar 2 ]
Ar 1 and Ar 2 represent a monovalent aromatic hydrocarbon group or an aromatic heterocyclic group which may have a substituent.
Examples of the aromatic hydrocarbon group include a benzene ring, a naphthalene ring, an anthracene ring, a phenanthrene ring, a perylene ring, a tetracene ring, a pyrene ring, a benzpyrene ring, a chrysen ring, a triphenylene ring, an acenaphthene ring, a fluoranthene ring, and a fluorene ring. , A monovalent group of a 6-membered monocyclic ring or a 2-5 fused ring.
芳香族複素環基としては、例えば、フラン環、ベンゾフラン環、チオフェン環、ベンゾチオフェン環、ピロール環、ピラゾール環、イミダゾール環、オキサジアゾール環、インドール環、カルバゾール環、ピロロイミダゾール環、ピロロピラゾール環、ピロロピロール環、チエノピロール環、チエノチオフェン環、フロピロール環、フロフラン環、チエノフラン環、ベンゾイソオキサゾール環、ベンゾイソチアゾール環、ベンゾイミダゾール環、ピリジン環、ピラジン環、ピリダジン環、ピリミジン環、トリアジン環、キノリン環、イソキノリン環、シンノリン環、キノキサリン環、フェナントリジン環、ベンゾイミダゾール環、ペリミジン環、キナゾリン環、キナゾリノン環、アズレン環などの、5又は6員環の単環又は2〜4縮合環の1価の基が挙げられる。 Examples of the aromatic heterocyclic group include a furan ring, a benzofuran ring, a thiophene ring, a benzothiophene ring, a pyrrole ring, a pyrazole ring, an imidazole ring, an oxadiazole ring, an indole ring, a carbazole ring, a pyroloide azole ring, and a pyrrolopyrazole ring. , Pyrrolopyrrole ring, thienopyrol ring, thienothiophene ring, flopyrol ring, flofuran ring, thienofuran ring, benzoisoxazole ring, benzoisothiazole ring, benzimidazole ring, pyridine ring, pyrazine ring, pyridazine ring, pyrimidine ring, triazine ring, A 5- or 6-membered monocyclic or 2-4 fused ring such as a quinoline ring, an isoquinoline ring, a cinnoline ring, a quinoxalin ring, a phenanthridin ring, a benzimidazole ring, a perimidine ring, a quinazoline ring, a quinazolinone ring, or an azulene ring. A monovalent group can be mentioned.
電荷輸送性が優れる点、耐久性に優れる点から、Ar1、Ar2は、芳香族炭化水素基が好ましく、中でもベンゼン環、フルオレン環の1価の基、すなわち、フェニル基、フルオレニル基がより好ましく、フルオレニル基が更に好ましく、2−フルオレニル基が特に好ましい。 Aromatic hydrocarbon groups are preferable for Ar 1 and Ar 2 from the viewpoints of excellent charge transportability and durability, and among them, monovalent groups of benzene ring and fluorene ring, that is, phenyl group and fluorenyl group are more preferable. Preferably, a fluorenyl group is more preferred, and a 2-fluorenyl group is particularly preferred.
芳香族炭化水素基、芳香族複素環基が有しても良い置換基としては、本重合体の特性を著しく低減させないものであれば、特に制限はないが、例えば、下記置換基群Zから選ばれる基が挙げられ、アルキル基、アルコキシ基、芳香族炭化水素基、芳香族複素環基が好ましく、アルキル基がより好ましい。 The substituents that the aromatic hydrocarbon group and the aromatic heterocyclic group may have are not particularly limited as long as they do not significantly reduce the characteristics of the present polymer. For example, from the following substituent group Z. Examples thereof include an alkyl group, an alkoxy group, an aromatic hydrocarbon group and an aromatic heterocyclic group, and an alkyl group is more preferable.
[置換基群Z]
例えばメチル基、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、i−ブチル基、sec−ブチル基、tert−ブチル基、n−ヘキシル基、シクロヘキシル基、ドデシル基などの、炭素数が通常1以上であり、通常24以下、好ましくは12以下である、直鎖、分岐、又は環状のアルキル基;
例えばビニル基等の、炭素数が通常2以上であり、通常24以下、好ましくは12以下であるアルケニル基;
例えばエチニル基等の、炭素数が通常2以上であり、通常24以下、好ましくは12以下であるアルキニル基;
例えばメトキシ基、エトキシ基等の、炭素数が通常1以上であり、通常24以下、好ましくは12以下であるアルコキシ基;
例えばフェノキシ基、ナフトキシ基、ピリジルオキシ基等の、炭素数が通常4以上、好ましくは5以上であり、通常36以下、好ましくは24以下であるアリールオキシ基;
例えばメトキシカルボニル基、エトキシカルボニル基等の、炭素数が通常2以上であり、通常24以下、好ましくは12以下であるアルコキシカルボニル基;
例えばジメチルアミノ基、ジエチルアミノ基等の、炭素数が通常2以上であり、通常24以下、好ましくは12以下であるジアルキルアミノ基;
例えばジフェニルアミノ基、ジトリルアミノ基、N−カルバゾリル基等の、炭素数が通常10以上、好ましくは12以上であり、通常36以下、好ましくは24以下のジアリールアミノ基;
例えばフェニルメチルアミノ基等の、炭素数が通常7以上であり、通常36以下、好ましくは24以下であるアリールアルキルアミノ基;
例えばアセチル基、ベンゾイル基等の、炭素数が通常2以上であり、通常24以下、好ましくは12以下であるアシル基;
例えばフッ素原子、塩素原子等のハロゲン原子;
例えばトリフルオロメチル基等の、炭素数が通常1以上であり、通常12以下、好ましくは6以下のハロアルキル基;
例えばメチルチオ基、エチルチオ基等の、炭素数が通常1以上であり、通常24以下、好ましくは12以下のアルキルチオ基;
例えばフェニルチオ基、ナフチルチオ基、ピリジルチオ基等の、炭素数が通常4以上、好ましくは5以上であり、通常36以下、好ましくは24以下であるアリールチオ基;
例えばトリメチルシリル基、トリフェニルシリル基等の、炭素数が通常2以上、好ましくは3以上であり、通常36以下、好ましくは24以下であるシリル基;
例えばトリメチルシロキシ基、トリフェニルシロキシ基等の、炭素数が通常2以上、好ましくは3以上であり、通常36以下、好ましくは24以下であるシロキシ基;
シアノ基;
例えばフェニル基、ナフチル基等の、炭素数が通常6以上であり、通常36以下、好ましくは24以下である芳香族炭化水素基;
例えばチエニル基、ピリジル基等の、炭素数が通常3以上、好ましくは4以上であり、通常36以下、好ましくは24以下である芳香族複素環基。
これらの置換基の中でも、溶解性の点から、炭素数1〜12のアルキル基及び炭素数1〜12のアルコキシ基が好ましい。
また、上記各置換基がさらに置換基を有していてもよく、その例としては前記(置換基群Z)の項に例示した基から選択される。
[Substituent group Z]
For example, methyl group, ethyl group, n-propyl group, i-propyl group, n-butyl group, i-butyl group, sec-butyl group, tert-butyl group, n-hexyl group, cyclohexyl group, dodecyl group and the like. A linear, branched, or cyclic alkyl group usually having 1 or more carbon atoms, usually 24 or less, preferably 12 or less;
An alkenyl group having a carbon number of usually 2 or more, usually 24 or less, preferably 12 or less, such as a vinyl group;
For example, an alkynyl group having 2 or more carbon atoms, usually 24 or less, preferably 12 or less, such as an ethynyl group;
For example, an alkoxy group such as a methoxy group or an ethoxy group having a carbon number of usually 1 or more, usually 24 or less, preferably 12 or less;
For example, an aryloxy group having a carbon number of usually 4 or more, preferably 5 or more, usually 36 or less, preferably 24 or less, such as a phenoxy group, a naphthoxy group, and a pyridyloxy group;
For example, an alkoxycarbonyl group such as a methoxycarbonyl group or an ethoxycarbonyl group, which usually has 2 or more carbon atoms and usually has 24 or less, preferably 12 or less carbon atoms;
For example, a dialkylamino group having 2 or more carbon atoms, usually 24 or less, preferably 12 or less, such as a dimethylamino group or a diethylamino group;
For example, a diarylamino group having a carbon number of usually 10 or more, preferably 12 or more, usually 36 or less, preferably 24 or less, such as a diphenylamino group, a ditrilamino group, and an N-carbazolyl group;
Arylalkylamino groups such as phenylmethylamino groups, which usually have 7 or more carbon atoms and usually 36 or less, preferably 24 or less carbon atoms;
Acyl groups such as acetyl groups and benzoyl groups having a carbon number of usually 2 or more, usually 24 or less, preferably 12 or less;
For example, halogen atoms such as fluorine atoms and chlorine atoms;
A haloalkyl group having a carbon number of usually 1 or more, usually 12 or less, preferably 6 or less, such as a trifluoromethyl group;
For example, an alkylthio group having a carbon number of usually 1 or more, usually 24 or less, preferably 12 or less, such as a methylthio group and an ethylthio group;
For example, an arylthio group having a carbon number of usually 4 or more, preferably 5 or more, usually 36 or less, preferably 24 or less, such as a phenylthio group, a naphthylthio group, and a pyridylthio group;
For example, a silyl group having a carbon number of usually 2 or more, preferably 3 or more, usually 36 or less, preferably 24 or less, such as a trimethylsilyl group or a triphenylsilyl group;
For example, a syroxy group having a carbon number of usually 2 or more, preferably 3 or more, usually 36 or less, preferably 24 or less, such as a trimethylsiloxy group or a triphenylsiloxy group;
Cyano group;
For example, an aromatic hydrocarbon group having 6 or more carbon atoms, usually 36 or less, preferably 24 or less, such as a phenyl group or a naphthyl group;
For example, an aromatic heterocyclic group having a carbon number of usually 3 or more, preferably 4 or more, and usually 36 or less, preferably 24 or less, such as a thienyl group or a pyridyl group.
Among these substituents, an alkyl group having 1 to 12 carbon atoms and an alkoxy group having 1 to 12 carbon atoms are preferable from the viewpoint of solubility.
Further, each of the above-mentioned substituents may further have a substituent, and an example thereof is selected from the groups exemplified in the above section (Substituent group Z).
[Ar3について]
Ar3は、置換基を有していてもよい、2価の芳香族炭化水素基又は芳香族複素環基を表す。前記芳香族炭化水素基及び芳香族複素環基は、複数個、結合したものでも良い。
芳香族炭化水素基としては、例えば、ベンゼン環、ナフタレン環、アントラセン環、フェナントレン環、ペリレン環、テトラセン環、ピレン環、ベンズピレン環、クリセン環、トリフェニレン環、アセナフテン環、フルオランテン環、フルオレン環などの、6員環の単環又は2〜5縮合環の2価の基が挙げられる。
[About Ar 3]
Ar 3 represents a divalent aromatic hydrocarbon group or an aromatic heterocyclic group which may have a substituent. A plurality of the aromatic hydrocarbon groups and aromatic heterocyclic groups may be bonded.
Examples of the aromatic hydrocarbon group include a benzene ring, a naphthalene ring, an anthracene ring, a phenanthrene ring, a perylene ring, a tetracene ring, a pyrene ring, a benzpyrene ring, a chrysen ring, a triphenylene ring, an acenaphthene ring, a fluoranthene ring, and a fluorene ring. , A 6-membered monocyclic ring or a divalent group of 2-5 fused rings.
芳香族複素環基としては、例えば、フラン環、ベンゾフラン環、チオフェン環、ベンゾチオフェン環、ピロール環、ピラゾール環、イミダゾール環、オキサジアゾール環、インドール環、カルバゾール環、ピロロイミダゾール環、ピロロピラゾール環、ピロロピロール環、チエノピロール環、チエノチオフェン環、フロピロール環、フロフラン環、チエノフラン環、ベンゾイソオキサゾール環、ベンゾイソチアゾール環、ベンゾイミダゾール環、ピリジン環、ピラジン環、ピリダジン環、ピリミジン環、トリアジン環、キノリン環、イソキノリン環、シンノリン環、キノキサリン環、フェナントリジン環、ベンゾイミダゾール環、ペリミジン環、キナゾリン環、キナゾリノン環、アズレン環などの、5又は6員環の単環又は2〜4縮合環の2価の基が挙げられる。 Examples of the aromatic heterocyclic group include a furan ring, a benzofuran ring, a thiophene ring, a benzothiophene ring, a pyrrole ring, a pyrazole ring, an imidazole ring, an oxadiazole ring, an indole ring, a carbazole ring, a pyroloide azole ring, and a pyrrolopyrazole ring. , Pyrrolopyrrole ring, thienopyrol ring, thienothiophene ring, flopyrol ring, flofuran ring, thienofuran ring, benzoisoxazole ring, benzoisothiazole ring, benzimidazole ring, pyridine ring, pyrazine ring, pyridazine ring, pyrimidine ring, triazine ring, A 5- or 6-membered monocyclic or 2-4 fused ring such as a quinoline ring, an isoquinoline ring, a cinnoline ring, a quinoxalin ring, a phenanthridin ring, a benzimidazole ring, a perimidine ring, a quinazoline ring, a quinazolinone ring, or an azulene ring. A divalent group can be mentioned.
電荷輸送性が優れる点、耐久性に優れる点から、Ar3については、芳香族炭化水素基が好ましく、中でもベンゼン環、フルオレン環の2価の基、すなわち、フェニレン基、フルオレニレン基がより好ましく、1,3−フェニレン基、1,4−フェニレン基、2,7−フルオレニル基が更に好ましい。 From the viewpoint of excellent charge transportability and durability , an aromatic hydrocarbon group is preferable for Ar 3 , and a divalent group of a benzene ring and a fluorene ring, that is, a phenylene group and a fluoreneylene group is more preferable. A 1,3-phenylene group, a 1,4-phenylene group and a 2,7-fluorenyl group are more preferable.
芳香族炭化水素基、芳香族複素環基が有しても良い置換基としては、本重合体の特性を著しく低減させないものであれば特に制限はないが、例えば、前記置換基群Zから選ばれる基が挙げられ、アルキル基、アルコキシ基、芳香族炭化水素基、芳香族複素環基が好ましく、アルキル基がより好ましい。 The substituents that the aromatic hydrocarbon group and the aromatic heterocyclic group may have are not particularly limited as long as they do not significantly reduce the characteristics of the present polymer, but are selected from, for example, the substituent group Z. Examples thereof include an alkyl group, an alkoxy group, an aromatic hydrocarbon group, and an aromatic heterocyclic group, and an alkyl group is more preferable.
Ar3が前記芳香族炭化水素基及び芳香族複素環基が複数個、結合した基である場合、電荷輸送性が優れる点、耐久性に優れる点から、それらの基が2〜6個連結されていることが好ましい。連結される芳香族炭化水素基及び芳香族複素環基は、1種であっても、複数種であってもよい。 When Ar 3 is a group in which a plurality of the aromatic hydrocarbon groups and aromatic heterocyclic groups are bonded, 2 to 6 of these groups are linked from the viewpoint of excellent charge transportability and durability. Is preferable. The aromatic hydrocarbon group and the aromatic heterocyclic group to be linked may be one kind or a plurality of kinds.
Ar3は、下記式(2)で表されるp−フェニレン基が1〜3個結合した基であることが、電荷輸送性、耐久性の他、陽極側からの正孔注入に優れる点で、特に好ましい。 Ar 3 is a group in which 1 to 3 p-phenylene groups represented by the following formula (2) are bonded, which is excellent in charge transportability, durability, and hole injection from the anode side. , Especially preferable.
(式中、mは1〜3の整数を表す。) (In the formula, m represents an integer from 1 to 3).
また、Ar3が前記芳香族炭化水素基及び芳香族複素環基が複数個、結合した基である場合、連結基を介して結合していても良い。この場合、連結基としては、―CR1R2―、―O―、―CO―、―NR3―、及び―S―からなる群より選ばれる基、及びそれらを2〜10連結した基が好ましい。また、2以上連結される場合、連結基は1種であっても、複数種であってもよい。ここでR1〜R3は、各々独立して、水素原子又は置換基を有していてもよいアルキル基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよい芳香族複素環基を表す。アルキル基、芳香族炭化水素基、または芳香族複素環基としては、前述の置換基群Zに記載してある基と同様の基が好ましい。連結基としては、耐久性の点で―CR1R2―、及び、2〜6連結した―CR1R2―が特に好ましく、―CR1R2―がより好ましい。
Ar3は、下記式(3)で表される連結基を介して複数個連結された芳香族炭化水素基及び芳香族複素環基であることが耐久性の点で特に好ましい。
Further, when Ar 3 is a group in which a plurality of the aromatic hydrocarbon groups and aromatic heterocyclic groups are bonded, they may be bonded via a linking group. In this case, as the linking group, a group selected from the group consisting of -CR 1 R 2- , -O-, -CO-, -NR 3- , and -S-, and a group in which 2 to 10 of them are linked are used. preferable. Further, when two or more are linked, the linking group may be one type or a plurality of types. Here, R 1 to R 3 each independently have an alkyl group which may have a hydrogen atom or a substituent, an aromatic hydrocarbon group which may have a substituent, and a substituent. Represents an aromatic heterocyclic group which may be used. As the alkyl group, aromatic hydrocarbon group, or aromatic heterocyclic group, a group similar to the group described in the above-mentioned substituent group Z is preferable. As the linking group, —CR 1 R 2 − and 2 to 6 linked —CR 1 R 2− are particularly preferable, and —CR 1 R 2− are more preferable in terms of durability.
Ar 3 is particularly preferably an aromatic hydrocarbon group and an aromatic heterocyclic group linked via a linking group represented by the following formula (3) in terms of durability.
(式中、pは1〜10の整数を表す。R1、R2は、各々独立して、水素原子又は置換基を有していてもよい、アルキル基、芳香族炭化水素基、又は芳香族複素環基を表す。アルキル基、芳香族炭化水素基、または芳香族複素環基としては、前述の置換基群Zに記載してある基と同様の基が好ましい。R1、R2が複数個存在する場合、同じであっても異なっていても良い。) (In the formula, p represents an integer of 1 to 10. R 1 and R 2 may each independently have a hydrogen atom or a substituent, an alkyl group, an aromatic hydrocarbon group, or an aromatic group. Representing a group heterocyclic group. As the alkyl group, aromatic hydrocarbon group, or aromatic heterocyclic group, a group similar to the group described in the above-mentioned substituent group Z is preferable. R 1 and R 2 are preferable. If there are more than one, they may be the same or different.)
[nについて]
nは4以上の整数を表す。正孔輸送能が高く陽極側からの正孔注入に優れる点で、nは4が好ましい。正孔輸送能が高く発光層へ正孔注入に優れる点で、nは5が好ましい。
[About n]
n represents an integer of 4 or more. 4 is preferable for n because it has a high hole transporting ability and is excellent in hole injection from the anode side. 5 is preferable for n because it has a high hole transporting ability and is excellent in injecting holes into the light emitting layer.
[架橋性基について]
本発明の重合体は、Ar1、Ar2及びAr3の少なくとも1つ以上に置換基として架橋性基を有することが好ましい。架橋性基を有することで、熱及び/又は活性エネルギー線の照射により起こる反応(難溶化反応)の前後で、有機溶媒に対する溶解性に大きな差を生じさせることができる。耐久性の点から、Ar3の置換基として架橋性基を有することがさらに好ましい。
[About crosslinkable groups]
The polymer of the present invention preferably has a crosslinkable group as a substituent at at least one of Ar 1 , Ar 2 and Ar 3. By having a crosslinkable group, it is possible to make a large difference in solubility in an organic solvent before and after a reaction (poor solubility reaction) caused by irradiation with heat and / or active energy rays. From the viewpoint of durability, it is more preferable to have a crosslinkable group as a substituent of Ar 3.
架橋性基とは、熱及び/又は活性エネルギー線の照射により、該架橋性基の近傍に位置する他の分子を構成している基と反応して、新規な化学結合を生成する基のことをいう。この場合、反応する基は架橋性基と同一の基でも異なった基でもよい。架橋性基としては、例えば、以下の架橋性基群Tに示す基が挙げられる。
〈架橋性基群T〉
A crosslinkable group is a group that forms a new chemical bond by reacting with a group constituting another molecule located in the vicinity of the crosslinkable group by irradiation with heat and / or active energy rays. To say. In this case, the reacting group may be the same group as the crosslinkable group or a different group. Examples of the crosslinkable group include the groups shown in the following crosslinkable group group T.
<Crosslinkable group T>
(式中、R1〜R3は、水素原子又はアルキル基を表す。R4、R5は、水素原子、アルキル基又はアルコキシ基を表す。Ar7は置換基を有していてもよい芳香族炭化水素基又は置換基を有していてもよい芳香族複素環基を表す。) (In the formula, R 1 to R 3 represent a hydrogen atom or an alkyl group. R 4 and R 5 represent a hydrogen atom, an alkyl group or an alkoxy group. Ar 7 is an aromatic group which may have a substituent. Represents an aromatic heterocyclic group which may have a group hydrocarbon group or a substituent.)
R1〜R5のアルキル基としては、通常、炭素数が6以下である直鎖又は分岐の鎖状アルキル基が好ましく、例えばメチル基、エチル基、n−プロピル基、2−プロピル基、n−ブチル基、イソブチル基等である。より好ましくはメチル基又はエチル基である。R1〜R5の炭素数が6以下であれば、架橋反応を立体的に阻害することもなく、膜の不溶化が起こりやすい傾向にある。 The alkyl group of R 1 to R 5 is usually preferably a linear or branched chain alkyl group having 6 or less carbon atoms, for example, a methyl group, an ethyl group, an n-propyl group, a 2-propyl group, or n. -Butyl group, isobutyl group, etc. More preferably, it is a methyl group or an ethyl group. When the number of carbon atoms of R 1 to R 5 is 6 or less, the cross-linking reaction is not sterically inhibited and the film tends to be insolubilized.
R4、R5のアルコキシ基としては、通常、炭素数が6以下である直鎖又は分岐の鎖状アルコキシ基が好ましく、例えばメトキシ基、エトキシ基、n−プロポキシ基、2−プロポキシ基、n−ブトキシ基等である。より好ましくはメトキシ基、エトキシ基である。R4、R5の炭素数が6以下であれば、架橋反応を立体的に阻害することもなく、膜の不溶化が起こりやすい傾向にある。 The alkoxy groups of R 4 and R 5 are usually preferably a linear or branched chain alkoxy group having 6 or less carbon atoms, for example, a methoxy group, an ethoxy group, an n-propoxy group, a 2-propoxy group, or n. -Butoxy group, etc. More preferably, it is a methoxy group or an ethoxy group. When the number of carbon atoms of R 4 and R 5 is 6 or less, the cross-linking reaction is not sterically inhibited and the film tends to be insolubilized.
また、Ar7の置換基を有していてもよい芳香族炭化水素基としては、例えば、1個の遊離原子価を有する、ベンゼン環、ナフタレン環などの6員環の単環又は2〜5縮合環が挙げられる。特に1個の遊離原子価を有するベンゼン環が好ましい。また、Ar7は、これらの置換基を有していてもよい芳香族炭化水素基を2以上結合させた基であっても良い。このような基としては、ビフェニレン基、ターフェニレン基などが挙げられ、4,4’−ビフェニレン基が好ましい。 The aromatic hydrocarbon group which may have a substituent of Ar 7 includes, for example, a single ring of a 6-membered ring such as a benzene ring or a naphthalene ring having one free valence, or 2 to 5 groups. A fused ring can be mentioned. In particular, a benzene ring having one free valence is preferable. Further, Ar 7 may be a group in which two or more aromatic hydrocarbon groups which may have these substituents are bonded. Examples of such a group include a biphenylene group and a terphenylene group, and a 4,4'-biphenylene group is preferable.
これらのうち、エポキシ基、オキセタン基などの環状エーテル基、ビニルエーテル基などのカチオン重合によって架橋反応する基が、反応性が高く、架橋による不溶化が容易な点で好ましい。中でも、カチオン重合の速度を制御しやすい点でオキセタン基がより好ましく、カチオン重合の際に素子の劣化をまねくおそれのあるヒドロキシル基が生成しにくい点でビニルエーテル基が好ましい。
また、シンナモイル基などアリールビニルカルボニル基、1価の遊離原子価を有するベンゾシクロブテン環などの環化付加反応する基が、素子の電気化学的安定性をさらに向上させる点で好ましい。
また、架橋性基の中でも、架橋後の構造が特に安定な点で、1価の遊離原子価を有するベンゾシクロブテン環が特に好ましい。
Of these, a cyclic ether group such as an epoxy group and an oxetane group, and a group that undergoes a cross-linking reaction by cationic polymerization such as a vinyl ether group are preferable because they have high reactivity and are easily insolubilized by cross-linking. Of these, an oxetane group is more preferable because it is easy to control the rate of cationic polymerization, and a vinyl ether group is preferable because it is difficult to generate a hydroxyl group which may cause deterioration of the device during cationic polymerization.
Further, an arylvinylcarbonyl group such as a cinnamoyl group and a cycloaddition-reactive group such as a benzocyclobutene ring having a monovalent free valence are preferable in that the electrochemical stability of the device is further improved.
Further, among the crosslinkable groups, a benzocyclobutene ring having a monovalent free valence is particularly preferable because the structure after cross-linking is particularly stable.
本発明の重合体において、架橋性基は、芳香族炭化水素基、芳香族複素環基、及び/又は、連結基に直接結合していてもよいし、芳香族炭化水素基及び/又は芳香族複素環基以外の基に直接結合してもよいし、これらの基に任意の2価の基を介して結合してもよい。任意の2価の基としては、−O−基、−C(=O)−基及び(置換基を有していてもよい)−CH2−基から選ばれる基を任意の順番で1〜30個連結してなる基が好ましい。 In the polymer of the present invention, the crosslinkable group may be directly bonded to an aromatic hydrocarbon group, an aromatic heterocyclic group and / or a linking group, or an aromatic hydrocarbon group and / or an aromatic group. It may be directly bonded to a group other than the heterocyclic group, or may be bonded to these groups via an arbitrary divalent group. The optional divalent group, -O- group, -C (= O) - group and (which may have a substituent) -CH 2 -. 1 to a group selected from the group in any order A group formed by connecting 30 groups is preferable.
本発明の重合体が有する架橋性基は、架橋することにより十分に不溶化し、その上に湿式成膜法で他の層を形成しやすくなる点では、多い方が好ましい。一方で、形成された層にクラックが生じ難く、未反応架橋性基が残りにくく、有機電界発光素子(有機EL素子)が長寿命になりやすい点では、架橋性基は少ないことが好ましい。 It is preferable that the crosslinkable group of the polymer of the present invention has a large number in that it is sufficiently insolubilized by crosslinking and that another layer can be easily formed on the crosslinkable group by a wet film forming method. On the other hand, it is preferable that the number of crosslinkable groups is small in that cracks are unlikely to occur in the formed layer, unreacted crosslinkable groups are unlikely to remain, and the organic electroluminescent element (organic EL element) tends to have a long life.
本発明の重合体における、1つのポリマー鎖の中に存在する架橋性基は、通常平均1以上、好ましくは平均2以上、また通常200以下、好ましくは100以下である。 In the polymer of the present invention, the number of crosslinkable groups present in one polymer chain is usually 1 or more on average, preferably 2 or more on average, and 200 or less, preferably 100 or less.
また、本発明の重合体が有する架橋性基の数は、重合体の分子量1000あたりの数で表すことができる。 Further, the number of crosslinkable groups contained in the polymer of the present invention can be expressed by the number per 1000 molecular weight of the polymer.
本発明の重合体が有する架橋性基の数を、重合体の分子量1000あたりの数で表した場合、分子量1000あたり、通常3.0個以下、好ましくは1.0個以下、より好ましくは0.5個以下、さらに好ましくは0.2個以下、また通常0個以上、好ましくは0.01個以上、より好ましくは0.02個以上、更に好ましくは0.05個以上である。 When the number of crosslinkable groups contained in the polymer of the present invention is expressed as the number per 1000 molecular weight of the polymer, it is usually 3.0 or less, preferably 1.0 or less, more preferably 0, per 1000 molecular weight. .5 or less, more preferably 0.2 or less, usually 0 or more, preferably 0.01 or more, more preferably 0.02 or more, still more preferably 0.05 or more.
架橋性基の数が上記範囲内であると、クラックなどが起き難く、平坦な膜が得られ易い。また、架橋密度が適度であるため、架橋反応後の層内に残る未反応の架橋性基が少なく、得られる素子の寿命に影響し難い。 When the number of crosslinkable groups is within the above range, cracks and the like are unlikely to occur, and a flat film can be easily obtained. Further, since the cross-linking density is appropriate, there are few unreacted cross-linking groups remaining in the layer after the cross-linking reaction, and it is unlikely to affect the life of the obtained device.
さらに、架橋反応後の、有機溶媒に対する難溶性が十分であるため、湿式成膜法での多層積層構造が形成し易い。 Further, since the poor solubility in the organic solvent after the crosslinking reaction is sufficient, it is easy to form a multilayer laminated structure by the wet film forming method.
ここで、重合体の分子量1000あたりの架橋性基の数は、重合体からその末端基を除いて、合成時の仕込みモノマーのモル比と、構造式から算出することができる。
例えば、後述の合成例1で合成した目的ポリマー1の場合で説明すると、目的ポリマー1において、末端基を除いた繰り返し単位の分子量は平均1148.69であり、また架橋性基は、1繰り返し単位当たり平均0.1156個である。これを単純比例により計算すると、分子量1000あたりの架橋性基の数は、0.10個と算出される。
Here, the number of crosslinkable groups per 1000 molecular weight of the polymer can be calculated from the molar ratio of the charged monomer at the time of synthesis and the structural formula, excluding the terminal groups thereof from the polymer.
For example, in the case of the
[重合体の分子量について]
本発明の重合体の重量平均分子量は、通常3,000,000以下、好ましくは1,000,000以下、より好ましくは500,000以下、さらに好ましくは200,000以下であり、また通常2,500以上、好ましくは5,000以上、より好ましくは10,000以上、さらに好ましくは30,000以上である。
[Molecular weight of polymer]
The weight average molecular weight of the polymer of the present invention is usually 3,000,000 or less, preferably 1,000,000 or less, more preferably 500,000 or less, still more preferably 200,000 or less, and usually 2, It is 500 or more, preferably 5,000 or more, more preferably 10,000 or more, still more preferably 30,000 or more.
重合体の重量平均分子量が上記上限値を超えると、溶媒に対する溶解性が低下するため、成膜性が損なわれるおそれがある。また、重合体の重量平均分子量が上記下限値を下回ると、重合体のガラス転移温度、融点及び気化温度が低下するため、耐熱性が低下する場合がある。 If the weight average molecular weight of the polymer exceeds the above upper limit value, the solubility in a solvent is lowered, so that the film forming property may be impaired. Further, when the weight average molecular weight of the polymer is less than the above lower limit value, the glass transition temperature, melting point and vaporization temperature of the polymer are lowered, so that the heat resistance may be lowered.
また、本発明の重合体における数平均分子量(Mn)は、通常2,500,000以下、好ましくは750,000以下、より好ましくは400,000以下であり、また通常2,000以上、好ましくは4,000以上、より好ましくは8,000以上、さらに好ましくは20,000以上である。 The number average molecular weight (Mn) of the polymer of the present invention is usually 2,500,000 or less, preferably 750,000 or less, more preferably 400,000 or less, and usually 2,000 or more, preferably 2,000 or more. It is 4,000 or more, more preferably 8,000 or more, and even more preferably 20,000 or more.
さらに、本発明の重合体における分散度(Mw/Mn)は、好ましくは3.5以下であり、さらに好ましくは2.5以下、特に好ましくは2.0以下である。尚、分散度は値が小さい程よいため、下限値は理想的には1である。該重合体の分散度が、上記上限値以下であると、精製が容易で、また溶媒に対する溶解性や電荷輸送能が良好である。 Further, the dispersity (Mw / Mn) in the polymer of the present invention is preferably 3.5 or less, more preferably 2.5 or less, and particularly preferably 2.0 or less. Since the smaller the value of the dispersion, the better, the lower limit is ideally 1. When the dispersity of the polymer is not more than the above upper limit value, purification is easy, and solubility in a solvent and charge transporting ability are good.
通常、重合体の重量平均分子量はSEC(サイズ排除クロマトグラフィー)測定により決定される。SEC測定では高分子量成分ほど溶出時間が短く、低分子量成分ほど溶出時間が長くなるが、分子量既知のポリスチレン(標準試料)の溶出時間から算出した校正曲線を用いて、サンプルの溶出時間を分子量に換算することによって、重量平均分子量が算出される。 Usually, the weight average molecular weight of a polymer is determined by SEC (Size Exclusion Chromatography) measurement. In SEC measurement, the higher the molecular weight component, the shorter the elution time, and the lower the molecular weight component, the longer the elution time. By conversion, the weight average molecular weight is calculated.
[具体例]
本発明の重合体の具体例を以下に示すが、本発明の重合体はこれらに限定されるものではない。なお、化学式中の数字は繰返し単位のモル比を表す。
化学式中の数字は繰返し単位のモル比に関して、例えば、上記式(1)において、架橋性基を有する繰り返し単位と架橋性基を有さない繰り返し単位が含まれる重合体の場合、モル比は、架橋性基を有する繰り返し単位に対して、架橋性基を有さない繰り返し単位が通常0以上、好ましくは1以上、より好ましくは2以上、更に好ましくは5以上であり、また通常100以下、好ましくは50以下、より好ましくは20以下、更に好ましくは10以下である。架橋性基を有する繰り返し単位のモル比が小さすぎると架橋反応後の、有機溶媒に対する難溶性が十分ではなく、湿式成膜法での多層積層構造が困難になる傾向があり、大きすぎるとクラックなどが起きやすく、平坦な膜が得られにくくなる傾向がある。
これらの重合体は、ランダム共重合体、交互共重合体、ブロック共重合体、又はグラフト共重合体などのいずれでもよく、単量体の配列順序には限定されない。
[Concrete example]
Specific examples of the polymer of the present invention are shown below, but the polymer of the present invention is not limited thereto. The numbers in the chemical formula represent the molar ratio of the repeating unit.
The numbers in the chemical formula are related to the molar ratio of the repeating unit. For example, in the above formula (1), in the case of a polymer containing a repeating unit having a crosslinkable group and a repeating unit having no crosslinkable group, the molar ratio is The number of repeating units having no crosslinkable group is usually 0 or more, preferably 1 or more, more preferably 2 or more, still more preferably 5 or more, and usually 100 or less, preferably 100 or less, with respect to the repeating unit having a crosslinkable group. Is 50 or less, more preferably 20 or less, still more preferably 10 or less. If the molar ratio of the repeating unit having a crosslinkable group is too small, the poor solubility in an organic solvent after the crosslinking reaction tends to be insufficient, and the multi-layer laminated structure by the wet film forming method tends to be difficult. Etc. are likely to occur, and it tends to be difficult to obtain a flat film.
These polymers may be random copolymers, alternate copolymers, block copolymers, graft copolymers, or the like, and the order of arrangement of the monomers is not limited.
<重合体の製造方法>
本発明の重合体の製造方法は特には制限されず、本発明の重合体が得られる限り任意である。例えば、Suzuki反応、Grignard反応、Ullmann反応、Buchwald−Hartwig反応等のC−C結合形成反応及びC−N結合形成反応を組み合わせることによって、製造することができる。ただし、本発明の重合体の特徴である、4つ以上の連続したp−フェニレン基の部分は、溶解性に乏しい構造であるため、Ar1及び/又はAr2に溶解性を高める置換基を導入した後に、4つ以上の連続したp−フェニレン基の部分を構築するといった工夫を行うことが好ましい。このような工夫により、単量体(繰り返し単位)の純度が高められ、所望の重合度及び分子量分布の重合体が得られやすくなる。
具体的には、9,9−ジアルキル−2−アミノフルオレン等の溶解性の高い1級アミンとブロモベンゼンを反応させ、2級アミンを得た後、アミノ基のp−位を、N−ブロモスクシンイミド等で臭素化し、さらに、4,4’−ビフェニルジボロン酸、4,4”−p−テルフェニルジボロン酸またはそれらのエステル誘導体等と反応させて、中間体1を構築することが好ましい。中間体1とジハロゲン化物とを反応させることで本発明の重合体が得られる。
<Method for producing polymer>
The method for producing the polymer of the present invention is not particularly limited, and is arbitrary as long as the polymer of the present invention can be obtained. For example, it can be produced by combining a CC bond forming reaction such as a Suzuki reaction, a Grignard reaction, an Ullmann reaction, and a Buchwald-Hartwig reaction and a CN bond forming reaction. However, since the portion of four or more consecutive p-phenylene groups, which is a feature of the polymer of the present invention, has a structure with poor solubility, Ar 1 and / or Ar 2 are provided with a substituent that enhances solubility. After the introduction, it is preferable to devise such as constructing a portion of four or more consecutive p-phenylene groups. By such a device, the purity of the monomer (repeating unit) is increased, and it becomes easy to obtain a polymer having a desired degree of polymerization and molecular weight distribution.
Specifically, a highly soluble primary amine such as 9,9-dialkyl-2-aminofluorene is reacted with bromobenzene to obtain a secondary amine, and then the p-position of the amino group is changed to N-bromo. It is preferable to brominate with succinimide or the like and further react with 4,4'-biphenyldiboronic acid, 4,4 "-p-terphenyldiboronic acid or an ester derivative thereof to construct
4,4’−ビフェニルジボロン酸、4,4”−p−テルフェニルジボロン酸またはそれらのエステル誘導体等と臭化物との反応を、片側ずつ行うことで、中間体1の2つのAr1を互いに異なる基とすることができる。 By reacting 4,4'-biphenyldiboronic acid, 4,4 "-p-terphenyldiboronic acid or their ester derivatives, etc. with bromide one side at a time, two Ar 1s of intermediate 1 can be obtained. It can be a different group from each other.
また、9,9−ジアルキル−2−アミノフルオレン等の溶解性の高い1級アミンと4,4’−ジブロモビフェニルとを反応させ、2級アミン部位を有するモノ臭化物を得た後、ビス(ピナコラト)ジボロン等でボロン酸エステルに変換し中間体2を得て、さらに、溶解性の高い1級アミンと4,4’−ジブロモビフェニル、4,4”−ジブロモ−p−テルフェニル等のジハロゲン化物を反応させて中間体3を得て、中間体2と中間体3を反応させて中間体4を構築することが好ましい。この中間体4とジハロゲン化物とを反応させることで本発明の重合体が得られる。 Further, a highly soluble primary amine such as 9,9-dialkyl-2-aminofluorene is reacted with 4,4'-dibromobiphenyl to obtain a monoboronic acid having a secondary amine moiety, and then bis (pinacolato) is obtained. ) Convert to boronic acid ester with diboron or the like to obtain intermediate 2, and further, highly soluble primary amine and dihalogenates such as 4,4'-dibromobiphenyl and 4,4 "-dibromo-p-terphenyl". It is preferable to react with the intermediate 2 to obtain the intermediate 3 and react the intermediate 2 with the intermediate 3 to construct the intermediate 4. By reacting the intermediate 4 with the dihalide, the polymer of the present invention is formed. Is obtained.
なお、通常、1級または2級アミン化合物とハロゲン化物との反応工程は、例えば炭酸カリウム、tert−ブトキシナトリウム、トリエチルアミン等の塩基存在下で行う。また、例えば銅やパラジウム錯体等の遷移金属触媒存在下で行うこともできる。
なお、通常、ホウ素誘導体とハロゲン化物との反応工程は例えば炭酸カリウム、tert−ブトキシナトリウム、トリエチルアミン等の塩基存在下で行う。また、必要に応じて、例えば銅やパラジウム錯体等の遷移金属触媒存在下で行うこともできる。さらにホウ素誘導体との反応工程では、例えば、炭酸カリウム、りん酸カリウム、tert−ブトキシナトリウム、トリエチルアミン等の塩基、又は、パラジウム錯体等の遷移金属触媒の存在下で行うことができる。
Usually, the reaction step between the primary or secondary amine compound and the halide is carried out in the presence of a base such as potassium carbonate, tert-butoxysodium or triethylamine. It can also be carried out in the presence of a transition metal catalyst such as a copper or palladium complex.
Usually, the reaction step between the boron derivative and the halide is carried out in the presence of a base such as potassium carbonate, tert-butoxysodium or triethylamine. Further, if necessary, it can be carried out in the presence of a transition metal catalyst such as copper or a palladium complex. Further, the reaction step with the boron derivative can be carried out in the presence of a base such as potassium carbonate, potassium phosphate, tert-butoxysodium or triethylamine, or a transition metal catalyst such as a palladium complex.
<有機電界発光素子材料>
本発明の重合体は、有機電界発光素子材料として用いられることが好ましい。つまり、本発明の重合体は有機電界発光素子材料であることが好ましい。
本発明の重合体が有機電界発光素子材料として用いられる場合は、有機電界発素子における正孔注入層及び正孔輸送層の少なくとも一方を形成する材料、つまり電荷輸送材料として用いることが好ましい。
電荷輸送材料として用いる場合、本発明の重合体を1種類含有するものであってもよく、2種類以上を任意の組み合わせ及び任意の比率で含有するものであってもよい。
<Organic electroluminescent device material>
The polymer of the present invention is preferably used as an organic electroluminescent device material. That is, the polymer of the present invention is preferably an organic electroluminescent device material.
When the polymer of the present invention is used as an organic electroluminescent device material, it is preferably used as a material that forms at least one of a hole injection layer and a hole transport layer in an organic electroluminescent device, that is, a charge transport material.
When used as a charge transport material, it may contain one type of the polymer of the present invention, or may contain two or more types in any combination and in any ratio.
本発明の重合体を用いて有機電界発光素子の正孔注入層及び正孔輸送層の少なくとも一方を形成する場合、正孔注入層及び/又は正孔輸送層中の本発明の重合体の含有量は、通常1〜100質量%、好ましくは5〜100質量%、さらに好ましくは10〜100質量%である。上記の範囲であると、正孔注入層及び/又は正孔輸送層の電荷輸送性が向上し、駆動電圧が低減し、駆動安定性が向上するため好ましい。 When the polymer of the present invention is used to form at least one of the hole injection layer and the hole transport layer of the organic electroluminescent device, the inclusion of the polymer of the present invention in the hole injection layer and / or the hole transport layer. The amount is usually 1 to 100% by mass, preferably 5 to 100% by mass, and more preferably 10 to 100% by mass. The above range is preferable because the charge transportability of the hole injection layer and / or the hole transport layer is improved, the drive voltage is reduced, and the drive stability is improved.
本発明に係る重合体が、前記正孔注入層及び/又は正孔輸送層中で100質量%でない場合に、正孔注入層及び/又は正孔輸送層を構成する成分としては後述する正孔輸送性化合物等が挙げられる。
また、有機電界発光素子を簡便に製造することができることから、本発明の重合体は、湿式成膜法で形成される有機層に用いることが好ましい。
When the polymer according to the present invention is not 100% by mass in the hole injection layer and / or the hole transport layer, the holes constituting the hole injection layer and / or the hole transport layer will be described later. Transportable compounds and the like can be mentioned.
Further, since the organic electroluminescent device can be easily manufactured, the polymer of the present invention is preferably used for the organic layer formed by the wet film forming method.
[有機電界発光素子用組成物]
本発明の有機電界発光素子用組成物は、本発明の重合体を含有するものである。なお、本発明の有機電界発光素子用組成物は、本発明の重合体を1種類含有するものであってもよく、2種類以上を任意の組み合わせ及び任意の比率で含有するものであってもよい。
[Composition for organic electroluminescent device]
The composition for an organic electroluminescent device of the present invention contains the polymer of the present invention. The composition for an organic electroluminescent device of the present invention may contain one type of the polymer of the present invention, or may contain two or more types in an arbitrary combination and an arbitrary ratio. Good.
{重合体の含有量}
本発明の有機電界発光素子用組成物中の本発明の重合体の含有量は、通常0.01〜70質量%、好ましくは0.1〜60質量%、さらに好ましくは0.5〜50質量%である。
上記範囲内であると、形成した有機層に欠陥が生じ難く、また膜厚ムラが生じ難いため好ましい。
本発明における有機電界発光素子用組成物は、本発明に係る重合体以外に溶媒等を含むことができる。
{Polymer content}
The content of the polymer of the present invention in the composition for an organic electroluminescent element of the present invention is usually 0.01 to 70% by mass, preferably 0.1 to 60% by mass, and more preferably 0.5 to 50% by mass. %.
When it is within the above range, defects are unlikely to occur in the formed organic layer and uneven film thickness is unlikely to occur, which is preferable.
The composition for an organic electroluminescent device in the present invention may contain a solvent or the like in addition to the polymer according to the present invention.
{溶媒}
本発明の有機電界発光素子用組成物は、通常、溶媒を含有する。この溶媒は、本発明の重合体を溶解するものが好ましい。具体的には、本発明の重合体を、室温で通常0.05質量%以上、好ましくは0.5質量%以上、さらに好ましくは1質量%以上溶解する溶媒が好適である。
溶媒の具体例としては、トルエン、キシレン、メシチレン、シクロヘキシルベンゼン等の芳香族系溶媒;1,2−ジクロロエタン、クロロベンゼン、o−ジクロロベンゼン等の含ハロゲン溶媒;エチレングリコールジメチルエーテル、エチレングリコールジエチルエーテル、プロピレングリコール−1−モノメチルエーテルアセタート(PGMEA)等の脂肪族エーテル、1,2−ジメトキシベンゼン、1,3−ジメトキシベンゼン、アニソール、フェネトール、2−メトキシトルエン、3−メトキシトルエン、4−メトキシトルエン、2,3−ジメチルアニソール、2,4−ジメチルアニソール等の芳香族エーテル等のエーテル系溶媒;酢酸エチル、酢酸n−ブチル、乳酸エチル、乳酸n−ブチル等の脂肪族エステル;酢酸フェニル、プロピオン酸フェニル、安息香酸メチル、安息香酸エチル、安息香酸イソプロピル、安息香酸プロピル、安息香酸n−ブチル等の芳香族エステル等のエステル系溶媒;などの有機溶媒、その他、後述の正孔注入層形成用組成物や正孔輸送層形成用組成物に用いられる有機溶媒が挙げられる。
なお、溶媒は、1種類を用いてもよく、2種類以上を任意の組み合わせ及び任意の比率で併用してもよい。
{solvent}
The composition for an organic electroluminescent device of the present invention usually contains a solvent. The solvent is preferably one that dissolves the polymer of the present invention. Specifically, a solvent that dissolves the polymer of the present invention in an amount of usually 0.05% by mass or more, preferably 0.5% by mass or more, and more preferably 1% by mass or more at room temperature is preferable.
Specific examples of the solvent include aromatic solvents such as toluene, xylene, mesityrene and cyclohexylbenzene; halogen-containing solvents such as 1,2-dichloroethane, chlorobenzene and o-dichlorobenzene; ethylene glycol dimethyl ether, ethylene glycol diethyl ether and propylene. Aliper ethers such as glycol-1-monomethyl ether acetate (PGMEA), 1,2-dimethoxybenzene, 1,3-dimethoxybenzene, anisole, phenetol, 2-methoxytoluene, 3-methoxytoluene, 4-methoxytoluene, Ether-based solvents such as aromatic ethers such as 2,3-dimethylanisole and 2,4-dimethylanisole; aliphatic esters such as ethyl acetate, n-butyl acetate, ethyl lactate and n-butyl lactate; phenyl acetate and propionic acid Ester-based solvents such as phenyl, methyl benzoate, ethyl benzoate, isopropyl benzoate, propyl benzoate, n-butyl benzoate and other aromatic esters; and other organic solvents, and other compositions for forming a hole injection layer, which will be described later. Examples thereof include organic solvents used for substances and compositions for forming a hole transport layer.
As the solvent, one type may be used, or two or more types may be used in any combination and in any ratio.
中でも、本発明の有機電界発光素子用組成物に含有される溶媒としては、20℃における表面張力が、通常40dyn/cm未満、好ましくは36dyn/cm以下、より好ましくは33dyn/cm以下である溶媒が好ましい。 Among them, as the solvent contained in the composition for an organic electroluminescent device of the present invention, a solvent having a surface tension at 20 ° C. of usually less than 40 dyn / cm, preferably 36 dyn / cm or less, more preferably 33 dyn / cm or less. Is preferable.
本発明の有機電界発光素子用組成物を用いて湿式成膜法により塗膜を形成し、本発明の重合体を架橋させて有機層を形成する場合、溶媒と下地の親和性が高いことが好ましい。これは、膜質の均一性が有機電界発光素子の発光の均一性及び安定性に大きく影響するためである。従って、湿式成膜法に用いる有機電界発光素子用組成物には、よりレベリング性が高く均一な塗膜を形成しうるように表面張力が低いことが求められる。そこで前記のような低い表面張力を有する溶媒を使用することにより、本発明の重合体を含有する均一な層を形成することができ、ひいては均一な架橋層を形成することができることから、好ましい。 When a coating film is formed by a wet film forming method using the composition for an organic electroluminescent element of the present invention and the polymer of the present invention is crosslinked to form an organic layer, the affinity between the solvent and the substrate is high. preferable. This is because the uniformity of the film quality greatly affects the uniformity and stability of the light emission of the organic electroluminescent device. Therefore, the composition for an organic electroluminescent device used in the wet film forming method is required to have a low surface tension so that a more levelable and uniform coating film can be formed. Therefore, by using a solvent having a low surface tension as described above, a uniform layer containing the polymer of the present invention can be formed, and a uniform crosslinked layer can be formed, which is preferable.
低表面張力の溶媒の具体例としては、前述したトルエン、キシレン、メシチレン、シクロヘキシルベンゼン等の芳香族系溶媒、安息香酸エチル等のエステル系溶媒、アニソール等のエーテル系溶媒、トリフルオロメトキシアニソール、ペンタフルオロメトキシベンゼン、3−(トリフルオロメチル)アニソール、エチル(ペンタフルオロベンゾエート)等が挙げられる。 Specific examples of the low surface tension solvent include the above-mentioned aromatic solvents such as toluene, xylene, mesityrene and cyclohexylbenzene, ester solvents such as ethyl benzoate, ether solvents such as anisole, trifluoromethoxyanisole and penta. Fluoromethoxybenzene, 3- (trifluoromethyl) anisole, ethyl (pentafluorobenzoate) and the like can be mentioned.
また一方で、本発明の有機電界発光素子用組成物に含有される溶媒としては、25℃における蒸気圧が、通常10mmHg以下、好ましくは5mmHg以下であり、通常0.1mmHg以上であるものが好ましい。このような溶媒を使用することにより、有機電界発光素子を湿式成膜法により製造するプロセスに好適で、本発明の重合体の性質に適した有機電界発光素子用組成物を調製することができる。 On the other hand, as the solvent contained in the composition for an organic electroluminescent device of the present invention, a solvent having a vapor pressure at 25 ° C. of usually 10 mmHg or less, preferably 5 mmHg or less, and usually 0.1 mmHg or more is preferable. .. By using such a solvent, a composition for an organic electroluminescent device suitable for the process of manufacturing an organic electroluminescent device by a wet film forming method and suitable for the properties of the polymer of the present invention can be prepared. ..
このような溶媒の具体例としては、前述したトルエン、キシレン、メシチレン等の芳香族系溶媒、エーテル系溶媒及びエステル系溶媒が挙げられる。 Specific examples of such a solvent include the above-mentioned aromatic solvents such as toluene, xylene and mesitylene, ether solvents and ester solvents.
ところで、水分は有機電界発光素子の性能劣化を引き起こす可能性があり、中でも特に連続駆動時の輝度低下を促進する可能性がある。そこで、湿式成膜中に残留する水分をできる限り低減するために、前記の溶媒の中でも、25℃における水の溶解度が1質量%以下であるものが好ましく、0.1質量%以下である溶媒がより好ましい。 By the way, moisture may cause deterioration of the performance of the organic electroluminescent device, and in particular, it may promote a decrease in brightness during continuous driving. Therefore, in order to reduce the water content remaining during the wet film formation as much as possible, among the above-mentioned solvents, those having a water solubility at 25 ° C. of 1% by mass or less are preferable, and those having a solubility of 0.1% by mass or less are preferable. Is more preferable.
本発明の有機電界発光素子用組成物に含有される溶媒の含有量は、通常10質量%以上、好ましくは30質量%以上、より好ましくは50質量%以上、特に好ましくは80質量%以上である。溶媒の含有量が上記下限以上であることにより、形成される層の平坦さ及び均一さを良好にすることができる。 The content of the solvent contained in the composition for an organic electroluminescent device of the present invention is usually 10% by mass or more, preferably 30% by mass or more, more preferably 50% by mass or more, and particularly preferably 80% by mass or more. .. When the content of the solvent is at least the above lower limit, the flatness and uniformity of the formed layer can be improved.
<電子受容性化合物>
本発明の有機電界発光素子用組成物は、正孔注入層を形成するために用いる場合、低抵抗化する点で、さらに電子受容性化合物を含有することが好ましい。
<Electron-receptive compound>
When the composition for an organic electroluminescent device of the present invention is used for forming a hole injection layer, it preferably further contains an electron-accepting compound in terms of lowering the resistance.
電子受容性化合物としては、酸化力を有し、本発明の重合体から一電子受容する能力を有する化合物が好ましい。具体的には、電子親和力が4eV以上である化合物が好ましく、5eV以上である化合物がさらに好ましい。 As the electron-accepting compound, a compound having an oxidizing power and an ability to accept one electron from the polymer of the present invention is preferable. Specifically, a compound having an electron affinity of 4 eV or more is preferable, and a compound having an electron affinity of 5 eV or more is more preferable.
このような電子受容性化合物としては、例えば、トリアリールホウ素化合物、ハロゲン化金属、ルイス酸、有機酸、オニウム塩、アリールアミンとハロゲン化金属との塩、及び、アリールアミンとルイス酸との塩よりなる群から選ばれる1種又は2種以上の化合物等が挙げられる。 Examples of such an electron-accepting compound include a triarylboron compound, a metal halide, a Lewis acid, an organic acid, an onium salt, a salt of an arylamine and a metal halide, and a salt of an arylamine and a Lewis acid. Examples thereof include one kind or two or more kinds of compounds selected from the group consisting of two or more kinds.
具体的には、4−イソプロピル−4’−メチルジフェニルヨードニウムテトラキス(ペンタフルオロフェニル)ボラート、トリフェニルスルホニウムテトラフルオロボラート等の有機基の置換したオニウム塩(国際公開第2005/089024号);塩化鉄(III)(日本国特開平11−251067号公報)、ペルオキソ二硫酸アンモニウム等の高原子価の無機化合物;テトラシアノエチレン等のシアノ化合物;トリス(ペンタフルオロフェニル)ボラン(日本国特開2003−31365号公報)等の芳香族ホウ素化合物;フラーレン誘導体及びヨウ素等が挙げられる。 Specifically, an onium salt substituted with an organic group such as 4-isopropyl-4'-methyldiphenyliodonium tetrakis (pentafluorophenyl) borate, triphenylsulfonium tetrafluoroborate (International Publication No. 2005/089024); chloride. High valence inorganic compounds such as iron (III) (Japanese Patent Laid-Open No. 11-251067), ammonium peroxodisulfate; cyano compounds such as tetracyanoethylene; tris (pentafluorophenyl) borane (Japanese Patent Laid-Open No. 2003-) Aromatic boron compounds such as 31365); fullerene derivatives, iodine and the like can be mentioned.
このような化合物として、長周期型周期表(以下、特に断り書きの無い限り「周期表」という場合には、長周期型周期表を指すものとする。)の第15〜17族に属する元素に、少なくとも一つの有機基が炭素原子で結合した構造を有するイオン化合物であることが好ましく、特に、下記式(4)で表される化合物であることが好ましい。 As such a compound, an element belonging to the 15th to 17th groups of the long-periodic periodic table (hereinafter, unless otherwise specified, the term "periodic table" refers to the long-periodic table). In addition, it is preferably an ionic compound having a structure in which at least one organic group is bonded by a carbon atom, and in particular, a compound represented by the following formula (4) is preferable.
式(4)中、R6は、A1と炭素原子で結合する有機基を表し、R7は、任意の置換基を表す。R6及びR7は、互いに結合して環を形成していてもよい。
R6としては、A1との結合部分に炭素原子を有する有機基であれば、本発明の趣旨に反しない限り、その種類は特に制限されない。R6の分子量は、置換基を含めた値で、通常1000以下、好ましくは500以下の範囲である。
In formula (4), R 6 represents an organic group bonded to A 1 at a carbon atom, and R 7 represents an arbitrary substituent. R 6 and R 7 may be coupled to each other to form a ring.
The type of R 6 is not particularly limited as long as it is an organic group having a carbon atom at the bonding portion with A 1, as long as it does not contradict the gist of the present invention. The molecular weight of R 6 is a value including a substituent and is usually in the range of 1000 or less, preferably 500 or less.
R6の好ましい例としては、正電荷を非局在化させる点から、アルキル基、アルケニル基、アルキニル基、芳香族炭化水素基、芳香族複素環基が挙げられる。中でも、正電荷を非局在化させるとともに熱的に安定であることから、芳香族炭化水素基又は芳香族複素環基が好ましい。 Preferred examples of R 6 include an alkyl group, an alkenyl group, an alkynyl group, an aromatic hydrocarbon group, and an aromatic heterocyclic group from the viewpoint of delocalizing the positive charge. Of these, an aromatic hydrocarbon group or an aromatic heterocyclic group is preferable because it delocalizes the positive charge and is thermally stable.
芳香族炭化水素基としては、1個の遊離原子価を有する、5員環若しくは6員環の単環又は2〜5縮合環であり、正電荷を当該基上により非局在化させられる基が挙げられる。その具体例としては、1個の遊離原子価を有する、ベンゼン環、ナフタレン環、アントラセン環、フェナントレン環、ペリレン環、テトラセン環、ピレン環、ベンズピレン環、クリセン環、トリフェニレン環、アセナフテン環、フルオレン環等が挙げられる。 The aromatic hydrocarbon group is a 5-membered ring or a 6-membered ring monocyclic ring or a 2-5 condensed ring having one free valence, and a group capable of delocalizing a positive charge on the group. Can be mentioned. Specific examples thereof include a benzene ring, a naphthalene ring, an anthracene ring, a phenanthrene ring, a perylene ring, a tetracene ring, a pyrene ring, a benzpyrene ring, a chrysene ring, a triphenylene ring, an acenaphthene ring, and a fluorene ring having one free valence. And so on.
芳香族複素環基としては、1個の遊離原子価を有する、5員環若しくは6員環の単環又は2〜4縮合環であり、正電荷を当該基上により非局在化させられる基が挙げられる。その具体例としては、1個の遊離原子価を有する、フラン環、ベンゾフラン環、チオフェン環、ベンゾチオフェン環、ピロール環、ピラゾール環、トリアゾール環、イミダゾール環、オキサジアゾール環、インドール環、カルバゾール環、ピロロイミダゾール環、ピロロピラゾール環、ピロロピロール環、チエノピロール環、チエノチオフェン環、フロピロール環、フロフラン環、チエノフラン環、ベンゾイソオキサゾール環、ベンゾイソチアゾール環、ベンゾイミダゾール環、ピリジン環、ピラジン環、ピリダジン環、ピリミジン環、トリアジン環、キノリン環、イソキノリン環、シンノリン環、キノキサリン環、フェナントリジン環、ベンゾイミダゾール環、ペリミジン環、キナゾリン環、キナゾリノン環、アズレン環等が挙げられる。 The aromatic heterocyclic group is a 5- or 6-membered monocyclic ring or a 2-4 condensed ring having one free valence, and a group capable of delocalizing a positive charge on the group. Can be mentioned. Specific examples thereof include a furan ring, a benzofuran ring, a thiophene ring, a benzothiophene ring, a pyrrole ring, a pyrazole ring, a triazole ring, an imidazole ring, an oxadiazole ring, an indol ring, and a carbazole ring, which have one free valence. , Pyrroylmidazole ring, pyrrolopyrazole ring, pyrrolopyrrole ring, thienopyrrole ring, thienothiophene ring, flopyrol ring, flofuran ring, thienofran ring, benzoisoxazole ring, benzoisothiazole ring, benzimidazole ring, pyridine ring, pyrazine ring, pyridazine Examples thereof include a ring, a pyrimidine ring, a triazine ring, a quinoline ring, an isoquinoline ring, a cinnoline ring, a quinoxaline ring, a phenanthridin ring, a benzimidazole ring, a perimidine ring, a quinazoline ring, a quinazolinone ring, and an azulene ring.
アルキル基としては、直鎖状、分岐鎖状又は環状のアルキル基であって、その炭素数が通常1以上、また、通常12以下、好ましくは6以下のものが挙げられる。具体例としては、メチル基、エチル基、n−プロピル基、2−プロピル基、n−ブチル基、イソブチル基、tert−ブチル基、シクロヘキシル基等が挙げられる。 Examples of the alkyl group include linear, branched or cyclic alkyl groups having a carbon number of usually 1 or more, and usually 12 or less, preferably 6 or less. Specific examples include a methyl group, an ethyl group, an n-propyl group, a 2-propyl group, an n-butyl group, an isobutyl group, a tert-butyl group, a cyclohexyl group and the like.
アルケニル基としては、炭素数が通常2以上、通常12以下、好ましくは6以下のものが挙げられる。具体例としては、ビニル基、アリル基、1−ブテニル基等が挙げられる。 Examples of the alkenyl group include those having a carbon number of usually 2 or more, usually 12 or less, and preferably 6 or less. Specific examples include a vinyl group, an allyl group, a 1-butenyl group and the like.
アルキニル基としては、炭素数が通常2以上、通常12以下、好ましくは6以下のものが挙げられる。具体例としては、エチニル基、プロパルギル基等が挙げられる。 Examples of the alkynyl group include those having a carbon number of usually 2 or more, usually 12 or less, and preferably 6 or less. Specific examples include an ethynyl group and a propargyl group.
R7は、本発明の趣旨に反しない限り特に制限されない。R7の分子量は、置換基を含めた値で、通常1000以下、好ましくは500以下の範囲である。 R 7 is not particularly limited as long as it does not contradict the gist of the present invention. The molecular weight of R 7 is a value including a substituent and is usually in the range of 1000 or less, preferably 500 or less.
R7の例としては、アルキル基、アルケニル基、アルキニル基、芳香族炭化水素基、芳香族複素環基、アミノ基、アルコキシ基、アリーロキシ基、アシル基、アルコキシカルボニル基、アリーロキシカルボニル基、アルキルカルボニルオキシ基、アルキルチオ基、アリールチオ基、スルホニル基、アルキルスルホニル基、アリールスルホニル基、シアノ基、水酸基、チオール基、シリル基等が挙げられる。 Examples of R 7 include alkyl group, alkenyl group, alkynyl group, aromatic hydrocarbon group, aromatic heterocyclic group, amino group, alkoxy group, allyloxy group, acyl group, alkoxycarbonyl group, allyloxycarbonyl group and alkyl. Examples thereof include a carbonyloxy group, an alkylthio group, an arylthio group, a sulfonyl group, an alkylsulfonyl group, an arylsulfonyl group, a cyano group, a hydroxyl group, a thiol group and a silyl group.
中でも、R6と同様、電子受容性が大きい点から、A1との結合部分に炭素原子を有する有機基が好ましく、例としては、アルキル基、アルケニル基、アルキニル基、芳香族炭化水素基、芳香族複素環基が好ましい。特に、電子受容性が大きいとともに熱的に安定であることから、芳香族炭化水素基又は芳香族複素環基が好ましい。 Among them, like R 6 , an organic group having a carbon atom at the bonding portion with A 1 is preferable because of its high electron acceptability, and examples thereof include an alkyl group, an alkenyl group, an alkynyl group, and an aromatic hydrocarbon group. Aromatic heterocyclic groups are preferred. In particular, an aromatic hydrocarbon group or an aromatic heterocyclic group is preferable because it has high electron acceptability and is thermally stable.
R7のアルキル基、アルケニル基、アルキニル基、芳香族炭化水素基、芳香族複素環基としては、R6について先に説明したものと同様のものが挙げられる。 Alkyl group, an alkenyl group of R 7, alkynyl group, aromatic hydrocarbon group, the aromatic heterocyclic group include the same as those described for R 6 above.
アミノ基としては、アルキルアミノ基、アリールアミノ基、アシルアミノ基等が挙げられる。 Examples of the amino group include an alkylamino group, an arylamino group, an acylamino group and the like.
アルキルアミノ基としては、炭素数が通常1以上、また、通常12以下、好ましくは6以下のアルキル基を1つ以上有するアルキルアミノ基が挙げられる。具体例としては、メチルアミノ基、ジメチルアミノ基、ジエチルアミノ基、ジベンジルアミノ基等が挙げられる。 Examples of the alkylamino group include an alkylamino group having at least one alkyl group having usually 1 or more carbon atoms and usually 12 or less, preferably 6 or less carbon atoms. Specific examples include a methylamino group, a dimethylamino group, a diethylamino group, a dibenzylamino group and the like.
アリールアミノ基としては、炭素数が通常3以上、好ましくは4以上、また、通常25以下、好ましくは15以下の芳香族炭化水素基又は芳香族複素環基を1つ以上有するアリールアミノ基が挙げられる。具体例としては、フェニルアミノ基、ジフェニルアミノ基、トリルアミノ基、ピリジルアミノ基、チエニルアミノ基等が挙げられる。 Examples of the arylamino group include an arylamino group having one or more aromatic hydrocarbon groups or aromatic heterocyclic groups having usually 3 or more carbon atoms, preferably 4 or more, and usually 25 or less, preferably 15 or less carbon atoms. Be done. Specific examples include a phenylamino group, a diphenylamino group, a tolylamino group, a pyridylamino group, a thienylamino group and the like.
アシルアミノ基としては、炭素数が通常2以上、また、通常25以下、好ましくは15以下のアシル基を1つ以上有するアシルアミノ基が挙げられる。具体例としては、アセチルアミノ基、ベンゾイルアミノ基等が挙げられる。 Examples of the acylamino group include an acylamino group having one or more acyl groups having usually 2 or more carbon atoms and usually 25 or less, preferably 15 or less carbon atoms. Specific examples include an acetylamino group and a benzoylamino group.
アルコキシ基としては、炭素数が通常1以上、また、通常12以下、好ましくは6以下のアルコキシ基が挙げられる。具体例としては、メトキシ基、エトキシ基、ブトキシ基等が挙げられる。 Examples of the alkoxy group include an alkoxy group having usually 1 or more carbon atoms and usually 12 or less, preferably 6 or less carbon atoms. Specific examples include a methoxy group, an ethoxy group, a butoxy group and the like.
アリールオキシ基としては、炭素数が通常3以上、好ましくは4以上、また、通常25以下、好ましくは15以下の芳香族炭化水素基又は芳香族複素環基を有するアリールオキシ基が挙げられる。具体例としては、フェニルオキシ基、ナフチルオキシ基、ピリジルオキシ基、チエニルオキシ基等が挙げられる。 Examples of the aryloxy group include an aryloxy group having an aromatic hydrocarbon group or an aromatic heterocyclic group having a carbon number of usually 3 or more, preferably 4 or more, and usually 25 or less, preferably 15 or less. Specific examples include a phenyloxy group, a naphthyloxy group, a pyridyloxy group, a thienyloxy group and the like.
アシル基としては、炭素数が通常1以上、また、通常25以下、好ましくは15以下のアシル基が挙げられる。具体例としては、ホルミル基、アセチル基、ベンゾイル基等が挙げられる。 Examples of the acyl group include an acyl group having usually 1 or more carbon atoms and usually 25 or less, preferably 15 or less carbon atoms. Specific examples include a formyl group, an acetyl group, a benzoyl group and the like.
アルコキシカルボニル基としては、炭素数が通常2以上、また、通常10以下、好ましくは7以下のアルコキシカルボニル基が挙げられる。具体例としては、メトキシカルボニル基、エトキシカルボニル基等が挙げられる。 Examples of the alkoxycarbonyl group include an alkoxycarbonyl group having usually 2 or more carbon atoms and usually 10 or less, preferably 7 or less carbon atoms. Specific examples include a methoxycarbonyl group and an ethoxycarbonyl group.
アリールオキシカルボニル基としては、炭素数が通常3以上、好ましくは4以上、また、通常25以下、好ましくは15以下の芳香族炭化水素基又は芳香族複素環基を有するものが挙げられる。具体例としては、フェノキシカルボニル基、ピリジルオキシカルボニル基等が挙げられる。 Examples of the aryloxycarbonyl group include those having an aromatic hydrocarbon group or an aromatic heterocyclic group having a carbon number of usually 3 or more, preferably 4 or more, and usually 25 or less, preferably 15 or less. Specific examples include a phenoxycarbonyl group and a pyridyloxycarbonyl group.
アルキルカルボニルオキシ基としては、炭素数が通常2以上、また、通常10以下、好ましくは7以下のアルキルカルボニルオキシ基が挙げられる。具体例としては、アセトキシ基、トリフルオロアセトキシ基等が挙げられる。 Examples of the alkylcarbonyloxy group include an alkylcarbonyloxy group having usually 2 or more carbon atoms and usually 10 or less, preferably 7 or less carbon atoms. Specific examples include an acetoxy group and a trifluoroacetoxy group.
アルキルチオ基としては、炭素数が通常1以上、また、通常12以下、好ましくは6以下のアルキルチオ基が挙げられる。具体例としては、メチルチオ基、エチルチオ基等が挙げられる。 Examples of the alkylthio group include an alkylthio group having usually 1 or more carbon atoms and usually 12 or less, preferably 6 or less carbon atoms. Specific examples include a methylthio group and an ethylthio group.
アリールチオ基としては、炭素数が通常3以上、好ましくは4以上、また、通常25以下、好ましくは14以下のアリールチオ基が挙げられる。具体例としては、フェニルチオ基、ナフチルチオ基、ピリジルチオ基等が挙げられる。 Examples of the arylthio group include an arylthio group having a carbon number of usually 3 or more, preferably 4 or more, and usually 25 or less, preferably 14 or less. Specific examples include a phenylthio group, a naphthylthio group, a pyridylthio group and the like.
アルキルスルホニル基及びアリールスルホニル基の具体例としては、メシル基、トシル基等が挙げられる。 Specific examples of the alkylsulfonyl group and the arylsulfonyl group include a mesylate group and a tosyl group.
スルホニルオキシ基の具体例としては、メシルオキシ基、トシルオキシ基等が挙げられる。 Specific examples of the sulfonyloxy group include a mesyloxy group and a tosyloxy group.
シリル基の具体例としては、トリメチルシリル基、トリフェニルシリル基などが挙げられる。 Specific examples of the silyl group include a trimethylsilyl group and a triphenylsilyl group.
以上、R6及びR7として例示した基は、本発明の趣旨に反しない限りにおいて、更に他の置換基によって置換されていてもよい。置換基の種類は特に制限されないが、例としては、上記R6及びR7、としてそれぞれ例示した基の他、ハロゲン原子、シアノ基、チオシアノ基、ニトロ基等が挙げられる。中でも、イオン化合物(電子受容性化合物)の耐熱性及び電子受容性の妨げにならない観点から、アルキル基、アルケニル基、アルキニル基、アルコキシ基、アリールオキシ基、芳香族炭化水素基、芳香族複素環基が好ましい。 As described above, the groups exemplified as R 6 and R 7 may be further substituted with other substituents as long as it does not contradict the gist of the present invention. The type of the substituent is not particularly limited, and examples thereof include a halogen atom, a cyano group, a thiocyano group, a nitro group, and the like, in addition to the groups exemplified as R 6 and R 7, respectively. Above all, from the viewpoint of not interfering with the heat resistance and electron acceptability of the ionic compound (electron-accepting compound), an alkyl group, an alkenyl group, an alkynyl group, an alkoxy group, an aryloxy group, an aromatic hydrocarbon group and an aromatic heterocycle Groups are preferred.
式(4)中、A1は、周期表の第17族に属する元素であることが好ましく、電子受容性及び入手容易性の観点から、周期表の第5周期以前(第3〜第5周期)の元素が好ましい。即ち、A1としてはヨウ素原子、臭素原子、塩素原子のうち何れかが好ましい。 In formula (4), A 1 is preferably an element belonging to Group 17 of the periodic table, and from the viewpoint of electron acceptability and availability, it is before the 5th cycle of the periodic table (3rd to 5th cycles). ) Is preferable. That is, an iodine atom as A 1, a bromine atom, either of the chlorine atoms are preferred.
特に、電子受容性、化合物の安定性の面から、式(4)におけるA1が臭素原子又はヨウ素原子であるイオン化合物が好ましく、ヨウ素原子であるイオン化合物が最も好ましい。 In particular, an electron-accepting, in view of stability of the compound, ionic compound is preferably A 1 in the formula (4) is a bromine atom or an iodine atom, ion compound is most preferably an iodine atom.
式(4)中、Z1 n1−は、対アニオンを表す。対アニオンの種類は特に制限されず、単原子イオンであっても錯イオンであってもよい。但し、対アニオンのサイズが大きいほど負電荷が非局在化し、それに伴い正電荷も非局在化して電子受容能が大きくなるため、単原子イオンよりも錯イオンの方が好ましい。 In formula (4), Z 1 n1- represents a counter anion. The type of counter anion is not particularly limited, and may be a monatomic ion or a complex ion. However, as the size of the counter anion is larger, the negative charge is delocalized, and the positive charge is also delocalized accordingly, so that the electron accepting capacity is increased. Therefore, the complex ion is preferable to the monatomic ion.
n1は、対アニオンZ1 n1−のイオン価に相当する任意の正の整数である。n1の値は特に制限されないが、1又は2であることが好ましく、1であることが最も好ましい。 n 1 is any positive integer corresponding to the ionic value of the counter anion Z 1 n1-. The value of n 1 is not particularly limited, but is preferably 1 or 2, and most preferably 1.
Z1 n1−の具体例としては、水酸化物イオン、フッ化物イオン、塩化物イオン、臭化物イオン、ヨウ化物イオン、シアン化物イオン、硝酸イオン、亜硝酸イオン、硫酸イオン、亜硫酸イオン、過塩素酸イオン、過臭素酸イオン、過ヨウ素酸イオン、塩素酸イオン、亜塩素酸イオン、次亜塩素酸イオン、リン酸イオン、亜リン酸イオン、次亜リン酸イオン、ホウ酸イオン、イソシアン酸イオン、硫化水素イオン、テトラフルオロホウ酸イオン、ヘキサフルオロリン酸イオン、ヘキサクロロアンチモン酸イオン;酢酸イオン、トリフルオロ酢酸イオン、安息香酸イオン等のカルボン酸イオン;メタンスルホン酸、トリフルオロメタンスルホン酸イオン等のスルホン酸イオン;メトキシイオン、t−ブトキシイオン等のアルコキシイオンなどが挙げられ、テトラフルオロホウ素酸イオン及びヘキサフルオロホウ素酸イオンが好ましい。 Specific examples of Z 1 n1- include hydroxide ion, fluoride ion, chloride ion, bromide ion, iodide ion, cyanide ion, nitrate ion, nitrite ion, sulfate ion, sulfite ion, and perchloric acid. Ion, perbromate ion, periodate ion, chlorate ion, chlorite ion, hypochlorite ion, phosphate ion, phosphite ion, hypophosphite ion, borate ion, isocyanate ion, Hydrogen sulfide ion, tetrafluoroborate ion, hexafluorophosphate ion, hexachloroantimonate ion; carboxylic acid ion such as acetate ion, trifluoroacetate ion, benzoate ion; sulfone such as methanesulfonic acid and trifluoromethanesulfonic acid ion Acid ion; Examples thereof include alkoxy ions such as methoxy ion and t-butoxy ion, and tetrafluoroborate ion and hexafluoroborate ion are preferable.
また、対アニオンZ1 n1−としては、化合物の安定性、溶媒への溶解性の点及び、サイズが大きいという点で、負電荷が非局在化し、それに伴い正電荷も非局在化して電子受容能が大きくなるため、下記式(5)で表される錯イオンが特に好ましい。 Further, as the counter anion Z 1 n1- , the negative charge is delocalized in terms of the stability of the compound, the solubility in the solvent, and the large size, and the positive charge is also delocalized accordingly. The complex ion represented by the following formula (5) is particularly preferable because the electron accepting capacity is increased.
式(5)中、E3は、各々独立に、長周期型周期表の第13族に属する元素を表す。中でもホウ素原子、アルミニウム原子、ガリウム原子が好ましく、化合物の安定性、合成及び精製のし易さの点から、ホウ素原子が好ましい。 In formula (5), E 3 independently represents an element belonging to Group 13 of the long periodic table. Of these, a boron atom, an aluminum atom, and a gallium atom are preferable, and a boron atom is preferable from the viewpoint of stability of the compound and ease of synthesis and purification.
式(5)中、Ar6〜Ar9は、各々独立に、芳香族炭化水素基又は芳香族複素環基を表す。芳香族炭化水素基、芳香族複素環基の例示としては、R6について先に例示したものと同様の、1個の遊離原子価を有する、5員環若しくは6員環の単環又は2〜4縮合環が挙げられる。中でも、化合物の安定性、耐熱性の点から、1個の遊離原子価を有する、ベンゼン環、ナフタレン環、ピリジン環、ピラジン環、ピリダジン環、ピリミジン環、トリアジン環、キノリン環、イソキノリン環が好ましい。 In formula (5), Ar 6 to Ar 9 each independently represent an aromatic hydrocarbon group or an aromatic heterocyclic group. Aromatic hydrocarbon group, Exemplary aromatic heterocyclic group, the same as those exemplified for R 6 above, having one free valence, mono- or 2 five- or six-membered ring Examples include 4-fused rings. Among them, a benzene ring, a naphthalene ring, a pyridine ring, a pyrazine ring, a pyridazine ring, a pyrimidine ring, a triazine ring, a quinoline ring, and an isoquinoline ring having one free atomic value are preferable from the viewpoint of compound stability and heat resistance. ..
Ar6〜Ar9として例示した芳香族炭化水素基、芳香族複素環基は、本発明の趣旨に反しない限りにおいて、更に別の置換基によって置換されていてもよい。置換基の種類は特に制限されず、任意の置換基が適用可能であるが、電子吸引性の基であることが好ましい。 The aromatic hydrocarbon groups and aromatic heterocyclic groups exemplified as Ar 6 to Ar 9 may be further substituted with another substituent as long as it does not contradict the gist of the present invention. The type of the substituent is not particularly limited, and any substituent can be applied, but an electron-withdrawing group is preferable.
Ar6〜Ar9が有してもよい置換基として好ましい電子吸引性の基を例示するならば、フッ素原子、塩素原子、臭素原子等のハロゲン原子;シアノ基;チオシアノ基;ニトロ基;メシル基等のアルキルスルホニル基;トシル基等のアリールスルホニル基;ホルミル基、アセチル基、ベンゾイル基等の、炭素数が通常1以上、通常12以下、好ましくは6以下のアシル基;メトキシカルボニル基、エトキシカルボニル基等の、炭素数が通常2以上、通常10以下、好ましくは7以下のアルコキシカルボニル基;フェノキシカルボニル基、ピリジルオキシカルボニル基等の、炭素数が通常3以上、好ましくは4以上、通常25以下、好ましくは15以下の芳香族炭化水素基又は芳香族複素環基を有するアリールオキシカルボニル基;アミノカルボニル基;アミノスルホニル基;トリフルオロメチル基、ペンタフルオロエチル基等の、炭素数が通常1以上、通常10以下、好ましくは6以下の直鎖状、分岐鎖状又は環状のアルキル基にフッ素原子、塩素原子などのハロゲン原子が置換したハロアルキル基、などが挙げられる。 To exemplify a preferable electron-withdrawing group as a substituent that Ar 6 to Ar 9 may have, a halogen atom such as a fluorine atom, a chlorine atom or a bromine atom; a cyano group; a thiocyano group; a nitro group; a mesyl group. Alkylsulfonyl groups such as; arylsulfonyl groups such as tosyl groups; acyl groups having a carbon number of usually 1 or more, usually 12 or less, preferably 6 or less, such as formyl groups, acetyl groups, benzoyl groups; methoxycarbonyl groups, ethoxycarbonyls, etc. An alkoxycarbonyl group having a group or the like having a carbon number of usually 2 or more, usually 10 or less, preferably 7 or less; a phenoxycarbonyl group, a pyridyloxycarbonyl group or the like having a carbon number of usually 3 or more, preferably 4 or more, usually 25 or less. An aryloxycarbonyl group having an aromatic hydrocarbon group or an aromatic heterocyclic group of 15 or less, preferably an aminocarbonyl group; an aminosulfonyl group; a trifluoromethyl group, a pentafluoroethyl group, etc., which usually have 1 or more carbon atoms. Examples thereof include a haloalkyl group in which a linear, branched or cyclic alkyl group of 10 or less, preferably 6 or less is substituted with a halogen atom such as a fluorine atom or a chlorine atom.
中でも、Ar6〜Ar9のうち少なくとも1つの基が、フッ素原子又は塩素原子を置換基として1つ又は2つ以上有することがより好ましい。特に、負電荷を効率よく非局在化する点、及び、適度な昇華性を有する点から、Ar6〜Ar9の水素原子がすべてフッ素原子で置換されたパーフルオロアリール基であることが最も好ましい。パーフルオロアリール基の具体例としては、ペンタフルオロフェニル基、ヘプタフルオロ−2−ナフチル基、テトラフルオロ−4−ピリジル基等が挙げられる。 Above all, it is more preferable that at least one group of Ar 6 to Ar 9 has one or two or more groups having a fluorine atom or a chlorine atom as a substituent. In particular, it is most likely that the hydrogen atoms of Ar 6 to Ar 9 are all perfluoroaryl groups substituted with fluorine atoms from the viewpoint of efficiently delocalizing negative charges and having appropriate sublimation properties. preferable. Specific examples of the perfluoroaryl group include a pentafluorophenyl group, a heptafluoro-2-naphthyl group, a tetrafluoro-4-pyridyl group and the like.
本発明における電子受容性化合物の分子量は、通常100〜5000、好ましくは300〜3000、更に好ましくは400〜2000である。 The molecular weight of the electron-accepting compound in the present invention is usually 100 to 5000, preferably 300 to 3000, and more preferably 400 to 2000.
上記範囲内であると、正電荷及び負電荷が十分に非局在化し、電子受容能が良好で、また電荷輸送の妨げになり難い点で好ましい。
以下に、本発明に好適な電子受容性化合物の具体例を示すが、本発明はこれらに限定されるものではない。
Within the above range, positive charges and negative charges are sufficiently delocalized, electron acceptability is good, and charge transport is not hindered, which is preferable.
Specific examples of electron-accepting compounds suitable for the present invention are shown below, but the present invention is not limited thereto.
本発明の有機電界発光素子用組成物は、上記のような電子受容性化合物の1種を単独で含んでいてもよく、また2種以上を任意の組み合わせ、及び比率で含んでいてもよい。 The composition for an organic electroluminescent device of the present invention may contain one kind of the above-mentioned electron-accepting compound alone, or may contain two or more kinds in any combination and ratio.
本発明の有機電界発光素子用組成物が電子受容性化合物を含む場合、本発明の有機電界発光素子用組成物の電子受容性化合物の含有量は通常0.0005質量%以上、好ましくは0.001質量%以上で、通常20質量%以下、好ましくは10質量%以下である。また、有機電界発光素子用組成物中の本発明の重合体に対する電子受容性化合物の割合は、通常0.5質量%以上、好ましくは1質量%以上、より好ましくは3質量%以上で、通常80質量%以下、好ましくは60質量%以下、さらに好ましくは40質量%以下である。 When the composition for an organic electroluminescent element of the present invention contains an electron-accepting compound, the content of the electron-accepting compound in the composition for an organic electroluminescent element of the present invention is usually 0.0005% by mass or more, preferably 0. It is 001% by mass or more, usually 20% by mass or less, preferably 10% by mass or less. The ratio of the electron-accepting compound to the polymer of the present invention in the composition for an organic electroluminescent element is usually 0.5% by mass or more, preferably 1% by mass or more, more preferably 3% by mass or more, and is usually used. It is 80% by mass or less, preferably 60% by mass or less, and more preferably 40% by mass or less.
有機電界発光素子用組成物中の電子受容性化合物の含有量が上記下限以上であると重合体から電子受容体が電子を受容し、形成した有機層が低抵抗化するため好ましく、上記上限以下であると形成した有機層に欠陥が生じ難く、また膜厚ムラが生じ難いため好ましい。 When the content of the electron-accepting compound in the composition for an organic electroluminescent device is at least the above lower limit, the electron acceptor receives electrons from the polymer and the formed organic layer has low resistance, which is preferable. This is preferable because defects are less likely to occur in the formed organic layer and uneven film thickness is less likely to occur.
<カチオンラジカル化合物>
本発明の有機電界発光素子用組成物は更にカチオンラジカル化合物を含有していてもよい。
カチオンラジカル化合物としては、正孔輸送性化合物から一電子取り除いた化学種であるカチオンラジカルと、対アニオンとからなるイオン化合物が好ましい。但し、カチオンラジカルが正孔輸送性の高分子化合物由来である場合、カチオンラジカルは高分子化合物の繰り返し単位から一電子取り除いた構造となる。
<Cation radical compound>
The composition for an organic electroluminescent device of the present invention may further contain a cationic radical compound.
As the cation radical compound, an ionic compound composed of a cation radical, which is a chemical species obtained by removing one electron from a hole transporting compound, and a counter anion is preferable. However, when the cation radical is derived from a hole-transporting polymer compound, the cation radical has a structure in which one electron is removed from the repeating unit of the polymer compound.
カチオンラジカルとしては、正孔輸送性化合物として前述した化合物から一電子取り除いた化学種であることが好ましい。正孔輸送性化合物として好ましい化合物から一電子取り除いた化学種であることが、非晶質性、可視光の透過率、耐熱性、及び溶解性などの点から好適である。 The cation radical is preferably a chemical species obtained by removing one electron from the above-mentioned compound as a hole transporting compound. A chemical species obtained by removing one electron from a preferable compound as a hole transporting compound is preferable from the viewpoints of amorphousness, visible light transmittance, heat resistance, solubility and the like.
ここで、カチオンラジカル化合物は、前述の正孔輸送性化合物と前述の電子受容性化合物を混合することにより生成させることができる。即ち、前述の正孔輸送性化合物と前述の電子受容性化合物とを混合することにより、正孔輸送性化合物から電子受容性化合物へと電子移動が起こり、正孔輸送性化合物のカチオンラジカルと対アニオンとからなるカチオンイオン化合物が生成する。 Here, the cationic radical compound can be produced by mixing the above-mentioned hole-transporting compound and the above-mentioned electron-accepting compound. That is, by mixing the above-mentioned hole-transporting compound and the above-mentioned electron-accepting compound, electron transfer occurs from the hole-transporting compound to the electron-accepting compound, and the pair is paired with the cation radical of the hole-transporting compound. A cationic ion compound composed of anions is produced.
本発明の有機電界発光素子用組成物がカチオンラジカル化合物を含む場合、本発明の有機電界発光素子用組成物のカチオンラジカル化合物の含有量は通常0.0005質量%以上、好ましくは0.001質量%以上で、通常40質量%以下、好ましくは20質量%以下である。カチオンラジカル化合物の含有量が上記下限以上であると形成した有機層が低抵抗化するため好ましく、上記上限以下であると形成した有機層に欠陥が生じ難く、また膜厚ムラが生じ難いため好ましい。
なお、本発明の有機電界発光素子用組成物には、上記の成分以外に、後述の正孔注入層形成用組成物や正孔輸送層形成用組成物に含まれる成分を、後述の含有量で含有していてもよい。
When the composition for an organic electroluminescent element of the present invention contains a cation radical compound, the content of the cation radical compound in the composition for an organic electroluminescent element of the present invention is usually 0.0005% by mass or more, preferably 0.001% by mass. % Or more, usually 40% by mass or less, preferably 20% by mass or less. When the content of the cationic radical compound is at least the above lower limit, the resistance of the formed organic layer is lowered, and when it is at least the above upper limit, defects are less likely to occur in the formed organic layer, and uneven film thickness is less likely to occur, which is preferable. ..
In addition to the above components, the composition for an organic electroluminescent device of the present invention contains components contained in the hole injection layer forming composition and the hole transport layer forming composition described later. It may be contained in.
[有機電界発光素子]
本発明の有機電界発光素子は、基板上に、陽極及び陰極と、該陽極と該陰極の間に有機層を有する有機電界発光素子において、該有機層が、本発明の重合体を含む本発明の有機電界発光素子用組成物を用いて湿式成膜法により形成された層を含むことを特徴とする。
本発明の有機電界発光素子において、湿式成膜法により形成された層は、正孔注入層及び正孔輸送層の少なくとも一方であることが好ましく、特に、この有機層が正孔注入層、正孔輸送層及び発光層を備え、これら正孔注入層、正孔輸送層及び発光層の全てが湿式成膜法により形成された層であることが好ましい。
[Organic electroluminescent device]
The organic electroluminescent device of the present invention is an organic electroluminescent device having an anode and a cathode and an organic layer between the anode and the cathode on a substrate, and the organic layer contains the polymer of the present invention. It is characterized by including a layer formed by a wet film forming method using the composition for an organic electroluminescent device of.
In the organic electroluminescent device of the present invention, the layer formed by the wet film forming method is preferably at least one of a hole injection layer and a hole transport layer, and in particular, this organic layer is a hole injection layer and a positive. It is preferable that the hole transport layer and the light emitting layer are provided, and all of the hole injection layer, the hole transport layer and the light emitting layer are formed by a wet film forming method.
本発明において湿式成膜法とは、成膜方法、即ち、塗布方法として、例えば、スピンコート法、ディップコート法、ダイコート法、バーコート法、ブレードコート法、ロールコート法、スプレーコート法、キャピラリーコート法、インクジェット法、ノズルプリンティング法、スクリーン印刷法、グラビア印刷法、フレキソ印刷法等の湿式で成膜させる方法を採用し、この塗布膜を乾燥させて膜形成を行う方法をいう。これらの成膜方法の中でも、スピンコート法、スプレーコート法、インクジェット法、ノズルプリンティング法などが好ましい。 In the present invention, the wet film forming method is a film forming method, that is, as a coating method, for example, a spin coating method, a dip coating method, a die coating method, a bar coating method, a blade coating method, a roll coating method, a spray coating method, and a capillary. A method of forming a film by adopting a wet film forming method such as a coating method, an inkjet method, a nozzle printing method, a screen printing method, a gravure printing method, or a flexographic printing method, and drying the coating film. Among these film forming methods, a spin coating method, a spray coating method, an inkjet method, a nozzle printing method and the like are preferable.
以下に、本発明の有機電界発光素子の層構成及びその一般的形成方法等の実施の形態の一例を、図1を参照して説明する。
図1は本発明の有機電界発光素子10の構造例を示す断面の模式図であり、図1において、1は基板、2は陽極、3は正孔注入層、4は正孔輸送層、5は発光層、6は正孔阻止層、7は電子輸送層、8は電子注入層、9は陰極を各々表す。
Hereinafter, an example of an embodiment such as a layer structure of the organic electroluminescent device of the present invention and a general method for forming the same will be described with reference to FIG.
FIG. 1 is a schematic cross-sectional view showing a structural example of the organic electroluminescent device 10 of the present invention. In FIG. 1, 1 is a substrate, 2 is an anode, 3 is a hole injection layer, 4 is a hole transport layer, and 5 is. Is a light emitting layer, 6 is a hole blocking layer, 7 is an electron transporting layer, 8 is an electron injection layer, and 9 is a cathode.
{基板}
基板1は、有機電界発光素子の支持体となるものであり、通常、石英やガラスの板、金属板や金属箔、プラスチックフィルムやシート等が用いられる。これらのうち、ガラス板や、ポリエステル、ポリメタクリレート、ポリカーボネート、ポリスルホン等の透明な合成樹脂の板が好ましい。基板は、外気による有機電界発光素子の劣化が起こり難いことからガスバリア性の高い材質とするのが好ましい。このため、特に合成樹脂製の基板等のようにガスバリア性の低い材質を用いる場合は、基板の少なくとも片面に緻密なシリコン酸化膜等を設けてガスバリア性を上げるのが好ましい。
{substrate}
The
{陽極}
陽極2は、発光層5側の層に正孔を注入する機能を担う。
陽極2は、通常、アルミニウム、金、銀、ニッケル、パラジウム、白金等の金属;インジウム及び/又はスズの酸化物等の金属酸化物;ヨウ化銅等のハロゲン化金属;カーボンブラック及びポリ(3−メチルチオフェン)、ポリピロール、ポリアニリン等の導電性高分子等により構成される。
{anode}
The
The
陽極2の形成は、通常、スパッタリング法、真空蒸着法等の乾式法により行われることが多い。また、銀等の金属微粒子、ヨウ化銅等の微粒子、カーボンブラック、導電性の金属酸化物微粒子、導電性高分子微粉末等を用いて陽極を形成する場合には、適当なバインダー樹脂溶液に分散させて、基板上に塗布することにより形成することもできる。また、導電性高分子の場合は、電解重合により直接基板上に薄膜を形成したり、基板上に導電性高分子を塗布して陽極を形成することもできる(Appl.Phys.Lett.,60巻,2711頁,1992年)。
The
陽極2は、通常、単層構造であるが、適宜、積層構造としてもよい。陽極2が積層構造である場合、1層目の陽極上に異なる導電材料を積層してもよい。
陽極2の厚みは、必要とされる透明性と材質等に応じて、決めればよい。特に高い透明性が必要とされる場合は、可視光の透過率が60%以上となる厚みが好ましく、80%以上となる厚みが更に好ましい。陽極2の厚みは、通常5nm以上、好ましくは10nm以上であり、また、通常1000nm以下、好ましくは500nm以下とするのが好ましい。一方、透明性が不要な場合は、陽極2の厚みは必要な強度等に応じて任意に厚みとすればよく、この場合、陽極2は基板と同一の厚みでもよい。
The
The thickness of the
陽極2の表面に他の層を成膜する場合は、成膜前に、紫外線/オゾン、酸素プラズマ、アルゴンプラズマ等の処理を施すことにより、陽極2上の不純物を除去すると共に、そのイオン化ポテンシャルを調整して正孔注入性を向上させておくことが好ましい。
When another layer is formed on the surface of the
{正孔注入層}
陽極2側から発光層5側に正孔を輸送する機能を担う層は、通常、正孔注入輸送層又は正孔輸送層と呼ばれる。そして、陽極2側から発光層5側に正孔を輸送する機能を担う層が2層以上ある場合に、より陽極側に近い方の層を正孔注入層3と呼ぶことがある。正孔注入層3は、陽極2から発光層5側に正孔を輸送する機能を強化する点で、形成することが好ましい。正孔注入層3を形成する場合、通常、正孔注入層3は、陽極2上に形成される。
{Hole injection layer}
The layer having a function of transporting holes from the
正孔注入層3の膜厚は、通常1nm以上、好ましくは5nm以上、また、通常1000nm以下、好ましくは500nm以下である。
The film thickness of the
正孔注入層の形成方法は、真空蒸着法でも、湿式成膜法でもよい。成膜性が優れる点では、湿式成膜法により形成することが好ましい。
正孔注入層3は、正孔輸送性化合物を含むことが好ましく、正孔輸送性化合物と電子受容性化合物とを含むことがより好ましい。更には、正孔注入層中にカチオンラジカル化合物を含むことが好ましく、カチオンラジカル化合物と正孔輸送性化合物とを含むことが特に好ましい。
The hole injection layer may be formed by either a vacuum vapor deposition method or a wet film deposition method. In terms of excellent film forming property, it is preferably formed by a wet film forming method.
The
以下に、一般的な正孔注入層の形成方法について説明するが、本発明の有機電界発光素子において、正孔注入層は、本発明の有機電界発光素子用組成物を用いて湿式成膜法により形成されることが好ましい。 A general method for forming the hole injection layer will be described below. In the organic electroluminescent device of the present invention, the hole injection layer is a wet film forming method using the composition for the organic electroluminescent device of the present invention. Is preferably formed by.
<正孔輸送性化合物>
正孔注入層形成用組成物は、通常、正孔注入層3となる正孔輸送性化合物を含有する。また、湿式成膜法の場合は、通常、更に溶媒も含有する。正孔注入層形成用組成物は、正孔輸送性が高く、注入された正孔を効率よく輸送できるのが好ましい。このため、正孔移動度が大きく、トラップとなる不純物が製造時や使用時等に発生し難いことが好ましい。また、安定性に優れ、イオン化ポテンシャルが小さく、可視光に対する透明性が高いことが好ましい。特に、正孔注入層が発光層と接する場合は、発光層からの発光を消光しないものや発光層とエキサイプレックスを形成して、発光効率を低下させないものが好ましい。
正孔輸送性化合物としては、陽極から正孔注入層への電荷注入障壁の観点から、4.5eV〜6.0eVのイオン化ポテンシャルを有する化合物が好ましい。正孔輸送性化合物の例としては、芳香族アミン系化合物、フタロシアニン系化合物、ポルフィリン系化合物、オリゴチオフェン系化合物、ポリチオフェン系化合物、ベンジルフェニル系化合物、フルオレン基で3級アミンを連結した化合物、ヒドラゾン系化合物、シラザン系化合物、キナクリドン系化合物等が挙げられる。
<Hole transporting compound>
The composition for forming a hole injection layer usually contains a hole transporting compound that becomes the
As the hole transporting compound, a compound having an ionization potential of 4.5 eV to 6.0 eV is preferable from the viewpoint of a charge injection barrier from the anode to the hole injection layer. Examples of hole-transporting compounds include aromatic amine compounds, phthalocyanine compounds, porphyrin compounds, oligothiophene compounds, polythiophene compounds, benzylphenyl compounds, compounds in which a tertiary amine is linked with a fluorene group, and hydrazone. Examples thereof include system compounds, silazane compounds, and quinacridone compounds.
上述の例示化合物のうち、非晶質性及び可視光透過性の点から、芳香族アミン化合物が好ましく、芳香族三級アミン化合物が特に好ましい。ここで、芳香族三級アミン化合物とは、芳香族三級アミン構造を有する化合物であって、芳香族三級アミン由来の基を有する化合物も含む。
芳香族三級アミン化合物の種類は、特に制限されないが、表面平滑化効果により均一な発光を得やすい点から、重量平均分子量が1000以上、1000000以下の高分子化合物(繰り返し単位が連なる重合型化合物)を用いることが好ましい。芳香族三級アミン高分子化合物の好ましい例としては、下記式(6)で表される繰り返し単位を有する高分子化合物等が挙げられる。
Among the above-mentioned exemplified compounds, aromatic amine compounds are preferable, and aromatic tertiary amine compounds are particularly preferable, from the viewpoint of amorphousness and visible light transmission. Here, the aromatic tertiary amine compound is a compound having an aromatic tertiary amine structure, and also includes a compound having a group derived from the aromatic tertiary amine.
The type of the aromatic tertiary amine compound is not particularly limited, but a polymer compound having a weight average molecular weight of 1000 or more and 1000,000 or less (polymerized compound in which repeating units are continuous) is easy to obtain uniform light emission due to the surface smoothing effect. ) Is preferably used. Preferred examples of the aromatic tertiary amine polymer compound include a polymer compound having a repeating unit represented by the following formula (6).
(式(6)中、Ar11及びAr12は、それぞれ独立して、置換基を有していてもよい芳香族炭化水素基又は置換基を有していてもよい芳香族複素環基を表す。Ar13〜Ar15は、それぞれ独立して、置換基を有していてもよい芳香族炭化水素基又は置換基を有していてもよい芳香族複素環基を表す。Yは、下記に示す連結基群の中から選ばれる連結基を表す。また、Ar11〜Ar15のうち、同一のN原子に結合する二つの基は互いに結合して環を形成してもよい。) (In the formula (6), Ar 11 and Ar 12 each independently represent an aromatic hydrocarbon group which may have a substituent or an aromatic heterocyclic group which may have a substituent. . Ar 13 to Ar 15 each independently represent an aromatic hydrocarbon group which may have a substituent or an aromatic heterocyclic group which may have a substituent. Y is described below. It represents a linking group selected from the group of linking groups shown. Further, of Ar 11 to Ar 15 , two groups bonded to the same N atom may be bonded to each other to form a ring.)
(上記各式中、Ar16〜Ar26は、それぞれ独立して、置換基を有していてもよい芳香族炭化水素基又は置換基を有していてもよい芳香族複素環基を表す。R8及びR9は、それぞれ独立して、水素原子又は任意の置換基を表す。) (In each of the above formulas, Ar 16 to Ar 26 each independently represent an aromatic hydrocarbon group which may have a substituent or an aromatic heterocyclic group which may have a substituent. R 8 and R 9 each independently represent a hydrogen atom or any substituent.)
Ar16〜Ar26の芳香族炭化水素基及び芳香族複素環基としては、高分子化合物の溶解性、耐熱性、正孔注入輸送性の点から、1個又は2個の遊離原子価を有する、ベンゼン環、ナフタレン環、フェナントレン環、チオフェン環、ピリジン環が好ましく、1個又は2個の遊離原子価を有する、ベンゼン環、ナフタレン環がさらに好ましい。 The aromatic hydrocarbon groups and aromatic heterocyclic groups of Ar 16 to Ar 26 have one or two free valences in terms of solubility, heat resistance, and hole injection transportability of the polymer compound. , Benzene ring, naphthalene ring, phenanthrene ring, thiophene ring, pyridine ring is preferable, and benzene ring and naphthalene ring having one or two free valences are more preferable.
式(4)で表される繰り返し単位を有する芳香族三級アミン高分子化合物の具体例としては、国際公開第2005/089024号に記載のもの等が挙げられる。 Specific examples of the aromatic tertiary amine polymer compound having a repeating unit represented by the formula (4) include those described in International Publication No. 2005/089024.
正孔注入層3には、正孔輸送性化合物の酸化により、正孔注入層の導電率を向上させることができるため、前述の電子受容性化合物や、前述のカチオンラジカル化合物を含有していることが好ましい。
Since the
PEDOT/PSS(Adv.Mater.,2000年,12巻,481頁)やエメラルジン塩酸塩(J.Phys.Chem.,1990年,94巻,7716頁)等の高分子化合物由来のカチオンラジカル化合物は、酸化重合(脱水素重合)することによっても生成する。 Cationic radical compounds derived from polymer compounds such as PEDOT / PSS (Adv. Mater., 2000, Vol. 12, p. 481) and emeraldine hydrochloride (J. Phys. Chem., 1990, Vol. 94, p. 7716) It is also produced by oxidative polymerization (dehydrogenation polymerization).
ここでいう酸化重合は、モノマーを酸性溶液中で、ペルオキソ二硫酸塩等を用いて化学的に、又は、電気化学的に酸化するものである。この酸化重合(脱水素重合)の場合、モノマーが酸化されることにより高分子化されるとともに、酸性溶液由来のアニオンを対アニオンとする、高分子の繰り返し単位から一電子取り除かれたカチオンラジカルが生成する。 The oxidative polymerization referred to here is to chemically or electrochemically oxidize a monomer in an acidic solution using peroxodisulfate or the like. In the case of this oxidative polymerization (dehydropolymerization), a cation radical obtained by removing one electron from a repeating unit of a polymer, which is polymerized by oxidizing a monomer and has an anion derived from an acidic solution as a counter anion, is generated. Generate.
<湿式成膜法による正孔注入層の形成>
湿式成膜法により正孔注入層3を形成する場合、通常、正孔注入層となる材料を可溶な溶媒(正孔注入層用溶媒)と混合して成膜用の組成物(正孔注入層形成用組成物)を調製し、この正孔注入層形成用組成物を正孔注入層の下層に該当する層(通常は、陽極)上に塗布して成膜し、乾燥させることにより形成する。
<Formation of hole injection layer by wet film formation method>
When the
正孔注入層形成用組成物中における正孔輸送性化合物の濃度は、本発明の効果を著しく損なわない限り任意であるが、膜厚の均一性の点では、低い方が好ましく、また、一方、正孔注入層に欠陥が生じ難い点では、高い方が好ましい。具体的には、0.01質量%以上であるのが好ましく、0.1質量%以上であるのが更に好ましく、0.5質量%以上であるのが特に好ましく、また、一方、70質量%以下であるのが好ましく、60質量%以下であるのが更に好ましく、50質量%以下であるのが特に好ましい。
溶媒としては、例えば、エーテル系溶媒、エステル系溶媒、芳香族炭化水素系溶媒、アミド系溶媒などが挙げられる。
The concentration of the hole transporting compound in the composition for forming a hole injection layer is arbitrary as long as the effect of the present invention is not significantly impaired, but it is preferable that the concentration is low in terms of film thickness uniformity. , A higher value is preferable in that defects are less likely to occur in the hole injection layer. Specifically, it is preferably 0.01% by mass or more, more preferably 0.1% by mass or more, particularly preferably 0.5% by mass or more, and on the other hand, 70% by mass. It is preferably less than or equal to, more preferably 60% by mass or less, and particularly preferably 50% by mass or less.
Examples of the solvent include ether solvents, ester solvents, aromatic hydrocarbon solvents, amide solvents and the like.
エーテル系溶媒としては、例えば、エチレングリコールジメチルエーテル、エチレングリコールジエチルエーテル、プロピレングリコール−1−モノメチルエーテルアセタート(PGMEA)等の脂肪族エーテル及び1,2−ジメトキシベンゼン、1,3−ジメトキシベンゼン、アニソール、フェネトール、2−メトキシトルエン、3−メトキシトルエン、4−メトキシトルエン、2,3−ジメチルアニソール、2,4−ジメチルアニソール等の芳香族エーテル等が挙げられる。 Examples of the ether-based solvent include aliphatic ethers such as ethylene glycol dimethyl ether, ethylene glycol diethyl ether, and propylene glycol-1-monomethyl ether acetate (PGMEA), and 1,2-dimethoxybenzene, 1,3-dimethoxybenzene, and anisole. , Fenetol, 2-methoxytoluene, 3-methoxytoluene, 4-methoxytoluene, 2,3-dimethylanisole, 2,4-dimethylanisole and other aromatic ethers.
エステル系溶媒としては、例えば、酢酸フェニル、プロピオン酸フェニル、安息香酸メチル、安息香酸エチル、安息香酸プロピル、安息香酸n−ブチル等の芳香族エステル等が挙げられる。 Examples of the ester-based solvent include aromatic esters such as phenyl acetate, phenyl propionate, methyl benzoate, ethyl benzoate, propyl benzoate, and n-butyl benzoate.
芳香族炭化水素系溶媒としては、例えば、トルエン、キシレン、シクロヘキシルベンゼン、3−イソプロピルビフェニル、1,2,3,4−テトラメチルベンゼン、1,4−ジイソプロピルベンゼン、シクロヘキシルベンゼン、メチルナフタレン等が挙げられる。アミド系溶媒としては、例えば、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド等が挙げられる。
これらの他、ジメチルスルホキシド等も用いることができる。
Examples of the aromatic hydrocarbon solvent include toluene, xylene, cyclohexylbenzene, 3-isopropylbiphenyl, 1,2,3,4-tetramethylbenzene, 1,4-diisopropylbenzene, cyclohexylbenzene, methylnaphthalene and the like. Be done. Examples of the amide-based solvent include N, N-dimethylformamide, N, N-dimethylacetamide and the like.
In addition to these, dimethyl sulfoxide and the like can also be used.
正孔注入層3の湿式成膜法による形成は、通常、正孔注入層形成用組成物を調製後に、これを、正孔注入層3の下層に該当する層(通常は、陽極2)上に塗布成膜し、乾燥することにより行われる。
正孔注入層3は、通常、成膜後に、加熱や減圧乾燥等により塗布膜を乾燥させる。
The formation of the
In the
<真空蒸着法による正孔注入層の形成>
真空蒸着法により正孔注入層3を形成する場合には、通常、正孔注入層3の構成材料(前述の正孔輸送性化合物、電子受容性化合物等)の1種類又は2種類以上を真空容器内に設置された坩堝に入れ(2種類以上の材料を用いる場合は、通常各々を別々の坩堝に入れ)、真空容器内を真空ポンプで10−4Pa程度まで排気した後、坩堝を加熱して(2種類以上の材料を用いる場合は、通常各々の坩堝を加熱して)、坩堝内の材料の蒸発量を制御しながら蒸発させ(2種類以上の材料を用いる場合は、通常各々独立に蒸発量を制御しながら蒸発させ)、坩堝に向き合って置かれた基板上の陽極上に正孔注入層を形成する。なお、2種類以上の材料を用いる場合は、それらの混合物を坩堝に入れ、加熱、蒸発させて正孔注入層を形成することもできる。
<Formation of hole injection layer by vacuum deposition method>
When the
蒸着時の真空度は、本発明の効果を著しく損なわない限り限定されないが、通常0.1×10−6Torr(0.13×10−4Pa)以上、9.0×10−6Torr(12.0×10−4Pa)以下である。蒸着速度は、本発明の効果を著しく損なわない限り限定されないが、通常0.1Å/秒以上、5.0Å/秒以下である。蒸着時の成膜温度は、本発明の効果を著しく損なわない限り限定されないが、好ましくは10℃以上、50℃以下で行われる。
なお、正孔注入層3は、後述の正孔輸送層4と同様に架橋されていてもよい。
The degree of vacuum during vapor deposition is not limited as long as the effect of the present invention is not significantly impaired, but is usually 0.1 × 10 -6 Torr (0.13 × 10 -4 Pa) or more, 9.0 × 10 -6 Torr ( It is 12.0 × 10 -4 Pa) or less. The vapor deposition rate is not limited as long as the effect of the present invention is not significantly impaired, but is usually 0.1 Å / sec or more and 5.0 Å / sec or less. The film formation temperature at the time of vapor deposition is not limited as long as the effect of the present invention is not significantly impaired, but is preferably 10 ° C. or higher and 50 ° C. or lower.
The
{正孔輸送層}
正孔輸送層4は、陽極2側から発光層5側に正孔を輸送する機能を担う層である。正孔輸送層4は、本発明の有機電界発光素子では、必須の層では無いが、陽極2から発光層5に正孔を輸送する機能を強化する点では、この層を形成することが好ましい。正孔輸送層4を形成する場合、通常、正孔輸送層4は、陽極2と発光層5の間に形成される。また、上述の正孔注入層3がある場合は、正孔注入層3と発光層5の間に形成される。
正孔輸送層4の膜厚は、通常5nm以上、好ましくは10nm以上であり、また、一方、通常300nm以下、好ましくは100nm以下である。
正孔輸送層4の形成方法は、真空蒸着法でも、湿式成膜法でもよい。成膜性が優れる点では、湿式成膜法により形成することが好ましい。
{Hole transport layer}
The
The film thickness of the
The
以下に一般的な正孔輸送層の形成方法について説明するが、本発明の有機電界発光素子において、正孔輸送層は、本発明の有機電界発光素子用組成物を用いて湿式成膜法により形成されることが好ましい。 A general method for forming the hole transport layer will be described below. In the organic electroluminescent device of the present invention, the hole transport layer is formed by a wet film forming method using the composition for the organic electroluminescent device of the present invention. It is preferably formed.
正孔輸送層4は、通常、正孔輸送性化合物を含有する。正孔輸送層4に含まれる正孔輸送性化合物としては、特に、4,4’−ビス[N−(1−ナフチル)−N−フェニルアミノ]ビフェニルで代表される、2個以上の3級アミンを含み2個以上の縮合芳香族環が窒素原子に置換した芳香族ジアミン(日本国特開平5−234681号公報)、4,4’,4’’−トリス(1−ナフチルフェニルアミノ)トリフェニルアミン等のスターバースト構造を有する芳香族アミン化合物(J.Lumin.,72−74巻、985頁、1997年)、トリフェニルアミンの四量体から成る芳香族アミン化合物(Chem.Commun.,2175頁、1996年)、2,2’,7,7’−テトラキス−(ジフェニルアミノ)−9,9’−スピロビフルオレン等のスピロ化合物(Synth.Metals,91巻、209頁、1997年)、4,4’−N,N’−ジカルバゾールビフェニルなどのカルバゾール誘導体などが挙げられる。また、例えばポリビニルカルバゾール、ポリビニルトリフェニルアミン(日本国特開平7−53953号公報)、テトラフェニルベンジジンを含有するポリアリーレンエーテルサルホン(Polym.Adv.Tech.,7巻、33頁、1996年)等も好ましく使用できる。
The
<湿式成膜法による正孔輸送層の形成>
湿式成膜法で正孔輸送層を形成する場合は、通常、上述の正孔注入層を湿式成膜法で形成する場合と同様にして、正孔注入層形成用組成物の代わりに正孔輸送層形成用組成物を用いて形成させる。
湿式成膜法で正孔輸送層を形成する場合は、通常、正孔輸送層形成用組成物は、更に溶媒を含有する。正孔輸送層形成用組成物に用いる溶媒は、上述の正孔注入層形成用組成物で用いる溶媒と同様の溶媒を使用することができる。
正孔輸送層形成用組成物中における正孔輸送性化合物の濃度は、正孔注入層形成用組成物中における正孔輸送性化合物の濃度と同様の範囲とすることができる。
正孔輸送層の湿式成膜法による形成は、前述の正孔注入層成膜法と同様に行うことができる。
<Formation of hole transport layer by wet film formation method>
When the hole transport layer is formed by the wet film forming method, holes are usually formed instead of the hole injection layer forming composition in the same manner as when the hole injection layer is formed by the wet film forming method. It is formed using a composition for forming a transport layer.
When the hole transport layer is formed by the wet film formation method, the hole transport layer forming composition usually further contains a solvent. As the solvent used in the hole transport layer forming composition, the same solvent as the solvent used in the hole injection layer forming composition described above can be used.
The concentration of the hole-transporting compound in the composition for forming the hole-transporting layer can be in the same range as the concentration of the hole-transporting compound in the composition for forming the hole-injecting layer.
The hole transport layer can be formed by the wet film formation method in the same manner as the hole injection layer film formation method described above.
<真空蒸着法による正孔輸送層の形成>
真空蒸着法で正孔輸送層を形成する場合についても、通常、上述の正孔注入層を真空蒸着法で形成する場合と同様にして、正孔注入層形成用組成物の代わりに正孔輸送層形成用組成物を用いて形成させることができる。蒸着時の真空度、蒸着速度及び温度などの成膜条件などは、前記正孔注入層の真空蒸着時と同様の条件で成膜することができる。
<Formation of hole transport layer by vacuum deposition method>
When the hole transport layer is formed by the vacuum vapor deposition method, the hole transport is usually performed instead of the hole injection layer forming composition in the same manner as in the case where the hole injection layer is formed by the vacuum vapor deposition method. It can be formed using a layer-forming composition. The film formation conditions such as the degree of vacuum, the vapor deposition rate, and the temperature at the time of vapor deposition can be the same as those at the time of vacuum vapor deposition of the hole injection layer.
{発光層}
発光層5は、一対の電極間に電界が与えられた時に、陽極2から注入される正孔と陰極9から注入される電子が再結合することにより励起され、発光する機能を担う層である。発光層5は、陽極2と陰極9の間に形成される層であり、発光層は、陽極の上に正孔注入層がある場合は、正孔注入層と陰極の間に形成され、陽極の上に正孔輸送層がある場合は、正孔輸送層と陰極の間に形成される。
発光層5の膜厚は、本発明の効果を著しく損なわない限り任意であるが、膜に欠陥が生じ難い点では厚い方が好ましく、また、一方、薄い方が低駆動電圧としやすい点で好ましい。このため、3nm以上であるのが好ましく、5nm以上であるのが更に好ましく、また、一方、通常200nm以下であるのが好ましく、100nm以下であるのが更に好ましい。
発光層5は、少なくとも、発光の性質を有する材料(発光材料)を含有するとともに、好ましくは、電荷輸送性を有する材料(電荷輸送性材料)とを含有する。
{Light emitting layer}
The
The film thickness of the
The
<発光材料>
発光材料は、所望の発光波長で発光し、本発明の効果を損なわない限りは特に制限はなく、公知の発光材料を適用可能である。発光材料は、蛍光発光材料でも、燐光発光材料でもよいが、発光効率が良好である材料が好ましく、内部量子効率の観点から燐光発光材料が好ましい。
蛍光発光材料としては、例えば、以下の材料が挙げられる。
青色発光を与える蛍光発光材料(青色蛍光発光材料)としては、例えば、ナフタレン、ペリレン、ピレン、アントラセン、クマリン、クリセン、p−ビス(2−フェニルエテニル)ベンゼン及びそれらの誘導体等が挙げられる。
緑色発光を与える蛍光発光材料(緑色蛍光発光材料)としては、例えば、キナクリドン誘導体、クマリン誘導体、Al(C9H6NO)3などのアルミニウム錯体等が挙げられる。
黄色発光を与える蛍光発光材料(黄色蛍光発光材料)としては、例えば、ルブレン、ペリミドン誘導体等が挙げられる。
赤色発光を与える蛍光発光材料(赤色蛍光発光材料)としては、例えば、DCM(4−(dicyanomethylene)−2−methyl−6−(p−dimethylaminostyryl)−4H−pyran)系化合物、ベンゾピラン誘導体、ローダミン誘導体、ベンゾチオキサンテン誘導体、アザベンゾチオキサンテン等が挙げられる。
<Luminescent material>
The light emitting material is not particularly limited as long as it emits light at a desired light emitting wavelength and the effect of the present invention is not impaired, and a known light emitting material can be applied. The light emitting material may be either a fluorescent light emitting material or a phosphorescent light emitting material, but a material having good luminous efficiency is preferable, and a phosphorescent light emitting material is preferable from the viewpoint of internal quantum efficiency.
Examples of the fluorescent light emitting material include the following materials.
Examples of the fluorescent light emitting material (blue fluorescent light emitting material) that gives blue light emission include naphthalene, perylene, pyrene, anthracene, coumarin, chrysene, p-bis (2-phenylethenyl) benzene, and derivatives thereof.
The fluorescent light-emitting material giving green luminescence (green fluorescent material), for example, quinacridone derivatives, coumarin derivatives, aluminum complexes such as Al (C 9 H 6 NO) 3 and the like.
Examples of the fluorescent light emitting material (yellow fluorescent light emitting material) that gives yellow light emission include rubrene, a perimidone derivative, and the like.
Examples of the fluorescent light emitting material (red fluorescent light emitting material) that gives red light emission include DCM (4- (dicyanomethyrene) -2-methyl-6- (p-dimethylaminostylyl) -4H-pyran) compounds, benzopyran derivatives, and rhodamine derivatives. , Benzothioxanthene derivatives, azabenzothioxanthene and the like.
また、燐光発光材料としては、例えば、長周期型周期表の第7〜11族から選ばれる金属を含む有機金属錯体等が挙げられる。周期表の第7〜11族から選ばれる金属として、好ましくは、ルテニウム、ロジウム、パラジウム、銀、レニウム、オスミウム、イリジウム、白金、金等が挙げられる。
Further, examples of the phosphorescent material include an organic metal complex containing a metal selected from
有機金属錯体の配位子としては、(ヘテロ)アリールピリジン配位子、(ヘテロ)アリールピラゾール配位子などの(ヘテロ)アリール基とピリジン、ピラゾール、フェナントロリンなどが連結した配位子が好ましく、特にフェニルピリジン配位子、フェニルピラゾール配位子が好ましい。ここで、(ヘテロ)アリールとは、アリール基又はヘテロアリール基を表す。 As the ligand of the organic metal complex, a ligand in which a (hetero) aryl group such as a (hetero) arylpyridine ligand or a (hetero) arylpyrazole ligand is linked to a pyridine, pyrazole, phenanthroline or the like is preferable. In particular, a phenylpyridine ligand and a phenylpyrazole ligand are preferable. Here, the (hetero) aryl represents an aryl group or a heteroaryl group.
好ましい燐光発光材料として、具体的には、例えば、トリス(2−フェニルピリジン)イリジウム、トリス(2−フェニルピリジン)ルテニウム、トリス(2−フェニルピリジン)パラジウム、ビス(2−フェニルピリジン)白金、トリス(2−フェニルピリジン)オスミウム、トリス(2−フェニルピリジン)レニウム等のフェニルピリジン錯体及びオクタエチル白金ポルフィリン、オクタフェニル白金ポルフィリン、オクタエチルパラジウムポルフィリン、オクタフェニルパラジウムポルフィリン等のポルフィリン錯体等が挙げられる。 Specific preferred phosphorescent materials include, for example, tris (2-phenylpyridine) iridium, tris (2-phenylpyridine) ruthenium, tris (2-phenylpyridine) palladium, bis (2-phenylpyridine) platinum, and tris. Examples thereof include phenylpyridine complexes such as (2-phenylpyridine) osmium and tris (2-phenylpyridine) renium, and porphyrin complexes such as octaethyl platinum porphyrin, octaphenyl platinum porphyrin, octaethyl palladium porphyrin, and octaphenyl palladium porphyrin.
高分子系の発光材料としては、ポリ(9,9−ジオクチルフルオレン−2,7−ジイル)、ポリ[(9,9−ジオクチルフルオレン−2,7−ジイル)−co−(4,4’−(N−(4−sec−ブチルフェニル))ジフェニルアミン)]、ポリ[(9,9−ジオクチルフルオレン−2,7−ジイル)−co−(1,4−ベンゾ−2{2,1’−3}−トリアゾール)]などのポリフルオレン系材料、ポリ[2−メトキシ−5−(2−ヘチルヘキシルオキシ)−1,4−フェニレンビニレン]などのポリフェニレンビニレン系材料が挙げられる。 Polymer-based luminescent materials include poly (9,9-dioctylfluorene-2,7-diyl) and poly [(9,9-dioctylfluorene-2,7-diyl) -co- (4,4'-). (N- (4-sec-Butylphenyl)) diphenylamine)], poly [(9,9-dioctylfluorene-2,7-diyl) -co- (1,4-benzo-2 {2,1'-3) } -Triazole)] and other polyfluorene-based materials, and poly-phenylene vinylene-based materials such as poly [2-methoxy-5- (2-hepylhexyloxy) -1,4-phenylene vinylene] can be mentioned.
<電荷輸送性材料>
電荷輸送性材料は、正電荷(正孔)又は負電荷(電子)輸送性を有する材料であり、本発明の効果を損なわない限り、特に制限はなく、公知の発光材料を適用可能である。
電荷輸送性材料は、従来、有機電界発光素子の発光層に用いられている化合物等を用いることができ、特に、発光層のホスト材料として使用されている化合物が好ましい。
電荷輸送性材料としては、具体的には、芳香族アミン系化合物、フタロシアニン系化合物、ポルフィリン系化合物、オリゴチオフェン系化合物、ポリチオフェン系化合物、ベンジルフェニル系化合物、フルオレン基で3級アミンを連結した化合物、ヒドラゾン系化合物、シラザン系化合物、シラナミン系化合物、ホスファミン系化合物、キナクリドン系化合物等の正孔注入層の正孔輸送性化合物として例示した化合物等が挙げられる他、アントラセン系化合物、ピレン系化合物、カルバゾール系化合物、ピリジン系化合物、フェナントロリン系化合物、オキサジアゾール系化合物、シロール系化合物等の電子輸送性化合物等が挙げられる。
<Charge transport material>
The charge transporting material is a material having a positive charge (hole) or negative charge (electron) transporting property, and is not particularly limited as long as the effect of the present invention is not impaired, and a known light emitting material can be applied.
As the charge transporting material, a compound or the like conventionally used for the light emitting layer of the organic electroluminescent device can be used, and a compound used as a host material for the light emitting layer is particularly preferable.
Specific examples of the charge transporting material include aromatic amine compounds, phthalocyanine compounds, porphyrin compounds, oligothiophene compounds, polythiophene compounds, benzylphenyl compounds, and compounds in which a tertiary amine is linked with a fluorene group. , Hydrazone-based compounds, silazane-based compounds, silanamin-based compounds, phosphamine-based compounds, quinacridone-based compounds, and other compounds exemplified as hole-transporting compounds in the hole injection layer, as well as anthracene-based compounds and pyrene-based compounds. Examples thereof include electron-transporting compounds such as carbazole-based compounds, pyridine-based compounds, phenanthroline-based compounds, oxadiazole-based compounds, and silol-based compounds.
また、例えば、4,4’−ビス[N−(1−ナフチル)−N−フェニルアミノ]ビフェニルで代表される2個以上の3級アミンを含み2個以上の縮合芳香族環が窒素原子に置換した芳香族ジアミン(日本国特開平5−234681号公報)、4,4’,4’’−トリス(1−ナフチルフェニルアミノ)トリフェニルアミン等のスターバースト構造を有する芳香族アミン系化合物(J.Lumin.,72−74巻、985頁、1997年)、トリフェニルアミンの四量体から成る芳香族アミン系化合物(Chem.Commun.,2175頁、1996年)、2,2’,7,7’−テトラキス−(ジフェニルアミノ)−9,9’−スピロビフルオレン等のフルオレン系化合物(Synth.Metals,91巻、209頁、1997年)、4,4’−N,N’−ジカルバゾールビフェニルなどのカルバゾール系化合物等の正孔輸送層の正孔輸送性化合物として例示した化合物等も好ましく用いることができる。また、この他、2−(4−ビフェニリル)−5−(p−ターシャルブチルフェニル)−1,3,4−オキサジアゾール(tBu−PBD)、2,5−ビス(1−ナフチル)−1,3,4−オキサジアゾール(BND)などのオキサジアゾール系化合物、2,5−ビス(6’−(2’,2’’−ビピリジル))−1,1−ジメチル−3,4−ジフェニルシロール(PyPySPyPy)等のシロール系化合物、バソフェナントロリン(BPhen)、2,9−ジメチル−4,7−ジフェニル−1,10−フェナントロリン(BCP、バソクプロイン)などのフェナントロリン系化合物等も挙げられる。 Further, for example, two or more fused aromatic rings containing two or more tertiary amines represented by 4,4'-bis [N- (1-naphthyl) -N-phenylamino] biphenyl are used as nitrogen atoms. Aromatic amine compounds having a starburst structure, such as substituted aromatic diamines (Japanese Patent Laid-Open No. 5-234681), 4,4', 4''-tris (1-naphthylphenylamino) triphenylamine, etc. J. Lumin., Vol. 72-74, pp. 985, 1997), Aromatic amine compounds consisting of triphenylamine tetramers (Chem. Commun., P. 2175, 1996), 2, 2', 7 , 7'-Tetrakiss- (diphenylamino) -9,9'-spirobifluorene and other fluorene compounds (Synth. Metals, Vol. 91, p. 209, 1997), 4,4'-N, N'-di Compounds exemplified as the hole-transporting compound of the hole-transporting layer such as a carbazole-based compound such as carbazole biphenyl can also be preferably used. In addition, 2- (4-biphenylyl) -5- (p-tershalbutylphenyl) -1,3,4-oxadiazole (tBu-PBD), 2,5-bis (1-naphthyl)- Oxadiazole compounds such as 1,3,4-oxadiazole (BND), 2,5-bis (6'-(2', 2''-bipyridyl))-1,1-dimethyl-3,4 Examples thereof include silol compounds such as −diphenylsilol (PyPySPyPy), phenanthroline compounds such as vasophenanthroline (BPhen) and 2,9-dimethyl-4,7-diphenyl-1,10-phenanthroline (BCP, vasocproin).
<湿式成膜法による発光層の形成>
発光層の形成方法は、真空蒸着法でも、湿式成膜法でもよいが、成膜性に優れることから、湿式成膜法が好ましく、スピンコート法及びインクジェット法が更に好ましい。特に、本発明の有機電界発光素子用組成物を用いて、発光層の下層となる正孔注入層又は正孔輸送層を形成すると、湿式成膜法による積層化が容易であるため、湿式成膜法を採用することが好ましい。湿式成膜法により発光層を形成する場合は、通常、上述の正孔注入層を湿式成膜法で形成する場合と同様にして、正孔注入層形成用組成物の代わりに、発光層となる材料を可溶な溶媒(発光層用溶媒)と混合して調製した発光層形成用組成物を用いて形成する。
溶媒としては、例えば、正孔注入層の形成について挙げたエーテル系溶媒、エステル系溶媒、芳香族炭化水素系溶媒、アミド系溶媒の他、アルカン系溶媒、ハロゲン化芳香族炭化水素系溶媒、脂肪族アルコール系溶媒、脂環族アルコール系溶媒、脂肪族ケトン系溶媒及び脂環族ケトン系溶媒などが挙げられる。以下に溶媒の具体例を挙げるが、本発明の効果を損なわない限り、これらに限定されるものではない。
<Formation of light emitting layer by wet film formation method>
The light emitting layer may be formed by a vacuum vapor deposition method or a wet film forming method, but the wet film forming method is preferable, and the spin coating method and the inkjet method are more preferable because of the excellent film forming property. In particular, when the hole injection layer or the hole transport layer to be the lower layer of the light emitting layer is formed by using the composition for an organic electroluminescent device of the present invention, it is easy to stack by the wet film forming method, so that it is wet-formed. It is preferable to adopt the membrane method. When the light emitting layer is formed by the wet film forming method, usually, in the same manner as when the hole injection layer is formed by the wet film forming method, a light emitting layer is used instead of the composition for forming the hole injection layer. The material is formed by using a composition for forming a light emitting layer prepared by mixing a soluble solvent (solvent for a light emitting layer).
Examples of the solvent include ether-based solvents, ester-based solvents, aromatic hydrocarbon-based solvents, and amide-based solvents mentioned for the formation of the hole injection layer, as well as alcan-based solvents, halogenated aromatic hydrocarbon-based solvents, and fats. Examples thereof include a group alcohol solvent, an alicyclic alcohol solvent, an aliphatic ketone solvent and an alicyclic ketone solvent. Specific examples of the solvent are given below, but the present invention is not limited thereto as long as the effect of the present invention is not impaired.
例えば、エチレングリコールジメチルエーテル、エチレングリコールジエチルエーテル、プロピレングリコール−1−モノメチルエーテルアセタート(PGMEA)等の脂肪族エーテル系溶媒;1,2−ジメトキシベンゼン、1,3−ジメトキシベンゼン、アニソール、フェネトール、2−メトキシトルエン、3−メトキシトルエン、4−メトキシトルエン、2,3−ジメチルアニソール、2,4−ジメチルアニソール、ジフェニルエーテル等の芳香族エーテル系溶媒;酢酸フェニル、プロピオン酸フェニル、安息香酸メチル、安息香酸エチル、安息香酸プロピル、安息香酸n−ブチル等の芳香族エステル系溶媒;トルエン、キシレン、メシチレン、シクロヘキシルベンゼン、テトラリン、3−イロプロピルビフェニル、1,2,3,4−テトラメチルベンゼン、1,4−ジイソプロピルベンゼン、シクロヘキシルベンゼン、メチルナフタレン等の芳香族炭化水素系溶媒;N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド等のアミド系溶媒;n−デカン、シクロヘキサン、エチルシクロヘキサン、デカリン、ビシクロヘキサン等のアルカン系溶媒;クロロベンゼン、ジクロロベンゼン、トリクロロベンゼン等のハロゲン化芳香族炭化水素系溶媒;ブタノール、ヘキサノール等の脂肪族アルコール系溶媒;シクロヘキサノール、シクロオクタノール等の脂環族アルコール系溶媒;メチルエチルケトン、ジブチルケトン等の脂肪族ケトン系溶媒;シクロヘキサノン、シクロオクタノン、フェンコン等の脂環族ケトン系溶媒等が挙げられる。これらのうち、アルカン系溶媒及び芳香族炭化水素系溶媒が特に好ましい。 For example, aliphatic ether solvents such as ethylene glycol dimethyl ether, ethylene glycol diethyl ether, propylene glycol-1-monomethyl ether acetate (PGMEA); 1,2-dimethoxybenzene, 1,3-dimethoxybenzene, anisole, phenetol, 2 Aromatic ether solvents such as −methoxytoluene, 3-methoxytoluene, 4-methoxytoluene, 2,3-dimethylanisole, 2,4-dimethylanisole, diphenyl ether; phenyl acetate, phenyl propionate, methyl benzoate, benzoic acid Aromatic ester solvents such as ethyl, propyl benzoate, n-butyl benzoate; toluene, xylene, mesitylene, cyclohexylbenzene, tetralin, 3-iropropylbiphenyl, 1,2,3,4-tetramethylbenzene, 1, Aromatic hydrocarbon solvents such as 4-diisopropylbenzene, cyclohexylbenzene and methylnaphthalene; amide solvents such as N, N-dimethylformamide and N, N-dimethylacetamide; n-decane, cyclohexane, ethylcyclohexane, decalin, bi Alcan solvents such as cyclohexane; halogenated aromatic hydrocarbon solvents such as chlorobenzene, dichlorobenzene and trichlorobenzene; aliphatic alcohol solvents such as butanol and hexanol; alicyclic alcohol solvents such as cyclohexanol and cyclooctanol; An aliphatic ketone solvent such as methyl ethyl ketone and dibutyl ketone; an alicyclic ketone solvent such as cyclohexanone, cyclooctanone and fencon can be mentioned. Of these, alkane-based solvents and aromatic hydrocarbon-based solvents are particularly preferable.
{正孔阻止層}
発光層5と後述の電子注入層8との間に、正孔阻止層6を設けてもよい。正孔阻止層6は、発光層5の上に、発光層5の陰極9側の界面に接するように積層される層である。
この正孔阻止層6は、陽極2から移動してくる正孔を陰極9に到達するのを阻止する役割と、陰極9から注入された電子を効率よく発光層5の方向に輸送する役割とを有する。正孔阻止層6を構成する材料に求められる物性としては、電子移動度が高く正孔移動度が低いこと、エネルギーギャップ(HOMO、LUMOの差)が大きいこと、励起三重項準位(T1)が高いことが挙げられる。
このような条件を満たす正孔阻止層の材料としては、例えば、ビス(2−メチル−8−キノリノラト)(フェノラト)アルミニウム、ビス(2−メチル−8−キノリノラト)(トリフェニルシラノラト)アルミニウム等の混合配位子錯体、ビス(2−メチル−8−キノラト)アルミニウム−μ−オキソ−ビス−(2−メチル−8−キノリラト)アルミニウム二核金属錯体等の金属錯体、ジスチリルビフェニル誘導体等のスチリル化合物(日本国特開平11−242996号公報)、3−(4−ビフェニルイル)−4−フェニル−5(4−tert−ブチルフェニル)−1,2,4−トリアゾール等のトリアゾール誘導体(日本国特開平7−41759号公報)、バソクプロイン等のフェナントロリン誘導体(日本国特開平10−79297号公報)などが挙げられる。更に、国際公開第2005/022962号に記載の2,4,6位が置換されたピリジン環を少なくとも1個有する化合物も、正孔阻止層の材料として好ましい。
{Hole blocking layer}
A
The
Examples of the material of the hole blocking layer satisfying such conditions include bis (2-methyl-8-quinolinolato) (phenolato) aluminum, bis (2-methyl-8-quinolinolato) (triphenylsilanorat) aluminum and the like. Mixed ligand complexes, bis (2-methyl-8-quinolato) aluminum-μ-oxo-bis- (2-methyl-8-quinolilato) aluminum dinuclear metal complexes and other metal complexes, distyrylbiphenyl derivatives and the like. Triazole derivatives such as styryl compounds (Japanese Patent Laid-Open No. 11-2429996), 3- (4-biphenylyl) -4-phenyl-5 (4-tert-butylphenyl) -1,2,4-triazole (Japan) Japanese Patent Application Laid-Open No. 7-41759), phenanthroline derivatives such as bassokproin (Japanese Patent Laid-Open No. 10-79297), and the like can be mentioned. Further, a compound having at least one pyridine ring in which the 2, 4 and 6 positions are substituted as described in WO 2005/022962 is also preferable as a material for the hole blocking layer.
正孔阻止層6の形成方法に制限はない。従って、湿式成膜法、蒸着法や、その他の方法で形成できる。
正孔阻止層6の膜厚は、本発明の効果を著しく損なわない限り任意であるが、通常0.3nm以上、好ましくは0.5nm以上であり、また、通常100nm以下、好ましくは50nm以下である。
There is no limitation on the method of forming the
The film thickness of the
{電子輸送層}
電子輸送層7は素子の電流効率をさらに向上させることを目的として、発光層5と電子注入層8との間に設けられる。
電子輸送層7は、電界を与えられた電極間において陰極9から注入された電子を効率よく発光層5の方向に輸送することができる化合物より形成される。電子輸送層7に用いられる電子輸送性化合物としては、陰極9又は電子注入層8からの電子注入効率が高く、かつ、高い電子移動度を有し、注入された電子を効率よく輸送することができる化合物であることが必要である。
電子輸送層に用いる電子輸送性化合物としては、具体的には、例えば、8−ヒドロキシキノリンのアルミニウム錯体などの金属錯体(日本国特開昭59−194393号公報)、10−ヒドロキシベンゾ[h]キノリンの金属錯体、オキサジアゾール誘導体、ジスチリルビフェニル誘導体、シロール誘導体、3−ヒドロキシフラボン金属錯体、5−ヒドロキシフラボン金属錯体、ベンズオキサゾール金属錯体、ベンゾチアゾール金属錯体、トリスベンズイミダゾリルベンゼン(米国特許第5645948号公報)、キノキサリン化合物(日本国特開平6−207169号公報)、フェナントロリン誘導体(日本国特開平5−331459号公報)、2−t−ブチル−9,10−N,N’−ジシアノアントラキノンジイミン、n型水素化非晶質炭化シリコン、n型硫化亜鉛、n型セレン化亜鉛などが挙げられる。
電子輸送層7の膜厚は、通常1nm以上、好ましくは5nm以上であり、また、通常300nm以下、好ましくは100nm以下である。
電子輸送層7は、前記と同様にして湿式成膜法、或いは真空蒸着法により正孔阻止層6上に積層することにより形成される。通常は、真空蒸着法が用いられる。
{Electron transport layer}
The
The
Specific examples of the electron-transporting compound used in the electron-transporting layer include a metal complex such as an aluminum complex of 8-hydroxyquinolin (Japanese Patent Laid-Open No. 59-194393), 10-hydroxybenzo [h]. Kinolin metal complex, oxadiazole derivative, distyrylbiphenyl derivative, silol derivative, 3-hydroxyflavon metal complex, 5-hydroxyflavon metal complex, benzoxazole metal complex, benzothiazole metal complex, trisbenzimidazolylbenzene (US Patent No. 1) 5645948), quinoxalin compounds (Japanese Patent Laid-Open No. 6-207169), phenanthroline derivatives (Japanese Patent Laid-Open No. 5-331459), 2-t-butyl-9,10-N, N'-dicyanoanthraquinone Examples thereof include diimine, n-type hydride amorphous silicon carbide, n-type zinc sulfide, and n-type zinc selenium.
The film thickness of the
The
{電子注入層}
電子注入層8は、陰極9から注入された電子を効率よく、電子輸送層7又は発光層5へ注入する役割を果たす。
電子注入を効率よく行うには、電子注入層8を形成する材料は、仕事関数の低い金属が好ましい。例としては、ナトリウムやセシウム等のアルカリ金属、バリウムやカルシウムなどのアルカリ土類金属等が用いられる。その膜厚は通常0.1nm以上、5nm以下が好ましい。
更に、バソフェナントロリン等の含窒素複素環化合物や8−ヒドロキシキノリンのアルミニウム錯体などの金属錯体に代表される有機電子輸送材料に、ナトリウム、カリウム、セシウム、リチウム、ルビジウム等のアルカリ金属をドープする(日本国特開平10−270171号公報、日本国特開2002−100478号公報、日本国特開2002−100482号公報などに記載)ことも、電子注入・輸送性が向上し優れた膜質を両立させることが可能となるため好ましい。
電子注入層8の膜厚は通常5nm以上、好ましくは10nm以上、また、通常200nm以下、好ましくは100nm以下の範囲である。
電子注入層8は、湿式成膜法或いは真空蒸着法により、発光層5又はその上の正孔阻止層6や電子輸送層7上に積層することにより形成される。
湿式成膜法の場合の詳細は、前述の発光層の場合と同様である。
{Electron injection layer}
The
In order to efficiently perform electron injection, the material forming the
Further, an organic electron transport material represented by a nitrogen-containing heterocyclic compound such as basophenanthroline or a metal complex such as an aluminum complex of 8-hydroxyquinoline is doped with an alkali metal such as sodium, potassium, cesium, lithium, or rubidium (). (Described in Japanese Patent Application Laid-Open No. 10-270171, Japanese Patent Application Laid-Open No. 2002-100478, Japanese Patent Application Laid-Open No. 2002-1000482, etc.) also improves electron injection and transportability and achieves both excellent film quality. It is preferable because it enables this.
The film thickness of the
The
The details in the case of the wet film forming method are the same as in the case of the light emitting layer described above.
{陰極}
陰極9は、発光層5側の層(電子注入層又は発光層など)に電子を注入する役割を果たす。
陰極9の材料としては、前記の陽極2に使用される材料を用いることが可能であるが、効率良く電子注入を行なう上では、仕事関数の低い金属を用いることが好ましく、例えば、スズ、マグネシウム、インジウム、カルシウム、アルミニウム、銀等の金属又はそれらの合金などが用いられる。具体例としては、例えば、マグネシウム−銀合金、マグネシウム−インジウム合金、アルミニウム−リチウム合金等の低仕事関数の合金電極などが挙げられる。
素子の安定性の点では、陰極の上に、仕事関数が高く、大気に対して安定な金属層を積層して、低仕事関数の金属からなる陰極を保護することが好ましい。積層する金属としては、例えば、アルミニウム、銀、銅、ニッケル、クロム、金、白金等の金属が挙げられる。
陰極の膜厚は通常、陽極と同様である。
{cathode}
The cathode 9 plays a role of injecting electrons into a layer (electron injection layer, light emitting layer, etc.) on the
As the material of the cathode 9, the material used for the
From the viewpoint of device stability, it is preferable to laminate a metal layer having a high work function and stable to the atmosphere on the cathode to protect the cathode made of a metal having a low work function. Examples of the metal to be laminated include metals such as aluminum, silver, copper, nickel, chromium, gold, and platinum.
The film thickness of the cathode is usually the same as that of the anode.
{その他の層}
本発明の有機電界発光素子は、本発明の効果を著しく損なわなければ、更に他の層を有していてもよい。すなわち、陽極と陰極との間に、上述の他の任意の層を有していてもよい。
{その他の素子構成}
本発明の有機電界発光素子は、上述の説明とは逆の構造、即ち、基板上に陰極、電子注入層、電子輸送層、正孔阻止層、発光層、正孔輸送層、正孔注入層、陽極の順に積層することも可能である。
本発明の有機電界発光素子を有機電界発光装置に適用する場合は、単一の有機電界発光素子として用いても、複数の有機電界発光素子がアレイ状に配置された構成にして用いても、陽極と陰極がX−Yマトリックス状に配置された構成にして用いてもよい。
{Other layers}
The organic electroluminescent device of the present invention may further have another layer as long as the effects of the present invention are not significantly impaired. That is, any of the above-mentioned other layers may be provided between the anode and the cathode.
{Other element configurations}
The organic electroluminescent device of the present invention has a structure opposite to that described above, that is, a cathode, an electron injection layer, an electron transport layer, a hole blocking layer, a light emitting layer, a hole transport layer, and a hole injection layer on a substrate. , It is also possible to stack in the order of anode.
When the organic electroluminescent device of the present invention is applied to an organic electroluminescent device, it may be used as a single organic electroluminescent device or may be used in a configuration in which a plurality of organic electroluminescent devices are arranged in an array. The anode and cathode may be arranged in an XY matrix.
[有機EL表示装置]
本発明の有機電界発光素子表示装置(有機EL表示装置)は、上述の本発明の有機電界発光素子を用いたものである。本発明の有機EL表示装置の型式や構造については特に制限はなく、本発明の有機電界発光素子を用いて常法に従って組み立てることができる。
例えば、「有機ELディスプレイ」(オーム社、平成16年8月20日発行、時任静士、安達千波矢、村田英幸著)に記載されているような方法で、本発明の有機EL表示装置を形成することができる。
[Organic EL display device]
The organic electroluminescent element display device (organic EL display device) of the present invention uses the above-mentioned organic electroluminescent element of the present invention. The model and structure of the organic EL display device of the present invention are not particularly limited, and can be assembled according to a conventional method using the organic electroluminescent device of the present invention.
For example, the organic EL display device of the present invention can be used by the method described in "Organic EL Display" (Ohmsha, published on August 20, 2004, by Shizushi Tokito, Chihaya Adachi, Hideyuki Murata). Can be formed.
[有機EL照明]
本発明の有機電界発光素子照明(有機EL照明)は、上述の本発明の有機電界発光素子を用いたものである。本発明の有機EL照明の型式や構造については特に制限はなく、本発明の有機電界発光素子を用いて常法に従って組み立てることができる。
[Organic EL lighting]
The organic electroluminescent element illumination (organic EL illumination) of the present invention uses the above-mentioned organic electroluminescent element of the present invention. The type and structure of the organic EL illumination of the present invention are not particularly limited, and can be assembled according to a conventional method using the organic electroluminescent device of the present invention.
以下、実施例を示して本発明について更に具体的に説明する。ただし、本発明は以下の実施例に限定されるものではなく、本発明はその要旨を逸脱しない限り任意に変更して実施できる。
<モノマーの合成>
Hereinafter, the present invention will be described in more detail with reference to Examples. However, the present invention is not limited to the following examples, and the present invention can be arbitrarily modified and implemented without departing from the gist thereof.
<Synthesis of monomer>
化合物1(10.0g、28.61mmol)、ブロモベンゼン(4.27g、27.18mmol)及びtert−ブトキシナトリウム(7.4g、77.25mmol)、トルエン(150ml)を仕込み、系内を窒素置換して、60℃まで加温した(溶液A)。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.089g、0.086mmol)のトルエン15ml溶液に、1,1’−ビス(ジフェニルホスフィノ)フェロセン(0.19g、0.344mmol)を加え、60℃まで加温した(溶液B)。窒素気流中、溶液Aに溶液Bを添加し、3.0時間、加熱還流した。室温まで放冷した後、反応液を酢酸エチル(300ml)および食塩水(100ml)を加え攪拌後、分液し、水層を酢酸エチル(100ml×2回)で抽出し、有機層を合わせ、硫酸マグネシウムで乾燥後、濃縮した。さらに、シリカゲルカラムクロマトグラフィー(n−ヘキサン/塩化メチレン=3/1)で精製することにより、淡黄色油状の化合物2(10.4g)を得た。 Compound 1 (10.0 g, 28.61 mmol), bromobenzene (4.27 g, 27.18 mmol), tert-butoxysodium (7.4 g, 77.25 mmol), and toluene (150 ml) were charged, and the system was nitrogen-substituted. Then, it was heated to 60 ° C. (solution A). To a solution of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.089 g, 0.086 mmol) in 15 ml of toluene was added 1,1'-bis (diphenylphosphino) ferrocene (0.19 g, 0.344 mmol) to 60. It was heated to ° C (solution B). Solution B was added to solution A in a nitrogen stream, and the mixture was heated under reflux for 3.0 hours. After allowing to cool to room temperature, the reaction solution was added with ethyl acetate (300 ml) and saline solution (100 ml), stirred, separated, the aqueous layer was extracted with ethyl acetate (100 ml × 2 times), and the organic layers were combined. After drying over magnesium sulfate, the mixture was concentrated. Further, purification by silica gel column chromatography (n-hexane / methylene chloride = 3/1) gave compound 2 (10.4 g) of a pale yellow oil.
化合物2(10.4g、24.43mmol)にN,N−ジメチルホルムアミド(200ml)および塩化メチレン(200ml)を加え、氷浴で冷却した。ここにN−ブロモスクシンイミド(4.35g、24.43mmol)のN,N−ジメチルホルムアミド(50ml)および塩化メチレン(50ml)溶液を滴下し、攪拌しながら3時間かけて室温まで昇温した。反応液に水を加え、塩化メチレンで抽出を行った。有機層を濃縮し、カラムクロマトグラフィー(展開液:ヘキサン/塩化メチレン=3/1)で精製することにより、淡黄色油状の化合物3(10.8g)を得た。 N, N-dimethylformamide (200 ml) and methylene chloride (200 ml) were added to Compound 2 (10.4 g, 24.43 mmol), and the mixture was cooled in an ice bath. A solution of N-N-dimethylformamide (50 ml) and methylene chloride (50 ml) of N-bromosuccinimide (4.35 g, 24.43 mmol) was added dropwise thereto, and the temperature was raised to room temperature over 3 hours with stirring. Water was added to the reaction solution, and extraction was performed with methylene chloride. The organic layer was concentrated and purified by column chromatography (developing solution: hexane / methylene chloride = 3/1) to obtain a pale yellow oily compound 3 (10.8 g).
化合物3(15.95g、31.61mmol)、4,4’−ビフェニルジボロン酸(3.9g、16.13mmol)、炭酸カリウム(10.9g、79.03mmol)、及びトルエン(120ml)、エタノール(60ml)、水(40ml)をフラスコに仕込み、系内を十分に窒素置換して80℃まで加温した。テトラキス(トリフェニルホスフィン)パラジウム(1.8g、1.58mmol)を加え、80℃で4時間攪拌した。反応液に水を加え、トルエンで抽出を行った。有機層を濃縮し、カラムクロマトグラフィー(展開液:ヘキサン/トルエン=2/1)により精製した。続いて再度カラムクロマトグラフィー(展開液:THF/アセトニトリル=1/2)により精製した。化合物4(8.5g、収率52.6%)を得た。化合物4のHPLC純度は99.7面積%であった。
Compound 3 (15.95 g, 31.61 mmol), 4,4'-biphenyldiboronic acid (3.9 g, 16.13 mmol), potassium carbonate (10.9 g, 79.03 mmol), and toluene (120 ml), ethanol. (60 ml) and water (40 ml) were placed in a flask, and the inside of the system was sufficiently replaced with nitrogen and heated to 80 ° C. Tetrakis (triphenylphosphine) palladium (1.8 g, 1.58 mmol) was added, and the mixture was stirred at 80 ° C. for 4 hours. Water was added to the reaction solution, and extraction was performed with toluene. The organic layer was concentrated and purified by column chromatography (developing solution: hexane / toluene = 2/1). Then, it was purified again by column chromatography (developing solution: THF / acetonitrile = 1/2). Compound 4 (8.5 g, yield 52.6%) was obtained. The HPLC purity of
4−(3−アミノフェニル)ベンゾシクロブテン(8.77g、45mmol)およびN−メチルピロリドン(60ml)を混合し、−5 ℃まで冷却した。濃塩酸(8.59ml、99mmol)、脱塩水(30ml)を加え、30分攪拌した。続いて、−5℃まで冷却した亜硝酸ナトリウム(3.20g、46.35mmol)水溶液(30ml)を5℃以下で加え、30分攪拌し、ジアゾニウム塩溶液とした。60℃に加熱したヨウ化カリウム(2263g、136.35mmol)水溶液(400ml)に、上記ジアゾニウム塩溶液を滴下し、2時間攪拌した。反応液に、ジクロロメタンを加えて、抽出し、水洗、チオ硫酸ナトリウム溶液での洗浄後、硫酸マグネシウムを加え、攪拌後、ろ過し、濾液を濃縮した。シリカゲルカラムクロマトグラフィー(展開溶媒:n−ヘキサン)により精製し、4−(3−ヨードフェニル)ベンゾシクロブテン(7.8g、収率56.6%)を得た。 4- (3-Aminophenyl) benzocyclobutene (8.77 g, 45 mmol) and N-methylpyrrolidone (60 ml) were mixed and cooled to -5 ° C. Concentrated hydrochloric acid (8.59 ml, 99 mmol) and desalted water (30 ml) were added, and the mixture was stirred for 30 minutes. Subsequently, an aqueous solution of sodium nitrite (3.20 g, 46.35 mmol) cooled to −5 ° C. (30 ml) was added at 5 ° C. or lower, and the mixture was stirred for 30 minutes to prepare a diazonium salt solution. The above diazonium salt solution was added dropwise to an aqueous solution (400 ml) of potassium iodide (2263 g, 136.35 mmol) heated to 60 ° C., and the mixture was stirred for 2 hours. Dichloromethane was added to the reaction solution, extracted, washed with water, washed with sodium thiosulfate solution, magnesium sulfate was added, stirred, filtered, and the filtrate was concentrated. Purification by silica gel column chromatography (developing solvent: n-hexane) gave 4- (3-iodophenyl) benzocyclobutene (7.8 g, yield 56.6%).
窒素気流下、ジメチルスルホキシド(100ml)、4−(3−ヨードフェニル)ベンゾシクロブテン(5.00g、16.3mmol)、ビス(ピナコラト)ジボロン(5.39g、21.2mmol)、酢酸カリウム(4.00g、40.8mmol)をフラスコに仕込み、60℃で30分間攪拌した。続いて、1,1’−ビス(ジフェニルホスフィノ)フェロセン−パラジウム(II)ジクロリド−ジクロロメタン〔PdCl2(dppf)CH2Cl2〕(0.33g、0.41mmol)を加え、85℃で8時間加熱攪拌した。反応液にトルエンを加え、水洗し、硫酸マグネシウムを加え、攪拌後、濾過した。濾液に活性白土を加え、攪拌後、濾過した。濾液を濃縮し、無色固体の化合物6(4.71g、収率94.2%)を得た。 Dimethyl sulfoxide (100 ml), 4- (3-iodophenyl) benzocyclobutene (5.00 g, 16.3 mmol), bis (pinacolato) diboron (5.39 g, 21.2 mmol), potassium acetate (4) under a nitrogen stream. 0.00 g, 40.8 mmol) was placed in a flask and stirred at 60 ° C. for 30 minutes. Subsequently, 1,1'-bis (diphenylphosphino) ferrocene-palladium (II) dichloride-dichloromethane [PdCl 2 (dppf) CH 2 Cl 2 ] (0.33 g, 0.41 mmol) was added, and 8 at 85 ° C. The mixture was heated and stirred for hours. Toluene was added to the reaction solution, washed with water, magnesium sulfate was added, and the mixture was stirred and then filtered. Active clay was added to the filtrate, and the mixture was stirred and then filtered. The filtrate was concentrated to give compound 6 (4.71 g, yield 94.2%) as a colorless solid.
窒素気流下、トルエン(100ml)、エタノール(50ml)、化合物6(4.00g、13.1mmol)、1,3,5−トリブロモベンゼン(4.11g、13.1mmol)、2Mの炭酸ナトリウム水溶液(50ml)をフラスコに仕込み、60℃で30分間加熱攪拌した。続いて、テトラキス(トリフェニルホスフィン)パラジウム(0.30g、0.26mmol)を加え、2時間還流した。反応液に水を加え、トルエンで抽出し、硫酸マグネシウムおよび活性白土を加え、攪拌後、ろ過し、濾液を濃縮した。シリカゲルカラムクロマトグラフィー(展開溶媒:n−ヘキサン:トルエン=5:1)により精製し、無色オイルの化合物7(3.89g、収率71.9%)を得た。 Under a nitrogen stream, toluene (100 ml), ethanol (50 ml), compound 6 (4.00 g, 13.1 mmol), 1,3,5-tribromobenzene (4.11 g, 13.1 mmol), 2 M aqueous sodium carbonate solution. (50 ml) was placed in a flask and heated and stirred at 60 ° C. for 30 minutes. Subsequently, tetrakis (triphenylphosphine) palladium (0.30 g, 0.26 mmol) was added, and the mixture was refluxed for 2 hours. Water was added to the reaction mixture, the mixture was extracted with toluene, magnesium sulfate and activated clay were added, and the mixture was stirred, filtered, and the filtrate was concentrated. Purification by silica gel column chromatography (developing solvent: n-hexane: toluene = 5: 1) gave compound 7 (3.89 g, yield 71.9%) of a colorless oil.
窒素気流下、ジメチルスルホキシド(300ml)、4,4”−ジブロモ−p−テルフェニル、3.0g(7.73mmol)、ビス(ピナコラト)ジボロン4.71g(18.55mmol)、酢酸カリウム4.55g(46.38mmol)を仕込み、系内を窒素置換して、60℃で30分間攪拌した。続いて、1,1’−ビス(ジフェニルホスフィノ)フェロセンパラジウム(II)ジクロリドジクロロメタン付加物0.32g(0.387mmol)を加え、83℃で4時間反応した。反応液を減圧濾過し、濾液に水を加え、トルエンで抽出を行った。有機層に無水硫酸マグネシウム、活性白土を加え、撹拌した後、減圧濾過し、濾液を濃縮した。析出した固体をメタノールで懸濁洗浄し、無色固体の化合物7を得た(収量2.8g、収率75%)。
Under nitrogen stream, dimethyl sulfoxide (300 ml), 4,4 "-dibromo-p-terphenyl, 3.0 g (7.73 mmol), bis (pinacolato) diboron 4.71 g (18.55 mmol), potassium acetate 4.55 g (46.38 mmol) was charged, the inside of the system was replaced with nitrogen, and the mixture was stirred at 60 ° C. for 30 minutes. Subsequently, 0.32 g of 1,1'-bis (diphenylphosphino) ferrocene palladium (II) dichloride dichloromethane adduct. (0.387 mmol) was added, and the reaction was carried out at 83 ° C. for 4 hours. The reaction solution was filtered under reduced pressure, water was added to the filtrate, and extraction was performed with toluene. Anhydrous magnesium sulfate and active white clay were added to the organic layer, and the mixture was stirred. Then, the filtrate was concentrated under reduced pressure. The precipitated solid was suspended and washed with methanol to obtain
化合物3(4.95g、9.95mmol)、化合物7(2.36g、4.97mmol)、炭酸カリウム(5.53g、40.0mmol)、及びトルエン(60ml)、エタノール(20ml)、水(20ml)を仕込み、系内を十分に窒素置換して60℃まで加温した。テトラキス(トリフェニルホスフィン)パラジウム(0.29g、0.25mmol)を加え、80℃で4時間攪拌した。反応液に水を加え、トルエンで抽出を行った。有機層を濃縮し、カラムクロマトグラフィー(展開液:ヘキサン/塩化メチレン=2/1)により精製し、化合物8(2.77g、収率51.7%)を得た。 Compound 3 (4.95 g, 9.95 mmol), Compound 7 (2.36 g, 4.97 mmol), potassium carbonate (5.53 g, 40.0 mmol), and toluene (60 ml), ethanol (20 ml), water (20 ml). ) Was charged, and the inside of the system was sufficiently replaced with nitrogen and heated to 60 ° C. Tetrakis (triphenylphosphine) palladium (0.29 g, 0.25 mmol) was added, and the mixture was stirred at 80 ° C. for 4 hours. Water was added to the reaction solution, and extraction was performed with toluene. The organic layer was concentrated and purified by column chromatography (developing solution: hexane / methylene chloride = 2/1) to obtain Compound 8 (2.77 g, yield 51.7%).
<重合体1の合成>
<Synthesis of
化合物4(2.0g、1.997mmol)、化合物6(0.095g、0.2296mmol)、及びtert−ブトキシナトリウム(1.48g、15.38mmol)、トルエン(30ml)を仕込み、系内を窒素置換して、60℃まで加温した(溶液A)。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.042g、0.0399mmol)のトルエン溶液(5ml)に、[4−(N,N−ジメチルアミノ)フェニル]ジ−tert−ブチルホスフィン(0.085g、0.3195mmol)を加え、60℃まで加温した(溶液B)。窒素気流中、溶液Aに溶液Bを添加し、1.0時間、加熱還流した。続いて、4,4’−ジブロモビフェニル(0.52g、1.667mmol)を添加した。1.0時間、加熱還流後、4,4’−ジブロモビフェニル(0.025g、0.08mmol)を追添加した。30分後、反応液を放冷して、反応液をエタノール500ml中に滴下し、粗ポリマーを晶出させた。
得られた粗ポリマーをトルエン(90ml)に溶解させ、N,N−ジフェニルアミン(0.068g、0.403mmol)、tert−ブトキシナトリウム(0.74g、7.7mmol)を仕込み、系内を窒素置換して、60℃まで加温した(溶液C)。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.021g、0.0203mmol)のトルエン溶液(3ml)に、[4−(N,N−ジメチルアミノ)フェニル]ジ−tert−ブチルホスフィン(0.043g、0.1598mmol)を加え、60℃まで加温した(溶液D)。窒素気流中、溶液Cに溶液Dを添加し、3時間、加熱還流した。この反応液に、ブロモベンゼン(0.35g、0.2229mmol)を添加した。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.021g、0.0203mmol)のトルエン溶液(3ml)に、[4−(N,N−ジメチルアミノ)フェニル]ジ−tert−ブチルホスフィン(0.043g、0.1598mmol)を加え、60℃まで加温した(溶液E)。窒素気流中、反応液に溶液Eを添加し、3時間、加熱還流した。反応液を放冷し、エタノール/水(1500ml/100ml)溶液に滴下し、エンドキャップした粗ポリマーを得た。
このエンドキャップした粗ポリマーをトルエンに溶解し、アセトンで再沈殿させ、析出したポリマーをトルエンに再溶解させ、希塩酸にて洗浄し、アンモニア含有エタノールにて再沈殿した。濾取したポリマーをカラムクロマトグラフィーにより精製し、重合体1(1.0g)を得た。
重量平均分子量(Mw)=47100
数平均分子量(Mn)=33400
分散度(Mw/Mn)=1.41
Compound 4 (2.0 g, 1.997 mmol), compound 6 (0.095 g, 0.2296 mmol), and tert-butoxysodium (1.48 g, 15.38 mmol) and toluene (30 ml) were charged, and nitrogen was added to the system. It was replaced and heated to 60 ° C. (solution A). [4- (N, N-dimethylamino) phenyl] di-tert-butylphosphine (0.085 g) in a toluene solution (5 ml) of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.042 g, 0.0399 mmol) , 0.3195 mmol) and heated to 60 ° C. (Solution B). Solution B was added to solution A in a nitrogen stream, and the mixture was heated under reflux for 1.0 hour. Subsequently, 4,4'-dibromobiphenyl (0.52 g, 1.667 mmol) was added. After heating under reflux for 1.0 hour, 4,4'-dibromobiphenyl (0.025 g, 0.08 mmol) was added. After 30 minutes, the reaction solution was allowed to cool, and the reaction solution was added dropwise to 500 ml of ethanol to crystallize the crude polymer.
The obtained crude polymer was dissolved in toluene (90 ml), N, N-diphenylamine (0.068 g, 0.403 mmol) and tert-butoxysodium (0.74 g, 7.7 mmol) were charged, and the inside of the system was replaced with nitrogen. Then, it was heated to 60 ° C. (solution C). [4- (N, N-dimethylamino) phenyl] di-tert-butylphosphine (0.043 g) in a toluene solution (3 ml) of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.021 g, 0.0203 mmol) , 0.1598 mmol) and heated to 60 ° C. (Solution D). Solution D was added to solution C in a nitrogen stream, and the mixture was heated under reflux for 3 hours. Bromobenzene (0.35 g, 0.2229 mmol) was added to this reaction solution. [4- (N, N-dimethylamino) phenyl] di-tert-butylphosphine (0.043 g) in a toluene solution (3 ml) of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.021 g, 0.0203 mmol) , 0.1598 mmol) and heated to 60 ° C. (solution E). Solution E was added to the reaction solution in a nitrogen stream, and the mixture was heated under reflux for 3 hours. The reaction mixture was allowed to cool and added dropwise to an ethanol / water (1500 ml / 100 ml) solution to obtain an end-capped crude polymer.
The end-capped crude polymer was dissolved in toluene and reprecipitated with acetone, the precipitated polymer was redissolved in toluene, washed with dilute hydrochloric acid, and reprecipitated with ammonia-containing ethanol. The polymer collected by filtration was purified by column chromatography to obtain Polymer 1 (1.0 g).
Weight average molecular weight (Mw) = 47100
Number average molecular weight (Mn) = 33400
Dispersity (Mw / Mn) = 1.41
<重合体2の合成>
<Synthesis of
化合物8(2.155g、2.00mmol)、化合物6(0.095g、0.23mmol)、及びtert−ブトキシナトリウム(1.48g、15.4mmol)、トルエン(35ml)を仕込み、系内を窒素置換して、60℃まで加温した(溶液A)。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.041g、0.041mmol)のトルエン溶液(5ml)に、[4−(N,N−ジメチルアミノ)フェニル]ジ−tert−ブチルホスフィン(0.085g、0.32mmol)を加え、60℃まで加温した(溶液B)。窒素気流中、溶液Aに溶液Bを添加し、1.0時間、加熱還流した。続いて、4,4’−ジブロモビフェニル(0.493g、1.58mmol)を添加した。1.0時間、加熱還流後、反応液を放冷して、反応液をエタノール500ml中に滴下し、粗ポリマーを晶出させた。
得られた粗ポリマーをトルエン(150ml)に溶解させ、N,N−ジフェニルアミン(0.068g、0.040mmol)、tert−ブトキシナトリウム(0.74g、7.7mmol)を仕込み、系内を窒素置換して、60℃まで加温した(溶液C)。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.021g、0.0203mmol)のトルエン溶液(3ml)に、[4−(N,N−ジメチルアミノ)フェニル]ジ−tert−ブチルホスフィン(0.043g、0.16mmol)を加え、60℃まで加温した(溶液D)。窒素気流中、溶液Cに溶液Dを添加し、3時間、加熱還流した。この反応液に、ブロモベンゼン(0.35g、0.223mmol)を添加した。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.021g、0.0203mmol)のトルエン溶液(3ml)に、[4−(N,N−ジメチルアミノ)フェニル]ジ−tert−ブチルホスフィン(0.043g、0.1598mmol)を加え、60℃まで加温した(溶液E)。窒素気流中、反応液に溶液Eを添加し、3時間、加熱還流した。反応液を放冷し、エタノール/水(1500ml/100ml)溶液に滴下し、エンドキャップした粗ポリマーを得た。
このエンドキャップした粗ポリマーをトルエンに溶解し、アセトンで再沈殿させ、析出したポリマーをトルエンに再溶解させ、希塩酸にて洗浄し、アンモニア含有エタノールにて再沈殿した。濾取したポリマーをカラムクロマトグラフィーにより精製し、重合体2を得た(1.2g)。
重量平均分子量(Mw)=110000
数平均分子量(Mn)=48200
分散度(Mw/Mn)=2.28
Compound 8 (2.155 g, 2.00 mmol), compound 6 (0.095 g, 0.23 mmol), and tert-butoxysodium (1.48 g, 15.4 mmol) and toluene (35 ml) were charged, and nitrogen was added to the system. It was replaced and heated to 60 ° C. (solution A). [4- (N, N-dimethylamino) phenyl] di-tert-butylphosphine (0.085 g) in a toluene solution (5 ml) of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.041 g, 0.041 mmol) , 0.32 mmol) and heated to 60 ° C. (Solution B). Solution B was added to solution A in a nitrogen stream, and the mixture was heated under reflux for 1.0 hour. Subsequently, 4,4'-dibromobiphenyl (0.493 g, 1.58 mmol) was added. After heating under reflux for 1.0 hour, the reaction solution was allowed to cool, and the reaction solution was added dropwise to 500 ml of ethanol to crystallize the crude polymer.
The obtained crude polymer was dissolved in toluene (150 ml), N, N-diphenylamine (0.068 g, 0.040 mmol) and tert-butoxysodium (0.74 g, 7.7 mmol) were charged, and the inside of the system was replaced with nitrogen. Then, it was heated to 60 ° C. (solution C). [4- (N, N-dimethylamino) phenyl] di-tert-butylphosphine (0.043 g) in a toluene solution (3 ml) of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.021 g, 0.0203 mmol) , 0.16 mmol) and heated to 60 ° C. (Solution D). Solution D was added to solution C in a nitrogen stream, and the mixture was heated under reflux for 3 hours. Bromobenzene (0.35 g, 0.223 mmol) was added to this reaction solution. [4- (N, N-dimethylamino) phenyl] di-tert-butylphosphine (0.043 g) in a toluene solution (3 ml) of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.021 g, 0.0203 mmol) , 0.1598 mmol) and heated to 60 ° C. (solution E). Solution E was added to the reaction solution in a nitrogen stream, and the mixture was heated under reflux for 3 hours. The reaction mixture was allowed to cool and added dropwise to an ethanol / water (1500 ml / 100 ml) solution to obtain an end-capped crude polymer.
The end-capped crude polymer was dissolved in toluene and reprecipitated with acetone, the precipitated polymer was redissolved in toluene, washed with dilute hydrochloric acid, and reprecipitated with ammonia-containing ethanol. The polymer collected by filtration was purified by column chromatography to obtain polymer 2 (1.2 g).
Weight average molecular weight (Mw) = 110,000
Number average molecular weight (Mn) = 48200
Dispersity (Mw / Mn) = 2.28
<重合体3の合成>
<Synthesis of
化合物4(9.0g、8.99mmol)、化合物9(0.911g、1.36mmol)、及びtert−ブトキシナトリウム(6.66g、69.3mmol)、トルエン(187ml)を仕込み、系内を十分に窒素置換して、60℃まで加温した(溶液A)。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.186g、1.8mmol)のトルエン31ml溶液に、[4−(N,N−ジメチルアミノ)フェニル]ジ−tert−ブチルホスフィン(0.382g、1.4mmol)を加え、60℃まで加温した(溶液B)。窒素気流中、溶液Aに溶液Bを添加し、1.0時間、加熱還流反応した。続いて、4,4”−ジブロモ−p−テルフェニル(2.546g、6.56mmol)を添加した。1.0時間加熱還流した。反応液を放冷して、トルエン(125ml)を入れ、反応液をエタノール1250ml中に滴下し、粗ポリマーを晶出させた。
得られた粗ポリマーをトルエン224mlに溶解させ、N,N−ジフェニルアミン(0.573g、3.4mmol)、tert−ブトキシナトリウム(3.125g、32.5mmol)を仕込み、系内を十分に窒素置換して、60℃まで加温した(溶液C)。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.088g、0.1mmol)のトルエン12.5ml溶液に、[4−(N,N−ジメチルアミノ)フェニル]ジ−tert−ブチルホスフィン(0.18g、0.7mmol)を加え、60℃まで加温した(溶液D)。窒素気流中、溶液Cに溶液Dを添加し、3時間、加熱還流反応した。この反応液に、ブロモベンゼン(2.659g、16.9mmol)を添加した。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.088g、0.1mmol)のトルエン12.5ml溶液に、[4−(N,N−ジメチルアミノ)フェニル]ジ−tert−ブチルホスフィン(0.18g、0.7mmol)を加え、60℃まで加温した(溶液E)。窒素気流中、反応液に溶液Eを添加し、3時間、加熱還流反応した。反応液を放冷し、エタノール/水(1120ml/108ml)溶液に滴下し、エンドキャップした粗ポリマーを得た。
このエンドキャップした粗ポリマーをトルエンに溶解し、アセトンで再沈殿させ、析出したポリマーをトルエンに再溶解させ、希塩酸にて洗浄し、アンモニア含有エタノールにて再沈殿した。濾取したポリマーをカラムクロマトグラフィーにより精製し、重合体3を得た(4.3g)。
重量平均分子量(Mw)=35900
数平均分子量(Mn)=27600
分散度(Mw/Mn)=1.30
Compound 4 (9.0 g, 8.99 mmol), compound 9 (0.911 g, 1.36 mmol), and tert-butoxysodium (6.66 g, 69.3 mmol) and toluene (187 ml) were charged to sufficiently fill the system. Was replaced with nitrogen and heated to 60 ° C. (solution A). [4- (N, N-dimethylamino) phenyl] di-tert-butylphosphine (0.382 g, 1) in a 31 ml solution of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.186 g, 1.8 mmol) in toluene. .4 mmol) was added and the mixture was heated to 60 ° C. (solution B). Solution B was added to solution A in a nitrogen stream, and the mixture was heated under reflux for 1.0 hour. Subsequently, 4,4 "-dibromo-p-terphenyl (2.546 g, 6.56 mmol) was added. The mixture was heated to reflux for 1.0 hour. The reaction solution was allowed to cool, and toluene (125 ml) was added. The reaction solution was added dropwise to 1250 ml of ethanol to crystallize the crude polymer.
The obtained crude polymer was dissolved in 224 ml of toluene, N, N-diphenylamine (0.573 g, 3.4 mmol) and tert-butoxysodium (3.125 g, 32.5 mmol) were charged, and the inside of the system was sufficiently replaced with nitrogen. Then, it was heated to 60 ° C. (solution C). [4- (N, N-dimethylamino) phenyl] di-tert-butylphosphine (0.18 g) in a 12.5 ml solution of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.088 g, 0.1 mmol) in toluene. , 0.7 mmol) and heated to 60 ° C. (Solution D). Solution D was added to solution C in a nitrogen stream, and a heating reflux reaction was carried out for 3 hours. Bromobenzene (2.659 g, 16.9 mmol) was added to this reaction solution. [4- (N, N-dimethylamino) phenyl] di-tert-butylphosphine (0.18 g) in a 12.5 ml solution of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.088 g, 0.1 mmol) in toluene. , 0.7 mmol) and heated to 60 ° C. (solution E). Solution E was added to the reaction solution in a nitrogen stream, and the mixture was heated under reflux for 3 hours. The reaction mixture was allowed to cool and added dropwise to an ethanol / water (1120 ml / 108 ml) solution to obtain an end-capped crude polymer.
The end-capped crude polymer was dissolved in toluene and reprecipitated with acetone, the precipitated polymer was redissolved in toluene, washed with dilute hydrochloric acid, and reprecipitated with ammonia-containing ethanol. The polymer collected by filtration was purified by column chromatography to obtain polymer 3 (4.3 g).
Weight average molecular weight (Mw) = 35900
Number average molecular weight (Mn) = 27600
Dispersity (Mw / Mn) = 1.30
<重合体4の合成>
<Synthesis of
化合物4(5.0g、4.99mmol)、化合物6(0.313g、0.756mmol)、及びtert−ブトキシナトリウム(3.699g、38.5mmol)、トルエン(104ml)を仕込み、系内を十分に窒素置換して、60℃まで加温した(溶液A)。トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0.103g、0.1mmol)のトルエン17ml溶液に、[4−(N,N−ジメチルアミノ)フェニル]ジ−tert−ブチルホスフィン(0.212g、0.8mmol)を加え、60℃まで加温した(溶液B)。窒素気流中、溶液Aに溶液Bを添加し、1.0時間、加熱還流反応した。続いて、化合物10(2.053g、3.74mmol)を添加した。1.0時間加熱還流した。
N,N−ジフェニルアミン(0.338g、2.0mmol)、1時間、加熱還流反応した。この反応液に、ブロモベンゼン(1.568g、10mmol)を添加した。2時間、加熱還流反応した。反応液を放冷し、エタノール/水(342ml/100ml)溶液に滴下し、エンドキャップした粗ポリマーを得た。
このエンドキャップした粗ポリマーをトルエンに溶解し、アセトンで再沈殿させ析出したポリマーをトルエンに再溶解させ、希塩酸にて洗浄し、アンモニア含有エタノールにて再沈殿した。濾取したポリマーをカラムクロマトグラフィーにより精製し、重合体4を得た(2.1g)。
重量平均分子量(Mw)=38800
数平均分子量(Mn)=29800
分散度(Mw/Mn)=1.30
Compound 4 (5.0 g, 4.99 mmol), compound 6 (0.313 g, 0.756 mmol), and tert-butoxysodium (3.699 g, 38.5 mmol) and toluene (104 ml) were charged to sufficiently fill the system. Was replaced with nitrogen and heated to 60 ° C. (solution A). [4- (N, N-dimethylamino) phenyl] di-tert-butylphosphine (0.212 g, 0) in a solution of tris (dibenzylideneacetone) dipalladium-chloroform complex (0.103 g, 0.1 mmol) in 17 ml of toluene. 8.8 mmol) was added and the mixture was heated to 60 ° C. (Solution B). Solution B was added to solution A in a nitrogen stream, and the mixture was heated under reflux for 1.0 hour. Subsequently, compound 10 (2.053 g, 3.74 mmol) was added. The mixture was heated under reflux for 1.0 hour.
N, N-diphenylamine (0.338 g, 2.0 mmol) was heated under reflux for 1 hour. Bromobenzene (1.568 g, 10 mmol) was added to this reaction solution. The mixture was heated under reflux for 2 hours. The reaction mixture was allowed to cool and added dropwise to an ethanol / water (342 ml / 100 ml) solution to obtain an end-capped crude polymer.
This end-capped crude polymer was dissolved in toluene, reprecipitated with acetone, the precipitated polymer was redissolved in toluene, washed with dilute hydrochloric acid, and reprecipitated with ammonia-containing ethanol. The polymer collected by filtration was purified by column chromatography to obtain polymer 4 (2.1 g).
Weight average molecular weight (Mw) = 38800
Number average molecular weight (Mn) = 29800
Dispersity (Mw / Mn) = 1.30
<有機電界発光素子の作製>
(実施例1)
図1に示す有機電界発光素子を作製した。
ガラス基板1上に、インジウム・スズ酸化物(ITO)透明導電膜をスパッタ成膜により堆積したものを、通常のフォトリソグラフィー技術と塩酸エッチングを用いて2mm幅のストライプにパターニングして膜厚70nmの陽極2を形成した。パターン形成したITO基板を、界面活性剤水溶液による超音波洗浄、超純水による水洗、超純水による超音波洗浄、超純水による水洗の順で洗浄後、圧縮空気で乾燥させ、最後に紫外線オゾン洗浄を行った。
次に、下の構造式(P1)に示すアリールアミンポリマー、構造式(A1)に示す4‐イソプロピル‐4’‐メチルジフェニルヨードニウムテトラキス(ペンタフルオロフェニル)ボラートおよび安息香酸エチルを含有する正孔注入層形成用塗布液を調製した。この塗布液を下記条件で陽極2上にスピンコートにより成膜して、膜厚31nmの正孔注入層を得た。
<Manufacturing of organic electroluminescent device>
(Example 1)
The organic electroluminescent device shown in FIG. 1 was manufactured.
An indium tin oxide (ITO) transparent conductive film deposited on a
Next, hole injection containing the arylamine polymer represented by the structural formula (P1) below, 4-isopropyl-4'-methyldiphenyliodonium tetrakis (pentafluorophenyl) borate represented by the structural formula (A1), and ethyl benzoate. A coating solution for layer formation was prepared. This coating liquid was formed on the
<正孔注入層形成用塗布液>
溶媒 安息香酸エチル
塗布液濃度 P1:2.5重量%
A1:0.5重量%
<正孔注入層3の成膜条件>
スピナ回転数 3100rpm
スピナ回転時間 30秒
スピンコート雰囲気 大気中
加熱条件 大気中 240℃ 1時間
引き続き、下記に示す構造式を有する重合体1(P2)を含有する正孔輸送層形成用塗布液を調製し、下記の条件で正孔注入層3上にスピンコートにより成膜、加熱して膜厚20nmの正孔輸送層を形成した。
<Coating liquid for forming hole injection layer>
Solvent Ethyl benzoate Coating solution concentration P1: 2.5% by weight
A1: 0.5% by weight
<Conditions for forming the
Spinner speed 3100 rpm
Spinner rotation time 30 seconds Spin coating atmosphere Atmosphere heating conditions Atmosphere 240 ° C. 1 hour Subsequently, a coating solution for forming a hole transport layer containing polymer 1 (P2) having the structural formula shown below was prepared, and the following was prepared. Under the conditions, a hole coating layer having a film thickness of 20 nm was formed on the
<正孔輸送層形成用塗布液>
溶媒 シクロヘキシルベンゼン
塗布液濃度 1.5重量%
<正孔輸送層4の成膜条件>
スピナ回転数 1950rpm
スピナ回転時間 120秒
スピンコート雰囲気 窒素中
加熱条件 窒素中 230℃ 1時間
次に、以下の構造式に示す、化合物(H1)、(H2)、および(D1)を含有する発光層形成用塗布液を調製し、下記の条件でスピンコートにより成膜を行い、加熱することで膜厚50nmの発光層を正孔輸送層4上に形成した。
<Coating liquid for forming hole transport layer>
Solvent Cyclohexylbenzene Coating solution concentration 1.5% by weight
<Conditions for forming the
Spinner speed 1950 rpm
Spinner rotation time 120 seconds Spin coating atmosphere In nitrogen Heating conditions In nitrogen 230 ° C for 1 hour Next, a coating liquid for forming a light emitting layer containing the compounds (H1), (H2), and (D1) shown in the following structural formula. Was prepared, a film was formed by spin coating under the following conditions, and a light emitting layer having a film thickness of 50 nm was formed on the
<発光層形成用塗布液>
溶媒 シクロヘキシルベンゼン
塗布液濃度 H1:1.2重量%
H2:3.6重量%
D1:0.48重量%
<発光層5の成膜条件>
スピナ回転数 2050rpm
スピナ回転時間 120秒
スピンコート雰囲気 窒素中
加熱条件 窒素中 130℃ 10分
<Coating liquid for forming a light emitting layer>
Solvent Cyclohexylbenzene Coating liquid concentration H1: 1.2% by weight
H2: 3.6% by weight
D1: 0.48% by weight
<Conditions for film formation of light emitting
Spinner speed 2050 rpm
Spinner rotation time 120 seconds Spin coating atmosphere In nitrogen Heating conditions In nitrogen 130 ° C 10 minutes
ここで、発光層までを成膜した基板を、真空蒸着装置内に移し、装置内の真空度が2.0x10−4Pa以下になるまで排気した後、下記に示す構造を有する有機化合物(E1)を真空蒸着法にて蒸着速度を0.9〜1.0Å/秒の範囲で制御し、発光層5の上に積層させ、膜厚10nmの正孔阻止層6を得た。
Here, the substrate on which the light emitting layer is formed is transferred into a vacuum vapor deposition apparatus, exhausted until the degree of vacuum in the apparatus becomes 2.0 × 10 -4 Pa or less, and then an organic compound having the structure shown below (E1). ) Was controlled in the range of 0.9 to 1.0 Å / sec by a vacuum vapor deposition method, and laminated on the
次に、下記に示す構造を有する有機化合物(E2)を真空蒸着法にて蒸着速度を0.9〜1.9Å/秒の範囲で制御し、正孔阻止層6の上に積層させ、膜厚20nmの電子輸送層7を得た。
Next, the organic compound (E2) having the structure shown below is laminated on the
ここで、電子輸送層7までの蒸着を行った素子を別の真空蒸着装置に移し、陰極蒸着用のマスクとして2mm幅のストライプ状シャドーマスクを、陽極2のITOストライプとは直交するように素子に密着させ、装置内の真空度が3.1x10−4Pa以下になるまで排気した。
電子注入層8として、先ずフッ化リチウム(LiF)を、モリブデンボートを用いて、蒸着速度0.1Å/秒で制御し、0.5nmの膜厚で電子輸送層7の上に成膜した。次に、陰極9としてアルミニウムを同様にモリブデンボートにより加熱して、蒸着速度1.1〜8.8Å/秒の範囲で制御して膜厚80nmのアルミニウム層を形成した。以上の2層の蒸着時の基板温度は室温に保持した。
引き続き、素子が保管中に大気中の水分等で劣化することを防ぐため、以下に記載の方法で封止処理を行った。
窒素グローブボックス中で、23mm×23mmサイズのガラス板の外周部に、約1mmの幅で光硬化性樹脂(スリーボンドファインケミカル株式会社製30Y‐437)を塗布し、中央部に水分ゲッターシート(ダイニック株式会社製)を設置した。この上に、陰極形成を終了した基板を、蒸着された面が乾燥剤シートと対向するように貼り合わせた。その後、光硬化性樹脂が塗布された領域のみに紫外光を照射し、樹脂を硬化させた。
以上の様にして、2mm×2mmのサイズの発光面積部分を有する有機電界発光素子が得られた。この素子の特性を表1に示す。
Here, the element that has been vapor-deposited up to the
As the
Subsequently, in order to prevent the device from being deteriorated by moisture in the atmosphere during storage, the sealing treatment was carried out by the method described below.
In the nitrogen glove box, a photocurable resin (30Y-437 manufactured by ThreeBond Fine Chemical Co., Ltd.) is applied to the outer periphery of a 23 mm x 23 mm size glass plate with a width of about 1 mm, and a moisture getter sheet (Dynic Co., Ltd.) is applied to the center. (Made by company) was installed. On this, the substrate for which the cathode formation was completed was bonded so that the vapor-deposited surface faced the desiccant sheet. Then, only the region coated with the photocurable resin was irradiated with ultraviolet light to cure the resin.
As described above, an organic electroluminescent device having a light emitting area portion having a size of 2 mm × 2 mm was obtained. The characteristics of this device are shown in Table 1.
(比較例1)
正孔輸送層4を、下記に示す構造式で示される(P3)を含有する正孔輸送層形成用塗布液を調製し、下記の条件で正孔注入層3上にスピンコートにより成膜、加熱して膜厚19nmの正孔輸送層を形成したほかは、実施例1と同様にして有機電界発光素子を作製した。得られた素子の特性を表9に示す。
(Comparative Example 1)
A coating liquid for forming a hole transport layer containing (P3) represented by the structural formula shown below was prepared for the
<正孔輸送層形成用塗布液>
溶媒 シクロヘキシルベンゼン
塗布液濃度 1.5重量%
<正孔輸送層4の成膜条件>
スピナ回転数 1850rpm
スピナ回転時間 120秒
スピンコート雰囲気 窒素中
加熱条件 窒素中 230℃ 1時間
<Coating liquid for forming hole transport layer>
Solvent Cyclohexylbenzene Coating solution concentration 1.5% by weight
<Conditions for forming the
Spinner speed 1850 rpm
Spinner rotation time 120 seconds Spin coating atmosphere In nitrogen Heating conditions In nitrogen 230 °
表9から明らかなように、本発明の重合体を使用した有機電界発光素子は電圧が低い。 As is clear from Table 9, the voltage of the organic electroluminescent device using the polymer of the present invention is low.
(実施例2)
正孔輸送層4を、下記に示す構造式で示される重合体2(P4)を含有する正孔輸送層形成用塗布液を調製し、下記の条件で正孔注入層3上にスピンコートにより成膜、加熱して膜厚20nmの正孔輸送層を形成した。
(Example 2)
A coating liquid for forming a hole transport layer containing the polymer 2 (P4) represented by the structural formula shown below was prepared for the
<正孔輸送層形成用塗布液>
溶媒 シクロヘキシルベンゼン
塗布液濃度 1.5重量%
<正孔輸送層4の成膜条件>
スピナ回転数 3000rpm
スピナ回転時間 120秒
スピンコート雰囲気 窒素中
加熱条件 窒素中 230℃ 1時間
発光層5を、以下の構造式に示す、化合物(H3)および(D2)を含有する発光層形成用塗布液を調製し、下記の条件でスピンコートにより成膜を行い、加熱することで膜厚41nmの発光層を正孔輸送層4上に形成した。
ほかは、実施例1と同様にして有機電界発光素子を作製した。得られた素子の特性を表10に示す。
<Coating liquid for forming hole transport layer>
Solvent Cyclohexylbenzene Coating solution concentration 1.5% by weight
<Conditions for forming the
Spinner speed 3000 rpm
Spinner rotation time 120 seconds Spin coating atmosphere In nitrogen Heating conditions In nitrogen 230 ° C. 1 hour A coating solution for forming a light emitting layer containing the compounds (H3) and (D2) represented by the following structural formula was prepared for the
Other than that, an organic electroluminescent device was produced in the same manner as in Example 1. The characteristics of the obtained device are shown in Table 10.
<発光層形成用塗布液>
溶媒 シクロヘキシルベンゼン
塗布液濃度 H3:3.5重量%
D2:0.35重量%
<発光層5の成膜条件>
スピナ回転数 1850rpm
スピナ回転時間 120秒
スピンコート雰囲気 窒素中
加熱条件 窒素中 130℃ 10分
<Coating liquid for forming a light emitting layer>
Solvent Cyclohexylbenzene Coating liquid concentration H3: 3.5% by weight
D2: 0.35% by weight
<Conditions for film formation of light emitting
Spinner speed 1850 rpm
Spinner rotation time 120 seconds Spin coating atmosphere In nitrogen Heating conditions In nitrogen 130 ° C 10 minutes
(比較例2)
正孔輸送層4を、構造式(P3)の化合物を含有する正孔輸送層形成用塗布液を比較例1と同様に成膜、加熱して膜厚19nmの正孔輸送層を形成したほかは、実施例2と同様にして有機電界発光素子を作製した。得られた素子の特性を表10に示す。
(Comparative Example 2)
The
(比較例3)
正孔輸送層4を、下記に示す構造式で示される(P5)を含有する正孔輸送層形成用塗布液を調製し、下記の条件で正孔注入層3上にスピンコートにより成膜、加熱して膜厚20nmの正孔輸送層を形成したほかは、実施例2と同様にして有機電界発光素子を作製した。得られた素子の特性を表10に示す。
(Comparative Example 3)
A coating liquid for forming a hole transport layer containing (P5) represented by the structural formula shown below was prepared for the
<正孔輸送層形成用塗布液>
溶媒 シクロヘキシルベンゼン
塗布液濃度 1.5重量%
<正孔輸送層4の成膜条件>
スピナ回転数 1850rpm
スピナ回転時間 120秒
スピンコート雰囲気 窒素中
加熱条件 窒素中 230℃ 1時間
<Coating liquid for forming hole transport layer>
Solvent Cyclohexylbenzene Coating solution concentration 1.5% by weight
<Conditions for forming the
Spinner speed 1850 rpm
Spinner rotation time 120 seconds Spin coating atmosphere In nitrogen Heating conditions In nitrogen 230 °
表10から明らかなように、本発明の重合体を使用した有機電界発光素子は電圧が低く、高効率である。 As is clear from Table 10, the organic electroluminescent device using the polymer of the present invention has a low voltage and high efficiency.
<正孔移動度の測定>
(実施例3)
Time of Flight(TOF)法を用いて、日本国特開2014−51667号公報に記載された方法と同様にして、重合体3(P6)の正孔移動度を測定した。
<Measurement of hole mobility>
(Example 3)
The hole mobility of the polymer 3 (P6) was measured using the Time of Flight (TOF) method in the same manner as described in Japanese Patent Application Laid-Open No. 2014-51667.
まず、ガラス基板上に、ITO透明導電膜(ITOストライプ)を70nmの厚さに堆積した基板(ジオマテック社製)に対して、界面活性剤水溶液による超音波洗浄、超純水による水洗、超純水による超音波洗浄、超純水による水洗の順で洗浄後、圧縮空気で乾燥させた後、紫外線オゾン洗浄を施した。
トルエンとシリコーンオイル(信越シリコーン社製:KF−96)を混合させた溶媒に、(P6)を10質量%の濃度で溶解させた溶液を作製し、この洗浄した基板上にスピンコート法にて成膜した。なお、成膜は全て窒素雰囲気中で行った。以上により、膜厚2μmの目的ポリマー1の膜を得た。次に,真空蒸着装置の真空チャンバーへサンプルを搬送した。陰極蒸着用のマスクとして2mm幅のストライプ状シャドーマスクを、ITOストライプと直交するように素子に密着させて設置した。その後、装置内を真空度が8.0×10−4Pa以下になるまで排気した後、アルミニウムをモリブデンボートを用いて加熱することにより、サンプル上に厚さ80nmの電極を形成した。なお、アルミニウムの成膜中は、チャンバー内の真空度を2.0×10−3Pa以下、かつ蒸着速度0.6〜10.0Å/秒に保った。
このサンプルについて、ITO膜が陽極、アルミニウム電極が陰極となるように電界強度をかけた状態で、スペクトラフィジクス社製「VSL−337ND−S(窒素レーザー)」(励起波長337nm、パルス幅<4ns)を用いて過渡光電流の測定を行った。なお、光照射エネルギーは反射型のNDフィルターで10μJに1パルス当たりの光量を調整し、ITO電極側から照射した。過渡光電流波形はオシロスコープ(テクトロニクス社製「TDS2022」)を用いて測定し、屈曲点から電荷移動度を算出した。この測定は、電界強度160kV/cmを印加した状態で行った。
正孔移動度の算出結果は、後掲の構造式(P7)の化合物の正孔移動度の算出結果を「1.0」としたときの相対値(規格化正孔移動度)で示した。結果を表11に示す。
First, on a glass substrate on which an ITO transparent conductive film (ITO stripe) is deposited to a thickness of 70 nm (manufactured by Geomatec), ultrasonic cleaning with an aqueous surfactant solution, water washing with ultrapure water, and ultrapure water are performed. After cleaning in the order of ultrasonic cleaning with water and water washing with ultrapure water, the mixture was dried with compressed air, and then subjected to ultraviolet ozone cleaning.
A solution in which (P6) was dissolved in a solvent obtained by mixing toluene and silicone oil (manufactured by Shinetsu Silicone Co., Ltd .: KF-96) at a concentration of 10% by mass was prepared, and a spin coating method was applied on the washed substrate. A film was formed. All film formation was performed in a nitrogen atmosphere. From the above, a film of the
For this sample, "VSL-337ND-S (nitrogen laser)" manufactured by Spectraphysics Co., Ltd. (excitation wavelength 337 nm, pulse width <4 ns) with the electric field strength applied so that the ITO film serves as the anode and the aluminum electrode serves as the cathode. ) Was used to measure the transient light current. The light irradiation energy was adjusted to 10 μJ with a reflective ND filter in the amount of light per pulse, and irradiated from the ITO electrode side. The transient photocurrent waveform was measured using an oscilloscope (“TDS2022” manufactured by Tektronix), and the charge mobility was calculated from the bending point. This measurement was performed with an electric field strength of 160 kV / cm applied.
The hole mobility calculation result is shown as a relative value (normalized hole mobility) when the hole mobility calculation result of the compound of the structural formula (P7) described later is set to “1.0”. .. The results are shown in Table 11.
(比較例4)
構造式(P6)の化合物を、構造式(P7)の化合物に変更したこと以外は、実施例3と同様にして、(P7)の測定を行い、算出された正孔移動度を1.0とした。
(Comparative Example 4)
The measurement of (P7) was carried out in the same manner as in Example 3 except that the compound of the structural formula (P6) was changed to the compound of the structural formula (P7), and the calculated hole mobility was 1.0. And said.
表11から明らかなように、本発明の重合体は正孔移動度が大きい。 As is clear from Table 11, the polymer of the present invention has a high hole mobility.
本発明を詳細にまた特定の実施態様を参照して説明したが、本発明の精神と範囲を逸脱することなく様々な変更や修正を加えることができることは当業者にとって明らかである。本出願は2013年10月4日出願の日本特許出願(特願2013−209111)、及び2014年1月28日出願の日本特許出願(特願2014−013358)に基づくものであり、その内容はここに参照として取り込まれる。 Although the present invention has been described in detail and with reference to specific embodiments, it will be apparent to those skilled in the art that various changes and modifications can be made without departing from the spirit and scope of the invention. This application is based on a Japanese patent application filed on October 4, 2013 (Japanese Patent Application No. 2013-209111) and a Japanese patent application filed on January 28, 2014 (Japanese Patent Application No. 2014-0133358). It is taken here as a reference.
1.基板
2.陽極
3.正孔注入層
4.正孔輸送層
5.発光層
6.正孔阻止層
7.電子輸送層
8.電子注入層
9.陰極
1. 1.
Claims (3)
前記製造方法は、前記正孔輸送層を、重合体及び溶媒を含む組成物を湿式成膜することによって形成する工程を含み、
前記製造方法は、前記正孔輸送層を放射線でパターン様に露光し、露光部と非露光部とをもたらし、前記非露光部を除去し、前記正孔輸送層のパターンを形成する工程を含まず、
前記重合体は、2種以上の下記式(1)で表される繰り返し単位からなり、
前記重合体は、少なくとも1種の繰り返し単位には架橋性基を含み、少なくとも1種の繰り返し単位には架橋性基を含まず、
前記架橋性基の数は、前記重合体の分子量1000あたり3.0個以下である、
有機電界発光素子の製造方法。
Ar3は、置換基を有していても良い6員環の単環若しくは2〜5縮合環の2価の芳香族炭化水素基、又は置換基を有していても良い5若しくは6員環の単環若しくは2〜4縮合環の2価の芳香族複素環基を表し、
nは4以上の整数を表す。
前記芳香族炭化水素基及び芳香族複素環基は、直接又は連結基を介して、複数個連結したものでも良い。) A method for manufacturing an organic electroluminescent device having an anode, a hole injection layer, a hole transport layer, a light emitting layer, and a cathode in this order on a substrate.
The production method includes a step of forming the hole transport layer by wet-forming a composition containing a polymer and a solvent.
The manufacturing method includes a step of exposing the hole transport layer in a pattern with radiation to provide an exposed portion and a non-exposed portion, removing the non-exposed portion, and forming a pattern of the hole transport layer. Zu,
The polymer is composed of two or more kinds of repeating units represented by the following formula (1).
In the polymer, at least one repeating unit contains a crosslinkable group, and at least one repeating unit does not contain a crosslinkable group.
The number of crosslinkable groups is 3.0 or less per 1000 molecular weight of the polymer.
A method for manufacturing an organic electroluminescent device.
Ar 3 is a 6-membered monocyclic ring or a 2-5 condensed ring divalent aromatic hydrocarbon group which may have a substituent, or a 5- or 6-membered ring which may have a substituent. It represents a divalent aromatic heterocyclic group of single ring or 2 to 4 condensed rings,
n represents an integer of 4 or more.
A plurality of the aromatic hydrocarbon groups and aromatic heterocyclic groups may be linked directly or via a linking group. )
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013209111 | 2013-10-04 | ||
| JP2013209111 | 2013-10-04 | ||
| JP2014013358 | 2014-01-28 | ||
| JP2014013358 | 2014-01-28 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015540561A Division JP6565678B2 (en) | 2013-10-04 | 2014-10-02 | Polymer, composition for organic electroluminescence device, organic electroluminescence device, organic EL display device and organic EL lighting |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2019218550A JP2019218550A (en) | 2019-12-26 |
| JP6879342B2 true JP6879342B2 (en) | 2021-06-02 |
Family
ID=52778816
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015540561A Active JP6565678B2 (en) | 2013-10-04 | 2014-10-02 | Polymer, composition for organic electroluminescence device, organic electroluminescence device, organic EL display device and organic EL lighting |
| JP2019141363A Active JP6879342B2 (en) | 2013-10-04 | 2019-07-31 | Polymers, compositions for organic electroluminescent devices, organic electroluminescent devices, organic EL display devices and organic EL lighting |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015540561A Active JP6565678B2 (en) | 2013-10-04 | 2014-10-02 | Polymer, composition for organic electroluminescence device, organic electroluminescence device, organic EL display device and organic EL lighting |
Country Status (5)
| Country | Link |
|---|---|
| JP (2) | JP6565678B2 (en) |
| KR (1) | KR102157997B1 (en) |
| CN (2) | CN105683255B (en) |
| TW (1) | TWI641630B (en) |
| WO (1) | WO2015050232A1 (en) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3766919B1 (en) * | 2016-04-20 | 2024-02-21 | JSR Corporation | Polymer, composition, molded article, cured product and laminate |
| JP6996240B2 (en) * | 2017-11-10 | 2022-01-17 | 東ソー株式会社 | Arylamine polymers and charge transport materials |
| WO2019177175A1 (en) * | 2018-03-16 | 2019-09-19 | 三菱ケミカル株式会社 | Polymer, composition for organic electroluminescent element, organic electroluminescent element, organic el display device, organic el lighting, and manufacturing method for organic electroluminescent element |
| KR102561759B1 (en) * | 2018-09-28 | 2023-07-28 | 주식회사 엘지화학 | Novel polymer and organic light emitting device comprising the same |
| KR102549459B1 (en) * | 2018-12-20 | 2023-06-28 | 주식회사 엘지화학 | Novel polymer and organic light emitting device comprising the same |
| KR20210100250A (en) | 2020-02-05 | 2021-08-17 | 삼성디스플레이 주식회사 | Composition with polymer, interlayer prepared from the composition and device comprising the same |
| CN112679471B (en) * | 2020-12-25 | 2022-03-29 | 华南理工大学 | Method for separating halogenated impurities in organic light-emitting material |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5246386B2 (en) | 1973-01-17 | 1977-11-24 | ||
| US5352906A (en) * | 1993-01-29 | 1994-10-04 | Iowa State University Research Foundation, Inc. | Poly (p-phenyleneneacetylene) light-emitting diodes |
| JP2009043896A (en) * | 2007-08-08 | 2009-02-26 | Canon Inc | Organic light-emitting element and display |
| US8063399B2 (en) * | 2007-11-19 | 2011-11-22 | E. I. Du Pont De Nemours And Company | Electroactive materials |
| WO2009102027A1 (en) * | 2008-02-15 | 2009-08-20 | Mitsubishi Chemical Corporation | Conjugated polymer, insolubilized polymer, organic electroluminescent device material, composition for organic electroluminescent device, method for producing polymer, organic electroluminescent device, organic el display, and organic el illuminator |
| EP2272894B1 (en) | 2008-04-02 | 2016-07-06 | Mitsubishi Chemical Corporation | Polymer compound, reticulated polymer compound produced by crosslinking the polymer compound, composition for organic electroluminescent element, organic electroluminescent element, organic el display, and organic el lighting |
| JP5491796B2 (en) * | 2008-08-11 | 2014-05-14 | 三菱化学株式会社 | Charge transporting polymer, composition for organic electroluminescent device, organic electroluminescent device, organic EL display and organic EL lighting |
| WO2010065700A2 (en) * | 2008-12-04 | 2010-06-10 | E. I. Du Pont De Nemours And Company | Electroactive materials |
| WO2011078387A1 (en) | 2009-12-25 | 2011-06-30 | 住友化学株式会社 | Composition and light emitting element using the composition |
| EP2530100B1 (en) | 2010-01-28 | 2015-10-21 | Sumitomo Chemical Co., Ltd | Polymer compound and light-emitting device using same |
| TW201200975A (en) * | 2010-06-17 | 2012-01-01 | Du Pont | Process and materials for making contained layers and devices made with same |
| TW201204687A (en) * | 2010-06-17 | 2012-02-01 | Du Pont | Electroactive materials |
| WO2012087977A1 (en) * | 2010-12-20 | 2012-06-28 | E. I. Du Pont De Nemours And Company | Process and materials for making contained layers and devices made with same |
-
2014
- 2014-10-02 WO PCT/JP2014/076459 patent/WO2015050232A1/en active Application Filing
- 2014-10-02 CN CN201480054297.8A patent/CN105683255B/en active Active
- 2014-10-02 KR KR1020167008575A patent/KR102157997B1/en active IP Right Grant
- 2014-10-02 CN CN201810377001.6A patent/CN108530624B/en active Active
- 2014-10-02 JP JP2015540561A patent/JP6565678B2/en active Active
- 2014-10-03 TW TW103134732A patent/TWI641630B/en active
-
2019
- 2019-07-31 JP JP2019141363A patent/JP6879342B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN105683255A (en) | 2016-06-15 |
| JP6565678B2 (en) | 2019-08-28 |
| CN105683255B (en) | 2018-05-29 |
| WO2015050232A1 (en) | 2015-04-09 |
| KR20160067847A (en) | 2016-06-14 |
| CN108530624A (en) | 2018-09-14 |
| TW201518340A (en) | 2015-05-16 |
| JPWO2015050232A1 (en) | 2017-03-09 |
| CN108530624B (en) | 2021-10-26 |
| TWI641630B (en) | 2018-11-21 |
| JP2019218550A (en) | 2019-12-26 |
| KR102157997B1 (en) | 2020-09-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6791311B2 (en) | Polymers, compositions for organic electroluminescent devices, organic electroluminescent devices, organic EL display devices and organic EL lighting | |
| JP6879342B2 (en) | Polymers, compositions for organic electroluminescent devices, organic electroluminescent devices, organic EL display devices and organic EL lighting | |
| JP5810417B2 (en) | Iridium complex compound, composition containing the compound, organic electroluminescent element, display device and lighting device | |
| JP5793878B2 (en) | Polymer, organic electroluminescent element material, composition for organic electroluminescent element, organic electroluminescent element, display device and lighting device | |
| JP5672858B2 (en) | Charge transport material, composition for charge transport film, organic electroluminescence device, organic EL display and organic EL lighting | |
| JP6442977B2 (en) | Polymer, composition for organic electroluminescence device, organic electroluminescence device, organic EL display device and organic EL lighting | |
| JP6866576B2 (en) | Polymers, compositions for organic electroluminescent devices, organic electroluminescent devices, organic EL display devices and organic EL lighting | |
| JPWO2019177175A1 (en) | Polymers, compositions for organic electroluminescent devices, organic electroluminescent devices, organic EL display devices, organic EL lighting, and methods for manufacturing organic electroluminescent devices. | |
| JP6593432B2 (en) | Polymer, composition for organic electroluminescence device, organic electroluminescence device, organic EL display device and organic EL lighting | |
| JP5392438B1 (en) | Polymer and organic electroluminescent device | |
| JP5573697B2 (en) | Polymer, organic electroluminescent element material, composition for organic electroluminescent element, organic electroluminescent element, organic EL display device, and organic EL lighting | |
| JP5609726B2 (en) | Polymer, organic electroluminescent element material, composition for organic electroluminescent element, organic electroluminescent element, organic EL display device, and organic EL lighting | |
| JP6922232B2 (en) | Polymers, compositions for organic electroluminescent devices, methods for manufacturing organic electroluminescent devices, methods for manufacturing organic EL display devices, and methods for manufacturing organic EL lighting. | |
| JP2021061316A (en) | Composition for organic electroluminescent element, organic electroluminescent element, display device, and lighting device | |
| JP2013181072A (en) | Catalyst for producing charge transfer material for organic el | |
| JP2021127325A (en) | Aromatic diamine derivative |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190827 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200915 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20201111 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210112 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210330 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210412 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 6879342 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |