JP6579938B2 - Photochromic composition, laminate comprising the composition, and article using the laminate - Google Patents
Photochromic composition, laminate comprising the composition, and article using the laminate Download PDFInfo
- Publication number
- JP6579938B2 JP6579938B2 JP2015244512A JP2015244512A JP6579938B2 JP 6579938 B2 JP6579938 B2 JP 6579938B2 JP 2015244512 A JP2015244512 A JP 2015244512A JP 2015244512 A JP2015244512 A JP 2015244512A JP 6579938 B2 JP6579938 B2 JP 6579938B2
- Authority
- JP
- Japan
- Prior art keywords
- component
- group
- photochromic
- compound
- resin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- JUGXXGMCGUARKQ-UHFFFAOYSA-O C(COCC1)N1c1ccc(C2(c3ccccc3)[OH+]c3c(cccc4)c4c4-c5ccccc5C5(CCCCCCC5)c4c3C=C2)cc1 Chemical compound C(COCC1)N1c1ccc(C2(c3ccccc3)[OH+]c3c(cccc4)c4c4-c5ccccc5C5(CCCCCCC5)c4c3C=C2)cc1 JUGXXGMCGUARKQ-UHFFFAOYSA-O 0.000 description 1
- 0 C*C1C=CC(C(C(C)=*)O)=CC1 Chemical compound C*C1C=CC(C(C(C)=*)O)=CC1 0.000 description 1
Landscapes
- Eyeglasses (AREA)
- Optical Filters (AREA)
- Laminated Bodies (AREA)
- Compositions Of Macromolecular Compounds (AREA)
Description
本発明は、フォトクロミック性接着剤、特にポリカーボネート樹脂製のシート又はフィルムどうしを接合するためのフォトクロミック性接着層として好適に使用できる新規なフォトクロミック組成物に関する。また、本発明は、該フォトクロミック組成物からなる接着層を介して樹脂製シート又はフィルムが互いに接合されてなる積層構造を含む積層体、及び該積層体を用いた物品に関する。 The present invention relates to a novel photochromic composition that can be suitably used as a photochromic adhesive layer, particularly a photochromic adhesive layer for joining sheets or films made of polycarbonate resin. The present invention also relates to a laminate including a laminate structure in which resin sheets or films are bonded to each other through an adhesive layer made of the photochromic composition, and an article using the laminate.
近年米国を中心として、防眩性を有するサングラスなどに、透明で優れた耐衝撃性を有するポリカーボネートを用いたプラスチック基材の需要が急速に高まっている。そして、このようなプラスチック製サングラスにおいては、フォトクロミック色素と組み合わせることによって、周囲の明るさに応じて透過率が変化することにより防眩性を調節できるプラスチック製フォトクロミックサングラスが急速に人気を得ている。このようなサングラスは以下の方法により製造されている。 In recent years, mainly in the United States, the demand for plastic substrates using transparent and excellent impact-resistant polycarbonate for sunglasses having anti-glare properties and the like is rapidly increasing. And in such plastic sunglasses, plastic photochromic sunglasses that can adjust the antiglare property by changing the transmittance according to the surrounding brightness by combining with the photochromic dye are rapidly gaining popularity. . Such sunglasses are manufactured by the following method.
例えば、2枚のプラスチックシートまたはフィルムの間に、防眩性を有する機能層を積層する方法としては、2枚のポリカーボネートシート間にフォトクロミック層を積層する方法が知られている(特許文献1参照)。具体的には、溶媒を含むフォトクロミック塗工液を一方のプラスチックシートに塗布し、それを特定の温度の乾燥器に、特定の速度で通過させることにより乾燥した後、他方のプラスチックシートを接合する方法(積層シートを製造する方法)が示されている。この方法によれば、連続して、平滑性の優れた接着層を有する積層シートを製造することができる。 For example, as a method of laminating a functional layer having antiglare properties between two plastic sheets or films, a method of laminating a photochromic layer between two polycarbonate sheets is known (see Patent Document 1). ). Specifically, a photochromic coating solution containing a solvent is applied to one plastic sheet, dried by passing it through a dryer at a specific temperature at a specific speed, and then the other plastic sheet is joined. A method (method of manufacturing a laminated sheet) is shown. According to this method, a laminated sheet having an adhesive layer with excellent smoothness can be produced continuously.
しかしながら、本発明者等の検討によれば、特許文献1記載の方法によっても積層シートの接着性(プラスチックシート同士の接着性)が十分ではない場合があった。特に、積層シートの2次加工(熱曲げ加工、射出成形)を安定して行うために、軟化点の高い接着性樹脂を使用した場合には、接着性が低下する場合があった。 However, according to the study by the present inventors, the adhesiveness of laminated sheets (adhesiveness between plastic sheets) may not be sufficient even by the method described in Patent Document 1. In particular, when an adhesive resin having a high softening point is used in order to stably perform the secondary processing (thermal bending processing, injection molding) of the laminated sheet, the adhesiveness may be lowered.
上記フォトクロミック層と樹脂製シート又はフィルムとの接着性を向上させる方法として、フォトクロミック接着層として、ポリウレタンウレア樹脂を使用して形成したフォトクロミック性ポリウレタン−ウレア樹脂を用い、該フォトクロミック層と樹脂製シート又はフィルムとを接着層を介して積層させる方法が提案されている(特許文献2参照)。 As a method for improving the adhesion between the photochromic layer and the resin sheet or film, a photochromic polyurethane-urea resin formed using a polyurethane urea resin is used as the photochromic adhesive layer, and the photochromic layer and the resin sheet or A method of laminating a film with an adhesive layer has been proposed (see Patent Document 2).
上記特許文献2記載の方法によって優れた密着性、フォトクロミック特性を示すフォトクロミック積層シートが得られるが、本発明者の検討により、同じ組成のフォトクロミック接着層を用いた場合において、ロット間で該接着層と樹脂製シート又はフィルムとの密着性にバラつきがあり、ポリカーボネートへの接着性が十分でない場合があることが判明した。また、該接着層の耐熱性に課題があることも判明した。
さらに、フォトクロミックサングラスは、その使用状況によって“耐汗性”が求められる(人間の汗が接触しても、その状態変化のないサングラスが求められる)場合があるが、従来の積層シートを使用したサングラスにおいては、ポリカーボネートシート等の剥離が見られ、十分にその要求に応えられるものがなかった。
A photochromic laminated sheet exhibiting excellent adhesion and photochromic properties can be obtained by the method described in Patent Document 2 above. However, when the photochromic adhesive layer having the same composition is used, the adhesive layer can be used between lots. It has been found that there is a variation in the adhesion between the resin and the resin sheet or film, and the adhesion to polycarbonate may not be sufficient. It has also been found that there is a problem with the heat resistance of the adhesive layer.
Furthermore, photochromic sunglasses may require “sweat resistance” depending on their usage (though sunglasses that do not change their state even when they come into contact with human sweat) may be used, but conventional laminated sheets are used. In sunglasses, peeling of a polycarbonate sheet or the like was observed, and there was no one that could fully meet the requirements.
従って、本発明の目的は、第一に、樹脂製シート又はフィルムを接合するときの接着層として使用した場合に、優れた接着性、耐熱性、耐汗性を有し、優れたフォトクロミック特性を発揮するフォトクロミック組成物を提供することである。
また、本発明の第二の目的は、樹脂製シート又はフィルムがフォトクロミック性を有する接着層により接合された積層構造を含んでなる光学物品であって、該積層構造における優れた接着性、並びに優れた耐熱性および優れたフォトクロミック特性を有する積層体を提供することである。
Therefore, the object of the present invention is, first of all, when used as an adhesive layer when joining a resin sheet or film, it has excellent adhesion, heat resistance, sweat resistance, and excellent photochromic properties. It is to provide a photochromic composition that exhibits.
The second object of the present invention is an optical article comprising a laminated structure in which a resin sheet or film is joined by an adhesive layer having photochromic properties, and has excellent adhesiveness in the laminated structure, as well as excellent It is to provide a laminate having excellent heat resistance and excellent photochromic properties.
本発明者等は上記課題を解決すべく、鋭意検討を行った。同じ組成のフォトクロミック接着層を用いた場合において、該接着層と樹脂製シート又は光学フィルムとの密着性にバラつきがある点に着目し、該接着層に用いるポリウレタンウレア樹脂の分析を行ったところ、低分子量と高分子量のポリウレタンウレア樹脂の混合物となっていることを確認した。そこで、ポリウレタンウレア樹脂の耐熱性には、低分子量のポリウレタンウレア樹脂の存在が影響しているものと推測し、検討を進めた結果、低分子量のポリウレタンウレア樹脂を多く含むポリウレタンウレア樹脂を用いた場合に得られるフォトクロミック接着層の耐熱性、及び密着性が低いという知見を得た。 The present inventors have intensively studied to solve the above problems. When using a photochromic adhesive layer of the same composition, paying attention to the fact that there is a variation in the adhesion between the adhesive layer and the resin sheet or optical film, the polyurethane urea resin used in the adhesive layer was analyzed, It was confirmed that this was a mixture of low and high molecular weight polyurethane urea resins. Therefore, it was speculated that the presence of low molecular weight polyurethane urea resin had an influence on the heat resistance of polyurethane urea resin, and as a result of investigation, a polyurethane urea resin containing a large amount of low molecular weight polyurethane urea resin was used. The knowledge that the heat resistance and adhesiveness of the photochromic adhesive layer obtained in this case is low was obtained.
上記の知見を基に、フォトクロミック接着層に用いるポリウレタンウレア樹脂の組成についてさらに検討を進めた結果、多分散度をある一定範囲に制御したポリウレタンウレア樹脂を接着層に用いた場合には、得られる積層体の接着性、耐熱性、耐汗性、フォトクロミック特性およびその耐久性などが優れたものとなることを見出し、本発明を完成するに至った。 Based on the above knowledge, as a result of further investigation on the composition of the polyurethane urea resin used in the photochromic adhesive layer, it can be obtained when a polyurethane urea resin whose polydispersity is controlled within a certain range is used for the adhesive layer. The present inventors have found that the laminate has excellent adhesiveness, heat resistance, sweat resistance, photochromic properties, durability thereof, and the like, and completed the present invention.
即ち、本発明は、(I)多分散度(重量平均分子量/数平均分子量)が、1.6〜2.4の範囲であるポリウレタンウレア樹脂、及び(II)フォトクロミック化合物を含んでなるフォトクロミック組成物である。
また、本発明の別の発明は、互いに対向する2枚の樹脂製シート又はフィルムが請求項1に記載のフォトクロミック組成物からなる接着層を介して接合された積層構造を含む積層体、及び該積層体を用いた遮光窓材、ディスプレイ材料、農業用フィルム、玩具、衣服、及び傘である。
That is, the present invention provides a photochromic composition comprising (I) a polyurethane urea resin having a polydispersity (weight average molecular weight / number average molecular weight) in the range of 1.6 to 2.4, and (II) a photochromic compound. It is a thing.
Another invention of the present invention is a laminate comprising a laminate structure in which two resin sheets or films facing each other are bonded via an adhesive layer comprising the photochromic composition according to claim 1, and the laminate A light shielding window material, a display material, an agricultural film, a toy, clothes, and an umbrella using a laminate.
本発明のフォトクロミック組成物は、多分散度(重量平均分子量/数平均分子量)が、1.6〜2.4の範囲であるポリウレタンウレア樹脂を用いることを特徴としている。該組成物からなる接着層によりポリカーボネート樹脂などからなる樹脂製シート又はフィルムを接合して積層体を製造した場合、得られた積層体は優れた接着性、特に高温における優れた接着性を示し、得られた積層体は、耐汗性も高い。すなわち、人工汗と接触させた後であっても、優れた接着性を示す。このような効果が得られた理由として詳細は不明であるが、本発明者らは、以下の通り推測している。すなわち多分散度(重量平均分子量/数平均分子量)が1.6〜2.4の範囲であることで、低分子量のポリウレタンウレアの含有量を低減でき、耐熱性が安定した点と、低分子量ポリウレタンウレアの影響による物理的な分子間相互作用(ポリマー鎖の分子間での絡み合い)の低下が抑制でき、ポリウレタンウレア樹脂を接着層に用いた際のポリウレタンウレア層内での破壊(凝集破壊)が抑制できたため、密着性が向上したものと推測される。 The photochromic composition of the present invention is characterized by using a polyurethane urea resin having a polydispersity (weight average molecular weight / number average molecular weight) in the range of 1.6 to 2.4. When a laminate is produced by joining a resin sheet or film made of a polycarbonate resin or the like with an adhesive layer made of the composition, the obtained laminate shows excellent adhesiveness, particularly excellent adhesiveness at high temperatures, The obtained laminate has high sweat resistance. That is, excellent adhesion is exhibited even after contact with artificial sweat. Although details are unknown as the reason why such an effect is obtained, the present inventors presume as follows. That is, when the polydispersity (weight average molecular weight / number average molecular weight) is in the range of 1.6 to 2.4, the content of low molecular weight polyurethane urea can be reduced, the heat resistance is stable, and the low molecular weight. Degradation of physical intermolecular interaction (entanglement of polymer chains between molecules) due to the influence of polyurethane urea can be suppressed, and destruction within the polyurethane urea layer (cohesive failure) when polyurethane urea resin is used for the adhesive layer It was presumed that the adhesiveness was improved because of being able to be suppressed.
さらに、本発明の積層体は、太陽光照射時における高い発色濃度、及び太陽光未照射時における高い退色速度を有し、しかも発退色による繰り返し耐久性が高い。従って、本発明の積層体は前述のプラスチックサングラス以外にも、遮光窓材、ディスプレイ材料、農業用フィルム、玩具、衣服、傘等の物品にフォトクロ物性を発現させるための積層体として用いることができる。 Furthermore, the laminate of the present invention has a high color density when irradiated with sunlight, a high fading speed when not irradiated with sunlight, and has high repetition durability due to color fading. Accordingly, the laminate of the present invention can be used as a laminate for developing photochromic properties in articles such as light shielding window materials, display materials, agricultural films, toys, clothes, umbrellas, etc., in addition to the above-mentioned plastic sunglasses. it can.
本発明のフォトクロミック組成物は、(I)多分散度(重量平均分子量/数平均分子量)が、1.6〜2.4の範囲であるポリウレタンウレア樹脂(以下、I成分とも言う。)、及び(II)フォトクロミック化合物(以下、II成分とも言う。)を含んでなることを特徴とする。以下、これらI成分およびII成分について説明する。 The photochromic composition of the present invention comprises (I) a polyurethane urea resin (hereinafter also referred to as “I component”) having a polydispersity (weight average molecular weight / number average molecular weight) in the range of 1.6 to 2.4. (II) A photochromic compound (hereinafter also referred to as II component) is included. Hereinafter, these I component and II component are demonstrated.
<I成分:多分散度(重量平均分子量/数平均分子量)が、1.6〜2.4の範囲であるポリウレタンウレア樹脂>
本発明のフォトクロミック組成物において、多分散度(重量平均分子量/数平均分子量)が、1.6〜2.4の範囲であるポリウレタンウレア樹脂(以下、単に「ポリウレタンウレア樹脂」とも言う)を用いることが特徴である。上記ポリウレタンウレア樹脂は、分子鎖中にウレア結合(−R−NH−CO−NH−)を有するポリウレタン樹脂である。このように狭い範囲の多分散度を有することによって、本発明のポリウレタンウレア樹脂は、良好な接着力、耐熱性、及び耐汗性を有する。なお、多分散度が低いほど、すなわち多分散度が1.0に近いほど、本発明の効果が発現する傾向にあるが、多分散度が1.6未満であるポリウレタンウレア樹脂は、工業的製造方法においては実質困難だと考えられ、多分散度が2.4を超える場合には、低分子量のポリウレタンウレア樹脂の影響により、軟化開始温度が低温となるため、多分散度が狭い樹脂と比較して、耐熱性に劣り、高温下での密着性が低下する。また、高分子量ポリウレタンウレア樹脂の影響により、多分散度が狭い樹脂と比較して、有機溶剤に溶解した際の粘度が著しく上昇し、塗工が困難となる。良好な接着力、耐熱性、及び塗工性の観点から、本発明のポリウレタンウレア樹脂の多分散度は、1.8〜2.2の範囲であることがより好ましい。
<I component: Polyurethane urea resin whose polydispersity (weight average molecular weight / number average molecular weight) is in the range of 1.6 to 2.4>
In the photochromic composition of the present invention, a polyurethane urea resin (hereinafter also simply referred to as “polyurethane urea resin”) having a polydispersity (weight average molecular weight / number average molecular weight) in the range of 1.6 to 2.4 is used. It is a feature. The polyurethane urea resin is a polyurethane resin having a urea bond (—R—NH—CO—NH—) in the molecular chain. By having such a narrow range of polydispersity, the polyurethane urea resin of the present invention has good adhesion, heat resistance, and sweat resistance. Note that the lower the polydispersity, that is, the closer the polydispersity is to 1.0, the more the effect of the present invention tends to be exhibited. However, the polyurethane urea resin having a polydispersity of less than 1.6 is industrially It is considered that it is substantially difficult in the production method, and when the polydispersity exceeds 2.4, the softening start temperature becomes low due to the influence of the low molecular weight polyurethane urea resin, so that the polydispersity is narrow. Compared with heat resistance, the adhesiveness under high temperature falls. Further, due to the influence of the high molecular weight polyurethane urea resin, the viscosity when dissolved in an organic solvent is remarkably increased as compared with a resin having a narrow polydispersity, and coating becomes difficult. From the viewpoint of good adhesive strength, heat resistance, and coatability, the polydispersity of the polyurethane urea resin of the present invention is more preferably in the range of 1.8 to 2.2.
また、本発明のポリウレタンウレア樹脂の分子量は、多分散度(重量平均分子量/数平均分子量)が上記範囲を満足するものであれば特に制限されるものではないが、接着力、耐熱性、及び耐汗性の観点から、数平均分子量が5千〜10万、特に8千〜5万であり、1万〜4万であることが最も好ましい。 The molecular weight of the polyurethane urea resin of the present invention is not particularly limited as long as the polydispersity (weight average molecular weight / number average molecular weight) satisfies the above range, but the adhesive strength, heat resistance, and From the viewpoint of sweat resistance, the number average molecular weight is 5,000 to 100,000, particularly 8,000 to 50,000, and most preferably 10,000 to 40,000.
なお、上記ポリウレタンウレア樹脂の数平均分子量、及び重量平均分子量は、ポリエチレンオキシド換算によるゲル・パーミエイション・クロマトグラフ(GPC)を用いて、カラム:Shodex KD−806M(昭和電工株式会社製)を2本直列接続、溶離液:LiBr(10mmol/L)/DMF溶液、流速:1ml/min、検出器:RI検出器、ポリウレタンウレア樹脂試料溶液:1.0%ジメチルホルムアミド(DMF)溶液の条件にて測定し、日本ウォーターズ株式会社製GPC解析ソフト『Empower Personal GPC Option』を用いて算出した値である。また、多分散度は、重量平均分子量/数平均分子量で算出される値であり、上記方法によって求められた数平均分子量、及び重量平均分子量より算出される値である。 The number average molecular weight and the weight average molecular weight of the polyurethane urea resin are as follows. Column: Shodex KD-806M (manufactured by Showa Denko KK) is used for gel permeation chromatography (GPC) in terms of polyethylene oxide. Two in series, eluent: LiBr (10 mmol / L) / DMF solution, flow rate: 1 ml / min, detector: RI detector, polyurethane urea resin sample solution: 1.0% dimethylformamide (DMF) solution It is a value calculated using the GPC analysis software “Empower Personal GPC Option” manufactured by Japan Waters Corporation. The polydispersity is a value calculated by weight average molecular weight / number average molecular weight, and is a value calculated from the number average molecular weight and the weight average molecular weight determined by the above method.
本発明のフォトクロミック組成物におけるI成分は、多分散度(重量平均分子量/数平均分子量)が上記の範囲を満たすポリウレタンウレア樹脂であれば特に制限されるものではないが、接着性、耐熱性、及び耐汗性の観点から、
(A)分子末端にイソシアネート基を有するウレタンプレポリマーと、
(B)分子内に2つ以上のアミノ基を有するポリアミン化合物と、
を反応して得られるものであることが好ましく、さらに、
(C)分子内にイソシアネート基と反応しうる基を1つ有する化合物と、
を反応して得られるものであることが好ましい。このようなポリウレタンウレア樹脂においては、原料である(B)成分としてポリアミン化合物を使用することに起因して、分子内にウレア結合が導入される。以下、これらの成分について説明する。
The component I in the photochromic composition of the present invention is not particularly limited as long as the polydispersity (weight average molecular weight / number average molecular weight) is a polyurethane urea resin satisfying the above range, but the adhesiveness, heat resistance, And from the viewpoint of sweat resistance,
(A) a urethane prepolymer having an isocyanate group at the molecular end;
(B) a polyamine compound having two or more amino groups in the molecule;
Is preferably obtained by reacting
(C) a compound having one group capable of reacting with an isocyanate group in the molecule;
It is preferable that it is obtained by reacting. In such a polyurethane urea resin, a urea bond is introduced into the molecule due to the use of a polyamine compound as the raw material (B) component. Hereinafter, these components will be described.
<A成分:分子末端にイソシアネート基を有するウレタンプレポリマー>
上記ポリウレタンウレア樹脂の構成成分である分子末端にイソシアネート基を有するウレタンプレポリマー(A成分)としては、公知のウレタンプレポリマーを用いることが可能である。中でも、
(A1)ポリエーテルポリオール、ポリエステルポリオール、ポリカーボネートポリオール、及びポリカプロラクトンポリオールなどの少なくとも2つ以上の水酸基を有するポリオールよりなる群から選ばれる少なくとも1種のポリオール化合物と、
(A2)分子内に2つのイソシアネート基を有するジイソシアネート化合物と、
を反応して得られるものであることが好ましい。
<Component A: Urethane prepolymer having an isocyanate group at the molecular end>
As the urethane prepolymer (component A) having an isocyanate group at the molecular terminal, which is a constituent component of the polyurethane urea resin, a known urethane prepolymer can be used. Above all,
(A1) at least one polyol compound selected from the group consisting of polyols having at least two or more hydroxyl groups such as polyether polyol, polyester polyol, polycarbonate polyol, and polycaprolactone polyol;
(A2) a diisocyanate compound having two isocyanate groups in the molecule;
It is preferable that it is obtained by reacting.
<A1成分:ポリエーテルポリオール、ポリエステルポリオール、ポリカーボネートポリオール、及びポリカプロラクトンポリオールなどの少なくとも2つ以上の水酸基を有するポリオールよりなる群から選ばれる少なくとも1種のポリオール化合物>
上記ポリオール化合物(A1成分)としては、生成するポリウレタンウレア樹脂(I成分)が高架橋体になり過ぎないという理由から分子中に含まれる水酸基数が2〜6であることが好ましく、有機溶剤への溶解性を考慮すれば、分子中に含まれる水酸基数は2〜3であることがより好ましい。また、前述のポリエーテルポリオール、ポリエステルポリオール、ポリカーボネートポリオール、及びポリカプロラクトンポリオールなどのポリオール化合物は、単独で使用しても良く、2種類以上を併用しても構わないが、耐熱性、接着性、耐候性、耐加水分解性などの観点から、特にポリカーボネートポリオール、及びポリカプロラクトンポリオールを使用することが好ましい。以下、A1成分として使用される各種化合物について詳しく説明する。
<A1 component: at least one polyol compound selected from the group consisting of polyols having at least two hydroxyl groups such as polyether polyol, polyester polyol, polycarbonate polyol, and polycaprolactone polyol>
As said polyol compound (A1 component), it is preferable that the number of hydroxyl groups contained in a molecule | numerator is 2-6 from the reason that the polyurethane urea resin (I component) to produce | generate does not become a highly crosslinked body, and to an organic solvent. In consideration of solubility, the number of hydroxyl groups contained in the molecule is more preferably 2 to 3. In addition, polyol compounds such as the above-described polyether polyol, polyester polyol, polycarbonate polyol, and polycaprolactone polyol may be used alone or in combination of two or more, but heat resistance, adhesiveness, From the viewpoints of weather resistance, hydrolysis resistance and the like, it is particularly preferable to use polycarbonate polyol and polycaprolactone polyol. Hereinafter, various compounds used as the A1 component will be described in detail.
<ポリカーボネートポリオール>
A1成分として使用されるポリカーボネートポリオールとしては、エチレングリコール、1,2−プロパンジオール、1,3−プロパンジオール、2−メチル−1,3−プロパンジオール、1,2−ブタンジオール、1,3−ブタンジオール、1,4−ブタンジオール、1,5−ペンタンジオール、1,6−ヘキサンジオール、1,8−オクタンジオール、1,9−ノナンジオール、1,10−デカンジオール、3−メチル−1,5−ペンタンジオール、2−エチル−4−ブチル−1,3−プロパンジオール、ジエチレングリコール、ジプロピレングリコール、ネオペンチルグリコール、シクロヘキサン−1,4−ジオール、シクロヘキサン−1,4−ジメタノール、ダイマー酸ジオール、ビスフェノールA のエチレンオキサイドやプロピレンオキサイド付加物、ビス(β−ヒドロキシエチル)ベンゼン、キシリレングリコール、グリセリン、トリメチロールプロパン、ペンタエリスリトール等の低分子ポリオール類の1種類以上のホスゲン化より得られるポリカーボネートポリオール、或いはエチレンカーボネート、ジエチルカーボネート、及びジフェニルカーボネート等によるエステル交換法により得られるポリカーボネートポリオール等を挙げることができる。この低分子ポリオール類なかでも、最終的に得られるポリウレタンウレア樹脂(I成分)の接着性、及び耐熱性の観点から、直鎖のアルキル鎖を有する低分子ポリオール類がより好ましく、側鎖にアルキル基を有する低分子ポリオールから合成されたポリカーボネートポリオールは、接着性が低下する傾向が見られる。
<Polycarbonate polyol>
Polycarbonate polyols used as the A1 component include ethylene glycol, 1,2-propanediol, 1,3-propanediol, 2-methyl-1,3-propanediol, 1,2-butanediol, 1,3- Butanediol, 1,4-butanediol, 1,5-pentanediol, 1,6-hexanediol, 1,8-octanediol, 1,9-nonanediol, 1,10-decanediol, 3-methyl-1 , 5-pentanediol, 2-ethyl-4-butyl-1,3-propanediol, diethylene glycol, dipropylene glycol, neopentyl glycol, cyclohexane-1,4-diol, cyclohexane-1,4-dimethanol, dimer acid Diol, bisphenol A ethylene oxide and propylene Oxide polyol, bis (β-hydroxyethyl) benzene, xylylene glycol, glycerin, trimethylolpropane, polycarbonate polyol obtained by phosgenation of one or more kinds of low molecular polyols such as pentaerythritol, ethylene carbonate, diethyl The polycarbonate polyol obtained by the transesterification method with carbonate, diphenyl carbonate, etc. can be mentioned. Among these low molecular polyols, low molecular polyols having a linear alkyl chain are more preferable from the viewpoint of adhesion and heat resistance of the finally obtained polyurethane urea resin (component I), and the side chain has an alkyl group. A polycarbonate polyol synthesized from a low-molecular polyol having a group tends to have poor adhesion.
A1成分としてのポリカーボネートポリオールにおいては、最終的に得られるポリウレタンウレア樹脂(I成分)の耐熱性の観点から、数平均分子量は好ましくは400〜2000、より好ましくは500〜1500、最も好ましくは600〜1200である。 In the polycarbonate polyol as the A1 component, the number average molecular weight is preferably 400 to 2000, more preferably 500 to 1500, and most preferably 600 to 600 from the viewpoint of heat resistance of the finally obtained polyurethane urea resin (component I). 1200.
これらポリカーボネートポリオールは、試薬としてまたは工業的に入手可能であり、市販されているものを例示すれば、旭化成ケミカルズ株式会社製「デュラノール(登録商標)」シリーズ、株式会社クラレ製「クラレポリオール(登録商標)」シリーズ、ダイセル化学工業株式会社製「プラクセル(登録商標)」シリーズ、日本ポリウレタン工業株式会社製「ニッポラン(登録商標)」シリーズ、宇部興産株式会社製「ETERNACOLL(登録商標)」シリーズなどを挙げることができる。 These polycarbonate polyols are available as reagents or industrially, and examples of those that are commercially available include "Duranol (registered trademark)" series manufactured by Asahi Kasei Chemicals Corporation, "Kuraray polyol (registered trademark)" manufactured by Kuraray Co., Ltd. ) "Series," Placcel (registered trademark) "series manufactured by Daicel Chemical Industries, Ltd.," Nipporan (registered trademark) "series manufactured by Nippon Polyurethane Industry Co., Ltd.," ETERNACOLL (registered trademark) "series manufactured by Ube Industries, Ltd. be able to.
<ポリカプロラクトンポリオール>
A1成分として使用されるポリカプロラクトンポリオールとしては、ε−カプロラクトンの開環重合により得られる化合物が使用できる。A1成分としてのポリカプロラクトンポリオールにおいては、ポリカーボネートポリオールにおける場合と同様な理由から、数平均分子量は好ましくは400〜2000、より好ましくは500〜1500、最も好ましくは600〜1200である。
<Polycaprolactone polyol>
As the polycaprolactone polyol used as the A1 component, a compound obtained by ring-opening polymerization of ε-caprolactone can be used. In the polycaprolactone polyol as the A1 component, the number average molecular weight is preferably 400 to 2000, more preferably 500 to 1500, and most preferably 600 to 1200 for the same reason as in the polycarbonate polyol.
このようなポリカプロラクトンポリオールは、試薬としてまたは工業的に入手可能であり、市販されているものを例示すれば、ダイセル化学工業株式会社製「プラクセル(登録商標)」シリーズなどを挙げることができる。 Such polycaprolactone polyol is commercially available as a reagent or industrially. Examples of commercially available products include “Placcel (registered trademark)” series manufactured by Daicel Chemical Industries, Ltd.
<ポリエーテルポリオール>
ポリエーテルポリオールとしては、分子中に活性水素含有基を2個以上有する化合物とアルキレンオキサイドとの反応により得られるポリエーテルポリオール化合物及び該ポリエーテルポリオール化合物の変性体である、ポリマーポリオール、ウレタン変性ポリエーテルポリオール、ポリエーテルエステルコポリマーポリオール等を挙げることが出来る。
<Polyether polyol>
Polyether polyols include polyether polyol compounds obtained by the reaction of a compound having two or more active hydrogen-containing groups in the molecule with an alkylene oxide, and polymer polyols and urethane-modified poly ures that are modified products of the polyether polyol compounds. Examples thereof include ether polyols and polyether ester copolymer polyols.
なお、上記分子中に活性水素含有基を2個以上有する化合物としては、水、エチレングリコール、プロピレングリコール、ブタンジオール、グリセリン、トリメチロールプロパン、ヘキサントリオール、トリエタノールアミン、ジグリセリン、ペンタエリスリトール、トリメチロールプロパン、ヘキサントリオールなどの分子中に水酸基を1個以上有するグリコール、グリセリン等のポリオール化合物が挙げられ、これらは単独で使用しても、2種類以上を混合して使用しても構わない。 The compounds having two or more active hydrogen-containing groups in the molecule include water, ethylene glycol, propylene glycol, butanediol, glycerin, trimethylolpropane, hexanetriol, triethanolamine, diglycerin, pentaerythritol, tritriol. Examples thereof include polyol compounds such as glycol and glycerin having one or more hydroxyl groups in the molecule such as methylolpropane and hexanetriol, and these may be used alone or in admixture of two or more.
また、前記アルキレンオキサイドとしては、エチレンオキサイド、プロピレンオキサイド、テトラヒドロフラン等の環状エーテル化合物が挙げられ、これらは単独で使用しても2種類以上を混合して使用しても構わない。 Moreover, as said alkylene oxide, cyclic ether compounds, such as ethylene oxide, a propylene oxide, and tetrahydrofuran, are mentioned, These may be used individually or may be used in mixture of 2 or more types.
ポリエーテルポリオールにおいては、ポリカーボネートポリオールにおける場合と同様な理由から、数平均分子量は好ましくは400〜2000、より好ましくは500〜1500、最も好ましくは600〜1200である。 In the polyether polyol, the number average molecular weight is preferably 400 to 2000, more preferably 500 to 1500, and most preferably 600 to 1200 for the same reason as in the polycarbonate polyol.
このようなポリエーテルポリオールは、試薬としてまたは工業的に入手可能であり、市販されているものを例示すれば、旭硝子株式会社製「エクセノール(登録商標)」シリーズ、「エマルスター(登録商標)」、株式会社ADEKA製「アデカポリエーテル」シリーズなどを挙げることができる。 Such polyether polyols are available as reagents or industrially, and examples of commercially available ones include “Excenol (registered trademark)” series, “Emulster (registered trademark)” manufactured by Asahi Glass Co., Ltd. ADEKA Co., Ltd. “ADEKA Polyether” series and the like can be mentioned.
<ポリエステルポリオール>
ポリエステルポリオールとしては、多価アルコールと多塩基酸との縮合反応により得られるポリエステルポリオールなどを挙げることができる。ここで、前記多価アルコールとしては、エチレングリコール、1,2−プロパンジオール、1,3−ブタンジオール、1,4−ブタンジオール、3−メチル−1,5−ペンタンジオール、1,6−ヘキサンジオール、3,3’−ジメチロールヘプタン、1,4−シクロヘキサンジメタノール、ネオペンチルグリコール、3,3−ビス(ヒドロキシメチル)ヘプタン、ジエチレングリコール、ジプロピレングリコール、グリセリン、トリメチロールプロパンなどが挙げられ、これらは単独で使用しても、2種類以上を混合して使用しても構わない。また、前記多塩基酸としては、コハク酸、アジピン酸、アゼライン酸、セバシン酸、ドデカンジカルボン酸、シクロペンタンジカルボン酸、シクロヘキサンジカルボン酸、オルトフタル酸、イソフタル酸、テレフタル酸、ナフタレンジカルボン酸などが挙げられ、これらは単独で使用しても、2種類以上を混合して使用しても構わない。
ポリエステルポリオールにおいては、ポリカーボネートポリオールにおける場合と同様な理由から、数平均分子量は好ましくは400〜2000、より好ましくは500〜1500、最も好ましくは600〜1200である。
<Polyester polyol>
Examples of the polyester polyol include a polyester polyol obtained by a condensation reaction between a polyhydric alcohol and a polybasic acid. Here, as the polyhydric alcohol, ethylene glycol, 1,2-propanediol, 1,3-butanediol, 1,4-butanediol, 3-methyl-1,5-pentanediol, 1,6-hexane Diol, 3,3′-dimethylol heptane, 1,4-cyclohexanedimethanol, neopentyl glycol, 3,3-bis (hydroxymethyl) heptane, diethylene glycol, dipropylene glycol, glycerin, trimethylolpropane, etc. These may be used alone or in combination of two or more. Examples of the polybasic acid include succinic acid, adipic acid, azelaic acid, sebacic acid, dodecanedicarboxylic acid, cyclopentanedicarboxylic acid, cyclohexanedicarboxylic acid, orthophthalic acid, isophthalic acid, terephthalic acid, and naphthalenedicarboxylic acid. These may be used alone or in combination of two or more.
In the polyester polyol, the number average molecular weight is preferably 400 to 2000, more preferably 500 to 1500, and most preferably 600 to 1200 for the same reason as in the polycarbonate polyol.
これらポリエステルポリオールは、試薬としてまたは工業的に入手可能であり、市販されているものを例示すれば、DIC株式会社製「ポリライト(登録商標)」シリーズ、日本ポリウレタン工業株式会社製「ニッポラン(登録商標)」シリーズ、川崎化成工業株式会社製「マキシモール(登録商標)」シリーズなどを挙げることができる。 These polyester polyols are available as reagents or industrially, and examples of commercially available ones include “Polylite (registered trademark)” series manufactured by DIC Corporation, “Nipporan (registered trademark)” manufactured by Nippon Polyurethane Industry Co., Ltd. ) ”Series,“ Maximol (registered trademark) ”series manufactured by Kawasaki Kasei Kogyo Co., Ltd., and the like.
<A2成分:分子内に2つのイソシアネート基を有するジイソシアネート化合物>
上記ジイソシアネート化合物(A2成分)としては、脂肪族ジイソシアネート化合物、脂環式ジイソシアネート化合物、芳香族ジイソシアネート化合物、及びこれらの混合物が使用される。これらの中でも、耐候性の観点から脂肪族ジイソシアネート化合物及び/又は脂環式ジイソシアネート化合物を使用することが好ましい。また、同様の理由からA2成分の30〜100質量%、特に50〜100質量%が脂肪族ジイソシアネート化合物であることが好ましい。
<A2 component: diisocyanate compound having two isocyanate groups in the molecule>
As said diisocyanate compound (A2 component), an aliphatic diisocyanate compound, an alicyclic diisocyanate compound, an aromatic diisocyanate compound, and a mixture thereof are used. Among these, it is preferable to use an aliphatic diisocyanate compound and / or an alicyclic diisocyanate compound from the viewpoint of weather resistance. For the same reason, it is preferable that 30 to 100% by mass, particularly 50 to 100% by mass of the A2 component is an aliphatic diisocyanate compound.
A2成分として好適に使用できるジイソシアネート化合物を例示すれば、テトラメチレン−1,4−ジイソシアネート、ヘキサメチレン−1,6−ジイソシアネート、オクタメチレン−1,8−ジイソシアネート、2,2,4−トリメチルヘキサン−1,6−ジイソシアネートなどの脂肪族ジイソシアネート化合物;シクロブタン−1,3−ジイソシアネート、シクロヘキサン−1,3−ジイソシアネート、シクロヘキサン−1,4−ジイソシアネート、2,4−メチルシクロヘキシルジイソシアネート、2,6−メチルシクロヘキシルジイソシアネート、イソホロンジイソシアネート、ノルボルネンジイソシアネート、4,4’−メチレンビス(シクロヘキシルイソシアネート)の異性体混合物、ヘキサヒドロトルエン−2,4−ジイソシアネート、ヘキサヒドロトルエン−2,6−ジイソシアネート、ヘキサヒドロフェニレン−1,3−ジイソシアネート、ヘキサヒドロフェニレン−1,4−ジイソシアネート、1,9−ジイソシアナト−5−メチルノナン、1,1−ビス(イソシアナトメチル)シクロヘキサン、2−イソシアナト−4−[(4−イソシアナトシクロヘキシル)メチル]−1−メチルシクロヘキサン、2−(3−イソシアナトプロピル)シクロヘキシルイソシアネート、ノルボルナンジイソシアネートなどの脂環式ジイソシアネート化合物;フェニルシクロヘキシルメタンジイソシアネート、4,4’−メチレンビス(フェニルイソシアネート)の異性体混合物、トルエン−2,3−ジイソシアネート、トルエン−2,4−ジイソシアネート、トルエン−2,6−ジイソシアネート、フェニレン−1,3−ジイソシアネート、フェニレン−1,4−ジイソシアネート、1,3−ビス(イソシアナトメチル)ベンゼン、キシリレンジイソシアネート、テトラメチルキシリレンジイソシアネート、ナフタレンジイソシアネート、ジフェニルエーテルジイソシアネート、1,3−ジイソシアナトメチルベンゼン、4,4’−ジイソシアナト−3,3’−ジメトキシ(1,1’−ビフェニル)、4,4’−ジイソシアナト−3,3’−ジメチルビフェニル、1,2−ジイソシアナトベンゼン、1,4−ビス(イソシアナトメチル)−2,3,5,6−テトラクロロベンゼン、2−ドデシル−1,3−ジイソシアナトベンゼン、1−イソシアナト−4−[(2−イソシアナトシクロヘキシル)メチル]2−メチルベンゼン、1−イソシアナト−3−[(4−イソシアナトフェニル)メチル)−2−メチルベンゼン、4−[(2−イソシアナトフェニル)オキシ]フェニルイソシアネート、ジフェニルメタンジイソシアネートなどの芳香族ジイソシアネート化合物などを挙げることができる。 Examples of diisocyanate compounds that can be suitably used as the A2 component include tetramethylene-1,4-diisocyanate, hexamethylene-1,6-diisocyanate, octamethylene-1,8-diisocyanate, 2,2,4-trimethylhexane- Aliphatic diisocyanate compounds such as 1,6-diisocyanate; cyclobutane-1,3-diisocyanate, cyclohexane-1,3-diisocyanate, cyclohexane-1,4-diisocyanate, 2,4-methylcyclohexyl diisocyanate, 2,6-methylcyclohexyl Diisocyanate, isophorone diisocyanate, norbornene diisocyanate, isomer mixture of 4,4′-methylenebis (cyclohexyl isocyanate), hexahydrotoluene-2,4-diisocyanate Nate, hexahydrotoluene-2,6-diisocyanate, hexahydrophenylene-1,3-diisocyanate, hexahydrophenylene-1,4-diisocyanate, 1,9-diisocyanato-5-methylnonane, 1,1-bis (isocyanato Cycloaliphatic diisocyanate compounds such as methyl) cyclohexane, 2-isocyanato-4-[(4-isocyanatocyclohexyl) methyl] -1-methylcyclohexane, 2- (3-isocyanatopropyl) cyclohexyl isocyanate, norbornane diisocyanate; phenylcyclohexyl Methane diisocyanate, 4,4′-methylenebis (phenylisocyanate) isomer mixture, toluene-2,3-diisocyanate, toluene-2,4-diisocyanate, toluene-2,6- Diisocyanate, phenylene-1,3-diisocyanate, phenylene-1,4-diisocyanate, 1,3-bis (isocyanatomethyl) benzene, xylylene diisocyanate, tetramethylxylylene diisocyanate, naphthalene diisocyanate, diphenyl ether diisocyanate, 1,3- Diisocyanatomethylbenzene, 4,4′-diisocyanato-3,3′-dimethoxy (1,1′-biphenyl), 4,4′-diisocyanato-3,3′-dimethylbiphenyl, 1,2-diisocyanato Benzene, 1,4-bis (isocyanatomethyl) -2,3,5,6-tetrachlorobenzene, 2-dodecyl-1,3-diisocyanatobenzene, 1-isocyanato-4-[(2-isocyanatocyclohexyl) ) Methyl] 2-methylbe Zen, aromatic diisocyanate compounds such as 1-isocyanato-3-[(4-isocyanatophenyl) methyl) -2-methylbenzene, 4-[(2-isocyanatophenyl) oxy] phenyl isocyanate, diphenylmethane diisocyanate, etc. be able to.
これらの中でも、得られるポリウレタンウレア樹脂(I成分)の耐候性の観点から、上記の通り、A2成分のジイソシアネート化合物の30〜100質量%、特に50〜100質量%が、脂肪族ジイソシアネート化合物、及び脂環式ジイソシアネート化合物よりなる群から選ばれる少なくとも1種のジイソシアネート化合物であることが好ましい。好適な化合物を具体的に例示すると、テトラメチレン−1,4−ジイソシアネート、ヘキサメチレン−1,6−ジイソシアネート、オクタメチレン−1,8−ジイソシアネート、2,2,4−トリメチルヘキサン−1,6−ジイソシアネート、シクロブタン−1,3−ジイソシアネート、シクロヘキサン−1,3−ジイソシアネート、シクロヘキサン−1,4−ジイソシアネート、2,4−メチルシクロヘキシルジイソシアネート、2,6−メチルシクロヘキシルジイソシアネート、イソホロンジイソシアネート、ノルボルナンジイソシアネート、4,4’−メチレンビス(シクロヘキシルイソシアネート)の異性体混合物、ヘキサヒドロトルエン−2,4−ジイソシアネート、ヘキサヒドロトルエン−2,6−ジイソシアネート、ヘキサヒドロフェニレン−1,3−ジイソシアネート、ヘキサヒドロフェニレン−1,4−ジイソシアネートが挙げられる。これらのイソシアネート化合物は、単独で使用してもよく、2種類以上を併用しても構わない。 Among these, from the viewpoint of the weather resistance of the resulting polyurethane urea resin (component I), as described above, 30 to 100% by mass, particularly 50 to 100% by mass of the diisocyanate compound of component A2 is an aliphatic diisocyanate compound, and It is preferably at least one diisocyanate compound selected from the group consisting of alicyclic diisocyanate compounds. Specific examples of suitable compounds include tetramethylene-1,4-diisocyanate, hexamethylene-1,6-diisocyanate, octamethylene-1,8-diisocyanate, 2,2,4-trimethylhexane-1,6- Diisocyanate, cyclobutane-1,3-diisocyanate, cyclohexane-1,3-diisocyanate, cyclohexane-1,4-diisocyanate, 2,4-methylcyclohexyl diisocyanate, 2,6-methylcyclohexyl diisocyanate, isophorone diisocyanate, norbornane diisocyanate, 4, 4'-methylenebis (cyclohexyl isocyanate) isomer mixture, hexahydrotoluene-2,4-diisocyanate, hexahydrotoluene-2,6-diisocyanate, hexahi Rofeniren 1,3 diisocyanate are hexahydrophthalate phenylene-1,4-diisocyanate. These isocyanate compounds may be used alone or in combination of two or more.
<(B)分子内に2つ以上のアミノ基を有するポリアミン化合物>
前記分子内に2つ以上のアミノ基を有するポリアミン化合物(B成分)は、分子内に2つ以上のアミノ基(−NH2、または−NH(R)。但し、Rはアルキル基、特に炭素数1〜5のアルキル基を意味する。)を有するポリアミン化合物である。
該B成分は、ポリウレタンウレア樹脂(I成分)を合成する際の鎖延長剤として機能するものであり、鎖延長剤として、B成分を用いることによりポリウレタン樹脂中にウレア結合が導入され、ポリウレタンウレア樹脂となる。
<(B) Polyamine compound having two or more amino groups in the molecule>
The polyamine compound (component B) having two or more amino groups in the molecule has two or more amino groups (—NH 2 or —NH (R) in the molecule, where R is an alkyl group, particularly carbon. A polyamine compound having an alkyl group of 1 to 5).
The component B functions as a chain extender when synthesizing a polyurethane urea resin (component I). By using the component B as the chain extender, a urea bond is introduced into the polyurethane resin, and the polyurethane urea It becomes resin.
得られるポリウレタンウレア樹脂(I成分)を適度の硬さにし、また、接着性、及び耐熱性を良好に維持するためには、ポリアミン化合物の分子量は、50〜300であることが好ましく、50〜250であることがより好ましく、100〜220であることが最も好ましい。 The molecular weight of the polyamine compound is preferably 50 to 300 in order to make the resulting polyurethane urea resin (component I) moderately hard and to maintain good adhesion and heat resistance. 250 is more preferable, and 100 to 220 is most preferable.
B成分のポリアミン化合物としては、ジアミン、及びトリアミンよりなる群から選ばれる少なくとも1種の化合物が好適に使用し得る。本発明においてポリアミン化合物として好適に使用される化合物を具体的に例示すれば、イソホロンジアミン、エチレンジアミン、1,2−ジアミノプロパン、1,3−ジアミノプロパン、1,2−ジアミノブタン、1,3−ジアミノブタン、1,4−ジアミノブタン、1,5−ジアミノペンタン、1,6−ジアミノヘキサン、ピペラジン、N,N−ビス−(2−アミノエチル)ピペラジン、ビス−(4−アミノシクロヘキシル)メタン、ビス−(4−アミノ−3−ブチルシクロヘキシル)メタン、1,2−、1,3−及び1,4−ジアミノシクロヘキサン、ノルボルナンジアミン、ヒドラジン、アジピン酸ジヒドラジン、フェニレンジアミン、4,4’−ジフェニルメタンジアミン、N,N’−ジエチルエチレンジアミン、N,N’−ジメチルエチレンジアミン、N,N’−ジプロピルエチレンジアミン、N,N’−ジブチルエチレンジアミン、N−メチルエチレンジアミン、N−エチルエチレンジアミン、ビス(ヘキサメチレン)トリアミン、1,2,5−ペンタントリアミン等を挙げることができる。 As the polyamine compound of component B, at least one compound selected from the group consisting of diamines and triamines can be suitably used. Specific examples of the compound suitably used as the polyamine compound in the present invention include isophorone diamine, ethylene diamine, 1,2-diaminopropane, 1,3-diaminopropane, 1,2-diaminobutane, 1,3- Diaminobutane, 1,4-diaminobutane, 1,5-diaminopentane, 1,6-diaminohexane, piperazine, N, N-bis- (2-aminoethyl) piperazine, bis- (4-aminocyclohexyl) methane, Bis- (4-amino-3-butylcyclohexyl) methane, 1,2-, 1,3- and 1,4-diaminocyclohexane, norbornanediamine, hydrazine, dihydrazine adipate, phenylenediamine, 4,4′-diphenylmethane Diamine, N, N'-diethylethylenediamine, N, N'-dimethyl Examples include ruethylenediamine, N, N′-dipropylethylenediamine, N, N′-dibutylethylenediamine, N-methylethylenediamine, N-ethylethylenediamine, bis (hexamethylene) triamine, 1,2,5-pentanetriamine, and the like. it can.
ポリアミン化合物においては、接着性、及び耐熱性などの観点から、特にジアミン化合物を使用することが好ましい。この理由は、ウレタンウレア樹脂(I成分)を合成する際に、ポリアミン化合物を用いることにより、ウレア結合を有することになり、分子の剛直性が高くなると共に、分子鎖間の水素結合がより強固となるため、耐熱性が向上するものと推定している。また、ウレア結合の存在により分子鎖間の水素結合がより強固となることによって、空気中の酸素が該ポリウレタンウレア樹脂(I成分)中へ拡散し難くなり、該ポリウレタンウレア樹脂の光酸化劣化が抑制されたためであると推定している。さらに、接着力が向上することに関しては、ウレア結合の存在により分子鎖間の水素結合が強固となって樹脂の凝集破壊が起こりにくくなったためであると推定している。 In the polyamine compound, it is particularly preferable to use a diamine compound from the viewpoints of adhesiveness and heat resistance. This is because when a urethane urea resin (component I) is synthesized, a polyamine compound is used to have a urea bond, resulting in higher molecular rigidity and stronger hydrogen bonds between molecular chains. Therefore, it is estimated that the heat resistance is improved. In addition, the presence of urea bonds makes the hydrogen bonds between the molecular chains stronger, making it difficult for oxygen in the air to diffuse into the polyurethane urea resin (component I), resulting in photooxidative degradation of the polyurethane urea resin. It is presumed that this was due to suppression. Furthermore, it is presumed that the adhesive force is improved because the hydrogen bond between the molecular chains is strengthened due to the presence of the urea bond and the cohesive failure of the resin hardly occurs.
また、前記ポリアミン化合物のなかにおいて、耐水性、及び耐汗試験への安定性の観点から、イソホロンジアミン、ビス−(4−アミノシクロヘキシル)メタン、ノルボルナンジアミンを用いることがより好ましく、その中でも、ビス−(4−アミノシクロヘキシル)メタンを用いることが最も好ましい。 Among the polyamine compounds, isophoronediamine, bis- (4-aminocyclohexyl) methane, and norbornanediamine are more preferable from the viewpoint of water resistance and stability to sweat resistance tests. Most preferably,-(4-aminocyclohexyl) methane is used.
<(C)分子内にイソシアネート基と反応しうる基を1つ有する化合物>
上記のポリウレタンウレア樹脂を合成する際に、分子内に1つのイソシアネート基と反応しうる基を有する化合物(C成分)を併用することも可能である。このC成分を使用することにより、分子鎖の末端がキャッピングされたポリウレタンウレア樹脂となる。前述のイソシアネート基と反応しうる基とは、アミノ基(−NH2基、及び−NH(R)基)、水酸基(−OH基)、メルカプト基(−SH基:チオール基)、カルボキシル基〔−C(=O)OH基〕、又は酸クロライド基〔−C(=O)OCl基〕が挙げられる。上記のC成分の中でも、分子内に少なくとも1つのピペリジン構造を有する機能性付与化合物であることが好ましい。この機能性付与化合物は、ピペリジン構造の代わりにヒンダードフェノール構造、トリアジン構造、またはベンゾトリアゾール構造を有するものであってもよい。ただし、最も優れた効果を発揮するのは、ピペリジン構造を有する機能性付与化合物である。
<(C) Compound having one group capable of reacting with an isocyanate group in the molecule>
When synthesizing the above polyurethane urea resin, it is also possible to use a compound (C component) having a group capable of reacting with one isocyanate group in the molecule. By using this C component, it becomes a polyurethane urea resin in which the end of the molecular chain is capped. Examples of the group capable of reacting with the isocyanate group include an amino group (—NH 2 group and —NH (R) group), a hydroxyl group (—OH group), a mercapto group (—SH group: thiol group), a carboxyl group [ -C (= O) OH group], or acid chloride group [-C (= O) OCl group]. Among the above C components, a functional compound having at least one piperidine structure in the molecule is preferable. The functional compound may have a hindered phenol structure, a triazine structure, or a benzotriazole structure instead of the piperidine structure. However, it is a functional compound having a piperidine structure that exhibits the most excellent effect.
このような機能性付与化合物を用いることによって、ポリウレタンウレア樹脂(I成分)にピペリジン構造を導入することができる。その結果、光安定性能、酸化防止性能、及び紫外線吸収性能等の機能性に優れたポリウレタンウレア樹脂(I成分)を得ることができる。
以下、C成分として使用される各種化合物について、代表例としてピペリジン構造を有する化合物などを詳しく説明する。
By using such a function-imparting compound, a piperidine structure can be introduced into the polyurethane urea resin (component I). As a result, it is possible to obtain a polyurethane urea resin (I component) excellent in functionality such as light stability performance, antioxidant performance, and ultraviolet absorption performance.
Hereinafter, as various examples of various compounds used as the component C, compounds having a piperidine structure will be described in detail.
<ピペリジン構造を有する化合物>
ポリウレタンウレア樹脂におけるC成分として使用されるピペリジン構造を有する化合物としては、下記一般式(i)で示される構造を分子内に有する化合物が好適に使用できる。
<Compound having piperidine structure>
As the compound having a piperidine structure used as the C component in the polyurethane urea resin, a compound having a structure represented by the following general formula (i) in the molecule can be preferably used.
(式中、
R1、R2、R3、及びR4は、それぞれ、炭素数1〜4のアルキル基であり、特に、メチル基であることが好ましい。)。そして、上記ピペリジン環の窒素原子、または、4位の炭素原子にイソシアネート基と反応しうる基を有する化合物が、ピペリジン構造を有する化合物に該当する。
以下、より具体的な化合物について説明する。
(Where
R 1 , R 2 , R 3 , and R 4 are each an alkyl group having 1 to 4 carbon atoms, and particularly preferably a methyl group. ). And the compound which has a group which can react with an isocyanate group in the nitrogen atom of the said piperidine ring or the 4-position carbon atom corresponds to the compound which has a piperidine structure.
Hereinafter, more specific compounds will be described.
本発明でC成分として使用される化合物の中で、本発明のI成分であるポリウレタンウレア樹脂の末端にピペリジン構造を導入しうる化合物としては、下記一般式(1)で示される化合物などを使用することが好適に挙げられる。 Among the compounds used as component C in the present invention, compounds that can introduce a piperidine structure at the end of the polyurethane urea resin that is component I of the present invention include compounds represented by the following general formula (1) It is preferably mentioned.
(式中、
R1、R2、R3、及びR4は、前記一般式(i)におけるものと同義であり、
R5は、炭素数1〜10アルキル基、または水素原子であり、
R6は炭素数1〜20のアルキレン基、又は炭素数3〜20のポリメチレン基であり、aは0または1であり、
Xは、イソシアネート基と反応しうる基である。)。
(Where
R 1 , R 2 , R 3 , and R 4 have the same meaning as in the general formula (i),
R 5 is a C 1-10 alkyl group or a hydrogen atom,
R 6 is an alkylene group having 1 to 20 carbon atoms, or a polymethylene group having 3 to 20 carbon atoms, a is 0 or 1,
X is a group capable of reacting with an isocyanate group. ).
上記一般式(1)において、R1、R2、R3、及びR4は、それぞれ独立に炭素数1〜4のアルキル基であるが、4つのアルキル基全てメチル基であることが好ましい。
R5は、炭素数1〜10アルキル基、または水素原子である。中でも、入手の容易さの観点から、炭素数1〜4アルキル基、または水素原子であることが好ましい。なお、R1〜R4が炭素数1〜4のアルキル基であるため、R5が水素原子であっても、立体障害の影響でR5が結合している窒素原子とイソシアネート基が反応することはない。
R6は、炭素数1〜20のアルキレン基、又は炭素数3〜20のポリメチレン基であり、好ましくは炭素数1〜10のアルキレン基、又は炭素数3〜10のポリメチレン基である。なお、aは、R6の数を示すが、aが0の場合は、Xが直接ピペリジン環に結合しているものを指す。
In the general formula (1), R 1 , R 2 , R 3 , and R 4 are each independently an alkyl group having 1 to 4 carbon atoms, but all four alkyl groups are preferably methyl groups.
R 5 is a C 1-10 alkyl group or a hydrogen atom. Especially, it is preferable that it is a C1-C4 alkyl group or a hydrogen atom from a viewpoint of availability. Since R 1 to R 4 is an alkyl group having 1 to 4 carbon atoms, even R 5 is a hydrogen atom, a nitrogen atom and an isocyanate group R 5 is attached to the influence of steric hindrance to react There is nothing.
R 6 is an alkylene group having 1 to 20 carbon atoms or a polymethylene group having 3 to 20 carbon atoms, preferably an alkylene group having 1 to 10 carbon atoms or a polymethylene group having 3 to 10 carbon atoms. In addition, although a shows the number of R6, when a is 0, it points to what X has couple | bonded with the piperidine ring directly.
Xは、イソシアネート基と反応しうる基であり、好ましくは、アミノ基、水酸基、カルボキシル基、またはチオール基である。中でも、イソシアネート基との反応性、入手の容易さなどの観点からアミノ基、及び水酸基であることが好適である。
上記式(1)で示される化合物を具体的に例示すれば、1,2,2,6,6−ペンタメチル−4−ヒドロキシピペリジン、1,2,2,6,6−ペンタメチル−4−アミノピペリジン、2,2,6,6−テトラメチル−4−ヒドロキシピペリジン、2,2,6,6−テトラメチル−4−アミノピペリジン、1,2,2,6,6−ペンタメチル−4−アミノメチルピペリジン、1,2,2,6,6−ペンタメチル−4−アミノブチルピペリジンなどを挙げることができる。
X is a group capable of reacting with an isocyanate group, and is preferably an amino group, a hydroxyl group, a carboxyl group, or a thiol group. Among these, an amino group and a hydroxyl group are preferable from the viewpoints of reactivity with an isocyanate group and availability.
Specific examples of the compound represented by the formula (1) include 1,2,2,6,6-pentamethyl-4-hydroxypiperidine, 1,2,2,6,6-pentamethyl-4-aminopiperidine. 2,2,6,6-tetramethyl-4-hydroxypiperidine, 2,2,6,6-tetramethyl-4-aminopiperidine, 1,2,2,6,6-pentamethyl-4-aminomethylpiperidine 1,2,2,6,6-pentamethyl-4-aminobutylpiperidine and the like.
<その他のC成分>
上記C成分としては、前述したピペリジン構造を有する耐候性の向上を目的とした化合物以外にも、一般的なアミン、アルコール、チオール、及びカルボン酸を用いることができる。これらの化合物は、分子内にイソシアネート基と反応しうる基を1つ有することにより、I成分であるポリウレタンウレア樹脂の末端を、不活性化することができる。
本発明で使用されるその他のC成分の中でも、好ましい化合物としては、下記一般式(2)、及び(3)を挙げることができる。
<Other C components>
As said C component, a general amine, alcohol, thiol, and carboxylic acid other than the compound aiming at the improvement of the weather resistance which has the piperidine structure mentioned above can be used. These compounds have one group capable of reacting with an isocyanate group in the molecule, and thus can inactivate the terminal of the polyurethane urea resin as the I component.
Among the other C components used in the present invention, preferred compounds include the following general formulas (2) and (3).
(式中、
R7は、炭素数1〜20のアルキル基、アリール基、アラルキル基、アルキルオキシカルボニル基または水素原子であり、
R8は、炭素数1〜20のアルキル基、アリール基、アラルキル基、またはエステル基である。)
R7が水素原子である化合物をC成分として用いた場合には、I成分であるポリウレタンウレア樹脂の末端は、−NH(R8)基となるが、この−NH(R8)基は、他のポリマー、およびイソシアネート化合物とは実質的に反応しない。そのため、−NH(R8)基は、イソシアネート基と反応しうる基には該当しない。
(Where
R 7 is an alkyl group having 1 to 20 carbon atoms, an aryl group, an aralkyl group, an alkyloxycarbonyl group, or a hydrogen atom,
R 8 is an alkyl group having 1 to 20 carbon atoms, an aryl group, an aralkyl group, or an ester group. )
When a compound in which R 7 is a hydrogen atom is used as the C component, the terminal of the polyurethane urea resin that is the I component is an —NH (R 8 ) group, and this —NH (R 8 ) group is It does not substantially react with other polymers and isocyanate compounds. Therefore, the —NH (R 8 ) group does not correspond to a group that can react with an isocyanate group.
上記一般式(2)において、R7は、炭素数1〜20のアルキル基、アリール基、アラルキル基、アルキルオキシカルボニル基または水素原子である。中でも、R7は、炭素数1〜10のアルキル基、アリール基、アラルキル基、アルキルオキシカルボニル基、または水素原子であることが好ましい。前記アリール基、及びアラルキル基は、炭素数1〜5のアルキル基、ハロゲン原子を置換基として有してもよい。
好適なR7を例示すれば、メチル基、エチル基、ノルマルプロピル基、イソプロピル基、ノルマルブチル基、tert−ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、1,1,3,3−テトラメチルブチル基、フェニル基、ベンジル基、1,1−ジメチルベンジル基、カルボキシメチル基、カルボキシエチル基、カルボキシプロピル基、又は水素原子等が挙げられる。
In the general formula (2), R 7 is an alkyl group having 1 to 20 carbon atoms, an aryl group, an aralkyl group, an alkyloxycarbonyl group, or a hydrogen atom. Among them, R 7 is preferably an alkyl group having 1 to 10 carbon atoms, an aryl group, an aralkyl group, an alkyloxycarbonyl group, or a hydrogen atom. The aryl group and aralkyl group may have an alkyl group having 1 to 5 carbon atoms or a halogen atom as a substituent.
Examples of suitable R 7 include methyl group, ethyl group, normal propyl group, isopropyl group, normal butyl group, tert-butyl group, pentyl group, hexyl group, heptyl group, octyl group, 1,1,3,3. -A tetramethylbutyl group, a phenyl group, a benzyl group, a 1,1-dimethylbenzyl group, a carboxymethyl group, a carboxyethyl group, a carboxypropyl group, or a hydrogen atom.
また、R8は、炭素数1〜20のアルキル基、アリール基、アラルキル基、またはアルキルオキシカルボニル基である。中でも、R8は、炭素数1〜10のアルキル基、アリール基、アラルキル基、またはアルキルオキシカルボニル基であることが好ましい。前記アリール基は、炭素数1〜5のアルキル基、ハロゲン原子を置換基として有してもよい。
好適なR8を例示すれば、メチル基、エチル基、ノルマルプロピル基、イソプロピル基、ノルマルブチル基、tert−ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、1,1,3,3−テトラメチルブチル基、フェニル基、ベンジル基、1,1−ジメチルベンジル基、カルボキシメチル基、カルボキシエチル基、又はカルボキシプロピル基等が挙げられる。
R 8 is an alkyl group having 1 to 20 carbon atoms, an aryl group, an aralkyl group, or an alkyloxycarbonyl group. Among these, R 8 is preferably an alkyl group having 1 to 10 carbon atoms, an aryl group, an aralkyl group, or an alkyloxycarbonyl group. The aryl group may have an alkyl group having 1 to 5 carbon atoms or a halogen atom as a substituent.
Examples of suitable R 8 are methyl group, ethyl group, normal propyl group, isopropyl group, normal butyl group, tert-butyl group, pentyl group, hexyl group, heptyl group, octyl group, 1,1,3,3. -A tetramethylbutyl group, a phenyl group, a benzyl group, a 1,1-dimethylbenzyl group, a carboxymethyl group, a carboxyethyl group, or a carboxypropyl group.
下記一般式(3) The following general formula (3)
(式中、
R9は、炭素数1〜20のアルキル基、アリール基、アラルキル基、またはアルキルオキシカルボニル基であり、
Zは、水酸基、カルボキシル基、またはチオール基である。)
で示される化合物も好適に使用できる。
(Where
R 9 is an alkyl group having 1 to 20 carbon atoms, an aryl group, an aralkyl group, or an alkyloxycarbonyl group,
Z is a hydroxyl group, a carboxyl group, or a thiol group. )
The compound represented by can also be used suitably.
上記一般式(3)において、R9は、炭素数1〜20のアルキル基、アリール基、アラルキル基、またはアルキルオキシカルボニル基であり、炭素数1〜10のアルキル基、アリール基、アラルキル基、またはアルキルオキシカルボニル基であることが好ましい。このアリール基、及びアラルキル基は、炭素数1〜5のアルキル基、ハロゲン原子を置換基として有してもよい。好ましい基としては、炭素数1〜5のアルキル基、フェニル基、ハロゲン原子を有するフェニル基が挙げられる。好適なR9を例示すれば、メチル基、エチル基、ノルマルプロピル基、イソプロピル基、ノルマルブチル基、tert−ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、1,1,3,3−テトラメチルブチル基、フェニル基、ベンジル基、1,1−ジメチルベンジル基、カルボキシメチル基、カルボキシエチル基、及びカルボキシプロピル基等が挙げられる。 In the general formula (3), R 9 is an alkyl group having 1 to 20 carbon atoms, an aryl group, an aralkyl group, or an alkyloxycarbonyl group, and an alkyl group having 1 to 10 carbon atoms, an aryl group, an aralkyl group, Or it is preferable that it is an alkyloxycarbonyl group. This aryl group and aralkyl group may have an alkyl group having 1 to 5 carbon atoms or a halogen atom as a substituent. Preferable groups include alkyl groups having 1 to 5 carbon atoms, phenyl groups, and phenyl groups having a halogen atom. Examples of suitable R 9 are methyl group, ethyl group, normal propyl group, isopropyl group, normal butyl group, tert-butyl group, pentyl group, hexyl group, heptyl group, octyl group, 1,1,3,3. -Tetramethylbutyl group, phenyl group, benzyl group, 1,1-dimethylbenzyl group, carboxymethyl group, carboxyethyl group, carboxypropyl group and the like.
上記一般式(3)におけるZは、イソシアネート基と反応しうる基であり、具体的には水酸基、カルボキシル基、またはチオール基であり、好ましくは水酸基である。 Z in the general formula (3) is a group capable of reacting with an isocyanate group, specifically a hydroxyl group, a carboxyl group, or a thiol group, preferably a hydroxyl group.
上記一般式(2)、及び(3)で示される具体的な化合物としては、メチルアミン、エチルアミン、プロピルアミン、イソプロピルアミン、ブチルアミン、tert−ブチルアミン、ペンチルアミン、ヘキシルアミン、ヘプチルアミン、4−ヘプチルアミン、オクチルアミン、1,1−ジプロピルブチルアミン、フェニルアミン、ベンジルアミン、ジメチルアミン、ジエチルアミン、ジプロピルアミン、ジイソプロピルアミン、ジブチルアミン、ジ−tert−ブチルアミン、ジペンチルアミン、ジヘキシルアミン、ジヘプチルアミン、ジオクチルアミン、メチルエチルアミン、メチルブチルアミン、メチルペンチルアミン、メチルヘキシルアミン、メチルヘプチルアミン、メチルオクチルアミン、エチルプロピルアミン、エチルブチルアミン、エチルペンチルアミン、エチルヘキシルアミン、エチルヘプチルアミン、エチルオクチルアミン、プロピルブチルアミン、イソプロピルブチルアミン、プロピルペンチルアミン、プロピルヘキシルアミン、プロピルヘプチルアミン、プロピルオクチルアミンなどのアミン類、メタノール、エタノール、プロパノール、イソプロパノール、ブタノール、2−ブタノール、tert−ブチルアルコール、ペンチルアルコール、ヘキシルアルコール、ヘプチルアルコール、オクチルアルコール、ノニルアルコール、デカノール、2−デカノールなどのアルコール類、メタンチオール、エタンチオール、1−プロパンチオール、2−プロパンチオール、1−ブタンチオール、2−ブタンチオール、プロパンチオール、ヘキサンチオール、ヘプタンチオール、オクタンチオール、ドデカンチオール、2−メチル−1−ブタンチオール、2−メチルプロパンチオール、3−メチル−2−ブテンチオール、1,1−ジメチルヘプタンチオール、シクロヘキサンチオール、シクロペンタンチオール、ベンゼンチオール、ベンゼンメタンチオール、2,6−ジメチルベンゼンチオールなどのチオール類、酢酸、プロピオン酸、酪酸、ペンタン酸、ヘキサン酸、ヘプタン酸、オクタン酸、ノナン酸、デカン酸、ドデカン酸などのカルボン酸類などが挙げられる。 Specific compounds represented by the general formulas (2) and (3) include methylamine, ethylamine, propylamine, isopropylamine, butylamine, tert-butylamine, pentylamine, hexylamine, heptylamine, 4-heptyl. Amine, octylamine, 1,1-dipropylbutylamine, phenylamine, benzylamine, dimethylamine, diethylamine, dipropylamine, diisopropylamine, dibutylamine, di-tert-butylamine, dipentylamine, dihexylamine, diheptylamine, Dioctylamine, methylethylamine, methylbutylamine, methylpentylamine, methylhexylamine, methylheptylamine, methyloctylamine, ethylpropylamine, ethylbutylamine , Amines such as ethylpentylamine, ethylhexylamine, ethylheptylamine, ethyloctylamine, propylbutylamine, isopropylbutylamine, propylpentylamine, propylhexylamine, propylheptylamine, propyloctylamine, methanol, ethanol, propanol, isopropanol, Butanol, 2-butanol, tert-butyl alcohol, pentyl alcohol, hexyl alcohol, heptyl alcohol, octyl alcohol, nonyl alcohol, decanol, 2-decanol and other alcohols, methanethiol, ethanethiol, 1-propanethiol, 2-propane Thiol, 1-butanethiol, 2-butanethiol, propanethiol, hexanethiol, heptane All, octanethiol, dodecanethiol, 2-methyl-1-butanethiol, 2-methylpropanethiol, 3-methyl-2-butenethiol, 1,1-dimethylheptanethiol, cyclohexanethiol, cyclopentanethiol, benzenethiol, Examples include thiols such as benzenemethanethiol and 2,6-dimethylbenzenethiol, carboxylic acids such as acetic acid, propionic acid, butyric acid, pentanoic acid, hexanoic acid, heptanoic acid, octanoic acid, nonanoic acid, decanoic acid, and dodecanoic acid. It is done.
以上のC成分は、単独で用いても、2種類以上を混合して用いても構わないが、ポリウレタンウレア樹脂の耐久性を向上させるという観点から、ピペリジン構造を有する化合物を用いることが好適である。 The above component C may be used alone or in combination of two or more, but from the viewpoint of improving the durability of the polyurethane urea resin, it is preferable to use a compound having a piperidine structure. is there.
<ポリウレタンウレア樹脂におけるA1、A2、B、及びC成分の使用量>
上記本発明のフォトクロミック組成物におけるポリウレタンウレア樹脂(I成分)を構成する上記各成分、即ちA1成分、A2成分、B成分、およびC成分の量比は、ポリウレタンウレア樹脂を使用する用途等を勘案して適宜決定すればよいが、得られるポリウレタンウレア樹脂の耐熱性、接着力などのバランスの観点から、次のような量比とすることが好ましい。すなわち、A1成分に含まれる水酸基の総モル数をn1とし、A2成分に含まれるイソシアネート基の総モル数をn2とし、B成分に含まれるアミノ基の総モル数をn3とし、C成分に含まれるイソシアネート基と反応しうる基(具体的にはアミノ基、水酸基、メルカプト基及び/又はカルボキシル基等)の総モル数をn4としたときに、n1:n2:n3:n4=0.4〜0.8/1.0/0.19〜0.59/0.01〜0.2となる量比、特にn1:n2:n3:n4=0.45〜0.75/1.0/0.23〜0.53/0.02〜0.15となる量比とすることが好ましく、n1:n2:n3:n4=0.65〜0.75/1.0/0.23〜0.33/0.02〜0.1となる量比とすることが最も好ましい。ここで、上記n1〜n4は、各成分として用いる化合物の使用モル数と該化合物1分子中に存在する各基の数の積として求めることができる。
<Use amount of A1, A2, B, and C component in polyurethane urea resin>
The above-mentioned components constituting the polyurethane urea resin (component I) in the photochromic composition of the present invention, that is, the amount ratio of the components A1, A2, B, and C, takes into account the use of the polyurethane urea resin, etc. However, from the viewpoint of balance between the heat resistance and adhesive strength of the resulting polyurethane urea resin, the following quantitative ratio is preferable. That is, the total number of moles of hydroxyl groups contained in the A1 component is n1, the total number of isocyanate groups contained in the A2 component is n2, the total number of amino groups contained in the B component is n3, and included in the C component. N1: n2: n3: n4 = 0.4 to when the total number of moles of the group capable of reacting with the isocyanate group (specifically, amino group, hydroxyl group, mercapto group and / or carboxyl group) is n4 0.8 / 1.0 / 0.19 to 0.59 / 0.01 to 0.2, particularly n1: n2: n3: n4 = 0.45 to 0.75 / 1.0 / 0 It is preferable that the quantity ratio is 23 to 0.53 / 0.02 to 0.15, and n1: n2: n3: n4 = 0.65 to 0.75 / 1.0 / 0.23 to 0. Most preferably, the quantity ratio is 33 / 0.02-0.1. Here, said n1-n4 can be calculated | required as a product of the use mole number of the compound used as each component, and the number of each group which exists in this compound 1 molecule.
上記ポリウレタンウレア樹脂(I成分)においては、末端には反応性の基を有さないことが好ましい。特に、末端にイソシアネート基が残存しないように不活性化させることが好ましい。そのため、製造時には、n2=n1+n3+n4となるような配合割合で製造することが好ましい。n2よりもn1、n3、及びn4の合計モル数(n1+n3+n4)が大きい場合には、再沈殿等により、未反応のA1、B、C成分を除去してやればよい。 The polyurethane urea resin (component I) preferably has no reactive group at the end. In particular, it is preferable to inactivate such that no isocyanate group remains at the terminal. Therefore, at the time of manufacture, it is preferable to manufacture at a blending ratio such that n2 = n1 + n3 + n4. When the total number of moles of n1, n3, and n4 (n1 + n3 + n4) is larger than n2, unreacted A1, B, and C components may be removed by reprecipitation or the like.
上記A1成分、A2成分、B成分、及び、必要に応じてC成分を反応させて、本発明のポリウレタンウレア樹脂(I成分)を得る方法としては、多分散度(重量平均分子量/数平均分子量)が上記範囲を満足する様に反応させればよく、所謂ワンショット法又はプレポリマー法のいずれの方法も採用することができる。しかしながら、多分散度を制御し効率良くポリウレタンウレア樹脂を得るという観点から、プレポリマー法が好ましい。特に後述する製造方法によれば、多分散度(重量平均分子量/数平均分子量)が上記範囲を満足するポリウレタンウレア樹脂を簡便に製造することが可能である。 As a method of obtaining the polyurethane urea resin (I component) of the present invention by reacting the above A1 component, A2 component, B component and, if necessary, the C component, polydispersity (weight average molecular weight / number average molecular weight) ) May satisfy the above range, and any one of the so-called one-shot method and prepolymer method can be employed. However, the prepolymer method is preferred from the viewpoint of controlling the polydispersity and obtaining a polyurethane urea resin efficiently. In particular, according to the production method described later, it is possible to easily produce a polyurethane urea resin having a polydispersity (weight average molecular weight / number average molecular weight) satisfying the above range.
<ポリウレタンウレア樹脂の製造方法>
<ウレタンプレポリマー(A)の製造方法>
本発明のフォトクロミック組成物に用いるポリウレタンウレア樹脂は、一般にウレタンプレポリマーとジアミン等のポリアミンとの反応によって製造することができるが、ウレタンプレポリマー(A成分)は、上記ポリオール化合物(A1成分)と、上記ジイソシアネート化合物(A2成分)とを反応(以下、「プレポリマー反応」ともいう)させることによって製造することができる。
<Method for producing polyurethane urea resin>
<Method for producing urethane prepolymer (A)>
The polyurethane urea resin used in the photochromic composition of the present invention can be generally produced by a reaction between a urethane prepolymer and a polyamine such as diamine. The urethane prepolymer (component A) is composed of the polyol compound (component A1) and , By reacting with the diisocyanate compound (component A2) (hereinafter also referred to as “prepolymer reaction”).
A1成分とA2成分を反応させる際の添加順序は特に制限されず、必要に応じて反応途中に適宜、A1成分及びA2成分を追加添加することも可能である。 The order of addition when the A1 component and the A2 component are reacted is not particularly limited, and it is possible to add the A1 component and the A2 component as needed during the reaction as needed.
A1成分とA2成分との反応は、有機溶媒の存在下または非存在下で両者を、好ましくは窒素あるいはアルゴンなどの不活性ガス雰囲気下中で、反応温度70〜130℃で反応させればよい。反応温度が70℃未満の場合には反応が完結せず、また130℃を超える場合にはA1成分の一部が分解してしまい、所望の物性のウレタンウレア樹脂を得られなくなってしまう。反応時間は、A1成分とA2成分の仕込み比、及び反応温度によっても変化するが、0.5〜24時間の範囲で反応させればよい。 The reaction between the A1 component and the A2 component may be performed in the presence or absence of an organic solvent, preferably in an inert gas atmosphere such as nitrogen or argon, at a reaction temperature of 70 to 130 ° C. . When the reaction temperature is less than 70 ° C., the reaction is not completed, and when it exceeds 130 ° C., a part of the A1 component is decomposed and a urethane urea resin having desired physical properties cannot be obtained. Although reaction time changes also with preparation ratio of A1 component and A2 component, and reaction temperature, what is necessary is just to make it react in the range of 0.5 to 24 hours.
有機溶媒としては、アセトン、メチルエチルケトン、メチルイソブチルケトン、ジエチルケトン、シクロヘキサノン、ジオキサン、トルエン、ヘキサン、ヘプタン、酢酸エチル、酢酸ブチル、ジメチルホルムアミド(DMF)、ジメチルスルホキシド(DMSO)、テトラヒドロフラン(THF)などの有機溶媒が使用できる。これらの有機溶媒は、2種類以上混合して使用することも出来る。 Examples of organic solvents include acetone, methyl ethyl ketone, methyl isobutyl ketone, diethyl ketone, cyclohexanone, dioxane, toluene, hexane, heptane, ethyl acetate, butyl acetate, dimethylformamide (DMF), dimethyl sulfoxide (DMSO), and tetrahydrofuran (THF). Organic solvents can be used. These organic solvents can be used in combination of two or more.
有機溶媒を使用する場合には、その使用量はA1成分とA2成分の合計量を100質量部とした際に、200質量部以下であることが好ましい。有機溶媒の使用量が200質量部を超える場合には、A1成分とA2成分の反応時間が長くなり、A1成分の一部が分解するおそれがある。 When an organic solvent is used, the amount used is preferably 200 parts by mass or less when the total amount of the A1 component and the A2 component is 100 parts by mass. When the usage-amount of an organic solvent exceeds 200 mass parts, there exists a possibility that reaction time of A1 component and A2 component may become long, and a part of A1 component may decompose | disassemble.
反応に際しては、ジイソシアネート化合物中のイソシアネート基と不純物としての水との反応を避けるため、各種反応試剤及び溶媒は、予め脱水処理を行い、十分に乾燥しておくことが好ましい。また、上記反応を行う際には、ジラウリル酸ジブチルスズ、ジメチルイミダゾール、トリエチレンジアミン、テトラメチル−1,6−ヘキサジアミン、テトラメチル−1,2−エタンジアミン、1,4−ジアザビシクロ[2,2,2]オクタンなどの触媒を用いてもよい。触媒を使用する際の添加量としては、A成分の合計100質量部に対して0.001〜1質量部であることが好ましい。 In the reaction, in order to avoid a reaction between an isocyanate group in the diisocyanate compound and water as an impurity, it is preferable that various reaction reagents and solvents are subjected to dehydration in advance and sufficiently dried. In the above reaction, dibutyltin dilaurate, dimethylimidazole, triethylenediamine, tetramethyl-1,6-hexadiamine, tetramethyl-1,2-ethanediamine, 1,4-diazabicyclo [2,2, 2] A catalyst such as octane may be used. As an addition amount at the time of using a catalyst, it is preferable that it is 0.001-1 mass part with respect to a total of 100 mass parts of A component.
<ポリウレタンウレア樹脂の製造方法>
ポリウレタンウレア樹脂は、一般にウレタンプレポリマーとジアミン等のポリアミンとの反応によって製造することができるが、ウレタンプレポリマー(A成分)と、ポリアミン化合物(B成分)とを反応させる際に、A成分とB成分との完全混合時間(θM)が30秒以下、好ましくは15秒以下にすることにより、多分散度(重量平均分子量/数平均分子量)が1.6〜2.4の範囲であるポリウレタンウレア樹脂を得ることができる。
<Method for producing polyurethane urea resin>
A polyurethane urea resin can be generally produced by a reaction between a urethane prepolymer and a polyamine such as diamine, but when the urethane prepolymer (component A) and the polyamine compound (component B) are reacted, The polydispersity (weight average molecular weight / number average molecular weight) is in the range of 1.6 to 2.4 by setting the complete mixing time (θ M ) with the component B to 30 seconds or less, preferably 15 seconds or less. A polyurethane urea resin can be obtained.
完全混合時間(θM)とは、撹拌槽(反応容器など)における混合特性を表わす指標であり、n・θM(nは撹拌翼の回転数(1/秒))とRe(レイノルズ数;液の乱れ状態を表す指標)との関係を示す「n・θM−Re曲線」から求められる。完全混合時間(θM)及びn・θM−Re曲線については、例えば、「住友重機械工業 技報 vol.35 No.104 1987年8月 p74−78」、特開昭61−200842号公報、特開平6−312122号公報などに記載されている。 The complete mixing time (θ M ) is an index representing mixing characteristics in a stirring tank (such as a reaction vessel), and n · θ M (n is the number of rotations of the stirring blade (1 / second)) and Re (Reynolds number; It is obtained from an “n · θ M -Re curve” showing the relationship with the index indicating the turbulent state of the liquid. For the complete mixing time (θ M ) and n · θ M -Re curve, see, for example, “Sumitomo Heavy Industries Technical Report vol.35 No.104 August 1987 p74-78”, Japanese Patent Application Laid-Open No. 61-200842. JP-A-6-312122 and the like.
完全混合時間(θM)を、30秒以下にするための手段としては、任意の適切な方法を採用すれば良いが、撹拌槽(反応容器など)内に邪魔板等を設置し乱流を発生させる方法や、任意の適切な撹拌翼を用いる方法などが挙げられる。適切な撹拌翼としては、マックスブレンド翼、フルゾーン翼などが挙げられる。 Any appropriate method may be adopted as a means for setting the complete mixing time (θ M ) to 30 seconds or less. However, a baffle plate or the like is installed in a stirring vessel (such as a reaction vessel) to prevent turbulent flow. The method of generating, the method of using arbitrary appropriate stirring blades, etc. are mentioned. Suitable agitation blades include max blend blades, full zone blades, and the like.
また、前記の方法にてウレタンプレポリマーを製造した場合には、上記プレポリマー化反応後の反応液にB成分を添加し、連続的にポリウレタンウレア樹脂の製造を行っても良い。 Moreover, when a urethane prepolymer is produced by the above-described method, the polyurethane component may be continuously produced by adding the component B to the reaction solution after the prepolymerization reaction.
上記のポリウレタンウレア樹脂の製造方法における他の反応条件については、製造設備等を勘案して適宜決定すれば良いが、多分散度が狭い範囲にあるポリウレタンウレア樹脂が得られるという観点から、有機溶媒の存在下で、必要に応じて窒素あるいはアルゴンなどの不活性ガス雰囲気下中で、反応温度−20〜40℃の範囲で、より好ましくは、−10〜20℃の範囲で反応させればよい。反応温度が−20℃未満の場合には、鎖延長反応後半で粘度が上昇し撹拌不足となるため、また、反応温度が40℃を超える場合には、ウレア結合の形成反応が速く、A成分とB成分が接触直後に反応することによって不均一な反応となりやすく、多分散度が広がる傾向にある。上記反応温度における反応時間は0.5〜3時間程度で十分である。 The other reaction conditions in the above polyurethane urea resin production method may be appropriately determined in consideration of production equipment and the like. From the viewpoint of obtaining a polyurethane urea resin having a narrow polydispersity, an organic solvent is used. In an inert gas atmosphere such as nitrogen or argon as necessary in the presence of the reaction temperature in the range of -20 to 40 ° C, more preferably in the range of -10 to 20 ° C. . When the reaction temperature is less than -20 ° C, the viscosity increases in the latter half of the chain extension reaction, resulting in insufficient stirring. When the reaction temperature exceeds 40 ° C, the urea bond formation reaction is fast, and the component A And the B component react immediately after contact, which tends to cause a non-uniform reaction and tends to increase the polydispersity. A reaction time of about 0.5 to 3 hours is sufficient at the reaction temperature.
上記本発明の製造方法における有機溶媒としては、アセトン、メチルエチルケトン、メチルイソブチルケトン、ジエチルケトン、シクロヘキサノン、ジオキサン、トルエン、ヘキサン、ヘプタン、酢酸エチル、酢酸ブチル、ジメチルホルムアミド(DMF)、ジメチルスルホキシド(DMSO)、テトラヒドロフラン(THF)、メタノール、エタノール、イソプロピルアルコール、t−ブタノール、2−ブタノール、n−ブタノール、エチレングリコールモノメチルエーテル、エチレングリコールモノエチルエーテル、エチレングリコールモノノルマルプロピルエーテル、エチレングリコールモノイソプロピルエーテル、エチレングリコールモノブチルエーテル、エチレングリコールモノt−ブチルエーテル、プロピレングリコールモノメチルエーテル、プロピレングリコールモノエチルエーテル、プロピレングリコールモノノルマルプロピルエーテル、プロピレングリコールモノイソプロピル、プロピレングリコールモノノルマルブチルエーテル、プロピレングリコールモノt−ブチルエーテルなどのアルコール系有機溶媒も使用できる。これらの有機溶媒は、2種類以上混合して使用することも出来る。 As the organic solvent in the production method of the present invention, acetone, methyl ethyl ketone, methyl isobutyl ketone, diethyl ketone, cyclohexanone, dioxane, toluene, hexane, heptane, ethyl acetate, butyl acetate, dimethylformamide (DMF), dimethyl sulfoxide (DMSO) , Tetrahydrofuran (THF), methanol, ethanol, isopropyl alcohol, t-butanol, 2-butanol, n-butanol, ethylene glycol monomethyl ether, ethylene glycol monoethyl ether, ethylene glycol mononormal propyl ether, ethylene glycol monoisopropyl ether, ethylene Glycol monobutyl ether, ethylene glycol mono t-butyl ether, propylene glycol monome Ether, propylene glycol monoethyl ether, propylene glycol mono normal propyl ether, propylene glycol mono-isopropyl, propylene glycol monobutyl n-butyl ether, also alcoholic organic solvents such as propylene glycol monobutyl t- butyl ether may be used. These organic solvents can be used in combination of two or more.
上記有機溶媒の使用量は、効率的に反応を行うとの観点や、残留する有機溶媒の影響等の観点から、最終的に得られるポリウレタンウレア樹脂の合計量を100質量部とした際に、130〜800質量部の範囲であることが好ましく、150〜500質量部の範囲であることがより好ましい。 The amount of the organic solvent used is such that when the total amount of the polyurethane urea resin finally obtained is 100 parts by mass from the viewpoint of performing the reaction efficiently and from the viewpoint of the influence of the remaining organic solvent, etc. The range is preferably 130 to 800 parts by mass, and more preferably 150 to 500 parts by mass.
反応に際しては、反応系中のイソシアネート基と不純物としての水との反応を避けるため、各種反応試剤及び有機溶媒は、予め脱水処理を行い、十分に乾燥しておくことが好ましい。また、上記反応を行う際には、ジラウリル酸ジブチルスズ、ジメチルイミダゾール、トリエチレンジアミン、テトラメチル−1,6−ヘキサジアミン、テトラメチル−1,2−エタンジアミン、1,4−ジアザビシクロ[2,2,2]オクタンなどの触媒を新たに加えても良いし、プレポリマー反応で使用した場合には除去することなくそのまま使用してもよい。触媒を使用する際の添加量としては、ポリウレタンウレア樹脂の合計100質量部に対して0.001〜1質量部であることが好ましい。 In the reaction, in order to avoid a reaction between an isocyanate group in the reaction system and water as an impurity, it is preferable that various reaction reagents and an organic solvent are subjected to dehydration in advance and sufficiently dried. In the above reaction, dibutyltin dilaurate, dimethylimidazole, triethylenediamine, tetramethyl-1,6-hexadiamine, tetramethyl-1,2-ethanediamine, 1,4-diazabicyclo [2,2, 2] A catalyst such as octane may be newly added, or when used in a prepolymer reaction, it may be used as it is without being removed. As an addition amount at the time of using a catalyst, it is preferable that it is 0.001-1 mass part with respect to a total of 100 mass parts of polyurethane urea resins.
本発明のポリウレタンウレア樹脂(I成分)を合成する際に、分子内に1つのイソシアネート基と反応しうる基を有する化合物(C成分)を併用することも可能である。このC成分を使用することにより、分子鎖の末端がキャッピングされたポリウレタンウレア樹脂となる。 When synthesizing the polyurethane urea resin (component I) of the present invention, it is also possible to use a compound (component C) having a group capable of reacting with one isocyanate group in the molecule. By using this C component, it becomes a polyurethane urea resin in which the end of the molecular chain is capped.
上記、分子鎖の末端がキャッピングされたポリウレタンウレア樹脂を得る方法(以下、「末端修飾反応」とも言う)は、前述のA成分とB成分の反応が終了し、末端にイソシアネート基を有するポリウレタンウレア樹脂が有機溶剤に溶解している反応液に、必要に応じて有機溶剤で希釈したC成分を滴下して加える方法が好適である。また、前述のA成分とB成分の反応の際に添加したアルコール系有機溶剤をC成分として末端修飾反応に使用する場合には、新たにC成分を添加しなくても良い。 The method for obtaining a polyurethane urea resin with the molecular chain end capped (hereinafter also referred to as “terminal modification reaction”) is the polyurethane urea having an isocyanate group at the terminal after the reaction of the above-mentioned component A and component B is completed. A method in which a component C diluted with an organic solvent is added dropwise to the reaction solution in which the resin is dissolved in the organic solvent, if necessary, is preferable. Further, when the alcohol-based organic solvent added at the time of the reaction between the A component and the B component is used as the C component for the terminal modification reaction, it is not necessary to newly add the C component.
上記の末端修飾反応は、有機溶媒の存在下で、必要に応じて窒素あるいはアルゴンなどの不活性ガス雰囲気下中で実施すれば良い。反応温度は、C成分に含まれるイソシアネート基と反応しうる基がアミノ基の場合には、前述のA成分とB成分の反応の時と同様な温度−20〜30℃で反応させればよい。しかしながら、C成分に含まれるイソシアネート基と反応しうる基がアミノ基以外の場合には、イソシアネート基との反応速度が遅いため、30℃を超え130℃以下で反応させることが好ましい。 The above terminal modification reaction may be performed in an inert gas atmosphere such as nitrogen or argon as required in the presence of an organic solvent. As for the reaction temperature, when the group capable of reacting with the isocyanate group contained in the C component is an amino group, the reaction may be carried out at a temperature of -20 to 30 ° C. similar to the reaction of the aforementioned A component and B component. . However, when the group capable of reacting with the isocyanate group contained in the component C is other than an amino group, the reaction rate with the isocyanate group is slow, so that the reaction is preferably performed at a temperature higher than 30 ° C. and not higher than 130 ° C.
反応時間は、C成分に含まれるイソシアネート基と反応しうる基がアミノ基の場合には0.5〜3時間程度で、C成分に含まれるイソシアネート基と反応しうる基がアミノ基以外の場合には1時間〜24時間程度反応させればよい。 The reaction time is about 0.5 to 3 hours when the group capable of reacting with the isocyanate group contained in the C component is an amino group, and when the group capable of reacting with the isocyanate group contained in the C component is other than an amino group Is allowed to react for about 1 to 24 hours.
有機溶媒としては、前述のプレポリマー反応、及びA成分とB成分の反応に使用した有機溶剤を使用できる。また、当然のことながら、前述のプレポリマー反応、及びA成分とB成分の反応で使用した有機溶剤を含んだ状態で、末端修飾反応を実施しても構わない。 As an organic solvent, the organic solvent used for the above-mentioned prepolymer reaction and reaction of A component and B component can be used. Moreover, as a matter of course, the terminal modification reaction may be performed in a state in which the organic solvent used in the above-described prepolymer reaction and the reaction between the A component and the B component is included.
末端修飾反応における有機溶媒の使用量は、最終的に得られるA成分の合計量を100質量部とした際に、130〜800質量部の範囲であることが好ましい。 The amount of the organic solvent used in the terminal modification reaction is preferably in the range of 130 to 800 parts by mass when the total amount of component A finally obtained is 100 parts by mass.
反応に際しては、反応系中のイソシアネート基と不純物としての水との反応を避けるため、各種反応試剤及び有機溶媒は、予め脱水処理を行い、十分に乾燥しておくことが好ましい。また、上記反応を行う際には、ジラウリル酸ジブチルスズ、ジメチルイミダゾール、トリエチレンジアミン、テトラメチル−1,6−ヘキサジアミン、テトラメチル−1,2−エタンジアミン、1,4−ジアザビシクロ[2,2,2]オクタンなどの触媒を新たに加えても良いし、プレポリマー反応までに触媒を使用した場合には除去することなくそのまま使用してもよい。触媒を使用する際の添加量としては、A成分の合計100質量部に対して0.001〜1質量部であることが好ましい。 In the reaction, in order to avoid a reaction between an isocyanate group in the reaction system and water as an impurity, it is preferable that various reaction reagents and an organic solvent are subjected to dehydration in advance and sufficiently dried. In the above reaction, dibutyltin dilaurate, dimethylimidazole, triethylenediamine, tetramethyl-1,6-hexadiamine, tetramethyl-1,2-ethanediamine, 1,4-diazabicyclo [2,2, 2] A catalyst such as octane may be newly added, or when the catalyst is used before the prepolymer reaction, it may be used as it is without being removed. As an addition amount at the time of using a catalyst, it is preferable that it is 0.001-1 mass part with respect to a total of 100 mass parts of A component.
次に、本発明のII成分であるフォトクロミック化合物について説明する。 Next, the photochromic compound which is the II component of the present invention will be described.
<II成分:フォトクロミック化合物>
本発明のフォトクロミック組成物でII成分として用いるフォトクロミック化合物をとしては、クロメン化合物、フルギミド化合物、スピロオキサジン化合物、スピロピラン化合物などの公知のフォトクロミック化合物を何ら制限なく使用することが出来る。これらは、単独使用でもよく、2種類以上を併用しても良い。
<II component: photochromic compound>
As the photochromic compound used as the II component in the photochromic composition of the present invention, known photochromic compounds such as a chromene compound, a fulgimide compound, a spirooxazine compound, and a spiropyran compound can be used without any limitation. These may be used alone or in combination of two or more.
上記のフルギミド化合物、スピロオキサジン化合物、スピロピラン化合物およびクロメン化合物としては、例えば特開平2−28154号公報、特開昭62−288830号公報、WO94/22850号パンフレット、WO96/14596号パンフレットなどに記載されている化合物を挙げることができる。 Examples of the fulgimide compound, spirooxazine compound, spiropyran compound and chromene compound described in JP-A-2-28154, JP-A-62-2288830, WO94 / 22850, WO96 / 14596, etc. Can be mentioned.
これら他のフォトクロミック化合物の中でも、発色濃度、初期着色、耐久性、退色速度などのフォトクロミック特性の観点から、インデノ(2,1−f)ナフト(2,1−b)ピラン骨格を有するクロメン化合物を1種類以上用いることがより好ましい。さらにこれらクロメン化合物中でもその分子量が540以上の化合物は、発色濃度および退色速度に特に優れるため好適である。 Among these other photochromic compounds, a chromene compound having an indeno (2,1-f) naphtho (2,1-b) pyran skeleton from the viewpoint of photochromic properties such as color density, initial coloring, durability, and fading speed. It is more preferable to use one or more types. Further, among these chromene compounds, compounds having a molecular weight of 540 or more are preferable because they are particularly excellent in color density and fading speed.
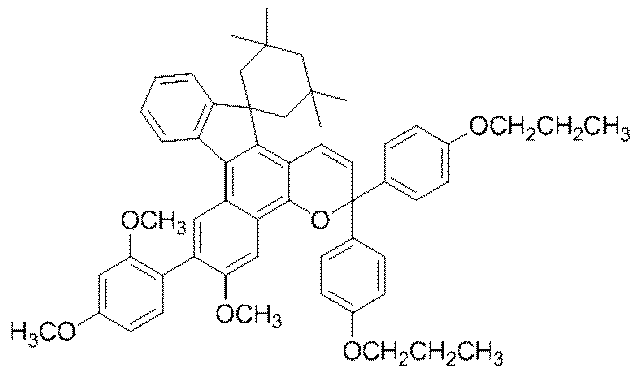
本発明において特に好適に使用できるフォトクロミック化合物を具体的に例示すると、以下のものが挙げられる。 Specific examples of photochromic compounds that can be particularly preferably used in the present invention include the following.
本発明のフォトクロミック組成物におけるII成分の配合量は、フォトクロミック特性の観点から、I成分100質量部に対して0.1〜20.0質量部とすることが好適である。上記配合量が少なすぎる場合には、十分な発色濃度や耐久性が得られない傾向があり、多すぎる場合には、フォトクロミック化合物の種類にもよるが、フォトクロミック組成物が溶解しにくくなり、組成物の均一性が低下する傾向があるばかりでなく、接着力(密着力)が低下する傾向もある。発色濃度や耐久性といったフォトクロミック特性を維持したまま、プラスチックフィルムなどの光学基材との接着性を十分に保持するためには、II成分の添加量はI成分100質量部に対して0.5〜10.0質量部、特に1.0〜7.0質量部とすることがより好ましい。ただし、本発明のフォトクロミック組成物にIII成分を配合する場合には、II成分の添加量は、I成分とIII成分の合計量100質量部に対して0.1〜20.0質量部とすることが好ましく、0.5〜10.0質量部とすることがより好ましく、1.0〜7.0質量部とすることがさらに好ましい。 The blending amount of the II component in the photochromic composition of the present invention is preferably 0.1 to 20.0 parts by mass with respect to 100 parts by mass of the I component from the viewpoint of photochromic properties. If the amount is too small, there is a tendency that sufficient color density and durability cannot be obtained.If the amount is too large, depending on the type of photochromic compound, the photochromic composition becomes difficult to dissolve, and the composition Not only the uniformity of the object tends to decrease, but also the adhesive strength (adhesion) tends to decrease. In order to maintain sufficient adhesion to an optical substrate such as a plastic film while maintaining photochromic properties such as color density and durability, the amount of II component added is 0.5 to 100 parts by mass of I component. To 10.0 parts by mass, more preferably 1.0 to 7.0 parts by mass. However, when III component is mix | blended with the photochromic composition of this invention, the addition amount of II component shall be 0.1-20.0 mass parts with respect to 100 mass parts of total amounts of I component and III component. It is preferably 0.5 to 10.0 parts by mass, and more preferably 1.0 to 7.0 parts by mass.
<III成分:分子内に少なくとも2つのイソシアネート基を有するポリイソシアネート化合物>
本発明のフォトクロミック組成物において、前記ポリウレタンウレア樹脂(I成分)と、分子内に少なくとも2つのイソシアネート基を有するポリイソシアネート化合物(III成分)とを反応させて得られる生成物を含むことにより、後述する光学物品の接着(密着)強度をより向上させることができるため好ましい。III成分の分子内に、2つ以上のイソシアネート基を有することにより、フォトクロミック性接着層を形成する際に、I成分と反応し、橋架け構造を有するポリウレタンウレア樹脂を生成することができる。この橋架け構造がI成分中に形成されたことによって、ポリウレタンウレア樹脂の耐熱性が向上するとともに、凝集破壊が起こりにくくなったため、接着性向上の効果が高くなると考えられる。ただし、操作性、得られるフォトクロミック組成物の粘度、保存安定性等を考慮すると、イソシアネート基の数は2〜3であることが好ましい。その中でも、2級炭素に結合したイソシアネート基を有する化合物を使用することが好ましい。これらは、単独で使用してもよく、2種類以上を併用してもよい。
<III component: polyisocyanate compound having at least two isocyanate groups in the molecule>
The photochromic composition of the present invention includes a product obtained by reacting the polyurethane urea resin (component I) with a polyisocyanate compound (component III) having at least two isocyanate groups in the molecule. This is preferable because the adhesion (adhesion) strength of the optical article can be further improved. By having two or more isocyanate groups in the molecule of the III component, it is possible to produce a polyurethane urea resin having a bridge structure by reacting with the I component when the photochromic adhesive layer is formed. By forming this bridge structure in the component I, the heat resistance of the polyurethane urea resin is improved, and cohesive failure is less likely to occur. However, considering the operability, the viscosity of the resulting photochromic composition, storage stability, etc., the number of isocyanate groups is preferably 2 to 3. Among these, it is preferable to use a compound having an isocyanate group bonded to secondary carbon. These may be used alone or in combination of two or more.
上記III成分として具体的には、4,4’−メチレンビス(シクロヘキシルイソシアネート)の異性体混合物、シクロブタン−1,3−ジイソシアネート、シクロヘキサン−1,3−ジイソシアネート、シクロヘキサン−1,4−ジイソシアネート、ヘキサヒドロトルエン−2,4−ジイソシアネート、ヘキサヒドロトルエン−2,6−ジイソシアネート、ヘキサヒドロフェニレン−1,3−ジイソシアネート、ヘキサヒドロフェニレン−1,4−ジイソシアネート、及びこれらイソシアネート化合物や、イソホロンジイソシアネートの3量体(イソシアヌレート化合物)などが挙げられる。 Specific examples of the III component include isomer mixtures of 4,4′-methylenebis (cyclohexyl isocyanate), cyclobutane-1,3-diisocyanate, cyclohexane-1,3-diisocyanate, cyclohexane-1,4-diisocyanate, hexahydro Toluene-2,4-diisocyanate, hexahydrotoluene-2,6-diisocyanate, hexahydrophenylene-1,3-diisocyanate, hexahydrophenylene-1,4-diisocyanate, and trimers of these isocyanate compounds and isophorone diisocyanate (Isocyanurate compound) and the like.
本発明のフォトクロミック組成物において、III成分の分子量は、特に制限されるものではないが、1000未満であることが好ましい。該III成分の分子量が1000以上の場合、得られるフォトクロミック性接着層の耐熱性、および膜強度が低下する傾向がある。これは、分子量が大きいIII成分を用いると、イソシアネート基間の結合数が増える傾向にあり、たとえ橋架け構造を形成したとしても架橋点間の距離が長くなり、耐熱性があまり向上しないために接着性も十分に向上しないと考えられる。よって、III成分の分子量は、1000未満であることが好ましく、より好ましくは800以下、最も好ましくは500以下である。このIII成分は、前記の通り、ポリマーではない方が好ましい。そのため、III成分の分子量は、III成分そのものの分子量を指す。III成分の分子量の下限は、その単体化合物の分子量であり、特に制限されるものではないが、100である。 In the photochromic composition of the present invention, the molecular weight of the III component is not particularly limited, but is preferably less than 1000. When the molecular weight of the III component is 1000 or more, the heat resistance and film strength of the resulting photochromic adhesive layer tend to decrease. This is because when the III component having a large molecular weight is used, the number of bonds between isocyanate groups tends to increase, and even if a bridge structure is formed, the distance between the cross-linking points becomes long and the heat resistance is not improved so much. It is considered that the adhesion is not sufficiently improved. Therefore, the molecular weight of the III component is preferably less than 1000, more preferably 800 or less, and most preferably 500 or less. As described above, the III component is preferably not a polymer. Therefore, the molecular weight of the III component refers to the molecular weight of the III component itself. The lower limit of the molecular weight of the III component is the molecular weight of the simple compound, and is 100, although not particularly limited.
本発明のフォトクロミック組成物におけるIII成分の配合量は、接着性、耐熱性、耐汗性、及びフォトクロミック特性の観点から、I成分100質量部に対して4.0〜20.0質量部とすることが好適である。III成分の配合量がこの範囲を満足することにより、得られるフォトクロミック組成物が優れた効果を発揮する。上記配合量が少なすぎる場合には、十分な接着性、及び耐熱性の向上効果が得られず、多すぎる場合には、該フォトクロミック組成物から得られる接着層の白濁、接着性の低下、フォトクロミック化合物の耐久性低下などが起こる傾向がある。発色濃度や耐久性といったフォトクロミック特性を維持したまま、プラスチックフィルムなどの光学基材との接着性を向上させるためには、III成分の配合量は、I成分100質量部に対して6.0〜17.5質量部、特に7.0〜15.0質量部とすることが好ましい。この際、III成分のイソシアネート基の割合は、I成分100質量部に対して1.0〜10.0質量部、より好ましくは1.5〜6.0質量部、もっとも好ましくは2.0〜5.0質量部である。ここで、イソシアネート基の量は、III成分の分子量、1分子当たりのイソシアネート基の数、及びイソシアネート基の分子量から求めることができる。 The compounding quantity of the III component in the photochromic composition of this invention shall be 4.0-20.0 mass parts with respect to 100 mass parts of I components from a viewpoint of adhesiveness, heat resistance, sweat resistance, and a photochromic characteristic. Is preferred. When the blending amount of the III component satisfies this range, the resulting photochromic composition exhibits an excellent effect. When the blending amount is too small, sufficient adhesion and heat resistance cannot be improved. When the blending amount is too large, the cloudiness of the adhesive layer obtained from the photochromic composition, a decrease in adhesiveness, and photochromic are obtained. There is a tendency for the durability of the compound to decrease. In order to improve adhesiveness with an optical substrate such as a plastic film while maintaining photochromic properties such as color density and durability, the amount of the III component is 6.0 to 100 parts by mass of the I component. It is preferable to set it as 17.5 mass parts, especially 7.0-15.0 mass parts. Under the present circumstances, the ratio of the isocyanate group of III component is 1.0-10.0 mass parts with respect to 100 mass parts of I components, More preferably, it is 1.5-6.0 mass parts, Most preferably, it is 2.0- 5.0 parts by mass. Here, the amount of the isocyanate group can be determined from the molecular weight of the III component, the number of isocyanate groups per molecule, and the molecular weight of the isocyanate group.
I成分とIII成分との反応生成物は、本発明のフォトクロミック組成物を用いて樹脂製シート又はフィルムどうしを貼付して得られる積層体の物性、得られた積層体を用いて曲げ加工や射出成型により成型体を製造する際の加工安定性の観点、及びそれら積層体の接着性の観点、さらにはこれら積層シート又は成型体の表面にハードコート層を形成する場合において、ハードコート液を塗布したり、硬化させたりするときの加工性の観点から、通常60〜200℃、特に80〜150℃の耐熱性を有していることが好ましい。なお、ここでいう耐熱性とは、熱機械測定装置(セイコーインスツルメント社製、TMA120C)を用いて、下記条件で測定した軟化点を意味する。
〔測定条件〕 昇温速度:10℃/分、測定温度範囲:30〜200℃、プローブ:先端径0.5mmの針入プローブ。
The reaction product of the I component and the III component is a physical property of a laminate obtained by pasting resin sheets or films using the photochromic composition of the present invention, and bending and injection using the obtained laminate. Applying a hard coat solution in the case of forming a hard coat layer on the surface of the laminated sheet or the molded product, from the viewpoint of processing stability when producing a molded product by molding, and the adhesive property of the laminate. From the viewpoint of workability when it is cured or cured, it preferably has a heat resistance of usually 60 to 200 ° C., particularly 80 to 150 ° C. In addition, heat resistance here means the softening point measured on the following conditions using the thermomechanical measuring apparatus (The Seiko Instruments company make, TMA120C).
[Measurement Conditions] Temperature rising rate: 10 ° C./min, measurement temperature range: 30 to 200 ° C., probe: needle-inserted probe with a tip diameter of 0.5 mm.
<その他の成分>
さらに、本発明で使用するフォトクロミック組成物には、フォトクロミック化合物の耐久性の向上、発色速度の向上、退色速度の向上や製膜性のために、I成分を溶解できる溶媒、界面活性剤、酸化防止剤、ラジカル補足剤、紫外線安定剤、紫外線吸収剤、離型剤、着色防止剤、帯電防止剤、蛍光染料、染料、顔料、香料、可塑剤等の添加剤を添加しても良い。添加するこれら添加剤としては、公知の化合物が何ら制限なく使用される。
<Other ingredients>
Furthermore, the photochromic composition used in the present invention includes a solvent capable of dissolving the component I, a surfactant, an oxidation agent for improving the durability of the photochromic compound, improving the color development speed, improving the fading speed, and forming the film. Additives such as inhibitors, radical scavengers, UV stabilizers, UV absorbers, mold release agents, anti-coloring agents, antistatic agents, fluorescent dyes, dyes, pigments, fragrances, and plasticizers may be added. As these additives to be added, known compounds are used without any limitation.
例えば、I成分を溶解できる溶媒としては、ジメチルホルムアミド、ジメチルスルホキシドなどが挙げられる。 For example, examples of the solvent capable of dissolving the component I include dimethylformamide and dimethyl sulfoxide.
例えば、界面活性剤としては、ノニオン系、アニオン系、カチオン系の何れも使用できるが、フォトクロミック組成物への溶解性からノニオン系界面活性剤を用いるのが好ましい。好適に使用できるノニオン性界面活性剤を具体的に挙げると、ソルビタン脂肪酸エステル、グリセリン脂肪酸エステル、デカグリセリン脂肪酸エステル、プロピレングリコール・ペンタエリスリトール脂肪酸エステル、ポリオキシエチレンソルビタン脂肪酸エステル、ポリオキシエチレンソルビット脂肪酸エステル、ポリオキシエチレングリセリン脂肪酸エステル、ポリエチレングリコール脂肪酸エステル、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンフィトステロール・フィトスタノール、ポリオキシエチレンポリオキシプロピレンアルキルエーテル、ポリオキシエチレンアルキルフェニルエーテル、ポリオキシエチレンヒマシ油・硬化ヒマシ油、ポリオキシエチレンラノリン・ラノリンアルコール・ミツロウ誘導体、ポリオキシエチレンアルキルアミン・脂肪酸アミド、ポリオキシエチレンアルキルフェニルホルムアルデヒド縮合物、単一鎖ポリオキシエチレンアルキルエーテル、さらにはシリコーン系やフッ素系の界面活性剤等を挙げることができる。 For example, as the surfactant, any of a nonionic surfactant, an anionic surfactant, and a cationic surfactant can be used, but it is preferable to use a nonionic surfactant because of its solubility in the photochromic composition. Specific examples of nonionic surfactants that can be suitably used include sorbitan fatty acid ester, glycerin fatty acid ester, decaglycerin fatty acid ester, propylene glycol / pentaerythritol fatty acid ester, polyoxyethylene sorbitan fatty acid ester, polyoxyethylene sorbit fatty acid ester , Polyoxyethylene glycerin fatty acid ester, polyethylene glycol fatty acid ester, polyoxyethylene alkyl ether, polyoxyethylene phytosterol / phytostanol, polyoxyethylene polyoxypropylene alkyl ether, polyoxyethylene alkylphenyl ether, polyoxyethylene castor oil / cured Castor oil, polyoxyethylene lanolin, lanolin alcohol, beeswax derivative, poly Alkoxy polyoxyethylene alkyl amine fatty acid amides, polyoxyethylene alkylphenyl formaldehyde condensate, a single-chain polyoxyethylene alkyl ethers, and more may be mentioned surfactants of the silicone-based or fluorine.
界面活性剤の使用に当たっては、2種以上を混合して使用しても良い。界面活性剤の添加量は、I成分100質量部に対し、0.001〜5質量部の範囲が好ましい。 In using the surfactant, two or more kinds may be mixed and used. The addition amount of the surfactant is preferably in the range of 0.001 to 5 parts by mass with respect to 100 parts by mass of the I component.
また、酸化防止剤、ラジカル補足剤、紫外線安定剤、紫外線吸収剤としては、ヒンダードアミン光安定剤、ヒンダードフェノール酸化防止剤、フェノール系ラジカル補足剤、イオウ系酸化防止剤、リン系酸化防止剤、トリアジン系化合物、ベンゾトリアゾール系化合物、ベンゾフェノン系化合物等を好適に使用できる。これら酸化防止剤、ラジカル補足剤、紫外線安定剤、紫外線吸収剤は、2種以上を混合して使用しても良い。さらにこれらの添加剤の使用に当たっては、界面活性剤と酸化防止剤、ラジカル補足剤、紫外線安定剤、紫外線吸収剤を併用して使用しても良い。これら酸化防止剤、ラジカル補足剤、紫外線安定剤、紫外線吸収剤の添加量は、I成分100質量部に対し、0.001〜20質量部の範囲が好ましい。但し、これらの添加剤を使用しすぎると、ポリカーボネート樹脂製の樹脂製シート又はフィルムなどへのフォトクロミック組成物の接着性が低下するため、その添加量は好ましくは7質量部以下、より好ましくは3質量部以下、最も好ましくは1質量部以下である。 Antioxidants, radical scavengers, UV stabilizers, UV absorbers include hindered amine light stabilizers, hindered phenol antioxidants, phenolic radical scavengers, sulfur antioxidants, phosphorus antioxidants, A triazine compound, a benzotriazole compound, a benzophenone compound, or the like can be preferably used. These antioxidants, radical scavengers, ultraviolet stabilizers, and ultraviolet absorbers may be used in combination of two or more. Furthermore, when using these additives, surfactants and antioxidants, radical scavengers, ultraviolet stabilizers, and ultraviolet absorbers may be used in combination. The addition amount of these antioxidants, radical scavengers, ultraviolet stabilizers and ultraviolet absorbers is preferably in the range of 0.001 to 20 parts by mass with respect to 100 parts by mass of the I component. However, if these additives are used excessively, the adhesion of the photochromic composition to a resin sheet or film made of polycarbonate resin is lowered, so the amount added is preferably 7 parts by mass or less, more preferably 3 It is 1 part by mass or less, most preferably 1 part by mass or less.
<フォトクロミック組成物の製造方法>
本発明のフォトクロミック組成物は、上記I成分、II成分、及びその他の成分を混合することにより製造することができる。各成分を混合する順序は、特に制限されるものではない。
<Method for producing photochromic composition>
The photochromic composition of this invention can be manufactured by mixing the said I component, II component, and another component. The order in which the components are mixed is not particularly limited.
例えば、各成分を溶融混練してフォトクロミック組成物としペレット化することも可能であり、そのままシート成型することも可能である。また、ジメチルホルムアミドのような有機溶媒を使用する場合には、各成分を有機溶剤に溶かすことでフォトクロミック組成物を得ることができる。 For example, each component can be melt-kneaded and pelletized into a photochromic composition, or it can be formed into a sheet as it is. When an organic solvent such as dimethylformamide is used, a photochromic composition can be obtained by dissolving each component in the organic solvent.
このようにして得られた本発明のフォトクロミック組成物は、フォトクロミック性接着剤、特にポリカーボネート樹脂製の樹脂製シート又はフィルムどうしを接合するためのフォトクロミック性接着剤として好適に使用できる。そして、本発明のフォトクロミック組成物からなる接着層を介して樹脂製シート又はフィルムを互いに接合することにより、積層体を得ることができる。 The photochromic composition of the present invention thus obtained can be suitably used as a photochromic adhesive, particularly a photochromic adhesive for joining resin sheets or films made of polycarbonate resin. And a laminated body can be obtained by mutually bonding a resin-made sheet | seat or a film through the contact bonding layer which consists of a photochromic composition of this invention.
以上のような製造方法の中でも、本発明のフォトクロミック組成物は、一般的な有機溶媒に溶解しない成分を含むため、次のような方法で製造することが好ましい。
すなわち、
(I)ポリウレタンウレア樹脂、(II)フォトクロミック化合物、必要に応じて、(III)ポリイソシアネート化合物、および、有機溶媒を所定の配合量で混合した後、乾燥して有機溶媒を除去すると共に、前記(I)ポリウレタンウレア樹脂と前記(III)ポリイソシアネート化合物とを反応させることにより、フォトクロミック組成物を製造する方法である。この方法では、I成分、II成分、III成分、及び有機溶媒を含む組成物から有機溶媒を除去する工程を経ることで本発明のフォトクロミック組成物を得ることができるため、以下、I成分、II成分、III成分、及び有機溶媒を含む組成物を前駆体組成物とする場合もある。この前記前駆体組成物には、上記した「その他成分」を配合することも可能である。
Among the production methods as described above, the photochromic composition of the present invention contains a component that is not dissolved in a general organic solvent, and thus is preferably produced by the following method.
That is,
(I) Polyurethane urea resin, (II) photochromic compound, and if necessary, (III) polyisocyanate compound, and organic solvent are mixed in a predetermined amount, and then dried to remove the organic solvent, (I) A method for producing a photochromic composition by reacting a polyurethane urea resin with the (III) polyisocyanate compound. In this method, since the photochromic composition of the present invention can be obtained through a step of removing the organic solvent from the composition containing the I component, the II component, the III component, and the organic solvent, hereinafter, the I component, II In some cases, the precursor composition is a composition containing the component, the III component, and the organic solvent. It is also possible to mix the above-mentioned “other components” with the precursor composition.
前駆体組成物からフォトクロミック組成物を製造するためには、例えば、前駆体組成物を基材上に塗布した後、乾燥して有機溶媒を除去する際に、I成分とIII成分とを反応させることが好ましい。先ず、有機溶媒について説明する。 In order to produce a photochromic composition from a precursor composition, for example, after applying the precursor composition on a substrate, the organic solvent is removed by drying, and then the I component and the III component are reacted. It is preferable. First, the organic solvent will be described.
<有機溶媒>
上記の製造方法において有機溶媒を使用することにより、ポリウレタンウレア樹脂(I成分)、ポリイソシアネート化合物(III成分)、及びフォトクロミック化合物(II成分)、さらには、必要に応じて添加されるその他の成分が混合しやすくなり、前駆体組成物の均一性を向上させることができる。また、前駆体組成物の粘度を適度に調整することができ、樹脂製シート又はフィルムに前駆体組成物を塗布するときの操作性および塗布層厚の均一性を高くすることもできる。なお、樹脂製シート又はフィルムとして有機溶媒に侵され易い材質のものを使用した場合には、外観不良が生じたり、フォトクロミック特性が低下したりするという問題が発生することが懸念されるが、このような問題は、後述する方法を採用することにより回避することが出来る。また、前駆体組成物においては、後述するように、様々な種類の溶媒が使用できるので、溶媒として樹脂製シート又はフィルムを侵し難い溶媒を選択して使用することによっても上記問題の発生を防止することができる。
<Organic solvent>
By using an organic solvent in the above production method, polyurethane urea resin (component I), polyisocyanate compound (component III), photochromic compound (component II), and other components added as necessary Can be easily mixed, and the uniformity of the precursor composition can be improved. Moreover, the viscosity of a precursor composition can be adjusted moderately, and the operativity at the time of apply | coating a precursor composition to a resin-made sheet | seat or a film, and the uniformity of the coating layer thickness can also be made high. If a resin sheet or film that is easily affected by an organic solvent is used, there may be a problem that the appearance is poor or the photochromic properties are deteriorated. Such a problem can be avoided by adopting a method described later. In the precursor composition, as described later, since various types of solvents can be used, the occurrence of the above problems can be prevented by selecting and using a solvent that does not easily attack the resin sheet or film. can do.
好適に使用できる有機溶媒を例示すれば、メタノール、エタノール、n−プロパノール、i−プロパノール、2−ペンタノール、3−ペンタノール、3−メチル−2−ブタノール、4−メチル−2−ペンタノール、n−ブタノール、t−ブタノール、2−ブタノール、t−ペンチルアルコール2,2,2−トリフルオロエタノール等のアルコール類;エチレングリコールモノメチルエーテル、エチレングリコールモノイソプロピルエーテル、エチレングリコールモノエチルエーテル、エチレングリコールモノ−n−プロピルエーテル、エチレングリコールモノ−n−ブチルエーテル、エチレングリコールモノ−t−ブチルエーテル、プロピレングリコールモノメチルエーテル、プロピレングリコールモノエチルエーテル、プロピレングリコール−n−ブチルエーテル、エチレングリコールジメチルエーテル等の多価アルコール誘導体;ジアセトンアルコール;メチルエチルケトン、ジエチルケトン、n−プロピルメチルケトン、メチルイソブチルケトン、ジイソプロピルケトン、n−ブチルメチルケトンなどのケトン類;トルエン;ヘキサン;ヘプタン;酢酸エチル、酢酸−2−メトキシエチル、酢酸−2−エトキシエチルなどのアセテート類;ジメチルホルムアミド(DMF);ジメチルスルホキシド(DMSO);テトラヒドロフラン(THF);シクロヘキサノン;クロロホルム;ジクロロメタン及びこれらの組み合せを挙げることができる。 Examples of organic solvents that can be suitably used include methanol, ethanol, n-propanol, i-propanol, 2-pentanol, 3-pentanol, 3-methyl-2-butanol, 4-methyl-2-pentanol, alcohols such as n-butanol, t-butanol, 2-butanol, t-pentyl alcohol 2,2,2-trifluoroethanol; ethylene glycol monomethyl ether, ethylene glycol monoisopropyl ether, ethylene glycol monoethyl ether, ethylene glycol mono -N-propyl ether, ethylene glycol mono-n-butyl ether, ethylene glycol mono-t-butyl ether, propylene glycol monomethyl ether, propylene glycol monoethyl ether, propylene glycol- Polyhydric alcohol derivatives such as butyl ether and ethylene glycol dimethyl ether; diacetone alcohol; ketones such as methyl ethyl ketone, diethyl ketone, n-propyl methyl ketone, methyl isobutyl ketone, diisopropyl ketone and n-butyl methyl ketone; toluene; hexane; heptane Acetates such as ethyl acetate, 2-methoxyethyl acetate, and 2-ethoxyethyl acetate; dimethylformamide (DMF); dimethyl sulfoxide (DMSO); tetrahydrofuran (THF); cyclohexanone; chloroform; dichloromethane and combinations thereof be able to.
これらの中から、使用するI成分の種類や樹脂製シート又はフィルムの材質に応じて適宜選定して使用すればよいが、前駆体組成物にはポリイソシアネート化合物(III成分)が含まれるため、イソシアネート基と反応する基を含まない有機溶剤を使用することがより好ましい。よって、より好適なD成分としては、I成分の溶解性、及びIII成分への非反応性の観点から、メチルエチルケトン、ジエチルケトン、n−プロピルメチルケトン、メチルイソブチルケトン、ジイソプロピルケトン、n−ブチルメチルケトンなどのケトン類、酢酸エチル、酢酸−2−メトキシエチル、酢酸−2−エトキシエチルなどのアセテート類;DMF;DMSO;THF;シクロペンタノン、シクロヘキサノン;クロロホルム;ジクロロメタンなどが挙げられる。 Among these, the precursor composition may contain a polyisocyanate compound (III component), although it may be appropriately selected and used depending on the type of the I component used and the material of the resin sheet or film. It is more preferable to use an organic solvent that does not contain a group that reacts with an isocyanate group. Therefore, more preferable D component is methyl ethyl ketone, diethyl ketone, n-propyl methyl ketone, methyl isobutyl ketone, diisopropyl ketone, n-butyl methyl from the viewpoint of solubility of I component and non-reactivity to III component. Examples include ketones such as ketone, acetates such as ethyl acetate, 2-methoxyethyl acetate, and 2-ethoxyethyl acetate; DMF; DMSO; THF; cyclopentanone, cyclohexanone; chloroform;
また、外観良好に塗工し、短時間で有機溶媒を揮発するためには、固形分濃度を高くし、さらには粘度を低くすることが重要である。溶解性を向上させるためには、上記のような有機溶媒を使用することが好ましいが、粘度を低下させるためには、アルコールなどのプロトン性有機溶媒を使用することが好ましい。その中でも、ポリイソシアネート化合物(III成分)のイソシアネート基との反応性を考慮すれば、2級及び3級アルコールが好ましく、3級アルコールであることがより好ましい。好適な2級アルコールとしてはi−プロパノール、2−ブタノール、2−ペンタノール、3−ペンタノール、3−メチル−2−ブタノール、4−メチル−2−ペンタノール、プロピレングリコールモノメチルエーテル、プロピレングリコールモノエチルエーテル、プロピレングリコール−n−ブチルエーテルなど、3級アルコールとしてはt−ブタノール、t−ペンチルアルコールなどが挙げられる。これら2級、または3級アルコールは、単独で使用することもできるし、2種類以上を混合して使用することもできる。 Further, in order to coat with good appearance and volatilize the organic solvent in a short time, it is important to increase the solid content concentration and further reduce the viscosity. In order to improve the solubility, it is preferable to use the organic solvent as described above, but in order to reduce the viscosity, it is preferable to use a protic organic solvent such as alcohol. Among these, secondary and tertiary alcohols are preferable, and tertiary alcohols are more preferable in consideration of reactivity with an isocyanate group of a polyisocyanate compound (III component). Suitable secondary alcohols include i-propanol, 2-butanol, 2-pentanol, 3-pentanol, 3-methyl-2-butanol, 4-methyl-2-pentanol, propylene glycol monomethyl ether, propylene glycol mono Examples of tertiary alcohols such as ethyl ether and propylene glycol-n-butyl ether include t-butanol and t-pentyl alcohol. These secondary or tertiary alcohols can be used alone or in combination of two or more.
しかしながら、本発明のフォトクロミック組成物に用いるポリウレタンウレア樹脂(I成分)の種類によっては、上記2級、または3級アルコールに溶け難い場合がある。よって、上述のケトン類などの良溶媒と、2級、または3級アルコールを組み合わせることが好ましい。良溶媒のケトン類と、2級または3級アルコールを組み合わせて使用することにより、I成分の溶解性を維持しながら、前駆体組成物の粘度を低下させることが可能となる。また、これら2種類以上の有機溶剤を組み合わせる場合には、良溶媒の沸点が、2級、または3級アルコールの沸点よりも高い温度となるように組み合わせることが好ましい。 However, depending on the type of polyurethane urea resin (component I) used in the photochromic composition of the present invention, it may be difficult to dissolve in the secondary or tertiary alcohol. Therefore, it is preferable to combine a good solvent such as the aforementioned ketones with a secondary or tertiary alcohol. By using a combination of a good solvent ketone and a secondary or tertiary alcohol, the viscosity of the precursor composition can be lowered while maintaining the solubility of the component I. Moreover, when combining these 2 or more types of organic solvents, it is preferable to combine so that the boiling point of a good solvent may become temperature higher than the boiling point of a secondary or tertiary alcohol.
用いる有機溶媒における2級、または3級アルコールの配合比率は、良溶媒のケトン類に対して質量比((2級、または3級アルコールの質量)/(ケトン類の質量))が0.10〜1.50であることが好ましく、0.15〜1.00であることがより好ましく、0.20〜0.70であることが最も好ましい。なお、複数種類のアルコールを使用した場合には、上記配合割合はアルコールの合計量を基準にしても算出したものである。2級、または3級アルコールの配合比率が0.10〜1.50の範囲を満足することにより、I成分の溶解性が高く、有機溶媒とIII成分のイソシアネート基の反応を抑制し、前駆体組成物の粘度を低下させることができる。 The mixing ratio of the secondary or tertiary alcohol in the organic solvent to be used is 0.10 (mass of the secondary or tertiary alcohol) / (mass of the ketone) relative to the ketone of the good solvent. It is preferably ˜1.50, more preferably 0.15 to 1.00, and most preferably 0.20 to 0.70. When a plurality of types of alcohol are used, the above blending ratio is calculated based on the total amount of alcohol. By satisfying the blending ratio of the secondary or tertiary alcohol in the range of 0.10 to 1.50, the solubility of the component I is high, the reaction between the organic solvent and the isocyanate group of the component III is suppressed, and the precursor The viscosity of the composition can be reduced.
また、樹脂製シート又はフィルムなどの基材上に前駆体組成物を塗布したときの塗布層、或いは後述する方法を採用した場合におけるフォトクロミック接着性シートの平滑性を保持しながら、有機溶媒が残りにくく、乾燥速度を速めることができるという理由から、90℃未満の沸点を有する有機溶媒と、90℃以上の沸点を有する有機溶媒を混合して用いることが好適である。沸点が90℃未満、90℃以上の有機溶媒の配合割合は、使用する他の成分に応じて適宜決定すればよい。中でも、優れた効果を発揮するためには、全有機溶媒量を100質量%としたとき、沸点が90℃未満の有機溶媒が20〜80質量%、沸点が90℃以上の有機溶媒が80〜20質量%とすることが好ましい。 In addition, the organic solvent remains while maintaining the smoothness of the coating layer when the precursor composition is applied on a substrate such as a resin sheet or film, or the photochromic adhesive sheet when the method described later is adopted. For the reason that it is difficult to increase the drying speed, it is preferable to use a mixture of an organic solvent having a boiling point of less than 90 ° C. and an organic solvent having a boiling point of 90 ° C. or more. What is necessary is just to determine suitably the mixture ratio of the organic solvent whose boiling point is less than 90 degreeC and 90 degreeC or more according to the other component to be used. Among them, in order to exert an excellent effect, when the total amount of organic solvent is 100% by mass, the organic solvent having a boiling point of less than 90 ° C. is 20 to 80% by mass, and the organic solvent having a boiling point of 90 ° C. or more is 80 to 80%. It is preferable to set it as 20 mass%.
また、有機溶媒の配合量は、前記したような配合により得られる効果の観点から、I成分100質量部に対して130〜800質量部であることが好ましく、150〜500質量部であることがより好ましい。 Moreover, the compounding amount of the organic solvent is preferably 130 to 800 parts by mass, and preferably 150 to 500 parts by mass with respect to 100 parts by mass of the I component, from the viewpoint of the effect obtained by the compounding as described above. More preferred.
本発明においては、前記前駆体組成物からフォトクロミック組成物を製造することが好ましい。そのため、効率よくI成分とIII成分とを反応させるためには、前駆体組成物には水を配合することもできる。
次に、水について説明する。
In the present invention, it is preferable to produce a photochromic composition from the precursor composition. Therefore, in order to efficiently react the I component and the III component, the precursor composition can be mixed with water.
Next, water will be described.
<水>
上記前駆体組成物には水を配合することもできる。特に、前駆体組成物にポリイソシアネート化合物であるIII成分を含む場合には、水を配合することにより、III成分に含まれるイソシアネート基を効率的に加水分解する(反応させる)ことができる。この水は、前駆体組成物に最初から配合することもできる。ただし、前駆体組成物の保存安定性を考慮すると、前駆体組成物の使用時、つまり、該組成物により塗膜を形成し、樹脂製シートを張り合わせる際に配合することが好ましい。また、この水は、下記に詳述するが、フォトクロミック性接着シートを形成する場合に、その雰囲気下に存在する湿気で代用することもできる。III成分に含まれるイソシアネート基の加水分解は、前駆体組成物を樹脂製シートにコートして塗膜を形成した後に、その環境下の水分(湿気)と接触することによっても進行する。
<Water>
Water can also be mix | blended with the said precursor composition. In particular, when the precursor composition contains a III component that is a polyisocyanate compound, the isocyanate group contained in the III component can be efficiently hydrolyzed (reacted) by blending water. This water can also be incorporated into the precursor composition from the beginning. However, when the storage stability of the precursor composition is taken into consideration, it is preferably blended when the precursor composition is used, that is, when a coating film is formed from the composition and the resin sheets are laminated. Further, this water will be described in detail below, but when forming a photochromic adhesive sheet, moisture existing in the atmosphere can be substituted. Hydrolysis of the isocyanate group contained in the III component proceeds also by contacting the moisture (humidity) in the environment after the precursor composition is coated on a resin sheet to form a coating film.
水の配合量は、特に制限されるものではなく、下記に詳述する、その環境下の湿気でも対応できる。好ましい配合量を記載すれば、III成分に含まれるイソシアネート基のモル数に対して、0.01倍モル〜5倍モル、好ましくは0.05倍モル〜3倍モル、より好ましくは0.1倍モル〜2倍モルの範囲であることが好ましい。 The blending amount of water is not particularly limited, and can be handled by moisture under the environment described in detail below. If a preferable compounding quantity is described, it is 0.01-fold mole to 5-fold mole, preferably 0.05-fold mole to 3-fold mole, more preferably 0.1-fold mole with respect to the number of moles of isocyanate groups contained in the III component. It is preferable that it is the range of 2 times mole-2 times mole.
本発明のフォトクロミック組成物は、前記前駆体組成物を準備し、該前駆体組成物を基材上に塗布し、有機溶媒を除去すると共に、I成分とIII成分とを反応させることにより製造することができる。 The photochromic composition of the present invention is produced by preparing the precursor composition, applying the precursor composition onto a substrate, removing the organic solvent, and reacting the I component and the III component. be able to.
以上のような方法、及び前駆体組成物を使用した方法により得られる本発明のフォトクロミック組成物は、フォトクロミック性接着剤、特にポリカーボネート樹脂製の樹脂製シート又はフィルムどうしを接合するためのフォトクロミック性接着剤として好適に使用できる。そして、本発明のフォトクロミック組成物からなる接着層を介して樹脂製シート又はフィルムを互いに接合することにより、積層体を得ることができる。以下、本発明における積層体及びその製造方法について説明する。 The photochromic composition of the present invention obtained by the above method and the method using the precursor composition is a photochromic adhesive, particularly a photochromic adhesive for joining resin sheets or films made of polycarbonate resin. It can be suitably used as an agent. And a laminated body can be obtained by mutually bonding a resin-made sheet | seat or a film through the contact bonding layer which consists of a photochromic composition of this invention. Hereinafter, the laminate and the manufacturing method thereof in the present invention will be described.
<積層体>
本発明の積層体は、互いに対向する2枚の樹脂製シート又はフィルムが本発明のフォトクロミック組成物からなる接着層を介して接合されてなる積層構造を含んでなる。このような積層体としては、上記積層構造のみからなる積層シート又はフィルム(以下、単に、本発明の積層体ともいう。);上記積層構造を形成する際に、フォトクロミック組成物からなる接着層の両側に別の接着層を介して2枚の樹脂製シート又はフィルムを接合してなる積層シート又はフィルム;これら積層シート又はフィルムに光学シート又はフィルムを更に積層したり、表面にハードコート層などのコート層を形成したりした複合積層シート又はフィルムなどを挙げることができる。
<Laminate>
The laminate of the present invention comprises a laminate structure in which two resin sheets or films facing each other are bonded via an adhesive layer made of the photochromic composition of the present invention. As such a laminated body, a laminated sheet or film consisting only of the above laminated structure (hereinafter, also simply referred to as a laminated body of the present invention); when forming the laminated structure, an adhesive layer comprising a photochromic composition is used. A laminated sheet or film formed by joining two resin sheets or films on both sides via separate adhesive layers; an optical sheet or film is further laminated on these laminated sheets or films, a hard coat layer or the like on the surface A composite laminated sheet or film in which a coat layer is formed can be mentioned.
本発明の積層体においては、上記のようにフォトクロミック組成物からなる接着層(以下、第1接着層ともいう。)の両側に、別の接着層(以下、第2接着層ともいう。)を積層し、該第2接着層を介して2枚の樹脂製シート又はフィルムを接合してなる積層シート又はフィルムを作製することも可能である。 In the laminate of the present invention, another adhesive layer (hereinafter also referred to as the second adhesive layer) is provided on both sides of the adhesive layer (hereinafter also referred to as the first adhesive layer) made of the photochromic composition as described above. It is also possible to produce a laminated sheet or film obtained by laminating and joining two resin sheets or films via the second adhesive layer.
第2接着層を積層することにより、本発明の積層体の接着性をより向上させることができる。該第2接着層を積層することにより、本発明の積層体の接着性が向上する要因としては、以下の2点が挙げられる。 By laminating the second adhesive layer, the adhesiveness of the laminate of the present invention can be further improved. By laminating the second adhesive layer, the following two points can be cited as factors for improving the adhesiveness of the laminate of the present invention.
1つ目は、フォトクロミック化合物などの光酸化劣化しやすい化合物を有する層を光学シート又は光学フィルムに直接接触させないことが挙げられる。これについては理由が定かではないが、光酸化劣化などにより分解して低分子量化したフォトクロミック化合物などが、接着層と樹脂製シート又は光学フィルムの界面に移行することにより、両者の接着性を低下させると推察している。 The first is that a layer having a compound that easily undergoes photo-oxidative degradation such as a photochromic compound is not brought into direct contact with the optical sheet or optical film. The reason for this is not clear, but the photochromic compound, etc., which has been decomposed by photooxidation degradation and reduced in molecular weight, migrates to the interface between the adhesive layer and the resin sheet or optical film, thereby reducing the adhesion between them. I guess it will.
2つ目は、特に熱可塑性樹脂からなる樹脂製シート又は光学フィルムに対して効果を発揮するが、硬化前、もしくは有機溶剤に溶解しているなど液体で流動性がある接着剤を直接樹脂製シート又はフィルムに塗布することにより、樹脂製シート又はフィルムを接着剤で侵しながら、また浸透することができるため、より密着力が向上すると考えられる。 The second is particularly effective for resin-made sheets or optical films made of thermoplastic resin, but it is made of resin and liquid adhesive before curing or dissolved in an organic solvent. By applying to the sheet or film, the resin sheet or film can be penetrated while being eroded with an adhesive, so that it is considered that the adhesion is further improved.
よって、本発明で使用される第2接着層は、フォトクロミック化合物を含有しないことが好ましく、更には液体で流動性がある接着剤の状態で直接樹脂製シート又はフィルムに塗布されることがより好ましい。 Therefore, the second adhesive layer used in the present invention preferably does not contain a photochromic compound, and more preferably is applied directly to a resin sheet or film in the form of a liquid and fluid adhesive. .
本発明の第2接着層に用いられる成分としては、I成分と同様なポリウレタンウレア樹脂を採用することが好ましい。特に、後述する軟化点、多分散度などを制御したポリウレタンウレア樹脂を使用することにより、本発明のフォトクロミック化合物を有する第1接着層、及び樹脂製シート又はフィルムとより強固な密着力が得られる。以下に、第2接着層に使用されるポリウレタンウレア樹脂(I’成分)について説明する。 As a component used for the second adhesive layer of the present invention, it is preferable to employ the same polyurethane urea resin as the component I. In particular, by using a polyurethane urea resin whose softening point, polydispersity, etc., which will be described later, are controlled, a stronger adhesion can be obtained with the first adhesive layer having the photochromic compound of the present invention and the resin sheet or film. . The polyurethane urea resin (I ′ component) used for the second adhesive layer will be described below.
<I’成分:第2接着層用ポリウレタンウレア樹脂>
本発明のI’成分は、I成分と同様に多分散度(重量平均分子量/数平均分子量)が1.6〜2.4の範囲であるポリウレタンウレア樹脂を用いることが好ましい。このように狭い範囲の多分散度を有することによって、I’成分を第2接着層に用いた場合に、第1接着層、及び樹脂製シート又はフィルムとの強固な密着性と、耐熱性、及び耐汗性を有することが可能になる。良好な接着力、耐熱性の観点から、I’成分に用いるポリウレタンウレア樹脂の多分散度は、1.8〜2.2の範囲であることがより好ましい。
<I ′ component: polyurethane urea resin for second adhesive layer>
As the component I ′ of the present invention, it is preferable to use a polyurethane urea resin having a polydispersity (weight average molecular weight / number average molecular weight) in the range of 1.6 to 2.4 as in the case of the component I. By having a polydispersity in such a narrow range, when the I ′ component is used for the second adhesive layer, the first adhesive layer and the strong adhesion to the resin sheet or film, heat resistance, And it becomes possible to have sweat resistance. From the viewpoint of good adhesive strength and heat resistance, the polydispersity of the polyurethane urea resin used for the component I ′ is more preferably in the range of 1.8 to 2.2.
本発明のI’成分は、前記I成分と同様なポリウレタンウレア樹脂であり、I成分の構成要素として記載したA1成分、A2成分、B成分、及び必要に応じてC成分を使用することができる。合成方法に関しても、前述のI成分と同様にして実施することができる。 The I ′ component of the present invention is a polyurethane urea resin similar to the above-mentioned I component, and the A1 component, the A2 component, the B component, and the C component as necessary can be used as constituents of the I component. . Regarding the synthesis method, it can be carried out in the same manner as the above-mentioned I component.
I’成分に使用される好適なA1成分としては、1,4−ブタンジオール、1,5−ペンタンジオール、1,6−ヘキサンジオール、1,8−オクタンジオールなどの低分子ポリオール類を原料に用いた、数平均分子量が600〜1200であるポリカーボネートポリオールが挙げられる。 Suitable A1 components used for the I ′ component are low molecular polyols such as 1,4-butanediol, 1,5-pentanediol, 1,6-hexanediol, and 1,8-octanediol. The polycarbonate polyol whose number average molecular weight is 600-1200 used is mentioned.
I’成分に使用される好適なA2成分としては、脂環式ジイソシアネート化合物を使用することが好ましく、具体的には、イソホロンジイソシアネート、ノルボルナンジイソシアネート、4,4’−メチレンビス(シクロヘキシルイソシアネート)の異性体混合物が挙げられる。 As a suitable A2 component used for the I ′ component, an alicyclic diisocyanate compound is preferably used. Specifically, isophorone diisocyanate, norbornane diisocyanate, and 4,4′-methylenebis (cyclohexyl isocyanate) isomers. A mixture is mentioned.
I’成分に使用される好適なB成分としては、ジアミン化合物が好ましく、具体的には、イソホロンジアミン、ビス−(4−アミノシクロヘキシル)メタン、ノルボルナンジアミンなどが挙げられる。 Suitable B component used for the I ′ component is preferably a diamine compound, and specific examples include isophorone diamine, bis- (4-aminocyclohexyl) methane, norbornane diamine and the like.
I’成分に使用される好適なC成分としては、前記一般式(2)で示される化合物を使用することが好ましく、具体的には、ノルマルブチルアミンのようなアルキルアミンが挙げられる。 As a suitable C component used for the I ′ component, it is preferable to use the compound represented by the general formula (2), and specifically, an alkylamine such as normal butylamine can be mentioned.
各成分の配合割合は適宜決定すればよいが、得られるI’成分の耐熱性、及び接着強度のバランスの観点から、次のような量比とすることが好ましい。なお、n1、n2、n3、及びn4の定義は、前述の通りである。好ましい配合割合の範囲は、n1:n2:n3:n4=0.30〜0.89/1/0.10〜0.69/0.00〜0.20である。さらに、得られるV成分がより優れた密着性を発揮するためには、より好ましくは、n1:n2:n3:n4=0.40〜0.80/1/0.15〜0.58/0.00〜0.15、最も好ましくは、n1:n2:n3:n4=0.51〜0.68/1/0.30〜0.48/0.01〜0.10である。中でも、n2=n1+n3+n4とすることが好ましく、長期の安定性を考慮すると末端を不活性化させることが好ましい。
I’成分は、以上のような配合割合でI成分の合成方法にならって製造できる。
The blending ratio of each component may be determined as appropriate, but the following ratio is preferable from the viewpoint of the balance between the heat resistance of the obtained I ′ component and the adhesive strength. The definitions of n1, n2, n3, and n4 are as described above. The range of a preferable mixture ratio is n1: n2: n3: n4 = 0.30-0.89 / 1 / 0.10-0.69 / 0.00-0.20. Furthermore, in order for the obtained V component to exhibit better adhesion, more preferably, n1: n2: n3: n4 = 0.40-0.80 / 1 / 0.15-0.58 / 0. 0.01 to 0.15, most preferably n1: n2: n3: n4 = 0.51 to 0.68 / 1 / 0.30 to 0.48 / 0.01 to 0.10. Especially, it is preferable to set it as n2 = n1 + n3 + n4, and considering the long-term stability, it is preferable to inactivate the terminal.
The I ′ component can be produced in accordance with the synthesis method of the I component at the blending ratio as described above.
また、その他のI’成分の特徴としては、耐熱性、接着強度などの観点から、I’成分の数平均分子量は、1万〜12万であることが好ましく、特に4万〜10万であることが最も好ましい。なお、この分子量は、上述したI成分と同様の条件で測定した値である。 Further, as other features of the I ′ component, the number average molecular weight of the I ′ component is preferably 10,000 to 120,000, particularly 40,000 to 100,000, from the viewpoints of heat resistance, adhesive strength, and the like. Most preferred. In addition, this molecular weight is the value measured on the same conditions as I component mentioned above.
また、I’成分は、樹脂製シート又はフィルムどうしを貼付して得られる積層体の物性、得られた積層体を用いて曲げ加工や射出成型により成型体を製造する際の加工安定性の観点、及びそれら積層シートの接着性の観点、さらにはこれら積層体又は成型体の表面にハードコート層を形成する場合において、ハードコート液を塗布したり、硬化させたりするときの加工性の観点から、通常80〜200℃、特に100〜180℃の耐熱性を有していることが好ましい。なお、ここでいう耐熱性とは、前記III成分の項目でI成分とIII成分とから得られる反応生成物を測定したものと同様の方法で測定した値である。 In addition, the component I ′ is a physical property of a laminate obtained by attaching resin sheets or films, and a processing stability viewpoint when a molded product is produced by bending or injection molding using the obtained laminate. From the viewpoint of the adhesiveness of these laminated sheets, and also from the viewpoint of workability when applying a hard coat liquid or curing in the case of forming a hard coat layer on the surface of these laminates or molded bodies Usually, it preferably has a heat resistance of 80 to 200 ° C., particularly 100 to 180 ° C. In addition, heat resistance here is the value measured by the method similar to what measured the reaction product obtained from I component and III component in the item of said III component.
<第2接着層の厚み、形成方法>
第2接着層の膜厚は、2〜40μmの範囲であることが好ましく、5〜15μmであることがより好ましい。膜厚が2μmより薄い場合には接着性が低下する傾向にあり、膜厚が40μmを越える場合には、有機溶剤が残存しやすくなる。また、フォトクロミック化合物の耐候性(耐久性)が低下する傾向にある。
<Thickness and formation method of second adhesive layer>
The film thickness of the second adhesive layer is preferably in the range of 2 to 40 μm, more preferably 5 to 15 μm. When the film thickness is less than 2 μm, the adhesion tends to decrease, and when the film thickness exceeds 40 μm, the organic solvent tends to remain. Moreover, it exists in the tendency for the weather resistance (durability) of a photochromic compound to fall.
第2接着層を形成する接着剤(I’成分を含む組成物)は、必要に応じて第1接着層(上記フォトクロミック組成物)で使用されるような有機溶剤を含んでいても良い。しかしながら、ポリカーボネートなどの熱可塑性樹脂を樹脂製シート又はフィルムとして使用する場合においては、第2接着層を形成する接着剤に使用する有機溶剤は熱可塑性樹脂に対して、低溶解性であることが好ましい。熱可塑性樹脂への溶解性が高いと、過剰に熱可塑性樹脂を溶解してしまい、外観不良(白濁)、接着性低下、及び第1接着層の積層時にフォトクロミック特性の低下を引き起こしてしまうおそれがある。また、熱可塑性樹脂への溶解性が低すぎると、樹脂製シート又はフィルムが溶解せず、第2接着層との接着性が十分に発揮されない。以上のことから、第2接着層に使用する有機溶剤としては、メタノール、エタノール、n−プロパノール、i−プロパノール、n−ブタノール、t−ブタノール、2−ブタノール等のアルコール類;エチレングリコールモノメチルエーテル、エチレングリコールモノイソプロピルエーテル、エチレングリコールモノエチルエーテル、エチレングリコールモノ−n−プロピルエーテル、エチレングリコールモノ−n−ブチルエーテル、エチレングリコールモノ−t−ブチルエーテル、プロピレングリコールモノメチルエーテル、プロピレングリコールモノエチルエーテル、プロピレングリコール−n−ブチルエーテル、エチレングリコールジメチルエーテル等の多価アルコール誘導体;ジアセトンアルコールを主溶剤として用いることが好ましい。 The adhesive (the composition containing the I ′ component) that forms the second adhesive layer may contain an organic solvent as used in the first adhesive layer (the photochromic composition) as necessary. However, when a thermoplastic resin such as polycarbonate is used as a resin sheet or film, the organic solvent used for the adhesive forming the second adhesive layer may have a low solubility in the thermoplastic resin. preferable. If the solubility in the thermoplastic resin is high, the thermoplastic resin may be excessively dissolved, which may cause poor appearance (white turbidity), reduced adhesiveness, and reduced photochromic properties when the first adhesive layer is laminated. is there. On the other hand, if the solubility in the thermoplastic resin is too low, the resin sheet or film is not dissolved and the adhesiveness with the second adhesive layer is not sufficiently exhibited. From the above, as the organic solvent used for the second adhesive layer, alcohols such as methanol, ethanol, n-propanol, i-propanol, n-butanol, t-butanol, 2-butanol; ethylene glycol monomethyl ether, Ethylene glycol monoisopropyl ether, ethylene glycol monoethyl ether, ethylene glycol mono-n-propyl ether, ethylene glycol mono-n-butyl ether, ethylene glycol mono-t-butyl ether, propylene glycol monomethyl ether, propylene glycol monoethyl ether, propylene glycol -Polyhydric alcohol derivatives such as n-butyl ether and ethylene glycol dimethyl ether; diacetone alcohol is preferably used as the main solvent.
更には、積層体の接着(密着)強度をより向上させるために、第1接着層に使用される前記III成分を含んでいてもよい。また、製膜性や耐候性を向上させるために、第1接着層に使用される界面活性剤、酸化防止剤、ラジカル補足剤、紫外線安定剤、紫外線吸収剤、染料などを含んでいても良い。
次に、本発明の積層体を構成する材料或いは部材について説明する。
Furthermore, in order to further improve the adhesion (adhesion) strength of the laminate, the III component used for the first adhesive layer may be included. Moreover, in order to improve film forming property and weather resistance, a surfactant, an antioxidant, a radical scavenger, an ultraviolet stabilizer, an ultraviolet absorber, a dye, and the like used for the first adhesive layer may be included. .
Next, the material or member which comprises the laminated body of this invention is demonstrated.
<樹脂製シート又はフィルム>
本発明において、樹脂製シート又はフィルムとしては、光透過性を有するシート又はフィルムが特に制限なく使用できるが、入手の容易性および加工のし易さなどの観点から樹脂製のものを使用することが好適である。樹脂製シート又はフィルムの原料として好適な樹脂を例示すれば、ポリカーボネート樹脂、ポリエチレンテレフタレート樹脂、ナイロン樹脂、トリアセチルセルロース樹脂、アクリル樹脂、ウレタン樹脂、アリル樹脂、エポキシ樹脂、ポリビニルアルコール樹脂などが挙げられる。その中でも、接着性が良好で射出成形法に対する適用性が高いという理由からポリカーボネート樹脂が特に好ましい。また、偏光フィルム(ポリビニルアルコール偏光フィルムをトリアセチルセルロース樹脂フィルムではさんだもの)、偏光シート(ポリビニルアルコール偏光フィルムをポリカーボネートシートではさんだもの)、染色されたフィルム、染色されたシートも、本発明の樹脂製シート又はフィルムとして使用することが可能である。なお、染色した樹脂製シート又はフィルムを使用する場合には、元々、染色されたものを使用することもできるし、本発明の積層シートを作製した後、表面の樹脂製シート又はフィルムを染色してもよい。
<Resin sheet or film>
In the present invention, as the resin sheet or film, a light-transmitting sheet or film can be used without particular limitation, but a resin-made sheet or film should be used from the viewpoints of availability and ease of processing. Is preferred. Examples of resins suitable as raw materials for resin sheets or films include polycarbonate resins, polyethylene terephthalate resins, nylon resins, triacetyl cellulose resins, acrylic resins, urethane resins, allyl resins, epoxy resins, polyvinyl alcohol resins, and the like. . Among these, polycarbonate resin is particularly preferable because it has good adhesiveness and high applicability to the injection molding method. In addition, a polarizing film (a polyvinyl alcohol polarizing film sandwiched between triacetyl cellulose resin films), a polarizing sheet (a polyvinyl alcohol polarizing film sandwiched between polycarbonate sheets), a dyed film, and a dyed sheet are also included in the resin of the present invention. It can be used as a sheet or film. In the case of using a dyed resin sheet or film, it is possible to use an originally dyed sheet, or after producing the laminated sheet of the present invention, dye the surface resin sheet or film. May be.
上記偏光フィルム、偏光シート、染色フィルム、及び染色シートを用いて光学物品を得る場合には、第1接着層の方が該偏光フィルム等よりも上側(太陽光や紫外線が照射される側)に積層されていることが好ましい。 When an optical article is obtained using the polarizing film, polarizing sheet, dyeing film, and dyeing sheet, the first adhesive layer is on the upper side (the side irradiated with sunlight or ultraviolet rays) than the polarizing film or the like. It is preferable that they are laminated.
本発明において使用する樹脂製シート又はフィルムの好適な厚みとしては、100〜1500μmが好ましく、200〜1000μmがより好ましい。また、これらの樹脂製シート又はフィルムは、異なる厚みを組み合わせて使用することも可能である。 As suitable thickness of the resin-made sheet | seat or film used in this invention, 100-1500 micrometers is preferable and 200-1000 micrometers is more preferable. In addition, these resin sheets or films can be used in combination with different thicknesses.
また、本発明の樹脂製シート及びフィルムの表面(上面および下面)には、下記のような塗膜層が形成されていてもよい。塗膜層は、水分散ポリウレタン樹脂、水分散ポリエステル樹脂、水分散アクリル樹脂、水分散ポリウレタン・アクリル樹脂などの水分散性ポリマー;前記水分散性ポリマーの内、カルボニル基を有するポリマーとヒドラジド化合物との架橋体;ポリビニルアルコールなどの水溶性ポリマーの架橋体;(メタ)アクリル基を有する重合性モノマー、及び/またはエポキシ基、(メタ)アクリル基、ビニル基、アミノ基、及びメルカプト基などから選ばれる基を有する加水分解性有機ケイ素化合物の組成物;シラノール基あるいは加水分解してシラノール基を形成しうる基、(メタ)アクリレート基、エポキシ基、及びビニル基から選ばれる重合性基を有するウレタンウレア樹脂の組成物;プロペニルエーテル基含有化合物、ポリエン化合物及びチオール化合物とを含むエン/チオール系組成物、オキセタン化合物などを含む光硬化性組成物などの、樹脂、架橋体、組成物から形成されればよい。該塗膜層を特に最表面(フォトクロミック接着性シートが存在しない側)に形成することにより、(メタ)アクリレート系モノマー組成物、アリル系モノマー組成物、チオウレタン系モノマー組成物、ウレタン系モノマー組成物、チオエポキシ系モノマー組成物などの熱硬化性樹脂(光学基材)を形成するモノマー組成物中に、馴染みよく、本発明の積層体を埋設することができる。その結果、該熱硬化性樹脂(光学基材)と該積層シートとの密着性が良好な、該熱硬化性樹脂(光学基材)中に該積層体が埋設した光学物品を得ることもできる。 Moreover, the following coating layers may be formed on the surfaces (upper surface and lower surface) of the resin sheet and film of the present invention. The coating layer comprises a water-dispersible polymer such as water-dispersed polyurethane resin, water-dispersed polyester resin, water-dispersed acrylic resin, water-dispersed polyurethane / acrylic resin; among the water-dispersible polymers, a polymer having a carbonyl group and a hydrazide compound A crosslinked product of a water-soluble polymer such as polyvinyl alcohol; a polymerizable monomer having a (meth) acrylic group and / or an epoxy group, a (meth) acrylic group, a vinyl group, an amino group, and a mercapto group. Of a hydrolyzable organosilicon compound having a group capable of forming a silanol group or a urethane having a polymerizable group selected from a group that can be hydrolyzed to form a silanol group, a (meth) acrylate group, an epoxy group, and a vinyl group Composition of urea resin; propenyl ether group-containing compound, polyene compound and Ene / thiol compositions comprising ol compound, such as light-curable composition comprising an oxetane compound, a resin, crosslinked, may be formed from the composition. By forming the coating layer on the outermost surface (the side where no photochromic adhesive sheet is present), a (meth) acrylate-based monomer composition, an allyl-based monomer composition, a thiourethane-based monomer composition, a urethane-based monomer composition The laminate of the present invention can be embedded in a monomer composition that forms a thermosetting resin (optical substrate) such as a thioepoxy monomer composition. As a result, it is possible to obtain an optical article in which the laminate is embedded in the thermosetting resin (optical substrate) having good adhesion between the thermosetting resin (optical substrate) and the laminated sheet. .
<本発明の積層体の製造方法>
本発明の積層体は、互いに対向する2枚の樹脂製シート又はフィルムを本発明のフォトクロミック組成物からなる接着層を介して接合させることにより製造される。なお、上記第1接着層の厚さは、フォトクロミック化合物の発色濃度、耐候性および接着強度などの観点から、5〜100μm、特に10〜50μmとすることが好ましい。また、第2接着層を使用する場合には、その膜厚は、前述の通り2〜40μmの範囲であることが好ましく、5〜15μmであることがより好ましい。得られる光学物品の厚みとしては、光学物品の製造の容易さや、後述する加工の加工性の観点から、500〜3000μmが好ましい。
<The manufacturing method of the laminated body of this invention>
The laminate of the present invention is produced by joining two resin sheets or films facing each other via an adhesive layer made of the photochromic composition of the present invention. The thickness of the first adhesive layer is preferably 5 to 100 μm, particularly 10 to 50 μm, from the viewpoint of the color density of the photochromic compound, weather resistance, adhesive strength, and the like. Moreover, when using a 2nd contact bonding layer, it is preferable that the film thickness is the range of 2-40 micrometers as above-mentioned, and it is more preferable that it is 5-15 micrometers. The thickness of the obtained optical article is preferably 500 to 3000 μm from the viewpoint of ease of manufacturing the optical article and the workability of processing described later.
上記第1接着層は、用いるフォトクロミック組成物の性状に応じて、次のような方法により得ることができる。すなわち、溶媒を配合することなどにより本発明のフォトクロミック組成物(又は前駆体組成物)が適度の粘度に調整されている場合には、一方の樹脂製シート又はフィルム上に本発明のフォトクロミック組成物を塗布し、必要に応じて(加熱)乾燥を行った後、他の樹脂製シート又はフィルムを(加熱)圧着すればよい。本発明のフォトクロミック組成物(又は前駆体組成物)の好適な動粘度は、25℃において、2,000〜50,000cStであり、より好ましくは、5,000〜40,000cStであり、さらに好ましくは8,000〜30,000cStである。フォトクロミック組成物(又は前駆体組成物)が2,000〜60,000cStであることにより、フォトクロミック接着性シートの平滑性を高め、ロール to ロールでの塗工により、縦筋や横筋のような外観不良の発生を抑制することができる。 The said 1st contact bonding layer can be obtained with the following methods according to the property of the photochromic composition to be used. That is, when the photochromic composition (or precursor composition) of the present invention is adjusted to an appropriate viscosity by blending a solvent or the like, the photochromic composition of the present invention is formed on one resin sheet or film. Is applied and (heated) drying is performed as necessary, and then another resin sheet or film may be (heated) pressed. The suitable kinematic viscosity of the photochromic composition (or precursor composition) of the present invention is 2,000 to 50,000 cSt at 25 ° C., more preferably 5,000 to 40,000 cSt, still more preferably. Is 8,000 to 30,000 cSt. When the photochromic composition (or precursor composition) is 2,000 to 60,000 cSt, the smoothness of the photochromic adhesive sheet is increased, and roll-to-roll coating allows the appearance of vertical and horizontal stripes. The occurrence of defects can be suppressed.
このとき、フォトクロミック組成物(又は前駆体組成物)の塗布方法としては、スピンコート法、スプレーコート法、ディップコート法、ディップ−スピンコート法、ドライラミネート法などの公知の方法が何ら制限なく用いられる。また、本発明で使用する樹脂製シート又はフィルムは、あらかじめメタノールなどの有機溶剤で洗浄・脱脂してもよい。さらに、コロナ放電処理、プラズマ放電処理、やUVオゾン処理などを施しておくことも可能である。また、塗工に用いる塗工機としては、ナイフコーター、ダイコーター、グラビアコーター、リバースロールコーター、バーコーターなど、一般的な塗工機を何ら制限なく用いられる。中でも、塗工液粘度の許容範囲が比較的広いナイフコーター、ダイコーターが好適に用いられる。 At this time, as a coating method of the photochromic composition (or precursor composition), a known method such as a spin coating method, a spray coating method, a dip coating method, a dip-spin coating method, or a dry laminating method is used without any limitation. It is done. The resin sheet or film used in the present invention may be washed and degreased with an organic solvent such as methanol in advance. Furthermore, corona discharge treatment, plasma discharge treatment, UV ozone treatment, or the like can be performed. Moreover, as a coating machine used for coating, general coating machines, such as a knife coater, a die coater, a gravure coater, a reverse roll coater, and a bar coater, can be used without any limitation. Among these, a knife coater and a die coater having a relatively wide allowable range of coating solution viscosity are preferably used.
また、有機溶媒を含む本発明のフォトクロミック組成物(又は前駆体組成物)を使用する場合には、平滑な基材上に本発明のフォトクロミック組成物(又は前駆体組成物)を延展せしめた後に乾燥することにより有機溶媒を除去し、その後、基材を剥がして、I成分(又はI成分、及びIII成分)と、I成分(又はI成分、及びIII成分)中に分散したII成分とを含んでなるフォトクロミック性接着シートを作製する。次いで互いに対向する2枚の樹脂製シート又はフィルムの間に上記フォトクロミック性接着シートを介在させて該2枚の樹脂製シート又はフィルムを接合することにより、本発明の積層体を製造することもできる。なお、前駆体組成物を使用した場合には、この積層体を製造する過程においてフォトクロミック組成物(フォトクロミック性接着シート:第1接着層)を形成することとなる。 Further, when the photochromic composition (or precursor composition) of the present invention containing an organic solvent is used, after the photochromic composition (or precursor composition) of the present invention is spread on a smooth substrate. The organic solvent is removed by drying, then the substrate is peeled off, and the component I (or component I and component III) and the component II dispersed in component I (or component I and component III) are mixed. A photochromic adhesive sheet is prepared. Next, the laminate of the present invention can also be produced by joining the two resin sheets or films with the photochromic adhesive sheet interposed between the two resin sheets or films facing each other. . When the precursor composition is used, a photochromic composition (photochromic adhesive sheet: first adhesive layer) is formed in the course of manufacturing this laminate.
上記平滑な基材の材質としては、本発明で使用する溶剤に耐性があるもの、またフォトクロミック組成物(又は前駆体組成物)が剥離しやすいものが好ましく、具体的に例示すれば、ガラス、ステンレス、テフロン(登録商標)、ポリエチレンテレフタレート、ポリプロピレン、さらにはシリコン系やフッ素系などの剥離性を向上させるコート層を積層させたプラスチックフィルムなどが挙げられる。 As the material for the smooth substrate, a material that is resistant to the solvent used in the present invention and a material that can easily be peeled off from the photochromic composition (or precursor composition) are preferable. Examples thereof include stainless steel, Teflon (registered trademark), polyethylene terephthalate, polypropylene, and a plastic film on which a coating layer that improves peelability such as silicon or fluorine is laminated.
このような方法を採用した場合には、溶媒の種類及び樹脂製シート又はフィルムの種類によらず、溶媒の使用に起因する悪影響を排除することが可能である。 When such a method is employed, it is possible to eliminate adverse effects caused by the use of the solvent regardless of the type of solvent and the type of resin sheet or film.
上記フォトクロミック組成物(又は前駆体組成物)の塗布、さらに乾燥は、室温〜130℃の温度で、10〜100%RHの湿度下で実施されることが好ましい。有機溶媒は、乾燥後のフォトクロミック接着性シートに残存することで、フォトクロミック特性に悪影響を及ぼす場合があり、乾燥後の有機溶媒の質量は、フォトクロミック接着性シートに対して0.1%以下にすることが好ましい。また、前駆体組成物を使用する場合、該前駆体組成物には、III成分としてイソシアネート化合物が配合されているため、湿度が存在する中で塗布、及び乾燥などの操作を実施することにより、III成分の加水分解反応を促進し、より強固な密着力が得られる。上記のような湿度(水分の存在下)下で乾燥を行うことにより、前駆体組成物に水を配合しなくとも、優れた性能を発揮するフォトクロミック性接着シートとすることができる。また、水を配合した場合には、乾燥条件下で該シートを形成することもできる。 The application and further drying of the photochromic composition (or precursor composition) are preferably performed at a temperature of room temperature to 130 ° C. and a humidity of 10 to 100% RH. The organic solvent may adversely affect the photochromic properties by remaining in the photochromic adhesive sheet after drying, and the mass of the organic solvent after drying is 0.1% or less with respect to the photochromic adhesive sheet. It is preferable. Moreover, when using a precursor composition, since an isocyanate compound is blended as the III component in the precursor composition, by performing operations such as coating and drying in the presence of humidity, The hydrolysis reaction of the III component is promoted, and a stronger adhesion can be obtained. By drying under the above humidity (in the presence of moisture), a photochromic adhesive sheet that exhibits excellent performance can be obtained without adding water to the precursor composition. When water is added, the sheet can be formed under dry conditions.
前記樹脂製シート又はフィルムを接合する工程で得られた積層体は、そのまま使用することもできるが、以下の方法により、その状態を安定化させて使用することもできる。具体的には、接合したばかりの積層体を20℃以上60℃以下の温度で4時間以上静置し、脱気することが好ましい。静置する時間の上限は、特に制限されるものではないが、50時間もあれば十分である。また、静置に際しては、常圧で静置することも可能であるし、真空下で静置することも可能である。さらに、この静置した積層体を60℃以上130℃以下の温度下、30分以上3時間以下放置しておくことが好ましい(以下、加熱処理とする)。この加熱処理を実施することにより、III成分のイソシアネート基の一部が、反応に供されるものと考える。その結果、このイソシアネート基がI成分のウレタン結合、又はウレア結合に結合し、アロファネート結合、又はビュレット結合を形成することを推進するものと考えられる。そして、この加熱処理して得られた積層シートは、その状態が非常に安定なものとなる。 The laminate obtained in the step of joining the resin sheet or film can be used as it is, but the state can be stabilized and used by the following method. Specifically, it is preferable to leave the laminated body just joined at a temperature of 20 ° C. or higher and 60 ° C. or lower for 4 hours or longer to deaerate. The upper limit of the standing time is not particularly limited, but 50 hours is sufficient. In addition, when standing, it can be left at normal pressure or left under vacuum. Furthermore, it is preferable to leave this standing laminate at a temperature of 60 ° C. to 130 ° C. for 30 minutes to 3 hours (hereinafter referred to as heat treatment). By performing this heat treatment, it is considered that a part of the isocyanate group of the III component is subjected to the reaction. As a result, it is considered that this isocyanate group is bonded to the urethane bond or urea bond of the I component to form an allophanate bond or a burette bond. And the laminated sheet obtained by this heat treatment has a very stable state.
また、III成分を配合した前駆体組成物を用いた場合には、室温〜100℃の温度、及び30〜100%RHの湿度下で加湿処理されることが好ましい。この加湿処理を実施することにより、III成分によるI成分どうしの橋架け構造を完結させるとともに、積層シート中に存在するIII成分由来のイソシアネート基を完全に消失させることができ、フォトクロミック特性、及び接着性をより安定化させることが可能となる。 Moreover, when the precursor composition which mix | blended III component is used, it is preferable to humidify under the temperature of room temperature-100 degreeC, and the humidity of 30-100% RH. By carrying out this humidification treatment, the bridge structure between the I components by the III component can be completed, and the isocyanate group derived from the III component present in the laminated sheet can be completely eliminated, and the photochromic properties and adhesion It is possible to further stabilize the property.
さらには、加湿処理後に、常圧下、もしくは真空下において、40〜130℃で静置することにより、積層体中に存在する過剰の水分を除去することができる。よって、前駆体組成物から、フォトクロミック積層体を作製後、1)脱気、2)加熱処理、3)加湿処理、4)水分除去の順に後処理を実施することが好ましく、塗布後の第1接着層中でI成分とIII成分を反応させることが好ましい。 Furthermore, after the humidification treatment, excess moisture present in the laminate can be removed by standing at 40 to 130 ° C. under normal pressure or under vacuum. Therefore, after preparing the photochromic laminate from the precursor composition, it is preferable to perform post-treatment in the order of 1) deaeration, 2) heat treatment, 3) humidification treatment, and 4) moisture removal. It is preferable to react the I component and the III component in the adhesive layer.
また、前述の第2接着層を有する積層シートを製造する方法としては、第1接着層と、樹脂製シート又は光学フィルムの間に第2接着層を積層する形態になっていれば、その製造方法は特に制限されない。 Moreover, as a method of manufacturing the laminated sheet having the above-mentioned second adhesive layer, if the second adhesive layer is laminated between the first adhesive layer and the resin sheet or the optical film, the manufacturing thereof is possible. The method is not particularly limited.
製造方法としては、
1)あらかじめ樹脂製シート又はフィルム上に第2接着層を積層させ、この第2接着層を有する2枚の樹脂製シート又はフィルムで、第1接着層を挟みこむ方法、
2)第1接着層の両面に第2接着層を塗布しておき、その両面に樹脂製シート又はフィルムを貼り付ける方法、
3)樹脂製シート又はフィルム上に、第1接着層、第2接着層、第1接着層、さらには樹脂製シート又はフィルムとなるように順次積層していく方法、
などが挙げられるが、製造効率などの観点から、1)の方法を採用することが最も好ましい。
As a manufacturing method,
1) A method of previously laminating a second adhesive layer on a resin sheet or film and sandwiching the first adhesive layer between two resin sheets or films having the second adhesive layer,
2) A method in which the second adhesive layer is applied on both surfaces of the first adhesive layer, and a resin sheet or film is pasted on both surfaces,
3) A method of sequentially laminating the first adhesive layer, the second adhesive layer, the first adhesive layer, and further the resin sheet or film on the resin sheet or film,
However, it is most preferable to adopt the method 1) from the viewpoint of production efficiency.
本発明の第2接着層の塗布方法、及び乾燥方法としては、第1接着層と同様な方法で実施することができる。 The application method and the drying method of the second adhesive layer of the present invention can be carried out by the same method as the first adhesive layer.
さらに、溶媒を含まない場合においては、前駆体組成物とポリイソシアネート化合物(III成分)の混合物を、共押し出し成型等によって積層体に加工することもできる。 Furthermore, when a solvent is not included, the mixture of the precursor composition and the polyisocyanate compound (III component) can be processed into a laminate by coextrusion molding or the like.
<積層体を用いた物品>
本発明のフォトクロミック組成物は、得られた積層体は優れた接着性、特に高温における優れた接着性を示し、得られた積層体は、耐汗性も高い。すなわち、人工汗と接触させた後であっても、優れた接着性を示す。さらに、本発明の積層体は、太陽光照射時における高い発色濃度、及び太陽光未照射時における高い退色速度を有し、しかも発退色による繰り返し耐久性が高い。従って、本発明の積層体は前述のプラスチックサングラス以外にも、遮光窓材、ディスプレイ材料、農業用フィルム、玩具、衣服、傘等の物品にフォトクロ物性を発現させるための積層体として用いることができる。
<Articles using laminates>
In the photochromic composition of the present invention, the obtained laminate exhibits excellent adhesiveness, particularly excellent adhesiveness at high temperatures, and the obtained laminate has high sweat resistance. That is, excellent adhesion is exhibited even after contact with artificial sweat. Furthermore, the laminate of the present invention has a high color density when irradiated with sunlight, a high fading speed when not irradiated with sunlight, and has high repetition durability due to color fading. Accordingly, the laminate of the present invention can be used as a laminate for developing photochromic properties in articles such as light shielding window materials, display materials, agricultural films, toys, clothes, umbrellas, etc., in addition to the above-mentioned plastic sunglasses. it can.
本発明においては、前記積層体をプラスチックレンズなどの光学基材と一体化する場合における光学基材としては、ポリカーボネート樹脂が好ましい。一体化する方法としては、前記積層体を金型内に装着し、ポリカーボネート樹脂などの光学基材を構成するための熱可塑性樹脂を射出成型する方法が挙げられる。また、本発明の積層体は光学基材と一体化する前に、曲げ加工を実施することにより、レンズ状の球面形状に加工することもできる。前記積層シートを曲げ加工する方法としては、例えば、熱プレス加工、加圧加工、減圧吸引加工などが挙げられる。曲げ加工する際の温度は、前記積層シートに使用している樹脂製シート又はフィルムの種類によって適宜、決定すれば良いが、120℃から200℃で実施することが好ましい。又、他の樹脂製シート又は及びガラスなどと一体化させることで、遮光窓材や農業用フィルムとすることができる。また、液晶表示パネル、フィールドエミッションディスプレイ、エレクトロルミネッセンスディスプレイ、及びプラズマディスプレイなどのディスプレイと組み合わせることで、ディスプレイ材料とすることができる。さらに、金属、ガラス、木、紙、及び綿、麻、及び絹などの布地などの部材と組み合わせることで、フォトクロ性を有する玩具や衣服類、傘などを得ることができる。 In the present invention, a polycarbonate resin is preferable as the optical substrate when the laminate is integrated with an optical substrate such as a plastic lens. Examples of the integration method include a method in which the laminate is mounted in a mold and a thermoplastic resin such as a polycarbonate resin is formed by injection molding. In addition, the laminated body of the present invention can be processed into a lens-shaped spherical shape by performing bending before being integrated with the optical substrate. Examples of the method for bending the laminated sheet include hot press processing, pressure processing, and vacuum suction processing. The temperature at the time of bending may be appropriately determined depending on the type of the resin sheet or film used in the laminated sheet, but it is preferably performed at 120 to 200 ° C. Moreover, it can be set as a light shielding window material or an agricultural film by integrating with other resin-made sheets or glass. Moreover, it can be set as a display material by combining with displays, such as a liquid crystal display panel, a field emission display, an electroluminescent display, and a plasma display. Furthermore, by combining with members such as metal, glass, wood, paper, and fabrics such as cotton, hemp, and silk, photochromic toys, clothes, umbrellas, and the like can be obtained.
具体的には、本発明の積層体の両面に珪酸塩ガラスを貼り合わせることにより、遮光窓材として有用な成型体を得ることができる。このような成形体は、貼り合わせた積層体の密着性が高く、耐久性に優れた窓材として期待できる。また、液晶パネルの背面に、本発明の積層体を貼り合わせることにより、屋外でのコントラストに優れたディスプレイ材料を得ることができる。このディスプレイ材料は、種々の形状に加工することが容易であり、特にヘッドアップディスプレイとして有用である。あるいは、本発明の積層体は密着性が高い大型の積層体を得ることができるため、プラズマディスプレイパネルの背面に、本発明の積層体を貼り合わせることにより、屋外でのコントラストに優れたディスプレイ材料、特に屋外ディスプレイとして長期の使用に耐えうる成型体を得ることができる。 Specifically, a molded body useful as a light shielding window material can be obtained by laminating silicate glass on both surfaces of the laminate of the present invention. Such a molded body can be expected as a window material with high adhesion of the laminated body and excellent durability. Moreover, the display material excellent in the contrast outdoors can be obtained by bonding the laminated body of this invention on the back surface of a liquid crystal panel. This display material can be easily processed into various shapes, and is particularly useful as a head-up display. Alternatively, since the laminate of the present invention can provide a large laminate having high adhesion, a display material excellent in contrast outdoors can be obtained by bonding the laminate of the present invention to the back surface of the plasma display panel. In particular, a molded product that can withstand long-term use as an outdoor display can be obtained.
さらに、本発明の積層体は種々の形状に加工することが容易であることからの片側にポリプロピレンフィルムを貼り合わせることにより、農業用フィルムとして長期の使用に耐えうる成型体を得ることができる。また、ポリプロピレンフィルムの代わりに、布地(綿、麻など)、樹脂材料、金属などを本発明の積層体に貼り合わせることで、長期の使用に耐えうる、玩具、及び衣服などの材料として使用できる。 Furthermore, since the laminate of the present invention can be easily processed into various shapes, a molded body that can withstand long-term use as an agricultural film can be obtained by laminating a polypropylene film on one side. Further, instead of polypropylene film, fabric (cotton, hemp, etc.), resin material, metal, etc., can be used as materials for toys, clothes, etc. that can withstand long-term use by bonding to the laminate of the present invention. .
以下に例示するいくつかの実施例によって、本発明をさらに詳しく説明する。これらの実施例は、単に、本発明を説明するためのものであり、本発明の精神及び範囲は、これら実施例に限定されるものではない。 The present invention is further illustrated by the following examples. These examples are merely to illustrate the present invention, and the spirit and scope of the present invention are not limited to these examples.
以下に、実施例及び比較例で各成分として使用した化合物等の略号を纏める。
A1成分;ポリオール化合物
PL1:旭化成ケミカルズ株式会社製デュラノール(1,5−ペンタンジオールとヘキサンジオールを原料とするポリカーボネートジオール、数平均分子量800)。
PL2:旭化成ケミカルズ株式会社製デュラノール(1,5−ペンタンジオールとヘキサンジオールを原料とするポリカーボネートジオール、数平均分子量1000)。
A2成分;ジイソシアネート化合物
NCO1:イソホロンジイソシアネート。
NCO2:4,4’−メチレンビス(シクロヘキシルイソシアネート)の異性体混合物。
B成分;ポリアミン化合物
CE1:イソホロンジアミン。
The abbreviations of the compounds used as the respective components in the examples and comparative examples are summarized below.
A1 component; polyol compound PL1: Duranol manufactured by Asahi Kasei Chemicals Corporation (polycarbonate diol using 1,5-pentanediol and hexanediol as raw materials, number average molecular weight 800).
PL2: Duranol manufactured by Asahi Kasei Chemicals Corporation (polycarbonate diol using 1,5-pentanediol and hexanediol as raw materials, number average molecular weight 1000).
A2 component; diisocyanate compound NCO1: isophorone diisocyanate.
NCO2: Isomeric mixture of 4,4′-methylenebis (cyclohexyl isocyanate).
B component; polyamine compound CE1: isophoronediamine.
CE2:ビス−(4−アミノシクロヘキシル)メタン。
C成分;分子内に1つのイソシアネート基と反応しうる基を有する化合物
HA1:1,2,2,6,6−ペンタメチル−4−アミノピペリジン。
HA2:ノルマルブチルアミン。
有機溶媒
D1:イソプロピルアルコール。
D2:プロピレングリコール−モノメチルエーテル。
D3:トルエン。
D4:ジエチルケトン。
D5:t−ブチルアルコール。
II成分;フォトクロミック化合物
PC1:下記式で示される化合物
CE2: bis- (4-aminocyclohexyl) methane.
Component C: Compound having a group capable of reacting with one isocyanate group in the molecule HA1: 1,2,2,6,6-pentamethyl-4-aminopiperidine.
HA2: normal butylamine.
Organic solvent D1: Isopropyl alcohol.
D2: Propylene glycol monomethyl ether.
D3: Toluene.
D4: Diethyl ketone.
D5: t-butyl alcohol.
II component; photochromic compound PC1: Compound represented by the following formula
PC2:下記式で示される化合物 PC2: Compound represented by the following formula
PC3:下記式で示される化合物 PC3: Compound represented by the following formula
III成分:ポリイソシアネート化合物
CA1:4,4’−メチレンビス(シクロヘキシルイソシアネート)の異性体混合物(分子量262)
その他の成分
L1:エチレンビス(オキシエチレン)ビス[3−(5−tert−ブチル−4−ヒドロキシ−m−トリル)プロピオネート](チバ・スペシャルティ・ケミカルズ社製、Irganox245)。
L2:DOW CORNING TORAY L−7001(東レ・ダウコーニング株式会社製、界面活性剤)。
III component: polyisocyanate compound CA1: isomer mixture of 4,4′-methylenebis (cyclohexyl isocyanate) (molecular weight 262)
Other components L1: Ethylenebis (oxyethylene) bis [3- (5-tert-butyl-4-hydroxy-m-tolyl) propionate] (Irganox 245, manufactured by Ciba Specialty Chemicals).
L2: DOW CORNING TORAY L-7001 (manufactured by Toray Dow Corning Co., Ltd., surfactant).
製造例1(ポリウレタンウレア樹脂の製造)
(ウレタンプレポリマーの製造)
翼径135mmのマックスブレンド翼、邪魔板を備える内径260mm、高さ280mm、仕込用量10Lの反応容器に、冷却管、温度計、窒素ガス導入管を接続した。マックスブレンド翼は100rpmで撹拌した。
この反応容器に、数平均分子量800のポリカーボネートジオール1770g、イソホロンジイソシアネート700g、トルエン500gを仕込み、窒素雰囲気下、100℃で7時間反応させ、末端にイソシアネート基を有するウレタンプレポリマーを合成した。反応の終点は、イソシアネート基の逆滴定法により確認した。
Production Example 1 (Production of polyurethane urea resin)
(Manufacture of urethane prepolymer)
A cooling tube, a thermometer, and a nitrogen gas introduction tube were connected to a reaction vessel having a blade diameter of 135 mm, a Max Blend blade, an inner diameter of 260 mm equipped with baffle plates, a height of 280 mm, and a charged amount of 10 L. The Max Blend blade was agitated at 100 rpm.
Into this reaction vessel, 1770 g of polycarbonate diol having a number average molecular weight of 800, 700 g of isophorone diisocyanate and 500 g of toluene were charged and reacted at 100 ° C. for 7 hours in a nitrogen atmosphere to synthesize a urethane prepolymer having an isocyanate group at the terminal. The end point of the reaction was confirmed by an isocyanate group back titration method.
(ポリウレタンウレア樹脂(U1)の製造)
ウレタンプレポリマー反応終了後、反応液を0℃付近まで冷却し、イソプロピルアルコール1430g、ジエチルケトン2670gに溶解させた後、液温を0℃に保持した。次いで、鎖延長剤であるビス−(4−アミノシクロヘキシル)メタン171gとジエチルケトン145gの混合溶液を30分以内に滴下し、0℃で1時間反応させた。その後さらに、1,2,2,6,6−ペンタメチル−4−アミノピペリジン42gを滴下し、0℃で1時間反応させることにより、ポリウレタンウレア樹脂のジエチルケトン溶液を得た。得られたポリウレタンウレア樹脂は、数平均分子量が19,000であり、重量平均分子量が41,000であり、多分散度が2.16であり、軟化点が105℃(軟化開始温度;約80℃)であり、動粘度が15,000cStであった。
なお、ポリアミン化合物であるビス−(4−アミノシクロヘキシル)メタンの滴下開始時の反応液の粘度が0.06kg/m・s、密度が900kg/m3、マックスブレンド翼の回転数が100rpmであり、レイノルズ数(Re)が456となり、マックスブレンド翼におけるn・θM−Re曲線より、混合時間数(n・θM)が14であることから、完全混合時間(θM)が8秒であった。
(Manufacture of polyurethane urea resin (U1))
After completion of the urethane prepolymer reaction, the reaction solution was cooled to around 0 ° C., dissolved in 1430 g of isopropyl alcohol and 2670 g of diethyl ketone, and the solution temperature was kept at 0 ° C. Next, a mixed solution of 171 g of chain extender bis- (4-aminocyclohexyl) methane and 145 g of diethyl ketone was added dropwise within 30 minutes and reacted at 0 ° C. for 1 hour. Thereafter, 42 g of 1,2,2,6,6-pentamethyl-4-aminopiperidine was further added dropwise and reacted at 0 ° C. for 1 hour to obtain a diethyl ketone solution of polyurethane urea resin. The resulting polyurethane urea resin has a number average molecular weight of 19,000, a weight average molecular weight of 41,000, a polydispersity of 2.16, and a softening point of 105 ° C. (softening start temperature; about 80 ° C) and the kinematic viscosity was 15,000 cSt.
The viscosity of the reaction liquid at the start of dropping of the polyamine compound bis- (4-aminocyclohexyl) methane is 0.06 kg / m · s, the density is 900 kg / m 3 , and the rotation speed of the Max Blend blade is 100 rpm. , The Reynolds number (Re) is 456, and the mixing time number (n · θ M ) is 14 from the n · θ M -Re curve in the Max blend blade, so the complete mixing time (θ M ) is 8 seconds. there were.
<評価方法>
上記ウレタンウレア樹脂の、数平均分子量、重量平均分子量、多分散度、軟化点、及び動粘度については以下の方法によって測定した。
<Evaluation method>
The number average molecular weight, weight average molecular weight, polydispersity, softening point, and kinematic viscosity of the urethane urea resin were measured by the following methods.
(数平均分子量、重量平均分子量、及び多分散度)
数平均分子量、重量平均分子量、及び多分散度に関しては、本文中に記載の方法に分析を実施した。
すなわち、ポリエチレンオキシド換算によるゲル・パーミエイション・クロマトグラフ(GPC)を用いて、カラム:Shodex KD−806M(昭和電工株式会社製)を2本直列接続、溶離液:LiBr(10mmol/L)/DMF溶液、流速:1ml/min、検出器:RI検出器、ポリウレタンウレア樹脂試料溶液:1.0%ジメチルホルムアミド(DMF)溶液の条件にて測定し、日本ウォーターズ株式会社製GPC解析ソフト『Empower Personal GPC Option』を用いて算出した。また、多分散度は、重量平均分子量/数平均分子量で算出される値であり、上記方法によって求められた数平均分子量、及び重量平均分子量より算出した。
(Number average molecular weight, weight average molecular weight, and polydispersity)
Regarding the number average molecular weight, weight average molecular weight, and polydispersity, the analysis was carried out by the method described in the text.
That is, using gel permeation chromatograph (GPC) in terms of polyethylene oxide, two columns: Shodex KD-806M (manufactured by Showa Denko KK) connected in series, eluent: LiBr (10 mmol / L) / Measured under the conditions of DMF solution, flow rate: 1 ml / min, detector: RI detector, polyurethane urea resin sample solution: 1.0% dimethylformamide (DMF) solution, GPC analysis software “Empower Personal” manufactured by Japan Waters Co., Ltd. It was calculated using “GPC Option”. The polydispersity is a value calculated by weight average molecular weight / number average molecular weight, and was calculated from the number average molecular weight and the weight average molecular weight determined by the above method.
(軟化点)
ポリウレタンウレア樹脂溶液を、ステンレスの容器に流し込み、40℃で10時間、60℃で10時間、さらに真空乾燥機にて60℃で12時間乾燥させることにより、厚み1mmの試験片を作製した。得られた試験片を、熱機械測定装置(セイコーインスツルメント社製、TMA120C)を用い、昇温速度:10℃/分、測定温度範囲:30〜200℃、プローブ:先端径0.5mmの針入プローブの条件にて軟化点を測定した。
(Softening point)
A polyurethane urea resin solution was poured into a stainless steel container, and dried at 40 ° C. for 10 hours, 60 ° C. for 10 hours, and further dried at 60 ° C. for 12 hours in a vacuum dryer to prepare a test piece having a thickness of 1 mm. The obtained test piece was measured using a thermomechanical measurement device (Seiko Instruments, TMA120C), with a temperature increase rate of 10 ° C./min, a measurement temperature range of 30 to 200 ° C., and a probe with a tip diameter of 0.5 mm. The softening point was measured under the conditions of the needle probe.
(動粘度)
ポリウレタン樹脂溶液約10gを、キャノンフェンスケ粘度計(#600)に入れ、このキャノンフェンスケ粘度計(柴田科学株式会社製)を25℃±0.1℃に制御した恒温水槽に15分浸した後、動粘度を測定した。
(Kinematic viscosity)
About 10 g of the polyurethane resin solution was put into a Canon Fenceke viscometer (# 600), and this Canon Fenceke viscometer (manufactured by Shibata Kagaku Co., Ltd.) was immersed in a constant temperature water bath controlled at 25 ° C. ± 0.1 ° C. for 15 minutes. Thereafter, the kinematic viscosity was measured.
製造例2〜17
表1に示すポリオール化合物(A1成分)、ジイソシアネート化合物(A2成分)、ポリアミン化合物(B成分)、分子内に1つのイソシアネート基と反応しうる基を有する化合物(C成分)及び有機溶媒を用い、表1、及び表2に示す反応条件を用いた以外は、U1の合成方法と同様にして、U2〜17のポリウレタンウレア樹脂を合成した。評価結果を表2に示す。なお、完全混合時間(θM)は、ポリアミン化合物(B成分)を滴下開始する際のウレタンプレポリマー(A成分)の反応液の粘度、密度、及びマックスブレンド翼の回転数からレイノルズ数(Re)を算出し、その後マックスブレンド翼におけるn・θM−Re曲線から導きだされるn・θMより算出した。
Production Examples 2 to 17
Using a polyol compound (A1 component), a diisocyanate compound (A2 component), a polyamine compound (B component), a compound having a group capable of reacting with one isocyanate group (C component) and an organic solvent shown in Table 1, Except for using the reaction conditions shown in Table 1 and Table 2, polyurethane urea resins of U2 to 17 were synthesized in the same manner as the synthesis method of U1. The evaluation results are shown in Table 2. The complete mixing time (θ M ) is determined from the Reynolds number (Re) based on the viscosity and density of the reaction liquid of the urethane prepolymer (component A) at the start of dropping of the polyamine compound (component B) and the rotation speed of the Max blend blade. ) was calculated, and then calculated from the n · θ M which is Dasa led from the n · θ M -Re curve in Max blend wing.
実施例1
(前駆体組成物の調製)
ポリウレタンウレア樹脂(U1)の溶液1000g、フォトクロミック化合物12.1g(PC1/PC2/PC3=8.7/2.0/1.4g)、4,4’−メチレンビス(シクロヘキシルイソシアネート)の異性体混合物 43.2g、さらに酸化防止剤としてエチレンビス(オキシエチレン)ビス[3−(5−tert−ブチル−4−ヒドロキシ−m−トリル)プロピオネート] 3.6g、界面活性剤としてDOW CORNING TORAY L−7001 0.5gを添加し、室温で攪拌・混合を行い、前駆体組成物を得た。
Example 1
(Preparation of precursor composition)
43 g of polyurethane urea resin (U1) solution, 12.1 g of photochromic compound (PC1 / PC2 / PC3 = 8.7 / 2.0 / 1.4 g), isomer mixture of 4,4′-methylenebis (cyclohexyl isocyanate) 43 .2 g, ethylene bis (oxyethylene) bis [3- (5-tert-butyl-4-hydroxy-m-tolyl) propionate] as an antioxidant, 3.6 g, DOW CORNING TORAY L-7001 as a surfactant 0.5 g was added and stirred and mixed at room temperature to obtain a precursor composition.
(第2接着層用接着剤の調整)
ポリウレタンウレア樹脂(U4)の溶液1000gに、界面活性剤としてDOW CORNING TORAY L−7001 0.7gを添加し、室温で攪拌・混合を行い、第2接着層用接着剤を得た。
(Adjustment of second adhesive layer adhesive)
To 1000 g of the polyurethane urea resin (U4) solution, 0.7 g of DOW CORNING TORAY L-7001 as a surfactant was added, and stirred and mixed at room temperature to obtain an adhesive for the second adhesive layer.
(積層シートの作製)
コーター(テスター産業製)を用いて、積層シートを作製した。第2接着層用接着剤を厚み300μmのポリカーボネートシート上に、塗工速度0.5m/minで塗工し、乾燥温度110℃で3分間乾燥させることにより、膜厚8μmの第2接着層を有するポリカーボネートシートを得た。
(Production of laminated sheet)
A laminated sheet was prepared using a coater (manufactured by Tester Sangyo). The second adhesive layer having a thickness of 8 μm is formed by applying the adhesive for the second adhesive layer onto a polycarbonate sheet having a thickness of 300 μm at a coating speed of 0.5 m / min and drying at a drying temperature of 110 ° C. for 3 minutes. A polycarbonate sheet was obtained.
上記前駆体組成物を、PET製フィルム(帝人デュポンフィルム株式会社製ピューレックスフィルム、シリコン塗膜付)上に、塗工速度0.3m/minで塗工し、乾燥温度100℃で5分間乾燥させ、厚み約40μmのフォトクロミック性接着層を得て、第2接着層を有するポリカーボネートシートを0.1MPaの圧力で張り合わせた。
次いで、上記前駆体組成物を塗布したPET製フィルムと第2接着層を有するポリカーボネートシートを張り合わせた積層体のPET製フィルムを剥離し、剥離した面と第2接着層を有するポリカーボネートシートを0.1MPaの圧力で張り合わせ、積層シートを得た。積層シートは、フォトクロミック性接着層である第1接着層の両面に第2接着層を有し、さらに第2接着層の外面(第1接着層が積層していない面)にポリカーボネートシートが積層した構成であった。得られた積層シートを40℃、真空下で24時間静置した後、110℃で60分加熱処理し、次いで60℃、100%RHで24時間の加湿処理を行い、最後に40℃、真空下で24時間静置することにより、目的のフォトクロミック特性を有する積層シートを得た。残存溶剤量を測定したところ、0.01%であった。なお、最終的に得られたフォトクロミック性接着シートをポリカーボネートシートから剥離し、赤外吸収スペクトルを確認したところ、該フォトクロミック性接着シート中にイソシアネート基のピークは検出されなかった。
The precursor composition is applied on a PET film (Purex film manufactured by Teijin DuPont Films Ltd., with silicon coating) at a coating speed of 0.3 m / min, and dried at a drying temperature of 100 ° C. for 5 minutes. Thus, a photochromic adhesive layer having a thickness of about 40 μm was obtained, and the polycarbonate sheet having the second adhesive layer was laminated with a pressure of 0.1 MPa.
Next, the PET film of the laminate obtained by laminating the PET film coated with the precursor composition and the polycarbonate sheet having the second adhesive layer is peeled, and the polycarbonate sheet having the peeled surface and the second adhesive layer is reduced to 0.00. Lamination was performed with a pressure of 1 MPa to obtain a laminated sheet. The laminated sheet has a second adhesive layer on both surfaces of the first adhesive layer which is a photochromic adhesive layer, and a polycarbonate sheet is laminated on the outer surface of the second adhesive layer (the surface on which the first adhesive layer is not laminated). It was a configuration. The obtained laminated sheet was allowed to stand at 40 ° C. under vacuum for 24 hours, and then heat-treated at 110 ° C. for 60 minutes, and then humidified at 60 ° C. and 100% RH for 24 hours. The laminated sheet which has the target photochromic characteristic was obtained by leaving still for 24 hours under. The amount of residual solvent was measured and found to be 0.01%. In addition, when the photochromic adhesive sheet finally obtained was peeled from the polycarbonate sheet and the infrared absorption spectrum was confirmed, the peak of isocyanate group was not detected in the photochromic adhesive sheet.
得られた積層シートのフォトクロミック特性としての発色濃度は1.0であり、退色速度は45秒であり、耐久性は93%であった。また、剥離強度は初期が200N/25mm、70℃雰囲気下での剥離強度が140N/25mm、が150℃雰囲気下での剥離強度が40N/25mmであり、耐汗試験における密着安定時間は1200時間であった。
なお、これらの評価は以下のようにして行った。
The resulting laminated sheet had a color density of 1.0 as a photochromic property, a fading speed of 45 seconds, and a durability of 93%. The peel strength is 200 N / 25 mm in the initial stage, the peel strength in a 70 ° C. atmosphere is 140 N / 25 mm, and the peel strength in a 150 ° C. atmosphere is 40 N / 25 mm. The adhesion stabilization time in the sweat resistance test is 1200 hours. Met.
These evaluations were performed as follows.
〔フォトクロミック特性〕
得られた積層シートを試料とし、これに、(株)浜松ホトニクス製のキセノンランプL−2480(300W)SHL−100を、エアロマスフィルター(コーニング社製)を介して23℃、積層シート表面でのビーム強度365nm=2.4mW/cm2、245nm=24μW/cm2で120秒間照射して発色させ、積層シートのフォトクロミック特性を測定した。
[Photochromic characteristics]
The obtained laminated sheet was used as a sample, and a xenon lamp L-2480 (300W) SHL-100 manufactured by Hamamatsu Photonics Co., Ltd. was applied to the laminated sheet surface through an aeromass filter (manufactured by Corning). The film was irradiated for 120 seconds with a beam intensity of 365 nm = 2.4 mW / cm 2 and 245 nm = 24 μW / cm 2 to develop color, and the photochromic characteristics of the laminated sheet were measured.
1)最大吸収波長(λmax):(株)大塚電子工業製の分光光度計(瞬間マルチチャンネルフォトディレクターMCPD1000)により求めた発色後の最大吸収波長である。該最大吸収波長は、発色時の色調に関係する。 1) Maximum absorption wavelength (λmax): This is the maximum absorption wavelength after color development determined by a spectrophotometer (instant multichannel photo director MCPD1000) manufactured by Otsuka Electronics Co., Ltd. The maximum absorption wavelength is related to the color tone at the time of color development.
2)発色濃度〔ε(120)−ε(0)〕:前記最大吸収波長における、120秒間照射した後の吸光度ε(120)と最大吸収波長における未照射時の吸光度ε(0)との差。この値が高いほどフォトクロミック性が優れていると言える。 2) Color density [ε (120) −ε (0)]: difference between absorbance ε (120) after irradiation for 120 seconds at the maximum absorption wavelength and absorbance ε (0) without irradiation at the maximum absorption wavelength . It can be said that the higher this value, the better the photochromic properties.
3)退色速度〔t1/2(sec.)〕:120秒間照射後、光の照射をとめたときに、試料の前記最大波長における吸光度が〔ε(120)−ε(0)〕の1/2まで低下するのに要する時間。この時間が短いほどフォトクロミック性が優れているといえる。 3) Fading speed [t1 / 2 (sec.)]: When light irradiation is stopped after irradiation for 120 seconds, the absorbance at the maximum wavelength of the sample is 1 / ([ε (120) −ε (0)]). Time required to drop to 2. It can be said that the shorter this time is, the better the photochromic property is.
4)耐久性(%)=〔(A96/A0)×100〕:光照射による発色の耐久性を評価するために次の劣化促進試験を行った。すなわち、得られた積層シートをスガ試験器(株)製キセノンウェザーメーターX25により96時間促進劣化させた。その後、前記発色濃度の評価を試験の前後で行い、試験前の発色濃度(A0)および試験後の発色濃度(A96)を測定し、〔(A96)/A0〕×100〕の値を残存率(%)とし、発色の耐久性の指標とした。残存率が高いほど発色の耐久性が高い。 4) Durability (%) = [(A96 / A0) × 100]: In order to evaluate the durability of color development by light irradiation, the following deterioration acceleration test was conducted. That is, the obtained laminated sheet was accelerated and deteriorated for 96 hours using a Xenon weather meter X25 manufactured by Suga Test Instruments Co., Ltd. Thereafter, the color density was evaluated before and after the test, the color density (A0) before the test and the color density (A96) after the test were measured, and the value of [(A96) / A0] × 100] was determined as the residual rate. (%) And used as an index of color durability. The higher the remaining rate, the higher the durability of coloring.
〔剥離強度〕
得られた積層シートを、25×100mmの接着部分を有する試験片とし、試験雰囲気温度が設定可能な恒温槽を備えた試験機(オートグラフAGS−500NX、島津製作所製)に装着し、クロスヘッドスピード100mm/minで引張り試験を行い、それぞれ下記1)〜3)の剥離強度を測定した。
[Peel strength]
The obtained laminated sheet is used as a test piece having an adhesive portion of 25 × 100 mm, and is mounted on a testing machine (Autograph AGS-500NX, manufactured by Shimadzu Corp.) equipped with a thermostatic bath capable of setting a test atmosphere temperature. A tensile test was performed at a speed of 100 mm / min, and the peel strengths 1) to 3) below were measured.
1)初期の剥離強度は、上記の通り試験を実施した。
2)70℃雰囲気下での剥離強度は、上記サイズに切り出した試験片を、70℃に設定した恒温槽内で10分加熱した後、上記のようにして測定した。
3)150℃雰囲気下での剥離強度は、上記にサイズに切り出した試験片を、150℃に設定した恒温槽内で10分加熱した後、上記のようにして測定した。
1) The initial peel strength was tested as described above.
2) The peel strength in a 70 ° C. atmosphere was measured as described above after heating a test piece cut out to the above size for 10 minutes in a thermostat set at 70 ° C.
3) The peel strength in an atmosphere at 150 ° C. was measured as described above after the test piece cut out in size was heated for 10 minutes in a thermostat set at 150 ° C.
〔耐汗試験〕
得られた積層シートを、直径50mmの円形に切り出し、この試験片の外周をリング状のステンレス製治具で締め付けた。別途、蓋付きのプラスチック容器に人工汗(10%の食塩、及び5%の乳酸を添加した蒸留水)を用意し、この人工汗中に前記試験片を浸漬した。この試験片、及び人工汗が入ったプラスチック容器を70℃で保管し、24時間毎に試験片端部の剥離有無を目視評価した。評価結果の数値は、安定した接着性を示した時間(剥離が生じる直前までの時間)である。
[Sweat resistance test]
The obtained laminated sheet was cut into a circle having a diameter of 50 mm, and the outer periphery of the test piece was clamped with a ring-shaped stainless steel jig. Separately, artificial sweat (distilled water added with 10% sodium chloride and 5% lactic acid) was prepared in a plastic container with a lid, and the test piece was immersed in the artificial sweat. This test piece and a plastic container containing artificial sweat were stored at 70 ° C., and the presence or absence of peeling at the end of the test piece was visually evaluated every 24 hours. The numerical value of the evaluation result is a time (time until immediately before peeling occurs) showing stable adhesiveness.
実施例2
(前駆体組成物の調整)
前駆体組成物は実施例1と同様の方法で得た。
Example 2
(Preparation of precursor composition)
The precursor composition was obtained in the same manner as in Example 1.
(積層シートの作製)
コーター(テスター産業製)を用いて、積層シートを作製した。上記前駆体組成物を、PET製フィルム(帝人デュポンフィルム株式会社製ピューレックスフィルム、シリコン塗膜付)上に、塗工速度0.3m/minで塗工し、乾燥温度100℃で5分間乾燥させ、厚み約40μmのフォトクロミック性接着層を得て、ポリカーボネートシートを0.1MPaの圧力で張り合わせた。
(Production of laminated sheet)
A laminated sheet was prepared using a coater (manufactured by Tester Sangyo). The precursor composition is applied on a PET film (Purex film manufactured by Teijin DuPont Films Ltd., with silicon coating) at a coating speed of 0.3 m / min, and dried at a drying temperature of 100 ° C. for 5 minutes. Thus, a photochromic adhesive layer having a thickness of about 40 μm was obtained, and the polycarbonate sheet was laminated with a pressure of 0.1 MPa.
次いで、上記前駆体組成物を塗布したPET製フィルムとポリカーボネートシートを張り合わせた積層体のPET製フィルムを剥離し、剥離した面とポリカーボネートシートを0.1MPaの圧力で張り合わせ、積層シートを得た。積層シートは、フォトクロミック性接着層である第1接着層の両面にポリカーボネートシートが積層した構成であった。得られた積層シートを40℃、真空下で24時間静置した後、110℃で60分加熱処理し、次いで60℃、100%RHで24時間の加湿処理を行い、最後に40℃、真空下で24時間静置することにより、目的のフォトクロミック特性を有する積層シートを得た。残存溶剤量を測定したところ、0.01%であった。なお、最終的に得られたフォトクロミック性接着シートをポリカーボネートシートから剥離し、赤外吸収スペクトルを確認したところ、該フォトクロミック性接着シート中にイソシアネート基のピークは検出されなかった。 Next, the PET film of the laminate obtained by laminating the PET film coated with the precursor composition and the polycarbonate sheet was peeled off, and the peeled surface and the polycarbonate sheet were stuck together at a pressure of 0.1 MPa to obtain a laminated sheet. The laminated sheet had a configuration in which polycarbonate sheets were laminated on both surfaces of the first adhesive layer which is a photochromic adhesive layer. The obtained laminated sheet was allowed to stand at 40 ° C. under vacuum for 24 hours, and then heat-treated at 110 ° C. for 60 minutes, and then humidified at 60 ° C. and 100% RH for 24 hours. The laminated sheet which has the target photochromic characteristic was obtained by leaving still for 24 hours under. The amount of residual solvent was measured and found to be 0.01%. In addition, when the photochromic adhesive sheet finally obtained was peeled from the polycarbonate sheet and the infrared absorption spectrum was confirmed, the peak of isocyanate group was not detected in the photochromic adhesive sheet.
得られた積層シートのフォトクロミック特性としての発色濃度は1.0であり、退色速度は47秒であり、耐久性は92%であった。また、剥離強度は初期が150N/25mm、70℃雰囲気下での剥離強度が100N/25mm、が150℃雰囲気下での剥離強度が20N/25mmであり、耐汗試験における密着安定時間は400時間であった。
なお、これらの評価は実施例1と同様の方法により実施した。
The resulting laminated sheet had a color density of 1.0 as a photochromic property, a fading speed of 47 seconds, and a durability of 92%. The peel strength is initially 150 N / 25 mm, the peel strength in a 70 ° C. atmosphere is 100 N / 25 mm, the peel strength in a 150 ° C. atmosphere is 20 N / 25 mm, and the adhesion stabilization time in the sweat resistance test is 400 hours. Met.
These evaluations were performed by the same method as in Example 1.
実施例3〜9、11〜16、比較例1
表3に示すポリウレタンウレア樹脂(I成分)、フォトクロミック化合物(II成分)、ポリイソシアネート化合物(III成分)、有機溶媒、その他の成分、第2接着層を用いた以外は実施例1と同様の方法で積層シートを得た。得られた各種積層シートの評価結果を表4に示した。
Examples 3-9, 11-16, Comparative Example 1
The same method as in Example 1 except that the polyurethane urea resin (I component), photochromic compound (II component), polyisocyanate compound (III component), organic solvent, other components, and second adhesive layer shown in Table 3 were used. A laminated sheet was obtained. Table 4 shows the evaluation results of the obtained various laminated sheets.
実施例10、比較例2
表3に示すポリウレタンウレア樹脂(I成分)、フォトクロミック化合物(II成分)、ポリイソシアネート化合物(III成分)、有機溶媒、その他の成分、を用いた以外は実施例2と同様の方法で積層シートを得た。得られた各種積層シートの評価結果を表4に示した
Example 10 and Comparative Example 2
A laminated sheet was prepared in the same manner as in Example 2 except that the polyurethane urea resin (I component), photochromic compound (II component), polyisocyanate compound (III component), organic solvent, and other components shown in Table 3 were used. Obtained. Table 4 shows the evaluation results of the obtained various laminated sheets.
上記実施例1〜16から明らかなように、多分散度が狭いウレタンウレア樹脂を用いた、本発明の積層シートは良好な密着性を有していることが分かる。特に、高温下における密着性に優れている。 As is clear from Examples 1 to 16, the laminated sheet of the present invention using a urethane urea resin having a narrow polydispersity has good adhesion. In particular, it has excellent adhesion at high temperatures.
一方、比較例1、及び2に示すように、多分散度が広いウレタンウレア樹脂を用いた積層シートは十分な密着性を得ることができなかった。 On the other hand, as shown in Comparative Examples 1 and 2, a laminated sheet using a urethane urea resin having a wide polydispersity could not obtain sufficient adhesion.
Claims (14)
(II)フォトクロミック化合物
を含んでなるフォトクロミック組成物。 (I) A photochromic composition comprising a polyurethane urea resin having a polydispersity (weight average molecular weight / number average molecular weight) in the range of 1.6 to 2.4, and (II) a photochromic compound.
(III)分子内に少なくとも2つのイソシアネート基を有するポリイソシアネート化合物
を含んでいることを特徴とする請求項1に記載のフォトクロミック組成物。 The photochromic composition according to claim 1, wherein the photochromic composition further comprises (III) a polyisocyanate compound having at least two isocyanate groups in the molecule.
(A)分子末端にイソシアネート基を有するウレタンプレポリマーと、
(B)分子内に2つ以上のアミノ基を有するポリアミン化合物と、
を反応して得られる樹脂である請求項1記載のフォトクロミック組成物。 The polyurethane urea resin is
(A) a urethane prepolymer having an isocyanate group at the molecular end;
(B) a polyamine compound having two or more amino groups in the molecule;
The photochromic composition according to claim 1, wherein the photochromic composition is a resin obtained by reaction.
(C)分子内にイソシアネート基と反応しうる基を1つ有する化合物と、
を反応して得られる樹脂である請求項4記載のフォトクロミック組成物。 Further, the polyurethane urea resin is
(C) a compound having one group capable of reacting with an isocyanate group in the molecule;
The photochromic composition according to claim 4, which is a resin obtained by reacting the above.
(A1)ポリエーテルポリオール、ポリエステルポリオール、ポリカーボネートポリオール、及びポリカプロラクトンポリオールの少なくとも2つ以上の水酸基を有するポリオールよりなる群から選ばれる少なくとも1種のポリオール化合物と、
(A2)分子内に2つのイソシアネート基を有するジイソシアネート化合物と、
を反応して得られるウレタンプレポリマーである請求項4記載のフォトクロミック組成物。 The urethane prepolymer is
(A1) a polyether polyol, a polyester polyol, polycarbonate polyol, and at least one polyol selected from the group consisting of a polyol having at least two or more hydroxyl groups of the polycaprolactone polyol Lumpur compound,
(A2) a diisocyanate compound having two isocyanate groups in the molecule;
The photochromic composition according to claim 4, wherein the photochromic composition is a urethane prepolymer obtained by reaction.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015049296 | 2015-03-12 | ||
| JP2015049296 | 2015-03-12 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016169363A JP2016169363A (en) | 2016-09-23 |
| JP6579938B2 true JP6579938B2 (en) | 2019-09-25 |
Family
ID=56982231
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015244512A Active JP6579938B2 (en) | 2015-03-12 | 2015-12-15 | Photochromic composition, laminate comprising the composition, and article using the laminate |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6579938B2 (en) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MX2018007795A (en) | 2015-12-28 | 2018-09-05 | Tokuyama Corp | Laminate and optical article using said laminate. |
| US20200283662A1 (en) | 2016-08-02 | 2020-09-10 | Tokuyama Corporation | Adhesive composition, laminate and optical article comprising the laminate |
| JP6542982B2 (en) * | 2016-10-11 | 2019-07-10 | 三井化学株式会社 | POLYMERIZABLE COMPOSITION FOR OPTICAL MATERIAL AND USE THEREOF |
| WO2019117305A1 (en) * | 2017-12-15 | 2019-06-20 | Mitsui Chemicals, Inc. | Polymerizable composition for optical materials and application of same |
| EP3757663A4 (en) * | 2018-02-23 | 2022-03-23 | Tokuyama Corporation | Functional multilayer body and functional lens using functional multilayer body |
| JP7152173B2 (en) * | 2018-04-17 | 2022-10-12 | 株式会社トクヤマ | Method for producing photochromic cured body |
| EP4088927A4 (en) * | 2020-02-27 | 2024-01-10 | Tokuyama Corporation | Primer composition for optical article, and laminate |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TW591047B (en) * | 2002-11-19 | 2004-06-11 | Chung Shan Inst Of Science | Process for preparing poly(urea-urethane) |
| CN102712736B (en) * | 2009-10-30 | 2014-12-17 | 三菱化学株式会社 | Polyester polyol, polyurethane utilizing the polyester polyol and process for production thereof, and polyurethane molded article |
| WO2013099640A1 (en) * | 2011-12-26 | 2013-07-04 | 株式会社トクヤマ | Photochromic composition |
| JP5895634B2 (en) * | 2012-03-16 | 2016-03-30 | Dic株式会社 | Polyurethane polyurea resin and printing ink |
-
2015
- 2015-12-15 JP JP2015244512A patent/JP6579938B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2016169363A (en) | 2016-09-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6049638B2 (en) | Photochromic composition | |
| JP6579938B2 (en) | Photochromic composition, laminate comprising the composition, and article using the laminate | |
| TWI712494B (en) | Laminated body and optical article using the laminated body | |
| KR102197929B1 (en) | Adhesive composition, laminate, and optical article using the laminate | |
| WO2012018070A1 (en) | Photochromic composition | |
| JP5743616B2 (en) | Photochromic composition | |
| JPWO2012141250A1 (en) | Photochromic composition | |
| JP5888895B2 (en) | Photochromic laminate and manufacturing method thereof | |
| JP5863317B2 (en) | Photochromic composition | |
| JP5967877B2 (en) | Photochromic composition and optical article | |
| JP2016132696A (en) | Photochromic composition for spray coating, and method for producing optical article having photochromic characteristics | |
| JP5591175B2 (en) | Photochromic polymerizable composition |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180912 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20190516 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190611 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190718 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20190730 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20190827 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6579938 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |