以下の記載において、システムのより完全な記載を提供するために、数多くの詳細が説明されている。しかしながら、当業者にとって、開示されたシステムがそれらの具体的な詳細なしで実行できることは明らかである。他の事例において、よく知られた特徴は、不必要にシステムを不明瞭にしないように、詳細に記載されていない。
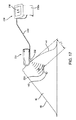
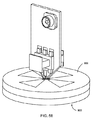
図面を参照すると、図1は、胸部内または体の中の他の場所の、腫瘍、病変または他の組織構造のような患者の体内のターゲットとなる組織領域の位置決めのためのシステム10の典型的な実施例を示す。システム10は、一般的に、マーカー装置または位置決めワイヤー20、および、電磁パルス、波またはレーザーなどの他の信号を使用して、位置決めワイヤー20の少なくとも部分を検知するためのプローブ30、を含む。位置決めワイヤー20は、近位端22a、遠位端22bおよび遠位端22b上のターゲット26を含む細長い部材またはシャフトを有してもよい。任意に、システム10は、位置決めワイヤー20に加えて、1つ以上の付加的な位置決め決定ワイヤーおよび/またはターゲット(図示せず)を含むことができる。
シャフト22は、組織を介しての位置決めワイヤー20の経皮的な導入を促進するために十分なコラム強さを有する、例えば固体ロッドまたは中空の管状体比較的固い材料から形成される。シャフト22は、例えば約0.5および10センチメートルの間(0.5−10cm)の、患者体外の位置から組織を介してターゲットとなる組織領域まで十分に延びる長さを有することができる。任意に、シャフト22は、例えば必要に応じてシャフト22が傾くことができあるいは希望の形状に形成されることができるように、可鍛性を有するかあるいは可塑変形可能とすることができる。
ターゲット26は、プローブ30を使用して遠位端22bの位置決めを促進するように、シャフト22の遠位端22b上で1つ以上の特徴を含む。ここで示した典型的な実施例において、ターゲット26は、例えば約0.5および5ミリメートルの間(0.5−5mm)の、例えばシャフト22の遠位端22bよりもより大きな直径を有する球状体などの、球状構造とすることができる。任意に、ターゲット26は、電磁信号の受信および反射を促進するための1つ以上の特徴を含むことができる。例えば、ターゲット26は、例えば明細書の他の場所に記載されたマーカーと同様に、1つ以上の材料から形成されるか、および/または、レーダーによる同定を高めることができる。別の実施例では、本書の他の実施例と同様に、レーダーの反射および/または検出を向上する1つ以上のコーナーおよび/またはエッジを含む、例えば立方体、三角形、らせん形などの、他の形態および/または形状のものが設けられてもよい。
それに加えてまたはその代わりに、ターゲット26は、例えば病変42の周囲の望ましいマージンの特定を促進するために、病変42のサイズおよび/または形状に近似したサイズおよび/または形状を有することができる。例えば、病変42のサイズおよび/または形状は前もって決定することができ、ターゲット26は、サイズおよび/または形状の異なるターゲットのセットから選択することができ、シャフト22に固定することができる(または各ターゲットはそれ自身のシャフトに設けられる)。それに加えてまたはその代わりに、複数の位置決めワイヤーおよび/またはターゲットが設けられる場合、各ターゲットは、例えばプローブ30を使用して、ターゲットと他のターゲットとの区別を促進するために、異なる形状および/または特徴を有することができる。
ある実施例において、シャフト22およびターゲット26は、同じ材料から一体に形成することができる。また、ターゲット26は、シャフト22と異なる材料から形成することができ、ターゲット26は、例えば、接着剤による接合、溶接、はんだ付け、締りばめ、糸や他の協働連結具などによって、遠位端22bに固定することができる。そのため、この変形例において、ターゲット26は、シャフト22に対するレーダーによる同定を高める材料から形成することができる。
任意に、複数のターゲットが植え込まれている場合、各ターゲットは、特定のターゲットを1つ以上の他のターゲットに対し区別可能な、表面、形状および/または付加的な材料の特徴を有することができる。例えば、各ターゲットは、そのターゲットに特定されており、それを一意的に特定するために使用される、特定の電磁信号を、吸収または反射することができる。
他のオプションにおいて、位置決めワイヤー20は、アンカーエレメント24が不必要なほど十分にターゲット26自身が位置決めワイヤー20を安定化することができたとしても、例えばターゲット26の近傍の遠位端22b上に1つ以上のアンカーエレメント24を含むことができる。
図のように、アンカーエレメント24は、例えば、ターゲット26から隣接して離れるように角度つけられた、シャフト22から横切るように延びる複数返し24(ここでは2つを示す)を含んでいる。そのため、返し24は、例えばその後の近位での離脱を防止しながら位置決めワイラー20が組織を通って遠位方向に前進することを許すように、位置決めワイヤー20が組織中に挿入された後、位置決めワイヤー20を所定の位置にアンカーするための構成とすることができる。例えば、返し24は、例えば前進を促進するように位置決めワイヤー20のプロファイルを最小にするために、シャフト22に対して、あるいは、シャフト22の近傍に、返し24が圧縮されるのに十分な可とう性を有することができるが、その一方で、図示のように、横断方向に対し外側に戻るように弾性的にバイアスをかけることができる。
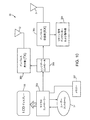
プローブ30は、例えば消費電力の小さいインパルスレーダー(MIR)プローブのように、電磁信号送信および受信能力を有する携帯機器とすることができる。例えば、図1に示されているように、プローブ30は、例えば患者の皮膚またはその下の組織のように、組織に対しまたは組織の近傍に配置されることを意図する第1の端部30aと、例えばユーザーによって保持される第2の対向端部30bと、を含む携帯端末とすることができる。図10を付加的に参照すると、プローブ30は、例えば送信アンテナ32および受信アンテナ34などの1つ以上のアンテナと、1つ以上のプロセッサーまたはコントローラー36と、ディスプレー38と、を含むことができる。
図10に戻ると、プロセッサ36は、送信アンテナ32による送信のための信号の生成、および/または、受信アンテナ34から受信された信号の処理、に必要な、1つ以上のコントローラー、回路、信号発生器、ゲートなど(図示せず)を含むことができる。プロセッサー36の構成要素は、要望に応じて、個別部品、半導体素子、プログラマブル素子、ソフトウェアコンポーネントなどを含むことができる。例えば、図示のように、プローブ30は、例えば送信信号を生成するために送信アンテナ32と結合した、パルス発生器および/または疑似雑音発生器(図示せず)などのインパルス発生器36b、および、受信アンテナ34によって検知された信号を受信するためのインパルス受信器36c、を含むことができる。プロセッサー36は、アンテナ32を介して電磁パルス、波または他の信号を送信し、次に、アンテナ34を介して反射した電磁信号を受信するために、インパルス発生器36bとインパルス受信器36cとを交互に動作させる、マイクロコントローラー36aおよびレンジゲートコントロール36dを含むことができる。使用できる典型的な信号は、例えば超低帯域領域における、マイクロインパルスレーダー信号などの、マイクロ波、電磁波を含むことができる。
典型的な実施例において、アンテナ32、34のそれぞれは、例えば、ダイヤモンドダイポールアンテナ、シングルエンド形楕円アンテナ(「SEA」)、パッチアンテナなど、ホーン状に突出した物理的プロファイル、ダイポールおよびパッチ、または、コプラナーアンテナなどの、UWBアンテナとすることができる。また、プロセッサー36は、分離したアンテナ32、34の代わりに、送信アンテナおよび受信アンテナ(図示せず)として交互に動作する単一のアンテナを作動させることができる。
例えば、各アンテナ32、34は、Progress in Electromagnetics Research B,Vol.13,59−74(2009)で公開された「超広帯域マイクロ波胸部イメージングのためのTEMホーン形アンテナ」に開示されているような、TEMホーン形アンテナとすることができる。また、各アンテナ32、34は、2008年3月20日に公開された米国特許出願公開第2008/0071169に開示されているような、また、Microwaves,Antennas,& Propagation,IET,Volume 1,Issue 2(2007年4月),pp.277−281で公開された、Nilavalanらによる「胸部がん腫瘍発見のための広帯域マイクロストリップパッチアンテナ設計」に開示されているような、パッチアンテナとすることができる。パッチアンテナは、例えばマイクロインパルスレーダーとの使用を促進するために、誘電体材料で満たされた筐体(図示せず)と結合することができる。
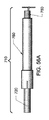
他の別の実施例において、各アンテナは、例えば図10Bに示されるような、導波管ホーンとすることができる。図示のように、アンテナ32’は、第1の端部32Bで閉じて、第2の端部32Cで開放されて、その内部に導波管32Dが搭載された、ケーシング32Aを含む。ケーシング32Aの壁は、Emerson & Cuming Microwave Products N.V.of Westerlo,Belgiumによって販売された、Eccosorb−FGM40のような、広帯域シリコン吸収材料である、吸収材料32Eで裏打ちされている。ケーシング32Aの体積は、例えば約10の比誘電率を有する、誘電体32Fで満たすことができる。典型的な実施例において、アンテナ32’は、例えば、約15×15ミリメートル(15×15mm)の広さを有し、約30ミリメートル(30mm)の第1および第2の端部32B−32C間の長さを有する、約3および10ギガヘルツの間(3−10Ghz)の超広帯域周波数(「UWB」)で動作するよう構成された四角形の導波管ホーンとすることができる。開放端32Bは、例えば、明細書の他の場所にも記載されているように、そこを介してアンテナ32’が信号を送信および/または受信することを意図されている組織に接触または組織と結合するように、内部にアンテナ32’を搭載したプローブから外側に向けることができる。
インパルス受信器36cからの信号は、さらなる処理、ディスプレー、ストレージ、送信などのためのマイクロコントローラー36aと通信する前に、例えばリターン信号ディクラッターおよび整形回路36eによって、フィルターにかけられるか処理されてもよい。回路36eは、必要に応じて例えばリターンエコーノイズやクラッターなどの信号をアンテナ34から受信し、これらの信号をLPFを用いてディクラッターし、および/または、デジタル適合フィルタリングおよび/またはパルス整形を含んでもよい。マイクロコントローラー36aは、さらに以下に記載するように、例えばプローブ30に対するターゲット26や他の構造の距離、角度、方向などの空間的な関係を同定するために、受信した、および/または、処理した信号を読み取る。プローブ30内に含まれるプロセッサーおよび/または他の構成要素の典型的な実施例は、McEwanに対し発行された米国特許第5,573,012号および第5,766,208号に開示されている。
他の実施例において、プローブ30は、McEwanに対し発行された米国特許第6,914,552号に開示されているように、磁気レーダーシステムとして動作するよう構成することができる。例えば、プローブ30は、例えばプローブ30の内部または外部に設けられる、発電機および/または電流コイルドライバー(図示せず)に結合した電磁石(図示せず)などの磁場励起源を含むことができる。例えば、プローブは、距離の測定または位置の調整を行うために、レーダーユニットが同定および/または認識できる特定周波数で極から極への振動を発生する、マーカーまたは他のターゲットに対する磁場を含むことができる。そのようなプローブは、レーダーパルスがターゲットに到達することを弱める、または、反射信号がレーダーアンテナに到達することを弱める、比較的高インピーダンスまたは誘電率を有する、組織、骨、または、体液中に、ターゲットが植え込まれているときに、有益である。
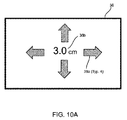
図10に戻ると、プローブのディスプレー38は、例えばアンテナ32、34を介して得た空間的または画像のデータである情報をプローブ30のユーザーに表示するための、マイクロコントローラー36aに結合されることができる。距離、角度、方向、および/または、例えば、さらに以下に記載するように、プローブ30に対するターゲット26の相対的な位置に基づく場合のように所定の基準に基づいたデータを提供するディスプレー38が、簡単に読み取ることができる。図10Aは、矢印のアレイまたは他の表示器38aおよび読み取られた距離38bを含むことができる、提供可能なディスプレー38のための出力の典型的な実施例を示している。例えば、マイクロコントローラー36aは、マーカー(図示せず)が位置するのがプローブ30に対してどの方向かを決定するために受信した信号を解析し、適切な矢印38aを作動させ、マーカーまでの距離(例えば、示された「3cm」)を表示する。そのため、ユーザーは、マーカーがどの方向にどのくらい離れて位置するのかを同定可能となり、それによって、マーカーおよびその内部にマーカーが埋め込まれているターゲットとなる組織領域に対するガイダンスをユーザーに提供することができる。
それに加えてまたはそれに代えて、ディスプレー38は、例えば、そこにプローブ30が方向付けられている、言い換えると、第1の端部30a、プローブ30の操作パラメーターなどを越えたリアルタイムの領域の画像などの他の情報を提供することができる。任意に、プローブ30は、ディスプレー38に加えて、またはその代わりに、1以上の出力デバイスを具えてもよい。例えば、プローブ30は、空間情報、操作パラメーターなどの情報を提供するために、音声出力を提供できる1つ以上のスピーカー(図示せず)、視覚出力を提供できる1つ以上のLEDまたは他の光源などを含むことができる。例えば、スピーカーまたはLEDは、プローブ30が例えば望ましいマージンなどのマーカーからの所定のしきい値距離に到達したとき動作させることができ、または、連続的により近い距離が達成されたとき動作させることもできる。
任意に、プローブ30は、1つ以上のユーザーインターフェース、メモリー、送信器、受信器、コネクター、ケーブル、電源など(図示せず)の、他の特徴または構成要素を含むことができる。例えば、プローブ30は、プローブ30の構成要素を操作するために、1つ以上のバッテリーまたは他の内部電源を含むことができる。また、プローブ30は、プローブ30の構成要素を操作するために、例えば標準的な交流電源などの外部電源に接続されたケーブル(図示せず)を具えてもよい。
図10に戻ると、ユーザーコントロール37は、キーパッド、タッチスクリーン、個別ボタンなど(図示せず)の1つ以上の入力装置を含むことができる。ユーザーコントロール37は、ユーザーが例えばプローブ30のオン、オフやプローブ30のリセットなどの単純な操作を行うことを認め、また、プローブ30のより複雑なコントロールも認めている。例えば、ユーザエーコントロール37は、プローブ30の検出感度や他のパラメーターの調整を可能とし、データのキャプチャー、記憶、遠隔通信などを可能とする。
任意に、プローブ30は、アンテナ32、34を介して得られたデータを記録または記憶可能な内部メモリー36fおよび/またはマイクロコントローラー36aを含むことができる。例えば、マイクロコントローラー36aは、操作中にデータを自動的に記録することができ、または、データを選択的にメモリー36fにセーブするよう指示されることもできる。それに加えてあるいはそれに代えて、マイクロコントローラー36aは、例えばストレージ、ディスプレーなどの1つ以上の外部装置にデータを転送することができる。例えば、プローブ30は、そのようなデータ転送を可能とする1つ以上のケーブル(図示せず)を含むことができ、および/または、プローブ30は、例えばラジオ周波数、赤外線または他の信号を介して、無線でデータを送信しおよび/またはコマンドを受信するための送信機および/または受信機(図示せず)を含むことができる。
図1および10に示されているように、プローブ30のすべての内部構成要素は、プローブ30が内蔵型となるように、筐体またはケーシング39内に設けられることができる。例えば、ケーシング39は、例えばプローブ30の全体がユーザーの手に保持できるように、比較的小さくてポータブルとすることができる。任意に、図1に示すように、ケーシング39の第1の端部30aは、ケーシング39の他の部分と同様または異なる材料から形成される。例えば、第1の端部30aは、送信アンテナ32からおよび/または受信アンテナ34へ、実質的な障害なく、そこを通る電磁信号の通路を簡単に収納する材料から形成されることができる。任意に、その材料は、障害、インピーダンス整合を減少するため、または、プローブ30を介して患者の体の内部へのあるいはそれから外部への信号の送信および受信を促進するため、選択されることができる。それに加えてあるいはそれに代わって、望むならば、プローブ30は、プローブ30の保持あるいは操作を促進するため、ハンドル、フィンガーグリップ、および/または、他の特徴(図示せず)を含むことができる。
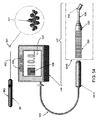
また、図11に示すように、携帯プローブ131から離れたケーシング内に1つ以上の構成要素を含む分離コントローラー139を含むプローブ機器130を設けることができる。例えば、携帯プローブ131は、1つ以上のアンテナ132を有する先端部131bを含む細長い筐体131aを含むことができる。コントローラー139は、前の実施例と同様に、アンテナ132、ディスプレー138などをコントロールするための1つ以上のプロセッサーを含むことができる。携帯プローブ131は、1つ以上のケーブル133によって、コントローラー139内のプロセッサーに連結される。例えば、インパルス発生器、インパルス受信器、および/またはゲートコントロールは、コントローラー139のケーシングの内部、または、望むならば筐体131aの内部に、設けられる。ある実施例において、ケーブル133は、携帯プローブ131のアンテナ132をコントローラー139内の電子機器に電気的に結合するために、コントローラー139のコネクター(図示せず)に着脱自在に接続可能とすることができる。そのため、携帯プローブ131はディスポーサブルで使い捨て可能な装置とすることができ、一方、コントローラー139は、多数の処置の間、新しい携帯プローブ131をコントローラー139に接続することによって使用されることができ、それは手術野から外側に残すことができるが、さらに後述するように、希望するならば、アクセス可能および/または視聴可能に残すこともできる。
図2A−5に戻ると、図1の位置決めシステム10は、例えば病変および/または他のターゲットとなる組織領域41の位置決めを促進するため、および/または、胸部41または他の体の構造から試料の切開および/または除去を促進するため、例えば乳房生検または腫瘍摘出手術の処置などの医学的処置の間、使用されることができる。システム10は胸部病変の位置決めに特に有効であると記載されているが、システム10は、また、例えば明細書のほかの場所に記載のあるように、体の別の領域中の他の対象物の位置決めに使用されることは、理解すべきである。
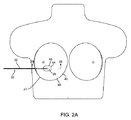
処置の前に、例えば腫瘍や他の病変などのターゲットとなる組織領域は、従来から知られている方法によって特定される。例えば、図2Aに示すように、胸部41内の病変42が、例えばマンモグラフィーおよび/または他のイメージングを使用して特定され、病変42を除去するとの決定がなされる。腫瘍42を囲む点線44は、例えば処置中に除去すべき望ましい組織試料46のサイズおよび形状を示す、「クリア」なマージンを定義する。例えば、マージン44は、試料46を除去した後残された組織が癌性のセルまたは他の望ましくないセルに対し実質的にクリアであることを保証するために、選択される。典型的な実施例において、病変42の外側の境界と組織試料46の外側エッジまたはマージン44との間の距離は、例えば少なくとも約2ミリメートル(2mm)または少なくとも約1センチメートル(1cm)などの、約1および10ミリメートルの間(1−10mm)とすることができる。
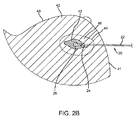
図2Aおよび2Bに戻ると、位置決めワイヤー20は、例えば患者の皮膚48から介在する組織を介してターゲット26が病変42内に位置するまで、組織40を介して経皮的に導入される。典型的な実施例において、位置決めワイヤー20は、明細書の他の箇所で図20−22を参照して記載されたカニューレ340と同様に、注射針および/または拡張器(図示せず)を使用して予め配置された供給シース(図示せず)を介して導入される。例えば、尖った先端部を有するカニューレまたは供給シースは、例えばガイダンスのための超音波またはX線イメージングを用いて、皮膚48および介在する組織40を介して病変42中に侵入し、次に、位置決めワイヤー20は、カニューレを介して前進する。また、尖った先端部を有する注射針は組織を介して前進し、次に、供給シースは、例えば注射針と供給シースとの間の拡張器に沿って、注射針(図示せず)を越えて前進する。一旦、供給シースが、それが皮膚48から病変42まで延びるように位置決めされると、注射針および任意の拡張器は取り除かれる。位置決めワイヤー22の遠位端22bは、次に、ターゲット26が病変42内に位置するまで、供給シースを介して前進し、その後供給シースは除去される。任意に、位置決めワイヤー22は、位置決めワイヤー22のターゲット26および/または遠位端22bのイメージングを促進するために、例えばターゲット26上またはそれに近接する放射線不透過性または音波を発生するマーカーなど、遠位端上に1つ以上のマーカー(図示せず)を含むことができる。外部イメージングは、ターゲット26が病変42内に適切に位置決めされたことを保証するために、位置決めワイヤー20の導入中および/またはその導入後に、使用される。
位置決めワイヤー20が返し24などのアンカーエレメントを含む場合、返し24は、位置決めワイヤー20が供給シースを介して前進するとき、内側に圧縮される。一旦ターゲット26が病変42内に位置決めされると、供給シースは引き出され、その後返し24は近接する組織内で弾性的に外側に広がる。そのため、シャフト22の遠位端22b上の返し24は、例えばターゲット26が病変42内の固定位置に実質的に装着されるように、病変42に対し位置決めワイヤー20をアンカーする。それに加えてまたはそれに代えて、包帯、テープなど(図示せず)が、例えば位置決めワイヤー22の移行を防止するように、患者の皮膚48に位置決めワイヤー22の近位端22aを装着するために、使用される。
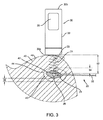
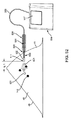
位置決めワイヤー20が正確に位置決めおよび/または装着された後、プローブ30の第1の端部30aは、例えば通常病変42上の患者の皮膚48に近接あるいは接触して配置され、および/または、あるいはターゲット26の方向に向けられ、図3に示すように動作する。プローブ30の送信アンテナ32(図示せず、図10を参照のこと)は、組織40を介して伝わってターゲット26で反射する電磁信号31を放射する。信号33は、プローブ30中で受信アンテナ34(図示せず、図10を参照のこと)に反射して戻る。プローブ30は、次に、例えば信号31が送られた距離や信号31の送信と反射信号33の受信との間の時間の経過などに基づき、例えばターゲット26とプローブ30(およびプローブ30の第1の端部30aが接触している場合は患者の皮膚48)との間の距離52などの、ターゲット26とプローブ30の第1の端部30aとの間の空間的な関係を決定することができる。任意に、プローブ30は、また、例えば切開の正しい方向の決定を促進するために、ターゲット26と第1の端部30aとの間の相対角度を決定することができる。
ある実施例において、プローブ30のマイクロコントローラー36a(図示せず、図10を参照のこと)は、例えばターゲット26のサイズ、形状、および/または、他の側面の認識に基づき、ターゲット26を特定するために、受信信号にフィルターをかけるか、あるいは、受信信号を解析することができる。そのため、マイクロコントローラー36aは、ターゲット26を自動的に特定することができ、それを患者の体内に存在する他の構成物から区別することができる。また、マイクロコントローラー36aは、多分ターゲット26を特定したであろう、プローブ30に信号を戻すよう反射するいかなる対象物を、簡単に特定することができる。例えば、マイクロコントローラー36aは、プローブ30の第1の端部30aから直角に延びる軸に対する距離52および/または角度を形成することができ、この空間的な情報をディスプレー38上に表示することができる。この情報は、例えば病変42を含むターゲットとなる組織領域にアクセスするための切開の方向および深さを提供することによって、病変42に横たわる執刀医の切開する組織に対するガイダンスを提供できる、ターゲット26の位置決め結果として病変42の位置決めを促進することができる。
それに加えてまたはそれに代えて、他の情報が希望に応じてディスプレー38上に表示することができる。例えば、ディスプレー38は、除去すべき組織試料46のターゲットとしたサイズおよび形状の定義を促進することができる、ターゲット26とターゲットとなる組織試料46の外側のマージン44との間の距離54を提供することができる。距離54を決定するために、プローブ30は、例えば、プローブ30のプロセッサー36中にプログラムされたプリセットされたパラメーターに基づき、あるいは、例えばユーザーコントロール37(図示せず、図10を参照)を介して処置の直前にユーザーによってマイクロコントローラー36aに提供された大きさに基づき、望ましいマージン44とターゲット42との間の所定の距離を自動的に減算することができる。
任意に、図3を参照し続けると、プローブ30は、皮膚48に対しまたはその近傍のいくつかの場所(および望むならば得られた空間情報)で、位置決めされる。そのような情報は、例えば病変42までの最も短いパスなどの切開のために最適なアプローチパスを決定する執刀医を補助することができ、あるいは、3次元において病変42に対する執刀医の方向を補助することができる。患者の皮膚48とターゲット26との間の皮膚48上の望ましい位置からの距離52が決定された後、図4に示すように、組織40は、組織試料46の所定の外側エッジ44に達するまで切開される。例えば、プローブ30が配置された場所で切開が患者の皮膚48中で行われ、介在する組織は、マージン44に対応する深さが達成されるまで、従来公知の方法で切断される。任意に、切開中いつでも、プローブ30は露出した組織に対しまたは組織の近傍に配置され、切断のアプローチおよび/または深さを確認するために空間情報を得る。
図4を続けて参照すると、望むならば、一旦執刀医が望ましいマージン44に達したと考えると、ターゲット26までの所定の距離54に到達したことを検証するために、別の距離測定がプローブ30により行われる。例えば、プローブ30が切開した組織領域の底面とターゲット26との間の距離を決定するために、プローブ30の第1の端部30aは切開した組織領域の底面と接触して位置決めすることができ、信号31は送信アンテナ32によって送信することができ、信号33は受信アンテナ34によって受信することができる。組織試料46の望ましいマージン44に到達したことを検証したのち、組織試料46は、除去された資料46内に残るターゲット26とともに、従来の腫瘍摘出手術による処置を使用して、切り取られるかあるいは除去されることができる。望むならば、ターゲット26は、例えばシャフト22とターゲット26との間のコネクター(図示せず)などの接続を外して、シャフト22の近位端22bを切断することによって、試料46の除去を促進するために、シャフト22から分離することができる。
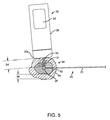
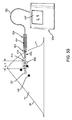
図5に戻り、望むならば、例えば、望ましいマージン44が、ターゲット26の周りで結果的に病変42の周りで、達成されたことを確認するために、プローブ30は切開された組織試料46を解析するために使用される。図示したように、送信信号31はプローブ30によって送信され、信号33はターゲット26で反射され、それにより、プローブ30は、距離54および/または他の空間情報を決定して表示することができる。このようにして、所定の組織マージンが達成されたことを検証することができる。
図6−9に戻ると、プローブ30および複数の植え込み可能なマーカーまたはターゲット120を含む、例えば複数の触診不可能な病変142のような病変または他の組織構造の場所を特定するためのシステム110の他の典型的な実施例が示されている。プローブ30は、明細書のいずれかに記載された実施例と同様に、電磁信号を送信可能であるとともに反射した信号を受信可能である携帯機器とすることができる。
マーカー120は、病変142の周りの領域中に組織を介して導入するための大きさを有する、複数の植え込み可能な要素を含むことができる。例えば、マーカー120は、図1を参照して上述したターゲット26と同様に、および/または、例えば図23A−28C、34A、34B、41Aおよび41Bを参照して明細書の他の場所に記載されたマーカーと同様に、プローブ30によって送信された電磁信号の反射を高めるための特徴を例えば有する、複数のストリップ、シリンダー、らせん、球などとして形成される。
図6に示すように、マーカー120は、約1/2から4ミリメートル(0.5−4.0mm)の間の長さ、約1/2から2ミリメートル(0.5−2.0mm)の間の幅、および、約1/2から3ミリメートル(0.5−3.0mm)の間の厚さを有する、例えば長方形や他の形状のマーカーなどの細長いストリップとすることができる。マーカー120は、例えば所定の誘電率を有する、金属またはプローブ30による検知を高めることができる他の材料によって、形成することができる。それに加えてあるいはそれに代えて、マーカー120は、例えばマーカー120が組織内に植え込まれて、次に、例えば何日、何週間、何月をかけて時間の経過とともに組織によって溶解されあるいは吸収されるような、生体吸収性材料から形成できる。
任意に、マーカー120は、例えば導入中における、あるいは、処置中の配置後における、あるいは、マーカー120が処置後に患者の体内に残った場合はその後における、マーカー120イメージングまたはモニタリングを促進することができる、放射線不透過物質、放射性材料および/または音波を発生する材料から、形成することができる。また、望むならば、各マーカー120は、明細書の他の箇所に記載されているように、1つ以上のマーカーを他のマーカーと区別可能な、表面の、形状の、および/または、付加的な材料の特徴を有することができる。例えば、各マーカー120は、プローブ30からの入力信号を所定の方法で変調すること、および/または、そのマーカー120に特有の特定の電磁信号を吸収または反射することができ、それを一意的に特定するために使用することができる。
また、図6に示すように、システム110は、患者の体内にマーカー120を導入するための1つ以上の供給装置160を含むことができる。例えば、ターゲットとなる組織領域(図示せず)に組織を介して導入するための大きさを有するとともに1つ以上のマーカー120を運ぶことができる、近位端162aおよび遠位端162bを含むシャフト162を含む供給装置160が提供される。供給装置160は、シャフト162の近位端162aおよび遠位端162bと、内腔164から連続するかあるいは独立した、1つ以上のマーカー120を選択的に供給するための、シャフト内をスライド可能なプッシャー部材166と、の間で少なくとも部分的に延びる内腔164を含むことができる。
図示のように、シャフト162の遠位端162bは、シャフト162が組織を介して直接導入可能なように、傾斜させるかおよび/または尖らせることができる。あるいは、供給装置160は、例えば明細書の別の場所に記載されているように、組織を介して事前に配置された、カニューレ、シースまたは他の管状部材(図示せず)を介して導入することができる。任意に、遠位端162bは、例えば蛍光透視、超音波、電磁信号などを使用して、導入中における遠位端162bのモニタリングを促進できる、例えば放射線不透過性または音波を発生する材料から形成された、バンドまたは他の特徴を含むことができる。
図示のように、プッシャー部材166は、マーカー120近傍の内腔164内に配置されたピストンまたは他の要素(図示せず)、および、内腔164からマーカー120を押出すようにピストンを前進させるための、ピストンに結合されたプランジャーまたは他のアクチュエーター168、を含む。図示のように、プランジャー168は、内腔164から連続して1つ以上のマーカー120を供給するために、マニュアルで前進することができる。あるいは、例えば遠位端162bから個々のマーカー120を供給するために、各作動において十分にピストンを前進させることができる、トリガー装置または他の自動化されたアクチュエーター(図示せず)は、シャフト162の近位端162a上に設けることができる。
図6−9に戻ると、胸部41または他の組織構造中の病変または他のターゲットとなる組織領域142の位置を特定するために、マーカー120およびプローブ30を使用するための典型的な方法が示されている。図6および7に示すように、マーカー120は、摘出すべき組織試料146の望ましいマージンまたは体積144の輪郭を描くために、組織40内に植え込まれることができる。例えば、供給装置160のシャフト162は、患者の皮膚48を介しておよび介在する組織40を介して、経皮的に挿入することができ、遠位端162bは、例えば遠位端162bを望ましい位置にガイドするための外部イメージングを使用して、病変142内またはその周囲に位置決めされる。一旦位置決めされると、プランジャー168は、マーカー120を組織中に供給するために、前進することができる(またはシャフト162がプランジャー168に対し取り除かれる)。供給装置160は、他の位置にさらに前進することおよび/または胸部41から完全に取り除かれることができ、例えば1つ以上の付加的なマーカー120を供給するために、皮膚48の他の場所を介してターゲットとなる組織領域に再導入することができる。
あるいは、供給装置160は単一のマーカー120のみを運ぶことができ、複数の供給装置(図示せず)が各マーカー120を供給するために設けられることができる。それに加えてまたはそれに代えて、定位装置(図示せず)は、例えば1つ以上の供給装置を、病変142の場所を特定するため、患者の体内の望ましい3次元アレイまたは他の配列中に導入するために、使用されることができる。さらに他の例において、マーカー120は、ワイヤー10と同様の複数の位置決めワイヤーや、連続してまたは同時に供給される1つ以上のカテーテル(図示せず)などと置き換えることができる。任意に、カテーテル、ワイヤーまたは他の装置は、試料体積または領域の拡張および/または位置決めを促進するために、例えば遠位端(図示せず)において、拡張可能とすることができる。
図6および7に示された典型的な実施例において、マーカー120は、例えば病変142を取り囲む試料体積を取り除くために処置前または処置中に、触診不可能な病変142のグループを取り囲む。組織試料146の外側エッジ144と病変142との間の距離156は、取り除かれた組織の体積が、上述した方法と同様に、クリアなマージンを保証するのに十分であることを保証するために、選択されることができる。
図7に示すように、マーカー120が植え込まれた後、プローブ30は患者の皮膚48に対しまたはその近傍に配置することができ(例えば信号を組織40へおよびそこから送信および受信するために、患者の皮膚48をプローブ30に接触させる必要はない)、プローブ30は、先の実施例と同様に、プローブ30とマーカー120との間の距離152(および/または他の空間的情報)を決定するために、使用することができる。特に、プローブ30によって発せられる信号31は、マーカー120で受信されてプローブ30中の受信器に信号33として反射して戻ることができ、プローブ30は、患者の皮膚48とマーカー120との間の距離152を決定するために、信号を使用することができる。
図8に示すように、病変142を取り囲む組織40は、次に、1つのマーカー120と遭遇するまで、切開することができる。この点で、他の測定が、適切な切開深さを保証するために、プローブ30で行われる。プローブ30は、組織試料146の周辺部144の周りに他のマーカー120を配置するために、図8の幻像に示されたように、再位置決めすることができる。結果としての距離測定が、病変142の周りの切開のための望ましいマージン体積を決定するために使用される。このプロセスは、病変142の周りの組織試料146の切除中、マーカー120までの距離に基づいて望ましいマージンの測定を促進するために、望むだけ繰り返すことができる。組織試料146は、全てのマーカー120が組織試料146とともに取り除かれるように、その中にマーカー120を含むことができる。あるいは、望ましいマージンは、組織試料120が取り除かれた後マーカー120が胸部内に残るように、マーカー120の内部に定義することができる。この選択肢において、マーカー120は、生体吸収性とすることができ、また、患者の胸部41内に不活性で永久に残るようにすることができる。
図11−15に戻ると、胸部41内に1つ以上の病変142の場所を特定するための、および/または、病変142を含む組織試料146(図14A−15Aに示された)を取り除くための、他の典型的なシステムおよび方法が示されている。先の実施例と同様に、システムは、病変142の場所の特定および/または望ましいマージンが胸部41から取り除かれた組織試料146に対し達成されていることの保証を促進できる、1つ以上のマーカー220およびプローブ機器130を含んでいる。プローブ機器130は、上述したように、プローブ131の動作をコントロールするための1つ以上のプロセッサーを含むプロセッサー139に結合された携帯プローブ131を含んでいる。また上述したように、携帯プローブ131は、皮膚48または他の組織に対して配置可能な、および/または、マーカー220および/または病変142に向けて方向付けが可能な、プローブ131の一端上の先端131b上またはその内部に1つ以上のアンテナ132を含む、細長い筐体131aを含んでいる。
プロセッサー139は、先の実施例と同様に、アンテナ132、ディスプレー138などをコントロールするための1つ以上のプロセッサーを含むことができる。携帯プローブ131は1つ以上のケーブル133によってプロセッサー139と結合することができる。例えば、インパルス発生器、インパルス受信器、および/または、ゲートコントロールは、アンテナ132を介して信号を送信および受信するようコントロールされるプロセッサー139内に、設けることができる。
任意に、図14および14Aに示すように、携帯プローブ131は、例えば筐体131aの先端131bから延びる、切断機能133を含むことができる。ある実施例において、切断機能133は、例えば約10から50ミリメートル(10−50mm)の長さおよび/または約1から10ミリメートル(1−10mm)の幅を有する、プローブ131の先端131bに固定された比較的平らな鈍的切開器とすることができる。あるいは、切断ン機能133は、例えば切断機能133が、最初は筐体131a内に折り畳まれており、マーカー220の近傍の組織にアクセスするために組織層の切断を希望するときは選択的に展開するように、折り畳み可能とすることができる。さらに他の例において、切断機能133は、患者の皮膚48および/または組織40の下位層を介しての切断を促進できる、尖ったブレードまたはエッジを含むことができる。
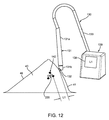
最初に、図11に示すように、使用中、1つ以上のマーカー220は、例えば明細書の他の箇所に記載されたマーカーおよび/または方法を使用して、ターゲットとなる組織領域内に植え込むことができる。プローブ131は、例えばケーブル133でプロセッサー139に接続され、その先端131bが皮膚48に配置される。プローブ131は、例えばアンテナ132を使用してプローブ131の先端131bからマーカー220までの初期の距離測定を得て、それにより病変142へのおおよその距離を提供するよう、動作することができる。距離測定は、例えば図12に示されるように、プロセッサー139のディスプレー138上に表示することができ、および/または、他の方法でユーザーに提供することができる。それに加えてまたはそれに代えて、上述したように、スピーカーは、距離を特定するために、例えば合成音声、対応する距離を特定するための1つ以上のトーンなどを使用して、距離測定を提供することができる。例えば、プロセッサー139は、プローブ131の先端131bからマーカー220までの実際の距離を決定するために、受信した信号を解析することができ、スピーカーを介して実際の測定結果を提供することができる。あるいは、スピーカーは、例えば第1のしきい値距離を第1のトーン、第2のしきい値距離を第2のトーン、それよりも近いしきい値距離を複数トーンとすることで、それらがマーカー220により近くなっていることをユーザーに示すように、所定のしきい値に対応するトーンを提供することができる。
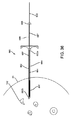
図11に示すように、胸部41の第1の側面上のプローブ131により、大きさL1を得て、胸部41の第2の反対の側面上に位置するプローブ131’により、L1より大きい大きさL2を得ている。この情報により、医師は、図12に示すように、それが第2の側面で行うパスよりもより少ない組織切開を要求するより短いパスを提供するため、第1の側面上で切開を行うことを決断することができる。
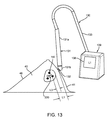
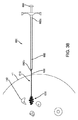
図13に戻ると、プローブ131は、マーカー220の周り結果として病変142の周りの望ましいマージンL3を特定するために使用することができる。例えば、1センチメートル(1cm)の望ましいマージンL3を希望する場合、プローブ131は、ディスプレー138上に示されたように、プローブ131からマーカーまでの実際の距離L1を表示または提供することができ、それによりプローブ131がマージンL3の外側に残っていることを示すことができる。あるいは、プロセッサー139が望ましいマージンL3を知っている場合、ディスプレー138は、実際の距離L1と望ましいマージンL3との間の相違(すなわちL1−L3)を提供することができ、それにより望ましいマージンを達成するために必要な切開深さを医師に伝えることができる。
任意に、図14および14Aに示すように、プローブ131が鈍的切開器144を含む場合、例えば望ましいマージンL3が達成するまで、鈍的切開器144は、プローブ131の先端131bから展開することができ(永久に展開しないにせよ)、組織40を介してマーカー220の方向に前進することができる。プローブ131は、次に、鈍的切開器144を使用して、および/または、1つ以上の付加的な切開器、外科用メス、または他のツール(図示せず)を使用して、マーカー220の周りの組織を切開するよう操作することができる。
図15および15Aに示すように、その内部にマーカー220および病変142を含む組織試料146が胸部41から取り除かれる。任意に、プローブ131は、次に、望ましいマージンL3がマーカー220の周りに達成されたことを確認するために使用することができ、それにより、先の実施例と同様に、十分な組織が胸部41から取り除かれたことの確認を提供することができる。
図16Aおよび16Bに戻ると、1つ以上のマーカー220、1つ以上のアンテナ232を運ぶ指サック231aを含むプローブ231、および、例えばケーブル233によってアンテナ232に結合されたプロセッサー239を含むシステムの更に他の実施例が示されている。指サック231aは、例えば、そこに指90が挿入される開放端231bと閉鎖端231cを含み、指90を安全に受けるために十分な長さを有する、可とう性スリーブとすることができる。例えば、指90を受けて収容できるよう広がる一方使用中指サック231aが指90から滑り落ちないよう内側に圧縮される十分な柔軟性を有する、例えば手術または検査用グローブと同様に、ラテックス、天然または合成ゴムなどの相対的に薄い層のような、弾性材料から構成することができる。
図示のように、アンテナ232は閉鎖端231cの近傍に設けることができる。例えば、アンテナ232は、先の実施例と同様に、筐体内に設けられた送信アンテナおよび受信アンテナ(図示せず)を含むことができる。筐体は、例えば接着剤、融解、1つ以上の付加バンド(図示せず)などによる接合によって、閉鎖端231cの近傍で、指サック231aに装着することができる。
プロセッサー239は、先の実施例と同様に、例えばケーブル233によってアンテナ232に結合されるとともにディスプレー238を含む、アンテナ232動作させるためおよび/またはアンテナ232から受信された信号を処理するための、1つ以上の構成要素を含むことができる。図示した実施例において、プロセッサー239は、プロセッサー239が、指が指サック231a中に挿入されたユーザーの腕に着脱自在に装着できるような、1つ以上のクリップ239a、ストラップ、ベルト、クランプ、または他の器具(図示せず)を含む。例えば、クリップ239aは、ユーザーの前腕の周りに部分的に広がるようカーブさせることができ、クリップ239aは、その中に腕を受けるためにそれを広げることができ、次に、腕の周りに少なくとも部分的に係合するために弾性的に閉じることができるのに十分な可とう性とすることができる。あるいは、プロセッサー239は、例えば上述したプロセッサー139と同様に、患者および/またはユーザーから離れた位置に置くことができる筐体(図示せず)中に設けることができる。
図17および18を付加的に参照すると、使用中、例えば人差し指または親指などの指90の一部を指サック231a内に挿入することができ、先の実施例と同様に、プロセッサー239は、アンテナ232を介して信号を送信および受信するよう動作させることができる。
図17に示すように、指サック231aに挿入された指90は、患者の皮膚48に対し配置することができ、マーカー220までの距離を特定するために距離測定が行われる。マーカー220を覆う組織が切開されるため、図18に示すように、ユーザーは生成されたパス内に指90を挿入することができ、それによって、ユーザーに、指90に関連してマーカー220の位置すなわち病変142の位置の直接フィードバックを提供することができる。そのため、プローブ231のこの実施例は、距離測定と同様に、内部にマーカー220および病変142を含む組織試料146の切開および/または除去を促進することができる、触覚フィードバックを提供することができる。例えば、図17に示すように、ユーザーに必要な切開深さの情報を与える、初期の距離測定L1を得ることができ、一方、図18に示すように、距離測定L2を得ることができ(望ましいマージンに対応)、それによって、先の実施例と同様に、ユーザーに、十分な切開が達成されたことおよび組織試料146が分離されて取り除かれたことを知らせることができる。
図19−22に戻ると、例えば1つ以上の病変142を含むターゲットとなる組織領域の場所を特定するためおよび/またはそれを切開するための、更に他のシステムが示されている。一般的に、システムは、先の実施例と同様に、プロセッサー339に結合した携帯プローブ331を含むプローブ機器330を含んでいる。例えば、プローブ331は1つ以上のアンテナ332を含み、プロセッサー238はディスプレー338を含んでいる。
また、システムは、近位端342、遠位端344およびそれらの間の内腔346を含む、カニューレまたは他の管状部材340を含んでいる。カニューレ340は、図19に示すように、プローブ331が内腔346内に受けることができるサイズを有する実質的に硬い管状ボディーとすることができる。図示したように、遠位端344は、傾斜させるか、尖らせるか、および/または、直接的な組織を介しての前進を促進するよう形成することができる。あるいは、遠位端344は、先の実施例と同様に、例えばカニューレ340が、注射針が組織40内に導入される前または後のいずれかに、注射針(図示せず)を越えて前進することができるように、テーパーを付けるかおよび/または丸める(図示せず)ことができる。
図19を参照すると、使用前に、プローブ330は、例えばアンテナ332がカニューレ340の遠位端344の直近に配置されるように、カニューレ340の内腔346内に挿入することができる。任意に、カニューレ340および/またはプローブ331は、例えばアンテナ332を遠位端344の近傍に維持するように、カニューレ340に対しプローブ331を解放可能に固定し、一方プローブ331が望んだときに取り外されることを可能とするため、1つ以上のコネクター(図示せず)を含むことができる。それに加えてあるいはそれに代えて、カニューレ340は、プローブ331が内腔346内に配置されたときおよび/またはプローブ331が取り除かれたとき、実質的に流体密封のシールを提供するために、例えば近位端342および/または遠位端344内に、1つ以上のシール(図示せず)を含むことができる。例えば、内腔346を介しての流体の流れを阻止し、その一方で、プローブ331または他の機器(図示せず)を、そこを通して受け取り収容するシールを提供できる、止血シール(図示せず)を近位端342に設けることができる。
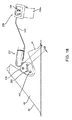
図20に戻ると、使用中、カニューレ340内でプローブ331が動作すると、カニューレ340の遠位端344は、患者の皮膚48および組織40を介してマーカー220に向かって挿入することができる。図示のように、プローブ331は、振動31を送信することができ、プロセッサー339のディスプレー338は、アンテナ332で受信した反射信号に基づき、アンテナ332に対するひいてはカニューレ340の遠位端344に対するマーカー220の相対的な位置の距離測定L1または他の表示を提供することができる。そのため、カニューレ340の侵入の深さおよび/またはその前身の方向は、プローブ331およびプロセッサー339によって提供された情報に基づき調整することができる。例えば、図21に示すように、カニューレ340は、望ましい距離L2が達成されるまで前進することができ、それによって、遠位端344を、例えば病変142近傍のターゲットとなる組織領域内の、マーカー220から望ましい距離だけ離れた位置に配置することができる。
図22に戻ると、病変142に対し望ましい位置に配置されたカニューレ340の遠位端344により、プローブ331は、図示のように、カニューレ340を所定の位置に残した状態で、取り除くことができる。カニューレ340は、それにより、例えば1つ以上の診断および/または治療処置を行うために、ターゲットとなる組織領域を切開するための通路を提供することができる。例えば、注射針や他のツール(図示せず)は、生検を行うためにおよび/または流体または他の診断または理療処置用の材料をターゲットとなる組織領域に供給するために、カニューレの内腔346を介して前進することができる。それに加えてまたはそれに代えて、1つ以上の機器(図示せず)は、放射線治療および/または他の処置を供給するため、例えば病変142を含む組織試料を取り除くために、カニューレ340を介して導入することができる。アクセスがそれ以上必要なくなると、カニューレ340は単に取り除くことができる。あるいは、処置の途中でカニューレ340を移動させることを望む場合は、プローブ331は体腔346内に再び導入され、プローブ331とともに組織内に移動したカニューレ340は付加的なガイダンスを提供することができる。
図11−22において、上述したものと同様の方法を使用して、例えば病変142内またはその近傍の、組織40内に植え込まれるか配置されることができる、マーカー220が示されている。図示のように、マーカー220は、一般的に、球形の端部の間に相対的に狭い中間ステム部を含む細長いボディーである。マーカー220は、望ましい材料から形成することができ、および/または、マーカー220の位置決めおよび/またはマーカーの他のものとの区別を促進することができる、ここに記載された他のマーカーと同様の表面上の特徴を含むことができる。
図23A−28Cに戻ると、明細書に記載されたいかなるシステムおよび方法においても使用することができる、マーカーの付加的な実施例が示されている。例えば、図23A−23Cに戻ると、複数のビードまたはセグメント324を運ぶコアワイヤー322を含む第1の典型的なマーカー320が示されている。コアワイヤー322は、約1/2と2ミリメートル(0.5−2mm)との間の直径または他の最大断面、および、約1と10ミリメートル(1.0−10mm)との間の長さを有する固体または中空構造である、細長い部材とすることができる。コアワイヤー322は、さらに以下に説明するように、コアワイヤー322が組織中で展開すると所定の形状に偏向するように、例えばステンレススチール、ニチノールなどの、弾性または超弾性材料からおよび/または形状記憶材料から形成されることができる。あるいは、コアワイヤー322は、さらに以下に説明するように、マーカー320が例えば直線状または曲線状などの固定形状で残るように、実質的に硬くすることができる。
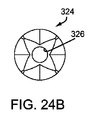
図24A−24Cにおいて最もよくわかるように、ビード324は、例えば各々が一般的に円筒形または球形の形状の部分を定義するように、複数の単独の輪状体を含むことができる。ビード324は、例えば、ステンレススチール、ニチノール、チタン等の金属、プラスチック材料などの、先の実施例と同様な望ましい材料から形成することができる。ビード324は、ベースメタルの射出成形、機械加工、切断、研削などによって形成することができる。また、望ましい仕上げ加工は、例えばサンドブラスト、エッチング、蒸着などにより、モールディングまたはキャスティング処理中に、ビード324に対し適用することができる。
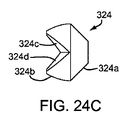
図24Bにおいて最もよくわかるように、各ビード324は、そこを通ってコアワイヤー322を受けるための(図示せず、例えば図23A−23Cを参照)、そこを通る通路326を含むことができる。ビード324は、コアワイヤー322上に装着されるとビード324が少なくとも部分的に近傍の他のものと入れ子になることを可能とし、一方、例えばコアワイヤー322が形状を変化させると、マーカー320が形状を変えることを可能とする、形状および/または表面特徴を含むことができる。また、ビード324は、例えば、約45と135度との間(45−135°)または約90度(90°)の、急峻な角度を定義する近傍表面を有する複数の表面を含む、ビードの周辺に1つ以上の溝を含む、例えばレーダーなどの電磁波の反射を高めるような表面形状を含む。例えば、図24Cにおいて最もよくわかるように、各ビード324は、第1の凸部または球状の端部324aおよび平面324dを含む第2の凹端部324bを含むことができる。図25Bに示すように、近傍のビード324’は、第1のビード324の凹端部324b’上の第1の表面324d’および近接するビード324’の球状の端部324a’上の表面324e’の間の水324c’を定義することができる。表面324d’および324e’は、例えば約90度(90°)の角度の定義のように、レーダーを使用した検知を高めることができる、それらの間の急峻なコーナーを定義することができる。
任意に、図25Aおよび25Bに示すように、ビード324’は、電磁信号がビード324’の表面に衝突するとき発生する反射信号をカスタマイズすることを意図した、望ましい表面仕上げ324fを含むことができる。例えば、表面仕上げ324fはビード324’中に形成されて望ましい直径および/または深さを有する複数の孔またはディンプルを含むことができる。上で説明したように、明細書のほかの場所に記載されたプローブおよびプロセッサーは、例えば複数のマーカーが患者の体内に植え込まれるか配置されたとき、特定のマーカーを個別に同定するような反射信号を解析することができる。
図23A−23Cに戻ると、アセンブリー中、複数のビード324は、完成マーカー320を提供するために、コアワイヤー322を超えて配置できるとともにそれに対し装着することができる。例えば、コアワイヤー322は、ビード324がコアワイヤー322の端部の間で実質的に広がるまで、ビード324中の通路326を介して連続して挿入される。ビード324は、例えば、個々のビード324をコアワイヤー322上に圧着する、十分なビード324上を滑らせた後コアワイヤー322の端部を圧着するか拡張する、接着剤で接合する、溶融するなどによって、コアワイヤー322に装着することができる。そのため、ビード324は、例えばコアワイヤー322ひいてはマーカー320の曲げ加工または形状形成を促進でき、ビード324が動かずまたビード324がコアワイヤー322上で自由に動くように、コアワイヤー322に実質的かつ永久に装着することができる。
あるいは、マーカー320は、例えば図23Aに示されたビード324によって定義される形状および表面は、ワーク中で形成することができる。この代替例において、コアワイヤー322は除去することができ、また、通路は、コアワイヤー322を受けるためにワークを介して形成することができる。
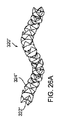
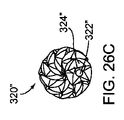
ある実施例において、マーカー320は、例えば、図23Aおよび23Bに示すような直線形状または図23Dおよび26A−26Cに示すような曲線形状の、実質的に固定された形状を定義することができる。例えば、マーカー320のコアワイヤー322は、例えば、マーカー320は、供給装置中へのマーカー320のロードおよび/またはマーカー320の供給を促進するために、直線状になることができ、一方マーカー320は曲線状または他の非直線形状に偏移できるように、十分にフレキシブルとすることができる。
図23Dに示すように、マーカー320は、例えば平面内に横たわる曲がりくねった形状または他の曲線状の形状の、ウェーブ構成を仮想するよう偏移することができる。例えば、コアワイヤー322が、ウェーブ構成に対しては偏移し、一方、リニア構成に対しては弾性的に直線状となるようにセットされた形状であるコアワイヤー322は、弾性材料または超弾性材料から形成することができる。ビード324は、例えば供給装置中へのマーカー320のロードおよび/またはマーカー320の体内への導入を促進するために、ビード324がリニア構成およびウェーブ構成との間でコアワイヤー322の変化の実質的に邪魔にならないように、空間を開けることができ、あるいは、入れ子にすることができる。
あるいは、図34Aおよび34Bに示すように、例えばテーパー状の端部領域320b’’’の間の相対的に広い中間領域320a’’’を含む、テーパー状のらせん形状を仮想するよう偏移したマーカー320’’’が提供されている。実質的に均一ならせん形状を仮想するよう偏移したマーカー320’’’’の他の別の実施例は、図41Aおよび41Bに示されている。マーカー320’’’および320’’’’の効果の1つは、それらが、プローブ(図示せず)のアンテナに対するマーカー320’’’および320’’’’の反射角および/または位置に関係なく、相対的に一定および/または一貫したレーダークロスセクション(RCS)を提供できる点にある。例えば、図34Bおよび41Bに示されたように、マーカー320’’’および320’’’’をらせん軸に沿って見た場合であっても、例えば図34Aおよび41Aに示すように、マーカー320’’’および320’’’’は、らせん軸に対し横方向に見たときと実質的に同等のRCSを提供することができる。
任意に、ここに記載されたマーカーのいずれもが、受動マーカー、能動マーカー、能動反射器または能動トランスポンダーとして提供することができる。例えば、図23A−23Dを参照すると、マーカー320は単に「受動反射器」とすることができ、すなわち、マーカー320は単にマーカー320と衝突する入射波または信号を反射することができる。入射信号は、マーカー320の種々の表面および/またはエッジで反射され、明細書の他の箇所にさらに記載されているように、例えばそれによってプローブによって検知される反射した波または信号を提供することができる。受動マーカーの効果の1つは、レーダークロスセクション(RCS)が、プローブのアンテナのアスペクト角、および、マーカー320から反射した戻り信号の強度の変化を起こすことができるマーカー320に基づき、変化可能である点である。
あるいは、マーカー320は、「能動反射器」、すなわち、反射した信号に対し外部エネルギーまたはパワーを加えることなく、所定の方法でマーカー320に衝突した信号を変調する1つ以上の電気回路を含むマーカー320、を提供するための1つ以上の特徴を含むことができる。そのようなマーカーは、例えば1つ以上の極小パワーのダイオードおよび/または極小電流で動作するFETトランジスターを含み、変調ダイポールまたは他のタイプの能動反射アンテナを含む、能動反射電波素子を含むことができる。能動反射器は、プローブによって検出して同定することができる、埋め込まれた組織環境中において実質的に単一のレーダー信号の痕跡を提供する。また、能動反射器は、プローブに戻る比較的大きい信号を提供でき、例えばそれによって、アンテナの性状を問わずターゲットとなるRCSを維持する。
例えば、マーカー320は、プローブからの入射波または入射信号を変調できる、マーカー320に結合されるかその中に埋め込まれた、1つ以上の回路または他の素子(図示せず)を含むことができる。典型的な実施例において、それ自身のエネルギー源を含まず、そのため、信号が受信されマーカー320で反射されたときに単に信号を処理して変調する、ナノスケール半導体チップは、マーカー320によって運ばれる。マーカ上に設けることができ能動反射器の典型的な実施例は、米国特許第6,492,933号において開示されている。
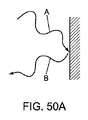
図50Aおよび50Bは、能動反射器を使用して達成できる、入射信号Aに対する反射信号Bの変調の例を示す。入射信号Aは、明細書の他の個所に記載されているように、プローブ(図示せず)によって伝達された波または信号を表すことができる。図50Aに示すように、入射信号Aは、例えばここに記載されたいずれのマーカーの表面に衝突して反射されることができ、その結果反射信号Bとなる。受動反射器で、マーカーの表面は単に入射信号Aを反射することができ、そのため、反射信号Bは、例えば、帯域幅、相などにおいて、入射信号Aと近似した性質を持つことができる。
その一方、能動反射器で、マーカーは、例えば反射信号Bの周波数および/または相を変えるなど、所定の方法で入射信号Aを変調することができる。例えば、図50Bに示すように、マーカー上の回路は、超広帯域のレーダー入射信号Aを、例えば、所定の相シフトを含む約1および10ギガヘルツの間(1−10GHz)の、比較的狭帯域の反射信号Bに変更することができる。比較的狭帯域の信号Bは、マーカーのRCSを高めることができ、それによりプローブによる検出を高めることができる。
また、図50Bに示すように、反射信号Bの相は、入射信号Aに対し90度(90°)だけ変調することができる。マーカーがこの相シフトに特有であれば、相シフトは、他の構造から、例えば異なる相シフト、組織構造などを有する他のマーカーから、プローブがマーカーを同定して区別する助けとなる。例えば、複数のマーカーが患者の体内に植え込まれている場合、各マーカーの回路は、反射信号中における、異なる相シフト(例えば、+90°、+180°、−90°など)および/または帯域幅を重畳するよう構成することができる。そのため、プローブは、患者の体内において、他のマーカーからおよび/または他の構造物から、マーカーを容易に同定して区別することができる。
能動反射器の1つの効果は、回路がそれ自身の電源を必要としない点にある。そのため、回路のサイズは実質的に小さくすることができ、望むならば、マーカーは、延長されたまたは不定期の期間、患者の体内に植え込むことができ、あるいは、マーカーは、マーカーの位置の特定および/または同定を促進するために、プローブからの信号に応答することができる。
さらに他の例において、参照エネルギーの励起に応じて検出可能なエネルギーを発生する1つ以上の特徴を含む「能動マーカー」が提供される。そのような能動マーカーの例は、米国特許第6,363,940号に開示されている。
さらに他の例において、例えば、埋め込まれた組織環境において、レーダー信号の痕跡に特異性を提供するMIRプローブのエネルギーを再送信または「中継」する能動トランスポンダーが提供される。能動トランスポンダーは、マーカー内に埋め込まれるかそれによって運ばれる、例えば1つ以上のバッテリー、キャパシターなどの内部エネルギー源を含む1つ以上の電気回路を含むことができる。典型的な実施例において、能動トランスポンダーは、マイクロ波受信器および/または送信器、データ処理および記憶素子、および、戻り信号のための変調システムを含むことができる。能動トランスポンダーは、例えば受動マーカーのみで可能な信号よりもより大きい信号をプローブに戻すため、プローブによって出射された励起マイクロ波エネルギーに応じてマイクロ波エネルギーを発生することができる。例えば、マーカーは、プローブからの特異なレーダー痕跡および/または周波数に応じて、フォーマットされたデータを含むRFエネルギーを発生することができる。典型的な実施例において、能動トランスポンダーは、MIRレーダーのアッパーサイドバンド(「USB」)またはローワーサイドバンド(「LSB」)のいずれかの形でシングルサイドバンド(「SSB」)信号を出射するよう方形に変調される。そのようなトランスポンダーは、RFスペクトラムを横断したマルチチャンネル操作の可能性を提供することができる。
図29Aおよび29Bに戻ると、組織を介して例えば胸部41内などのターゲットとなる組織領域に導入するための大きさとした、近位端262aおよび遠位端262bを含むとともにマーカー320(または任意に複数のマーカー、図示せず)を運ぶ、シャフト262を含む供給装置260が提供される。供給装置260は、シャフト262の近位端262aおよび遠位端262bの間に延びる内腔264、および、内腔264から図23A−23Dのマーカー320を供給するためのシャフト262内をスライド可能なプッシャー部材266、を含むことができる。図示のように、シャフト262の遠位端262bは、シャフト262が直接組織を介して導入されるように、傾斜する形状および/または尖った形状とすることができる。あるいは、供給装置260は、例えば明細書他の箇所に記載されているように、組織を介して配置されたカニューレ、シースまたは他の管状部材(図示せず)を介して導入することができる。任意に、遠位端262bは、明細書の他の箇所に記載されているように、導入中の遠位端262bのモニタリングを促進できるように、例えば放射性不透過材料、音波発生材料、または他の材料で形成された、バンドまたは他の特徴を含むことができる。
図29Aに示すように、プッシャー部材266は、マーカー320近傍の内腔264内に配置された遠位端267および内腔264からマーカー320を押すために遠位端267を前進させるためのプランジャーまたは他のアクチュエーター268を含む。図29Bに示すように、一旦供給装置260の遠位端264が組織40内の望ましい位置まで前進すると、シャフト262は、内腔264から連続してマーカー320を押出すために、プランジャー268に対し引っ込めることができる。あるいは、トリガー装置または他の自動アクチュエーター(図示せず)は、遠位端262bからマーカー320を供給するために、シャフト262の近位端262b上に提供することができる。
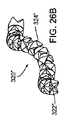
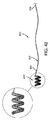
図26A−26Cに戻ると、例えば複数のビード324’’を運ぶコアワイヤー322’’を含む、図23A−23Dに示されたマーカー320と一般的に近似したマーカー320’’の他の実施例が示されている。しかしながら、マーカー320とは異なり、コアワイヤー322’’は、マーカー320’’が図示したようならせん構造に偏向するように、らせん形状に偏向される。そのため、マーカー320’’は、図29Aおよび29Bに示された供給装置260のように、例えば供給装置中へのローディングを促進するために、直線形状とすることができ、一方、弾性的にらせん構造に戻すよう変更させることもできる。
他の実施例において、マーカー320、320’または320’’のいずれも、例えばマーカーがターゲットとする温度まで加熱されたとき所定の構造となるよう偏向できるように、少なくとも部分的に形状記憶材料から形成することができる。例えば、図24のマーカー320を参照すると、コアワイヤー322は、コアワイヤー322が、例えば摂氏20度(20℃)またはそれ未満の大気温度またはそれ以下でマルテンサイト状態となり、摂氏37度(37℃)またはそれ以上の体温またはそれ以上でオーステナイト状態となる、例えばニチノールなどの、形状記憶材料から形成することができる。マルテンサイト状態において、コアワイヤー322は、例えばマーカー320が直線形状で図29Aおよび29Bの供給装置260中にロードできるように、比較的柔らかくて可鍛性を有することができる。コアワイヤー322の形状記憶は、コアワイヤー322がターゲットとなる温度まで加熱されると、コアワイヤー322が波状、らせん状、または他の非直線状の形状に偏向できるように、材料中で温度設定またはプログラムすることができる。そのため、たとえマーカー320がマルテンサイト状態においてその望ましい展開構造から変形した曲がった形状または直線形状であったとしても、マーカー320は、一旦ターゲットとする温度まで加熱した患者の体または他の部分に導入されると、展開構造となるよう自動的に偏向することができる。
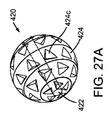
図27A−27Cに戻ると、マーカー420の他の典型的な実施例が示されている。マーカー320と同様に、マーカー420は複数のビードまたはセグメント424を運ぶコアワイヤー422を含む。ビード424のそれぞれは、明細書の他の箇所に記載されているように、例えばプローブ(図示せず)からの信号の反射を高めるために、複数の溝424cを含む。コアワイヤー422およびビード424は、例えばビード424が、コアワイヤー422上で自由に回転するように、あるいは、コアワイヤー422に固定されるように、先の実施例と同様に、製造および組み立てをすることができる。溝424cは、先の実施例と同様に、各ビード424で完全に形成することができ、あるいは、近接するビード(図示せず)の表面を協働させることによって定義することもできる。溝424は、レーダー検出を高めることができるコーナーを定義する急峻なエッジと整合する平面または曲面を実質的に定義することができる。
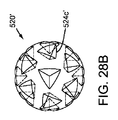
任意に、図28A−28Cに示すように、異なる形状および/または構造を有する溝524c、524c’、524c’’を含む球状のマーカー520、520’、520’’の他の実施例が示されている。溝524c、524c’、524c’’は、例えば以下に示すように、プローブのプロセッサーが異なる反射信号に基づき異なるマーカーを区別できるように、実質的に互いに異なる反射信号を発生することができる。
図28A−28Cに示す実施例において、マーカー520、520’、520’’は、材料の単一の部分品から形成されており、コアワイヤーおよび複数のビードを含んでいない。コアワイヤーおよび複数のビードが、望むならば、マーカー520、520’、520’’に対し提供できること、および/または、図27A−27Cのマーカー420が、望むならば、材料の単一の部分品から形成されること、は理解される。
図30A−31Bに戻ると、明細書の他の箇所に記載されたいずれのマーカーとすることもできる、図23A−23Dに示されたマーカー320のように、マーカー320を供給するために使用することができる供給装置360の他の実施例が示されている。一般的に、供給装置360は、例えば胸部41内のターゲットとなる組織領域に組織を介して導入するための大きさとした、近位端362aおよび遠位端362bを含む、注射針または他の管状シャフト362、および、近位端362aと遠位端382bとの間に延びる内腔364、を含む。供給装置360は、また、内腔364からマーカー320を供給するため、シャフト362内をスライド可能なプッシャー部材366を含む。図示のように、シャフト362の遠位端362bは、シャフト362が直接組織を介して導入されるように、傾斜する形状および/または尖った形状とすることができる。あるいは、供給装置360は、例えば明細書他の箇所に記載されているように、組織を介して配置されたカニューレ、シースまたは他の管状部材(図示せず)を介して導入することができる。任意に、遠位端362bは、明細書の他の箇所に記載されているように、例えばX線または超音波イメージングなどを使用した、導入中の遠位端362bのモニタリングを促進できるように、例えば放射性不透過材料、音波発生材料、または他の材料で形成された、バンドまたは他の特徴を含むことができる。
図30Bおよび31Bに戻ると、プッシャー部材366は、例えば図30Bに示すように初期にマーカー320の近傍の内腔364内に設けられた遠位端367を含む。プッシャー部材は366は、供給装置360のハンドル370に対し実質的に固定され、一方、以下にさらに記載するように、例えばマーカー320を露出するため、シャフト362は引き込み可能とすることができる。例えば、図30Bに示すように、プッシャー部材366の近位端366aは、ハンドル370内に搭載されたプッシャー部材372に固定することができる。
シャフト362は、ハンドル370内でスライド可能なシャフトホルダー374に結合することができる。例えば、シャフトホルダー374は、図30Bに示された第1または遠位位置から図31Bに示された第2または近位位置まで、軸方向にスライド可能とすることができる。そのため、第1位置のシャフトホルダー374により、プッシャー部材366の遠位端367はシャフト362の遠位端362bの近くにオフセットされ、それにより、図30Bに示されるように、マーカー320を受けるためのシャフト内腔364内に十分なスペースを提供する。シャフトホルダー374が第2位置に導かれると、シャフト362は、例えば図31Bに示されるように、シャフト362の遠位端362bがプッシャー部材366の遠位端367近傍に配置されるまで、引き込まれる。プッシャー部材366の遠位端367は、マーカー320がシャフト362の引き込み動作の間において近くへ移動することを防止し、その結果、マーカー320は、図33および33Aに示されているように、シャフト362の内腔364から結局展開される。
シャフトホルダー372およびシャフト362は、第2位置に偏向させることができるが、例えば供給装置360を使用してマーカー320がその内部にロードされることおよび供給されることを可能とするため、選択的に第1位置に保持されることもできる。例えば、図30Bおよび31Bに示すように、ハンドル370は、筐体の溝378で受け取られ、シャフトホルダー374に隣接する、スプリングまたは他のメカニズムを含む。第1位置において、図30Bに示すように、スプリング376は圧縮され、一方、第2位置において、図31Bに示すように、スプリング376は解放される低潜在エネルギー状態となる。
ハンドル370は、また、第1位置でシャフトホルダー374およびシャフト362を選択的に保持および解放するためのアクチュエーターを含む。例えば、図30Bに示すように、第1位置のシャフトホルダー374により、シャフトホルダー374は、シャフトホルダー374の近位端374aがプッシャーホルダー372の遠位端372aに近接または係合するまで、ハンドル370内で回転することができる。あるいは、ハンドル370は、第1位置のシャフトホルダー374を選択的に係合できる、1つ以上の他の特徴(図示せず)を含むことができる。図31Bに示すように、シャフトホルダー374が、プッシャーホルダー372の遠位端372aの近位端374aに対する係合を解くために、ハンドル370内で回転する場合、近位端372aは、ハンドル370内を近接して自由に移動することができる。そのため、一旦シャフトホルダー374が回転すると、スプリング376が自動的にシャフトホルダー374を近くに導くことができ、それによってマーカー320を展開する。例えば解放できるデントやロックなどの他のアクチュエーターが、前進した位置でシャフト362を解放可能に装着して、アクチュエーターが動作するときシャフト362が自動的に待避することを可能とするよう相互作用できる、ハンドル370および/またはシャフトホルダー374上に設けられることは理解できるであろう。
図32および33に戻ると、供給装置360は、先の実施例と同様に、例えば1つ以上の内腔142を含む、ターゲットとなる組織領域内の胸部40または他の組織構造中にマーカー320を供給するために使用される。一旦マーカー320が供給されると、マーカー320は、例えば明細書の他の箇所に記載されたシステムおよび方法のいずれかを使用して、ターゲットとなる組織領域の場所を見つけ出すために使用される。
図35に戻ると、テザーまたは他の細長い要素630と結合したマーカー620を含むマーカー装置610のさらに他の実施例が示されている。テザー630は、マーカーがターゲットとなる組織領域中に導入されたとき、患者の体から延びる十分な長さを有する、例えば生体吸収性または非吸収性材料から形成される縫合糸、例えば可とう性、硬質または可鍛性材料から形成されるワイヤーなどとすることができる。マーカー620は、図34Aおよび34Bに示されたマーカー320’’または明細書の他の箇所に記載された他の実施例のいずれかと同様とすることができ、例えば明細書の他の箇所に記載されている位置決めワイヤーと同様に、テザー630の遠位端634に、解放可能または実質的に永久に装着することができる。マーカー620から延びる細長いテザー630の付加は、組織内に植え込まれたときマーカー620の位置の付加的な参照を提供することができる。例えば、テザー630は、腫瘍摘出手術中マーカー620の正確な位置に執刀医を導く助けとすることができ、および/または、取り除いた腫瘍体積内のマーカー620の存在を確認することができる。テザー630は、また、ターゲットとなる組織領域中でのマーカー620の方向を同定する助けとなるタグを配置するために使用することができ、望むならば、所定の場所に残すか取り除くこともできる。
図36−41に戻ると、例えばマーカー620を胸部41内の触診不可能な病変142内に植え込むための、ターゲットとなる組織領域中にマーカー装置610を植え込むための供給装置660および方法が示されている。先の実施例と同様に、供給装置660は、近位端262aと遠位端262bを含み、例えば胸部41内のターゲットとなる組織領域に組織を介して導入される大きさとした、マーカー装置610を運ぶ、シャフト262を含んでいる。供給装置660は、少なくとも部分的にシャフト662の近位端662aと遠位端662bとの間に延びる内腔664、および、内腔664からマーカー620を供給するためのシャフト662内をスライド可能なプッシャー部材666、を含むことができる。図示のように、シャフト662の遠位端662bは、シャフト662が組織を介して直接導入可能なように、傾斜させるかおよび/または尖らせることができる。あるいは、供給装置660は、例えば明細書の別の場所に記載されているように、組織を介して配置された、カニューレ、シースまたは他の管状部材(図示せず)を介して導入することができる。任意に、遠位端662bは、明細書の他の箇所に記載されているように、例えば導入中における遠位端662bのモニタリングを促進できる、例えば放射線不透過性または音波を発生するまたは他の材料から形成された、バンドまたは他の特徴を含むことができる。
図36に示すように、プッシャー部材666は、そこを通ってテザー630をスライド可能に受けるための内腔667を含む。そのため、製造中または使用前のいつでも、マーカー装置610は、マーカー620が遠位端662b近傍の内腔664内に配置されて、テザー630がプッシャー部材666の内腔667を介して、プッシャー部材666に結合したプランジャー668から延びるように、供給装置660内にロードすることができる。マーカー620がらせん形状または他の形状に偏向している場合、マーカー620は、図36に示すように、それがシャフト662中にロードされるように、直線形状とすることができる。マーカー装置610は、ワイヤー位置決め処置に変えて、腫瘍摘出手術前にあるいは生検のときに、植え込むことができる。あるいは、マーカー装置610は、コアニードル生検機器または真空コアニードルシステム(図示せず)を介して、供給することもできる。
例えば処置中、図36に示すように、遠位端662bは、例えば病変142内のターゲットとなる組織領域に組織を介して挿入することができる。一旦供給装置660の遠位端662bが組織内の望ましい位置まで前進すると、図37に示すように、シャフト662は、内腔664からマーカー620を供給するため、プッシャー部材666に結合したプランジャー668に対し引き込むことができる。図示のように、マーカー620は、例えば図37に示されたテーパーを有するらせん形状に戻るように、展開により自動的および/または弾性的に形状を変化させることができる。図38に戻ると、供給装置660は、例えば病変142内などのターゲットとなる組織領域内にマーカー620を残したまま、患者の体から引き出すことができる。テザー630は、図39に示すように、端部が胸部41から露出するまで、プッシャー部材666を介して簡単にスライドすることができる。
任意に、図40に示すように、テザー630は、マーカー620を病変142内の位置に残したまま、マーカー620から分離することができる。例えば、テザー630は、所定の張力の適用により破壊する、マーカー620直近の弱い領域(図示せず)を含むことができる。あるいは、テザー630は、マーカー620から遠位端634の糸を抜くようにテザー630を回転することによって、マーカー620から解放される、糸を通した遠位端634または他のコネクターを含むことができる。さらに他の例において、テザー630は、以降の腫瘍摘出手術または他の処置中マーカー620に装着されたまま残ることができる。
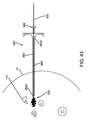
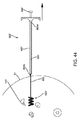
図42に戻ると、マーカー装置610と一般的に近似した、すなわち、テザー630およびマーカー620’を含む、マーカー装置610’の他の典型的な実施例が示されている。しかしながら、マーカー装置610’は、図41Aおよび41Bに示されたマーカー320’’’’と近似したものとすることもできる。図43−46は、図36−40に示されたものと一般的に近似した、マーカー装置610’を植え込むための、供給装置620’および方法の典型的な実施例を示す。
上述したシステムおよび方法は胸部内の病変に関するものであるが、1つ以上のマーカーまたはターゲットは、上述したプローブ30などのプローブを使用した次の位置決定のために、患者の体の他の領域に植え込まれまたは導入されることができる。例えば、1つ以上のターゲットは、次の位置決めのために、胆管、大腿動脈または静脈、卵管または他の体の内腔の内部または近傍に配置することができる。ターゲットは、カテーテル、ワイヤーまたは他の供給装置により体の内腔内に運ぶことができ、例えばカテーテルまたはワイヤーを固定することによって、または、マーカーを体の内腔の壁にあるいはその内部にあるいはそれを介してまたは体の内腔内に固定することによって、その内部に装着することができる。
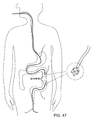
例えば、図47は、1回以上の診断および/または治療が実行される患者の胃腸管3を示している。図示のように、マーカー2を運ぶカテーテル1は、例えば口または直腸を介して、患者の胃腸管3内に導入することができる。図48からわかるように、カテーテル1は、例えば明細書の他の箇所で記載された他のマーカーと近似したマーカー2を含むことができる。例えば、マーカー2は、図23A−23Cに示されて上述されている1つ以上のビード320に近似した特徴を含むことができる。カテーテル1およびマーカー2は、例えばX線透視装置、超音波または他の外部イメージングを使用して、胃腸管3内の望ましい位置まで前進することができる。
明細書の他の箇所で記載されたプローブのいずれかのようなプローブは、次に、マーカー2の場所を見つけて、それにより胃腸管3内の位置を決めるために使用することができる。他の体の内腔が、例えば患者の体の外部からの侵襲の少ない方法で、例えば体の内腔へのアクセスを促進するために、同様の方法で位置決めできることは理解できるであろう。例えば、図49に示すように、マーカー2は、例えば壁の穿刺を促進して、クリップ、カット、結紮ために、体の内腔に入るようにあるいは体の内腔を閉じるように、胃腸管3内の特定の位置の場所を見つけるために使用することができる。図49は、例えば従来の腹腔鏡処置を使用する、送気された腹腔4の断面図である。明細書の他の場所で記載されたプローブのいずれかと近似するプローブ5は、カテーテル1上のマーカー2の位置をスキャンおよび/または検出するために、アクセスカニューレ6を介して挿入することができる。腹腔鏡7は、次に、マーカー2に対するプローブ5の位置を視覚化するために使用することができる。一旦マーカー2が位置決めされると、アクセスシース8は、例えば1回以上の診断および/または治療を行うために、望ましい位置での胃腸管3へのアクセスを起こすために使用することができる。マーカー2およびカテーテル1は、一旦アクセスが達成されると、あるいは望むならば処置が終了した後に、取り除くことができる。
典型的な実施例において、マーカーはカテーテルを使用して卵管内に導入することができ、次に、注射針または他の装置は、例えば結紮、麻痺のため卵管にアクセスするためあるいは卵管を分離または閉止するため、マーカー上の患者の皮膚および組織を穿刺するなどの侵襲の少ない方法で、導入することができる。あるいは、マーカーが胆管内に配置された場合、内視鏡的なアクセスは、例えば患者の腸内での処置を行うなど胆管にアクセスするために、プローブ30のガイドのもとで使用することができる。さらに他の例において、マーカーは、収容の対象となる大腿動脈、静脈または他の管の長さと連通するブランチに配置することができ、次に、プローブ30は、近傍の管から分離されて収容すべき管の長さを許すよう、例えば核ブランチがカット、結紮、麻痺および/または分離されるために、管外部のブランチの各々の場所を見つけ出すために使用することができる。
さらに他の例において、1つ以上のマーカーは、明細書に記載されたシステムを使用する位置決めされた治療のために、ターゲットとなる組織構造内に植え込むことができる。例えば、マーカーは、それらが植え込まれているターゲットとなる組織領域の内部または周囲に延長時間を超えて解放できる、1つ以上の薬物、放射性物質または他の治療剤を運ぶことができる。例えば治療剤が実質的かつ完全に使い果たされたあるいは十分に供給された後などの、十分な時間が経過した後、プローブ30は、例えば侵襲の少ない方法でマーカーの回復および/または除去を促進するために、マーカーの場所を見つけ出すために使用することができる。
図51に戻ると、マイクロ波アンテナを用いる、体内のマーカーの場所を見つけ出すための方法510の典型的な実施例のフローチャートが示されている。方法510の開始において、送信アンテナは、高周波(RF)送信信号を体内に送信する:520。次に、受信アンテナは、マーカーから反射されたRF受信信号を受信する:530。受信信号が受信された後、少なくとも1つのプロセッサーが、送信信号が送信アンテナによって送られた時から受信信号が受信アンテナによって受信された時までの時間の差を計算する:540。一旦プロセッサーが時間差を形成すると、少なくとも1つのプロセッサーが、計算された時間差を使用して、(送信アンテナおよび受信アンテナの両者を収容する)プローブの先端からマーカーまでの距離を決定する:550。一旦距離が決定されると、プローブの先端からマーカーまでの距離がディスプレー上に表示される:560。距離が表示された後、方法510は終了する:570。
図52および53に戻ると、マーカー521の場所を見つけ出すため図51の方法510を実行する典型的なマイクロ波アンテナプローブ531を含む、胸部41の断面図が示されている。方法510は、胸部以外の体の他の領域に配置されたマーカーの場所を見つけ出すためにも使用できることは注意すべきである。特に、図52は、その送信アンテナ511を介して送信信号501を送信するためのマイクロ波アンテナプローブ531を示し、図53は、その受信アンテナ512を介して受信信号502を受信するためのマイクロ波アンテナプローブ531を示している。
図52に戻ると、先に詳細に議論したように、マーカー521は、例えば超音波セッションの間に、外科的に取り除かれる病変(または腫瘍)142近傍の胸部41の組織40中に、皮膚48を介して、埋め込むことができる。マーカー521は、図23A−28Cに示されたマーカーなどの、いかなるタイプのマーカーとすることができる。典型的な実施例において、マーカー521は、複数のビードまたはセグメントを運ぶ内部コアワイヤーから主として構成することができる。内部コアワイヤーは、例えばステンレススチール、ニチノールなどの、弾性材料、超弾性材料および/または形状記録材料から形成することができ、その結果、明細書の他の実施例と同様に、内部コアワイヤーは、組織40内で展開されたとき、所定の形状(例えばコイル形状)を形成するよう偏向することができる。マーカー521のビードまたはセグメントは、例えば、ステンレススチール、ニチノール、チタンまたは複合材料などの金属などの、電磁反射特性を有する材料から形成することができる。ビードまたはセグメントは、ビードまたはセグメントの表面に衝突する電磁信号を反射するようカスタマイズされた表面仕上げを含むことができる。
マーカー521が組織40中に展開された後、患者が手術中、マイクロ波アンテナプローブ531は、胸部41内のマーカー521の場所を見つけ出すために使用することができる。マーカー521の位置は、執刀医に、胸部41から取り除かれる病変142の一般的な位置を示す。マイクロ波アンテナプローブ531の動作中、マイクロ波アンテナプローブ531の送信アンテナ511は、胸部41の組織40を介して、送信信号501を送信することができる。例えば、送信信号501は一連のパルスから構成することができる。また、送信信号501は、スタート周波数(例えば1.5GHz)からストップ周波数(例えば4.5GHz)まで、所定の周波数増分(例えば100MHz増分)で、スイープすることができる。スタート周波数はストップ周波数よりも低い周波数とすることができ、それとは逆に、スタート周波数はストップ周波数よりも高い周波数とすることができる。所定の増分は、大きさにおいて均一とすることができ、あるいは、大きさにおいて不均一とすることができる。
図53に戻ると、一旦送信信号501がマーカー521に衝突すると、送信信号501は、マーカー521のビードまたはセグメントの少なくとも1つの、少なくとも1つの反射面で反射する。反射された信号(すなわち受信信号)502は、マイクロ波アンテナプローブ531に向かって戻るように伝播する。マイクロ波アンテナプローブ531の受信アンテナ512は、一連のパルスで構成される受信信号502を受信することができる。
マイクロ波アンテナプローブ531は、バヨネットまたは他のコネクター533で互いに接続される、アコーディオン部534およびバヨネット535を含むことができる。マイクロ波アンテナプローブ531は、また、バヨネット535の他の端部に接続されたアンテナ部532を備えることができる。例えば、アンテナ部532の先端は、例えば以下に更に記載するように、送信アンテナ511および受信アンテナ512の両者を含むことができる。
マイクロ波アンテナプローブ531の受信アンテナ512が受信信号502を受信した後、マイクロ波アンテナプローブ531またはディスプレーユニット536内に含まれることができる、少なくとも1つのプロセッサー(例えばデジタル信号プロセッサー(DSP))(図示せず)は、送信信号501が送信アンテナ511によって送信された時間(T1)と受信信号502が受信アンテナ512によって受信された時間(T2)との間の時間の差(T)(すなわちT=T2−T1)を計算することができる。プロセッサーが時間の差(T)を計算した後、少なくとも1つのプロセッサー(例えばDSP)は、時間の差(T)を使用して、プローブの先端からマーカー521までの距離(L1)を決定することができる(すなわち、プロセッサーは、信号反応の計算した時間の遅延(T)を使用することによって、距離(L1)のための距離計算を行うことができる)。
一旦プロセッサーがプローブ531の先端からマーカー521までの距離(L1)を決定すると、プロセッサーは、距離情報(L1)を、ケーブル333を介してディスプレーユニット536に送ることができる。典型的な実施例において、ケーブル333は、RS232同軸ケーブルなどの同軸ケーブルとすることができる。ある実施例において、距離情報(L1)は、例えばプローブ531内の送信器(図示せず)によって、無線でディスプレーユニット536に送ることができることに注意すべきである。ディスプレーユニット536が距離情報(L1)を受信した後、ティスプレーユニット536は、例えば執刀医にマーカー521の位置を伝えるように、そのディスプレースクリーン537上に距離情報(L1)を表示することができる。距離情報は、例えばインチ(in.)またはセンチメートル(cm)などの長さの単位で距離を表す数値として、表示することができる。例えば、ディスプレースクリーン上で「3cm」と表示される。長さの単位に代えてまたはそれに加えて、ディスプレースクリーン537は、マーカー、マイクロ波アンテナプローブ531、マイクロ波アンテナプローブ531の先端からマーカーまでの距離、および/または、マーカーを含む体の部分の生理学的絵画(例えば胸部)を表す、グラフィックイメージ(例えば2次元または3次元イメージ)を表示することができる。
ある実施例によれば、マイクロ波アンテナプローブ531の受信アンテナ512が受信信号502を受信した後、マイクロ波アンテナプローブ531またはディスプレーユニット536内に含まれる、少なくとも1つのプロセッサー(例えばDSP)(図示せず)は、受信信号502の振幅を測定することができる。プロセッサーが受信信号502の振幅を測定した後、少なくとも1つのプロセッサー(例えばDSP)は、受信信号502の振幅を使用することによって、マーカー521がマイクロ波アンテナプローブ531の先端に関して配置された方向を決定することができる。
例えば、執刀医が、マーカー521に向けるあるいはそこから離れる異なる角度で、マイクロ波アンテナプローブ531を移動させるとき、受信信号502の振幅は、マーカー521に向けるあるいはそこから離れる方向にマイクロ波アンテナプローブ531が向いているかどうかに従って、増加するかまたは減少する。マイクロ波アンテナプローブ531がマーカー521の方向に向く角度で保持されているときは、受信信号502の振幅は増加し;マイクロ波アンテナプローブ531がマーカー521から離れる方向に向く角度で保持されているときは、受信信号502の振幅は減少する。そのように、受信信号502の相対的または絶対的な振幅は、マイクロ波アンテナプローブ531の先端に関してマーカー521の位置を決定するために、プロセッサーによって、使用することができる。
他の実施例によれば、マイクロ波アンテナプローブ531のアンテナ部532は、加速度計(図示せず)を含むことができる。加速度計は、マイクロ波アンテナプローブ531がマーカー521に関し傾く角度(すなわち「傾斜角」)を測定することができる。マイクロ波アンテナプローブ531の受信アンテナ512が受信信号502を受信した後、マイクロ波アンテナプローブ531またはディスプレーユニット536内に含まれる、少なくとも1つのプロセッサー(例えばDSP)(図示せず)は、マイクロ波アンテナプローブ531の時間の差(T)および傾斜角度を使用することによって、マイクロ波アンテナプローブ531に関しマーカー521の位置を決定することができる。
図54は、図51の方法510を実行できるシステムの典型的な部品の線図的表示である。方法510で使用される部品は、供給装置561、マーカー521、マイクロ波アンテナプローブ531およびディスプレーユニット536を一般的に含んでいる。供給装置561は、図29A−31Bで示されて明細書の他の箇所で記載されたような、いかなるタイプの供給装置とすることができる。一般的に、供給装置561は、組織を介してのターゲットとなる組織領域内(例えば胸部内)へ導入するため、および、マーカー521をターゲットとなる組織領域内に投入するため、ハンドル563およびシャフト562を含むことができる。先に説明したように、マーカー521は、図23A−28Cで示されて明細書の他の箇所で記載されたような、いかなるタイプのマーカーとすることができる。例えば、マーカー521は、複数のビードまたはセグメントを運ぶ内部コアワイヤーから構成することができる。
マイクロ波アンテナプローブ531は、非無菌の再利用可能な部分531Aおよび無菌の使い捨てで再利用不可能な部分531Bの2つの主要部を含むことができる。非無菌の再利用可能な部分531Aは、送信信号の発生のためにおよび受信信号の処理のために使用される電子部品を含むことができる。しかしながら、これらの電子部品は、ディスプレーユニット536内などの、マイクロ波アンテナプローブ531以外のどこかに配置することができることに注意すべきである。再利用可能な部分531Aに収容された電子部品は、例えば図55の記載などの明細書の他の箇所でさらに議論される。
無菌の使い捨てで再利用不可能な部分531Bは、アンテナ部535、バヨネット535、バヨネットコネクター533およびアコーディオンシース534を含むことができる。アンテナ部の内部の詳細は、図56A−58の記載でさらに議論される。アンテナ部535の一端は、バヨネット535に接続することができる。バヨネット535は、バヨネットコネクター533を介して、アコーディオンシース534に接続することができる。マイクロ波アンテナプローブ531の操作の前に、無菌の使い捨てで再利用不可能な部分531Bのアコーディオンシース534は、非無菌の再利用可能な部分531Aを超えてスライド可能とすることができ、それにより、2つのユニット531Aおよび531Bがマイクロ波アンテナプローブ531となる単一のユニット531を形成するために互いに接合される。マイクロ波アンテナプローブ531の操作の後、無菌の使い捨てで再利用不可能な部分531Bは非無菌の再利用可能な部分531Aから除去することができ、無菌の使い捨てで再利用不可能な部分531Bは、再び再利用しないように、廃棄することができる。非無菌の再利用可能な部分531Aは、消毒され、殺菌され、他の処置で再び使用するための準備をすることができる。
非無菌の再利用可能な部分531Aの一端は、ケーブル333(例えばRS−232同軸ケーブル)を介してディスプレーユニット536に接続することができる。ディスプレーユニット536は、マイクロ波アンテナプローブ531の先端からマーカー521までの距離および/または他の情報を表示するための、ディスプレースクリーン537を含むことができる。距離情報は、長さの単位(例えば図54に示されているように10.0cm)に関し、ディスプレースクリーン537上に表示することができる。また、受信信号502の振幅は、バーグラフ538あるいは数値測定値(図示せず)によって、ディスプレースクリーン537上に表示することができる。ディスプレーユニット536は、また、少なくとも1つの音声スピーカー539を含むことができる。音声スピーカー539は、マイクロ波アンテナプローブ531の先端に関しマーカー521の位置を示すために、可聴ノイズおよび/または言葉を発生することができる。
図55は、図54のマイクロ波アンテナプローブ531の典型的な構成要素を示すブロックダイアグラム600である。非無菌の再利用可能な部分531Aは、信号発生器620、増幅器640、アナログツーデジタル(A/D)変換器650およびデジタル信号プロセッサー(DSP)660を含むことができる。例えば参照オッシレーターなどの信号発生器620は、方形波信号、三角波信号または正弦波信号などの振動信号を発生する。
例えば、方形波信号625は、信号発生器620からマイクロ波アンテナプローブ531のアンテナ部532の送信アンテナ511に送ることができる。方形波信号625が送信アンテナ511を通過すると、送信アンテナ511は、バンドパスフィルター(「BPF」)として動作し、方形波信号625を一連のパルス630に変換する。そのようにして、送信アンテナ511から送信された送信信号501は一連のパルス630を含む。送信信号501は、組織中に送信することができ、マーカー521から反射することができる。一旦送信信号501がマーカー521から反射されると、反射された信号(すなわち受信信号502)は一連の減衰したパルス635を含む。
マイクロ波アンテナプローブ531のアンテナ部532の受信アンテナ512は、受信信号502を受信することができる。一連の減衰したパルス635を含む受信信号502は、パルス635のゲインを増幅するために、増幅器640に入力することができる。増幅器640の出力は、増幅したアナログ信号をデジタル信号に変換するために、A/D変換器650に入力することができる。A/D変換器650から出力されたデジタル信号は、処理のためにDSP660に入力することができる。先に説明したように、DSP660は、限定されるものでないが、送信信号501が送られた時から受信信号502が受信された時までの時間の差の計算、マイクロ波アンテナプローブ531の先端からマーカー521までの距離の決定、マイクロ波アンテナプローブ531の先端位監視マーカーの位置の決定、受信信号502の振幅の測定、および/または、マーカー521がマイクロ波アンテナプローブ531の先端に関し配置された方向の決定、を含む数多くの機能を実行することができる。DSP660の出力は、ワイヤー(例えばケーブル333)または無線によって、ディスプレーユニット536に送ることができる。
マイクロ波アンテナプローブ531のための電源(図示せず)は、ディスプレーユニット536内に含むことができる。例えば、マイクロ波アンテナプローブ531のための電源は、バッテリーとすることもでき、および/または、電源コードによって供給することもできる。あるいは、マイクロ波アンテナプローブ531のための電源は、マイクロ波アンテナプローブ531自身の内部に含むことができる。
図56A−56Cは、図54のプローブ531の送信アンテナ511または受信アンテナ512のいずれかあるいは両方のために使用することができる、アンテナサブユニット700の典型的な実施例を示す。図56Bおよび56Cに戻ると、マイクロ波アンテナプローブ531は、送信アンテナ511のための一つのアンテナサブユニット700および受信アンテナ512のための一つのアンテナユニット700とならかる、図示された2つのアンテナサブユニット700を収容することができる。図56Bに示されたアンテナサブユニット700が図56Cに示されたアンテナサブユニット700と同じであることに注意すべきである。図56Cは、単に、図56Bのアンテナサブユニット700の異なる図を示している。
アンテナサブユニット700は、アンテナユニット部710、外側同軸部720、サブミニチュアバージョンA(SMA)コネクター730の部分、を含むことができる。アンテナユニット部710は、外側同軸部720を介してSMAコネクター730に接続することができる。アンテナサブユニット700は、マイクロ波アンテナプローブ531の無菌の使い捨てで再利用不可能な部分531Bの、アンテナ部532、バヨネット部535およびバヨネットコネクター部533内に収容することができる(図示せず、例えば図54を参照)。
図56Aに戻ると、アンテナユニット部710は、ナイロンチューブ750内に収容できるボータイ型アンテナ740とすることができる。ナイロンチューブ750は、同様に、真鍮チューブ760内に収容することができる。真鍮チューブ760の端部は、アンテナサブユニット700の外側同軸部720に接続することができる。アンテナユニット部710は、例えば明細書の他の箇所に記載されているように、パッチ型アンテナ、ホーン型アンテナ、らせん型アンテナなどの、ボータイ型アンテナ740以外の他のタイプのアンテナを含むことができる。アンテナユニット部710によって用いられるアンテナの偏光は、用いるアンテナのタイプに応じて、直線偏光(例えば水平方向または垂直方向への)とすることができ、または、円偏光(例えば右円偏光(RHCP)または左円偏光(LHCP))とすることができる。
図56Cに戻ると、ボータイ型アンテナ740は、ストリップライン746によって分離される、2つの三角型アンテナ745a、745bから形成することができる。三角型アンテナ745a、745bは、例えば金属または複合材料などの電磁反射特性を有する材料から製造することができる。図56Cに示された2つの三角型アンテナ745a、745bは、垂直方向に偏光されている。図56Cに示された2つの三角型アンテナ745a、745bが90度(90°)回転する場合、2つの三角波アンテナ745a、745bは水平方向に偏光するであろう。
先に説明したように、マイクロ波アンテナプローブ531は、1つのアンテナサブユニット700が送信アンテナ511のためであり、もう1つのアンテナサブユニット700が受信アンテナ512のためである、2つのアンテナサブユニット700を収容することができる。送信アンテナ511のための1つのアンテナサブユニット700は、水平方向に偏光したボータイ型アンテナ740を含むことができ、受信アンテナ512のための他のアンテナサブユニット700は、垂直方向に偏光したボータイ型アンテナ740を含むことができる。そのため、送信アンテナは、受信アンテナの偏光(例えば、垂直偏光)の交差分極である偏光(例えば、水平偏光)を有することができる。マイクロ波アンテナプローブ531の動作中、水平方向に偏光した送信アンテナ511が水平方向に偏光した送信信号501を送信すると、水平方向に偏光した送信信号501はマーカー521と衝突し、垂直方向に偏光した受信信号502として反射されて戻る。垂直方向に偏光した受信アンテナ512は、次に、水平方向に偏光した受信信号502を受信することができる。
図57は、マルタクロス型アンテナ800を形成するために組み合わされた、図54のプローブ531の送信アンテナ511および受信アンテナ512を示す線図的表示である。マルタクロス型アンテナ800を形成するために、送信アンテナ511のためのボータイ型アンテナ740(図57において800として示される)は、受信アンテナ512のためのボータイ型アンテナ740(図57において810として示される)と組み合わすことができる。マルタクロス型アンテナ800は、マイクロ波アンテナプローブ531の無菌の使い捨てで再利用不可能な部分531Bのアンテナ部532の先端内に収容することができる(図示せず、例えば図54を参照)。図57に戻ると、送信アンテナ511および受信アンテナ512の両者のための外側同軸部720a、720bは、マイクロ波アンテナプローブ531の無菌の使い捨てで再利用不可能な部分531Bのバヨネット部535内に収容することができ、送信アンテナ511および受信アンテナ512の両者のためのSMAコネクター部730a、730bは、マイクロ波アンテナプローブ531の無菌の使い捨てで再利用不可能な部分531Bのバヨネットコネクター部533内に収容することができる(図示せず、例えば図54を参照)。
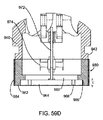
図58Aおよび58Bは、図57のマルタクロス型アンテナ800の詳細を示している。セラミック材料900は、インピーダンス整合のために、マルタクロス型アンテナ800の表面に搭載することができる。空気の誘電率が約ワン(1)であり、組織の誘電率が約テン(10)であるため、アンテナの性能を高めるために(すなわち、送信アンテナ501の有効等方性放射パワー(EIRP)を改善するために)、組織の誘電率と近似した約テン(10)の誘電率を持つセラミック材料900が、マルタクロス800の表面に搭載される。セラミック材料900の付加は、それが空気を介して組織中に伝播するため、送信信号501の減衰を防止するか減少することができる。
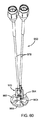
図59A−59Dに戻ると、明細書の他の箇所で記載されたシステムおよび方法のいずれでも使用できる、アンテナプローブ930の他の典型的な実施例が示されている。一般的に、プローブ930は、筐体940、アンテナサブアセンブリー950およびシールディング980を含む。任意に、汚染、露出を減少させるため、および/または、プローブ930の内部部品を保護するため、例えば筐体940内の開口を取り囲む、プローブ930の1つ以上の部品を取り囲む、外側スリーブまたはカバー(図示せず)を含むことができる。
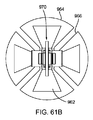
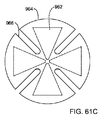
図60を付加的に参照すると、アンテナサブアセンブリー950は、通常明細書の他の実施例と同様に、マルタクロス型アンテナを形成するために組合わされた、それぞれがボータイ型構造を有する、送信アンテナ960tおよび受信アンテナ960rを含む。図61A−61Cに示すように、各アンテナ960は、誘電材料964のディスクまたは他のベース上に、互いに90度(90°)オフセットした、1対のアンテナ素子962を含む。各アンテナ素子962は、別々に形成されて次にディスク964に装着することができ、または、ディスク964の上面の上に直接堆積させることもできる。典型的な実施例において、アンテナ素子962は、ディスク964の上面の上に堆積した銀フィルムまたは他の材料から形成することができる。
回路970は、例えば1つ以上のトランス974および適当なリードによって各アンテナ素子962に結合したコネクター976がその上に設けられたPCB972を含む、アンテナ960に結合することができる。同軸ケーブル978は、明細書の他の箇所に記載された他の実施例と同様に、アンテナ960がシステムの他の部品と結合することを可能とするために、コネクター976に結合することができる。
図61A−61Cでよくわかるように、ディスク964は、アンテナ素子962の間に複数の放射状スロット966を含む、そのため、アンテナ素子962は、スロット966内の空気によって互いに実質的に分離することができ、それにより、感度を増加させることができ、クロストークおよび/またはノイズなどを減少することができる。あるいは、スロット966は、例えば、アンテナ素子962を互いに実質的に分離するために望ましい相対的に低い誘電率を有するフォームなど(図示せず)の、他の絶縁材料で満たすことができる。
図59Dでよくわかるように、ディスク964は、例えば、接着剤による接合、超音波溶接、融着、共働コネクター(図示せず)などの1つ以上によって、同様に、筐体940の先端942に結合されたシールディング980内に搭載することができる。図示のように、シールディング980は、ファラデーシールドを提供するために、例えば銅または他の材料から形成された相対的に薄い外側シールド984によって囲まれた、例えばナイロンまたは他のポリマー材料のカラーから形成された、内側絶縁層を含む。典型的な実施例において、銅テープの層は、互いの固定端部で、内側シールド982の周りにラップすることができる。あるいは、外側シールド984は、例えば接着剤による接合、締りばめ、などによって、その中に内側シールド982が挿入されて装着されている、シールド材料のスリーブとすることができる。
図59Dに示すように、シールディング980は、ディスク964の厚さ「t」より実質的に大きい長さを有することができる。例えば、内側シールド982は、例えば締りばめ、接着剤による接合、などによって、その中にディスク964が挿入されて装着されている、環状の溝986を含むことができる。図示のように、ディスク964の底面は、明細書の他の箇所に記載されているように、使用中にディスク964が組織と接触するよう、シールディング980の遠位端と実質的に同一平面にすることができる。任意に、マイラーフィルムまたは他の相対的に薄い材料の層(図示せず)は、例えば、流体または他の材料が先端に侵入することを防止し、汚染を減少し、および/または、プローブ930の先端を保護するために、ディスク964および/またはシールディング980の底面全体にけることができる。
図59Dを連続して参照すると、ディスク964の上面(その上にアンテナ素子962を有する、図示せず)は、シールディング980内で空気の領域に露出することができる。空気の低い誘電率のため、送信アンテナ960tからの送信は、遠心にすなわちディスク964と接触する組織方向に、集中する。組織の誘電率と実質的にマッチするよう選択されたディスク964の材料により、組織中への送信の深さは拡大することができる。ディスク964の背後の空気は、そうでなければ送信アンテナ960tによって組織から離れて出射するエネルギー損失を最小限にすることができる。同様に、ディスク964は、組織に向く受信アンテナ960rの感度を合わせることができる。シールド980内(同様にアンテナ素子962間のスロット966内)のディスク964の背後の空気は、クロストークやノイズを最小にすることができ、あるいはプローブ930の操作を拡大することができる。
図62に戻ると、例えば胸部内の腫瘍、病変または他の組織構造などの患者の体内のターゲットとなる組織領域、または、体内の他の位置、の場所を見つけ出すための、システム1010の他の典型的な実施例が示されている。システム1010は、一般的に、例えば明細書の他の実施例と同様に、タグ、マーカーまたはターゲット1040、および、電磁パルス、電磁波またはレーダーなどの他の信号を使用して、タグ1020を検出および/または位置決めするためのプローブ1020、を含む。任意に、システム1010は、タグ1040に加えて1つ以上の付加的なターゲット(図示せず)を含むことができる。
プローブ1020は、明細書の他の実施例と同様に、例えば低消費電力のインパルスレーダー(MIR)プローブなどの、電磁信号の出射および受信能力を有する携帯装置とすることができる。例えば、図62に示すように、プローブ1020は、例えば患者の皮膚またはその下の組織などの組織に対しまたはその近傍に配置することを意図されている、第1または遠位端1024と、例えばユーザーによって保持される第2または近位端1022とを含む、手持ちサイズの装置とすることができる。一般的に、プローブ1020は、明細書の他の実施例と同様に、例えばセラミックディスク1032(図63に示されている)の上に搭載された送信アンテナおよび受信アンテナ(図示せず)などの、1つ以上のアンテナ、1つ以上のプロセッサーまたはコントローラー、および、ディスプレー(図示せず)、を含む。
また、プローブ1030は、図62に示すように、例えば胸部組織90などの遠位端1024と接触する組織内に、光パルス(図62において1038aに破線によって表されている)を送信するよう構成された、例えば複数の光ファイバー1038(図63に示される)などの光送信器を含む。光ファイバー1038は、光源からの光がプローブ1020の遠位端1024から光ファイバー1038を通過するように、例えばカップリング1039によって、光源(図示せず)に結合することができる。典型的な実施例において、光源は、例えば800から950ナノメートルの間(800−950nm)の波長の近赤外線光を供給することができる、赤外線光源である。任意に、光ファイバーは、プローブ1030の中心軸と実質的に平行に延びる相対的に狭いビームとしてあるいはより広いビームとしてなどの望ましい方法で、プローブ1020によって送信された光の焦点を合わせるための、望ましくは、レンズ、フィルターなど(図示せず)の1つを含むことができる。
あるいは、プローブ1020は、光送信器1038の代わりに他のエネルギー源を含むことができる。例えば、電磁エネルギー、高周波(RF)エネルギー、振動エネルギーなどの(図示せず)源は、明細書の他の箇所に記載されているように、タグ1040を動作させるようにエネルギーパルスを供給するために、プローブ1020の遠位端1024上に設けることができる。エネルギー源は、明細書の他の箇所に記載されているように、例えばタグ1040の回路を交互に動作状態と非動作状態とするような、所定の方法でパルス状とすることができる。
プローブ1020は、送信アンテナによって送信するための信号を発生するため、および/または、受信アンテナから受信された信号を処理するため、に必要とされる、1つ以上のコントローラー、回路、信号発生器、ゲートなど(図示せず)を含むプロセッサーを含むことができる。プロセッサーの部品は、望みに応じて、個別部品、半導体素子、プログラム可能な装置、ソフトウェアコンポーネントなどを含むことができる。例えば、プローブ1020は、送信信号を発生するために送信アンテナと結合した、例えばパルス発生器および/または疑似雑音発生器(図示せず)などの、インパルス発生器、および、受信アンテナによって検出された信号を受信するためのインパルス受信器、を含むことができる。プロセッサーは、明細書の他の実施例と同様に、送信アンテナを介して、電磁パルス、電磁波、または、他の信号を送信して、次に、受信アンテナを介して、いかなる反射した電磁信号をも受信するように、高度にインパルス発生器およびインパルス受信器を動作させる、マイクロコントローラーおよびレンジゲートコントロールを含むことができる。使用できる典型的な信号は、例えば超低帯域幅の領域におけるマイクロインパルスレーダー信号のような、マイクロ波、高周波を含む。
プローブ1020は、例えばアンテナを介して得られた空間的またはイメージ的なデータなどの、プローブ1020のユーザーに対する情報を表示するために、例えばケーブル1036によって、ディスプレー(図示せず)に結合することができる。任意に、プローブ1020は、1つ以上のユーザーインターフェース、メモリー、送信器、受信器、コネクター、ケーブル、電源など(図示せず)の、他の特徴または構成部品を含むことができる。例えば、プローブ1020は、プローブ1020の部品を動作するために、1つ以上のバッテリーまたは他の内部電源を含むことができる。あるいは、プローブ1020は、プローブ1020の部品を動作するために、例えば標準的なAC電源などの外微電源と結合できる1つのケーブル1036などのケーブルを含むことができる。
図62に示すように、プローブ1020の内部部品は、プローブ1020が内蔵できるように、筐体またはケーシング内に提供することができる。例えば、ケーシングは、例えばプローブ1020の全体がユーザーの手で保持できるように、相対的に小さくポータブルにすることができる。任意に、例えば、遠位端1024の近傍の部分などのプローブ1020の部分は廃棄可能とすることができ、または、廃棄可能なカバー、スリーブなど(図示せず)は、望むならば明細書の他の実施例と同様に、プローブ1020の少なくとも近位の部分が再利用可能となるように、提供することができる。あるいは、例えば1つ以上のケーブル1036によってプローブ1020に結合されるように、手持ちサイズのプローブ1020から離れた1つ以上の部品を含む分離コントローラー(図示せず)を設けることができる。この他の例において、プローブ1020全体が廃棄可能で単一の使用用途の装置とすることができ、一方、コントローラーは、望むならば手術野の外部に残るがアクセス可能および/または視覚可能に残ることができる、新しいプローブ1020をコントローラーに接続することによって、複数の処置の間使用することができる。プローブ1020の構造および/または操作に関する付加的な情報は、明細書の他の箇所で特性された応用例に見つけることができる。
図64A−64Dに戻ると、図62に示すように胸部90内などの患者の体内に植え込むことができる受動タグ1040の典型的な実施例が示されている。一般的に、タグ1040は、任意に1つ以上のビードまたは他の要素(図示せず)を運ぶことができる、1対のワイヤー1044に結合した電子パッケージ1042を含む。
例えば、明細書の他の箇所に記載された実施例や明細書の他の箇所で特定された応用例と同様に、ワイヤー1044は、タグ1040の検出を高めるために、複数の表面、角度および/またはエッジを含む、複数のビードまたはセグメント(図示せず)を運ぶコアワイヤーを提供することができる。また、明細書の他の箇所に記載されているように、ワイヤー1044は、アンテナとして動作すること、および/または、電子パッケージ1042内の電子部品と協働すること、ができる。
典型的な実施例において、各ワイヤー1044は、約1/2から2ミリメートルの間(0.5−2mm)の直径または他の最大断面と約1および10ミリメートルの間(1.0−10mm)の長さを有する例えば固体または中空構造の細長い部材とすることができる。ワイヤー1044は、例えばステンレススチール、ニチノールなどの、弾性または超弾性材料および/または形状記憶材料から形成することができ、明細書の他の箇所で説明されているように、ワイヤー1044は、組織内で展開すると所定の形状に偏向するが、例えば供給を促進するために直線形状または弾性的に変形した形状となることができる。あるいは、ワイヤー1044は実質的に剛体とすることができ、タグ1040は例えば直線または曲線などの実質的に固定した形状で残る。
典型的な実施例において、ビードは、それぞれが通常円筒形状または球形状の部分を定義する、複数の管状体を含むことができる。ビードは、明細書で特定された応用例で記載されているように、例えば、ステンレススチール、ニチノール、チタンなどの金属、プラスチック材料または複合材料などの望ましい材料から形成することができる。アセンブリー中、複数のビードは、明細書の他の箇所にさらに記載されているように、例えばワイヤー1044を電子パッケージに装着する前後に、ワイヤー1044に配置して装着することができる。あるいは、ビードは除外することができる。
図64A−64Dに示すように、タグ1040は、中央の縦軸1048の周りに、例えばらせん形状、蛇行形状または他の曲面形状などの曲線形状を想定するよう偏向することができる。例えば、ワイヤー1044は、ワイヤー1044が示されたらせん構造に偏向するが実質的に直線構造になるため弾性的に直線状となることができる形状である、弾性または超弾性材料から形成することができる。ビード(図示せず)は、間隔を開けるか入れ子にすることができ、それにより、ビードは、例えば供給装置へのタグ1040のロードおよび/または患者の体へのタグ1040の導入を促進するため、直線構造とらせん構造との間のワイヤー1044の変形に実質的に邪魔になることはない。
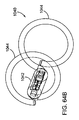
図65を付加的に参照すると、タグ1040は、プローブ1020からの入力信号を変調するよう構成された電子パッケージ1042中に入れられるか埋め込まれた、1つ以上の回路または他の電子部品1050を含むことができる。典型的な実施例において、半導体チップ(図示せず)は、例えばそれらと衝突する入力光(例えば赤外線光)を電子エネルギー(例えば、最小電圧)に変換することができる複数の感光性ダイオード、および、ダイオードが電子エネルギーを発生するとき解放状態および停止状態となることができるスイッチ1054、などの、電圧源または電力源あるいは他の電力変換装置1052を含む、パッケージ1042内に運ぶことができる。
図示のように、ダイオード1052の複数対は直接に接続することができ、それらはパッケージ1042内で互いに直角に空間的に配置することができる。例えば、感光性ダイオードが指向性であるとすると、例えば、ダイオードの少なくとも1対が、植え込まれた後のプローブ1020に関するタグ1040の方向にかかわらず、プローブ1020の光送信器からの光を受け取ることができるように、ダイオード1052の少なくとも2対は、180度(180°)オフセットしてまたは互いに関連して、パッケージ1042内に搭載することができる。パッケージ1042は少なくとも部分的に透明とすることができ、あるいは、パッケージ1042に向く光がダイオード1052によって受信できるように、ダイオード1052は露出することができる。
他の実施例において、電源は、外部エネルギーを望ましい電圧に変換することができる他の部品とすることができる。例えば、プローブ1020が、例えばEMF、RFまたは振動エネルギーの源などの他の電源を含む場合、電源1052は、ピックアップコイル、アンテナ、または、例えばキャパシターおよび/または望ましい電圧をスイッチ1054に供給するよう設けられた他の部品を含む、入力エネルギーを望ましい電圧に変換することができる他の装置、を含むことができる。赤外線エネルギーの1つの有利な点は、図62に示すように、患者の皮膚に対し配置されたプローブ1020が、例えば胸部90などの患者の体内に数インチ離れて植え込まれた相対的に小さいタグ1040を動作させるのに十分なエネルギーを供給することができるように、それが組織を介して十分に通過することができる点である。
図65に示す実施例において、スイッチ1054は、例えば接合型電界効果トランジスター(JFET)などの電界効果トランジスター(FET)とすることができ、ダイオード1052の一端はゲート(G)に結合されるとともにその他端はソース(S)に結合されており、抵抗1056が両端の間に結合されている。また図示のように、例えばワイヤー1044がタグ1040に対する効果的なアンテナを提供するように、ソース(S)は1つのワイヤー1044に電気的に結合することができ、ドレイン(D)は他のワイヤー1044に結合することができる。他の実施例において、スイッチ1054は、例えばダイオードの反対側の端部がワイヤー1044と結合するダイオード1052(または他の電源)に結合した、ショットキーダイオードとすることができる。例えば、回路1050の部品は、部品が図65の線図で結合されている以外は互いに電気的に絶縁されるように、パッケージ1052内に搭載することができる。ワイヤー1044は、ワイヤー1044の端部が図示のようにスイッチ1054に電気的に結合されるように、パッケージ1052に接合または装着することができる。
各ダイオード1052は、開くために光に曝されたとき、十分な電圧(例えば0.5V)を発生することができ、ほとんどまたは全く負荷がないとき(電流引き込み)、スイッチ1054を閉じることができる。回路1050はただ単にプローブ1020からの信号を変調することを意図されているだけであるため、ほとんどまたは全く電流を必要とせず、そのため、ダイオード1052から(および結果にはプローブ1020から)必要とされる電力は最小限とすることができ、それによって、システム1010の電力需要を減少させる。
図65に示された配置において、断続的にダイオード1052と衝突する光は、図66に示されているように、スイッチ1054を開閉することができるコントロール信号を提供するために、ゲート(G)およびソース(S)を横切る電圧を発生することができる。そのため、受動タグ1040が、タグ1040の中央に、高周波スイッチと同等のものを含む結果となる。閉じた状態から開いた状態へスイッチ1054を変化させることができることにより、ワイヤー1044によって提供されたアンテナの反射特性は、かなり変化することができる。例えば、スイッチ1054は、極性を変化することができ、または、スイッチ1054が開いた状態および閉じた状態となることで、タグ1040から反射された信号を変調することができる。
使用中、プローブ1020は、その内部にタグ1040が植え込まれている例えば図62の胸部90などの患者の皮膚に対して、配置することができる。プローブ1020のアンテナからの信号は、タグ1040が信号を受信してプローブ1020に戻すように反射することでスイッチ1054を開いた状態から閉じた状態にするため、光源からのパルス信号とともに供給することができる。例えば、タグ1040などの近傍の患者の体内のプローブアンテナ、組織または他の構造体のために、プローブ1020によって受信される実質的なクラッター、クロストークまたは他のノイズがある場合、2つの状態(スイッチ1054が開いた状態および閉じた状態)からの反射信号は互いに除算することができ、実質的に他のノイズを除去することができ、プローブ1020がタグ1040を特定および/または位置決めすることを可能とする。そのため、プローブ1020は、信号の信号対雑音比を増加させるために、変調された反射信号を使用することができる。
明細書の他の箇所に記載された実施例および明細書の他の箇所で特定された応用例と同様に、図62のシステム1010は、例えば、病変または他のターゲットとなる組織領域の位置決めを促進するために、および/または、胸部90または他の体の構造からの試料の切開および/または除去を促進するために、乳房生検または腫瘍摘出手術中における医療処置の間、使用することができる。例えば明細書の他の箇所に記載されているように、システム1010が胸部病変の位置決めに特に有効であると記載されているが、システム1010は、また、体の他の領域の他の対象物の位置決めにも使用できることは、注意すべきである。
処置の前に、例えば腫瘍または他の病変などのターゲットとなる組織領域は、従来の方法を使用して、特定することができる。例えば、胸部90内の病変(図示せず)は、例えばマンモグラフィーおよび/または他のイメージングを使用して、特定することができ、決定は病変を除去するために行われる。タグ1040は、例えば、病変内またはその近傍のタグ40まで、介在組織を介して患者の皮膚から経皮的に導入された、注射針または他の供給装置(図示せず)を使用して、ターゲットとなる病変近傍の胸部90内に植え込むことができる。例えば、図64A−64Dのタグ1040のワイヤー1044は、実質的に直線状とすることができ、供給装置内にロードすることができる。明細書で特定された応用例に記載されているように、タグ1040はターゲットとなる位置で露出されおよび/またはそこに供給されるため、ワイヤー1044は、検出を促進するために、移動のリスクを減少させることができおよび/またはタグ1040の断面を増加させることができる、緩やかな曲線構造に弾性的に戻ることができる。
タグ1040が望み通り植え込まれた後、プローブ1020の遠位端1024は、例えば通常病変上の患者の皮膚の近傍あるいはそれに接触して配置すること、および/または、通常病変およびタグ1040に向けること、ができ、作動する。プローブ1020の送信アンテナ(図示せず)は、組織中を移動してタグ1040で反射する電磁信号1034Tを出射することができる。戻り信号1034Rは、プローブ1020中の受信アンテナ(図示せず)に戻るよう反射することができ、それは、次に、執刀医のための切開の正しい方向の決定を促進するために、例えば距離および/または配向角などの、タグ1040とプローブ1020の遠位端1024との間の空間的な関係を決定することができる。
また、実質的に同時に、プローブ1020は、ダイオード1052によって受信される、光パルス1038aを送信することができる。ダイオード1052は、スイッチ54を開いた状態および閉じた状態とする電圧を交互に発生することができる。このことは、タグ40にプローブ1020に反射して戻った信号の相を変えさせ、タグ1040および結果的にはターゲットとなる病変を特定および/または位置決めするために、例えば減算を行うことによって、信号を処理することができる。
組織は、次に、例えば患者の皮膚で切開を行うことにより、および、病変の周りのターゲットとなるマージンに対応する望ましい深さまで介在する組織を切開することにより、切開することができる。組織試料は、明細書の他の実施例と同様に、例えば除去された資料1046内に残るタグ1040とともに、従来の腫瘍摘出手術の処理を使用して、摘出または除去することができる。
明細書のいずれの実施例で示された要素および部品は、特定の実施例に対し典型的なものであり、明細書に記載された他の実施例においてあるいはそれらと組み合わせて使用できることは理解すべきである。
本発明は各種の変更および代替形式を受け入れることができるが、その具体例の例は、図面中に表されており、明細書中に詳細に記載されている。しかしながら、本発明は記載された特的の形式または方法に限定されるべきでなく、それとは反対に、本発明は、添付された特許請求の範囲内に入る、全ての変形例、同等物および代替物をカバーするものであることは、理解すべきである。