JP6259772B2 - イメージング装置 - Google Patents
イメージング装置 Download PDFInfo
- Publication number
- JP6259772B2 JP6259772B2 JP2014551721A JP2014551721A JP6259772B2 JP 6259772 B2 JP6259772 B2 JP 6259772B2 JP 2014551721 A JP2014551721 A JP 2014551721A JP 2014551721 A JP2014551721 A JP 2014551721A JP 6259772 B2 JP6259772 B2 JP 6259772B2
- Authority
- JP
- Japan
- Prior art keywords
- image
- minimum margin
- unit
- area
- ablation
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T7/00—Image analysis
- G06T7/0002—Inspection of images, e.g. flaw detection
- G06T7/0012—Biomedical image inspection
- G06T7/0014—Biomedical image inspection using an image reference approach
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T7/00—Image analysis
- G06T7/0002—Inspection of images, e.g. flaw detection
- G06T7/0012—Biomedical image inspection
- G06T7/0014—Biomedical image inspection using an image reference approach
- G06T7/0016—Biomedical image inspection using an image reference approach involving temporal comparison
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06V—IMAGE OR VIDEO RECOGNITION OR UNDERSTANDING
- G06V20/00—Scenes; Scene-specific elements
- G06V20/60—Type of objects
- G06V20/69—Microscopic objects, e.g. biological cells or cellular parts
- G06V20/695—Preprocessing, e.g. image segmentation
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/10—Image acquisition modality
- G06T2207/10072—Tomographic images
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/10—Image acquisition modality
- G06T2207/10132—Ultrasound image
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/20—Special algorithmic details
- G06T2207/20212—Image combination
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/30—Subject of image; Context of image processing
- G06T2207/30004—Biomedical image processing
- G06T2207/30024—Cell structures in vitro; Tissue sections in vitro
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/30—Subject of image; Context of image processing
- G06T2207/30004—Biomedical image processing
- G06T2207/30096—Tumor; Lesion
Description
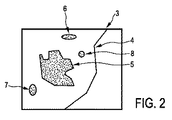
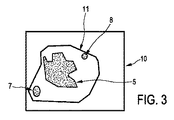
第1切除手順によって切除されるべき切除部分を含む、オブジェクトの領域を示す第1画像を提供するための第1画像提供ユニットと、
第1切除手順が実行された後のオブジェクトの領域を示す、又はオブジェクトの、切除されている切除済部分を示す、第2画像を提供するための第2画像提供ユニットと、
第1画像と第2画像を互いに対してレジストレーションするためのレジストレーションユニットと、
レジストレーションされた第1及び第2画像に基づいて切除部分と切除済部分の間のマージンが最小の領域である、最小マージン領域を決定するための最小マージン決定ユニットとを有する。
請求項1に記載のイメージング装置と、
最小マージン領域及び隣接領域の少なくとも一つによって定義されるオブジェクトの部分をプローブするためのオブジェクトタイプ決定器であって、隣接領域は第1切除手順が実行される前に最小マージン領域に隣接しており、オブジェクトタイプ決定器はプローブ部分におけるオブジェクトのタイプを決定するように構成される、オブジェクトタイプ決定器と、
プローブ部分におけるオブジェクトの決定されたタイプに応じて第2切除手順において隣接領域を切除するための切除器とを有する。
第1画像提供ユニットによって、第1切除手順によって切除されるべき切除部分を含む、オブジェクトの領域を示す第1画像を提供するステップと、
第2画像提供ユニットによって、第1切除手順が実行された後のオブジェクトの領域を示す、若しくはオブジェクトの切除されている切除済部分を示す第2画像を提供するステップと、
レジストレーションユニットによって第1画像と第2画像を互いに対してレジストレーションするステップと、
最小マージン決定ユニットによって、レジストレーションされた第1及び第2画像に基づいて切除部分と切除済部分の間のマージンが最小の領域である最小マージン領域を決定するステップとを有する。
請求項12に記載のイメージングと、
オブジェクトタイプ決定器によって最小マージン領域と隣接領域の少なくとも一つによって定義されるオブジェクトの部分をプローブするステップであって、隣接領域は第1切除手順が実行される前に最小マージン領域に隣接しており、オブジェクトタイプ決定器はプローブ部分におけるオブジェクトのタイプを決定する、ステップと、
切除器によって、プローブ部分におけるオブジェクトの決定されたタイプに応じて第2切除手順において隣接領域を切除するステップとを有する。
Claims (12)
- 第1切除手順によって切除されるべき切除部分を含む、オブジェクトの領域を示す第1画像を提供するための第1画像提供ユニットと、
前記オブジェクトの、切除されている切除済部分を示す、第2画像を提供するための第2画像提供ユニットと、
前記第1画像と前記第2画像を互いに対してレジストレーションするためのレジストレーションユニットと、
前記レジストレーションされた第1及び第2画像に基づいて前記切除部分と前記切除済部分の間のマージンが最小の画像領域である最小マージン領域を決定するための最小マージン決定ユニットと、
前記第1及び第2画像の少なくとも一つにおいて前記最小マージン領域を表示するための表示ユニットと
を有する、イメージング装置。 - 前記第1画像提供ユニットが、前記切除部分の外縁がセグメンテーションによって検出可能であるような前記第1画像を提供し、
前記第2画像提供ユニットが、前記切除済部分の外縁がセグメンテーションによって検出可能であるような前記第2画像を提供し、
前記最小マージン決定ユニットが、前記切除部分の外縁と前記切除済部分の外縁の間のマージンを決定すること、及び前記決定されたマージンが最小である領域を最小マージン領域として決定することによって、前記最小マージン領域を決定する、
請求項1に記載のイメージング装置。 - 前記イメージング装置が、前記最小マージン領域と隣接領域の少なくとも一つによって定義される前記オブジェクトの部分をプローブするためのオブジェクトタイプ決定器をさらに有し、前記隣接領域は前記第1切除手順が実行される前に前記最小マージン領域に隣接しており、前記オブジェクトタイプ決定器は前記プローブ部分における前記オブジェクトのタイプを決定する、請求項1に記載のイメージング装置。
- 前記オブジェクトが生体組織であり、前記オブジェクトタイプ決定器が前記生体組織が前記プローブ部分において癌性であるかどうかを決定する、請求項3に記載のイメージング装置。
- 前記イメージング装置が前記プローブ部分を表示するための表示ユニットをさらに有し、前記表示ユニットは前記プローブ部分が癌組織を有すると決定された場合前記プローブ部分を強調する、請求項4に記載のイメージング装置。
- 統合ユニットが前記第2画像を提供し、前記最小マージン領域と前記隣接領域の少なくとも一つによって定義される前記オブジェクトの部分をプローブするように、前記オブジェクトタイプ決定器と前記第2画像提供ユニットが統合されて当該統合ユニットを形成する、請求項3に記載のイメージング装置。
- 前記最小マージン決定ユニットがマージン閾値を提供し、前記切除部分と前記切除済部分の間のマージンが前記提供されるマージン閾値よりも小さい追加領域を決定する、請求項1に記載のイメージング装置。
- 切除手順を実行するための切除装置であって、
請求項1に記載のイメージング装置と、
前記最小マージン領域と隣接領域の少なくとも一つによって定義される前記オブジェクトの部分をプローブするためのオブジェクトタイプ決定器であって、前記隣接領域は第1切除手順が実行される前に前記最小マージン領域に隣接しており、前記オブジェクトタイプ決定器は前記プローブ部分における前記オブジェクトのタイプを決定する、オブジェクトタイプ決定器と、
前記プローブ部分における前記オブジェクトの決定されたタイプに応じて第2切除手順において前記隣接領域を切除するための切除器とを有する、切除装置。 - 前記オブジェクトが生体組織であり、前記オブジェクトタイプ決定器は前記生体組織が前記プローブ部分において癌性であるかどうかを決定し、前記切除器は前記プローブ部分が癌組織を有すると決定された場合前記隣接領域を切除する、請求項8に記載の切除装置。
- 統合器が、前記隣接領域によって定義される前記オブジェクトの部分をプローブし、前記プローブ部分が癌組織を有すると決定された場合前記隣接領域を切除するように、前記オブジェクトタイプ決定器と前記切除器が当該統合器に統合される、請求項9に記載の切除装置。
- イメージング装置の作動方法であって、前記イメージング装置は、
第1画像提供ユニット、第2画像提供ユニット、レジストレーションユニット、最小マージン決定ユニット、及び表示ユニットを有し、
前記第1画像提供ユニットによって、第1切除手順によって切除されるべき切除部分を含む、オブジェクトの領域を示す第1画像を提供するステップと、
前記第2画像提供ユニットによって、前記オブジェクトの、切除されている切除済部分を示す、第2画像を提供するステップと、
前記レジストレーションユニットによって前記第1画像と前記第2画像を互いに対してレジストレーションするステップと、
前記最小マージン決定ユニットによって、前記レジストレーションされた第1及び第2画像に基づいて前記切除部分と前記切除済部分の間のマージンが最小の画像領域である最小マージン領域を決定するステップと、
前記表示ユニットによって前記第1及び第2画像の少なくとも一つにおいて前記最小マージン領域を表示するステップと
を有する、イメージング装置の作動方法。 - イメージングコンピュータプログラムが前記イメージング装置を制御するコンピュータ上で実行されるとき、請求項1に記載のイメージング装置に請求項11に記載のイメージング装置の作動方法のステップを実行させるためのプログラムコード手段を有する、イメージングコンピュータプログラム。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261586860P | 2012-01-16 | 2012-01-16 | |
| US61/586,860 | 2012-01-16 | ||
| PCT/IB2013/050385 WO2013108182A1 (en) | 2012-01-16 | 2013-01-16 | Imaging apparatus |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2015504737A JP2015504737A (ja) | 2015-02-16 |
| JP2015504737A5 JP2015504737A5 (ja) | 2016-03-03 |
| JP6259772B2 true JP6259772B2 (ja) | 2018-01-10 |
Family
ID=47754905
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014551721A Expired - Fee Related JP6259772B2 (ja) | 2012-01-16 | 2013-01-16 | イメージング装置 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US10204415B2 (ja) |
| EP (1) | EP2805304B1 (ja) |
| JP (1) | JP6259772B2 (ja) |
| CN (1) | CN104067313B (ja) |
| BR (1) | BR112014017144A8 (ja) |
| RU (1) | RU2014133533A (ja) |
| WO (1) | WO2013108182A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9689817B2 (en) * | 2012-03-21 | 2017-06-27 | Clear-Cut Medical Ltd. | MRI system for margin assessment of ex-vivo sample |
| US9824440B2 (en) * | 2012-11-20 | 2017-11-21 | Vanderbilt University | Methods and systems for three-dimensional real-time intraoperative surgical margin evaluation of tumor tissues |
| US11382586B2 (en) * | 2013-09-25 | 2022-07-12 | Richard R. Black | Patient-specific analysis of raw positron emission tomography data |
| US10674983B2 (en) * | 2013-09-25 | 2020-06-09 | Richard R. Black | Patient-specific analysis of positron emission tomography data |
| KR102372351B1 (ko) * | 2014-08-19 | 2022-03-08 | 삼성메디슨 주식회사 | 초음파 진단 장치 및 초음파 진단 방법 |
| WO2016109878A1 (en) * | 2015-01-07 | 2016-07-14 | Synaptive Medical (Barbados) Inc. | Method, system and apparatus for automatically evaluating resection accuracy |
| US11850004B2 (en) | 2018-05-15 | 2023-12-26 | Intuitive Surgical Operations, Inc. | Systems and methods for determining an arrangement of explanted tissue and for displaying tissue information |
| CN109003269B (zh) * | 2018-07-19 | 2021-10-08 | 哈尔滨工业大学 | 一种能提高医生效率的医学影像病灶的标注提取方法 |
| DE102019208355A1 (de) * | 2019-06-07 | 2020-12-10 | Siemens Healthcare Gmbh | Verfahren und System zur Navigationsunterstützung einer Person zur Navigation bezüglich eines Resektats, Computerprogramm und elektronisch lesbarer Datenträger |
Family Cites Families (44)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6671540B1 (en) * | 1990-08-10 | 2003-12-30 | Daryl W. Hochman | Methods and systems for detecting abnormal tissue using spectroscopic techniques |
| GB9920401D0 (en) * | 1999-08-27 | 1999-11-03 | Isis Innovation | Non-rigid motion image analysis |
| US6690816B2 (en) * | 2000-04-07 | 2004-02-10 | The University Of North Carolina At Chapel Hill | Systems and methods for tubular object processing |
| US7079674B2 (en) * | 2001-05-17 | 2006-07-18 | Siemens Corporate Research, Inc. | Variational approach for the segmentation of the left ventricle in MR cardiac images |
| US20070255169A1 (en) | 2001-11-19 | 2007-11-01 | Dune Medical Devices Ltd. | Clean margin assessment tool |
| US7769432B2 (en) * | 2001-12-10 | 2010-08-03 | Board Of Trustees Of The University Of Arkansas | Minimally invasive diagnosis and treatment for breast cancer |
| US20040199072A1 (en) * | 2003-04-01 | 2004-10-07 | Stacy Sprouse | Integrated electromagnetic navigation and patient positioning device |
| DE10322739B4 (de) * | 2003-05-20 | 2006-10-26 | Siemens Ag | Verfahren zur markerlosen Navigation in präoperativen 3D-Bildern unter Verwendung eines intraoperativ gewonnenen 3D-C-Bogen-Bildes |
| WO2005029372A1 (en) * | 2003-09-25 | 2005-03-31 | Synthetron Nv | Method and apparatus for scalable meetings in a discussion synthesis environment |
| CA2553368A1 (en) * | 2004-01-16 | 2005-08-11 | Smith & Nephew, Inc. | Computer-assisted ligament balancing in total knee arthroplasty |
| US7035371B2 (en) * | 2004-03-22 | 2006-04-25 | Siemens Aktiengesellschaft | Method and device for medical imaging |
| US7904145B2 (en) * | 2004-03-23 | 2011-03-08 | Dune Medical Devices Ltd. | Clean margin assessment tool |
| US7397935B2 (en) * | 2004-05-10 | 2008-07-08 | Mediguide Ltd. | Method for segmentation of IVUS image sequences |
| JP4612379B2 (ja) | 2004-09-22 | 2011-01-12 | 株式会社東芝 | 医用画像診断支援システム、医用画像診断支援装置、医用画像診断支援方法、コンピュータ読み取り可能な記憶媒体及びコンピュータプログラム |
| US8068896B2 (en) * | 2005-02-25 | 2011-11-29 | Intramedical Imaging, Llc | Detection of radiation labeled sites using a radiation detection probe or camera incorporating a solid state photo-multiplier |
| DE102005035430A1 (de) * | 2005-07-28 | 2007-02-01 | Siemens Ag | Verfahren zur verbesserten Darstellung co-registrierter 2D-3D-Bilder in der medizinischen Bildgebung |
| EP1865464B1 (en) * | 2006-06-08 | 2013-11-20 | National University Corporation Kobe University | Processing device and program product for computer-aided image based diagnosis |
| US8560047B2 (en) * | 2006-06-16 | 2013-10-15 | Board Of Regents Of The University Of Nebraska | Method and apparatus for computer aided surgery |
| EP2081494B1 (en) * | 2006-11-16 | 2018-07-11 | Vanderbilt University | System and method of compensating for organ deformation |
| CN101795636B (zh) * | 2007-01-24 | 2013-06-19 | 皇家飞利浦电子股份有限公司 | Rf消融计划器 |
| US7735349B2 (en) * | 2007-01-31 | 2010-06-15 | Biosense Websters, Inc. | Correlation of ultrasound images and gated position measurements |
| US7853089B2 (en) * | 2007-02-27 | 2010-12-14 | The Board Of Trustees Of The University Of Arkansas | Image processing apparatus and method for histological analysis |
| US20080269582A1 (en) * | 2007-04-28 | 2008-10-30 | Hebah Noshy Mansour | Methods and devices for surgical drains with sensors |
| US20090088628A1 (en) * | 2007-09-27 | 2009-04-02 | Klaus Klingenbeck-Regn | Efficient workflow for afib treatment in the ep lab |
| US20090177089A1 (en) * | 2008-01-04 | 2009-07-09 | Assaf Govari | Three-dimensional image reconstruction using doppler ultrasound |
| FR2936889B1 (fr) * | 2008-10-03 | 2012-09-28 | Univ Grenoble 1 | Procede pour le recalage d'un ensemble de points dans des images |
| CN106943153B (zh) | 2008-12-11 | 2021-01-22 | 皇家飞利浦电子股份有限公司 | 用于产生患者内部和外部图像的系统和方法 |
| US20100179522A1 (en) * | 2009-01-14 | 2010-07-15 | Medsci Technologies, Inc. | System for endosurgical removal of tumors by laser ablation with treatment verification - particularly tumors of the prostate |
| JP5397938B2 (ja) | 2009-02-16 | 2014-01-22 | ジーイー・メディカル・システムズ・グローバル・テクノロジー・カンパニー・エルエルシー | 医用画像作成装置及びプログラム |
| JP5689591B2 (ja) | 2009-06-01 | 2015-03-25 | 株式会社東芝 | 超音波診断装置及び超音波画像処理プログラム |
| AU2010265891B2 (en) * | 2009-06-26 | 2016-06-23 | Cianna Medical, Inc. | Apparatus, systems, and methods for localizing markers or tissue structures within a body |
| US8934684B2 (en) | 2009-07-31 | 2015-01-13 | Siemens Aktiengesellschaft | Method and system for facilitating an image guided medical procedure |
| EP2329786A2 (en) * | 2009-10-01 | 2011-06-08 | Navotek Medical Ltd. | Guided surgery |
| US9366772B2 (en) * | 2009-11-05 | 2016-06-14 | Exxonmobil Upstream Research Company | Method for creating a hierarchically layered earth model |
| JP5680110B2 (ja) * | 2010-02-01 | 2015-03-04 | クリア−カット メディカル エル・ティー・ディー | 体外サンプルの断端評価 |
| US8774481B2 (en) * | 2010-03-25 | 2014-07-08 | Emory University | Atlas-assisted synthetic computed tomography using deformable image registration |
| US8594401B2 (en) * | 2010-03-30 | 2013-11-26 | The Johns Hopkins University | Automated characterization of time-dependent tissue change |
| CN102906784B (zh) | 2010-05-19 | 2016-05-11 | 皇家飞利浦电子股份有限公司 | 处理样本图像 |
| JP5559642B2 (ja) * | 2010-08-30 | 2014-07-23 | 富士フイルム株式会社 | 手術支援装置、手術支援方法および手術支援プログラム |
| US20120078088A1 (en) * | 2010-09-28 | 2012-03-29 | Point of Contact, LLC. | Medical image projection and tracking system |
| US9192422B2 (en) * | 2011-07-19 | 2015-11-24 | Covidien Lp | System and method of matching impedances of an electrosurgical generator and/or a microwave generator |
| US9824440B2 (en) * | 2012-11-20 | 2017-11-21 | Vanderbilt University | Methods and systems for three-dimensional real-time intraoperative surgical margin evaluation of tumor tissues |
| WO2015035178A2 (en) * | 2013-09-06 | 2015-03-12 | Brigham And Women's Hospital, Inc. | System and method for a tissue resection margin measurement device |
| CN107949337A (zh) * | 2015-06-12 | 2018-04-20 | 达特默斯大学托管会 | 引导组织切除的系统和方法 |
-
2013
- 2013-01-16 BR BR112014017144A patent/BR112014017144A8/pt not_active Application Discontinuation
- 2013-01-16 US US14/372,286 patent/US10204415B2/en not_active Expired - Fee Related
- 2013-01-16 CN CN201380005550.6A patent/CN104067313B/zh not_active Expired - Fee Related
- 2013-01-16 EP EP13706736.9A patent/EP2805304B1/en active Active
- 2013-01-16 JP JP2014551721A patent/JP6259772B2/ja not_active Expired - Fee Related
- 2013-01-16 RU RU2014133533A patent/RU2014133533A/ru not_active Application Discontinuation
- 2013-01-16 WO PCT/IB2013/050385 patent/WO2013108182A1/en active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| BR112014017144A8 (pt) | 2017-07-04 |
| CN104067313A (zh) | 2014-09-24 |
| US20140363063A1 (en) | 2014-12-11 |
| JP2015504737A (ja) | 2015-02-16 |
| EP2805304B1 (en) | 2019-10-09 |
| US10204415B2 (en) | 2019-02-12 |
| EP2805304A1 (en) | 2014-11-26 |
| CN104067313B (zh) | 2019-02-01 |
| RU2014133533A (ru) | 2016-03-20 |
| WO2013108182A1 (en) | 2013-07-25 |
| BR112014017144A2 (pt) | 2017-06-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6259772B2 (ja) | イメージング装置 | |
| US11412985B2 (en) | Biopsy guidance by image-based X-ray system and photonic needle | |
| JP5701615B2 (ja) | 電磁トラッキング及び光針による生検誘導 | |
| RU2544465C2 (ru) | Алгоритм для консоли фотонной иглы | |
| JP6045916B2 (ja) | 組織識別能力を持つ介入的な切除デバイス | |
| JP6188829B2 (ja) | 光学的にガイドされる真空補助生検装置 | |
| EP2744398B1 (en) | Detection apparatus for determining a state of tissue | |
| CN106793948B (zh) | 侧视肺部活检装置 | |
| US20160030022A1 (en) | Optical Biopsy Needle and Endoscope System | |
| US20210045721A1 (en) | Surgical instrument and surgical system | |
| JP6198731B2 (ja) | エネルギー適用計画装置 | |
| US10605736B2 (en) | Optical pathology systems and methods |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160115 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160115 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20161025 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20161028 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20170124 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20170214 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170330 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170627 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20170925 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20171113 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20171205 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20171211 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6259772 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |