JP5407980B2 - Fluorine-containing polyether compound and method for producing the same - Google Patents
Fluorine-containing polyether compound and method for producing the same Download PDFInfo
- Publication number
- JP5407980B2 JP5407980B2 JP2010071441A JP2010071441A JP5407980B2 JP 5407980 B2 JP5407980 B2 JP 5407980B2 JP 2010071441 A JP2010071441 A JP 2010071441A JP 2010071441 A JP2010071441 A JP 2010071441A JP 5407980 B2 JP5407980 B2 JP 5407980B2
- Authority
- JP
- Japan
- Prior art keywords
- fluorine
- polyether compound
- bromotetrafluoroethoxy
- compound
- containing polyether
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Landscapes
- Polyethers (AREA)
Description
本発明は、含フッ素ポリエーテル化合物およびその製造方法に関する。さらに詳しくは、高分子主鎖両末端に反応活性部位を有する含フッ素ポリエーテル化合物およびその製造方法に関する。 The present invention relates to a fluorine-containing polyether compound and a method for producing the same. More specifically, the present invention relates to a fluorine-containing polyether compound having a reactive site at both ends of a polymer main chain and a method for producing the same.
分子末端に官能基を有する含フッ素ポリエーテル化合物としては、例えば一般式
で表わされる化合物が知られている(特許文献1参照)。
As the fluorine-containing polyether compound having a functional group at the molecular end, for example, a general formula
Is known (see Patent Document 1).
また、上記化合物の主鎖構造をオリゴマー化したより一般的な化合物として、一般式
で表わされる化合物が知られている(特許文献2参照)。
Further, as a more general compound obtained by oligomerizing the main chain structure of the above compound, a general formula
Is known (see Patent Document 2).
これらの一般式で表わされる化合物群は、Si-H基を分子内に複数個有する含フッ素オルガノ水素シロキサン化合物および白金化合物触媒により硬化し、非常に優れた特性(耐薬品性、耐熱性、低温特性)を有するエラストマー性成形物を与え得るとされ、特に-50℃程度の低温条件下でも柔軟性を失わずに、使用に耐え得るとされる。また、これらを主成分とする硬化性組成物は、抜群の成形加工性を有し、RIM成形も可能とさせる。しかしながら、この硬化物は、分子内架橋構造にシロキサン結合を有するため、フッ化水素などの酸性物質が存在する条件下で使用されると、化学的劣化によりそれの機械的な強度が低下するなどの好ましくない結果を与えることもある。 The compounds represented by these general formulas are cured by a fluorine-containing organohydrogensiloxane compound having a plurality of Si-H groups in the molecule and a platinum compound catalyst, and have excellent properties (chemical resistance, heat resistance, low temperature It is said that an elastomeric molded product having characteristics) can be provided, and in particular, it can be used without loss of flexibility even under a low temperature condition of about -50 ° C. Moreover, the curable composition which has these as a main component has outstanding moldability, and also enables RIM molding. However, since this cured product has a siloxane bond in its intramolecular cross-linked structure, its mechanical strength decreases due to chemical degradation when used under conditions where acidic substances such as hydrogen fluoride are present. May give undesirable results.
本発明者は先に、Si-H結合を有する含フッ素オルガノ水素シロキサン化合物を必要としないで硬化可能であり、その上耐熱性、低温特性および成形加工性に優れ、しかも酸性条件下での使用に耐え得る硬化物を与える含フッ素ポリエーテル化合物として、一般式
(ここで、R1は水素原子、炭素数1〜3のアルキル基またはフェニル基であり、Xはヨウ素原子または臭素原子であり、Xのフェニル基上の置換位置はNR1結合置換基に対してm-またはp-位であり、lおよびmはそれぞれ独立に10以上の整数であり、l+mは30〜130である)で表わされる含フッ素ポリエーテル化合物を提案している(特許文献3参照)。
The present inventor previously can cure without the need for a fluorine-containing organohydrogensiloxane compound having a Si—H bond, and is excellent in heat resistance, low temperature characteristics and moldability, and used under acidic conditions. As a fluorine-containing polyether compound that gives a cured product that can withstand
(Wherein R 1 is a hydrogen atom, an alkyl group having 1 to 3 carbon atoms or a phenyl group, X is an iodine atom or a bromine atom, and the substitution position on the phenyl group of X is relative to the NR 1 bond substituent. M- or p-position, l and m are each independently an integer of 10 or more, and l + m is 30 to 130) (Patent Document) 3).
この含フッ素ポリエーテル化合物は、ボロン酸エステル化合物により硬化し、エラストマー性成形物を与えることができるが、より一般的な架橋方法である過酸化物架橋には不適である。 This fluorine-containing polyether compound can be cured with a boronic acid ester compound to give an elastomeric molded product, but is not suitable for peroxide crosslinking, which is a more general crosslinking method.
本発明の目的は、高分子主鎖両末端により反応性にすぐれたハロゲノアルコキシ基を有し、過酸化物架橋が可能な含フッ素ポリエーテル化合物およびその製造方法を提供することにある。 An object of the present invention is to provide a fluorine-containing polyether compound having a halogenoalkoxy group having excellent reactivity at both ends of a polymer main chain and capable of peroxide crosslinking, and a method for producing the same.
本発明によって、一般式〔I〕
(ここで、R1は水素原子、炭素数1〜3のアルキル基またはフェニル基であり、Xは臭素原子またはヨウ素原子であり、lおよびmはそれぞれ独立に10以上の整数であり、l+mは30〜200である)で表わされる含フッ素ポリエーテル化合物が提供される。
According to the present invention, the general formula [I]
(Wherein R 1 is a hydrogen atom, an alkyl group having 1 to 3 carbon atoms or a phenyl group, X is a bromine atom or an iodine atom, l and m are each independently an integer of 10 or more, and l + m is 30 to 200).
かかる含フッ素ポリエーテル化合物は、一般式〔II〕
(ここで、lおよびmはそれぞれ独立に10以上の整数であり、l+mは30〜200である)で表わされる含フッ素ジカルボン酸フルオリド化合物を、一般式〔III〕
(ここで、R1は水素原子、炭素数1〜3のアルキル基またはフェニル基であり、R2は水素原子またはトリメチルシリル基であり、Xは臭素原子またはヨウ素原子である)で表わされるアニリン化合物と、好ましくはピリジンまたはトリエチルアミン等の3級アミン化合物の存在下で、反応させることにより製造される。
Such a fluorine-containing polyether compound has the general formula [II]
(Wherein l and m are each independently an integer of 10 or more, and l + m is 30 to 200), a fluorine-containing dicarboxylic acid fluoride compound represented by the general formula [III]
Where R 1 is a hydrogen atom, an alkyl group having 1 to 3 carbon atoms or a phenyl group, R 2 is a hydrogen atom or a trimethylsilyl group, and X is a bromine atom or an iodine atom. And preferably in the presence of a tertiary amine compound such as pyridine or triethylamine.
本発明に係る含フッ素ポリエーテル化合物は、高分子主鎖両末端に反応部位として2-ブロモテトラフルオロエトキシ基または2-ヨードテトラフルオロエトキシ基を有しているので、有機過酸化物による過酸化物架橋を可能とし、過酸化物架橋によりエラストマー性成形物を与えることができる。かかる組成物を硬化して得られる成形物は、低温特性、耐薬品性などにすぐれているため、自動車燃料供給系シール材、オイルシール材、航空機燃料系および油圧系シール材、半導体製造装置シール材等の各種用途に好適に使用される。 The fluorine-containing polyether compound according to the present invention has a 2-bromotetrafluoroethoxy group or a 2-iodotetrafluoroethoxy group as a reactive site at both ends of the polymer main chain. The product can be crosslinked, and an elastomeric molded product can be obtained by peroxide crosslinking. Molded products obtained by curing such compositions are excellent in low-temperature characteristics, chemical resistance, etc., so that they are excellent in automobile fuel supply system seal materials, oil seal materials, aircraft fuel systems and hydraulic system seal materials, and semiconductor manufacturing equipment seals. It is suitably used for various applications such as materials.
本発明の含フッ素ポリエーテル化合物
において、lおよびmはそれぞれ独立に10以上の整数であり、l+mは30〜200の整数である。特に、エラストマー性高分子材料の主原料として用いる場合には、硬化後十分な機械的強度を有する成形物を得るために、l+mは50〜150であることが好ましい。R1は水素原子、炭素数1〜3のアルキル基またはフェニル基である。なお、R1がアルキル基またはフェニル基の場合、分子間水素結合の形成が妨げられることにより、含フッ素ポリエーテル化合物の粘度を低下させることができる。
Fluorinated polyether compound of the present invention
In the formula, l and m are each independently an integer of 10 or more, and l + m is an integer of 30 to 200. In particular, when used as a main raw material for an elastomeric polymer material, l + m is preferably 50 to 150 in order to obtain a molded product having sufficient mechanical strength after curing. R 1 is a hydrogen atom, an alkyl group having 1 to 3 carbon atoms, or a phenyl group. In the case where R 1 is an alkyl group or a phenyl group, the viscosity of the fluorinated polyether compound can be lowered by preventing the formation of intermolecular hydrogen bonds.
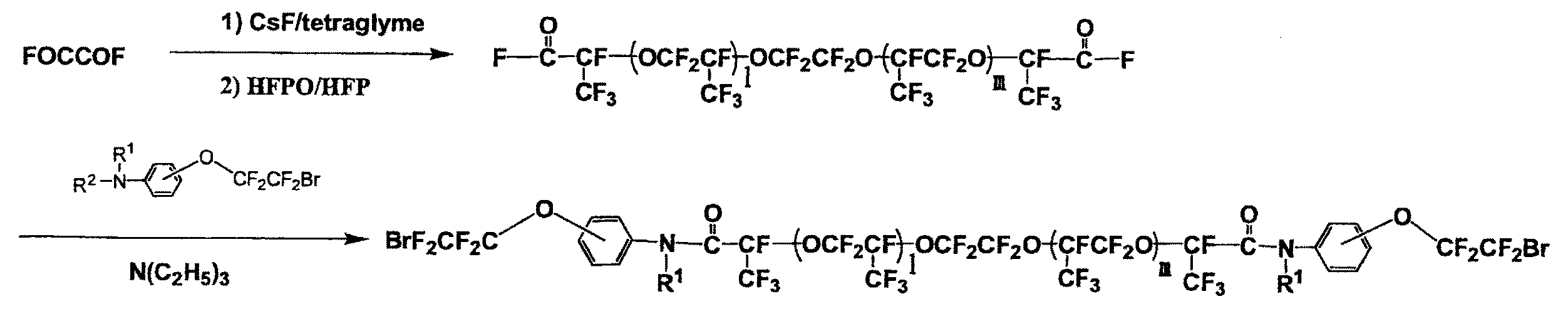
本発明の含フッ素ポリエーテル化合物(X=Br)は、例えば以下のような一連の工程を経て製造することができる。
注) HFPO:ヘキサフルオロプロペンオキシド
HFP:ヘキサフルオロプロペン
The fluorine-containing polyether compound (X = Br) of the present invention can be produced, for example, through the following series of steps.
Note) HFPO: Hexafluoropropene oxide
HFP: Hexafluoropropene
第二工程で用いられるアニリン化合物〔III〕において、R1は水素原子、炭素数1〜3のアルキル基またはフェニル基であり、R2は水素原子またはトリメチルシリル基である。また、2-ブロモテトラフルオロエトキシ基(BrCF2CF2O-)のベンゼン環上の置換位置は、アミノ基(-NR1 -)に対してo-、m-またはp-位である。アニリン化合物〔III〕の具体例としては、2-(2-ブロモテトラフルオロエトキシ)アニリン、3-(2-ブロモテトラフルオロエトキシ)アニリン、4-(2-ブロモテトラフルオロエトキシ)アニリン、2-(2-ブロモテトラフルオロエトキシ)-N-メチルアニリン、3-(2-ブロモテトラフルオロエトキシ)-N-メチルアニリン、4-(2-ブロモテトラフルオロエトキシ)-N-メチルアニリンまたはこれらのN-トリメチルシリル誘導体等が挙げられる。なお、2-ブロモテトラフルオロエトキシ基の末端臭素原子はヨウ素原子であってもかまわない。 In the aniline compound [III] used in the second step, R 1 is a hydrogen atom, an alkyl group having 1 to 3 carbon atoms or a phenyl group, and R 2 is a hydrogen atom or a trimethylsilyl group. The substitution position on the benzene ring of the 2 -bromotetrafluoroethoxy group (BrCF 2 CF 2 O—) is the o-, m-, or p-position with respect to the amino group (—NR 1 − ). Specific examples of the aniline compound [III] include 2- (2-bromotetrafluoroethoxy) aniline, 3- (2-bromotetrafluoroethoxy) aniline, 4- (2-bromotetrafluoroethoxy) aniline, 2- ( 2-bromotetrafluoroethoxy) -N-methylaniline, 3- (2-bromotetrafluoroethoxy) -N-methylaniline, 4- (2-bromotetrafluoroethoxy) -N-methylaniline or their N-trimethylsilyl Derivatives and the like. The terminal bromine atom of the 2-bromotetrafluoroethoxy group may be an iodine atom.
かかるアニリン化合物〔III〕において、1級アニリン化合物は、特許文献4および非特許文献1に記載されているように、アセトアミドフェノールまたはヒドロキシ安息香酸メチルに、1,2-ジブロモテトラフルオロエタンを反応させた後、数工程を経て製造することができる。また、2級アニリン化合物は、1級アニリン化合物を、ジアルキル硫酸またはヨウ化アルキル等のアルキル化剤によりN-アルキル化することによって、製造することができる。なお、この場合にはN-アルキル化体の他にN,N-ジアルキル化体が副生するので、分離・精製が必要である。 In the aniline compound [III], the primary aniline compound is prepared by reacting 1,2-dibromotetrafluoroethane with acetamidophenol or methyl hydroxybenzoate as described in Patent Document 4 and Non-Patent Document 1. After that, it can be manufactured through several steps. The secondary aniline compound can be produced by N-alkylating the primary aniline compound with an alkylating agent such as dialkyl sulfuric acid or alkyl iodide. In this case, an N, N-dialkylated product is produced as a by-product in addition to the N-alkylated product, and thus separation and purification are necessary.
N-モノアルキル化のより好ましい方法は、非特許文献2および3に記載されている選択的なN-モノアルキル化である。具体的には、1級アニリン化合物を、2-ニトロベンゼンスルホニルクロリドまたは2,4-ジニトロベンゼンスルホニルクロリドと反応させ、スルホンアミド化した後、ヨウ化アルキル等によりN-アルキル化し、その後チオフェノールまたはメルカプト酢酸と反応させることにより、目的とする2級アニリン化合物を選択的に得ることができる。 A more preferable method of N-monoalkylation is the selective N-monoalkylation described in Non-Patent Documents 2 and 3. Specifically, a primary aniline compound is reacted with 2-nitrobenzenesulfonyl chloride or 2,4-dinitrobenzenesulfonyl chloride, sulfonamidated, then N-alkylated with alkyl iodide or the like, and then thiophenol or mercapto. By reacting with acetic acid, the desired secondary aniline compound can be selectively obtained.
含フッ素ジカルボン酸フルオリド〔II〕とアニリン化合物〔III〕との反応は、ピリジン等の活性水素を有しない塩基性含窒素複素環式化合物またはトリエチルアミン等の3級アミン化合物の存在下で、ハイドロクロロフルオロカーボン、ハイドロフルオロカーボン、ハイドロフルオロエーテル等の含フッ素溶媒、またはこれらの含フッ素溶媒と非プロトン性非フッ素系溶媒との混合溶媒中で、-50〜150℃、好ましくは0〜100℃の反応温度で行われる。含フッ素溶媒の具体例としては、HCFC-225、HFE-449(住友3M製品HFE7100)、HFE-569(住友3M製品HFE-7200)、1,3-ビス(トリフルオロメチル)ベンゼン等が挙げられる。非プロトン性非フッ素系溶媒としては、ジエチルエーテル、ジイソプロピルエーテル、シクロペンチルメチルエーテル、テトラヒドロフラン、ジオキサン等が挙げられる。アニリン化合物〔III〕の溶解性を考慮すると、含フッ素溶媒と非プロトン性非フッ素系溶媒の混合溶媒を用いるのがより好ましい。 The reaction between the fluorine-containing dicarboxylic acid fluoride [II] and the aniline compound [III] is carried out in the presence of a basic nitrogen-containing heterocyclic compound having no active hydrogen such as pyridine or a tertiary amine compound such as triethylamine. In a fluorine-containing solvent such as fluorocarbon, hydrofluorocarbon, hydrofluoroether, or a mixed solvent of these fluorine-containing solvent and aprotic non-fluorine solvent, a reaction temperature of -50 to 150 ° C, preferably 0 to 100 ° C Done in Specific examples of the fluorine-containing solvent include HCFC-225, HFE-449 (Sumitomo 3M product HFE7100), HFE-569 (Sumitomo 3M product HFE-7200), 1,3-bis (trifluoromethyl) benzene, and the like. . Examples of the aprotic non-fluorinated solvent include diethyl ether, diisopropyl ether, cyclopentyl methyl ether, tetrahydrofuran, dioxane and the like. Considering the solubility of the aniline compound [III], it is more preferable to use a mixed solvent of a fluorinated solvent and an aprotic non-fluorinated solvent.
本発明の含フッ素ポリエーテル化合物の具体例として、
またはこれらに対応するヨウ素化物等が例示される。
As a specific example of the fluorine-containing polyether compound of the present invention,
Or the iodinated thing etc. corresponding to these are illustrated.
本発明に係る含フッ素ポリエーテル化合物は、有機過酸化物によって過酸化物架橋せしめることができる。過酸化物架橋に際しては、多官能性不飽和化合物を併用することが好ましい。 The fluorine-containing polyether compound according to the present invention can be peroxide-crosslinked with an organic peroxide. In peroxide crosslinking, it is preferable to use a polyfunctional unsaturated compound in combination.
有機過酸化物としては、例えば2,5-ジメチル-2,5-ジ(第3ブチルパーオキシ)ヘキサン、2,5-ジメチル-2,5-ジ(第3ブチルパーオキシ)ヘキシン-3、2,5-ジメチル-2,5-ジ(ベンゾイルパーオキシ)ヘキサン、ベンゾイルパーオキシド、ジ第3ブチルパーオキシド、第3ブチルクミルパーオキシド、第3ブチルパーオキシベンゼン、1,1-ビス(第3ブチルパーオキシ)-3,5,5-トリメチルシクロヘキサン、2,5-ジメチルヘキサン-2,5-ジヒドロキシパーオキシド、ジクミルパーオキシド等が、含フッ素ポリエーテル化合物100重量部当り約0.1〜5重量部、好ましくは約0.1〜2重量部の割合で用いられる。 Examples of the organic peroxide include 2,5-dimethyl-2,5-di (tert-butylperoxy) hexane, 2,5-dimethyl-2,5-di (tert-butylperoxy) hexyne-3, 2,5-dimethyl-2,5-di (benzoylperoxy) hexane, benzoyl peroxide, di-tert-butyl peroxide, tert-butyl cumyl peroxide, tert-butyl peroxybenzene, 1,1-bis (3 butyl peroxy) -3,5,5-trimethylcyclohexane, 2,5-dimethylhexane-2,5-dihydroxy peroxide, dicumyl peroxide, etc. is about 0.1 to 5 per 100 parts by weight of the fluorinated polyether compound. Part by weight, preferably about 0.1 to 2 parts by weight is used.
また、多官能性不飽和化合物としては、例えばトリアリルイソシアヌレート、トリアリルシアヌレート、トリアクリルホルマール、トリアリルトリメリテート等が、含フッ素ポリエーテル化合物100重量部に対し約0.1〜10重量部、好ましくは約0.5〜5重量部の割合で用いられる。 In addition, as the polyfunctional unsaturated compound, for example, triallyl isocyanurate, triallyl cyanurate, triacryl formal, triallyl trimellitate and the like are about 0.1 to 10 parts by weight with respect to 100 parts by weight of the fluorine-containing polyether compound. , Preferably about 0.5 to 5 parts by weight.
含フッ素ポリエーテル化合物の硬化は、これに有機過酸化物、好ましくは有機過酸化物と多官能性不飽和化合物の両者を加え、さらに必要に応じてカーボンブラック、シリカ等の補強剤その他を加え、約100〜180℃で約5〜30分間圧縮成形し、必要に応じて約150〜250℃で約5〜24時間程度オーブン加硫することにより行われる。なお、成形は、RIM成形によっても可能である。 To cure the fluorine-containing polyether compound, an organic peroxide, preferably both an organic peroxide and a polyfunctional unsaturated compound, is added, and a reinforcing agent such as carbon black or silica is added as necessary. It is performed by compression molding at about 100 to 180 ° C. for about 5 to 30 minutes and, if necessary, oven vulcanization at about 150 to 250 ° C. for about 5 to 24 hours. The molding can also be performed by RIM molding.
次に、実施例について本発明を説明する。 Next, the present invention will be described with reference to examples.
参考例1
4-(2-ブロモテトラフルオロエトキシ)-N-メチルアニリンの合成
(1) 4-ヒドロキシ安息香酸メチル100g(0.657モル)およびメタノール300mlからなる溶液に、反応容器を氷水で冷却しながら、水酸化カリウム(純度85%)43.4g(0.657モル)を少量ずつ加え、さらに3時間反応を継続した。減圧下でメタノールを除去した後、140℃、27Paで8時間減圧乾燥した。4-ヒドロキシ安息香酸メチルのカリウム塩が、無色の固体として119g(収率95%)得られた。
(2) 4-ヒドロキシ安息香酸メチルのカリウム塩50g(0.26モル)をジメチルスルホキシド150mlに溶解した溶液中に、窒素雰囲気下、60℃で、1,2-ジブロモテトラフルオロエタン89g(0.34モル)を1時間かけて滴下した。滴下終了後、さらに70℃、2時間および90℃、30分間の反応を行った。反応混合物を室温に冷却した後水150mlを加え、ジクロロメタンで生成物を抽出した。その後、通常の後処理を行い粗生成物を84g得た。これを減圧蒸留することで、4-(2-ブロモテトラフルオロエトキシ)安息香酸メチル(沸点75〜77℃、13Pa)を、無色の液体として81g(収率93%)得た。
(3) 4-(2-ブロモテトラフルオロエトキシ)安息香酸メチル70g(0.211モル)およびメタノール100mlからなる溶液に、水酸化カリウム(純度85%)18.1g(0.274モル)およびメタノール100mlからなるアルカリ溶液を室温条件下で加え、さらに4時間反応を継続した。得られた溶液に、水110mlおよび濃塩酸43gを加え、内容物を十分に混合した。遊離した生成物をジエチルエーテルで抽出し、その後通常の後処理を行い、4-(2-ブロモテトラフルオロエトキシ)安息香酸を、無色の固体として65.8g(収率98%)得た。
(4) 4-(2-ブロモテトラフルオロエトキシ)安息香酸65.6g(0.207モル)、塩化チオニル32.1g(0.270モル)、ジメチルホルムアミド2.0g(0.027モル)およびクロロホルム160mlからなる混合物を、50℃で2時間反応させた。減圧下でクロロホルムおよび未反応の塩化チオニルを留去した後、さらに残渣を減圧蒸留した。4-(2-ブロモテトラフルオロエトキシ)ベンゾイルクロリド(沸点68〜72℃、9Pa)を、無色の液体として67.3g(収率97%)得た。
(5) 4-(2-ブロモテトラフルオロエトキシ)ベンゾイルクロリド67.3g(0.201モル)およびテトラヒドロフラン200mlからなる溶液に、アジ化ナトリウム43.1g(0.663モル)および水140mlからなる水溶液を、反応容器を氷水で冷却しながら加えた。1.5時間反応を継続した後水200mlを加え、生成物をジクロロメタンで抽出した。その後通常の後処理を行い、〔4-(2-ブロモテトラフルオロエトキシ)フェニル〕アジドメタノンを、無色の液体として67.8g(収率99%)得た。
(6) 〔4-(2-ブロモテトラフルオロエトキシ)フェニル〕アジドメタノン67.7g(0.198モル)およびトルエン溶媒650mlからなる溶液を、100℃で1.5時間反応させた。熱分解反応によるアジドメタノンからのイソシアナト基への変換は、クルチウス反応として進行する。減圧下でトルエンを留去し、次いで残渣を減圧蒸留した。4-イソシアナト-(2-ブロモテトラフルオロエトキシ)ベンゼン(沸点54〜56℃、33Pa)を無色の液体として53.8g(収率87%)得た。
(7) 4-イソシアナト-(2-ブロモテトラフルオロエトキシ)ベンゼン41.3g(0.132モル)、濃塩酸74mlおよび1,2-ジメトキシエタン150mlからなる混合物を、80℃で2時間反応させた。得られた反応混合物に、水酸化カリウム(純度85%)56gおよび水500mlからなるアルカリ水溶液を加えた。生成物をジエチルエーテルで抽出し、次いで通常の後処理を行った。さらに減圧蒸留を行い、4-(2-ブロモテトラフルオロエトキシ)アニリン(沸点65〜68℃、53Pa)を、無色の液体として33.6g(収率88%)得た。
(8) 4-(2-ブロモテトラフルオロエトキシ)アニリン41.6g(144ミリモル)、ピリジン16.3g(207ミリモル)およびクロロホルム250mlからなる溶液に、2-ニトロベンゼンスルホニルクロリド38.1g(172ミリモル)を加え、1時間室温条件下で反応させた。通常の反応後処理により、N-〔4-(2-ブロモテトラフルオロエトキシ)フェニル〕-2-ニトロベンゼンスルホンアミドを、橙色の固体として66.9g(収率98%)得た。
(9) N-〔4-(2-ブロモテトラフルオロエトキシ)フェニル〕-2-ニトロベンゼンスルホンアミド66.9g(141ミリモル)、炭酸カリウム97g(705ミリモル)およびジメチルホルムアミド400mlからなる溶液にヨウ化メチル26g(183ミリモル)を加え、室温条件下で2時間反応を行った。通常の反応後処理を行い、N-メチル-N-〔4-(2-ブロモテトラフルオロエトキシ)フェニル〕-2-ニトロベンゼンスルホンアミドを、黄色の固体として68.4g(収率99%)得た。
(10) N-メチル-N-〔4-(2-ブロモテトラフルオロエトキシ)フェニル〕-2-ニトロベンゼンスルホンアミド55.5g(114ミリモル)、水酸化リチウム・1水和物19.1g(456ミリモル)およびジメチルホルムアミド400mlからなる溶液に、メルカプト酢酸21.0g(228ミリモル)を加え、60℃で2時間反応させた。通常の反応後処理を行った後、反応生成物を蒸留し、4-(2-ブロモテトラフルオロエトキシ)-N-メチルアニリン(沸点60〜67℃、13Pa)を、淡黄色の液体として28.5g(収率83%)得た。
Reference example 1
Synthesis of 4- (2-bromotetrafluoroethoxy) -N-methylaniline
(1) To a solution consisting of 100 g (0.657 mol) of methyl 4-hydroxybenzoate and 300 ml of methanol, 43.4 g (0.657 mol) of potassium hydroxide (purity 85%) was added little by little while cooling the reaction vessel with ice water. The reaction was continued for another 3 hours. After removing methanol under reduced pressure, it was dried under reduced pressure at 140 ° C. and 27 Pa for 8 hours. 119 g (95% yield) of potassium salt of methyl 4-hydroxybenzoate was obtained as a colorless solid.
(2) In a solution of 50 g (0.26 mol) of potassium 4-hydroxybenzoate in 150 ml of dimethyl sulfoxide, 89 g (0.34 mol) of 1,2-dibromotetrafluoroethane was added at 60 ° C. in a nitrogen atmosphere. It was added dropwise over 1 hour. After completion of dropping, the reaction was further carried out at 70 ° C. for 2 hours and 90 ° C. for 30 minutes. The reaction mixture was cooled to room temperature, 150 ml of water was added, and the product was extracted with dichloromethane. Thereafter, usual post-treatment was performed to obtain 84 g of a crude product. This was distilled under reduced pressure to obtain 81 g (yield: 93%) of methyl 4- (2-bromotetrafluoroethoxy) benzoate (boiling point: 75-77 ° C., 13 Pa) as a colorless liquid.
(3) Alkaline solution consisting of 70 g (0.211 mol) of methyl 4- (2-bromotetrafluoroethoxy) benzoate and 100 ml of methanol and 18.1 g (0.274 mol) of potassium hydroxide (purity 85%) and 100 ml of methanol Was added at room temperature and the reaction was continued for another 4 hours. To the obtained solution, 110 ml of water and 43 g of concentrated hydrochloric acid were added, and the contents were mixed well. The liberated product was extracted with diethyl ether, and then subjected to usual work-up to obtain 65.8 g (yield 98%) of 4- (2-bromotetrafluoroethoxy) benzoic acid as a colorless solid.
(4) A mixture of 65.6 g (0.207 mol) 4- (2-bromotetrafluoroethoxy) benzoic acid, 32.1 g (0.270 mol) thionyl chloride, 2.0 g (0.027 mol) dimethylformamide and 160 ml chloroform was prepared at 50 ° C. The reaction was performed for 2 hours. After distilling off chloroform and unreacted thionyl chloride under reduced pressure, the residue was further distilled under reduced pressure. 67.3 g (yield 97%) of 4- (2-bromotetrafluoroethoxy) benzoyl chloride (boiling point 68-72 ° C., 9 Pa) was obtained as a colorless liquid.
(5) To a solution consisting of 67.3 g (0.201 mol) 4- (2-bromotetrafluoroethoxy) benzoyl chloride and 200 ml tetrahydrofuran, an aqueous solution consisting of 43.1 g (0.663 mol) sodium azide and 140 ml water was added. It was added while cooling. After continuing the reaction for 1.5 hours, 200 ml of water was added, and the product was extracted with dichloromethane. Thereafter, usual post-treatment was performed to obtain 67.8 g (yield 99%) of [4- (2-bromotetrafluoroethoxy) phenyl] azidomethanone as a colorless liquid.
(6) A solution comprising 67.7 g (0.198 mol) of [4- (2-bromotetrafluoroethoxy) phenyl] azidomethanone and 650 ml of toluene solvent was reacted at 100 ° C. for 1.5 hours. Conversion from azidomethanone to an isocyanato group by pyrolysis proceeds as a Curtius reaction. Toluene was distilled off under reduced pressure, and then the residue was distilled under reduced pressure. 53.8 g (yield 87%) of 4-isocyanato- (2-bromotetrafluoroethoxy) benzene (boiling point 54-56 ° C., 33 Pa) was obtained as a colorless liquid.
(7) A mixture consisting of 41.3 g (0.132 mol) of 4-isocyanato- (2-bromotetrafluoroethoxy) benzene, 74 ml of concentrated hydrochloric acid and 150 ml of 1,2-dimethoxyethane was reacted at 80 ° C. for 2 hours. To the obtained reaction mixture, an alkaline aqueous solution consisting of 56 g of potassium hydroxide (purity 85%) and 500 ml of water was added. The product was extracted with diethyl ether and then subjected to normal workup. Further, distillation under reduced pressure was carried out to obtain 33.6 g (yield 88%) of 4- (2-bromotetrafluoroethoxy) aniline (boiling point 65 to 68 ° C., 53 Pa) as a colorless liquid.
(8) To a solution consisting of 41.6 g (144 mmol) of 4- (2-bromotetrafluoroethoxy) aniline, 16.3 g (207 mmol) of pyridine and 250 ml of chloroform, 38.1 g (172 mmol) of 2-nitrobenzenesulfonyl chloride was added, The reaction was performed at room temperature for 1 hour. The usual post-reaction treatment gave 66.9 g (98% yield) of N- [4- (2-bromotetrafluoroethoxy) phenyl] -2-nitrobenzenesulfonamide as an orange solid.
(9) N- [4- (2-bromotetrafluoroethoxy) phenyl] -2-nitrobenzenesulfonamide 66.9 g (141 mmol), potassium carbonate 97 g (705 mmol) and dimethylformamide 400 ml (183 mmol) was added and the reaction was allowed to proceed for 2 hours at room temperature. After usual reaction post-treatment, 68.4 g (99% yield) of N-methyl-N- [4- (2-bromotetrafluoroethoxy) phenyl] -2-nitrobenzenesulfonamide was obtained as a yellow solid.
(10) N-methyl-N- [4- (2-bromotetrafluoroethoxy) phenyl] -2-nitrobenzenesulfonamide 55.5 g (114 mmol), lithium hydroxide monohydrate 19.1 g (456 mmol) and To a solution consisting of 400 ml of dimethylformamide was added 21.0 g (228 mmol) of mercaptoacetic acid and reacted at 60 ° C. for 2 hours. After carrying out the usual post-reaction treatment, the reaction product was distilled to give 4- (2-bromotetrafluoroethoxy) -N-methylaniline (boiling point 60-67 ° C., 13 Pa) as a pale yellow liquid, 28.5 g (Yield 83%).
参考例2
含フッ素ジカルボン酸フルオリド化合物の調製
攪拌装置、温度センサ、ガス導入口およびドライアイス/エタノール冷却凝縮器を備えた内容量1Lのガラス製反応容器を低温恒温槽に設置し、ジアルコキシド化合物 CsOCF2CF(CF3)OCF2CF2OCF(CF3)CF2OCs を23ミリモルを含むテトラグライム溶液60gを仕込んだ。内温を-33〜-30℃に調整した後、ガス導入口よりヘキサフルオロプロペンを40g仕込んだ。次に、ヘキサフルオロプロペンオキシドを10g/hr、ヘキサフルオロプロペンを4g/hrの供給速度で反応容器内に仕込んだ。42時間経過後、ガスの供給を停止し(ヘキサフルオロプロペンオキシド総仕込量428g)、さらに1時間-33〜-30℃に内温を保った。減圧下でヘキサフルオロプロペンを反応系内より除去した後、室温までゆっくり昇温した。さらに100℃まで昇温し、減圧下でヘキサフルオロプロペンオリゴマーを反応混合物より除去した。このようにして、フッ化セシウム、テトラグライムおよび含フッ素ジカルボン酸フルオリドからなる混合物を淡黄色粘稠な懸濁液として478g得た。これを精製せずに、次の工程に用いた。
Reference example 2
Preparation of fluorinated dicarboxylic acid fluoride compounds
A 1-liter glass reaction vessel equipped with a stirrer, temperature sensor, gas inlet, and dry ice / ethanol cooled condenser is placed in a low-temperature thermostatic chamber, and the dialkoxide compound CsOCF 2 CF (CF 3 ) OCF 2 CF 2 60 g of a tetraglyme solution containing 23 mmol of OCF (CF 3 ) CF 2 OCs was charged. After adjusting the internal temperature to -33 to -30 ° C, 40 g of hexafluoropropene was charged from the gas inlet. Next, hexafluoropropene oxide was charged into the reaction vessel at a feed rate of 10 g / hr and hexafluoropropene at 4 g / hr. After 42 hours, the gas supply was stopped (total amount of hexafluoropropene oxide charged: 428 g), and the internal temperature was kept at -33 to -30 ° C for 1 hour. After removing hexafluoropropene from the reaction system under reduced pressure, the temperature was slowly raised to room temperature. The temperature was further raised to 100 ° C., and the hexafluoropropene oligomer was removed from the reaction mixture under reduced pressure. Thus, 478 g of a mixture composed of cesium fluoride, tetraglyme and fluorine-containing dicarboxylic acid fluoride was obtained as a pale yellow viscous suspension. This was used in the next step without purification.
また、上記混合物の一部をメタノールによりジエステル体〔A〕とした後、19F-NMRによりヘキサフルオロプロペンオキシド数平均重合度および二官能性比(ヘキサフルオロプロペンオキシドオリゴマー〔B〕とのモル分率)を求めた。
s=Fa(-131ppm)ピーク積分値
t=Fb(-133ppm)ピーク積分値
u=Fc(-146ppm)ピーク積分値
注) ケミカルシフトはCFCl3基準
二官能性比=(t/s-0.5)/(t/s+0.5)=0.89
ヘキサフルオロプロペンオキシド数平均重合度=4u/(2t+s)=102
Further, after a part of the above mixture was converted to a diester form [A] with methanol, the number average polymerization degree of hexafluoropropene oxide and the bifunctional ratio (mole fraction with hexafluoropropene oxide oligomer [B] were determined by 19 F-NMR. Rate).
s = F a (-131ppm) Peak integrated value
t = F b (-133ppm) Peak integral value
u = F c (-146ppm) peak integral value
Note) Chemical shift is based on CFCl 3 Bifunctional ratio = (t / s-0.5) / (t / s + 0.5) = 0.89
Hexafluoropropene oxide number average degree of polymerization = 4u / (2t + s) = 102
実施例
参考例2で得られた含フッ素ジカルボン酸フルオリド、フッ化セシウムおよびテトラグライムからなる混合物78g(約4.5ミリモル)を、含フッ素系溶媒(住友3M製品HFE-7100)90mlに溶解し、そこにトリエチルアミン1.9g(19ミリモル)およびジエチルエーテル36mlを加えた。そこに、4-(2-ブロモテトラフルオロエトキシ)-N-メチルアニリン4.0g(13ミリモル)を加え、30℃で3時間反応を行った。得られた反応混合物を飽和食塩水に加え、分離した有機層を1.5重量%水酸化カリウム水溶液で洗浄した後、無水硫酸マグネシウムで乾燥、ロ過した。減圧下でロ液から含フッ素系溶媒およびジエチルエーテルを留去した後、得られた粘稠な液体をジエチルエーテルで数回洗浄し、次いで減圧下でジエチルエーテルを完全に留去した。このようにして、含フッ素ポリエーテル化合物
を、僅かに黄色味を帯びた透明な液体として65g得た。E型粘度計(東機産業製TEV-22)により粘度を測定したところ、14Pa・s(25℃)であった。
19F-NMR(ケミカルシフトはCFCl3基準): -125ppm(Fb)
-147ppm(Fc)
-72ppm(Fd)
-90ppm(Fe)
1H-NMR(ケミカルシフトはTMS基準): 7.0ppm(Ha,Hb)
3.1ppm(Hc)
IR(neat): 1704cm-1(C=O)
1508cm-1(Ar)
Example 78 g (about 4.5 mmol) of a mixture comprising fluorine-containing dicarboxylic acid fluoride, cesium fluoride and tetraglyme obtained in Reference Example 2 was dissolved in 90 ml of a fluorine-containing solvent (Sumitomo 3M product HFE-7100). To this was added 1.9 g (19 mmol) of triethylamine and 36 ml of diethyl ether. 4- (2-Bromotetrafluoroethoxy) -N-methylaniline (4.0 g, 13 mmol) was added thereto, and the reaction was performed at 30 ° C. for 3 hours. The obtained reaction mixture was added to saturated brine, and the separated organic layer was washed with 1.5 wt% aqueous potassium hydroxide solution, dried over anhydrous magnesium sulfate and filtered. After distilling off the fluorine-containing solvent and diethyl ether from the filtrate under reduced pressure, the resulting viscous liquid was washed several times with diethyl ether, and then diethyl ether was completely distilled off under reduced pressure. Thus, a fluorine-containing polyether compound
65 g were obtained as a slightly yellowish transparent liquid. When the viscosity was measured with an E-type viscometer (TEV-22 manufactured by Toki Sangyo), it was 14 Pa · s (25 ° C.).
19 F-NMR (chemical shift based on CFCl 3 ): -125 ppm (F b )
-147ppm (F c )
-72ppm (F d )
-90ppm (F e )
1 H-NMR (chemical shift is based on TMS): 7.0 ppm (H a , H b )
3.1ppm (H c)
IR (neat): 1704cm -1 (C = O)
1508cm -1 (Ar)
参考例3
実施例で得られた含フッ素ポリエーテル化合物 100重量部
2,5-ジメチル-2,5-ジ(第3ブチルパーオキシ)ヘキサン 1 〃
トリアリルイソシアヌレート 3 〃
アセチレンカーボンブラック 13 〃
以上の各成分をプラネタリーミキサを用いて混合し、硬化性組成物を調製した。
Reference example 3
100 parts by weight of the fluorinated polyether compound obtained in the examples
2,5-dimethyl-2,5-di (tert-butylperoxy) hexane 1〃
Triallyl isocyanurate 3 〃
Acetylene carbon black 13 〃
The above components were mixed using a planetary mixer to prepare a curable composition.
この硬化性組成物について、モンサントディスクレオメーターを使用して、150℃、30分間の硬化挙動を測定し、次のような結果を得た。
ML 0.6 dN・m
MH 6.0 dN・m
t10 1.4 分
t50 6.6 分
t90 20.4 分
This curable composition was measured for curing behavior at 150 ° C. for 30 minutes using a Monsanto disc rheometer, and the following results were obtained.
ML 0.6 dN ・ m
MH 6.0 dN ・ m
t 10 1.4 minutes
t 50 6.6 min
t 90 20.4 min
さらに、150℃で30分間圧縮成形してP24 Oリングを成形し、次いで、80℃、5時間および230℃、15時間のオーブン加硫(二次加硫)を、窒素雰囲気下で行った。これについて、圧縮永久歪(ASTM D395 Method B準拠;200℃、70時間)の測定を行い、50%という値を得た。 Further, a P24 O-ring was formed by compression molding at 150 ° C. for 30 minutes, and then oven vulcanization (secondary vulcanization) at 80 ° C. for 5 hours and 230 ° C. for 15 hours was performed in a nitrogen atmosphere. The compression set (according to ASTM D395 Method B; 200 ° C., 70 hours) was measured and a value of 50% was obtained.
また、このP24 Oリングのガラス転移温度Tgを、示差走査熱量分析計(SIIナノテクノロジー社製DSC6220)を用いて測定すると、-55℃という値が得られた。 Further, when the glass transition temperature Tg of the P24 O-ring was measured using a differential scanning calorimeter (DSC6220 manufactured by SII Nanotechnology), a value of −55 ° C. was obtained.
Claims (5)
(ここで、R1は水素原子、炭素数1〜3のアルキル基またはフェニル基であり、Xは臭素原子またはヨウ素原子であり、lおよびmはそれぞれ独立に10以上の整数であり、l+mは30〜200である)で表わされる含フッ素ポリエーテル化合物。 General formula [I]
(Wherein R 1 is a hydrogen atom, an alkyl group having 1 to 3 carbon atoms or a phenyl group, X is a bromine atom or an iodine atom, l and m are each independently an integer of 10 or more, and l + m is 30 to 200).
(ここで、lおよびmはそれぞれ独立に10以上の整数であり、l+mは30〜200である)で表わされる含フッ素ジカルボン酸フルオリド化合物を、一般式〔III〕
(ここで、R1は水素原子、炭素数1〜3のアルキル基またはフェニル基であり、R2は水素原子またはトリメチルシリル基であり、Xは臭素原子またはヨウ素原子である)で表わされるアニリン化合物と反応させることを特徴とする請求項1記載の含フッ素ポリエーテル化合物の製造方法。 General formula [II]
(Wherein l and m are each independently an integer of 10 or more, and l + m is 30 to 200), a fluorine-containing dicarboxylic acid fluoride compound represented by the general formula [III]
Where R 1 is a hydrogen atom, an alkyl group having 1 to 3 carbon atoms or a phenyl group, R 2 is a hydrogen atom or a trimethylsilyl group, and X is a bromine atom or an iodine atom. The method for producing a fluorine-containing polyether compound according to claim 1, wherein
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010071441A JP5407980B2 (en) | 2010-03-26 | 2010-03-26 | Fluorine-containing polyether compound and method for producing the same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010071441A JP5407980B2 (en) | 2010-03-26 | 2010-03-26 | Fluorine-containing polyether compound and method for producing the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2011202055A JP2011202055A (en) | 2011-10-13 |
| JP5407980B2 true JP5407980B2 (en) | 2014-02-05 |
Family
ID=44879040
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010071441A Expired - Fee Related JP5407980B2 (en) | 2010-03-26 | 2010-03-26 | Fluorine-containing polyether compound and method for producing the same |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5407980B2 (en) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9758470B2 (en) | 2013-08-09 | 2017-09-12 | Unimatec Co., Ltd. | Bis(perfluoroether carboxylic acid alkyl)amino ester and method for producing the same |
| US10000444B2 (en) | 2015-02-03 | 2018-06-19 | Unimatec Co., Ltd. | Fluorine-containing ether monocarboxylic acid aminoalkyl ester and a method for producing the same |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5099123B2 (en) * | 2007-04-06 | 2012-12-12 | ユニマテック株式会社 | Fluorine-containing polyether compound, process for producing the same, and curable composition containing the same |
| JP5169247B2 (en) * | 2008-01-25 | 2013-03-27 | ユニマテック株式会社 | Method for producing curable fluorine-containing polyether composition |
| US7977510B2 (en) * | 2008-05-19 | 2011-07-12 | Unimatec Co., Ltd. | Fluorine-containing polyether compound and process for producing the same |
-
2010
- 2010-03-26 JP JP2010071441A patent/JP5407980B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2011202055A (en) | 2011-10-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5099123B2 (en) | Fluorine-containing polyether compound, process for producing the same, and curable composition containing the same | |
| JP2012041557A (en) | Fluoroelastomer | |
| KR102128542B1 (en) | Crosslinking agent and fluorine-containing aromatic compound | |
| JP5098460B2 (en) | Fluorine-containing polyether compound, process for producing the same, and curable composition containing the same | |
| US20090318650A1 (en) | Novel fluorine-containing polymer and method of producing fluorine-containing polymer | |
| JP2019534847A (en) | Bisflanged halide, bisflanged halide production method, and bisfuran diacid, bisflangol or bisflangamine production method using bisflanged halide | |
| JP2011213837A (en) | Fluorine-containing polyether compound, method for producing the same, and curable composition containing the same | |
| CN103524658B (en) | Fluoroelastomer | |
| JP5099141B2 (en) | Fluorine-containing polyether compound and method for producing the same | |
| JP5407980B2 (en) | Fluorine-containing polyether compound and method for producing the same | |
| JP5790423B2 (en) | Fluorine-containing polyether compound and process for producing the same | |
| JP5092502B2 (en) | Fluoric acid fluoride compounds | |
| JP5757189B2 (en) | Thermosetting fluorine-containing polyether compound and method for producing the same | |
| JP2011213837A5 (en) | ||
| CN113950505B (en) | Hydroxy-functional triazine compounds, curable fluoropolymer compositions comprising such compounds, and cured articles made therefrom | |
| JP2009001771A (en) | Fluorine-containing polyether compound, method for producing the same and curable composition containing the same | |
| JP5194525B2 (en) | Fluorine-containing polyether compound, process for producing the same, and curable composition containing the same | |
| JP5194536B2 (en) | Fluorine-containing polyether compound, process for producing the same, and curable composition containing the same | |
| JP5895454B2 (en) | ω-Iodoperfluoroalkyl-substituted aniline derivative and process for producing the same | |
| JP2009173780A (en) | Manufacturing method of curable fluorine-containing polyether composition | |
| JP5663926B2 (en) | Trifluorovinyloxy-N-monoalkylaniline compound and method for producing the same | |
| JP2021535261A (en) | Peroxide curable hyperfluorinated polymer containing internal fluorinated plasticizer and articles from it | |
| CA2736551A1 (en) | Fluoroolefin iodide mixture and method for producing the same | |
| JP5918678B2 (en) | Method for producing dibenzyltrithiocarbonate derivative | |
| RU2621343C1 (en) | 2-[4'-(2",6"-dimethylphenoxy)benzoyl]benzoic acid and the method of preparation of the invention |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130212 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130920 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20131008 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20131021 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5407980 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |