JP5345929B2 - 環状アルファ−コノトキシンペプチド - Google Patents
環状アルファ−コノトキシンペプチド Download PDFInfo
- Publication number
- JP5345929B2 JP5345929B2 JP2009504526A JP2009504526A JP5345929B2 JP 5345929 B2 JP5345929 B2 JP 5345929B2 JP 2009504526 A JP2009504526 A JP 2009504526A JP 2009504526 A JP2009504526 A JP 2009504526A JP 5345929 B2 JP5345929 B2 JP 5345929B2
- Authority
- JP
- Japan
- Prior art keywords
- peptide
- conotoxin
- terminus
- cyclic
- pain
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/12—Cyclic peptides, e.g. bacitracins; Polymyxins; Gramicidins S, C; Tyrocidins A, B or C
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/02—Drugs for disorders of the urinary system of urine or of the urinary tract, e.g. urine acidifiers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
- A61P25/10—Antiepileptics; Anticonvulsants for petit-mal
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
- A61P25/12—Antiepileptics; Anticonvulsants for grand-mal
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
- A61P25/34—Tobacco-abuse
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Pain & Pain Management (AREA)
- Psychiatry (AREA)
- Immunology (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Epidemiology (AREA)
- Urology & Nephrology (AREA)
- Addiction (AREA)
- Zoology (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Vascular Medicine (AREA)
- Psychology (AREA)
- Rheumatology (AREA)
- Hospice & Palliative Care (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
α-コノトキシンクラスは、文献中に数百の例が記載されている非常に大きなコノトキシンペプチドのクラスである。大部分のα-コノトキシンペプチドは、対になって結合した4個のシステイン残基を有し、システイン残基IとIII、およびシステイン残基IIとIVの間で2個のジスルフィド結合を形成するA-スーパーファミリーのメンバーである。文献中に記載されているα-コノトキシンペプチドの一部の例を以下の表1に示す。
Xaa1 CCS Xaa2 P Xaa3 C Xaa4 Xaa5 Xaa6 Xaa7 Xaa8 Xaa9 Xaa10 C 配列番号1
(配列中、Xaa1はグリシンまたはアスパラギン酸であり、Xaa2からXaa7は任意の天然または非天然アミノ酸を表し、Xaa8はプロリン、ヒドロキシプロリンまたはグルタミンを表し、Xaa9はアスパラギン酸、グルタミン酸またはγ-カルボキシグルタミン酸を表し、Xaa10は任意の天然または非天然アミノ酸を表すか、なくてもよい)。
Xaa1はグリシンまたはアスパラギン酸であり、
Xaa2はアスパラギン酸、アスパラギン、ヒスチジン、チロシン、アルギニンまたはリシンから、さらにより好ましくはアスパラギン酸、アスパラギン、およびヒスチジン、最も好ましくはアスパラギン酸から選択され、
Xaa3はアルギニン、プロリン、アラニン、バリンまたはセリン、より好ましくはアルギニン、プロリンまたはアラニン、最も好ましくはアルギニンから選択され、
Xaa4はアスパラギン、アラニン、アルギニン、チロシン、ヒスチジン、フェニルアラニン、セリン、イソロイシンまたはリシン、より好ましくはアスパラギン、アラニンまたはチロシン、および最も好ましくはアスパラギンから選択され、
Xaa5はチロシン、ヒスチジン、アラニン、バリン、グルタミン、グリシン、ロイシン、セリン、チオニン、アスパラギン、アスパラギン酸、グルタミン酸、リシンまたはアルギニン、より好ましくは親水性アミノ酸残基、および最も好ましくはチロシンから選択され、
Xaa6はアスパラギン酸、アスパラギン、セリン、チロシン、グルタミン酸、グリシン、アルギニンまたはヒスチジン、より好ましくはアスパラギン酸またはアスパラギン、および最も好ましくはアスパラギン酸から選択され、
Xaa7はヒスチジン、アスパラギンまたはチロシン、より好ましくはヒスチジンから選択され、
Xaa8はプロリン、ヒドロキシプロリン、グルタミンまたはセリン、より好ましくはプロリンから選択され、
Xaa9はグルタミン酸、γ-カルボキシグルタミン酸、アスパラギン酸、グリシンまたはアスパラギン、より好ましくはグルタミン酸、γ-カルボキシグルタミン酸、および最も好ましくはグルタミン酸から選択され、
Xaa10はイソロイシン、チロシン、ロイシンまたはdes-Xaa10、より好ましくはイソロイシンから選択される。
Xaa1はグリシンまたはアスパラギン酸であり、
Xaa2はアスパラギン酸であり、
Xaa3はアルギニンであり、
Xaa4はアスパラギンであり、
Xaa5はチロシンであり、
Xaa6はアスパラギン酸であり、
Xaa7はヒスチジンであり、
Xaa8はプロリンであり、
Xaa9はグルタミン酸であり、
Xaa10はイソロイシンである。
このアプローチでは、伸長された直鎖ペプチドが、固相ペプチド合成法を使用して「on resin」で最初に合成される。この伸長直鎖ペプチドは、新たな連結部分を含むN末端とC末端伸長部の、またはその近くのシステイン残基から始まる天然配列を含む。固相合成は実際には逆の順序で、すなわち、伸長直鎖ペプチドのC末端で開始する。樹脂からの切断後、伸長コノトキシンはチオエステル中間体に環化され、続いてアミド環状ペプチドに再配置される。この還元ペプチドは次に酸化されてジスルフィド結合を形成する。環化に関する反応の概略図を図1に示す。樹脂(R)へのリンカーが付着したまま、直鎖ペプチドを樹脂から切断した。Rはペプチドと樹脂間のリンカーに相当し、環化で使用される連結部分とは異なる。第1の反応は、N末端システインのチオールとカルボキシ末端との間のチオエステルの形成を伴う。これは次に、S、Nアシル基転移を受け、天然ペプチド結合を有する環状ペプチドを形成する。
このアプローチでは、固相ペプチド合成を使用して伸長ペプチドをアセンブルする。伸長直鎖ペプチドは、Nおよび/またはC末端に付加された追加の残基を有する天然コノトキシン配列を含む。(新しい)N末端とC末端は、好ましくはグリシン残基とするべきである。ペプチドは折り畳まれ、コノトキシン様ペプチドの場合、折り畳まれた分子の両末端は一般に間隙を介してすぐそばにある。このことは、標準的な化学反応を使用した溶液中でのペプチドの環化を容易にする。配列中に多数のリシン、グルタミン酸またはアスパラギン酸残基が存在する場合は問題が起こりうるので、そのときは方法1が好ましい。
この方法では、出発物質は成熟コノトキシンである。ペプチドリンカーは、ペプチドライゲーションに関する公開された手順を使用して、コノトキシンを用いて合成および連結される。伸長ペプチドは次いで環化および酸化される。
本発明を、いくつかの環状コノトキシンペプチドの生成およびその生物活性を説明する添付の実施例および図を参照して、以下に説明する。しかしながら、以下の説明の独自性は、本発明の前述の説明の一般性に取ってかわるものではないことが理解されるべきである。
(a)設計および合成
天然MIIペプチドのN末端とC末端をつなぐために必要なリンカーの大きさは、周知の分子モデリング法を使用して決定した。MIIの3次元モデルは、Protein Data Bank (PDB)からダウンロードした。分子モデリングプログラムAccelrys (Insight II Modeling Environment、2000年リリース、サンディエゴ、Accelrys社 2001年)を使用して、適切なリンカーの長さを決定した。つまり、N末端とC末端間にアミノ酸リンカーを組み込み、次いで親コノトキシン構造の立体構造をロックし、簡易なエネルギー最小化を行った。次いで、親コノトキシンの立体構造をロック解除し、ペプチド構造全体を再度最小化した。リンカーの大きさが小さすぎるモデルは、天然構造を乱さない長さのリンカーを有するものよりもエネルギーが高い構造をもたらす。最小で5残基を含有するリンカーが、N末端とC末端をつなぐために必要とされることが決定された。そのため、N末端グリシンに加えて、5(GGAAG)、6(GGAAGG)、および7(GGAGAAG)残基のリンカーを含有するペプチドを合成した。これは、6〜8残基にわたるシステイン間の全長に相当する。距離の測定によって、リンカー中の各残基が約2.0〜2.4オングストローム(これは、約3.5オングストロームにわたるであろう、つまり緩んだ立体構造を表す伸長立体構造よりも短いことに注意されたい)にわたる必要となることが明らかになった。大きな、または高度に官能化されたアミノ酸残基と比較して、天然ペプチドの他の残基と相互作用しにくい、またはフォールディングを阻害しにくい小さな側鎖を有する比較的不活性なアミノ酸であるため、グリシンおよびアラニンをリンカーアミノ酸に選択した。
チオエステルリンカーを利用するin situ中和と一緒にBOC/HBTU化学反応を使用して、ペプチドを合成した(Schnolzerら、(1992) Int. J. Pept. Protein Res. 40、180〜193頁; Dawsonら、(1994) Science 266、776〜9頁; Tamら、(1999) J. Am. Chem. Soc. 121、4316〜4324頁; Yan, L.Z.およびDawson, P.E. (2001) J Am Chem Soc 123、526〜33頁)。
次いで、3つの秩序だったアナログ(これよりcMII-5、cMII-6およびcMII-7と称する)について、2次元NMRスペクトルデータを得た。NMR完全帰属を行い、HαおよびHNプロトンの化学シフトを天然MIIのものと比較した。化学シフトデータの比較により、これらの構造がいかに類似しているかが示された。結果により、cMII-5の化学シフトがMIIのものとほとんど一致せず、構造の変化を示したことが明らかとなった。対照的に、cMII-6およびcMII-7の化学シフトは、天然コノトキシンのものと高度に相関性があった。このことは、cMII-6およびcMII-7が天然MIIに類似の構造を採用し、cMII-5が天然の構造から明らかに逸脱していることを示す。
非選択的酸化が、環状コノトキシンの合成で使用される好ましい方法であるが、cMII-6について例証した特異的ジスルフィド結合形成を使用して製造することもできる。ペプチドは前述のように合成したが、システイン3および16の側鎖をAcm基で保護した。ペプチドを樹脂から切断し、前述の条件を使用して精製および酸化/環化した。第2のジスルフィド結合を、I2を使用した脱保護/酸化によって、3および16位のシステイン間に選択的に形成した。ペプチド(20mg)を、1mg/mLの濃度で50%酢酸水溶液に溶解し、フラスコを窒素でフラッシュした。フラスコへ、2mLの1M HCl、続いて十分量の50%酢酸水溶液中の0.1M I2(約1mL)を加え溶液を淡黄色にした。次いで反応物を窒素下、室温で1.5時間撹拌した。反応混合物が無色になるまで1Mアスコルビン酸を加えることにより、反応をクエンチした。次いで、混合物を緩衝液Aで希釈し、RP-HPLCにより精製し、完全に酸化された環状ペプチドを得た。このペプチドはcMII-6と共溶出され、したがって天然ペプチドのジスルフィド連結性、すなわちCys2-Cys8およびCys3-Cys16(1-3、2-4)に対応するとしてcMII-6のジスルフィド連結性を確認した。
クロム親和細胞をウシ副腎から調製し、標準的な文献の手順に記載のとおり24ウェルプレート(Nunc)に維持した[Lawrence, G.W.、Weller, U.およびDolly, J.O. (1994) Eur J Biochem 222、325〜33頁; Meunier, F.A.、Mattei, C.、Chameau, P.、Lawrence, G.、Colasante, C.、Kreger, A.S.、Dolly, J.O.およびMolgo, J. (2000) J Cell Sci 113 (Pt 7)、1119〜25頁; Meunier, F.A.、Feng, Z.P.、Molgo, J.、Zamponi, G.W.およびSchiavo, G. (2002) Embo J 21、6733-43頁]。無傷細胞を緩衝液A(mM): NaCl、145; KCl、5、Na2HPO4、1.2;グルコース、10; HEPES-NaOH、20(pH7.4)で簡単に1回洗い、天然および環状コノトキシンと一緒に20分間、2mM CaCl2の存在下でインキュベートし、ニコチン(5μM)で20分間刺激した。各実験の最後に上清のアリコートを採取し、細胞を1%(v/v)Triton X-100(Shigma)で溶解させた。両方のサンプルの組を、カテコールアミンについて蛍光分析により試験し、放出量を文献中に記載のように対照の割合として表した(上記参照)。
cMII-6およびcMII-7のタンパク質分解酵素による作用に対する安定性を、ペプチドをエンドプロティナーゼGlu-C(Endo Glu-C)と一緒にインキュベートすることにより試験した。MII、cMII-6およびcMII-7は、末端(MIIの場合)およびリンカー(cMII-6およびcMII-7の場合)の対面に同じプロセシング部位を有する可能性がある。ペプチドを、20μg/mLの濃度で0.1M NH4HCO3(pH8.0)緩衝液に溶解させた。次いで、Endo GluCを50:1のペプチド:酵素比(wt/wt)で加え、溶液を37℃でインキュベートした。アリコート(3μL)を抜き取り、0〜10の毎時間5%ギ酸(57μL)でクエンチした。次いで、サンプルをLC/MSにより分析し、各時点において残存する無傷のペプチド量を測定した。各試験は、適切な陽性(Endo GluC切断点を有する直鎖の非ジスルフィドペプチド)および陰性(酵素を含まない緩衝液中のペプチド)対照を用いて3連で行った。
タンパク質分解作用に対するcMII-6およびcMII-7の抵抗性を試験し、これをMIIと比較するために、これらのコノトキシンをヒト血漿中でインキュベートした。MII、cMII-6およびcMII-7(10μM)を、50%ヒト血漿中で24時間インキュベートした。いくつかの時点でアリコートを採取し、15%トリクロロ酢酸水溶液でクエンチし、遠心分離機にかけた。次いで上清をRP-HPLCにより分析した。
(a)Vc1.1の設計
α-コノトキシンVc1.1は、MIIを含むα-コノトキシンの4/7クラスのメンバーであり、疼痛治療の可能性を有する(Sandall DW、Satkunanathan N、Keays DA、Polidano MA、Liping X、Pham V、Down .JG、Khalil Z、Livett BG、Gayler KR、Biochemistry 2003 42(22):6904〜11頁)。文献中にVc1.1の利用できる構造データがなかったので、環状MIIアナログの設計のための前述の手順に従うことができなかった。しかしながら、この同じ骨格を有する他のコノトキシンが構造的に研究されていたため、Vc1.1のリンカーの最適な長さを、MIIおよびPnIAを含む同じファミリーの他のメンバーの距離の簡易測定により推定した。Protein Data Bankには、重複構造、およびN末端に伸長された柔軟性の「テール」を有するコノトキシンGIDを除いて、4つのα4/7コノトキシン構造がある。これらの4つの化合物のこれらの構造のN末端とC末端間の距離を平均することにより得た値は、よく一致していた(12.2±0.8Å)。後に、Vc1.1の3次元構造が報告され(Clarkら、J. Biol. Chem. (2006) 281 23254-23263頁)、Vc1.1のN末端とC末端間の距離は、11.9±0.5Åであり、α4/7コノトキシンのこの算出された平均の範囲内に入ることが明らかになった。したがって、環状Vc1.1に適したリンカーの長さは、環状MIIに使用されるものと同様、例えば6〜7残基であろうと推定することができる。この場合もまた、これらの6残基を既存のグリシン残基のN末端に付加する。
環状Vc1.1の合成を、環状MII(実施例1)について記載した合成手順を使用して行った。環状Vc1.1に使用した環化/酸化緩衝液は、0.1M NH4HCO3(pH8.1)であった。環化/酸化により1種の優勢な異性体(これよりcVc1.1-6と称する)が生じ、これを精製し、1H NMR分光法により分析した。Vc1.1(C末端がアミド化されている)およびcVc1.1-6の配列を以下に示す。
Vc1.1を、TCEPと一緒にクエン酸緩衝液中、低pHでインキュベートすることにより部分的に還元した。反応混合物をRP-HPLCにより精製し、1つのジスルフィド種をN-エチルマレイミドでアルキル化した。次いで、アルキル化されたペプチドを完全に還元し、MS/MSにより分析した。MS/MSデータは、C2およびC8がN-エチルマレイミドでアルキル化されたことをはっきりと示した。ペプチド鎖の両末端からのフラグメンテーションパターンを観察すると、そのパターンは推定アルキル化パターンを完全に支持した。したがって、Vc1.1のジスルフィド連結性はC2-C8およびC3-C16であるという結論に達した。これは、他のα-コノトキシンに見られるI-III、II-IVジスルフィド結合パターンに一致する。
cVc1.1-6の生物活性を、環状MIIの実施例で記載したように、ウシ副腎クロム親和細胞からのカテコールアミン放出を測定することにより分析した。cVc1.1-6活性が直鎖Vc1.1の活性と実験誤差の範囲内で等しいことを例証する試験結果を図7に示す。
cVc1.1-6がタンパク質分解酵素による攻撃に抵抗する能力を、環状MIIについて概説した実験を使用して評価することができる。哺乳動物の胃液および血漿中での分解に対する抵抗性もまた、実施例1で示した手順を使用して評価することができる。
AChに誘導される電流のVc1.1抑制を、種々のnAChRサブユニットの組合せを発現するアフリカツメガエル卵母細胞において調べた。Achに誘発される応答を10分毎に調べ、毒素を4分間、溶液添加した後、アゴニストと毒素を同時適用した。Vc1.1(10μM)は、中枢型nAChRサブタイプであるα4β2およびα4β4、または骨格筋型nAChRサブタイプであるαβγδ(n=7〜12)のいずれかが仲介する、AChに誘発される電流を抑制できなかった。同様に、10μM Vc1.1は、ホモ五量体ニューロンnAChRであるα7(n=11)が仲介するAChに誘発される電流をわずか14±2%しか抑制しなかった。しかしながら、10μM Vc1.1は、末梢nAChRサブタイプα3β2およびα3β4を同程度、それぞれ対照の58±7%(n=8)および56±7%(n=12)抑制した。α3α5β2(n=7)のnAChRの組合せにα5サブユニットを加えると、同様の有効性が観察されたが、Vc1.1は5倍以上低いα3α5β4(n=15)抑制の有効性を示した。AChに誘導される電流の大きさは、nAChRサブタイプα3α6β2(n=13)を含有するα6で、30μM Vc1.1によって約50%しか抑制されなかった。100nM以下の濃度でVc1.1を溶液添加しても、AChに誘発される電流を遮断せず、α3含有nAChRに対して検出可能な応答すら(すなわち50nAより大きい)導くこともなかった。
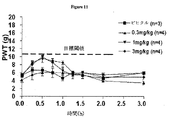
よく定義された神経因性疼痛モデル(CCIラット)を使用して、皮下(s.c.)および経口ボーラス投与により投与された場合のVc1.1およびcVc1.1-6の抗異痛(疼痛緩和)作用を比較するために、試験を行った。
CCIラットにおけるcVc1.1-6の単回経口ボーラス投与の抗異痛有効性を実証するために、試験を行った。
Claims (7)
- 遊離N末端およびC末端を有さないようなアミド環状骨格を有する少なくとも1種の合成環状α-コノトキシンペプチドを、医薬として経口投与に適したビヒクル中に含む経口医薬製剤であって、前記ペプチドは、システイン残基IとIIIの間の1つのジスルフィド結合、および、システイン残基IIとIVの間の1つのジスルフィド結合である、2個のジスルフィド結合を形成するように対になって結合した4個のシステイン残基を含み、
対応する直鎖/非環状α-コノトキシンペプチドのN末端はペプチドリンカーを介してC末端に連結されており、
対応する直鎖/非環状α-コノトキシンペプチドが、リンカーがシステイン残基IとIVの間に7個のアミノ酸残基が存在するように選択されるVc1.1(配列番号5)である、
医薬製剤。 - リンカーが、直鎖α-コノトキシン中にすでに存在する任意のアミノ酸残基に加えてグ
リシンおよび/またはアラニン残基からなる、請求項1に記載の医薬製剤。 - 疼痛の治療または予防のための経口投与用の医薬の製造における請求項1に定義された
合成環状α-コノトキシンペプチドの使用。 - 疼痛が神経因性疼痛である、請求項4に記載の使用。
- 疼痛が糖尿病性神経因性疼痛である、請求項5に記載の使用。
- 疼痛が炎症性疼痛である、請求項4に記載の使用。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2006901976A AU2006901976A0 (en) | 2006-04-13 | Cyclised a-Conotoxin Peptides | |
| AU2006901976 | 2006-04-13 | ||
| AU2006236006 | 2006-11-15 | ||
| AU2006236006A AU2006236006B2 (en) | 2006-04-13 | 2006-11-15 | Cyclised a-conotoxin peptides |
| PCT/AU2007/000439 WO2007118270A1 (en) | 2006-04-13 | 2007-04-03 | Cyclised alpha-conotoxin peptides |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2009533355A JP2009533355A (ja) | 2009-09-17 |
| JP2009533355A5 JP2009533355A5 (ja) | 2012-10-04 |
| JP5345929B2 true JP5345929B2 (ja) | 2013-11-20 |
Family
ID=38608961
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009504526A Expired - Fee Related JP5345929B2 (ja) | 2006-04-13 | 2007-04-03 | 環状アルファ−コノトキシンペプチド |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US8354372B2 (ja) |
| EP (1) | EP2015766B1 (ja) |
| JP (1) | JP5345929B2 (ja) |
| AU (1) | AU2006236006B2 (ja) |
| WO (1) | WO2007118270A1 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9284358B2 (en) | 2006-07-18 | 2016-03-15 | University Of Utah Research Foundation | Conotoxin peptides |
| EP2051726B1 (en) * | 2006-07-18 | 2018-04-18 | University of Utah Research Foundation | Methods for treating pain and screening analgesic compounds |
| CN101381403B (zh) * | 2008-09-17 | 2011-03-16 | 中国人民解放军军事医学科学院生物工程研究所 | α型芋螺多肽衍生物及其应用 |
| EP2379087B1 (en) * | 2008-12-19 | 2014-08-20 | DePuy Synthes Products, LLC | Umbilical cord tissue derived cells for treating neuropathic pain and spasticity |
| WO2011032233A1 (en) | 2009-09-21 | 2011-03-24 | The University Of Queensland | Novel omega conotoxin peptides |
| JP6336979B2 (ja) * | 2012-08-07 | 2018-06-06 | ハイナン ユニバーシティ | α−コノトキシンペプチド、その医薬組成物及びそれらの使用 |
| BR112018016648A2 (pt) * | 2016-02-16 | 2018-12-26 | The University Of Queensland | peptídeos alfa-conotoxina |
| RU2731217C2 (ru) * | 2016-11-28 | 2020-08-31 | Общество с ограниченной ответственностью "Синейро" | Аналог альфа-конотоксина RgIA для лечения боли |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5614219A (en) * | 1991-12-05 | 1997-03-25 | Alfatec-Pharma Gmbh | Oral administration form for peptide pharmaceutical substances, in particular insulin |
| US5464633A (en) * | 1994-05-24 | 1995-11-07 | Jagotec Ag | Pharmaceutical tablets releasing the active substance after a definite period of time |
| GB9623205D0 (en) * | 1996-11-07 | 1997-01-08 | Eurand Int | Novel pharmaceutical compositions |
| US5866682A (en) | 1997-05-15 | 1999-02-02 | University Of Utah Research Foundation | Conopeptides AuIA, AuIB and AuIC |
| WO1999059535A1 (en) * | 1998-05-15 | 1999-11-25 | Unilever Plc | Oral composition comprising capsules |
| AUPP589598A0 (en) | 1998-09-14 | 1998-10-08 | University Of Queensland, The | Novel peptides |
| US7316819B2 (en) * | 2001-03-08 | 2008-01-08 | Unigene Laboratories, Inc. | Oral peptide pharmaceutical dosage form and method of production |
| AUPR409401A0 (en) * | 2001-03-29 | 2001-04-26 | University Of Melbourne, The | Analgesic compound |
| EP1919506A1 (en) | 2005-08-02 | 2008-05-14 | Metabolic Pharmaceuticals Ltd. | Peptide conjugate for oral delivery of hydrophilic peptide analgesics |
-
2006
- 2006-11-15 AU AU2006236006A patent/AU2006236006B2/en not_active Ceased
-
2007
- 2007-04-03 US US12/297,110 patent/US8354372B2/en not_active Expired - Fee Related
- 2007-04-03 EP EP07718686.4A patent/EP2015766B1/en not_active Not-in-force
- 2007-04-03 WO PCT/AU2007/000439 patent/WO2007118270A1/en active Application Filing
- 2007-04-03 JP JP2009504526A patent/JP5345929B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2009533355A (ja) | 2009-09-17 |
| US8354372B2 (en) | 2013-01-15 |
| AU2006236006B2 (en) | 2012-09-06 |
| EP2015766A1 (en) | 2009-01-21 |
| AU2006236006A1 (en) | 2007-11-01 |
| EP2015766B1 (en) | 2013-12-18 |
| WO2007118270A1 (en) | 2007-10-25 |
| US20100120670A1 (en) | 2010-05-13 |
| EP2015766A4 (en) | 2011-01-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5345929B2 (ja) | 環状アルファ−コノトキシンペプチド | |
| US10766936B2 (en) | Treatment of ischemia | |
| AU2010296994B2 (en) | Novel peptides isolated from spider venom, and uses thereof | |
| McCarthy et al. | PcTx1 affords neuroprotection in a conscious model of stroke in hypertensive rats via selective inhibition of ASIC1a | |
| US11802140B2 (en) | Treatment of ischemia | |
| CN101448516A (zh) | 环化α-芋螺毒素肽 | |
| US6265541B1 (en) | Uses of α-conotoxin peptides | |
| Kem et al. | Sea anemone toxins as templates for the design of immunosuppressant drugs | |
| EP3169344B1 (en) | Epha4 cyclic peptide antagonists for neuroprotection and neural repair | |
| US5866682A (en) | Conopeptides AuIA, AuIB and AuIC | |
| Jimenez | Post-translationally modified conopeptides: Biological activities and pharmacological applications | |
| JP2017526644A5 (ja) | ||
| WO2024149230A1 (zh) | 一种神经保护性psd-95多肽抑制剂及其应用 | |
| Mueller | Engineering an optimized analgesic from the NaV1. 7 selective spider venom peptide Pn3a | |
| Norton et al. | CALCIUM CHANNEL BLOCKING POLYPEPTIDES | |
| DE10018335A1 (de) | Raumform von TPR-Strukturmotiv enthaltenden Polypeptiden mit Chaperon-Bindungsfunktion, deren Kristalle und Verbindungen zur Inhibierung derartiger Polypeptide |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100311 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120424 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120724 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120731 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20120814 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20120814 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20121127 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130327 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20130530 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130716 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130815 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |