JP5226308B2 - 肝細胞増殖因子活性化を制御するための方法及び組成物 - Google Patents
肝細胞増殖因子活性化を制御するための方法及び組成物 Download PDFInfo
- Publication number
- JP5226308B2 JP5226308B2 JP2007523715A JP2007523715A JP5226308B2 JP 5226308 B2 JP5226308 B2 JP 5226308B2 JP 2007523715 A JP2007523715 A JP 2007523715A JP 2007523715 A JP2007523715 A JP 2007523715A JP 5226308 B2 JP5226308 B2 JP 5226308B2
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- hgf
- hepsin
- antibodies
- polypeptide
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6872—Intracellular protein regulatory factors and their receptors, e.g. including ion channels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/34—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving hydrolase
- C12Q1/37—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving hydrolase involving peptidase or proteinase
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/74—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving hormones or other non-cytokine intercellular protein regulatory factors such as growth factors, including receptors to hormones and growth factors
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/475—Assays involving growth factors
- G01N2333/4753—Hepatocyte growth factor; Scatter factor; Tumor cytotoxic factor II
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/02—Screening involving studying the effect of compounds C on the interaction between interacting molecules A and B (e.g. A = enzyme and B = substrate for A, or A = receptor and B = ligand for the receptor)
Description
本出願は、米国特許法規則1.53(b)(1)に基づき出願した非仮出願であり、米国特許法119条(e)に基づき、2004年7月26日出願の米国特許仮出願番号60/591339号の優先権を主張するものであり、その全体の開示が出典明記によりそのままここに組み込まれる。
一般的に本発明は分子生検及び成長因子制御の分野に関する。より具体的には、本発明はHGF/c-metシグナル伝達経路のモジュレータ、及び該モジュレータの使用に関する。
ヘプシン(Hepsin)(別名TMRPRSS1)は細胞表面発現型キモトリプシン様セリンプロテアーゼであり、マトリプターゼ(matriptase)(別名MT-SP1)およびエンテロペプチダーゼ(1)も含むタイプII膜貫通型セリンプロテアーゼ(TTSP)のファミリのメンバーである。第19染色体のq11-13.2に位置する(2)ヒトヘプシン遺伝子は、スカベンジャーレセプターシステイン-豊富な(SRCR)、プロテアーゼドメインから成る細胞外ドメイン(Arg45-Leu417)、膜貫通領域及び短いN末端細胞質尾部を含んでなる417のアミノ酸ポリペプチド(3)をコードする。
ヘプシン酵素前駆体は、Arg162-Ile163 (4)の切断によって、自己触媒的に活性化され、SRCRドメインにジスルフィド結合されたプロテアーゼドメイン(Cys153-Cys277)によって、ヘテロ二量体の酵素を形成する。共有結合性Cys-Cys結合に加えて、ヘプシンの最近決定された結晶構造により、SRCRとプロテアーゼドメインは、およそ1200Å2を覆い隠す各々のドメインである広い作用領域を共有していることが明らかとなった(5)。この作用領域がSRCRドメインの膜貫通の近位残基の近くに位置するので、ヘプシンプロテアーゼドメインおよび活性部位は細胞表面の近くに位置しうる(5)。これは、活性部位が膜表面のはるか上流(60−80Å)に位置する、凝固因子VIIa(FVIIa)1、IXa及びXaなどの他の細胞表面集積性セリンプロテアーゼと基本的に異なる(6-8)。
特許出願および刊行物を含む、本願明細書中のすべての引例は出典明記によりその全体が組み込まれる。
本願明細書において、記述されるように、複数の癌において、非常に過剰発現する細胞-表面タンパク質であるヘプシンの生理的基質は、それ自体が癌発生の多くの態様において、重要な役割を果たすことが知られている肝細胞増殖因子である。ヘプシンは、強力な生理学的プロHGF転換酵素であるHGFA(肝細胞増殖因子活性化因子)と同等の活性を有するプロHGFを切断することが本明細書において、示されている。ヘプシンにより生成される2鎖(活性化型) HGFは、Metチロシンリン酸化の誘導、細胞増殖の刺激及び細胞移動の刺激などの正常な生物活性を表す。加えて、2つのクーニッツ(Kunitz)ドメインインヒビターであるHAI-1BおよびHAI-2は、ヘプシン酵素活性の生理学的調節因子として、本願明細書において、特定される。本発明は、これらの所見の少なくとも一部をベースとした、さらに詳細に後述される方法および組成物を提供する。ヘプシンおよびHGF及び/又はその生理学的インヒビターとの相互作用は固有のものであり、HGF/Met(「c-met」とも称される)経路の異常又は不必要なシグナル伝達と関係する病的状態に対する予防的方法及び/又は治療的方法を設定する際の重大な微調整のための有益な標的となりうることを示す。ゆえに、本発明は、HGF活性化の調節に伴う生理学的相互作用分子の制御を介してHGF/c-met経路を制御できる物質を同定するための、及び該物質を使用するための方法、組成物、キット及び製造品を提供する。
一態様では、本発明は、HGF/c-metシグナル伝達経路を崩壊させるHGF/c-metアンタゴニストを提供する。例えば、本発明は、プロHGFのヘプシン切断(例えばR494-V495位置での切断)を阻害する分子を提供する。分子は、限定するものではないが、プロHGFのヘプシン切断が阻害されるヘプシン又はプロHGF何れかへの結合、プロHGFの切断が阻害されるヘプシン-プロHGF複合体への結合、および/またはヘプシンによるHGF切断の効果が阻害される(例えばヘプシンによる切断に続くHGFの放出の阻害)プロHGF又はヘプシンへの結合など、任意の方法でその阻害性機能を発揮してもよい。一実施態様では、本発明のアンタゴニスト分子は、c-metへのHGF結合を阻害しない。例えば、一実施態様では、アメリカ培養細胞系統保存機関寄託番号ATCC HB-11894(ハイブリドーマ1A3.3.13)又はHB-11895(ハイブリドーマ5D5.11.6)の下に寄託されるハイブリドーマ細胞株により産生される抗体と、本発明のアンタゴニスト分子は同種の抑制性及び/又は結合能力を有する抗体又はその断片でない。一実施態様では、本発明のアンタゴニスト分子は、HGF/c-met活性化と関係する生物学的活性を阻害する。
いくつかの実施態様では、本発明のアンタゴニストは本明細書に記載の発明のスクリーニング方法又は同定方法によって、得られる。
一態様では、本発明のアンタゴニスト分子は、細胞障害性剤などの毒素に結合される。これらの分子/物質は、添加物/促進剤、例えば放射線及び/又は化学療法剤と組み合わせて製剤されるか、投与されてもよい。
また、本発明は、HGF/c-metシグナル伝達中枢の調節不全と関係する疾患状態を調整するために有用な方法および組成物を提供する。ゆえに、一態様では、本発明は、被検体のc-met活性化の調節方法であって、被検体に本発明のHGF/c-metモジュレータ分子(例えば、本願明細書において、記述されるような、プロHGFのヘプシン切断を阻害するアンタゴニスト分子)が投与されることを含み、それによって、c-met活性化が調整される方法を提供する。一実施態様では、前記分子は、HGF/c-met活性を阻害するHGF/c-metアンタゴニストである。一実施態様では、前記分子は、HGF/c-met活性を増やすエンハンサー分子である。一態様では、本発明は、被検体のc-metの活性化に関する病的状態の治療方法であって、被検体に本発明のc-metアンタゴニスト(例えば本明細書に記載のヘプシンによるプロHGF切断の任意のアンタゴニスト)が投与されることを含み、それによって、c-met活性化が阻害される方法を提供する。
一態様では、本発明は、癌、腫瘍、細胞増殖性疾患、免疫性(例えば自己免疫性)疾患及び/又は血管新生関連疾患などの疾患の治療的処置及び/又は予防的処置をするための医薬の製造における本発明のアンタゴニストの使用を提供する。アンタゴニストは、抗体、抗体断片、小分子(例えば有機分子)、ポリペプチド(例えばオリゴペプチド)、核酸(例えば、アンチセンスオリゴヌクレオチド又は干渉RNAなどのオリゴヌクレオチド)、アプタマー、又はそれらの組合せを含む本願明細書に記述される任意の形態のものであってもよい。
一態様では、本発明は、癌、腫瘍、細胞増殖性疾患、免疫性(例えば自己免疫性)疾患及び/又は血管新生関連疾患(例えば創傷治癒)などの疾患の治療的処置及び/又は予防的処置をするための医薬の製造における本発明の核酸の使用を提供する。
一態様では、本発明は、癌、腫瘍、細胞増殖性疾患、免疫性(例えば自己免疫性)疾患及び/又は血管新生関連疾患(例えば創傷治癒)などの疾患の治療的処置及び/又は予防的処置をするための医薬の製造における本発明のベクターの使用を提供する。
一態様では、本発明は、癌、腫瘍、細胞増殖性疾患、免疫性(例えば自己免疫性)疾患及び/又は血管新生関連疾患(例えば創傷治癒)などの疾患の治療的処置及び/又は予防的処置をするための医薬の製造における本発明の宿主細胞の使用を提供する。
一態様では、本発明は、癌、腫瘍、細胞増殖性疾患、免疫性(例えば自己免疫性)疾患及び/又は血管新生関連疾患(創傷治癒)などの疾患の治療的処置及び/又は予防的処置をするための医薬の製造における本発明の製造品の使用を提供する。
一態様では、本発明はc-met活性化細胞増殖を阻害する方法であって、細胞又は組織と有効量の本発明のアンタゴニストとを反応させることを含み、それによって、c-met活性化に関係する細胞増殖が阻害される方法を提供する。
一態様では、本発明は被検体のc-met活性化の調節不全に関与する病理的症状を治療する方法であって、被検体に有効量の本発明のアンタゴニストが投与されることを含み、それによって、該症状が治療される方法を提供する。
一態様では、本発明は、c-met又は肝細胞増殖因子又はその両方を発現する細胞の成長を阻害する方法であって、該細胞と本発明のアンタゴニストとを反応させ、それによって、該細胞の成長が阻害されることを含む方法を提供する。一実施態様では、前記細胞は、異なる細胞により発現されるHGFと(例えば、パラ分泌を介して)反応する。
一態様では、本発明は、c-met又は肝細胞増殖因子又はその両方を発現する細胞を含有する癌性腫瘍を有する哺乳動物を治療的に処置する方法であって、該哺乳動物に有効量の本発明のアンタゴニストが投与されることを含み、それによって、該哺乳動物が有効に治療される方法を提供する。一実施態様では、前記細胞は、異なる細胞により発現されるHGFと(例えば、パラ分泌を介して)反応する。
一態様では、本発明は、細胞の成長がヘプシン、c-met及び/又は肝細胞増殖因子の成長促進効果に少なくともある程度依存している細胞の成長を阻害する方法であって、該細胞と有効量の本発明のアンタゴニストとを反応させることを含み、それによって、該細胞の成長が阻害される方法を提供する。一実施態様では、前記細胞は、異なる細胞により発現されるHGFと(例えば、パラ分泌を介して)反応する。
一態様では、本発明は、腫瘍の成長がヘプシン、c-met及び/又は肝細胞増殖因子の成長促進効果に少なくともある程度依存している哺乳動物の腫瘍を治療的に処置する方法であって、該細胞と有効量の本発明のアンタゴニストとを反応させることを含み、それによって、該腫瘍が有効に治療される方法を提供する。一実施態様では、前記細胞は、異なる細胞により発現されるHGFと(例えば、パラ分泌を介して)反応する。
本発明の方法は、さらに後処理工程を含んでもよい。例えば、一実施態様では、方法は、標的とされる細胞及び/又は組織(例えば癌細胞)が放射線治療又は化学療法剤にさらされる工程を更に含む。
本願明細書において、記述されるように、c-met活性化は、その調節不全によって、数多くの病的状態が引き起こされる、重要な生物学的工程である。したがって、本発明の方法の一実施態様では、標的とされる細胞(例えば癌細胞)は、同じ組織起源の正常細胞と比較してc-metの活性が亢進されているものである。一実施態様では、本発明の方法によって、標的とされる細胞の死が引き起こされる。例えば、本発明のアンタゴニストと反応すると、細胞死となるc-met経路を介するシグナルに対して細胞が不活性となりうる。
一態様では、本発明は、被検体に本発明のエンハンサー分子を投与することを含んでなる方法を提供する。この方法により治療される症状には、被検体のHGF/c-met活性が関与する血管新生の異常/望ましくない低生理的レベルと関係する任意の病的状態が、含まれる。このような症状の例として、創傷治癒、心肥大、心筋梗塞、肢乏血、末梢性動脈系疾患などがあるが、これに限定されるものではない。一態様では、本発明は、本発明の一つ以上のアンタゴニスト又はエンハンサーと担体を含有する組成物を提供する。一実施態様では、担体は薬学的に受容可能である。
一態様では、本発明は、本発明の核酸を含んでなるベクターを提供する。
一態様では、本発明は、本発明の核酸又はベクターを含んでなる宿主細胞を提供する。ベクターは、例えば発現ベクターなどの組換えベクターなど任意の種類のものでよい。任意の様々な宿主細胞が用いられうる。一実施態様では、宿主細胞は原核細胞、例えば大腸菌である。一実施態様では、宿主細胞は、真核細胞、例えばチャイニーズハムスター卵巣(CHO)細胞などの哺乳類の細胞である。
一態様では、本発明は、本発明のアンタゴニスト又はエンハンサー分子の作製方法を提供する。例えば、本発明は、抗体(又はその断片)であるか、ないしは抗体(又はその断片)を含有するアンタゴニストの作製方法であって、該抗体(又はその断片)をコードする本発明の組み換えベクターを好適な宿主細胞で発現させ、該抗体を回収することを含む方法を提供する。他の例では、本発明は、ポリペプチド(例えばオリゴペプチド)であるか、ないしはポリペプチド(例えばオリゴペプチド)を含有するアンタゴニスト又はエンハンサー分子の作製方法であって、該ポリペプチド(例えばオリゴペプチド)をコードする本発明の組み換えベクターを好適な宿主細胞で発現させ、該ポリペプチド(例えばオリゴペプチド)を回収することを含む方法を提供する。
一態様では、本発明は、本発明の一つ以上のアンタゴニスト又はエンハンサー分子を含有する組成物を具備する第一容器と、バッファを具備する第二容器を含むキットを提供する。一実施態様では、バッファは薬学的に受容可能である。一実施態様では、アンタゴニスト又はエンハンサー分子を含有する組成物は、いくつかの実施態様では、薬学的に受容可能である担体をさらに含有する。一実施態様では、キットは、被検体に組成物(例えばアンタゴニスト又はエンハンサー分子)を投与するための指示書を更に含む。
本発明は、HGF/c-metシグナル伝達経路のモジュレータを含む方法、組成物、キット及び製造品、並びにそのモジュレータの使用方法を提供するものである。
これら方法、組成物、キット及び製造品の詳細は本明細書中に示される。
本発明の実施は、特に明記しない限り、当業者の技術範囲内の分子生物学(組換え技術を含む)、微生物学、細胞生物学、生化学及び免疫学の従来技術を使用して行う。このような技術は、例えば以下のような文献に完全に明記されている。「Molecular Cloning: A Laboratory Manual」, 第2版(Sambrookら, 1989);「Oligonucleotide Synthesis」(M. J. Gait, 編, 1984);「Animal Cell Culture」(R. I. Freshney, 編, 1987);「Methods in Enzymology」(Academic Press, Inc.);「Current Protocols in Molecular Biology」(F. M. Ausubelら, 編., 1987, and periodic updates);「PCR: The Polymerase Chain Reaction」, (Mullisら, 編, 1994);「A Practical Guide to Molecular Cloning」(Perbal Bernard V., 1988);「Phage Display: A Laboratory Manual」(Barbas 等, 2001)。
本明細書にて用いる「ヘプシン」なる用語は、天然配列のポリペプチド、天然配列のポリペプチドのポリペプチド変異体及びその断片、及び野生型ヘプシンと類似の様式でプロHGFを切断することができるポリペプチド変異体(本明細書中でさらに定義される)を包含する。本明細書中で記載のヘプシンは、ヒト組織種類ないしは他の供給源などの様々な供給源から単離するか、組み換え法ないしは合成法によって調整されたものでもよい。また、「ヘプシン」、「ヘプシンポリペプチド」、「ヘプシン酵素」及び「ヘプシンタンパク質」なる用語は、本明細書中で記載のようなヘプシンポリペプチドの変異体を含む。
「天然配列ヘプシンポリペプチド」には、天然由来のヘプシンポリペプチドに対応する同一のアミノ酸配列を有するポリペプチドが含まれる。一実施形態では、天然配列ヘプシンポリペプチドは、配列番号1(図7参照)のアミノ酸配列を含む。一実施形態では、天然配列ヘプシンポリペプチドは、配列番号2(図8参照)のアミノ酸配列を含む。このような天然配列ヘプシンポリペプチドは、天然から単離することもできるし、組換え又は合成手段により生成することもできる。「天然配列ヘプシンポリペプチド」という用語には、特に、特定のヘプシンポリペプチドの天然に生じる切断又は分泌形態(例えば、細胞外ドメイン配列)、天然に生じる変異形態(例えば、選択的にスプライシングされた形態)及びそのポリペプチドの天然に生じる対立遺伝子変異体が含まれる。
ここで使用される「ベクター」という用語は、それが結合している他の核酸を輸送することのできる核酸分子を意味するものである。一つのタイプのベクターは「プラスミド」であり、これは付加的なDNAセグメントが結合されうる円形の二重鎖DNAループを意味する。他の型のベクターはファージベクターである。他の型のベクターはウイルスベクターであり、付加的なDNAセグメントをウイルスゲノムへ結合させうる。所定のベクターは、それらが導入される宿主細胞内において自己複製することができる(例えば、細菌の複製開始点を有する細菌ベクターとエピソーム哺乳動物ベクター)。他のベクター(例えば、非エピソーム哺乳動物ベクター)は、宿主細胞への導入時に宿主細胞のゲノム中に組み込まれ、宿主ゲノムと共に複製する。更に、所定のベクターは、それらが作用可能に結合している遺伝子の発現を指令し得る。このようなベクターはここでは「組換え発現ベクター」(又は単に「組換えベクター」)と呼ぶ。一般に、組換えDNA技術で有用な発現ベクターはしばしばプラスミドの形をとる。本明細書では、プラスミドが最も広く使用されているベクターの形態であるので、「プラスミド」と「ベクター」を相互交換可能に使用する場合が多い。
本願明細書において用いられるように、「肝細胞増殖因子」又は「HGF」なる用語は、特別に又は文脈上別途示されない限り、HGF/c-metシグナル伝達過程を生じる条件下においてこの経路を活性化しうる任意の(天然/天然に生じるもの又は合成のもののいずれにせよ)天然の又は変異形のHGFポリペプチドを指す。「野生型HGF」なる用語は、一般に、天然に生じるHGFタンパク質のアミノ酸配列を含有してなるポリペプチドを指す。「野生型HGF配列」なる用語は、一般に、天然に生じるHGFにおいてみられるアミノ酸配列を指す。
「抗体」及び「免疫グロブリン」なる用語は互換性をもって広義な意味で使われ、モノクローナル抗体(例えば完全長又は無傷のモノクローナル抗体)、ポリクローナル抗体、単価抗体、多価抗体、多特異性抗体(例えば所望の生物学的活性を示す限りの二重特異性抗体)及び本明細書で記載される抗体断片が含まれる。抗体はヒト、ヒト化及び/又は親和性成熟したものであり得る。
ここで使用される「モノクローナル抗体」という用語は、実質的に均一な抗体の集団から得られる抗体を意味する、すなわち、集団に含まれる個々の抗体が、少量で存在しうる自然に生じる可能性のある突然変異を除いて同一である。モノクローナル抗体は高度に特異的であり、一つの抗原に対している。さらに、典型的に異なる決定基(エピトープ)に対する異なる抗体を含むポリクローナル抗体調製物と比べて、各モノクローナル抗体は、抗原上の単一の決定基に対するものである。
非ヒト(例えばマウス)抗体の「ヒト化」形とは、非ヒト免疫グロブリンから得られた最小配列を含むキメラ抗体である。多くの場合、ヒト化抗体は、レシピエントの高頻度可変領域の残基が、マウス、ラット、ウサギ又は非ヒト霊長類のような所望の特異性、親和性及び能力を有する非ヒト種(ドナー抗体)の高頻度可変領域の残基によって置換されたヒト免疫グロブリン(レシピエント抗体)である。ある場合には、ヒト免疫グロブリンのフレームワーク領域(FR)残基は、対応する非ヒト残基によって置換される。さらに、ヒト化抗体は、レシピエント抗体にもドナー抗体にも見出されない残基を含んでいてもよい。これらの修飾は抗体の特性をさらに洗練するために行われる。一般的に、ヒト化抗体は、全て又はほとんど全ての高頻度可変ループが非ヒト免疫グロブリンのものに一致し、全て又はほとんど全てのFRがヒト免疫グロブリン配列である、少なくとも1つ、典型的には2つの可変ドメインの実質的に全てを含む。ヒト化抗体は、状況に応じて免疫グロブリン定常領域(Fc)、典型的にはヒトの免疫グロブリンの定常領域の少なくとも一部を含む。さらなる詳細は、Jones等, Nature 321, 522-525(1986);Riechmann等, Nature 332, 323-329(1988);及びPresta, Curr. Op. Struct. Biol. 2, 593-596(1992)を参照のこと。また、以下の概説文献及びここに挙げる引用文献も参照のこと:Vaswani及びHamilton, Ann. Allergy, Asthma & Immunol. 1:105-115 (1998);Harris, Biochem. Soc. Transactions 23:1035-1038 (1995);Hurle and Gross, Curr. Op. Biotech. 5:428-433 (1994)。
「親和性成熟」抗体は、その1つ以上のCDRに1つ以上の変更を有する抗体であって、そのような変更を有しない親抗体と比較して、抗原に対する抗体の親和性を向上させる。好ましい親和性成熟抗体は、標的抗原に対して、ナノモル単位の、さらにはピコモル単位の親和性を有する。親和成熟抗体は、当技術分野において既知の方法により生産できる。Marks他は、Bio/Technology, 10:779-783(1992年)において、VHドメインとVLドメインのシャフリングによる親和成熟を開示している。CDRおよび/またはフレームワーク残基のランダムな突然変異誘発が、Barbas他、Proc Nat. Acad. Sci, USA 91:3809-3813(1994);Schier他、Gene, 169:147-155 (1995);Yelton他、J. Immunol., 155:1994-2004 (1995);Jackson他, J. Immunol., 154(7):3310-9 (1995);およびHawkins他, J. Mol. Biol., 226:889-896 (1992)に開示されている。
本明細書中で用いられる「アゴニスト抗体」は、対象のポリペプチドの機能的な活性の少なくとも一を擬態する抗体である。
「疾病」は、本発明の物質/分子又は方法を用いた治療によって利益を得る任意の症状である。これには、問題とする疾患に哺乳動物がかかりやすくなる病理学的症状を含む慢性及び急性の疾病又は疾患を含む。限定的なものではなく、ここで治療する疾患の例には、悪性及び良性の腫瘍;非白血病性及びリンパ球性悪性腫瘍;神経系、神経膠系、星状性、視床下部系及び他の腺性、マクロファージ性、上皮性、間質性及び胚盤胞性疾患;及び炎症性、免疫性及び他の血管形成性関連疾患が含まれる。
「細胞増殖性疾患」及び「増殖性疾患」なる用語は、異常な細胞増殖にある程度関連している疾患を意味する。一実施態様では、細胞増殖性疾患は癌である。
「癌」及び「癌性」という用語は、典型的には調節されない細胞成長を特徴とする、哺乳動物における生理学的状態を指すか記述する。癌の例には、これらに限定されるものではないが、癌腫、リンパ腫、芽細胞腫、肉腫、及び白血病が含まれる。このような癌のより特定の例には、扁平細胞癌(squamous cell cancer)、小細胞肺癌、非小細胞肺癌、肺の腺癌、及び肺の扁平癌腫(squamous carcinoma)、腹膜癌、肝細胞癌、胃腸癌、膵臓癌、神経膠芽腫、子宮頸管癌、肝臓癌、膀胱癌、肝癌、乳癌、結腸癌、直腸癌、子宮内膜又は子宮癌、唾液腺癌、腎臓癌、肝臓癌、前立腺癌、産卵口癌、甲状腺癌、肝臓性癌、並びに様々な頭頸部の癌が含まれる。
「有効量」とは所望の治療又は予防結果を達成するために必要な用量及び時間での効果的な量を意味する。
本発明の物質/分子の「治療的有効量」は、例えば個体の疾病ステージ、年齢、性別、及び個体の体重、並びに個体に所望の応答を誘発する物質/分子、アゴニスト又はアンタゴニストの能力のような因子に従って変わりうる。また、治療的有効量は物質/分子、アゴニスト又はアンタゴニストの任意の毒性又は有害な効果よりも治療的に恩恵のある効果が上回るものである。「予防的有効量」とは所望の予防結果を達成するために必要な用量及び時間での効果的な量を意味する。典型的には、予防的用量は疾患の初期ステージ又はその前の患者に用いるので、予防的有効量は治療的有効量よりも少ないであろう。
「ドキソルビシン」はアントラサイクリン抗生物質である。ドキソルビシンの完全な化学名は、(8S-シス)-10-[(3-アミノ-2,3,6-トリデオキシ-α-L-リキソ-ヘキサピラノシル)オキシ]-7,8,9,10-テトラヒドロ-6,8,11-トリヒドロキシ-8-(ヒドロキシアセチル)-1-メトキシ-5,12-ナフタセンジオンである。
A.抗体
一実施形態では、本発明は、ここで治療及び/又は診断薬としての用途が見出され得る抗体を提供する。例示的な抗体には、ポリクローナル、モノクローナル、ヒト化、二重特異性及びヘテロコンジュゲート抗体が含まれる。
1.ポリクローナル抗体
ポリクローナル抗体は、好ましくは、関連する抗原とアジュバントを複数回皮下(sc)又は腹腔内(ip)注射することにより、動物に産生される。それは、免疫化されるべき種において免疫原性であるタンパク質へ、関連する抗原(特に、合成ペプチドが用いられる場合)を結合させるために有用である。例えば、この抗原を、キーホールリンペットヘモシアニン(KLH)、血清アルブミン、ウシサイログロブリン、又は大豆トリプシンインヒビターへ、二重官能性又は誘導体形成剤、例えばマレイミドベンゾイルスルホスクシンイミドエステル(システイン残基を介する抱合)、N-ヒドロキシスクシンイミド(リジン残基を介する抱合)、グルタルアルデヒド、及び無水コハク酸、SOCl2、又はR及びR1が異なるアルキル基であるR1N=C=NRを用いて結合させることができる。
動物を、例えばタンパク質又はコンジュゲート100μg又は5μg(それぞれウサギ又はマウスの場合)を完全フロイントアジュバント3容量と併せ、この溶液を複数部位に皮内注射することによって、抗原、免疫原性コンジュゲート、又は誘導体に対して免疫する。1ヶ月後、該動物を、完全フロイントアジュバントに入れた初回量の1/5ないし1/10のペプチド又はコンジュゲートを用いて複数部位に皮下注射することにより、追加免疫する。7ないし14日後に動物を採血し、抗体価について血清を検定する。動物は、力価がプラトーに達するまで追加免疫する。コンジュゲートはまた、タンパク融合として組換え細胞培養中で調製することができる。また、ミョウバンのような凝集化剤が、免疫反応の増強のために好適に使用される。
モノクローナル抗体は、Kohler等, Nature, 256:495 (1975)により最初に記載されたハイブリドーマ法、又は組換えDNA法(米国特許第4816567号)によって作成することができる。
ハイブリドーマ法においては、マウス又はその他の適当な宿主動物、例えばハムスターを上記のように免疫し、免疫化に用いられたタンパク質と特異的に結合する抗体を産生する、又は産生することのできるリンパ球を導き出す。別法として、リンパ球をインビトロで免疫することもできる。免疫化の後、リンパ球を単離し、ポリエチレングリコールのような適当な融合剤を用いて骨髄腫細胞と融合させ、ハイブリドーマ細胞を形成させる(Goding, Monoclonal Antibodies: Principles and Practice, 59-103頁(Academic Press, 1986))。
このようにして調製されたハイブリドーマ細胞を、融合していない親の骨髄腫細胞(融合のパートナーとも呼ばれる)の増殖または生存を阻害する一又は複数の物質を好ましくは含む適当な培地に蒔き、増殖させる。例えば、親の骨髄腫細胞が酵素ヒポキサンチングアニンホスホリボシルトランスフェラーゼ(HGPRT又はHPRT)を欠失するならば、ハイブリドーマのための培地は、典型的には、HGPRT−欠失細胞の増殖を妨げる物質であるヒポキサンチン、アミノプテリン、及びチミジンを含有するであろう(HAT培地)。
ハイブリドーマ細胞が生育している培地を、抗原に対するモノクローナル抗体の産生について検定する。好ましくは、ハイブリドーマ細胞により産生されるモノクローナル抗体の結合特異性は、免疫沈降又はインビトロ結合検定、例えばラジオイムノアッセイ(RIA)又は酵素結合免疫吸着検定(ELISA)によって測定する。
所望の特異性、親和性、及び/又は活性の抗体を産生するハイブリドーマ細胞が確定された後、そのクローンを限界希釈法によりサブクローニングし、標準的な方法により増殖させることができる(Goding, Monoclonal Antibodies: Principles and Practice, 59-103頁(Academic Press, 1986))。この目的に対して好適な培地は、例えば、D-MEM又はRPMI-1640培地を包含する。また、このハイブリドーマ細胞は、動物の腹水症腫瘍として、例えばマウスへの細胞の腹腔内注射によって、インビボで増殖させることができる。
サブクローンにより分泌されたモノクローナル抗体は、例えばアフィニティークロマトグラフィー(例えばプロテインA又はプロテインG-セファロースを用いる)又はイオン交換クロマトグラフィー、ヒドロキシアパタイトクロマトグラフィー、ゲル電気泳動、透析等のような常套的な抗体精製法によって、培地、腹水、又は血清から上手く分離される。
モノクローナル抗体をコードするDNAは、常法を用いて(例えば、マウス抗体の重鎖および軽鎖をコードしている遺伝子に特異的に結合できるオリゴヌクレオチドプローブを用いることにより)即座に分離されて、配列決定される。ハイブリドーマ細胞は、このようなDNAの好ましい供給源となる。ひとたび分離されたならば、DNAを発現ベクター中に入れ、ついでこれを、この状況以外では抗体タンパク質を産生しない大腸菌細胞、サルCOS細胞、チャイニーズハムスター卵巣(CHO)細胞、又は骨髄腫細胞のような宿主細胞中に形質移入し、組換え宿主細胞におけるモノクローナル抗体の合成を獲得することができる。抗体をコードするDNAの細菌での組み換え発現に関する概説論文には、Skerra等, Curr. Opinion in Immunol., 5:256-262(1993)及びPluckthun, Immunol. Revs. 130: 151-188(1992)が含まれる。
抗体をコードするDNAは、例えば、ヒト重鎖及び軽鎖定常ドメイン(CH及びCL)の配列を、相同的マウス配列に代えて置換することによって(米国特許第4,816,567号;Morrison等, Proc.Nat.Acad.Sci.,USA,81:6851(1984))、又は免疫グロブリンコード配列に非免疫グロブリンポリペプチド(異種ポリペプチド)のコード配列の全部又は一部を共有結合させることによって修飾してキメラ又は融合抗体ポリペプチドを生成することができる。非免疫グロブリンポリペプチド配列は、抗体の定常ドメインと置き代わることができるか、又は抗体の1つの抗原結合部位の可変ドメインが置換されて、抗原に対する特異性を有する1つの抗原結合部位と異なる抗原に対する特異性を有するもう一つの抗原結合部位とを含むキメラ二価抗体を作り出す。
本発明の抗体は、さらにヒト化抗体又はヒト抗体を含む。非ヒト(例えばマウス)抗体のヒト化形とは、キメラ免疫グロブリン、免疫グロブリン鎖又はその断片(例えばFv、Fab、Fab’、F(ab’)2あるいは抗体の他の抗原結合サブ配列)であって、非ヒト免疫グロブリンに由来する最小配列を含むものである。ヒト化抗体は、レシピエントの相補性決定領域(CDR)の残基が、マウス、ラット又はウサギのような所望の特異性、親和性及び能力を有する非ヒト種(ドナー抗体)のCDRの残基によって置換されたヒト免疫グロブリン(レシピエント抗体)を含む。幾つかの例では、ヒト免疫グロブリンのFvフレームワーク残基は、対応する非ヒト残基によって置換されている。また、ヒト化抗体は、レシピエント抗体にも、移入されたCDRもしくはフレームワーク配列にも見出されない残基を含んでいてもよい。一般的に、ヒト化抗体は、全て又はほとんど全てのCDR領域が非ヒト免疫グロブリンのものに一致し、全て又はほとんど全てのFR領域がヒト免疫グロブリンのコンセンサス配列である、少なくとも1つ、典型的には2つの可変ドメインの実質的に全てを含む。ヒト化抗体は、最適には免疫グロブリン定常領域(Fc)、典型的にはヒトの免疫グロブリンの定常領域の少なくとも一部を含む[Jones等, Nature, 321:522-525 (1986); Riechmann等, Nature, 332:323-329 (1988); 及びPresta, Curr. Op Struct. Biol., 2:593-596 (1992)]。
非ヒト抗体をヒト化する方法はこの分野でよく知られている。一般的に、ヒト化抗体には非ヒト由来の一又は複数のアミノ酸残基が導入される。これら非ヒトアミノ酸残基は、しばしば、典型的には「移入」可変ドメインから得られる「移入」残基と称される。ヒト化は基本的にウィンター(Winter)及び共同研究者[Jones等, Nature, 321:522-525 (1986);Riechmann等, Nature, 332:323-327 (1988);Verhoeyen等, Science, 239:1534-1536 (1988)]の方法に従って、齧歯類CDR又はCDR配列をヒト抗体の対応する配列に置換することにより実施される。よって、このような「ヒト化」抗体は、無傷のヒト可変ドメインより実質的に少ない分が非ヒト種由来の対応する配列で置換されたキメラ抗体(米国特許第4,816,567号)である。実際には、ヒト化抗体は典型的には幾つかのCDR残基及び場合によっては幾つかのFR残基が齧歯類抗体の類似する部位からの残基によって置換されたヒト抗体である。
更に、抗体を、抗原に対する高結合親和性や他の好ましい生物学的性質を保持してヒト化することが重要である。この目標を達成するべく、好ましい方法では、親及びヒト化配列の三次元モデルを使用して、親配列及び様々な概念的ヒト化産物の分析工程を経てヒト化抗体を調製する。三次元免疫グロブリンモデルは一般的に入手可能であり、当業者にはよく知られている。選択された候補免疫グロブリン配列の推測三次元立体配座構造を図解し、表示するコンピュータプログラムは購入可能である。これら表示を見ることで、候補免疫グロブリン配列の機能における残基のありそうな役割の分析、すなわち候補免疫グログリンの抗原との結合能力に影響を及ぼす残基の分析が可能になる。このようにして、例えば標的抗原に対する親和性が高まるといった、望ましい抗体特性が達成されるように、FR残基をレシピエント及び移入配列から選択し、組み合わせることができる。一般的に、高頻度可変領域残基は、直接かつ最も実質的に抗原結合性に影響を及ぼしている。
ヒト化の別法として、ヒト抗体を生成することができる。例えば、現在では、免疫化することで、内因性免疫グロブリンの産生がなく、ヒト抗体の全レパートリーを産生することのできるトランスジェニック動物(例えば、マウス)を作ることが可能である。例えば、キメラ及び生殖細胞系突然変異体マウスにおける抗体重鎖結合領域(JH)遺伝子のホモ接合体欠失によって、結果として内因性抗体産生の完全な阻害が起こることが説明されてきた。ヒト生殖系列免疫グロブリン遺伝子配列の、このような生殖細胞系突然変異体マウスへの転移によって、結果として抗原投与時にヒト抗体の産生がおこる。Jakobovits等, Proc.Natl.Acad.Sci.USA, 90:2551 (1993);Jakobovits等, Nature 362:255-258 (1993); Bruggeman等, Year in Immuno., 7:33 (1993);米国特許第5545806号、同5569825号、同5591669号(全てジェンファーム(GenPharm));同5545807号;及び国際公開第97/17852号を参照されたい。
上述したように、ヒト抗体はインビトロで活性化したB細胞により産生することができる(米国特許第5567610号及び同5229275号)。
ある状況下では、抗体全体よりも、抗体断片を用いることに利点がある。より小さな大きさの断片によって迅速なクリアランスが可能となり、固形腫瘍への接近の改良につながり得る。
抗体断片を産生するために様々な技術が開発されている。伝統的には、これらの断片は、無傷の抗体のタンパク分解性消化によって誘導された(例えば、Morimoto等, Journal of Biochemical and Biophysical Methods 24:107-117 (1992)及びBrennan等, Science, 229:81(1985)を参照されたい)。しかし、これらの断片は、現在は組換え宿主細胞により直接産生することができる。Fab、Fv及びScFv抗体断片は、すべて大腸菌で発現させ分泌させることができ、従って、大量のこれら断片の産生が容易となった。抗体断片は、上で論じた抗体ファージライブラリーから単離することができる。別法として、Fab'-SH断片は大腸菌から直接回収することができ、化学的に結合させてF(ab')2断片を形成することができる(Carter等, Bio/Technology 10:163-167(1992))。他のアプローチ法では、F(ab')2断片を組換え宿主細胞培養から直接分離することができる。インビボ半減期が増した、サルベージレセプター結合性エピトープ残基を含むFab及びF(ab’)2が、米国特許第5869046号に記載されている。抗体断片を生成するのための他の方法は、当業者には明らかであろう。他の実施形態では、選択する抗体は一本鎖Fv断片(scFv)である。国際公開93/16185号;米国特許第5571894号;及び米国特許第5587458号を参照のこと。Fv及びsFvは、定常領域を欠く無傷の連結部位を有する唯一の種である;従って、インビボで使用している間の減少した非特異的結合に適している。sFv融合タンパク質は、sFvのアミノ又はカルボキシ末端のどちらかで、エフェクタータンパク質の融合体が生成されるように構成されてもよい。上掲のAntibody Engineering, Borrebaeck編を参照のこと。また、抗体断片は、例えば米国特許第5641870号に記載されているような「直鎖状抗体」であってもよい。そのような直鎖状抗体断片は単一特異性又は二重特異性であってもよい。
二重特異性抗体は、少なくとも2つの異なるエピトープに対して結合特異性を有する抗体である。例示的な二重特異性抗体は、本明細書に記載のヘプシン、HGF及び/又はヘプシン:HGF複合体の2つの異なるエピトープに結合しうる。他のこのような抗体では他のポリペプチドに対する結合部位とそのものの結合部位とが結合しうる。あるいは、抗体は、ヘプシン及び/又はHGFを発現する細胞及び/又はヘプシン及び/又はHGFに結合する細胞に細胞防御メカニズムを集中させ局在させるように、FcγRI(CD64)、FcγRII(CD32)及びFcγRIII(CD16)等のIgG(FcγR)に対するFcレセプター、又はT細胞レセプター分子(例えばCD3)等の白血球上のトリガー分子に結合するアームと結合しうる。また、二重特異性抗体はヘプシン、HGF及び/又はヘプシン:HGF複合体を発現する及び/又はヘプシン、HGF及び/又はヘプシン:HGF複合体に結合する細胞に細胞障害剤を局在化するためにも使用されうる。これらの抗体はポリペプチド結合アーム及び細胞障害剤(例えば、サポリン(saporin)、抗インターフェロン-α、ビンカアルカロイド、リシンA鎖、メトトレキセート又は放射性同位体ハプテン)と結合するアームを有する。二重特異性抗体は完全長抗体又は抗体断片(例えばF(ab')2二重特異性抗体)として調製することができる。
国際公開第96/16673号には、二重特異性抗-ErbB2/抗-FcγRIII抗体が記載されており、米国特許第5837234号には、二重特異性抗-ErbB2/抗-FcγRI抗体が開示されている。二重特異性抗-ErbB2/Fcα抗体は国際公開第98/02463号に示されている。米国特許第5821337号は、二重特異性抗-ErbB2/抗-CD3抗体を教示するものである。
異なったアプローチ法では、所望の結合特異性を有する抗体可変ドメイン(抗原-抗体結合部位)を免疫グロブリン定常ドメイン配列と融合させる。該融合は好ましくは、少なくともヒンジの一部、CH2及びCH3領域を含むIg重鎖定常ドメインである。軽鎖の結合に必要な部位を含む第一の重鎖定常領域(CH1)を、融合の少なくとも一つに存在させることが望ましい。免疫グロブリン重鎖の融合、望まれるならば免疫グロブリン軽鎖をコードしているDNAを、別個の発現ベクター中に挿入し、適当な宿主生物に同時トランスフェクトする。これにより、組立に使用される三つのポリペプチド鎖の等しくない比率が所望の二重特異性抗体の最適な収率をもたらす態様において、三つのポリペプチド断片の相互の割合の調節に大きな融通性が与えられる。しかし、少なくとも二つのポリペプチド鎖の等しい比率での発現が高収率をもたらすとき、又はその比率が所望の鎖の結合にあまり影響がないときは、2または3個全てのポリペプチド鎖のためのコード化配列を一つの発現ベクターに挿入することが可能である。
米国特許第5731168号に記載された他の手法によれば、一対の抗体分子間の界面を操作して組換え細胞培養から回収されるヘテロダイマーのパーセントを最大にすることができる。好適な界面はCH3ドメインの少なくとも一部を含む。この方法では、第1抗体分子の界面からの一又は複数の小さいアミノ酸側鎖がより大きな側鎖(例えばチロシン又はトリプトファン)と置き換えられる。大きな側鎖と同じ又は類似のサイズの相補的「キャビティ」を、大きなアミノ酸側鎖を小さいもの(例えばアラニン又はスレオニン)と置き換えることにより第2の抗体分子の界面に作り出す。これにより、ホモダイマーのような不要の他の最終産物に対してヘテロダイマーの収量を増大させるメカニズムが提供される。
抗体断片から二重特異性抗体を産生する技術もまた文献に記載されている。例えば、化学結合を使用して二重特異性抗体を調製することができる。Brennan等, Science, 229:81 (1985) は無傷の抗体をタンパク分解性に切断してF(ab')2断片を産生する手順を記述している。これらの断片は、ジチオール錯体形成剤、亜砒酸ナトリウムの存在下で還元して近接ジチオールを安定化させ、分子間ジスルフィド形成を防止する。産生されたFab'断片はついでチオニトロベンゾアート(TNB)誘導体に変換される。Fab'-TNB誘導体の一つをついでメルカプトエチルアミンでの還元によりFab'-チオールに再変換し、他のFab'-TNB誘導体の等モル量と混合して二重特異性抗体を形成する。作られた二重特異性抗体は酵素の選択的固定化用の薬剤として使用することができる。
二価より多い抗体も考えられる。例えば、三重特異性抗体を調製することができる。Tutt等 J.Immunol. 147:60(1991)。
ヘテロコンジュゲート抗体もまた本発明の範囲に入る。ヘテロコンジュゲート抗体は、2つの共有結合した抗体からなる。このような抗体は、例えば、免疫系細胞を不要な細胞に対してターゲティングさせるため[米国特許第4676980号]及びHIV感染の治療のために[国際公開第91/00360;国際公開第92/200373;欧州特許第03089号]提案されている。この抗体は、架橋剤に関連したものを含む合成タンパク化学における既知の方法を使用して、インビトロで調製することができると考えられる。例えば、ジスルフィド交換反応を使用するか又はチオエーテル結合を形成することによって、免疫毒素を作成することができる。この目的に対して好適な試薬の例には、イミノチオレート及びメチル-4-メルカプトブチルイミダート、及び例えば米国特許第4676980号に開示されたものが含まれる。
多価抗体は、抗体が結合する抗原を発現する細胞により、二価抗体よりも早くインターナリゼーション(及び/又は異化)されうる。本発明の抗体は、3又はそれ以上の結合部位を有する多価抗体(IgMクラス以外のもの)であり得(例えば四価抗体)、抗体のポリペプチド鎖をコードする核酸の組換え発現により容易に生成することができる。多価抗体は二量化ドメインと3又はそれ以上の抗原結合部位を有する。好ましい二量化ドメインはFc領域又はヒンジ領域を有する(又はそれらからなる)。このシナリオにおいて、抗体はFc領域と、Fc領域のアミノ末端に3又はそれ以上の抗原結合部位を有しているであろう。ここで、好ましい多価抗体は3ないし8、好ましくは4の抗原結合部位を有する(又はそれらからなる)。多価抗体は少なくとも1つのポリペプチド鎖(好ましくは2つのポリペプチド鎖)を有し、ポリペプチド鎖(類)は2又はそれ以上の可変ドメインを有する。例えば、ポリペプチド鎖(類)はVD1-(X1)n-VD2-(X2)n-Fcを有し、ここでVD1は第1の可変ドメインであり、VD2は第2の可変ドメインであり、FcはFc領域のポリペプチド鎖の一つであり、X1及びX2はアミノ酸又はポリペプチドを表し、nは0又は1である。例えば、ポリペプチド鎖(類)は:VH-CH1-柔軟なリンカー-VH-CH1-Fc領域鎖;又はVH-CH1-VH-CH1-Fc領域鎖を有し得る。ここで多価抗体は、好ましくは少なくとも2つ(好ましくは4つ)の軽鎖可変ドメインポリペプチドをさらに有する。ここで多価抗体は、例えば約2〜約8の軽鎖可変ドメインポリペプチドを有する。ここで考察される軽鎖可変ドメインポリペプチドは軽鎖可変ドメインを有し、場合によってはCLドメインを更に有する。
本発明の抗体をエフェクター機能について改変し、例えば抗体の抗原-依存細胞媒介細胞障害性(ADCC)及び/又は補体依存細胞障害性(CDC)を向上させることは望ましい。これは、抗体のFc領域で一又は複数のアミノ酸置換を誘導することによりなされうる。あるいは又はさらに、システイン残基をFc領域に導入し、それにより、この領域に鎖間ジスルフィド結合を形成するようにしてもよい。そのようにして生成された同種二量体抗体は、向上したインターナリゼーション能力及び/又は増加した補体媒介細胞殺傷及び抗体−依存細胞性細胞障害性(ADCC)を有する可能性がある。Caron等, J. Exp. Med. 176: 1191-1195 (1992)及びShopes, B. J. Immunol. 148: 2918-2922 (1992)参照。また、向上した抗腫瘍活性を持つ同種二量体抗体は、Wolff等, Cancer Research 53: 2560-2565 (1993)に記載されている異種二官能性架橋を用いて調製することができる。あるいは、抗体は、2つのFc領域を有するように加工して、それにより補体溶解及びADCC能力を向上させることもできる。Stevenson等, Anti-Cancer Drug Design 3: 219-230 (1989)参照。抗体の血清半減期を増大させるために、例えば米国特許第5739277号に記載のように、抗体(特に抗体断片)へサルベージレセプター結合エピトープを導入してもよい。ここで使用される場合の「サルベージレセプター結合エピトープ」なる用語は、IgG分子のインビボ血清半減期を増加させる原因であるIgG分子(例えば、IgG1、IgG2、IgG3又はIgG4)のFc領域のエピトープを意味する。
また、本発明は、化学治療薬、薬剤、成長阻害剤、毒素(例えば、細菌、真菌、植物又は動物由来の酵素活性毒素、又はその断片)などの細胞障害性剤、あるいは放射性同位体(即ち、放射性コンジュゲート)と抱合している抗体を含む免疫コンジュゲート、又は抗体−薬剤コンジュゲート(ADC)に関する。
細胞障害性又は細胞分裂停止性の薬剤、すなわち癌治療における腫瘍細胞を殺す又は阻害するための薬剤の局部運搬に抗体−薬剤コンジュゲートを用いると(Syrigos及びEpenetos (1999) Anticancer Research 19:605-614; Niculescu-Duvaz and Springer (1997) Adv. Drg Del. Rev. 26:151-172;米国特許第4,975,278号)、論理的に腫瘍への薬剤成分の標的とする運搬とそこでの細胞内集積が可能となるものであり、この非コンジュゲート薬物作用剤の全身性投与により正常細胞並びに除去しようとする腫瘍細胞への毒性が容認できないレベルとなりうる(Baldwinら., (1986) Lancet pp. (Mar. 15, 1986):603-05; Thorpe, (1985) 「Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review,」 in Monoclonal Antibodies '84: Biological And Clinical Applications, A. Pincheraら. (ed.s), pp. 475-506)。これによって、最小限の毒性で最大限の効果を求める。ポリクローナル抗体及びモノクローナル抗体はこの方策に有用であるとして報告されている(Rowlandら., (1986) Cancer Immunol. Immunother., 21:183-87)。この方法に用いる薬物には、ダウノマイシン、ドキソルビジン、メトトレキサート及びビンデジンが含まれる(Rowlandら., (1986)、上掲)。抗体−毒素コンジュゲートに用いる毒素には、ジフテリア毒素などの細菌性毒素、ゲルダナマイシン(Mandlerら(2000) Jour. of the Nat. Cancer Inst. 92(19):1573-1581;Mandlerら(2000) Bioorganic & Med. Chem. Letters 10:1025-1028;Mandlerら(2002) Bioconjugate Chem. 13:786-791)、メイタンシノイド(EP 1391213;Liuら., (1996) Proc. Natl. Acad. Sci. USA 93:8618-8623)、及びカリケアマイシン(Lodeら (1998) Cancer Res. 58:2928;Hinmanら (1993) Cancer Res. 53:3336-3342)などのリシン、小分子毒素などの植物毒が含まれる。該毒素は、チューブリン結合、DNA結合又はトポイソメラーゼ阻害を含む機能によりその細胞障害性及び細胞分裂停止性の効果に影響しうる。ある種の細胞障害性剤は、大きな抗体又はタンパク質レセプターリガンドにコンジュゲートした場合に、不活性又は活性が低減する傾向がある。
抗体のコンジュゲートと一又は複数の小分子毒素、例えばカリケアマイシン、メイタンシノイド、トリコセン(trichothene)及びCC1065、及び毒性活性を有するこれらの毒素の誘導体が、ここで考察される。
一実施態様では、本発明の抗体(完全長又は断片)は一又は複数のメイタンシノイド分子と結合している。
メイタンシノイドは、チューブリン重合を阻害するように作用する分裂阻害剤である。メイタンシンは、最初、東アフリカシラブMaytenus serrataから単離されたものである(米国特許第3896111号)。その後、ある種の微生物がメイタンシノイド類、例えばメイタンシノール及びC-3メイタンシノールエステルを生成することが発見された(米国特許第4151042号)。合成メイタンシノール及びその誘導体及び類似体は、例えば米国特許第4137230号;同4248870号;同4256746号;同4260608号;同4265814号;同4294757号;同4307016号;同4308268号;同4308269号;同4309428号;同4313946号;同4315929号;同4317821号;同4322348号;同4331598号;同4361650号;同4364866号;同4424219号;同4450254号;同4362663号;及び同4371533号に開示されており、その開示は出典を明示してここに取り込まれる。
治療指標を改善する試みにおいて、メイタンシン及びメイタンシノイドは、腫瘍細胞抗原に特異的に結合する抗体と結合している。メイタンシノイドを含有する免疫コンジュゲート及びそれらの治療用途は、例えば米国特許第5,208,020号、同5,416,064号、欧州特許第0425235B1号に開示されており、その開示は出典を明示してここに取り込まれる。Liu等, Proc. Natl. Acad. Sci. USA 93:8618-8623(1996)には、ヒト結腸直腸癌に対するモノクローナル抗体C242に結合するDM1と命名されたメイタンシノイドを含有する免疫コンジュゲートが記載されている。前記コンジュゲートは培養された結腸癌細胞に対して高い細胞障害性を有することが見出されており、インビボ腫瘍成長アッセイにおいて抗腫瘍活性を示す。Chari等, Cancer Research, 52:127-131(1992)には、メイタンシノイドが、ジスルフィド結合を介して、ヒト結腸癌株化細胞の抗原に結合するマウス抗体A7、又はHER-2/neuオンコジーンに結合する他のマウスモノクローナル抗体TA.1に結合している免疫コンジュゲートが記載されている。TA.1-メイタンシノイドコンジュゲートの細胞障害性はヒト乳癌株化細胞SK-BR-3におけるインビトロで試験され、細胞当たり3×105HER-2表面抗原が発現した。薬剤コンジュゲートにより、遊離のメイタンシノイド剤に類似した細胞障害度が達成され、該細胞障害度は、抗体分子当たりのメイタンシノイド分子の数を増加させることにより増加する。A7-メイタンシノイドコンジュゲートはマウスにおいては低い全身性細胞障害性を示した。
抗体-メイタンシノイドコンジュゲートは、抗体又はメイタンシノイド分子のいずれの生物学的活性もほとんど低減することなく、メイタンシノイド分子に抗体を化学的に結合させることにより調製される。1分子の毒素/抗体は、裸抗体の使用において細胞障害性を高めることが予期されているが、抗体分子当たり、平均3-4のメイタンシノイド分子が結合したものは、抗体の機能又は溶解性に悪影響を与えることなく、標的細胞に対する細胞障害性を向上させるといった効力を示す。メイタンシノイドは当該技術分野でよく知られており、公知の技術で合成することも、天然源から単離することもできる。適切なメイタンシノイドは、例えば米国特許第5208020号、及び他の特許、及び上述した特許ではない刊行物に開示されている。好ましいメイタンシノイドは、メイタンシノール、及び種々のメイタンシノールエステル等の、メイタンシノール分子の芳香環又は他の位置が修飾されたメイタンシノール類似体である。
例えば、米国特許第5208020号又は欧州特許第0425235B1号、及びChari等, Cancer Research, 52:127-131(1992)に開示されているもの等を含む、抗体-メイタンシノイドコンジュゲートを作製するために、当該技術で公知の多くの結合基がある。結合基には、上述した特許に開示されているようなジスルフィド基、チオエーテル基、酸不安定性基、光不安定性基、ペプチターゼ不安定性基、又はエステラーゼ不安定性基が含まれるが、ジスルフィド及びチオエーテル基が好ましい。
リンカーは結合の種類に応じて、種々の位置でメイタンシノイド分子に結合し得る。例えば、従来からのカップリング技術を使用してヒドロキシル基と反応させることによりエステル結合を形成することができる。反応はヒドロキシル基を有するC-3位、ヒドロキシメチルで修飾されたC-14位、ヒドロキシル基で修飾されたC-15位、及びヒドロキシル基を有するC-20位で生じる。好ましい実施形態において、結合はメイタンシノール又はメイタンシノールの類似体のC-3位で形成される。
対象の他の免疫コンジュゲートには、一又は複数のカリケアマイシン分子と結合した抗体が含まれる。抗生物質のカリケアマイシンファミリーはサブ-ピコモルの濃度で二重鎖DNA破壊を生じることができる。カリケアマイシンファミリーのコンジュゲートの調製については、米国特許第5712374号、同5714586号、同5739116号、同5767285号、同5770701号、同5770710号、同5773001号、同5877296号(全て、American Cyanamid Company)を参照のこと。使用可能なカリケアマイシンの構造類似体には、限定するものではないが、γ1 I、α2 I、α3 I、N-アセチル-γ1 I、PSAG及びθI 1(Hinman等, Cancer Research, 53:3336-3342(1993)、Lode等 Cancer Research, 58:2925-2928(1998)及び上述したAmerican Cyanamidの米国特許)が含まれる。抗体が結合可能な他の抗腫瘍剤は、葉酸代謝拮抗薬であるQFAである。カリケアマイシン及びQFAは双方共、細胞内に作用部位を有し、原形質膜を容易に通過しない。よって抗体媒介性インターナリゼーションによるこれらの薬剤の細胞への取込により、細胞障害効果が大きく向上する。
本発明の抗体と結合可能な他の抗腫瘍剤には、BCNU、ストレプトゾイシン、ビンクリスチン及び5-フルオロウラシル、米国特許第5053394号、同5770710号に記載されており、集合的にLL-E33288複合体として公知の薬剤のファミリー、並びにエスペラマイシン(esperamicine)(米国特許第5877296号)が含まれる。
使用可能な酵素活性毒及びその断片には、ジフテリアA鎖、ジフテリア毒素の非結合性活性断片、外毒素A鎖(シュードモナス・アエルギノーサ(Pseudomonas aeruginosa))、リシンA鎖、アブリンA鎖、モデシン(modeccin)A鎖、アルファ-サルシン(sarcin)、アレウライツ・フォルディイ(Aleurites fordii)プロテイン、ジアンシン(dianthin)プロテイン、フィトラッカ・アメリカーナ(Phytolaca americana)プロテイン(PAPI、PAPII及びPAP-S)、モモルディカ・キャランティア(momordica charantia)インヒビター、クルシン(curcin)、クロチン、サパオナリア(sapaonaria)オフィシナリスインヒビター、ゲロニン(gelonin)、マイトゲリン(mitogellin)、レストリクトシン(restrictocin)、フェノマイシン、エノマイシン及びトリコセセンス(tricothecenes)が含まれる。例えば、1993年10月28日公開の国際公開第93/21232号を参照のこと。
本発明は、抗体と核酸分解活性を有する化合物(例えばリボヌクレアーゼ又はDNAエンドヌクレアーゼ、例えばデオキシリボヌクレアーゼ;DNアーゼ)との間に形成される免疫コンジュゲートをさらに考察する。
放射-又は他の標識が、公知の方法でコンジュゲートに導入される。例えば、ペプチドは生物合成されるか、又は水素の代わりにフッ素-19を含む適切なアミノ酸前駆体を使用する化学的なアミノ酸合成により合成される。標識、例えばtc99m又はI123、Re186、Re188及びIn111は、ペプチドのシステイン残基を介して結合可能である。イットリウム-90はリジン残基を介して結合可能である。IODOGEN法(Fraker等(1978) Biochem. Biophys. Res. Commun. 80:49-57)は、ヨウ素-123の導入に使用することができる。他の方法の詳細は、「Monoclonal Antibodies in Immunoscintigraphy」(Chatal, CRC Press 1989)に記載されている。
本発明の化合物は、限定するものではないが、架橋剤:市販されている(例えば、Pierce Biotechnology, Inc., Rockford, IL., U.S.Aより)BMPS、EMCS、GMBS、HBVS、LC-SMCC、MBS、MPBH、SBAP、SIA、SIAB、SMCC、SMPB、SMPH、スルホ-EMCS、スルホ-GMBS、スルホ-KMUS、スルホ-MBS、スルホ-SIAB、スルホ-SMCC、及びスルホ-SMPB、及びSVSB (succinimidyl-(4-ビニルスルホン)安息香酸塩)にて調製したADCが特に考えられる。2003-2004 Applications Handbook and Catalogの467−498頁を参照。
本発明の抗体薬剤コンジュゲート(ADC)において、抗体(Ab)を、リンカー(L)を介して、一つ以上の薬剤部分(D)、例えば抗体につき約1〜約20の薬剤部分にコンジュゲートする。式IのADCはいくつかの手段、当業者に公知の有機化学反応、状態および試薬を用いて調製されうる:(1)共有結合の後に薬剤部分Dと反応してAb-Lを形成するための、二価のリンカー試薬を用いた抗体の求核基の反応;及び(2)共有結合の後に抗体の求核基と反応してD-Lを形成するための、二価のリンカー試薬を用いた薬剤部分の求核基の反応、が含まれる。
Ab−(L−D)p I
抗体上の求核基には、限定するものでなく、以下のものを含む:(i)N末端アミン基、(ii)側鎖アミン基、例えばリシン、(iii)側鎖チオール基、例えばシステイン、および(iv)抗体がグリコシル化される糖水酸基又はアミノ基。アミン、チオールおよび水酸基は、求核であり、反応して、リンカー部分上の求電子性の群およびリンカー試薬により共有結合を形成することができる:(i)活性エステル、例えばNHSエステル、HOBtエステル、ハロギ酸および酸ハロゲン化物;(ii)アルキルおよびベンジルハライド、例えばハロアセトアミド;(iii)アルデヒド、ケトン、カルボキシルおよびマレイミド群、が含まれる。特定の抗体は、還元しうる鎖間ジスルフィド、すなわちシステイン架橋を有する。抗体は、還元剤、例えばDTT(ジチオトレイトール)による処置によって、リンカー試薬を用いたコンジュゲート反応を行ってもよい。ゆえに、各々のシステイン架橋は、理論的には、2の反応性のチオール求核基を形成する。チオールにアミンを転換させる2-イミノチオラン(トラウトの試薬)を用いてリシンを反応させることによって抗体に付加的な求核基を導入することができる。
同様に、薬剤部分上の求核基には、限定するものではないが、以下のものを含む:反応して、リンカー部分およびリンカー試薬上の求電子性の基と共有結合することができるアミン、チオール、ヒドロキシル、ヒドラジド、オキシム、ヒドラジン、チオセミカルバゾン、ヒドラジンカルボン酸エステルおよびアリールヒドラジド基:(i)活性エステル(例えばNHSエステル、HOBtエステル、ハロギ酸および酸ハロゲン化物);(ii)アルキルおよびベンジルハライド、例えばハロアセトアミド;(iii)アルデヒド、ケトン、カルボキシルおよびマレイミド基、が含まれる。
他の実施態様において、腫瘍の事前ターゲティングに利用するために、「レセプター」(例えばストレプトアビジン)に抗体をコンジュゲートし、ここで抗体-レセプターコンジュゲートを患者に投与し、続いて清澄剤を使用し、循環から非結合コンジュゲートを除去し、細胞障害剤(例えば放射性ヌクレオチド)にコンジュゲートする「リガンド」(例えばアビジン)を投与する。
ここで開示されている抗体は、免疫リポソームとして処方することもできる。「リポソーム」は、哺乳動物への薬物輸送に有用な、脂質、リン脂質及び/又は界面活性剤を含む種々のタイプの小胞体である。リポソームの成分は、通常は生物膜の脂質配向に類似した2層構造に配列される。抗体を含有するリポソームは、例えばEpstein等, Proc. Natl. Acad. Sci. USA 82:3688(1985);Hwang等, Proc. Natl. Acad. Sci. USA 77:4030(1980);及び米国特許第4485045号及び同4544545号;及び1997年10月23日に公開の国際公開97/38731に記載されているように、当該分野において既知の方法により調製される。循環時間が増したリポソームは米国特許第5013556号に開示されている。
特に有用なリポソームは、ホスファチジルコリン、コレステロール及びPEG-誘導体化ホスファチジルエタノールアミン(PEG-PE)を含有する脂質組成物を用いた逆相蒸発法により作製することができる。リポソームは孔径が定められたフィルターを通して押し出され、所望の直径を有するリポソームが得られる。本発明の抗体のFab'断片は、ジスルフィド交換反応を介して、Martin等, J. Biol. Chem. 257:286-288(1982)に記載されているようにしてリポソームにコンジュゲートすることができる。場合によっては、化学療法剤はリポソーム内に包含される。Gabizon等, J. National Cancer Inst. 81(19)1484(1989)を参照されたい。
本発明の結合オリゴペプチドはここで記載される様なヘプシン、HGF及び/又はヘプシン:HGF複合体に、好ましくは特異的に、結合するオリゴペプチドである。結合オリゴペプチドは、既知のオリゴペプチド合成法を用いて化学的に合成することができ、あるいは組換え技術を用いて調製及び生成することができる。結合オリゴペプチドは通常、少なくとも約5のアミノ酸長であり、或いは少なくとも約6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99又は100のアミノ酸長以上であり、このようなオリゴペプチドはここに記載される様なポリペプチドに対して好ましくは特異的に結合する能力がある。結合オリゴペプチドは、よく知られた技術を用いて過度の実験をすることなしに同定することができる。この点において、ポリペプチド標的に特異的に結合する能力のあるオリゴペプチドのオリゴペプチドライブラリーを検索する技術は当分野でよく知られていることを注記する(例えば、米国特許第5556762号、同第5750373号、同第4708871号、同第4833092号、同第5223409号、同第5403484号、同第5571689号、同第5663143号;PCT公開第WO84/03506号、及びWO84/03564号;Geysen等, Proc. Natl. Acad. Sci. U.S.A., 81:3998-4002 (1984);Geysen等, Proc. Natl. Acad. Sci. U.S.A., 82:178-182 (1985);Geysen等, in Synthetic Peptides as Antigens, 130-149 (1986);Geysen等, J. Immunol. Meth., 102:259-274 (1987);Schoofs等, J. Immunol., 140:611-616 (1988), Cwirla,S.E.等(1990) Proc. Natl. Acad. Sci. USA, 87:6378;Lowman,H.B.等 (1991) Biochemistry, 30:10832;Clackson,T.等 (1991) Nature, 352:624;Marks,J.D.等 (1991) J. Mol. Biol., 222:581;Kang,A.S.等 (1991) Proc. Natl. Acad. Sci. USA, 88:8363、及びSmith, G.P. (1991) Current Opin. Biotechnol., 2:668参照)。
ペプチドライブラリーの作製及びこれらのライブラリーのスクリーニングの方法は、米国特許第5723286号、同第5432018号、同第5580717号、同第5427908号、同第5498530号、同第5770434号、同第5734018号、同第5698426号、同第5763192号、及び同第5723323号に記載される。
結合小分子とは、好ましくは、ヘプシン、HGF及び/又はヘプシン:HGF複合体に、好ましくは特異的に結合する、ここに定義されるようなオリゴペプチド又は抗体以外の有機分子である。結合有機小分子は既知の方法(例えばPCT公開第WO00/00823及びWO00/39585号参照)を用いて同定され、化学的に合成されうる。結合有機小分子は通常、約2000ダルトンの大きさ未満であり、あるいは約1500、750、500、250又は200ダルトンの大きさであり、ここに記載される様なヘプシン、HGF及び/又はヘプシン:HGF複合体に、好ましくは特異的に結合する能力のあるこのような有機小分子は、よく知られた技術を用いて過度の実験をすることなしに同定されうる。この点において、ポリペプチド標的に結合する能力のある分子の有機小分子ライブラリーを検索する技術は当分野でよく知られていることを注記する(例えばPCT公開第WO00/00823及びWO00/39585号参照)。結合有機小分子は、例えばアルデヒド、ケトン、オキシム、ヒドラゾン、セミカルバゾン、カルバジド、一級アミン、二級アミン、三級アミン、N置換ヒドラジン、ヒドラジド、アルコール、エーテル、チオール、チオエーテル、ジスルフィド、カルボン酸、エステル、アミド、尿素、カルバミン酸塩、炭酸塩、ケタール、チオケタール、アセタール、チオアセタール、ハロゲン化アリール、アリールスルホン酸、ハロゲン化アルキル、アルキルスルホン酸、芳香族化合物、複素環化合物、アニリン、アルケン、アルキン、ジオール、アミノアルコール、オキサゾリジン、オキサゾリン、チアゾリジン、チアゾリン、エナミン、スルホンアミド、エポキシド、アジリジン、イソシアン酸塩、塩化スルホニル、ジアゾ化合物、酸塩化物等であり得る。
抗体、オリゴペプチド及び小分子を生成する技術を、上記にて記載した。所望するような、所定の生物学的特性を有する抗体、オリゴペプチド又は他の小分子をさらに選択することができる。
本発明の抗体、オリゴペプチド又は他の小分子の成長阻害効果を、例えば、内因的又はそれぞれの遺伝子によるトランスフェクション後のいずれかでヘプシン及び/又はプロHGFを発現する細胞を用いる当該分野で周知の方法によって評価することができる。例えば、適切な腫瘍細胞株、及びヘプシン及び/又はHGFポリペプチド形質移入細胞は、数日間(例えば、2−7)、種々の濃度の本発明のモノクローナル抗体、オリゴペプチド又は他の小分子で処理し、クリスタル・バイオレット又はMTTで染色、又は幾つかの他の比色アッセイによって分析し得る。増殖を測定するその他の方法は、本発明の抗体、結合オリゴペプチド又は結合小分子の存在又は非存在下で処理した細胞の3H-チミジン取り込みを比較することによる。処理の後、細胞を収集し、DNAへ取り込まれた放射能をシンチレーションカウンターで定量化した。適切なポジティブコントロールには、細胞株の成長を阻害することが知られている成長阻害抗体でその選択した細胞株を処理することが含まれる。インビボでの腫瘍細胞の成長阻害は、当該分野で知られている種々の方法で確かめることができる。腫瘍細胞は、ヘプシン及び/又はプロHGFポリペプチドを過剰発現するものとすることができる。抗体、結合オリゴペプチド又は結合有機小分子は、ある実施形態では約0.5から30μg/mlの抗体濃度で、未処理腫瘍細胞と比べて約25−100%、より好ましくは約30−100%、そしてさらにより好ましくは約50−100%又は70−100%のヘプシン及び/又はプロHGFを発現する腫瘍細胞の増殖をインビトロ又はインビボで阻害する。成長阻害は、細胞培養で、約0.5から30μg/ml又は0.5nMから200nMの抗体濃度で測定することができ、その成長阻害は、抗体への腫瘍細胞の曝露後1−10日で確かめられる。約1μg/kgから約100mg/kg体重での抗体の投与が、抗体の最初の投与から約5日から3ヶ月、好ましくは約5から30日以内に腫瘍の大きさの減少又は腫瘍細胞増殖の減少を引き起こすならば、抗体はインビボで成長阻害作用がある。
関心のある抗体が結合したポリペプチド上のエピトープに結合する抗体、オリゴペプチド又は他の有機小分子をスクリーニングするために、Antibodies, A Laboratory Manual, Cold Spring Harbor Laboratory, Ed Harlow及びDavid Lane編(1988)に記載されているような通常の交差ブロッキングアッセイを実施することができる。既知の抗体のように、試験抗体、オリゴペプチド又は他の有機小分子が同じ部位又はエピトープと結合するならば、このアッセイを確定するために用いることができる。あるいは、又は付加的に、エピトープマッピングを、当該分野で周知の方法によって行うことができる。例えば、接触残基を同定するために、例えばアラニンスキャンニングによって抗体配列を変異させることができる。この変異体抗体は、適切なフォールディングを確かめるために、最初にポリクローナル抗体との結合について試験される。異なる方法では、ポリペプチドの異なる領域と一致するペプチドを、試験抗体群又は試験抗体及び特徴付けられた又は既知のエピトープを有する抗体による競合アッセイで用いることができる。
また、本発明の抗体は、プロドラッグ(例えばペプチジル化学療法剤、国際公開81/01145を参照)を活性な抗癌剤へ変換するプロドラッグ活性化酵素へ抗体をコンジュゲートすることによって、ADEPTにおいて使用することができる。例えば国際公開88/07378及び米国特許第4975278号を参照されたい。
ADEPTに有用な免疫コンジュゲートの酵素成分には、より活性な細胞毒形態に変換するようにプロドラッグへ作用し得る任意の酵素が含まれる。
限定するものではないが、この発明の方法に有用な酵素には、ホスファート含有プロドラッグを遊離の薬剤に変換するのに有用なアルカリ性ホスファターゼ;スルファート含有プロドラッグを遊離の薬剤に変換するのに有用なアリールスルファターゼ;非毒性5-フルオロシトシンを抗癌剤5-フルオロウラシルに変換するのに有用なシトシンデアミナーゼ;プロテアーゼ、例えばセラチアプロテアーゼ、サーモリシン、サブチリシン、カルボキシペプチダーゼ及びカテプシン(例えば、カテプシンB及びL)で、ペプチド含有プロドラッグを遊離の薬剤に変換するのに有用なもの;D-アミノ酸置換基を含有するプロドラッグの変換に有用なD-アラニルカルボキシペプチダーゼ;炭水化物切断酵素、例えばグリコシル化プロドラッグを遊離の薬剤に変換するのに有用なノイラミニダーゼ及びβガラクトシダーゼ;βラクタムで誘導体化された薬剤を遊離の薬剤に変換させるのに有用なβラクタマーゼ;及びペニシリンアミダーゼ、例えばそれぞれフェノキシアセチル又はフェニルアセチル基で、それらのアミン性窒素において誘導体化された薬剤を遊離の薬剤に変換するのに有用なペニシリンVアミダーゼ又はペニシリンGアミダーゼが含まれる。あるいは、「アブザイム」としてもまた公知の酵素活性を有する抗体を、遊離の活性薬剤に本発明のプロドラッグを変換させるために使用することもできる(例えば、Massey, Nature 328:457-458(1987)を参照)。抗体-アブザイムコンジュゲートは、ここで記載されているようにして、腫瘍細胞個体群にアブザイムを送達するために調製することができる。
この発明の酵素は、当該分野においてよく知られている技術、例えば上で検討したヘテロ二官能性架橋試薬を使用することにより、抗体に共有的に結合させることができる。あるいは、本発明の抗体の少なくとも抗原結合領域を本発明の酵素の少なくとも機能的に活性な部位に結合せしめてなる融合タンパク質を、当該技術においてよく知られている組換えDNA技術を使用して作成することができる(Neuberger等, Nature 312:604-608[1984])。
ここに記載した抗体に加えて、抗体変異体も調製できると考えられる。抗体変異体は、コード化DNAに適当なヌクレオチド変化を導入することによって、及び/又は所望の抗体を合成することによって調製できる。当業者は、アミノ酸変化がグリコシル化部位の数又は位置の変化あるいは膜固着特性の変化などの抗体の翻訳後プロセスを変え得るのを理解するであろう。
ここに記載した抗体の変異は、例えば、米国特許第5364934号に示す保存的及び非保存的変異に関する技術及び指針のいずれかを用いて作成することができる。変異は、結果として天然配列抗体又はポリペプチドと比較してアミノ酸配列の変化を生じる、抗体をコードする一又は複数のコドンの置換、欠失又は挿入であってもよい。場合によっては、変異は、抗体の一つ又は複数のドメインにおける、少なくとも一つのアミノ酸の他の任意のアミノ酸との置換による。どのアミノ酸残基が所望の活性に悪影響を与えることなく挿入、置換又は欠失され得るかを確かめる指針は、抗体の配列を既知の相同タンパク質分子の配列と比較し、相同性の高い領域内で生じたアミノ酸配列変化の数を最小にすることによって見出される。アミノ酸置換は、一のアミノ酸を類似した構造及び/又は化学特性を持つ他のアミノ酸で置換すること、例えばロイシンのセリンでの置換、即ち保存的アミノ酸置換の結果であるとすることができる。挿入及び欠失は、場合によっては1から5のアミノ酸の範囲内であり得る。許容され得る変異は、配列にアミノ酸の挿入、欠失又は置換を系統的に作成し、生じた変異体を、親配列によって示される活性に関して試験することによって確かめられる。
抗体及びポリペプチド断片は、多くの従来技術のいずれかによって調製してもよい。所望のペプチド断片は化学合成してもよい。代替的方法には、酵素的消化、例えば特定のアミノ酸残基で確定した部位でタンパク質を切断することが知られた酵素によってタンパク質を処理することで、又は適当な制限酵素でDNAを消化して所望の断片を単離することによって抗体又はポリペプチド断片を生成することが含まれる。さらにその他の好適な技術には、ポリメラーゼ連鎖反応(PCR)によって、所望の抗体又はポリペプチド断片をコードするDNA断片を単離し増幅することが含まれる。DNA断片の所望の末端を確定するオリゴヌクレオチドは、PCRの5’及び3’プライマーで用いられる。好ましくは、抗体及びポリペプチド断片は、ここに開示した天然抗体又はポリペプチドと少なくとも1つの生物学的及び/又は免疫学的活性を共有する。
(1) 無極性: Ala (A), Val (V), Leu (L), Ile (I), Pro (P), Phe (F), Trp (W), Met (M)
(2)無電荷極性: Gly (G), Ser (S), Thr (T), Cys (C), Tyr (Y), Asn (N), Gln (Q)
(3)酸性: Asp (D), Glu (E)
(4)塩基性: Lys (K), Arg (R), His(H)
或いは、共通の側鎖特性に基づいて天然に発生する残基をグループ分けすることができる:
(1)疎水性: ノルロイシン、Met, Ala, Val, Leu, Ile;
(2)中性親水性: Cys, Ser, Thr, Asn, Gln;
(3)酸性: Asp, Glu;
(4)塩基性: His, Lys, Arg;
(5)鎖の方向に影響する残基: Gly, Pro;
(6)芳香性: Trp, Tyr, Phe
変異は、オリゴヌクレオチド媒介(部位特異的)突然変異誘発、アラニンスキャンニング、及びPCR突然変異誘発等のこの分野で知られた方法を用いてなすことができる。部位特異的突然変異誘発[Carter等, Nucl. Acids Res., 13: 4331 (1986); Zoller等, Nucl. Acids Res., 10: 6487 (1987)]、カセット突然変異誘発[Wells等, Gene, 34: 315 (1985)]、制限的選択突然変異誘発[Wells等, Philos. Trans. R. Soc. London SerA, 317: 415 (1986)]又は他の知られた技術をクローニングしたDNAに実施して、抗体又はポリペプチド変異体DNAを作成することもできる。
抗体又はポリペプチドの適切なコンフォメーションを維持することに関与していない任意のシステイン残基も、分子の酸化的安定性を向上させ、異常な架橋を防ぐために、概してセリンと置換され得る。逆に、抗体又はポリペプチドの安定性(特に、抗体がFv断片のような抗体断片)を向上させるために、それにシステイン結合(複数でも)を加えてもよい。
抗体のアミノ酸配列変異体をコードする核酸分子は、当該分野で周知の種々の方法によって調製される。これらの方法には、限定されるものではないが、オリゴヌクレオチド媒介(又は部位特異的)突然変異誘発、PCR突然変異誘発、そして抗体の早期に調製した変異体又は非変異体形のカセット突然変異誘発による、天然ソースからの単離(天然発生アミノ酸配列変異体の場合)又は調製が含まれる。
抗体及びポリペプチドの共有結合的修飾は本発明の範囲内に含まれる。共有結合的修飾の一型には、抗体又はポリペプチドの標的とするアミノ酸残基を、抗体又はポリペプチドの選択された側鎖又はN又はC末端残基と反応できる有機誘導体化試薬と反応させることが含まれる。二官能性試薬による誘導体化は、例えば抗体又はポリペプチドを、抗体の精製方法で用いる水不溶性支持体マトリクス又は表面と架橋させるために有用であり、その逆も同じである。通常用いられる架橋剤には、例えば、1,1-ビス(ジアゾアセチル)-2-フェニルエタン、グルタルアルデヒド、N-ヒドロキシスクシンイミドエステル、例えば4-アジドサリチル酸を有するエステル、3,3'-ジチオビス(スクシンイミジルプロピオネート)等のジスクシンイミジルエステルを含むホモ二官能性イミドエステル、ビス-N-マレイミド-1,8-オクタン等の二官能性マレイミド、及びメチル-3-[(p-アジドフェニル)-ジチオ]プロピオイミダート等の試薬が含まれる。
他の修飾には、グルタミニル及びアスパラギニル残基の各々対応するグルタミル及びアスパルチル残基への脱アミノ化、プロリン及びリシンのヒドロキシル化、セリル又はトレオニル残基のヒドロキシル基のリン酸化、リシン、アルギニン、及びヒスチジン側鎖のα-アミノ基のメチル化[T.E. Creighton, Proteins: Structure and Molecular Properties, W.H. Freeman & Co., San Francisco, pp.79-86 (1983)]、N末端アミンのアセチル化、及び任意のC末端カルボキシル基のアミド化を含む。
抗体及び他のポリペプチドのグリコシル化とは、典型的にはN-結合又はO-結合のいずれかである。N-結合とは、アスパラギン残基の側鎖への炭水化物部分の付与を指す。トリペプチドは、Xがプロリンを除く任意のアミノ酸である、アスパラギン-X-セリン及びアスパラギン-X-スレオニンの配列であり、アスパラギン側鎖への炭水化物部分が酵素的に付与される認識部位である。従って、ポリペプチドのこれらトリペプチド配列のいずれかの存在によって、潜在的なグリコシル化部位が作り出される。O-結合グリコシル化とは、5-ヒドロキシプロリン又は5-ヒドロキシリジンも用いられるが、殆どの場合にはセリン又はスレオニンへN-アセチルガラクトサミン、ガラクトース、又はキシロースのうちの一つの糖をヒドロキシアミノ酸へ付与することを指す。
抗体又はポリペプチドへのグリコシル化部位の付加は、アミノ酸配列を改変して、それが上記に記載のトリペプチド配列(N-結合グリコシル化部位について)の一つ又は複数を含むようにすることによって簡便に完遂できる。この改変は、また、最初の抗体又はポリペプチドの配列へ一つ又は複数のセリン又はスレオニン残基を付加、又は置換することによって生成される(O-結合グリコシル化部位について)。抗体又はポリペプチドアミノ酸配列は、DNAレベルでの変化を通して、特に、コドンが所望するアミノ酸へ翻訳される、あらかじめ選択した塩基での抗体又はポリペプチドをコードするDNAを変異させることによって、場合によっては改変され得る。
抗体又はポリペプチド上に存在する炭水化物部分の除去は、化学的又は酵素的に、あるいはグルコシル化の標的として提示されたアミノ酸残基をコードするコドンの変異的置換によってなすことができる。化学的脱グリコシル化技術は、この分野で知られており、例えば、Hakimuddin等, Arch. Biochem. Biophys., 259:52 (1987)によって、そしてEdge等, Anal. Biochem., 118: 131 (1981)によって記載されている。ポリペプチド上の炭水化物部分の酵素的切断は、Thotakura等, Meth. Enzymol. 138:350 (1987)に記載されているように、種々のエンド及びエキソグリコシダーゼを用いることにより達成される。
抗体又はポリペプチド共有結合的修飾の他の型は、抗体又はポリペプチドを種々の非タンパク質様ポリマーの1つ、例えばポリエチレングリコール(PEG)、ポリプロピレングリコール、又はポリオキシアルキレンへ、米国特許第4640835号;第4496689号;第4301144号;第4670417号;第4791192号又は第4179337号に記載された方法で結合させることをを含む。また、抗体又はポリペプチドは、例えばコアセルベーション法によって又は界面重合によって調製されたマイクロカプセル(例えば、それぞれヒドロキシメチルセルロース又はゼラチン-マイクロカプセル及びポリ-(メチルメタクリレート)マイクロカプセル)に、コロイド状薬物送達系(例えば、リポソーム、アルブミンミクロスフィア、マイクロエマルション、ナノ粒子及びナノカプセル)又はマクロエマルションで捕捉することができる。このような技術はRemington's Pharmaceutical Sciences, 16版, A. Oslo編(1980)に開示されている。
また、本発明の抗体又はポリペプチドは、その他の異種ポリペプチド又はアミノ酸配列と融合した抗体又はポリペプチドを含むキメラ分子が形成される方法で修飾されてもよい。
それに換わる実施形態では、キメラ分子は抗体又はポリペプチドの免疫グロブリン又は免疫グロブリンの特定領域との融合体を含んでもよい。キメラ分子の二価形態(「イムノアドヘシン」とも呼ばれる)については、そのような融合体はIgG分子のFc領域であり得る。Ig融合体は、好ましくはIg分子内の少なくとも1つの可変領域に換えて抗体又はポリペプチドの可溶化(膜貫通ドメイン欠失又は不活性化)形態を含む。特に好ましい実施形態では、免疫グロブリン融合体は、IgG分子のヒンジ、CH2及びCH3、又はヒンジ、CH1、CH2及びCH3領域を含む。免疫グロブリン融合体の製造については、1995年6月27日発行の米国特許第5428130号を参照のこと。
以下の説明は、主として、抗体及びポリペプチドコード化核酸を含むベクターで形質転換又は形質移入された細胞を培養することにより抗体及びポリペプチドを産生させる方法に関する。勿論、当該分野においてよく知られている他の方法を用いて抗体及びポリペプチドを調製することができると考えられている。例えば、適切なアミノ酸配列、又はその一部分を、固相技術を用いた直接ペプチド合成によって生成してもよい[例えば、Stewart等, Solid-Phase Peptide Synthesis, W.H. Freeman Co., サン フランシスコ, カリフォルニア(1969);Merrifield, J. Am. Chem. Soc., 85:2149-2154 (1963)参照]。手動技術又は自動を使用することによってインビトロタンパク質合成を行ってもよい。自動合成は、例えば、アプライド・バイオシステムズ・ペプチド合成機(フォスター シティー, カリフォルニア)を用いて、製造者の指示によって実施してもよい。抗体又はポリペプチドの種々の部分を別々に化学的に合成し、化学的又は酵素的方法を用いて結合させて所望する抗体又はポリペプチドを生成させてもよい。
抗体又はポリペプチドをコードするDNAは、抗体又はポリペプチドmRNAを保有していてそれを検出可能なレベルで発現すると考えられる組織から調製されたcDNAライブラリーから得ることができる。従って、ヒト抗体又はポリペプチドDNAは、ヒトの組織から調製されたcDNAライブラリーから簡便に得ることができる。また抗体又はポリペプチド-コード化遺伝子は、ゲノムライブラリーから又は公知の合成方法(例えば、自動核酸合成)により得ることもできる。
ライブラリーは、対象となる遺伝子あるいはその遺伝子によりコードされるタンパク質を同定するために設計されたプローブ(少なくとも約20-80塩基のオリゴヌクレオチド等)によってスクリーニングできる。選択されたプローブによるcDNA又はゲノムライブラリーのスクリーニングは、例えばSambrook等, Molecular Cloning: A Laboratory Manual(New York: Cold Spring Harbor Laboratory Press, 1989)に記載されている標準的な手順を使用して実施することができる。抗体又はポリペプチドをコードする遺伝子を単離する他の方法は、PCR法を使用するものである[Sambrook等,上掲;Dieffenbach等, PCR Primer:A Laboratory Manual(Cold Spring Harbor Laboratory Press, 1995)]。
このようなライブラリースクリーニング法において同定された配列は、GenBankらの公共データベース又は他の個人の配列データベースに寄託され利用可能となっている他の周知の配列と比較及びアラインメントすることができる。分子の決定された領域内の又は完全長配列に渡っての(アミノ酸又はヌクレオチドレベルのいずれかでの)配列同一性は、当該分野で知られた、及びここに記載した方法を用いて決定することができる。
タンパク質コード化配列を有する核酸は、初めてここで開示された推定アミノ酸配列を使用し、また必要ならば、cDNAに逆転写されていないmRNAの生成中間体及び先駆物質を検出する上掲のSambrook等に記述されているような従来のプライマー伸展法を使用して、選択されたcDNA又はゲノムライブラリーをスクリーニングすることによって得られる。
宿主細胞を、ここに記載した抗体又はポリペプチド生成のための発現又はクローニングベクターで形質移入又は形質転換し、プロモーターを誘導し、形質転換体を選択し、又は所望の配列をコードする遺伝子を増幅するために適当に変性された常套的栄養培地で培養する。培養条件、例えば培地、温度、pH等々は、過度の実験をすることなく当業者が選ぶことができる。一般に、細胞培養の生産性を最大にするための原理、プロトコール、及び実用技術は、Mammalian Cell Biotechnology: a Practical Approach, M.Butler編 (IRL Press, 1991)及び上掲のSambrook等に見出すことができる。
真核生物細胞形質移入及び原核生物細胞形質転換の方法、例えば、CaCl2、CaPO4、リポソーム媒介及びエレクトロポレーションは当業者に知られている。用いられる宿主細胞に応じて、その細胞に対して適した標準的な方法を用いて形質転換はなされる。前掲のSambrook等に記載された塩化カルシウムを用いるカルシウム処理又はエレクトロポレーションが、一般的に原核生物に対して用いられる。アグロバクテリウム・トゥメファシエンスによる感染が、Shaw等, Gene, 23:315(1983)及び1989年6月29日公開の国際公開89/05859に記載されているように、或る種の植物細胞の形質転換に用いられる。このような細胞壁のない哺乳動物の細胞に対しては、Graham及びvan der Eb, Virology, 52:456-457 (1978)のリン酸カルシウム沈降法が用いられる。哺乳動物細胞の宿主系形質転換の一般的な態様は米国特許第4,399,216号に記載されている。酵母菌中への形質転換は、典型的には、Van Solingen等, J. Bact., 130:946 (1977)及びHsiao等, Proc. Natl. Acad. Sci. (USA), 76:3829 (1979)の方法に従って実施される。しかしながら、DNAを細胞中に導入する他の方法、例えば、核マイクロインジェクション、エレクトロポレーション、無傷の細胞、又はポリカチオン、例えばポリブレン、ポリオルニチン等を用いる細菌プロトプラスト融合もまた用いることもできる。哺乳動物細胞を形質転換するための種々の技術については、Keown等, Methods in Enzymology, 185:527-537 (1990)及び Mansour等, Nature, 336:348-352 (1988)を参照のこと。
しかし、最大の関心は脊椎動物細胞に向けられ、培養(組織培養)した脊椎動物細胞の増殖がルーチン作業となった。有用な哺乳動物宿主細胞株の例は、SV40(COS−7,ATCC CRL1651)で形質転換させたサル腎CV1細胞株;ヒト胚芽腎細胞株(293又は懸濁培養で成長するようにサブクローン化された293細胞,Graham等,J.Gen Virol.,36:59 (1977));ベビーハムスター腎細胞(BHK,ATCC CCL10);チヤイニーズハムスター卵巣細胞/-DHFR(CHO,Urlaub等, Proc.Natl.Acad.Sci.USA 77:4216 (1980));マウスセルトリ細胞(TM4,Mather,Biol.Reprod.,23:243-251 (1980));サル腎細胞(CV1 ATCC CCL70);アフリカミドリザル腎細胞(VERO−76,ATCC CRL-1587);ヒト頚管腫瘍細胞(HELA,ATCC CCL2);イヌ腎細胞(MDCK,ATCC CCL34);バッファローラット肝細胞(BRL 3A,ATCC CRL1442);ヒト肺細胞(W138,ATCC CCL75);ヒト肝細胞(Hep G2,HB 8065);マウス乳房腫瘍細胞(MMT 060562,ATCC CCL51);TRI細胞(Mather等,Annals N.Y.Acad.Sci.,383:44-68 (1982));MRC5細胞;FS4細胞;及びヒト肝臓癌細胞(HepG2)である。
宿主細胞は、抗体又はポリペプチド生成のために上述の発現又はクローニングベクターで形質転換され、プロモーターを誘発し、形質転換体を選出し、又は所望の配列をコードする遺伝子を増幅するために適切に修正した通常の栄養培地で培養される。
抗体又はポリペプチドをコードする核酸(例えば、cDNA又はゲノムDNA)は、クローニング(DNAの増幅)又は発現のために複製可能なベクター内に挿入される。様々なベクターが公的に入手可能である。ベクターは、例えば、プラスミド、コスミド、ウイルス粒子、又はファージの形態とすることができる。適切な核酸配列が、種々の手法によってベクターに挿入される。一般に、DNAはこの分野で周知の技術を用いて適当な制限エンドヌクレアーゼ部位に挿入される。ベクター成分としては、一般に、これらに制限されるものではないが、一又は複数のシグナル配列、複製開始点、一又は複数のマーカー遺伝子、エンハンサーエレメント、プロモーター、及び転写終結配列を含む。これらの成分の一又は複数を含む適当なベクターの作成には、当業者に知られた標準的なライゲーション技術を用いる。
ポリペプチドは直接的に組換え手法によって生成されるだけではなく、シグナル配列あるいは成熟タンパク質あるいはポリペプチドのN-末端に特異的切断部位を有する他のポリペプチドである異種性ポリペプチドとの融合ペプチドとしても生成される。一般に、シグナル配列はベクターの成分であるか、ベクターに挿入される抗体又はポリペプチド-コード化DNAの一部である。シグナル配列は、例えばアルカリフォスファターゼ、ペニシリナーゼ、lppあるいは熱安定性エンテロトキシンIIリーダーの群から選択される原核生物シグナル配列であってよい。酵母の分泌に関しては、シグナル配列は、酵母インベルターゼリーダー、アルファ因子リーダー(酵母菌属(Saccharomyces)及びクリュイベロミセス(Kluyveromyces)α因子リーダーを含み、後者は米国特許第5,010,182号に記載されている)、又は酸ホスフォターゼリーダー、カンジダ・アルビカンス(C.albicans)グルコアミラーゼリーダー(1990年4月4日発行の欧州特許第362179号)、又は1990年11月15日に公開された国際公開90/13646に記載されているシグナルであり得る。哺乳動物細胞の発現においては、哺乳動物シグナル配列は、同一あるいは関連種の分泌ポリペプチド由来のシグナル配列並びにウイルス分泌リーダーのようなタンパク質の直接分泌に使用してもよい。
発現及びクローニングベクターは、典型的には、選べるマーカーとも称される選択遺伝子を含む。典型的な選択遺伝子は、(a)アンピシリン、ネオマイシン、メトトレキセートあるいはテトラサイクリンのような抗生物質あるいは他の毒素に耐性を与え、(b)栄養要求性欠陥を補い、又は(c)複合培地から得られない重要な栄養素を供給するタンパク質をコードしており、例えばバシリのD-アラニンラセマーゼをコードする遺伝子がある。
哺乳動物細胞に適切な選べるマーカーの例は、DHFRあるいはチミジンキナーゼのように、抗体又はポリペプチド-コード化核酸を取り込むことのできる細胞成分を同定することのできるものである。野生型DHFRを用いた場合の好適な宿主細胞は、Urlaub等により, Proc. Natl. Acad. Sci. USA, 77:4216 (1980)に記載されているようにして調製され増殖されたDHFR活性に欠陥のあるCHO株化細胞である。酵母菌中での使用に好適な選択遺伝子は酵母プラスミドYRp7に存在するtrp1遺伝子である[Stinchcomb等, Nature, 282:39(1979);Kingsman等, Gene, 7:141(1979);Tschemper等, Gene, 10:157(1980)]。trp1遺伝子は、例えば、ATCC番号44076あるいはPEP4-1のようなトリプトファンで成長する能力を欠く酵母菌の突然変異株に対する選択マーカーを提供する[Jones, Genetics, 85:12 (1977)]。
酵母宿主との使用に適したプロモーター配列の例としては、3-ホスホグリセラートキナーゼ[Hitzeman 等, J. Biol. Chem., 255:2073 (1980)]又は他の糖分解酵素[Hess 等, J. Adv. Enzyme Reg., 7:149 (1968);Holland, Biochemistry, 17:4900(1978)]、例えばエノラーゼ、グリセルアルデヒド-3-リン酸デヒドロゲナーゼ、ヘキソキナーゼ、ピルビン酸デカルボキシラーゼ、ホスホフルクトキナーゼ、グルコース-6-リン酸イソメラーゼ、3-ホスホグリセレートムターゼ、ピルビン酸キナーゼ、トリオセリン酸イソメラーゼ、ホスホグルコースイソメラーゼ、及びグルコキナーゼが含まれる。
他の酵母プロモーターとしては、成長条件によって転写が制御される付加的効果を有する誘発的プロモーターであり、アルコールデヒドロゲナーゼ2、イソチトクロムC、酸フォスファターゼ、窒素代謝と関連する分解性酵素、メタロチオネイン、グリセルアルデヒド-3-リン酸デヒドロゲナーゼ、及びマルトース及びガラクトースの利用を支配する酵素のプロモーター領域がある。酵母菌での発現に好適に用いられるベクターとプロモーターは欧州特許第73657号に更に記載されている。
より高等の真核生物による抗体又はポリペプチドをコードするDNAの転写は、ベクター中にエンハンサー配列を挿入することによって増強され得る。エンハンサーは、通常は約10から300塩基対で、プロモーターに作用してその転写を増強するDNAのシス作動要素である。哺乳動物遺伝子由来の多くのエンハンサー配列が現在知られている(グロビン、エラスターゼ、アルブミン、α-フェトプロテイン及びインスリン)。しかしながら、典型的には、真核細胞ウィルス由来のエンハンサーが用いられるであろう。例としては、複製開始点の後期側のSV40エンハンサー(100−270塩基対)、サイトメガロウィルス初期プロモーターエンハンサー、複製開始点の後期側のポリオーマエンハンサー及びアデノウィルスエンハンサーが含まれる。エンハンサーは、抗体又はポリペプチドコード化配列の5’又は3’位でベクター中にスプライシングされ得るが、好ましくはプロモーターから5’位に位置している。
また真核生物宿主細胞(酵母、真菌、昆虫、植物、動物、ヒト、又は他の多細胞生物由来の有核細胞)に用いられる発現ベクターは、転写の終結及びmRNAの安定化に必要な配列も含む。このような配列は、真核生物又はウィルスのDNA又はcDNAの通常は5’、時には3’の非翻訳領域から取得できる。これらの領域は、抗体又はポリペプチドをコードするmRNAの非翻訳部分にポリアデニル化断片として転写されるヌクレオチドセグメントを含む。
組換え脊椎動物細胞培養での抗体又はポリペプチドの合成に適応化するのに適切な他の方法、ベクター及び宿主細胞は、Gething等, Nature, 293:620-625 (1981); Mantei等, Nature, 281:40-46 (1979); 欧州特許第117060号;及び欧州特許第117058号に記載されている。
本発明の抗体又はポリペプチドを生成するために用いられる宿主細胞は種々の培地において培養することができる。市販培地の例としては、ハム(Ham)のF10(シグマ)、最小必須培地((MEM),シグマ)、RPMI-1640(シグマ)及びダルベッコの改良イーグル培地((DMEM),シグマ)が宿主細胞の培養に好適である。また、Ham等, Meth. Enz. 58:44 (1979), Barnes等, Anal. Biochem. 102:255 (1980), 米国特許第4767704号;同4657866号;同4927762号;同4560655号;又は同5122469号;国際公開第90/03430号;国際公開第87/00195号;又は米国特許再発行第30985号に記載された任意の培地も宿主細胞に対する培養培地として使用できる。これらの培地はいずれも、ホルモン及び/又は他の成長因子(例えばインスリン、トランスフェリン、又は表皮成長因子)、塩類(例えば、塩化ナトリウム、カルシウム、マグネシウム及びリン酸塩)、バッファー(例えばHEPES)、ヌクレオシド(例えばアデノシン及びチミジン)、抗生物質(例えば、ゲンタマイシン(商品名)薬)、微量元素(マイクロモル範囲の最終濃度で通常は存在する無機化合物として定義される)及びグルコース又は同等のエネルギー源を必要に応じて補充することができる。任意の他の必要な補充物質もまた当業者に知られている適当な濃度で含まれてもよい。培養条件、例えば温度、pH等々は、発現のために選ばれた宿主細胞について以前から用いられているものであり、当業者には明らかであろう。
遺伝子の増幅及び/又は発現は、ここで提供された配列に基づき、適切に標識されたプローブを用い、例えば、従来よりのサザンブロット法、mRNAの転写を定量化するノーザンブロット法[Thomas, Proc. Natl. Acad. Sci. USA,77:5201-5205 (1980)]、ドットブロット法(DNA分析)、又はインサイツハイブリダイゼーションによって、直接的に試料中で測定することができる。あるいは、DNA二本鎖、RNA二本鎖、及びDNA−RNAハイブリッド二本鎖又はDNA-タンパク二本鎖を含む、特異的二本鎖を認識することができる抗体を用いることもできる。ついで、抗体を標識し、アッセイを実施することができ、ここで二本鎖は表面に結合しており、その結果、表面での二本鎖の形成の時点でその二本鎖に結合した抗体の存在を検出することができる。
あるいは、遺伝子の発現は、遺伝子産物の発現を直接的に定量化する免疫学的な方法、例えば細胞又は組織切片の免疫組織化学的染色及び細胞培養又は体液のアッセイによって、測定することもできる。試料液の免疫組織化学的染色及び/又はアッセイに有用な抗体は、モノクローナルでもポリクローナルでもよく、任意の哺乳動物で調製することができる。簡便には、抗体は、天然配列ポリペプチドに対して、又はここで提供されるDNA配列をベースとした合成ペプチドに対して、又はポリペプチドDNAに融合し特異的抗体エピトープをコードする外因性配列に対して調製され得る。
抗体及びポリペプチドの形態は、培地又は宿主細胞の溶菌液から回収することができる。膜結合性であるならば、適切な洗浄液(例えばトリトン-X100)を用いて又は酵素的切断により膜から引き離すことができる。抗体及びポリペプチドの発現に用いられる細胞は、凍結融解サイクル、超音波処理、機械的破壊、又は細胞溶解剤などの種々の化学的又は物理的手段によって破壊することができる。
抗体及びポリペプチドは、組換え細胞タンパク又はポリペプチドから精製することが望ましい。適切な精製手順の例である次の手順により精製される:すなわち、イオン交換カラムでの分画;エタノール沈殿;逆相HPLC;シリカ又はカチオン交換樹脂、例えばDEAEによるクロマトグラフィー;クロマトフォーカシング;SDS-PAGE;硫酸アンモニウム沈殿;例えばセファデックスG-75を用いるゲル濾過;IgGのような汚染物を除くプロテインAセファロースカラム;及び抗体及びポリペプチドのエピトープタグ形態を結合させる金属キレート化カラムである。この分野で知られ、例えば、Deutscher, Methods in Enzymology, 182 (1990);Scopes, Protein Purification: Principles and Practice, Springer-Verlag, New York (1982)に記載された多くのタンパク質精製方法を用いることができる。選ばれる精製過程は、例えば、用いられる生成方法及び特に生成される特定の抗体又はポリペプチドの性質に依存する。
細胞から調製した抗体組成物は、例えば、ヒドロキシルアパタイトクロマトグラフィー、ゲル電気泳動、透析、及びアフィニティクロマトグラフィーを用いて精製でき、アフィニティクロマトグラフィーが好ましい精製技術である。アフィニティリガンドとしてのプロテインAの適合性は抗体に存在する免疫グロブリンFc領域の種及びアイソタイプに依存する。プロテインAは、ヒトγ1、γ2、又はγ4重鎖に基づく抗体の精製に用いることができる(Lindmark等, J. Immunol. Meth. 62: 1-13 [1983])。プロテインGは、全てのマウスアイソタイプ及びヒトγ3に推奨されている(Guss等, EMBO J. 5: 15671575 [1986])。アフィニティリガンドが結合されるマトリクスはアガロースであることが最も多いが、他の材料も使用可能である。孔制御ガラスやポリ(スチレンジビニル)ベンゼン等の機械的に安定なマトリクスは、アガロースで達成できるものより早い流速及び短い処理時間を可能にする。抗体がCH3ドメインを含む場合、Bakerbond ABX(商標)樹脂(J.T. Baker, Phillipsburg, NJ)が精製に有用である。イオン交換カラムでの分画、エタノール沈殿、逆相HPLC、シリカ上のクロマトグラフィー、アニオン又はカチオン交換樹脂(ポリアスパラギン酸カラム)上でのヘパリンSEPHAROSE(商品名)クロマトグラフィー、クロマトフォーカシング、SDS-PAGE、及び硫酸アンモニウム沈殿などの他のタンパク質精製技術も、回収される抗体に応じて利用可能である。
任意の予備精製工程に続いて、対象とする抗体と汚染物とを含む混合物に、約2.5−4.5のpHでの溶離バッファーを用いて、低pH疎水性相互作用クロマトグラフィーを施してもよく、好ましくは低い塩濃度(例えば、約0−0.25M塩)で実施される。
本発明に係る抗体、結合オリゴペプチド、結合有機又は無機小分子及び/又は本発明で用いられるポリペプチドの治療的製剤は、所望される程度の純度を持つ抗体、ポリペプチド、オリゴペプチド又は有機/無機小分子を凍結乾燥製剤又は水性溶液の形態で、最適な製薬上許容される担体、賦形剤又は安定化剤と混合することにより調製され保存される(Remington's Pharmaceutical Sciences 16th 版, Osol, A. 編. [1980])。許容される担体、賦形剤、又は安定化剤は、用いられる用量及び濃度で受容者に非毒性であり、酢酸、Tris、リン酸、クエン酸、及び他の有機酸などの緩衝液;アスコルビン酸及びメチオニンを含む酸化防止剤;防腐剤(オクタデシルジメチルベンジルアンモニウムクロライド;ヘキサメトニウムクロライド;ベンズアルコニウムクロライド、ベンズエトニウムクロライド;フェノール、ブチル又はベンジルアルコール;メチル又はプロピルパラベン等のアルキルパラベン;カテコール;レゾルシノール;シクロヘキサノール;3-ペンタノール;及びm-クレゾールなど);低分子量(約10残基未満)ポリペプチド;血清アルブミン、ゼラチン、又は免疫グロブリン等のタンパク質;ポリビニルピロリドン等の親水性ポリマー;グリシン、グルタミン、アスパラギン、ヒスチジン、アルギニン、又はリジン等のアミノ酸;グルコース、マンノース、又はデキストリンを含む単糖類、二糖類、及び他の炭水化物;EDTA等のキレート剤;トレハロース及び塩化ナトリウムなどのトニシファイヤー;スクロース、マンニトール、トレハロース又はソルビトールなどの糖;ポリソルベート等の界面活性剤;ナトリウムなどの塩形成対イオン;金属錯体(例えば、Zn-タンパク質錯体);及び/又はトゥイーン(TWEEN)(登録商標)、プルロニクス(PLURONICS)(登録商標)、又はポリエチレングリコール(PEG)等の非イオン性界面活性剤を含む。抗体は、好ましくは5−200mg/mlの間、好ましくは10−100mg/mlの間の濃度の抗体で構成される。
また、活性成分は、例えばコアセルベーション技術により又は界面重合により調製されたマイクロカプセル、例えば、各々ヒドロキシメチルセルロース又はゼラチン-マイクロカプセル及びポリ(メタクリル酸メチル)マイクロカプセル中、コロイド状薬物送達系(例えば、リポソーム、アルブミン小球、マイクロエマルション、ナノ粒子及びナノカプセル)中、又はマイクロエマルション中に包括されていてもよい。これらの技術は、Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980)に開示されている。
徐放性製剤を調製してもよい。徐放性製剤の好適な例は、抗体を含有する固体疎水性ポリマーの半透性マトリクスを含み、このマトリクスは成形された物品、例えばフィルム、又はマイクロカプセルの形状である。徐放性マトリクスの例には、ポリエステル、ヒドロゲル(例えば、ポリ(2-ヒドロキシエチル-メタクリレート)又はポリ(ビニルアルコール))、ポリアクチド(米国特許第3773919号)、L-グルタミン酸及びγエチル-L-グルタメートのコポリマー、非分解性エチレン-酢酸ビニル、LUPRON DEPOT(登録商標)(乳酸-グリコール酸コポリマーと酢酸リュープロリドの注射可能な小球)などの分解性乳酸-グリコール酸コポリマー、ポリ-(D)-(-)-3-ヒドロキシブチル酸が含まれる。
インビボ投与に使用される製剤は無菌でなければならない。これは、滅菌濾過膜を通した濾過により容易に達成される。
癌におけるポリペプチド(ヘプシン及び/又はHGF)発現を定量するために、種々の検出アッセイが利用可能である。一実施形態では、ポリペプチド過剰発現は、免疫組織化学(IHC)によって分析される。腫瘍生検からのパラフィン包埋組織切片をIHCアッセイへ供してもよいし、次のようなポリペプチド染色強度基準と合致させてもよい:
スコア0 - 染色が観察されないか、又は膜染色が腫瘍細胞の10%未満で観察される。
スコア1+ - わずかに/弱く認知できる程度の膜染色が腫瘍細胞の10%を越えて検出される。細胞はそれらの膜の一部のみが染色される。
スコア2+ - 弱いないしは中程度の完全な膜染色が腫瘍細胞の10%を越えて観察される。
スコア3+ - 中程度から強い完全な膜染色が腫瘍細胞の10%を越えて観察される。
ポリペプチド発現に関して0又は1+スコアの腫瘍は、ポリペプチドが過剰発現していないことを特徴としうるものであるのに対し、2+又は3+スコアの腫瘍はポリペプチドが過剰発現していることを特徴としうる。
ポリペプチド過剰発現又は増幅は、インビボ検出アッセイを使用して評価することができ、例えば検出される分子に結合し、検出可能な標識(例えば、放射性同位体又は蛍光標識)が付けられた分子(例えば抗体、オリゴペプチド又は有機小分子)を投与し、標識の局在化について患者を外部スキャニングする。
上に記載したように、本発明の抗体、オリゴペプチド又は有機小分子には、種々の非治療的用途がある。本発明の抗体、オリゴペプチド又は有機/無機小分子は、ポリペプチドを発現している癌の染色にとって有用である(例えば、ラジオイメージングで)。他の細胞の精製の工程として、混合細胞の集団からポリペプチド発現細胞を死滅させて除去するために、この抗体、オリゴペプチド又は有機小分子は、また、例えば、ELISA又はウェスタンブロットにおいて、インビトロでポリペプチドの検出及び定量化のために、細胞からポリペプチドを精製又は免疫沈降するのに有用である。
抗体、オリゴペプチド又は有機/無機小分子又はその免疫コンジュゲートは、公知の方法、例えばボーラス、もしくは一定時間にわたる連続注入による静脈内投与、筋肉内、腹腔内、脳脊髄内、皮下、関節内、滑液包内、くも膜下腔内、経口、局所的、又は吸入経路により、ヒトの患者に投与される。抗体、オリゴペプチド又は有機小分子の静脈内又は皮下投与が好ましい。
他の治療計画を抗体、オリゴペプチド又は有機/無機小分子の投与と組合せてもよい。組合せ投与には、別々の製剤又は単一の医薬製剤を使用する同時投与、及び好ましくは両方(又は全ての)活性剤が同時にその生物学的活性を働かせる時間があるいずれかの順での連続投与が含まれる。このような組合せ治療により、結果として相乗的治療効果が生じることが好ましい。
他の実施形態では、本発明の治療方法は、異なる化学療法剤の混合物の同時投与を含む、抗体(一又は複数)、オリゴペプチド又は有機/無機小分子と一又は複数の化学療法剤又は成長阻害剤との組合せ投与を含む。化学療法剤には、リン酸エストラムスチン、プレドニムスチン、シスプラチン、5-フルオロウラシル、メルファラン、シクロホスファミド、ヒドロキシ尿素及びヒドロキシ尿素タキサン類(hydroxyureataxanes)(例えばパクリタキセル及びドキセタキセル)及び/又はアントラサイクリン抗生物質が含まれる。このような化学療法剤の調製及び投与スケジュールは製造者の注意書きに従い使用されるか、又は熟練した実務者により経験的に決定される。このような化学療法の調製及び投与スケジュールは、Chemotherapy Service編 M.C.Perry, Williams & Wilkins, Baltimore, MD(1992)にも記載されている。
抗体、オリゴペプチド又は有機/無機小分子は、抗ホルモン化合物;例えばタモキシフェン等の抗-エストロゲン化合物;抗-プロゲステロン、例えばオナプリストン(onapristone)(欧州特許第616812号を参照);又は抗アンドロゲン、例えばフルタミドを、このような分子に対して既知の用量で組合せてもよい。治療される癌がアンドロゲン非依存性癌である場合、患者は予め抗アンドロゲン治療を受け、癌がアンドロゲン非依存性になった後、抗体、オリゴペプチド又は有機/無機小分子(及び場合によってはここに記載した他の薬剤)を患者に投与してもよい。
疾患の予防又は治療のための投与量及び方式は、公知の基準に従い、医師により選択されるであろう。抗体、オリゴペプチド又は有機/無機小分子の適切な用量は、上記のような治療される疾患の種類、疾患の重症度及び過程、抗体、オリゴペプチド又は有機/無機小分子を予防目的で投与するのか治療目的で投与するのか、過去の治療、患者の臨床歴及び抗体、オリゴペプチド又は有機/無機小分子の応答性、手当てをする医師の裁量に依存するであろう。抗体、オリゴペプチド又は有機/無機小分子は一度に又は一連の処置にわたって患者に適切に投与される。好ましくは、抗体、オリゴペプチド又は有機/無機小分子は静脈注入又は皮下注射により投与される。疾患の種類及び重症度に応じて、例えば一又は複数の別個の投与又は連続注入のいずれであれ、体重1kg当たり約1μgないし50mg(例えば0.1−15mg/kg/用量)の抗体を患者への最初の投与量の候補とすることができる。投薬計画は、約4mg/kgの初期負荷量、続いて1週間に約2mg/kgの維持用量の抗体を投与することからなってよい。しかしながら、他の投薬計画も有効であろう。上述した因子に応じて、典型的な一日の投与量は約1μg/kgから100mg/kgあるいはそれ以上の範囲である。数日間又はそれ以上の繰り返し投与の場合、状態によっては、疾患の徴候の望ましい抑制が生じるまで処置を維持する。この治療の進行状態は、医師又は他の当業者に公知の基準をベースにした通常の方法やアッセイで容易にモニターされる。
核酸(場合によってはベクター内に含まれたもの)を患者の細胞に入れるために:インビボ及びエキソビボという2つの主要な方法がある。インビボ送達では、核酸は、通常は抗体が必要とされている部位に直接注入される。エキソビボ処理では、患者の細胞を取り出し、核酸をこれらの単離された細胞に導入し、修飾された細胞を患者に、直接、又は例えば患者に埋め込まれる多孔性膜にカプセル化して投与する(米国特許第4892538号及び第5283187号参照)。核酸を生細胞に導入するために利用可能な種々の技術がある。これらの技術は、核酸が培養された細胞にインビトロで移入されるか、又は対象とする宿主にインビボで移入されるかによって異なる。哺乳動物細胞にインビトロで核酸を移入するのに適した技術は、リポソーム、エレクトロポレーション、マイクロインジェクション、細胞融合、DEAE-デキストラン、リン酸カルシウム沈降法などの使用を含む。遺伝子のエキソビボ送達に通常用いられるベクターはレトロウイルスベクターである。
本発明の抗体は、ここでの「抗体」の定義により包含される様々な形態であってよい。よって、抗体には、完全長又は無傷抗体、抗体断片、天然配列抗体又はアミノ酸変異体、ヒト化、キメラ又は融合抗体、免疫コンジュゲート、及びそれらの機能的断片が含まれる。融合抗体において、抗体配列は異種ポリペプチド配列に融合している。抗体はFc領域が修飾されて、所望のエフェクター機能を提供することができる。以下の段落に詳細に記載されるように、適切なFc領域と共に、細胞表面に結合したそのままの抗体は、例えば抗体-依存性細胞障害(ADCC)を介して又は補体依存性細胞障害において補体を補充することにより、又は他のいくつかのメカニズムにより、細胞障害性を誘発し得る。また、副作用及び治療による合併症を最小にするようにエフェクター機能を除去又は低減することが望ましい場合には、所定の他のFc領域が使用される。
一実施形態では、抗体は、本発明の抗体と同じエピトープとの結合に関して競合するか、又はこれに実質的に結合する。また、本発明の該抗体の生物学的特徴を有する抗体、特にインビボ腫瘍ターゲティング及び任意の細胞増殖阻害又は細胞障害特性を含むものが考察される。
上述した抗体の産生方法をここで詳細に記載する。
本発明の他の態様は、抗体をコードする単離された核酸分子である。H及びL鎖、特に高頻度可変領域残基をコードする核酸、天然配列抗体及び変異体をコードする鎖、該抗体の修飾体及びヒト化形態を含む。
本発明は、抗体、オリゴペプチド又は有機/無機小分子を治療的有効量、哺乳動物に投与することを含む、哺乳動物における癌の治療又は癌の一又は複数の徴候を緩和するのに有用な方法を提供する。抗体、オリゴペプチド又は有機/無機小分子治療組成物は、医師の指示通りに、短い期間(急性)又は慢性的に、又は間欠的に投与することができる。また、ポリペプチド(ヘプシン及び/又はHGF)を発現する細胞及び/又はポリペプチド(ヘプシン及び/又はHGF)に応答する細胞の成長を阻害し、該細胞を殺傷する方法も提供される。
本発明は少なくとも一つの抗体、オリゴペプチド又は有機/無機小分子を含有するキット又は製造品も提供する。抗体、オリゴペプチド又は有機/無機小分子を含有するキットは、例えば細胞殺傷アッセイ、細胞からのポリペプチドの精製又は免疫沈降における用途が見出されている。例えば、ポリペプチドの単離及び精製のためには、キットはビーズ(例えばセファロースビース)に結合した抗体、オリゴペプチド又は有機/無機小分子を含有することができる。インビトロにおけるポリペプチドの検出及び定量化、例えばELISA又はウェスタンブロットにおける抗体、オリゴペプチド又は有機/無機小分子を含有するキットを提供することもできる。検出に有用なこのような抗体、オリゴペプチド又は有機/無機小分子は、蛍光又は放射標識などの標識が付されて提供され得る。
本発明の他の実施形態は、非ホジキンリンパ腫等のポリペプチド(ヘプシン及び/又はHGF)発現癌の治療に有用な物質を含有する製造品である。この製造品は容器と容器に付与又は添付されるラベル又はパッケージ挿入物を含んでなる。好適な容器は、例えば、ビン、バイアル、シリンジ等を含む。容器は、ガラス又はプラスチックなどの多様な材料から形成されてよい。容器は、癌の状態の治療に有効な組成物を収容し、無菌のアクセスポートを有し得る(例えば、容器は皮下注射針で貫通可能なストッパーを有する静脈内溶液バッグ又はバイアルであってよい)。組成物中の少なくとも一つの活性剤は本発明の抗体、オリゴペプチド又は有機/無機小分子である。ラベル又はパッケージ挿入物は、組成物が癌の治療のために使用されることを示す。ラベル又はパッケージ挿入物は、癌患者に抗体、オリゴペプチド又は有機/無機小分子組成物を投与する際の注意書きをさらに含む。製造品はさらに、製薬的に許容可能なバッファー、例えば注射用の静菌水(BWFI)、リン酸緩衝塩水、リンガー液及びデキストロース溶液を含む第2の容器を具備してもよい。さらに、他のバッファー、希釈剤、フィルター、針及びシリンジを含む商業的及び使用者の見地から望ましい他の材料を含んでもよい。
種々の目的、例えばポリペプチド発現又は細胞殺傷アッセイ、細胞からのポリペプチドの精製又は免疫沈降に有用なキットも提供される。ポリペプチドの単離及び精製において、キットはビーズ(例えばセファロースビーズ)に結合した抗体、オリゴペプチド又は有機/無機小分子を含むことが可能である。インビトロにおけるポリペプチドの検出及び定量化、例えばELISA又はウエスタンブロットのための抗体、オリゴペプチド又は有機/無機小分子を含むキットを提供することもできる。製造品と同様、キットも容器と容器に付与又は添付されるラベル又は能書を含んでなる。容器には少なくとも1つの本発明の抗体、オリゴペプチド又は有機/無機小分子を含有する組成物が収容されている。希釈液及びバッファー、コントロール抗体等を収容する付加的な容器を具備していてもよい。ラベル又は能書は、組成物についての記載、並びに意図するインビトロ又は診断での使用に関する注意書きを提供するものである。
ポリペプチドをコードする核酸配列(又はそれらの相補鎖)は、ハイブリダイゼーションプローブとしての使用を含む分子生物学の分野において、染色体及び遺伝子マッピングにおいて、及びアンチセンスRNA及びDNAプローブの生成において種々の用途を有している。また、ポリペプチドコード化核酸は、ここに記載される組換え技術によるポリペプチドの調製に有用であり、これらポリペプチドは、例えば、ここで記載の抗体の調製において用途を見出し得る。
完全長天然配列ポリペプチド遺伝子又はその一部は、ここに開示した天然ポリペプチド配列に対して所望の配列同一性を持つ他のcDNA(例えば、天然に生じる変異体又は他の種からのポリペプチドをコードするもの)の単離のために、cDNAライブラリ用のハイブリダイゼーションプローブとして使用できる。場合によっては、プローブの長さは約20〜約50塩基である。このハイブリダイゼーションプローブは、少なくとも部分的に完全長天然ヌクレオチド配列の新規な領域から誘導してもよく、それらの領域は、過度の実験をすることなく、天然配列ポリペプチドのプロモーター、エンハンサー成分及びイントロンを含むゲノム配列から判定され得る。例えば、スクリーニング法は、ポリペプチド遺伝子のコード化領域を周知のDNA配列を用いて単離して約40塩基の選択されたプローブを合成することを含む。ハイブリダイゼーションプローブは、32P又は35S等の放射性ヌクレオチド、又はアビジン/ビオチン結合系を介してプローブに結合したアルカリホスファターゼ等の酵素標識を含む種々の標識で標識され得る。本発明のポリペプチド遺伝子の配列に相補的な配列を有する標識されたプローブは、ヒトcDNA、ゲノムDNA又はmRNAのライブラリーをスクリーニングし、そのライブラリーの何れのメンバーにプローブがハイブッド形成するかを決定するのに使用できる。ハイブリダイゼーション技術を、以下の実施例において更に詳細に記載する。本出願に開示されている任意のEST配列は、ここに開示している方法を利用して、同じようにプローブとして用い得る。
アンチセンス又はセンスオリゴヌクレオチドの標的核酸配列への結合は二重鎖の形成をもたらし、それは、二重鎖の分解の促進、転写又は翻訳の未熟終止を含む幾つかの方法の一つ、又は他の方法により、標的配列の転写又は翻訳を阻止する。そのような方法は、本発明に含まれている。よって、アンチセンスオリゴヌクレオチドは、タンパク質の発現を阻止するのに用いられ、それらタンパク質は、哺乳動物での癌の誘導を担い得る。アンチセンス又はセンスオリゴヌクレオチドは、修飾糖−ホスホジエステル骨格(又は他の糖結合、国際公開91/06629に記載のもの等)を有するオリゴヌクレオチドを更に含み、そのような糖結合は内因性ヌクレアーゼ耐性である。そのような耐性糖結合を持つオリゴヌクレオチドは、インビボで安定であるが(つまり、酵素分解に耐えうるが)、標的ヌクレオチド配列に結合できる配列特異性は保持している。
好適なアンチセンスオリゴヌクレオチドはホスホロチオネート骨格及び/又はヘテロ原子骨格、特に-CH2-NH-O-CH2-、-CH2-N(CH3)-O-CH2-[メチレン(メチルイミノ)又はMMI骨格として知られる]、-CH2-O-N(CH3)-CH2-、-CH2-N(CH3)-N(CH3)-CH2-、及び上で参照した米国特許第5489677号に記載された-O-N(CH3)-CH2-CH2-[ここで天然ホスホジエステル骨格は-O-P-O-CH2-と表される]及び上で参照された米国特許第5602240号のアミド骨格を含む。また好ましいものは上で参照した米国特許第5034506号のモルホリノ骨格構造を有するアンチセンスオリゴヌクレオチドである。
他の好適な修飾は2'-メトキシ(2'-O-CH3)、2'-アミノプロポキシ(2'-OCH2CH2CH2NH2)、2'-アリル(2'-CH2-CH=CH2)、2'-O-アリル(2'-O-CH2-CH=CH2)及び2'-フルオロ(2'-F)を含む。2'-修飾はアラビノ(上)位置又はリボ(下)位置においてでありうる。好適な2'-アラビノ修飾は2'-Fである。同様の修飾はまたオリゴヌクレオチドの他の位置、特に3'末端ヌクレオチドの糖の3'位又は2'−5'結合オリゴヌクレオチド及び5'末端ヌクレオチドの5'位になすことができる。オリゴヌクレオチドはまたペントフラノシル糖の代わりにシクロブチル部分のような糖擬態体を有しうる。そのような修飾糖構造の調製を教唆する代表的な米国特許には、限定されるものではないが、米国特許4981957;5118800;5319080;5359044;5393878;5446137;5466786;5514785;5519134;5567811;5576427;5591722;5597909;5610300;5627053;5639873;5646265;5658873;5670633;5792747;及び5700920が含まれ、その各々は出典明示により全体がここに取り込まれる。
アンチセンス又はセンスオリゴヌクレオチドは、例えば、CaPO4-媒介DNAトランスフェクション、エレクトロポレーションを含む任意の遺伝子転換方法により、又はエプスタイン-バーウイルスなどの遺伝子転換ベクターを用いることにより、標的核酸配列を含む細胞に導入される。好ましい方法では、アンチセンス又はセンスオリゴヌクレオチドは、適切なレトロウイルスベクターに挿入される。標的核酸配列を含む細胞は、インビボ又はエキソビボで組換えレトロウイルスベクターに接触させる。好適なレトロウイルスベクターは、これらに限られないが、マウスレトロウイルスM-MuLVから誘導されるもの、N2(M-MuLVから誘導されたレトロウイルス)、又はDCT5A、DCT5B及びDCT5Cと命名されたダブルコピーベクター(国際公開90/13641参照)を含む。
あるいは、センス又はアンチセンスオリゴヌクレオチドは、国際公開90/10448に記載されたように、オリゴヌクレオチド−脂質複合体の形成により標的核酸配列を含む細胞に導入してもよい。センス又はアンチセンスオリゴヌクレオチド−脂質複合体は、好ましくは内因性リパーゼにより細胞内で分解される。
また、プローブをPCR技術に用いて、密接に関連したポリペプチドコード化配列の同定のための配列のプールを作成することができる。
また、ポリペプチドをコードするヌクレオチド配列は、そのポリペプチドをコードする遺伝子のマッピングのため、及び遺伝子疾患を持つ個体の遺伝子分析のためのハイブリダイゼーションプローブの作成にも用いることができる。ここに提供されるヌクレオチド配列は、インサイツハイブリダイゼーション、既知の染色体マーカーに対する連鎖分析、及びライブラリーでのハイブリダイゼーションスクリーニング等の周知の技術を用いて、染色体及び染色体の特定領域にマッピングすることができる。
また、ポリペプチド又はその修飾型をコードする核酸は、トランスジェニック動物又は「ノックアウト」動物のいずれかを産生することに使用でき、これらは治療的に有用な試薬の開発やスクリーニングに有用である。トランスジェニック動物(例えばマウス又はラット)とは、出生前、例えば胚段階で、その動物又はその動物の祖先に導入された導入遺伝子を含む細胞を有する動物である。導入遺伝子とは、トランスジェニック動物が発生する細胞のゲノムに組み込まれたDNAである。一実施形態では、ポリペプチドをコードするcDNAは、ポリペプチドをコードするDNAを発現する細胞を含むトランスジェニック動物を作製するために使用するゲノム配列及び確立された技術に基づいて、ポリペプチドをコードするゲノムDNAをクローン化するために使用することができる。トランスジェニック動物、特にマウス又はラット等を産生する方法は、当該分野において常套的になっており、例えば米国特許第4736866号や第4870009号に記述されている。典型的には、特定の細胞を組織特異的エンハンサーでのポリペプチド導入遺伝子の導入の標的にする。胚段階で動物の生殖系列に導入されたポリペプチドをコードする導入遺伝子のコピーを含むトランスジェニック動物はポリペプチドをコードするDNAの増大した発現の影響を調べるために使用できる。このような動物は、例えばその過剰発現を伴う病理学的状態に対して保護をもたらすと思われる試薬のテスター動物として使用できる。本発明のこの態様においては、動物を試薬で治療し、導入遺伝子を有する未治療の動物に比べ病理学的状態の発症率が低ければ、病理学的状態に対する治療上の処置の可能性が示される。
また、ポリペプチドをコードする核酸は遺伝子治療にも使用できる。遺伝子治療用途においては、例えば欠陥遺伝子を置換するため、治療的に有効な遺伝子産物のインビボ合成を達成するために遺伝子が細胞内に導入される。「遺伝子治療」とは、1回の処理により継続的効果が達成される従来の遺伝子治療と、治療的に有効なDNA又はmRNAの1回又は繰り返し投与を含む遺伝子治療薬の投与の両方を含む。アンチセンスRNA及びDNAは、ある種の遺伝子のインビボ発現を阻止する治療薬として用いることができる。短いアンチセンスオリゴヌクレオチドを、細胞膜による制限された取り込みに起因する低い細胞内濃度にもかかわらず、それが阻害剤として作用する細胞中に移入できることは既に示されている(Zamecnik等, Proc. Natl. Acad. Sci. USA 83:4143-4146 [1986])。オリゴヌクレオチドは、それらの負に荷電したリン酸ジエステル基を非荷電基で置換することによって取り込みを促進するように修飾してもよい。
ここに記載したポリペプチド又はその断片をコードする核酸分子は、染色体の同定に有用である。この点において、実際の配列データに基づく染色体マーキング試薬は殆ど利用可能ではないため、目下のところ新規な染色体マーカーの同定の必要である。本発明の各核酸分子は染色体マーカーとして使用できる。
本発明のポリペプチド及び核酸分子は組織タイピングの診断に使用でき、ポリペプチドは、その他の組織と比較して1つの組織において、好ましくは同じ組織型の正常組織に比較して疾患性組織において特異的に発現する。核酸分子には、PCR、ノーザン分析、サザン分析及びウェスタン分析のプローブ生成のための用途が見出されるであろう。
このアッセイは、タンパク質-タンパク質結合アッセイ、生化学スクリーニングアッセイ、免疫アッセイ、そして細胞ベースアッセイを含む、当該分野で良く特徴付けられている種々の形式で行うことができる。
アンタゴニストに関する全てのアッセイは、薬候補をここで同定された核酸によってコードされているポリペプチドと、これら両成分が相互作用するのに十分な条件下及び時間にわたって接触させることを必要とする点で共通である。
アンタゴニストを検定するために、ポリペプチドを、特定の活性についてスクリーニングされる化合物とともに細胞に添加してもよく、ポリペプチド存在下で対象とする活性を阻害する当該化合物の能力が、当該化合物がポリペプチドのアンタゴニストであることを示す。あるいは、アンタゴニストは、ポリペプチド及び潜在的アンタゴニストを、膜結合ポリペプチドレセプター又はコード化されたレセプターと、競合的阻害アッセイに適した条件下で結合させることにより検出してもよい。ポリペプチドは、放射活性等で標識でき、レセプターに結合したポリペプチド分子の数を潜在的アンタゴニストの有効性を決定するのに使用できる。レセプターをコードする遺伝子は、当業者に知られた多くの方法、例えばリガンドパニング及びFACSソーティングにより同定できる。Coligan等, Current Protocols in Immun., 1(2): Chapter 5 (1991)。好ましくは発現クローニングが用いられ、そこではポリアデニル化RNAがポリペプチドに反応性の細胞から調製され、このRNAから生成されたcDNAライブラリがプールに分配され、COS細胞又は他のポリペプチドに反応性でない細胞の形質移入に使用される。スライドガラスで成長させた形質移入細胞を、標識したポリペプチドへ曝露する。ポリペプチドは、ヨウ素化又は部位特異的タンパク質キナーゼの認識部位の包含を含む種々の手段で標識できる。固定及びインキュベーションの後、スライドにオートラジオグラフ分析を施す。ポジティブプールを同定し、対話型サブプール化及び再スクリーニング法を用いてサブプールを調製して再形質移入し、最終的に推定レセプターをコードする単一のクローンを生成する。
アンタゴニストの他の検定では、レセプターを発現する哺乳動物細胞又は膜調製物を、候補化合物の存在下で標識ポリペプチドとともにインキュベートする。次いで、この相互作用を促進又は阻止する化合物の能力を測定する。
潜在的なアンタゴニストのより特別な例は、免疫グロブリンとポリペプチドとの融合体に結合するオリゴヌクレオチド、特に、限られないが、ポリ-及びモノクローナル抗体及び抗体断片、一本鎖抗体、抗-イディオタイプ抗体、及びこれらの抗体又は断片のキメラ又はヒト化形態、並びにヒト抗体及び抗体断片を含む抗体を含んでいる。あるいは、潜在的アンタゴニストは、密接に関連したタンパク質、例えば、レセプターを認識するが効果を与えず、よってポリペプチドの作用を競合的に阻害するポリペプチドの変異形態であってもよい。
リボザイムは、RNAの特異的切断を触媒できる酵素的RNA分子である。リボザイムは、相補的標的RNAへの配列特異的ハイブリダイゼーション、次いでヌクレオチド鎖切断的開裂により作用する。潜在的RNA標的内の特異的リボザイム切断部位は、既知の技術で同定できる。更なる詳細は、例えば、Rossi, Current Biology 4: 469-471 (1994)及びPCT公報、国際公開 97/33551(1997年9月18日公開)を参照。
転写阻害に用いられる三重螺旋形成における核酸分子は一本鎖でデオキシヌクレオチドからなる。これらのオリゴヌクレオチドの基本組成は、フーグスティン(Hoogsteen)塩基対則を介する三重螺旋形成を促進するように設計され、それは一般に二重鎖の一方の鎖上のプリン又はピリミジンのかなり大きな伸張を必要とする。さらなる詳細は、例えば、上掲のPCT公報、国際公開97/33551を参照。
これらの小分子は、上記で議論したスクリーニングアッセイの一又は複数の任意のものにより及び/又は当業者に良く知られた他の任意のスクリーニング技術により同定できる。
ここで同定されるポリペプチドに特異的に結合する抗体、並びに上記に開示したスクリーニングアッセイによって同定された他の分子は、種々の疾患の治療のために、製薬組成物の形態で投与することができる。
ポリペプチドが細胞内にあり、全抗体が阻害剤として用いられる場合、取り込める抗体が好ましい。しかし、リポフェクション又はリポソームも抗体、又は抗体断片を細胞に搬送するために使用できる。抗体断片が用いられる場合、標的タンパク質の結合ドメインに特異的に結合する最小阻害断片が好ましい。例えば、抗体の可変領域配列に基づいて、標的タンパク質配列に結合する能力を保持したペプチド分子が設計できる。このようなペプチドは、化学的に合成でき、及び/又は組換えDNA技術によって生成できる。例えば、Marasco等, Proc. Natl. Acad. Sci. USA 90, 7889-7893 (1993)参照。
ここでの製剤は、治療すべき特定の徴候に必要な場合に1つ以上の活性化合物、好ましくは互いに悪影響を及ぼさない相補的活性を持つものも含んでよい。あるいは、又はそれに加えて、組成物は、細胞障害性薬、サイトカイン、化学療法剤、又は成長阻害剤のようなその機能を高める薬剤を含んでもよい。これらの分子は、適切には、意図する目的に有効な量の組み合わせで存在する。
本明細書で引用した全ての特許及び参考文献の全体を、出典明示によりここに取り込む。
色素生産性基質S2366はDiaPharma Group, Inc. (West Chester, OH)、Lys-プラスミノーゲンはHaematologic Technologies Inc. (Essex Junction, VT)から、および組織型プラスミノーゲン活性化因子(t-PA)はGenentech, Inc. (South San Francisco, CA)から入手した。血清がない条件下でチャイニーズハムスター卵巣(CHO)細胞において、発現され、HiTrapセファロースSPクロマトグラフィにより精製されたプロHGFは、David Kahn (Genentech)により入手した。記述される(34)ように、残基Val373−Arg407を含有するHGFAはバキュロウイルス発現系において、発現され、精製された。ヒトの293細胞において、発現される、精製されたヒト組換えFVIIは、Mark O'Connell (Genentech)から贈与されたものであり、最近記述されている(42)。記述される(43)ように、基本的に、ジオレイル1,2-ジアシル-sn-グリセロ-3-(ホスホ-L-セリン)(PS)およびオレオイル1,2-ジアシル-sn-グリセロ-3-ホスホコリン(PC)(Avanti Polar Lipids Inc., Alabaster, AL)は、PCPSベシクル(7:3モル比)を生産するために用いた。分子量マーカーは、SeeBlue Plus2およびMultiMark標準物質(Invitrogen, Carlsbad, CA)を用いた。
I.M.A.G.E. consortium (ATCC, Manassas, VA)から入手の完全長ヘプシンのcDNAは、限定エンドヌクレアーゼEcoRIおよびNotI (New England Biolabs Inc. Beverly, MA)によって、消化し、真核生物発現ベクターpRK5Eに挿入した。分泌されたHisタグ付加ヘプシンcDNAは、ヒトヘプシンの細胞外ドメイン(Arg45−Leu417:番号付けシステムSomoza 等, 2003(5)に従う)をコードするcDNAとヒトHGF(アミノ酸Met1−Gly31)のシグナル配列をコードするcDNAを融合することによって、構築した。加えて、真核生物発現ベクターpCMV.PD5に挿入された最終的なcDNAコンストラクトとLeu417の後のC末端にHis8タグを付加した。基本的に、野生型sHAI-1Bの産生について記述される(34)ように、チャイニーズハムスター卵巣(CHO)細胞一時的発現システムでヘプシンを発現させ、ニッケル-ニトリロトリ酢酸(Ni-NTA)親和性クロマトグラフィによって精製した。
既に記述される(34)ように、全ての細胞外ドメインを含有するHAI-1Bの可溶型(sHAI-1B)はCHO細胞一時的発現システムで生産して、精製した。部位特異的突然変異を用いて、KD1(Arg260)およびKD2(Lys401)のP1残基をAlaにそれぞれ変異させ、結果として生じるタンパク質、sHAI-1B(R260A)およびsHAI-1B(K401A)を、記述される(34)ように、発現させて、精製した。
完全長HAI-2は、オリゴdT/NotI部位をプライマーおよび二本目の鎖のSalI部位を有するアダプターとして用いて、ヒト胎児肺RNA由来のcDNAライブラリ (BD Biosciences Clontech, Palto Alto, CA)から入手した。cDNAはSalIおよびNotIによって消化し、2.8kbより大きいcDNAはpRK5Dに挿入した。ヒト肺cDNA/pRK5Dライブラリの一本鎖DNAは、標準物質分子生物学的方法を用いて生成した。リバースプライマ(5'-TTTCTTGAGGCACTCCTCCTTG-3')は、一本鎖cDNAプールにアニールし、T7又はT4DNAポリメラーゼを用いて伸展させた。大腸菌に合成された二本鎖DNAを形質移入し、コロニーを標準的なフィルタハイブリダイゼーション法を使用してスクリーニングした。挿入サイズは、PCRおよび制限エンドヌクレアーゼ消化(XbaI)によって分析した。HAI-2完全長クローンを同定して、DNA塩基配列決定によって確認した。HAI-2の可溶型(sHAI-2)は、HAI-2の細胞外ドメイン(Ala28−Lys197、番号付けシステムKawaguchi 等, 1997(39)に従う)をコードするcDNAを構築して、Glyスペーサを有するC末端His8タグを付加することによって産生した。次いで、得られたcDNAを、pVL1393 (BD Biosciences Pharmingen, San Diego, CA)から得られるバキュロウイルス発現ベクターに挿入した。基本的に、HGFβ鎖の産生について記述される(44)ように、sHAI-2は、バキュロウイルス発現系において、発現させ、Ni-NTA親和性クロマトグラフィによって精製した。タンパク質濃度は定量的アミノ酸分析で測定した。
0.11mg/ml濃度のFVIIを、230nMのヘプシンを含有する30mM トリス-HCl、pH8.4、30mM イミダゾール、0.5mM PCPS溶媒存在下での200mM NaCl(トリス緩衝液)および5mM CaCl2によって、37℃で活性化した。異なる時間点で採取した反応分割量を、4−20%の勾配ゲル(Invitrogen, Carlsbad, CA)を用いてSDS-PAGE(還元条件)によって分析した。ゲルはSimply Blue Safe Stain(Invitrogen)にて染色した。
0.12mg/mlのプラスミノーゲンを、40nMのヘプシン又は40nMのt-PA(ポジティブコントロール)を含有する20mM Hepes pH7.5、150mM NaCl(Hepesバッファ)にて、37℃でインキュベートした。FVII活性化アッセイについて記述されるように、異なる時間点で採取した反応分割量をSDS-PAGEによって、分析した。
プロHGF(0.3mg/ml)を、40nMのヘプシンを有するHepesバッファ又は40nMのHGFAを有するHepesバッファ中で37℃で4時間インキュベートし、後の使用まで−20℃で保存した。SDS-PAGEによる消化された材料、HGFhepsinおよびHGFHGFAの分析により、95%より多くのプロHGFが2-鎖HGFに転換したことが示された。
記述される(34、45)ように、プロHGF活性化アッセイおよびプロHGFの125I-標識を行った。簡潔には、0.05mg/mlの125I標識プロHGFを含有するHepesバッファを、漸増濃度(0.16−40nM)のヘプシン又はHGFAとともに37℃でインキュベートした。4時間後、分割量を採取し、SDS-PAGE( 4−20%の勾配ゲル) (Invitrogen Corp., Carlsbad, CA)によって分析した。阻害研究のために、ヘプシン(15nM)を1μMのsHAI-1B、sHAI-1B(K401A)、sHAI-1B(R260A)又はsHAI-2とともにHepesバッファ中で37℃でインキュベートした。4時間後、試料をSDS-PAGEによって分析し、Simply Blue Safe Stain(Invitrogen)によって染色した。
アッセイ条件は、色素生産性基質S2366(L-ピログルタミル-L-プロイル-L-アルギニン-p-ニトロアニリンヒドロクロライド)を用いたSomoza 等 2003(5)により記述されるものと類似である。ヘプシン(終濃度0.4nM)を、漸増濃度のインヒビターとともにトリスバッファ中で室温で30分間インキュベートした。基質S2366を添加し、405nmの吸光度の変化を動態学的マイクロプレート読み取り機(Molecular Devices, Sunnyvale CA)にて測定した。この最終反応混合物中のヘプシン及びS2366の濃度はそれぞれ、0.4nMおよび0.2mM(Km=0.2mMを測定)であった。阻害活性は、阻害されない酵素活性の部分的活性(vi/v0)として表した。50%阻害(IC50)を示すインヒビター濃度は、4つのパラメータ回帰曲線適合プログラム(Kaleidagraph, Synergy Software, Reading, PA)にデータを合わせることによって算出した。それぞれのインヒビターについて少なくとも3回の独立した実験を行った。
増殖アッセイは、European Collection of Cell Cultures (CAMR, Centre for Applied Microbiology and Research, Salisbury, Wiltshire, UKから入手したヒト膵臓腺癌細胞株BxPC3を用いて行った。細胞は、10% FCS (Sigma, St. Louis, MO)、10mM hepes、2mM グルタミン、ペニシリン-ストレプトマイシン(Invitrogen, Carlsbad, CA)および250μg/ml G418(Invitrogen)を含有しているRPMI培養液中で生育した。集密的な細胞層をPBSで洗浄した後、10mM EDTA/PBSにて洗浄し、トリプシンにてインキュベーションの後に取り出した。細胞を、細胞増殖培養液中に再懸濁して、96ウェル白底のMTプレート(Cultur PlateTM, Packard/PerkinElmer, Boston, MA)に播種した(10,000−15,000細胞/ウェル)。24時間後、細胞増殖培養液をRPMI-0.1%BSAと置き換えた。さらに24時間後、培養液を除去し、RPMI-0.1%BSA中に様々な濃度のHGFhepsin及びHGFHGFAを添加し、細胞を72時間生育させた。次いで、製造業者の指示に従ってCellTiter-Glo Luminescentキット(Promega, Madison, WI)を用いて細胞増殖を定量化した。Tropix TR717マイクロプレート照度計(Berthold 75323, Bad Wildbad, Germany)にて発光を測定した。バックグラウンドの値(HGFの非存在下での増殖量)を減算した後、HGFhepsinおよびHGFHGFAの活性を、100ng/mlのHGFコントロール調製物(Dr. Ralph Schwall, Genentechから入手)に対するBxPC3増殖の割合として表した。
記述される(44)ように、乳癌細胞株MDA-MB435 (HTB-129, ATCC, Manassas, VA)を用いて細胞移動アッセイを行った。簡単に言うと、無血清培地に懸濁した0.2mlの細胞(0.6−0.8×106細胞/ml)を、10μg/mlのラット尾部コラーゲンタイプI (Upstate, Lake Placid, NY)でプレコーティングした24ウェルトランスウェルプレート(8μm細孔径) (HTS MultiwellTM Insert System, Falcon, Franklin Lakes, NJ)の上部チャンバに添加した。HGF調製物を、無血清培地中の下部チャンバに添加した。13−14時間インキュベーションした後、膜の先端面上の細胞を除去し、基礎側に移動したものを4%パラホルムアルデヒドに固定して、0.5%クリスタルバイオレット溶液にて染色した。細胞を10%酢酸で溶解し、A560をMolecular Devicesマイクロプレート読み取り機にて測定した。HGF突然変異体のプロ移動性活性を、HGFの非存在下での基礎移動を減算した後の、HGFコントロール調製物に対する割合として表した。
記述される(44)ように、キナーゼレセプター活性化アッセイ(KIRA)を行った。簡単に言うと、肺上皮癌A549細胞(CCL-185、ATCC、Manassas, VA)を1ウェルにつき50,000細胞の密度で、96ウェルプレートに播いた。37℃で一晩インキュベーションした後、細胞増殖培養液を除去し、細胞を0.1%FBSを含有する培養液中で30〜60分間おいて、血清欠乏状態にした。0.1%FBSを含有する培養液中に漸増濃度のHGFhepsin及びHGFHGFAを添加した。対照として、我々は、切断部位が変異した(Arg494Glu) HGFの非切断一本鎖型(scHGF)を用いた(44)。37℃で10分インキュベーションした後、培養液を除去し、細胞をプロテアーゼインヒビター反応混液を添加した溶解バッファ(Cell Signaling Technologies, Beverly, MA)にて溶解した。BV-TAG標識4G10抗体およびビオチン化抗Met抗体を細胞溶解物に加えた。1.5〜2時間インキュベーションした後、ストレプトアビジン磁気ビーズ(Dynabeads, Bio Veris)を添加して、45分間インキュベートした。結合した材料(抗Met抗体/Met/抗ホスホチロシン抗体)を有するビーズを、外部から磁石にあてることによって、捕獲した。洗浄工程の後、光源により生成される化学発光シグナルを、Bio Veris計測器にて相対的な発光の単位として測定した。各々の実験について、HGFhepsin、HGFHGFA又はscHGFによるMetリン酸化を、HGFコントロール調整物で得られた最大シグナルに対する割合として表した。
ヘプシンによるプロHGFのタンパク分解処理
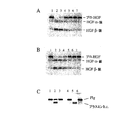
全ての細胞外ドメインを含有するヘプシンの可溶型(Arg45−Leu417、番号付けシステムSomoza 等, 2003(5)に従う)と、C末端His8タグを、CHO細胞において、発現させた。精製工程の間、ヘプシン酵素前駆体は、おそらく自己活性化によって、自然発生的にその2-鎖型に変換した(図1A)(4)。30kDa以下のプロテアーゼドメイン(163IVGGRDTSLGR173)のN末端配列決定によって、予想されたArg162-Ile163ペプチド結合での切断が活性な酵素を生じることが確認された。ヘプシンが、能動的にFVII酵素前駆体を2-鎖FVIIaに変換することは(図1B)、FVII活性を決定するための細胞表面発現ヘプシンを用いたKazama 等, 1995(9)により報告された実験と一致した。プロHGFに対するヘプシン活性は、125I標識プロHGFの2-鎖HGFへの変換を測定することによって、調べられた。結果は、プロHGFが濃度依存的な様式でヘプシンにより切断されることが示された(図2A)。ヘプシン活性はHGFAのものと同等であり(図2B)、両方の酵素は4 −13nM濃度のプロHGFを完全に変換した。同じアッセイシステムにおいて、プロHGF活性化第XIa因子、第XIIa因子および血漿カリクレインは、完全にプロHGFを変換するためにはおよそ5−6倍の濃度が必要である(45)。36kDa以下および39kDa以下のHGFβ鎖のN末端配列決定によって、ヘプシンが予想されたArg494-Val495ペプチド結合でプロHGFをプロセシングしたことを示す、同一の配列(495VVNGIPTRTNIG506)が明らかとなった。第XIa因子および血漿カリクレインとは異なり、さらに長時間反応させた後であっても、ヘプシンは、(Arg424-His425間の切断によって)HGFα2-鎖断片を生成しなかった(45)。さらに、ヘプシン(40nM)は、5時間の反応の間、プラスミノーゲンを活性化する能力を完全に欠いていた(図2C)。相対的に、およそ50%の酵素前駆体によって、t-PAに効率的に処理されたプラスミノーゲンは、0.5時間後には既に切断した(図2C)。
非標識プロHGF(0.3mg/ml)を、HGFhepsinおよびHGFHGFAそれぞれを求めるために、40nMのヘプシン又は40nMのHGFAにてHGFに完全に(>95%)変換させた(図3A)。A549肺カルシノーマ細胞を用いたキナーゼレセプターアッセイ(KIRA)では、両方のHGF調製物は同じように濃度依存的にMetリン酸化を誘導し、250ng/mlで最大活性となった(図3B)。既に示されている(44)ように、変更した切断部位(R494E)により切断されなかったHGFの一本鎖型(scHGF)は、活性を示さなかった(図3B)。対照実験では、ヘプシン又はHGFA単独は無効であったことが示された(データは示さない)。さらに、HGFhepsinは、BxPC3膵癌細胞の増殖を効率的に促進した。活性は、5−100ng/mlの範囲で試験したHGFHGFAの活性と比較した(図4A)。コラーゲンコートトランスウェル移動システムを用いたMDA-MB435細胞による細胞移動アッセイでは同様の結果が得られた。細胞増殖アッセイでみられるように、HGFhepsinのプロ遊走性の効果は濃度依存性であり、HGFHGFAの活性と区別がつかなかった(図4B)。
26個の市販の色素生産性基質の最初のスクリーニングでは、Somoza 等, 2003(5)により報告される基質であるS2366が最も高い割合でヘプシンにより加水分解されたことが示された(データは示さない)。基質としてS2366を使用して、野生型HAI-1B(sHAI-1B)及びHAI-2(sHAI-2)の高度に精製された、可溶性型の阻害活性を測定した。加えて、我々は、2つのsHAI-1B突然変異体sHAI-1B(R260A)及びsHAI-1B(K401A)を生産した。この突然変異体はそれぞれのクーニッツドメインがP1残基(KD1のArg260およびKD2のLys401)をアラニンに置換されることによって、不活性である(34)。sHAI-1B及びsHAI-2の両方が、それぞれIC50値21.1± 2.7nM及び1.3±0.3nMで、ヘプシン酵素活性を強力に阻害したことを示した(図5)。さらに、機能しないKD2を含有する変異体sHAI-1B(K401A)は野生型sHAI-1Bと同等の効力であるが、一方sHAI-1B(R260A)は活性が47分の1より小さくなった(図5)。得られたIC50値を表1にまとめる。
高分子基質処理を妨げるsHAI-1B及びsHAI-2の能力を、125I-プロHGF活性化アッセイにおいて、測定した。得られた結果は、アミノリシスアッセイにおいて、測定されるそれらの阻害力と完全に一致した。1μM濃度のsHAI-2、野生型sHAI-1B及びsHAI-1B(K401A)では、プロHGFの切断が完全に阻害された(図6)。対照的に、1μMのsHAI-1B(R260A)は阻害を示さず、プロHGF活性化により完全に転換した(図6)。
HGF/Metシグナル伝達経路は、腫瘍浸潤及び転移を含むヒト生理機能及び病理学において、重要な役割を果たす。活性なHGFの局所の有効性は、細胞外環境における不活性なプロHGFの処理を制御する、キモトリプシン様セリンプロテアーゼおよびその同族インヒビターにより制御される。したがって、癌におけるこの「上流の」プロHGF転換酵素経路の混乱は、プロHGFプロセシングを促進することによって、腫瘍成長を促進しうる。ここで、我々は、前立腺癌及び卵巣癌において、高度に上方制御されるセリンプロテアーゼであるヘプシンは、プロHGFの強力な活性化因子である。ゆえに、ヘプシンはおそらく、前立腺癌(46−48)並びに卵巣がん(49、50)に関係している、HGF/Metシグナル伝達経路を活性化することによって、腫瘍成長をもたらすことにおいて、重要な役割を果たす。
ヘプシンは、第XIa因子および血漿カリクレインにより認識される部位であるクリングルドメイン4のArg424-His425でいかなる付加的な切断をすることなく、Arg494−Val495ペプチド結合でプロHGFを蛋白質加水分解的に切断する(45)。ヘプシンにより生成される2-鎖HGFは十分に機能的であり、Metレセプターリン酸化を誘発して、HGFAにより生成されるHGFと同等の活性で細胞増殖および移動を促進した。不活性なプロHGFの活性な成長因子へのヘプシン媒介性変換の基本となる分子メカニズムは、キモトリプシン様セリンプロテアーゼの酵素変換に対するタンパク分解性酵素前駆体と類似している。このことはプロHGF活性化の構造的結果についての近年の研究に裏付けられており、Arg494−Val495で切断されると、プロテアーゼ様HGFβ鎖での立体配置的変化とMetレセプター結合部位の完全な成熟が引き起こされることが示されている(44、51)。この、HGFの「活性部位領域」及び「活性化ドメイン」に集中しているMet結合部位は、セリンプロテアーゼの基質処理領域と著しく似ている(44、51)。ゆえに、ヘプシンによるプロHGF切断により、HGFβ上の構造再配置が起こり、生産的なHGF/Metシグナル伝達複合体の形成を可能にする。プロHGFの非常に近い構造的ホモログであるプラスミノーゲンを切断しなかったので、プロHGFに対するヘプシンのタンパク分解性活性は非常に特異的であるようである。ヘプシンは、他のセリンプロテアーゼ基質、例えばプロトロンビン、プロテインC、第X因子および第IX因子に対するタンパク分解性活性を有しなかった(9)。
HAI-1B、HAI-1及びHAI-2は、上皮細胞表面インヒビターであって、多くの正常組織及び腫瘍において、発現される(34、58−63)。このように、それらは、上皮細胞発現型TTSP及びおそらく他の細胞表面関連セリンプロテアーゼの酵素活性を制御するために、理想的に位置する。実際、HAI-1スプライシング変異体HAI-1及びHAI-1Bは、強力にTTSPマトリプターゼ(MT-SP1)を阻害し、マトリプターゼとのHAI-1の複合体はヒト母乳において、みられた(38)。ここで、我々はsHAI-1B及びsHAI-2の両方がヘプシン酵素活性の強力なインヒビターでもあることを示した。さらに、P1残基-定方向突然変異実験では、変異体sHAI-1B(R260A)がプロHGFアッセイにおいては不活性であり、アミド溶解性アッセイにおいては野生型及びKD2変異体活性の1%未満であったので、ヘプシンの阻害はsHAI-BのKD1に完全に媒介されることが示された。
結論として、示された結果により、ヘプシンが効率的にプロHGFを活性化することが示され、したがって、腫瘍上皮表面のヘプシンと不活性成長因子前駆体を含有する細胞外基質との機能的な関連が明らかとなった。HAI-1B及びHAI-2が、前立腺癌や卵巣癌で上方制御されるヘプシンの強力なインヒビターであるという発見により、癌治療のための新規な方法が提供される。例えば、HAI-1B又はHAI-2の機能的なクーニッツドメインはファージディスプレイ技術を用いてより特異的及び/又はより強力な酵素インヒビターを生成するための足場として役立ちうる。その技術は他のクーニッツドメイン足場にうまく応用されている(69、70)。
1第VIIa因子、第FVIIa因子;Hepesバッファ、20mM Hepes pH7.5、150mM NaCl;トリス緩衝液、30mM トリス-HCl、pH8.4、30mM イミダゾール、200mM NaCl;プロHGF、一本鎖肝細胞増殖因子、HGF、2-鎖肝細胞増殖因子;HGFA肝細胞増殖因子活性化因子;HAI-1、肝細胞増殖因子活性化因子インヒビター-1;HAI-1B、肝細胞増殖因子活性化因子インヒビター-1のスプライシング変異体;HAI-2、肝細胞増殖因子活性化因子インヒビター-2;KD1及びKD2、HAI-1BのN-及びC-末端クーニッツドメイン;sHAI-1B、細胞外ドメインを包含するHAI-1Bの可溶型;sHAI-2、細胞外ドメインを包含するHAI-2の可溶型;HGFhepsin、ヘプシンによるプロHGFの活性化により生産されるHGF;HGFHGFA、HGFAによるプロHGFの活性化により生産されるHGF;scHGF、変異した切断部位(Arg494Glu)により切断されない一本鎖HGF;u-PA、ウロキナーゼ型プラスミノーゲン活性化因子;t-PA、組織型プラスミノーゲン活性化因子。Ni-NTA、ニッケル-ニトリロトリ酢酸。
1. Szabo, R., Wu, Q., Dickson, R. B., Netzel-Arnett, S., Antalis, T. M., and Bugge, T. H. (2003) Thromb. Haemost. 90, 185-193
2. Tsuji, A., Torres-Rosado, A., Arai, T., Le Beau, M. M., Lemons, R. S., Chou, S.-H., and Kurachi, K. (1991) J Biol Chem 266, 16948-16953
3. Leytus, S. P., Loeb, K. R., Hagen, F. S., Kurachi, K., and Davie, E. W. (1988) Biochemistry 27, 1067-1074
4. Vu, T.-K. H., Liu, R. W., Haaksma, C. J., Tomasek, J. J., and Howard, E. W. (1997) J Biol Chem 272, 31315-31320
5. Somoza, J. R., Ho, J. D., Luong, C., Ghate, M., Sprengeler, P. A., Mortara, K., Shrader, W. D., Sperandio, D., Chan, H., McGrath, M. E., and Katz, B. A. (2003) Structure 11, 1123-1131
6. McCallum, C. D., Hapak, R. C., Neuenschwander, P. F., Morrissey, J. H., and Johnson, A. E. (1996) J. Biol. Chem. 271, 28168-28175
7. Mutucumarana, V. P., Duffy, E. J., Lollar, P., and Johnson, A. E. (1992) J. Biol. Chem. 267, 17012-17021
8. Husten, E. J., Esmon, C. T., and Johnson, A. E. (1987) J. Biol. Chem. 262, 12953-12961
9. Kazama, Y., Hamamoto, T., Foster, D. C., and Kisiel, W. (1995) J. Biol. Chem. 270, 66-72
10. Wu, Q., Yu, D., Post, J., Halks-Miller, M., Sadler, J. E., and Morser, J. (1998) J. Clin. Invest. 101, 321-326
11. Yu, I.-S., Chen, H.-J., Lee, Y.-S. E., Huang, P.-H., Lin, S.-R., Tsai, T.-W., and Lin, S.-W. (2000) Thromb. Haemost. 84, 865-870
12. Zacharski, L. R., Ornstein, D. L., Memoli, V. A., Rousseau, S. M., and Kisiel, W. (1998) Thromb. Haemost. 79, 876-877
13. Rapaport, S. I., and Rao, L. V. M. (1995) Thromb. Haemost. 74, 7-17
14. Mann, K. G. (1999) Thromb. Haemost. 82, 165-174
15. Torres-Rosado, A., O'Shea, K. S., Tsuji, A., Chou, S.-H., and Kurachi, K. (1993) Proc Natl Acad Sci U S A 90, 7181-7185
16. Srikantan, V., Valladares, M., Rhim, J. S., Moul, J. W., and Srivastava, S. (2002) Cancer Res. 62, 6812-6816
17. Welsh, J. B., Sapinoso, L. M., Su, A. I., Kern, S. G., Wang-Rodriguez, J., Moskaluk, C. A., Frierson Jr., H. F., and Hampton, G. M. (2001) Cancer Res. 61, 5974-5978
18. Stamey, T. A., Warrington, J. A., Caldwell, M. C., Chen, Z., Fan, Z., Mahadevappa, M., McNeal, J. E., Nolley, R., and Zhang, Z. (2001) J. Urol. 166, 2171-2177
19. Magee, J. A., Araki, T., Patil, S., Ehrig, T., True, L., Humphrey, P. A., Catalona, W. J., Watson, M. A., and Milbrandt, J. (2001) Cancer Res. 61, 5692-5696
20. Dhanasekaran, S. M., Barrette, T. R., Ghosh, D., Shah, R., Varambally, S., Kurachi, K., Pienta, K. J., Rubin, M. A., and Chinnaiyan, A. M. (2001) Nature 412, 822-826
21. Luo, J., Duggan, D. J., Chen, Y., Sauvageot, J., Ewing, C. M., Bittner, M. L., Trent, J. M., and Isaacs, W. B. (2001) Cancer Res. 61, 4683-4688
22. Stephan, C., Yousef, G. M., Scorilas, A., Jung, K., Jung, M., Kristiansen, G., Hauptmann, S., Kishi, T., Nakamura, T., Loening, S. A., and Diamandis, E. P. (2004) J. Urol. 171, 187-191
23. Tanimoto, H., Yan, Y., Clarke, J., Korourian, S., Shigemasa, K., Parmley, T. H., Parham, G. P., and O'Brien, T. J. (1997) Cancer Res. 57, 2884-2887
24. Lin, C.-Y., Anders, J., Johnson, M., Sang, Q. A., and Dickson, R. B. (1999) J. Biol. Chem. 274, 18231-18236
25. Takeuchi, T., Shuman, M. A., and Craik, C. S. (1999) Proc. Natl. Acad. Sci. USA 96, 11054-11061
26. Birchmeier, C., Birchmeier, W., Gherardi, E., and Vande Woude, G. F. (2003) Nature Rev. Mol. Cell Biol. 4, 915-925
27. Trusolino, L., and Comoglio, P. M. (2002) Nature Rev. Cancer 2, 289-300
28. Hartmann, G., Naldini, L., Weidner, K. M., Sachs, M., Vigna, E., Comoglio, P. M., and Birchmeier, W. (1992) Proc. Natl. Acad. Sci. USA 89, 11574-11578
29. Lokker, N. A., Mark, M. R., Luis, E. A., Bennett, G. L., Robbins, K. A., Baker, J. B., and Godowski, P. J. (1992) EMBO J 11, 2503-2510
30. Naka, D., Ishii, T., Yoshiyama, Y., Miyazawa, K., Hara, H., Hishida, T., and Kitamura, N. (1992) J. Biol. Chem. 267, 20114-20119
31. Gak, E., Taylor, W. G., Chan, A. M.-L., and Rubin, J. S. (1992) FEBS Lett. 311, 17-21
32. Miyazawa, K., Shimomura, T., Kitamura, A., Kondo, J., Morimoto, Y., and Kitamura, N. (1993) J. Biol. Chem. 268, 10024-10028
33. Lee, S.-L., Dickson, R. B., and Lin, C.-Y. (2000) J. Biol. Chem. 275, 36720-36725
34. Kirchhofer, D., Peek, M., Li, W., Stamos, J., Eigenbrot, C., Kadkhodayan, S., Elliott, J. M., Corpuz, R. T., Lazarus, R. A., and Moran, P. (2003) J. Biol. Chem. 278, 36341-36349
35. Naldini, L., Tamagnone, L., Vigna, E., Sachs, M., Hartmann, G., Birchmeier, W., Daikuhara, Y., Tsubouchi, H., Blasi, F., and Comoglio, P. M. (1992) EMBO J. 11, 4825-4833
36. Shimomura, T., Miyazawa, K., Komiyama, Y., Hiraoka, H., Naka, D., Morimoto, Y., and Kitamura, N. (1995) Eur. J. Biochem. 229, 257-261
37. Shimomura, T., Denda, K., Kitamura, A., Kawaguchi, T., Kito, M., Kondo, J., Kagaya, S., Qin, L., Takata, H., Miyazawa, K., and Kitamura, N. (1997) J. Biol. Chem. 272, 6370-6376
38. Lin, C.-Y., Anders, J., Johnson, M., and Dickson, R. B. (1999) J. Biol. Chem. 274, 18237-18242
39. Kawaguchi, T., Qin, L., Shimomura, T., Kondo, J., Matsumoto, K., Denda, K., and Kitamura, N. (1997) J. Biol. Chem. 272, 27558-27564
40. Marlor, C. W., Delaria, K. A., Davis, G., Muller, D. K., Greve, J. M., and Tamburini, P. P. (1997) J. Biol. Chem. 272, 12202-12208
41. Delaria, K. A., Muller, D. K., Marlor, C. W., Brown, J. E., Das, R. C., Roczniak, S. O., and Tamburini, P. P. (1997) J. Biol. Chem. 272, 12209-12214
42. Kelley, R. F., Yang, J., Eigenbrot, C., Moran, P., Peek, M., Lipari, M. T., and Kirchhofer, D. (2004) Biochemistry 43, 1223-1229
43. Mimms, L. T., Zampighi, G., Nozaki, Y., Tanford, C., and Reynolds, J. A. (1981) Biochemistry 20, 833-840
44. Kirchhofer, D., Yao, X., Peek, M., Eigenbrot, C., Lipari, M. T., Billeci, K. L., Maun, H. R., Moran, P., Santell, L., Wiesmann, C., and Lazarus, R. A. (2004) J. Biol. Chem. (in press)
45. Peek, M., Moran, P., Mendoza, N., Wickramasinghe, D., and Kirchhofer, D. (2002) J. Biol. Chem. 277, 47804-47809
46. Gmyrek, G. A., Walburg, M., Webb, C. P., Yu, H.-M., You, X., Darracott Vaughan, E., Vande Woude, G. F., and Kundsen, B. S. (2001) Am. J. Pathol. 159, 579-590
47. Knudsen, B. S., Gmyrek, G. A., Inra, J., Scherr, D. S., Vaughan, E. D., Nanus, D. M., Kattan, M. W., Gerald, W. L., and Vande Woude, G. F. (2002) Urology 60, 1113-1117
48. Zhu, X., and Humphrey, P. A. (2000) Urology 56, 1071-1074
49. Huntsman, D., Resau, J. H., Klineberg, E., and Auersperg, N. (1999) Am. J. Pathol. 155, 343-348
50. Wong, A. S. T., Pelech, S. L., Woo, M. M. M., Yim, G., Rosen, B., Ehlen, T., Leung, P. C. K., and Auersperg, N. (2001) Oncogene 20, 1318-1328
51. Stamos, J., Lazarus, R. A., Yao, X., Kirchhofer, D., and Wiesmann, C. (2004) EMBO J. 23, 2325-2335
52. Schmidt, C., Bladt, F., Goedecke, S., Brinkmann, V., Zschiesche, W., Sharpe, M., Gherardi, E., and Birchmeier, C. (1995) Nature (London) 373, 699-702
53. Uehara, Y., Minowa, O., Mori, C., Shiota, K., Kuno, J., Noda, T., and Kitamura, N. (1995) Nature (London) 373, 702-705
54. List, K., Haudenschild, C. C., Szabo, R., Chen, W., Wahl, S. M., Swaim, W., Engelholm, L. H., Behrendt, N., and Bugge, T. H. (2002) Oncogene 21, 3765-3779
55. Gailani, D., Lasky, N. M., and Broze Jr., G. J. (1997) Blood Coag. Fibrinol. 8, 134-144
56. Hathaway, W. E., Wuepper, K. D., Weston, W. L., Humbert, J. R., Rivers, R. P. A., Genton, E., August, C. S., Montgomery, R. R., and Mass, M. F. (1976) Am. J. Med. 60, 654-664
57. Carmeliet, P., Schoonjans, L., Kieckens, L., Ream, B., Degen, J., Bronson, R., De Vos, R., van den Oord, J. J., Collen, D., and Mulligan, R. C. (1994) Nature 368, 419-424
58. Hamasuna, R., Kataoka, H., Meng, J.-Y., Itoh, H., Moriyama, T., Wakisaka, S., and Koono, M. (2001) Int. J. Cancer 93, 339-345
59. Kataoka, H., Suganuma, T., Shimomura, T., Itoh, H., Kitamura, N., Nabeshima, K., and Koono, M. (1999) J. Histochem. Cytochem. 47, 673-682
60. Kataoka, H., Itoh, H., Uchino, H., Hamasuna, R., Kitamura, N., Nabeshima, K., and Koono, M. (2000) Cancer Lett. 148, 127-134
61. Parr, C., and Jiang, W. G. (2001) Int. J. Oncol. 19, 857-863
62. Oberst, M., Anders, J., Xie, B., Singh, B., Ossandon, M., Johnson, M., Dickson, R. B., and Lin, C.-Y. (2001) Am. J. Pathol. 158, 1301-1311
63. Oberst, M. D., Johnson, M. D., Dickson, R. B., Lin, C.-Y., Singh, B., Stewart, M., Williams, A., al-Nafussi, A., Smyth, J. F., Gabra, H., and Sellar, G. C. (2002) Clin. Cancer Res. 8, 1101-1107
64. Denda, K., Shimomura, T., Kawaguchi, T., Miyazawa, K., and Kitamura, N. (2002) J. Biol. Chem. 277, 14053-14059
65. Qin, L., Denda, K., Shimomura, T., Kawaguchi, T., and Kitamura, N. (1998) FEBS lett. 436, 111-114
66. Kataoka, H., Hamasuna, R., Itoh, H., Kitamura, N., and Koono, M. (2000) Cancer Res. 60, 6148-6159
67. Kataoka, H., Uchino, H., Denda, K., Kitamura, N., Itoh, H., Tsubouchi, H., Nabeshima, K., and Koono, M. (1998) Cancer Lett. 128, 219-227
68. Yamauchi, M., Kataoka, H., Itoh, H., Seguchi, T., Hasui, Y., and Osada, Y. (2004) J. Urol. 171, 890-896
69. Dennis, M. S., and Lazarus, R. A. (1994) J. Biol. Chem. 269, 22129-22136
70. Dennis, M. S., Herzka, A., and Lazarus, R. A. (1995) J. Biol. Chem. 270, 25411-25417
Claims (4)
- 肝細胞増殖因子(HGF)のヘプシンによる活性化を阻害する候補インヒビター物質の同定方法であって、
(a)候補物質をヘプシンとプロHGF基質とを含有する第一試料と接触させる工程であって、前記プロHGF基質はプロHGFであり、ヘプシンは天然ヘプシンであるか又は天然ヘプシンに対して少なくとも90%のアミノ酸配列同一性を有するヘプシン変異体であって前記プロHGF基質を活性化することが可能である工程、及び
(b)前記第一試料中のプロHGF基質の活性化量を、第一試料と同等量のヘプシンとプロHGF基質とを含有するが該候補物質と接触させていない対照試料中のプロHGF基質の活性化量と比較する工程であって、対照試料中のプロHGF基質の活性化量と比較して第一試料中のプロHGF基質の活性化量が少ない場合に、該候補物質が単鎖HGF(プロHGF)のヘプシンによる活性化を阻害することができることが示される工程を含む、方法。 - 物質が肝細胞増殖因子(HGF)のヘプシンによる活性化を阻害するかどうかを確かめる方法であって、
(a)候補物質をヘプシンとプロHGF基質とを含有する第一試料と接触させる工程であって、前記プロHGF基質はプロHGFであり、ヘプシンは天然ヘプシンであるか又は天然ヘプシンに対して少なくとも90%のアミノ酸配列同一性を有するヘプシン変異体であって前記プロHGF基質を活性化することが可能である工程、及び
(b)前記第一試料中のプロHGF基質の活性化量を、第一試料と同等量のヘプシンとプロHGF基質とを含有するが該候補物質と接触させていない対照試料中のプロHGF基質の活性化量と比較する工程であって、対照試料中のプロHGF基質の活性化量と比較して第一試料中のプロHGF基質の活性化量が少ない場合に、該候補物質が単鎖HGF(プロHGF)のヘプシンによる活性化を阻害することができることが示される工程を含む、方法。 - 前記物質が、ヘプシンもしくはプロHGFと結合する、請求項1又は2に記載の方法。
- 前記試料中のヘプシンが前記プロHGFを活性化するために有効な量である、請求項1から3の何れか一項に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US59133904P | 2004-07-26 | 2004-07-26 | |
| US60/591,339 | 2004-07-26 | ||
| PCT/US2005/026446 WO2006014928A1 (en) | 2004-07-26 | 2005-07-25 | Methods and compositions for modulating hepatocyte growth factor activation |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012115809A Division JP2012196217A (ja) | 2004-07-26 | 2012-05-21 | 肝細胞増殖因子活性化を制御するための方法及び組成物 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2008507295A JP2008507295A (ja) | 2008-03-13 |
| JP2008507295A5 JP2008507295A5 (ja) | 2008-09-04 |
| JP5226308B2 true JP5226308B2 (ja) | 2013-07-03 |
Family
ID=35094502
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007523715A Expired - Fee Related JP5226308B2 (ja) | 2004-07-26 | 2005-07-25 | 肝細胞増殖因子活性化を制御するための方法及び組成物 |
| JP2012115809A Withdrawn JP2012196217A (ja) | 2004-07-26 | 2012-05-21 | 肝細胞増殖因子活性化を制御するための方法及び組成物 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012115809A Withdrawn JP2012196217A (ja) | 2004-07-26 | 2012-05-21 | 肝細胞増殖因子活性化を制御するための方法及び組成物 |
Country Status (16)
| Country | Link |
|---|---|
| US (3) | US7432044B2 (ja) |
| EP (1) | EP1774022B1 (ja) |
| JP (2) | JP5226308B2 (ja) |
| KR (1) | KR101222254B1 (ja) |
| CN (1) | CN101023182B (ja) |
| AU (1) | AU2005269463B2 (ja) |
| BR (1) | BRPI0512482A (ja) |
| CA (1) | CA2570323C (ja) |
| ES (1) | ES2532610T3 (ja) |
| HK (1) | HK1100294A1 (ja) |
| IL (1) | IL179917A0 (ja) |
| MX (1) | MX2007001064A (ja) |
| NZ (1) | NZ551908A (ja) |
| RU (1) | RU2405041C2 (ja) |
| WO (1) | WO2006014928A1 (ja) |
| ZA (1) | ZA200700745B (ja) |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5962639A (en) | 1987-11-06 | 1999-10-05 | Washington Research Foundation | Synthetic peptides corresponding to telopeptide sequences of cross-linked type I collagen metabolites |
| EP1169642B1 (en) * | 1999-04-09 | 2006-01-04 | THE GOVERNMENT OF THE UNITED STATES OF AMERICA, as represented by THE SECRETARY, DEPARTMENT OF HEALTH AND HUMAN SERVICES | Complex formed by n-linked glycoproteins (siblings) and factor h |
| EP2275547B1 (en) | 2004-12-13 | 2014-03-05 | Alethia Biotherapeutics Inc. | Polynucleotides and polypeptide sequences involved in the process of bone remodeling |
| US20100061996A1 (en) * | 2006-06-22 | 2010-03-11 | Genentech, Inc. | Methods and compositions for modulating hepsin activation of urokinase-type plasminogen activator |
| JP2009540835A (ja) | 2006-06-22 | 2009-11-26 | ジェネンテック・インコーポレーテッド | ヘプシンをターゲティングするための方法と組成物 |
| WO2008102452A1 (ja) * | 2007-02-22 | 2008-08-28 | Kringle Pharma Inc. | Hgf製剤 |
| US20110206704A1 (en) * | 2009-10-19 | 2011-08-25 | Genentech, Inc. | Methods and compositions for modulating hepatocyte growth factor activator |
| AU2010310585A1 (en) | 2009-10-22 | 2012-05-03 | Genentech, Inc. | Anti-hepsin antibodies and methods using same |
| CA2778442A1 (en) * | 2009-10-22 | 2011-04-28 | Genentech, Inc. | Methods and compositions for modulating hepsin activation of macrophage-stimulating protein |
| WO2011161189A1 (en) | 2010-06-24 | 2011-12-29 | F. Hoffmann-La Roche Ag | Anti-hepsin antibodies and methods of use |
| KR20120100027A (ko) | 2011-03-02 | 2012-09-12 | 한국생명공학연구원 | 엔도사이토시스 모티프 및 단백질 도입 도메인을 포함하는 암 예방 또는 치료용 약학적 조성물 |
| AU2012327227A1 (en) * | 2011-11-07 | 2013-05-23 | Isis Pharmaceuticals, Inc. | Administration of Factor XI antisense oligonucleotides |
| US10260089B2 (en) | 2012-10-29 | 2019-04-16 | The Research Foundation Of The State University Of New York | Compositions and methods for recognition of RNA using triple helical peptide nucleic acids |
| US11547743B2 (en) | 2014-04-28 | 2023-01-10 | Eisai R&D Management Co., Ltd. | Lyophilized formulation of HGF |
| US11130780B2 (en) | 2015-03-09 | 2021-09-28 | Washington University | Inhibitors of growth factor activation enzymes |
| EP3420087B1 (en) * | 2016-02-23 | 2021-09-01 | The Regents of The University of Colorado, A Body Corporate | Peptide-based methods for treating neurological injury |
| AU2017232582B2 (en) | 2016-03-17 | 2022-07-14 | Eisai R&D Management Co., Ltd. | Method for producing activated hepatocyte growth factor (HGF) |
| EP3919128A4 (en) * | 2019-01-28 | 2023-01-11 | Toray Industries, Inc. | POLYETHYLENE GLYCOL MODIFIED BODY FOR HEPATORYTE GROWTH FACTOR OR ACTIVE FRAGMENT THEREOF |
Family Cites Families (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3896111A (en) | 1973-02-20 | 1975-07-22 | Research Corp | Ansa macrolides |
| US4151042A (en) | 1977-03-31 | 1979-04-24 | Takeda Chemical Industries, Ltd. | Method for producing maytansinol and its derivatives |
| US4137230A (en) | 1977-11-14 | 1979-01-30 | Takeda Chemical Industries, Ltd. | Method for the production of maytansinoids |
| US4265814A (en) | 1978-03-24 | 1981-05-05 | Takeda Chemical Industries | Matansinol 3-n-hexadecanoate |
| US4307016A (en) | 1978-03-24 | 1981-12-22 | Takeda Chemical Industries, Ltd. | Demethyl maytansinoids |
| JPS5562090A (en) | 1978-10-27 | 1980-05-10 | Takeda Chem Ind Ltd | Novel maytansinoid compound and its preparation |
| US4256746A (en) | 1978-11-14 | 1981-03-17 | Takeda Chemical Industries | Dechloromaytansinoids, their pharmaceutical compositions and method of use |
| JPS5566585A (en) | 1978-11-14 | 1980-05-20 | Takeda Chem Ind Ltd | Novel maytansinoid compound and its preparation |
| JPS55164687A (en) | 1979-06-11 | 1980-12-22 | Takeda Chem Ind Ltd | Novel maytansinoid compound and its preparation |
| JPS55102583A (en) | 1979-01-31 | 1980-08-05 | Takeda Chem Ind Ltd | 20-acyloxy-20-demethylmaytansinoid compound |
| JPS55162791A (en) | 1979-06-05 | 1980-12-18 | Takeda Chem Ind Ltd | Antibiotic c-15003pnd and its preparation |
| JPS55164685A (en) | 1979-06-08 | 1980-12-22 | Takeda Chem Ind Ltd | Novel maytansinoid compound and its preparation |
| JPS55164686A (en) | 1979-06-11 | 1980-12-22 | Takeda Chem Ind Ltd | Novel maytansinoid compound and its preparation |
| US4309428A (en) | 1979-07-30 | 1982-01-05 | Takeda Chemical Industries, Ltd. | Maytansinoids |
| JPS5645483A (en) | 1979-09-19 | 1981-04-25 | Takeda Chem Ind Ltd | C-15003phm and its preparation |
| JPS5645485A (en) | 1979-09-21 | 1981-04-25 | Takeda Chem Ind Ltd | Production of c-15003pnd |
| EP0028683A1 (en) | 1979-09-21 | 1981-05-20 | Takeda Chemical Industries, Ltd. | Antibiotic C-15003 PHO and production thereof |
| WO1982001188A1 (en) | 1980-10-08 | 1982-04-15 | Takeda Chemical Industries Ltd | 4,5-deoxymaytansinoide compounds and process for preparing same |
| US4450254A (en) | 1980-11-03 | 1984-05-22 | Standard Oil Company | Impact improvement of high nitrile resins |
| US4313946A (en) | 1981-01-27 | 1982-02-02 | The United States Of America As Represented By The Secretary Of Agriculture | Chemotherapeutically active maytansinoids from Trewia nudiflora |
| US4315929A (en) | 1981-01-27 | 1982-02-16 | The United States Of America As Represented By The Secretary Of Agriculture | Method of controlling the European corn borer with trewiasine |
| JPS57192389A (en) | 1981-05-20 | 1982-11-26 | Takeda Chem Ind Ltd | Novel maytansinoid |
| US4485045A (en) | 1981-07-06 | 1984-11-27 | Research Corporation | Synthetic phosphatidyl cholines useful in forming liposomes |
| AU2353384A (en) | 1983-01-19 | 1984-07-26 | Genentech Inc. | Amplification in eukaryotic host cells |
| US4713339A (en) | 1983-01-19 | 1987-12-15 | Genentech, Inc. | Polycistronic expression vector construction |
| US4544545A (en) | 1983-06-20 | 1985-10-01 | Trustees University Of Massachusetts | Liposomes containing modified cholesterol for organ targeting |
| US4676980A (en) | 1985-09-23 | 1987-06-30 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Target specific cross-linked heteroantibodies |
| US5606040A (en) | 1987-10-30 | 1997-02-25 | American Cyanamid Company | Antitumor and antibacterial substituted disulfide derivatives prepared from compounds possessing a methyl-trithio group |
| US5770701A (en) | 1987-10-30 | 1998-06-23 | American Cyanamid Company | Process for preparing targeted forms of methyltrithio antitumor agents |
| US5225538A (en) | 1989-02-23 | 1993-07-06 | Genentech, Inc. | Lymphocyte homing receptor/immunoglobulin fusion proteins |
| US5013556A (en) | 1989-10-20 | 1991-05-07 | Liposome Technology, Inc. | Liposomes with enhanced circulation time |
| US5208020A (en) | 1989-10-25 | 1993-05-04 | Immunogen Inc. | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| CA2026147C (en) | 1989-10-25 | 2006-02-07 | Ravi J. Chari | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| US5206161A (en) | 1991-02-01 | 1993-04-27 | Genentech, Inc. | Human plasma carboxypeptidase B |
| ZA932522B (en) | 1992-04-10 | 1993-12-20 | Res Dev Foundation | Immunotoxins directed against c-erbB-2(HER/neu) related surface antigens |
| DK0669836T3 (da) | 1992-11-13 | 1996-10-14 | Idec Pharma Corp | Terapeutisk anvendelse af kimære og radioaktivt mærkede antistoffer og humant B-lymfocytbegrænset differentieringsantigen til behandling af B-cellelymfom |
| US5773001A (en) | 1994-06-03 | 1998-06-30 | American Cyanamid Company | Conjugates of methyltrithio antitumor agents and intermediates for their synthesis |
| US6037136A (en) * | 1994-10-24 | 2000-03-14 | Cold Spring Harbor Laboratory | Interactions between RaF proto-oncogenes and CDC25 phosphatases, and uses related thereto |
| US6214388B1 (en) | 1994-11-09 | 2001-04-10 | The Regents Of The University Of California | Immunoliposomes that optimize internalization into target cells |
| US5739277A (en) | 1995-04-14 | 1998-04-14 | Genentech Inc. | Altered polypeptides with increased half-life |
| US5714586A (en) | 1995-06-07 | 1998-02-03 | American Cyanamid Company | Methods for the preparation of monomeric calicheamicin derivative/carrier conjugates |
| US5712374A (en) | 1995-06-07 | 1998-01-27 | American Cyanamid Company | Method for the preparation of substantiallly monomeric calicheamicin derivative/carrier conjugates |
| JP3431633B2 (ja) * | 1995-08-29 | 2003-07-28 | アンジェスエムジー株式会社 | Hgf遺伝子からなる医薬 |
| US7282198B2 (en) * | 1997-03-19 | 2007-10-16 | The University Of Arkansas For Medical Sciences | Immunotherapeutic methods targeted towards stratum corneum chymotryptic enzyme |
| US5981830A (en) * | 1997-05-30 | 1999-11-09 | Schering Aktiengesellschaft | Knockout mice and their progeny with a disrupted hepsin gene |
| US6423543B1 (en) * | 2000-12-20 | 2002-07-23 | Isis Pharmaceuticals, Inc. | Antisense modulation of hepsin expression |
| WO2002059373A2 (en) | 2001-01-23 | 2002-08-01 | Irm, Llc | Genes overexpressed in prostate disorders as diagnostic and therapeutic targets |
| AU2002240336A1 (en) | 2001-02-14 | 2002-08-28 | Tularik Inc. | Methods for the diagnosis and treatment of tumors employing the hepsin gene |
| US6482630B2 (en) * | 2001-03-29 | 2002-11-19 | Applera Corporation | Isolated human protease proteins, nucleic acid molecules encoding human protease proteins, and uses thereof |
| US7229774B2 (en) * | 2001-08-02 | 2007-06-12 | Regents Of The University Of Michigan | Expression profile of prostate cancer |
| US20040009911A1 (en) * | 2002-01-31 | 2004-01-15 | Irm, Llc | Hepsin substrates and prodrugs |
| US20040001801A1 (en) * | 2002-05-23 | 2004-01-01 | Corvas International, Inc. | Conjugates activated by cell surface proteases and therapeutic uses thereof |
| WO2004009803A2 (en) | 2002-07-23 | 2004-01-29 | Bayer Healthcare Ag | Regulation of human hepsin |
| EP1558731A4 (en) * | 2002-10-04 | 2007-01-10 | Schering Ag | MODIFIED HEPSINE MOLECULES COMPRISING A SUBSTITUTION ACTIVATION SEQUENCE AND USES THEREOF |
-
2005
- 2005-07-25 MX MX2007001064A patent/MX2007001064A/es active IP Right Grant
- 2005-07-25 EP EP05775274.3A patent/EP1774022B1/en active Active
- 2005-07-25 AU AU2005269463A patent/AU2005269463B2/en not_active Ceased
- 2005-07-25 WO PCT/US2005/026446 patent/WO2006014928A1/en active Application Filing
- 2005-07-25 CN CN2005800316874A patent/CN101023182B/zh not_active Expired - Fee Related
- 2005-07-25 RU RU2007106862/10A patent/RU2405041C2/ru not_active IP Right Cessation
- 2005-07-25 NZ NZ551908A patent/NZ551908A/en not_active IP Right Cessation
- 2005-07-25 ZA ZA200700745A patent/ZA200700745B/en unknown
- 2005-07-25 BR BRPI0512482-4A patent/BRPI0512482A/pt not_active IP Right Cessation
- 2005-07-25 CA CA2570323A patent/CA2570323C/en not_active Expired - Fee Related
- 2005-07-25 KR KR1020077001874A patent/KR101222254B1/ko not_active IP Right Cessation
- 2005-07-25 JP JP2007523715A patent/JP5226308B2/ja not_active Expired - Fee Related
- 2005-07-25 ES ES05775274.3T patent/ES2532610T3/es active Active
- 2005-07-25 US US11/189,230 patent/US7432044B2/en not_active Expired - Fee Related
-
2006
- 2006-12-07 IL IL179917A patent/IL179917A0/en not_active IP Right Cessation
-
2007
- 2007-06-16 HK HK07106500.3A patent/HK1100294A1/xx not_active IP Right Cessation
-
2008
- 2008-08-29 US US12/201,481 patent/US20090075317A1/en not_active Abandoned
-
2010
- 2010-03-10 US US12/721,474 patent/US20100209956A1/en not_active Abandoned
-
2012
- 2012-05-21 JP JP2012115809A patent/JP2012196217A/ja not_active Withdrawn
Also Published As
| Publication number | Publication date |
|---|---|
| US20060084120A1 (en) | 2006-04-20 |
| WO2006014928A1 (en) | 2006-02-09 |
| US7432044B2 (en) | 2008-10-07 |
| RU2007106862A (ru) | 2008-09-10 |
| EP1774022A1 (en) | 2007-04-18 |
| ES2532610T3 (es) | 2015-03-30 |
| CN101023182A (zh) | 2007-08-22 |
| KR101222254B1 (ko) | 2013-01-16 |
| CN101023182B (zh) | 2013-04-17 |
| JP2012196217A (ja) | 2012-10-18 |
| BRPI0512482A (pt) | 2008-03-11 |
| IL179917A0 (en) | 2007-05-15 |
| CA2570323C (en) | 2014-08-26 |
| HK1100294A1 (en) | 2007-09-14 |
| CA2570323A1 (en) | 2006-02-09 |
| KR20070037499A (ko) | 2007-04-04 |
| JP2008507295A (ja) | 2008-03-13 |
| EP1774022B1 (en) | 2014-12-31 |
| US20100209956A1 (en) | 2010-08-19 |
| AU2005269463A1 (en) | 2006-02-09 |
| AU2005269463B2 (en) | 2011-08-18 |
| NZ551908A (en) | 2009-10-30 |
| RU2405041C2 (ru) | 2010-11-27 |
| MX2007001064A (es) | 2007-04-12 |
| US20090075317A1 (en) | 2009-03-19 |
| ZA200700745B (en) | 2008-07-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5226308B2 (ja) | 肝細胞増殖因子活性化を制御するための方法及び組成物 | |
| US20130022611A1 (en) | Methods and compositions for modulating hepsin activation of urokinase-type plasminogen activator | |
| JP2008505182A (ja) | 非ホジキンリンパ腫の治療のための組成物と方法 | |
| US20130034570A1 (en) | Methods and compositions for modulating prostasin | |
| US8697386B2 (en) | Methods and compositions for modulating hepsin activation of macrophage-stimulating protein | |
| AU2011250759B2 (en) | Methods and compositions for modulating hepatocyte growth factor activation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080717 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080717 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110329 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110620 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120221 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120521 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120612 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121005 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20121016 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121225 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130122 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130219 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130314 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5226308 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20160322 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |