JP4122425B2 - Oocyte culture method and growth method - Google Patents
Oocyte culture method and growth method Download PDFInfo
- Publication number
- JP4122425B2 JP4122425B2 JP2002346327A JP2002346327A JP4122425B2 JP 4122425 B2 JP4122425 B2 JP 4122425B2 JP 2002346327 A JP2002346327 A JP 2002346327A JP 2002346327 A JP2002346327 A JP 2002346327A JP 4122425 B2 JP4122425 B2 JP 4122425B2
- Authority
- JP
- Japan
- Prior art keywords
- culture
- oocyte
- oocytes
- complex
- pvp
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Landscapes
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
【0001】
【発明の属する技術分野】
本発明は、動物の卵母細胞の培養技術に関する。より詳細には、発育途上にある卵母細胞をその周囲の体細胞との複合体の状態で培養し、卵母細胞を発育させる技術に関する。
【0002】
【従来の技術】
卵母細胞とは、それが発育期・成熟過程を経て、受精が可能な卵子となる前駆細胞であり、全ての卵母細胞が胎児期に形成され、発育期に入る前や発育途上の卵母細胞は分裂することはなく、発育を終えて成熟する段階で初めて「減数分裂」を行うことが知られている。「卵母細胞の発育」とは、卵母細胞の体積が著しく増大するプロセスを指し、細胞分裂によって細胞集団が増大することを意味しない。発育達成の目安となる卵母細胞の直径は、細胞膜の外側を包む透明帯の厚さを除いて、マウスなどの小型動物では約75μm、ブタやウシなどの中型・大型動物では120〜130μmである。
【0003】
卵母細胞の体積はそれぞれ220,000μm3及び1,020,000μm3程度であり、中型・大型動物の卵母細胞の体積は、小型動物の約4.6倍にもなる。サイズの違いは発育に要する時間にも反映され、マウスの卵母細胞が発育を開始してから完了するまでの期間は16〜18日、ウシやブタではマウスほど厳密には調べられていないが、およそ1.5〜2ヶ月であると考えられる。
【0004】
動物の卵巣内には、発育期以前の卵母細胞や、発育途上の卵母細胞が数多く存在する。その多くは卵巣内で失われるが、培養技術を用いてそのような卵母細胞を発育させることができれば、優良家畜の増産や卵母細胞を必要とするバイオテクノロジーへ卵母細胞を供給することが可能となる。そのような技術が研究されているが、マウスを除き、成熟卵母細胞を得ることは困難を極めており、試行錯誤の域を脱していない。
【0005】
卵巣内の卵母細胞の生存と発育には周囲の体細胞との連絡が必須である。培養においても、周囲の細胞を失った「裸化」卵母細胞は発育することができない。例えばEppigらによって開発された方法(例えば、非特許文献1及び2参照)では、マウスの発育途上の卵母細胞を包むように体細胞が付着した状態のまま分離し、培養皿やインサートメンブレン上に付着させて培養することによって、卵母細胞を発育させ、成熟卵子を得ている。従って、体外培養において卵母細胞の発育を可能とする最小限の構成は、卵母細胞とそれを包む体細胞層である。この培養系は、卵母細胞を包む顆粒膜細胞層のみで構成されており、本来その外側を包む基底膜とその周囲の細胞は含まれない。このような単純な培養方法を用いた例では、ラットを使った報告があるものの(例えば、非特許文献3参照)、マウスの成績には遠く及ばず、他の動物種(例えば、ブタやウシなどの中型・大型動物)にいたっては、卵母細胞を発育させ、成熟させたとする報告はない。
【0006】
従来の培養液を用いて、上述した方法でブタやウシなどの中型・大型動物の卵母細胞を培養した場合、体細胞が培養皿やインサートメンブレン表面を好んで伸展し、遊走する結果、卵母細胞が裸化し、死滅することが多い。あるいは、裸化を防ぐ目的で、大きな細胞塊に卵母細胞が包まれるような条件を整えて培養した場合、大きくなった細胞塊の内部で卵母細胞が死滅する。いずれの場合にも、卵母細胞を中心とする機能的で適切な3次元構造が維持されていないことが培養の失敗の原因である。
【0007】
上述した方法とならび、卵胞組織を単離して丸ごと培養する卵胞培養と称する方法がある。ハムスター、ブタ、ウシ、ヒツジ、ヒトなどのマウス以外の動物では、専らこの卵胞培養が試みられている(例えば、非特許文献4〜10参照)。卵胞構造は、最内部の卵母細胞を顆粒膜細胞層が包み、その外側を基底膜が覆い、さらにその外側を卵胞膜細胞層が取り囲むものである。上記の卵母細胞と顆粒膜細胞で構成される組織で卵母細胞を培養する系を開放型の培養系とした場合、この卵胞培養は、卵母細胞にとっては卵胞組織の最深部において閉鎖されている培養系となる。生体内での発育に要する時間を考慮した場合、卵母細胞を発育させる培養は一般に長期間にならざるを得ないことが明らかである。ウシやブタの卵胞培養については2〜4週間にも及ぶ長期培養の報告があるが、そのような長期培養後の卵母細胞に関する情報は少なく、得られている卵母細胞の能力も成熟卵子として利用する段階までには至らない(例えば、非特許文献5〜8参照)。
【0008】
また、卵胞培養では、上述した通り、培養系の深部に卵母細胞が保持されるため、卵胞内部にある卵母細胞の発育段階を直接知ることができず、また健康状態を判断することも困難である。従って卵胞培養では、卵胞を開いた時点で培養を終了することとなり、その時点で卵母細胞の成熟の適期であることのほうがむしろまれである。また、培養に長期間を要するものでは、この問題はさらに深刻なものになる。
さらにこの方法では、最初の操作段階において完全な状態で卵胞が採取された場合にのみ、培養を行うことができるという点でも制約が大きい。
【0009】
卵胞培養と類似の方法として、卵胞を一度破り、内部の発育途上卵母細胞と顆粒膜細胞群の複合体を採取し、コラーゲンゲルに包埋して培養することにより、擬似的な卵胞を形成させる方法も報告されている(例えば、非特許文献11参照)。この方法によりウシでは2週間の培養の後に成熟卵子が得られているが、卵胞腔様の構造が再び形成されるため、内部にある卵母細胞の発育段階を直接知ることができず、健康状態を判断することが困難であるという制約は残されたままである。従って、このような問題を回避し、最終段階までコラーゲンゲルに包埋することなく卵母細胞を直接観察できるように培養することができれば、さらに有用な培養系となるはずである。
【0010】
従って、様々な動物種の発育途上にある卵母細胞を、機能的な最小限の細胞構成で培養することができれば、上記の問題が解消され、卵母細胞の簡便な培養系が提供される。
【0011】
【非特許文献1】
Eppig及びSchroeder,Biology of Reproduction(USA),1989年,第41巻,p.268-276
【非特許文献2】
Eppig及びO'Brien,Biology of Reproduction(USA),1996年,第54巻,p.197-207
【非特許文献3】
Danielら,Gamete Research(USA),1989年,第24巻,p.109-121
【非特許文献4】
Roy及びGreenwald,Journal of Reproduction and Fertility(UK),1989年,第87巻,p.103-114
【非特許文献5】
Hiraoら,Journal of Reproduction and Fertility(UK),1994年,第100巻,p.333-339
【非特許文献6】
Shuttleworthら,Reproduction(UK),2002年,第123巻,p.807-818
【非特許文献7】
Gutierresら,Biology of Reproduction(USA),2000年,第62巻,p.1322-1328
【非特許文献8】
Telferら,Molecular and Cellular Endocrinology(IR),2000年,第163巻,p.117-123
【非特許文献9】
Cecconiら,Biology of Reproduction(USA),1999年,第60巻,p.594-601
【非特許文献10】
Wuら,Human Reproduction(UK),1998年,第13巻,p.2562-2563
【非特許文献11】
Yamamotoら,Theriogenology(USA),1999年,第52巻,p.81-89
【0012】
【発明が解決しようとする課題】
上記のように、ほぼ全ての動物種(特に中型・大型動物)では、卵母細胞を含む組織培養系において卵母細胞を発育させることに成功していない。従って、本発明は、そのような動物の卵母細胞を体外で発育させうる簡便な培養方法を提供することを目的とする。
【0013】
【課題を解決するための手段】
本発明者は、前記課題を解決するため鋭意検討した結果、PVP等の高分子化合物を非常に高い濃度で培養液に添加することによって、動物の卵母細胞とその周囲の体細胞とが良好に培養されることを見出した。またさらに本発明者は、発育途上にある卵母細胞をその周囲の体細胞との複合体の状態で上記条件で培養した場合には、卵母細胞が正常に発育し、得られる卵母細胞をさらに成熟させて卵子として利用可能なことを見出し、本発明を完成するに至った。
【0014】
すなわち、本発明は、卵母細胞とその周囲の体細胞との複合体を、高分子化合物を1〜12%(w/v)の濃度で含む培養液で培養することを特徴とする、卵母細胞の培養方法である。
【0015】
上記培養方法において、高分子化合物としては、合成ポリマー、多糖類系ポリマー、タンパク質、プロテオグリカン、並びにこれらの組み合わせからなる群より選択されるものを用いることができる。また高分子化合物としては、ポリビニルピロリドン(PVP)、フィコール(Ficoll)、ヒドロキシプロピルメチルセルロース、及び血清アルブミン、並びにこれらの組み合わせからなる群より選択されるものが好ましい。
【0016】
高分子化合物としてPVP単独を使用する場合、特に約4〜6%(w/v)の濃度でPVPを含む培養液を用いることが好ましい。また高分子化合物としてフィコール単独を使用する場合には、特に約2〜6%(w/v)の濃度でフィコールを含む培養液を用いることが好ましい。ヒドロキシプロピルメチルセルロースの場合には、約1〜2%(w/v)の濃度でヒドロキシプロピルメチルセルロースを含む培養液を用いることが好ましい。
【0017】
上記培養方法において、上記複合体は、例えば哺乳動物に由来するものとすることができる。哺乳動物としては、ブタ、ウシ、ヒツジ、ヤギ、イヌ、ネコ、ウサギ、ハムスター、ラット、マウス、又はヒトが挙げられる。
【0018】
また上記培養方法において、卵母細胞は発育途上のものであってもよい。さらに、上記周囲の体細胞としては、卵丘細胞、顆粒膜細胞塊及び/又は顆粒膜細胞層が挙げられる。
本発明はまた、上記培養方法により得られた卵母細胞である。
【0019】
さらに本発明は、発育途上の卵母細胞とその周囲の体細胞との複合体を、高分子化合物を1〜12%(w/v)の濃度で含む培養液で培養することを特徴とする、卵母細胞の発育方法である。
【0020】
また本発明は、上記発育方法で発育させた卵母細胞である。
本発明はさらに、上記発育させた卵母細胞を成熟させることを特徴とする、成熟卵子の作製方法である。
【0021】
【発明の実施の形態】
本発明は、卵母細胞の培養方法及び発育方法に係るものであり、卵母細胞とその周囲の体細胞との複合体を、高分子化合物を1〜12%(w/v)の濃度で含む培養液で培養することを特徴とする。
【0022】
本発明において培養対象となる「卵母細胞」とは、それが発育期・成熟過程を経て、受精が可能な卵子となる生殖細胞を指す。卵母細胞は、全ての卵母細胞が胎児期に形成され、発育期に入る前や発育途上の卵母細胞は分裂することはなく、「減数分裂」前期にあり、発育を終えて卵子に成熟する段階で初めて「減数分裂」を行うことが知られており、卵子への成熟には卵母細胞の発育完了が必須要件となる。「卵母細胞の発育」とは、卵母細胞の体積が著しく増大するプロセスを指し、細胞分裂によって細胞集団が増大することを意味しない。発育達成の目安となる卵母細胞の直径及び体積は、小型動物と大型動物では異なり、例えば大型動物の卵母細胞の体積は、小型動物の約4.6倍にもなる。このサイズの違いは発育に要する時間にも反映されるため、発育途上にある卵母細胞のサイズによって発育の完了に必要かつ適当な培養日数が決定される。従来は、発育期間の短い小型動物の卵母細胞においてその人工的培養及び発育が成功しているが、発育期間の長い大型動物の卵母細胞では、好ましい結果が得られていない。
【0023】
本発明において「発育途上にある卵母細胞」又は「発育途上卵母細胞」とは、大きさに関しては動物種固有の卵母細胞の最大直径に達していないものと定義され、能力に関しては健康であるにもかかわらず、第一減数分裂前期(卵核胞期)で停止したまま減数分裂を再開する能力を有さないもの、又は直ちに減数分裂を再開する潜在能力は有するものの第二減数分裂中期へと進む潜在能力を有さないものと定義される。また、一般に発育途上卵母細胞は、体外受精を施しても、胚発生能力を伴わない。
また卵母細胞の「成熟」とは、減数分裂を再開し、第二減数分裂中期へと分裂が進行すること、並びに受精以降の過程が可能となることを指す。
【0024】
さらに「卵胞」とは、発育期から成熟期に至るまでの卵母細胞を包む構造を指し、卵母細胞の発育とともに卵胞の体積は増大する。卵胞は細胞増殖によって発達する点で、細胞分裂を行わない発育途上卵母細胞とは異なる。卵胞はまず、単層から数層の顆粒膜細胞層が卵母細胞を包み、その外側を基底膜が覆い、さらにその外側を卵胞膜細胞層が取り囲む構造をとる。卵胞の発達期の後半では、著しく増数した顆粒膜細胞の層に出現した間隙が発達して卵胞腔となる。卵胞腔は卵胞液と呼ばれる液体で満たされ、次第に大きくなって最終的には卵胞の体積の大部分を占めるようになる。卵胞腔が形成されると、卵母細胞は数層の顆粒膜細胞に包まれて、卵胞の内壁を構成する顆粒膜細胞層の一点に付着した状態となる。このとき、卵母細胞周囲で層を形成する細胞を特に卵丘細胞と呼び、卵胞の内壁を構成する他の顆粒膜細胞とは区別されている。
【0025】
本発明においては、卵母細胞を中心とする「機能的な最小限の細胞構成」と想定される部分を培養する。この最小限の細胞構成とは、卵胞を構成する要素のうち、基底膜で仕切られている内側にあるもの、特に卵母細胞周辺の細胞群を指す。例えば、卵母細胞と卵丘細胞との複合体、卵母細胞と卵丘細胞の複合体に壁側の顆粒膜細胞集団を残したままのもの(卵母細胞・卵丘細胞・顆粒膜細胞の複合体)などである。
【0026】
以下に本発明に係る卵母細胞の培養方法及び発育方法の操作を詳細に説明する。以下の操作はすべて、室温が25℃程度の部屋で作業するとき良好な結果が得られているが、細胞や組織に障害を与えない限り、それに限定されるものではない。
【0027】
最初に、卵母細胞とその周囲の体細胞との複合体を採取するため、卵巣を採取する。
卵巣は、動物から採取する。本発明において「動物」とは、卵母細胞を有する動物であれば限定されるものではないが、特に哺乳動物、例えば、ウシ、ブタ、ヒツジ、ヤギ、イヌ、ネコ、ウサギ、ハムスター、ラット、マウス又はヒトなどが好ましい。
【0028】
動物から卵巣を採取するには、動物の生死を問わず、通常開腹して切り離す。動物の死後、あるいは生体から切り離された時点から、卵巣内は虚血状態へと向かうため、卵巣組織への障害を軽減するためにできるだけ速やかに以下の操作に移ることが好ましい。
【0029】
卵巣を生理的濃度のリン酸緩衝液(phosphate buffered saline;PBS)で洗浄した後、表面から1〜2mmの厚さで組織片を切り離して、組織培養液に移す。組織培養液は、ウェイマウス培地(Waymouth's medium)、最少必須培地(Minimum Essential Medium)、199培地(Medium 199)などの通常の組織培養に用いられるものであれば本発明において利用可能である。また、実験台上での操作に使用する培養液は、そのpHが大気中の気相で7前後に安定するようHEPES(2−[4−(2−ヒドロキシエチル)−1−ピペラジニル]エタンスルホン酸)などの緩衝液で緩衝されているものが望ましい。組織の切断は、どのような刃物を用いて行ってもよく、一般的に用いられている外科手術用の替刃メス(メスハンドルに装着したもの)やスカルペルなどを用いて行うことができる。
【0030】
続いて、培養液中の組織をさらに細切し、卵胞組織を切り出す。卵胞組織は、過度の圧迫によって傷つけることのないよう留意して切り出し、卵胞内部に細胞の脱落などの明らかな退行の兆候が認められるものは使用しない。卵胞をサイズで分類しておくと、卵母細胞をサイズで分けるうえで都合が良い(例えば、Hiraoら,Zygote(UK),1995年,第3巻,p.325-332参照)。
【0031】
次に、切り出した卵胞組織の一箇所に、基底膜内部に達する切れ込みを入れる。この切開した部分から、卵母細胞とその周囲の体細胞との複合体を採取する。本発明において「卵母細胞とその周囲の体細胞との複合体」又は「複合体」とは、卵母細胞とその周囲に存在する体細胞から構成される複合組織を指し、例えば、卵母細胞と卵丘細胞との複合体、卵母細胞・卵丘細胞・顆粒膜細胞の複合体などが含まれる。従って、「周囲の体細胞」としては、限定されるものではないが、卵丘細胞、顆粒膜細胞が挙げられる。卵胞を卵巣(の組織片)を酵素処理することによって採取し、培養皿内において複合体を形成させるような場合には、卵胞膜細胞が混入する可能性がある。
【0032】
卵母細胞とその周囲の体細胞との複合体の採取は、上述した以外にも、卵胞を単離するプロセスを省き、卵巣にカミソリ等で切りこみを入れたのちに培養液で洗い流し、培養液中に放出された複合体を直接回収する方法により行ってもよい。また、複合体の採取においては、卵巣内の卵胞から、注射針と注射筒を用いて複合体を吸引する方法も利用できる。また生体内の卵巣から、生体内卵子吸引と称する手法を用いて複合体を吸引する方法も採用することができる。
【0033】
以上、卵母細胞とその周囲の体細胞との複合体を採取するための物理的な分離方法について述べたが、本発明において複合体の採取方法は、上記の方法に限定されるものではない。
【0034】
また、上述した物理的方法だけでなく、酵素(例えばコラゲナーゼなど)で卵巣断片を処理することによって卵胞を分離したり、又は、卵巣を酵素と共に培養することによって卵母細胞とその周囲の体細胞との複合体の形状を形成させることにより、卵母細胞とその周囲の体細胞との複合体を採取することもできる。
【0035】
さらに、本発明において「複合体」には、本発明において使用する前に、予め一時的に培養(例えば卵胞培養や卵巣器官培養)したもの、又は他の動物種の臓器に一定期間にわたり移植された後に採取されたものも含まれる。また、別途調製した体細胞を「複合体」と一緒に培養することも含まれる。従って、本発明の「複合体」には、卵母細胞とその周囲の体細胞とから構成されるものである限り、任意の形態及び状態のものが含まれる。例えば本発明において培養対象となる「複合体」には、卵胞全体も含まれるものとする。
【0036】
複合体を採取した後、採取時の卵母細胞の状態を調べておくことが好ましい。通常、採取時の卵母細胞の直径、卵母細胞の生死及びその健康状態が、その後の培養における重要な情報となる。
【0037】
卵母細胞の直径(透明帯を含まない部分)の測定方法としては、以下に限定されるものではないが、顕微鏡に接続した測微接眼レンズを用いて直径を測定する方法や、顕微鏡を通して見える画面をコンピュータに取り込み、画像解析ソフトウェアで測定する方法がある。
【0038】
発育途上にある卵母細胞の直径と卵胞の直径との間には相関があり(例えば、Hiraoら,Zygote(UK),1995年,第3巻,p.325-332参照)、直接卵母細胞の直径を測定する前に、卵胞の直径から卵母細胞の直径を推測することもできる。例えば、本発明において実施例4において用いた直径約90〜99μmのウシ発育途上卵母細胞は、直径約0.5〜0.7mm程度の卵胞に存在すると推測される。このような相関は当技術分野で周知であり、相関を利用することによって卵母細胞の直径を容易に求めることができる。
【0039】
また、卵母細胞の生死及び健康状態は、該細胞の細胞質又は細胞膜が崩壊していないかどうかを顕微鏡下に観察して判定することができる。
上述した直径の測定や観察の方法は、培養後の卵母細胞にも適用される。
【0040】
続いて、上述のようにして採取した卵母細胞とその周囲の体細胞との複合体、好ましくは発育段階にある卵母細胞を含む複合体を、培養液を準備しておいた培養皿又は培養皿に装着したインサートメンブレン上に導入する。
【0041】
複合体培養用の培養液は、基本となる組織培養液に、修正を加えて用いる。本発明において利用可能な基本組織培養液は、通常の細胞培養に使用されているものであれば特に限定されるものではなく、例えば、ウェイマウス培地、最少必須培地、199培地などが挙げられる。
【0042】
複合体の培養に用いる培養液に加える最も重要な修正は、高分子化合物の添加である。本発明において「高分子化合物」とは、分子量が数万〜数百万の有機物質であり、天然高分子(生体高分子など)及び合成高分子のいずれをも含む。本発明において用いる「高分子化合物」は、特に、水に溶解しやすいこと、細胞毒性が極めて低いこと、培養中に培養液のpH等を不安定にさせる性質を有さないこと、また、その他にも初期の特性が長期間安定して維持されること、などの条件を満たすものが好ましい。例えば本発明において利用可能な高分子化合物としては、合成ポリマー、多糖類系ポリマー、タンパク質、プロテオグリカンなどが挙げられる。例えば合成ポリマーとしては、ポリビニルピロリドン(PVP;分子量約36万)、ポリビニルアルコール(PVA;分子量約7万〜10万)などが挙げられる。多糖類系ポリマーとしては、デキストラン、ヒドロキシエチル化デンプン、セルロース類の誘導体(例えばヒドロキシプロピルメチルセルロース)などが挙げられる。また多糖類系ポリマーとしては、スクロースの合成ポリマーであるフィコール(分子量40万)、ヒアルロン酸やコンドロイチン硫酸のグリコサミノグリカンなども挙げられる。タンパク質としては血清アルブミン(分子量約6.9万)などが挙げられる。また、プロテオグリカンとしてはコンドロイチン硫酸プロテオグリカンなどが挙げられる。
【0043】
本発明において特に好ましい高分子化合物としては、限定されるものではないが、PVP、フィコール、ヒドロキシプロピルメチルセルロース((Hydroxypropyl)methyl cellulose)、血清アルブミンが挙げられる。
【0044】
上述した以外にも、本発明において利用可能な高分子化合物としては、現在知られている同等の機能を示す化合物、あるいは今後見出される又は合成される化合物も包含される。ある化合物が、本発明において利用可能な「同等の機能」を示す化合物であるかどうかを確認するには、培養に使用した際、卵母細胞の生存性を損なわないこと、卵母細胞周囲の体細胞が脱落しないこと、かつ卵母細胞を中心とした構造を失わないこと(不規則で広範な細胞増殖が起こらないこと)に留意しながら「複合体」を長期培養することが有効である。また、良好な状態が十分な期間維持され、その結果卵母細胞が最終段階にまで発育することを確認することが重要である。
【0045】
培養液に添加する高分子化合物の濃度は、培養液に対し、約1〜12%(w/v)、好ましくは2〜8%(w/v)、より好ましくは4〜6%(w/v)、最も好ましくは約4%(w/v)である。
【0046】
高分子化合物の濃度は、上述した範囲であれば本発明の目的を達成することが可能であるが、その他の範囲の濃度であっても本発明の目的を達成することができる場合もある。具体的には、ヒドロキシプロピルメチルセルロースやグリコサミノグリカンなど、濃度が低くとも高い粘度を示す化合物を添加する場合である。例えば、培養液にある種のヒドロキシプロピルメチルセルロースを1%(w/v)の濃度で添加したとき、卵母細胞と体細胞の複合体の形態も4%(w/v)PVP(分子量36万)の良好な結果と類似しており、本発明の効果が達成されることが観察された。
【0047】
PVPやPVAなどの高分子化合物は、卵子培養液に慣例的に用いられているという事実がある。特にウシ胎児血清や血清アルブミンを含まない培養液に対し、高分子の代替物として添加されることが多い。この場合、卵子細胞が培養皿の底面又は壁面、及び胚操作用極細ガラス管の外面又は内面に付着して失われることを防ぐためにも有用であるとされている。しかし、そのような目的を果たすための濃度は一般的に約0.1%〜0.4%で十分であり、それが通常用いられる濃度となっている。また、基本となる培養液に血清等が添加される場合には、高分子化合物は添加されないことが多い。それに対し、本発明では約1〜12%にまで濃度を上げることにより、全く異なる効果が達成されることを導き出した。一方、従来用いられている0.1%〜0.4%の濃度で添加した場合には、本発明の目的とする効果は発揮されない。従って、本発明においては、従来の濃度を0.4%としても、その約2.5倍以上、好ましくは約10〜15倍の濃度で高分子化合物を添加することが重要である。
【0048】
上述した高分子化合物の添加のほか、培養液には一般の細胞培養で行われる修正もなされるが、特定の修正に限定されるものではない。例えば、5%ウシ胎児血清、抗生物質の添加などである。
【0049】
また、培養液には、顆粒膜細胞や卵母細胞などの細胞培養に適した培養液にするための修正を行ってもよい。例えば限定されるものではないが、ピルビン酸ナトリウムは、特定の動物種に限らず、卵母細胞の培養液に一般的に添加されている。
【0050】
その他にも、例えばウシの顆粒膜細胞を含む複合体の培養においては、2mM〜4mMのヒポキサンチン及び10〜100ng/mlのエストラジオール17βなどを添加した場合に、細胞の増殖が良好であることが知られている。またブタの卵丘細胞を含む複合体の培養においては、低濃度の卵胞刺激ホルモン(follicle stimulating hormone;FSH)(例えば10ng/ml)をさらに添加した場合に、細胞の増殖が良好であることが知られている。本発明においては、このような動物種及び培養対象の複合体に含まれる細胞種に応じて、適宜培養液に修正を加えることが好ましい。
使用する培養皿は、一般に動物細胞の培養に用いられるものであれば、その形態・材質などは特に限定されない。
【0051】
また培養皿は、細胞が付着するための基質を備えることが好ましく、それにより、培養基質上に細胞層があり、その上に卵母細胞とその周囲の体細胞との複合体が配置されている状態を維持することが可能となり、本発明の目的を良好に達成することができる。このような細胞が付着する基質しては、細胞群の接着と増殖を妨げないもの、例えば種々のインサートメンブレンを用いることが好ましい。また、コラーゲンコートを施した培養皿も好適である。しかし、細胞増殖という条件を満たすものであれば、上述した培養基質に特に限定されるものではない。
【0052】
培養皿あたりの卵母細胞の個数は、卵母細胞源、培養液量、培養皿の種類などに応じて変更することができ、例えば、容量の比較的大きい6ウエルの培養皿(培養液量約4.5ml/ウエル)では、顆粒膜細胞塊が付着する大きな複合体については10〜20個を培養することが好ましく、卵丘細胞と卵母細胞からなる複合体については、20〜50個の複合体を培養することができる。一方、24ウエルやさらにウエル当たりの容量の小さい培養皿においては、顆粒膜細胞塊が付着する大きな複合体では、複合体当たりの培養液量を約200〜500μl、卵丘細胞と卵母細胞からなる複合体では約50〜150μlとして培養を行うことが好ましい。上記例は一例であり、細胞の形態や細胞の代謝によるpHの変化を考慮して、培養液当たりの複合体の数を増やすことができる。
【0053】
培養皿を設置するインキュベータは、一般に動物細胞培養に使用されるものであればよい。培養条件は、例えば、37℃〜39℃、5%炭酸ガス95%空気の気相で、高湿度の環境が好ましく、このような条件を設定可能なインキュベータを使用する。上記培養条件は、一例として記載しており、培養液の種類やpHの調整方法などを考慮して、細胞の増殖や生存を妨げない範囲で変更可能である。卵母細胞の培養に好ましい培養条件は、当技術分野で公知である。
【0054】
培養を開始した後、卵母細胞は、その周囲の体細胞に包まれた状態で発育を続ける。本発明により、その培養過程において、卵母細胞に最も近い体細胞層との結合が良好に維持される。
【0055】
培養期間中、2〜4日に一度、培養液の一部を新鮮なものに交換することが常識的に行われており、本発明においても適宜培養液を交換することが好ましい。培養期間は、使用する動物種及び採取した卵母細胞の状態により異なるが、一般的にウシやブタでは数日から約4週間であり、当業者であれば適宜設定することが可能である。
【0056】
本発明により、多くの卵母細胞とその周囲の体細胞との結合状態を保ったまま、発育した卵母細胞を回収することができる。培養後に回収した複合体において、体細胞につつまれている卵母細胞の割合は、本発明を用いることによって顕著に(例えば約2〜5倍)増加する。
【0057】
培養後の卵母細胞の直径は、前述した方法で測定する。それによって、培養期間中における卵母細胞の発育の程度を知ることができる。卵母細胞の直径が動物種固有の最大値となった時点で、発育は完了したとみなしてよいが、卵母細胞とその周囲の体細胞の形態が正常であることを確認しつつ、さらに数日間から1週間程度培養を継続してもよい。
【0058】
本発明により、卵母細胞の発育を単に促進するだけではなく、体細胞との複合体の状態で卵母細胞を発育させることができる。このことは、その後行う卵母細胞の成熟過程において、この体細胞に包まれたままの状態であることが、体細胞を介して行われるホルモンや成長因子による成熟誘起や、成熟培養において酸化ストレスを代表とする種々のストレスから卵母細胞を保護する作用の点で極めて重要となる。
【0059】
本培養方法はまた、培養の開始までの操作、培養中の観察、さらには培養後の卵母細胞の回収操作が、従来のコラーゲンゲルに包埋する培養方法や卵胞培養と比較して簡便なものである。
【0060】
本発明は、長期間の培養を可能にするものであるが、卵母細胞の発育を観察することができることから、卵母細胞のサイズ、すなわち発育の程度に応じて培養期間を変えることが可能である。また、培養期間中に発育を達成した卵母細胞も、体細胞との結合を維持した状態で生存していることから、本培養方法は、発育途上の卵母細胞に限るものではなく、発育後の卵母細胞にも有効である。
【0061】
また、本発明の目的は、卵母細胞とその周囲の体細胞との複合体の機能的で最小限の3次元構造を維持することにあるが、コラーゲンゲルに包埋した複合体の培養方法又は卵胞培養にも、本発明で用いる培養液を適用することができ、培養を有効に行うことができる。
【0062】
上述のようにして得られた卵母細胞は、核酸、化学物質又は抗体などのタンパク質を顕微注入した後に、培養するなどの物理的な操作を加えることも可能である。従って、本発明により得られる卵母細胞は、卵母細胞の研究に有用である。
【0063】
また上述のようにして得られた卵母細胞は、一般に使用されている未成熟卵母細胞を体外成熟させるための培養方法を行うことにより、卵子に成熟させてそれを利用することができる。
【0064】
成熟培養への転換は、通常、発育培養を終えた培養皿から卵母細胞と体細胞の複合体を回収し、成熟用培養液で洗浄したのち、最終的な成熟用培養液に移すことで行う。成熟用組織培養液は、199培地などを基本培地として、ピルビン酸ナトリウムや抗生物質などの必須要素を加え、さらに性腺刺激ホルモン、成長因子、血清、卵胞液などが適宜添加されて用いられる。このような卵母細胞の成熟培養に好ましい培養条件は、広範に調べられており、当技術分野で公知である。培養皿を設置するインキュベータは、通常発育培養に使用されるものと同様の設定で用いられる。
【0065】
このようにして成熟させた卵子は、通常の体外受精に用いることができるほか、単為発生胚の作製やクローン動物作出におけるレシピエント卵子などに用いることができる。
【0066】
【実施例】
以下、実施例により本発明を説明する。但し、本発明はこれら実施例にその技術的範囲が限定されるものではない。
【0067】
〔実施例1〕PVP添加培養液を用いたブタ卵母細胞の培養
食肉処理場で採取したブタの卵巣をPBSで洗浄した後、表面から1〜2mmの厚さで組織片を切り離して、組織洗浄用培養液を入れた培養皿(径100mm)に移した。組織洗浄用培養液には、0.1%のウシ血清アルブミンを含むHEPES緩衝199培養液(Medium 199;シグマ(Sigma)社製)(pH7.2)を用いた。実体顕微鏡下に発達途上の卵胞を探し、柄に装着した使い捨て手術用刃を用いて、直径0.5〜1mmの卵胞を切り出し、新鮮な組織洗浄用培養液に移した。次いで、基底膜内部に達する切れ込みを入れ、反対側をピンセットで押すことにより、開口部分から卵母細胞・卵丘細胞の複合体を採取した。
【0068】
個々の卵母細胞・卵丘細胞の複合体は、それぞれ洗浄用培養液の小滴に移し、倒立顕微鏡に接続した測微接眼レンズを用いて、200倍の倍率で、一個ずつ卵母細胞の直径を測定した。この段階で、明らかに退行の兆しが見える卵母細胞を除去し、残りの健康な卵母細胞・卵丘細胞の複合体を培養に供した。
【0069】
培養液には、基本となる組織培養液として、5%ウシ胎児血清、4mMヒポキサンチン、10ng/ml FSH、100μg/mlピルビン酸ナトリウム、80μg/mlカナマイシン及び0.1μg/mlエストラジオール17βを添加したウェイマウス培養液(ギブコ(Gibco)社製)を用いた。PVP(シグマ社製、平均分子量36万)については、0%〜10%の濃度で添加したものを使用した(0、1、2、4、6、8及び10%)。
【0070】
培養皿として、6ウエルあるいは24ウエルの培養プレートに、コラーゲンコートが施してあるインサートメンブレン(バイオコート、ベクトン・ディキンソン(Becton Dickinson)社製)を装着して用いた。そのような培養皿にあらかじめ培養液を加えて(6ウエルではインサートの内側2ml、外側2.5ml、24ウエルでは内側500μl、外側600μl)、38.5℃、5%CO2・95%空気の条件に整えたインキュベータ(三洋電機社製)の中で平衡させておき、培養前の観察がなされた卵母細胞・卵丘細胞の複合体を、培養皿のメンブレン上に導入した。その後、直ちにインキュベータに移して培養を開始した。培養は12日間行い、4日に一度、培養液の半分を新鮮なものに交換した。
【0071】
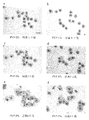
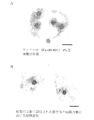
培養の進行に伴う、複合体の形態の変化を図1Aのa〜f及び図1Bのg〜jに示す。図1のa、c、e、g及びiがPVP無添加区における培養1日、3日、6日、9日及び12日後の形態を示す。一方、図1のb、d、f、h及びjがPVP4%添加区において、上記PVP無添加区と同様の日数が経過した場合の形態を示している。図1Aのa及びbからわかるように、培養1日後の複合体の形態には、PVPの添加の有無による影響はあまり認められない。しかし、培養3日後には、PVP4%添加区において明らかに卵母細胞周囲の整然とした体細胞増殖が見られるのに対し(図1Aのd)、無添加区においては、十分かつ均一な厚さで細胞層が卵母細胞を覆う基本的な構造がすでに乱れている(図1Aのc)。その傾向は培養6日以降では、さらに顕著になる(図1Aのe及びf)。図1Bのg及びiに見られるように、PVP無添加区においては、体細胞は増殖するが、卵母細胞の存在と関わらない形で、規則性のない増殖となった。それに対し、図1Bのh及びjで明らかなように、PVP4%添加区においては、卵母細胞を安定した厚さの細胞層が取り囲むように増殖する傾向が認められた。
【0072】
PVP4%添加区において卵母細胞と体細胞の連絡が好適に維持されたことは、培養後に回収された卵母細胞の形態をみても明らかであった(図2A及びB)。PVP無添加区(図2A)においては、培養中に裸化、退行した卵母細胞が多く、最終的に回収されたものについても、卵丘細胞を多く失った卵母細胞などであった。それに対し、PVP4%添加区(図2B)において回収された卵母細胞は、PVP無添加区と比較して、体細胞と付着の程度や形態がより充実していた(図2B)。
【0073】
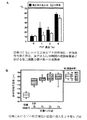
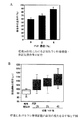
回収された卵母細胞と体細胞の複合体の生存率を調べるとともに、この複合体に対し、妊馬血清製性腺刺激ホルモン(PMSG)及びヒト絨毛性性腺刺激ホルモン(hCG)をそれぞれ10IU/mlで作用させ、48時間の成熟培養を行った。その後、卵母細胞を固定・染色し、第二減数分裂中期への成熟率を調べた。PVP添加区において回収された卵母細胞の割合は、PVP無添加区と比較して高くなり、4%で顕著に高い値を示した(図3A)。また、成熟培養後に第二減数分裂中期へと達した卵母細胞の割合も高い値を示した。PVP濃度は8%及びそれ以上では顆粒膜細胞の増殖が抑えられる傾向にあった。図3Aで示した卵母細胞の直径を調べたところ、培養開始時よりもはるかに大きくなり、最終的なサイズにまで発育していた(図3B)。
【0074】
〔実施例2〕フィコール添加培養液を用いたブタ卵母細胞の培養
実施例1と同様の方法で発育途上卵母細胞・卵丘細胞の複合体を採取して培養に供した。実施例1と同様の培養液に、PVPに代えてフィコール(Ficoll(登録商標)400、平均分子量40万、シグマ社製)を0〜10%(w/v)の濃度で添加して使用した(0、1、2、4、6、8及び10%)。また、培養皿及びインキュベータの設定についても、実施例1と同様であった。
【0075】
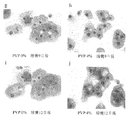
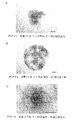
図4Aがフィコール4%(w/v)添加区において培養が12日経過した場合の形態を示している。実施例1のPVP4%添加区において認められたと同じように、卵母細胞を安定した厚さの細胞層が取り囲むように増殖する傾向が認められ、卵母細胞と体細胞の連絡が好適に維持されることが知られた。
【0076】
実施例1と同様の方法で成熟培養を行ったところ、卵丘細胞の膨潤化が認められた(図4B、成熟培養24時間後の写真)。図4Bは、PMSG及びhCGの刺激に反応した結果、卵丘細胞内でヒアルロン酸が合成されたことを示し、長期培養後の複合体において、卵丘細胞にそれらホルモンの受容体が配置されていること、刺激後にヒアルロン酸合成に至るプロセスが機能していることなどが示された。同時に卵母細胞の成熟も確認されたことから、卵丘細胞と卵母細胞の連絡が正常に行われること、その結果、卵母細胞の成熟を誘起することができることなどが示された。
【0077】
図5にフィコール 0%、1%、2%及び4%(w/v)添加区における培養12日後に得られた正常な形態のブタ卵母細胞と体細胞との複合体の割合、及びさらに48時間の成熟培養を施した場合の第二減数分裂中期への成熟率を示す。通常、フィコールは卵母細胞の長期培養に添加物として使用されるものではないが、もし用いられたとしても、常識的な高分子の添加量の範囲である0.1%から1%未満では、卵母細胞を安定した厚さの細胞層が取り囲むという良好な形態は得られないことが明らかとなった。一方、高濃度(特に4%以上)にフィコールの添加濃度を高めた結果、卵母細胞と体細胞との複合体の生存率及び卵母細胞の成熟率が高まることがわかった。
【0078】
〔実施例3〕ヒドロキシプロピルメチルセルロース添加培養液を用いたブタ卵母細胞の培養
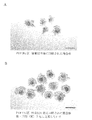
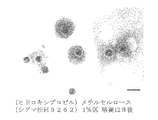
実施例1と同様の方法で発育途上卵母細胞・卵丘細胞の複合体を採取して培養に供した。実施例1と同様の培養液に、PVPに代えてヒドロキシプロピルメチルセルロース((Hydroxypropyl)methyl cellulose)(シグマ社、H9262)を1%の濃度で添加して使用した。また、培養皿及びインキュベータの設定についても、実施例1と同様であった。使用したヒドロキシプロピルメチルセルロースはその分子性状から、実施例1のPVPと同じ濃度でも溶液中で異なる粘度を示した。培養12日後の写真(図6)から明らかなように、卵母細胞を安定した厚さの細胞層が取り囲むように増殖する傾向が認められた。
【0079】
〔実施例4〕PVPを用いたウシ卵母細胞の培養
食肉処理場で採取したウシの卵巣をPBSで洗浄した後、表面から1〜2mmの厚さで組織片を切り離して、実施例1と同様の方法で卵胞を切り出した。そのうち、直径0.5〜0.7mmのものを選び、新鮮な組織洗浄用培養液に移して、基底膜内部に達する切れ込みを入れた。実施例1と同様、切り口の反対側をピンセットで押すことにより複合体を得たが、この実施例4では、卵母細胞・卵丘細胞・顆粒膜細胞の複合体を採取して培養に供した。採取後ただちに、実施例1に示した方法で卵母細胞の直径の測定及び健康な複合体の選択を行った。
【0080】
培養液には、基本となる組織培養液として、5%ウシ胎児血清、4mMヒポキサンチン、100μg/mlピルビン酸ナトリウム、80μg/mlカナマイシン及び0.1μg/mlエストラジオール17βを添加したウェイマウス培養液(ギブコ社製)あるいは199培養液(日水製薬社製)を用い、PVPを0%〜12%の濃度で添加したものを最終的に使用した(0、0.25、1、2、4、6及び12%)。培養皿やインキュベータの設定については、実施例1と同様であった。
【0081】
ブタにおける実施例1と同様、PVPの添加濃度を4%程度又はそれ以上に高くするに伴い、培養14日後において卵母細胞と卵丘細胞の複合体を安定した成績で回収することができるようになった。最も高い濃度である12%添加区においても卵子は裸化することなく複合体として回収され、24時間の成熟培養後には第一極体を放出した卵母細胞を確認することができた。体細胞の増殖や、その外観の健康状態は4〜6%添加区の複合体の場合が最も良好であり、また複合体を導入する際の操作性を考えて、培養液の比重が過度に重くならないようにする意味からも、PVPは4〜6%で培養液に添加することが特に好ましい。一方、0.25%添加区では、効果は認められず、1%添加区では、複合体の形態がやや改善されたものの、2%以上の添加区において認められた効果には及ばなかった。4%添加区で最も良い値を示し、2%添加区では、4%区と0%区の間を示す結果となった。
【0082】
培養の進行に伴う、PVP4%添加区における複合体の形態の変化を図7のA、B及びCに示す。培養2日後に比べ、培養9日後においては卵母細胞を体細胞が取り囲みながら、増殖して広がっている様子が明らかである。図7Cには、PVP4%添加区における培養14日後の典型的な複合体の形態を示す。中央の大きな卵母細胞を中心に、緊密な細胞層が卵母細胞に最も近いところを取り囲み、その周囲には放射状に配列していることが認められる。
【0083】
培養14日後に回収された正常な卵母細胞・卵丘細胞の複合体の割合を比較して見ると、ブタにおける実験(実施例1)と同様、PVP無添加区及び2%添加区に比べて、PVP4%添加区において高い値を示した(図8A)。また、卵母細胞の直径が培養開始時よりもはるかに大きくなり、最終的なサイズに発育するものが認められた(図8B)。
【0084】
〔実施例5〕卵子への成熟及び受精
基本培養液に199培養液(ギブコ社製)を用い、実施例3と同様にPVP0%又は4%添加培養液においてウシ卵母細胞を14日間発育培養した。発育培養後に卵母細胞と卵丘細胞の複合体を回収し、成熟培養及び体外受精を行った。
【0085】
体外成熟は、199培養液(ギブコ社製)に5%ウシ胎児血清、ピルビン酸ナトリウム及び20mAU/mlの卵胞刺激ホルモン(アントリン、デンカ製薬製)を添加した培養液を用いて行い、38.5℃、5%炭酸ガス95%空気の気相で、高湿度の環境において24時間培養を行った。成熟培養後、膨潤化した卵丘細胞に包まれた卵母細胞を回収し、カフェイン、ヘパリン及びウシ血清アルブミンを含む媒精用基礎培地(BO液)で洗浄して、卵子を得た。
【0086】
一方、凍結ウシ精液を融解して精子の洗浄処理を施し、上述の通り調製した卵子を含む培養液に加えて体外受精に供した。媒精から6時間後、卵子を受精卵培養液(IVD−101,機能性ペプチド研究所製)に移し、38.5℃、5%酸素5%炭酸ガス90%窒素の気相で、高湿度の条件に整えたインキュベータ(ヒラサワ社製)において7日ないし8日間培養し、胚盤胞のステージへと進んだものの割合を調べた。その結果、実際に胚発生能力を獲得しうることを見出した(図9)。PVP無添加区において体外発育した卵子28個のうち、体外受精後に胚盤胞期へと発生したものは1個(4%)であったのに対し、PVP4%添加区において体外発育した卵子60個のうち、胚盤胞期へと発生したものは7個(12%)であった。
【0087】
【発明の効果】
本発明により、卵母細胞の簡便な培養方法及び発育方法が提供される。本培養方法においては、卵母細胞とその周囲の体細胞の複合体を、形態的及び機能的な関係を良好に保ちつつ培養することができる。また発育途上にある卵母細胞を培養に供した場合にも、卵母細胞を最終段階まで発育させることが可能となる。本培養方法又は発育方法においては、培養後にも卵母細胞とその周囲の体細胞との結合は良好に維持されており、発育に成功した卵母細胞は、卵子にまで成熟させて、それを利用することが可能となる。
【図面の簡単な説明】
【図1A】発育途上ブタ卵母細胞と体細胞との複合体の、PVP0%添加区(無添加区)又はPVP4%(w/v)添加区における培養中の写真を示す。
a:PVP0%添加区、培養1日後。スケールは200μmを示す。
b:PVP4%添加区、培養1日後
c:PVP0%添加区、培養3日後
d:PVP4%添加区、培養3日後
e:PVP0%添加区、培養6日後
f:PVP4%添加区、培養6日後
【図1B】ブタ卵母細胞と体細胞との複合体の、PVP0%添加区(無添加区)又はPVP4%添加区における培養中の写真を示す。
g:PVP0%添加区、培養9日後
h:PVP4%添加区、培養9日後
i:PVP0%添加区、培養12日後
j:PVP4%添加区、培養12日後
【図2】PVP0%添加区(A)及びPVP4%添加区(B)における培養12日後に得られたブタ卵母細胞と体細胞との複合体の写真を示す。スケールはいずれも200μmを示す。
【図3】A:PVP0%、1%、2%及び4%(w/v)添加区における培養12日後に得られた正常な形態のブタ卵母細胞と体細胞との複合体の割合、並びにさらに48時間の成熟培養を施した場合の第二減数分裂中期への成熟率を示す。
B:培養前及び12日間の培養後におけるブタ卵母細胞の直径(B)を示す。
【図4】発育途上ブタ卵母細胞と体細胞との複合体の、フィコール(Ficoll)(登録商標)400、平均分子量40万、シグマ社製)4%(w/v)添加区における培養12日後の写真(A)及び成熟培養における卵丘細胞の膨潤化(B)の写真を示す。スケールはいずれも200μmを示す。
【図5】フィコール 0%、1%、2%及び4%(w/v)添加区における培養12日後に得られた正常な形態のブタ卵母細胞と体細胞との複合体の割合、並びにさらに48時間の成熟培養を施した場合の第二減数分裂中期への成熟率を示す。
【図6】ブタ卵母細胞と体細胞との複合体の、ヒドロキシプロピルメチルセルロース((Hydroxypropyl)methyl cellulose、シグマ社H9262)1%(w/v)添加区における培養12日後の写真。スケールは200μmを示す。
【図7】発育途上ウシ卵母細胞と体細胞との複合体のPVP4%(w/v)添加区における培養2日(A)、9日(B)及び14日(C)後の写真を示す。スケールはいずれも200μmを示す。
【図8】PVP0%、2%及びPVP4%(w/v)添加区における培養14日後に得られた正常な形態のウシ卵母細胞と体細胞との複合体の割合(A)、及びウシ卵母細胞の直径(B)を示す。
【図9】PVP4%(w/v)添加区において14日間培養したウシ卵母細胞・体細胞複合体由来の卵子を成熟させ、体外受精することによって得られた胚を撮影した写真を示す。スケールは100μmを示す。[0001]
BACKGROUND OF THE INVENTION
The present invention relates to a technique for culturing animal oocytes. More specifically, the present invention relates to a technique for growing an oocyte by culturing a developing oocyte in a complex state with surrounding somatic cells.
[0002]
[Prior art]
An oocyte is a progenitor cell that becomes an egg that can be fertilized through its developmental stage and maturation process, and all the oocytes are formed in the fetal period and before entering the developmental stage or in the developing egg. It is known that mother cells do not divide and perform "meiosis" for the first time at the stage of development and maturation. “Oocyte development” refers to a process in which the volume of the oocyte increases significantly and does not mean that the cell population increases due to cell division. The diameter of the oocyte, which is a standard for achieving growth, is about 75 μm for small animals such as mice, and 120 to 130 μm for medium and large animals such as pigs and cows, excluding the thickness of the zona pellucida that wraps outside the cell membrane. is there.
[0003]
Each oocyte volume is 220,000 μm Three And 1,020,000 μm Three The volume of oocytes in medium and large animals is about 4.6 times that of small animals. The difference in size is also reflected in the time required for development, and the period from the start of development of mouse oocytes to completion is 16-18 days, although in cattle and pigs it has not been examined as closely as mice , Approximately 1.5 to 2 months.
[0004]
In the ovary of an animal, there are many oocytes before the development period and developing oocytes. Many of them are lost in the ovaries, but if such oocytes can be grown using culture techniques, they can increase production of good livestock and supply oocytes to biotechnology that requires oocytes. Is possible. Although such techniques have been studied, it has been extremely difficult to obtain mature oocytes except for mice, and it has not left the range of trial and error.
[0005]
Communication with surrounding somatic cells is essential for the survival and development of oocytes in the ovary. Even in culture, “naked” oocytes that have lost surrounding cells cannot develop. For example, in the method developed by Eppig et al. (See, for example,
[0006]
When culturing oocytes of medium-sized or large animals such as pigs and cows using conventional culture medium by the above-mentioned method, somatic cells prefer to spread on the surface of the culture dish or insert membrane and migrate, Mother cells often become naked and die. Alternatively, in order to prevent nakedness, when cultured under conditions that allow the oocyte to be wrapped in a large cell mass, the oocyte is killed inside the enlarged cell mass. In any case, the failure of the culture is that the functional and appropriate three-dimensional structure centering on the oocyte is not maintained.
[0007]
In addition to the above-described method, there is a method called follicular culture in which follicular tissue is isolated and cultured as a whole. In animals other than mice such as hamsters, pigs, cows, sheep, and humans, this follicular culture has been attempted exclusively (see, for example, Non-Patent
[0008]
In addition, as described above, in follicular culture, the oocyte is retained in the deep part of the culture system, so it is not possible to directly know the developmental stage of the oocyte inside the follicle, and it is also possible to judge the health condition. Have difficulty. Therefore, in follicular culture, the culture is terminated when the follicle is opened, and it is rather rare that the oocyte matures at the appropriate time. In addition, this problem becomes more serious when the culture takes a long time.
Furthermore, this method has a great limitation in that the culture can be performed only when the follicle is collected in a complete state in the first operation stage.
[0009]
As a method similar to follicular culture, a follicular follicle is formed by breaking the follicle once, collecting a complex of the inner developing oocyte and granulosa cell group, and embedding it in a collagen gel and culturing. The method of making it report is also reported (for example, refer nonpatent literature 11). In this method, matured ova are obtained after 2 weeks of culture in cattle, but the follicular cavity-like structure is formed again, so it is impossible to directly know the developmental stage of the oocyte inside, The constraint that it is difficult to determine the state remains. Therefore, if such problems can be avoided and the oocytes can be directly observed without being embedded in the collagen gel until the final stage, it should be a more useful culture system.
[0010]
Therefore, if the oocytes under development of various animal species can be cultured with a minimal functional cell configuration, the above problems are solved and a simple culture system for oocytes is provided. .
[0011]
[Non-Patent Document 1]
Eppig and Schroeder, Biology of Reproduction (USA), 1989, 41, 268-276.
[Non-Patent Document 2]
Eppig and O'Brien, Biology of Reproduction (USA), 1996, Vol. 54, p.197-207
[Non-Patent Document 3]
Daniel et al., Gamete Research (USA), 1989, 24, p.109-121
[Non-Patent Document 4]
Roy and Greenwald, Journal of Reproduction and Fertility (UK), 1989, 87, p.103-114
[Non-Patent Document 5]
Hirao et al., Journal of Reproduction and Fertility (UK), 1994, 100, p.333-339.
[Non-Patent Document 6]
Shuttleworth et al., Reproduction (UK), 2002, 123, 807-818
[Non-Patent Document 7]
Gutierres et al., Biology of Reproduction (USA), 2000, 62, p.1322-1328
[Non-Patent Document 8]
Telfer et al., Molecular and Cellular Endocrinology (IR), 2000, 163, p.117-123
[Non-patent document 9]
Cecconi et al., Biology of Reproduction (USA), 1999, Vol. 60, p.594-601
[Non-Patent Document 10]
Wu et al., Human Reproduction (UK), 1998, Vol. 13, p. 2562-2563
[Non-Patent Document 11]
Yamamoto et al., Theriogenology (USA), 1999, Vol. 52, p.81-89
[0012]
[Problems to be solved by the invention]
As described above, almost all animal species (particularly medium-sized and large animals) have not succeeded in growing oocytes in a tissue culture system containing oocytes. Accordingly, an object of the present invention is to provide a simple culture method capable of growing such an animal oocyte in vitro.
[0013]
[Means for Solving the Problems]
As a result of intensive studies to solve the above-mentioned problems, the present inventors have found that animal oocytes and surrounding somatic cells are good by adding a polymer compound such as PVP to the culture solution at a very high concentration. It was found that the cells were cultured. Furthermore, the present inventor, when the developing oocyte is cultured under the above conditions in a complex state with the surrounding somatic cells, the oocyte grows normally and is obtained. Was further matured and found to be usable as an egg, and the present invention was completed.
[0014]
That is, the present invention provides an egg comprising culturing a complex of an oocyte and surrounding somatic cells in a culture solution containing a polymer compound at a concentration of 1 to 12% (w / v). This is a method for culturing mother cells.
[0015]
In the above culture method, as the polymer compound, a polymer selected from the group consisting of synthetic polymers, polysaccharide polymers, proteins, proteoglycans, and combinations thereof can be used. The polymer compound is preferably selected from the group consisting of polyvinylpyrrolidone (PVP), Ficoll, hydroxypropylmethylcellulose, serum albumin, and combinations thereof.
[0016]
When using PVP alone as the polymer compound, it is particularly preferable to use a culture solution containing PVP at a concentration of about 4 to 6% (w / v). When Ficoll alone is used as the polymer compound, it is particularly preferable to use a culture solution containing Ficoll at a concentration of about 2 to 6% (w / v). In the case of hydroxypropylmethylcellulose, it is preferable to use a culture solution containing hydroxypropylmethylcellulose at a concentration of about 1-2% (w / v).
[0017]
In the culture method, the complex can be derived from a mammal, for example. Mammals include pigs, cows, sheep, goats, dogs, cats, rabbits, hamsters, rats, mice, or humans.
[0018]
In the above culture method, the oocyte may be a developing one. Furthermore, examples of the surrounding somatic cell include cumulus cells, granulosa cell mass, and / or granulosa cell layer.
The present invention is also an oocyte obtained by the above culture method.
[0019]
Furthermore, the present invention is characterized in that a complex of a developing oocyte and its surrounding somatic cells is cultured in a culture solution containing a polymer compound at a concentration of 1 to 12% (w / v). This is a method for developing oocytes.
[0020]
The present invention also provides an oocyte grown by the above growth method.
The present invention further relates to a method for producing a mature egg, characterized in that the grown oocyte is matured.
[0021]
DETAILED DESCRIPTION OF THE INVENTION
The present invention relates to an oocyte culture method and a growth method, wherein a complex of an oocyte and a surrounding somatic cell is mixed with a polymer compound at a concentration of 1 to 12% (w / v). It culture | cultivates with the culture solution containing.
[0022]
The “oocyte” to be cultured in the present invention refers to a germ cell that becomes an oocyte that can be fertilized through the developmental stage / maturation process. All oocytes are formed in the fetal period, and the oocytes that are in the developmental stage or in the developing stage do not divide, and are in the first stage of “meiosis”. It is known to perform “meiosis” for the first time at the stage of maturity, and completion of oocyte development is an essential requirement for maturation into an egg. “Oocyte development” refers to a process in which the volume of the oocyte increases significantly and does not mean that the cell population increases due to cell division. The diameter and volume of an oocyte that serves as a standard for achieving growth differs between a small animal and a large animal. For example, the volume of an oocyte in a large animal is about 4.6 times that of a small animal. Since this difference in size is also reflected in the time required for development, the number of culture days necessary and appropriate for the completion of development is determined by the size of the developing oocyte. Conventionally, artificial culture and growth have been successful in small animal oocytes with a short development period, but favorable results have not been obtained with large animal oocytes with a long development period.
[0023]
In the present invention, the term “developing oocyte” or “developing oocyte” is defined as that the size does not reach the maximum oocyte diameter specific to the animal species, and the ability is healthy. Nonetheless, it has no ability to resume meiosis while being stopped in the first meiotic prophase (the germinal vesicle stage), or has the potential to resume meiosis immediately, but has the second potential It is defined as having no potential to progress to the medium term. In general, developing oocytes are not accompanied by embryogenic ability even after in vitro fertilization.
“Maturation” of an oocyte means that meiosis is resumed, division proceeds to the second middle meiosis stage, and a process after fertilization becomes possible.
[0024]
Furthermore, the “follicle” refers to a structure that wraps an oocyte from the developmental stage to the mature stage, and the volume of the follicle increases with the development of the oocyte. Follicles differ from developing oocytes that do not undergo cell division in that they develop by cell proliferation. First, the follicle has a structure in which a single layer to several granule membrane cell layers enclose the oocyte, the basement membrane covers the outside, and the outside is surrounded by the follicle membrane cell layer. In the second half of the follicular development period, gaps appearing in the layer of granulosa cells that have increased significantly develop to become follicular cavities. The follicular cavity is filled with a fluid called follicular fluid that gradually grows and eventually occupies most of the follicular volume. When the follicular cavity is formed, the oocyte is enveloped in several layers of granulosa cells, and is attached to one point of the granulosa cell layer constituting the inner wall of the follicle. At this time, the cells forming a layer around the oocyte are particularly called cumulus cells, and are distinguished from other granulosa cells constituting the inner wall of the follicle.
[0025]
In the present invention, a portion assumed to be a “functional minimum cell configuration” centering on an oocyte is cultured. This minimum cell structure refers to the elements that constitute the follicle, that is, the inner part partitioned by the basement membrane, particularly a group of cells around the oocyte. For example, a complex of an oocyte and cumulus cell, or a complex of an oocyte and cumulus cell with the granule membrane cell population remaining on the wall side (oocyte, cumulus cell, granulosa cell) Complex).
[0026]
The operation of the oocyte culture method and growth method according to the present invention will be described in detail below. All of the following operations have good results when working in a room having a room temperature of about 25 ° C., but are not limited thereto as long as they do not damage cells or tissues.
[0027]
First, the ovaries are collected to collect the complex of the oocyte and the surrounding somatic cells.
The ovaries are collected from the animals. In the present invention, the “animal” is not limited as long as it is an animal having an oocyte, but in particular, mammals such as cows, pigs, sheep, goats, dogs, cats, rabbits, hamsters, rats, Mouse or human is preferred.
[0028]
To collect ovaries from animals, the animals are usually opened and separated, regardless of whether the animals are alive or dead. Since the inside of the ovary goes to an ischemic state after the animal is killed or separated from the living body, it is preferable to move to the following operation as soon as possible in order to reduce damage to the ovarian tissue.
[0029]
After the ovary is washed with a physiological buffer phosphate buffer (PBS), a tissue piece is cut from the surface with a thickness of 1 to 2 mm and transferred to a tissue culture solution. The tissue culture solution can be used in the present invention as long as it is used for normal tissue culture such as Waymouth's medium, Minimum Essential Medium, and 199 medium (Medium 199). Moreover, the culture solution used for the operation on the laboratory bench is HEPES (2- [4- (2-hydroxyethyl) -1-piperazinyl] ethanesulfone so that its pH is stabilized at around 7 in the gas phase in the atmosphere. What is buffered with a buffer solution such as acid) is desirable. The cutting of the tissue may be performed using any blade, and may be performed using a generally used replacement knife for surgical operation (attached to a knife handle) or a scalpel.
[0030]
Subsequently, the tissue in the culture medium is further minced to cut out follicular tissue. The follicular tissue should be excised with care so as not to be injured by excessive pressure, and any follicles that show obvious signs of regression, such as cell shedding, should not be used. Sorting the follicles by size is convenient for separating the oocytes by size (see, for example, Hirao et al., Zygote (UK), 1995, Vol. 3, pages 325-332).
[0031]
Next, a cut reaching the inside of the basement membrane is made at one location of the cut follicular tissue. From this incised portion, a complex of the oocyte and the surrounding somatic cells is collected. In the present invention, “complex of an oocyte and its surrounding somatic cells” or “complex” refers to a complex tissue composed of an oocyte and its surrounding somatic cells. Examples include complexes of cells and cumulus cells, and complexes of oocytes, cumulus cells, granulosa cells, and the like. Accordingly, “surrounding somatic cells” include, but are not limited to cumulus cells and granulosa cells. When follicles are collected by enzymatic treatment of ovaries (tissue fragments thereof) to form a complex in the culture dish, follicular membrane cells may be contaminated.
[0032]
In addition to the above, collecting the complex of the oocyte and its surrounding somatic cells omits the process of isolating the follicle, cut the ovary with a razor or the like, and then rinses it with the culture solution. You may carry out by the method of collect | recovering the composite_body | complex released in the inside directly. In collecting the complex, a method of sucking the complex from the follicle in the ovary using an injection needle and a syringe can be used. Further, a method of sucking a complex from a ovary in a living body using a technique called in vivo ovum suction can also be employed.
[0033]
As described above, the physical separation method for collecting the complex of the oocyte and the surrounding somatic cells has been described. However, in the present invention, the method of collecting the complex is not limited to the above method. .
[0034]
In addition to the physical method described above, the follicles are separated by treating the ovary fragment with an enzyme (eg, collagenase), or the ovary is cultured with the enzyme so that the oocyte and its surrounding somatic cells The complex of the oocyte and the surrounding somatic cells can also be collected.
[0035]
Furthermore, in the present invention, the “complex” is temporarily transplanted to an organ of another animal species that has been temporarily cultured (for example, follicular culture or ovarian organ culture) before being used in the present invention. Also included after collection. In addition, culturing separately prepared somatic cells together with the “complex” is also included. Accordingly, the “complex” of the present invention includes any form and state as long as it is composed of oocytes and surrounding somatic cells. For example, the “complex” to be cultured in the present invention includes the entire follicle.
[0036]
After collecting the complex, it is preferable to examine the state of the oocyte at the time of collection. Usually, the diameter of the oocyte at the time of collection, the viability of the oocyte, and its health state are important information in the subsequent culture.
[0037]
The method for measuring the diameter of the oocyte (the portion not including the zona pellucida) is not limited to the following, but a method for measuring the diameter using a microscopic eyepiece connected to a microscope, and a method that is visible through a microscope There is a method of taking a screen into a computer and measuring it with image analysis software.
[0038]
There is a correlation between the diameter of the developing oocyte and the diameter of the follicle (see, for example, Hirao et al., Zygote (UK), 1995, Vol. 3, pages 325-332), and the direct oocyte It is also possible to infer the diameter of the oocyte from the diameter of the follicle before measuring the cell diameter. For example, it is estimated that bovine developing oocytes having a diameter of about 90 to 99 μm used in Example 4 in the present invention are present in follicles having a diameter of about 0.5 to 0.7 mm. Such correlation is well known in the art, and the diameter of the oocyte can be easily determined by utilizing the correlation.
[0039]
In addition, the viability and health status of the oocyte can be determined by observing under a microscope whether the cytoplasm or cell membrane of the cell is broken.
The diameter measurement and observation methods described above are also applied to cultured oocytes.
[0040]
Subsequently, a complex of the oocyte collected as described above and its surrounding somatic cells, preferably a complex containing an oocyte in the developmental stage, is prepared in a culture dish or Introduce onto the insert membrane attached to the culture dish.
[0041]
The culture medium for complex culture is used by modifying the basic tissue culture medium. The basic tissue culture medium that can be used in the present invention is not particularly limited as long as it is used for normal cell culture. Examples thereof include Weymouth medium, minimum essential medium, and 199 medium.
[0042]
The most important modification added to the culture medium used for culturing the complex is the addition of a polymer compound. In the present invention, the “polymer compound” is an organic substance having a molecular weight of tens of thousands to millions, and includes both natural polymers (such as biopolymers) and synthetic polymers. The “polymer compound” used in the present invention is particularly easy to dissolve in water, has extremely low cytotoxicity, does not have the property of destabilizing the pH of the culture solution during culture, In addition, it is preferable to satisfy the conditions such that the initial characteristics are stably maintained for a long time. For example, examples of the polymer compound that can be used in the present invention include synthetic polymers, polysaccharide polymers, proteins, proteoglycans, and the like. Examples of synthetic polymers include polyvinyl pyrrolidone (PVP; molecular weight of about 360,000), polyvinyl alcohol (PVA; molecular weight of about 70,000 to 100,000), and the like. Examples of the polysaccharide polymer include dextran, hydroxyethylated starch, and derivatives of cellulose (for example, hydroxypropylmethylcellulose). Examples of the polysaccharide polymer include sucrose synthetic polymer Ficoll (molecular weight 400,000), hyaluronic acid and chondroitin sulfate glycosaminoglycan. Examples of proteins include serum albumin (molecular weight of about 69,000). Examples of proteoglycans include chondroitin sulfate proteoglycans.
[0043]
Particularly preferred polymer compounds in the present invention include, but are not limited to, PVP, Ficoll, hydroxypropyl methylcellulose, and serum albumin.
[0044]
In addition to those described above, the high molecular compounds usable in the present invention include compounds that are presently known to exhibit equivalent functions, or compounds that will be found or synthesized in the future. In order to confirm whether or not a certain compound is a compound exhibiting an “equivalent function” that can be used in the present invention, when used in culture, it does not impair the viability of the oocyte. It is effective to cultivate the "complex" for a long time, keeping in mind that somatic cells do not fall off and that the structure centered on the oocyte is not lost (irregular and extensive cell proliferation does not occur) . It is also important to ensure that good conditions are maintained for a sufficient period of time so that the oocyte develops to the final stage.
[0045]
The concentration of the polymer compound added to the culture solution is about 1 to 12% (w / v), preferably 2 to 8% (w / v), more preferably 4 to 6% (w / v) with respect to the culture solution. v), most preferably about 4% (w / v).
[0046]
If the concentration of the polymer compound is within the above-mentioned range, the object of the present invention can be achieved. However, the object of the present invention may be achieved even when the concentration is in other ranges. Specifically, this is a case where a compound having a high viscosity is added even if the concentration is low, such as hydroxypropylmethylcellulose and glycosaminoglycan. For example, when a certain kind of hydroxypropylmethylcellulose is added to the culture solution at a concentration of 1% (w / v), the form of the complex of oocyte and somatic cell is 4% (w / v) PVP (molecular weight 360,000). It was observed that the effect of the present invention was achieved.
[0047]
There is a fact that polymer compounds such as PVP and PVA are conventionally used in egg cultures. In particular, it is often added as a substitute for a polymer to a culture solution not containing fetal bovine serum or serum albumin. In this case, it is said that it is useful for preventing the oocyte from being attached to the bottom surface or wall surface of the culture dish and the outer surface or inner surface of the ultrafine glass tube for embryo manipulation. However, a concentration of about 0.1% to 0.4% is generally sufficient to achieve such a purpose, which is a concentration that is usually used. Further, when serum or the like is added to the basic culture solution, the polymer compound is often not added. In contrast, in the present invention, it was derived that a completely different effect can be achieved by increasing the concentration to about 1 to 12%. On the other hand, when it is added at a conventionally used concentration of 0.1% to 0.4%, the intended effect of the present invention is not exhibited. Therefore, in the present invention, it is important to add the polymer compound at a concentration of about 2.5 times or more, preferably about 10 to 15 times the conventional concentration of 0.4%.
[0048]
In addition to the addition of the above-described polymer compound, the culture medium is also modified in general cell culture, but is not limited to a specific modification. For example, addition of 5% fetal bovine serum and antibiotics.
[0049]
In addition, the culture solution may be modified to be a culture solution suitable for cell culture such as granulosa cells and oocytes. For example, but not limited thereto, sodium pyruvate is not limited to specific animal species, and is generally added to the culture medium of oocytes.
[0050]
In addition, for example, in the culture of a complex containing bovine granulosa cells, cell growth may be good when 2 mM to 4 mM hypoxanthine and 10 to 100 ng / ml estradiol 17β are added. Are known. In addition, in the culture of a complex containing pig cumulus cells, when a low concentration of follicle stimulating hormone (FSH) (for example, 10 ng / ml) is further added, cell growth may be good. Are known. In the present invention, it is preferable to appropriately modify the culture solution according to such animal species and cell types contained in the complex to be cultured.
The culture dish to be used is not particularly limited as long as it is generally used for culturing animal cells.
[0051]
In addition, the culture dish is preferably provided with a substrate for cell attachment, whereby a cell layer is provided on the culture substrate, and a complex of the oocyte and surrounding somatic cells is disposed thereon. It is possible to maintain the state of being present, and the object of the present invention can be satisfactorily achieved. As the substrate to which such cells adhere, it is preferable to use a substrate that does not interfere with the adhesion and proliferation of the cell group, for example, various insert membranes. A culture dish with a collagen coat is also suitable. However, as long as the condition of cell growth is satisfied, the culture substrate is not particularly limited.
[0052]
The number of oocytes per culture dish can be changed according to the source of the oocyte, the amount of the culture medium, the type of the culture dish, and the like. In the case of about 4.5 ml / well), it is preferable to culture 10 to 20 large complexes to which granulosa cell mass adheres, and 20 to 50 for complexes composed of cumulus cells and oocytes. The complex can be cultured. On the other hand, in a 24-well or smaller culture dish with a small volume per well, in the case of a large complex to which granulosa cell mass adheres, the amount of the culture solution per complex is about 200 to 500 μl, from cumulus cells and oocytes. In the complex, the culture is preferably performed at about 50 to 150 μl. The above example is an example, and the number of complexes per culture solution can be increased in consideration of changes in pH due to cell morphology and cell metabolism.
[0053]
The incubator in which the culture dish is installed may be any one that is generally used for animal cell culture. The culture conditions are, for example, a gas phase of 37 ° C. to 39 ° C., 5
[0054]
After the culture is started, the oocyte continues to grow in a state of being wrapped by surrounding somatic cells. According to the present invention, in the culturing process, the binding with the somatic cell layer closest to the oocyte is well maintained.
[0055]
It is common sense to exchange a part of the culture solution with a fresh one once every 2 to 4 days during the culture period, and it is preferable to change the culture solution as appropriate in the present invention. The culture period varies depending on the animal species to be used and the state of the collected oocyte, but is generally several days to about 4 weeks for cattle and pigs, and can be appropriately set by those skilled in the art.
[0056]
According to the present invention, it is possible to recover the developed oocyte while maintaining the binding state between many oocytes and surrounding somatic cells. In the complex recovered after culturing, the ratio of oocytes wrapped in somatic cells is significantly increased (for example, about 2 to 5 times) by using the present invention.
[0057]
The diameter of the oocyte after culture is measured by the method described above. Thereby, the degree of oocyte development during the culture period can be known. Development may be considered complete when the diameter of the oocyte reaches the maximum value specific to the animal species, but further confirming that the oocyte and surrounding somatic morphology are normal, The culture may be continued for several days to about 1 week.
[0058]
According to the present invention, it is possible not only to promote the growth of an oocyte but also to develop an oocyte in a complex state with a somatic cell. This means that in the subsequent maturation process of the oocyte, it remains encased in somatic cells. It is extremely important in terms of the effect of protecting the oocyte from various stresses such as
[0059]
This culture method is also easier to operate than the start of culture, observation during culture, and recovery of oocytes after culture compared to conventional culture methods and follicular culture embedded in collagen gel. Is.
[0060]
Although the present invention enables long-term culture, since the growth of the oocyte can be observed, the culture period can be changed according to the size of the oocyte, that is, the degree of development. It is. In addition, since the oocytes that have developed during the culture period are still alive in a state of maintaining the association with somatic cells, this culture method is not limited to the developing oocytes. It is also effective for later oocytes.
[0061]
Another object of the present invention is to maintain a functional and minimal three-dimensional structure of a complex of an oocyte and its surrounding somatic cells, and a method for culturing a complex embedded in a collagen gel. Or the culture solution used by this invention can be applied also to follicular culture, and culture | cultivation can be performed effectively.
[0062]
The oocytes obtained as described above can be subjected to physical operations such as culturing after microinjection of proteins such as nucleic acids, chemical substances or antibodies. Therefore, the oocyte obtained by the present invention is useful for oocyte research.
[0063]
In addition, the oocytes obtained as described above can be used by allowing them to mature into oocytes by performing a culture method for in vitro maturation of commonly used immature oocytes.
[0064]
Conversion to mature culture is usually performed by recovering the complex of oocytes and somatic cells from the culture dish that has undergone growth culture, washing it with the maturation medium, and then transferring it to the final maturation medium. Do. The tissue culture solution for maturation is used with a 199 medium or the like as a basic medium to which essential elements such as sodium pyruvate and antibiotics are added, and gonadotropin, growth factor, serum, follicular fluid and the like are appropriately added. Preferred culture conditions for such oocyte maturation culture have been extensively investigated and are known in the art. The incubator in which the culture dish is installed is used with the same settings as those normally used for growth culture.
[0065]
Eggs matured in this way can be used for normal in vitro fertilization, and can also be used for recipient eggs in the production of parthenogenetic embryos and cloned animals.
[0066]
【Example】
Hereinafter, the present invention will be described by way of examples. However, the technical scope of the present invention is not limited to these examples.
[0067]
[Example 1] Culture of porcine oocytes using PVP-added culture medium
Porcine ovaries collected at the slaughterhouse were washed with PBS, and tissue pieces were cut from the surface to a thickness of 1 to 2 mm, and transferred to a culture dish (
[0068]
Each oocyte / cumulus cell complex is transferred to a small drop of the washing medium, and the oocytes are individually collected at a magnification of 200 times using a microscopic eyepiece connected to an inverted microscope. Diameter was measured. At this stage, oocytes that clearly showed signs of regression were removed, and the remaining healthy oocyte / cumulus cell complex was subjected to culture.
[0069]
To the culture solution, 5% fetal calf serum, 4 mM hypoxanthine, 10 ng / ml FSH, 100 μg / ml sodium pyruvate, 80 μg / ml kanamycin and 0.1 μg / ml estradiol 17β were added as a basic tissue culture solution. Weymouth culture solution (Gibco) was used. For PVP (manufactured by Sigma, average molecular weight 360,000), those added at a concentration of 0% to 10% were used (0, 1, 2, 4, 6, 8 and 10%).
[0070]
As a culture dish, a 6-well or 24-well culture plate was used with an insert membrane (Biocoat, manufactured by Becton Dickinson) provided with a collagen coat. In such a culture dish, the culture medium is added in advance (in the case of 6 wells, 2 ml of the inside of the insert, 2.5 ml of the outside, in the case of 24 wells, 500 μl of the inside, 600 μl of the outside), 2 ・ Equilibrated in an incubator (manufactured by Sanyo Electric Co., Ltd.) with 95% air conditions and introduced the oocyte / cumulus cell complex, which was observed before culture, onto the membrane of the culture dish did. Thereafter, it was immediately transferred to an incubator and culture was started. The culture was performed for 12 days, and once every four days, half of the culture solution was replaced with fresh one.
[0071]
Changes in the morphology of the complex as the culture progresses are shown in FIGS. 1A to f and FIGS. 1B to g. In FIG. 1, a, c, e, g and i show the forms after 1 day, 3 days, 6 days, 9 days and 12 days of culture in the PVP-free group. On the other hand, b, d, f, h, and j in FIG. 1 show the forms when the same number of days as in the PVP non-added section has elapsed in the
[0072]
It was clear from the form of the oocytes collected after the culture that the communication between the oocytes and the somatic cells was suitably maintained in the
[0073]
In addition to examining the viability of the recovered oocyte-somatic complex, 10 IU / ml of pregnant mare serum gonadotropin (PMSG) and human chorionic gonadotropin (hCG) were respectively added to the complex. For 48 hours of maturation culture. Thereafter, the oocytes were fixed and stained, and the maturation rate to the second metaphase was examined. The proportion of oocytes collected in the PVP-added group was higher than that in the PVP-free group, showing a significantly higher value at 4% (FIG. 3A). The percentage of oocytes that reached the second meiotic metaphase after maturation culture was also high. When the PVP concentration was 8% or more, the proliferation of granulosa cells tended to be suppressed. When the diameter of the oocyte shown in FIG. 3A was examined, it was much larger than that at the start of culture, and it had grown to the final size (FIG. 3B).
[0074]
[Example 2] Culture of pig oocytes using ficoll-added culture medium
In the same manner as in Example 1, a developing oocyte / cumulus cell complex was collected and subjected to culture. Ficoll (Ficoll (registered trademark) 400, average molecular weight 400,000, manufactured by Sigma) was added to the same culture broth as in Example 1 at a concentration of 0 to 10% (w / v) instead of PVP. (0, 1, 2, 4, 6, 8 and 10%). The setting of the culture dish and the incubator was the same as in Example 1.
[0075]
FIG. 4A shows a form in the case where 12 days have passed in the
[0076]
When mature culture was performed in the same manner as in Example 1, cumulus cells were swollen (FIG. 4B, photograph after 24 hours of mature culture). FIG. 4B shows that hyaluronic acid was synthesized in cumulus cells as a result of responding to stimulation of PMSG and hCG, and in the complex after long-term culture, receptors for these hormones were placed on cumulus cells. It was shown that the process leading to hyaluronic acid synthesis after stimulation was functioning. At the same time, maturation of the oocyte was confirmed, indicating that the cumulus cell and oocyte communicate normally, and as a result, it is possible to induce maturation of the oocyte.
[0077]
FIG. 5 shows the ratio of the complex of porcine oocytes and somatic cells in normal form obtained after 12 days of culture in the areas where
[0078]
[Example 3] Culture of porcine oocytes using a culture solution supplemented with hydroxypropylmethylcellulose
In the same manner as in Example 1, a developing oocyte / cumulus cell complex was collected and subjected to culture. Hydroxypropylmethyl cellulose ((Hydroxypropyl) methyl cellulose) (Sigma, H9262) was added to the same culture broth as in Example 1 at a concentration of 1% instead of PVP. The setting of the culture dish and the incubator was the same as in Example 1. Due to its molecular properties, the used hydroxypropylmethylcellulose exhibited different viscosities in the solution even at the same concentration as the PVP of Example 1. As is clear from the photograph after 12 days of culture (FIG. 6), the oocytes tended to proliferate so as to be surrounded by a cell layer having a stable thickness.
[0079]
[Example 4] Culture of bovine oocytes using PVP
After washing bovine ovaries collected at the slaughterhouse with PBS, tissue pieces were cut from the surface with a thickness of 1 to 2 mm, and follicles were cut out in the same manner as in Example 1. Among them, one having a diameter of 0.5 to 0.7 mm was selected, transferred to a fresh tissue washing culture medium, and a cut reaching the inside of the basement membrane was made. As in Example 1, a complex was obtained by pressing the opposite side of the cut with tweezers. In Example 4, a complex of oocytes, cumulus cells, and granulosa cells was collected and used for culture. did. Immediately after collection, the diameter of the oocyte was measured and a healthy complex was selected by the method shown in Example 1.
[0080]
As a basic tissue culture medium, the culture medium is a way mouse culture medium (5% fetal bovine serum, 4 mM hypoxanthine, 100 μg / ml sodium pyruvate, 80 μg / ml kanamycin and 0.1 μg / ml estradiol 17β added). Gibco) or 199 culture solution (Nissui Pharmaceutical Co., Ltd.) and finally added PVP at a concentration of 0% to 12% (0, 0.25, 1, 2, 4, 6 and 12%). The setting of the culture dish and the incubator was the same as in Example 1.
[0081]
As in Example 1 in pigs, the complex of oocytes and cumulus cells can be recovered with stable results after 14 days in culture as the concentration of PVP added is increased to about 4% or more. Became. Even in the group with the highest concentration of 12%, the ovum was recovered as a complex without being naked, and after 24 hours of maturation culture, the oocytes that released the first polar body could be confirmed. The proliferation of somatic cells and the health condition of their appearance are best in the case of the complex with 4-6% added, and the specific gravity of the culture solution is excessive due to the operability when introducing the complex. It is particularly preferable to add 4 to 6% of PVP to the culture medium from the viewpoint of preventing the weight from becoming heavy. On the other hand, in the 0.25% addition group, the effect was not recognized, but in the 1% addition group, although the form of the composite was slightly improved, it did not reach the effect observed in the addition group of 2% or more. The 4% added group showed the best value, and the 2% added group showed the result between 4% and 0%.
[0082]
7A, 7B, and 7C show changes in the form of the complex in the
[0083]
A comparison of the ratio of the complex of normal oocytes / cumulus cells recovered after 14 days of culture, as compared with the experiment in Example (Example 1) in swine, compared to the group without PVP and the group with 2% addition. In addition, a high value was shown in the
[0084]
[Example 5] Maturation and fertilization into eggs
A 199 culture solution (manufactured by Gibco) was used as a basic culture solution, and bovine oocytes were grown and cultured in a culture solution supplemented with 0% or 4% PVP for 14 days in the same manner as in Example 3. After the growth culture, the complex of the oocyte and cumulus cell was collected and matured and in vitro fertilized.
[0085]
In vitro maturation is performed using a culture solution obtained by adding 5% fetal bovine serum, sodium pyruvate and 20 mAU / ml follicle stimulating hormone (Antoline, manufactured by Denka Pharmaceutical Co., Ltd.) to a 199 culture solution (manufactured by Gibco). Cultivation was performed for 24 hours in a high humidity environment at 5 ° C. in a gas phase of 5% carbon dioxide gas and 95% air. After maturation culture, oocytes wrapped in swollen cumulus cells were collected and washed with a basic medium for medium (BO solution) containing caffeine, heparin and bovine serum albumin to obtain an egg.
[0086]
On the other hand, frozen bovine semen was thawed and subjected to sperm washing treatment, and in addition to the culture solution containing eggs prepared as described above, it was subjected to in vitro fertilization. Six hours after the nymph, the ovum was transferred to a fertilized egg culture solution (IVD-101, manufactured by Functional Peptide Institute), in a gas phase of 38.5 ° C., 5% oxygen 5
[0087]
【The invention's effect】
The present invention provides a simple culture method and growth method for oocytes. In this culturing method, a complex of an oocyte and surrounding somatic cells can be cultured while maintaining a good morphological and functional relationship. In addition, even when the developing oocyte is subjected to culture, the oocyte can be grown to the final stage. In the main culture method or the growth method, the binding between the oocyte and the surrounding somatic cells is well maintained even after the culture, and the oocyte that has succeeded in the growth is matured to an oocyte and It can be used.
[Brief description of the drawings]
FIG. 1A is a photograph of a complex of a developing porcine oocyte and a somatic cell in culture in a
a:
b:
c:
d:
e:
f:
FIG. 1B shows a photograph of the complex of porcine oocytes and somatic cells during culture in a group with 0% PVP added (no addition group) or a group with 4% PVP added.
g:
h:
i: PVP added at 0%, after 12 days of culture
j:
FIG. 2 is a photograph of a complex of porcine oocytes and somatic cells obtained after 12 days of culture in a group with 0% PVP added (A) and a group with 4% PVP added (B). All scales indicate 200 μm.
FIG. 3A: Percentage of normal form porcine oocyte-somatic complex obtained after 12 days of culture in the 0%, 1%, 2% and 4% (w / v) groups of PVP. In addition, the maturation rate to the second meiotic metaphase when a further 48 hours of maturation culture is applied is shown.
B: Shows the diameter (B) of porcine oocytes before culturing and after culturing for 12 days.
[Fig. 4] Culture 12 of a complex of developing porcine oocytes and somatic cells in a group with 4% (w / v) addition of Ficoll (registered trademark) 400, average molecular weight of 400,000, manufactured by Sigma. The photograph after a day (A) and the swelling (B) of the cumulus cell in a mature culture are shown. All scales indicate 200 μm.
FIG. 5 shows the proportion of normal form porcine oocyte / somatic complex obtained after 12 days of culture in the
FIG. 6 is a photograph of a complex of porcine oocytes and somatic cells after 12 days of culture in a group containing 1% (w / v) hydroxypropylmethylcellulose ((hydroxypropyl) methyl cellulose, Sigma H9262). The scale indicates 200 μm.
FIG. 7 shows photographs after 2 days (A), 9 days (B), and 14 days (C) of culture of a complex of developing bovine oocytes and somatic cells in a
FIG. 8 shows the ratio (A) of the complex of bovine oocytes and somatic cells in normal form obtained after 14 days of culture in the
FIG. 9 shows photographs of embryos obtained by in vitro fertilization of matured eggs derived from bovine oocytes / somatic cell complexes cultured for 14 days in a
Claims (6)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002346327A JP4122425B2 (en) | 2002-11-28 | 2002-11-28 | Oocyte culture method and growth method |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002346327A JP4122425B2 (en) | 2002-11-28 | 2002-11-28 | Oocyte culture method and growth method |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2004173635A JP2004173635A (en) | 2004-06-24 |
| JP4122425B2 true JP4122425B2 (en) | 2008-07-23 |
Family
ID=32707269
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002346327A Expired - Lifetime JP4122425B2 (en) | 2002-11-28 | 2002-11-28 | Oocyte culture method and growth method |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4122425B2 (en) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4855778B2 (en) * | 2005-01-31 | 2012-01-18 | 知 藤澤 | Egg observation device |
| JP5083952B2 (en) * | 2007-07-26 | 2012-11-28 | 国立大学法人 岡山大学 | Egg cell culture equipment |
| JP2012210199A (en) * | 2011-03-31 | 2012-11-01 | National Agriculture & Food Research Organization | Method for cloning clone animal individual with in vitro developing oocyte as recipient ovum |
| HK1257701A1 (en) * | 2015-09-17 | 2019-10-25 | 学校法人东京农业大学 | Culture method for differentiating primordial germ cells into functionally mature oocytes |
| CN108118027B (en) * | 2018-01-08 | 2021-12-10 | 内蒙古农业大学 | Sheep oocyte in-vitro 'two-stage' maturation method, and pre-incubation liquid and kit thereof |
| CN109112100A (en) * | 2018-09-04 | 2019-01-01 | 安徽农业大学 | The collection method of the small cumulus oocyte complex for having chamber of one boar |
| CN110811907A (en) * | 2019-11-18 | 2020-02-21 | 内蒙古自治区农牧业科学院 | A method for superovulation of goat and lamb |
| CN114032207A (en) * | 2021-08-02 | 2022-02-11 | 四川农业大学 | A kind of separation and culture method of porcine ovarian granulosa cells |
| CN114075542B (en) * | 2021-11-02 | 2024-02-20 | 上海交通大学医学院附属第九人民医院 | Culture solution for cytoplasmatic mechanical separation and application method thereof |
| CN115786249A (en) * | 2022-11-28 | 2023-03-14 | 中国农业科学院特产研究所 | Method for culturing pig oocyte |
| CN116218768A (en) * | 2023-02-20 | 2023-06-06 | 艾尔斯(浙江)医学科技有限公司 | A kind of ovum flushing liquid and its application |
-
2002
- 2002-11-28 JP JP2002346327A patent/JP4122425B2/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| JP2004173635A (en) | 2004-06-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Xu et al. | Secondary follicle growth and oocyte maturation by culture in alginate hydrogel following cryopreservation of the ovary or individual follicles | |
| Paramio et al. | Recent advances in in vitro embryo production in small ruminants | |
| JPH06508527A (en) | Hormone-secreting cells maintained in long-term culture | |
| Baker et al. | Commercial splitting of bovine embryos | |
| Edwards et al. | New advances in human embryology: implications of the preimplantation diagnosis of genetic disease | |
| JP4122425B2 (en) | Oocyte culture method and growth method | |
| Kątska-Książkiewicz et al. | Effect of donor stimulation, frozen semen and heparin treatment on the efficiency of in vitro embryo production in goats | |
| Gutnisky et al. | Evaluation of the Cryotech Vitrification Kit for bovine embryos | |
| JPH02138929A (en) | Culture of cattle fotus in vitro | |
| Skidmore et al. | Micromanipulation of equine embryos to produce monozygotic twins | |
| WO2019061560A1 (en) | In vitro maturation culture medium of immature oocytes and use thereof | |
| US20240052303A1 (en) | Methods of embryo twinning | |
| Nagashima et al. | The domestic dog embryo: in vitro fertilization, culture, and transfer | |
| CN1423692A (en) | Human Müllerian duct derived epithelial cells and methods of isolating and using the same | |
| Singh et al. | Biotechnology in livestock reproduction | |
| Katska et al. | The effect of co-culture system on developmental capacity of bovine IVM/IVF oocytes | |
| JP2009005651A (en) | How to store sperm cells | |
| CN119752773A (en) | A method for efficiently constructing pig testicular organoids in vitro | |
| KR101763343B1 (en) | Method for Producing Cloned Canidae Using Nuclear Transfer of Somatic Cells or Stem Cells | |
| Selwood et al. | Establishing long-term colonies of marsupials to provide models for studying developmental mechanisms and their application to fertility control | |
| JP5234535B2 (en) | Additive for in vitro maturation culture of mammalian immature ovum and method for producing mature ovum using the same | |
| US20250099219A1 (en) | Methods of embryo multiplication | |
| JP2012210199A (en) | Method for cloning clone animal individual with in vitro developing oocyte as recipient ovum | |
| RU2730597C2 (en) | Ungulate embryo cryopreservation | |
| 加藤行男 et al. | Microsurgical bisection of expanding blastocysts for sexing of pig embryos. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20051129 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060127 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20071016 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20071211 |
|
| TRDD | Decision of grant or rejection written | ||
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20071211 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080122 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4122425 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| EXPY | Cancellation because of completion of term |