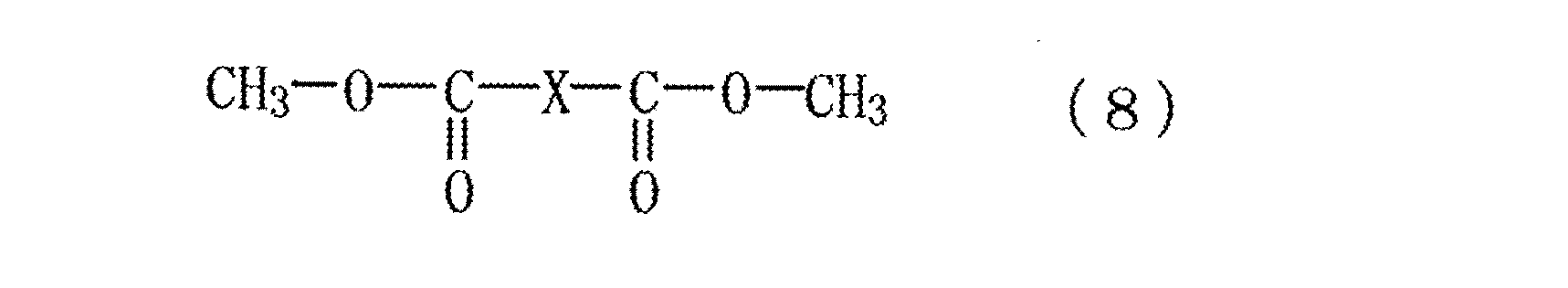JP3851996B2 - Polyester polymer and method for producing the same - Google Patents
Polyester polymer and method for producing the same Download PDFInfo
- Publication number
- JP3851996B2 JP3851996B2 JP16155599A JP16155599A JP3851996B2 JP 3851996 B2 JP3851996 B2 JP 3851996B2 JP 16155599 A JP16155599 A JP 16155599A JP 16155599 A JP16155599 A JP 16155599A JP 3851996 B2 JP3851996 B2 JP 3851996B2
- Authority
- JP
- Japan
- Prior art keywords
- formula
- group
- polyester polymer
- same
- represented
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Description
【0001】
【発明の属する技術分野】
本発明は、プリント配線基板をはじめとする電気・電子部品材料として有用な新規なポリエステル重合体およびその製造方法に関する。本発明のポリエステル重合体は、特定の骨格(フルオレン構造とポリシラン構造)を有しており、耐熱性および機械的強度のバランスに優れる。
【0002】
【従来の技術と発明が解決しようとする課題】
ポリエステル樹脂、例えばアルキレンテレフタレート樹脂等は、耐熱性、電気的性質、その他、物理的、化学的特性に優れ、且つ加工性が良好であるため、エンジニアリングプラスチックとして、自動車、電気・電子部品等の広範な用途に使用されている。このようなポリエステル樹脂は、単独でも種々の成形品に用いられてはいるが、用途によっては、その性質、特に機械的強度を向上させる必要が生じる場合が多い。例えば、プリント配線基板の用途では、はんだ耐熱性を有し、薄膜形成時に機械的強度を有することが必要であることから、現時点ではガラスエポキシ積層板が主流となっているが、ポリエステル樹脂の使用も検討されつつある。
【0003】
機械的強度を高める解決策として、ポリエステル樹脂に、様々な強化剤、添加剤等を配合することが挙げられる。しかしながら、強化剤、添加剤を配合する方法では、仕様ごとに、強化剤、添加剤の種類・添加量を試行錯誤により決定しなければならず、また場合によっては、強化剤、添加剤を使用できない場合も発生する。
【0004】
そこで、耐熱性、加工性を維持しつつ、十分な機械的強度を有する新たなポリエステル樹脂の開発が望まれていた。
【0005】
【課題を解決するための手段】
本発明者らは、上記従来技術の問題点に鑑み、鋭意研究を重ねた結果、カルド構造を有するために耐熱性を発揮するハードセグメントであるフルオレンと、機械的強度を発揮するソフトセグメントであるポリシランとの両方を分子内に有するポリエステル重合体が、耐熱性、加工性を維持しつつ、十分な機械的強度を有することを見出し、本発明を完成するに至った。
【0006】
すなわち、本発明は下記に示すとおりのポリエステル重合体およびその製造方法を提供するものである。
項1. 式(1)
【0007】
【化12】
【0008】
〔式中、Xは脂肪族炭化水素残基または芳香族炭化水素残基を示す。
Yは式(2)
【0009】
【化13】
【0010】
(R1、R2、R3およびR4は、同一または異なって、水素原子または炭素数1〜4のアルキル基を示す。pは2〜4を示す。)で表される基を示す。
Zは式(3)
【0011】
【化14】
【0012】
(R5およびR6は、同一または異なって、水素原子、アルキル基、アリール基、またはシリル基を示す。qは2〜100を示す。)で表される基を示す。
aは2〜10を示し、l、mおよびnは、同一または異なって、2以上を示す。〕
で表されるポリエステル重合体。
項2. Xがシクロアルキレン基である項1に記載のポリエステル重合体。
項3. Xがアリーレン基である項1に記載のポリエステル重合体。
項4. Yが式(4)
【0013】
【化15】
【0014】
で表される基である項1〜3のいずれか1項に記載のポリエステル重合体。
項5. Zが式(5)
【0015】
【化16】
【0016】
〔式中、qは2〜100を示す。〕で表される基または式(6)
【0017】
【化17】
【0018】
〔式中、q1およびq2は、同一または異なって、1以上を示し、q1とq2の和は2〜100である。〕で表される基または式(7)
【0019】
【化18】
【0020】
〔式中、qは前記に同じ。〕で表される基である項1〜4のいずれか1項に記載のポリエステル重合体。
項6. 重量平均分子量が1000以上であることを特徴とする項1〜5のいずれか1項に記載のポリエステル重合体。
項7. 式(8)
【0021】
【化19】
【0022】
〔式中、Xは脂肪族炭化水素残基または芳香族炭化水素残基を示す。〕で表されるジカルボン酸ジメチルと、
式(9)
【0023】
【化20】
【0024】
〔式中、aは2〜10を示す。〕で表されるアルキレングリコール、式(10)
【0025】
【化21】
【0026】
〔式中、R1、R2、R3およびR4は、同一または異なって、水素原子または炭素数1〜4のアルキル基を示す。pは2〜4を示す。〕で表されるフルオレン化合物および式(11)
【0027】
【化22】
【0028】
〔式中、R5およびR6は、同一または異なって、水素原子、アルキル基、アリール基、またはシリル基を示す。qは2〜100を示す。〕で表されるポリシランとを、縮合重合させることを特徴とする、項1に記載のポリエステル重合体を製造する方法。
【0029】
【発明の実施の形態】
以下、本発明をその実施の形態とともに説明する。
【0030】
式(1)で表される本発明のポリエステル重合体は、式(8)で表されるジカルボン酸ジメチルと、式(9)で表されるアルキレングリコール、式(10)で表されるフルオレン化合物および式(11)で表されるポリシランとを、触媒の存在下、高温減圧下の溶融状態で、縮合重合させることにより得られる構造のものである。
【0031】
本発明に用いる式(8)のジカルボン酸ジメチルとしては、1,4−シクロヘキサンジカルボン酸ジメチル、1,3−シクロヘキサンジカルボン酸ジメチル、1,2−シクロヘキサンジカルボン酸ジメチル、シクロヘキセン−1,2−ジカルボン酸ジメチルなどの脂肪族ジカルボン酸のジメチルエステル、および、テレフタル酸ジメチル、1,4−ナフタレンジカルボン酸ジメチル、2,6−ナフタレンジカルボン酸ジメチルなどの芳香族ジカルボン酸のジメチルエステルが挙げられる。これらの中でも、1,4−シクロヘキサンジカルボン酸ジメチル、テレフタル酸ジメチルが好ましい。
【0032】
式(1)で表されるポリエステル重合体においては、Xがシクロアルキレン基、アリーレン基であるものが好ましく、1,4−シクロへキシレン基、p−フェニレン基であるものがより好ましい。
【0033】
本発明に用いる式(9)のアルキレングリコールとしては、メチレン基の数aが2〜10のものが挙げられ、これらの中でも2〜6のものが好ましい。具体的には、エチレングリコール、プロピレングリコール、1,4−ブタンジオール、ネオペンチルグリコールなどが挙げられる。
【0034】
式(1)で表されるポリエステル重合体においては、aが2〜6のものが好ましい。
【0035】
本発明に用いる式(10)のフルオレン化合物において、R1、R2、R3およびR4は、同一または異なって、水素原子または炭素数1〜4のアルキル基を示す。
アルキル基としてはメチル基が好ましい。pは2〜4を示し、その中でもp=2の場合が好ましい。より具体的には、9,9−ビス{4−(2−ヒドロキシエトキシ)フェニル}フルオレン、9,9−ビス[{3−メチル−4−(2−ヒドロキシエトキシ)}フェニル]フルオレン、9,9−ビス{4−(2−ヒドロキシプロポキシ)フェニル}フルオレン、9,9−ビス[{3−メチル−4−(2−ヒドロキシプロポキシ)}フェニル]フルオレン等があり、特に9,9−ビス{4−(2−ヒドロキシエトキシ)フェニル}フルオレンが好ましい。例えば、9,9−ビス{4−(2−ヒドロキシエトキシ)フェニル}フルオレンの製造方法は、特開平7−165657に開示されている。本発明に用いるフルオレン化合物の純度は95%以上であり、好ましくは98%以上である。
【0036】
式(2)で表される基においては、R1、R2、R3およびR4で示される基がアルキル基の場合には、メチル基が好ましい。pとしては2が好ましい。
【0037】
本発明に用いる式(11)のポリシランは、側鎖置換基(R5、R6)として水素原子、アルキル基、アリール基、シリル基を有する。アルキル基としては、炭素数1〜10程度のものが挙げられ、炭素数1〜6のものが好ましい。アリール基としては、フェニル基、炭素数1〜10のアルキル基を1つ以上置換基として有するフェニル基、p−アルコキシフェニル基、ナフチル基などが挙げられる。シリル基としては、ケイ素数1〜10程度のものが挙げられ、ケイ素数1〜6のものが好ましい。また、シリル基上の水素原子の少なくとも1つが、アルキル基、アリール基などの置換基により置換されていても良い。このような置換基としては、上記と同様なものが挙げられる。式(11)のqとしては、2〜100であり、好ましくは5〜50である。式(11)のポリシランとしては、メチルフェニルポリシラン、n−ヘキシルメチル−メチルフェニル共重合ポリシラン、n−ヘキシルメチルポリシランがより好ましい。
【0038】
ポリシランの製造方法としては、(1)クロロシラン類をアルカリ金属を用いて脱塩素縮合させる方法(J.Am.Chem.Soc.,103(1981)7352)、(2)クロロシラン類を電極還元法を用いて脱塩素縮合させる方法(特開平4-348128、特開平4-331235)、(3)ヒドロシラン類を触媒存在下で脱水素縮合させる方法(Chem.Lett.,83(1989))などが知られている。これらの中でも(1)および(2)などの脱塩素縮合法により得られたポリシランを使用することが好ましい。
【0039】
式(3)で表される基においては、R5、R6で示される基がアルキル基の場合には、炭素数1〜10程度のアルキル基が挙げられ、炭素数1〜6のものが好ましい。アリール基の場合には、フェニル基、炭素数1〜10のアルキル基を1つ以上置換基として有するフェニル基、p−アルコキシフェニル基、ナフチル基などが挙げられる。シリル基の場合には、ケイ素数1〜10程度のシリル基が挙げられ、ケイ素数1〜6のものが好ましい。また、シリル基上の水素原子の少なくとも1つが、アルキル基、アリール基などの置換基により置換されていても良い。このような置換基としては、上記と同様なものが挙げられる。式(3)のqとしては、2〜100であり、好ましくは5〜50である。
【0040】
本発明のポリエステル重合体を縮合重合するに際しては、上記のジカルボン酸ジメチル(8)と、アルキレングリコール(9)、フルオレン化合物(10)およびポリシラン(11)とを、反応器内に収容し、不活性ガス雰囲気下で加熱溶融させることにより、エステル交換反応を行なう。各原料の混合割合としては、モル比で、ジカルボン酸ジメチル1.0に対してアルキレングリコールは2.0〜10.0であり、好ましくは2.0〜5.0である。同様にフルオレン化合物は0.01〜2.0であり、好ましくは0.1〜1.0である。ポリシランの使用量については、ポリシランの分子量によりモル数が異なるため、ジカルボン酸ジメチルに対する重量百分率で表すと、通常0.1〜200%であり、好ましくは0.2〜100%である。また、反応をより円滑に進めるためには、触媒を用いたほうが好ましい。触媒としては、公知のリチウム、カリウム、ナトリウム、バリウム、カルシウム、アルミニウム、アンチモン、スズ、マグネシウム、セリウム、マンガン、カドミウム、コバルト、亜鉛、鉛、チタン、イットリウムの各酢酸塩、アンチモン、亜鉛、チタン、ゲルマニウムの各酸化物、モノ(ジ)−n−ブチルスズオキサイド、テトラブチルチタネート、リン酸トリメチルなどが挙げられる。これらの中でも、カルシウム、マグネシウム、セリウム、マンガン、コバルト、亜鉛、イットリウムの各酢酸塩、酸化ゲルマニウム、モノ(ジ)−n−ブチルスズオキサイド、リン酸トリメチルが好ましい。これらの触媒は、1種単独でもあるいは2種以上混合して用いてもよい。触媒の使用量としては、重量割合で、ジカルボン酸ジメチル1.0に対して1×10-5〜1×10-2であり、好ましくは1×10-4〜2×10-3である。エステル交換反応に要する時間は、使用する原料、触媒の有無により異なるが、概ね1時間程度以上であればよい。また、反応温度についても同様であるが、概ね100〜300℃程度で行なえば良い。
【0041】
エステル交換反応終了後、昇温・減圧することによって、重合反応を進行させる。重合温度は、使用する原料、触媒の有無により異なるが、概ね200〜350℃であり、好ましくは240〜300℃である。反応器内の圧力は0.1〜5torr程度にする。重合時間については、長くすると高重合度のポリエステルが得られるが、必要以上に長くすると分解反応が起こり、分子量低下、着色などが起こる可能性があるため、通常5分〜24時間であり、好ましくは10分〜10時間である。反応終了後は、反応器内に窒素、アルゴンなどの不活性ガスを導入し、加圧しつつ押し出すことによってポリエステルを収集すれば良い。
【0042】
式(1)で表される本発明のポリエステル重合体においては、l、m、nは、同一または異なって、2以上であり、好ましくは2〜500であり、さらに好ましくは10〜200である。
【0043】
本発明のポリエステル重合体は、ゲルパーミエーションクロマトグラフィーを用いてポリスチレンを標準として換算した重量平均分子量が1000以上、好ましくは1000〜1000000、さらに好ましくは5000〜400000である。
【0044】
【実施例】
以下に、実施例により本発明を具体的に説明する。
【0045】
なお、重量平均分子量は、ゲルパーミエーションクロマトグラフィー(東ソー社製HLC−8020GPC)を用い、以下の条件で測定した。
溶媒:テトラヒドロフラン
流速:1.0ml/min
カラム:TSKgelGMHHR−L(東ソー社製)。
【0046】
実施例1
1,4−シクロヘキサンジカルボン酸ジメチル48g(0.24モル)、9,9−ビス{4−(2−ヒドロキシエトキシ)フェニル}フルオレン53g(0.12モル)、エチレングリコール33g(0.53モル)、n−ヘキシルメチル−メチルフェニル共重合ポリシラン(共重合割合1:1で重量平均分子量1100)1.2g、および触媒としてジ−n−ブチルスズオキサイド0.03gを、300ml3ツ口フラスコに収容し、N2雰囲気下、攪拌しながら240℃に徐々に加熱し、気化したメタノールを留去することによってエステル交換を行った。所定量のメタノールを留去した後、発生するエチレングリコールを留去しながら、反応槽を270℃まで昇温し、1torr以下まで減圧を徐々に行った。この条件を1.5時間維持した後、反応槽にN2を導入し、加圧しつつ押し出してペレット状のポリエステル105gを得た。
【0047】
ゲルパーミエーションクロマトグラフィー(GPC)により分子量を測定したところ、重量平均分子量は71500であった。H−NMRチャートを図1に示す。
【0048】
実施例2
使用するポリシラン量を6.0gとする以外は実施例1と同様にして行った。その結果、106gのポリエステルが得られた。GPCにより分子量を測定したところ、重量平均分子量は51800であった。
【0049】
実施例3
ポリシランとしてメチルフェニルポリシラン(重量平均分子量7200)1.2gを用いる以外は実施例1と同様にして行った。その結果、100gのポリエステルが得られた。GPCにより分子量を測定したところ、重量平均分子量377000であった。H−NMRチャートを図2に示す。
【0050】
実施例4
フルオレンとして9,9−ビス[{3−メチル−4−(2−ヒドロキシエトキシ)}フェニル]フルオレン48g(0.10モル)を用いる以外は実施例1と同様にして行った。その結果、92gのポリエステルが得られた。
【0051】
実施例5
重合時の温度を270℃から300℃に変える以外は実施例1と同様にして行った。その結果、重合時間を1.0時間に短縮しても実施例1と同等のポリエステルが得られた。
【0052】
比較例1
ポリシランを用いずに実施例1と同様にして行った。その結果、重量平均分子量66200のポリエステルが得られた。
【0053】
比較例2
フルオレンを用いずに実施例1と同様にして行った。その結果、重量平均分子量145700のポリエステルが得られた。
【0054】
上記で得られたポリエステルを用いて機械的強度試験と耐熱性評価試験を行った。
[機械的強度試験]
得られたポリエステルをテーバー磨耗測定器(テスター産業社製、AB−101型)を用いてテーバー削れ量を測定することにより、機械的強度を評価した。その結果を表1に示す。表1より、ポリシラン構造の導入により機械的強度が向上していることがわかった。
[耐熱性評価試験]
示差走査熱量測定(DSC)によりガラス転移温度(Tg)を測定した。
示差走査熱量計:理学電気社製、TAS−100
昇温速度:10℃/分
測定結果を表2に示す。表2より、フルオレン構造の導入により、Tgの上昇が確認された。
【0055】
【発明の効果】
本発明のポリエステル重合体は、カルド構造を有し耐熱性を発揮するハードセグメントであるフルオレンと、機械的強度を発揮するソフトセグメントであるポリシランとの両方を分子内に有するため、強化剤、添加剤を配合することなく、耐熱性、加工性を維持しつつ、十分な機械的強度を有する。そのため、プリント配線基板用途をはじめ、従来のポリエステルでは機械的強度が不足していた他の自動車、電気・電子部品等への応用が可能となる。
【0056】
本発明のポリエステル重合体の製造方法は、使用原料を反応器に収容し、加熱するのみで製造できる1段階反応であるため、経済効果が大きい。
【図面の簡単な説明】
【図1】実施例1で得られたポリエステルのH−NMRチャートである。
【図2】実施例3で得られたポリエステルのH−NMRチャートである。[0001]
BACKGROUND OF THE INVENTION
The present invention relates to a novel polyester polymer useful as a material for electric / electronic parts such as a printed wiring board and a method for producing the same. The polyester polymer of the present invention has a specific skeleton (fluorene structure and polysilane structure) and is excellent in the balance between heat resistance and mechanical strength.
[0002]
[Prior art and problems to be solved by the invention]
Polyester resins, such as alkylene terephthalate resins, are excellent in heat resistance, electrical properties, other physical and chemical properties, and have good workability. Therefore, they are widely used as engineering plastics in automobiles, electrical and electronic parts, etc. It is used for various purposes. Although such a polyester resin is used alone in various molded products, it is often necessary to improve its properties, particularly mechanical strength, depending on the application. For example, in the use of printed wiring boards, it is necessary to have solder heat resistance and mechanical strength at the time of thin film formation. Are also being considered.
[0003]
As a solution for increasing the mechanical strength, blending various reinforcing agents, additives and the like with the polyester resin can be mentioned. However, in the method of blending reinforcing agents and additives, the type and amount of the reinforcing agent and additives must be determined by trial and error for each specification. In some cases, reinforcing agents and additives are used. It also occurs when it is not possible.
[0004]
Therefore, development of a new polyester resin having sufficient mechanical strength while maintaining heat resistance and workability has been desired.
[0005]
[Means for Solving the Problems]
In light of the problems of the prior art described above, the present inventors have conducted extensive research, and as a result, have a cardo structure and are a fluorene that is a hard segment that exhibits heat resistance and a soft segment that exhibits mechanical strength. It has been found that a polyester polymer having both polysilane in the molecule has sufficient mechanical strength while maintaining heat resistance and processability, and has completed the present invention.
[0006]
That is, this invention provides the polyester polymer as shown below, and its manufacturing method.
Item 1. Formula (1)
[0007]
Embedded image
[0008]
[Wherein, X represents an aliphatic hydrocarbon residue or an aromatic hydrocarbon residue.
Y is the formula (2)
[0009]
Embedded image
[0010]
(R 1 , R 2 , R 3 and R 4 are the same or different and each represents a hydrogen atom or an alkyl group having 1 to 4 carbon atoms. P represents 2 to 4).
Z is the formula (3)
[0011]
Embedded image
[0012]
(R 5 and R 6 are the same or different and each represents a hydrogen atom, an alkyl group, an aryl group, or a silyl group. Q represents 2 to 100).
a represents 2 to 10, and l, m and n are the same or different and represent 2 or more. ]
A polyester polymer represented by:
Item 2. Item 2. The polyester polymer according to Item 1, wherein X is a cycloalkylene group.
Item 3. Item 2. The polyester polymer according to Item 1, wherein X is an arylene group.
Item 4. Y is the formula (4)
[0013]
Embedded image
[0014]
Item 4. The polyester polymer according to any one of Items 1 to 3, which is a group represented by:
Item 5. Z is the formula (5)
[0015]
Embedded image
[0016]
[In formula, q shows 2-100. Or a group represented by formula (6)
[0017]
Embedded image
[0018]
[In formula, q1 and q2 are the same or different, and show one or more, The sum of q1 and q2 is 2-100. Or a group represented by formula (7)
[0019]
Embedded image
[0020]
[Wherein q is the same as defined above. The polyester polymer of any one of claim | item 1-4 which is group represented by these.
Item 6. Item 6. The polyester polymer according to any one of Items 1 to 5, having a weight average molecular weight of 1000 or more.
Item 7. Formula (8)
[0021]
Embedded image
[0022]
[Wherein, X represents an aliphatic hydrocarbon residue or an aromatic hydrocarbon residue. Dimethyl dicarboxylate represented by
Formula (9)
[0023]
Embedded image
[0024]
[In formula, a shows 2-10. An alkylene glycol represented by the formula (10):
[0025]
Embedded image
[0026]
Wherein, R 1, R 2, R 3 and R 4 are the same or different, represent a hydrogen atom or an alkyl group having 1 to 4 carbon atoms. p shows 2-4. And a fluorene compound represented by the formula (11)
[0027]
Embedded image
[0028]
[Wherein, R 5 and R 6 are the same or different and each represents a hydrogen atom, an alkyl group, an aryl group, or a silyl group. q shows 2-100. Item 2. A method for producing a polyester polymer according to Item 1, wherein the polysilane represented by the formula is subjected to condensation polymerization.
[0029]
DETAILED DESCRIPTION OF THE INVENTION
Hereinafter, the present invention will be described together with embodiments thereof.
[0030]
The polyester polymer of the present invention represented by the formula (1) includes a dimethyl dicarboxylate represented by the formula (8), an alkylene glycol represented by the formula (9), and a fluorene compound represented by the formula (10). And a polysilane represented by the formula (11) having a structure obtained by condensation polymerization in the presence of a catalyst in a molten state under high temperature and reduced pressure.
[0031]
Examples of the dimethyl dicarboxylate of formula (8) used in the present invention include dimethyl 1,4-cyclohexanedicarboxylate, dimethyl 1,3-cyclohexanedicarboxylate, dimethyl 1,2-cyclohexanedicarboxylate, and cyclohexene-1,2-dicarboxylic acid. Examples thereof include dimethyl esters of aliphatic dicarboxylic acids such as dimethyl, and dimethyl esters of aromatic dicarboxylic acids such as dimethyl terephthalate, dimethyl 1,4-naphthalenedicarboxylate, and dimethyl 2,6-naphthalenedicarboxylate. Among these, dimethyl 1,4-cyclohexanedicarboxylate and dimethyl terephthalate are preferable.
[0032]
In the polyester polymer represented by the formula (1), X is preferably a cycloalkylene group or an arylene group, and more preferably a 1,4-cyclohexylene group or a p-phenylene group.
[0033]
Examples of the alkylene glycol of the formula (9) used in the present invention include those having 2 to 10 methylene groups, and 2 to 6 are preferable among these. Specific examples include ethylene glycol, propylene glycol, 1,4-butanediol, neopentyl glycol and the like.
[0034]
In the polyester polymer represented by the formula (1), those having a of 2 to 6 are preferable.
[0035]
In the fluorene compound of the formula (10) used in the present invention, R 1 , R 2 , R 3 and R 4 are the same or different and represent a hydrogen atom or an alkyl group having 1 to 4 carbon atoms.
The alkyl group is preferably a methyl group. p shows 2-4, and the case where p = 2 is preferable among them. More specifically, 9,9-bis {4- (2-hydroxyethoxy) phenyl} fluorene, 9,9-bis [{3-methyl-4- (2-hydroxyethoxy)} phenyl] fluorene, 9-bis {4- (2-hydroxypropoxy) phenyl} fluorene, 9,9-bis [{3-methyl-4- (2-hydroxypropoxy)} phenyl] fluorene and the like, and in particular, 9,9-bis { 4- (2-hydroxyethoxy) phenyl} fluorene is preferred. For example, a method for producing 9,9-bis {4- (2-hydroxyethoxy) phenyl} fluorene is disclosed in JP-A-7-165657. The purity of the fluorene compound used in the present invention is 95% or more, preferably 98% or more.
[0036]
In the group represented by the formula (2), when the groups represented by R 1 , R 2 , R 3 and R 4 are alkyl groups, a methyl group is preferable. p is preferably 2.
[0037]
The polysilane of the formula (11) used in the present invention has a hydrogen atom, an alkyl group, an aryl group, or a silyl group as a side chain substituent (R 5 , R 6 ). As an alkyl group, a C1-C10 thing is mentioned, A C1-C6 thing is preferable. Examples of the aryl group include a phenyl group, a phenyl group having one or more alkyl groups having 1 to 10 carbon atoms as a substituent, a p-alkoxyphenyl group, and a naphthyl group. Examples of the silyl group include those having about 1 to 10 silicon, and those having 1 to 6 silicon are preferable. Further, at least one of the hydrogen atoms on the silyl group may be substituted with a substituent such as an alkyl group or an aryl group. Examples of such a substituent include the same ones as described above. As q of Formula (11), it is 2-100, Preferably it is 5-50. As the polysilane of the formula (11), methylphenyl polysilane, n-hexylmethyl-methylphenyl copolymerized polysilane, and n-hexylmethyl polysilane are more preferable.
[0038]
Polysilane production methods include: (1) Dechlorination condensation of chlorosilanes using alkali metals (J. Am. Chem. Soc., 103 (1981) 7352), (2) Electroreduction of chlorosilanes. Known methods for dechlorination condensation (JP-A-4-348128, JP-A-4-331235), (3) a method for dehydrocondensation of hydrosilanes in the presence of a catalyst (Chem. Lett., 83 (1989)), etc. It has been. Among these, it is preferable to use polysilane obtained by dechlorination condensation methods such as (1) and (2).
[0039]
In the group represented by the formula (3), when the groups represented by R 5 and R 6 are alkyl groups, examples thereof include alkyl groups having about 1 to 10 carbon atoms, and those having 1 to 6 carbon atoms. preferable. In the case of an aryl group, a phenyl group, a phenyl group having one or more alkyl groups having 1 to 10 carbon atoms as a substituent, a p-alkoxyphenyl group, a naphthyl group, and the like can be given. In the case of a silyl group, a silyl group having about 1 to 10 silicon is exemplified, and one having 1 to 6 silicon is preferable. Further, at least one of the hydrogen atoms on the silyl group may be substituted with a substituent such as an alkyl group or an aryl group. Examples of such a substituent include the same ones as described above. As q of Formula (3), it is 2-100, Preferably it is 5-50.
[0040]
In the condensation polymerization of the polyester polymer of the present invention, the dimethyl dicarboxylate (8), the alkylene glycol (9), the fluorene compound (10) and the polysilane (11) are accommodated in a reactor, The transesterification reaction is carried out by heating and melting under an active gas atmosphere. The mixing ratio of each raw material is 2.0 to 10.0, preferably 2.0 to 5.0, in terms of molar ratio, with respect to dimethyl dicarboxylate 1.0. Similarly, a fluorene compound is 0.01-2.0, Preferably it is 0.1-1.0. About the usage-amount of polysilane, since the number of moles changes with the molecular weight of polysilane, when it represents with the weight percentage with respect to dimethyl dicarboxylate, it is 0.1-200% normally, Preferably it is 0.2-100%. Moreover, in order to advance reaction more smoothly, it is more preferable to use a catalyst. As the catalyst, known lithium, potassium, sodium, barium, calcium, aluminum, antimony, tin, magnesium, cerium, manganese, cadmium, cobalt, zinc, lead, titanium, yttrium acetates, antimony, zinc, titanium, Examples thereof include germanium oxides, mono (di) -n-butyltin oxide, tetrabutyl titanate, and trimethyl phosphate. Among these, calcium, magnesium, cerium, manganese, cobalt, zinc, yttrium acetate, germanium oxide, mono (di) -n-butyltin oxide, and trimethyl phosphate are preferable. These catalysts may be used alone or in combination of two or more. The amount of the catalyst used is, by weight, 1 × 10 −5 to 1 × 10 −2 , preferably 1 × 10 −4 to 2 × 10 −3 with respect to 1.0 dimethyl dicarboxylate. The time required for the transesterification reaction varies depending on the raw materials used and the presence or absence of a catalyst, but may be about 1 hour or longer. The reaction temperature is the same, but it may be performed at about 100 to 300 ° C.
[0041]
After completion of the transesterification reaction, the polymerization reaction is allowed to proceed by raising the temperature and reducing the pressure. Although superposition | polymerization temperature changes with the raw materials to be used and the presence or absence of a catalyst, it is 200-350 degreeC in general, Preferably it is 240-300 degreeC. The pressure in the reactor is about 0.1 to 5 torr. As for the polymerization time, a polyester having a high degree of polymerization can be obtained if the polymerization time is increased, but if it is longer than necessary, a decomposition reaction may occur, resulting in a decrease in molecular weight, coloring, and the like. Is 10 minutes to 10 hours. After completion of the reaction, the polyester may be collected by introducing an inert gas such as nitrogen or argon into the reactor and extruding it while applying pressure.
[0042]
In the polyester polymer of the present invention represented by the formula (1), l, m and n are the same or different and are 2 or more, preferably 2 to 500, more preferably 10 to 200. .
[0043]
The polyester polymer of the present invention has a weight average molecular weight of 1000 or more, preferably 1000 to 1000000, and more preferably 5000 to 400000, converted using polystyrene as a standard using gel permeation chromatography.
[0044]
【Example】
Hereinafter, the present invention will be described specifically by way of examples.
[0045]
In addition, the weight average molecular weight was measured on condition of the following using the gel permeation chromatography (HLC-8020GPC by Tosoh Corporation).
Solvent: Tetrahydrofuran Flow rate: 1.0 ml / min
Column: TSKgelGMHHR-L (manufactured by Tosoh Corporation).
[0046]
Example 1
48 g (0.24 mol) of dimethyl 1,4-cyclohexanedicarboxylate, 53 g (0.12 mol) of 9,9-bis {4- (2-hydroxyethoxy) phenyl} fluorene, 33 g (0.53 mol) of ethylene glycol , 1.2 g of n-hexylmethyl-methylphenyl copolymerized polysilane (copolymerization ratio 1: 1 and weight average molecular weight 1100) and 0.03 g of di-n-butyltin oxide as a catalyst were placed in a 300 ml three-necked flask, Transesterification was performed by gradually heating to 240 ° C. with stirring in an N 2 atmosphere and distilling off the vaporized methanol. After distilling off a predetermined amount of methanol, the reaction vessel was heated to 270 ° C. while distilling off the generated ethylene glycol, and the pressure was gradually reduced to 1 torr or less. After maintaining this condition for 1.5 hours, N 2 was introduced into the reaction vessel and extruded while applying pressure to obtain 105 g of pellet-shaped polyester.
[0047]
When the molecular weight was measured by gel permeation chromatography (GPC), the weight average molecular weight was 71500. The H-NMR chart is shown in FIG.
[0048]
Example 2
The same operation as in Example 1 was conducted except that the amount of polysilane used was 6.0 g. As a result, 106 g of polyester was obtained. When the molecular weight was measured by GPC, the weight average molecular weight was 51800.
[0049]
Example 3
This was carried out in the same manner as in Example 1 except that 1.2 g of methylphenylpolysilane (weight average molecular weight 7200) was used as polysilane. As a result, 100 g of polyester was obtained. When the molecular weight was measured by GPC, the weight average molecular weight was 377,000. The H-NMR chart is shown in FIG.
[0050]
Example 4
The same operation as in Example 1 was conducted except that 48 g (0.10 mol) of 9,9-bis [{3-methyl-4- (2-hydroxyethoxy)} phenyl] fluorene was used as the fluorene. As a result, 92 g of polyester was obtained.
[0051]
Example 5
The same procedure as in Example 1 was performed except that the temperature during polymerization was changed from 270 ° C. to 300 ° C. As a result, even when the polymerization time was shortened to 1.0 hour, a polyester equivalent to Example 1 was obtained.
[0052]
Comparative Example 1
The same procedure as in Example 1 was performed without using polysilane. As a result, a polyester having a weight average molecular weight of 66200 was obtained.
[0053]
Comparative Example 2
The same procedure as in Example 1 was performed without using fluorene. As a result, a polyester having a weight average molecular weight of 145700 was obtained.
[0054]
A mechanical strength test and a heat resistance evaluation test were performed using the polyester obtained above.
[Mechanical strength test]
The obtained polyester was evaluated for mechanical strength by measuring the amount of Taber abrasion using a Taber abrasion measuring device (AB-101 type, manufactured by Tester Sangyo Co., Ltd.). The results are shown in Table 1. From Table 1, it was found that the mechanical strength was improved by introducing the polysilane structure.
[Heat resistance evaluation test]
The glass transition temperature (Tg) was measured by differential scanning calorimetry (DSC).
Differential scanning calorimeter: TAS-100, manufactured by Rigaku Corporation
Temperature increase rate: 10 ° C./min Measurement results are shown in Table 2. From Table 2, an increase in Tg was confirmed by the introduction of the fluorene structure.
[0055]
【The invention's effect】
The polyester polymer of the present invention has both a fluorene, which is a hard segment that has a cardo structure and exhibits heat resistance, and a polysilane, which is a soft segment that exhibits mechanical strength, in the molecule. Without blending the agent, it has sufficient mechanical strength while maintaining heat resistance and processability. Therefore, it can be applied to other automobiles, electrical / electronic components, etc., which have insufficient mechanical strength with conventional polyesters, including printed wiring board applications.
[0056]
The production method of the polyester polymer of the present invention has a large economic effect because it is a one-step reaction that can be produced simply by storing the raw material used in the reactor and heating it.
[Brief description of the drawings]
1 is an H-NMR chart of the polyester obtained in Example 1. FIG.
2 is a H-NMR chart of the polyester obtained in Example 3. FIG.
Claims (7)
Yは式(2)
Zは式(3)
aは2〜10を示し、l、mおよびnは、同一または異なって、2以上を示す。〕
で表されるポリエステル重合体。Formula (1)
Y is the formula (2)
Z is the formula (3)
a represents 2 to 10, and l, m and n are the same or different and represent 2 or more. ]
A polyester polymer represented by:
式(9)
Formula (9)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP16155599A JP3851996B2 (en) | 1999-06-08 | 1999-06-08 | Polyester polymer and method for producing the same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP16155599A JP3851996B2 (en) | 1999-06-08 | 1999-06-08 | Polyester polymer and method for producing the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2000344878A JP2000344878A (en) | 2000-12-12 |
| JP3851996B2 true JP3851996B2 (en) | 2006-11-29 |
Family
ID=15737344
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP16155599A Expired - Lifetime JP3851996B2 (en) | 1999-06-08 | 1999-06-08 | Polyester polymer and method for producing the same |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP3851996B2 (en) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5154958B2 (en) * | 2007-02-28 | 2013-02-27 | 国立大学法人東京工業大学 | Method for producing silicon-containing polymer having fluorene skeleton |
| JP5154957B2 (en) * | 2007-02-28 | 2013-02-27 | 国立大学法人東京工業大学 | New fluorene skeleton-containing polymer |
| JP5469313B2 (en) * | 2008-03-26 | 2014-04-16 | 大阪瓦斯株式会社 | Silicon compound having a fluorene skeleton |
| JP5297079B2 (en) * | 2008-05-07 | 2013-09-25 | 大阪瓦斯株式会社 | Silicon compound having fluorene skeleton and polymerizable composition thereof |
-
1999
- 1999-06-08 JP JP16155599A patent/JP3851996B2/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| JP2000344878A (en) | 2000-12-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JPS5913531B2 (en) | Copolyester manufacturing method | |
| JPS582325A (en) | Linear block copolyester having improved lubricant properties | |
| GB1581894A (en) | Yesterification catalysts metal and silicon-containing coordination complexes as pol | |
| GB1579887A (en) | Copolyesters | |
| JP3851996B2 (en) | Polyester polymer and method for producing the same | |
| TW201728614A (en) | Terminally modified polybutylene terephthalate resin, thermoplastic resin composition including same, and molded article | |
| JPS63125528A (en) | Silicon-containing copolyester and its production | |
| JPH0565531B2 (en) | ||
| JP4662633B2 (en) | Blend of poly (1,3-propylene 2,6-naphthalate) | |
| JP7369178B2 (en) | Polyester resin and its manufacturing method | |
| WO2021210488A1 (en) | Copolyester resin, molded article, heat-shrinkable film, and fiber | |
| JP3164889B2 (en) | Method for producing aromatic polyester | |
| JP2005060645A (en) | Polyester-based block copolymer and method for producing the same | |
| JP3732754B2 (en) | Method for producing biodegradable copolymer polyester | |
| JPH0859809A (en) | Preparation of polyester with high degree of polymerization | |
| JP2000212266A (en) | Preparation of flame-retardant polyester | |
| JP2002284869A (en) | Process for preparation of polyester | |
| JP2665074B2 (en) | Polyester production method | |
| JP3732753B2 (en) | Biodegradable copolyester and method for producing the same | |
| JP2537524B2 (en) | Method for producing polyester | |
| JPH0364320A (en) | Preparation of aromatic polyester | |
| JPH0790066A (en) | Copolymerized polyester | |
| JPS5936652B2 (en) | Method for manufacturing polyester elastomer | |
| JPH1135665A (en) | New polyester and its production | |
| JPH0488078A (en) | New adhesive composition |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050201 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20060731 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20060809 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20060821 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 3851996 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20090915 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120915 Year of fee payment: 6 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120915 Year of fee payment: 6 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150915 Year of fee payment: 9 |
|
| EXPY | Cancellation because of completion of term |