JP2024538136A - 改善された抗菌表面を有するデバイス - Google Patents
改善された抗菌表面を有するデバイス Download PDFInfo
- Publication number
- JP2024538136A JP2024538136A JP2024522570A JP2024522570A JP2024538136A JP 2024538136 A JP2024538136 A JP 2024538136A JP 2024522570 A JP2024522570 A JP 2024522570A JP 2024522570 A JP2024522570 A JP 2024522570A JP 2024538136 A JP2024538136 A JP 2024538136A
- Authority
- JP
- Japan
- Prior art keywords
- coating
- medical device
- ald
- laser
- coated
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/02—Inorganic materials
- A61L27/04—Metals or alloys
- A61L27/045—Cobalt or cobalt alloys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/02—Inorganic materials
- A61L27/04—Metals or alloys
- A61L27/047—Other specific metals or alloys not covered by A61L27/042 - A61L27/045 or A61L27/06
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/02—Inorganic materials
- A61L27/04—Metals or alloys
- A61L27/06—Titanium or titanium alloys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/28—Materials for coating prostheses
- A61L27/30—Inorganic materials
- A61L27/306—Other specific inorganic materials not covered by A61L27/303 - A61L27/32
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/54—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/02—Inorganic materials
- A61L31/022—Metals or alloys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/08—Materials for coatings
- A61L31/082—Inorganic materials
- A61L31/088—Other specific inorganic materials not covered by A61L31/084 or A61L31/086
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L31/16—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/10—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices containing or releasing inorganic materials
- A61L2300/102—Metals or metal compounds, e.g. salts such as bicarbonates, carbonates, oxides, zeolites, silicates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/10—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices containing or releasing inorganic materials
- A61L2300/102—Metals or metal compounds, e.g. salts such as bicarbonates, carbonates, oxides, zeolites, silicates
- A61L2300/104—Silver, e.g. silver sulfadiazine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/404—Biocides, antimicrobial agents, antiseptic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2400/00—Materials characterised by their function or physical properties
- A61L2400/12—Nanosized materials, e.g. nanofibres, nanoparticles, nanowires, nanotubes; Nanostructured surfaces
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2400/00—Materials characterised by their function or physical properties
- A61L2400/18—Modification of implant surfaces in order to improve biocompatibility, cell growth, fixation of biomolecules, e.g. plasma treatment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2420/00—Materials or methods for coatings medical devices
- A61L2420/02—Methods for coating medical devices
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Dermatology (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Transplantation (AREA)
- Vascular Medicine (AREA)
- Surgery (AREA)
- Heart & Thoracic Surgery (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Engineering & Computer Science (AREA)
- Materials For Medical Uses (AREA)
Abstract
医療デバイスは、表面を有する基板構造体を含む。表面は、該表面に対して延びる少なくとも1つの突起および/または少なくとも1つの空隙を規定するように、レーザー処理されている。抗菌特性、抗微生物特性および/または薬剤溶出特性を有するコーティングが、1つ以上の前記突起および/または前記空隙の表面部分内または該表面部分に沿って係合するように前記基板構造体に適用されている。
Description
本出願は、2021年10月12日に出願された米国出願第63/254,752号の利益を主張するものであり、その内容は参照により本明細書に組み込む。
[本開示の技術分野]
本開示は、電極および生物医学的な、埋め込み型(implantable)または診断用医療デバイスに関する。このデバイスは、抗菌特性、抗微生物特性、または薬剤溶出特性を付与するコーティングを支持する(またはサポートする)。改良された表面トポグラフィーを有する。
本開示は、電極および生物医学的な、埋め込み型(implantable)または診断用医療デバイスに関する。このデバイスは、抗菌特性、抗微生物特性、または薬剤溶出特性を付与するコーティングを支持する(またはサポートする)。改良された表面トポグラフィーを有する。
[背景]
高齢化と、薬物療法だけでは緩和できない多くの神経疾患および心血管系疾患により、植え込み型神経刺激デバイスを必要とする患者の数が大幅に増加している。これらは、センサー、胃および心臓ペースメーカー、除細動器、脳深部、神経、および骨刺激装置など多岐にわたる。再吸収性電子機器(Resorbable electronics)は、外科的な除去を必要とせず、優れた短期的性能を発揮する可能性がある。しかし、ほとんどの電子材料は生体および細胞適合性が低く、免疫反応および感染症を引き起こす。
高齢化と、薬物療法だけでは緩和できない多くの神経疾患および心血管系疾患により、植え込み型神経刺激デバイスを必要とする患者の数が大幅に増加している。これらは、センサー、胃および心臓ペースメーカー、除細動器、脳深部、神経、および骨刺激装置など多岐にわたる。再吸収性電子機器(Resorbable electronics)は、外科的な除去を必要とせず、優れた短期的性能を発揮する可能性がある。しかし、ほとんどの電子材料は生体および細胞適合性が低く、免疫反応および感染症を引き起こす。
感染は、人体に埋め込まれた(または移植された)デバイスの深刻な合併症である。深部感染は治療が困難であり、感染を根絶するためには感染したインプラントの除去が必要となることがしばしばあり、これは、多くの医療処置における深刻な合併症として残されている。深部感染症の治療は、感染部位に抗生物質を供給することが難しいため困難であり、治療期間は3ヵ月から14ヵ月の間で変動し得、また、二次手術が必要になることもある。
金属や金属酸化物、特に微粒子やナノ粒子の形態における抗微生物特性(antimicrobial properties)は以前から認識されており、その効果を報告する文献も多数存在する。既知の金属含有コーティングの一般的な欠点は、そのようなコーティングの付着性を改善する努力(例えば、耐久性や耐スクラッチ性を提供すること)が、その抗微生物特性に悪影響を及ぼす可能性があることである。逆に、このようなコーティングの抗微生物効果を改善しようとすると、インプラント表面に安定的に付着する能力に悪影響を及ぼす可能性がある。
階層的表面再構築(Hierarchical surface restructuring:HSR(商標))技術では、超高表面積(ultrahigh surface area)と、強化された電気化学的に活性な表面積(enhanced electrochemically-active-surface-area)のために、マイクロ電極上(または微小電極上)に階層的構造化表面(hierarchically structured surfaces:HSS)を作製することができる。しかしながら、電極材料(例えば、Pt10Ir)または電極材料上に堆積された一般的な表面コーティング(例えば、TiNまたはIrO2)は、抗微生物性(antimicrobial)ではない場合がある。一方、例えばCuxOなどの非常に効果的な広域抗微生物材料(broad-spectrum antimicrobial materials)は、電気化学的特性に乏しい絶縁体であり、電極として使用することはできない。原子レベルの薄さのウルトラコンフォーマル(ultra-conformal:超適合)な抗微生物材料により、表面を階層的に再構築した電極またはマイクロ電極アレイをコーティングすることで、電極またはマイクロ電極アレイに抗微生物特性を付与することができる。
ここで、原子レベルで薄い厚さ(atomically thin thickness)は、HSSのナノスケールの形態および機能(例えば、超高表面積、電荷蓄積容量、インピーダンス、比静電容量など)への影響を最小限に抑えるために不可欠である。また、複雑なナノ構造を有するHSSのための完全な抗微生物性カバレッジ(complete antimicrobial coverage)のためには、ウルトラコンフォーマリティー(ultra-conformality:超適合性)が不可欠である。ここで、ウルトラコンフォーマリティーと原子レベルで薄い厚さ、という2つの本質的な特徴は、(1)視線効果と、(2)100nm未満のナノコーティングにおける原子レベルの厚さ制御の困難性から、従来のコーティング技術(スパッタリング、PVD、CVDなど)では極めて困難である。これに対し、原子層堆積(ALD)コーティング技術は、本質的に自己制限的(self-limiting)なコーティングメカニズムにより、2つの本質的な特徴と超高再現性を達成する理想的な(唯一の)技術である。さらに、ALD技術は、自動化された高並列処理スループットを備えた最新の用途に使用されている。
少なくとも1つの実施形態において、本開示は、表面を有する基板構造体を含む医療デバイスを提供する。表面は、その表面に対して延びる少なくとも1つの突出および/または少なくとも1つの空隙を規定するように、レーザー処理されている。抗菌特性(antibacterial properties)、抗微生物特性および/または薬剤溶出特性を有するコーティングが、1つ以上の突起および/または空隙の表面部分内(within a surface portion)または表面部分に沿って(along a surface portion)係合するように、基板構造体に適用される。
[図面の簡単な説明]
本明細書に組み込まれ、本明細書の一部を構成する添付図面は、本発明の現在の好ましい実施形態を示すものであり、上記の一般的な説明および下記の詳細な説明とともに、本発明の特徴を説明するのに役立つ。
本明細書に組み込まれ、本明細書の一部を構成する添付図面は、本発明の現在の好ましい実施形態を示すものであり、上記の一般的な説明および下記の詳細な説明とともに、本発明の特徴を説明するのに役立つ。
[詳細な説明]
図面では、全体を通して同様の数字は同様の要素を示す。本明細書において、特定の用語は便宜上使用されているに過ぎず、本発明を限定するものではない。以下、本発明の好ましい実施形態について説明する。しかしながら、本開示に基づいて、本発明は、本明細書に記載された好ましい実施形態によって限定されないと理解されるべきである。
図面では、全体を通して同様の数字は同様の要素を示す。本明細書において、特定の用語は便宜上使用されているに過ぎず、本発明を限定するものではない。以下、本発明の好ましい実施形態について説明する。しかしながら、本開示に基づいて、本発明は、本明細書に記載された好ましい実施形態によって限定されないと理解されるべきである。
図1A~図3を参照して、本開示の実施形態による例示的な医療デバイス基板構造体10を説明する。潜在的な医療デバイスとしては、電極、マイクロ電極アレイ、ステント、整形外科用および歯科用インプラントなどが挙げられるが、これらに限定されない。医療デバイス30の基板構造体10およびコーティング32は、所望の構造特性および抗菌特性の組み合わせを提供するように選択され得る。図示された基板構造体10は、複数のマクロ突起14、マイクロ突起16およびナノ突起18によって規定された表面12のトポグラフィーを有する。表面12は、複数の空隙20も含み得る。例示的な構造として説明したが、医療デバイス30の基板構造体10は、より多くの、またはより少ない突起を有してもよく、空隙を含んでも含まなくてもよい。
図示した実施形態では、外周面は、外周面12について分布し、外周面12から外側に延びる複数の離散的なマクロ突起14によって規定されるトポグラフィーを有する(図1A参照)。一実施形態では、マクロ突起14は、固体モノリシック基板の外周面全体にわたって実質的に均一に分布している。一実施形態では、マクロ突起の幅は、約0.15μm~約50μmである。別の実施形態では、マクロ突起の幅は、約0.2μm~約30μmである。さらに別の実施形態では、マクロ突起の幅は、約1μm~約20μmである。
複数の離散的な(discrete)マイクロ突起16がマクロ突起14上に分布し、マクロ突起14から外側に延びる(図1B参照)。一実施形態では、マイクロ突起16の幅は、約0.15μm~約5μmである。別の実施形態では、マイクロ突起16の幅は、約0.2μm~約2μmである。さらに別の実施形態では、マイクロ突起16の幅は、約0.4μm~約1.5μmである。一実施形態では、マイクロ突起16は、マイクロ突起の高さの周期的な波状の形態でマクロ突起14を横切って分布している。周期的な波状は、レーザー照射の波長によって発生し、制御されると考えられる。
複数の離散的なナノ突起18がマイクロ突起16上に分布し、マイクロ突起16から外側に延びる(図1C参照)。一実施形態では、ナノ突起18の幅は、約0.01μm~約1μmである。別の実施形態では、ナノ突起18の幅は、約0.02μm~約1μmである。さらに別の実施形態では、ナノ突起18の幅は、約0.075μm~約0.8μmである。一実施形態では、ナノ突起18は、チューブ状および/または球状の形態でマイクロ突起16を横切って分布している。ナノ突起18は、パルス数とパルス持続時間によって発生し、制御されると考えられる。特定の理論に拘束されることなく、マクロ、マイクロ、およびナノ突起は、レーザーが基板表面に空隙を掘削(または穿孔:drilling)され、その後に空隙からの材料(空隙材料:void material)がこれらの突起として基板表面に再析出することによって形成されると考えられる。したがって、レーザー照射は、基板をガスでパージしたり、実質的なガス圧力をかけたりせずに行うことが重要である。空隙からの材料が基板上に再堆積されずに、吹き飛ばされてしまう傾向にあるためである。除去された空隙材料が吹き飛ばされず、基板上に再析出できる限り、レーザー照射が実施される雰囲気は一般に重要ではないと考えられる。例えば、Tiなどの材料の場合、窒素は、Tiと反応して電気化学的に活性な高表面積TiNを形成するのに必要である。掘削効果は、レーザースポットの中心で最も強くなるため、レーザースポットが基板表面を横切ることにより、スポットの重なりが生じ、その結果、適用されるレーザー放射のガウス分布が生じる。
本発明の別の実施形態では、基板表面から外側に延びるこれらの離散的なマクロ、マイクロ、およびナノ突起に加えて、表面構造12は、使用するレーザーパラメータに応じて長さと深さが決まるレーザー誘起の空隙20のアレイ(配列:array)(図2参照)を有してもよい。したがって、この実施形態では、外周面はさらに、基板を貫通する深さで延びた、外周面に分布する複数の空隙20を備えたトポグラフィーを有する。空隙は、約50nm~約500nm、好ましくは約100nm~約250nmの、基板を貫通する深さを有する。空隙の幅は、約50nm~約500nm、好ましくは約100nm~約250nmである。空隙は、隣接する空隙から約50nm~約250nmの距離で離間している。
本開示に係る基板表面10は、生体適合性金属の固体モノリシック基板の外周面を、レーザー照射パルス(pulses of laser irradiation)に曝すことによって製造される。一実施形態では、レーザーのスポット径は、約1μm~約1000μmである。別の実施形態では、レーザーのスポット径は、約2μm~約250μmであり、さらに別の実施形態では、レーザーのスポット径は、約5μm~約200μmである。一実施形態では、1スポットあたりのレーザー照射のパルス数は、約10~約1500パルスである。別の実施形態では、1スポット当たりのレーザー照射のパルス数は約20~約1000であり、さらに別の実施形態では、1スポット当たりのレーザー照射のパルス数は約100~約500である。一実施形態では、レーザーのパルス波長は、約200nm~約1500nmである。別の実施形態では、パルス波長は約400~約1000であり、さらに別の実施形態では、パルス波長は約400~約800の範囲である。一実施形態では、レーザーパルス幅は約1フェムト秒~約5ピコ秒である。別の実施形態では、レーザーパルス幅は、約1フェムト秒~約3ピコ秒である。一実施形態では、レーザー照度は、約200ワット/cm2~約5000ワット/cm2である。露光は、固体モノリシック基板の外周面を横切って、約50mm/分~約1000mm/分の速度でレーザー放射(またはレーザー照射)のスポットを移動させることによって実施されてもよいが、速度は本発明にとって重要ではなく、本発明の方法を実施する際の費用対効果にのみ影響する。
好適なレーザーの例としては、Coherent Libra-F Ti:サファイア増幅器レーザーシステム、Rofin Startfemto、およびCoherent AVIAレーザーが挙げられる。本開示によれば、得られる電極は、約1000mV以下、好ましくは約500mV以下、より好ましくは約200mV以下の分極を有する。
図4を参照すると、医療デバイス30は、基板構造体10の表面12全体に適用されたコーティング32を含む。コーティング32は、様々な特性、例えば、抗菌特性および/または抗微生物特性を有し得る。コーティング32はまた、例えば、抗癌剤、および/または抗菌剤もしくは抗微生物剤などの薬剤溶出特性を有していてもよい。
亜鉛、銅および/または銀などの殺菌性元素を含む抗菌性コーティングまたは薄膜は、イオンの形態である場合に殺菌性を有することが知られている。これらの元素のほとんどは、特定の処理および/または操作条件下で酸素にさらされると酸化物を形成し、その酸化物も抗菌特性を発揮し得る。例えば、酸化亜鉛、酸化銀、酸化銅などである。
基本的なコーティングは既知であるが、基板構造体10のレーザー再構築またはテクスチャリングにより、コーティングが最大の効果を発揮するように表面12が構成される。
例えば、図4に示す実施形態では、突起14、16、18および空隙20によって、拡大された表面積が規定され、それによりコーティングを容易に最大量にすることができる。
例えば、図4に示す実施形態では、突起14、16、18および空隙20によって、拡大された表面積が規定され、それによりコーティングを容易に最大量にすることができる。
図5に示される医療デバイス30’に目を向けると、コーティング32'は空隙20内にのみ適用される。このような構成では、コーティング32'の露出は最小限であり、ゆっくりとした徐放が望まれる用途に利用することができる。図6に示される実施形態では、医療デバイス30''のコーティング32''は、マクロ突起14間の表面12に沿って、そして空隙20内に適用される。前の実施形態と比較して、コーティング32''は、より広い表面積に沿って露出され、したがってより迅速に放出され得るが、それでも突起16、18の外側延長部よりも下にあるため保護される。
図7に図示された医療デバイス32'''では、コーティング32'''は、マイクロ突起16間の表面12に沿って適用される。この構成では、コーティング32'''は、接触してより迅速に放出されるように外表面に近接しているが、それでもなお、さらに外側に延びるナノ突起18によって保護される。逆に、図8に示された医療デバイス32ivでは、コーティング32ivはナノ突起18にのみ適用される。この構成により、コーティング32ivの露出は最大になり、それに応じて急速に放出される。
以下に詳細に説明するように、上記の様々な特徴を組み込んだサンプル構造体を製造して試験を行った。より具体的には、ALDにより、シリコン、平坦なPt10Ir、およびPt10Ir HSS上に、ウルトラコンフォーマルな原子レベルの薄さのCuxO抗微生物コーティングを作製した。一例として、これは熱ALDまたはプラズマ強化ALD(PEALD)の堆積(または成膜:deposit)が可能なVeeco Fiji プラズマ強化ALDを使用して、CuxO ALDコーティングを堆積(成膜)に使用した。
サンプルを、Cu含有前駆体および酸化反応物(例えば、O3、Oプラズマ、またはH2O)の反復サイクルに曝露した。各サイクルにおいて、Cu含有前駆体およびガス反応物は同時に、逐次的かつ自己限定的に基板と反応する。こうして、ウルトラコンフォーマルなCuxOプレサイクル(または事前サイクル:pre cycle)をサンプル上に成長させる。CuxO ALDコーティングの品質と特性は、様々な特性評価技術によって評価した:エリプソメーターと原子間力顕微鏡(AFM)による膜厚と光学特性の評価、高分解能走査型電子顕微鏡(SEM)とAFMによる微細構造とナノ形態の評価、エネルギー分散型分光法(EDS)によるマイクロスケールの化学プローブの評価、X線光電子分光法(XPS)による化学組成の評価、斜入射X線回折法(GIXRD)による結晶構造と組成の評価、光学顕微鏡とSEMによるコーティングの適合性(conformity)と均一性の評価、ナノインデンターによる機械的耐久性の評価を行った。XPSに基づいて、Oプラズマを用いたPEALDとO3を用いた熱ALDによるALDコーティングはCuOであることが確認された。
以下に詳細に説明するように、コーティングされたサンプルの抗微生物特性を調査した。コーティングされていないSiと平坦なPt10Irは抗微生物特性を有さないが、興味深いことに、コーティングされていないPt10Ir HSSサンプルは、おそらくナノスケールの表面のシャープさに起因して、特定の固有の抗微生物特性を示す。CuOコーティングされたサンプルはすべて、異なる程度の抗微生物特性を示した。CuOコーティングされたHSSサンプルは、最も高い抗微生物特性を示した。
[コーティング手順]
CuxO膜は、Veeco Fiji PEALDシステムを使用して成長させた。Cu含有前駆体として(ビス(ジメチルアミノ-2-プロポキシド)銅(II))を使用し、Veeco低蒸気圧供給(LVPD)モジュールを使用して前駆体源を125℃に維持した。キャリアガスとしてアルゴンガスを使用し、流量は30sccmで一定とした。
CuxO膜は、Veeco Fiji PEALDシステムを使用して成長させた。Cu含有前駆体として(ビス(ジメチルアミノ-2-プロポキシド)銅(II))を使用し、Veeco低蒸気圧供給(LVPD)モジュールを使用して前駆体源を125℃に維持した。キャリアガスとしてアルゴンガスを使用し、流量は30sccmで一定とした。
2つのALD堆積条件を研究した:(1)酸素プラズマを共反応物として使用するプラズマ強化ALD(PEALD)、および(2)オゾン(O3)を共反応物として使用する熱ALDである。基板温度は150℃に維持した。PEALDでは、各ALDサイクルは2秒間の銅前駆体パルスと10秒間の酸素プラズマパルスから構成され、1サイクルあたりの成長(GPC)は~0.05nmであった。O3ベースのALDでは、各ALDサイクルは2秒のCu前駆体パルスと0.075秒のO3パルスから構成され、1サイクルあたりの成長(GPC)は~0.02nmであった。
3種類の基板を使用した:原子レベルの平坦なシリコン、受け取ったままの(または、処理していない:as-received)Pt10Ir、およびレーザー処理したPt10Ir HSSである。ALDコーティングの厚さを分析するために、カプトンテープ(Kapton tape)を使用してALDコーティングをブロック/マスクし、マスクされていない領域のみをALDコーティングできるようにした。
[材料の特性評価]
J.A.Woollam社製の分光エリプソメーターM-2000を使用して、ALDコーティングの厚さと光学特性を分析した。オリンパス社製の顕微鏡を使用して、サンプルの形態(morphology)を評価した。日立製作所製のEDSモジュール付S-4800走査型電子顕微鏡(SEM)を使用して、ナノスケールの形態とEDS組成マッピングを評価した。XPS組成分析には、VersaProbe5000XPSを使用した。XPSスポットサイズは200μmであり、284.8eVのC1sピークのC-C成分を用いてキャリブレーションを行った。パークシステム社製のAFMを使用して、マスクSiサンプル(またはマスクされたSiサンプル:masked-Si sample)の表面形態と膜厚を分析した。
J.A.Woollam社製の分光エリプソメーターM-2000を使用して、ALDコーティングの厚さと光学特性を分析した。オリンパス社製の顕微鏡を使用して、サンプルの形態(morphology)を評価した。日立製作所製のEDSモジュール付S-4800走査型電子顕微鏡(SEM)を使用して、ナノスケールの形態とEDS組成マッピングを評価した。XPS組成分析には、VersaProbe5000XPSを使用した。XPSスポットサイズは200μmであり、284.8eVのC1sピークのC-C成分を用いてキャリブレーションを行った。パークシステム社製のAFMを使用して、マスクSiサンプル(またはマスクされたSiサンプル:masked-Si sample)の表面形態と膜厚を分析した。
[結果と考察]
(CuOのPEALD)
-3種類の基板に対して、225サイクルのPEALD CuxOを実施した。エリプソメトリーを使用して膜厚を測定したところ12nmであり、成長速度は~0.05nm/サイクルであった。図9Aおよび図9Bは、コーティングされたPt10IrおよびPt10Ir HSSサンプルのSEM像を示しており、PEALD堆積(成膜)の前後で表面形態の変化は最小限であり、サンプル表面の膜の適合性が良好であることを示唆している。
(CuOのPEALD)
-3種類の基板に対して、225サイクルのPEALD CuxOを実施した。エリプソメトリーを使用して膜厚を測定したところ12nmであり、成長速度は~0.05nm/サイクルであった。図9Aおよび図9Bは、コーティングされたPt10IrおよびPt10Ir HSSサンプルのSEM像を示しており、PEALD堆積(成膜)の前後で表面形態の変化は最小限であり、サンプル表面の膜の適合性が良好であることを示唆している。
図10A~図10CのEDSスペクトルは、3種類の基板の全てにおいて、CuxO堆積(成膜)が予想通りCuとOであることを示している。以下の表1に示すように、定量EDS分析によると、Cuの表面組成は、シリコンサンプルでは4.8重量%、Pt10Irでは3.9重量%、Pt10Ir HSSサンプルでは13.7重量%であった。
図11は、PEALD薄膜のXPS Cu2pスペクトルを示しており、Cu2+、すなわちx=2のCuxOがCuOとして堆積(成膜)されたことを明示している。すべてのサンプルで、Cu2p3/2、Cu2p1/2、およびCu2+のサテライトピークが、約929.6eV、949.8eV、958.5eV、937.0~939.9eVに観測される。
(CuOのO3-ALD)
-3種類の基板に対して、950サイクルのO3ベースALD堆積(成膜)を実施した。エリプソメトリーを使用して膜厚を測定したところ22nmであり、成長速度は~0.05nm/サイクルであった。図12は、コーティングされたSi、Pt10IrおよびPt10Ir HSSサンプルのSEM像を示しており、O3-ALDの前後で表面形態の変化は最小限であることを示唆している。
-3種類の基板に対して、950サイクルのO3ベースALD堆積(成膜)を実施した。エリプソメトリーを使用して膜厚を測定したところ22nmであり、成長速度は~0.05nm/サイクルであった。図12は、コーティングされたSi、Pt10IrおよびPt10Ir HSSサンプルのSEM像を示しており、O3-ALDの前後で表面形態の変化は最小限であることを示唆している。
EDSスペクトル(図示せず)も、3種類の基板の全てにおいて、CuxO堆積(成膜)が予想通りCuとOであることを示している。以下の表2に示すように、表1と同様の定量的EDS分析によると、Cuの表面組成は、シリコンサンプルでは69.2重量%、Pt10Irでは2.5重量%、Pt10Ir HSSサンプルでは31.5重量%であった。これらはコーティング表面の組成であることに留意されたい。
O3-ALD酸化銅膜の組成を確認するためにXPSを実施した。図13はCu2pスペクトルを示しており、これもCu2+の酸化状態であること、すなわちO3-ALDコーティング膜がCuOであることを示している。
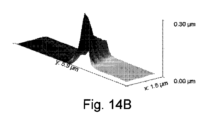
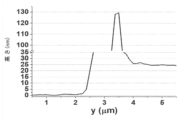
図14A~図14Dは、境界におけるO3-ALDコーティングされた、カプトンテープマスクされたSiサンプルのAFMスキャンを示しており、膜厚が~24nmであることを示しており、~22nmのエリプソメトリー測定とよく一致している。Si基板上に22nmのコーティングが見られることは興味深い。
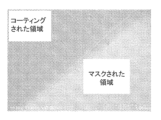
~22nmのO3-ALD CuOコーティングは、図15~図17に示すように、マスキング境界周辺の光学像、SEM像、およびEDSマッピングによって容易に識別できる。異なる倍率の光学像(図15A~図15D)は、コーティングされた領域とコーティングされていない領域の間の色のコントラストを示している。コーティングされた側(coated side)はコーティングされていない側(uncoated side)より暗く見える。HSSサンプルのSEM像(図16A~図16E)は、マスクされた境界付近でサンプルの構造に急激に変化していることを示している。図16Dおよび図16Eは、22nmのCuOコーティングがHSSナノ構造を良好かつコンフォーマルにコーティングしており、コーティングされていないHSS構造と比較して、コーティングによる鈍化効果(blunting effect)を引き起こしていることを示している。
EDSマッピング(図17A~図17F)は、マスクされた領域とマスクされていない領域の境界付近で行われた。ここで、左側がマスキングされた領域、右側がコーティングされた領域である。プラチナとイリジウムがサンプル全体に存在することがわかる。Cuは右側に存在し、マスクされた領域には存在しない。これは、カプトンテープによる表面のマスキングと、CuOコーティングの有効性を証明するさらなる証拠である。
[詳細分析]
(表面からのイオン放出)
-コーティングされた基板と、剥き出しの基板(コントロールとして)について、提供されたコーティング組成に基づく銅イオンの静的放出を試験した。実験計画は以下の通りであった:サンプルを10mlの液体培地(滅菌蒸留H2Oまたは細菌増殖用の滅菌LB培地のいずれか)に浸漬し、37℃でインキュベートした。時間=0分と、その後10分間隔で、溶液から500mlのアリコート(分取:aliquots)を取り出し、すぐに4.5mlの2%硝酸と混合した。次に、これらのサンプルを、銅イオン検出用に調整したICP-MSに注入した。
(表面からのイオン放出)
-コーティングされた基板と、剥き出しの基板(コントロールとして)について、提供されたコーティング組成に基づく銅イオンの静的放出を試験した。実験計画は以下の通りであった:サンプルを10mlの液体培地(滅菌蒸留H2Oまたは細菌増殖用の滅菌LB培地のいずれか)に浸漬し、37℃でインキュベートした。時間=0分と、その後10分間隔で、溶液から500mlのアリコート(分取:aliquots)を取り出し、すぐに4.5mlの2%硝酸と混合した。次に、これらのサンプルを、銅イオン検出用に調整したICP-MSに注入した。
最初の実験セットは、CuOコーティングのないシリコン基板を使用して行った。これらの結果を図18および図19に示す。コーティングされていないシリコンサンプルでは、サンプル中に存在するCuのレベルが非常に低いことがわかった。それらは、最終時点で50~70ppbであった。これらのサンプル中のCuイオンがどこから発生したのかは不明であるが、信号は一貫して、液体培地に由来するバックグラウンドを2~3倍上回っていた。
第2の実験セットは、CuOコーティングのある、およびコーティングのないプラチナ基板を使用して行った。この実験はまた、CuOコーティングのある、およびコーティングのない、未処理または「平坦な」Pt基板と、CuOコーティング前に表面をレーザー再構築したPt HSS基板を比較することによって、多様化された。これらのICP-MS実験の結果を図20および図21に示す。これらの結果は、水とLB培地の両方で、コーティングされたPt HSS基板からCuイオンが急速かつ大量に放出されることを明示している。この放出量は、「平坦な」Pt基板と比較すると、1桁高い(実験終点で~1900ppb対~200ppb)。特筆すべきは、CuOコーティングした「平坦な」基板は、バックグラウンドと比較して、若干のCuイオンを放出したことである(~200ppb対~60ppb)。
(細菌付着)
-コーティングされた材料を、提供されたコーティング組成物に基づいて、細菌付着および接触依存性抗菌活性について試験した。実験計画では、既知量の細菌(1×105CFU/mlに調整させた細菌培養液10ml)を表面に堆積することを含んでいた。37℃で60分間インキュベートした後、滅菌綿棒を使用して表面を拭き取り、残っている生菌を分離した。この綿棒を使用して、固体培地であるLB寒天プレートに接種し、その後3mlの滅菌LB培地に浸漬して最終接種を行った。LB寒天シャーレと液体培養物の両方を37℃で18時間インキュベートし、液体サンプルを250rpmで振とうして増殖を最大にした。18時間後、コロニーの成長を確認するためにプレートの写真を撮影し、OD600を使用して液体サンプルの濁度を測定した。大腸菌(グラム陰性)と黄色ブドウ球菌(グラム陽性)の両方の細菌株について、同じ手順を使用した。
-コーティングされた材料を、提供されたコーティング組成物に基づいて、細菌付着および接触依存性抗菌活性について試験した。実験計画では、既知量の細菌(1×105CFU/mlに調整させた細菌培養液10ml)を表面に堆積することを含んでいた。37℃で60分間インキュベートした後、滅菌綿棒を使用して表面を拭き取り、残っている生菌を分離した。この綿棒を使用して、固体培地であるLB寒天プレートに接種し、その後3mlの滅菌LB培地に浸漬して最終接種を行った。LB寒天シャーレと液体培養物の両方を37℃で18時間インキュベートし、液体サンプルを250rpmで振とうして増殖を最大にした。18時間後、コロニーの成長を確認するためにプレートの写真を撮影し、OD600を使用して液体サンプルの濁度を測定した。大腸菌(グラム陰性)と黄色ブドウ球菌(グラム陽性)の両方の細菌株について、同じ手順を使用した。
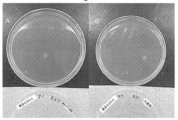
最初の実験セットは、CuOコーティングのある、およびコーティングのないシリコン基板を使用して行った。これらの結果を図22および図23に示す。図22は、CuOコーティングしたSi基板を拭き取った後に接種した寒天プレートを示し、図23は、液体培養物を接種した後のOD600を示す。このデータは、プレート上にコロニーが現れず、液体培養物中に光の散乱が観察されないことからも明らかなように、大腸菌がCuO表面との接触によって死滅したことを示している。対照的に、シャーレ上にコロニーが存在し、液体培養物に高いレベルの散乱が観察されたことからも明らかなように、黄色ブドウ球菌は、CuOコーティングされた表面に接触しても死滅しなかった。
ここでも、CuOコーティングのある、およびコーティングのないプラチナ基板を使用して、第2セットの実験を行った。この実験はまた、CuOコーティングのある、およびコーティングのない、未処理または「平坦な」Pt基板と、CuOコーティング前に表面をレーザー再構築したPt HSS基板を比較することによって、多様化された。結果を図24~図27に示す。これらの実験では、大腸菌はいずれの表面条件でも増殖できなかった。しかし、黄色ブドウ球菌は、CuOコーティングの有無に関係なく、「平坦な」表面でのみ増殖することができた。最も重要なことは、レーザー再構築サンプルから得られたサンプルでは、黄色ブドウ球菌のコロニーの増殖が確認されなかったことであり、これらの表面による殺菌効果が大幅に改善されたことを示している。
図28および図29は、図24~図27と同じスワブ(綿棒)から接種した液体培養物のデータを示す。コーティングされていないプラチナサンプルから採取した綿棒は、寒天プレートアッセイで見られるものと同じパターンを示したが、1つだけ例外があった:黄色ブドウ球菌の培養物の1つは、液体培養物で中程度の増殖を示した(図28)。このことは、綿棒(つまり表面)上には少数の生存可能な黄色ブドウ球菌が存在していた可能性が高いが、それらの細胞は固体培地に移行しなかったことを示している。しかしながら、コーティングされたサンプルは、プレートアッセイと同一の増殖パターンを示した(図29)。これらのデータを総合すると、黄色ブドウ球菌は、コーティングされていない構造化サンプルでは完全に根絶できないが、レーザー再構築表面とCuOコーティングの組み合わせによって完全に根絶できることが示された。
特定の構造およびコーティングパターンが図示されているが、本開示は図示された実施形態に限定されるものではない。レーザー再構築またはテクスチャリングにより、抗菌性/薬剤溶出コーティングの効果が最大限に発揮されるように表面が構成されており、例えば、コーティングを保護、またはコーティングの露出/放出を遅延させるような、ポケットまたは棚(ledges)を有している。この構造はまた、複数のコーティングまたは酸化物の混合物、もしくは多層コーティング材料が容易になるように構成することもできる。
コーティングは、例えば、物理蒸着法、化学蒸着法、原子層蒸着法など、様々な技術を利用して適用することができる。さらに、レーザー再構築は、コーティングを適用する前に行っても、後に行ってもよい。一例として、銀または銅などの金属コーティングを、コーティング技術を用いて表面に適用し、その後、酸素が豊富な環境でレーザー再構築を行って、レーザー再構築中に金属酸化物コーティングをその場で形成してもよい。
本発明のこれらおよび他の利点は、前述の明細書から当業者には明らかであろう。したがって、本発明の広範な発明概念から逸脱することなく、上述の実施形態に変更または修正を加え得ると、当業者に認識されるであろう。よって、本発明は、本明細書に記載された特定の実施形態に限定されるものではなく、特許請求の範囲に規定された本発明の範囲および精神の範囲内にある全ての変更および修正を含むことが意図されていると理解されたい。
Claims (20)
- 表面を有する基板構造体、ここで前記表面は、該表面に対して延びる少なくとも1つの突起および/または少なくとも1つの空隙を規定するように、レーザー処理されている;および
抗菌特性、抗微生物特性および/または薬剤溶出特性を有し、1つ以上の前記突起および/または前記空隙の表面部分内または該表面部分に沿って係合するように前記基板構造体に適用されたコーティング
を含む医療デバイス。 - 前記表面は、階層的レーザー再構築トポグラフィーを有する、請求項1に記載の医療デバイス。
- 表面トポグラフィーは、マイクロ突起から延びるナノ突起を含む、請求項2に記載の医療デバイス。
- 前記表面トポグラフィーは、前記マイクロ突起が延びるマクロ突起によってさらに規定される、請求項3に記載の医療デバイス。
- 前記コーティングは、前記表面の全体に沿って適用されている、請求項1に記載の医療デバイス。
- 前記コーティングは、原子レベルで薄い厚さを有する、請求項1に記載の医療デバイス。
- 前記コーティングは、亜鉛、銅および/または銀を含む、請求項1に記載の医療デバイス。
- 前記コーティングはCuxOを含む、請求項1に記載の医療デバイス。
- 前記コーティングは蒸着プロセスを利用して適用される、請求項1に記載の医療デバイス。
- 前記コーティングは原子層堆積プロセス(ALD)を利用して適用される、請求項1に記載の医療デバイス。
- 前記コーティングは、プラズマ強化ALDまたは熱ALDを利用して適用される、請求項10に記載の医療デバイス。
- 前記基板構造体は、白金、鋼、白金-イリジウム合金、ニッケル-コバルト合金、チタン、チタン合金、タンタル、またはそれらの組み合わせを含む、請求項1に記載の医療デバイス。
- 表面を有する基板構造体を有する医療デバイスの製造方法であって、
前記表面をレーザー処理して、前記表面に対して延びる少なくとも1つの突起および/または少なくとも1つの空隙を規定する、レーザー処理工程と、
抗菌特性、抗微生物特性および/または薬剤溶出特性を有するコーティングを前記基板構造体に適用して、1つ以上の前記突起および/または前記空隙の表面部分内または該表面部分に沿って係合する、コーティング適用工程と、
を含む、医療デバイスの製造方法。
前記表面は、階層的レーザー再構築トポグラフィーを有する、請求項1に記載の医療デバイス。 - 前記表面は、階層的レーザー再構築トポグラフィーを有する、請求項13に記載の方法。
- 前記コーティングは、前記表面の全体に沿って適用される、請求項13に記載の方法。
- 前記コーティングは、原子レベルで薄い厚さを有する、請求項13に記載の方法。
- 前記コーティングは、亜鉛、銅および/または銀を含む、請求項13に記載の方法。
- 前記コーティングは蒸着プロセスを利用して適用される、請求項13に記載の方法。
- 前記コーティングは原子層堆積プロセス(ALD)を利用して適用される、請求項18に記載の方法。
- 前記コーティングは、プラズマ強化ALDまたは熱ALDを利用して適用される、請求項19に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202163254752P | 2021-10-12 | 2021-10-12 | |
| US63/254,752 | 2021-10-12 | ||
| PCT/US2022/046272 WO2023064267A1 (en) | 2021-10-12 | 2022-10-11 | Devices with improved antibacterial surface |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2024538136A true JP2024538136A (ja) | 2024-10-18 |
| JPWO2023064267A5 JPWO2023064267A5 (ja) | 2025-10-20 |
| JP2024538136A5 JP2024538136A5 (ja) | 2025-10-20 |
Family
ID=85798801
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024522570A Pending JP2024538136A (ja) | 2021-10-12 | 2022-10-11 | 改善された抗菌表面を有するデバイス |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20230111815A1 (ja) |
| EP (1) | EP4415772A4 (ja) |
| JP (1) | JP2024538136A (ja) |
| AU (1) | AU2022363516A1 (ja) |
| CA (1) | CA3234251A1 (ja) |
| IL (1) | IL312021A (ja) |
| WO (1) | WO2023064267A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20240387791A1 (en) * | 2021-08-25 | 2024-11-21 | Industry Academic Cooperation Foundation Of Yeungnam University | Electrode, method for preparing same, and electrostatic discharge system comprising same |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6582715B1 (en) * | 1999-04-27 | 2003-06-24 | Agion Technologies, Inc. | Antimicrobial orthopedic implants |
| US20050266039A1 (en) * | 2004-05-27 | 2005-12-01 | Jan Weber | Coated medical device and method for making the same |
| US20070135699A1 (en) * | 2005-12-12 | 2007-06-14 | Isense Corporation | Biosensor with antimicrobial agent |
| US9117680B2 (en) * | 2013-12-20 | 2015-08-25 | Pulse Technologies Inc. | Biomedical electrode |
| US10610621B2 (en) * | 2017-03-21 | 2020-04-07 | International Business Machines Corporation | Antibacterial medical implant surface |
-
2022
- 2022-10-11 IL IL312021A patent/IL312021A/en unknown
- 2022-10-11 US US17/963,653 patent/US20230111815A1/en active Pending
- 2022-10-11 CA CA3234251A patent/CA3234251A1/en active Pending
- 2022-10-11 EP EP22881650.0A patent/EP4415772A4/en active Pending
- 2022-10-11 JP JP2024522570A patent/JP2024538136A/ja active Pending
- 2022-10-11 WO PCT/US2022/046272 patent/WO2023064267A1/en not_active Ceased
- 2022-10-11 AU AU2022363516A patent/AU2022363516A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| EP4415772A4 (en) | 2025-08-20 |
| CA3234251A1 (en) | 2023-04-20 |
| EP4415772A1 (en) | 2024-08-21 |
| IL312021A (en) | 2024-06-01 |
| AU2022363516A1 (en) | 2024-05-02 |
| US20230111815A1 (en) | 2023-04-13 |
| WO2023064267A1 (en) | 2023-04-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101177104B1 (ko) | 항미생물성의 조합된 물질 | |
| EP0641224B1 (en) | Anti-microbial coating for medical devices | |
| EP0729302B1 (en) | Anti-microbial materials | |
| AU703141B2 (en) | Anti-microbial materials | |
| US5837275A (en) | Anti-microbial materials | |
| CN101790596B (zh) | 制备金属氧化物涂覆的具有可预定疏水行为的工件表面的方法 | |
| US20050003019A1 (en) | Ionic plasma deposition of anti-microbial surfaces and the anti-microbial surfaces resulting therefrom | |
| US20110046747A1 (en) | Antibacterial surface and method of fabrication | |
| Cazalini et al. | Antimicrobial and anti-biofilm properties of polypropylene meshes coated with metal-containing DLC thin films | |
| Hegemann et al. | Plasma‐deposited AgOx‐doped TiOx coatings enable rapid antibacterial activity based on ROS generation | |
| Khosla et al. | Development of antibacterial neural stimulation electrodes via hierarchical surface restructuring and atomic layer deposition | |
| JP2024538136A (ja) | 改善された抗菌表面を有するデバイス | |
| ITRM20110438A1 (it) | Procedimento per la realizzazione via plasma di rivestimenti di spessore nanometrico che permettano il rilascio controllato di ioni argento o di altri elementi, o di molecole di interesse biomedico, da prodotti solidi, e prodotti cosi rivestiti. | |
| RU2167526C2 (ru) | Антимикробные материалы | |
| EP0875146A1 (en) | Anti-microbial materials | |
| EP3432941A1 (de) | Implantatkörper mit wirkstoffträgerschicht und abgabekontrollschicht | |
| Jakubowski et al. | Multifunctional cerium-tetracycline coating for titanium implants: A dual approach to antibacterial and corrosion resistance | |
| Kasi et al. | Cold atmospheric plasma-assisted deposition of ammonium functionalized glass coatings for enhanced antibacterial properties | |
| CN120022417A (zh) | 具有pH响应控释功能的纳米管涂层及其制备方法和应用 | |
| Hsieh et al. | A combinatorial hollow cathode discharge/plasma polymerization system for silver containing plasma parylene coating | |
| Zheng et al. | TiCu-CMC/PDA coatings with long-term antimicrobial activity and cytocompatibility for surface engineering of implants | |
| AU731730B2 (en) | Process for producing anti-microbial effect with complex silver ions | |
| US20200061242A1 (en) | Ta2o5 and ta2o5 - tio2 hybrid surfaces for invasive surgical devices | |
| RO132032B1 (ro) | Procedeu de acoperire antibacteriană a unei suprafeţe dintr-un aliaj ternar de titan prin metoda sonochimică | |
| AU731732B2 (en) | Anti-microbial materials |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20251009 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20251009 |