JP2021526793A - 魚類からの外部寄生虫類の除去処理 - Google Patents
魚類からの外部寄生虫類の除去処理 Download PDFInfo
- Publication number
- JP2021526793A JP2021526793A JP2020567594A JP2020567594A JP2021526793A JP 2021526793 A JP2021526793 A JP 2021526793A JP 2020567594 A JP2020567594 A JP 2020567594A JP 2020567594 A JP2020567594 A JP 2020567594A JP 2021526793 A JP2021526793 A JP 2021526793A
- Authority
- JP
- Japan
- Prior art keywords
- fish
- neonicotinoid
- ectoparasite
- minutes
- ppm
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 241000251468 Actinopterygii Species 0.000 title claims abstract description 152
- 244000078703 ectoparasite Species 0.000 title claims abstract description 129
- 241001674048 Phthiraptera Species 0.000 claims abstract description 160
- 239000005906 Imidacloprid Substances 0.000 claims abstract description 95
- YWTYJOPNNQFBPC-UHFFFAOYSA-N imidacloprid Chemical compound [O-][N+](=O)\N=C1/NCCN1CC1=CC=C(Cl)N=C1 YWTYJOPNNQFBPC-UHFFFAOYSA-N 0.000 claims abstract description 95
- 229940056881 imidacloprid Drugs 0.000 claims abstract description 95
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 61
- 238000000034 method Methods 0.000 claims abstract description 44
- 241000973618 Labroides dimidiatus Species 0.000 claims abstract description 8
- 241001507086 salmonid fish Species 0.000 claims abstract description 5
- 238000011282 treatment Methods 0.000 claims description 121
- 150000003839 salts Chemical class 0.000 claims description 21
- 150000002148 esters Chemical class 0.000 claims description 20
- PGOOBECODWQEAB-UHFFFAOYSA-N (E)-clothianidin Chemical compound [O-][N+](=O)\N=C(/NC)NCC1=CN=C(Cl)S1 PGOOBECODWQEAB-UHFFFAOYSA-N 0.000 claims description 19
- 239000005888 Clothianidin Substances 0.000 claims description 19
- 239000005871 repellent Substances 0.000 claims description 18
- 230000002940 repellent Effects 0.000 claims description 18
- YKBZOVFACRVRJN-UHFFFAOYSA-N dinotefuran Chemical compound [O-][N+](=O)\N=C(/NC)NCC1CCOC1 YKBZOVFACRVRJN-UHFFFAOYSA-N 0.000 claims description 16
- NWWZPOKUUAIXIW-FLIBITNWSA-N thiamethoxam Chemical compound [O-][N+](=O)\N=C/1N(C)COCN\1CC1=CN=C(Cl)S1 NWWZPOKUUAIXIW-FLIBITNWSA-N 0.000 claims description 16
- 239000005941 Thiamethoxam Substances 0.000 claims description 15
- CFRPSFYHXJZSBI-DHZHZOJOSA-N (E)-nitenpyram Chemical compound [O-][N+](=O)/C=C(\NC)N(CC)CC1=CC=C(Cl)N=C1 CFRPSFYHXJZSBI-DHZHZOJOSA-N 0.000 claims description 14
- 229940079888 nitenpyram Drugs 0.000 claims description 14
- 239000000203 mixture Substances 0.000 claims description 11
- -1 acetoamiprid Chemical compound 0.000 claims description 7
- LZTIMERBDGGAJD-SNAWJCMRSA-N (2e)-2-(nitromethylidene)-1,3-thiazinane Chemical compound [O-][N+](=O)\C=C1/NCCCS1 LZTIMERBDGGAJD-SNAWJCMRSA-N 0.000 claims description 5
- HOKKPVIRMVDYPB-UVTDQMKNSA-N (Z)-thiacloprid Chemical compound C1=NC(Cl)=CC=C1CN1C(=N/C#N)/SCC1 HOKKPVIRMVDYPB-UVTDQMKNSA-N 0.000 claims description 4
- 239000005940 Thiacloprid Substances 0.000 claims description 4
- 230000024241 parasitism Effects 0.000 claims description 3
- WCXDHFDTOYPNIE-RIYZIHGNSA-N (E)-acetamiprid Chemical compound N#C/N=C(\C)N(C)CC1=CC=C(Cl)N=C1 WCXDHFDTOYPNIE-RIYZIHGNSA-N 0.000 claims description 2
- 239000005875 Acetamiprid Substances 0.000 claims description 2
- 231100000518 lethal Toxicity 0.000 abstract description 6
- 230000001665 lethal effect Effects 0.000 abstract description 6
- 235000019688 fish Nutrition 0.000 description 146
- 239000013535 sea water Substances 0.000 description 27
- 238000012360 testing method Methods 0.000 description 27
- 244000045947 parasite Species 0.000 description 22
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 16
- 241000972773 Aulopiformes Species 0.000 description 15
- 238000012545 processing Methods 0.000 description 15
- 230000009257 reactivity Effects 0.000 description 15
- 235000019515 salmon Nutrition 0.000 description 14
- 238000003197 gene knockdown Methods 0.000 description 13
- 230000000694 effects Effects 0.000 description 12
- 230000008855 peristalsis Effects 0.000 description 12
- 239000000243 solution Substances 0.000 description 12
- 239000005892 Deltamethrin Substances 0.000 description 11
- 229960002483 decamethrin Drugs 0.000 description 11
- OWZREIFADZCYQD-NSHGMRRFSA-N deltamethrin Chemical compound CC1(C)[C@@H](C=C(Br)Br)[C@H]1C(=O)O[C@H](C#N)C1=CC=CC(OC=2C=CC=CC=2)=C1 OWZREIFADZCYQD-NSHGMRRFSA-N 0.000 description 11
- 208000005392 Spasm Diseases 0.000 description 10
- 241001465754 Metazoa Species 0.000 description 9
- VNKBTWQZTQIWDV-UHFFFAOYSA-N azamethiphos Chemical compound C1=C(Cl)C=C2OC(=O)N(CSP(=O)(OC)OC)C2=N1 VNKBTWQZTQIWDV-UHFFFAOYSA-N 0.000 description 9
- 208000007101 Muscle Cramp Diseases 0.000 description 8
- 230000002147 killing effect Effects 0.000 description 8
- 230000000968 intestinal effect Effects 0.000 description 7
- 241001611011 Caligus Species 0.000 description 6
- 208000015181 infectious disease Diseases 0.000 description 6
- 238000011084 recovery Methods 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 238000005273 aeration Methods 0.000 description 5
- 238000011156 evaluation Methods 0.000 description 5
- 229920003023 plastic Polymers 0.000 description 5
- 241000269951 Labridae Species 0.000 description 4
- 241001266066 Ligia exotica Species 0.000 description 4
- 241000277331 Salmonidae Species 0.000 description 4
- 230000006399 behavior Effects 0.000 description 4
- 238000001727 in vivo Methods 0.000 description 4
- 230000001965 increasing effect Effects 0.000 description 4
- 239000002917 insecticide Substances 0.000 description 4
- 239000013642 negative control Substances 0.000 description 4
- 239000004033 plastic Substances 0.000 description 4
- 235000019512 sardine Nutrition 0.000 description 4
- 230000009182 swimming Effects 0.000 description 4
- PGOOBECODWQEAB-FIBGUPNXSA-N 2-[(2-chloro-1,3-thiazol-5-yl)methyl]-1-nitro-3-(trideuteriomethyl)guanidine Chemical group [2H]C([2H])([2H])NC(N[N+]([O-])=O)=NCC1=CN=C(Cl)S1 PGOOBECODWQEAB-FIBGUPNXSA-N 0.000 description 3
- QMEQBOSUJUOXMX-UHFFFAOYSA-N 2h-oxadiazine Chemical compound N1OC=CC=N1 QMEQBOSUJUOXMX-UHFFFAOYSA-N 0.000 description 3
- OEDUIFSDODUDRK-UHFFFAOYSA-N 5-phenyl-1h-pyrazole Chemical compound N1N=CC=C1C1=CC=CC=C1 OEDUIFSDODUDRK-UHFFFAOYSA-N 0.000 description 3
- 241000239250 Copepoda Species 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 241000238631 Hexapoda Species 0.000 description 3
- 241000277263 Salmo Species 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 238000009360 aquaculture Methods 0.000 description 3
- 244000144974 aquaculture Species 0.000 description 3
- 230000003542 behavioural effect Effects 0.000 description 3
- 238000011284 combination treatment Methods 0.000 description 3
- 230000008602 contraction Effects 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 230000002496 gastric effect Effects 0.000 description 3
- 210000003128 head Anatomy 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- 206010002091 Anaesthesia Diseases 0.000 description 2
- 241001213700 Benthosema panamense Species 0.000 description 2
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 2
- 241000555825 Clupeidae Species 0.000 description 2
- 241000556575 Eleginops maclovinus Species 0.000 description 2
- 206010061217 Infestation Diseases 0.000 description 2
- 241001247234 Lepeophtheirus salmonis Species 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 208000030852 Parasitic disease Diseases 0.000 description 2
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 2
- 241001125048 Sardina Species 0.000 description 2
- 241000555745 Sciuridae Species 0.000 description 2
- 230000037005 anaesthesia Effects 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- 239000002246 antineoplastic agent Substances 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- VEMKTZHHVJILDY-UXHICEINSA-N bioresmethrin Chemical compound CC1(C)[C@H](C=C(C)C)[C@H]1C(=O)OCC1=COC(CC=2C=CC=CC=2)=C1 VEMKTZHHVJILDY-UXHICEINSA-N 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 230000006835 compression Effects 0.000 description 2
- 238000007906 compression Methods 0.000 description 2
- 229940127089 cytotoxic agent Drugs 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 230000007613 environmental effect Effects 0.000 description 2
- 238000007654 immersion Methods 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 230000003902 lesion Effects 0.000 description 2
- 231100000636 lethal dose Toxicity 0.000 description 2
- 238000007477 logistic regression Methods 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 210000000214 mouth Anatomy 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 230000036281 parasite infection Effects 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- HYJYGLGUBUDSLJ-UHFFFAOYSA-N pyrethrin Natural products CCC(=O)OC1CC(=C)C2CC3OC3(C)C2C2OC(=O)C(=C)C12 HYJYGLGUBUDSLJ-UHFFFAOYSA-N 0.000 description 2
- 239000002728 pyrethroid Substances 0.000 description 2
- 238000007789 sealing Methods 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 239000012085 test solution Substances 0.000 description 2
- SNICXCGAKADSCV-JTQLQIEISA-N (-)-Nicotine Chemical compound CN1CCC[C@H]1C1=CC=CN=C1 SNICXCGAKADSCV-JTQLQIEISA-N 0.000 description 1
- 241000239267 Arguloida Species 0.000 description 1
- 241000271566 Aves Species 0.000 description 1
- 241000693349 Centrolabrus exoletus Species 0.000 description 1
- 241000693339 Ctenolabrus Species 0.000 description 1
- 241000544061 Cuculus canorus Species 0.000 description 1
- 241000276603 Cyclopteridae Species 0.000 description 1
- 241000276604 Cyclopterus Species 0.000 description 1
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 1
- 240000001973 Ficus microcarpa Species 0.000 description 1
- 235000004036 Glehnia littoralis Nutrition 0.000 description 1
- 244000146486 Glehnia littoralis Species 0.000 description 1
- 241000556695 Labrus bergylta Species 0.000 description 1
- 241001135786 Lactobacillus cerevisiae Species 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 241000133262 Nauplius Species 0.000 description 1
- 102000019315 Nicotinic acetylcholine receptors Human genes 0.000 description 1
- 108050006807 Nicotinic acetylcholine receptors Proteins 0.000 description 1
- 206010034133 Pathogen resistance Diseases 0.000 description 1
- VQXSOUPNOZTNAI-UHFFFAOYSA-N Pyrethrin I Natural products CC(=CC1CC1C(=O)OC2CC(=O)C(=C2C)CC=C/C=C)C VQXSOUPNOZTNAI-UHFFFAOYSA-N 0.000 description 1
- 238000006178 Rupe rearrangement reaction Methods 0.000 description 1
- 241000693337 Symphodus melops Species 0.000 description 1
- VXSIXFKKSNGRRO-MXOVTSAMSA-N [(1s)-2-methyl-4-oxo-3-[(2z)-penta-2,4-dienyl]cyclopent-2-en-1-yl] (1r,3r)-2,2-dimethyl-3-(2-methylprop-1-enyl)cyclopropane-1-carboxylate;[(1s)-2-methyl-4-oxo-3-[(2z)-penta-2,4-dienyl]cyclopent-2-en-1-yl] (1r,3r)-3-[(e)-3-methoxy-2-methyl-3-oxoprop-1-enyl Chemical class CC1(C)[C@H](C=C(C)C)[C@H]1C(=O)O[C@@H]1C(C)=C(C\C=C/C=C)C(=O)C1.CC1(C)[C@H](/C=C(\C)C(=O)OC)[C@H]1C(=O)O[C@@H]1C(C)=C(C\C=C/C=C)C(=O)C1 VXSIXFKKSNGRRO-MXOVTSAMSA-N 0.000 description 1
- 210000001015 abdomen Anatomy 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 230000003444 anaesthetic effect Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 229940124339 anthelmintic agent Drugs 0.000 description 1
- 239000000921 anthelmintic agent Substances 0.000 description 1
- 210000000436 anus Anatomy 0.000 description 1
- 238000011888 autopsy Methods 0.000 description 1
- 238000003287 bathing Methods 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 239000003139 biocide Substances 0.000 description 1
- 239000003124 biologic agent Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N carbonic acid monoamide Natural products NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 238000000586 desensitisation Methods 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 238000004299 exfoliation Methods 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 230000004634 feeding behavior Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 210000003953 foreskin Anatomy 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 210000002816 gill Anatomy 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 231100001231 less toxic Toxicity 0.000 description 1
- 231100000225 lethality Toxicity 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000001325 log-rank test Methods 0.000 description 1
- 229920001684 low density polyethylene Polymers 0.000 description 1
- 239000004702 low-density polyethylene Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 210000002050 maxilla Anatomy 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 230000004899 motility Effects 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 229960002715 nicotine Drugs 0.000 description 1
- SNICXCGAKADSCV-UHFFFAOYSA-N nicotine Natural products CN1CCCC1C1=CC=CN=C1 SNICXCGAKADSCV-UHFFFAOYSA-N 0.000 description 1
- 231100000957 no side effect Toxicity 0.000 description 1
- 210000000287 oocyte Anatomy 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 239000005416 organic matter Substances 0.000 description 1
- 238000006213 oxygenation reaction Methods 0.000 description 1
- 231100000915 pathological change Toxicity 0.000 description 1
- 230000036285 pathological change Effects 0.000 description 1
- 239000000575 pesticide Substances 0.000 description 1
- 231100000572 poisoning Toxicity 0.000 description 1
- 230000000607 poisoning effect Effects 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 238000002203 pretreatment Methods 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 150000003217 pyrazoles Chemical class 0.000 description 1
- VJFUPGQZSXIULQ-XIGJTORUSA-N pyrethrin II Chemical compound CC1(C)[C@H](/C=C(\C)C(=O)OC)[C@H]1C(=O)O[C@@H]1C(C)=C(C\C=C/C=C)C(=O)C1 VJFUPGQZSXIULQ-XIGJTORUSA-N 0.000 description 1
- 229940070846 pyrethrins Drugs 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 102000037983 regulatory factors Human genes 0.000 description 1
- 108091008025 regulatory factors Proteins 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 210000001991 scapula Anatomy 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000020509 sex determination Effects 0.000 description 1
- 235000015170 shellfish Nutrition 0.000 description 1
- 238000004088 simulation Methods 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 230000009897 systematic effect Effects 0.000 description 1
- KJAMZCVTJDTESW-UHFFFAOYSA-N tiracizine Chemical compound C1CC2=CC=CC=C2N(C(=O)CN(C)C)C2=CC(NC(=O)OCC)=CC=C21 KJAMZCVTJDTESW-UHFFFAOYSA-N 0.000 description 1
- 229940072040 tricaine Drugs 0.000 description 1
- FQZJYWMRQDKBQN-UHFFFAOYSA-N tricaine methanesulfonate Chemical compound CS([O-])(=O)=O.CCOC(=O)C1=CC=CC([NH3+])=C1 FQZJYWMRQDKBQN-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/14—Ectoparasiticides, e.g. scabicides
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N47/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid
- A01N47/40—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having a double or triple bond to nitrogen, e.g. cyanates, cyanamides
- A01N47/42—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having a double or triple bond to nitrogen, e.g. cyanates, cyanamides containing —N=CX2 groups, e.g. isothiourea
- A01N47/44—Guanidine; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K61/00—Culture of aquatic animals
- A01K61/10—Culture of aquatic animals of fish
- A01K61/13—Prevention or treatment of fish diseases
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/18—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids containing the group —CO—N<, e.g. carboxylic acid amides or imides; Thio analogues thereof
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/34—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom
- A01N43/40—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom six-membered rings
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/86—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms six-membered rings with one nitrogen atom and either one oxygen atom or one sulfur atom in positions 1,3
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/88—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms six-membered rings with three ring hetero atoms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N47/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid
- A01N47/40—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having a double or triple bond to nitrogen, e.g. cyanates, cyanamides
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N51/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds having the sequences of atoms O—N—S, X—O—S, N—N—S, O—N—N or O-halogen, regardless of the number of bonds each atom has and with no atom of these sequences forming part of a heterocyclic ring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61D—VETERINARY INSTRUMENTS, IMPLEMENTS, TOOLS, OR METHODS
- A61D7/00—Devices or methods for introducing solid, liquid, or gaseous remedies or other materials into or onto the bodies of animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/34—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having five-membered rings with one oxygen as the only ring hetero atom, e.g. isosorbide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/426—1,3-Thiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines having two or more nitrogen atoms in the same ring, e.g. oxadiazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F3/00—Biological treatment of water, waste water, or sewage
- C02F3/32—Biological treatment of water, waste water, or sewage characterised by the animals or plants used, e.g. algae
- C02F3/327—Biological treatment of water, waste water, or sewage characterised by the animals or plants used, e.g. algae characterised by animals and plants
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Wood Science & Technology (AREA)
- Dentistry (AREA)
- Plant Pathology (AREA)
- Pest Control & Pesticides (AREA)
- Agronomy & Crop Science (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Biodiversity & Conservation Biology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Hydrology & Water Resources (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Animal Husbandry (AREA)
- Marine Sciences & Fisheries (AREA)
- Biotechnology (AREA)
- Botany (AREA)
- Microbiology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Environmental & Geological Engineering (AREA)
- Water Supply & Treatment (AREA)
- Farming Of Fish And Shellfish (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Meat, Egg Or Seafood Products (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
(i) 水の試料を採取する工程;
(ii) 前記試料から前記外部寄生虫を採取する工程;
を含む方法を提供する。
好ましくは、ネオニコチノイドは浸水投与用に構成又は処方される。
以下、添付の図面を参照して、本発明を例示する:
1.1.船虫チャレンジ
各々15匹の魚を入れた8基の流水処理槽を設置した。魚は平均体重約270g、性別は混在するサケ(Salmo salar)である。
卵性メスLepeophtheirus salmonisから採取した卵糸を採取し、感染性のコペポダイドが産生されるまで培養した。およそ330〜350個のコペポダイドを含む8本のボトルを、それぞれ無作為に処理タンクに割り付けた(魚当たり平均22匹のシラミを得るために)。
チャレンジに備えて、タンク内の水流を停止し、光レベルを低下させた。次いで、シラミを各タンクに添加し、タンクを6時間完全暗所に維持した後、光レベルを上昇させ、水流を再開した。
魚に1週間又は6週間、船虫を接種した。
1.2.1 1週間投与後の処理
船虫チャレンジから1週間後、3つのタンクの魚を10ppm w/v、30ppm w/v、又は50ppm w/vのイミダクロプリドで処理した。一方のタンクは0.03% DMSOで処理し、もう一方のタンクは対照として海水で処理した。
各処理タンクについて、適当な量のイミダクロプリド(表1参照)を100mlのDMSOに溶解し、実験タンクからの約900mlの海水と混合して処理溶液を得た。実験用タンクの水流を遮断し、処理液を添加した。
魚は、60分間、全曝気の静水中で曝露され、曝露期間中に観察された。曝露期間の終了時には、水は約1/3の容量に急速に排水され、その後、タンク内で流れが再開された。
表1
6週間後に、残りの3つの処理タンクの魚を10ppm w/v、30ppm w/v、又は50ppm w/vのイミダクロプリドで処理した。処理は、惹起1週間後の処理用タンクと同様に行った(1.2.1参照)。各処理槽に添加したイミダクロプリドの量を表1に示す。
イミダクロプリド添加2〜6分後の観察では、50ppm w/v投与群の水柱にシラミは認められなかった。
12分間の処理後、約10匹のシラミが宿主から分離され、水柱中に遊離したことが観察された。18分間の処理後、約20匹のシラミが水柱で観察された。当該シラミの活発な運動は記録されなかった。イミダクロプリド添加の44分後、シラミはタンクの底部に不活性で残存残していることが認められた。さらに、感染した魚はわずか5匹で、各々1匹のシラミであった。イミダクロプリド添加53分後、2〜3匹の魚のみが単一のシラミ感染をおこしたようだ。イミダクロプリド添加58分後、1匹の魚に1匹のシラミのみが認められた。イミダクロプリド添加81分後、魚にシラミは認められなかった。
投与2日後、シラミの摂食及び付着に関連する病変はほぼ完全に消失したことが認められた。
添加10分後にイミダクロプリド30ppm w/vで処理した魚を入れたタンクの水柱では、約1〜2匹のシラミが観察された。添加18分後、約10匹のシラミが水柱に存在した。添加25分後、水中に約20匹のシラミが認められ、6匹未満の魚が1匹あたり推定1〜2匹のシラミに感染したようだ。イミダクロプリドの添加33分後、ほとんどの魚はシラミ感染に対して陰性であると考えられた。宿主から隔離されたシラミはすべて不動であった。添加47分後、3匹の魚のみが感染しているようであり、各々1匹のシラミがいた。イミダクロプリド添加59分後、シラミに明らかに感染した魚はいなかった。イミダクロプリド添加78分後、4匹の魚に4匹のシラミが付着し、4匹の魚に1匹のシラミが観察された。6分後、これらの魚ではシラミは観察されず、タンク内のシラミはすべて不動であった。
投与2日後、シラミの摂食及び付着に関連する病変はほぼ完全に消失したことが認められた。
イミダクロプリド添加後の最初の19分以内に水柱でシラミは観察されなかった。添加後21日目、いくつかのシラミが水柱で活発に泳ぐのが観察された。4分後、これらのシラミの大部分は不動であった。添加54分後、2匹の感染魚が認められ、各々1匹の卵性メスが寄生していた。添加86分後、単一メスシラミが宿主から分離されたのが観察された。直接観察されなかったが、残りの卵性メスは、宿主から隔離されたことが認められた。添加91分後、単一のオスシラミが宿主の頭部で観察された。このシラミは処理後少なくとも5日間宿主で観察された。
魚に船虫を投与してから8週間後に試験を中止した。魚をMS222(トリカインメタンスルホン酸)で麻酔し、Iki Jimeツールを用いてピッチングした。各魚の体長、体重、外表症状を記録した。すべてのシラミを各々の魚から除去し、性別と発育段階を記録した。シラミをエタノール及び性別で保存し、ステージを実体顕微鏡で確認した。
表2
2.1 船虫チャレンジ
120匹のサケ(Salmo salar)を5つの流水処理槽に分割し、寄生虫誘発前に24時間馴化した。
卵性メスLepeophtheirus salmonisから採取した卵糸を採取し、感染性のコペポダイドが産生されるまで培養した。その後、コペポダイドを海水の入った5本の瓶に均等に分配し、〜10℃で一晩保存した。
惹起に備えて、処理槽内の水流を停止し、光レベルを低下させた。650 静水に±20種のコペポダイド(宿主当たり約27種)を添加し、タンクを7時間完全暗所に維持した後、光レベルを上昇させ、水流を再開した。
表3に示すように、魚を無作為に10匹ずつ10群に分け、30 Lの水と高曝気を含む静止した「処理バケツ」に入れた。
表3
実験動物は、副作用及び寄生虫感染の状態について注意深く追跡した。可能なかぎり、すべての寄生虫が隔離されたと考えられる時間を記録した。処理は静止系で行われたので、温度と溶存酸素を手順全体を通して定期的にモニターし、必要に応じてエアレーションを調整した。
4種類の処理濃度10、15、20及び25mg/Lのイミダクロプリドと0.03%のDMSO濃度を組み合わせたシラミの総除去率を表4及び図1に示す(n=2、t=60分、エラーバーは±SEMを示す)。
表4
ロジスティック回帰を用いて、各濃度で処理後の寄生虫クリアランスを比較した。ロジスティック回帰分析は、R.v.2.13.0のglm関数を用いて行い、二項分布又は準二項分布(帰無偏差と自由度の比較により決定)を仮定した。
イミダクロプリド10mg/Lに曝露された船虫は、30mg/Lに曝露されたシラミと比較して、宿主から落下するのに時間がかかるようであった。
濃度と影響時間との関係を定量するために、20匹の宿主動物をイミダクロプリド10mg/L又は20mg/L(10匹/濃度)のいずれかの処理濃度に無作為に割り付けた。速度決定試験のロジスティックスは、本質的には相対的有効性試験と同じであったが、例外として、魚を処理液から除去し、寄生虫の総クリアランスが生じたらすぐに安楽死させ、手順及び関連する福祉的考慮のもと時間を最小限にすることができた。
イミダクロプリドを10mg/L及び20mg/Lで処理すると、宿主からの寄生虫の総クリアランスがもたらされた。実験動物を処理の間中厳密にモニターし、総クリアランスまでの時間を最も近い分まで記録した。この事象は実験エンドポイントを表しており、この時点で動物を摘出し、安楽死させた。
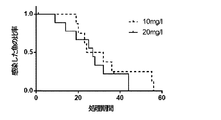
生存分析を用いて、寄生虫クリアランスまでの時間が10mg/Lと20mg/Lの間で有意差があるかどうかを決定した。図2は、Kaplan−Meierグラフで速度を視覚的に表し、Mantel−Cox(ログランク検定)は、両者間に有意差がないと判定する(p=0.48、n=10、t≦56分)。その結果、イミダクロプリドの濃度は寄生虫クリアランスまでの時間に影響を及ぼさず、致死時間50%(LT50)は約27.5分と推定された。
相対的有効性試験(2.2参照)のサンプリング時点で、多数の寄生者が宿主に付着したままであった(10mg/Lに曝露した人の20%、15及び20mg/Lに曝露した人の8%、25mg/Lに曝露した人の3%)。
イミダクロプリドに曝露した寄生虫(宿主の処理後に手動で除去した寄生虫及び処理中に剥離した寄生虫)の相対的有効性及び速度決定試験の双方から、清浄な海水に浸漬し、回復の兆候を観察した。
最初の観察時に、曝露された個体が死滅しているか、あるいは活動的であることが確認された。なお活動的な個体のうち、筋興奮は協調不能、コントロール不能、制限されていた。これらの個体は明らかに基本的な機能(宿主への付着と標的への移動)を果たすことができなかったことから、処理後も宿主に付着したままであった寄生虫は、その後下流に移動した可能性が示唆された。
曝露後の期間(最長6時間)では、どの濃度のイミダクロプリドに曝露した寄生虫にも、明らかな機能回復の徴候は認められなかった。
処理対象のサケを標準的な養殖ケージに混ぜ、ウェルボートの酸素添加したウェルにポンプで注入し、各ウェルの魚の密度を水1立方メートルあたり90kg又は120kgとした。予混合イミダクロプリドをウェルに20ppm w/vの用量まで添加した。その後、魚を60分間処理した。処理期間の終了時に、魚をウェルから揚水し、脱水して、処理水を確実にウェルに戻す。これを行うために、魚を格子状の棒状の上を通過させ、未処理の海水で洗い流して、魚の外側に残った処理水を取り除いた後、海洋ペンに戻した。使用後はすべての洗流水を保持した。
約50μm又は約150μmのメッシュサイズのメッシュフィルタに水を通して、瀕死及び死んだ船虫及びそれらの卵弦を含む有機物を除去した。
L.salmonis及びCaligus属の感染の成体前及び成体期に対するイミダクロプリドの有効性を、イミダクロプリドによる処理を受けているサケについて、処理前及び処理後の船虫数を測定することにより調べた。本試験は、ノルウェーの市販のサケ水槽で実施された。サケをウェルボートにポンプで注入し、20ppmのイミダクロプリドに60分間曝露した。サケの平均体重は3.5kgで、水槽当たりの平均サケの数は18万匹であった。L.salmonis及びCaligus属について水槽当たり30匹の魚を評価し、見つかったL.salmonisの各ライフステージの数を記録した。投与前24時間以内、投与後24時間以内に実施した。
これらの評価は、合計4頭のサケ水槽で行った。処理に先立ち、魚は、処理前の船虫評価が行われたウェルボートに送り込まれるように、水槽内で密な状態であった。処理後のシラミの評価は、ウェルボートの流出管から魚を取り除くことによって行った。
いずれの時点においても、3匹の魚を採取し、麻酔浴に入れた。これを30匹の魚が評価されるまで10回繰り返した。
試験に供した4つの水槽各々について、試験前又は投与後の活性シラミのライフサイクルの状態に応じて、本試験で魚当たりに観察されたシラミの数を表5に示す。いずれの魚も投与期間中観察されたが、有害な行動は認められなかった。
表5−処理前の船虫数
イミダクロプリドの効果の時間スケールを決定するために、成体前及び成体前の船虫に感染したサケをストックタンクから取り出し、頭部に鋭い打撃を与えて殺傷した。魚をイミダクロプリド0、20、50、100、200、500ppmの存在下で30リットルの水に懸濁させ、船虫を30〜60分間観察し、宿主から分離するかどうか、いつ分離するかを観察した。
0ppmのイミダクロプリドに曝露した魚(陰性対照)では、60分間観察が行われた。500ppmのイミダクロプリドを60分間曝露した1匹の魚を除き、他の処理した魚はすべて30分間観察された。各投与群につき3匹の魚を試験した。
シラミが宿主から離れた時期、及び船虫の性と段階についての観察が認められた。宿主を離れたシラミはすぐに清浄な海水に移された。さらに、曝露期間終了時に宿主上に残っていたシラミは宿主から除去され、清浄な海水に移された。
メスオスのシラミの割合は約50:50であった。水温は12℃前後であった。
死んだ魚のシラミは、未処理の海水中に置かれ、60分間の観察期間を通して宿主を離れることはなく、いったんペトリ皿に移すと正常な動きを示した。これらの動きには、水泳や付属肢の典型的な制御された動きが含まれていた。
20〜200ppmのイミダクロプリドに曝露された群では、シラミの約50%が最初の15分以内に宿主を離れた。500ppmのイミダクロプリドに曝露した魚では、シラミの約70%が最初の9分以内に宿主を離れた。残りのシラミは曝露期間の終わりまで宿主に留まった。宿主上のシラミは処理中に甲殻状面の側方圧迫を受け、シラミのハンチバック様外観を生じた。
このように、大部分の船虫は15分以内に処理宿主から離れた。
オスシラミはメスに比べて宿主を離れる可能性が高いようであった。イミダクロプリドに曝露されたシラミは、通常、運動性の完全な喪失と付属肢の急速な攣縮を示した。メスシラミはオスよりも付属肢の運動が少なかったが、腸の蠕動運動を示した。
陰性対照−イミダクロプリドを投与されなかったシラミは、宿主から除去されたシラミに典型的な行動を示した。これには消化管の活発な遊泳と蠕動運動が含まれた。付属器の動きは系統的で制御されていると考えられた。シラミは物理的刺激に反応し、活発に移動した。
20mg/Lのイミダクロプリドに曝露された49匹のシラミのうち、2匹は曝露後30分で死滅したと考えられた(p.e.)。ピンセットで触れると、シラミはペトリ皿の側面から落ち、逆さまになって短時間泳いだ。しかし、遊泳は不安定で、大部分の付属肢の過剰な動きが原因であるように思われた。残りのシラミは、脚、第2上顎及び一次触角を含むそれらの付属肢の急速な攣縮を伴う瀕死状態と考えられた。20ppmのイミダクロプリドに30分間曝露したメスでは、腸管の蠕動が認められた。49例中12例は生きており、刺激なしに活発に泳いでいるとみなされた。30分間曝露したシラミは回復の兆候を示さなかった。
50ppmのイミダクロプリドに曝露された21匹のシラミのうち、4匹は30分後に死滅したと考えられた。主要な付属肢の攣縮が残りのシラミで認められたが、30分間曝露した2匹の成体メスでは蠕動が認められた。シラミ14匹を生後2時間に検査したが、運動は検出されず、死滅したとみなされた。2つの個体は1本の脚の攣縮を示し、4人の成体メスは腸の蠕動運動を示した。
100ppmのイミダクロプリドに曝露された28匹のシラミのうち、4匹は曝露期間終了時に死滅したと考えられた。シラミは典型的に二次触角と二次上顎骨の攣縮を示した。さらに11匹のシラミが腸の蠕動運動を示した。甲骨の側方圧迫が多数の個体で認められた。2時間後、17/28匹のシラミが死滅したとみなされた。消化管の蠕動運動は、2時間後にシラミ28匹中9匹で認められ、すべて成体メスであった。最後に、シラミの1本と他のシラミの脚4の触角は、2時間後に限定された攣縮運動を示した。
200ppmのイミダクロプリドに曝露された26匹のシラミのうち、4匹は曝露期間終了時に死滅したと考えられた。残りのシラミは、通常二次アンテナの攣縮を除いて動かず、4匹の成体メスシラミで腸の蠕動運動が認められた。1匹のシラミの肛門の捻転が午後30分に認められた。6匹のシラミが曝露2時間後に死滅したと考えられた。さらに、残りの動物では限定的な攣縮が記録され、主に成体メス3匹の一次及び二次触角の収縮と消化管の蠕動からなっていた。
20匹のシラミのうち6匹が、30分後に死滅したと考えられた。このうち2例は、2時間後に腸蠕動又は軽微な攣縮が認められたことが記録された。30分後に調べた残りのシラミは、1番目と2番目の触角が急速に収縮し、4匹の上顎脚がいくらか収縮し、腸の蠕動運動が認められた。生後2時間で、シラミの15/20が死滅したと考えられた。3匹のシラミは二次触角の攣縮を示し、2匹のシラミで消化管蠕動が記録された。
アザメチホス耐性及びデルタメトリン耐性の船虫とネオニコチノイドとの間に交差耐性がないことを確認するために試験を実施した。両性の成体前及び成体期(移動期)の両方を用い、それらは群間で均等に分布した。イミダクロプリドを60分間、アザメチホスを60分間、デルタメトリンを30分間、1リットルの浴中で一定の濃度範囲で曝露した(表6、7及び8)。シラミを処理後清浄な曝気海水に移した。実験中の海水の温度は12℃であったが、曝露中は60分間曝露(イミダクロプリド及びアザメチホス)で約14℃、30分間曝露(デルタメトリン)で13℃に上昇した。
各レジームにおいて、生シラミ及び固定(死んだものを含む)シラミの数は、曝露終了から約20時間後に記録された。各シラミを個別に調べた。
このインビトロ試験におけるイミダクロプリド、アザメチホス及びデルタメトリンの比例効果を表6、7及び8に示す。
表6−イミダクロプリドのシラミへの影響
インビボでのイミダクロプリド処理の濃度及び時間依存性を測定するために、アトランティックサーモン(平均320.9g)に海水(32.5%塩分)中のイミダクロプリドを12℃で負荷した。活性剤の投与中、タンク内の水位を下げ、エアレーションを行った。各チャレンジ時点で、チャレンジタンク中の魚当たり約40個のコペポダイドの目標レベルが得られるように、サケシラミのカイアシ培養物を計数し、調整した。
タンク水又はタンク壁に付着した解離シラミの数を記録した。タンク水中のシラミを採取し、処理直後及び30〜60分後に再度(回復の可能性を評価するために)平滑なプラスチック表面に吸引によって付着する能力について評価した。生きているシラミ及び生存可能なシラミも参考のために模擬処理対照群から採取し、システムを評価するために同期間、リバイバルチャンバーで飼育した。
魚の行動/外観は、各試験期間中にインビボで評価した。死滅率を含む行動及び/又は外観の変化を記録した。試験中に死滅した魚はなく、剖検も行われなかった。
保持タンクから3匹のシラミに感染した魚を無作為に集め、内側の区画(直径=34.5〜40cm、高さ=54cm)を形成する樽に注意深く操縦した。これはタンク内に沈められ、基部は9mm2の角穴を有するプラスチック製のメッシュスクリーンに置き換えられた。
各試験開始から3分以内に魚を内部コンパートメントに移した。内部コンパートメントは、処理を待つ間、保持タンク内に懸濁/浸漬された。
処理及び模擬処理は、魚で内部コンパートメントを排水し、試験液を入れた樽に移すことによって実施した。処理/模擬処理は、曝気/酸素化を伴う静水中で行った。酸素飽和度を70〜100%に設定するためにエアレーションを調整した。
処理浴中の残りのシラミを、清浄な海水で水浴中に懸濁させたプランクトンメッシュ(孔径2mm)を通して歪めた。このコレクター中のシラミをプラスチックビーカー(1リットル)に移し、次に再びリバイバルチューブ(直径5cm、長さ10cm)に移した。各試験終了後3分以内に処理槽又はビーカーの壁に付着できるシラミは、生菌数と判定した。壁に付着しなかったシラミを、再生チューブで30〜60分間モニターした。30〜60分後にリバイバルチューブで生存可能と思われるシラミとそうでないシラミは、別々のカテゴリーで採点した。
模擬処理対照は、同様の方法で行った。
各魚は処理前に1匹あたり平均11匹のシラミがいた。イミダクロプリドの曝露時間は3〜60分、用量は20〜200ppmであった。
試験中に死滅した魚はいなかった。
表9は、イミダクロプリド処理によって魚から除去されたシラミの割合を示している。
表9−イミダクロプリドによる入浴処理の結果
従って、イミダクロプリドは、処理時間を用いてシラミを除去するのに有効であった。
表10は、処理によって魚から切り離された船虫の割合と、処理中に付着したまま回収され、処理後30〜60分で活性化した船虫の割合を示したものである。
表10−船虫の復活率
表11−アザメチホス及びデルタメトリンによる浴処理の結果
魚類に対するイミダクロプリド処理の安全性を評価した。271.8Lの海水を入れた流水タンクに入れた魚を65ppm w/vの活性成分イミダクロプリドに曝露した。17.67gのイミダクロプリドを100mlのジメチルスルホキシド(DMSO)に溶解し、その溶液を約900mlの海水に添加し、混合した。スルータンク上の流動が無効になり、イミダクロプリドの溶液を添加した。
65ppmのイミダクロプリドを静水中で1時間曝露し、5〜10分間隔で行動変化を観察した。その後、魚をさらに7日間飼育した後、終了した。曝露期間中、魚類の行動に観察可能な変化は認められなかった。魚をさらに7日間モニターしたが、副作用は認められなかった。終了時には、外部からの病理学的変化は認められなかった。
約233gの18か月齢の大西洋サケにおいて、シラミLepeophtheirus salmonisの移動性幼虫で、約20ppmの4種の新規ネオニコチノイドへの様々な時間の曝露中又は曝露の結果としてのノックダウン時間とその後の反応性/死滅率を調べた。試験開始時、魚の健康状態に重大な問題はなかった。
通常の摂餌行動が再開されるまで、誘発前に最大10日間まで順応させた。魚は750リットルのタンクに35kg/m3以下のストッキング密度で収容された。タンクには、4.8〜10.4℃の温度で5L/分を超える流量の海水を連続的に供給した。光周期は12時間明:12時間暗に設定した。
Lepeophtheirus salmonisのコペポダイドの幼虫を、1タンク当たり1,250〜1,700の目標力価で成体メスシラミから新たに取り出した卵弦の出現により、静止浴中で誘発した。
卵弦を妊娠した船虫から収穫し、ノープリウス包皮形成まで湧昇室でインキュベートした。Naupliiをコペポダイドの齢まで脱皮させ(約10℃で5日間)、タンク水を100μmのメッシュで濾過した後、コペポダイドを225mLの海水中に再懸濁させた。25mLの試料を取り出し、次いで、24ウェルプレート中で1〜2mLの試料に分割し、ナウプリ/コペポディドを実体顕微鏡下で計数した。存在量が十分で、最低80%がコペポダイドである場合には、暗所での静水流下で8時間チャレンジした。
魚をタンクから無作為に選び、90ppmのMS222溶液で軽く鎮静させて、平衡の喪失を誘導した後、頭部に回収不能な打撃を与えて犠牲にした。4〜33匹の魚が処理ごとに必要であった。
次いで、カレット化した魚を処理タンクに懸濁した。魚はケーブルタイ(1本は弁蓋を貫通し、1本は茎の周囲を通る)と木製ロッドに取り付けられたワイヤから水平にタンク内に懸垂された。20ppmの被験物質の20Lタンクを1日1槽使用した。殺処分した魚のシラミを5、10、15、30、60分のいずれかに曝露した(陰性対照は、試験する最長の曝露期間をカバーするため、60分間のみ曝露した)。処理中の順序を無作為に割り付けた。
シラミは、曝露期間中継続的にモニターされ、魚からのシラミの剥離を含め、観察された行動学的観察が行われた。曝露終了時に、シラミをタンク又は魚から取り出し、通気口の付いた小さなプラスチック製スクリュートップ容器(125mL、LDPE、25mm穴)に入れ、蓋に穴をあけ、200μmのメッシュで固定し、濾過した海水を供給された清浄なタンクに移し、そこで24時間保持した。魚から離れたシラミは離れていないシラミと離れていた。
処理24時間後にシラミをスクリュートップ容器から取り出し、生存しているかどうか、生存している場合は反応性があるかどうかを確認した。カテゴリーは以下のように定義された:生存−検出された動き;反応−生存であり、協調して刺激を能動的に回避する;死−検出されなかった動き。
反応性と定義されたシラミは、魚に再付着する可能性がある。評価後、幼虫及び性の決定が必要な場合には、シラミを70%アルコールに移した。
対照処理は海水であった。試験した外部寄生虫処理は、ネオニコチノイド:イミダクロプリド、ジノテフラン、ニテンピラム、クロチアニジン及びチアメトキサム(すべてSigmaAldrich,Dorset,UKから入手)であった。
曝露日に、200mgの試験外部寄生虫処理を1Lの海水に添加した。ニテンピラム192mgのみを供給した。溶液を、撹拌プレート及び磁気ノミ(VWR)を用いて、均一な溶液を確実にするために強い渦を発生させるのに十分な速度で、30分間機械的に撹拌した。その後、9Lの海水を入れた約25 Lの透明プラスチック製タンクに移送した。次いで、溶液を、小型ポンプ(フルバルシーCP1)を用いてさらに10分間混合し、次いで、魚の添加前にタンクから除去した。最終濃度は、19ppmの濃度のニテンピラムを除き、すべての試験外部寄生虫処理について20ppmであった。
〔処理成績〕
各処理には、1回あたり1〜4匹/回、1群あたり2〜13匹/回が必要である。陰性対照(海水)、ジノテフラン、クロチアニジン及びチアメトキサムによる処理を2回、イミダクロプリドについては3回複製した。ニテンピラムの反復投与は1回につき1回のみであった。個々の処理ごとに用いたシラミの平均数は5.5〜10個で、1群当たりの平均数は6.2〜7.2個であった。
表12−魚から落下した船虫の割合
ニテンピラムに曝露された2匹のシラミは落下したが、試験の結果、シラミは物理的に損傷を受けていることがわかり(おそらくは魚の殺傷時)、これがニテンピラムよりもむしろノックダウンの原因であった可能性がある。
イミダクロプリド及びクロチアニジン処理では、ノックダウン時間が曝露時間に等しいシラミの割合は、曝露時間と負の相関を示す(図3)。処理中、イミダクロプリドに曝露されたシラミは、魚から離れる前に活性があることが認められた。クロチアニジンに曝露したシラミは比較的不活性であることがわかった。このことは、ノックダウン時間が曝露時間と同じであるシラミの割合に反映されているようだ(表13及び14)。
表13−ノックダウン時間
表14−ノックダウン期間が曝露期間に等しい船虫の割合
(i)曝露終了時に魚の上に残っているシラミ
海水処理したシラミはすべて反応性であった(表15)。イミダクロプリドで処理したシラミの反応性は15分以降に徐々に影響を受け、60分間の処理ではシラミ反応性は認められなかった。ジノテフランに曝露されたシラミは、影響を受けなかった10分間の曝露を除いて、反応性が低下した。クロチアニジンは、10、15及び30分曝露でシラミの反応性に影響したが、5及び60分曝露では影響しなかった。これは、低複製のためにアーチファクトである可能性がある。チアメトキサムに曝露されたシラミは、1匹のシラミのために、曝露60分後にわずかに影響を受け、ニテンピラムに曝露されたシラミは、曝露期間中ずっと影響を受けなかった。
表15−魚から採取されたシラミの反応性
(ii)曝露終了により魚をノックアウトしたシラミ
ノックダウンは、イミダクロプリド、ジノテフラン、ニテンピラム及びクロチアニジン基で認められた(表16)。これは陽性対照群で最も顕著であり、10分間の曝露からノックダウンがあった。曝露時間の増加に伴い、反応性は漸進的に消失した。60分間曝露したシラミは反応性を示さなかった。ジノテフラン群では、15分目に100%、30分目に0%の反応性が認められたが、これはシラミ1匹の反応性によるものであった。これらの各曝露時間にシラミが1匹だけ落下したので、この結果はある程度の注意を払って処理すべきである。ニテンピラム投与では、シラミは物理的に損傷を受け、死滅した。損傷は、サケ殺傷時に起こった可能性が最も高い。クロチアニジンは、15、30、60分曝露でそれぞれ0%、44%、33%の反応性を示した。15分間の曝露での0%の反応性は、1匹のシラミでは反応性がなかったためであった。
表16−魚から採取されたシラミの反応性
Claims (26)
- 水中の魚から外部寄生虫を除去する方法であって、以下の:
(i) ネオニコチノイドを投与して、前記魚から前記外部寄生虫を除去する工程;及び、
(ii) 除去された前記外部寄生虫を含む水を置換水で交換して、前記除去された外部寄生虫と魚を分離する工程;を含む方法であって、ここで、
前記ネオニコチノイドは、イミダクロプリド、又はその医薬上有効な塩若しくはエステルではなく;かつ、
前記ネオニコチノイドは、飼料内投与用には構成又は処方されていない、方法。 - 前記ネオニコチノイドは、1〜500ppm、1〜200ppm、20〜200ppm、1〜64ppm、10〜64ppm、10〜50ppm、50ppm以上、100ppm以上、又は200ppm以上の濃度(w/v)で投与される、請求項1に記載の方法。
- 前記ネオニコチノイドは、180分以下、120分以下、60分以下、30分未満、20分未満、15分以下、10分未満、又は5分以下で適用される、請求項1又は2に記載の方法。
- 前記魚は、サケ科魚、イワナ属魚、又は掃除魚(cleaner fish)である、請求項1〜3のいずれか一項に記載の方法。
- 前記ネオニコチノイドは、致死未満量及び/若しくは致死未満時間で適用され、並びに/又は、前記ネオニコチノイドは、外部寄生虫をノックダウンする量で適用される、請求項1〜4のいずれか一項に記載の方法。
- 前記ネオニコチノイドは、投与される唯一の外部寄生虫駆除剤である、請求項1〜5のいずれか一項に記載の方法。
- 前記ネオニコチノイドは、クロチアニジン、ジノテフラン、アセトアミプリド、イミダクロプリド、ニテンピラム、ニチアジン、チアクロプリド若しくはチアメトキサム、又はその医薬上有効な塩若しくはエステルである、請求項1〜6のいずれか一項に記載の方法。
- 前記ネオニコチノイドは、チアメトキサム、又はその医薬上有効な塩若しくはエステルではない、請求項1〜7のいずれか一項に記載の方法。
- 前記ネオニコチノイドは、クロチアニジン、又はその医薬上有効な塩若しくはエステルではない、請求項1〜8のいずれか一項に記載の方法。
- さらに、以下の:
(iii) 前記除去された外部寄生虫の環境への放出を防ぐ工程;
を含む、請求項1〜9のいずれか一項に記載の方法。 - 前記除去された外部寄生虫の放出を防ぐ工程は、前記除去された外部寄生虫を含む水の試料から前記外部寄生虫を採取する工程を含む、請求項10に記載の方法。
- 外部寄生虫駆除剤及び外部寄生虫を含む水の除染方法であって、以下の:
(i) 水の試料を採取する工程;
(ii) 前記試料から前記外部寄生虫を採取する工程;
を含む、方法。 - 前記水の試料から前記外部寄生虫を採取する工程は、前記試料をフィルタ、好ましくはメッシュフィルタに通すことを含み、場合によっては、前記フィルタのサイズは、少なくとも0.2μm、少なくとも30μm、少なくとも60μm、又は少なくとも150μmの孔又はギャップである、請求項11又は12に記載の方法。
- 前記外部寄生虫は、船虫(sea louse)である、請求項1〜13のいずれか一項に記載の方法。
- 生存する前記外部寄生虫を、場合によっては、外部寄生虫駆除剤を適用して、死滅する、請求項14に記載の方法。
- 魚の外部寄生虫の寄生の処理の使用のためのネオニコチノイドであって、前記ネオニコチノイドはイミダクロプリド、又はその医薬上有効な塩若しくはエステルではなく、前記ネオニコチノイドは飼料内投与用に構成又は処方されていない、使用のためのネオニコチノイド。
- 前記ネオニコチノイドは、180分以下、120分以下、60分以下、30分未満、20分未満、15分以下、10分未満、又は5分以下で投与される、請求項16に記載の使用のためのネオニコチノイド。
- 前記ネオニコチノイドは、1〜500ppm、1〜200ppm、20〜200ppm、1〜64ppm、10〜64ppm、10〜50ppm、50ppm以上、100ppm以上、又は200ppm以上の濃度(w/v)で投与される、請求項16又は17に記載の使用のためのネオニコチノイド。
- 前記外部寄生虫は、船虫である、請求項16〜18のいずれか一項に記載の使用のためのネオニコチノイド。
- 前記魚は、サケ科魚、イワナ属魚、又は掃除魚である、請求項16〜19のいずれか一項に記載の使用のためのネオニコチノイド。
- 前記ネオニコチノイドは、クロチアニジン、ジノテフラン、イミダクロプリド、アセトアミプリド、ニテンピラム、ニチアジン、チアクロプリド若しくはチアメトキサム、又はその医薬上有効な塩若しくはエステルである、請求項16〜20のいずれか一項に記載の使用のためのネオニコチノイド。
- 前記ネオニコチノイドは、チアメトキサム又はその医薬上有効な塩若しくはエステルでない、請求項16〜21のいずれか一項に記載の使用のためのネオニコチノイド。
- 前記ネオニコチノイドは、クロチアニジン又はその医薬上有効な塩若しくはエステルでない、請求項16〜22のいずれか一項に記載の使用のためのネオニコチノイド。
- 前記ネオニコチノイドは、致死未満量及び/若しくは致死未満時間で適用され、並びに/又は、前記ネオニコチノイドは、外部寄生虫をノックダウンする量で適用される、請求項16〜23のいずれか一項に記載の使用のためのネオニコチノイド。
- 1又はそれ以上の外部寄生虫駆除剤を含む魚の外部寄生虫の寄生の処理に用いる組成物であって、1又はそれ以上の前記外部寄生虫駆除剤の1つが、請求項16〜24のいずれか一項に記載の使用のためのネオニコチノイドである、組成物。
- 前記組成物がわずか1つの外部寄生虫駆除剤を含む、請求項25に記載の組成物。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB1809374.0 | 2018-06-07 | ||
| GBGB1809374.0A GB201809374D0 (en) | 2018-06-07 | 2018-06-07 | Treatment for removing ectoparasites from fish |
| GB1809620.6 | 2018-06-12 | ||
| GBGB1809620.6A GB201809620D0 (en) | 2018-06-07 | 2018-06-12 | Treatment for removing ectoparasites from fish |
| PCT/GB2019/051519 WO2019234396A1 (en) | 2018-06-07 | 2019-05-31 | Treatment for removing ectoparasites from fish |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021526793A true JP2021526793A (ja) | 2021-10-11 |
| JPWO2019234396A5 JPWO2019234396A5 (ja) | 2022-06-02 |
Family
ID=62975617
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020567594A Pending JP2021526793A (ja) | 2018-06-07 | 2019-05-31 | 魚類からの外部寄生虫類の除去処理 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US20210244028A1 (ja) |
| EP (1) | EP3801023A1 (ja) |
| JP (1) | JP2021526793A (ja) |
| CN (1) | CN112243346A (ja) |
| AU (1) | AU2019283445A1 (ja) |
| CA (1) | CA3101882A1 (ja) |
| CL (1) | CL2020003185A1 (ja) |
| DK (1) | DK181729B1 (ja) |
| GB (2) | GB201809374D0 (ja) |
| WO (1) | WO2019234396A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115517207B (zh) * | 2022-09-26 | 2023-05-09 | 中国科学院水生生物研究所 | 一种多子小瓜虫在体阶段药物杀灭效果的评价方法和装置 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5504081A (en) * | 1992-09-29 | 1996-04-02 | Bayer Aktiengesellschaft | Combating fish parasites |
| WO2009010755A2 (en) * | 2007-07-16 | 2009-01-22 | Nettforsk As | Method of combating sea lice |
| JP2011523944A (ja) * | 2008-05-21 | 2011-08-25 | バイエル・クロツプサイエンス・アクチエンゲゼルシヤフト | 表面に対する改善された長期効果を有する殺虫剤製剤 |
| WO2014064184A1 (en) * | 2012-10-26 | 2014-05-01 | Novartis Ag | New treatment |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10320505A1 (de) * | 2003-05-08 | 2004-11-25 | Bayer Healthcare Ag | Mittel zum Bekämpfen von Parasiten an Tieren |
| TWI430995B (zh) * | 2007-06-26 | 2014-03-21 | Du Pont | 萘異唑啉無脊椎有害動物控制劑 |
| KR101680912B1 (ko) * | 2008-07-09 | 2016-11-29 | 바스프 에스이 | 이속사졸린 화합물 ⅰ을 포함하는 살충 활성 혼합물 |
| GB0905331D0 (en) | 2009-03-27 | 2009-05-13 | Avecia Biolog Ltd | Expression process |
| DK178277B1 (da) * | 2010-06-18 | 2015-10-26 | Novartis Tiergesundheit Ag | Diaryloxazolinforbindelser til bekæmpelse af fiskelus |
| CA2711191A1 (en) * | 2010-07-27 | 2012-01-27 | Aquaculture Engineering Group Inc. | Treatment system for fish |
| CN103957701B (zh) * | 2011-09-12 | 2017-05-03 | 梅里亚有限公司 | 包含异噁唑啉活性剂的杀寄生物组合物,其方法和用途 |
| CA2879477A1 (en) * | 2012-07-27 | 2014-01-30 | Novartis Ag | New treatment of fish with a nanosuspension of lufenuron or hexaflumuron |
| GB2550559B (en) * | 2016-05-17 | 2022-05-04 | Univ Dundee | Methods, systems and apparatus for control of parasite infestation in aquatic animals |
| ES2937941T3 (es) * | 2016-12-08 | 2023-04-03 | Benchmark Animal Health Ltd | Tratamiento para quitar ectoparásitos a los peces |
-
2018
- 2018-06-07 GB GBGB1809374.0A patent/GB201809374D0/en not_active Ceased
- 2018-06-12 GB GBGB1809620.6A patent/GB201809620D0/en not_active Ceased
-
2019
- 2019-05-31 CA CA3101882A patent/CA3101882A1/en active Pending
- 2019-05-31 EP EP19730475.1A patent/EP3801023A1/en not_active Withdrawn
- 2019-05-31 WO PCT/GB2019/051519 patent/WO2019234396A1/en active Application Filing
- 2019-05-31 AU AU2019283445A patent/AU2019283445A1/en not_active Abandoned
- 2019-05-31 JP JP2020567594A patent/JP2021526793A/ja active Pending
- 2019-05-31 US US16/972,795 patent/US20210244028A1/en not_active Abandoned
- 2019-05-31 CN CN201980038085.3A patent/CN112243346A/zh active Pending
-
2020
- 2020-12-07 CL CL2020003185A patent/CL2020003185A1/es unknown
- 2020-12-17 DK DKPA202070848A patent/DK181729B1/en active IP Right Grant
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5504081A (en) * | 1992-09-29 | 1996-04-02 | Bayer Aktiengesellschaft | Combating fish parasites |
| WO2009010755A2 (en) * | 2007-07-16 | 2009-01-22 | Nettforsk As | Method of combating sea lice |
| JP2010533693A (ja) * | 2007-07-16 | 2010-10-28 | ネットフォルスク エーエス | フナムシの駆除方法 |
| JP2011523944A (ja) * | 2008-05-21 | 2011-08-25 | バイエル・クロツプサイエンス・アクチエンゲゼルシヤフト | 表面に対する改善された長期効果を有する殺虫剤製剤 |
| WO2014064184A1 (en) * | 2012-10-26 | 2014-05-01 | Novartis Ag | New treatment |
Also Published As
| Publication number | Publication date |
|---|---|
| CL2020003185A1 (es) | 2021-06-25 |
| DK181729B1 (en) | 2024-11-12 |
| CA3101882A1 (en) | 2019-12-12 |
| DK202070848A1 (en) | 2020-12-23 |
| AU2019283445A1 (en) | 2021-01-07 |
| CN112243346A (zh) | 2021-01-19 |
| GB201809374D0 (en) | 2018-07-25 |
| EP3801023A1 (en) | 2021-04-14 |
| WO2019234396A1 (en) | 2019-12-12 |
| GB201809620D0 (en) | 2018-07-25 |
| US20210244028A1 (en) | 2021-08-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DK181334B1 (en) | Neonicotinoid for use in removing ectoparasites from fish | |
| US9320771B2 (en) | TTO-based wide spectrum therapeutics, disinfectants and anesthetics for use in aquaculture | |
| Hakalahti-Sirén et al. | Control of freshwater fish louse Argulus coregoni: a step towards an integrated management strategy | |
| NO333012B1 (no) | Anvendelse av nellikolje mot fiskelus. | |
| JP2021526793A (ja) | 魚類からの外部寄生虫類の除去処理 | |
| US11020364B2 (en) | Palmitoleic acid for use in inhibiting the attachment of sea lice to fish | |
| RU2788121C2 (ru) | Обработка с целью удаления эктопаразитов у рыб | |
| JP2817753B2 (ja) | 海水養殖場におけるトラフグのヘテロボツリウム症の予防方法 | |
| US20220030882A1 (en) | Composition and Method to Remove Parasites From Fish and to Prevent or Treat Infestation or Infection of Parasites on Fish | |
| NO20131294A1 (no) | Medium for behandling av eksterne fiskeparasitter hos oppdrettsfisk og framgangsmåte for bruk av mediet | |
| Woke et al. | Effects of pesticide (Chlorpyrifos Ethyl) on the fingerlings of catfish (Clarias gariepinus) | |
| WO2023131615A1 (en) | Method to detach ectoparasites from fish | |
| NO20160382A1 (no) | Preparat som inneholder sjøvann tilsatt en kaliumforbindelse | |
| Shillinger | Diseases of Fur Animals | |
| Shillinger | Diseases of fur animals | |
| GB2500381A (en) | The combination of pyrethroid and hydrogen peroxide for control of ectoparasite infestation in fish |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220525 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220525 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20230228 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230314 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20231010 |