JP2013523842A - 造血機能を提供するための組成物および方法 - Google Patents
造血機能を提供するための組成物および方法 Download PDFInfo
- Publication number
- JP2013523842A JP2013523842A JP2013504020A JP2013504020A JP2013523842A JP 2013523842 A JP2013523842 A JP 2013523842A JP 2013504020 A JP2013504020 A JP 2013504020A JP 2013504020 A JP2013504020 A JP 2013504020A JP 2013523842 A JP2013523842 A JP 2013523842A
- Authority
- JP
- Japan
- Prior art keywords
- cord blood
- cells
- pool
- umbilical cord
- patient
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/48—Reproductive organs
- A61K35/51—Umbilical cord; Umbilical cord blood; Umbilical stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/28—Bone marrow; Haematopoietic stem cells; Mesenchymal stem cells of any origin, e.g. adipose-derived stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/48—Reproductive organs
- A61K35/50—Placenta; Placental stem cells; Amniotic fluid; Amnion; Amniotic stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0647—Haematopoietic stem cells; Uncommitted or multipotent progenitors
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B30/00—ICT specially adapted for sequence analysis involving nucleotides or amino acids
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B30/00—ICT specially adapted for sequence analysis involving nucleotides or amino acids
- G16B30/10—Sequence alignment; Homology search
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/90—Serum-free medium, which may still contain naturally-sourced components
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/125—Stem cell factor [SCF], c-kit ligand [KL]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/145—Thrombopoietin [TPO]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/26—Flt-3 ligand (CD135L, flk-2 ligand)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/40—Regulators of development
- C12N2501/42—Notch; Delta; Jagged; Serrate
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/58—Adhesion molecules, e.g. ICAM, VCAM, CD18 (ligand), CD11 (ligand), CD49 (ligand)
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Developmental Biology & Embryology (AREA)
- Cell Biology (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Zoology (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Physics & Mathematics (AREA)
- Organic Chemistry (AREA)
- Epidemiology (AREA)
- Virology (AREA)
- Reproductive Health (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Analytical Chemistry (AREA)
- Theoretical Computer Science (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Medical Informatics (AREA)
- Evolutionary Biology (AREA)
- Bioinformatics & Computational Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Microbiology (AREA)
- Pregnancy & Childbirth (AREA)
- General Engineering & Computer Science (AREA)
- Biochemistry (AREA)
Abstract
Description
本発明は、プール中のサンプルが患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならないように、患者への投与のために増殖ヒト臍帯血幹/前駆細胞サンプルプールを選択し、上記選択された増殖ヒト臍帯血幹/前駆細胞サンプルプールを患者に投与することによって、造血機能を必要とする人間の患者に造血機能を提供するための方法および組成物に関する。また、本明細書において、上記増殖ヒト臍帯血幹/前駆細胞サンプルプールを得るための方法、および凍結増殖ヒト臍帯血幹/前駆細胞サンプルプールのバンク、そのようなバンクを生成するための方法が提供される。
持続性汎血球減少症は、強化化学療法レジメン、造血細胞移植(hematopoietic cell transplantation;HCT)のための骨髄機能を廃絶する強度低下療法、および急性電離放射線への暴露の後によく見られる症状である。特に懸念されるのは、抗菌療法の向上にも関わらず感染の大きなリスクを招き、罹患率及び死亡率を増加させる好中球減少症である。従って、高用量化学療法および/または高線量放射線治療の後に見られる持続性汎血球減少症/好中球減少症を根絶し、より迅速な造血機能回復を潜在的に促すことのできる新規な治療法が必要とされている。
ヒト白血球抗原(human leukocyte antigen;HLA)とは、ヒトにおける主要組織適合複合体(major histocompatibility complex;MHC)の名称である。超遺伝子座には、ヒトにおける免疫系の機能に関連する遺伝子が多数含まれている。この遺伝子群は、染色体6に座乗し、細胞表面の抗原提示細胞及びその他たくさんの遺伝子をコードする。HLA遺伝子は、ほとんどの脊椎動物に見られ(よってMHC遺伝子の中で最も研究されている)ヒト版のMHC細胞である。HLA遺伝子によってコードされたタンパク質は、臓器移植要因としての歴史的発見により、抗原としても知られている。主要なHLA抗原は、免疫機能にとって必須要素であるとともに、異なるクラスがあり、それぞれに異なる機能がある。
造血幹細胞は、多能性であり、最終的に全種類の最終分化血液細胞を生み出す。造血幹細胞は、自己再生したり、より方向が決まった(committed)前駆細胞に分化したりすることができる。これらの前駆細胞は、ほんの数種類の血液細胞の原細胞であると不可逆的に決定される。例えば、造血幹細胞は、(i)最終的に単球、およびマクロファージ、好中球、好塩基球、好酸球、赤血球、巨核球/血小板、樹状細胞を生み出す骨髄前駆細胞、または、(ii)最終的にT細胞、B細胞、およびナチュラルキラー細胞(NK細胞)と呼ばれるリンパ球様細胞を生み出すリンパ球前駆細胞に分化することができる。幹細胞が骨髄前駆細胞に分化すると、その後代はリンパ球系細胞を生み出すことができない。同様に、リンパ球前駆細胞は骨髄系細胞を生み出すことができない。血液生成と造血幹細胞分化の一般的な説明については、Chapter 17, Differentiated Cells and the Maintenance of Tissues, Alberts et al, 1989, Molecular Biology of the Cell, 2nd Ed., Garland Publishing, New York, NY; Chapter 2 of Regenerative Medicine, Department of Health and Human Services, August 2006(http://stemcells.nih.gov/info/scireport/2006report.htm)、およびChapter 5 of Hematopoietic Stem Cells,2009,Stem Cell Information, Department of Health and Human Services (http://stemcells.nih.gov/info/scireport/chapter5.asp)を参照。
Notchファミリーのメンバーは、多くの無脊椎動物系における初期の発達段階で細胞間相互作用や細胞運命の決定において中心的な役割を担う巨大膜貫通タンパクコードする(Simpson, 1995, Nature 375:736-7; Artavanis-Tsakonis et al, 1995, Science. 268:225-232; Simpson, 1998, Semin. Cell Dev. Biol. 9:581-2; Go et al, 1998, Development. 125:2031-2040; Artavanis-Tsakonas and Simpson, 1991, Trends Genet. 7:403-408)。Notch受容体は、さまざまな種類の細胞が、直接隣接した細胞がとった分化経路に基づいて、選択的分化経路の中から分化経路を選択することを可能にする高度に保存された経路の一部である。この受容体は、明らかでない共通ステップを通して作用すると考えられる。この共通ステップは、方向が決まっていない細胞の反応性を阻害し2つの選択的運命のうち1つを選ぶことによって、方向が決まっていない(uncommitted)細胞の分化状態への進行を制御する。これによって、細胞は、分化を遅らせたり、適切な発生信号の存在下では、非抑制経路に沿って分化したりすることができる。
ヒトCD34+前駆細胞におけるNotch−1 mRNA発現を根拠にして、血液形成におけるNotchシグナリングが果たす役割が推測された(Milner et al, 1994, Blood 3:2057-62)。このことは、Notch−1およびNotch−2タンパク質が造血前駆細胞中に存在し、T細胞、B細胞、および単球中により多く存在しているという実証と、造血基質におけるJagged−1タンパク質の実証とによって支持されている(Ohishi et al, 2000, Blood 95:2847-2854; Varnum-Finney et al, 1998, Blood 91:4084-91; Li et al, 1998, Immunity 8:43-55)。
上記技術において、迅速に造血機能を再構成するための、製造後長期にわたって備蓄可能な「既製の(off-the-shelf)」製剤が必要とされている。本発明は、そのような必要を満たすものである。本発明は、造血機能を必要とする人間の患者に造血機能を提供するための方法であって、上記患者に増殖ヒト臍帯血幹/前駆細胞サンプルプールを投与する工程を含み、上記プール中の上記サンプルは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない、方法を提供する。また、本発明は、造血機能を必要とする人間の患者に造血機能を提供するための方法であって、増殖ヒト臍帯血幹細胞サンプルプールまたはそのアリコートを上記患者に投与する工程を含み、上記プールは、2つ以上の異なる増殖ヒト臍帯血幹細胞サンプルを含み、上記プール中の各サンプルは、異なる人間の出生時の臍帯血および/または胎盤血から由来し、上記プール中の上記サンプルは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない。ある具体的な実施形態では、上記プール中の2つ以上のサンプルは、患者によって確立しかつサンプルによって確立した1つまたは2つのHLA抗原または対立遺伝子の型で患者と不適合となる。他の具体的な実施形態では、上記プール中の2つ以上のサンプルは、患者によって確立した2つのHLA抗原または対立遺伝子の型で患者と不適合となる。
本明細書に記載された方法および材料に類似する、あるいは相当するいかなる方法および材料も本発明の実施および試験に用いることができるが、好ましい方法および材料を記載する。本発明のために、以下の用語を下記の通り定義する。
図1は、本発明の方法を実施するために有用なコンピュータシステムの例示的な実施形態を示す。
本発明は、造血機能を必要とする人間の患者に造血機能を提供するための方法であって、上記患者に増殖ヒト臍帯血幹細胞サンプルプールを投与する工程を含み、上記プール中の上記サンプルは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない。一実施形態では、上記増殖ヒト臍帯血幹細胞は骨髄球系細胞へ分化する。別の実施形態では、上記増殖ヒト臍帯血幹細胞はリンパ球系細胞へ分化する。
本発明によれば、ヒト臍帯血および/またはヒト胎盤血が、CB幹細胞の供給源である。このような血液は、上記技術分野において公知の方法によっても入手することができる。幹細胞の原料として臍帯血または胎盤血を使用することには、多くの利点がある。例えば、臍帯血および胎盤血の入手が容易であることや、ドナーに対する外傷がないことが挙げられる。例えば、人間の出産時に臍帯血および胎盤血を採取することを記載した、米国特許第5,004,681号を参照すればよい。一実施形態では、Goodmanらによる米国特許第7,147,626号B2に開示されている方法によって臍帯血が採取されている。
出生時の一人の人間から臍帯血か胎盤血のいずれか一方、またはその両方を採取した後、血液を処理して、濃縮した造血幹細胞の集団または濃縮した造血幹前駆細胞の集団を生成し、CB幹細胞集団を形成する。造血幹細胞または造血幹前駆細胞は、他の種類の造血細胞と比較して、造血幹細胞または造血幹前駆細胞の濃度増加で発現する特定のマーカーに対して陽性であってもよい。そのようなマーカーとしては、特に限定されないが、例えば、CD34、CD43、CD45RO、CD45RA、CD59、CD90、CD109、CD117、CD133、CD166、HLA DR、またはそれらの組み合わせが挙げられる。また、造血幹細胞または造血幹前駆細胞は、他の種類の造血細胞と比較して、発現マーカーに対して陰性であってもよい。そのようなマーカーとしては、特に限定されないが、例えば、Lin、CD38、またはそれらの組み合わせが挙げられる。好ましくは、造血幹細胞または造血幹前駆細胞は、CD34+細胞である。好ましくは、上記CB幹細胞集団は、CD34+幹細胞またはCD34+幹細胞・前駆細胞(したがって、T−細胞が欠乏している)である。従って、「濃縮」とは、(濃縮処理前のサンプル中の割合と比較して)サンプル中の造血幹細胞または造血幹前駆細胞の割合を増加させる処理を指す。精製は濃縮の一例である。ある特定の実施形態では、濃縮処理前のサンプルに対して、濃縮させたサンプル中の細胞の割合として、CD34+細胞(または他の好適な抗原陽性細胞)数の増加は、少なくとも25倍、50倍、75倍、100倍、150倍、200倍、250倍、300倍、350倍であり、好ましくは100倍から200倍である。好ましい実施形態では、磁気ビーズと共役させた、CD34に対するモノクローナル抗体、および上記CD34+細胞を分離する磁気細胞分離装置を用いて、上記CD34+細胞を濃縮する。
上記の濃縮方法または上記技術分野における他の公知方法によって、出生時の一人以上の人間から採取したヒト臍帯血および/またはヒト胎盤血から、上記CB幹細胞を単離した後、例えばCD34+細胞等の、造血幹細胞または造血幹前駆細胞の数を増加させるために、上記CB幹細胞を増殖する。上記技術分野における任意の公知方法を用いて、増殖CB幹細胞を産生するCB幹細胞の数を増やすことができる。好ましくは、上記増殖CB幹細胞の集団を得るために、上記CB幹細胞を成長および分裂(増殖)させるような細胞成長条件下(例えば、有糸分裂を促進させる等)で、上記CB幹細胞を培養する。ある実施形態では、出生時の一人の人間の臍帯血および/または胎盤血に由来する各CB幹細胞の個体群を、増殖の前または後にプールする。別の実施形態では、増殖サンプルは、サンプルプールではない。好ましくは、増殖に用いる技術とは、(i)結果として、増殖前のCB幹細胞サンプルに対し、増殖サンプルにおいて、例えばCD34+細胞等の、造血幹細胞または造血幹前駆細胞の数を増加させる技術、または(ii)結果として、増殖前のサンプルによって見られるSCID再構築細胞に対して、増殖サンプルを注入したNOD/SCIDマウスにおける生着の強化によって示される、限定希釈分析によって決定した、上記増殖サンプル中のSCID再構築細胞の数を増加させる技術である。ただし、上記増殖サンプルおよび上記増殖前のサンプルは、同じサンプルの異なるアリコートに由来するものであり、上記増殖前のサンプルではなく、上記増殖サンプルには、上記増殖技術が施されている。ある実施形態では、上記増殖技術は、上記増殖させていないCB幹細胞サンプルに比べて、上記増殖サンプルにおいて、50、75、100、150、200、250、300、350、400、450、または500倍の造血幹細胞または造血幹前駆細胞の数の増加をもたらし、好ましくは、100〜200倍の増加をもたらす。上記造血幹細胞または造血幹前駆細胞は、CD34、CD43、CD45RO、CD45RA、CD59、CD90、CD109、CD117、CD133、CD166、およびHLA DRの1以上のものに対して陽性および/またはLinおよび/またはCD38に対して陰性であってもよい。ある具体的な実施形態では、上記生着の強化は、増殖前のサンプルのアリコートを注入したマウスに対して、増殖サンプルのアリコートを注入したマウスの骨髄におけるヒトCD45+細胞のパーセンテージの増加を、例えば注入10日後、3週間後、または9週間後に検出することによって検出できる(Delaney et al., 2010, Nature Medicine. 16(2): 232-236参照)。
本発明の好ましい実施形態では、Notch機能を持つアゴニスト、ならびに1以上の成長因子またはサイトカインの存在下において上記CB幹細胞を所定の時間培養することによって、上記CB幹細胞を増殖する。上記CB幹細胞の培養は、上記技術分野の任意の公知の培地/条件において行なわれる(Freshney Culture of Animal Cells, Wiley-Liss, Inc., New York, NY (1994)参照)。培養時間は、本明細書において定義されるように、増殖CB幹細胞集団を産生するのに十分な時間とする。例えば、上記CB幹細胞 Notch機能を持つアゴニスト、ならびに1以上の成長因子またはサイトカインの存在下において、上記CB幹細胞を、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、または25日間、好ましくは、少なくとも10日間培養する。必要に応じて、上記培養期間中の任意の時点で、培地を新鮮な培地と交換してもよいし、新鮮な培地を追加してもよい。
本発明の好ましい実施形態では、上述したようにNotch機能を持つアゴニスト、および1以上の成長因子もしくはサイトカインの存在下で、上記CB幹細胞をある一定時間培養することによって、上記CB幹細胞を増殖する。あるいは、1以上の成長因子またはサイトカインの存在下で、上記CB幹細胞をある一定時間培養することによって、上記CB幹細胞を増殖する。分化させずに上記CB幹細胞を増殖させる場合、成長をサポートするが分化をサポートしない成長因子の存在下で本発明のCB幹細胞を培養させる。上記成長因子としては、例えばタンパク質や化学物質等、細胞の増殖および/または生存を促進させる任意の種類の分子が用いられる。
本発明のCB幹細胞を増殖させるための具体的な実施形態では、100ng/mlのSCF、100ng/mlのTPO、および10ng/mlのGM−CSFの存在下、例えばDeltaの細胞外ドメイン等の固定化したDeltaリガンドとフィブロネクチンとを含むプラスチックの組織培養皿の上で上記細胞を培養する。CB幹細胞を増殖させるための別の具体的な実施形態では、100ng/mlのSCF、100ng/mlのFlt−3L、100ng/mlのTPO、100ng/mlのIL−6、および10ng/mlのIL−3の存在下、固定化したDeltaリガンドとフィブロネクチンとを含むプラスチックの組織培養皿の上で上記細胞を培養する。本発明の幹細胞を増殖させるための別の具体的な実施形態では、100ng/mlのSCF、100ng/mlのFlt−3L、10mg/mlのG−CSF、および10mg/mlのGM−CSFの存在下、固定化したDeltaリガンドとフィブロネクチンとを含むプラスチックの組織培養皿の上で上記細胞を培養する。CB幹細胞を増殖させるための別の具体的な実施形態では、100ng/mlのSCF、100ng/mlのFlt−3L、100ng/mlのTPO、および10mg/mlのGM−CSFの存在下、固定化したDeltaリガンドとフィブロネクチンとを含むプラスチックの組織培養皿の上で上記細胞を培養する。CB幹細胞を増殖させるためのさらに別の具体的な実施形態では、300ng/mlのSCF、300ng/mlのFlt−3L、100ng/mlのTPO、100ng/mlのIL−6、および10mg/mlのIL−3の存在下、固定化したDeltaリガンドとフィブロネクチンとを含むプラスチックの組織培養皿の上で上記細胞を培養する。本発明の幹細胞を増殖させるための別の具体的な実施形態では、100ng/mlのSCF、100ng/mlのFlt−3L、100ng/mlのTPO、10mg/mlのG−CSF、および10mg/mlのGM−CSFの存在下、固定化したDeltaリガンドとフィブロネクチンとを含むプラスチックの組織培養皿の上で上記細胞を培養する。上記培養条件に代わる別の実施形態では、フィブロネクチンは上記組織培養皿から除外され、別の細胞外マトリックスタンパク質に置き換えられる。CB幹細胞増殖のさらなる例示的な培養条件については、Bernsteinらによる米国特許第7,399,633号B2も参照するとよい。
6.4.1 凍結保存
臍帯血からCB幹細胞を増殖させて増殖CB幹細胞集団を得た後、上記増殖CB幹細胞集団を凍結保存する。ある実施形態では、プールする(および続いて解凍した状態でプールする)前に、上記増殖CB幹細胞集団を分離して、1以上の袋(または器具)の中で凍結させる。別の実施形態では、2以上の増殖CB幹細胞の集団をプールし凍結して、あるいは必要に応じてプールして別々のアリコートに分けた後、それぞれのアリコートを凍結させる。好ましい実施形態では、最大約40億個の有核細胞が1つの袋の中で冷凍されている。好ましい実施形態では、増殖CB幹細胞は新鮮である。つまり、増殖CB幹細胞は、増殖または凍結保存前に事前に冷凍させてある。「冷凍(frozen/freezing)」と「凍結保存(cryopreservaed/cryopreservation)」という用語は、本願において同義で使われる。凍結保存は、生存した状態で細胞を冷凍させる上記技術分野において任意の公知方法によって行なわれる。細胞の冷凍には、通常破壊性がある。冷却すると、細胞内の水が凍る。その後、細胞膜への浸透圧作用、細胞の脱水、溶質の濃縮、および氷の結晶の形成によって、損傷が起きる。上記細胞の外に氷が形成されると、有効水は、溶液から除去され、上記細胞から取り除かれる。これによって、浸透圧による脱水および溶質の濃度上昇が起こり、結果として上記細胞が破壊される。この説明については、Mazur, P., 1977, Cryobiology 14:251-272を参照するとよい。
好ましい実施形態では、本発明の新生児の細胞の場合に、この冷却速度で行なわれる。細胞を収容している容器は、低温貯蔵温度での安定性が必要であり、これにより冷凍および解凍の両方を効果的に制御するための急速な熱伝導が可能となる。複数個で少量ずつ(1〜2ml)の場合、プラスチック製の密閉バイアル(例えば、Nunc製やWheaton cryules製)またはガラス製のアンプルを用いる。一方、大量(100〜200ml)の場合、冷却時の熱伝導がよくなるように金属製の皿の間に挟んだポリオレフィン製の袋(例えば、Delmed製)の中で凍結させる。骨髄細胞が入った袋を、偶然にも毎分約3℃の冷却速度を持つ−80℃のフリーザーの中に入れておくことで、その凍結が成功した。
凍結細胞は、急速に解凍され(例えば、37〜41℃の温度に保った水浴中に)、解凍後直ちに冷却されることが好ましい。ある特定の実施形態では、上記凍結細胞を含むバイアルを温水浴中にその首まで浸漬し、穏やかに回転させることで、解凍させながら細胞懸濁液が確実に混合するともに、該温水から内部の氷の塊への熱伝達が増大する。氷が完全に溶けたらすぐに、上記バイアルを速やかに氷上に置く。
2.T細胞(CD3+、CD4+およびCD8+サブセットの両方を含む)
3.B細胞(CD19+またはCD20+)
4.NK細胞(CD56+)
5.単球(CD14+)
6.骨髄単球(CD15+)
7.巨核球(CD41 +)
8.樹状細胞(HLA−DRbrightおよびCD123brightに対して陰性を示す系統、またはHLA−DRbrightおよびCD11cbrightに対して陰性を示す系統)。
好ましい実施形態では、上記患者に投与される上記増殖CB幹細胞は非組換え型である。しかしながら、他の実施形態では、増殖前の上記CB幹細胞または上記増殖CB幹細胞は、遺伝子を組み換えることで、被検者に対して移植する場合に有益な遺伝子産物を生成することができる。そのような遺伝子産物は、特に限定されないが、例えば抗TNF、抗IL−1、抗IL−2などの抗炎症性因子が含まれる。上記CB幹細胞は、遺伝子治療に用いるために遺伝子を組み換えることで、被検者の遺伝子活性の程度を調節することができる。これにより、移植を助け、または移植の結果を向上させ、もしくは、例えば組換え遺伝子における障害によって引き起こされる病気を治療する。上記CB幹細胞は、上記CB幹細胞または上記増殖CB幹細胞に対して組換え型の核酸を移入することにより、組換え型にする。
本発明に従って、増殖CB幹細胞サンプルプールが選択され、上記増殖CB幹細胞サンプルを必要とする人間の患者に対して、造血機能を提供するために投与される。ここで、上記プール中の上記サンプルは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない。ここでいう「上記プール中の上記サンプルは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない」は、上記プール中の上記サンプルにおける上記細胞すべてについて、上記患者によって確立したHLA型と適合しないHLA型を勘定したとき、2つ以上の不適合が存在しないことを意味する。例えば、6つのHLA抗原/対立遺伝子の型が上記患者によって決められ、上記プール中の1つのサンプルが2つの抗原/対立遺伝子で適合しないとき、上記プール中の他のサンプルは、抗原/対立遺伝子が適合する残りの任意の4つで不適合になり得ない(上記プール中の上記他のサンプルは、抗原/対立遺伝子が適合しない同じ2つのうち、0、1つ、または両方で不適合となり得る)。具体的な実施形態では、上記患者は、1つ、2つ、3つ、4つ、5つ、または6つのHLA抗原/対立遺伝子の型、より好ましくは少なくとも4つのHLA抗原/対立遺伝子の型、最も好ましくは6つのHLA抗原/対立遺伝子の型が決められる。
上記増殖CB幹細胞サンプルプールは、所望の遺伝子を組換えで発現しているか否かに関わらず、上記技術において既知の、増殖CB幹細胞および移植サイトにとって適切な任意の方法によって、病気または損傷に対する治療もしくは遺伝子治療において造血機能を提供するために、上記増殖CB幹細胞集団を必要とする人間の患者に投与することができる。上記増殖CB幹細胞サンプルプールは、静脈内に移植する(注入する)ことが好ましい。ある実施形態では、上記増殖CB幹細胞サンプルは、患者の骨髄系細胞に分化する。別の実施形態では、上記増殖CB幹細胞サンプルは、患者のリンパ球系細胞に分化する。2つ以上の増殖CB幹細胞サンプルからなるプールの投与は、上記プール中の増殖CB幹細胞サンプルが、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない場合にのみ行われる。ある実施形態では、増殖臍帯血幹細胞サンプルプールと、これらの間でHLA抗原または対立遺伝子の型が確立したレピシエント患者との間で、1つのHLA抗原または対立遺伝子が集合的に異なる。他の実施形態では、増殖臍帯血幹細胞サンプルプールと、これらの間でHLA抗原または対立遺伝子の型が確立したレピシエント患者との間で、2つのHLA抗原または対立遺伝子が集合的に異なる。
本発明によれば、治療上効果的な量の、本明細書において上述される本発明の上記各方法によって生成される組換え型または非組換え型増殖CB幹細胞サンプルプールを含んでいる医薬(治療効果のある)組成物を患者に投与することで治療する方法が提供される。ここで、上記プール中の上記サンプルは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない。上記増殖ヒト臍帯血幹細胞サンプルプールの上記投与から12時間以内には、骨髄系前駆細胞集団が上記患者に投与されないことが好ましく、上記骨髄系前駆細胞集団における細胞の大部分は細胞培養においてリンパ球系細胞を生成しない。他の実施形態では、上記増殖ヒト臍帯血幹細胞サンプルプールの上記投与から18、20、24、36、48、または72時間もしくは1週間以内には、骨髄系前駆細胞集団が上記患者に投与されず、上記骨髄系前駆細胞集団における細胞の大部分は細胞培養においてリンパ球系細胞を生成しない。具体的な実施形態では、上記骨髄系細胞集団における細胞の大部分は、細胞表面マーカーCD33を発現し、および/または細胞表面マーカーCD45RAを発現しない。
本発明の2つ以上の異なる増殖CB幹細胞サンプルプールは、上記増殖CB幹細胞を必要とする患者(好ましくは人間の患者)に造血機能を提供するために用いることができる。ここで、上記プール中の上記サンプルは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない。上記増殖CB幹細胞を必要とする患者に投与する増殖CB幹細胞サンプルプールは、上述したように、少なくとも2人の異なる人間の出生時の臍帯血および/または胎盤血に由来するものとすることができる。ある実施形態では、本発明の増殖CB幹細胞サンプルプールの投与は、免疫不全症の治療のために行われる。好ましい実施形態では、本発明の増殖CB幹細胞サンプルプールの投与は、汎血球減少症の治療のため、または好中球減少症の治療のために行われる。患者の罹患する、汎血球減少症または好中球減少症等の免疫不全症は、強化化学療法レジメン、造血細胞移植(HCT)のための骨髄機能廃絶療法、または急性電離放射線への暴露、の結果であることがある。持続性汎血球減少症または持続性好中球減少症を引き起こすおそれがある化学療法薬の例は、特に限定されないが、シスプラチン、カルボプラチン、オキサリプラチン等のアルキル化剤、メクロレタミン、シクロホスファミド、クロラムブシル、およびイホスファミドが含まれる。持続性汎血球減少症または持続性好中球減少症を引き起こすおそれがある他の化学療法剤には、アザチオプリン、メルカプトプリン、並びにビンクリスチン、ビンブラスチン、ビノレルビン、ビンデシン、およびタキサン等のビンカアルカロイドが含まれる。特に、持続性汎血球減少症または持続性好中球減少症を引き起こすおそれがある化学療法レジメンは、クロファラビンおよびAra−Cの投与である。
本発明によれば、上記増殖CB幹細胞を治療に使用する際に限られたHLA型の適合のみが必要である。したがって、本発明では、有用な量を実用的に保存することができると教示されるので、凍結された増殖CB幹細胞の保存は実用的になった。先行技術では、治療に使用する目的で増殖CB幹細胞の有用なサンプルを見つけるために、HLAをレシピエントに適合させることが概して必要になることが予期された。したがって、患者に適合するサンプルを見つけることを概して実行可能とするためには、入手不可能な多さの数の異なる増殖CB幹細胞サンプルを保存しなければならなかった。そのように多数であったので、さらに大きな保存スペースが、増殖ユニットを保存するために必要となって、増殖サンプルを保存することが非実用的となっていた。これに対して、本発明によると、限られたHLAの適合が必要であり、よって、一般的なヒトの集団にとって幹細胞移植において有用な、プールされ、増殖され、その後低温保存された、あるいは、増殖され、プールされ、その後低温保存されたCB幹細胞の「バンク」の生成が実行可能である。これは、本発明の治療の方法において、上記バンク内の任意の増殖CB幹細胞サンプルプールを多数のレシピエントに対して実行可能に用いることができるからである。なお、CB幹細胞サンプルプール、すなわち増殖CB幹細胞サンプルプールは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない。
上記患者に投与される、適切な凍結増殖CB幹細胞サンプルプールおよび/またはそのようにプールされたサンプルの選択は、コンピュータ読み取り可能な記憶媒体に埋め込まれたコンピュータプログラム機構を含むコンピュータプログラムプロダクトを用いて実施することができる。本発明のいくつかの実施形態では、識別子の選択および出力を行い、さらに、凍結保存された増殖CB幹細胞サンプル、またはサンプルプールに対して、任意でロボットを用いた検索を行うための命令をコード化または有するコンピュータシステムもしくはコンピュータプログラムプロダクトが提供される。上記識別子は、上述したように、特定の凍結増殖CB幹細胞サンプルまたは凍結増殖CB幹細胞サンプルの凍結プールを、凍結増殖CB幹細胞サンプルおよび/またはそのプールのバンクに保存された他の凍結増殖CB幹細胞サンプルおよび/またはそのプールと区別する。よって、上記識別子は、サンプルまたはプールごとに固有である。識別子の収集物は、一つまたは複数のコンピュータデータベースに格納されることが好ましく、この場合、各識別子は、好ましくは上記識別子に関連付けられている増殖CB幹細胞サンプル、または場合に応じて増殖CB幹細胞サンプルプールの物理的な位置に関する情報に関連付けられ、および/または上記プールまたはサンプルの一つまたは複数の他の特性に関する情報に関連付けられている。上記他の特性は、特に限定されないが、第6.6部に記載されているように、上記プールまたはサンプルの合計造血幹細胞または造血幹前駆細胞計数(例えば、合計CD34+細胞計数)、上記プールまたはサンプルの合計有核細胞計数、造血幹細胞または造血幹前駆細胞のパーセンテージ(例えば、CD34+細胞のパーセンテージ)、上記プールまたはサンプルの容積、ドナーの性別、上記プールまたはサンプルを凍結させた日、および上記プールまたはサンプルのHLA型、が含まれる。よって、一つまたは複数のデータベースが各凍結増殖CB幹細胞サンプルまたはサンプルプールに関するデータ格納する。上記データベースは、上記保存された凍結増殖CB幹細胞サンプルまたはサンプルプールに関する特性のうちの一つまたは複数を格納する。上記特性は、特に限定されないが、上記プールまたはサンプルの合計CD34+細胞計数、上記プールまたはサンプルの合計有核細胞計数、上記プールまたはサンプルの容積、ドナーの性別、上記プールまたはサンプルの人種または民族、上記プールまたはサンプルを凍結させた日、および上記プールまたはサンプルのHLA型、が含まれる。
ここに記述された本発明の全ての態様に適用可能な本発明の代替的な実施形態では、2つ以上の異なる増殖ヒト臍帯血幹細胞サンプルプールは、「上記プール中の上記サンプルが、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない」ことを特徴とする代わりに、上記プール中の少なくとも1つのサンプルが、上記患者および上記サンプルによって確立した6つのHLA抗原または対立遺伝子の型のうち3つ、4つ、5つ、または6つで上記患者と適合することを特徴としている。このような代替的な実施形態では、上記プール中の他のサンプルは、もしあれば、上記患者のHLA抗原または対立遺伝子と適合せずに、あるいは適合について考慮せずに、投与される。
本実施例に提示されたデータは、迅速かつ一過性の骨髄生着を提供し、免疫不全症患者の自己造血回復を促進する可能性がある既製のHLA不適合製剤として、Notch機能の作動物質を用いて生体外で増殖されたCD34+臍帯血幹細胞の有用性を支持するものである。従来技術においては、HLA適合が求められるため、個々の患者が適合するユニットを得るには、実現不可能な数の増殖前ユニットが必要となり、予め生体外増殖を行っておくことは不可能であった。一方、臍帯血幹細胞にHLA適合が不要または制限付HLA適合が必要である場合、増殖されていない低温保存の細胞の「バンク」を生成することができ、その製剤はすぐに利用できるであろう。
CD34+またはCD34+CD38-ヒト臍帯血前駆細胞集団から出発したSCID再構築細胞(SRC)の成長特性および生成が比較された。濃縮CD34+CD38-臍帯血前駆細胞は、Delaney et al(2005,Blood 106: 1784-1789)に記載されているように、Notchを介した増殖のための出発細胞集団として用いた。細胞は、シトキン(SCF 300ng/ml、Flt3L 300ng/ml、TPO 100ng/ml、IL-6 100ng/ml、IL-3 10ng/ml、「5GF」と称する)が補充された無血清状態で、フィブロネクチン断片と固定化培養Notchリガンド(Delta1ext-IgG)または対照ヒトIgGとの存在下で17〜21日間培養した。Delta1ext-IgGは、ヒトIgG1のFcドメインを融合したDelta1の細胞外ドメインからなる。CD34+出発細胞集団とCD34+CD38-出発細胞集団とにおいて、CD34+細胞増殖倍率138±64および163±64(平均±標準誤差、p=0.1612、データ不図示)での、それぞれの発生したCD34+細胞の絶対数には大きな差は見られなかった。しかしながら、注入後3週間、6週間、10週間の生体内NOD/SCID再構築力を評価したところ、CD34+出発細胞集団がCD34+CD38-出発細胞集団と比較して用いられた場合に、レシピエントマウスの骨髄においてヒト生着が向上していた(Delta1ext-IgGの存在下で培養された、CD34+出発細胞集団とCD34+CD38-出発細胞集団とにおいて、平均CD45%:3週間で6.7%対1.6%、p=0.02;10週間で1.0%対0.2%、p=0.1)。また、5GFの組み合わせは、CD34+細胞の生体内生成と、限界希釈法によって得られたSRC出現率とに対して少量のシトキンを利用した組み合わせより優れていた(データ不図示)。
UCB再構築細胞のNotchを介した生成のための最適条件を確認し、臍帯血幹・前駆細胞の発生のための閉鎖系を調べるための実験を行った。無血清培地においてシトキン(10ng/mlのIL-3、100ng/mlのIL-6およびTPO,300ng/mlのSCFおよびFlt3リガンド)と低濃度リポタンパク(20ng/mlのLDL)との存在下、CH−296フィブロネクチン断片とともに組織培養容器の表面に固定されたDelta1ext-IgGを用いて、ヒトCD34+臍帯血細胞を17日間培養した。再構築細胞の生成数は、定量限定希釈法によって求めた。ここで、8〜15匹のマウスが1.5×105、3×104、または6×103の非培養細胞あるいは3×104、6×103、または1.2×103の培養後代細胞を受容していた。ただし、非培養細胞を受容していたマウスは、アクセサリー細胞として放射線照射された2×105のCD34-細胞をも受容しており、生着が促進されていた。一方、そのようなアクセサリー細胞の機能は培養中に分化骨髄細胞によってもたらされるため、培養細胞はアクセサリー細胞を必要としない。
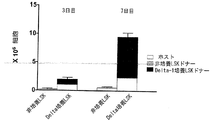
三つの独立した実験において、上記8.2に示すように製造されたDelta1ext-IgG培養ヒト臍帯血幹・前駆細胞の生着を、Delta1ext-IgGで培養されていないヒト臍帯血幹・前駆細胞の生着と比較したところ、非培養臍帯血幹細胞を受容したマウスへの移植後10日での生着はほとんど見られなかった。一方、Delta1ext-IgG培養ヒト臍帯血幹・前駆細胞を受容したすべてのマウスにおいては、ヒト抗体CD33/CD45の共発現によって測定されたとき、>95%の骨髄性細胞からなるヒト生着が>0.5%の水準で生着した(図3参照)。よって、上記データを総合すれば明らかなように、Delta1ext-IgGを用いて臍帯血前駆細胞を培養することによって、NOD/SCID再構築細胞の生体内生成と出現率が著しく向上し、その結果、NOD/SCIDマウスモデルにおけるヒト生着の動態と水準とが向上する。
免疫不全マウスモデルを使って、低温保存された生体外増殖前駆細胞の生着能を評価した。低温保存された生体外増殖前駆細胞は、上記8.2に記載の方法に従って増殖した。最初の実験として、採取直後に免疫不全マウスに直接注入されたヒト増殖細胞と、増殖後に採取し、後の使用のために低温保存しておいたヒト増殖細胞とについて生体内再構築能を比較した。培養し、(造血細胞の低温保存に使用されるDMSO含有標準培地中にて)低温保存し、そして移植前に解凍した細胞と、培養の終了時に採取し、新鮮な状態で注入した増殖前駆細胞との生体内再構築能において、顕著な差は見られなかった(図4a参照)。また、実験をさらに行い、増殖細胞産物の再構築能は、低温保存後でも維持されることがわかった。図4bに示すように、ヒト増殖低温保存細胞を受容したすべてのマウスは、注入後2週間で8%、4週間で7%の総合的な平均ヒト生着率で生着した(骨髄中>0.5%のヒト抗体CD45で定義)。またさらに、個々に異なる三つの解凍方法(解凍と洗浄、解凍と多糖体/ヒト血清アルブミンでの希釈、解凍と直接注入)においても比較されたが、これら評価した三つの方法においても顕著な差は見られなかった(図4c参照)。
以下で説明されるマウスモデルを用いた研究によれば、マウス造血前駆細胞(LSK細胞)に由来する前駆細胞の数を増やすことで、H−2不適合レシピエントに移植した場合に短期生着を提供することができるということが分かっている。C57BL/6.J Ly5.1(CD45.1)マウスのLSK細胞は、上述したようにDelta1ext-IgGを用いて4週間培養された(Dallas et al.,2007, Blood 109: 3579-3587参照)。類似遺伝子型移植については、致死量の放射能が照射されたC57BL/6(H−2b、CD45.1)マウスは、105個のC57BL/6(H−2b、CD45.1)同系の全骨髄とともに、106個のDelta1ext-IgG培養Ly5.2(H−2b、CD45.2)初代LSK細胞を受容した。一方、異質遺伝子型移植については、致死量の放射能が照射されたBALB.c(H−2d、CD45.1)レシピエントは、106個のBALB.c(H−2d、CD45.1)同系の全骨髄とともに、106個のLy5.2(H−2b、CD45.2)Delta1ext-IgG培養LSK細胞を受容した。マウスの末梢血に対して、移植後数回にわたってFACS分析を行い、ドナーキメリズムを評価した(図5参照)。データによれば、上記Delta培養細胞は、主なH−2不適合で移植した場合に短期ドナー生着を提供することができるとういことが分かる。
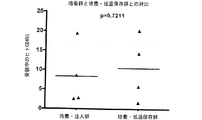
上記を臨床的に直接解釈すると、骨髄機能廃絶移植前処置の後、進行中の臍帯血移植試験段階1(FHCRC Protocol 2044)に生体外増殖臍帯血前駆細胞を使用するとの結論に至った。上記試験段階1の結果、このプロトコルが安全であるということだけでなく、さらに重要なことに、生体外増殖造血前駆細胞による骨髄生着が迅速であったこと、そしてその結果、絶対好中球係数500/μlに到達するまでの中位時間がたった14日にまで大幅に減少したことが明らかになった。このことは、本研究機関にて同じ治療計画で二つの非操作臍帯血ユニットを用いて中央値26日で生着した患者群(N=20)と比較しても、統計的に有意な(p=0.002)生着時間の減少である(図12参照)。これら二つの群は、年齢、体重、診断、非操作臍帯血ユニットによる細胞注入量の点で、大きく異ならなかった。>100/μlのANC閾値は、異質遺伝子型幹細胞移植後の延命効果と強い相関があることが示唆された(Offner et al., 1996, Blood 88:4058参照)。登録患者のうち、>100/μlのANC閾値に到達するのに必要な時間の中央値は、(上述の)従来の設定(p=0.006、データ不図示)では19日であるのに対して、9日であった。
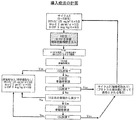
以下、図13のフローチャートを参照しながら、増殖ヒト臍帯血幹細胞サンプルの製造と保存について説明する。
10.1 設計
増殖ヒト臍帯血幹細胞の投与による、強化導入化学療を受けた急性骨髄性白血病(AML)患者における造血機能の急速な回復を目的とした、臨床実験の設計について説明すれば以下の通りである。本研究では、1群当たり10〜15人の患者からなる3群が登録される。各群に対して、病状に応じた個別の試験対象患者基準を設けた。A群にはまず合計10人の患者が登録された。安全基準を満たすのであれば、合計15人の患者でB群を構成する。さらに、安全基準が満たされるのであれば、合計15人の患者でC群を構成する。
A群:WHO基準で急性骨髄性白血病と診断。再発性または治療抵抗性。急性前骨髄球性白血病[t(15;17)(q22;q12)転座と変種を持つ急性前骨髄球性白血病]患者で三酸化ヒ素を用いた療法に効果のなかった患者はA群に含まれる。この群に属する患者は1年未満の初期寛解期を経ており、かつ救援化学療法は受けた経験がない。
B群:予後不良の細胞遺伝学的異常または分子的異常をもった未治療急性骨髄性白血病患者。
C群:予後中度の未治療急性骨髄性白血病患者。
1.まず、各グループに3人の60歳未満の患者を登録する。その後、18歳以上70歳以下の患者を適格とする。
2.各グループの3患者は、ECOG一般状態が0〜1であり、その後、ECOG一般状態が0〜2であることが求められる。
3.患者は、以下の検査値で示されるような適切な腎臓機能および肝臓機能を有する。
a.血清クレアチニン≦1.0mg/dL。血清クレアチニン>1.0mg/dLの場合、推定糸球体濾過速度(glomerular filtration rate;GFR)は60mL/min/1.73m2より高くなければならない。推定糸球体濾過速度(GFR)は、Modification of Diet in Renal Diseaseの式によって求められる。上記式では、推定GFR(ml/min/1.73m2)=186×(血清クレアチニン)−1.154×(年齢)−0.023×0.742(女性患者の場合)×1.212(黒人患者の場合)で表される。
b.血清総または直接ビリルビン≦1.5×正常上限(upper limit of normal;ULN)、アスパラギン酸トランスアミナーゼ(AST)/アラニントランスアミナーゼ(ALT)≦2.5×ULN、アルカリン・ホスファターゼ≦2.5×ULN
4.研究の治験的性質、潜在的リスク、および利益への理解と、有効なインフォームド・コンセントの提示。
5.妊娠能力がある女性患者は、登録前2週間以内に行う血清娠検査で陰性であること。
6.男性および女性患者とも治験中と治験後最低6ヶ月間は効果的な避妊方法をいとわずに用いなければならない。
7.パネル反応性抗体(panel reactive antibody;PRA)が陰性、あるいは臍帯血抗原に対してドナー指向でないことが特徴付けられ分かっている特異抗体を持っている。
1.異質遺伝子型移植物のレシピエント。
2.現在、併用化学療法、放射線療法、または上記プロトコルに記載された以外の免疫療法を受けている者。
3.重度の併発症を患っている者、または心臓・腎臓・肺に関連する重度の臓器機能不全または疾患(症候性肺炎、肺静脈閉塞性疾患を含む)あるいはその他の臓器機能不全の病歴のある者。
4.制御不可能な全身系の真菌感染、細菌感染、ウイルス感染、あるいは他の感染を患っている者(適切な抗生物質や他の治療を施しているにもかかわらず、感染の兆候を示し回復の兆しのない者)。
5.妊婦または授乳中の女性。
6.患者の安全やコンプライアンスを脅かしたり、同意・治験への参加・フォローアップ・治験結果の解釈に影響を及ぼしたりする併発症または疾患、精神疾患を抱えている者。
1.2回目の増殖細胞製剤を投与する患者に対しては、その製剤の選定の前に再度パネル反応性抗体(PRA)検査を行う。
1.レシピエントの体重(kg)当たりに注入される総有核細胞投与量は、1×108個を超えてはならない。
2.レシピエントの体重(kg)当たりに注入されるCD34+細胞数の上限はない。
3.すべての増殖細胞産物を、凍結前にCD3+細胞に対して、免疫表現型検査によって評価する。CD3+細胞集団の存在が確認されず、T細胞(CD3+)集団が確認された製剤は、CD3+細胞数がレシピエントの体重(kg)当たり5×105個未満でない限り、使用されない。
1.形態学に基づいて骨髄芽球中に5%未満と定義される、残存白血病ではない。
2.これまで、髄外毒性のグレードが3〜4ではない。
3.好中球計数が500/μlにまで回復している(G-CSF上外に関係なく)
4.制御不可能な感染症に罹患していない。
5.初回の増殖細胞産物注入時に重度の拒絶反応を示していない。
1.すべての患者に対して、1回目の導入サイクルを行い、その後、増殖臍帯血前駆細胞を注入する(図14の「サイクル1」参照)。適格者に対してのみ、図14の「導入サイクル2の連続増殖細胞導入適格」に示すように、導入サイクル2で2回目の増殖臍帯血前駆細胞の注入を行う。適格者以外のすべての患者に対しては、図14に示すように、増殖臍帯血前駆細胞を注入せず再寛解導入療法を行う。
2.患者が2回目の増殖前駆細胞の注入が適格かどうかにかかわらず、クロファラビン、Ara−C、G-CSFの投与量は導入サイクル1と2において同じである。
3.最も近いバイアルサイズに切り上げた5μg/kgのG-CSFを、化学療法の24時間前に皮下注入し、1日に1回5日目まで注入し続ける。増殖細胞製剤の注入を6日目に行い、その日にG-CSF行う。7日目にG-CSFの注入を再開し、2日連続で絶対好中球計数(ANC)が2000を超えるまでG-CSFを毎日継続する。
4.25mg/m2のクロファラビンを、1日に1回1時間かけて5日間静脈投与する。
5.クロファラビン注入開始4時間後、2mg/m2のAra−Cを、1日に1回2時間かけて5日間静脈投与する。
6.本発明の増殖・低温保存臍帯血幹細胞を注入する。
1.幹細胞移植などの治療を別途今後受けるかどうかによって、寛解期(形態学に基づいて骨髄芽球中に5%未満と定義)にある患者に対して、2サイクル分の地固め療法を行うことができる。2サイクルの増殖細胞注入または増殖細胞注入なしの再導入を行ったあと治療抵抗性を示す患者は、本治験から除外される。
2.最も近いバイアルサイズに切り上げた5μg/kgのG-CSFを、化学療法の24時間前に皮下注入し、2日連続で絶対好中球計数(ANC)が2000を超えるまでG-CSFを毎日継続する。
3.20mg/m2のクロファラビンを、1日1回1時間かけて5日間静脈投与する。
4.クロファラビン注入開始4時間後に、2mg/m2のAra−Cを、1日1回2時間かけて5日間静脈投与する。幹細胞移植などの治療を別途今後受けるかどうかによって、寛解期(形態学に基づいて骨髄芽球中に5%未満と定義)にある患者に対して、2サイクル分の地固め療法を行うことができる。2サイクルの増殖細胞注入または増殖細胞注入なしの再導入を行ったあと治療抵抗性を示す患者は、本治験から除外される。
A.治療前の評価
1.精密検査
2.病歴: 病歴、治療歴、治療成績に関する詳細な書類の作成
3.ECOG一般状態
4.12誘導心電図
5.血液学:分画と血小板数を含むCBC、および末梢血塗抹標本
6.血液生化学検査:電解質(ナトリウム、カリウム、塩素、重炭酸塩)、血中尿素窒素(BUN)、クレアチニン、グルコース、肝機能検査(アスパラギン酸アミノトランスフェラーゼ(AST)かつ/またはアラニン・アミノトランスフェラーゼ(ALT)、アルカリホスファターゼ(ALP)、総ビリルビン、乳酸脱水素酵素(LDH))。
8.G-CSF初回投与時からの有害事象評価
9.血液病理学、細胞遺伝学/FISH、フローサイトメトリーを含む、骨髄医療診断報告書の初期基準
10.移植後キメリズムを順次決定するために、患者からヘパリン添加末梢血を採取し、DNA鑑定によるキメリズム解析。
1.健康診断、および提供者によるシステムレビュー
2.看護師による体重測定(weight by nursing)
3. CBC[CBD](HCT、HGB、WBC、RBC、指数、血小板、分画/塗抹標本の評価を含む)
4.[SRFM]と[SHFL](マグネシウムを含む造血幹細胞移植(HSCT)腎機能パネル)と、乳酸脱水素酵素(LD)を含むHSCT肝機能パネル;SRFMはナトリウム、カリウム、塩素、二酸化炭素、グルコース、血中尿素窒素、クレアチニン、カルシウム、リン、アルブミン、マグネシウムを含む。SHFLは、ALT、AST、ALK、BILIT/D、トリポネーマパリダム(TP)、アルブミン、LDを含む)
5.精密尿検査。
1.生体外増殖臍帯血前駆細胞注入中は、正看護師(RN)が立会わなければならない。
1.CBC[CBD](HCT、HGB、WBC、RBC、指数、血小板、分画/塗抹標本の評価を含む)。
3.精密的尿検査。
1.生着率の研究:増殖細胞産物注入後7、14、21、28、56日目に(あるいは化学療法サイクルの13、20、27、34、62日目に)、増殖細胞産物による造血機能回復への寄与率を、選別された末梢血(CD3+、CD33+、CD14+、CD56+分画ごとに選別された細胞)から評価する。14日目時点で患者が100%ホストの場合は、それ以降の分析はその患者に対して一切行わない。注入された増殖細胞による生着が56日目においても持続していることが明らかな場合は、ドナーとホストの生着の動態を観察する必要に応じてドナーとホストのキメリズム解析を2〜4週間ごとに行う。ドナーとホストのキメリズムの割合は、ポリメラーゼ鎖反応(PCR)に基づいた反復配列多型分析(VNTR)配列の増殖によって評価される。VNTR配列はドナーとホスト固有のものであり、ホスホイメージ分析によって定量化される。
a.化学療法開始前(かつ同意を得たあと):40mlの末梢血を上部が緑色の管に採集し、ドナー/ホスト免疫学的相互反応を評価する研究のためにEBV性トランスフォームLCL株を発生させる。
b.最初の2年間は3〜6ヶ月ごとに、その後3年間は年1回担当医または患者と接触し、病気の発生の有無と生存率に関するデータを評価する。
1.血液製剤:すべての血液製剤に対して放射線を照射し、白血球を減少させておく。また、CMV陰性患者に対して、制度的標準技法ガイドラインにしたがって、血液製剤を投与する。症候性貧血の場合、または臨床環境に対応した標準閾値を下回る場合には輸血を行う。
1.増殖細胞産物の注入投与に対して重度の拒絶反応を示した場合。この場合、患者に対して増殖細胞産物をさらに投与することはできない。
2.患者の病気の進行が明らかな場合。
3.患者の様態の変化のため治療続行不可能であると治験者が判断した場合。
4.患者自身が治験対象から外れることを選択した場合。
5.患者が妊娠、あるいは妊娠する可能性があるにもかかわらず適切な避妊を怠った場合。
6.患者がプロトコル要件を満たすことができない場合。
感染症の頻発は、AML治療で用いられる導入化学療法および救助療法によく見られる合併症であり、実際、治療失敗の主な原因のひとつである。クロファラビンおよび高用量ara−cを顆粒細胞コロニー刺激因子(G−CSF)と組み合わせて用いることは、AML治療におけるI/II段階の試験(Becker et al., 2008, Blood 112 ASH Annual Meeting Abstracts)で研究されている(以下、このような化学治療サイクルを「GCLAC」と称する)。クロファラビンは強い抗白血病作用があり、クロファラビンおよび高用量ara−cをG−CSFと組み合わせることは、より一般的に使用されるイダルビシンとara−cとの組み合わせと少なくとも同等の効果を有するものと考えられる。しかしながら、クロファラビンはまた、3週間を超えるGCLACの後で持続性好中球減少症の期間を経ると、免疫抑制性が高く、ara−cと組み合わせると高い骨髄抑制効果を示す。クロファラビンにおける免疫抑制効果と骨髄抑制効果とが組み合わさること、および造血機能回復が遅れることによって、感染症が頻発し高用量治療の妨げになる。当センターで治療を受けた患者群のうち、50%未満にはGCLACの後で感染合併症がみられ、約13%には4級感染症がみられた(Becker et ah, 2008, Blood 112 ASH Annual Meeting Abstracts)。重要なことは、増殖ヒト臍帯血幹細胞および前駆細胞の注入によって上記双方の問題を解決できるということである。また、クロファラビンに基づいた療法による免疫抑制は、増殖ヒト臍帯血幹細胞サンプルが一時的に生着し臨床的利点をもたらす可能性を高める。
増殖ヒト臍帯血幹細胞を投与することによって、自家移植に備えて強化化学療法および/または放射線治療を受けたホジキンリンパ腫、非ホジキンリンパ腫、多発性骨髄腫の患者に対して造血機能の迅速な回復を提供することを目的とした臨床実験の設計について説明すれば以下の通りである。本研究には、以下に挙げる特徴を有する患者が登録される。
血清クレアチニン≦2.0mg/dL
血清クレアチニン>2.0mg/dlの場合、推定糸球体濾過量(glomerular filtration rate;GFR)は、Modification of Diet in Renal Diseaseの式で計算されるように60ml/min/1.73m2未満でなければならない。上記式では、推定GFR(ml/min/1.73m2)=186×(血清クレアチニン)−1.154×(年齢)−0.023×(0.724 女性患者の場合)×(1.212 黒人患者の場合)で表される。
アスパラドン酸トランスアミナーセ(AST)/アラニントランスアミナーゼ(ALT)≦2.5×ULN、
アルカリホスファターゼ≦2.5×ULN。
1.細胞投与量を1×109TNC/kg以下に維持することを目的に解凍時約20%の細胞消失を見込んで、TNC/kg低温保存前細胞投与量は、レシピエントの体重(kg)当たりの総有核細胞計数は1.2×109個を超えてはならない。
2.レシピエントの体重(kg)当たりに注入されるCD34+細胞数の上限はない。
3.すべての増殖細胞産物を、凍結前にCD3+細胞に対して、免疫表現型検査によって評価する。CD3+細胞集団の存在が確認されず、T細胞(CD3+)集団が確認された製剤は、CD3+細胞投与量がレシピエントの体重(kg)当たり5×105個未満でない限り、使用されない。
A.末梢血幹細胞採取:末梢血幹細胞(peripheral blood stem cell;PBSC)は既知の動員方法の何れかを使用し、白血球除去療法によって採取される。少なくとも1.0×106CD34+cells/kgが移植に利用可能でなければならない。
B.高用量移植前処置療法
多発性骨髄腫患者
メルファラン200mg/m2を使用する標準移植前処置が全患者に使用される。
全身被爆(total body irradiation: TBI)ベースの療法は、事前の高線量TBIを受けていない患者に行われる(何れのcritical normalの臓器(肺、肝臓、脊髄など)に対しても>20Gy)。
投与量:移植前処置7日目、300mg/m2のカルムスチンが3時間かけて1回静脈投与される。カルムスチンは、溶液と注入されたり重炭酸塩溶液を含んでいるまたは含んでいたチューブで注入されたりするべきではない。
投与量:移植前処置6、5、4、3日目、エトポシド100mg/m2が1日2回、2時間にわたり静脈投与される。通常の塩水500〜1000ccで投与され、計800mg/m2投与される。
投与量:移植前処置6、5、4、3日目、1日2回シタラビン100mg/m2が3時間かけて静脈投与される。
投与量:移植前処置2日目、メルファラン140mg/m2が1回、30分かけて静脈投与される。
1.0日目の朝に自家PBSCが解凍され注入される。
G−CSF:自家幹細胞注入および増殖細胞注入の翌日より最も近いバイアルサイズに切り上げた5mcg/kgが皮下投与(SQ)される。G−CSFは2日間連続でANC>2000となるまで毎日継続される。
A.移植前の評価
1.病歴、健康診断、カルノフスキー・スコア
2.CBC、血清ナトリウム、カリウム、CO2、BUN、クレアチニン、尿酸、LDH、カルシウム、ビリルビン、アルカリホスファターゼ、AST、ALT、肝炎検査、ABO/RH血液型、血液クロスマッチ、CMV、VZV、HSV、HIV、トキソプラズマ症血清学
3.CT/PET(リンパ腫)
4.骨格のMRI、病期診断に必要となる骨測量(骨髄腫)
5.骨髄穿刺吸引および生検、病理学・流動細胞計測・FISHを含む細胞遺伝学へのサンプル
6.血清タンパク質電気流動および免疫固定(骨髄腫)
7.定量的血清免疫グロブリンレベル、ベータ2ミクログロブリン
8.クレアチニンクリアランスおよびタンパク質総排出量を調べるための24時間にわたる採尿、尿タンパク質電気流動、定量的ベンス・ジョーンズ排出および免疫固定(骨髄腫)
9.肺機能検査(pulmonary function tests:PFTS)、マルチゲート収集法(multigated acquisition scan:MUGA)
10.臨床免疫再構築研究。
1.最下点の後(following the nadir)、ANC>500/ul、血小板数>20,000/μlに到達するまでCBCを毎日実施
2.電解室パネル(ナトリウム、カリウム、クロライド、CO2、カルシウム、マグネシウム、リン、アルブミン、BUN クレアチニン)を少なくとも週3回
3.肝機能テスト(ALT,AST、ALKホスファターゼ、ビリルビン、LDH)を少なくとも週2回。
1.健康診断、および提供者によるシステムレビュー
2.看護師による体重測定
3.CBC[CBD](HCT、HGB、WBC、RBC、指数、血小板、分画/塗抹標本の評価を含む)
4.[SRFM]と[SHFL](マグネシウムを含む造血幹細胞移植(HSCT)腎機能パネル)と、乳酸脱水素酵素(LD)を含むHSCT肝機能パネル;SRFMはナトリウム、カリウム、塩素、二酸化炭素、グルコース、血中尿素窒素、クレアチニン、カルシウム、リン、アルブミン、マグネシウムを含む。SHFLは、ALT、AST、ALK、BILIT/D、トリポネーマパリダム(TP)、アルブミン、LDを含む)
5.精密尿検査。
1.注入中は正看護師(RN)が立ち会わなければならない。
1.CBC[CBD](HCT、HGB、WBC、RBC、指数、血小板、分画/塗抹標本の評価を含む)。
1.最下点の後、ANC>500/ul、血小板数>20,000/μlに到達するまでCBCを毎日行う。その後の28日目までは週3回、60日目までは週2回CBCが行われる。
1.病歴、健康診断、カルノフスキー・スコア。
臨床研究(可能であれば行う)
1.28日目、60日目、100日目、6ヵ月目、1年目、2年目に定量的免疫グロブリンレベル(IgG、IgA,IgM)を評価する。
1.臨床的理由により、6ヶ月間の完全血球算定、腎機能、肝機能検査を行う。必要に応じて毒性または反応期間を規定。
1.すべての血液製剤に対して放射線を照射し、白血球を減少させておく。また、CMV陰性の患者にはCMVに安全な血液産物が与えられる。症候性貧血の場合、または臨床設定に対応した標準閾値を下回る場合には輸血を行う。
このプロトコルは、人間の患者における急性骨髄性白血病(acute myeloid leukemia;AML)の治療のための本発明の増殖ヒト臍帯血幹細胞サンプルと併用した一つまたは複数の臍帯血/胎盤血ユニットの投与を含む。臍帯血移植物は、赤血球細胞を除去したことを除いて、臍帯および/または胎盤全血であった。
Claims (54)
- 造血機能を必要とする人間の患者に造血機能を提供するための方法であって、
上記患者に増殖ヒト臍帯血幹細胞サンプルプール、またはそのアリコートを投与する工程を含み、
上記プールは、2つ以上の異なる増殖ヒト臍帯血幹細胞サンプルを含み、上記プール中の各サンプルは、異なる人間の出生時の臍帯血および/または胎盤血から由来し、上記プール中の上記サンプルは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならず、
上記プール中の上記増殖ヒト臍帯血幹細胞サンプルそれぞれには、増殖技術が施されており、この増殖技術によって、増殖技術が施されたヒト臍帯血幹細胞サンプルのアリコートにおける造血幹細胞、または造血幹前駆細胞は、増殖技術が施される前の上記ヒト臍帯血幹細胞サンプルのアリコートに対して、少なくとも50倍増加することが示される、方法。 - 上記造血幹細胞、または造血幹前駆細胞は、CD34+であることを特徴とする請求項1に記載の方法。
- 上記プール中の2つ以上のサンプルは、上記患者によって確立しかつ上記サンプルによって確立した1つまたは2つのHLA抗原または対立遺伝子の型で、上記患者と不適合となる、請求項1または2に記載の方法。
- 上記プール中の2つ以上のサンプルは、上記患者によって確立した2つのHLA抗原または対立遺伝子の型で、上記患者と不適合となる、請求項1〜3の何れか一項に記載の方法。
- 造血機能を必要とする人間の患者に造血機能を提供するための方法であって、
(a)複数の増殖ヒト臍帯血幹細胞サンプルプールから上記患者に投与するための増殖ヒト臍帯血幹細胞サンプルプールを選択する工程と、
(b)上記患者に上記選択したサンプルまたはそのアリコートを投与する工程と、を含み、
上記プールは、2つ以上の異なる増殖ヒト臍帯血幹細胞サンプルを含み、上記プール中の各サンプルは、異なる人間の出生時の臍帯血および/または胎盤血から由来し、上記プール中の上記サンプルは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない、方法。 - 上記選択する工程は、さらに、2つを超えるHLA抗原または対立遺伝子が上記患者によって確立したHLA抗原または対立遺伝子の型の患者と不適合となるサンプルを有するサンプルプールを取り除く工程を含む、請求項5に記載の方法。
- 上記選択する工程は、さらに、2つまたは1つのHLA抗原または対立遺伝子が上記患者によって確立したHLA抗原または対立遺伝子の型の患者と不適合となるサンプルを有するサンプルプールを受入れる工程を含む、請求項5または6に記載の方法。
- 上記選択する工程は、さらに、2つまたは1つのHLA抗原または対立遺伝子が上記患者によって確立したHLA抗原または対立遺伝子の型の患者と不適合となるサンプルを有するサンプルプールを受入れる工程を含む、請求項5〜7の何れか一項に記載の方法。
- 上記選択は、少なくとも50個の凍結された増殖ヒト臍帯血幹細胞サンプルプールの中から行われる、請求項5〜8の何れか一項に記載の方法。
- 各プール内のすべてのサンプルは、同じ人種の人間の臍帯血および/または胎盤血に由来する、請求項1〜9の何れか一項に記載の方法。
- 各プール内のすべてのサンプルは、同じ民族の人間の臍帯血および/または胎盤血に由来する、請求項1〜9の何れか一項に記載の方法。
- 上記各増殖ヒト臍帯血幹細胞サンプルプールは、少なくとも7、500万個の生存CD34+細胞を含んでいる、請求項1〜11のいずれか一項に記載の方法。
- 一人の人間の出生時の臍帯血および/または胎盤血から得られ単離された、ヒト臍帯血幹細胞またはヒト臍帯血幹前駆細胞を生体外で増殖させる工程を含む方法によって、各プール中の異なる増殖ヒト臍帯血幹細胞サンプルそれぞれを生成する工程をさらに含む、請求項1〜12のいずれか一項に記載の方法。
- 各プール中の異なる増殖ヒト臍帯血幹細胞サンプルそれぞれには、増殖技術が施されており、この増殖技術によって、増殖技術が施されたヒト臍帯血幹細胞サンプルのアリコートにおける造血幹細胞、または造血幹前駆細胞は、上記増殖技術が施される前の上記ヒト臍帯血幹細胞サンプルのアリコートに対して、少なくとも50倍増加することが示される、請求項5〜13のいずれか一項に記載の方法。
- 上記造血幹細胞、または造血幹前駆細胞は、陽性のCD34+である、請求項14に記載の方法。
- 上記増殖させる工程は、上記ヒト臍帯血幹細胞を、Notch機能を持つアゴニストに接触させる工程を含む、請求項13に記載の方法。
- 各プール中の異なる増殖ヒト臍帯血幹細胞サンプルそれぞれには、増殖技術が施されており、この増殖技術によって、増殖技術が施されたヒト臍帯血幹細胞サンプルにおけるSCID再構築細胞の数は、上記増殖技術が施される前の上記ヒト臍帯血幹細胞サンプルに対して、増加することが示される、請求項1〜13のいずれか一項に記載の方法。
- 上記増殖技術によって、増殖技術が施されたヒト臍帯血幹細胞サンプルのアリコートにおけるCD34+細胞は、上記増殖技術が施される前の上記ヒト臍帯血幹細胞サンプルのアリコートに対して、少なくとも50倍増加することが示される、請求項14に記載の方法。
- 上記各増殖ヒト臍帯血幹細胞サンプルプールは、上記投与する工程の前に凍結され、
上記投与する工程の前に各プールを解凍する工程をさらに含むことを特徴とする請求項1〜18のいずれか一項に記載の方法。 - 造血機能を必要とする人間の患者に造血機能を提供するための方法であって、
(a)それぞれが出生時の異なる人間から得られた少なくとも2つの臍帯血および/または胎盤血のサンプルをプールして、プールされた臍帯血を生成する工程と、
(b)プールされた臍帯血からの造血幹細胞または造血幹前駆細胞を濃縮して、造血幹細胞または造血幹前駆細胞を濃縮した集団を生成する工程と、
(c)造血幹細胞または造血幹前駆細胞を濃縮した集団を生体外で増殖させて、増殖幹細胞サンプルを生成する工程と、
(d)造血機能を必要とする人間の患者に上記増殖幹細胞サンプルまたはそのアリコートを投与する工程とを含み、
上記増殖幹細胞サンプルは、上記患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で不適合とならない、方法。 - 上記工程(c)の後かつ上記工程(d)の前に、上記増殖幹細胞サンプルを凍結し解凍する工程をさらに含む、請求項20に記載の方法。
- 上記患者は、汎血球減少症または好中球減少症に罹患している、請求項1〜21のいずれか一項に記載の方法。
- 上記汎血球減少症または好中球減少症は、強化化学療法、造血細胞移植のための骨髄機能廃絶療法、または急性電離放射線への暴露によって引き起こされる、請求項22に記載の方法。
- 増殖ヒト臍帯血幹細胞サンプルの凍結バンクを生成するための方法であって、
(a)異なる二人以上の人間の出生時の臍帯血および/または胎盤血のプールから得られた造血幹細胞または造血幹前駆細胞を濃縮した集団内に存在するヒト臍帯血幹細胞を生体外で増殖させて、増殖ヒト臍帯血幹細胞サンプルを生成する工程と、
(b)上記増殖ヒト臍帯血幹細胞サンプルを凍結して、増殖ヒト臍帯血幹細胞の凍結サンプルを生成する工程と、
(c)上記増殖ヒト臍帯血幹細胞の凍結サンプルを保存する工程と、
(d)上記工程(a)〜(c)を少なくとも50回繰り返して、少なくとも50個の増殖ヒト臍帯血幹細胞サンプルの凍結保存バンクを生成する工程と、を含み、
上記工程(a)〜(d)は、上記記載の順序で行われる、方法。 - 上記増殖ヒト臍帯血幹細胞の各凍結サンプルに対して、増殖ヒト臍帯血幹細胞の凍結サンプルを他の増殖ヒト臍帯血幹細胞の凍結サンプルと区別する識別子を割り当てる工程をさらに含む、請求項24に記載の方法。
- 一つまたは複数のコンピュータデータベースに各識別子を格納する工程をさらに含み、
上記格納された識別子は、上記識別子に対応する増殖ヒト臍帯血幹細胞の凍結サンプルが保存される上記バンク内の物理的な位置情報に関連付けられている、請求項24または25に記載の方法。 - 少なくとも50ユニットの増殖ヒト臍帯血幹細胞の凍結サンプルプールを含み、各プールは、2つ以上の異なる増殖ヒト臍帯血幹細胞サンプルを含み、上記プール中の各サンプルは、異なる人間の出生時の臍帯血および/または胎盤血から由来し、上記プール中の上記サンプルは、各プール中のサンプルそれぞれによって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない、血液バンク。
- 造血機能を必要とする人間の患者に造血機能を提供するために用いられる増殖ヒト臍帯血幹細胞の凍結サンプルを選択するためのコンピュータで行われる方法であって、
(a)コンピュータデータベースに格納されている少なくとも50個の複数の識別子から識別子を選択する工程と、
(b)上記選択された識別子を出力または表示する工程と、を含み、
上記工程(a)において、各識別子は、増殖ヒト臍帯血幹細胞サンプルの凍結保存プールを識別し、各プールは、2つ以上の異なる増殖ヒト臍帯血幹細胞サンプルを含み、上記プール中の各サンプルは、異なる人間の出生時の臍帯血および/または胎盤血から由来し、選択された識別子によって識別されたプール中のサンプルは、患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならず、上記選択では、上記識別子によって識別されるプールまたはそのアリコートの、必要とする患者への投与のために、増殖ヒト臍帯血幹細胞サンプルプールを識別するとともに、
上記工程(a)および(b)は、適切にプログラムされたコンピュータによって実行される、方法。 - 上記出力または表示する工程では、さらに、上記識別子によって識別された増殖ヒト臍帯血幹細胞サンプルの各プールの物理的な位置情報を出力または表示する、請求項28に記載の方法。
- 識別された各増殖ヒト臍帯血幹細胞サンプルプールのロボット検索を実行する工程をさらに含む、請求項28または29に記載の方法。
- コンピュータシステムと併用され、コンピュータ読み取り可能な記憶媒体とその中に埋め込まれたコンピュータプログラム機構とを含むコンピュータプログラムプロダクトであって、
上記コンピュータプログラム機構は、
(a)コンピュータデータベースに格納されている少なくとも50個の複数の識別子から識別子を選択するための実行可能な命令と、
(b)上記選択された識別子を出力または表示するための実行可能な命令と、を含み、
上記実行可能な命令(a)において、各識別子は、増殖ヒト臍帯血幹細胞サンプルの凍結保存プールを識別し、各プールは、2つ以上の異なる増殖ヒト臍帯血幹細胞サンプルを含み、上記プール中の各サンプルは、異なる人間の出生時の臍帯血および/または胎盤血から由来し、選択された識別子によって識別されたプール中のサンプルは、患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならず、上記選択では、上記識別子によって識別されるプールまたはそのアリコートの、必要とする患者への投与のために、増殖ヒト臍帯血幹細胞サンプルプールを識別する、コンピュータプログラムプロダクト。 - プロセッサと、
上記プロセッサに結合され、モジュールを格納しているメモリと、を備え、
上記モジュールは、
(a)コンピュータデータベースに格納されている少なくとも50個の複数の識別子から識別子を選択するための実行可能な命令と、
(b)上記選択された識別子を出力または表示するための実行可能な命令と、を含み、
上記実行可能な命令(a)において、各識別子は、増殖ヒト臍帯血幹細胞サンプルプールを識別し、各プールは、2つ以上の異なる増殖ヒト臍帯血幹細胞サンプルを含み、上記プール中の各サンプルは、異なる人間の出生時の臍帯血および/または胎盤血から由来し、選択された識別子によって識別されたプール中のサンプルは、患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならず、上記選択では、上記識別子によって識別されるプールまたはそのアリコートの、必要とする患者への投与のために、増殖ヒト臍帯血幹細胞サンプルプールを識別する、装置。 - 上記選択は、少なくとも7,500万個のCD34+細胞を有さないサンプル含むプールを除外することを含む、請求項4〜18のいずれか一項に記載の方法。
- 上記選択は、患者の体重1kg当たり50万個を超えるCD3+細胞を有するサンプルを含むプールを除外することをさらに含む、請求項4〜18および33のいずれか一項に記載の方法。
- 上記選択は、少なくとも7,500万個のCD34+細胞を含まないプールを除外することを含む、請求項28〜30のいずれか一項に記載のコンピュータで行われる方法。
- 上記選択は、患者の体重1kg当たり50万個を超えるCD3+細胞を含むプールを除外することをさらに含む、請求項28〜30および35のいずれか一項に記載のコンピュータで行われる方法。
- 上記選択は、さらに、サンプルプールを受入れることを含み、上記プール中のサンプルは、患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない、請求項28〜30、35、および36のいずれか一項に記載のコンピュータで行われる方法。
- 上記選択するための実行可能な命令は、少なくとも7,500万個のCD34+細胞を含まないプールを識別する識別子を除外する指令を含む、請求項31に記載のコンピュータプログラムプロダクト。
- 上記選択するための実行可能な命令は、患者の体重1kg当たり50万個を超えるCD3+細胞を含むプールを識別する識別子を除外することをさらに含む、請求項31または38に記載のコンピュータプログラムプロダクト。
- 上記選択するための実行可能な命令は、サンプルプールを識別する識別子を受入れることを含み、上記プール中のサンプルは、患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない、請求項31、38および39の何れか一項に記載のコンピュータプログラムプロダクト。
- 上記選択するための実行可能な命令は、少なくとも7,500万個のCD34+細胞を含まないプールを識別する識別子を除外する命令を含む、請求項32に記載の装置。
- 上記選択するための実行可能な命令は、患者の体重1kg当たり50万個を超えるCD3+細胞を含むプールを識別する識別子を除外する命令をさらに含む、請求項32または41に記載の装置。
- 上記選択するための実行可能な命令は、サンプルプールを識別する識別子を受入れることを含み、上記プール中のサンプルは、患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならない、請求項32、41および42の何れか一項に記載の装置。
- 上記選択は、患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合となるサンプルプールを識別する識別子を取り除くことを含む、請求項28〜30、および35〜37のいずれか一項に記載のコンピュータで行われる方法。
- 上記選択するための実行可能な命令は、さらに、患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合となるサンプルプールを識別する識別子を取り除く命令を含む、請求項31、および38〜40の何れか一項に記載のコンピュータプログラムプロダクト。
- 上記選択するための実行可能な命令は、さらに、患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合となるサンプルプールを識別する識別子を取り除く命令を含む、請求項32、および41〜43の何れか一項に記載の装置。
- 上記投与する工程の前に、上記2つ以上の異なる増殖ヒト臍帯血幹細胞サンプルをプールし上記プールを作成する工程を含む、請求項1に記載の方法。
- 上記プールする工程の前に、上記2つ以上の増殖ヒト臍帯血幹細胞サンプルを選択し上記プールを作成する工程を含む、請求項47に記載の方法。
- 上記異なるサンプルそれぞれは、上記選択する時点で凍結されており、
上記選択する工程後で、かつ上記プールする工程前に、選択されたサンプルを解凍する工程を含む、請求項48に記載の方法。 - 上記選択する工程は、続いて、患者によって確立した2つを超えるHLA抗原または対立遺伝子の型で集合的に上記患者と不適合とならないようにプールするためにサンプルを受入れる工程を含む、請求項49に記載の方法。
- 造血機能を必要とする人間の患者に造血機能を提供するために用いられる増殖ヒト臍帯血幹細胞の凍結サンプルを選択するためのコンピュータで行われる方法であって、
(a)コンピュータデータベースに格納されている少なくとも50個の複数の識別子を選択する工程と、
(b)上記選択された識別子を出力または表示する工程と、を含み、
上記工程(a)において、各識別子は、1人以上の異なる人間の出生時の臍帯血および/または胎盤血から由来する増殖ヒト臍帯血幹細胞サンプルの凍結保存プールを識別し、選択された識別子は、その識別子により識別された、増殖ヒト臍帯血幹細胞サンプルまたはそのアリコートの必要とする患者への投与のために解凍されプールされる増殖ヒト臍帯血幹細胞の凍結サンプルを識別する、方法。 - コンピュータシステムと併用され、コンピュータ読み取り可能な記憶媒体とその中に埋め込まれたコンピュータプログラム機構とを含むコンピュータプログラムプロダクトであって、
上記コンピュータプログラム機構は、
(a)コンピュータデータベースに格納されている少なくとも50個の複数の識別子を選択するための実行可能な命令と、
(b)上記選択された識別子を出力または表示するための実行可能な命令と、を含み、
上記実行可能な命令(a)において、各識別子は、1人以上の異なる人間の出生時の臍帯血および/または胎盤血から由来する増殖ヒト臍帯血幹細胞サンプルの凍結保存プールを識別し、選択された識別子は、その識別子により識別された、増殖ヒト臍帯血幹細胞サンプルまたはそのアリコートの必要とする患者への投与のために解凍されプールされる増殖ヒト臍帯血幹細胞の凍結サンプルを識別する、コンピュータプログラムプロダクト。 - プロセッサと、
上記プロセッサに結合され、モジュールを格納しているメモリと、を備え、
上記モジュールは、
(a)コンピュータデータベースに格納されている少なくとも50個の複数の識別子から識別子を選択するための実行可能な命令と、
(b)上記選択された識別子を出力または表示するための実行可能な命令と、を含み、
上記実行可能な命令(a)において、各識別子は、1人以上の異なる人間の出生時の臍帯血および/または胎盤血から由来する増殖ヒト臍帯血幹細胞サンプルの凍結保存プールを識別し、選択された識別子は、その識別子により識別された、増殖ヒト臍帯血幹細胞サンプルまたはそのアリコートの必要とする患者への投与のために解凍されプールされる増殖ヒト臍帯血幹細胞の凍結サンプルを識別する、装置。 - 6つのHLA抗原または対立遺伝子の型が上記患者によって確立した、請求項1に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US32257510P | 2010-04-09 | 2010-04-09 | |
| US61/322,575 | 2010-04-09 | ||
| PCT/US2011/031957 WO2011127472A1 (en) | 2010-04-09 | 2011-04-11 | Compositions and methods for providing hematopoietic function |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017079812A Division JP2017149752A (ja) | 2010-04-09 | 2017-04-13 | 臍帯血移植体を補うための方法、造血機能を提供するための方法および増殖臍帯血幹細胞の採取物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013523842A true JP2013523842A (ja) | 2013-06-17 |
| JP2013523842A5 JP2013523842A5 (ja) | 2015-05-07 |
Family
ID=44120971
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013504020A Pending JP2013523842A (ja) | 2010-04-09 | 2011-04-11 | 造血機能を提供するための組成物および方法 |
| JP2017079812A Pending JP2017149752A (ja) | 2010-04-09 | 2017-04-13 | 臍帯血移植体を補うための方法、造血機能を提供するための方法および増殖臍帯血幹細胞の採取物 |
| JP2020020612A Active JP7041179B2 (ja) | 2010-04-09 | 2020-02-10 | 造血機能を提供するための組成物および方法 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017079812A Pending JP2017149752A (ja) | 2010-04-09 | 2017-04-13 | 臍帯血移植体を補うための方法、造血機能を提供するための方法および増殖臍帯血幹細胞の採取物 |
| JP2020020612A Active JP7041179B2 (ja) | 2010-04-09 | 2020-02-10 | 造血機能を提供するための組成物および方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (3) | US20130095080A1 (ja) |
| EP (2) | EP2555781A1 (ja) |
| JP (3) | JP2013523842A (ja) |
| CA (2) | CA2795938C (ja) |
| WO (1) | WO2011127472A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016104711A (ja) * | 2014-11-21 | 2016-06-09 | 国立大学法人 東京大学 | 造血幹細胞移植を補助することに用いるための医薬組成物およびその製造方法 |
| JP2020072694A (ja) * | 2014-06-04 | 2020-05-14 | フレッド ハッチンソン キャンサー リサーチ センター | Notch 1および/またはNotch 2アゴニストを用いた幹細胞の増殖および生着 |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013086436A1 (en) | 2011-12-08 | 2013-06-13 | Fred Hutchinson Cancer Research Center | Compositions and methods for enhanced generation of hematopoietic stem/progenitor cells |
| WO2013188851A1 (en) * | 2012-06-14 | 2013-12-19 | Fred Hutchinson Cancer Research Center | Ex vivo expansion of myogenic stem cells by notch activation |
| AU2014205662B2 (en) | 2013-01-08 | 2019-09-05 | Fred Hutchinson Cancer Research Center | Compositions and methods for expansion of embryonic hematopoietic stem cells |
| CN105873952A (zh) | 2013-10-31 | 2016-08-17 | 弗莱德哈钦森癌症研究中心 | 经修饰的造血干细胞/祖细胞和非t效应细胞及其用途 |
| US20150342165A1 (en) * | 2014-05-29 | 2015-12-03 | City Of Hope | Humanized mouse and methods of using the same |
| US10350245B2 (en) | 2015-01-21 | 2019-07-16 | Fred Hutchinson Cancer Research Center | Point-of-care and/or portable platform for gene therapy |
| US11827904B2 (en) | 2015-04-29 | 2023-11-28 | Fred Hutchinson Cancer Center | Modified stem cells and uses thereof |
| US20180355318A1 (en) | 2015-04-29 | 2018-12-13 | Fred Hutchinson Cancer Research Center | Modified hematopoietic stem/progenitor and non-t effector cells, and uses thereof |
| RU2747728C2 (ru) * | 2015-12-04 | 2021-05-13 | Фред Хатчинсон Кэнсер Рисерч Сентер | Применение размноженных популяций гематопоэтических стволовых клеток/клеток-предшественников |
| CA2968946A1 (en) * | 2016-05-30 | 2017-11-30 | Ottawa Heart Institute Research Corporation | Serum-free and xenogen-free human cardiac explant-derived stem cells and uses and methods for the production thereof |
| AU2018212634A1 (en) * | 2017-01-24 | 2019-08-08 | Fred Hutchinson Cancer Research Center | Systems and methods for hematopoietic cell expansion utilizing hydrogels |
| US20220098613A1 (en) | 2018-09-12 | 2022-03-31 | Fred Hutchinson Cancer Research Center | Reducing cd33 expression to selectively protect therapeutic cells |
| MX2021014039A (es) * | 2019-05-17 | 2022-02-11 | Deverra Therapeutics Inc | Composiciones y métodos para mejorar resultados de tratamiento para pacientes que tienen neoplasias malignas hematológicas usando un producto de células madre expandidas. |
| WO2023150393A2 (en) | 2022-02-07 | 2023-08-10 | Ensoma, Inc. | Inhibitor-resistant mgmt modifications and modification of mgmt-encoding nucleic acids |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040067583A1 (en) * | 2000-10-27 | 2004-04-08 | Bernstein Irwin D | Methods for immortalizing cells |
| JP2005102656A (ja) * | 2003-10-02 | 2005-04-21 | Toray Ind Inc | 細胞培養器具およびそれを用いた細胞製剤の製造方法 |
| JP2006517975A (ja) * | 2003-02-13 | 2006-08-03 | アンスロジェネシス コーポレーション | 疾患、障害または症状を患っている個体を治療するための臍帯血の使用 |
| JP2008517948A (ja) * | 2004-10-25 | 2008-05-29 | セルラント セラピューティクス,インコーポレイティド | 骨髄細胞集団の増殖方法及びその使用 |
| JP2008545755A (ja) * | 2005-06-02 | 2008-12-18 | ステムサイト インコーポレーテッド | 血漿が除去され、赤血球が除去されていない臍帯血組成物および使用方法 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3753357A (en) | 1970-12-14 | 1973-08-21 | Ovitron Res Corp | Method and apparatus for the preservation of cells and tissues |
| US4199022A (en) | 1978-12-08 | 1980-04-22 | The United States Of America As Represented By The Department Of Energy | Method of freezing living cells and tissues with improved subsequent survival |
| US4559298A (en) | 1982-11-23 | 1985-12-17 | American National Red Cross | Cryopreservation of biological materials in a non-frozen or vitreous state |
| US5004681B1 (en) | 1987-11-12 | 2000-04-11 | Biocyte Corp | Preservation of fetal and neonatal hematopoietic stem and progenitor cells of the blood |
| IL101728A (en) | 1991-05-03 | 2007-08-19 | Univ Yale | Human Abandonment and Delta, Restrictive Areas of Effect in Tophoric Proteins, and Methods Based on Them |
| IE20030749A1 (en) | 1991-05-03 | 2003-11-12 | Indiana University Foundation | Human notch and delta binding domains in torporythmic proteins, and methods based thereon |
| US5856441A (en) | 1991-05-03 | 1999-01-05 | Yale University | Serrate fragments and derivatives |
| US5869282A (en) | 1991-12-11 | 1999-02-09 | Imperial Cancer Research Technology, Ltd. | Nucleotide and protein sequences of the serrate gene and methods based thereon |
| WO1993012141A1 (en) | 1991-12-11 | 1993-06-24 | Yale University | Nucleotide and protein sequences of the serrate gene and methods based thereon |
| PT861261E (pt) | 1995-06-28 | 2009-12-16 | Imp Cancer Res Tech | Sequências nucleotídicas e proteicas de genes delta de vertebrado e métodos nelas baseados |
| US5780300A (en) | 1995-09-29 | 1998-07-14 | Yale University | Manipulation of non-terminally differentiated cells using the notch pathway |
| AU2003219966A1 (en) * | 2002-03-05 | 2003-09-22 | Daniel D. Richard | Dual blood donation plus method |
| US7569385B2 (en) * | 2003-08-14 | 2009-08-04 | The Regents Of The University Of California | Multipotent amniotic fetal stem cells |
| BRPI0509141A (pt) * | 2004-03-26 | 2007-09-04 | Celgene Corp | método para manter um registro de células-tronco, produto de programa de computação para uso junto com um sistema de computador, sistema de computador, e, meio legìvel por computador |
| US7147626B2 (en) | 2004-09-23 | 2006-12-12 | Celgene Corporation | Cord blood and placenta collection kit |
| US8383095B2 (en) | 2006-02-14 | 2013-02-26 | Cellerant Therapeutics, Inc. | Methods and compositions for enhancing engraftment of hematopoietic stem cells |
-
2011
- 2011-04-11 CA CA2795938A patent/CA2795938C/en active Active
- 2011-04-11 WO PCT/US2011/031957 patent/WO2011127472A1/en active Application Filing
- 2011-04-11 EP EP11717077A patent/EP2555781A1/en not_active Withdrawn
- 2011-04-11 EP EP16162911.8A patent/EP3097916B1/en active Active
- 2011-04-11 CA CA3090548A patent/CA3090548A1/en active Pending
- 2011-04-11 JP JP2013504020A patent/JP2013523842A/ja active Pending
- 2011-04-11 US US13/640,298 patent/US20130095080A1/en not_active Abandoned
-
2015
- 2015-07-16 US US14/801,771 patent/US20160199418A1/en not_active Abandoned
-
2017
- 2017-04-13 JP JP2017079812A patent/JP2017149752A/ja active Pending
-
2019
- 2019-10-01 US US16/590,255 patent/US20200030384A1/en active Pending
-
2020
- 2020-02-10 JP JP2020020612A patent/JP7041179B2/ja active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040067583A1 (en) * | 2000-10-27 | 2004-04-08 | Bernstein Irwin D | Methods for immortalizing cells |
| JP2006517975A (ja) * | 2003-02-13 | 2006-08-03 | アンスロジェネシス コーポレーション | 疾患、障害または症状を患っている個体を治療するための臍帯血の使用 |
| JP2005102656A (ja) * | 2003-10-02 | 2005-04-21 | Toray Ind Inc | 細胞培養器具およびそれを用いた細胞製剤の製造方法 |
| JP2008517948A (ja) * | 2004-10-25 | 2008-05-29 | セルラント セラピューティクス,インコーポレイティド | 骨髄細胞集団の増殖方法及びその使用 |
| JP2008545755A (ja) * | 2005-06-02 | 2008-12-18 | ステムサイト インコーポレーテッド | 血漿が除去され、赤血球が除去されていない臍帯血組成物および使用方法 |
Non-Patent Citations (4)
| Title |
|---|
| ANNUAL REVIEW 血液 2008, 18-26, JPN6015012176, ISSN: 0003038302 * |
| CURR OPIN IMMUNOL. 2006 OCT;18(5):571-5, JPN6015012177, ISSN: 0003038303 * |
| EXP HEMATOL. 2005 OCT;33(10):1249-56., JPN6015012179, ISSN: 0003038304 * |
| NAT MED. 2010 FEB;16(2):232-6, JPN6015012174, ISSN: 0003038301 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020072694A (ja) * | 2014-06-04 | 2020-05-14 | フレッド ハッチンソン キャンサー リサーチ センター | Notch 1および/またはNotch 2アゴニストを用いた幹細胞の増殖および生着 |
| JP2016104711A (ja) * | 2014-11-21 | 2016-06-09 | 国立大学法人 東京大学 | 造血幹細胞移植を補助することに用いるための医薬組成物およびその製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20200030384A1 (en) | 2020-01-30 |
| EP2555781A1 (en) | 2013-02-13 |
| US20160199418A1 (en) | 2016-07-14 |
| EP3097916B1 (en) | 2021-07-07 |
| US20130095080A1 (en) | 2013-04-18 |
| CA2795938C (en) | 2020-10-27 |
| EP3097916A1 (en) | 2016-11-30 |
| WO2011127472A1 (en) | 2011-10-13 |
| JP7041179B2 (ja) | 2022-03-23 |
| JP2020090529A (ja) | 2020-06-11 |
| CA3090548A1 (en) | 2011-10-13 |
| CA2795938A1 (en) | 2011-10-13 |
| JP2017149752A (ja) | 2017-08-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6998911B2 (ja) | Hlaの適合なしに造血機能を提供するための組成物 | |
| JP7041179B2 (ja) | 造血機能を提供するための組成物および方法 | |
| US6569427B1 (en) | Isolation and preservation of fetal and neonatal hematopoietic stem and progenitor cells of the blood | |
| EP0343217A1 (en) | Isolation and preservation of fetal and neonatal hematopoietic stem and progenitor cells of the blood | |
| US9956249B2 (en) | Compositions and methods for expansion of embryonic hematopoietic stem cells | |
| US20220218759A1 (en) | Compositions and methods for improving treatment outcomes for patients having hematological malignancies using an expanded stem cell product |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20140409 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150319 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150331 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150626 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150930 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160308 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160510 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160908 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20161213 |