JP2012506860A - アルホルモテロール及びチオトロピウムの組成物及びその使用方法 - Google Patents
アルホルモテロール及びチオトロピウムの組成物及びその使用方法 Download PDFInfo
- Publication number
- JP2012506860A JP2012506860A JP2011533326A JP2011533326A JP2012506860A JP 2012506860 A JP2012506860 A JP 2012506860A JP 2011533326 A JP2011533326 A JP 2011533326A JP 2011533326 A JP2011533326 A JP 2011533326A JP 2012506860 A JP2012506860 A JP 2012506860A
- Authority
- JP
- Japan
- Prior art keywords
- tiotropium
- pharmaceutical composition
- alformoterol
- formoterol
- pharmaceutically acceptable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
- A61K9/008—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy comprising drug dissolved or suspended in liquid propellant for inhalation via a pressurized metered dose inhaler [MDI]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/46—8-Azabicyclo [3.2.1] octane; Derivatives thereof, e.g. atropine, cocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/137—Arylalkylamines, e.g. amphetamine, epinephrine, salbutamol, ephedrine or methadone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/167—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the nitrogen of a carboxamide group directly attached to the aromatic ring, e.g. lidocaine, paracetamol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/439—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom the ring forming part of a bridged ring system, e.g. quinuclidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
- A61K9/0078—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy for inhalation via a nebulizer such as a jet nebulizer, ultrasonic nebulizer, e.g. in the form of aqueous drug solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/08—Bronchodilators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Pulmonology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Otolaryngology (AREA)
- Emergency Medicine (AREA)
- Dispersion Chemistry (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicinal Preparation (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
本明細書中で用いる「ホルモテロール成分」という用語は、本発明の組成物中のホルモテロールのすべての立体異性体の総体を意味する。
その化学名が(+/−)N−[2−ヒドロキシ−5−[1−ヒドロキシ−2−[[2−(p−メトキシフェニル)−2−プロピル]アミノ]エチル]フェニル]−ホルムアミドであるホルモテロールは、極めて強力であり、そして吸入されたときに長時間持続性の気管支拡張効果を有するβ2選択的アドレナリンレセプターアゴニストである。ホルモテロールは、分子内に2つのキラル中心を有しており、その各々は2つの可能な立体配置で存在していることができる。これにより、次の4つの組み合わせ:(R,R)、(S,S)、(R,S)、及び(S,R)が生じる。(R,R)及び(S,S)は相互に鏡像であり、従ってそれらはエナンチオマーであり;(R,S)及び(S,R)は同様にエナンチオマーの対である。しかしながら、(R,R)及び(S,S)の鏡像は、ジアステレオマーである(R,S)及び(S,R)に重ね合わせることができない。アルホルモテロールはホルモテロールの(R,R)立体異性体である。
本発明の医薬組成物は、活性成分として(R,R)ホルモテロール及びチオトロピウムを含む。前記活性成分は、その薬学的に許容することのできる塩、水和物又は溶媒和物として存在していることができる。本発明の組成物は、1種又はそれ以上の薬学的に許容することのできる担体及び添加剤も含んでいることができる。「薬学的に許容することのできる担体及び添加剤」という用語は、限定されないが、賦形剤(vehicle)、噴射剤、希釈剤、賦形剤(excipient)、錯化剤、安定剤、造粒剤、潤滑剤、結合剤、崩壊剤、共溶媒、佐剤、添加剤及び医薬組成物に添加するのに適切な他の成分を含む。1種又はそれ以上の担体及び1種又はそれ以上の添加剤は、本発明の組成物の他の成分と相溶性でありかつその受容者(recipient)に対して有害とならないという意味において「許容することができる」。
実施例1:臨床試験:COPD患者
無作為化二重盲検試験を行って、アルホルモテロール単独治療、チオトロピウム単独治療、及びそれらの併用治療によって処理された患者間での肺の機能及び症状の改善を比較することにより、この併用治療がいずれかの単独治療より有意に高い効果を及ぼすであろうという仮説を検証した。
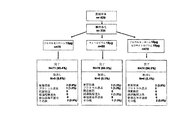
スクリーニングした429名の患者の中から235名を無作為抽出して治療しそして234名に試験用薬剤を少なくとも1回投与した(包括解析(intent-to-treat population)、[ITT])(図1参照)。すべての患者は非喘息性(non-asthmatic)COPD(気腫及び/又は慢性気管支炎を含む)を有していた。適格患者は、少なくとも45歳であり、≧15箱年(pack-year)の喫煙歴を有し、そして医学研究評議会呼吸困難スコア(Medical Research Council Dyspnea Score)(34)に基づく息切れ度(breathlessness severity)≧2を有していた。適格患者は、FEV1>0.7L、FEV1/FVC比≦70%、及び予測FEV1≦65%の気管支拡張剤投与前(pre-bronchodilator)ベースライン肺機能を有していることも必要であった。スクリーニング受診(screening visit)の30日間以内に生命にかかわる又は不安定な呼吸状態を示した場合にはその患者を除外した。スクリーニング前14日間以内にCODP薬物療法で処方された用量若しくは様式(type)を変更したか又は今までに臭化チオトロピウム吸入パウダーを用いていた患者を除外した。
スクリーニング受診時に、COPD症状、変更された医学研究評議会(MMRC)呼吸困難スケール(Modified Medical Research Council (MMRC) Dyspnea Scale)、心拍数、バイタルサイン、及び肺機能試験についてのベースライン値を得た。毎日完了すべき予定の医療イベントカレンダー(medical event calendar)及び投薬ログ(medication log)、及び救急薬治療も処方した。実施されたUDV/DPI投与の数を監視することにより、投薬ログを用いてコンプライアンスを評価した。
この試験は、両側検定の5%有意水準を用いて併用療法を単独療法と比較したときに、24時間(主要エンドポイント)を通しての時間平均化FEV1AUC(FEV1AUC0−24)の平均治療差0.075L及び標準偏差0.016Lを検出し、その後2週間の投与を行なって80%検出力による主要比較を行なうように計画された。すべての有効性解析はITT母集団に基づいて実施した。すべての統計的検定は、他に断らない限りは、両側検定でありそして5%有意水準で実施した。主要比較は、チオトロピウム単独群とアルホルモテロール及びチオトロピウム群との間での比較である。重要な二次的解析比較は、アルホルモテロール単独群とアルホルモテロール及びチオトロピウム群との間における比較であった。多重比較をコントロールするために、モデル内の全治療効果が統計的に5%水準で有意であった場合には、平均治療群差の統計的検定は有意であると判断した。GOLD COPDガイドライン(例えば、参考までにその全体を本明細書に引用する、Pauwels RA, Buist AS, Calverley PM, Jenkins CR, Hurd SS. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. NHLBI/WHO Global Initiative for Chronic Obstructive Lung Disease (GOLD) Workshop summary. Am J Respir Crit Care Med 2001;163:1256-1276参照)に従って患者を分類することによって(それぞれ、<30%、≧30%〜<50%、及び≧50%)、肺機能重症度サブグループ解析を事後に実施した。共変量として試験ベースライン(又は適用できる場合には前投与(predose))を及び固定効果として治療群を用いた線形モデルから最小二乗法(LS法)を用いて、治療群間の対比較を行なった。
この試験において登録された429名の患者のうち235名を無作為化しそして234名に試験薬剤を少なくとも1回投与した(ITT母集団)(図1参照)。FEV1、FVC、及び最大吸気量値を含む人口学的特性及びベースライン特性は治療群の間で同様であった(表1参照)。ITT母集団の患者の94.4%は、3つの治療群のすべてについて同様の遂行速度で2週間の試験を完了した(図1参照)。中止の場合の最も共通の理由は、有害事象の発生であった(n=5[2.1%])(図1参照)。治療群の中で約97%の患者は、試験を通じて治療を遵守した。
各時点のFEV1及び時間正規化FEV1AUC0−24は、すべての治療群でベースラインから好転した。2つの単独治療には同程度の改善が見られ、併用治療群は2週間の治療後に最も大きな改善を示した(表2;図2A及び2B参照)。各単独治療に対する併用治療のFEV1AUC0−24(主要なエンドポイント)におけるより大きな変化は有意であった(p<0.001)。FEV1のピーク変化、トラフ(投与間隔のエンド時)の変化、及びFVCのピーク変化は、すべての治療前のベースラインから有意に改善した(表2参照)。各単独治療群は同程度に改善し、そして併用治療群は最も大きく改善した。併用治療のピークFEV1のより大きな増加は、いずれの単独治療に対しても有意であった(p<0.005)。併用治療でのトラフFEV1の150mLの改善は、チオトロピウム単独治療に対して統計的に有意であり(p=0.002)そしてアルホルモテロール単独治療に対して有意性はなかった(p=0.07)。併用治療でのピークFVCの60mLの平均的改善は、いずれの単独治療について観察された改善よりも大きく(チオトロピウム40mL及びアルホルモテロール48mL)、達成された差はチオトロピウムに対しては統計的に有意であった(p=0.03)が、アルホルモテロールに対しては有意性はなかった(p<0.21)。
スクリーニングと無作為化との間(投与前0週間)、全治療群の患者の約80%が救急治療薬としてレバルブテロールMDIを使用した(表3参照)。ベースライン救急薬使用は、平均して1日当たり約3回の作動(actuation)及び1週間当たり約4.5日であった。レバルブテロールMDIの使用は、3つの治療群のすべてで2週間を通した治療の間に減少し、単独治療では1日当たり平均1.8回の作動及び併用治療群では1日当たり平均2.5回の作動まで減少した。単独治療に対する併用治療の差は統計的に有意性がなかった。
ベースライン疾病重症度(投与前FEV1<50%予測値又は≧50%予測値)によって分類された肺の治療の結果、すべての肺機能測定で、ベースラインの低い肺機能の患者はベースラインの高い肺機能の患者より大きい改善があったことが示された(表5、6及び7参照)。より低下したベースラインの肺機能(FEV1<50%予測値)を有する患者についての肺機能測定値のより大きい改善は、絶対的(L)及び相対的(百分率)改善の両方について明らかであった。<50%FEV1予測値を有する患者は、単独治療群及び併用治療群の両方で、評価した5回の努力呼気測定値のすべてについて有意の改善を示した。対照的に、>50%FEV1予測値を有する患者は、いずれの治療群でもトラフFEV1における有意性のある改善を示さず、そしてFEV1AUC0−24だけ併用治療群で改善を示した。
有害事象は多くなく、3つの治療群の間で同様の発生状況であった(表10参照)。COPD増悪及び心血管有害事象はごく一部の患者でのみ観察された(0〜3.9%)。1人の患者(アルホルモテロール15μg)だけが重症の有害事象(小腸閉塞)を報告した。
この試験は、2種類の長時間作用型気管支拡張剤の組合せである、ネブライザーにより投与されるアルホルモテロール及びDPIとして投与されるチオトロピウムの有効性及び安全性を調査した。とりわけ、この2種類の薬剤の単独治療との間の有効性を比較しそしてこれらの薬剤の併用がいずれかの薬剤の単独投与より高い肺の機能の改善をもたらすか否かを評価した。
Claims (24)
- チオトロピウム又はその薬学的に許容することのできる塩、及びアルホルモテロール又はその薬学的に許容することのできる塩を共に、水又は水−エタノール混合物中に含む医薬組成物。
- (a)チオトロピウム又はその薬学的に許容することのできる塩、水和物若しくは溶媒和物を、チオトロピウムに換算して約5μg〜約30μgの量で、及び
(b)アルホルモテロールを含むホルモテロール成分又はその薬学的に許容することのできる塩、水和物若しくは溶媒和物を、アルホルモテロールに換算して約6μg〜約40μgの量で
含む噴射剤不含の液体医薬組成物であって、前記チオトロピウム及びホルモテロール成分が共に液体担体中に溶解しており、そして前記ホルモテロール成分がアルホルモテロール以外のホルモテロールの立体異性体を約10重量%より少ない量で含む、前記医薬組成物。 - 前記液体組成物が約3.0〜約5.5の範囲内のpHを有する、請求項2に記載の医薬組成物。
- 前記液体組成物が約3.0〜約4.0の範囲内のpHを有する、請求項3に記載の医薬組成物。
- 前記ホルモテロール成分が約99重量%より多い量のアルホルモテロール及び約1重量%より少ない量のアルホルモテロール以外のホルモテロールの立体異性体を含む、請求項2に記載の医薬組成物。
- 前記担体が水を含む、請求項2に記載の医薬組成物。
- 前記担体が水/エタノール混合物である、請求項6に記載の医薬組成物。
- 前記チオトロピウム又はその薬学的に許容することのできる塩、水和物若しくは溶媒和物が、チオトロピウムに換算して約5μg〜約15μgの量で存在する、請求項2に記載の医薬組成物。
- 前記ホルモテロール成分のアルホルモテロール部分又はその薬学的に許容することのできる塩、水和物若しくは溶媒和物が、アルホルモテロールに換算して約6μg〜約30μgの量で存在する、請求項2に記載の医薬組成物。
- (a)前記チオトロピウム又はその薬学的に許容することのできる塩、水和物若しくは溶媒和物が、チオトロピウムに換算して約5μg〜約15μgの量で存在し、及び
(b)前記ホルモテロール成分のアルホルモテロール部分又はその薬学的に許容することのできる塩、水和物若しくは溶媒和物が、アルホルモテロールに換算して約12μg〜約30μgの量で存在する、請求項2に記載の医薬組成物。 - 前記噴射剤不含の液体医薬組成物が、総液体体積約1mL〜約3mLで提供される、請求項2、8、9又は10に記載の医薬組成物。
- 前記噴射剤不含の液体医薬組成物が、約2mLより少ない量の総液体体積で提供される、請求項2、8、9又は10に記載の医薬組成物。
- 請求項2に記載の医薬組成物を含む医薬であって、噴霧用の液体としてアンプルにより提供される前記医薬。
- 請求項2に記載の医薬組成物を投与することを含む可逆性気道閉塞に関連した症状を治療する方法であって、1日当たり総投与量約6〜約150μgのアルホルモテロール及び1日当たり総投与量約8〜約150μgのチオトロピウムを投与することを含む前記治療方法。
- 1日当たり総投与量約15〜約45μgのアルホルモテロール及び1日当たり総投与量約18〜約54μgのチオトロピウムを投与することを含む、請求項14に記載の可逆性気道閉塞に関連した状態の治療方法。
- 前記可逆性気道閉塞に関連した症状がCOPDを含む、請求項14又は15に記載の可逆性気道閉塞に関連した症状の治療方法。
- 前記可逆性気道閉塞に関連した症状が喘息を含む、請求項14又は15に記載の可逆性気道閉塞に関連した症状の治療方法。
- 前記方法が噴霧による前記医薬組成物の投与を含む、請求項14又は15に記載の可逆性気道閉塞に関連した症状の治療方法。
- 請求項2、3、4、5、6、7、8、9又は10に記載の医薬組成物を投与することにより哺乳動物において気管支収縮を予防するか、又は気管支拡張を誘導する方法。
- 前記方法が、1日当たり総投与量約6〜約150μgのアルホルモテロール及び1日当たり総投与量約8〜約150μgのチオトロピウムを投与することを含む、請求項19に記載の方法。
- 前記方法が、1日当たり総投与量約15〜約45μgのアルホルモテロール及び1日当たり総投与量約18〜約54μgのチオトロピウムを投与することを含む、請求項19に記載の方法。
- 前記方法が、噴霧による前記医薬組成物の投与を含む、請求項19に記載の方法。
- 前記医薬組成物が、噴射剤不含の液体組成物として、総液体体積約1mL〜約3mLで提供される、請求項22に記載の方法。
- 前記医薬組成物が、噴射剤不含の液体組成物として、約2mLより少ない量の総液体体積で提供される、請求項22に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10796408P | 2008-10-23 | 2008-10-23 | |
| US61/107,964 | 2008-10-23 | ||
| PCT/US2009/061652 WO2010048384A2 (en) | 2008-10-23 | 2009-10-22 | Arformoterol and tiotropium compositions and methods for use |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014143813A Division JP2014237666A (ja) | 2008-10-23 | 2014-07-14 | アルホルモテロール及びチオトロピウムの組成物及びその使用方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012506860A true JP2012506860A (ja) | 2012-03-22 |
| JP2012506860A5 JP2012506860A5 (ja) | 2012-12-20 |
Family
ID=42119978
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011533326A Pending JP2012506860A (ja) | 2008-10-23 | 2009-10-22 | アルホルモテロール及びチオトロピウムの組成物及びその使用方法 |
| JP2014143813A Pending JP2014237666A (ja) | 2008-10-23 | 2014-07-14 | アルホルモテロール及びチオトロピウムの組成物及びその使用方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014143813A Pending JP2014237666A (ja) | 2008-10-23 | 2014-07-14 | アルホルモテロール及びチオトロピウムの組成物及びその使用方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US20110250242A1 (ja) |
| EP (1) | EP2355808A4 (ja) |
| JP (2) | JP2012506860A (ja) |
| AU (1) | AU2009308412B2 (ja) |
| CA (1) | CA2741078A1 (ja) |
| TW (1) | TW201021792A (ja) |
| WO (1) | WO2010048384A2 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2019142214A1 (en) * | 2018-01-19 | 2019-07-25 | Cipla Limited | Pharmaceutical composition comprising tiotropium for inhalation |
| CN111481550A (zh) * | 2020-05-14 | 2020-08-04 | 王兆霖 | 含有噻托溴铵和阿福特罗的药物制剂 |
| CN115267024B (zh) * | 2022-07-31 | 2023-06-30 | 浙江知一药业有限责任公司 | 治疗呼吸系统疾病的药物组合物及其检测方法 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11508547A (ja) * | 1995-06-27 | 1999-07-27 | ベーリンガー インゲルハイム コマンディトゲゼルシャフト | 噴射剤を含まないエアゾールを製造するための新規で安定な医薬調製物 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040019025A1 (en) * | 2000-04-18 | 2004-01-29 | Gavin Brian Charles | Medical compositions comprising (r,r)-formoterol and rofleponide |
| AU2000250701B2 (en) * | 2000-05-22 | 2004-07-01 | Chiesi Farmaceutici S.P.A. | Stable pharmaceutical solution formulations for pressurised metered dose inhalers |
| CN100398094C (zh) * | 2002-03-01 | 2008-07-02 | 奇斯药制品公司 | 福莫特罗超细制剂 |
| US20060079544A1 (en) * | 2004-08-13 | 2006-04-13 | Boehringer Ingelheim International Gmbh | Medicaments for the prevention or treatment of alveolar pneumonia comprising an anticholinergic |
| US20070264202A1 (en) * | 2004-09-09 | 2007-11-15 | Cipla Limited | Pharmaceutical Composition Comprising an Isomer of Betamimetic Agent and an Anti-Cholinergic Agent |
| US20070293460A1 (en) * | 2005-10-31 | 2007-12-20 | Richie's Pharmacy And Medical Supply, Incorporated | Delivery of a combination therapy for asthma and chronic obstructive pulmonary disease |
| WO2008102128A2 (en) * | 2007-02-19 | 2008-08-28 | Cipla Limited | Pharmaceutical combinations of at least two bronchodilators or of a bronchodilator with a corticosteroid |
-
2009
- 2009-10-22 EP EP09822693A patent/EP2355808A4/en not_active Withdrawn
- 2009-10-22 JP JP2011533326A patent/JP2012506860A/ja active Pending
- 2009-10-22 US US13/125,506 patent/US20110250242A1/en not_active Abandoned
- 2009-10-22 WO PCT/US2009/061652 patent/WO2010048384A2/en active Application Filing
- 2009-10-22 AU AU2009308412A patent/AU2009308412B2/en not_active Ceased
- 2009-10-22 CA CA2741078A patent/CA2741078A1/en not_active Abandoned
- 2009-10-23 TW TW098135905A patent/TW201021792A/zh unknown
-
2014
- 2014-07-14 JP JP2014143813A patent/JP2014237666A/ja active Pending
- 2014-07-25 US US14/340,736 patent/US20140336218A1/en not_active Abandoned
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11508547A (ja) * | 1995-06-27 | 1999-07-27 | ベーリンガー インゲルハイム コマンディトゲゼルシャフト | 噴射剤を含まないエアゾールを製造するための新規で安定な医薬調製物 |
Non-Patent Citations (2)
| Title |
|---|
| JPN5011003942; TROFAST J: 'STERIC ASPECTS OF AGONISM AND ANTAGONISM AT BETA-ADRENOCEPTORS: 以下備考' CHIRALITY V3 N6, 19910101, P443-450, WILEY-LISS * |
| JPN6014000207; Tashkin DP et al: 'Concomitant treatment with nebulized formoterol and tiotropium in subjects with COPD: a placebo-cont' Respiratory medicine 102(4), 200804, 479-487 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2741078A1 (en) | 2010-04-29 |
| US20140336218A1 (en) | 2014-11-13 |
| TW201021792A (en) | 2010-06-16 |
| EP2355808A4 (en) | 2012-04-25 |
| WO2010048384A3 (en) | 2010-09-02 |
| AU2009308412A1 (en) | 2010-04-29 |
| US20110250242A1 (en) | 2011-10-13 |
| JP2014237666A (ja) | 2014-12-18 |
| WO2010048384A2 (en) | 2010-04-29 |
| AU2009308412B2 (en) | 2015-11-26 |
| EP2355808A2 (en) | 2011-08-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20210401740A1 (en) | Method and system for the treatment of chronic copd with nebulized anticholinergic administrations | |
| EP1718336B1 (en) | Novel combination of anticholinergic and beta mimetics for the treatment of respiratory diseases | |
| CA2764867C (en) | Treatment of chronic obstructive pulmonary disease with nebulized beta 2-agonist or combined nebulized beta 2-agonist and anticholinergic administration | |
| CA2716936C (en) | Method and system for the treatment of chronic obstructive pulmonary disease with nebulized anticholinergic administrations | |
| US20090192187A1 (en) | Dry powder formulation comprising an anticholinergic drug | |
| US20090181935A1 (en) | Compositions comprising an antimuscarinic and a long-acting beta-agonist | |
| US20070167496A1 (en) | Roflumilast and glycopyrronium combination | |
| JP2014237666A (ja) | アルホルモテロール及びチオトロピウムの組成物及びその使用方法 | |
| US20130302260A1 (en) | Novel propellant containing preparations for tiotropium | |
| JP2012506860A5 (ja) | ||
| CA2815035A1 (en) | Carbonate derivatives for the treatment of cough | |
| US20230270754A1 (en) | Combination therapy for inhalation administration |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20121022 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121026 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20121026 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140114 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140409 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140416 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140613 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140620 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140714 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20141028 |