JP2010059130A - ペプチド及び自然細胞性免疫促進剤 - Google Patents
ペプチド及び自然細胞性免疫促進剤 Download PDFInfo
- Publication number
- JP2010059130A JP2010059130A JP2008228726A JP2008228726A JP2010059130A JP 2010059130 A JP2010059130 A JP 2010059130A JP 2008228726 A JP2008228726 A JP 2008228726A JP 2008228726 A JP2008228726 A JP 2008228726A JP 2010059130 A JP2010059130 A JP 2010059130A
- Authority
- JP
- Japan
- Prior art keywords
- gln
- peptide
- glu
- natural cell
- cells
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Landscapes
- Coloring Foods And Improving Nutritive Qualities (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
Abstract
【解決手段】下記のアミノ酸配列(配列番号1又は2)を有するペプチド;該ペプチドを有効成分として含有する自然細胞性免疫促進剤。
Gln-Gln-Gln-Gln-Gln-Gln-Lys-Ser-His-Gly-Gly-Arg(配列番号1)
Lys-Gln-Gly-Gln-His-Gln-Gln-Glu-Glu-Glu-Glu-Glu(配列番号2)
【選択図】なし
Description
従来の免疫賦活作用を有する大豆たんぱく質消化物およびペプチドに関連する公知例として特許文献1〜4などが挙げられる。
特許文献3には、H-Gln-Arg-Pro-Arg-OH(配列番号3)で示されるペプチドがマクロファージ及び多形核白血球などの貪食能を有し、免疫増強剤として有用であることが、特許文献4には、Gln-Arg-Pro-Arg (配列番号3)(I)または/およびHis-Cys-Gln-Arg-Pro-Arg(配列番号4)(II)で示されるペプチドが抗体産生増強作用を有することが記載されている。特許文献3および4に記載されている免疫調節ペプチドは、免疫グロブリンG(IgG)から派生する食作用促進ペプチド、タフトシンおよびリギンの一次構造を大豆たんぱく質中に探索したものであり、その構造および活性はタフトシンと極めて類似している。
このように、大豆たんぱく質の消化により生じる免疫賦活ペプチドの特性付けに関する報告は少ない。
本発明の他の目的は、大豆たんぱく質の酵素消化物より免疫賦活ペプチドを単離し、特性付けることにより全く新規の免疫賦活ペプチドを提供することである。
1.下記のアミノ酸配列(配列番号1)を有するペプチド。
Gln-Gln-Gln-Gln-Gln-Gln-Lys-Ser-His-Gly-Gly-Arg (QQQQQQKSHGGR)
2.下記のアミノ酸配列(配列番号2)を有するペプチド。
Lys-Gln-Gly-Gln-His-Gln-Gln-Glu-Glu-Glu-Glu-Glu (KQGQHQQEEEEE)
3.上記1又は2記載のペプチドを有効成分として含有する自然細胞性免疫促進剤。
摂取時の消化(トリプシンはArgまたはLysの後を切断する)を考慮し、本発明では、単離したペプチドの活性部位と考えられる配列番号1:QQQQQQKSHGGRと配列番号2:KQGQHQQEEEEEのペプチドを化学合成し、その活性を確認した。
本発明のペプチドを有効成分とする自然細胞性免疫促進剤の剤型も特に限定されない。本発明の自然細胞性免疫促進剤は食品や医薬品の形態としても良い。例えば、飲料、粉末、カプセル等の形態が挙げられる。
本発明の自然細胞性免疫促進剤の投与量は、本発明のペプチドの量として好ましくは0.1mg/kg体重/日〜1g/kg体重/日程度である。
本発明の自然細胞性免疫促進剤中の本発明のペプチドの含有量は、投与形態により異なるが、上記投与量となるように適宜調整すれば良い。
実施例1 (Ro-消化物ならびに活性ペプチド(H1)の調製)
脱脂大豆100gを20倍量の0.03Mトリス-塩酸緩衝液(pH 8.0)に分散させ、室温で2時間攪拌した。上澄みを遠心分離(9000×g、30分)により回収し、0.02M HClによりpHを4.5に調整した。最終的に沈殿物を水200mlに分散させ、透析膜(透析用セルロースチューブ)を使用して透析し、凍結乾燥し、大豆酸沈殿たんぱく質画分約40gを得た。大豆酸沈殿たんぱく質画分(1g)を15mlの蒸留水に再溶解した。2分間煮沸し、水溶液をPeptidase R(アマノ社製)の至適pH 7.0に調整し、蒸留水を総量20mlになるように加えた。大豆酸沈殿たんぱく質画分酵素水溶液の反応(基質:酵素 = 50:1)は45℃で2時間行った。その後、反応を10分間の煮沸により停止し酵素を失活させ、pHを4.5に調整した。遠心分離により得られた上澄みをRo-消化物とし、透析、凍結乾燥後用いた。
Ro-消化物をSP-Sepharoseカラムを装着したイオン交換クロマトグラフィーに供し、溶媒中の塩濃度を変えることにより、消化物を溶出させた。活性画分をTSK-Gel ODS-80 TMを装着した逆相高速液体クロマトグラフィーに供し、アセトニトリル濃度35%〜51.4%、30分のリニアグラジェントにより溶出させ、主要ピークH1を回収した。クロマトグラムを図1に示す。
グリシニンG4サブユニットのアミノ酸配列の202-213に相当する配列番号1:Gln-Gln-Gln-Gln-Gln-Gln-Lys-Ser-His-Gly-Gly-Arg (QQQQQQKSHGGR)のペプチドをFmoc固相法により合成した。MASSおよびHPLCスペクトルデータからこの合成品は、純度80%以上であることを確認した。
実施例3(配列番号2のペプチドの合成)
実施例2と同様にして、グリシニンG4サブユニットのアミノ酸配列の214-223に相当する(但し、特徴的なアミノ酸配列の連続Gluを2個追加している)配列番号2:Lys-Gln-Gly-Gln-His-Gln-Gln-Glu-Glu-Glu-Glu-Glu (KQGQHQQEEEEE)のペプチドを合成した。
4週齢C3H/HeN系マウス(雄)を市販飼料で1週間予備飼育後、この5週齢マウスを、実施例1〜3のペプチドを含むRo-消化物12.5質量%を含む飼料又はこれを含まない対照飼料で5週間飼育した。各試験群は6匹とした。飼料組成は以下のとおりである。
また、ヒト白血病患者由来NKターゲット細胞であるK562細胞に対する脾臓細胞の細胞傷害性(K562細胞の生存率)を蛍光免疫染色法により測定した。結果を図3に示す。図3において、横軸Spleen/K562は、K562細胞数に対する添加した脾臓細胞数の比を示す。
C3H/HeN系マウスから脾臓細胞を摘出し、5%牛胎児血清、100単位/mlペニシリンおよび100単位/mlストレプトマイシンを含むRPMI-1640 培地に5×106 個/mlの濃度で加え、上記単離ペプチドH1を終濃度0〜50μg/mlとなるように添加し、24穴プレートを用い、37℃で72時間、5% CO2インキュベーター内で培養した。培養後の脾臓細胞を回収し、蛍光免疫染色法により各種免疫担当細胞数(CD8+、CD11b+およびCD49b+細胞数)を測定した。結果を表1に示す。
化学合成したペプチド、配列番号1:QQQQQQKSHGGRと配列番号2:KQGQHQQEEEEEを終濃度0〜50μmol/Lとなるように添加し、脾臓細胞と48時間培養し、免疫担当細胞数(CD49b+、IL-12+CD11b+、IL-2+CD4+、IFN-γ+CD4+およびIL-4+CD4+細胞数)を蛍光免疫染色法により測定した。結果を表2に示す。
また、ヒト白血病細胞株K562に対する脾臓細胞の細胞傷害性はRo-消化物添加飼料で飼育したマウスの脾臓細胞において有意に高くなった(図3)。しかし、両飼料群においてCD49b+細胞数には殆んど違いは見られなかった。
上記単離ペプチドH1と培養した脾臓細胞中のCD8+、CD11b+およびCD49b+細胞数は無添加の場合と比較して有意に増加した(表1)。
化学合成したペプチドと培養した脾臓細胞中のIL-12+CD11b+細胞数は両ペプチド存在下において有意に増加した。CD49b+、IL-2+CD4+およびIFN-γ+CD4+細胞数は配列番号1のペプチドの存在下においてのみ有意に増加した。IL-4+CD4+細胞は両ペプチド存在下において有意な差は見られなかった(表2)。
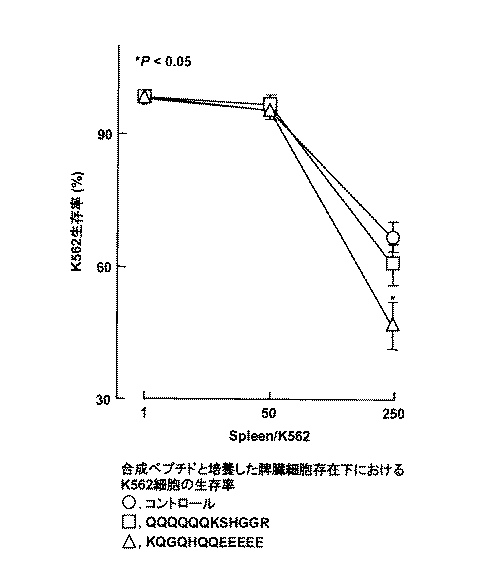
加えて、ヒト白血病細胞株K562に対する細胞傷害性は配列番号1のペプチドと培養した脾臓細胞の存在下において、配列番号2のペプチドおよびコントロールと比較して有意に高かった。(図4)
Claims (3)
- 下記のアミノ酸配列(配列番号1)を有するペプチド。
Gln-Gln-Gln-Gln-Gln-Gln-Lys-Ser-His-Gly-Gly-Arg (QQQQQQKSHGGR) - 下記のアミノ酸配列(配列番号2)を有するペプチド。
Lys-Gln-Gly-Gln-His-Gln-Gln-Glu-Glu-Glu-Glu-Glu (KQGQHQQEEEEE) - 請求項1又は2記載のペプチドを有効成分として含有する自然細胞性免疫促進剤。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008228726A JP5386696B2 (ja) | 2008-09-05 | 2008-09-05 | ペプチド及び自然細胞性免疫促進剤 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008228726A JP5386696B2 (ja) | 2008-09-05 | 2008-09-05 | ペプチド及び自然細胞性免疫促進剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010059130A true JP2010059130A (ja) | 2010-03-18 |
| JP5386696B2 JP5386696B2 (ja) | 2014-01-15 |
Family
ID=42186374
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008228726A Active JP5386696B2 (ja) | 2008-09-05 | 2008-09-05 | ペプチド及び自然細胞性免疫促進剤 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5386696B2 (ja) |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS61132189A (ja) * | 1984-12-03 | 1986-06-19 | Norin Suisansyo Shokuhin Sogo Kenkyusho | ダイズグリシニンcDNA |
| JPH01249800A (ja) * | 1988-03-31 | 1989-10-05 | Snow Brand Milk Prod Co Ltd | 新規ペプチド |
| JPH04229189A (ja) * | 1990-12-27 | 1992-08-18 | Kikkoman Corp | マクロファージ活性化能を有する大豆蛋白質酵素分解物の製造法 |
| JPH06312939A (ja) * | 1993-05-01 | 1994-11-08 | Honen Corp | 抗体産生増強作用を有する医薬組成物 |
| JPH09255699A (ja) * | 1996-03-21 | 1997-09-30 | Fuji Oil Co Ltd | 免疫活性化性ペプチド混合物及びその製造法 |
| WO2008131008A2 (en) * | 2007-04-16 | 2008-10-30 | Solae, Llc | Protein hydrolysate compositions having improved sensory characteristics and physical properties |
-
2008
- 2008-09-05 JP JP2008228726A patent/JP5386696B2/ja active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS61132189A (ja) * | 1984-12-03 | 1986-06-19 | Norin Suisansyo Shokuhin Sogo Kenkyusho | ダイズグリシニンcDNA |
| JPH01249800A (ja) * | 1988-03-31 | 1989-10-05 | Snow Brand Milk Prod Co Ltd | 新規ペプチド |
| JPH04229189A (ja) * | 1990-12-27 | 1992-08-18 | Kikkoman Corp | マクロファージ活性化能を有する大豆蛋白質酵素分解物の製造法 |
| JPH06312939A (ja) * | 1993-05-01 | 1994-11-08 | Honen Corp | 抗体産生増強作用を有する医薬組成物 |
| JPH09255699A (ja) * | 1996-03-21 | 1997-09-30 | Fuji Oil Co Ltd | 免疫活性化性ペプチド混合物及びその製造法 |
| WO2008131008A2 (en) * | 2007-04-16 | 2008-10-30 | Solae, Llc | Protein hydrolysate compositions having improved sensory characteristics and physical properties |
Non-Patent Citations (2)
| Title |
|---|
| CSNC200902114056; '一般講演' 日本農芸化学会大会講演要旨集 2007年度(平成19年度)大会[東京] NIPPON NOGEIKAGAKU KAISHI , 社団法人 日本農芸化学会 * |
| JPN6013023778; '一般講演' 日本農芸化学会大会講演要旨集 2007年度(平成19年度)大会[東京] NIPPON NOGEIKAGAKU KAISHI , 社団法人 日本農芸化学会 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5386696B2 (ja) | 2014-01-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Zhu et al. | A comprehensive review of corn protein‐derived bioactive peptides: production, characterization, bioactivities, and transport pathways | |
| Dang et al. | In vitro and in vivo studies on the angiotensin-converting enzyme inhibitory activity peptides isolated from broccoli protein hydrolysate | |
| Zhou et al. | Research progress of bioactive proteins from the edible and medicinal mushrooms | |
| Wen et al. | Production technology and functionality of bioactive peptides | |
| CN114376141B (zh) | 用于降解脱氧雪腐镰刀菌烯醇的方法和组合物 | |
| Xu et al. | Isolation, identification and molecular docking of anti-inflammatory peptides from walnut (Juglans regia L.) meal hydrolysates | |
| KR20110105761A (ko) | 안지오텐신 변환 효소 저해 펩티드 | |
| Gao et al. | The beneficial potential of protein hydrolysates as prebiotic for probiotics and its biological activity: a review | |
| KR101655696B1 (ko) | rDNA NTS 기반 유전자 다중 삽입 카세트 세트 및 이를 이용한 GRAS 등급의 재조합 효모 균주 | |
| CN116606369A (zh) | 螺旋藻免疫调节肽及其制备方法与应用 | |
| CN116514957A (zh) | 具有免疫调节活性的螺旋藻藻蓝蛋白活性肽及其制备方法与应用 | |
| Toldrá et al. | Biologically active peptides: from basic science to applications for human health | |
| WO2011014925A1 (en) | Process for obtaining peptide fractions | |
| Li et al. | Antimicrobial peptides: sources, expression systems, and applications | |
| JPWO2019044960A1 (ja) | 腸内環境改善用組成物及びその製造法 | |
| JP5386696B2 (ja) | ペプチド及び自然細胞性免疫促進剤 | |
| CN1894273A (zh) | 血管紧张素转化酶抑制肽 | |
| Wu et al. | Bioactive ingredients and medicinal values of Grifola frondosa (Maitake). Foods 2021; 10: 95 | |
| US10464982B2 (en) | Compositions of GM-CSF and interleukin fusions for immune modulation and uses related thereto | |
| EP3424943A1 (en) | Peptide | |
| Su et al. | Characterization of an immunomodulatory Der p 2-FIP-fve fusion protein produced in transformed rice suspension cell culture | |
| KR102291069B1 (ko) | 항염증 활성을 갖는 신규한 펩티드 및 이의 용도 | |
| Ko et al. | Isolation and Activity Evaluation of Peptides with Anti-hypertensive Activity from Commercial Enzymatic Flounder Fish Hydrolysate | |
| KR102110837B1 (ko) | 다중불포화지방산의 트리-하이드록시 또는 테트라-하이드록시 유도체 생산 방법 | |
| EP2534963A1 (en) | Protein synthesis promoter |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110902 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130520 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130719 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130812 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130910 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130910 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5386696 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |