JP2009124976A - Fluorescent dye-decomposing agent - Google Patents
Fluorescent dye-decomposing agent Download PDFInfo
- Publication number
- JP2009124976A JP2009124976A JP2007302145A JP2007302145A JP2009124976A JP 2009124976 A JP2009124976 A JP 2009124976A JP 2007302145 A JP2007302145 A JP 2007302145A JP 2007302145 A JP2007302145 A JP 2007302145A JP 2009124976 A JP2009124976 A JP 2009124976A
- Authority
- JP
- Japan
- Prior art keywords
- fluorescent dye
- manganese peroxidase
- decomposing
- fluorescent
- pulp
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02W—CLIMATE CHANGE MITIGATION TECHNOLOGIES RELATED TO WASTEWATER TREATMENT OR WASTE MANAGEMENT
- Y02W30/00—Technologies for solid waste management
- Y02W30/50—Reuse, recycling or recovery technologies
- Y02W30/64—Paper recycling
Landscapes
- Enzymes And Modification Thereof (AREA)
- Paper (AREA)
Abstract
Description
本発明は、蛍光染料分解剤に関する。特に、環境、食品環境分野に於いて使用される蛍光染料分解剤に関する。 The present invention relates to a fluorescent dye decomposing agent. In particular, it relates to a fluorescent dye decomposing agent used in the environment and food environment fields.
近年、再生紙から漏出する蛍光染料に対する問題が顕在化しつつある。古紙パルプ(再生パルプ)は、いわゆる白版紙や上質紙、再生紙、新聞用紙などの古紙を原料としており、古紙パルプの多くは再度、白版紙などに再利用される。そのため、古紙パルプから得られる再生紙を白く見せるために再生パルプの製造工程において蛍光染料が使用されている。しかしながら、蛍光染料は有害物質に化学構造が似ており、発ガン性の疑いも持たれているため、蛍光染料を含む再生紙の安全性が疑われている。特に、食品分野では、蛍光染料を含む再生紙を食品用の包装用紙などの用途に用いることは禁じられている。食品衛生法によれば、食品に接触する可能性のある紙からは蛍光染料が検出されてはならないことになっている。 In recent years, problems with fluorescent dyes leaking from recycled paper are becoming apparent. Waste paper pulp (recycled pulp) uses waste paper such as so-called white stencil paper, high-quality paper, recycled paper, and newsprint paper, and most of the used paper pulp is reused as white stencil paper. For this reason, fluorescent dyes are used in the process for producing recycled pulp in order to make the recycled paper obtained from used paper pulp appear white. However, since the fluorescent dye has a chemical structure similar to that of harmful substances and is suspected to be carcinogenic, the safety of recycled paper containing the fluorescent dye is suspected. In particular, in the food field, it is forbidden to use recycled paper containing fluorescent dyes for applications such as food packaging paper. According to the Food Sanitation Law, fluorescent dyes should not be detected from paper that may come into contact with food.
したがって、食品包装用紙などは再生パルプではなくバージンパルプが使われることが多い。しかし、コスト的な問題もあり、菓子箱や宅配ピザの敷き紙、ファーストフード店で使われるフライドポテトを入れる紙箱などには一部古紙パルプが使われているのが実状である。 Therefore, virgin pulp is often used instead of recycled pulp for food packaging paper. However, due to cost problems, some waste paper pulp is actually used in confectionery boxes, pizza wrapping paper, and paper boxes for French fries used in fast food stores.
上述の理由から、古紙パルプ中の蛍光染料を取り除く方法の開発が望まれている。蛍光染料を取り除く方法として、従来では、古紙パルプを直接アルカリや酸で再処理し蛍光染料を分解する方法、蛍光染料の漏出を防ぐために紙の表面に薬剤を塗工する、フィルムを張るなどの方法(特許文献1)などが行われている。また、塩素系の蛍光染料分解剤も用いられている(特許文献2〜5)。 For the above reasons, development of a method for removing fluorescent dyes in waste paper pulp is desired. Conventional methods for removing fluorescent dyes include reprocessing waste paper pulp directly with alkali or acid to decompose fluorescent dyes, applying chemicals to the surface of paper to prevent leakage of fluorescent dyes, stretching films, etc. The method (patent document 1) etc. are performed. In addition, chlorine-based fluorescent dye decomposing agents are also used (Patent Documents 2 to 5).
しかしながら、古紙パルプを直接アルカリや酸で処理し蛍光染料を分解する場合、処理の過程で古紙パルプの分解も生じるため、古紙パルプの収率が悪化するという問題点があった。また、紙の表面に薬剤を塗工する、フィルムを張るなどの方法は、いずれもコストが上昇するという問題があった。また、塩素系の蛍光染料分解剤は、蛍光染料の分解能力に優れてはいるが、非常に毒性が強いという問題点があった。この薬品の取り扱いには操業者であっても習熟を要し、取り扱いに厳重な注意が必要である。さらに、塩素系の蛍光染料分解剤は排水処理にも問題が残る。すなわち、未反応の薬品が残っている排水を排水処理設備に供給した場合、活性汚泥処理槽中の微生物が死滅する可能性があり、その結果、排水処理を行うことができなくなる。 However, when the waste paper pulp is directly treated with alkali or acid to decompose the fluorescent dye, there is a problem that the waste paper pulp is deteriorated because the waste paper pulp is decomposed during the treatment. In addition, any of the methods such as coating the surface of the paper with a drug or stretching a film has a problem that the cost increases. In addition, although the chlorine-based fluorescent dye decomposing agent is excellent in the ability to decompose fluorescent dyes, it has a problem that it is very toxic. The handling of this chemical requires skill even for operators, and strict handling is required. Furthermore, chlorine-based fluorescent dye decomposing agents still have problems in wastewater treatment. That is, when wastewater in which unreacted chemicals remain is supplied to a wastewater treatment facility, microorganisms in the activated sludge treatment tank may be killed, and as a result, wastewater treatment cannot be performed.
本発明は、上記従来技術の有する課題に鑑みてなされたものであり、安全性が高く、蛍光染料の分解力に優れた蛍光染料分解剤を提供することを目的とする。 The present invention has been made in view of the above-described problems of the prior art, and an object of the present invention is to provide a fluorescent dye decomposing agent having high safety and excellent decomposing ability of fluorescent dyes.
本発明者らは、鋭意研究した結果、マンガンペルオキシダーゼが蛍光染料を分解できることを見出した。さらに、本発明者は、マンガンペルオキシダーゼが優れた蛍光染料分解効果と高い安全性を有していることを見出した。かかる知見に基づき、本発明者は、安全性が高く、蛍光染料の分解力に優れた蛍光染料分解剤を提供することを可能とし、本発明を完成した。 As a result of intensive studies, the present inventors have found that manganese peroxidase can decompose fluorescent dyes. Furthermore, the present inventor has found that manganese peroxidase has an excellent fluorescent dye decomposition effect and high safety. Based on this knowledge, the present inventor has made it possible to provide a fluorescent dye decomposing agent that is highly safe and excellent in decomposing ability of the fluorescent dye, and has completed the present invention.
すなわち、本発明は、マンガンペルオキシターゼを有効成分とし、蛍光染料を分解する蛍光染料分解剤を提供する。 That is, the present invention provides a fluorescent dye decomposing agent that decomposes a fluorescent dye using manganese peroxidase as an active ingredient.
本発明に用いられているマンガンペルオキシダーゼについては、既にいくつかの機能が報告されている。すなわち、トリクロロエチレンなどの難分解性ハロゲン化炭水化物の化合物を分解する作用(特許文献6)、酵素の活性を増強するための媒介物質と併用することで染料を分解する作用(特許文献7)、パルプ繊維中のリグニンを分解する作用(特許文献8)、排水中のダイオキシン類などの難分解性物質の分解(特許文献9)などである。またリグニン討論会(1999)においてはマンガンペルオキシダーゼを用いた古紙パルプの処理法が発表され、脱リグニンに基づく漂白が可能であること等が示されたが、その中では直接的な蛍光染料の分解については考察されていない(非特許文献1)。このように、いくつかの機能が明らかになっているが、マンガンペルオキシダーゼによる直接的な蛍光染料分解作用は今まで報告されておらず、蛍光染料分解作用は今回初めて見出された作用である。 Several functions have already been reported for the manganese peroxidase used in the present invention. That is, an action of decomposing a hardly decomposable halogenated carbohydrate compound such as trichlorethylene (Patent Document 6), an action of decomposing a dye by using it together with a mediator for enhancing the activity of the enzyme (Patent Document 7), pulp These include the action of decomposing lignin in the fiber (Patent Document 8), the decomposition of hardly decomposable substances such as dioxins in the waste water (Patent Document 9), and the like. In addition, at the lignin debate (1999), a method for treating waste paper pulp using manganese peroxidase was announced, and it was shown that bleaching based on delignification is possible, among which direct decomposition of fluorescent dyes Is not considered (Non-Patent Document 1). Thus, although several functions have been clarified, a direct fluorescent dye degrading action by manganese peroxidase has not been reported so far, and the fluorescent dye degrading action has been found for the first time this time.
本発明に用いられているマンガンペルオキシダーゼは多くの微生物から分離されており、弱酸性の条件下で2価のマンガンイオンから3価のマンガンイオンを生成する。この3価のマンガンイオンはその酸化力を使って難分解性のフェノール性化合物や色素を分解することができる。酵素が直接フェノール性化合物や色素を分解するのではなく、分子量の小さいマンガンイオンが対象化合物を酸化するため、分子量の大きな酵素が進入しにくい繊維中や多くの化合物がゆるく結合するような比較的大きな粒子中にも3価のマンガンは進入することができる。そのため対象化合物の分解効率は非常に高い。 Manganese peroxidase used in the present invention is isolated from many microorganisms and produces trivalent manganese ions from divalent manganese ions under mildly acidic conditions. These trivalent manganese ions can decompose hardly decomposable phenolic compounds and pigments using their oxidizing power. Enzymes do not directly decompose phenolic compounds or pigments, but manganese ions with low molecular weight oxidize target compounds, so it is relatively difficult for large molecular weight enzymes to enter easily in fibers or many compounds that bind loosely. Trivalent manganese can also enter large particles. Therefore, the decomposition efficiency of the target compound is very high.
したがって、本発明の蛍光染料分解剤は、反応溶液中の蛍光染料を効率よく分解することができる。また、マンガンペルオキシダーゼ自体は皮膚に接した場合でも腐食性は非常に低く、水にて洗い流すだけで良い。したがって、本発明の蛍光染料分解剤は、従来、蛍光染料の分解に用いられているアルカリ、酸および塩素系の蛍光分解剤に比べて、非常に安全性が高い。 Therefore, the fluorescent dye decomposing agent of the present invention can efficiently decompose the fluorescent dye in the reaction solution. Further, even when manganese peroxidase itself is in contact with the skin, the corrosiveness is very low, and it is only necessary to wash away with water. Therefore, the fluorescent dye decomposing agent of the present invention is extremely safer than the alkali, acid and chlorine based fluorescent decomposing agents conventionally used for decomposing fluorescent dyes.
本発明に用いるマンガンペルオキシターゼは、食用担子菌に由来するマンガンペルオキシターゼであることが好ましい。
食用担子菌に由来するマンガンペルオキシターゼを有効成分とすることによって、より人体などへの安全性を高めることができる。
The manganese peroxidase used in the present invention is preferably a manganese peroxidase derived from an edible basidiomycete.
By using manganese peroxidase derived from edible basidiomycetes as an active ingredient, safety to the human body and the like can be further enhanced.
本発明における蛍光染料は、ウンベリフェロンおよび/またはスチルベン系蛍光増白剤であることが好ましく、さらに、スチルベン系蛍光増白剤であることが好ましい。
本発明の蛍光染料分解剤は、ウンベリフェロンおよび/またはスチルベン系蛍光増白剤を効率的に分解することができる。また、30分間の反応で、ウンベリフェロンならば50%以上、スチルベン系蛍光増白剤ならば90%程度が分解されるため、本発明の蛍光染料分解剤は実用性にも優れている。
The fluorescent dye in the present invention is preferably umbelliferone and / or a stilbene fluorescent brightener, and more preferably a stilbene fluorescent brightener.
The fluorescent dye decomposing agent of the present invention can efficiently decompose umbelliferone and / or a stilbene-based fluorescent brightening agent. Further, in the reaction for 30 minutes, umbelliferone decomposes 50% or more, and stilbene fluorescent whitening agent decomposes about 90%. Therefore, the fluorescent dye decomposing agent of the present invention is excellent in practicality.
また、本発明は、蛍光染料を含む溶液中でグルコースオキシダーゼおよびグルコースを反応させ、過酸化水素を生成する工程と、上記溶液にマンガンペルオキシターゼおよび2価のマンガンイオンを添加し、溶液中の蛍光染料と反応させて蛍光染料を分解する工程と、を備える蛍光染料の分解方法を提供する。本発明に用いるマンガンペルオキシターゼは、食用担子菌に由来するマンガンペルオキシターゼであることが好ましい。本発明における蛍光染料は、ウンベリフェロンおよび/またはスチルベン系蛍光増白剤であることが好ましく、さらに、スチルベン系蛍光増白剤であることが好ましい。 The present invention also includes a step of reacting glucose oxidase and glucose in a solution containing a fluorescent dye to produce hydrogen peroxide, adding manganese peroxidase and divalent manganese ions to the solution, and adding the fluorescent dye in the solution. And a method for decomposing the fluorescent dye, and a method for decomposing the fluorescent dye. The manganese peroxidase used in the present invention is preferably a manganese peroxidase derived from an edible basidiomycete. The fluorescent dye in the present invention is preferably umbelliferone and / or a stilbene fluorescent brightener, and more preferably a stilbene fluorescent brightener.
本発明の蛍光染料の分解方法によれば、溶液中の蛍光染料を効率よく分解することができる。また、本発明の蛍光染料の分解方法は安全性が高い。したがって、本発明の蛍光染料の分解方法はパルプの製造に適用することができ、蛍光染料を含む排水の排水処理に利用することができ、また、環境浄化作用を有する。マンガンペルオキシダーゼ自体は、活性汚泥中の微生物に悪影響を与えることはなく、通常の排水のラインで使用しても何ら問題はない。したがって、本発明の蛍光染料の分解方法はコスト面、設備面においても優れている。 According to the method for decomposing a fluorescent dye of the present invention, the fluorescent dye in a solution can be efficiently decomposed. In addition, the method for decomposing a fluorescent dye of the present invention is highly safe. Therefore, the method for decomposing a fluorescent dye of the present invention can be applied to pulp production, can be used for wastewater treatment of wastewater containing a fluorescent dye, and has an environmental purification action. Manganese peroxidase itself does not adversely affect microorganisms in the activated sludge, and there is no problem even if it is used in a normal drainage line. Therefore, the method for decomposing the fluorescent dye of the present invention is excellent in terms of cost and equipment.
さらに、本発明は、蛍光染料を含有する古紙を原料に用いる再生パルプの製造方法において、上記本発明の蛍光染料の分解方法を行い、パルプ中の蛍光染料を分解する再生パルプの製造方法を提供する。加えて、上記再生パルプの製造方法によって得られる再生パルプを提供する。また、再生パルプは食品用包装紙として用いられることが好ましい。 Furthermore, the present invention provides a method for producing regenerated pulp in which the method for decomposing a fluorescent dye of the present invention is performed in the method for producing regenerated pulp using waste paper containing a fluorescent dye as a raw material, and the fluorescent dye in the pulp is decomposed. To do. In addition, a regenerated pulp obtained by the above-described method for producing regenerated pulp is provided. The recycled pulp is preferably used as a food packaging paper.
本発明の再生パルプの製造方法によれば、再生パルプの原料である古紙中に含まれる蛍光染料を分解することができるため、効率的かつ安全に蛍光染料が分解された再生パルプを製造することができる。また、蛍光染料が効率的に低減された再生パルプを提供することができる。蛍光染料が効率的に低減されているため、再生紙からの蛍光染料の漏洩を低減することができ、安全性が高く、食品用包装紙としての用途に適した再生パルプを提供することができる。 According to the method for producing regenerated pulp of the present invention, since the fluorescent dye contained in the waste paper that is the raw material of the regenerated pulp can be decomposed, the regenerated pulp in which the fluorescent dye is decomposed efficiently and safely is produced. Can do. Moreover, the regenerated pulp in which the fluorescent dye was efficiently reduced can be provided. Since the fluorescent dye is efficiently reduced, leakage of the fluorescent dye from the recycled paper can be reduced, and a recycled pulp that is highly safe and suitable for use as a food packaging paper can be provided. .
本発明により、安全性が高く、優れた効果をもつ蛍光染料分解剤および蛍光染料の分解方法が提供される。また、蛍光染料が低減された再生パルプおよびその製造方法を提供することができる。本発明は、環境浄化・排水処理においても有効であり、蛍光増白剤を使用する洗剤工場の排水、その他、蛍光染料を含有する排水であれば、いかなる排水の蛍光染料の分解に使用することができる。コスト面、設備面においても優れている。 INDUSTRIAL APPLICABILITY According to the present invention, a fluorescent dye decomposing agent and a fluorescent dye decomposing method having high safety and excellent effects are provided. Moreover, the regenerated pulp in which fluorescent dye was reduced and the manufacturing method thereof can be provided. The present invention is effective in environmental purification and wastewater treatment, and is used for decomposing fluorescent dyes in any wastewater as long as it is wastewater from detergent factories that use fluorescent whitening agents, or other wastewater containing fluorescent dyes. Can do. It is excellent in terms of cost and equipment.
以下、本発明の構成および好適な実施形態について詳述するが、本発明はこれにより限定されるものではない。 Hereinafter, although the structure and preferred embodiment of this invention are explained in full detail, this invention is not limited by this.
まず、本実施形態における蛍光染料分解剤を説明する。本実施形態における蛍光染料分解剤は、マンガンペルオキシダーゼを有効成分として含有する。 First, the fluorescent dye decomposing agent in this embodiment will be described. The fluorescent dye decomposing agent in this embodiment contains manganese peroxidase as an active ingredient.
マンガンペルオキシダーゼとは、2価のマンガンイオンを3価のマンガンイオンに酸化する酵素である。本発明で使用するマンガンペルオキシダーゼは活性の発現に過酸化水素を必要とし、酵素は弱酸性領域で最大活性を発揮する。活性の更なる発現のために脂肪酸やTween80のような界面活性剤を反応系に含んでも良い。マンガンペルオキシダーゼは担子菌に属する白色腐朽菌や褐色腐朽菌などの微生物から得られるものであればどのようなものであっても構わない。中でも、食用担子菌が、安全上の理由から好ましい。また白色腐朽菌や褐色腐朽菌のゲノム中に存在するマンガンペルオキシダーゼ遺伝子を別の宿主に導入し、高発現させ、マンガンペルオキシダーゼを大量に入手することも可能である。具体的には、マンガンペルオキシダーゼをコードするmRNAよりcDNAを調製し、そのcDNAを大量発現プロモーターの下流に接続することで、マンガンペルオキシダーゼの大量発現コンストラクトを調製する。このコンストラクトをピヒア・パストリス(Pichia pastoris)などの酵母に導入し、大量のマンガンペルオキシダーゼを調製する方法がある。上記のようなマンガンペルオキシダーゼを得ることができれば、その製法は特に限定されない。また、本実施形態における蛍光染料分解剤は、マンガンペルオキシダーゼの他に、2価のマンガンイオン、過酸化水素または過酸化水素の供給源、緩衝液などを備えていてもよく、反応開始直前に調製するように、複数の反応剤(好ましくは、反応液)からなっていてもよい。 Manganese peroxidase is an enzyme that oxidizes divalent manganese ions to trivalent manganese ions. The manganese peroxidase used in the present invention requires hydrogen peroxide for the expression of activity, and the enzyme exhibits maximum activity in a weakly acidic region. In order to further develop the activity, a surfactant such as fatty acid or Tween 80 may be included in the reaction system. Manganese peroxidase may be any one as long as it is obtained from microorganisms such as white rot fungi and brown rot fungi belonging to basidiomycetes. Of these, edible basidiomycetes are preferred for safety reasons. It is also possible to obtain a large amount of manganese peroxidase by introducing the manganese peroxidase gene present in the genome of white rot fungi or brown rot fungus into another host and expressing it high. Specifically, a manganese peroxidase mass expression construct is prepared by preparing cDNA from mRNA encoding manganese peroxidase and connecting the cDNA downstream of the mass expression promoter. There is a method for preparing a large amount of manganese peroxidase by introducing this construct into a yeast such as Pichia pastoris. If the above manganese peroxidase can be obtained, the manufacturing method will not be specifically limited. In addition to the manganese peroxidase, the fluorescent dye decomposing agent in this embodiment may be provided with a divalent manganese ion, a hydrogen peroxide or hydrogen peroxide source, a buffer solution, etc., and prepared immediately before the start of the reaction. As such, it may be composed of a plurality of reactants (preferably, a reaction solution).
次に、本実施形態における蛍光染料の分解方法を説明する。本実施形態における蛍光染料の分解方法は、蛍光染料を含む溶液中でグルコースオキシダーゼおよびグルコースを反応させ、過酸化水素を生成する工程(過酸化水素生成工程)と、上記溶液にマンガンペルオキシターゼおよび2価のマンガンイオンを添加し、溶液中の蛍光染料と反応させて蛍光染料を分解する工程(蛍光染料分解工程)と、を備える。本実施形態で使用するマンガンペルオキシダーゼは、上記の蛍光染料分解剤であってよい。 Next, a method for decomposing the fluorescent dye in this embodiment will be described. The method for decomposing a fluorescent dye in the present embodiment includes a step of reacting glucose oxidase and glucose in a solution containing the fluorescent dye to generate hydrogen peroxide (hydrogen peroxide generating step), manganese peroxidase and divalent in the solution. And a step of decomposing the fluorescent dye by reacting with the fluorescent dye in the solution (fluorescent dye decomposition step). Manganese peroxidase used in the present embodiment may be the fluorescent dye decomposing agent described above.
マンガンペルオキシダーゼを使用する際は過酸化水素を必要とするため過酸化水素の添加系についても考慮する必要がある。(1)過酸化水素を直接反応系に添加する場合、(2)グルコースオキシダーゼを用い、グルコースを基質として過酸化水素を発生させる場合、の2通りの方法が挙げられる。特に、本実施形態の過酸化水素生成工程においては、(2)の方法が、継続的に過酸化水素を反応系に供給することができ、マンガンペルオキシダーゼの活性を維持するうえで好ましい。過酸化水素の反応系での濃度は1mM以下が好ましく、更に好ましくは0.05mM以上0.5mM以下である。過酸化水素の反応系での濃度が、1mMよりも大きい場合、マンガンペルオキシダーゼの活性が低下したり、活性そのものが失われたりする場合もある。また、過酸化水素の反応系での濃度が、0.05mM未満である場合、反応に関与する過酸化水素量が不十分となり、反応が効率的に進まない可能性がある。(1)の添加方法では、過酸化水素の濃度を均一にすることや一定量または一定範囲内に保つことが難しい場合があり、その場合、マンガンペルオキシダーゼの活性が低下したり、活性そのものが失われたりすることもある。 Since hydrogen peroxide is required when using manganese peroxidase, it is necessary to consider the hydrogen peroxide addition system. (1) When hydrogen peroxide is added directly to the reaction system, (2) When using glucose oxidase and generating hydrogen peroxide using glucose as a substrate, there are two methods. In particular, in the hydrogen peroxide generation step of the present embodiment, the method (2) is preferable in that hydrogen peroxide can be continuously supplied to the reaction system and the activity of manganese peroxidase is maintained. The concentration of hydrogen peroxide in the reaction system is preferably 1 mM or less, more preferably 0.05 mM or more and 0.5 mM or less. When the concentration of hydrogen peroxide in the reaction system is higher than 1 mM, the activity of manganese peroxidase may be reduced or the activity itself may be lost. Further, when the concentration of hydrogen peroxide in the reaction system is less than 0.05 mM, the amount of hydrogen peroxide involved in the reaction becomes insufficient, and the reaction may not proceed efficiently. In the addition method (1), it may be difficult to make the concentration of hydrogen peroxide uniform or to keep it within a certain amount or within a certain range. In this case, the activity of manganese peroxidase decreases or the activity itself is lost. Sometimes it breaks.
次の蛍光染料分解工程において、マンガンペルオキシダーゼを使用するときの条件は、温度は、30℃〜70℃、好ましくは37℃〜60℃、更に好ましくは45℃〜55℃である。反応pHは、pH3.0〜6.9、好ましくはpH4.0〜6.0、更に好ましくはpH4.5〜5.5である。蛍光染料分解に際し、使用されるマンガンペルオキシダーゼは適当量の添加であれば全く問題はないが、経済性を考慮した場合、反応系における酵素力価は0.01U/mlから100U/ml、好ましくは0.05U/mlから5U/ml、更に好ましくは0.05U/mlから2U/mlの範囲である。 In the next fluorescent dye decomposition step, the conditions for using manganese peroxidase are 30 ° C. to 70 ° C., preferably 37 ° C. to 60 ° C., more preferably 45 ° C. to 55 ° C. The reaction pH is pH 3.0 to 6.9, preferably pH 4.0 to 6.0, and more preferably pH 4.5 to 5.5. In the decomposition of the fluorescent dye, there is no problem if the manganese peroxidase to be used is added in an appropriate amount. However, in consideration of economy, the enzyme titer in the reaction system is 0.01 U / ml to 100 U / ml, preferably The range is 0.05 U / ml to 5 U / ml, more preferably 0.05 U / ml to 2 U / ml.
蛍光染料の分解に際して、パルプ繊維中の蛍光染料の分解効率を上げるために、公知のリグニン分解酵素である、リグニンペルオキシダーゼやラッカーゼといった酵素との併用も可能である。また、多糖分解酵素であるキシラナーゼやアミラーゼといった酵素との併用も可能である。 When the fluorescent dye is decomposed, in order to increase the decomposition efficiency of the fluorescent dye in the pulp fiber, it can be used in combination with known lignin-degrading enzymes such as lignin peroxidase and laccase. Further, it can be used in combination with enzymes such as xylanase and amylase which are polysaccharide degrading enzymes.
蛍光染料とは、色素が蛍光物質である染料をいい、蛍光剤とも言う。特に、蛍光による増白効果を狙って古紙パルプや衣料用洗剤に添加される蛍光染料を蛍光増白剤と言う。蛍光染料の中には、有害物質に化学構造が似ているものがあり発ガン性の疑いも持たれているため、蛍光染料の安全性が疑われている。また、蛍光染料は一般に極めて分解性が悪く、環境中で完全に分解されるには2ヶ月以上かかるとも言われている。つまり、再生パルプ製造時の排水に混じって河川に放流されて残留し、環境汚染の元凶となっている。 A fluorescent dye refers to a dye whose pigment is a fluorescent substance and is also referred to as a fluorescent agent. In particular, a fluorescent dye added to waste paper pulp or laundry detergent for the purpose of whitening effect by fluorescence is called fluorescent whitening agent. Some fluorescent dyes have similar chemical structures to harmful substances and are suspected to be carcinogenic, so the safety of fluorescent dyes is suspected. In addition, fluorescent dyes are generally very poorly degradable, and it is said that it takes more than two months to be completely decomposed in the environment. In other words, it is mixed with wastewater from the production of recycled pulp and discharged into the river and remains, causing environmental pollution.
マンガンペルオキシダーゼは蛍光染料の中でも(1)ウンベリフェロンのようなクマリン系蛍光染料、(2)スチルベン系の蛍光増白剤、の2種の分解特性に優れていることを、本発明者は見出した。現在、古紙や洗剤などに使用される蛍光増白剤はスチルベン系の化合物が多く、マンガンペルオキシダーゼはこの蛍光増白剤を効率的に分解することができる。 The present inventors have found that manganese peroxidase is excellent in two decomposition properties among fluorescent dyes: (1) a coumarin fluorescent dye such as umbelliferone and (2) a stilbene fluorescent brightener. It was. At present, there are many stilbene compounds as fluorescent brighteners used in waste paper and detergents, and manganese peroxidase can efficiently decompose the fluorescent brightener.
マンガンペルオキシダーゼを有効成分とする蛍光染料分解剤は、塩素系蛍光染料分解剤と比較して非常に安全である。マンガンペルオキシダーゼ自体は皮膚に接した場合でも腐食性は非常に低く、水にて洗い流すだけで良い。一方の塩素系蛍光染料分解剤は皮膚に接触した場合、炎症、糜爛といった症状を起こし、医師の処置を受ける必要があることもある。 A fluorescent dye decomposing agent containing manganese peroxidase as an active ingredient is very safe compared to a chlorine-based fluorescent dye decomposing agent. Manganese peroxidase itself is very corrosive even when it comes into contact with the skin, and it can be washed away with water. On the other hand, when a chlorine-based fluorescent dye decomposing agent comes into contact with the skin, it causes symptoms such as inflammation and wrinkles, and may require treatment by a doctor.
本発明のマンガンペルオキシダーゼを有効成分とする蛍光染料分解剤を用いる場合、マンガンペルオキシダーゼを含む酵素液を直接反応系に添加しても良いが、マンガンペルオキシダーゼを担体に固定化し、過酸化水素と反応させて生成する3価のマンガンイオンのみを分解剤として使っても良い。 When using a fluorescent dye decomposing agent comprising manganese peroxidase of the present invention as an active ingredient, an enzyme solution containing manganese peroxidase may be added directly to the reaction system, but manganese peroxidase is immobilized on a carrier and reacted with hydrogen peroxide. Only trivalent manganese ions produced in this manner may be used as a decomposing agent.
本願のマンガンペルオキシダーゼを有効成分とする蛍光染料分解剤は、蛍光染料の存在する古紙パルプ、古紙パルプの排水、蛍光増白剤を使用する洗剤工場の排水、その他、蛍光染料を含有する排水であれば、いかなる排水の蛍光染料の分解に使用することができる。マンガンペルオキシダーゼ自体は、活性汚泥中の微生物に悪影響を与えることはなく、通常の排水のラインで使用しても何ら問題はない。 The fluorescent dye degrading agent containing manganese peroxidase as an active ingredient of the present application may be waste paper pulp containing fluorescent dye, waste paper pulp waste water, waste water from detergent factories using fluorescent whitening agents, or waste water containing fluorescent dyes. For example, it can be used for decomposition of any wastewater fluorescent dye. Manganese peroxidase itself does not adversely affect microorganisms in the activated sludge, and there is no problem even if it is used in a normal drainage line.
最後に、本実施形態における再生パルプの製造方法を説明する。本実施形態における再生パルプの製造方法は、蛍光染料を含有する古紙を原料に用いる再生パルプの製造方法において、上記の蛍光染料の分解方法を行い、パルプ中の蛍光染料を分解する再生パルプの製造方法である。 Finally, the manufacturing method of the regenerated pulp in this embodiment is demonstrated. The method for producing regenerated pulp in the present embodiment is a method for producing regenerated pulp that decomposes the fluorescent dye in the pulp by performing the method for decomposing the fluorescent dye in the method for producing regenerated pulp using the waste paper containing the fluorescent dye as a raw material. Is the method.
従来の再生パルプの製造方法は、一般的には、古紙を離解してパルプ懸濁液を得る離解工程と、パルプ懸濁液中の異物を分離する粗選・精選工程と、印刷インキを分離する脱墨工程と、再生パルプの色を白くする漂白工程とを経て再生パルプ化が行われている。 Conventional methods for producing recycled pulp generally include a disaggregation process in which waste paper is disaggregated to obtain a pulp suspension, a coarse selection / selection process in which foreign matter in the pulp suspension is separated, and a printing ink is separated. Regenerated pulping is carried out through a deinking process that performs and a bleaching process that whitens the color of the regenerated pulp.
本実施形態における再生パルプの製造方法においては、従来の漂白工程の代わりに上述した蛍光染料の分解方法を行う。これによって、再生パルプの原料である古紙中に含まれる蛍光染料を効率的かつ安全に分解することができる。したがって、含有される蛍光染料が低減された再生パルプを得ることができる。蛍光染料が効率的に低減されているため、再生紙からの蛍光染料の漏洩を低減することができ、安全性が高く、食品用包装紙としての用途に適した再生パルプを提供することができる。 In the method for producing regenerated pulp in the present embodiment, the above-described method for decomposing a fluorescent dye is performed instead of the conventional bleaching step. Thereby, the fluorescent dye contained in the waste paper which is the raw material of the recycled pulp can be decomposed efficiently and safely. Therefore, a regenerated pulp in which the contained fluorescent dye is reduced can be obtained. Since the fluorescent dye is efficiently reduced, leakage of the fluorescent dye from the recycled paper can be reduced, and a recycled pulp that is highly safe and suitable for use as a food packaging paper can be provided. .
以下、本発明を実施例により詳細に説明するが、本発明はこれにより限定されるものではない。 EXAMPLES Hereinafter, although an Example demonstrates this invention in detail, this invention is not limited by this.
まず、本実施例のマンガンペルオキシダーゼの調製例、ならびに、酵素活性および蛍光染料分解活性の測定例を示す。次に、本実施例の蛍光染料分解剤を用いた蛍光染料の分解能を検査した実施例を示し、最後に、本実施例の蛍光染料分解剤の安全性を検査した実施例を示す。 First, preparation examples of manganese peroxidase of this example and measurement examples of enzyme activity and fluorescent dye decomposing activity are shown. Next, an example in which the resolution of the fluorescent dye using the fluorescent dye decomposing agent of this example was inspected is shown, and finally, an example in which the safety of the fluorescent dye decomposing agent of this example was inspected is shown.
<調製例1:白色腐朽菌の培養>
使用菌株として、白色腐朽菌Phanerochaete sordida(ATCC90872)を用いた。白色腐朽菌の培養液から白色腐朽菌由来のマンガンペルオキシダーゼを含む酵素液を調製した。
<Preparation Example 1: Culture of white rot fungi>
The white rot fungus Phanerochaete sordida (ATCC 90872) was used as the strain used. An enzyme solution containing manganese peroxidase derived from white rot fungi was prepared from a culture solution of white rot fungi.
白色腐朽菌の培養方法は、以下の通りである。まず、白色腐朽菌の種菌をポテトデキストロース寒天培地上で30℃、3日間前培養した。次に、前培養の後に集菌し、ミキサーでホモジナイズした菌体を本培養の液体培地に接種して本培養を行った。本培養の液体培地は、10g/l グルコース、0.22g/l(1.2mM) 酒石酸アンモニウム、1.64g/l(20mM) 酢酸ナトリウム、1.0g/l Tween80、および微量金属塩を含む液体培地(pH4.5)であり、500ml三角フラスコに対し、200mlの液体培地を用いた。本培養は以下の条件で行った。菌体の接種後、30℃、150rpmで振とう培養した。培養3日目に、終濃度が1.25g/lとなるようにベラトリルアルコールを添加した。その後、フラスコのヘッドスペース内を毎日1時間ほど酸素ガスで置換しながら、引き続き、30℃、150rpmで振とう培養を行った。最終的に7日間培養した。 The method for cultivating white rot fungi is as follows. First, a white rot fungus was pre-cultured on a potato dextrose agar medium at 30 ° C. for 3 days. Next, the cells were collected after pre-culture and homogenized with a mixer to inoculate the liquid culture medium for main culture. The liquid medium of the main culture is a liquid containing 10 g / l glucose, 0.22 g / l (1.2 mM) ammonium tartrate, 1.64 g / l (20 mM) sodium acetate, 1.0 g / l Tween 80, and a trace metal salt. It was a medium (pH 4.5), and 200 ml of liquid medium was used for a 500 ml Erlenmeyer flask. The main culture was performed under the following conditions. After inoculation of the cells, the cells were cultured with shaking at 30 ° C. and 150 rpm. On the third day of culture, veratryl alcohol was added to a final concentration of 1.25 g / l. Thereafter, while the inside of the flask head space was replaced with oxygen gas for about 1 hour every day, the culture was continued with shaking at 30 ° C. and 150 rpm. Finally, it was cultured for 7 days.
そして、得られた白色腐朽菌の培養液から、以下の方法で白色腐朽菌由来のマンガンペルオキシダーゼを含む酵素液を調製した。ろ紙にて菌体を除去した後、ポアサイズ0.2μmのメンブレンフィルターでろ過したろ液を回収し、これを酵素液1とした。
培養最終日の培養液から得られた酵素液1のマンガンペルオキシダーゼ酵素活性は、2.5U/mlであった。酵素活性の測定法には、次に述べる方法を用いた。
Then, an enzyme solution containing manganese peroxidase derived from white rot fungi was prepared from the obtained white rot fungus culture solution by the following method. After removing the cells with filter paper, the filtrate filtered through a membrane filter having a pore size of 0.2 μm was collected, and this was designated as enzyme solution 1.
Manganese peroxidase enzyme activity of enzyme solution 1 obtained from the culture solution on the last day of culture was 2.5 U / ml. The following method was used for measuring the enzyme activity.
<マンガンペルオキシダーゼ酵素活性の測定方法>
酵素活性の測定に用いる反応液は、以下の組成とした。1.0mM 2,6−ジメトキシフェノール、1.0mM 硫酸マンガン(II)、50mM マロン酸ナトリウム緩衝液(pH4.5)、0.2mM 過酸化水素水。反応開始前に、セル中に過酸化酸素以外の反応液と酵素液100μlとを混合し、37℃にて5分間保温した。そして、終濃度0.2mMとなるように過酸化水素水を添加して混合液の終量を1mlとし、37℃にて反応を開始した。生成したMn(III)−マロン酸錯体による2,6−ジメトキシフェノールの酸化に基づく469nmの吸光度変化を測定した。モル吸光係数は49.6mM−1cm−1として酵素活性を算出した。マンガンペルオキシダーゼの酵素活性1ユニット〔U〕は、1分間に2,6−ジメトキシフェノール酸化物が1μmol生成される値として定義した。
<Method for Measuring Manganese Peroxidase Enzyme Activity>
The reaction solution used for measuring enzyme activity had the following composition. 1.0 mM 2,6-dimethoxyphenol, 1.0 mM manganese sulfate (II), 50 mM sodium malonate buffer (pH 4.5), 0.2 mM hydrogen peroxide solution. Prior to the start of the reaction, a reaction solution other than oxygen peroxide and 100 μl of enzyme solution were mixed in the cell and kept at 37 ° C. for 5 minutes. And hydrogen peroxide water was added so that it might become final concentration of 0.2 mM, the final amount of the liquid mixture was made into 1 ml, and reaction was started at 37 degreeC. The absorbance change at 469 nm based on the oxidation of 2,6-dimethoxyphenol by the produced Mn (III) -malonic acid complex was measured. The enzyme activity was calculated with a molar extinction coefficient of 49.6 mM −1 cm −1 . One unit [U] of the enzyme activity of manganese peroxidase was defined as the value at which 1 μmol of 2,6-dimethoxyphenol oxide was produced per minute.
<調製例2:遺伝子組み換えによるマンガンペルオキシダーゼの大量調製>
(1)マンガンペルオキシダーゼ遺伝子のクローニング
白色腐朽担子菌Phanerochaete chrysosporium(ATCC24725)のマンガンペルオキシダーゼcDNAを以下の手法によりクローニングした。菌体の培養には、基質としてCF11(コットン由来セルロースファイバー)を用い、基質濃度は2%、窒素源として尿素を0.06%、リン酸水素アンモニウムを0.026%添加した。前述の本培養の液体培地に植菌後、37℃、150rpmにて4日間振とう培養し、培養後、グラスフィルターにて菌体を濾別回収した。得られた菌体は液体窒素にて凍結粉砕し、これをmRNA抽出のための材料として供した。まず、E.Z.N.A.(商標)FungalRNA抽出キット(Omega Bio−Tek製)を用いて全RNAを抽出した。次に、Oligotex(商標)−dt30<Super>mRNA Purification kit(タカラバイオ製)を用いてmRNAを精製した。得られたmRNAからcDNAへの逆転写反応は、ReverTra Ace(東洋紡製)およびoligo(dT)30プライマーを用いて行った。得られたcDNAを鋳型として、マンガンペルオキシダーゼ5遺伝子の特異的プライマーを用いてPCRを行い、マンガンペルオキシダーゼの全長cDNAをクローニングした。マンガンペルオキシダーゼ5の遺伝子特異的プライマーは、Phanerochaete chrysosporiumのゲノム情報を元に設計した。特異的プライマーの配列は以下の通りである。Foward:5’−CGACAGACAG GGCTGCCGTG TGCG−3’(配列番号1)、および、Reverse:5’−TCAAGCCGGG CCGTCGAA−3’(配列番号2)。
<Preparation Example 2: Large-scale preparation of manganese peroxidase by genetic recombination>
(1) Cloning of Manganese Peroxidase Gene Manganese peroxidase cDNA of white-rot basidiomycete Phanerochaete chrysosporum (ATCC 24725) was cloned by the following method. For culturing cells, CF11 (cotton-derived cellulose fiber) was used as a substrate, the substrate concentration was 2%, urea was added as a nitrogen source, 0.06%, and ammonium hydrogenphosphate was added as 0.026%. After inoculating the above-mentioned liquid culture of the main culture, the cells were cultured with shaking at 37 ° C. and 150 rpm for 4 days. After the culture, the cells were collected by filtration with a glass filter. The obtained microbial cells were freeze-ground with liquid nitrogen and used as a material for mRNA extraction. First, E.I. Z. N. A. Total RNA was extracted using a (trademark) Fungal RNA extraction kit (Omega Bio-Tek). Next, mRNA was purified using Oligotex (trademark) -dt30 <Super> mRNA Purification kit (manufactured by Takara Bio Inc.). The reverse transcription reaction from the obtained mRNA to cDNA was performed using RiverTra Ace (Toyobo) and oligo (dT) 30 primer. Using the obtained cDNA as a template, PCR was performed using specific primers of the manganese peroxidase 5 gene, and the full-length manganese peroxidase cDNA was cloned. The gene-specific primer for manganese peroxidase 5 was designed based on the genome information of Phanerochaete chrysosporium. Specific primer sequences are as follows. Foward: 5′-CGACAGACAG GGCTCGCCGTG TGCG-3 ′ (SEQ ID NO: 1) and Reverse: 5′-TCAAGCCGGGG CCGTCGAA-3 ′ (SEQ ID NO: 2).
(2)マンガンペルオキシダーゼ発現コンストラクトの構築
得られたcDNAをEcoRIおよびNotI(タカラバイオ製)を用いて制限酵素処理し、ライゲーションキットとしてDNA ligationKit(タカラバイオ製)を用い、ピヒア・パストリス(Pichia pastoris)発現用ベクターであるpPICZαA(Invitrogen社製)にライゲーションした。そしてこの反応液を用い、コンピテントセルJMI09(タカラバイオ製)に形質転換してクローニングし、マンガンペルオキシダーゼ発現コンストラクト(MnP5/pPICZαA)を得た。
(2) Construction of Manganese Peroxidase Expression Construct The obtained cDNA was subjected to restriction enzyme treatment using EcoRI and NotI (manufactured by Takara Bio), and DNA ligation Kit (manufactured by Takara Bio) as a ligation kit, and Pichia pastoris (Pichia pastoris) Ligation was performed with pPICZαA (manufactured by Invitrogen), which is an expression vector. Then, using this reaction solution, it was transformed into competent cell JMI09 (manufactured by Takara Bio Inc.) and cloned to obtain a manganese peroxidase expression construct (MnP5 / pPICZαA).
(3)マンガンペルオキシダーゼタンパク質の発現
マンガンペルオキシダーゼ発現コンストラクトをBpu1102I(タカラバイオ製)で制限酵素処理し、得られた2本鎖直鎖DNAをエレクトロポレーション法にて、ピヒア・パストリスKM−71株に導入した。形質転換体の選抜は、抗生物質耐性(Zeocin耐性)を指標に行った。
(3) Manganese peroxidase protein expression Manganese peroxidase expression construct was subjected to restriction enzyme treatment with Bpu1102I (manufactured by Takara Bio Inc.), and the resulting double-stranded linear DNA was transformed into Pichia pastoris KM-71 strain by electroporation. Introduced. Selection of transformants was performed using antibiotic resistance (Zeocin resistance) as an index.
上述の形質転換体をYPG培地(25ug/ml Zeocin含有)にて培養し、菌体を回収した。次に、Hemin(1000μモル)および炭素源としてメタノール(1%)を含むYP培地を用いて27℃、150rpmにて振とう培養を3日間行った後に、菌体外液を5000rpmで20分間遠心分離して上清液を回収し、酵素液2とした。この酵素液のマンガンペルオキシダーゼ活性は1U/mlであった。 The above transformant was cultured in a YPG medium (containing 25 ug / ml Zeocin), and the cells were collected. Next, after shaking culture at 27 ° C. and 150 rpm for 3 days using YP medium containing Hemin (1000 μmol) and methanol (1%) as a carbon source, the extracellular solution was centrifuged at 5000 rpm for 20 minutes. After separation, the supernatant was recovered and used as enzyme solution 2. The manganese peroxidase activity of this enzyme solution was 1 U / ml.
<実施例1:ウンベリフェロンの分解>
調製例1および調製例2により得られた酵素液1および酵素液2を用いて蛍光染料の分解能を調べるための実験を行った。基質には蛍光染料ウンベリフェロンを用いた。
4−0−メチルウンベリフェロン(Sigma社製)を100μモル/lとなるように50mM マロン酸緩衝液(pH4.5)に溶解し、これを基質溶液とした。酵素ストック溶液には、酵素液1および2を酵素活性1U/mlに調製したものを用いた。酵素液の酵素力価の希釈調製には50mM マロン酸緩衝液(pH4.5)を用いた。
<Example 1: Decomposition of umbelliferone>
Using the enzyme solution 1 and the enzyme solution 2 obtained in Preparation Example 1 and Preparation Example 2, an experiment for examining the resolution of the fluorescent dye was performed. The substrate used was the fluorescent dye umbelliferone.
4-0-methylumbelliferone (manufactured by Sigma) was dissolved in 50 mM malonate buffer (pH 4.5) so as to be 100 μmol / l, and this was used as a substrate solution. As the enzyme stock solution, the enzyme solutions 1 and 2 prepared to have an enzyme activity of 1 U / ml were used. A 50 mM malonate buffer solution (pH 4.5) was used for dilution preparation of the enzyme titer of the enzyme solution.
実施例1の反応系は、最終的に200μlとなるように50mM マロン酸緩衝液(pH4.5)を用いて調製した。反応系中には、基質溶液(終濃度0.1mM)に加え、硫酸マンガンを終濃度0.5mM、過酸化水素を終濃度0.5mMとなるように添加した。また、酵素液は0.05U/mlとなるように反応系に添加した。対照実験用には、熱失活させた酵素液1を使用した。なお、反応は37℃にて実施した。 The reaction system of Example 1 was prepared using 50 mM malonate buffer (pH 4.5) so that the final volume was 200 μl. In the reaction system, manganese sulfate was added to a final concentration of 0.5 mM, and hydrogen peroxide was added to a final concentration of 0.5 mM in addition to the substrate solution (final concentration of 0.1 mM). Moreover, the enzyme solution was added to the reaction system so that it might become 0.05 U / ml. For the control experiment, the heat-inactivated enzyme solution 1 was used. The reaction was carried out at 37 ° C.
蛍光強度の測定には、大日本住友製薬製のフルオロスキャン・アセントを使用し、励起波長355nm、測定波長450nmにて測定した。酵素添加後(反応開始後)、0min、15minおよび30minにおける蛍光強度を測定した。 The fluorescence intensity was measured using Fluoroscan Ascent manufactured by Dainippon Sumitomo Pharma Co., Ltd. at an excitation wavelength of 355 nm and a measurement wavelength of 450 nm. After enzyme addition (after the start of the reaction), the fluorescence intensity at 0 min, 15 min and 30 min was measured.
<結果>
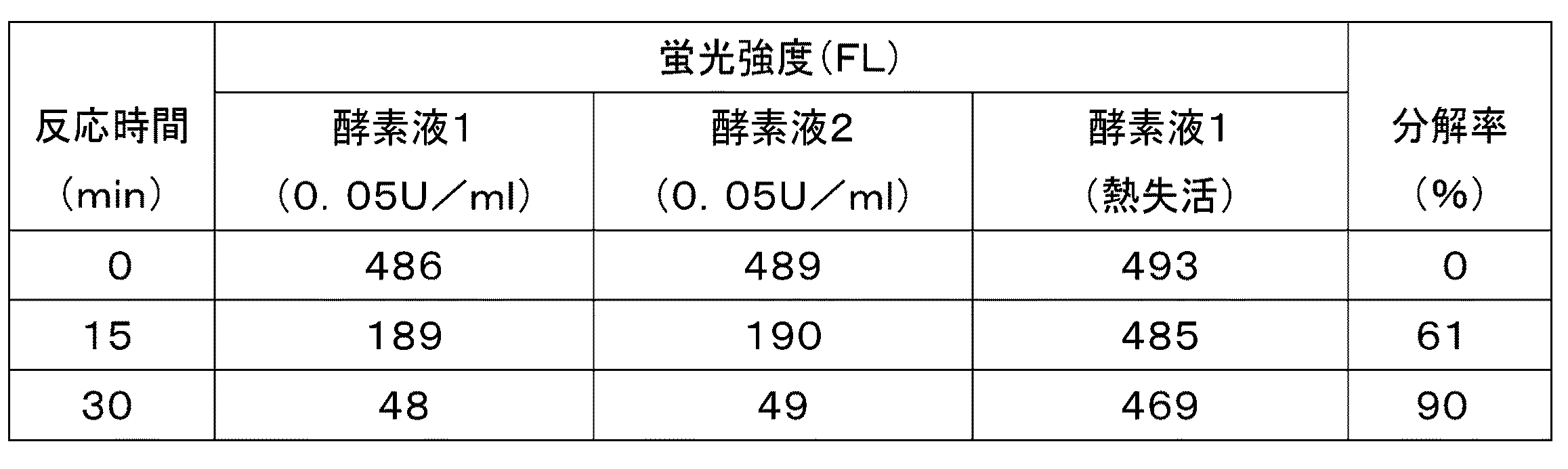
実施例1の結果を表1に示す。表1は、マンガンペルオキシダーゼによる蛍光染料の分解に伴う蛍光強度の変化を示す。実施例1の結果から、マンガンペルオキシダーゼ酵素活性をもつ酵素液1および2は、4−0−メチルウンベリフェロン分解能を有することが明らかとなった。また、反応開始30min後には47%の4−0−メチルウンベリフェロンが分解されることが分かった。
<Result>
The results of Example 1 are shown in Table 1. Table 1 shows the change in fluorescence intensity associated with the decomposition of the fluorescent dye by manganese peroxidase. From the results of Example 1, it was revealed that enzyme solutions 1 and 2 having manganese peroxidase enzyme activity have 4-0-methylumbelliferone resolution. It was also found that 47% of 4-0-methylumbelliferone was decomposed 30 minutes after the start of the reaction.
<実施例2:スチルベン系増白剤の分解>
基質にもちいる蛍光物質以外は、実施例1と同様にして、実施例2を行った。基質には、スチルベン系増白剤であるKayaphor NW(日本化薬製)を用い、反応系での基質濃度を0.001%とした。
<Example 2: Decomposition of stilbene brightener>
Example 2 was carried out in the same manner as Example 1 except for the fluorescent material used for the substrate. As the substrate, Kyaphor NW (manufactured by Nippon Kayaku), which is a stilbene brightener, was used, and the substrate concentration in the reaction system was 0.001%.
<結果>
実施例2の結果を表2に示す。表2は、マンガンペルオキシダーゼによる蛍光染料の分解に伴う蛍光強度の変化を示す。実施例2の結果から、マンガンペルオキシダーゼ酵素活性をもつ酵素液1および2は、Kayaphor NW分解能を有することが明らかとなった。また、反応開始30min後には90%のKayaphor NWが分解されることが分かった。
<Result>
The results of Example 2 are shown in Table 2. Table 2 shows changes in fluorescence intensity accompanying the decomposition of the fluorescent dye by manganese peroxidase. From the results of Example 2, it was revealed that enzyme solutions 1 and 2 having manganese peroxidase enzyme activity have Kayphor NW resolution. It was also found that 90% Kyaphor NW was decomposed 30 minutes after the start of the reaction.
実施例1および2の結果から、マンガンペルオキシダーゼは、蛍光染料および蛍光増白剤を分解できることが分かった。また本実施例の条件(反応時間30min)において、マンガンペルオキシダーゼは、ウンベリフェロンおよびスチルベン系増白剤をそれぞれ半分以下および90%分解することから、本実施例における酵素液1および酵素液2の反応系は、実用的かつ効率的であることが明らかとなった。特許文献9には、微生物によるダイオキシンの分解が開示されているが、この文献において、ダイオキシンを90%分解するのに1ヶ月を要している。このことから、マンガンペルオキシダーゼは、クマリン系蛍光染料およびスチルベン系増白剤の分解特性が著しく優れていることが分かる。したがって、マンガンペルオキシダーゼ処理することによって、蛍光染料、蛍光増白剤が存在する古紙パルプやパルプ製造時の排水を効率的かつ実用的に蛍光物質を分解することができる。 From the results of Examples 1 and 2, it was found that manganese peroxidase can decompose fluorescent dyes and fluorescent brighteners. Further, under the conditions of this example (reaction time 30 min), manganese peroxidase decomposes umbelliferone and stilbene-based brighteners by less than half and 90%, respectively, so that enzyme solution 1 and enzyme solution 2 in this example The reaction system was found to be practical and efficient. Patent Document 9 discloses the decomposition of dioxins by microorganisms. In this document, it takes one month to decompose 90% of dioxins. From this, it can be seen that manganese peroxidase is remarkably excellent in the decomposition characteristics of coumarin fluorescent dyes and stilbene brighteners. Therefore, by treating with manganese peroxidase, the fluorescent material can be efficiently and practically decomposed in waste paper pulp containing fluorescent dyes and fluorescent whitening agents and wastewater during pulp production.
<安全性試験>
マンガンペルオキシダーゼの安全性を確認するため、以下の方法で「皮膚刺激性試験」および「急性経口毒性試験」を実施した。
<Safety test>
In order to confirm the safety of manganese peroxidase, a “skin irritation test” and an “acute oral toxicity test” were performed by the following methods.
<皮膚刺激性試験>
調製例1および調製例2により得られた酵素液1および酵素液2(それぞれ1.0U/ml、100ul)を、各々、除毛後のC3Hマウス(オス、6週齢、各群10匹、日本チャールズリバー(株)製)の背中に連続塗布した(1回/日、約1ヶ月間)。塗布期間および塗布終了後の2週間、マウスの背中において、紅斑、浮腫、炎症などの異常は特に観察されなかった。また、対照群(水塗布群)と比較し、体重推移においても有意差(P<0.05)は認められなかった。
<Skin irritation test>
Enzyme solution 1 and enzyme solution 2 obtained by Preparation Example 1 and Preparation Example 2 (1.0 U / ml, 100 ul, respectively) were respectively removed from C3H mice (male, 6 weeks of age, 10 mice in each group) It was continuously applied to the back of Nippon Charles River Co., Ltd. (once / day for about 1 month). Abnormalities such as erythema, edema and inflammation were not particularly observed on the back of the mice during the application period and 2 weeks after the application was completed. In addition, no significant difference (P <0.05) was observed in the body weight transition as compared with the control group (water application group).
酵素液1および酵素液2(それぞれ1.0U/ml)を、各々、除毛後のICR系マウス(オス、6週齢、各群10匹、日本チャールズリバー(株)製)に胃ゾンデを用いて経口投与した(投与量5g/マウス体重1kg)。投与してから2週間後まで、死亡例はなかった。また、体重推移においても対照群(水投与群)と比較して有意差(P<0.05)は認められなかった。 Enzyme Solution 1 and Enzyme Solution 2 (each 1.0 U / ml) were each treated with a gastric sonde on ICR mice (male, 6 weeks old, 10 per group, manufactured by Charles River Japan) after hair removal. And orally administered (dosage 5 g / mouse body weight 1 kg). There were no deaths until 2 weeks after administration. In addition, there was no significant difference (P <0.05) in the body weight transition compared to the control group (water administration group).
本発明で得られるマンガンペルオキシダーゼを有効成分として含む蛍光染料分解剤は、安全性が高く、環境浄化、排水処理、パルプの製造分野に利用することができる。 The fluorescent dye decomposing agent containing manganese peroxidase obtained as an active ingredient in the present invention is highly safe and can be used in the fields of environmental purification, wastewater treatment, and pulp production.
Claims (9)
前記溶液にマンガンペルオキシターゼおよび2価のマンガンイオンを添加し、溶液中の蛍光染料と反応させて蛍光染料を分解する工程と、
を備える蛍光染料の分解方法。 Reacting glucose oxidase and glucose in a solution containing a fluorescent dye to produce hydrogen peroxide;
Adding manganese peroxidase and divalent manganese ions to the solution and reacting with the fluorescent dye in the solution to decompose the fluorescent dye;
A method for decomposing a fluorescent dye comprising:
請求項4〜6のいずれか一項に記載の蛍光染料の分解方法を行い、パルプ中の蛍光染料を分解する再生パルプの製造方法。 In a method for producing recycled pulp using waste paper containing a fluorescent dye as a raw material,
The manufacturing method of the regenerated pulp which performs the decomposition | disassembly method of the fluorescent dye as described in any one of Claims 4-6, and decomposes | disassembles the fluorescent dye in a pulp.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007302145A JP2009124976A (en) | 2007-11-21 | 2007-11-21 | Fluorescent dye-decomposing agent |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007302145A JP2009124976A (en) | 2007-11-21 | 2007-11-21 | Fluorescent dye-decomposing agent |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2009124976A true JP2009124976A (en) | 2009-06-11 |
Family
ID=40816511
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007302145A Pending JP2009124976A (en) | 2007-11-21 | 2007-11-21 | Fluorescent dye-decomposing agent |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2009124976A (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015533197A (en) * | 2012-10-10 | 2015-11-19 | バックマン・ラボラトリーズ・インターナショナル・インコーポレーテッドBuckman Laboratories International Incorporated | Immobilization of mineral oil in paper food packaging containing laccase to prevent movement of mineral oil into food |
| CN109628331A (en) * | 2019-02-25 | 2019-04-16 | 大连大学 | The basidiomycetes of one plant of production low temperature glucose oxidase |
-
2007
- 2007-11-21 JP JP2007302145A patent/JP2009124976A/en active Pending
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015533197A (en) * | 2012-10-10 | 2015-11-19 | バックマン・ラボラトリーズ・インターナショナル・インコーポレーテッドBuckman Laboratories International Incorporated | Immobilization of mineral oil in paper food packaging containing laccase to prevent movement of mineral oil into food |
| CN109628331A (en) * | 2019-02-25 | 2019-04-16 | 大连大学 | The basidiomycetes of one plant of production low temperature glucose oxidase |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Archibald | Lignin peroxidase activity is not important in biological bleaching and delignification of unbleached kraft pulp by Trametes versicolor | |
| Pereira et al. | Environmentally friendly bleaching of cotton using laccases | |
| AU663501B2 (en) | Process, using enhanced-action laccase enzymes, for the delignification or bleaching of lignocellulose-containing material or for the treatment of waste water | |
| Moldes et al. | Comparative study of the efficiency of synthetic and natural mediators in laccase-assisted bleaching of eucalyptus kraft pulp | |
| Couto et al. | Lacasses in the textile industry | |
| Shoham et al. | Delignification of wood pulp by a thermostable xylanase from Bacillus stearothermophilus strain T-6 | |
| RU2130523C1 (en) | Multicomponent system for changing, decomposing, and bleaching lignin, lignin-containing materials, method of treating lignin, and mediator of multicomponent system for changing, decomposing, and bleaching lignin | |
| EP2085070A1 (en) | Cleaning and/or treatment compositions | |
| JPH02500990A (en) | Method for producing cellulose from lignin-containing raw materials | |
| CA2271937A1 (en) | Multicomponent system for modifying, decomposing or bleaching lignin, lignin-containing materials or similar substances, and process for using the same | |
| Flitsch et al. | Cellulose oxidation and bleaching processes based on recombinant Myriococcum thermophilum cellobiose dehydrogenase | |
| SK157995A3 (en) | Multicomponent bleaching system | |
| Periasamy et al. | White rot fungi and their enzymes for the treatment of industrial dye effluents | |
| JP2009124976A (en) | Fluorescent dye-decomposing agent | |
| T Moreira et al. | Semipilot-scale bleaching of Kraft pulp with manganese peroxide | |
| Lobos et al. | Enzymology and Molecular Genetics of the Ligninolytic System of the Basidiomycete Ceriporiopsis Sybvermispora | |
| EP0513140B1 (en) | A process for the bleaching of chemical pulp | |
| Feijoo et al. | Evaluation of the enzyme manganese peroxidase in an industrial sequence for the lignin oxidation and bleaching of eucalyptus kraft pulp | |
| CN107142734A (en) | A kind of pretreating reagent and its method for cotton cheese dyeing pre-treatment | |
| El-Hennawi | New approaches of biotechnology in textile coloration | |
| FR2557605A1 (en) | PROCESS FOR BLEACHING PAPER PULP BY HYDROGEN PEROXIDE | |
| RU2224061C2 (en) | Multicomponent system for enzymatic oxidation of substrates and enzymatic oxidation method | |
| Duarte et al. | Cellobiose dehydrogenase. Possible roles and importance for pulp and paper biotechnology | |
| Bendl et al. | Characterization of the oxidative inactivation of xylanase by laccase and a redox mediator | |
| US20030094251A1 (en) | Enhancing laccase activity using pro-oxidants and pro-degradants |