JP2007160102A - Polymeric stent having modified molecular structures in selected regions of flexible connectors - Google Patents
Polymeric stent having modified molecular structures in selected regions of flexible connectors Download PDFInfo
- Publication number
- JP2007160102A JP2007160102A JP2006334809A JP2006334809A JP2007160102A JP 2007160102 A JP2007160102 A JP 2007160102A JP 2006334809 A JP2006334809 A JP 2006334809A JP 2006334809 A JP2006334809 A JP 2006334809A JP 2007160102 A JP2007160102 A JP 2007160102A
- Authority
- JP
- Japan
- Prior art keywords
- polymer
- orientation
- poly
- stent
- radial
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Abstract
Description
〔発明の背景〕
〔1.発明の分野〕
本発明は、管腔内ポリマーステントに関し、更に詳しくは、応力が加わることに起因する修飾された(modified)分子配向を有する管腔内ポリマーステントに関する。
BACKGROUND OF THE INVENTION
[1. (Field of Invention)
The present invention relates to intraluminal polymer stents, and more particularly to intraluminal polymer stents having a modified molecular orientation resulting from the application of stress.
〔2.関連技術の解説〕
現在製造されている管腔内ステントは、臨床関連の生体内負荷条件の下でのデバイスの所望の機械的挙動に対する、該ステントを形成している材料の特性の十分な調整を適切に提供している訳ではない。あらゆる管腔内デバイスは好ましくは、意図された拡張直径の全範囲に渡って十分な保護(coverage)を提供するために、該脈管をそれの意図された内腔直径に再構築するのに役立つ、短期的および/または長期的な外向きの力(outward force)によって脈管の開通性(patency)を維持する特性、配置される時、半径方向の過剰の跳ね返り(recoil)を防止する特性、十分な疲労抵抗(fatigue resistance)を示す特性、ならびに、十分な柔軟性を示す特性を包含する幾つかの特性を示すことが望ましい。
[2. (Explanation of related technology)
Currently manufactured intraluminal stents adequately provide adequate adjustment of the properties of the material forming the stent to the desired mechanical behavior of the device under clinically relevant in vivo loading conditions. I don't mean. Any intraluminal device is preferably used to reconstruct the vessel to its intended lumen diameter to provide sufficient coverage over the entire range of intended expansion diameters. Useful short-term and / or long-term outward force to maintain vascular patency, properties to prevent excessive radial recoil when deployed It is desirable to exhibit several properties, including properties that exhibit sufficient fatigue resistance, as well as properties that exhibit sufficient flexibility.
したがって、管腔内ステントを製造するための材料および関連方法であって、工学技術によってデバイスを特定の用途に設計する機会をデバイスの設計者に提供する該材料および該方法を開発する必要性が存在する。 Accordingly, there is a need to develop materials and related methods for manufacturing endoluminal stents that provide device designers with an opportunity to design devices for specific applications through engineering techniques. Exists.
〔発明の概要〕
一般に入手可能な材料を、上記に簡潔に記述されるような特定の管腔内治療用途に適用する限界が、本発明によって克服される。
[Summary of the Invention]
The limitations of applying commonly available materials to specific endoluminal therapeutic applications as briefly described above are overcome by the present invention.
本発明は、一つの具体例によると、縦軸と半径方向軸(radial axis)とを有する、実質的に管状の管腔内医療デバイスに向けられている。該デバイスは、半径方向の(radial:放射状に配置された)複数のストラット、および半径方向の複数の円弧部材を有する、ポリマー材料で形成された複数のフープと;前記の複数のフープを相互連結している、ポリマー材料で形成された複数のブリッジであって、前記の複数のブリッジの各々が、機械的変形によって生じる所定のポリマー鎖整列度(predetermined amount of polymer chain alignment)を有する少なくとも1つの部材を有している、前記の複数のブリッジと;を備えている。 The present invention, according to one embodiment, is directed to a substantially tubular intraluminal medical device having a longitudinal axis and a radial axis. The device comprises a plurality of hoops formed of a polymer material having a plurality of radial struts and a plurality of radial arc members; interconnecting the plurality of hoops A plurality of bridges formed of a polymer material, each of said plurality of bridges having a predetermined amount of polymer chain alignment caused by mechanical deformation A plurality of bridges having a member.
本発明の、植え込み可能な医療デバイスのための生体適合性材料は、脈管開通性デバイス(vessel patency devices)(例えば、脈管用ステント、胆管用ステント、尿管用ステント)、脈管閉塞用デバイス(vessel occlusion devices)(例えば、心房中隔閉鎖器具および心室中隔閉鎖器具(atrial septal and ventricular septal occluders)、卵円孔開存閉鎖器具(patent foramen ovale occluders))、ならびに、整形外科デバイス(例えば、固定用デバイス(fixation devices))を包含する、かなり多数の医療用途のために利用することができる。 The biocompatible materials for implantable medical devices of the present invention include vessel patency devices (eg, vascular stents, biliary stents, ureteral stents), vascular occlusion devices ( vessel occlusion devices) (eg, atrial septal and ventricular septal occluders, patent foramen ovale occluders), and orthopedic devices (eg, It can be utilized for a number of medical applications, including fixation devices.
本発明の生体適合性材料は、現在入手可能なステントに比べてより広い範囲の負荷条件に耐え得るステントを製造することのできる、ユニークな組成と設計された特性(designed-in properties)とを有する。更に詳しくは、生体適合性材料の中に設計されている分子構造によって、広範囲に渡る幾何学的配列(geometries)であって様々な負荷条件に適合できる該幾何学的配列を有するステントを設計することが容易となる。 The biocompatible material of the present invention has a unique composition and designed-in properties that can produce stents that can withstand a wider range of loading conditions than currently available stents. Have. More specifically, a molecular structure designed in a biocompatible material designs a stent having a wide range of geometries that can be adapted to various loading conditions. It becomes easy.
本発明の管腔内デバイスは、かなり多数の種類の生体適合性ポリマー材料で形成されることができる。所望の機械的特性を得るために、該ポリマー材料は、それが原料の状態であろうと管またはシートの状態であろうと、いずれの場合も、物理的に変形させて、ある整列度(degree of alignment)のポリマー鎖を得ることができる。この整列を利用して、ステントの1個以上の部品の物理的および/または機械的特性を改善することができる。 The endoluminal device of the present invention can be formed from a large number of types of biocompatible polymeric materials. In order to obtain the desired mechanical properties, the polymer material, whether it is in the raw state or in the tube or sheet state, is physically deformed to a certain degree of alignment. alignment) polymer chains can be obtained. This alignment can be utilized to improve the physical and / or mechanical properties of one or more parts of the stent.
本発明の、前述の特徴および利点、ならびに、他の特徴および利点は、添付図面に例示されるような、本発明の好ましい具体例に関する、次のより詳細な記述から明らかになるであろう。 The foregoing features and advantages of the invention, as well as other features and advantages, will become apparent from the following more detailed description of the preferred embodiments of the invention, as illustrated in the accompanying drawings.
〔好ましい具体例の詳細な記述〕
植え込み可能な医療デバイスは、ポリマー材料を包含する、かなり多数の適切な生体適合性材料で作ることができる。これらのポリマー材料の内部構造は、該ポリマーの機械操作および/または化学操作(mechanical and/or chemical manipulation)を利用して変更されうる。これらの、内部構造の部分変更を利用して、以下に詳細に説明されているような固有の総合特性(例えば、結晶および非晶質の形態、ならびに、結晶および非晶質の配列)を有するデバイスを作り出すことができる。本発明は、かなり多数の植え込み可能な医療デバイスに適用されるが、説明を容易にするため、次の詳細な記述は、典型的なステントに焦点が当てられている。
[Detailed Description of Preferred Embodiments]
Implantable medical devices can be made of any number of suitable biocompatible materials, including polymeric materials. The internal structure of these polymeric materials can be altered utilizing mechanical and / or chemical manipulation of the polymer. Utilizing these internal modification of the internal structure, it has unique overall properties (eg, crystalline and amorphous forms, and crystalline and amorphous arrangements) as described in detail below A device can be created. Although the present invention applies to a large number of implantable medical devices, for ease of explanation, the following detailed description focuses on a typical stent.
図1に関連し、本発明による典型的なステント100の部分平面図を例示する。典型的なステント100は、複数個の可撓性コネクター104によって相互接続されている、複数個のフープ(hoop)部品102を備えている。フープ部品102は、連続的な一連の、実質的に長手方向または軸方向に配向された半径方向の(radial)ストラット(strut)部材106、および、交互に並んだ、実質的に円周方向に配列された半径方向の円弧部材108として形成されている。フープ部品102は、平面図に示されているが、可撓性コネクター104によって一緒に連結されて、実質的に管状ステント構造体を形成している、本質的に環状の部材である。半径方向のストラット部材106と、交互に並んだ、半径方向の円弧部材108との組合せによって、実質的に正弦波のパターンが形成される。フープ部品102は、かなり多数の種類の、構造上の特徴(design features)で設計することができ、また、かなり多数の種類の形状(configurations)を想定することができるが、典型的な具体例において、半径方向のストラット部材106は、それらの中央領域110においていっそう広くなっている。この構造上の特徴は、薬物運搬のための増大した表面積を包含する多数の目的のために利用することができる。
With reference to FIG. 1, a partial plan view of an exemplary stent 100 according to the present invention is illustrated. A typical stent 100 includes a plurality of
可撓性コネクター104は、可撓性ストラット部材112、および、交互に並んだ、可撓性円弧部材114で作られている。可撓性コネクター104は、上述の通り、隣接するフープ部品102同士を連結している。この典型的な具体例において、可撓性コネクター104は実質的にNの形をしており、一方の端部は一方のフープ部品上の半径方向の円弧部材に連結されており、他方の端部は隣接するフープ部品上の半径方向の円弧部材に連結されている。フープ部品102と同様、可撓性コネクター104は、かなり多数の種類の、構造上の特徴と、かなり多数の種類の形状とを有することができる。典型的な具体例において、ステントのクリンプ加工(crimping)が行われる間、ネスティング(nesting)を容易にするため、可撓性コネクター104の両端部は、隣接するフープ部品の半径方向の円弧部材の異なる部分に連結されている。この典型的な形状に関し、隣接するフープ部品上の半径方向の円弧部材は、僅かに位相が異なっているのに対して、1つおきのフープ部品上の半径方向の円弧部材は、実質的に同位相であることに注目することは、興味深い。加えて、各々のフープ部品上の半径方向の全ての円弧部材が、隣接するフープ部品の半径方向の全ての円弧部材に連結される必要がある訳ではないことに注目することは、重要である。
The
管腔内の足場(scaffold)即ちステントの可撓性コネクターまたはコネクターのために、かなり多数の種類の構造を利用し得ることに注目することは、重要である。例えば、上述の構造において、コネクターは、2種類の要素、実質的に長手方向に配向されたストラット部材と可撓性円弧部材とを有する。しかし、代わりの構造において、コネクターは、実質的に長手方向に配向されたストラット部材のみを有し可撓性円弧部材を全く有さないことがあるか、または、可撓性円弧部材を有し実質的に長手方向に配向されたストラット部材を全く有さないこともある。 It is important to note that a large number of types of structures can be utilized for the intraluminal scaffold or stent flexible connector or connector. For example, in the structure described above, the connector has two types of elements, a strut member oriented in a substantially longitudinal direction and a flexible arc member. However, in alternative constructions, the connector may have only a substantially longitudinally oriented strut member and no flexible arc member, or may have a flexible arc member. There may be no strut members oriented substantially longitudinally.
ステント100の実質的に管状の構造は、動脈等の実質的に管状の器官の開通性を維持するための、一時的または半永久的な足場を提供する。ステント100は、管腔表面(luminal surface)と反管腔側面(abluminal surface)とを有する。それら2つの表面の間の距離によって、壁の厚さは規定される。ステント100は、運搬のための拡張されていない直径と、拡張されている直径であって、中にステント100が運搬される器官の正常直径におおよそ一致する該拡張されている直径とを有する。動脈等の管状器官は、直径が変化することがあるので、本発明の趣旨から逸脱することなく、拡張されていない直径と拡張されている直径との異なる組を有する異なる寸法のステントを設計することができる。本明細書に記述されるように、ステント100は、多数の種類のポリマー材料で作ることができる。 The substantially tubular structure of stent 100 provides a temporary or semi-permanent scaffold for maintaining the patency of a substantially tubular organ such as an artery. Stent 100 has a luminal surface and an abluminal surface. The distance between the two surfaces defines the wall thickness. Stent 100 has an unexpanded diameter for delivery and an expanded diameter that approximately matches the normal diameter of the organ into which stent 100 is delivered. Since tubular organs such as arteries can vary in diameter, design different sized stents with different sets of unexpanded and expanded diameters without departing from the spirit of the present invention. be able to. As described herein, the stent 100 can be made of many types of polymeric materials.
したがって、1つの典型的な具体例において、管腔内足場要素(intraluminal scaffold element)は、非架橋熱可塑性樹脂、架橋熱硬化性樹脂、それらの複合材料および混合物を包含するポリマー材料のような非金属材料で作ることができる。ポリマーが固体に関連する機械的特性を示し得る、典型的には3種の形態、即ち、結晶構造、半結晶構造、および/または非晶質構造としての形態、が存在する。結晶化が起こるには、ポリマー鎖内部における高度な分子の規則性が不可欠であるので、全てのポリマーは、完全に結晶化し得る訳ではない。結晶化するポリマーにおいてさえ、結晶化度は一般に、100%未満である。完全なる結晶構造と非晶質構造との間の連続体(continuum)の内部には、2つの熱転移、即ち、結晶−液体転移(即ち、融点温度,Tm)およびガラス−液体転移(即ち、ガラス転移温度,Tg)、が存在する。これらの2つの転移の間の温度範囲には、規則正しく配列した結晶と、無秩序な非晶質ポリマー領域との混合物が存在することがある。 Accordingly, in one exemplary embodiment, an intraluminal scaffold element is a non-crosslinked thermoplastic resin, a cross-linked thermoset resin, a non-polymeric material such as a composite material and mixtures thereof. Can be made of metal material. There are typically three forms in which the polymer can exhibit mechanical properties associated with solids: a crystalline structure, a semi-crystalline structure, and / or an amorphous structure. Not all polymers can be fully crystallized because high molecular regularity within the polymer chain is essential for crystallization to occur. Even in polymers that crystallize, the degree of crystallinity is generally less than 100%. Within the continuum between the complete crystal structure and the amorphous structure, there are two thermal transitions: a crystal-liquid transition (ie, melting temperature, T m ) and a glass-liquid transition (ie, , Glass transition temperature, T g ). In the temperature range between these two transitions, there may be a mixture of regularly arranged crystals and disordered amorphous polymer regions.
「折り畳み(folded)」鎖を有するポリマー結晶の形成に関するホフマン−ローリッツェン(Hoffman-Lauritzen)理論は、それの源を、ポリエチレンの薄い単結晶を希薄溶液から成長させることができるという1957年の発見に負うている。折り畳み鎖は好ましくは、実質的に結晶性の構造を形成する必要がある。ホフマンおよびローリッツェンは、鎖折り畳み核(chain-folded nuclei)の形成に関連する熱力学に対する特別な認識によって、「溶液(solution)」および「溶融体(melt)」からポリマーを結晶化させることに関する運動論の基礎を確立した。 The Hoffman-Lauritzen theory for the formation of polymer crystals with “folded” chains was based on the discovery in 1957 that thin single crystals of polyethylene could be grown from dilute solutions. Owes. The folded strands should preferably form a substantially crystalline structure. Hoffman and Loritzen have been involved in the crystallization of polymers from "solutions" and "melts" with special recognition of the thermodynamics associated with the formation of chain-folded nuclei. The basis of the theory was established.
希薄溶液から結晶化を行うためには、巨視的完全無欠さ(macroscopic perfection)(典型的には、約200倍〜約400倍の範囲の倍率)を有する単結晶を生成する必要がある。この点に関し、ポリマーは、無機塩等の低分子量化合物と実質的に相違する訳ではない。温度、溶媒および溶質濃度のような結晶化条件は、結晶の形成と最終形態とに影響を及ぼすことがある。ポリマーは、複数の薄板、即ち、「ラメラ(lamellae:板晶)」の形態で結晶化する。これらラメラの厚さは、10ナノメータ(即ち、nm)程度である。小さい寸法(small dimensions)に垂直な結晶プレート(crystal plates)の寸法は、結晶化条件によって決まるが、十分に成長した結晶の小板(platelets)の厚さより何倍も大きい。結晶内部における鎖の方向は、該結晶の短い幅(short dimension)と並行する。このことは、分子が(例えば、折り畳まれた消火用ホースのように)前後に折り重なり、結果的に、折り畳まれた分子(folded molecules)の連続層がそれら小板の横方向成長(lateral growth)を引き起こすことを示している。結晶は単一分子から成る訳ではないし、分子が専ら単一結晶で存在する訳でもない。鎖によって形成されるループ(loop)は、鎖が結晶から現われるときに、結晶の向きを変えて、この結晶を再び入れる。2つの結晶質セクションを連結する部分は、非晶質ポリマーと見なすことができる。更に、ポリマー鎖の端部は、上述のような、結晶の整然とした折り畳みパターン(fold patterns)を破壊し、該結晶から排除される傾向にある。それゆえに、ポリマー鎖の端部は、該ポリマーの非晶質部分となる。したがって、現在知られているいかなるポリマー材料も、100%の結晶質であるとは考えられない。結晶構造は、後重合(post polymerization)の処理条件に十分なほどに影響を受ける。 In order to crystallize from a dilute solution, it is necessary to produce a single crystal having a macroscopic perfection (typically a magnification in the range of about 200 times to about 400 times). In this regard, the polymer is not substantially different from low molecular weight compounds such as inorganic salts. Crystallization conditions such as temperature, solvent and solute concentration can affect crystal formation and final morphology. The polymer crystallizes in the form of a plurality of laminae, ie “lamellae”. The thickness of these lamellae is about 10 nanometers (ie, nm). The dimensions of the crystal plates perpendicular to the small dimensions depend on the crystallization conditions but are many times larger than the thickness of the fully grown crystal platelets. The direction of the chain inside the crystal is parallel to the short dimension of the crystal. This means that the molecules fold back and forth (for example, like a folded fire hose), and as a result, a continuous layer of folded molecules forms a lateral growth of the platelets. ). A crystal does not consist of a single molecule, and molecules do not exist exclusively in a single crystal. The loop formed by the chain changes the orientation of the crystal when the chain emerges from the crystal and reintroduces the crystal. The portion connecting the two crystalline sections can be considered an amorphous polymer. In addition, the ends of the polymer chain tend to break and be excluded from the crystal's orderly fold patterns, as described above. Therefore, the end of the polymer chain becomes an amorphous part of the polymer. Thus, any currently known polymeric material is not considered 100% crystalline. The crystal structure is sufficiently affected by the processing conditions for post polymerization.
単結晶は、バルク処理(bulk processing)による結晶化では観察されない。溶融体(melt)からのバルク結晶化ポリマーは、核形成中心の周りに対称である、「スフェルライト(spherulites:球晶)」と呼ばれるドメイン(domains:領域)を示す。スフェルライトの成長が、拡張しているもう一つのスフェルライトと接触することによって衝突しなければ、対称性は完全に円形である。鎖の折り畳み(chain folding)は、ポリマーが溶融状態から結晶化することの本質的特徴である。スフェルライトは、核形成部位から放射状に広がる「ラメラ(lamellar)」結晶の凝集体で構成される。したがって、溶液とバルク成長結晶との間には関連がある。 Single crystals are not observed in crystallization by bulk processing. Bulk crystallized polymers from melt exhibit domains called “spherulites” that are symmetrical about the nucleation center. If the spherulite growth does not collide by contacting another expanding spherulite, the symmetry is perfectly circular. Chain folding is an essential feature of polymer crystallization from a molten state. Spherulite is composed of aggregates of “lamellar” crystals that radiate from the nucleation site. Thus, there is a relationship between solution and bulk grown crystals.
球対称は、時間と共に成長する。樹枝状結晶の成長の場合のように、繊維結晶またはラス様結晶(lathlike crystals)が、枝分かれし四方八方に広がり始める。ラメラ(lamellae)が、核から立体的に広がるにつれて、微結晶の枝分かれは、球状形態を生成し続ける。鎖の連続層が、放射状に広がるラス(laths)の端部に付加されることによって、成長は達成される。所与の分子が、2個以上のラメラの中に含有されることに成り、したがって、同一または隣接するスフェルライトからの、放射状に広がる微結晶を連結することができるということを、ポリマー分子の鎖構造は示唆する。これらの層間結合(interlamellar links)は、低分子量化合物のスフェルライト中では起こり得ず、該スフェルライトは、結果として、より小さい機械的強度を示す。 Spherical symmetry grows with time. As in the case of dendritic growth, fiber crystals or lathlike crystals begin to branch and spread in all directions. As lamellae spread sterically from the nucleus, the microcrystalline branching continues to produce a spherical morphology. Growth is achieved by adding a continuous layer of chains to the ends of the radially spreading laths. A polymer molecule that a given molecule will be contained in two or more lamellae and thus can link radially extending crystallites from the same or adjacent spherulites. Suggests a chain structure. These interlamellar links cannot occur in the low molecular weight compound spherulite, which results in less mechanical strength.
分子鎖の折り畳みは、直交偏光子(crossed polarizers)の下、スフェルライトを同定する「マルテーゼ(Maltese)」クロス(cross)の起源(origin)である。所与のポリマー系の結晶粒径分布は、初期核形成密度と、核形成速度と、結晶成長の速度と、配向状態とに影響される。ポリマーが、核形成が半径方向の成長(radial growth)より優勢である条件にさらされる場合、より小さい結晶が生じる。比較的少ない核形成部位が存在し、かつ、成長速度がより速い場合、より大きい結晶が形成される。スフェルライトの直径は、約数μmから数百μmに及ぶことがあり、ポリマー系と結晶化条件とによって決まる。 Molecular chain folding is the origin of the “Maltese” cross that identifies spherulites under crossed polarizers. The crystal grain size distribution for a given polymer system is affected by the initial nucleation density, the nucleation rate, the rate of crystal growth, and the orientation state. When the polymer is subjected to conditions where nucleation predominates over radial growth, smaller crystals result. Larger crystals are formed when there are relatively few nucleation sites and the growth rate is faster. The diameter of spherulite can range from about a few μm to a few hundred μm, depending on the polymer system and crystallization conditions.
したがって、バルク結晶化ポリマー(bulk-crystallized polymer)中のスフェルライト形態には、組織体(organization)(すなわち、次には配向して球状凝集体になる微結晶の中に折り畳まれる個々の分子)の、様々なレベルでの規則配列(ordering)が含まれる。スフェルライトは、合成物質と、生物学的製剤と、月の石(moon rocks)を包含する地質的素因(geological origin)との有機系ならびに無機系の中で観察されてきたのであり、したがって、ポリマーにとってユニークではない。 Thus, the spherulite form in a bulk-crystallized polymer includes an individual molecule that is folded into an organization (ie, a microcrystal that is then oriented into a spherical aggregate). ) Of various levels of ordering. Spherulite has been observed in organic and inorganic systems of synthetic materials, biological agents, and geological origins, including moon rocks, and therefore Not unique to polymers.
応力誘起結晶化度(stress induced crystallinity)は、膜および繊維の技術において重要である。ポリマーの希薄溶液が急速に撹拌されるとき、独特の構造体が成長し、これは、「シシカバブ(shish kebab)」形態を有すると言われている。これらの構造体は、繊維質中心カラム(fibrous central column)に沿って延ばされている、折り畳み鎖結晶(folded chain crystals)の大きい塊(chunks)から成る。該構造体の「シシ(shish)」部分と「カバブ(kebab)」部分との両方において、ポリマー鎖は、該構造体の全体軸に平行である。 Stress induced crystallinity is important in membrane and fiber technology. When a dilute solution of polymer is rapidly stirred, a unique structure grows, which is said to have a “shish kebab” morphology. These structures consist of large chunks of folded chain crystals that extend along a fibrous central column. In both the “shish” and “kebab” portions of the structure, the polymer chains are parallel to the overall axis of the structure.
ポリマー溶融体が、剪断されて、熱的に安定な状態まで冷却される時、ポリマー鎖は、それらのランダムコイル(random coils)でかき乱されて、剪断方向に平行に容易に伸びる。このことによって、変形スフェルライト(deformed spherulites)から小さい結晶凝集体が形成される結果となることがある。スフェルライトからフィブリルへの転換(transformation)、多形結晶形成(polymorphic crystal formation)の変化、既に形成された結晶質ラメラの再配向、配向した微結晶の形成、非晶質ポリマー鎖の配向、および/または、それらの組合せを包含する他の形態学的変化が生じることがある。 When the polymer melt is sheared and cooled to a thermally stable state, the polymer chains are easily perturbed by their random coils and easily extend parallel to the shear direction. This can result in the formation of small crystal aggregates from deformed spherulites. Transformation from spherulite to fibrils, change of polymorphic crystal formation, reorientation of already formed crystalline lamellae, formation of oriented microcrystals, orientation of amorphous polymer chains, And / or other morphological changes may occur, including combinations thereof.
分子配向は重要である。なぜなら、分子配向は、主として、バルクポリマーの特性に影響を及ぼし、したがって、様々な材料用途に不可欠である最終特性に強い影響を持つからである。配向によって影響を受ける特性の幾つかは、透過性(permeability)、耐磨耗性(wear)、屈折率、吸収性(absorption)、分解速度、引張り強度、降伏応力、引裂き強度、弾性率(modulus)および破断点伸びのような物理的および機械的特性である。配向は異方性挙動(anisotropic behavior)を促進するため、配向は、必ずしも有利であるとは限らない。配向は、一軸配向、二軸配向および多軸配向のような幾つかの方向で生じることがある。配向は、延伸(drawing)、ローリング(rolling)、カレンダリング(calendaring)、スピニング(spinning)、吹込み成形(blowing)、等によって誘起される場合があり、繊維、膜、管、瓶(bottles)、成形品、押出し成形品、コーティングおよび複合材料を包含する系の中に存在する。ポリマー材料が処理されるとき、特定方向の選択配向(preferential orientation)が存在することとなる。選択配向は通常、処理が行われる方向となり、縦方向(machine direction:流れ方向)(MD)と呼ばれる。生成物の多くは、特性を改善するために、意図的に特定方向に配向させられる。生成物が溶融処理される場合、該生成物は、ある程度の選択配向を有する。溶媒処理材料の場合、例えば、ポリマー溶液を剪断し、次いで、剪断処理の間、配向を固定するために、所望の幾何学的条件まで直ちに沈降させるかまたは急冷するような方法によって処理される間に配向が誘起されることがある。代替的に、ポリマーが、剛体棒(rigid rod)のような化学構造を有する場合、ポリマー溶液中で液晶形態であることに起因して処理が行われる間に、該剛体棒は配向するであろう。 Molecular orientation is important. This is because molecular orientation primarily affects the properties of the bulk polymer and therefore has a strong impact on the final properties that are essential for various material applications. Some of the properties affected by orientation are permeability, wear resistance, refractive index, absorption, degradation rate, tensile strength, yield stress, tear strength, modulus of elasticity. And physical and mechanical properties such as elongation at break. Because orientation promotes anisotropic behavior, orientation is not always advantageous. Orientation can occur in several directions, such as uniaxial orientation, biaxial orientation, and multiaxial orientation. Orientation can be induced by drawing, rolling, calendaring, spinning, blowing, etc., fibers, membranes, tubes, bottles Present in systems including molded articles, extruded articles, coatings and composite materials. When the polymer material is processed, there will be a preferential orientation in a specific direction. The preferred orientation is usually the direction in which processing takes place and is referred to as the machine direction (MD). Many of the products are intentionally oriented in a specific direction to improve properties. When the product is melt processed, the product has some degree of selective orientation. In the case of solvent-treated materials, for example, while the polymer solution is sheared and then processed by methods such as immediate sedimentation or quenching to the desired geometric conditions to fix the orientation during the shearing process. In some cases, orientation is induced. Alternatively, if the polymer has a chemical structure such as a rigid rod, the rigid rod will be oriented during processing due to its liquid crystal form in the polymer solution. Let's go.
配向状態は、変形(deformation)の種類とポリマーの種類とによって決まる。材料がたとえ著しく変形されようと、または延伸されようと、ポリマー鎖はそれの最初の状態に戻ることができるため、高レベルの配向を与える必要はない。このことは一般に、延伸温度で非常に可撓性であるポリマーで起こる。したがって、幾つかの要因が、所与のポリマー系の配向状態に影響を及ぼすことがある。それら要因には、変形の速度(例えば、ひずみ速度、剪断速度、頻度、等);変形の量(例えば、延伸比);温度;分子量および分子量分布;鎖の立体配置(configuration)(例えば、立体規則性、幾何異性体、等);鎖の構造(直鎖、枝分かれ鎖、架橋、樹枝状鎖、等);鎖の剛性(可撓性、硬質、半硬質、等);共重合体の種類(ランダム共重合体、ブロック共重合体、交互共重合体、等);ならびに、添加剤(可塑剤、硬質充填剤、軟質充填剤、長繊維、短繊維、治療薬、混合物、等)の存在、が包含される。 The orientation state depends on the type of deformation and the type of polymer. Whether the material is significantly deformed or stretched, the polymer chain can return to its original state, so it is not necessary to provide a high level of orientation. This generally occurs with polymers that are very flexible at the stretching temperature. Thus, several factors can affect the orientation state of a given polymer system. These factors include the rate of deformation (eg, strain rate, shear rate, frequency, etc.); amount of deformation (eg, stretch ratio); temperature; molecular weight and molecular weight distribution; chain configuration (eg, steric Regularity, geometric isomers, etc.); chain structure (straight chain, branched chain, bridged, dendritic chain, etc.); chain stiffness (flexible, rigid, semi-rigid, etc.); (Random copolymer, block copolymer, alternating copolymer, etc.); and presence of additives (plasticizer, hard filler, soft filler, long fiber, short fiber, therapeutic agent, mixture, etc.) Are included.
ポリマーは2つの相(即ち、結晶質相および非晶質相)からなるので、これらの相に対する配向の影響は異なる。したがって、半結晶質ポリマー系中のこれら2つの相に対する最終的な配向は同一でない場合がある。これは、可撓性の非晶質鎖が、変形および負荷条件に対して、硬質の結晶質相とは異なるように反応するからである。 Since the polymer consists of two phases (ie, a crystalline phase and an amorphous phase), the effect of orientation on these phases is different. Thus, the final orientation for these two phases in the semicrystalline polymer system may not be identical. This is because the flexible amorphous chain reacts differently to deformation and loading conditions than the hard crystalline phase.
配向を誘起した後、様々な相を形成することができ、それの挙動は、ポリマー骨格の化学的性質によって決まる。完全に非晶質材料のような均質状態は、単一の配向挙動を有するであろう。しかし、半結晶質、ブロック共重合体または複合材料(繊維強化、充填系、液晶)であるポリマーの配向挙動は、2個以上のパラメータによって記述する必要がある。配向挙動は一般に、材料の構造と配向状態とに正比例する。ポリマー系に存在する、構造に関する幾つかの共通標準(common levels)(例えば、結晶の単位セル、ラメラの厚さ、ドメイン寸法(domain size)、スフェルライト構造、配向した超構造(superstructures)、ポリマー混合物中の相分離ドメイン(phase separated domains)、等)が存在する。 After inducing orientation, various phases can be formed, the behavior of which depends on the chemical nature of the polymer backbone. A homogeneous state, such as a completely amorphous material, will have a single orientation behavior. However, the orientation behavior of polymers that are semicrystalline, block copolymers or composites (fiber reinforced, filled systems, liquid crystals) needs to be described by two or more parameters. The orientation behavior is generally directly proportional to the material structure and orientation state. Some common levels of structure present in polymer systems (eg, crystal unit cells, lamellar thickness, domain size, spherulite structure, oriented superstructures, There are phase separated domains in the polymer mixture, etc.).
例えば、押出しポリエチレンの構造は、積層された折り畳み鎖のラメラ構造である。該構造内部における複数のラメラの配向は縦方向に並行するが、小板(platelets)は、縦方向に垂直に配向する。それらラメラ間の非晶質構造は一般に、配向しない。材料の機械的特性は、様々な方向(縦方向に対して0°、縦方向に対して45°、および、縦方向に対して90°)で試験したとき、異なる。伸び値は通常、材料が縦方向に引っ張られたとき、最小となる。縦方向に45°で引っ張られたとき、ラメラの剪断変形が生じて、より大きい伸び値が与えられる。縦方向に90°で引っ張られたとき、材料は、鎖軸(chain axis)が広がっている時、最大の伸び率を示す。 For example, the structure of extruded polyethylene is a laminated folded chain lamellar structure. The orientation of the lamellae inside the structure is parallel to the longitudinal direction, but the platelets are oriented perpendicular to the longitudinal direction. The amorphous structure between the lamellas is generally not oriented. The mechanical properties of the materials are different when tested in various directions (0 ° for the longitudinal direction, 45 ° for the longitudinal direction and 90 ° for the longitudinal direction). The elongation value is usually minimal when the material is pulled in the machine direction. When pulled in the machine direction at 45 °, lamella shear deformation occurs, giving higher elongation values. When pulled in the longitudinal direction at 90 °, the material exhibits maximum elongation when the chain axis is widened.
ポリマー鎖が、所与の変形軸(deformation axis)に関連し、ある角度で配向されるとき、鎖の配向性は、ヘルマンズ配向関数(Hermans orientation function)fによって規定することができる。ヘルマンズ配向関数fは、0、1および−1/2であって、それぞれ、軸と並行するランダム配向、完全配向および垂直配向を表わす値から変化する。これは、主として、一軸配向系に適用される。配向を測定するために使用される幾つかの技術[例えば、複屈折技術、直線二色性技術、広角X線散乱技術、偏光ラマン散乱技術、偏光蛍光技術およびNMR(核磁気共鳴分析法)]が存在する。 When a polymer chain is related to a given deformation axis and oriented at an angle, the orientation of the chain can be defined by a Hermans orientation function f. The Hermans orientation function f is 0, 1 and −1/2, and varies from values representing random orientation, complete orientation and vertical orientation parallel to the axis, respectively. This applies mainly to uniaxially oriented systems. Several techniques used to measure orientation [eg birefringence technique, linear dichroism technique, wide angle X-ray scattering technique, polarized Raman scattering technique, polarized fluorescence technique and NMR (nuclear magnetic resonance analysis)] Exists.
本発明のステントは、溶融法および溶解法のような様々な方法で調製することができる。典型的な溶融法(melt processes)には、射出成形法、押出し成形法、紡糸法、圧縮成形法、吹込み成形法、連続式引抜き成形(pultrusion)法、等が包含される。典型的な溶解法(solution processes)には、溶媒キャストチューブおよびフィルム(solvent cast tubes and films)法、静電繊維紡糸(electrostatic fiber spinning)法、乾式および湿式紡糸(dry and wet spinning)法、中空繊維および膜紡糸(hollow fiber and membrane spinning)法、スピニングディスク(spinning disk)法が包含される。ステントを調製するためには、純ポリマー、混合物および複合材料を使用することができる。前駆体材料は、上述の方法のいずれかによって調製され、次いで、レーザーで切断される管またはフィルムである場合がある。前駆体材料は、調製されたまま使用することができるか、または、様々な条件の下、それのアニーリング、配向または緩和(relaxing)を行うことによって修飾することができる。代替的に、レーザーで切断されたステントは、調製されたまま使用することができるか、または、様々な条件の下、それのアニーリング、配向または緩和(relaxing)を行うことによって修飾することができる。 The stent of the present invention can be prepared by various methods such as a melting method and a dissolving method. Typical melt processes include injection molding, extrusion molding, spinning, compression molding, blow molding, continuous pultrusion, and the like. Typical solution processes include solvent cast tubes and films, electrostatic fiber spinning, dry and wet spinning, hollow Included are fiber and membrane spinning methods, spinning disk methods. Pure polymers, blends and composites can be used to prepare the stent. The precursor material may be a tube or film prepared by any of the methods described above and then laser cut. The precursor material can be used as prepared or can be modified by annealing, orienting or relaxing it under various conditions. Alternatively, a laser cut stent can be used as prepared or can be modified by annealing, orienting or relaxing it under various conditions. .
ステントまたはデバイスにおけるポリマー配向の効果は、半径方向の強度、跳ね返り(recoil)および可撓性を包含するデバイス性能を改善することができる。配向は更に、ステントの分解時間を変えることができ、したがって、ステントの異なるセクションは、要望通り、異なるように配向させることができる。配向は、軸方向および円周方向または半径方向だけでなく、単位セル(unit cell)および可撓性コネクターにおける他のあらゆる方向と並行して、それらの各々の方向におけるステントの性能を改善することができる。配向は、一つの方向(一軸)のみに制限される場合もあり、2つの方向(二軸)および/または多数の方向(多軸)である場合もある。配向は、所与の材料に様々な手順(例えば、先ず、軸方向の配向を行い、次いで、半径方向の配向を誘起すること、および、逆の場合も同様)で誘起することができる。代替的に、材料は、同時に、両方の方向に配向させることができる。軸方向の配向は、所与の材料(例えば、管またはフィルム)の軸方向または縦方向に沿って、通常、ポリマーのガラス転移温度より高い温度で引き伸ばすことによって誘起することができる。半径方向または円周方向の配向は、幾つかの異なる方法[例えば、加熱されたガス(例えば、窒素)によるか、または、鋳型の内側にバルーン(balloon)を使用することにより、材料に吹き込みを行うこと]によって誘起することができる。代替的に、複合材料またはサンドイッチ構造体は、様々な方向に配向された材料の複数の層を積み重ねて、異方特性(anisotropic properties)を与えることによって形成することができる。二軸配向および/または多軸配向を誘起するために、吹込み成形を使用することもできる。 The effects of polymer orientation in a stent or device can improve device performance, including radial strength, recoil, and flexibility. The orientation can further change the degradation time of the stent, so that different sections of the stent can be oriented differently as desired. Orientation improves the performance of the stent in each of those directions, not only in the axial and circumferential or radial directions, but in parallel with any other direction in the unit cell and flexible connector Can do. The orientation may be limited to only one direction (uniaxial) or may be two directions (biaxial) and / or multiple directions (multiaxial). Orientation can be induced in a given material by various procedures (eg, first, axial orientation and then induce radial orientation, and vice versa). Alternatively, the material can be oriented in both directions simultaneously. Axial orientation can be induced by stretching along the axial or longitudinal direction of a given material (eg, a tube or film), usually at a temperature above the glass transition temperature of the polymer. The radial or circumferential orientation can be blown into the material in several different ways [eg, by a heated gas (eg, nitrogen) or by using a balloon inside the mold. To do]. Alternatively, composite materials or sandwich structures can be formed by stacking multiple layers of materials oriented in various directions to provide anisotropic properties. Blow molding can also be used to induce biaxial and / or multiaxial orientation.
図2に関連し、本明細書に記述されるポリマー材料で形成されたフープ部品102のセクション200を例示する。図示されるように、フープ部品102のセクション200は、2つの第1の帯域t2と1つの第2の帯域t1とを有するように設計されている。2つの帯域t2は、1つの第2の帯域t1と比べてより大きいポリマー鎖配向度を有するように設計または構成されている。帯域t2における、より大きいポリマー鎖配向度は、前駆体物質を、ステントの縦軸に並行する方向またはその軸方向に延伸することによって達成することができる。加えて、配向はまた、上述の方法によっても達成することができる。図2に例示される典型的な具体例において、t2領域は、意図的にt1領域よりも薄くなっており、このため、t2領域は、t1領域に比べてひずみ(strain)が大きい帯域である。デバイスの性能特性(performance characteristics)は、ポリマー鎖配向の種類および配向度と機能特性(feature characteristics)とを最適化することによって改善することができる。ステントのフープ部品のための性能特性には、典型的には、半径方向の強度、半径方向の剛性、および、半径方向の跳ね返り(radial recoil)が包含される。加えて、好ましくは、脈動(pulsatile motion)等の動負荷(dynamic loads)を考慮することが望ましい。
FIG. 2 illustrates a
図3に関連し、本明細書に記述されるポリマー材料で形成されたフープ部品102のセクション300を例示する。図示されるように、フープ部品102のセクション300は、1つの第1の帯域t1と2つの第2の帯域t2とを有するように設計されている。1つの第1の帯域t1は、2つの帯域t2と比べてより大きいポリマー鎖配向度を有するように設計または構成されている。帯域t1における、より大きいポリマー鎖配向度は、前駆体物質を、ステントの半径方向または円周方向の軸に並行する方向に延伸することによって達成することができる。加えて、配向はまた、上述の方法によっても達成することができる。図3に例示される典型的な具体例において、t1領域は、意図的にt2領域よりも薄くなっており、このため、t1領域は、t2領域に比べてひずみが大きい帯域である。デバイスの性能特性は、ポリマー鎖配向の種類および配向度と機能特性とを最適化することによって改善することができる。ステントのフープ部品のための性能特性には、典型的には、半径方向の強度、半径方向の剛性、および、半径方向の跳ね返りが包含される。加えて、好ましくは、脈動等の動負荷を考慮することが望ましい。
FIG. 3 illustrates a
更に、図4に関連し、本明細書に記述されるポリマー材料で形成されたフープ部品102のセクション400を例示する。この図は、図2および図3に例示されるポリマー鎖配向の組合せを示している。換言すれば、帯域t1およびt2における整列度(degree of alignment)は実質的に同等になる場合がある。
In addition, with reference to FIG. 4, a
図5に関連し、本明細書に記述されるポリマー材料で形成された可撓性コネクター104のセクション500を例示する。図示されるように、可撓性コネクター104のセクション500は、2つの第1の帯域t2と1つの第2の帯域t1とを有するように設計されている。2つの帯域t2は、1つの第2の帯域t1と比べてより大きいポリマー鎖配向度を有するように設計または構成されている。帯域t2における、より大きいポリマー鎖配向度は、前駆体物質を、ステントの半径方向または円周方向の軸に並行する方向に延伸することによって達成することができる。加えて、配向はまた、上述の方法によっても達成することができる。図5に例示される典型的な具体例において、t2領域は、意図的にt1領域よりも薄くなっており、このため、t2領域は、t1領域に比べてひずみが大きい帯域である。デバイスの性能特性は、ポリマー鎖配向の種類および配向度と機能特性とを最適化することによって改善することができる。ステントの可撓性コネクターの諸部品のための性能特性は、動負荷状況を考慮すれば、複数軸およびねじれの可撓性(multiaxial and torsional flexibility)であり、また、展開(deployment)を考慮すれば、短縮性(foreshortening)である。
FIG. 6 illustrates a
図6に関連し、本明細書に記述されるポリマー材料で形成された可撓性コネクター104のセクション600を例示する。図示されるように、可撓性コネクター104のセクション600は、1つの第1の帯域t1と2つの第2の帯域t2とを有するように設計されている。1つの第1の帯域t1は、2つの帯域t2と比べてより大きいポリマー鎖配向度を有するように設計または構成されている。帯域t1における、より大きいポリマー鎖配向度は、前駆体物質を、ステントの縦軸に並行する方向に延伸することによって達成することができる。加えて、配向はまた、上述の方法によっても達成することができる。図6に例示される典型的な具体例において、t1領域は、t2領域に比べてひずみが大きい帯域である。デバイスの性能特性は、ポリマー鎖配向の種類および配向度と機能特性とを最適化することによって改善することができる。ステントの可撓性コネクター部品のための性能特性は、動負荷状況を考慮すれば、複数軸およびねじれの可撓性であり、また、展開を考慮すれば、短縮性である。
FIG. 6 illustrates a
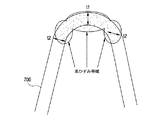
図7に関連し、本明細書に記述されるポリマー材料で形成された可撓性コネクター104のセクション700を例示する。この図は、図5および図6に例示されるポリマー鎖配向の組合せを示している。換言すれば、帯域t1およびt2における整列度(degree of alignment)は実質的に同等になる場合がある。
FIG. 7 illustrates a
当業者には、最適なステント性能を達成するためにはどの形状(configuration)が好ましいかを決定する、設計に関する多数の検討事項が存在する。上記の諸図面は、幾つかの可能性を例示するに過ぎない。設計と材料との組合せを最適化するためには、短期的かつ長期的性能特性(performance attributes)を考慮することが適切である。これらの因子の一つには、可撓性コネクター要素の設計が包含される。例えば、可撓性コネクターが、半径方向の(radial:放射状に配置された)円弧部材の頂点で、半径方向のフープに接合する場合、設計者は、高ひずみ領域が含まれるように、半径方向のフープの長手方向の部品を選定するかもしれない。したがって、材料と設計との最適化を行えば、結果的にポリマー鎖の長手方向配向が選択的に生じるであろう。代替的に、可撓性コネクターが、半径方向の円弧部材の端部で、または、半径方向のストラットのセクションにおいて、半径方向のフープに接合する場合、設計者は、高ひずみ領域が含まれるように、半径方向の円弧部材の頂点を選定するかもしれない。したがって、材料と設計との設計最適化(design optimization)を行えば、結果的にポリマー鎖の円周方向配向が選択的に生じるであろう。 There are a number of design considerations in the art to determine which configuration is preferred to achieve optimal stent performance. The above figures merely illustrate some possibilities. In order to optimize the combination of design and material, it is appropriate to consider short-term and long-term performance attributes. One of these factors includes the design of the flexible connector element. For example, if the flexible connector is joined to a radial hoop at the apex of a radial arc member, the designer may use the radial direction to include a high strain region. You may choose the longitudinal part of the hoop. Thus, optimization of materials and design will result in selective longitudinal orientation of the polymer chains. Alternatively, if the flexible connector joins the radial hoop at the end of the radial arc member or at the section of the radial strut, the designer may include a high strain region. In addition, the apex of the radial arc member may be selected. Therefore, design optimization between material and design will result in selective circumferential orientation of polymer chains.
加えて、可撓性コネクター上の負荷が、該可撓性コネクターの、長手方向に配向した要素と一直線に並ぶ場合、材料と設計との最適化を行えば、結果的にポリマー鎖の長手方向配向が選択的に生じるであろう。同様に、可撓性コネクター上の負荷が、該可撓性コネクターの、円周方向に配向した要素と一直線に整列する場合、材料と設計との最適化を行えば、結果的にポリマー鎖の円周方向配向が選択的に生じるであろう。 In addition, if the load on the flexible connector is aligned with the longitudinally oriented elements of the flexible connector, material and design optimization results in the longitudinal direction of the polymer chain. Orientation will occur selectively. Similarly, if the load on the flexible connector is aligned with the circumferentially oriented elements of the flexible connector, material and design optimization will result in polymer chain Circumferential orientation will selectively occur.
上記記述は、単に例示的なものであり、設計と材料配向との最適化に関する決定を行うために考慮すべき事項を全て捕らえているものと解釈されるべきでない。 The above description is merely exemplary and should not be construed as capturing all considerations for making decisions regarding optimization of design and material orientation.
特定の形状(configuration:相対的配置)が例示され記述されているものの、記述された原理が、フープと可撓性コネクターとの設計に関するいかなる形状にも同等に適用され得ることに注目することは、重要である。加えて、整列軸は、単一方向に(例えば、長手方向または半径方向に)一致する訳ではなく、2つの方向の組合せに一致する。 It should be noted that although specific configurations are illustrated and described, the described principles can be equally applied to any shape related to the design of the hoop and flexible connector. ,is important. In addition, the alignment axis does not coincide with a single direction (eg, longitudinal or radial), but coincides with a combination of the two directions.
ポリマー材料は概して、合成のもの、天然のもの、および/または、それらの組合せに分類することができる。ポリマー材料は、これらの概略分類の中で、生物学的安定性または生分解性なものとして規定することができる。生物学的安定性ポリマーの例には、ポリオレフィン、ポリアミド、ポリエステル、フルオロポリマーおよびアクリル樹脂が包含される。天然ポリマーの例には、多糖類およびタンパク質が包含される。 Polymeric materials can generally be classified as synthetic, natural, and / or combinations thereof. Polymeric materials can be defined within these general classifications as being biostable or biodegradable. Examples of biologically stable polymers include polyolefins, polyamides, polyesters, fluoropolymers and acrylic resins. Examples of natural polymers include polysaccharides and proteins.
生体吸収性ポリマーは、バルクエロージョン性材料および表面エロージョン性材料(bulk and surface erodable materials)から成る。表面エロージョン性材料(Surface erosion polymers)は典型的には、疎水性であり、水に不安定な結合(water labile linkages)を有する。加水分解は、そのような表面エロージョン性ポリマーの表面では急速に生じる傾向があり、多量の透水は生じない。しかし、そのような表面エロージョン性ポリマーの初期強度は、低くなる傾向があり、そのような表面エロージョン性ポリマーはしばしば、商業的に容易に入手することができない。とは言え、そのような表面エロージョン性ポリマーの例には、ポリ無水物類(polyanhydrides)、例えば、ポリ(カルボキシフェノキシヘキサン−セバシン酸)、ポリ(フマル酸−セバシン酸)、ポリ(カルボキシフェノキシヘキサン−セバシン酸)、ポリ(イミド−セバシン酸)(50−50)、ポリ(イミド−カルボキシフェノキシヘキサン−)(33−67)およびポリオルトエステル(ジケトンアセタールベースのポリマー)、が包含される。 Bioabsorbable polymers are comprised of bulk erodible materials and surface erodable materials. Surface erosion polymers are typically hydrophobic and have water labile linkages. Hydrolysis tends to occur rapidly on the surface of such surface erodible polymers and does not produce a large amount of water permeation. However, the initial strength of such surface erosion polymers tends to be low and such surface erosion polymers are often not readily available commercially. Nonetheless, examples of such surface erosion polymers include polyanhydrides such as poly (carboxyphenoxyhexane-sebacic acid), poly (fumaric acid-sebacic acid), poly (carboxyphenoxyhexane). -Sebacic acid), poly (imide-sebacic acid) (50-50), poly (imide-carboxyphenoxyhexane-) (33-67) and polyorthoesters (diketone acetal based polymers).
一方、バルクエロージョン性ポリマー(Bulk erosion polymers)は典型的には、親水性であり、水に不安定な結合を有する。バルクエロージョン性ポリマーの加水分解は、前記デバイスのポリマーマトリックスの端から端まで、より均一な速度で生じる傾向がある。バルクエロージョン性ポリマーは、優れた初期強度を示し、かつ、商業的に容易に入手することができる。 On the other hand, bulk erosion polymers are typically hydrophilic and have water labile bonds. Hydrolysis of the bulk erodible polymer tends to occur at a more uniform rate across the polymer matrix of the device. Bulk erosion polymers exhibit excellent initial strength and are readily available commercially.
バルクエロージョン性ポリマーの例には、ポリ(αヒドロキシエステル)類、例えば、ポリ(乳酸)、ポリ(グリコール酸)、ポリ(カプロラクトン)、ポリ(p−ジオキサノン)(poly (p-dioxanone))、ポリ(トリメチレンカーボネート)、ポリ(オキサエステル)[poly(oxaesters)]、ポリ(オキサアミド)[poly(oxaamides)]、ならびに、それらの共重合体および混合物が包含される。商業的に容易に入手することのできる幾つかの種類のバルクエロージョン性ポリマー、および、それらの一般に関連する医療用途には、ポリ(ジオキサノン)[ニュージャージー州サマービル(Somerville)、エチコン社(Ethicon, Inc.)から入手することのできるPDS(登録商標)縫合糸]、ポリ(グリコリド)[コネチカット州ノースヘーヴン(North Haven)、ユナイテッド・ステイツ・サージカル社(United States Surgical Corporation)から入手することのできるDexon(登録商標)縫合糸]、ポリ(ラクチド)−PLLA[骨修復]、ポリ(ラクチド/グリコリド)[ニュージャージー州サマービル、エチコン社から入手することのできるVicryl(登録商標)(10/90)縫合糸およびPanacryl(登録商標)(95/5)縫合糸]、ポリ(グリコリド/カプロラクトン(75/25))[ニュージャージー州サマービル、エチコン社から入手することのできるMonocryl(登録商標)縫合糸]、および、ポリ(グリコリド/トリメチレンカーボネート)[コネチカット州ノースヘーヴン、ユナイテッド・ステイツ・サージカル社から入手することのできるMaxon(登録商標)縫合糸]が包含される。 Examples of bulk erosion polymers include poly (α-hydroxy esters) such as poly (lactic acid), poly (glycolic acid), poly (caprolactone), poly (p-dioxanone), Poly (trimethylene carbonate), poly (oxaesters), poly (oxaamides), and copolymers and mixtures thereof are included. Some types of commercially available bulk erodible polymers and their commonly associated medical applications include poly (dioxanone) [Somerville, NJ, Ethicon, Inc. PDS® sutures available from.), Poly (glycolide) [Dexon (available from United States Surgical Corporation, North Haven, Connecticut) Registered suture), poly (lactide) -PLLA [bone repair], poly (lactide / glycolide) [Vicryl® (10/90) suture available from Ethicon, Somerville, NJ and Panacryl® (95/5) suture, poly ( Glycolide / Caprolactone (75/25)) (Monocryl® suture available from Ethicon, Somerville, NJ) and poly (glycolide / trimethylene carbonate) [North Haven, Connecticut, United States Maxon® sutures available from Surgical Inc.] are included.
他のバルクエロージョン性ポリマーは、チロシンから誘導されるポリアミノ酸[例えば、ポリ(DTH)カーボネート、ポリ(アリレート)[poly(arylates)]およびポリ(イミノカーボネート)]、リン含有ポリマー[例えば、ポリ(ホスホエステル)およびポリ(ホスファゼン)]、ポリ(エチレングリコール)[PEG]ベースのブロック共重合体[PEG−PLA、PEG−ポリ(プロピレングリコール)、PEG−ポリ(ブチレンテレフタレート)]、ポリ(αリンゴ酸)、ポリ(エステルアミド)、ならびに、ポリアルカノエート(polyalkanoates)[例えば、ポリ(ヒドロキシブチラート)(HB)とポリ(ヒドロキシバレラート)[poly(hydroxyvalerate)](HV)との共重合体]である。 Other bulk erosion polymers include polyamino acids derived from tyrosine [eg, poly (DTH) carbonate, poly (arylates) and poly (iminocarbonate)], phosphorus-containing polymers [eg, poly ( Phosphoesters) and poly (phosphazenes)], poly (ethylene glycol) [PEG] based block copolymers [PEG-PLA, PEG-poly (propylene glycol), PEG-poly (butylene terephthalate)], poly (α-apple) Acid), poly (ester amide), and polyalkanoates [e.g., copolymers of poly (hydroxybutyrate) (HB) and poly (hydroxyvalerate) (HV) ].
もちろん、前記デバイスは、所望の物理的特性を達成し、かつ、分解機構を制御するために、表面エロージョン性ポリマーとバルクエロージョン性ポリマーとの組合せから作ることができる。所望の物理的特性とデバイスの分解速度とを達成するために、例えば、2種類以上のポリマーを混合することができる。代替的に、デバイスは、表面エロージョン性ポリマーで被覆されているバルクエロージョン性ポリマーで作ることができる。 Of course, the device can be made from a combination of surface erodible polymer and bulk erodible polymer to achieve the desired physical properties and control the degradation mechanism. For example, two or more polymers can be mixed to achieve the desired physical properties and device degradation rate. Alternatively, the device can be made of a bulk erosion polymer that is coated with a surface erosion polymer.
形状記憶ポリマー(shape memory polymers)も使用することができる。形状記憶ポリマーは、硬質セグメントと軟質セグメントとを有する相分離線形ブロック共重合体(phase segregated linear block co-polymers)としての特徴を示す。硬質セグメントは典型的には、規定された融点を有する結晶であり、軟質セグメントは典型的には、規定されたガラス転移温度を有する非晶質である。形状記憶ポリマーにおいて、軟質セグメントの転移温度は、硬質セグメントの転移温度よりも実質的に低い。形状記憶ポリマーの形状は、加熱技術および冷却技術によって、該形状記憶ポリマーの硬質セグメントおよび軟質セグメントの中に記憶される。形状記憶ポリマーは、生物学的安定性かつ生体吸収性である場合がある。生体吸収性形状記憶ポリマーは、比較的新しく、熱可塑性物質および熱硬化性物質を含有する。形状記憶熱硬化性物質は、ポリ(カプロラクトン)ジメチルアクリレートを含有することができ、また、形状記憶熱可塑性物質は、軟質セグメントとしてのポリ(カプロラクトン)と、硬質セグメントとしてのポリ(グリコリド)とを含有することができる。 Shape memory polymers can also be used. Shape memory polymers exhibit characteristics as phase segregated linear block co-polymers having hard and soft segments. Hard segments are typically crystals having a defined melting point, and soft segments are typically amorphous having a defined glass transition temperature. In shape memory polymers, the soft segment transition temperature is substantially lower than the hard segment transition temperature. The shape of the shape memory polymer is stored in the hard and soft segments of the shape memory polymer by heating and cooling techniques. Shape memory polymers may be biologically stable and bioabsorbable. Bioabsorbable shape memory polymers are relatively new and contain thermoplastic and thermoset materials. The shape memory thermoset can contain poly (caprolactone) dimethyl acrylate, and the shape memory thermoplastic can contain poly (caprolactone) as a soft segment and poly (glycolide) as a hard segment. Can be contained.
高い柔軟性(ductility)および靭性(toughness)、例えば、整形外科用のインプラント、縫合糸、ステント、移植片(grafts)、および、薬物運搬デバイスを包含する他の医療用途のためにしばしば必要とされるような柔軟性および靭性を有する材料を提供するために、複数の生体吸収性ポリマー材料を修飾して、それらの複合材料または混合物を形成することができる。そのような複合材料または混合物は、ポリマー主鎖の化学構造を変えることによるか、または、それら生体吸収性ポリマー材料を異なるポリマーおよび可塑剤と混合することにより複合材料を作り出すことによって、得ることができる。基礎を成す生体吸収性ポリマーを修飾するために使用されるいかなる追加材料も、好ましくは、主ポリマー系と相溶性である(compatible)ことが望ましい。それらの追加材料は、該生体吸収性ポリマーのガラス転移温度を低下させる傾向があり、そのことによって、基礎を成すポリマーは、より柔軟性となり、かつ、剛性が低下する。 High ductility and toughness, for example orthopedic implants, sutures, stents, grafts, and other medical applications that include drug delivery devices are often required In order to provide such a flexible and tough material, a plurality of bioabsorbable polymer materials can be modified to form a composite material or mixture thereof. Such composite materials or mixtures can be obtained by altering the chemical structure of the polymer backbone or by creating the composite material by mixing the bioabsorbable polymer materials with different polymers and plasticizers. it can. Any additional material used to modify the underlying bioabsorbable polymer is preferably compatible with the main polymer system. These additional materials tend to reduce the glass transition temperature of the bioabsorbable polymer, which makes the underlying polymer more flexible and less rigid.
複合材料または混合材料を生成する例として、非常に堅いポリマー[例えば、ポリ(乳酸)、ポリ(グリコリド)およびポリ(ラクチド−コ−グリコリド)共重合体]を、軟質で柔軟性のポリマー[例えば、ポリ(カプロラクトン)およびポリ(ジオキサノン)]と混合する工程によって、高柔軟性および高剛性を有する材料が生成される傾向がある。様々な割合の剛性ポリマーと軟質ポリマーとから、弾性共重合体を合成することができる。例えば、ポリ(グリコリド)またはポリ(ラクチド)は、ポリ(カプロラクトン)またはポリ(ジオキサノン)と共重合して、ポリ(グリコリド−コ−カプロラクトン)共重合体またはポリ(グリコリド−コ−ジオキサノン)共重合体、および、ポリ(ラクチド−コ−カプロラクトン)共重合体またはポリ(ラクチド−コ−ジオキサノン)共重合体を調製することができる。次いで、これらの弾性共重合体を剛性材料[例えば、ポリ(ラクチド)、ポリ(グリコリド)およびポリ(ラクチド−コ−グリコリド)共重合体]と混合して、高柔軟性を有する材料を生成することができる。代わりに、様々なモノマーから三元重合体(terpolymers)を調製して、所望の特性を得ることができる。マクロマー(Macromers)および他の架橋性ポリマー系を使用して、所望の特性を得ることができる。 As an example of producing a composite or mixed material, very stiff polymers [eg, poly (lactic acid), poly (glycolide) and poly (lactide-co-glycolide) copolymers] can be converted into soft, flexible polymers [eg, , Poly (caprolactone) and poly (dioxanone)] tend to produce materials with high flexibility and rigidity. Elastic copolymers can be synthesized from various proportions of rigid and soft polymers. For example, poly (glycolide) or poly (lactide) is copolymerized with poly (caprolactone) or poly (dioxanone) to produce a poly (glycolide-co-caprolactone) copolymer or poly (glycolide-co-dioxanone) copolymer. Polymers and poly (lactide-co-caprolactone) copolymers or poly (lactide-co-dioxanone) copolymers can be prepared. These elastic copolymers are then mixed with a rigid material [eg, poly (lactide), poly (glycolide) and poly (lactide-co-glycolide) copolymers] to produce a highly flexible material. be able to. Alternatively, terpolymers can be prepared from various monomers to obtain the desired properties. Macromers and other crosslinkable polymer systems can be used to obtain the desired properties.
前記デバイスが患者に植え込まれる時、該デバイスを視覚化することは、該デバイスを配置する医師にとって重要であるので、該デバイスに放射線不透過性物質が添加されることがある。放射線不透過性物質は、処理の間、デバイスを構成する生体吸収性材料のマトリックスに直接添加することができ、その結果として、該放射線不透過性物質は該デバイスの全体に渡ってかなり均一に組み入れられる。もう一つの方法として、放射線不透過性物質は、デバイスに、層、コーティング、バンド(band)または粉末の形態で、該デバイスの所定の部分に付け加えることができ、これは、該デバイスの幾何学的条件と該デバイスを形成するために使用されるプロセスとによって決まる。コーティングは、当該技術分野で知られている様々な方法(例えば、化学蒸着(CVD)、物理蒸着(PVD)、電気メッキ、高真空蒸着法、マイクロ溶融(microfusion)、吹付け塗装、浸漬塗装、静電塗装、または、他の表面被覆技術もしくは表面修飾技術)で、デバイスに施用することができる。デバイスが、内部にデバイスが配置される組織(anatomy)を容易に通過することができるように、放射線不透過性物質は有意な剛性をデバイスに付加しないことが理想的である。放射線不透過性物質は、該デバイスが内部に配置される組織(tissue)と生体適合性であることが望ましい。そのような生体適合性によって、デバイスとの望ましくない組織反応(tissue reactions)の可能性が最小限に抑えられる。不活性な貴金属(例えば、金、白金、イリジウム、パラジウムおよびロジウム)は、生体適合性の放射線不透過性物質として十分認識されている。他の放射線不透過性物質には、硫酸バリウム(BaSO4)、次炭酸ビスマス[(BiO)2CO3]、および、酸化ビスマスが包含される。デバイスからの、放射線不透過性物質のピーリング(peeling:剥脱)もしくは剥離が、最小限に抑えられるような具合に、または、理想的には該ピーリングもしくは該剥離が生じないような具合に、該放射線不透過性物質はデバイスに十分に付着することが理想的である。放射線不透過性物質が、金属バンドとしてデバイスに付加される場合、該金属バンドは、該デバイスの所定のセクションで波状の表面を作る(crimped)ことができる。代替的に、デバイスの所定のセクションは、放射線不透過性の金属粉末で被覆することができるのに対し、該デバイスの他の部分には該金属粉末がない。 As the device is implanted in a patient, visualizing the device is important to the physician placing the device, so a radiopaque material may be added to the device. The radiopaque material can be added directly to the matrix of the bioabsorbable material comprising the device during processing, so that the radiopaque material is fairly uniform throughout the device. Be incorporated. Alternatively, the radiopaque material can be added to the device in the form of a layer, coating, band or powder to a predetermined portion of the device, which is the geometry of the device. Depending on the physical conditions and the process used to form the device. Coatings can be made by various methods known in the art (eg, chemical vapor deposition (CVD), physical vapor deposition (PVD), electroplating, high vacuum deposition, microfusion, spray coating, dip coating, It can be applied to the device by electrostatic coating or other surface coating or surface modification techniques. Ideally, the radiopaque material does not add significant stiffness to the device so that the device can easily pass through the anatomy in which the device is placed. The radiopaque material is desirably biocompatible with the tissue in which the device is placed. Such biocompatibility minimizes the possibility of undesirable tissue reactions with the device. Inert noble metals (eg, gold, platinum, iridium, palladium and rhodium) are well recognized as biocompatible radiopaque materials. Other radiopaque materials include barium sulfate (BaSO 4 ), bismuth hypocarbonate [(BiO) 2 CO 3 ], and bismuth oxide. In such a way that peeling or peeling of the radiopaque material from the device is minimized or ideally such that peeling or peeling does not occur. Ideally, the radiopaque material adheres well to the device. If the radiopaque material is applied to the device as a metal band, the metal band can be crimped on a given section of the device. Alternatively, certain sections of the device can be coated with a radiopaque metal powder, while other portions of the device are free of the metal powder.
治療薬/治療薬の組合せの局所運搬(local delivery)を利用し、かなり多数の種類の医療デバイスを利用しながら多種多様の容態を処置することができるか、または、医療デバイスの機能および/または耐用期間を高めることができる。例えば、白内障手術の後に視力を回復させるために設置された眼内レンズは、二次性白内障(secondary cataract)の形成によってしばしば傷付けられる。二次性白内障は、しばしば、レンズ表面で細胞が過成長した結果であり、また、1種以上の薬剤をデバイスと組合せることによって、潜在的に(potentially)二次性白内障を最小限に抑えることができる。組織の内方成長(in-growth)に起因して、または、デバイスの中、デバイスの上、もしくは、デバイスの周りへのタンパク質物質の蓄積に起因して、しばしば作動しなくなる他の医療デバイス[例えば、水頭症用シャント、透析グラフト(dialysis grafts)、結腸瘻バッグ取り付けデバイス、耳排膿管、ペースメーカー用リード、および、植え込み可能な細動除去器(defibrillators)]もまた、デバイス−薬物の組合せのアプローチによって利点を得ることができる。組織または器官の構造と機能とを改善するのに役立つデバイスもまた、1種以上の適切な薬剤と組合されたとき、利点を示すことができる。例えば、整形外科用デバイスのオステオインテグレーション(osteointegration:骨との結合)を改善して、植え込まれたデバイスの安定化を高めることは、該デバイスを薬剤(例えば、骨形成タンパク質)と組合せることによって、潜在的に達成することができるであろう。同様に、他の外科用器具、縫合糸、ステープル、吻合デバイス、椎骨板(vertebral disks)、骨ピン(bone pins)、縫合糸固定用アンカー(suture anchors)、止血用障壁(hemostatic barriers)、留め具(clamps)、ネジ、プレート(plates)、クリップ、脈管インプラント、組織接着剤および組織シーラント(tissue adhesives and sealants)、組織用足場(tissue scaffolds)、様々な種類の包帯(dressings)、骨代用品、管腔内デバイス(intraluminal devices)、ならびに、脈管支持体(vascular supports)もまた、この、薬剤−デバイスの組合せのアプローチを用いて、患者の利益を高めることができるであろう。血管周囲ラップ(perivascular wraps)は、単独か、または、他の医療デバイスと組合せて、とりわけ好都合となる場合がある。血管周囲ラップは、処置部位に追加の薬剤を供給することができる。本質的に、他のいかなるタイプの医療デバイスも、ある方法で、薬物、または、薬物の組合せで被覆することができ、そのことによって、処置は、医療デバイスまたは薬剤を単一的使用で用いる場合よりも改善される。 The local delivery of therapeutic / therapeutic drug combinations can be used to treat a wide variety of conditions while utilizing a fairly large number of types of medical devices, or the function of medical devices and / or The service life can be increased. For example, intraocular lenses placed to restore vision after cataract surgery are often damaged by the formation of secondary cataract. Secondary cataracts are often a result of cell overgrowth on the lens surface and potentially minimize secondary cataracts by combining one or more drugs with the device. be able to. Other medical devices that often fail due to tissue in-growth or due to the accumulation of protein material in, on or around the device [ For example, hydrocephalus shunts, dialysis grafts, colon fistula bag attachment devices, ear drainage tubes, pacemaker leads, and implantable defibrillators] are also device-drug combinations Benefit from this approach. Devices that help to improve the structure and function of a tissue or organ can also show advantages when combined with one or more appropriate agents. For example, improving the osteointegration of an orthopedic device and increasing the stability of the implanted device can be combined with a drug (eg, a bone morphogenetic protein). Could potentially be achieved. Similarly, other surgical instruments, sutures, staples, anastomosis devices, vertebral disks, bone pins, suture anchors, hemostatic barriers, fasteners Clamps, screws, plates, clips, vascular implants, tissue adhesives and sealants, tissue scaffolds, various types of dressings, bone stock Articles, intraluminal devices, and vascular supports could also increase patient benefit using this drug-device combination approach. Perivascular wraps may be particularly advantageous either alone or in combination with other medical devices. The perivascular wrap can supply additional medication to the treatment site. Essentially any other type of medical device can be coated in some way with a drug, or combination of drugs, so that the treatment is used when the medical device or drug is used in a single use Better than.
様々な医療デバイスに加えて、これらのデバイス上のコーティングを使用して、複数種の治療薬および薬剤を運搬することができる。それらの治療薬および薬剤には、天然物を包含する抗増殖剤/抗有糸分裂物質(anti-proliferative/antimitotic agents)[例えば、ビンカアルカロイド(vinca alkaloids)(即ち、ビンブラスチン(vinblastine)、ビンクリスチン(vincristine)およびビノレルビン(vinorelbine))、パクリタキセル(paclitaxel)、エピジポドフィロトキシン(epidipodophyllotoxins)(即ち、エトポシド(etoposide)、テニポシド(teniposide))、抗生物質(ダクチノマイシン(dactinomycin)(アクチノマイシンD(actinomycin D))、ダウノルビシン(daunorubicin)、ドキソルビシン(doxorubicin)およびイダルビシン(idarubicin))、アントラサイクリン(anthracyclines)、ミトキサントロン(mitoxantrone)、ブレオマイシン(bleomycins)、プリカマイシン(plicamycin)(ミトラマイシン(mithramycin))およびマイトマイシン(mitomycin)、酵素(全身的にL−アスパラギンを代謝し、かつ、細胞自体のアスパラギンを合成する機能を有していない該細胞を排除するL−アスパラギナーゼ(L-asparaginase))];抗血小板凝集阻害剤[例えば、G(GP)IIb/IIIa阻害剤およびビトロネクチン受容体拮抗薬];抗増殖性アルキル化剤/抗有糸分裂性アルキル化剤[例えば、ナイトロジェンマスタード(メクロレタミン(mechlorethamine)、シクロホスファミド(cyclophosphamide)および類似体、メルファラン(melphalan)、クロラムブシル(chlorambucil))、エチレンイミン(ethylenimines)およびメチルメラミン(methylmelamines)(ヘキサメチルメラミンおよびチオテパ(thiotepa))、アルキルスルホネート−ブスルファン(alkyl sulfonates-busulfan)、ニトロソウレア(nirtosoureas)(カルムスチン(carmustine)(BCNU)および類似体、ストレプトゾシン(streptozocin))、トラゼン(trazenes)−ダカルバジン(dacarbazinine)(DTIC)];抗増殖性代謝拮抗剤/抗有糸分裂性代謝拮抗剤[例えば、葉酸類似体(メトトレキサート(methotrexate))、ピリミジン類似体(フルオロウラシル、フロクスウリジン(floxuridine)およびシタラビン(cytarabine))、プリン類似体ならびに関連阻害剤(メルカプトプリン(mercaptopurine)、チオグアニン(thioguanine)、ペントスタチン(pentostatin)および2−クロロデオキシアデノシン(2-chlorodeoxyadenosine){クラドリビン(cladribine)})];白金配位錯体(シスプラチン(cisplatin)、カルボプラチン(carboplatin))、プロカルバジン(procarbazine)、ヒドロキシウレア(hydroxyurea)、ミトタン(mitotane)、アミノグルテチミド(aminoglutethimide);ホルモン(即ち、エストロゲン);抗凝血剤(ヘパリン、合成ヘパリン塩、および、他のトロンビン阻害薬);線維素溶解薬[例えば、組織プラスミノゲンアクチベーター(tissue plasminogen activator)、ストレプトキナーゼ(streptokinase)およびウロキナーゼ(urokinase)]、アスピリン、ジピリダモール(dipyridamole)、チクロピジン(ticlopidine)、クロピドグレル(clopidogrel)、アブシキシマブ(abciximab);アンチミグラトリー(antimigratory);分泌抑制薬(antisecretory)(ブレベルジン(breveldin));抗炎症薬[例えば、副腎皮質ステロイド(コルチゾール(cortisol)、コルチゾン(cortisone)、フルドロコルチゾン(fludrocortisone)、プレドニゾン(prednisone)、プレドニゾロン(prednisolone)、6α-メチルプレドニゾロン(6α-methylprednisolone)、トリアムシノロン(triamcinolone)、ベタメタゾン(betamethasone)およびデキサメタゾン(dexamethasone))、非ステロイド剤(サリチル酸誘導体、即ち、アスピリン)];パラアミノフェノール誘導体、即ち、アセトアミノフェン(acetaminophen);インドールおよびインデン酢酸(インドメタシン(indomethacin)、スリンダク(sulindac)およびエトダレク(etodalec))、ヘテロアリール酢酸(トルメチン(tolmetin)、ジクロフェナク(diclofenac)およびケテロラック(ketorolac))、アリールプロピオン酸(イブプロフェン(ibuprofen)および誘導体)、アントラニル酸(anthranilic acids)(メフェナム酸(mefenamic acid)およびメクロフェナム酸(meclofenamic acid))、エノール酸(ピロキシカム(piroxicam)、テノキシカム(tenoxicam)、フェニルブタゾン(phenylbutazone)およびオキシフェンタトラゾン(oxyphenthatrazone))、ナブメトン(nabumetone)、金化合物(オーラノフィン(auranofin)、オーロチオグルコース(aurothioglucose)、金チオリンゴ酸ナトリウム(gold sodium thiomalate));免疫抑制薬[シクロスポリン(cyclosporine)、タクロリムス(tacrolimus)(FK−506)、シロリムス(sirolimus)(ラパマイシン(rapamycin))、アザチオプリン(azathioprine)、ミコフェノレート・モフェチル(mycophenolate mofetil)];血管新生剤[血管内皮増殖因子(vascular endothelial growth factor)(VEGF)、線維芽細胞増殖因子(fibroblast growth factor)(FGF)];アンジオテンシン受容体遮断薬(angiotensin receptor blockers);酸化窒素ドナー(nitric oxide donors)、アンチセンスオリゴヌクレオチド(antisense oligionucleotides)およびそれらの組合せ;細胞周期阻害剤(cell cycle inhibitors)、mTOR阻害剤、および、増殖因子受容体シグナル伝達キナーゼ阻害剤(growth factor receptor signal transduction kinase inhibitors);レテノイド(retenoids);サイクリン(cyclin)/CDK阻害剤;HMG補酵素還元酵素阻害薬(スタチン(statins));ならびに、プロテアーゼ阻害薬(protease inhibitors)が包含される。 In addition to various medical devices, coatings on these devices can be used to carry multiple types of therapeutic agents and drugs. These therapeutic agents and drugs include natural products, including anti-proliferative / anti-proliferative / antimitotic agents [eg, vinca alkaloids (ie, vinblastine, vincristine ( vincristine and vinorelbine), paclitaxel, epidipodophyllotoxins (ie, etoposide, teniposide), antibiotics (dactinomycin) (actinomycin D) (actinomycin D)), daunorubicin, doxorubicin and idarubicin), anthracyclines, mitoxantrone, bleomycins, plicamycin (mitramycin) )) And mitomycin, enzyme (systemically L-aspa It metabolizes Gin, and eliminates the cells do not have the ability to synthesize asparagine cells themselves L- asparaginase (L-asparaginase))]; anti-platelet aggregation inhibitors [for example, G (GP) II b / III a inhibitors and vitronectin receptor antagonists]; antiproliferative alkylating agent / antimitotic alkylating agents [e.g., nitrogen mustards (mechlorethamine (mechlorethamine), cyclophosphamide (cyclophosphamide) and analogs , Melphalan, chlorambucil, ethylenimines and methylmelamines (hexamethylmelamine and thiotepa), alkyl sulfonates-busulfan, nirtosoureas ) (Carmustine (BCNU) and analogues, streptozocin (strep tozocin)), trazenes-dacarbazinine (DTIC)]; antiproliferative antimetabolite / anti-mitotic antimetabolite [eg folic acid analogue (methotrexate), pyrimidine analogue ( Fluorouracil, floxuridine and cytarabine), purine analogues and related inhibitors (mercaptopurine, thioguanine, pentostatin and 2-chlorodeoxyadenosine) {Cladribine})]; platinum coordination complex (cisplatin, carboplatin), procarbazine, hydroxyurea, mitotane, aminoglutethimide; hormone (Ie, estrogen); anticoagulants (heparin, synthetic heparin salts, And other thrombin inhibitors); fibrinolytic agents [eg tissue plasminogen activator, streptokinase and urokinase], aspirin, dipyridamole, ticlopidine, Clopidogrel, abciximab; antiimigratory; antisecretory (breveldin); anti-inflammatory drugs [eg corticol, cortisone, cortisone, Fludrocortisone (fludrocortisone), prednisone (prednisone), prednisolone (prednisolone), 6α-methylprednisolone (6α-methylprednisolone), triamcinolone (betamethasone) and dexamethasone (dexamethasone), non-steroidal agent (dexamethasone) That is Aspirin)]; paraaminophenol derivatives, ie acetaminophen; indole and indene acetic acid (indomethacin, sulindac and etodalec), heteroaryl acetic acid (tolmetin, diclofenac) ) And ketorolac), arylpropionic acids (ibuprofen and derivatives), anthranilic acids (mefenamic acid and meclofenamic acid), enolic acid (piroxicam), Tenoxicam, phenylbutazone and oxyphenthatrazone), nabumetone, gold compounds (auranofin), aurothioglucose, gold sodium sodium thiomalate thi immunosuppressants [cyclosporine, tacrolimus (FK-506), sirolimus (rapamycin), azathioprine, mycophenolate mofetil]; Angiogenic agents [vascular endothelial growth factor (VEGF), fibroblast growth factor (FGF)]; angiotensin receptor blockers; nitric oxide donors donors), antisense oligonucleotides and combinations thereof; cell cycle inhibitors, mTOR inhibitors, and growth factor receptor signal transduction kinase inhibitors Retenoids; cyclin / CDK inhibitors; HMG co-fermentation Elemental reductase inhibitors (statins); and protease inhibitors are included.
もう一つの典型的な具体例によると、本明細書に記載のステントは、金属製であろうとポリマー製であろうと、治療薬または薬剤の運搬デバイスとして利用することができる。金属製ステントは、生物学的安定性もしくは生体吸収性のポリマーまたはそれらの組合せであって、その中に治療薬が組み込まれている該ポリマーで被覆することができる。コーティングのための典型的な材料特性には、可撓性、柔軟性(ductility)、粘着性(tackiness)、耐久性、付着性(adhesion)および凝集性(cohesion)が包含される。これらの所望の特性を示す生物学的安定性もしくは生体吸収性のポリマーには、メタクリレート、ポリウレタン、シリコーン、ポリ(酢酸ビニル)、ポリ(ビニルアルコール)、エチレンビニルアルコール、ポリ(フッ化ビニリデン)、ポリ(乳酸)、ポリ(グリコール酸)、ポリ(カプロラクトン)、ポリ(トリメチレンカーボネート)、ポリ(ジオキサノン)、ポリオルトエステル、ポリ無水物、ポリホスホエステル、ポリアミノ酸、ならびに、それらの共重合体および混合物が包含される。 According to another exemplary embodiment, the stents described herein, whether metallic or polymeric, can be utilized as therapeutic or drug delivery devices. Metallic stents can be coated with a biostable or bioabsorbable polymer, or a combination thereof, in which the therapeutic agent is incorporated. Typical material properties for coatings include flexibility, ductility, tackiness, durability, adhesion and cohesion. Biologically stable or bioabsorbable polymers that exhibit these desired properties include methacrylates, polyurethanes, silicones, poly (vinyl acetate), poly (vinyl alcohol), ethylene vinyl alcohol, poly (vinylidene fluoride), Poly (lactic acid), poly (glycolic acid), poly (caprolactone), poly (trimethylene carbonate), poly (dioxanone), polyorthoester, polyanhydride, polyphosphoester, polyamino acid, and copolymers thereof And mixtures.
コーティングは、治療薬が組み入れられることに加えて、他の添加剤[例えば、放射線不透過性構成物質、該コーティングおよび/または該治療薬のための化学安定剤、放射性薬剤、トレーシング試薬(tracing agents)(例えば、放射性同位元素(例えば、トリチウム、即ち重水)および強磁性体粒子)、ならびに、機械的修飾剤(mechanical modifiers)(例えば、後で、より詳細に記述されるセラミック微小球(ceramic microspheres))]をも含有することができる。代替的に、デバイスの表面とコーティングとの間、および/または、コーティングそれ自体の内部に、エントラップトギャップ(entrapped gaps:閉じ込められた隙間)を作り出すことができる。これらのギャップの例には、空気だけでなく他のガス、および、物質不在(absence of matter)(即ち、真空環境)が包含される。これらのエントラップトギャップは、かなり多数の既知技術(例えば、マイクロカプセル化ガス(microencapsulated gaseous matter)の注入)を利用して作り出すことができる。 In addition to the therapeutic agent being incorporated, the coating may contain other additives [eg, radiopaque components, chemical stabilizers for the coating and / or the therapeutic agent, radiopharmaceuticals, tracing reagents. agents (eg, radioisotopes (eg, tritium or heavy water) and ferromagnetic particles), and mechanical modifiers (eg, ceramic microspheres (described later in more detail) microspheres))]. Alternatively, entrapped gaps can be created between the surface of the device and the coating and / or within the coating itself. Examples of these gaps include not only air but also other gases and the absence of matter (ie, a vacuum environment). These entrapped gaps can be created utilizing any number of known techniques (eg, injection of microencapsulated gaseous matter).
上述のように、治療薬として、様々な薬剤を利用することができる。それら薬剤には、シロリムス(sirolimus)、ヘパリン(heparin)、エベロリムス(everolimus)、タクロリムス(tacrolimus)、パクリタキセル(paclitaxel)、クラドリビン(cladribine)だけでなく、スタチン(statins)等の種類の薬剤も包含される。これらの薬剤および/または作用物質は、親水性、疎水性、親油性および/または疎油性であってもよい。作用物質の種類は、ポリマーの種類を決定する場合の役割を果たす。コーティング中の薬剤の量は、様々である場合があり、該コーティングの貯蔵能力、該薬剤、該薬剤の濃度、該薬剤の溶出速度だけでなく、多くの付加的要因をも包含する、多数の要因によって決まる。薬剤の量は、実質的に0%から実質的に100%まで様々である場合がある。典型的な範囲は、約1%未満から約40%までまたはそれ以上である場合がある。コーティング中での薬剤の分布は、様々である場合がある。単一層、複数層、拡散障壁を有する単一層、または、それらのいずれかの組合せの中に1種以上の薬剤を分布させることができる。 As described above, various drugs can be used as therapeutic agents. These drugs include not only sirolimus, heparin, everolimus, tacrolimus, paclitaxel, cladribine, but also statins. The These agents and / or agents may be hydrophilic, hydrophobic, lipophilic and / or oleophobic. The type of agent plays a role in determining the type of polymer. The amount of drug in the coating can vary and includes a number of factors including not only the storage capacity of the coating, the drug, the concentration of the drug, the dissolution rate of the drug, but also many additional factors. It depends on the factors. The amount of drug may vary from substantially 0% to substantially 100%. A typical range may be less than about 1% to about 40% or more. The distribution of the drug in the coating can vary. One or more drugs can be distributed in a single layer, multiple layers, a single layer with a diffusion barrier, or any combination thereof.
薬物/ポリマーの混合物を溶解するために様々な溶媒を使用して、コーティング配合物を調製することができる。それら溶媒の幾種類かは、良溶媒または貧溶媒である場合があり、これは、所望の薬剤溶出プロフィールと薬剤の形態と薬剤の安定性とに基づく。 Various solvents can be used to dissolve the drug / polymer mixture to prepare the coating formulation. Some of these solvents may be good or poor solvents, which are based on the desired drug elution profile, drug form and drug stability.
従来技術に開示されている、ステントを被覆するための幾つかの方法が存在する。通常使用される方法の幾つかには、吹付け塗装、浸漬塗装、静電塗装、流動層塗装(fluidized bed coating)、および、超臨界流体塗装(supercritical fluid coatings)が包含される。 There are several methods for coating stents that are disclosed in the prior art. Some commonly used methods include spray coating, dip coating, electrostatic coating, fluidized bed coating, and supercritical fluid coatings.
使用することのできる、本明細書に記述されている諸方法と修飾(modifications)との幾つかによって、ステント上に薬剤を保持するポリマーの必要性が排除されるであろう。薬剤含有量と組織−デバイスとの相互作用を増大させるため、ステント表面を部分的に修正して、表面積を大きくすることができる。ナノテクノロジーを応用して、組織特定薬剤を含有するナノ粒子を含有することのできる自己組織化ナノ材料(self-assembled nanomaterials)を作り出すことができる。これらのナノ粒子を組み入れることのできるマイクロエッチング(microetching)によって、表面上に微構造(microstructures)を形成することができる。それらの微構造は、レーザーマイクロマシニング(laser micromachining)、リソグラフィー(lithography)、化学蒸着および化学エッチングのような方法によって形成することができる。微構造は、微小電気機械システム(micro electro-mechanical systems)(MEMS)およびマイクロ流体力学(microfluidics:マイクロフルイディクス)の進展を利用することによって、ポリマーおよび金属の上に作られてきた。ナノ材料の例には、ゾルゲル技術によって形成されたカーボンナノチューブおよびナノ粒子が包含される。治療薬は、これらの表面上に化学的もしくは物理的に付着させ得るか、または、直接的に堆積させ得る。これらの諸表面修飾の組合せによって、薬剤を所望速度で放出することができる。ポリマーの保護膜(top-coat)を施用して、ポリマーコーティングが存在しない場合に薬剤が直接暴露されることに起因する初期バースト(initial burst)を制御することができる。 Some of the methods and modifications described herein that can be used will eliminate the need for a polymer to retain the drug on the stent. To increase the drug content and tissue-device interaction, the stent surface can be partially modified to increase the surface area. Nanotechnology can be applied to create self-assembled nanomaterials that can contain nanoparticles containing tissue specific drugs. Microetching, which can incorporate these nanoparticles, can form microstructures on the surface. These microstructures can be formed by methods such as laser micromachining, lithography, chemical vapor deposition and chemical etching. Microstructures have been created on polymers and metals by taking advantage of advances in micro electro-mechanical systems (MEMS) and microfluidics. Examples of nanomaterials include carbon nanotubes and nanoparticles formed by sol-gel technology. The therapeutic agent can be chemically or physically deposited on these surfaces, or can be deposited directly. The combination of these surface modifications can release the drug at the desired rate. A polymer top-coat can be applied to control the initial burst due to direct exposure of the drug in the absence of the polymer coating.
上述のように、ポリマー製ステントは、コーティング(例えば、表面修飾)として、治療薬を含有することができる。代替的に、治療薬は、コーティングを必要としなくてよいステント構造体(例えばバルク修飾(bulk modification))の中に組み入れることができる。生物学的安定性ポリマーおよび/または生体吸収性ポリマーで作られたステントのためのコーティングは、使用される場合、生物学的安定性および/または生体吸収性である筈である。しかし、上述のように、デバイスそれ自体が運搬デポー(delivery depot)で作られているので、コーティングは必要でない場合がある。この具体例によって、多数の利点が提供される。例えば、より高い濃度の1種以上の治療薬を得ることができる。加えて、より高い濃度の1種以上の治療薬を用いて、より長い期間の間、局所への薬剤運搬を達成することができる。 As described above, the polymeric stent can contain a therapeutic agent as a coating (eg, surface modification). Alternatively, the therapeutic agent can be incorporated into a stent structure (eg, bulk modification) that may not require a coating. Coatings for stents made of biostable polymers and / or bioabsorbable polymers, when used, should be biostable and / or bioabsorbable. However, as mentioned above, the coating may not be necessary because the device itself is made with a delivery depot. This embodiment provides a number of advantages. For example, higher concentrations of one or more therapeutic agents can be obtained. In addition, higher drug concentrations of one or more therapeutic agents can be used to achieve local drug delivery for a longer period of time.
更にもう一つの代替的具体例において、基礎材料の物理特性を修飾するため、該基礎材料の中にセラミックおよび/またはガラスを意図的に混合することを利用することができる。セラミックおよび/またはガラスの意図的混合は典型的には、医療用途に使用されるポリマー材料の中に行われるであろう。生物学的安定性セラミックおよび/もしくは生物学的安定性ガラス、ならびに/または、生体吸収性セラミックおよび/もしくは生体吸収性ガラスの例には、ハイドロキシアパタイト(hydroxyapatite)、リン酸三カルシウム、マグネシア、アルミナ、ジルコニア、イットリウム正方晶多結晶質ジルコニア(yittrium tetragonal polycrystalline zirconia)、非晶質シリコン、非晶質カルシウムおよび非晶質リン酸化物が包含される。非常に多くの技術を用いることができるが、生物学的安定性ガラスは、工業的に適したゾルゲル法を用いて形成することができる。ゾルゲル技術は、セラミックとガラスとのハイブリッド(hybrids)を作るための溶解法である。ゾルゲル法には典型的には、大部分がコロイド状である液体(ゾル)からゲルへの系の転換が包含される。 In yet another alternative embodiment, intentional mixing of ceramic and / or glass into the base material can be utilized to modify the physical properties of the base material. Intentional mixing of ceramic and / or glass will typically occur in polymeric materials used for medical applications. Examples of biologically stable ceramics and / or biologically stable glasses and / or bioabsorbable ceramics and / or bioabsorbable glasses include hydroxyapatite, tricalcium phosphate, magnesia, alumina Zirconia, yttrium tetragonal polycrystalline zirconia, amorphous silicon, amorphous calcium and amorphous phosphate. Although numerous techniques can be used, biologically stable glasses can be formed using industrially suitable sol-gel methods. The sol-gel technique is a melting method for making hybrids of ceramic and glass. The sol-gel process typically involves the transformation of a system from a liquid (sol), which is mostly colloidal, to a gel.
最も実用的かつ好ましい具体例であると思われるものが図示され記述されてきたものの、記述され図示された特定の設計および方法から変更したものは、当業者によって思い付かれるであろうし、本発明の趣旨または範囲から逸脱することなく、使用することができることは明らかである。本発明は、記述され例示された特定の構成に限定される訳ではなく、特許請求の範囲に含まれ得るあらゆる部分的修正と首尾一貫するように構成されることが望ましい。 While what has been illustrated and described are believed to be the most practical and preferred embodiments, variations from the specific designs and methods described and illustrated will occur to those of skill in the art and are contemplated by the present invention. Clearly, it can be used without departing from the spirit or scope. The present invention is not limited to the specific configurations described and illustrated, but is preferably configured to be consistent with any partial modifications that may be included in the claims.
〔実施の態様〕
(1)縦軸および半径方向軸を有する、実質的に管状の管腔内医療デバイスにおいて、
半径方向の複数のストラット、および半径方向の複数の円弧部材を有する、ポリマー材料で形成された複数のフープと、
前記複数のフープを相互連結している、ポリマー材料で形成された複数のブリッジであって、前記複数のブリッジの各々が、機械的変形によって生じる所定のポリマー鎖整列度を有する少なくとも1つの部材を有している、前記複数のブリッジと、
を備えている、デバイス。
(2)実施態様1に記載のデバイスにおいて、
前記ポリマー材料は、生体吸収性ポリマーを含有している、デバイス。
(3)実施態様2に記載のデバイスにおいて、
前記生体吸収性ポリマーは、ポリ(α−ヒドロキシエステル)(poly(α-hydroxy esters))を含有している、デバイス。
(4)実施態様2に記載のデバイスにおいて、
前記生体吸収性ポリマーは、チロシン誘導ポリアミノ酸を含有している、デバイス。
(5)実施態様2に記載のデバイスにおいて、
前記生体吸収性ポリマーは、リン含有材料を含有している、デバイス。
(6)実施態様2に記載のデバイスにおいて、
前記生体吸収性ポリマーは、ポリアルカノアート(polyalkanoates)を含有している、デバイス。
(7)実施態様2に記載のデバイスにおいて、
前記生体吸収性ポリマーは、ポリ無水物を含有している、デバイス。
(8)実施態様2に記載のデバイスにおいて、
前記生体吸収性ポリマーは、ポリオルトエステル(polyorthoesters)を含有している、デバイス。
(9)実施態様1に記載のデバイスにおいて、
前記ポリマー材料は、生物学的安定性ポリマー(biostable polymers)を含有している、デバイス。
(10)実施態様9に記載のデバイスにおいて、
前記生物学的安定性ポリマーは、ポリオレフィンを含有している、デバイス。
(11)実施態様9に記載のデバイスにおいて、
前記生物学的安定性ポリマーは、ポリウレタンを含有している、デバイス。
(12)実施態様9に記載のデバイスにおいて、
前記生物学的安定性ポリマーは、フッ素ポリマーを含有している、デバイス。
(13)実施態様9に記載のデバイスにおいて、
前記生物学的安定性ポリマーは、ポリアミドを含有している、デバイス。
(14)実施態様9に記載のデバイスにおいて、
前記生物学的安定性ポリマーは、ポリエステルを含有している、デバイス。
(15)実施態様9に記載のデバイスにおいて、
前記生物学的安定性ポリマーは、アクリル樹脂を含有している、デバイス。
(16)実施態様1に記載のデバイスにおいて、
少なくとも1種の治療薬、
を更に備えている、デバイス。
(17)実施態様16に記載のデバイスにおいて、
前記少なくとも1種の治療薬は、抗再狭窄薬(antirestenotic agent)を含有している、デバイス。
(18)実施態様17に記載のデバイスにおいて、
前記抗再狭窄薬は、ラパマイシン(rapamycin)を含有している、デバイス。
(19)実施態様17に記載のデバイスにおいて、
前記抗再狭窄薬は、パクリタキセル(paclitaxel)を含有している、デバイス。
(20)実施態様16に記載のデバイスにおいて、
前記治療薬は、抗炎症薬を含有している、デバイス。
(21)実施態様19に記載のデバイスにおいて、
前記抗炎症薬は、ラパマイシンを含有している、デバイス。
(22)実施態様19に記載のデバイスにおいて、
前記抗炎症薬は、デキサメタゾン(dexamethasone)を含有している、デバイス。
(23)実施態様16に記載のデバイスにおいて、
前記治療薬は、抗凝血剤を含有している、デバイス。
(24)実施態様23に記載のデバイスにおいて、
前記抗凝血剤は、ヘパリン(heparin)である、デバイス。
(25)実施態様1に記載のデバイスにおいて、
放射線不透過性物質、
を更に備えている、デバイス。
(26)実施態様1に記載のデバイスにおいて、
前記ステントは、自己拡張性である、デバイス。
(27)実施態様1に記載のデバイスにおいて、
前記ステントは、バルーン拡張性である、デバイス
Embodiment
(1) In a substantially tubular intraluminal medical device having a longitudinal axis and a radial axis,
A plurality of hoops formed of a polymer material having a plurality of radial struts and a plurality of radial arc members;
A plurality of bridges formed of a polymer material interconnecting the plurality of hoops, each of the plurality of bridges having a predetermined degree of polymer chain alignment caused by mechanical deformation; Having the plurality of bridges;
Equipped with a device.
(2) In the device according to embodiment 1,
The device, wherein the polymer material contains a bioabsorbable polymer.
(3) In the device according to embodiment 2,
The device, wherein the bioabsorbable polymer contains poly (α-hydroxy esters).
(4) In the device according to embodiment 2,
The device wherein the bioabsorbable polymer contains a tyrosine-derived polyamino acid.
(5) In the device according to embodiment 2,
The device, wherein the bioabsorbable polymer contains a phosphorus-containing material.
(6) In the device according to embodiment 2,
The device, wherein the bioabsorbable polymer contains polyalkanoates.
(7) In the device according to embodiment 2,
The device, wherein the bioabsorbable polymer contains a polyanhydride.
(8) In the device according to embodiment 2,
The device wherein the bioabsorbable polymer contains polyorthoesters.
(9) In the device according to embodiment 1,
The device, wherein the polymeric material contains biostable polymers.
(10) In the device according to embodiment 9,
The device, wherein the biostable polymer contains a polyolefin.
(11) In the device according to embodiment 9,
The device wherein the biologically stable polymer contains polyurethane.
(12) In the device according to embodiment 9,
The device, wherein the biologically stable polymer comprises a fluoropolymer.
(13) In the device according to embodiment 9,
The device, wherein the biostable polymer contains a polyamide.
(14) In the device according to embodiment 9,
The device, wherein the biostable polymer contains a polyester.
(15) In the device according to embodiment 9,
The device, wherein the biologically stable polymer contains an acrylic resin.
(16) In the device according to embodiment 1,
At least one therapeutic agent,
The device further comprising:
(17) In the device according to embodiment 16,
The device, wherein the at least one therapeutic agent comprises an antirestenotic agent.
(18) In the device according to embodiment 17,
The device, wherein the anti-restenosis drug comprises rapamycin.
(19) In the device according to embodiment 17,
The device, wherein the anti-restenosis drug comprises paclitaxel.
(20) In the device of embodiment 16,
The device wherein the therapeutic agent contains an anti-inflammatory agent.
(21) In the device of embodiment 19,
The device, wherein the anti-inflammatory drug contains rapamycin.
(22) In the device of embodiment 19,
The device, wherein the anti-inflammatory agent contains dexamethasone.
(23) In the device of embodiment 16,
The device wherein the therapeutic agent contains an anticoagulant.
(24) In the device of embodiment 23,
The device, wherein the anticoagulant is heparin.
(25) In the device according to embodiment 1,
Radiopaque materials,
The device further comprising:
(26) In the device of embodiment 1,
The device, wherein the stent is self-expanding.
(27) In the device according to embodiment 1,
The stent is balloon expandable, the device
Claims (27)
半径方向の複数のストラット、および半径方向の複数の円弧部材を有する、ポリマー材料で形成された複数のフープと、
前記複数のフープを相互連結している、ポリマー材料で形成された複数のブリッジであって、前記複数のブリッジの各々が、機械的変形によって生じる所定のポリマー鎖整列度を有する少なくとも1つの部材を有している、前記複数のブリッジと、
を備えている、デバイス。 In a substantially tubular intraluminal medical device having a longitudinal axis and a radial axis,
A plurality of hoops formed of a polymer material having a plurality of radial struts and a plurality of radial arc members;
A plurality of bridges formed of a polymer material interconnecting the plurality of hoops, each of the plurality of bridges having a predetermined degree of polymer chain alignment caused by mechanical deformation; Having the plurality of bridges;
Equipped with a device.
前記ポリマー材料は、生体吸収性ポリマーを含有している、デバイス。 The device of claim 1, wherein
The device, wherein the polymer material contains a bioabsorbable polymer.
前記生体吸収性ポリマーは、ポリ(α−ヒドロキシエステル)を含有している、デバイス。 The device of claim 2, wherein
The device, wherein the bioabsorbable polymer contains poly (α-hydroxyester).
前記生体吸収性ポリマーは、チロシン誘導ポリアミノ酸を含有している、デバイス。 The device of claim 2, wherein
The device wherein the bioabsorbable polymer contains a tyrosine-derived polyamino acid.
前記生体吸収性ポリマーは、リン含有材料を含有している、デバイス。 The device of claim 2, wherein
The device, wherein the bioabsorbable polymer contains a phosphorus-containing material.
前記生体吸収性ポリマーは、ポリアルカノアートを含有している、デバイス。 The device of claim 2, wherein
The device wherein the bioabsorbable polymer contains a polyalkanoate.
前記生体吸収性ポリマーは、ポリ無水物を含有している、デバイス。 The device of claim 2, wherein
The device, wherein the bioabsorbable polymer contains a polyanhydride.
前記生体吸収性ポリマーは、ポリオルトエステルを含有している、デバイス。 The device of claim 2, wherein
The device, wherein the bioabsorbable polymer contains a polyorthoester.
前記ポリマー材料は、生物学的安定性ポリマーを含有している、デバイス。 The device of claim 1, wherein
The device, wherein the polymeric material contains a biologically stable polymer.
前記生物学的安定性ポリマーは、ポリオレフィンを含有している、デバイス。 The device of claim 9, wherein
The device, wherein the biostable polymer contains a polyolefin.
前記生物学的安定性ポリマーは、ポリウレタンを含有している、デバイス。 The device of claim 9, wherein
The device wherein the biologically stable polymer contains polyurethane.
前記生物学的安定性ポリマーは、フッ素ポリマーを含有している、デバイス。 The device of claim 9, wherein
The device, wherein the biologically stable polymer comprises a fluoropolymer.
前記生物学的安定性ポリマーは、ポリアミドを含有している、デバイス。 The device of claim 9, wherein
The device, wherein the biostable polymer contains a polyamide.
前記生物学的安定性ポリマーは、ポリエステルを含有している、デバイス。 The device of claim 9, wherein
The device, wherein the biostable polymer contains a polyester.
前記生物学的安定性ポリマーは、アクリル樹脂を含有している、デバイス。 The device of claim 9, wherein
The device, wherein the biologically stable polymer contains an acrylic resin.
少なくとも1種の治療薬、
を更に備えている、デバイス。 The device of claim 1, wherein
At least one therapeutic agent,
The device further comprising:
前記少なくとも1種の治療薬は、抗再狭窄薬を含有している、デバイス。 The device of claim 16, wherein
The device, wherein the at least one therapeutic agent comprises an anti-restenosis agent.
前記抗再狭窄薬は、ラパマイシンを含有している、デバイス。 The device of claim 17, wherein
The device, wherein the anti-restenosis drug contains rapamycin.
前記抗再狭窄薬は、パクリタキセルを含有している、デバイス。 The device of claim 17, wherein
The device, wherein the anti-restenosis drug comprises paclitaxel.
前記治療薬は、抗炎症薬を含有している、デバイス。 The device of claim 16, wherein
The device wherein the therapeutic agent contains an anti-inflammatory agent.
前記抗炎症薬は、ラパマイシンを含有している、デバイス。 The device of claim 19, wherein
The device, wherein the anti-inflammatory drug contains rapamycin.
前記抗炎症薬は、デキサメタゾンを含有している、デバイス。 The device of claim 19, wherein
The device, wherein the anti-inflammatory drug contains dexamethasone.
前記治療薬は、抗凝血剤を含有している、デバイス。 The device of claim 16, wherein
The device wherein the therapeutic agent contains an anticoagulant.
前記抗凝血剤は、ヘパリンである、デバイス。 24. The device of claim 23.
The device, wherein the anticoagulant is heparin.
放射線不透過性物質、
を更に備えている、デバイス。 The device of claim 1, wherein
Radiopaque materials,
The device further comprising:
前記ステントは、自己拡張性である、デバイス。 The device of claim 1, wherein
The device, wherein the stent is self-expanding.
前記ステントは、バルーン拡張性である、デバイス。 The device of claim 1, wherein
The device, wherein the stent is balloon expandable.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11/301,876 US20070134294A1 (en) | 2005-12-13 | 2005-12-13 | Polymeric stent having modified molecular structures in selected regions of the flexible connectors |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2007160102A true JP2007160102A (en) | 2007-06-28 |
Family
ID=38243631
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006334809A Withdrawn JP2007160102A (en) | 2005-12-13 | 2006-12-12 | Polymeric stent having modified molecular structures in selected regions of flexible connectors |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2007160102A (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011505982A (en) * | 2007-12-11 | 2011-03-03 | アボット カルディオバスキュラー システムズ インコーポレーテッド | Method for making a stent from a blow molded tube |
-
2006
- 2006-12-12 JP JP2006334809A patent/JP2007160102A/en not_active Withdrawn
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011505982A (en) * | 2007-12-11 | 2011-03-03 | アボット カルディオバスキュラー システムズ インコーポレーテッド | Method for making a stent from a blow molded tube |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2007160105A (en) | Polymeric stent having modified molecular structures in flexible connectors and in radial struts and radial arcs of hoops | |
| US7914573B2 (en) | Polymeric stent having modified molecular structures | |
| JP2007313324A (en) | Polymeric stent having molecular structure modified into flexible connector and arc member in radial direction of hoop | |
| JP2007313327A (en) | Polymeric stent having modified molecular structure in selected region of hoop, and method for increasing elongation at break | |
| JP2007313323A (en) | Polymeric stent with modified molecular structure in flexible connection part | |
| JP2008012912A (en) | Polymer stent having modified molecular structure in selected area of hoop and its manufacturing method | |
| JP2007160104A (en) | Polymeric stent having modified molecular structures in flexible connectors and radial struts of hoops | |
| JP2007160106A (en) | Polymeric stent having modified molecular structures in selected regions of hoops | |
| JP2007325921A (en) | Polymeric stent having modified molecular structure in flexible connector and radial strut of hoop | |
| JP2007185497A (en) | Polymeric stent having modified molecular structures | |
| JP2007167640A (en) | Polymer stent having modified molecule structure inside flexible connector | |
| JP2007325923A (en) | Polymeric stent having modified molecular structure both in hoop and selected segment of flexible connector | |
| JP2007319671A (en) | Polymer stent having modified molecular structure in radial strut and radial arc member for flexible connector and hoop | |
| JP2007160102A (en) | Polymeric stent having modified molecular structures in selected regions of flexible connectors | |
| JP2007167641A (en) | Polymer stent having modified molecule structure in flexible connector and radial arc member of hoop |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20071130 |
|
| A300 | Withdrawal of application because of no request for examination |
Free format text: JAPANESE INTERMEDIATE CODE: A300 Effective date: 20100302 |