JP2005298345A - Phenol compound and process for producing the same - Google Patents
Phenol compound and process for producing the same Download PDFInfo
- Publication number
- JP2005298345A JP2005298345A JP2002228230A JP2002228230A JP2005298345A JP 2005298345 A JP2005298345 A JP 2005298345A JP 2002228230 A JP2002228230 A JP 2002228230A JP 2002228230 A JP2002228230 A JP 2002228230A JP 2005298345 A JP2005298345 A JP 2005298345A
- Authority
- JP
- Japan
- Prior art keywords
- group
- alk
- formula
- compound
- general formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 *N1CCOCC1 Chemical compound *N1CCOCC1 0.000 description 2
Landscapes
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
【課題】本発明は、優れた抗酸化作用を有し、虚血性心疾患等の予防又は治療薬として有用な新規フェノール誘導体を提供するものである。
【解決手段】一般式[I]:
【化1】
(式中、OR1は保護されていてもよい水酸基、R2は低級アルキル基、Alk1は低級アルキレン基、Alk2は単結合手又は低級アルキレン基、Xは酸素原子又は低級アルキル基及びヒドロキシ低級アルキル基から選ばれる基で置換されていてもよいイミノ基を表す。)
で示される新規フェノール誘導体又はその薬理的に許容し得る塩。
【選択図】 なしThe present invention provides a novel phenol derivative which has an excellent antioxidant action and is useful as a preventive or therapeutic agent for ischemic heart disease and the like.
The general formula [I]:
[Chemical 1]
(In the formula, OR 1 is an optionally protected hydroxyl group, R 2 is a lower alkyl group, Alk 1 is a lower alkylene group, Alk 2 is a single bond or a lower alkylene group, X is an oxygen atom or a lower alkyl group, and hydroxy. It represents an imino group which may be substituted with a group selected from lower alkyl groups.)
Or a pharmacologically acceptable salt thereof.
[Selection figure] None
Description
【0001】
【発明の属する技術分野】
本発明は、優れた抗酸化作用を有する新規フェノール化合物に関する。
【0002】
【従来の技術】
虚血性疾患の発症における細胞膜傷害(細胞死を含む)の発生機序は必ずしも解明されているわけではないが、かかる細胞傷害過程においては、活性酸素の産生亢進が重要な役割を担っているものと考えられている。また、活性酸素は脂質の過酸化のみならず、酵素や蛋白質の変性、及び核酸の傷害等を引き起こし、これらが種々の臓器障害の原因となることも知られている。例えば、冠動脈閉塞による心筋梗塞発作を発症した場合、これが心原性ショックや致死性不整脈等の重篤な症状を惹起しやすいため、初期治療として、梗塞部位の血流再開を目的とした再灌流療法(血栓溶解療法、経皮的冠形成術(PTCA)、冠動脈バイパス手術(CABG)等)がしばしば施行される。しかしながら、この場合、血行再開によって心筋組織障害が悪化すること(虚血/再灌流障害)も少なくない。この虚血/再灌流障害の発症機序の一つとして、活性酸素の関与が報告されており、再灌流時に発生した酸素ラジカルが再灌流不整脈を惹起し、ATP産生障害に伴う細胞障害や酵素蛋白活性増加に伴う細胞膜破壊によって心筋障害をきたすと考えられている。
【0003】
一方、ラジカル消去作用や抗酸化作用を有する化合物としては、例えば、特開平10−195037又は特開平9−278741に、2−[4−(4−アミノフェニル)ピペラジン−1−イル]アミド−4−メトキシ−6−tert−ブチルフェノール、2−(2−フェニル−1−シクロヘキシルエチルカルボニルアミノ)−4−メトキシ−6−tert−ブチルフェノール等のフェノール化合物が開示されている。しかしながら、虚血性疾患の薬物治療に際しては、特に、注射剤として有効かつ安全に投与できる薬剤が望まれるが、前記既知フェノール誘導体は、溶解度その他の面で、注射剤として好適な特性を具備するものとはいい難い。このため、優れた抗酸化作用のみならず、注射用薬としても好適な特性を具有する薬物を見出す必要があった。
【0004】
【発明が解決しようとする課題】
本発明は、優れた抗酸化作用を有するとともに、注射剤としても好適な特性を具備し、心筋梗塞や虚血/再灌流時の細胞傷害及び不整脈等の予防・治療に有用な新規フェノール化合物を提供するものである。また、本発明は、このような新規フェノール化合物の製法をも提供するものである。
【0005】
【課題を解決するための手段】
本発明は、一般式[I]:
【0006】
【化10】
【0007】
(式中、OR1は保護されていてもよい水酸基、R2は低級アルキル基、Alk1は低級アルキレン基、Alk2は単結合手又は低級アルキレン基、Xは酸素原子又は低級アルキル基及びヒドロキシ低級アルキル基から選ばれる基で置換されていてもよいイミノ基を表す。)
で示されるフェノール化合物又はその薬理的に許容し得る塩に関する。
【0008】
【発明の実施の形態】
本発明のフェノール誘導体[I]の具体例としては、例えば、一般式[I]において、OR1が低級アルコキシ低級アルキル基で保護されていてもよい水酸基、R2が炭素数1から4個のアルキル基、Alk1が炭素数1から4個のアルキレン基、Alk2が単結合手又は炭素数1から4個のアルキレン基、Xが酸素原子又は低級アルキル基及びヒドロキシ低級アルキル基から選ばれる基で置換されたイミノ基である化合物が挙げられる。
【0009】
上記のうち、好ましい化合物としては、例えば、一般式[I]において、OR1が水酸基又はメトキシメトキシ基、R2がtert−ブチル基、Alk1がメチレン基又はエチレン基、Alk2が単結合手又はエチレン基、Xが酸素原子又はメチル基及びヒドロキシエチル基から選ばれる基で置換されたイミノ基である化合物が挙げられる。
【0010】
更に好ましい化合物としては、例えば、一般式[I]において、OR1が水酸基、R2がtert−ブチル基、Alk1がエチレン基、Alk2が単結合手又はエチレン基、Xが酸素原子、メチルイミノ基又は2−ヒドロキシエチルイミノ基である化合物が挙げられる。
【0011】
上記本発明の化合物のうち、とりわけ好ましい化合物としては、N−[3−(tert−ブチル)−2−ヒドロキシ−5−(2−(モルホリン−4−イル)エトキシ)フェニル](4−メチルピペラジニル)カルボキサミド、N−[3−(tert−ブチル)−2−ヒドロキシー5−(2−(モルホリン−4−イル)エトキシ)フェニル](4−(2−ヒドロキシエチル)ピペラジニル)カルボキサミド又はN−[3−(tert−ブチル)−2−ヒドロキシ−5−(2−(モルホリン−4−イル)エトキシ)フェニル]−3−(モルホリン−4−イル)プロパンアミドがあげられる。
【0012】
本発明のフェノール誘導体[I]は、遊離の形でも、また薬理的に許容し得る塩の形のいずれでも医薬用途に用いることができる。かかる薬理的に許容し得る塩としては、例えば塩酸塩、硫酸塩、臭化水素酸塩等の如き無機酸塩、酢酸塩、フマル酸塩、シュウ酸塩、マレイン酸塩、メタンスルホン酸塩、p−トルエンスルホン酸塩の如き有機酸塩等が挙げられる。また、本発明のフェノール誘導体[I]又はその薬理的に許容し得る塩には、その水和物もしくは溶媒和物をも含む。
【0013】
本発明のフェノール誘導体[I]又はその薬理的に許容し得る塩は、優れた脂質過酸化抑制作用、酸化LDL生成抑制作用、イン・ビボ(マウス)抗酸化作用、スーパーオキシドアニオン消去作用、ヒドロキシラジカル消去作用等を有し、虚血性疾患(心筋梗塞、脳梗塞、虚血再灌流時の細胞傷害、不整脈等)、動脈硬化、炎症等の各種疾患の予防・治療薬として有用である。
【0014】
本発明のフェノール誘導体[I]又はその薬理的に許容し得る塩は、経口的にも非経口的にも投与することができるが、とりわけ注射剤として非経口的(例えば、静脈内)に投与するのが好ましい。特に、本発明の化合物であるN−[3−(tert−ブチル)−2−ヒドロキシ−5−(2−(モルホリン−4−イル)エトキシ)フェニル](4−メチルピペラジニル)カルボキサミド・2塩酸塩・1/5エタノールは、水に対する溶解度が高く(>100mg/mL,pH7.4)、また、局所刺激性(細胞毒性)も低いため、注射剤等の形態での非経口投与に好適な化合物である。
【0015】
更に、本発明のフェノール誘導体[I]又はその薬理的に許容し得る塩は、薬物代謝酵素に対する非特異的阻害活性が低いため、薬物動態面でも好ましい特性を有する。
本発明のフェノール誘導体[I]又はその薬理的に許容し得る塩の投与量は、投与方法、患者の年齢、体重、状態等によっても異なるが、経口的に投与する場合、通常、1日当たり0.1〜1000mg/kg、とりわけ1〜100mg/kgとするのが好ましく、非経口的に(例えば注射剤として)投与する場合、通常、1日当たり0.01〜100mg/kg、とりわけ0.1〜10mg/kgとするのが好ましい。
【0016】
本発明のフェノール誘導体[I]は、例えば、A−1)一般式[II]:
【0017】
【化11】
【0018】
(式中、記号は前記と同一意味を表す。)
で示されるアニリン化合物又はその塩とホスゲン等価体と反応させ、次いで、該反応生成物と一般式[III]:
【0019】
【化12】
【0020】
(式中、記号は前記と同一意味をを表す。)
で示される化合物又はその塩とを反応させて一般式[I−A]:
【0021】
【化13】
【0022】
(式中、記号は前記と同一意味を有する。)
で示される化合物とするか、
B−1)化合物[II]又はその塩と一般式[IV]:
【0023】
【化14】
【0024】
(式中、Alk21は低級アルキレン基を表し、他の記号は前記と同一意味を有する。)
で示されるカルボン酸化合物またはその反応性誘導体とを反応させて一般式[I−B]:
【0025】
【化15】
【0026】
(式中、記号は前記と同一意味を表す。)
で示される化合物とするか、或いは、
C−1)化合物[II]又はその塩とアクリル酸又はその反応性誘導体とを反応させて一般式[V]:
【0027】
【化16】
【0028】
(式中、記号は前記と同一意味を有する。)
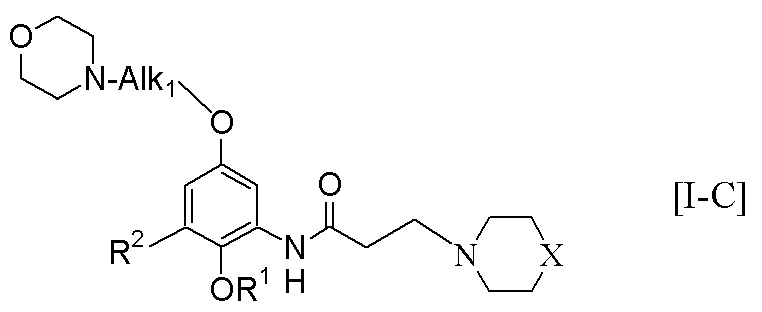
で示される化合物とし、次いで該反応生成物[V]と化合物[III]又はその塩とを反応させることにより、一般式[I−C]:
【0029】
【化17】
【0030】
(式中、記号は前記と同一意味を有する。)
で示される化合物とし、
2)上記化合物[I−A]、[I−B]又は[I−C]において、OR1が保護された水酸基である場合には、所望により該化合物から当該水酸基の保護基を除去することにより製することができる。
【0031】
上記アニリン化合物[II]および含窒素複素環式化合物[III]の塩としては、例えば、塩酸、硫酸等の如き無機酸との塩、酢酸等の如き有機酸との塩等が挙げられる。カルボン酸化合物[IV]の塩としては、例えば、ナトリウム塩等のアルカリ金属塩又はカルシウム塩等のアルカリ土類金属塩の如き無機塩基との塩等が挙げられる。
【0032】
上記本発明にかかる反応において、カルボン酸化合物[IV]は、そのカルボキシル基における反応性誘導体の形でも使用することができる。このような反応性誘導体としては、対応酸ハライド(酸クロリド等)、対応活性エステル等があげられる。
【0033】
アニリン化合物[II]又はその塩とホスゲン等価体(例えば、ホスゲン、トリホスゲン等)との反応、並びに当該反応生成物と化合物[III]又はその塩との反応は、塩基の存在下、適当な溶媒中又は無溶媒で実施することができる。本反応は、−78℃〜100℃で実施することができ、とりわけ−78℃〜30℃で好適に進行する。
【0034】
アニリン化合物[II]又はその塩とカルボン酸化合物[IV]もしくはその反応性誘導体との反応は、適当な脱水剤もしくは塩基の存在下、適当な溶媒中又は無溶媒で実施することができる。本反応は、−78℃〜100℃で実施することができ、とりわけ0℃〜30℃で好適に進行する。
【0035】
アニリン化合物[II]又はその塩とアクリル酸もしくはその反応性誘導体(例えば、その対応酸クロリド等)との反応は、適当な脱水剤もしくは塩基の存在下、適当な溶媒中又は無溶媒で実施することができる。本反応は、−78℃〜100℃で実施することができ、とりわけ0℃〜30℃で好適に進行する。
【0036】
カルボキサミド化合物[V]と化合物[III]との反応は、適当な脱水剤または塩基の存在下又は非存在下、適当な溶媒中又は無溶媒で実施することができる。溶媒としては、例えば、等が挙げられる。本反応は、−78℃〜100℃で実施することができ、とりわけ0℃〜30℃で好適に進行する。
【0037】
上記各反応において溶媒を使用する場合、当該溶媒としては、例えば、ジクロロメタン、ジメチルスルホキシド、クロロホルム、ジエチルエーテル、テトラヒドロフラン、トルエン、ベンゼン、ジオキサン、ジメチルホルムアミド、エチレングリコールジメチルエーテル、1,2−ジクロロエタン等が挙げられる。
【0038】
上記各反応において使用し得る脱水剤としては、例えば、カルボニルジイミダゾール、メタンスルホニルクロリド、ベンゾイルクロリド、ベンゼンスルホニルクロリド、ジフェニルホスホロクロリデート、光延試薬、クロロ炭酸エステル(クロロ炭酸エチル、クロロ炭酸メチル、クロロ炭酸イソブチル)等があげられる。また、塩基としては、例えば、トリエチルアミン、ジイソプロピルエチルアミン、ジメチルアニリン、ピリジン、1,8−ジアザビシクロ[5.4.0]−7−ウンデセン(DBU)、ジアザビシクロ[2.2.2]オクタン(DABCO)等があげられる。
【0039】
上記方法において、OR1が保護された水酸基である場合、当該保護基の除去は、保護基の種類に応じて、公知の方法(加水分解、酸処理、還元等)によって実施することができる。
【0040】
本発明にかかる原料化合物のうち、アニリン化合物[II]は、例えば下記反応スキームに従い、一般式[VII]で示されるフェノール化合物とp−アニシジンとを反応(ジアゾカップリング)指せ、生成物を還元することにより製することができる。
【0041】
【化18】
【0042】
(式中、記号は前記と同一意味を有する。)
なお、本発明において、低級アルキル基としては、例えばメチル基、エチル基、n−プロピル基、tert−ブチル基の如き炭素数1〜6個の直鎖又は分枝鎖アルキル基があげられ、低級アルコキシ基としては、メトキシ基、エトキシ基、プピルオキシ基等の如き炭素数1〜6個の直鎖または分枝鎖アルコキシ基があげられる。低級アルキレン基としては、例えばメチレン基、エチレン基等の如き炭素数1〜6個のアルキレン基があげられる。水酸基の保護基としては、通常、フェノール性水酸基の保護基として使用されるものが挙げられ、このような保護基としては、例えば、アルコキシアルキル基、テトラヒドロフリル基、ベンジル基等が挙げられる。このうち、好ましい保護基としては、アルコキシアルキル基が挙げられ、とりわけメトキシメチル基が挙げられる。
【0043】
以下、本発明の目的化合物[I]の具体例を示すが、これにより本発明が限定されるものではない。
【0044】
【実施例】
実施例1
(1)2−tert−ブチルヒドロキノン(96.1g)のアセトン(1L)溶液に4−(2−クロロエチル)モルホリン塩酸塩(112g)、炭酸カリウム(207g)を加え、55〜65℃で3日間攪拌する。不溶物を濾去し、濾液を濃縮後、残渣を塩酸に溶解し、酢酸エチルで洗浄する。水層に炭酸カリウムを注意深く加えて中和後、酢酸エチルで抽出し、有機層を硫酸マグネシウムで乾燥後、溶媒を留去する。これをシリカゲルカラムクロマトグラフィー(クロロホルム:酢酸エチル=1:1→1:2)にて精製し、2−(tert−ブチル)−4−(2−(モルホリン−4−イル)エトキシ)フェノール(橙色油状物、89.6g、収率53%)を得る。
IR(film): 3370、2956、1210cm-1
MS(APCI): 280(M+1)
(2) p−アニシジン(49.3g)の塩酸(2N,500ml)水溶液に5〜10℃で亜硝酸ナトリウム(30g)の水溶液(70ml)を滴下し、1時間攪拌する。この溶液を、前記(1)で得られた化合物(89.5g)の2N水酸化ナトリウム水溶液/1,4−ジオキサン混液の溶液に激しく撹拌しながら0℃で徐々に加え、その後2時間攪拌する。反応液から1,4−ジオキサンを留去し、残渣に塩酸を徐々に加えて中和した後、酢酸エチルで3回抽出する。有機層を合わせて硫酸マグネシウムで乾燥後、溶媒を留去する。残渣をシリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル=1:1→1:2)にて精製することにより、2−(tert−ブチル)−6−[(4−メトキシフェニル)ジアゼニル]−4−(2−(モルホリン−4−イル)エトキシ)フェノール(暗橙色カラメル、90.9g、収率69%)を得る。
IR(film): 3437、2958、1602、1253cm-1
MS(APCI): 414(M+1)
(3) 前記(2)で得られた化合物(90.0g)のジメチルホルムアミド(250ml)溶液に氷冷下で水素化ナトリウム(9.6g)を注意深く加え、30分攪拌する。該溶液にクロロメチルメチルエーテル(19.3g)のジメチルホルムアミド(50ml)溶液を徐々に加え、該混合物を2時間攪拌する。反応液に水を加えてクエンチした後、濃縮し、残渣にジエチルエーテルを加えて水洗する。有機層を硫酸マグネシウムで乾燥後、溶媒を留去する。残渣をシリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル=2:1→1:1→2:3)にて精製後、冷メタノールを加えて固化する。固形物を少量の冷メタノールで洗浄後、乾燥することにより、 [3−(tert−ブチル)−2−(メトキシメトキシ)−5−(2−(モルホリン−4−イル)エトキシ)フェニル](4−メトキシフェニル)ジアゼン(黄色粉末、63.4g、収率64%)を得る。
m.p.92−93℃
IR(film): 3437、2953、1599cm-1
MS(APCI): 458(M+1)
(4)前記(3)で得られた化合物(60.5g)にメタノール(250ml)を加え、窒素気流下で10%パラジウム炭素を加える。該混合物をParr接触還元装置を用いて、水素(5気圧)充填下で1日振とうする。反応液中の不溶物をセライトを用いて濾去し、濾液から溶媒を留去する。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム:酢酸エチル=4:1→クロロホルム:アセトン=5:1→2:1→1:1)で精製することにより、3−(tert−ブチル)−2−(メトキシメトキシ)−5−(2−(モルホリン−4−イル)エトキシ)フェニルアミン(橙色油状物、36.9g、収率82.6%)を得る。
IR(film): 3460、3370、2957、1595、1445、976cm-1
MS(APCI): 339(M+1)
(5)トリホスゲン(17.8g)の塩化メチレン(300ml)溶液に−78℃、窒素置換下で前記(4)で得られる化合物(27.1g)とトリエチルアミン(42ml)の塩化メチレン(100ml)溶液を3時間かけて滴下する。−78℃下で1時間攪拌後、反応液の温度を攪拌下徐々に室温まで昇温した後、濃縮する。残渣にトルエンを加えて濃縮する。残渣に塩化メチレン(300ml)を加え、0℃下で1−メチルピペラジン(15g)の塩化メチレン(100ml)溶液を20分かけて滴下し、該混合物を室温で2時間攪拌する。反応液に塩化メチレンを加え、炭酸カリウム水溶液で洗浄後、硫酸マグネシウムで乾燥し溶媒を留去する。残渣をNH−シリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル=5:1→3:1→1:1→酢酸エチル:アセトン=1:1→4:1)およびシリカゲルカラムクロマトグラフィー(アセトン:メタノール=1:0→10:1→5:1→2:1→1:1→0:1)で精製することにより、N−[3−(tert−ブチル)−2−(メトキシメトキシ)−5−(2−(モルホリン−4−イル)エトキシ)フェニル](4−メチルピペラジニル)カルボキサミド(淡黄色カラメル、30.3g、収率82%)を得る。
IR(film): 3392、2954、1668、1537、1436、1230、1058cm-1
MS(APCI): 465(M+1)
(6)前記(5)で得られる化合物(29.9g)のメタノール(150ml)溶液に0℃下で4N塩酸/酢酸エチル(150ml)をゆっくり滴下し、さらに1時間攪拌した後に反応液を濃縮する。残渣に熱エタノール(300ml)を加えて溶解し、0℃まで徐々に冷却して結晶を析出させる。結晶を濾取し、冷エタノールで洗浄後、乾燥することにより、N−[3−(tert−ブチル)−2−ヒドロキシー5−(2−(モルホリン−4−イル)エトキシ)フェニル](4−メチルピペラジニル)カルボキサミド・2塩酸塩・1/5エタノール(無色結晶、30.5g、収率94%)を得る。
m.p.147−150℃
IR(film): 3402、2957、2690、1632、1447、1272cm-1
MS(APCI): 421(M+1)
(7)上記(5)で得られる化合物(4.34g)のメタノール(80ml)溶液に、氷冷攪拌下、p−トルエンスルホン酸1水和物(6.88g)を加え、同温にて30分間、室温にて3時間攪拌する。濃縮後、残渣に酢酸エチルを加えて氷冷し、析出晶を濾取する。得られる結晶を水/エタノール混液から再結晶することにより、N−[3−(tert−ブチル)−2−ヒドロキシ−5−(2−(モルホリン−4−イル)エトキシ)フェニル](4−メチルピペラジニル)カルボキサミド・二p−トルエンスルホン酸塩(無色針状結晶、5.47g、収率77%)を得る。
IR(ATR): 1653cm-1
MS(APCI): 436(M+1)+
実施例2
(1)トリホスゲン(445mg)の塩化メチレン(10ml)溶液に−70℃、窒素置換下で、上記実施例(5)で得られる化合物(677mg)、トリエチルアミン(1.0g)及び塩化メチレン(10ml)の混合物を3時間かけて滴下する。同温で1時間攪拌後、徐々に室温まで昇温する。反応液を濃縮し、残渣にトルエンを加えて再び濃縮する。残渣に4−(2−ヒドロキシエチル)ピペラジン(1.2g)/トリエチルアミン(0.5ml)/テトラヒドロフラン(10ml)を加え、室温で4時間攪拌する。反応液にジエチルエーテルを加え、飽和重曹水及び飽和食塩水で洗浄後、硫酸マグネシウムで乾燥し、溶媒を留去する。残渣をシリカゲルカラムクロマトグラフィー(アセトン:メタノール=10:1→7:1→5:1→4:1)で精製することにより、N−[3−(tert−ブチル)−2−(メトキシメトキシ)−5−(2−(モルホリン−4−イル)エトキシ)フェニル][4−(2−ヒドロキシエチル)ピペラジニル]カルボキサミド(無色油状、377mg、収率38%)を得る。
MS(APCI): 495(M+1)+
(2)上記(1)で得られる化合物(340mg)/メタノール(10ml)に0℃下で4N塩酸/酢酸エチル(10ml)を加え、同温で4時間攪拌した後に反応液を濃縮する。残渣にエタノールを加えて溶解し、該溶液を、激しく撹拌しながら酢酸エチル中へ加える。生じた固体を濾取することにより、N−[3−(tert−ブチル)−2−ヒドロキシ−5−(2−(モルホリン−4−イル)エトキシ)フェニル[4−(2−ヒドロキシエチル)ピペラジニル]カルボキサミド・二塩酸塩(無色粉末、313mg、収率87%)を得る。
MS(APCI): 451(M+1)+
実施例3
(1)3−(tert−ブチル)−2−(メトキシメトキシ)−5−(2−(モルホリン−4−イル)エトキシ)フェニルアミン(3g)、トリエチルアミン(1.85ml)及びテトラヒドロフラン(20ml)の混合物に、氷冷攪拌下、塩化アクリロイル(959mg)のテトラヒドロフラン(10ml)溶液を約5分間で滴下する。該混合物を同温で30分間撹拌後、室温で終夜撹拌する。反応混合物に飽和重曹水、ジエチルエーテルを加えて分液し、有機層を水(2回)、飽和食塩水にて洗浄後、無水硫酸ナトリウムで乾燥する。該有機層を濃縮後、残渣をNH−シリカゲルカラムクロマトグラフィー(クロロホルム→クロロホルム:アセトン=4:1)で精製することにより、N−[3−(tert−ブチル)−2−(メトキシメトキシ)−5−(2−(モルホリンー4−イル)エトキシ)フェニル]プロプ−2−エナミド(淡黄色油状、2.2g、収率63%)を得る。
IR(ATR):1691、1738cm-1
MS(APCI):363(M+1)+
(2)上記(1)で得られる化合物(2.1g)にモルホリン(2.8g)を加え、60℃で2時間攪拌する。反応混合物に飽和重曹水、ジエチルエーテルを加え分液し、有機層を水(3回)、飽和食塩水で洗浄後、無水硫酸ナトリウムにて乾燥する。該有機層を濃縮後、残渣をNH−シリカゲルカラムクロマトグラフィー(ヘキサン→ヘキサン:酢酸エチル=5:1→4:1→2:1)にて精製することにより、N−[3−(tert−ブチル)−2−(メトキシメトキシ)−5−(2−(モルホリン−4−イル)エトキシ)フェニル]−3−モルホリン−4−イルプロパンアミド(淡黄色油状、1.72g、収率63%)を得る。
IR(ART):1694cm-1
MS(APCI):480(M+1)+
(3)上記(2)で得られる化合物(1.58g)のメタノール(5ml)溶液に、氷冷攪拌下、4N塩酸/酢酸エチル(20ml)を加え、同温にて1時間攪拌する。反応混合物を濃縮後、残渣にイソプロパノールを加え、さらに濃縮する。得られる残渣をエタノール-イソプロパノールに溶解し、該溶液をジエチルエーテル中へ加える。該溶液にジイソプロピルエーテルを添加し、生じた不溶物を濾取することにより、N−[3−(tert−ブチル)−2−ヒドロキシ−5−(2−(モルホリン−4−イル)エトキシ)フェニル]−3−モルホリン−4−イルプロパンアミド・二塩酸塩(灰白色粉末、1.60g、収率96%)を得る。IR(ART): 1651cm-1
MS(APCI): 436(M+1)+ [0001]
BACKGROUND OF THE INVENTION
The present invention relates to a novel phenol compound having an excellent antioxidant action.
[0002]
[Prior art]
Although the mechanism of cell membrane damage (including cell death) in the development of ischemic diseases has not yet been elucidated, the active oxygen production plays an important role in this cytotoxic process. It is believed that. It is also known that active oxygen causes not only lipid peroxidation but also enzyme and protein denaturation, nucleic acid damage, and the like, which cause various organ damages. For example, if a myocardial infarction due to coronary artery occlusion develops, it tends to cause serious symptoms such as cardiogenic shock and fatal arrhythmia, so reperfusion for the purpose of resuming blood flow at the infarct site as the initial treatment Therapies (thrombolytic therapy, percutaneous coronary angioplasty (PTCA), coronary artery bypass surgery (CABG), etc.) are often performed. However, in this case, myocardial tissue damage is often aggravated (ischemia / reperfusion injury) by restarting blood circulation. As one of the onset mechanisms of this ischemia / reperfusion injury, the involvement of active oxygen has been reported. Oxygen radicals generated during reperfusion cause reperfusion arrhythmia, resulting in cell damage and enzymes associated with ATP production disorder. It is thought that myocardial damage is caused by cell membrane destruction accompanying increased protein activity.
[0003]
On the other hand, examples of the compound having a radical scavenging action and an antioxidant action include 2- [4- (4-aminophenyl) piperazin-1-yl] amide-4 described in JP-A-10-195037 or JP-A-9-278874. Phenol compounds such as -methoxy-6-tert-butylphenol and 2- (2-phenyl-1-cyclohexylethylcarbonylamino) -4-methoxy-6-tert-butylphenol are disclosed. However, in the drug treatment of ischemic diseases, a drug that can be effectively and safely administered as an injection is particularly desired. However, the known phenol derivative has properties suitable as an injection in terms of solubility and other aspects. It is hard to say. For this reason, it has been necessary to find a drug that has not only an excellent antioxidant action but also suitable characteristics as an injectable drug.
[0004]
[Problems to be solved by the invention]
The present invention provides a novel phenolic compound having excellent antioxidant action and suitable characteristics as an injection, and useful for the prevention and treatment of cell damage and arrhythmia during myocardial infarction or ischemia / reperfusion. It is to provide. The present invention also provides a method for producing such a novel phenol compound.
[0005]
[Means for Solving the Problems]
The present invention relates to general formula [I]:
[0006]
[Chemical Formula 10]
[0007]
(In the formula, OR 1 is an optionally protected hydroxyl group, R 2 is a lower alkyl group, Alk 1 is a lower alkylene group, Alk 2 is a single bond or a lower alkylene group, X is an oxygen atom or a lower alkyl group, and hydroxy. It represents an imino group which may be substituted with a group selected from lower alkyl groups.)
Or a pharmacologically acceptable salt thereof.
[0008]
DETAILED DESCRIPTION OF THE INVENTION
As specific examples of the phenol derivative [I] of the present invention, for example, in the general formula [I], OR 1 may be a hydroxyl group which may be protected by a lower alkoxy lower alkyl group, and R 2 may have 1 to 4 carbon atoms. An alkyl group, Alk 1 is an alkylene group having 1 to 4 carbon atoms, Alk 2 is a single bond or an alkylene group having 1 to 4 carbon atoms, X is a group selected from an oxygen atom or a lower alkyl group and a hydroxy lower alkyl group And a compound which is an imino group substituted with.
[0009]
Among the above, preferred compounds include, for example, in the general formula [I], OR 1 is a hydroxyl group or a methoxymethoxy group, R 2 is a tert-butyl group, Alk 1 is a methylene group or an ethylene group, and Alk 2 is a single bond. Or the compound which is an imino group substituted by ethylene group and group in which X is selected from an oxygen atom or a methyl group, and a hydroxyethyl group is mentioned.
[0010]
More preferable compounds include, for example, in the general formula [I], OR 1 is a hydroxyl group, R 2 is a tert-butyl group, Alk 1 is an ethylene group, Alk 2 is a single bond or an ethylene group, X is an oxygen atom, methylimino And a compound which is a 2-hydroxyethylimino group.
[0011]
Among the compounds of the present invention, particularly preferable compounds include N- [3- (tert-butyl) -2-hydroxy-5- (2- (morpholin-4-yl) ethoxy) phenyl] (4-methylpipe Razinyl) carboxamide, N- [3- (tert-butyl) -2-hydroxy-5- (2- (morpholin-4-yl) ethoxy) phenyl] (4- (2-hydroxyethyl) piperazinyl) carboxamide or N- [3- (tert-butyl) -2-hydroxy-5- (2- (morpholin-4-yl) ethoxy) phenyl] -3- (morpholin-4-yl) propanamide.
[0012]
The phenol derivative [I] of the present invention can be used for pharmaceutical use either in a free form or in the form of a pharmacologically acceptable salt. Examples of such pharmacologically acceptable salts include inorganic acid salts such as hydrochloride, sulfate, hydrobromide, acetate, fumarate, oxalate, maleate, methanesulfonate, Examples thereof include organic acid salts such as p-toluenesulfonate. In addition, the phenol derivative [I] of the present invention or a pharmaceutically acceptable salt thereof includes a hydrate or a solvate thereof.
[0013]
The phenol derivative [I] of the present invention or a pharmacologically acceptable salt thereof has an excellent lipid peroxidation inhibitory action, oxidized LDL production inhibitory action, in vivo (mouse) antioxidant action, superoxide anion scavenging action, hydroxy It has a radical scavenging action and the like, and is useful as a prophylactic / therapeutic agent for various diseases such as ischemic diseases (myocardial infarction, cerebral infarction, cell injury during ischemia reperfusion, arrhythmia, etc.), arteriosclerosis, inflammation and the like.
[0014]
The phenol derivative [I] or a pharmacologically acceptable salt thereof of the present invention can be administered orally or parenterally, but is administered parenterally (for example, intravenously), particularly as an injection. It is preferable to do this. In particular, N- [3- (tert-butyl) -2-hydroxy-5- (2- (morpholin-4-yl) ethoxy) phenyl] (4-methylpiperazinyl) carboxamide 2 Hydrochloride / 1/5 ethanol has high solubility in water (> 100 mg / mL, pH 7.4) and low local irritation (cytotoxicity), suitable for parenteral administration in the form of injections Compound.
[0015]
Furthermore, since the phenol derivative [I] of the present invention or a pharmacologically acceptable salt thereof has a low non-specific inhibitory activity against drug-metabolizing enzymes, it has favorable characteristics in terms of pharmacokinetics.
The dosage of the phenol derivative [I] of the present invention or a pharmacologically acceptable salt thereof varies depending on the administration method, patient age, weight, condition, etc., but when administered orally, it is usually 0 per day. .1 to 1000 mg / kg, preferably 1 to 100 mg / kg, and when administered parenterally (for example, as an injection), usually 0.01 to 100 mg / kg per day, especially 0.1 to 100 mg / kg 10 mg / kg is preferable.
[0016]
The phenol derivative [I] of the present invention includes, for example, A-1) general formula [II]:
[0017]
Embedded image
[0018]
(In the formula, the symbols have the same meaning as described above.)
Is reacted with a phosgene equivalent, and the reaction product is then reacted with the general formula [III]:
[0019]
Embedded image
[0020]
(Wherein the symbols have the same meaning as described above.)
And a compound represented by the general formula [IA]:
[0021]
Embedded image
[0022]
(In the formula, the symbols have the same meaning as described above.)
Or a compound represented by
B-1) Compound [II] or a salt thereof and general formula [IV]:
[0023]
Embedded image
[0024]
(In the formula, Alk 21 represents a lower alkylene group, and other symbols have the same meanings as described above.)
Is reacted with a carboxylic acid compound represented by the general formula [IB]:
[0025]
Embedded image
[0026]
(In the formula, the symbols have the same meaning as described above.)
Or a compound represented by
C-1) Compound [II] or a salt thereof and acrylic acid or a reactive derivative thereof are reacted to form a general formula [V]:
[0027]
Embedded image
[0028]
(In the formula, the symbols have the same meaning as described above.)
And then reacting the reaction product [V] with the compound [III] or a salt thereof, to obtain a compound represented by the general formula [IC]:
[0029]
Embedded image
[0030]
(In the formula, the symbols have the same meaning as described above.)
A compound represented by
2) In the above compound [IA], [IB] or [IC], when OR 1 is a protected hydroxyl group, the protecting group for the hydroxyl group is optionally removed from the compound. Can be manufactured.
[0031]
Examples of the salts of the aniline compound [II] and the nitrogen-containing heterocyclic compound [III] include salts with inorganic acids such as hydrochloric acid and sulfuric acid, salts with organic acids such as acetic acid, and the like. Examples of the salt of the carboxylic acid compound [IV] include salts with inorganic bases such as alkali metal salts such as sodium salts or alkaline earth metal salts such as calcium salts.
[0032]
In the reaction according to the present invention, the carboxylic acid compound [IV] can also be used in the form of a reactive derivative at the carboxyl group. Examples of such reactive derivatives include corresponding acid halides (acid chlorides, etc.), corresponding active esters, and the like.
[0033]
The reaction of the aniline compound [II] or a salt thereof with a phosgene equivalent (for example, phosgene, triphosgene, etc.), and the reaction of the reaction product with the compound [III] or a salt thereof are carried out in a suitable solvent in the presence of a base. It can be carried out in the middle or without solvent. This reaction can be carried out at −78 ° C. to 100 ° C., and particularly preferably proceeds at −78 ° C. to 30 ° C.
[0034]
The reaction of aniline compound [II] or a salt thereof and carboxylic acid compound [IV] or a reactive derivative thereof can be carried out in the presence of a suitable dehydrating agent or base, in a suitable solvent or without solvent. This reaction can be carried out at −78 ° C. to 100 ° C., and particularly preferably proceeds at 0 ° C. to 30 ° C.
[0035]
The reaction of aniline compound [II] or a salt thereof and acrylic acid or a reactive derivative thereof (for example, a corresponding acid chloride thereof) is carried out in a suitable solvent or without solvent in the presence of a suitable dehydrating agent or base. be able to. This reaction can be carried out at −78 ° C. to 100 ° C., and particularly preferably proceeds at 0 ° C. to 30 ° C.
[0036]
The reaction between the carboxamide compound [V] and the compound [III] can be carried out in a suitable solvent or without a solvent in the presence or absence of a suitable dehydrating agent or base. Examples of the solvent include, for example. This reaction can be carried out at −78 ° C. to 100 ° C., and particularly preferably proceeds at 0 ° C. to 30 ° C.
[0037]
When a solvent is used in each of the above reactions, examples of the solvent include dichloromethane, dimethyl sulfoxide, chloroform, diethyl ether, tetrahydrofuran, toluene, benzene, dioxane, dimethylformamide, ethylene glycol dimethyl ether, 1,2-dichloroethane, and the like. It is done.
[0038]
Examples of the dehydrating agent that can be used in each of the above reactions include carbonyldiimidazole, methanesulfonyl chloride, benzoyl chloride, benzenesulfonyl chloride, diphenylphosphorochloridate, Mitsunobu reagent, chlorocarbonate (ethyl chlorocarbonate, methyl chlorocarbonate, Isobutyl chlorocarbonate) and the like. Examples of the base include triethylamine, diisopropylethylamine, dimethylaniline, pyridine, 1,8-diazabicyclo [5.4.0] -7-undecene (DBU), diazabicyclo [2.2.2] octane (DABCO). Etc.
[0039]
In the above method, when OR 1 is a protected hydroxyl group, the protective group can be removed by a known method (hydrolysis, acid treatment, reduction, etc.) depending on the type of the protective group.
[0040]
Of the raw material compounds according to the present invention, the aniline compound [II] refers to the reaction of the phenol compound represented by the general formula [VII] with p-anisidine (diazo coupling), for example, according to the following reaction scheme, and reduces the product. Can be manufactured.
[0041]
Embedded image
[0042]
(In the formula, the symbols have the same meaning as described above.)
In the present invention, examples of the lower alkyl group include linear or branched alkyl groups having 1 to 6 carbon atoms such as a methyl group, an ethyl group, an n-propyl group, and a tert-butyl group. Examples of the alkoxy group include linear or branched alkoxy groups having 1 to 6 carbon atoms such as a methoxy group, an ethoxy group, and a propyloxy group. Examples of the lower alkylene group include alkylene groups having 1 to 6 carbon atoms such as a methylene group and an ethylene group. Examples of the hydroxyl-protecting group include those usually used as a phenolic hydroxyl-protecting group. Examples of such a protecting group include an alkoxyalkyl group, a tetrahydrofuryl group, and a benzyl group. Among these, a preferable protecting group includes an alkoxyalkyl group, and particularly a methoxymethyl group.
[0043]
Specific examples of the target compound [I] of the present invention are shown below, but the present invention is not limited thereby.
[0044]
【Example】
Example 1
(1) 4- (2-Chloroethyl) morpholine hydrochloride (112 g) and potassium carbonate (207 g) were added to a solution of 2-tert-butylhydroquinone (96.1 g) in acetone (1 L) at 55 to 65 ° C. for 3 days. Stir. The insoluble material is removed by filtration, and the filtrate is concentrated. The residue is dissolved in hydrochloric acid and washed with ethyl acetate. The aqueous layer is carefully neutralized with potassium carbonate, extracted with ethyl acetate, the organic layer is dried over magnesium sulfate, and the solvent is distilled off. This was purified by silica gel column chromatography (chloroform: ethyl acetate = 1: 1 → 1: 2) to give 2- (tert-butyl) -4- (2- (morpholin-4-yl) ethoxy) phenol (orange) An oil, 89.6 g, 53% yield) is obtained.
IR (film): 3370, 2956, 1210 cm −1
MS (APCI): 280 (M + 1)
(2) An aqueous solution (70 ml) of sodium nitrite (30 g) is added dropwise to an aqueous solution of p-anisidine (49.3 g) in hydrochloric acid (2N, 500 ml) at 5 to 10 ° C. and stirred for 1 hour. This solution is gradually added to a solution of the compound (89.5 g) obtained in (1) above in a 2N aqueous solution of sodium hydroxide / 1,4-dioxane at 0 ° C. with vigorous stirring, and then stirred for 2 hours. . 1,4-Dioxane is distilled off from the reaction solution, and hydrochloric acid is gradually added to the residue for neutralization, followed by extraction three times with ethyl acetate. The organic layers are combined and dried over magnesium sulfate, and then the solvent is distilled off. The residue was purified by silica gel column chromatography (hexane: ethyl acetate = 1: 1 → 1: 2) to give 2- (tert-butyl) -6-[(4-methoxyphenyl) diazenyl] -4- ( 2- (Morpholin-4-yl) ethoxy) phenol (dark orange caramel, 90.9 g, 69% yield) is obtained.
IR (film): 3437, 2958, 1602, 1253 cm −1
MS (APCI): 414 (M + 1)
(3) Sodium hydride (9.6 g) is carefully added to a solution of the compound (90.0 g) obtained in (2) above in dimethylformamide (250 ml) under ice cooling, and the mixture is stirred for 30 minutes. To this solution is slowly added a solution of chloromethyl methyl ether (19.3 g) in dimethylformamide (50 ml) and the mixture is stirred for 2 hours. The reaction mixture is quenched by adding water, and concentrated, and diethyl ether is added to the residue and washed with water. The organic layer is dried over magnesium sulfate and the solvent is distilled off. The residue is purified by silica gel column chromatography (hexane: ethyl acetate = 2: 1 → 1: 1 → 2: 3), and then solidified by adding cold methanol. The solid was washed with a small amount of cold methanol and dried to give [3- (tert-butyl) -2- (methoxymethoxy) -5- (2- (morpholin-4-yl) ethoxy) phenyl] (4 -Methoxyphenyl) diazene (yellow powder, 63.4 g, 64% yield) is obtained.
m. p. 92-93 ° C
IR (film): 3437, 2953, 1599 cm −1
MS (APCI): 458 (M + 1)
(4) Methanol (250 ml) is added to the compound (60.5 g) obtained in (3) above, and 10% palladium carbon is added under a nitrogen stream. The mixture is shaken using a Parr catalytic reduction apparatus for 1 day under hydrogen (5 atm) charge. Insoluble matters in the reaction solution are filtered off using Celite, and the solvent is distilled off from the filtrate. The residue was purified by silica gel column chromatography (chloroform: ethyl acetate = 4: 1 → chloroform: acetone = 5: 1 → 2: 1 → 1: 1) to give 3- (tert-butyl) -2- (methoxy Methoxy) -5- (2- (morpholin-4-yl) ethoxy) phenylamine (orange oil, 36.9 g, 82.6% yield) is obtained.
IR (film): 3460, 3370, 2957, 1595, 1445, 976 cm −1
MS (APCI): 339 (M + 1)
(5) A solution of triphosgene (17.8 g) in methylene chloride (300 ml) at −78 ° C. under nitrogen substitution with the compound (27.1 g) obtained in the above (4) and triethylamine (42 ml) in methylene chloride (100 ml) Is added dropwise over 3 hours. After stirring at −78 ° C. for 1 hour, the temperature of the reaction solution is gradually raised to room temperature with stirring and then concentrated. Add toluene to the residue and concentrate. Methylene chloride (300 ml) is added to the residue, a solution of 1-methylpiperazine (15 g) in methylene chloride (100 ml) is added dropwise at 0 ° C. over 20 minutes, and the mixture is stirred at room temperature for 2 hours. Methylene chloride is added to the reaction solution, washed with an aqueous potassium carbonate solution, dried over magnesium sulfate, and the solvent is distilled off. The residue was subjected to NH-silica gel column chromatography (hexane: ethyl acetate = 5: 1 → 3: 1 → 1: 1 → ethyl acetate: acetone = 1: 1 → 4: 1) and silica gel column chromatography (acetone: methanol = 1). : 0 → 10: 1 → 5: 1 → 2: 1 → 1: 1 → 0: 1) to give N- [3- (tert-butyl) -2- (methoxymethoxy) -5- ( 2- (morpholin-4-yl) ethoxy) phenyl] (4-methylpiperazinyl) carboxamide (light yellow caramel, 30.3 g, 82% yield) is obtained.
IR (film): 3392, 2954, 1668, 1537, 1436, 1230, 1058 cm −1
MS (APCI): 465 (M + 1)
(6) To a solution of the compound (29.9 g) obtained in (5) above in methanol (150 ml), 4N hydrochloric acid / ethyl acetate (150 ml) was slowly added dropwise at 0 ° C., followed by further stirring for 1 hour, and then the reaction solution was concentrated. To do. Hot ethanol (300 ml) is added to the residue to dissolve it, and it is gradually cooled to 0 ° C. to precipitate crystals. The crystals were collected by filtration, washed with cold ethanol, and dried to give N- [3- (tert-butyl) -2-hydroxy-5- (2- (morpholin-4-yl) ethoxy) phenyl] (4- Methylpiperazinyl) carboxamide dihydrochloride 1/5 ethanol (colorless crystals, 30.5 g, 94% yield) is obtained.
m. p. 147-150 ° C
IR (film): 3402, 2957, 2690, 1632, 1447, 1272 cm −1
MS (APCI): 421 (M + 1)
(7) To a solution of the compound (4.34 g) obtained in (5) above in methanol (80 ml), p-toluenesulfonic acid monohydrate (6.88 g) was added with stirring under ice-cooling, and at the same temperature. Stir for 30 minutes at room temperature for 3 hours. After concentration, ethyl acetate is added to the residue and the mixture is cooled with ice, and the precipitated crystals are collected by filtration. The resulting crystals are recrystallized from a water / ethanol mixture to give N- [3- (tert-butyl) -2-hydroxy-5- (2- (morpholin-4-yl) ethoxy) phenyl] (4-methyl Piperazinyl) carboxamide di-p-toluenesulfonate (colorless needles, 5.47 g, 77% yield) is obtained.
IR (ATR): 1653 cm -1
MS (APCI): 436 (M + 1) +
Example 2
(1) A compound obtained in Example (5) (677 mg), triethylamine (1.0 g) and methylene chloride (10 ml) in a solution of triphosgene (445 mg) in methylene chloride (10 ml) at -70 ° C. under nitrogen substitution. Is added dropwise over 3 hours. After stirring for 1 hour at the same temperature, the temperature is gradually raised to room temperature. The reaction mixture is concentrated, toluene is added to the residue, and the mixture is concentrated again. 4- (2-Hydroxyethyl) piperazine (1.2 g) / triethylamine (0.5 ml) / tetrahydrofuran (10 ml) is added to the residue and stirred at room temperature for 4 hours. Diethyl ether is added to the reaction mixture, washed with saturated aqueous sodium hydrogen carbonate and saturated brine, dried over magnesium sulfate, and the solvent is evaporated. The residue was purified by silica gel column chromatography (acetone: methanol = 10: 1 → 7: 1 → 5: 1 → 4: 1) to give N- [3- (tert-butyl) -2- (methoxymethoxy). -5- (2- (morpholin-4-yl) ethoxy) phenyl] [4- (2-hydroxyethyl) piperazinyl] carboxamide (colorless oil, 377 mg, 38% yield) is obtained.
MS (APCI): 495 (M + 1) +
(2) To the compound (340 mg) / methanol (10 ml) obtained in (1) above is added 4N hydrochloric acid / ethyl acetate (10 ml) at 0 ° C., and the mixture is stirred at the same temperature for 4 hours, and then the reaction mixture is concentrated. Ethanol is added to the residue to dissolve, and the solution is added into ethyl acetate with vigorous stirring. The resulting solid was collected by filtration to give N- [3- (tert-butyl) -2-hydroxy-5- (2- (morpholin-4-yl) ethoxy) phenyl [4- (2-hydroxyethyl) piperazinyl ] Carboxamide dihydrochloride (colorless powder, 313 mg, yield 87%) is obtained.
MS (APCI): 451 (M + 1) +
Example 3
(1) 3- (tert-butyl) -2- (methoxymethoxy) -5- (2- (morpholin-4-yl) ethoxy) phenylamine (3 g), triethylamine (1.85 ml) and tetrahydrofuran (20 ml) To the mixture, a solution of acryloyl chloride (959 mg) in tetrahydrofuran (10 ml) is added dropwise over about 5 minutes with ice cooling. The mixture is stirred at the same temperature for 30 minutes and then at room temperature overnight. To the reaction mixture are added a saturated aqueous sodium bicarbonate solution and diethyl ether, and the mixture is separated, and the organic layer is washed with water (twice) and saturated brine, and dried over anhydrous sodium sulfate. The organic layer was concentrated, and the residue was purified by NH-silica gel column chromatography (chloroform → chloroform: acetone = 4: 1) to give N- [3- (tert-butyl) -2- (methoxymethoxy)- 5- (2- (morpholin-4-yl) ethoxy) phenyl] prop-2-enamide (pale yellow oil, 2.2 g, 63% yield) is obtained.
IR (ATR): 1691, 1738 cm −1
MS (APCI): 363 (M + 1) +
(2) Add morpholine (2.8 g) to the compound (2.1 g) obtained in (1) above and stir at 60 ° C. for 2 hours. To the reaction mixture are added a saturated aqueous sodium bicarbonate solution and diethyl ether, and the mixture is separated, and the organic layer is washed with water (3 times) and saturated brine, and dried over anhydrous sodium sulfate. The organic layer was concentrated, and the residue was purified by NH-silica gel column chromatography (hexane → hexane: ethyl acetate = 5: 1 → 4: 1 → 2: 1) to give N- [3- (tert- Butyl) -2- (methoxymethoxy) -5- (2- (morpholin-4-yl) ethoxy) phenyl] -3-morpholin-4-ylpropanamide (pale yellow oil, 1.72 g, 63% yield) Get.
IR (ART): 1694 cm −1
MS (APCI): 480 (M + 1) +
(3) To a methanol (5 ml) solution of the compound (1.58 g) obtained in (2) above, 4N hydrochloric acid / ethyl acetate (20 ml) is added under ice-cooling and stirring, and the mixture is stirred at the same temperature for 1 hour. After the reaction mixture is concentrated, isopropanol is added to the residue and the mixture is further concentrated. The resulting residue is dissolved in ethanol-isopropanol and the solution is added into diethyl ether. Diisopropyl ether was added to the solution, and the resulting insoluble material was collected by filtration to give N- [3- (tert-butyl) -2-hydroxy-5- (2- (morpholin-4-yl) ethoxy) phenyl. ] -3-morpholin-4-ylpropanamide dihydrochloride (off-white powder, 1.60 g, 96% yield) is obtained. IR (ART): 1651 cm -1
MS (APCI): 436 (M + 1) +
Claims (8)
で示されるフェノール化合物又はその薬理的に許容し得る塩。Formula [I]:
Or a pharmacologically acceptable salt thereof.
で示されるアニリン化合物又はその塩とホスゲン等価体と反応させ、次いで、該反応生成物と一般式[III]:
で示される化合物又はその塩とを反応させて一般式[I−A]:
で示される化合物とするか、
B−1)化合物[II]又はその塩と一般式[IV]:
で示されるカルボン酸化合物またはその反応性誘導体とを反応させて一般式[I−B]:
で示される化合物とするか、或いは、
C−1)化合物[II]又はその塩とアクリル酸又はその反応性誘導体とを反応させることにより一般式[V]:
で示される化合物とし、次いで該反応生成物[V]と化合物[III]又はその塩とを反応させることにより、一般式[I−C]:
で示される化合物とし、
2)上記化合物[I−A]、[I−B]又は[I−C]においてOR1が保護された水酸基である場合には、所望により該化合物から当該水酸基の保護基を除去することを特徴とする一般式[I]:
で示されるフェノール化合物又はその薬理的に許容し得る塩の製法。A-1) General formula [II]:
Is reacted with a phosgene equivalent, and the reaction product is then reacted with the general formula [III]:
And a compound represented by the general formula [IA]:
Or a compound represented by
B-1) Compound [II] or a salt thereof and general formula [IV]:
Is reacted with a carboxylic acid compound represented by the general formula [IB]:
Or a compound represented by
C-1) By reacting compound [II] or a salt thereof with acrylic acid or a reactive derivative thereof, general formula [V]:
And then reacting the reaction product [V] with the compound [III] or a salt thereof, to obtain a compound represented by the general formula [IC]:
A compound represented by
2) When OR 1 is a protected hydroxyl group in the above compound [IA], [IB] or [IC], the protecting group for the hydroxyl group may be removed from the compound as desired. General formula [I] characterized:
Or a pharmacologically acceptable salt thereof.
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002228230A JP2005298345A (en) | 2002-08-06 | 2002-08-06 | Phenol compound and process for producing the same |
| TW092108617A TW200307551A (en) | 2002-04-16 | 2003-04-15 | Phenol compound, process for preparing the same and synthetic intermediate thereof |
| PCT/JP2003/004798 WO2003087074A1 (en) | 2002-04-16 | 2003-04-16 | Phenol compound, process for producing the same, and intermediate therefor |
| AU2003235169A AU2003235169A1 (en) | 2002-04-16 | 2003-04-16 | Phenol compound, process for producing the same, and intermediate therefor |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002228230A JP2005298345A (en) | 2002-08-06 | 2002-08-06 | Phenol compound and process for producing the same |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005298345A true JP2005298345A (en) | 2005-10-27 |
Family
ID=35330329
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002228230A Pending JP2005298345A (en) | 2002-04-16 | 2002-08-06 | Phenol compound and process for producing the same |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005298345A (en) |
-
2002
- 2002-08-06 JP JP2002228230A patent/JP2005298345A/en active Pending
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8377949B2 (en) | Quinazolinedione chymase inhibitors | |
| EP0513379A1 (en) | 2-arylthiazole derivative and pharmaceutical composition containing the same | |
| CN101641358A (en) | Aza-pyridopyrimidinone derivatives | |
| EA022076B1 (en) | Hexafluoroisopropyl carbamate derivatives, their preparation and their therapeutic application | |
| WO2008071421A1 (en) | Nitrate esters of carbonic anhydrase inhibitors | |
| JPH10510536A (en) | 2-Substituted 1,2,5-thiadiazolidine-3-one 1,1-dioxides and compositions thereof | |
| EA035576B1 (en) | 1,2-naphthoquinone derivative and method for preparing same | |
| HUE031506T2 (en) | Aldose reductase inhibitors and uses thereof | |
| WO2006098342A1 (en) | Piperazinyl compounds | |
| MX2011007991A (en) | Thiadiazole and oxadiazole derivatives, preparation thereof, and therapeutic use thereof. | |
| WO2004113345A1 (en) | Fused pyrrole compound and medicinal use thereof | |
| EP2733144B1 (en) | Novel compound having parp inhibitory activity | |
| EA029745B1 (en) | Fused imidazobenzothiazole compounds | |
| WO2016034137A1 (en) | Pyrazolo[3,4-c]pyridine derivatives | |
| EP2253632A1 (en) | Pyrazolopyramidinone derivatives, their preparation and their use | |
| CZ296266B6 (en) | 5-Substituted 1,2,4-thiadiazolyl derivative, process and intermediate for its preparation, its use and pharmaceutical composition in which the derivative is comprised | |
| TW202045515A (en) | Ester compound | |
| US20030130325A1 (en) | Substituted tryptophan derivatives | |
| WO2020153434A1 (en) | Pyrazole compound | |
| JPH0753500A (en) | Guanidinobenzoic acid derivative and protease inhibitor with the same as active ingredient | |
| CN114671856B (en) | Polysubstituted uracil derivative and use thereof | |
| JP2005298345A (en) | Phenol compound and process for producing the same | |
| JPWO1998042680A1 (en) | Novel anilide compound and medicine containing the same | |
| CN114539237A (en) | IDO inhibitor, preparation method, pharmaceutical composition and application | |
| WO2022135534A1 (en) | Substituted nitrogen-containing bicyclic compound and use thereof |