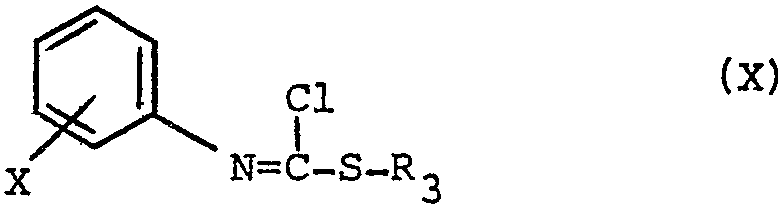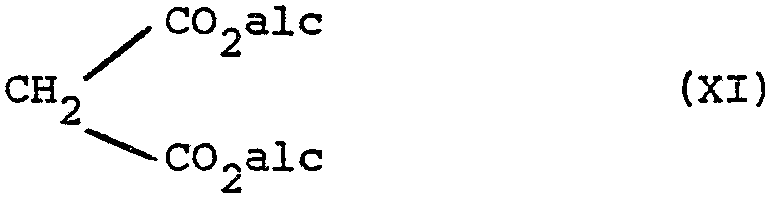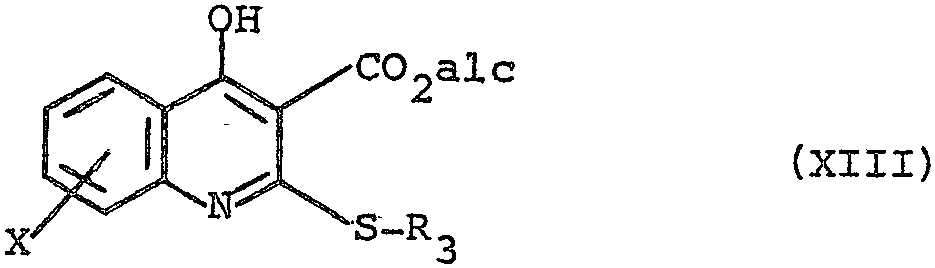FR2532939A1 - New 4-hydroxy-3-quinolinecarboxylic acid derivatives substituted at position 2, their preparation, their use as medicaments, compositions containing them and new intermediates obtained - Google Patents
New 4-hydroxy-3-quinolinecarboxylic acid derivatives substituted at position 2, their preparation, their use as medicaments, compositions containing them and new intermediates obtained Download PDFInfo
- Publication number
- FR2532939A1 FR2532939A1 FR8215423A FR8215423A FR2532939A1 FR 2532939 A1 FR2532939 A1 FR 2532939A1 FR 8215423 A FR8215423 A FR 8215423A FR 8215423 A FR8215423 A FR 8215423A FR 2532939 A1 FR2532939 A1 FR 2532939A1
- Authority
- FR
- France
- Prior art keywords
- formula
- products
- radical
- compound
- acids
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D265/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom and one oxygen atom as the only ring hetero atoms
- C07D265/04—1,3-Oxazines; Hydrogenated 1,3-oxazines
- C07D265/12—1,3-Oxazines; Hydrogenated 1,3-oxazines condensed with carbocyclic rings or ring systems
- C07D265/14—1,3-Oxazines; Hydrogenated 1,3-oxazines condensed with carbocyclic rings or ring systems condensed with one six-membered ring
- C07D265/20—1,3-Oxazines; Hydrogenated 1,3-oxazines condensed with carbocyclic rings or ring systems condensed with one six-membered ring with hetero atoms directly attached in position 4
- C07D265/22—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D215/00—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems
- C07D215/02—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom
- C07D215/16—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D215/48—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen
- C07D215/54—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen attached in position 3
- C07D215/56—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen attached in position 3 with oxygen atoms in position 4
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/32—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D277/38—Nitrogen atoms
- C07D277/44—Acylated amino or imino radicals
- C07D277/46—Acylated amino or imino radicals by carboxylic acids, or sulfur or nitrogen analogues thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
La présente invention concerne de nouveaux dérivés de l'acide 4-hydroxy 3-quinoléine carboxylique substitués en 2, leur procédé de préparation, leur application comme médicaments, les compositions les renfermant et les nouveaux intermédiaires obtenus. The present invention relates to new derivatives of 4-hydroxy 3-quinoline carboxylic acid substituted in 2, their preparation process, their application as medicaments, the compositions containing them and the new intermediates obtained.
L'invention a pour objet les- composés de formule < I)
dans laquelle X, en position 5, 6, 7 ou 8, représente un atome d'hydrogène, un atome d'halogène, un radical alcoyle linéaire ou ramifié, renfermant de 1 à 5 atomes de carbone, un radical alcoxy linéaire ou ramifié renfermant de 1 à 4 atomes de carbone, un radical trifluorométhyle, un radical trifluorométhylthio,ou un radical trifluorométhoxy, R1 représente un atome d'hydrogène, ou un radical alcoyle renfermant de 1 à 4 atomes de carbone, R2 représente un radical choisi parmi les radicaux thiazolyle, 4,5dihydrothiazolyle, pyridinyle, oxazolyle, isoxazolyle, imidazolyle, pyrimidyle et tétrazolyle, éventuellement substitués par un radical alcoyle renfermant de 1 à 4 atomes de carbone ou R2 représente un radical phényle, éventuellement substitué par au moins un radical choisi dans le groupe formé par les radicaux hydroxyt les radicaux alcoyles renfermant de 1 à 4 atomes de carbone, les radicaux alcoxy renfermant de 1 à 4 atomes de carbone, le radical trifluorométhyle, le radical nitro et les atomes d'halogène, m représente un nombre entier pouvant varier de O à 7, n represente 0, 1 ou 2, R3 un radical alcoyle linéaire ou ramifié renfermant de 1à 5 atomes de carbone, ainsi que les sels d'addition des produits de formule (I) avec les acides et les bases.The subject of the invention is the compounds of formula <I)
in which X, in position 5, 6, 7 or 8, represents a hydrogen atom, a halogen atom, a linear or branched alkyl radical containing from 1 to 5 carbon atoms, a linear or branched alkoxy radical containing from 1 to 4 carbon atoms, a trifluoromethyl radical, a trifluoromethylthio radical, or a trifluoromethoxy radical, R1 represents a hydrogen atom, or an alkyl radical containing from 1 to 4 carbon atoms, R2 represents a radical chosen from the radicals thiazolyle, 4,5dihydrothiazolyle, pyridinyle, oxazolyle, isoxazolyle, imidazolyle, pyrimidyle et tétrazolyle, optionally substituted by an alkyl radical containing 1 to 4 carbon atoms or R2 represents a phenyl radical, optionally substituted by at least one radical chosen from the group formed by the hydroxyt radicals, the alkyl radicals containing from 1 to 4 carbon atoms, the alkoxy radicals containing from 1 to 4 carbon atoms, the trifluoromethyl radical, the nitro radical and l he halogen atoms, m represents an integer which can vary from 0 to 7, n represents 0, 1 or 2, R3 a linear or branched alkyl radical containing from 1 to 5 carbon atoms, as well as the addition salts of the products of formula (I) with acids and bases.
Lorsque X représente un atome d'halogène, il s'agit de preférence d'un atome de chlore. When X represents a halogen atom, it is preferably a chlorine atom.
Lorsque X représente un radical alcoyle, il s'agit de préférence du radical méthyle, éthyle, n-propyle, n-butyle, n-pentyle, isopropyle ou isobutyle. When X represents an alkyl radical, it is preferably a methyl, ethyl, n-propyl, n-butyl, n-pentyl, isopropyl or isobutyl radical.
Lorsque X représente un radical alcoxy, il agit de préfé rence du racical méthoxy, éthoxy ou n-propoxy. When X represents an alkoxy radical, it preferably acts on the methoxy, ethoxy or n-propoxy racical.
Lorsque R1 représente un radical alcoyle, il stagit de préférence du radical méthyle ou éthyle. When R1 represents an alkyl radical, it preferably starts from the methyl or ethyl radical.
Lorsque R2 représente un radical hétérocyclique substitué par un radical alcoyle, il s'agit de préférence d'un radical hétérocyclique substitué par un radical méthyle ou éthyle. When R2 represents a heterocyclic radical substituted by an alkyl radical, it is preferably a heterocyclic radical substituted by a methyl or ethyl radical.
Lorsque R2 représente un radical phényle substitué, il s'agit de préférence d'un radical phényle substitué par au moins un radical choisi dans le groupe formé par les radicaux hydroxy, les radicaux méthyle ou éthyle, les radicaux méthoxy ou éthoxy, le radical trifluorométhyle, le radical nitro et l'atome de chlore. When R2 represents a substituted phenyl radical, it is preferably a phenyl radical substituted by at least one radical chosen from the group formed by hydroxy radicals, methyl or ethyl radicals, methoxy or ethoxy radicals, the trifluoromethyl radical , the nitro radical and the chlorine atom.
Lorsque R3 représente un radical alcoyle, il s'agit de préférence,du radical méthyle ou éthyle. When R3 represents an alkyl radical, it is preferably a methyl or ethyl radical.
n représente 0, 1 ou 2, m représente un nombre entier pouvant varier de O à 7 qui est de préférence égal à O ou à 1, 2 ou 3. n represents 0, 1 or 2, m represents an integer which can vary from O to 7 which is preferably equal to O or 1, 2 or 3.
Parmi les sels d'addition avec les acides, on peut citer ceux formés avec les acides minéraux-tels que les acides chlorhydrique, bromhydrique, sulfurique ou phosphorique ainsi que ceux formés avec les acides sulfonîques tels que les acides alcoyle ou arylsulfoniques, par exemple l'acide méthanesulfonique ou paratoluènesulfonique. Among the addition salts with acids, there may be mentioned those formed with mineral acids - such as hydrochloric, hydrobromic, sulfuric or phosphoric acids as well as those formed with sulfonic acids such as alkyl or arylsulfonic acids, for example l methanesulfonic or paratoluenesulfonic acid.
Parmi les sels d'addition avec les bases, on peut citer ceux formés avec les métaux alcalins comme le sodium et le potassium et les amines, par exemple la triméthylamine ou la diméthylamine. Among the addition salts with bases, mention may be made of those formed with alkali metals such as sodium and potassium and amines, for example trimethylamine or dimethylamine.
L'invention a notamment pour objet les composés de formule (I) pour lesquels X est en position 8 ainsi que leurs sels d'addition avec les acides et les bases.et ceux pour lesquels X représente un radical trifluorométhyle, ainsi que leurs sels d'addition avec les acides et les bases. The subject of the invention is in particular the compounds of formula (I) for which X is in position 8 as well as their addition salts with acids and bases. And those for which X represents a trifluoromethyl radical, as well as their salts of 'addition with acids and bases.
L'invention a plus particulièrement pour objet les composés de formule (I) pour lesquels R1 représente un atome d'hydrogène, ainsi que leurs sels d'addition avec les acides et les bases et notamment ceux pour lesquels R2 représente un radical thiazolyle, ainsi que leurs sels d'addition avec les acides et les bases et tout particulièrement ceux pour lesquels R3 représente un radical méthyle, ainsi que léurs sels d'addition avec les acides et les bases. A more particular subject of the invention is the compounds of formula (I) for which R1 represents a hydrogen atom, as well as their addition salts with acids and bases and in particular those for which R2 represents a thiazolyl radical, as well as their addition salts with acids and bases and very particularly those for which R3 represents a methyl radical, as well as their addition salts with acids and bases.
Parmi les composés de l'invention, on peut citer notamment les composés pour lesquels m = 1, et n = 0, 1 ou 2, ainsi que leurs sels d'addition avec les acides et les bases et ceux pour lesquels m = 0, n = 0 ou n = 1, ainsi que leurs sels d'addition avec les acides et les bases
On retient également les produits cités dans les exemples et tout particulièrement - le a-hydroxy 2-/(méthylsulfinyl) méthyl/ N-(2-thiazolyl) 8-
trifluorométhyl 3-quinoléine carboxamide et - le 4-hydroxy 2-(méthylthio) N-(2-thiazolyl) 8 trifluorométhyl 3~quinoléine carboxamide.Among the compounds of the invention, there may be mentioned in particular the compounds for which m = 1, and n = 0, 1 or 2, as well as their addition salts with acids and bases and those for which m = 0, n = 0 or n = 1, as well as their addition salts with acids and bases
We also retain the products mentioned in the examples and very particularly - a-hydroxy 2 - / (methylsulfinyl) methyl / N- (2-thiazolyl) 8-
trifluoromethyl 3-quinoline carboxamide and - 4-hydroxy 2- (methylthio) N- (2-thiazolyl) 8 trifluoromethyl 3 ~ quinoline carboxamide.
L'invention a également pour objet un procédé de préparation des produits de formule (I)- dans laquelle X, R1, R2, R3 ont la signification déjà donnée précédemment et dans laquelle m représente un nombre entier pouvant varier de i à 7 et n = 0, caractérisé en ce que l'on soumet un composé de formule (II)
dans laquelle X conserve la signification donnée ci-dessus, à l'action~d'un acide de formule (III)
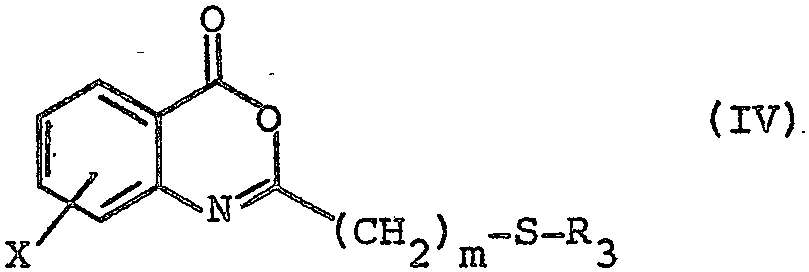
R3-S-(CH2)m-COOH (III) dans laquelle m et R3 ont les significations précédentes; ou d'un dérivé fonctionnel de cet acide, pour obtenir un composé de formule (IV) :
dans laquelle X, m et R3 conservent leurs significations précé
Rentes, que l'on soumet à l'action d'un composé de formule (V)
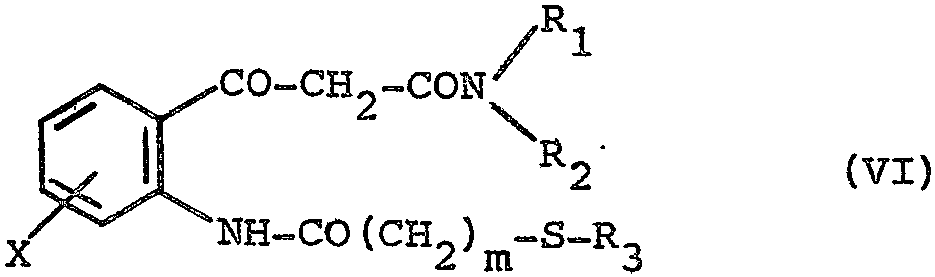
dans laquelle R1 et R2 ont les significations precedentes, pour obtenir un composé de formule (VI)
dans laquelle X, R1, R2, m et R3 conservent leurs significations précédentes, que l'on cyclise en présence d'un agent alcalin, pour obtenir un composé de formule (I) dans laquelle X, R1, R2 et R3 ont leurs significations précédentes et dans laquelle m représente un nombre entier pouvant varier de 1 à 7 et n = 0, que Si désiré, l'on soumet à l'action d'un acide ou d'une base pour en former le sel.The invention also relates to a process for the preparation of products of formula (I) - in which X, R1, R2, R3 have the meaning already given above and in which m represents an integer which can vary from i to 7 and n = 0, characterized in that a compound of formula (II) is subjected
in which X retains the meaning given above, to the action ~ of an acid of formula (III)
R3-S- (CH2) m-COOH (III) in which m and R3 have the above meanings; or a functional derivative of this acid, to obtain a compound of formula (IV):
in which X, m and R3 keep their meanings before
Annuities, which are subjected to the action of a compound of formula (V)
in which R1 and R2 have the above meanings, to obtain a compound of formula (VI)
in which X, R1, R2, m and R3 retain their previous meanings, which are cyclized in the presence of an alkaline agent, to obtain a compound of formula (I) in which X, R1, R2 and R3 have their meanings above and in which m represents an integer which can vary from 1 to 7 and n = 0, that If desired, subject to the action of an acid or a base to form the salt.
Dans les conditions préférentielles de mise en oeuvre de l'invention, le procédé ci-dessus décrit est réalisé de la manière suivante - le dérivé fonctionnel de l'acide de formule (III) est un halogénure ou un anhydride; - la réaction entre le composé de formule (1V) et le composé de formule (V) a lieu en présence d'un organolithien ou d'un amidure de lithium, par exemple de butyllithium ou de diisopropylami dure de lithium;; - la cyclisation du composé de formule (VI) est effectuée en présence d'un agent alcalin, tel qu'un hydrure ou un carbonate alcalin, ou une amine, par exemple en présence d'hydrure de so- dium, de carbonate de sodium ou de potassium, de pipéridine, de 4-aminopyridine, de diméthylaminopyrldine, de triéthylamine, de 1,5-diazabicyclo /4,3,0/ pon-5 > ène, de 1,4-diazabicyclo /2,2,2/ octane ou de 1,5-diazabicyclo /5,4,0/ undec-5-ène. Under the preferred conditions for implementing the invention, the process described above is carried out as follows - the functional derivative of the acid of formula (III) is a halide or an anhydride; - The reaction between the compound of formula (1V) and the compound of formula (V) takes place in the presence of an organolithian or a lithium amide, for example of butyllithium or of hard lithium diisopropylami; the cyclization of the compound of formula (VI) is carried out in the presence of an alkaline agent, such as a hydride or an alkali carbonate, or an amine, for example in the presence of sodium hydride, of sodium carbonate or potassium, piperidine, 4-aminopyridine, dimethylaminopyrldine, triethylamine, 1,5-diazabicyclo / 4,3,0 / pon-5> ene, 1,4-diazabicyclo / 2,2,2 / octane or 1,5-diazabicyclo / 5,4,0 / undec-5-ene.
L'invention a également pour objet un procédé de préparation des produits de formule (I) dans laquelle X, R1, R2 et R3 ont la signification donnée précédemment et dans laquelle m = 0, et n = 0, caractérisé en ce que l'on soumet un acide de formule (vii)
dans laquelle X et R3 ont leurs significations précédentes, ouun dérivé fonctionnel de cet acide, à l'action d'un dérivé de formule (VIII)
dans laquelle R1 et R2 sont définis comme précédemment, pour obtenir le composé de formule (I) correspondant, défini comme ci-dessusr que l'on soumet, si désiré, à l'action d'un acide ou d'une base pour en former le sel.The invention also relates to a process for preparing the products of formula (I) in which X, R1, R2 and R3 have the meaning given above and in which m = 0, and n = 0, characterized in that the we submit an acid of formula (vii)
in which X and R3 have their previous meanings, or a functional derivative of this acid, to the action of a derivative of formula (VIII)
in which R1 and R2 are defined as above, to obtain the corresponding compound of formula (I), defined as above, which is subjected, if desired, to the action of an acid or a base to form the salt.
Dans un mode de réalisation préférée du procédé de l'invention - on utilise comme dérivé fonctionnel d'acide, un chlorure d'acide, un ester d'alcoyle inférieur, un anhydride ou un anhydride mixte. In a preferred embodiment of the process of the invention - as the functional acid derivative, an acid chloride, a lower alkyl ester, an anhydride or a mixed anhydride is used.
- ta condensation de l'acide de formule (VII) ou du dérivé fonctionnel d'acide avec le composé de formule (viii) a lieu au sein d'un solvant inerte comme par exemple le benzène, le toluène, le chlorure de méthylène, l'acétate d'éthyle en présence d'un agent basique comme par exemple un dérivé trîalkylalumique, tels le triméthylaluminium ou le triisobutylaluminium.the condensation of the acid of formula (VII) or of the functional acid derivative with the compound of formula (viii) takes place in an inert solvent such as, for example, benzene, toluene, methylene chloride, ethyl acetate in the presence of a basic agent such as for example a trialkylalumique derivative, such as trimethylaluminium or triisobutylaluminium.
L'invention a aussi pour objet un procédé de préparation caractérisé en ce que pour préparer le composé (VII), on soumet un composé de formule (six)
dans laquelle X conserve la meme signification que précédemment, à l'action d'un agent de sulfuration, on obtient ainsi un composé de formule (X)
dans laquelle X et R3 ont les significations données précédemment, que l'on fait réagir avec un malonate d'alcoyle de formule (XI)
dans laquelle alc représente un radical alcoyle renfermant de 1 à 8 atomes de carbone, en présence d'une base forte, pour obtenir un composé de formule (XII)
que l'on cyclise pour obtenir un composé de formule (xiii)
que l'on saponifie pour obtenir un composé de formule (VII) correspondant
The invention also relates to a preparation process characterized in that to prepare the compound (VII), subjecting a compound of formula (six)
in which X retains the same meaning as above, to the action of a sulphurizing agent, a compound of formula (X) is thus obtained
in which X and R3 have the meanings given above, which are reacted with an alkyl malonate of formula (XI)
in which alk represents an alkyl radical containing from 1 to 8 carbon atoms, in the presence of a strong base, to obtain a compound of formula (XII)
which we cyclize to obtain a compound of formula (xiii)
which is saponified to obtain a compound of formula (VII) corresponding
Dans un mode de réalisation préférée du procédé de préparation du composé de formule (VII) : - L'agent de sulfuration utilisé est un thiolate de métal alcalin ou un thiol utilisé en présence d'une base comme par exemple un carbonate de métal alcalin ou la triéthylamine. In a preferred embodiment of the process for the preparation of the compound of formula (VII): the sulfurizing agent used is an alkali metal thiolate or a thiol used in the presence of a base such as, for example, an alkali metal carbonate or triethylamine.
- La réaction du composé de formule (IX) avec l'agent de sulfu ration a lieu en présence d'un solvant inerte tel le toluène, le benzène, le tétrahydrofuranne - Le malonate d'alcoyle utilisé est la malonate d'éthyle, et la réaction avec le composé de formule (x) est effectuée en présence d'hydrure de sodium, la réaction étant réalisée de préfé rence a une température de 100 OC. - The reaction of the compound of formula (IX) with the sulfurizing agent takes place in the presence of an inert solvent such as toluene, benzene, tetrahydrofuran - The alkyl malonate used is ethyl malonate, and the reaction with the compound of formula (x) is carried out in the presence of sodium hydride, the reaction being preferably carried out at a temperature of 100 OC.
- La cyclisation du composé de formule (xii) est réalisée par chauffage, par exemple à une température comprise entre 150 0C et 25Q0C. - The cyclization of the compound of formula (xii) is carried out by heating, for example at a temperature between 150 ° C. and 25 ° C.
- On saponifie le composé de formule (xiii) au moyen de la soude ou de la potasse.- We saponify the compound of formula (xiii) using soda or potash.
L'invention a aussi pour objet un procédé de préparation des produits de formule (I), dans laquelle X, R1, R2 et R3 ont les significations données précédemment et dans laquelle m représente un nombre entier pouvant varier de O à 7 et n = 1 ou n = 2, caractérisé en ce qur l'on traite les produits de formule (I) dans laquelle n = O par un agent d'oxydation pour obtenir les produits de formule (I) définis ci-dessus, que si désiré, l'on traite par un acide ou une base pour en former le sel. The invention also relates to a process for the preparation of products of formula (I), in which X, R1, R2 and R3 have the meanings given above and in which m represents an integer which can vary from 0 to 7 and n = 1 or n = 2, characterized in that the products of formula (I) in which n = O are treated with an oxidizing agent to obtain the products of formula (I) defined above, only if desired, it is treated with an acid or a base to form the salt.
Le procédé ci-dessus est de préférence caractérisé en ce que l'agent d'oxydation est l'eau oxygénée en milieu hydrométhanolique en présence de chlorure de titane pour obtenir les produits de formule (I) dans laquelle n = 1 et en ce que l'agent d'oxydation est l'eau oxygénée additionnée d'acide acétique, pour obtenir les produits de formule (I) dans laquelle n = 2
Les composés de formule (I) tels que définis ci-dessus ainsi que leurs sels d'addition avec les acides et les bases présentent d'intéressantes propriétés pharmacologiques. Ils présentent, en particulier, une très bonne activité analgésique ainsi qu'une activité anti-inflammatoire non négligeable.The above process is preferably characterized in that the oxidizing agent is hydrogen peroxide in a hydromethanolic medium in the presence of titanium chloride to obtain the products of formula (I) in which n = 1 and in that the oxidizing agent is hydrogen peroxide added with acetic acid, to obtain the products of formula (I) in which n = 2
The compounds of formula (I) as defined above as well as their addition salts with acids and bases have interesting pharmacological properties. They exhibit, in particular, a very good analgesic activity as well as a non-negligible anti-inflammatory activity.
Ces propriétés justifient leur application en thérapeutique et l'invention a également pour objet, à titre de médicaments, les produits tels que définis par la formule (I) ci-dessus, ainsi que les sels d'addition avec les acides et les bases pharmaceutiquement acceptables desdits produits de formule (I). These properties justify their application in therapy and the subject of the invention is also, as medicaments, the products as defined by formula (I) above, as well as the addition salts with acids and pharmaceutically bases. acceptable of said products of formula (I).
La présente invention a tout particulièrement pour objet, à titre de médicaments, le 4-hydroxy 2-/(méthylsufinyl) méthyl/ N-(2-thiazolyl) 8- trifluorométhyl 3-quinoléine carboxamide, ainsi que ses sels d'addition avec les acides et les bases pharmaceutiquement acceptables, et le 4-hyroxy 2-(méthylthio) N-(2 thiazolyl) 8- trifluorométhyl 3-quinoléine carbôxamide, ainsi que ses sels d'addition avec les acides et les bases pharmaceutiquement acceptables. The subject of the present invention is very particularly, as medicaments, 4-hydroxy 2 - / (methylsufinyl) methyl / N- (2-thiazolyl) 8-trifluoromethyl 3-quinoline carboxamide, as well as its addition salts with pharmaceutically acceptable acids and bases, and 4-hydroxy 2- (methylthio) N- (2 thiazolyl) 8-trifluoromethyl 3-quinoline carboxamide, as well as its addition salts with pharmaceutically acceptable acids and bases.
Les médicaments1 objet de l'invention, peuvent être utilisés dans le traitement des algies musculaires, articulaires ou nerveuses, des affections rhumatismales, des douleurs dentaires, des zonas et des migraines, ainsi que dans le traitement des maladies inflammatoires1 notamment des arthroses, des lumbagos, et aussi à titre de traitaient complémentaire dans les états infectieux et fébriles. The medicaments1 which are the subject of the invention can be used in the treatment of muscle, joint or nerve pain, rheumatic affections, dental pain, zonas and migraines, as well as in the treatment of inflammatory diseases1 in particular arthritis, lumbago , and also as additional treatment in infectious and febrile states.
L'invention s'étend aux compositions pharmaceutiques renfermant comme principe actif, les médicaments définis ci-dessus. The invention extends to pharmaceutical compositions containing, as active principle, the medicaments defined above.
Ces compositions pharmaceutiques peuvent être administrées par voie buccale, rectale, par voie parentérale ou par voie locale en application topique sur la peau et les muqueuses. These pharmaceutical compositions can be administered by the oral, rectal, parenteral or local route by topical application to the skin and mucous membranes.
Ces compositions peuvent être solides ou liquides et se présenter sous les formes pnarmaceutiques couramment utilisées en médecine humaine comme, par exemple, les comprimés simples ou dragéifiés1 les gélules, les granulés, les suppositoires, les préparations injectables, les pommades, les crèmes, les gels et les préparations en aérosols, elles sont préparées selon les méthodes usuelles.Le principe actif peut yêtre incorporés à des excipients habituellement employés dans ces compositions pharmaceutiques, tels que le tale, la gomme arabique, le lactose, l'amidon, le stéarate de magnésium, le beurre de cacao, les véhicules aqueux ou non, les corps gras d'origine animale ou végétale, les dérivés paraffiniques, les glycols, les divers agents mouillants, dispersants ou émulsifiants, les conservateurs
La posologie varie notamment en fonction de la voie d'admi- nistration, de l'affection traitée et du sujet en cause.These compositions may be solid or liquid and may be in the pharmaceutical forms commonly used in human medicine such as, for example, simple or coated tablets1 capsules, granules, suppositories, injections, ointments, creams, gels and aerosol preparations, they are prepared according to the usual methods. The active ingredient can be incorporated therein into excipients usually used in these pharmaceutical compositions, such as tale, gum arabic, lactose, starch, magnesium stearate. , cocoa butter, aqueous or non-aqueous vehicles, fatty substances of animal or vegetable origin, paraffinic derivatives, glycols, various wetting agents, dispersants or emulsifiers, preservatives
The dosage varies in particular depending on the route of administration, the condition treated and the subject concerned.
Par exemple, chez l'adulte, elle peut varier entre 20 mg et 2 g de principe actif par jour, par voie orale. For example, in adults, it can vary between 20 mg and 2 g of active ingredient per day, orally.
Les composés de formule (II) utilisés comme produits de départ d'un des procédés de l'invention sont des produits connus d'une façon générale, qui peuvent être préparés selon les procédés indiqués dans la demande de brevet français nO 2 157 874. The compounds of formula (II) used as starting materials for one of the methods of the invention are generally known products, which can be prepared according to the methods indicated in French patent application No. 2 157 874.
Les composés dé formule (IX) utilisés comme produits de départ d'un des procédés de l'invention sont des produits connus d'une façon générale. Ils peuvent être préparés selon la technique de E. KUHLE /Augem. Chem. ed. int. 1, 648 (1962)/. The compounds of formula (IX) used as starting materials for one of the processes of the invention are generally known products. They can be prepared according to the technique of E. KUHLE / Augem. Chem. ed. int. 1, 648 (1962) /.
Les composés de formule (IV), (VI), (VII), (X), (XII), (XIII) et le dichlorure de N-(2-trifluorométhyl phényl) carbonimide sont des produits chimiques nouveaux; l'invention a donc pour objet ces produits à titre de produits industriels nouveaux, notamment à-titre de produits intermédiaires nécessaires à la mise en oeuvre du procédé de l'invention. The compounds of formula (IV), (VI), (VII), (X), (XII), (XIII) and N- (2-trifluoromethyl phenyl) carbonimide dichloride are new chemicals; the invention therefore relates to these products as new industrial products, in particular as intermediate products necessary for the implementation of the process of the invention.
Les exemples suivants illustrent l'invention sans toutefois la limiter
Exemple 1 a 4-hydroxy 2-(méthylthiométhuyl) N'-(2'-tbiazolyl) '8-
trifluorométhyl 3-quinoléine arbaxairride
Stade A : 2-(méthylthiométhyl) 8-tri-fluorométhyl 4H,-3,1-benzoxa- zine 4-one. The following examples illustrate the invention without however limiting it
Example 1 a 4-hydroxy 2- (methylthiométhuyl) N '- (2'-tbiazolyl)' 8-
trifluoromethyl 3-quinoline arbaxairride
Stage A: 2- (methylthiomethyl) 8-tri-fluoromethyl 4H, -3,1-benzoxazine 4-one.
On mélange 39,84 g de chlorure dans l'acide 2-methyl thioacétique préparé selon la technique indiquée dans J Org. Chem. 39.84 g of chloride are mixed in 2-methyl thioacetic acid prepared according to the technique indicated in J Org. Chem.
22 (1957) 1721 et 24,6 g d'acide 2-amino 3- trifluorométhyl benzolque préparé selon le procédé indiqué dans J Med. Chem 16(2) 101,6 (1973). On chauffe progressivement et maintient 1 heure 20 minutes à 1350C. L'excès de chlorure d'acide est éliminé par distillation sous pression réduite vers 1250C Le résidu obtenu est repris dans 150 cm3 d'éther, séché, concentre-sous pression réduite, l'huile obtenue est purifiée sur silice en éluant an chlorure de méthylène On récupère 24,7 g de produit brut que l'on empate dans 25 cm3 d'éther de pétrole (eb :: 600- 800C), essore, lave, sèche sous pression réduite à 350C et obtient 20,4 g de produit attendu fondant vers 48-50 C.22 (1957) 1721 and 24.6 g of 2-amino-3-trifluoromethyl benzolque acid prepared according to the method indicated in J Med. Chem 16 (2) 101.6 (1973). It is gradually heated and maintained for 1 hour 20 minutes at 1350C. The excess acid chloride is removed by distillation under reduced pressure around 1250C. The residue obtained is taken up in 150 cm3 of ether, dried, concentrated under reduced pressure, the oil obtained is purified on silica, eluting with chloride of methylene 24.7 g of crude product are recovered, which is mashed in 25 cm 3 of petroleum ether (eb :: 600-800C), drained, washed, dried under reduced pressure at 350C and 20.4 g of product are obtained. expected melting around 48-50 C.
Stade B : 2-(méthylthioacétylamino)ss-oxo N-(2-thiazolyl) 3-trifluorométhyl benzène propanamide.Stage B: 2- (methylthioacetylamino) ss-oxo N- (2-thiazolyl) 3-trifluoromethyl benzene propanamide.
On ajoute à OOC, sous agitation, 50 cm3 d'une solution de n-butyllithium dans l'hexane titrant 1,4 mole par litre, dans une solution renfermant 4,86 g de N-(2-thiazolyl) acétamide (Beilstein 27, 155) et 200 cm3 de tétrahydrofurane. On refroidit à -70 C et ajoute 4,7 g du produit obtenu au stade A dans 50 cm3 de tétrahydrofurane. On verse la solution obtenue sur un mélange d'eau, de glace et d'acide chlorhydrique, extrait à l'éther, lave avec une solution aqueuse d'acide chlorhydrique, sèche et concentre sous pression réduite. On empâte le résidu dans 50 cm3 d'éther, essore, lave à l'éther, sèche sous pression réduite à 50 C et obtient 2,5 g de produit attendu fondant à 1800C. 50 cm3 of a solution of n-butyllithium in hexane grading 1.4 mol per liter are added to OOC, with stirring, in a solution containing 4.86 g of N- (2-thiazolyl) acetamide (Beilstein 27 , 155) and 200 cm3 of tetrahydrofuran. The mixture is cooled to -70 ° C. and 4.7 g of the product obtained in Stage A are added to 50 cm3 of tetrahydrofuran. The solution obtained is poured onto a mixture of water, ice and hydrochloric acid, extracted with ether, washed with an aqueous solution of hydrochloric acid, dried and concentrated under reduced pressure. The residue is pasted in 50 cm3 of ether, drained, washed with ether, dried under reduced pressure at 50 ° C. and 2.5 g of the expected product melting at 1800 ° C. are obtained.
Stade C : 4-hydroxy 2-(méthylthipméthyl) N-(2-thiazolyl) 8-tri- fluorométhyl 3-quinoléine carboxamide. Stage C: 4-hydroxy 2- (methylthipmethyl) N- (2-thiazolyl) 8-tri-fluoromethyl 3-quinoline carboxamide.
On mélange 2 g de produit obtenu au stade B, 20 cm3 de tétrahydrofurane, 0,584 g de diméthylaminopyridine, puis agite la solution obtenue 5 heures à température ambiante. On chasse le solvant sous pression réduite, reprend le résidu dans 20 cm3 d'eau, ajoute 4,8 cm3 d'acide chlorhydrique N, agite 1 heure à température ambiante, essore, lave à l'eau et sèche sous pression réduite à 1000C. On dissout au reflux le produit brut obtenu dans 250 cm3 d'acétonitrile, refroidit, essore, sèche sous pression réduite à 800C et obtient 1,45 g'de produit attendu fondant à 250OC. 2 g of product obtained in stage B, 20 cm 3 of tetrahydrofuran, 0.584 g of dimethylaminopyridine are mixed, then the solution obtained is stirred for 5 hours at room temperature. The solvent is removed under reduced pressure, the residue is taken up in 20 cm3 of water, 4.8 cm3 of N hydrochloric acid is added, the mixture is stirred for 1 hour at room temperature, drained, washed with water and dried under reduced pressure at 1000C . The crude product obtained is refluxed in 250 cm3 of acetonitrile, cooled, wrung, dried under reduced pressure at 800C and 1.45 g of the expected product melting at 250OC are obtained.
Exemple 2 :4-hydroxy 2-/(méthylsulfinyl) méthyl/ N-(2-thiazolyl) 8- trifluorométhtl -3-quinoléine carboxamide. Example 2: 4-hydroxy 2 - / (methylsulfinyl) methyl / N- (2-thiazolyl) 8-trifluorométhtl -3-quinoline carboxamide.
On introduit sous agitation k cm3 d'eau oxygénée à 30% et 30 cm3 de méthanol dans un mélange de 2 g de produit de l'exem- ple 1, de 200 cm3 de méthanol , 40 cm3 d'eau et de 10,28 cm3 d'une solution aqueuse de chlorure de titane à 15%. On agite à température ambiante 30 à 45 minutes, verse la solution obtenue sur un mélange eau et glace, essore, lave à l'eau, sèche sous pression réduite à 900C. Le produit brut obtenu est recristallisé dans le dioxanne et puis dans l'éthanol aqueux à 95%, on obtient après séchage sous pression réduite à 900C1 1,3 g de produit attendu fondant à 2380C. K cm3 of 30% hydrogen peroxide and 30 cm3 of methanol are introduced with stirring into a mixture of 2 g of product of Example 1, 200 cm3 of methanol, 40 cm3 of water and 10.28 cm3 of a 15% aqueous solution of titanium chloride. The mixture is stirred at room temperature for 30 to 45 minutes, the solution obtained is poured onto a mixture of water and ice, drained, washed with water, dried under reduced pressure at 900C. The crude product obtained is recrystallized from dioxane and then from 95% aqueous ethanol, 1.3 g of expected product melting at 2380C is obtained after drying under reduced pressure at 900C1.
Exemple 3 : 4-bvdroxv 2-/(métholsulfonyl! méthvl/ N-(2-thiazolyl) 8- trifluorométhyl 3-qui-nolé-ine carboxaraide. Example 3: 4-bvdroxv 2 - / (metholsulfonyl! Methvl / N- (2-thiazolyl) 8-trifluoromethyl 3-qui-nolé-ine carboxaraide.
On mélange 3 g de produit de l'exemple 1, 60 cm3 d'acide acétique, 1,86 cm3 d'eau oxygénée à 30%, chauffe à 80-820C et maintient 2 heures cette température. On refroidit le mélange, essore les cristaux obtenus1 les lave à l'acide acétique puis à l'éther, sèche sous pression réduite à 100 C. Le produit brut est dissous au reflux dans 70 cm3 d'acide acétique; on refroidit, essore les cristaux obtenus, les lave à l'acide acétique puis à l'éther, sèche sous pression réduite à 110 C et obtient 1,7 g de produit attendu fondant à 2750C. 3 g of product of Example 1 are mixed, 60 cm3 of acetic acid, 1.86 cm3 of 30% hydrogen peroxide, heating to 80-820C and maintaining this temperature for 2 hours. The mixture is cooled, the crystals obtained are drained 1 washed with acetic acid and then with ether, dried under pressure reduced to 100 C. The crude product is dissolved at reflux in 70 cm 3 of acetic acid; cooled, drained the crystals obtained, washed with acetic acid and then with ether, dried under reduced pressure at 110 C and 1.7 g of expected product melting at 2750C.
Exemple 4 : 4-hodroxy 2-(méthvlthio) N-(2-thiazolvl) 8- trifluo rométhyl 3-auinoléin carboxamide. Example 4: 4-hodroxy 2- (methvlthio) N- (2-thiazolvl) 8- trifluo romethyl 3-auinoline carboxamide.
Stade A : N-/2-(t,riîluorométhyl) phényl/ carbonochlorurimido thioate de méthyle.Stage A: N- / 2- (t, riluoromethyl) phenyl / carbonochlorurimido methyl thioate.
thioate de méthyle. methyl thioate.
On ajoute à -150C, 10,12 g de triéthylamine, 24,2 g de dichlorure de N-(2-trifluorométhyl phényl) carbonimidoyle (préparation donnée ci-dessous) en solution dans 250 cm3 de toluène,, puis entre -10 et -15 C en 15 minutes. 5,29 g de méthylmercaptan en solution dans 15 cm3 de toluène. On laisse revenir à température ambiante puis porte 1 heure au reflux. Après refroidi-s- sement, on élimine par filtration le chlorhydrate de triéthylamine formée puis lave le filtrat à l'eau puis avec une solution aqueuse d'acide chlorhydrique à 10%, puis de nouveau à l'eau1 sèche, et élimine les solvants à 500C sous pression réduite.On distille le produit obtenu et recueille 17,99 g de produit attendu (eb : 0,3 mmHg = 68-70 C). 10.12 g of triethylamine, 24.2 g of N- (2-trifluoromethyl phenyl) carbonimidoyl dichloride (preparation given below) dissolved in 250 cm3 of toluene are added at -150 ° C., then between -10 and -15 C in 15 minutes. 5.29 g of methyl mercaptan in solution in 15 cm3 of toluene. The mixture is left to return to ambient temperature and then brought to reflux for 1 hour. After cooling, the triethylamine hydrochloride formed is filtered off, then the filtrate is washed with water and then with a 10% aqueous hydrochloric acid solution, then again with dry water and the solvents are removed. at 500C under reduced pressure. The product obtained is distilled and 17.99 g of expected product is collected (eb: 0.3 mmHg = 68-70 C).
Stade B /méthylthio //2-(trifluo,rpméthyl), phényl/ amino/ méthylène/ propane dioate d'éthyle
On ajoute en 15 minutes 13D45 g de malonate d'éthyle en solution dans 20 cm3 de diméthylformamide à 3,7 g d'hydrure de sodium à 50% dans l'huile en suspension dans 150 cm3 de diméthyl formamide, agite 30 minutes à température ambiante, puis ajoute sous azote 17,76 g du produit obtenu au stade A en solution dans 20 CZ3 de diméthylformamide.On chauffe à 95 /105 C pendant 30 minutes Après refroidissement, on verse le mélange obtenu sur un mélange d'eau et d'acide chlorhydrique à 20S, extrait à l'éther, lave les phases éthérées à l'eau jusqu'à neutralité, sèche, élimine les solvants à 300C puis à 500C sous pression réduite. Après distillation des fractions volatiles, on chromatographie le résidu en éluant au chlorure de méthylène-éther de pétrole (1-1) eb : 60-80 C puis chlorure de méthylène On obtient 10,43 g de produit attendu.Stage B / methylthio // 2- (trifluo, rpmethyl), phenyl / amino / methylene / ethyl propane dioate
13D45 g of ethyl malonate dissolved in 20 cm3 of dimethylformamide containing 3.7 g of 50% sodium hydride in oil in suspension in 150 cm3 of dimethylformamide are added over 15 minutes, the mixture is stirred for 30 minutes at temperature ambient, then added under nitrogen 17.76 g of the product obtained in stage A dissolved in 20 CZ3 of dimethylformamide. Heating is carried out at 95/105 C for 30 minutes After cooling, the mixture obtained is poured onto a mixture of water and d hydrochloric acid at 20S, extracted with ether, washing the ethereal phases with water until neutral, drying, eliminating the solvents at 300C then at 500C under reduced pressure. After distillation of the volatile fractions, the residue is chromatographed, eluting with methylene chloride-petroleum ether (1-1) eb: 60-80 C then methylene chloride. 10.43 g of expected product is obtained.
Analyse : C16 H18 NF3 O4 S = 377,385
Calculé . C% 50,92 8x 4,81 N% 3,71 F% 15110 S 8,50
Trouvé : 50,9 4,7 3,7 14,9 8,4 Stade C 6 4-hydroxy 2-méthylthio 8- trifluorométhyl 3-quinoléì- ne carboxylate d'éthyle. Analysis: C16 H18 NF3 O4 S = 377.385
Calculated. C% 50.92 8x 4.81 N% 3.71 F% 15 110 S 8.50
Found: 50.9 4.7 3.7 14.9 8.4 Stage C 6 4-hydroxy 2-methylthio 8-trifluoromethyl 3-quinoline ethyl carboxylate.
On chauffe progressivement jusqu'à 1800C sous pression réduite, 10,74 g de produit obtenu au stade et maintient pendant 30 minutes sous agitation On refroidit, essore le produit brut, le recristallise dans l'éthanol et obtient 6,66 g de produit attendu fondant à 1050C
Stade D ç 4-hydroxy l-(méthythio) N-(2-thiazolyl) 8- trifluorométhyl 3-quinoléine carboxami,de
On introduit sous argon et sous agitation en 15 minutes entre 8 et 12 C, 77 cm3 d'une solution toluénique à 25% de triisobutylaluminium dans 16,87 g de 2-aminothiazole en solution dans 370 cm3 de chlorure de méthylène, agite 15 minutes le mélange obtenu et laisse revenir à température ambiante.On ajoute en 1 fois 11,18 g du produit obtenu au stade C et porte au reflux 28 heures 30 minutes. On refroidit, ajoute 380 cm3 d'acide chlorhydrique à 20%, agite 75 minutes, essore, lave à l'eau, seche sous pression réduite à 1000C. On recristallise le produit brut dans l'acide acétique, essore, lave à l'éther, sèche sous pression réduite à 1000C et obtient 6,6 g de produit attendu.Gradually heated to 1800C under reduced pressure, 10.74 g of product obtained in the stage and maintained for 30 minutes with stirring. melting at 1050C
Stage D ç 4-hydroxy l- (methythio) N- (2-thiazolyl) 8- trifluoromethyl 3-quinoline carboxami, of
Is introduced under argon and with stirring in 15 minutes between 8 and 12 C, 77 cm3 of a 25% toluene solution of triisobutylaluminium in 16.87 g of 2-aminothiazole dissolved in 370 cm3 of methylene chloride, stirred for 15 minutes the mixture obtained and allowed to return to ambient temperature. 11.18 g of the product obtained in stage C is added in one portion and the mixture is brought to reflux for 28 hours 30 minutes. Cooled, added 380 cm3 of 20% hydrochloric acid, stirred for 75 minutes, wrung, washed with water, dried under reduced pressure at 1000C. The crude product is recrystallized from acetic acid, drained, washed with ether, dried under reduced pressure at 1000C and 6.6 g of the expected product is obtained.
Analyse : C15H10F3N3O2S2 = 385î389
Calculé g C% 46,75 H% 2,61 N% 10,90 F% 14,79 S% 16,64
Trouvé : 46,6 2,6 11,0 15,0 16,3
Préparation du dichlorure de N-(2-trifluoroniéthyl phényl) carbo- nimide.Analysis: C15H10F3N3O2S2 = 385î389
Calculated g C% 46.75 H% 2.61 N% 10.90 F% 14.79 S% 16.64
Found: 46.6 2.6 11.0 15.0 16.3
Preparation of N- (2-trifluoroniethyl phenyl) carbonimide dichloride.
Stade A : N-/2-(trifluorométhyl)phényl / formamide. Stage A: N- / 2- (trifluoromethyl) phenyl / formamide.
On mélange 108 g d'orthotrifluor,ométhyl aniline à 200 cm3 d'acide formique, porte 30 minutes au reflux, refroidit puis verse sur un mélange d'eau et de glace. On essore les cristaux formés, les lave à l'eau, les reprend par 750 cm3 d'éther. On lave les phases éthérées à l'eau, puis avec une solution aqueuse de carbonate acide de sodium à 5% puis de nouveau à l'eau, sèche, élimine les solvants sous pression réduite et obtient 111,1 g de produit attendu fondant à 790C. 108 g of orthotrifluor, omethyl aniline are mixed with 200 cm 3 of formic acid, the mixture is brought to reflux for 30 minutes, cooled and then poured onto a mixture of water and ice. The crystals formed are drained, washed with water and taken up in 750 cm3 of ether. The ethereal phases are washed with water, then with an aqueous solution of sodium hydrogen carbonate at 5%, then again with water, dried, the solvents are removed under reduced pressure and 111.1 g of expected product melting at 790C.
Stade B : Dichlorure de N-(2-trifluorométhyl phényl) carbonimide.Stage B: N- (2-trifluoromethyl phenyl) carbonimide dichloride.
On verse 63,57 g de chlorure de sulfuryle dans 23S,42 g de chlorure de thionyle puis ajoute à la solution par petites frac- tions en 75 minutes 89,1 g de N-/2-(trifluorométhyl) phényl/ formamide.préparé au stade A. On chauffe à 220C, agite 1 heure, porte au reflux en 2 heures et le maintient 1 heure. On refroidit, élimine les solvants sous pression réduite et obtient une huile. 63.57 g of sulfuryl chloride are poured into 23S, 42 g of thionyl chloride and then added to the solution in small portions over 75 minutes 89.1 g of N- / 2- (trifluoromethyl) phenyl / formamide. in stage A. It is heated to 220C, stirred for 1 hour, brought to reflux in 2 hours and maintained for 1 hour. The mixture is cooled, the solvents are removed under reduced pressure and an oil is obtained.
On filtre, distille et recueille 100, OS g de produit attendu.Filtered, distilled and collected 100, OS g of expected product.
(Eb/7mmEg = 76-770C). (Eb / 7mmEg = 76-770C).
Exemple 5 4-hydroxy 2-(méthylsulfinyl) N-(2-thiazolyl) 8-tri- fluorométhvî 3-cuinoléine carboxamide.
Example 5 4-hydroxy 2- (methylsulfinyl) N- (2-thiazolyl) 8-tri-fluorometh 3-cuinoline carboxamide.
On ajoute 12,6 cm3 de chlorure de titane en solution aqueuse à 15% dans 2,312 g de produit obtenu à l'exemple o en suspension dans 240 cm3 de méthanol et 48 cm3 d'eau; on introduit ensuite en 15 minutes 4,8 cm3 d'une solution aqueuse à 30% de peroxyde d'hydrogène mélange à 36 cm3 de méthanol.On agite 20 heures à température ambiante le milieu réactionnel, le verse sur un mélange eau-glace, essore, lave à l'eau, sèche sous pression réduite à 10'00-C. On dissout le produit brut obtenu dand 430 cm3 de tétrahydrofuranneà ébullition. Onfiltre;, concentre jusqu'à 150 cm3 sous pression réduite, essore, lave au tetrahydrofuranne puis à l'éther et obtient après séchage 'à 100 C, 1,79 g de produit attendu fondant à 28.00C, 'Exemie : Composition phamaceutique. 12.6 cm3 of titanium chloride are added in 15% aqueous solution in 2.312 g of product obtained in Example o suspended in 240 cm3 of methanol and 48 cm3 of water; 4.8 cm3 of a 30% aqueous solution of hydrogen peroxide mixed with 36 cm3 of methanol are then introduced over 15 minutes. The reaction medium is stirred for 20 hours at room temperature, poured onto a water-ice mixture, spin, wash with water, dry under reduced pressure at 10'00-C. The crude product obtained is dissolved in 430 cm3 of tetrahydrofuran at the boil. Onfiltre ;, concentrates up to 150 cm3 under reduced pressure, wrung, washed with tetrahydrofuran then with ether and after drying 'at 100 ° C., 1.79 g of expected product melting at 28.00C,' Example: Pharmaceutical composition.
On a préparé des comprimés répondant à la formule suivante - produit de l'exemple 2 ou D o o e c ........... .. ...... 50 mg - Excipient q.s. pour un comprimé termine à .... ..... 350 mg. Tablets corresponding to the following formula were prepared - product of Example 2 or D o o e c ........... .. ...... 50 mg - Excipient q.s. for one tablet ends at .... ..... 350 mg.
(Détail de l'excipient lactose, talc, amidon, stéarate de magnésium).(Detail of the excipient lactose, talc, starch, magnesium stearate).
ETUDE PHARMACOLOGIQUE 1) Etude de l'activité analgésique
Le test employé est basé sur le fait signalé par R. POSTER et Coll., (Fed. Prolo 1959, 1B 412) selon lequel l'injection intrapéritonéale d'acide acétique provoque, chez la souris, des mouvements répétés d'étirement et de torsion pouvant persister pendant plus de 6 heures. Les analgésiques préviennent ou diminuent ce syndrome qui peut être considéré comme l'extérioris-a- tion d'une douleur abdominale diffuse. On utilise une solution d'acide-acétique à 1% dans l'eau. La dose déclenchant le syndrome est dans ces conditions de 0,01 cm3/g, soit 100 mg/kg d'acide acétique.PHARMACOLOGICAL STUDY 1) Study of analgesic activity
The test used is based on the fact reported by R. POSTER et al., (Fed. Prolo 1959, 1B 412) according to which the intraperitoneal injection of acetic acid causes, in mice, repeated movements of stretching and torsion which may persist for more than 6 hours. Pain relievers prevent or decrease this syndrome, which can be thought of as the exacerbation of diffuse abdominal pain. A 1% acetic acid solution in water is used. The dose triggering the syndrome is under these conditions 0.01 cm3 / g, or 100 mg / kg of acetic acid.
Le produit étudié est administré par voie buccale, une demi-heure avant l'injection d'acide acétique, les souris étant à jeun depuis la veille de l'expérience. The product studied is administered orally, half an hour before the injection of acetic acid, the mice having been fasting since the day before the experiment.
Les étirements sont observés et comptés pour chaque souris pendant une période d'observation de 15 minutes commençant aussitôt après l'injection d'acide acétique
Les résultats sont exprimés au moyen de la DA50, c'est-a- dire la dose qui permet d'obtenir une diminution de 50% du nombre des étirements par rapport aux animaux témoins. La DA50 trouvée a été de 10 mg/kg pour les produits de l'exemple 2 et de l'exemple 4 et de 15mg/kg pour les produits de l'exemple 3 et de l'exemple 5.The stretches are observed and counted for each mouse during a 15-minute observation period starting immediately after the injection of acetic acid.
The results are expressed by means of the DA50, that is to say the dose which makes it possible to obtain a reduction of 50% in the number of stretches compared to the control animals. The DA50 found was 10 mg / kg for the products of Example 2 and of Example 4 and 15 mg / kg for the products of Example 3 and of Example 5.
2) Etude de l'activité anti-inflammatoire.2) Study of anti-inflammatory activity.
L'activité anti-inflammatoire a été déterminée sur le test de l'oedème plantaire provoqué par la carraghénine chez le rat. The anti-inflammatory activity was determined on the test of plantar edema caused by carrageenan in rats.
On administre,à des rats mâles pesant de 130 à 150 g, 0,05 cm3 d'une suspension stérile à 1% de carraghénine dans l'articulation tibio-tarsienne d'une patte postérieure. 0.05 cm3 of a sterile 1% carrageenan suspension in the tibio-tarsal joint of a hind leg is administered to male rats weighing 130 to 150 g.
Simultanément, on administre le produit à étudier dans une suspension de carboxyméthylcellulose à 0,25% et de Tween à 0,02% par voie orale. Simultaneously, the product to be studied is administered in a suspension of 0.25% carboxymethylcellulose and 0.02% Tween by mouth.
Le volume de la patte est mesuré avant l'administration, puis 2-heures, 4 heures, 6 heures, 8 heures et 24 heures après. The volume of the paw is measured before administration, then 2-hours, 4 hours, 6 hours, 8 hours and 24 hours after.
L'intensîré de l'inflammation est amxima 4 à 6 heures après l'injection de carraghénine. La différence du volume des pattes des animaux traités et des témoins met en évidence l'action anti-inflammatoire du médicament. The intensity of the inflammation is amxima 4 to 6 hours after the injection of carrageenan. The difference in the volume of the legs of the treated animals and of the controls highlights the anti-inflammatory action of the drug.
On determine la DA501 c1 est-à-dire la dose qui permet d 'ob- tenir une diminition de l'oedème de 50x. The DA501 c1 is determined, that is to say the dose which makes it possible to obtain a reduction in the edema of 50x.
La DA50 a été trouvée égale à 25 mg/kg pour le produit de l'exemple 4 et à 50 mg/kg pour le produit de l'exemple 2. The DA50 was found to be 25 mg / kg for the product of Example 4 and 50 mg / kg for the product of Example 2.
Claims (8)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR8215423A FR2532939A1 (en) | 1982-09-13 | 1982-09-13 | New 4-hydroxy-3-quinolinecarboxylic acid derivatives substituted at position 2, their preparation, their use as medicaments, compositions containing them and new intermediates obtained |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR8215423A FR2532939A1 (en) | 1982-09-13 | 1982-09-13 | New 4-hydroxy-3-quinolinecarboxylic acid derivatives substituted at position 2, their preparation, their use as medicaments, compositions containing them and new intermediates obtained |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| FR2532939A1 true FR2532939A1 (en) | 1984-03-16 |
| FR2532939B1 FR2532939B1 (en) | 1985-02-22 |
Family
ID=9277390
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| FR8215423A Granted FR2532939A1 (en) | 1982-09-13 | 1982-09-13 | New 4-hydroxy-3-quinolinecarboxylic acid derivatives substituted at position 2, their preparation, their use as medicaments, compositions containing them and new intermediates obtained |
Country Status (1)
| Country | Link |
|---|---|
| FR (1) | FR2532939A1 (en) |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2564835A1 (en) * | 1984-05-23 | 1985-11-29 | Roussel Uclaf | Novel 4-hydroxy-3-quinolinecarboxylic acid derivatives substituted at the 2-position with a sulphur-containing group, process for their preparation, their application as medicaments and the compositions which contain them |
| FR2566405A1 (en) * | 1984-06-25 | 1985-12-27 | Roussel Uclaf | NOVEL 4-HYDROXY 3-QUINOLINE CARBOXYLIC ACID DERIVATIVES SUBSTITUTED INTO 2 BY AMINE FUNCTION, THEIR PREPARATION, THEIR USE AS MEDICAMENTS, THE COMPOSITIONS COMPRISING THE SAME AND THE NEW INTERMEDIATES OBTAINED |
| US5011931A (en) * | 1987-11-18 | 1991-04-30 | The Boots Company Plc | Process for the preparation of 1-methyl-3-methylthio-4-quinolone and the sulfinyl, and sulfonyl analogs thereof |
| WO2010102811A1 (en) | 2009-03-12 | 2010-09-16 | Grünenthal GmbH | Substituted 2-mercaptoquinoline-3-carboxamides as kcnq2/3 modulators |
| WO2011058113A1 (en) * | 2009-11-12 | 2011-05-19 | Ucb Pharma S.A. | Fused bicyclic pyridine and pyrazine derivatives as kinase inhibitors |
| WO2012025238A1 (en) | 2010-08-27 | 2012-03-01 | Grünenthal GmbH | Substituted quinoline-3-carboxamides as kcnq2/3 modulators |
| WO2012025237A1 (en) | 2010-08-27 | 2012-03-01 | Grünenthal GmbH | Substituted 2-amino-quinoline-3-carboxamides as kcnq2/3 modulators |
| WO2012025236A1 (en) | 2010-08-27 | 2012-03-01 | Grünenthal GmbH | Substituted 2-oxy-quinoline-3-carboxamides as kcnq2/3 modulators |
| US8178684B2 (en) | 2009-03-12 | 2012-05-15 | Gruenenthal Gmbh | Substituted nicotinamides as KCNQ2/3 modulators |
| US8207342B2 (en) | 2009-03-10 | 2012-06-26 | Gruenenthal Gmbh | Substituted 3-amino-2-mercaptoquinolines as KCNQ2/3 modulators |
| US8247573B2 (en) | 2009-03-12 | 2012-08-21 | Gruenenthal Gmbh | Substituted N-(2-mercaptopyridin-3-yl)amides as KCNQ2/3 modulators |
| US8618129B2 (en) | 2010-09-01 | 2013-12-31 | Gruenenthal Gmbh | Substituted 1-oxo-dihydroisoquinoline-3-carboxamides as KCNQ2/3 modulators |
| US8653102B2 (en) | 2010-08-27 | 2014-02-18 | Gruenenthal Gmbh | Substituted 2-oxo- and 2-thioxo-dihydroquinoline-3-carboxamides as KCNQ2/3 modulators |
| EP2322516B1 (en) * | 2005-07-29 | 2015-09-23 | Janssen Sciences Ireland UC | Intermediates for the preparation of Macrocyclic inhibitors of hepatitis c virus |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2340735A1 (en) * | 1976-02-11 | 1977-09-09 | Roussel Uclaf | NEW DERIVATIVES OF 3-QUINOLEINE CARBOXYLIC ACID, THEIR METHOD OF PREPARATION AND THEIR APPLICATION AS A MEDICINAL PRODUCT |
-
1982
- 1982-09-13 FR FR8215423A patent/FR2532939A1/en active Granted
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2340735A1 (en) * | 1976-02-11 | 1977-09-09 | Roussel Uclaf | NEW DERIVATIVES OF 3-QUINOLEINE CARBOXYLIC ACID, THEIR METHOD OF PREPARATION AND THEIR APPLICATION AS A MEDICINAL PRODUCT |
Cited By (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2564835A1 (en) * | 1984-05-23 | 1985-11-29 | Roussel Uclaf | Novel 4-hydroxy-3-quinolinecarboxylic acid derivatives substituted at the 2-position with a sulphur-containing group, process for their preparation, their application as medicaments and the compositions which contain them |
| FR2566405A1 (en) * | 1984-06-25 | 1985-12-27 | Roussel Uclaf | NOVEL 4-HYDROXY 3-QUINOLINE CARBOXYLIC ACID DERIVATIVES SUBSTITUTED INTO 2 BY AMINE FUNCTION, THEIR PREPARATION, THEIR USE AS MEDICAMENTS, THE COMPOSITIONS COMPRISING THE SAME AND THE NEW INTERMEDIATES OBTAINED |
| EP0169755A2 (en) * | 1984-06-25 | 1986-01-29 | Roussel-Uclaf | 4-Hydroxy-3-quinoline-carboxylic-acid derivatives substituted at 2 by a nitrogen-containing group, their preparation, their use as medicaments, compositions containing them and intermediates |
| EP0169755A3 (en) * | 1984-06-25 | 1986-04-09 | Roussel-Uclaf | 4-hydroxy-3-quinoline-carboxylic-acid derivatives substituted at 2 by a nitrogen-containing group, their preparation, their use as medicaments, compositions containing them and intermediates |
| US5011931A (en) * | 1987-11-18 | 1991-04-30 | The Boots Company Plc | Process for the preparation of 1-methyl-3-methylthio-4-quinolone and the sulfinyl, and sulfonyl analogs thereof |
| US5079264A (en) * | 1987-11-18 | 1992-01-07 | The Boots Co. Plc | Chemical process |
| EP2322516B1 (en) * | 2005-07-29 | 2015-09-23 | Janssen Sciences Ireland UC | Intermediates for the preparation of Macrocyclic inhibitors of hepatitis c virus |
| US8207342B2 (en) | 2009-03-10 | 2012-06-26 | Gruenenthal Gmbh | Substituted 3-amino-2-mercaptoquinolines as KCNQ2/3 modulators |
| US8399673B2 (en) | 2009-03-12 | 2013-03-19 | Gruenenthal Gmbh | Substituted 2-mercaptoquinoline-3-carboxamides as KCNQ2/3 modulators |
| US8586755B2 (en) | 2009-03-12 | 2013-11-19 | Grünenthal GmbH | Substituted nicotinamides as KCNQ2/3 modulators |
| WO2010102811A1 (en) | 2009-03-12 | 2010-09-16 | Grünenthal GmbH | Substituted 2-mercaptoquinoline-3-carboxamides as kcnq2/3 modulators |
| TWI461197B (en) * | 2009-03-12 | 2014-11-21 | 2-mercaptoquinoline-3-carboxamide as a KCNQ2 / 3 modifier | |
| US8178684B2 (en) | 2009-03-12 | 2012-05-15 | Gruenenthal Gmbh | Substituted nicotinamides as KCNQ2/3 modulators |
| CN102348692A (en) * | 2009-03-12 | 2012-02-08 | 格吕伦塔尔有限公司 | Substituted 2-mercaptoquinoline-3-carboxamides as kcnq2/3 modulators |
| US8247573B2 (en) | 2009-03-12 | 2012-08-21 | Gruenenthal Gmbh | Substituted N-(2-mercaptopyridin-3-yl)amides as KCNQ2/3 modulators |
| JP2012520249A (en) * | 2009-03-12 | 2012-09-06 | グリュネンタール・ゲゼルシャフト・ミト・ベシュレンクテル・ハフツング | Substituted 2-mercaptoquinoline-3-carboxamides as KCNQ2 / 3 modulators |
| US8957090B2 (en) | 2009-11-12 | 2015-02-17 | Ucb Pharma S.A. | Fused bicyclic pyridine and pyrazine derivatives as kinase inhibitors |
| WO2011058113A1 (en) * | 2009-11-12 | 2011-05-19 | Ucb Pharma S.A. | Fused bicyclic pyridine and pyrazine derivatives as kinase inhibitors |
| US8653101B2 (en) | 2010-08-27 | 2014-02-18 | Gruenenthal Gmbh | Substituted 2-oxy-quinoline-3-carboxamides as KCNQ2/3 modulators |
| WO2012025236A1 (en) | 2010-08-27 | 2012-03-01 | Grünenthal GmbH | Substituted 2-oxy-quinoline-3-carboxamides as kcnq2/3 modulators |
| JP2013536212A (en) * | 2010-08-27 | 2013-09-19 | グリュネンタール・ゲゼルシャフト・ミト・ベシュレンクテル・ハフツング | Substituted quinoline-3-carboxamides as KCNQ2 / 3 modulators |
| JP2013536211A (en) * | 2010-08-27 | 2013-09-19 | グリュネンタール・ゲゼルシャフト・ミト・ベシュレンクテル・ハフツング | Substituted 2-amino-quinoline-3-carboxamides as KCNQ2 / 3 modulators |
| US8445512B2 (en) | 2010-08-27 | 2013-05-21 | Gruenenthal Gmbh | Substituted quinoline-3-carboxamides as KCNQ2/3 modulators |
| RU2595894C2 (en) * | 2010-08-27 | 2016-08-27 | Грюненталь Гмбх | Substituted 2-oxy-quinoline-3-carboxamides as kcnq2/3 modulators |
| US8470852B2 (en) | 2010-08-27 | 2013-06-25 | Gruenenthal Gmbh | Substituted 2-amino-quinoline-3-carboxamides as KCNQ2/3 modulators |
| CN103068804A (en) * | 2010-08-27 | 2013-04-24 | 格吕伦塔尔有限公司 | Substituted 2-oxy-quinoline-3-carboxamides as kcnq2/3 modulators |
| US8653102B2 (en) | 2010-08-27 | 2014-02-18 | Gruenenthal Gmbh | Substituted 2-oxo- and 2-thioxo-dihydroquinoline-3-carboxamides as KCNQ2/3 modulators |
| WO2012025238A1 (en) | 2010-08-27 | 2012-03-01 | Grünenthal GmbH | Substituted quinoline-3-carboxamides as kcnq2/3 modulators |
| US9073862B2 (en) | 2010-08-27 | 2015-07-07 | Gruenenthal Gmbh | Substituted 2-oxy-quinoline-3-carboxamides as KCNQ2/3 modulators |
| AU2011295406B2 (en) * | 2010-08-27 | 2015-08-06 | Grunenthal Gmbh | Substituted 2-amino-quinoline-3-carboxamides as KCNQ2/3 modulators |
| CN103068804B (en) * | 2010-08-27 | 2015-08-19 | 格吕伦塔尔有限公司 | As the 2-oxy-quinoline-3-methane amide of the replacement of KCNQ2/3 conditioning agent |
| WO2012025237A1 (en) | 2010-08-27 | 2012-03-01 | Grünenthal GmbH | Substituted 2-amino-quinoline-3-carboxamides as kcnq2/3 modulators |
| US8618129B2 (en) | 2010-09-01 | 2013-12-31 | Gruenenthal Gmbh | Substituted 1-oxo-dihydroisoquinoline-3-carboxamides as KCNQ2/3 modulators |
Also Published As
| Publication number | Publication date |
|---|---|
| FR2532939B1 (en) | 1985-02-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA1089464A (en) | Process for the preparation of novel derivatives of 3- quinolein carboxylic acid | |
| EP0115997B1 (en) | Derivatives of omega mercaptopropanamides, and their homologues, process for their preparation, their use as medicines, compositions containing them and intermediates obtained | |
| EP0040573B1 (en) | 2-substituted-4-hydroxy-3-quinolinecarboxylic acids, their preparation, their use as medicaments, compositions containing them and intermediates | |
| EP0012639B1 (en) | Quinolein-3-carboxylic acid derivatives, process for their preparation, their use in medicines and pharmaceutical compositions containing them | |
| FR2532939A1 (en) | New 4-hydroxy-3-quinolinecarboxylic acid derivatives substituted at position 2, their preparation, their use as medicaments, compositions containing them and new intermediates obtained | |
| CA1204116A (en) | Process for preparing new 2-substituted 4-hydroxy 3-quinoline carboxylic acid derivatives | |
| EP0573318A1 (en) | Phenyl carboxamide isoxazole derivatives and salts, process for their preparation and the new intermediates thereof. Their use as pharmaceuticals and pharmaceutical compositions containing them | |
| EP0214004B1 (en) | 4-oh-quinoline-carboxylic-acid derivatives substituted in position 2 by a dihydroxy-substituted group, possibly etherified or esterified, process and intermediates for their preparation, their use as medicaments and compositions containing them | |
| CH675245A5 (en) | ||
| CA1215648A (en) | Pharmaceutical composition containing amid derivatives of mercaptoacetic and 3-mercaptoacetic acids | |
| EP0169755B1 (en) | 4-hydroxy-3-quinoline-carboxylic-acid derivatives substituted at 2 by a nitrogen-containing group, their preparation, their use as medicaments, compositions containing them and intermediates | |
| EP0196943B1 (en) | 8-thiotetrahydroquinoleine derivatives and their salts | |
| EP0159254B1 (en) | Derivatives of omega-mercaptopropanamide and their salts, their preparation, their use as medicines and compositions containing them | |
| EP0183584B1 (en) | Esters of derivatives of 2-alpha-hydroxy-substituted 4-hydroxy-3-quinoline carboxylic acid, their preparation, their use as medicaments and compositions containing them | |
| CA1105022A (en) | Process for the preparation of novel benzophenone derivatives | |
| CA1064489A (en) | Process for the preparation of new benzenesulfonamides | |
| FR2600065A1 (en) | New derivatives of 5-[(2-benzoyfuranyl)carbonyl]thiopheneacetic acid, their salts, processes for their preparation, their application as medicaments and the pharmaceutical compositions containing them | |
| FR2551437A2 (en) | New position 2-substituted 4-hydroxy-3-quinolinecarboxylic acid derivatives, new process for preparing them, their use as medicinal products, the compositions containing them and products required for their preparation | |
| FR2636329A2 (en) | New pyridine derivatives, process for their preparation, their application as medicaments and the compositions containing them | |
| FR2532314A1 (en) | New process for preparing 3-quinolinecarboxylic acid derivatives, new halogenated 3-quinolinecarboxylic acid derivatives, their use as medicaments, pharmaceutical compositions containing them and new intermediates obtained | |
| CH636350A5 (en) | 2 - / (4-QUINOLEINYL) AMINO / 5-FLUOROBENZOIC ACID DERIVATIVES, THEIR PREPARATION PROCESSES AND THE PHARMACEUTICAL COMPOSITIONS CONTAINING THEM. | |
| FR2611712A1 (en) | NOVEL N-SUBSTITUTED ALPHA-MERCAPTOMETHYL BENZENE PROPANAMIDE DERIVATIVES, PROCESS FOR PREPARING THEM, THEIR APPLICATION AS MEDICAMENTS AND THE COMPOSITIONS COMPRISING THE SAME | |
| FR2589468A1 (en) | New 2-substituted 2-(acylamino)ethanethiol derivatives, process for their preparation, their application as medicaments and the pharmaceutical compositions which contain them | |
| FR2564835A1 (en) | Novel 4-hydroxy-3-quinolinecarboxylic acid derivatives substituted at the 2-position with a sulphur-containing group, process for their preparation, their application as medicaments and the compositions which contain them | |
| FR2672595A1 (en) | New nitrogenous bicyclic derivatives substituted with a benzyl radical, process for their preparation, the new intermediates obtained and their application as medicaments |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| CA | Change of address | ||
| CD | Change of name or company name | ||
| ST | Notification of lapse |