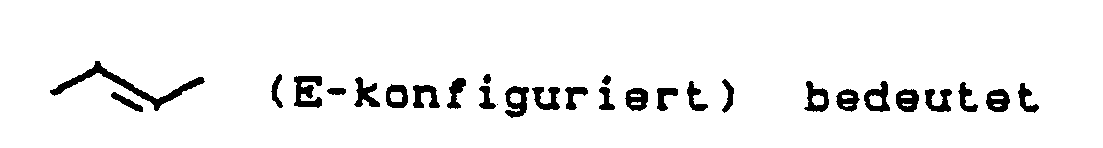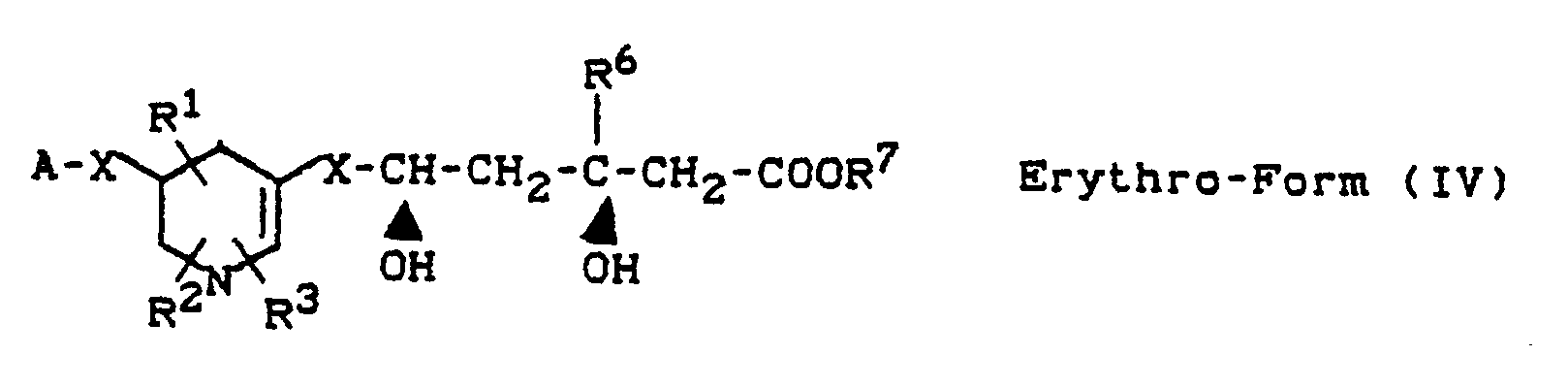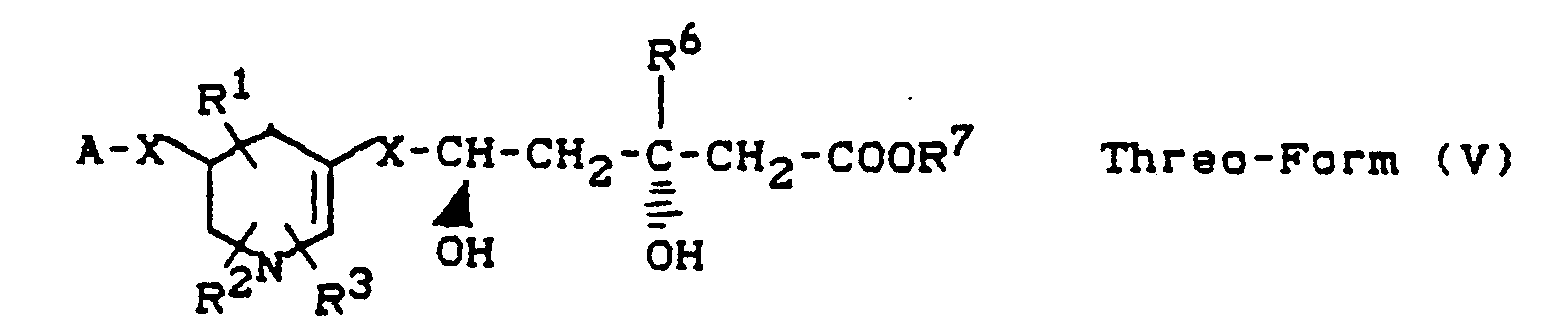EP0325129A2 - Disubstituted pyridines - Google Patents
Disubstituted pyridines Download PDFInfo
- Publication number
- EP0325129A2 EP0325129A2 EP89100249A EP89100249A EP0325129A2 EP 0325129 A2 EP0325129 A2 EP 0325129A2 EP 89100249 A EP89100249 A EP 89100249A EP 89100249 A EP89100249 A EP 89100249A EP 0325129 A2 EP0325129 A2 EP 0325129A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- alkyl
- trifluoromethyl
- aryl
- substituted
- alkylsulfonyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 C*C(C(*)CC(C=C1)=CCC1F)O Chemical compound C*C(C(*)CC(C=C1)=CCC1F)O 0.000 description 7
- XQPGXDOHVAAMDH-UHFFFAOYSA-N CC(C)C(C1CO)=NC(C(C)C)=C(C)C1C1C=CCCC1 Chemical compound CC(C)C(C1CO)=NC(C(C)C)=C(C)C1C1C=CCCC1 XQPGXDOHVAAMDH-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/54—Radicals substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/55—Acids; Esters
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
Definitions
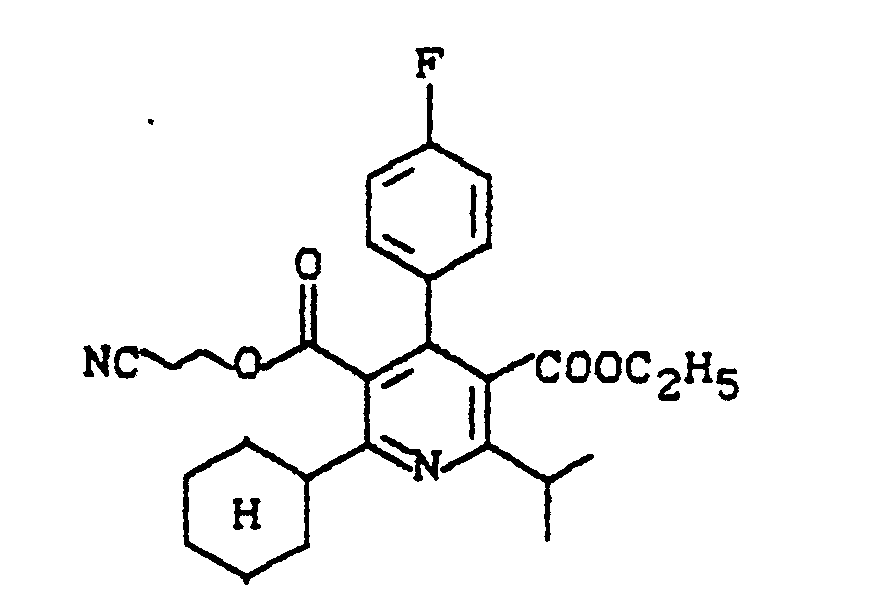
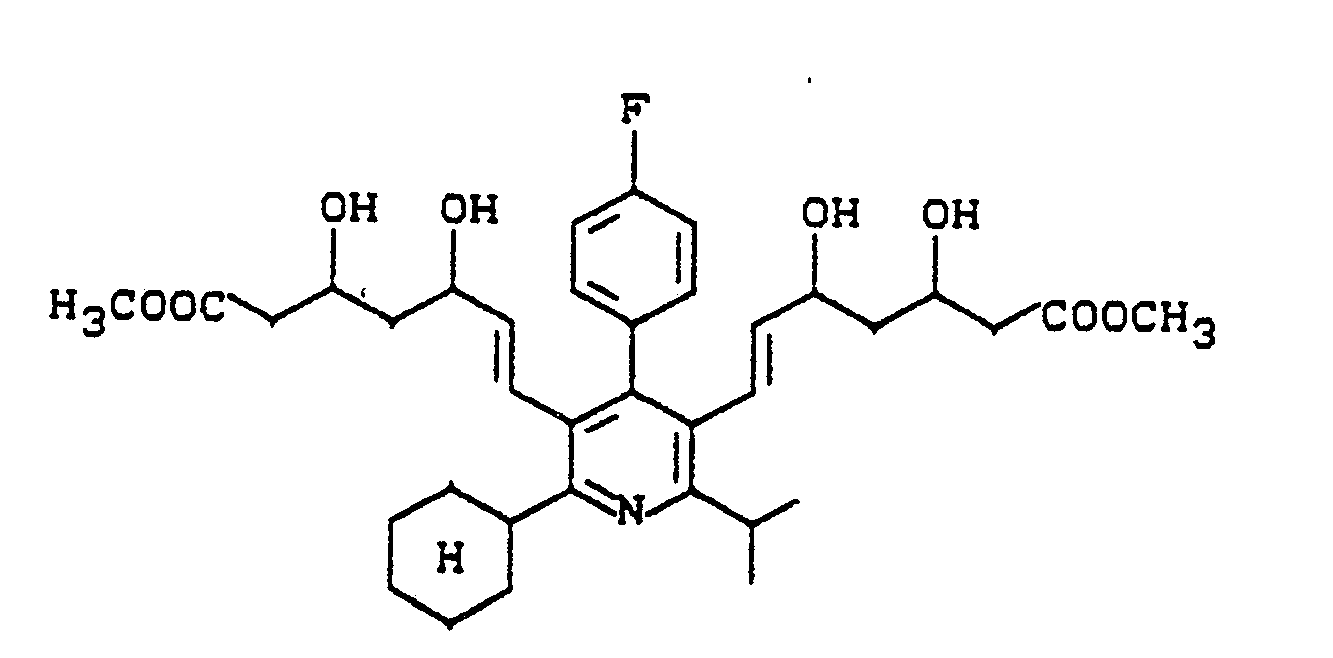
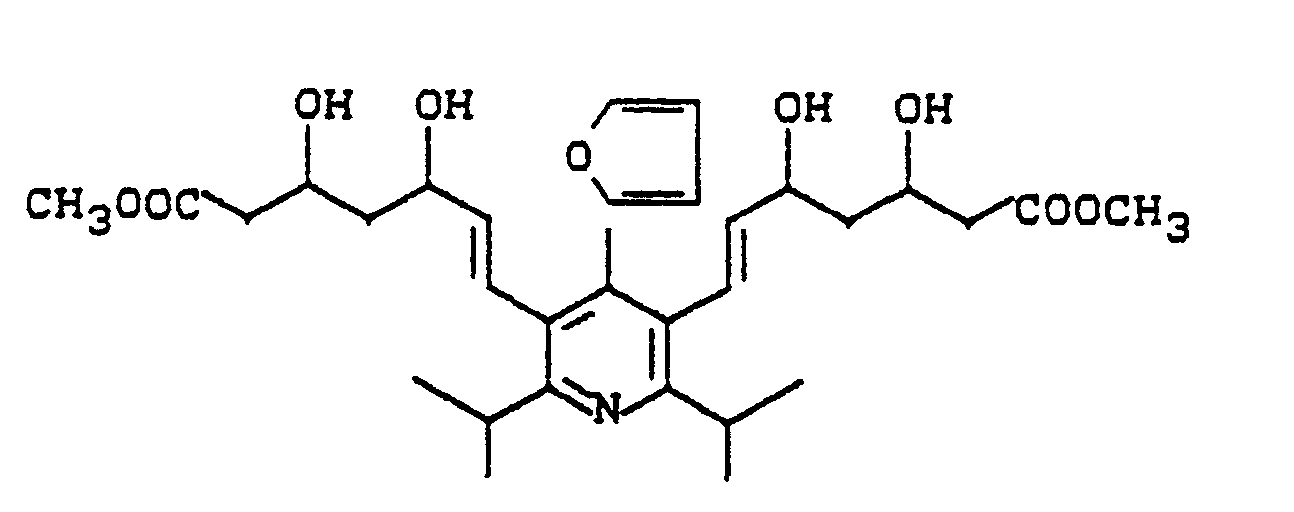
- the invention relates to disubstituted pyridines, intermediates for their preparation, their preparation and their use in medicaments.
- lactone derivatives isolated from fungal cultures are inhibitors of 3-hydroxy-3-methyl-glutaryl coenzyme A reductase (HMG-CoA reductase) [Mevinolin, EP-A 22 478; US 4,231,938].
- HMG-CoA reductase 3-hydroxy-3-methyl-glutaryl coenzyme A reductase
- certain indole derivatives or pyrazole derivatives are inhibitors of HMG-CoA reductase [EP-A 1 114 027; US 4,613,610].
- the disubstituted pyridines according to the invention show a superior inhibitory effect on the HMG-CoA reductase (3-hydroxy-3-methyl-glutaryl coenzyme A reductase).
- Cycloalkyl generally represents a cyclic hydrocarbon radical with 3 to 8 carbon atoms.
- the cyclopropyl, cyclopentane and cyclohexane rings are preferred. Examples include cyclopropyl, cyclopentyl, cyclohexyl, cycloheptyl and cyclooctyl.
- Alkyl generally represents a straight-chain or branched hydrocarbon radical having 1 to 12 carbon atoms. Lower alkyl having 1 to about 6 carbon atoms is preferred. Examples include methyl, ethyl, propyl, isopropyl, butyl, isobutyl, pentyl, isopentyl, hexyl, isohexyl, heptyl, isoheptyl, octyl and isooctyl.
- Alkoxy generally represents a straight-chain or branched hydrocarbon radical having 1 to 12 carbon atoms which is bonded via an oxygen atom. Lower alkoxy having 1 to about 6 carbon atoms is preferred. An alkoxy radical having 1 to 4 carbon atoms is particularly preferred. Examples include methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy, pentoxy, isopentoxy, hexoxy, isohexoxy, heptoxy, isoheptoxy, octoxy or isooctoxy.
- Alkylthio generally represents a straight-chain or branched hydrocarbon radical having 1 to 12 carbon atoms which is bonded via a sulfur atom. Lower alkylthio having 1 to about 6 carbon atoms is preferred. An alkylthio radical having 1 to 4 carbon atoms is particularly preferred. Examples include methylthio, ethylthio, propylthio, isopropylthio, butylthio, isobutylthio, pentylthio, isopentylthio, hexylthio, isohexylthio, heptylthio, isoheptylthio, octylthio or isooctylthio.
- Alkylsulfonyl generally represents a straight-chain or branched hydrocarbon radical having 1 to 12 carbon atoms, which is bonded via an S0 2 group. Lower alkylsulfonyl having 1 to about 6 carbon atoms is preferred. Examples include: methylsulfonyl, ethylsulfonyl, propylsulfonyl, isopropylsulfonyl, butylsulfonyl, isobutylsulfonyl, pentylsulfonyl, isopentylsulfonyl, hexylsulfonyl, isohexylsulfonyl.
- Sulfamoyl (aminosulfonyl) stands for the group -S0 2 -NH2.
- Aryl generally represents an aromatic radical having 6 to about 12 carbon atoms.
- Preferred aryl radicals are phenyl, naphthyl and biphenyl.
- Aryloxy generally represents an aromatic radical having 6 to about 12 carbon atoms, which is bonded via an oxygen atom.
- Preferred aryloxy radicals are phenoxy or naphthyloxy.
- Arylthio generally represents an aromatic radical having 6 to about 12 carbon atoms, to which a sulfur atom is attached.
- Preferred arylthio radicals are phenylthio or naphthylthio.
- Arylsulfonyl generally represents an aromatic radical having 6 to about 12 carbon atoms, which is bonded via an S0 2 group. Examples include: phenylsulfonyl, naphthylsulfonyl and biphenylsulfonyl.
- Aralkyl generally represents an aryl radical having 7 to 14 carbon atoms bonded via an alkylene chain.
- Aralkyl radicals having 1 to 6 carbon atoms in the aliphatic part and 6 to 12 carbon atoms in the aromatic part are preferred.
- the following aralkyl radicals may be mentioned, for example: benzyl, naphthylmethyl, phenethyl and phenylpropyl.
- Aralkoxy generally represents an aralkyl radical having 7 to 14 carbon atoms, the alkylene chain being bonded via an oxygen atom.
- Aralkoxy radicals having 1 to 6 carbon atoms in the aliphatic part and 6 to 1'2 carbon atoms in the aromatic part are preferred.
- the following aralkoxy radicals may be mentioned, for example: benzyloxy, naphthylmethoxy, phenethoxy and phenylpropoxy.
- Aralkylthio generally represents an aralkyl radical having 7 to about 14 carbon atoms, the alkyl chain being bonded via a sulfur atom.
- Aralkylthio radicals having 1 to 6 carbon atoms in the aliphatic part and 6 to 12 carbon atoms in the aromatic part are preferred. Examples include the following aralkylthio radicals: benzylthio, naphthylmethylthio, phenethylthio and phenylpropylthio.
- Aralkylsulfonyl generally represents an aralkyl radical having 7 to about 14 carbon atoms, the alkyl radicals being bonded via an SO 2 chain.
- Aralkylsulfonyl radicals having 1 to 6 carbon atoms in the aliphatic part and 6 to 12 carbon atoms in the aromatic part are preferred. Examples include the following aralkylsulfonyl radicals: benzylsulfonyl, naphthylmethylsulfonyl, phenethylsulfonyl and phenylpropylsulfonyl.
- Acyl generally represents phenyl or straight-chain or branched lower alkyl having 1 to about 6 carbon atoms which are bonded via a carbonyl group. Phenyl and alkyl radicals having up to 4 carbon atoms are preferred. Examples include: benzoyl, acetyl, ethylcarbonyl, propylcarbonyl, isopropylcarbonyl, butylcarbonyl and isobutylcarbonyl.
- Halogen generally represents fluorine, chlorine, bromine or iodine, preferably fluorine, chlorine or bromine. Halogen is particularly preferably fluorine or chlorine.
- Heteroaryl generally represents a 5- to 6-membered aromatic ring which can contain oxygen, sulfur and / or nitrogen as heteroatoms and to which further aromatic rings can be fused.
- 5- and 6-membered aromatic rings are preferred which contain an oxygen, a sulfur and or up to 2 nitrogen atoms and which are optionally benzo-condensed.
- heteroaryl residues are: thienyl, furyl, pyrolyl, pyrazolyl, pyridyl, pyrimidyl, pyridazinyl, quinolyl, isoquinolyl, quinazolyl, phthalazinyl, cinnolyl, thiazolyl, benzothiazolyl, isothiazoiyl, oxazylyl , Indolyl, and isoindolyl.
- the disubstituted pyridines of the general formula (I) according to the invention have several asymmetric carbon atoms and can therefore exist in various stereochemical forms. Both the individual isomers and their mixtures are the subject of the invention.
- Both the cis-lactone and the trans-lactone each exist.
- two isomers namely the 4R, 6R isomer or the 4S, 6S isomer (cis-lactone), and the 4R, 6S isomer or 4S, 6R isomer (trans-lactone).
- Preferred isomers are the trans lactones.
- the 4R, 6S isomer (trans) and the 4R, 6S-4S, 6R racemate are particularly preferred.
- the reduction can be carried out using the customary reducing agents, preferably those which are suitable for the reduction of ketones to hydroxy compounds.
- the reduction is preferably carried out with complex metal hydrides such as, for example, lithium boranate, sodium boranate, potassium boranate, zinc boranate, lithium trialkyl hydridoborates, sodium trialkyl hydridoborates, sodium cyano-trihydridoborate or lithium aluminum hydride.
- the reduction with sodium borohydride is very particularly preferably carried out in the presence of triethylborane.
- organic solvents which do not change under the reaction conditions are suitable as solvents.
- solvents preferably include ethers such as diethyl ether, dioxane, tetrahydrofuran or dimethoxyethane, or halogenated hydrocarbons such as dichloromethane, trichloromethane, carbon tetrachloride, 1,2-dichloroethane, or hydrocarbons such as benzene, toluene or xylene. It is also possible to use mixtures of the solvents mentioned.
- the reduction of the ketone group to the hydroxyl group is particularly preferably carried out under conditions in which the other functional groups such as the alkoxycarbonyl group are not changed.
- the use of sodium borohydride as reduc is particularly suitable for this tion agent, in the presence of triethylborane in inert solvents such as preferably ethers.
- the reduction is generally carried out in a temperature range from -80 ° C. to + 30 ° C., preferably from -78 ° C. to 0 ° C.
- the process according to the invention is generally carried out at normal pressure. However, it is also possible to carry out the process under negative pressure or under positive pressure (e.g. in a range from 0.5 to 5 bar).
- the reducing agent is used in an amount of 1 to 2 mol, preferably 1 to 1.5 mol, based on 1 mol of the keto compound.
- the carbonyl group is generally reduced to the hydroxyl group without the double bond being reduced to the single bond.
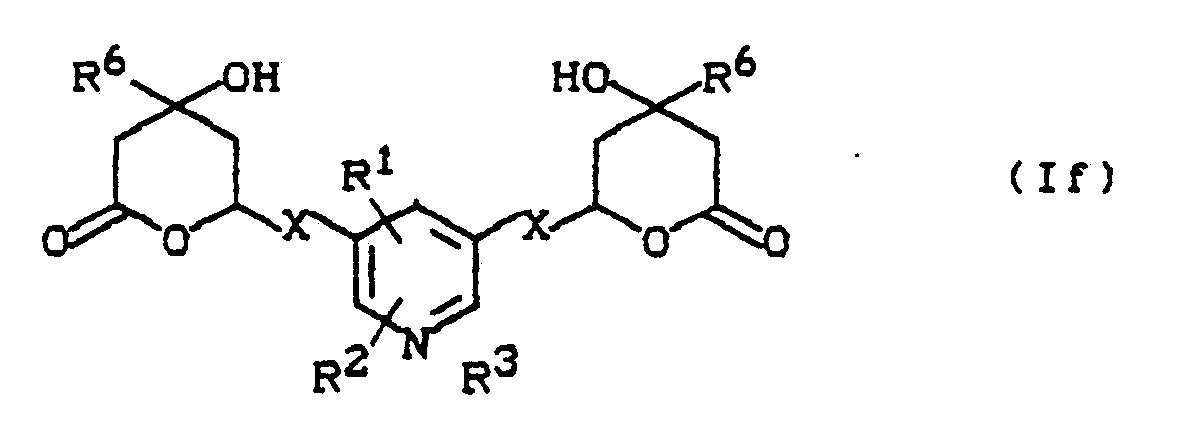
- the carboxylic acid esters of the general formula (Id) or the lactones of the general formula (If) are in general saponified by customary methods.
- the saponification is generally carried out by treating the esters or the lactones in inert solvents with customary bases, the salts of the general formula (Ie) generally being formed first, which are then treated in a second step with acid in the free acids of the general Formula (Ic) can be transferred.
- the usual inorganic bases are suitable as bases for the saponification.
- bases preferably include alkali metal hydroxides or alkaline earth metal hydroxides such as sodium hydroxide, potassium hydroxide or barium hydroxide, or alkali metal carbonates such as sodium or potassium carbonate or sodium hydrogen carbonate, or alkali metal alcoholates such as sodium ethanolate, sodium methoxide, potassium methoxide, potassium ethoxide or potassium tert-butoxide.
- alkali metal hydroxides or alkaline earth metal hydroxides such as sodium hydroxide, potassium hydroxide or barium hydroxide
- alkali metal carbonates such as sodium or potassium carbonate or sodium hydrogen carbonate
- alkali metal alcoholates such as sodium ethanolate, sodium methoxide, potassium methoxide, potassium ethoxide or potassium tert-butoxide.
- Sodium hydroxide or potassium hydroxide are particularly preferably used.
- Suitable solvents for the saponification are water or the organic solvents customary for saponification. These preferably include alcohols such as methanol, ethanol, propanol, isopropanol or butanol, or ethers such as tetrahydrofuran or dioxane, or dimethylformamide or dimethyl sulfoxide. Alcohols such as methanol, ethanol, propanol or isopropanol are particularly preferably used. It is also possible to use mixtures of the solvents mentioned.
- the saponification is generally carried out in a temperature range from 0 ° C. to + 100 ° C., preferably from + 20 ° C. to + 80 ° C.
- the saponification is generally carried out at normal pressure. However, it is also possible to work under negative pressure or overpressure (e.g. from 0.5 to 5 bar).
- the base is generally used in an amount of 1 to 3 mol, preferably 1 to 1.5 mol, based on 1 mol of the ester or lactone. Molar amounts of the reactants are particularly preferably used.
- the salts of the compounds (Ie) according to the invention are formed in the first step as intermediates which can be isolated.
- the acids (Ic) according to the invention are obtained by treating the salts (le) with customary inorganic acids. These preferably include mineral acids such as, for example, hydrochloric acid, hydrobromic acid, sulfuric acid or phosphoric acid.
- mineral acids such as, for example, hydrochloric acid, hydrobromic acid, sulfuric acid or phosphoric acid.
- carboxylic acids (Ic) it has proven advantageous here to acidify the basic reaction mixture of the saponification in a second step without isolating the salts. The acids can then be isolated in the usual way.
- the carboxylic acids (Ic) according to the invention are generally cyclized by customary methods, for example by heating the corresponding acid in inert organic solvents, if appropriate in the presence of molecular sieve.
- Suitable solvents here are hydrocarbons such as benzene, toluene, xylene, petroleum fractions, or tetralin or diglyme or triglyme. Benzene, toluene or xylene are preferably used. It is also possible to use mixtures of the solvents mentioned. Hydrocarbons, in particular toluene, are particularly preferably used in the presence of molecular sieve.
- the cyclization is generally in a temperature range from -40 ° C to + 200 ° C. preferably carried out from -25 C to + 50 ° C.
- the cyclization is generally carried out at normal pressure, but it is also possible to carry out the process under reduced pressure or under elevated pressure (e.g. in a range from 0.5 to 5 bar).
- the cyclization is also carried out in inert organic solvents with the aid of cyclizing or water-releasing agents.
- Carbodiimides are preferably used as water-releasing agents.
- Preferred carbondiimides are N, N'-dicyclohexylcarbodiimide paratoluenesulfonate, N-cyclohexyl-N '- [2- (N "-methylmorpholinium) ethyl] carbodiimide or N- (3-dimethylamino propyl) -N'-ethylcarbodiimide hydrochloride used.
- organic solvents are suitable as solvents. These preferably include ethers such as diethyl ether, tetrahydrofuran or dioxane, or chlorinated hydrocarbons such as methylene chloride, chloroform or carbon tetrachloride, or hydrocarbons such as benzene, toluene, xylene or petroleum fractions. Chlorinated hydrocarbons such as, for example, methylene chloride, chloroform or carbon tetrachloride, or hydrocarbons such as benzene, toluene, xylene, or petroleum fractions are particularly preferred. Chlorinated hydrocarbons such as methylene chloride, chloroform or carbon tetrachloride are particularly preferably used.
- the reaction is generally carried out in a temperature range from 0 ° C. to + 80 ° C., preferably from + 10 ° C. to + 50 ° C.
- the separation of the isomers into the stereoisomerically uniform constituents is generally carried out by customary methods as described, for example, by EL Eliel, Stereochemistry of Carbon Compounds, McGraw Hili, 1 962.
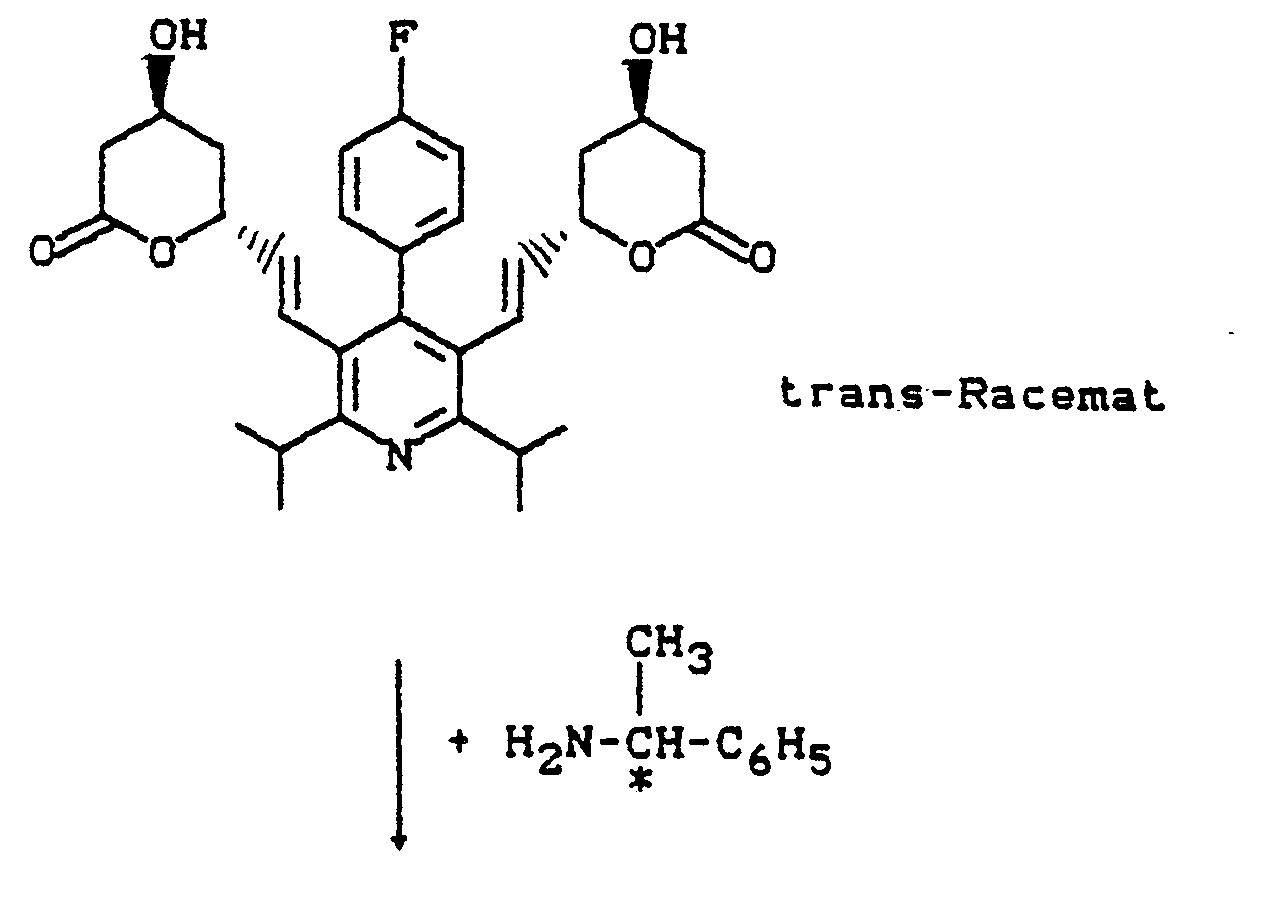
- the separation of the isomers at the racemic lactone stage is preferred.
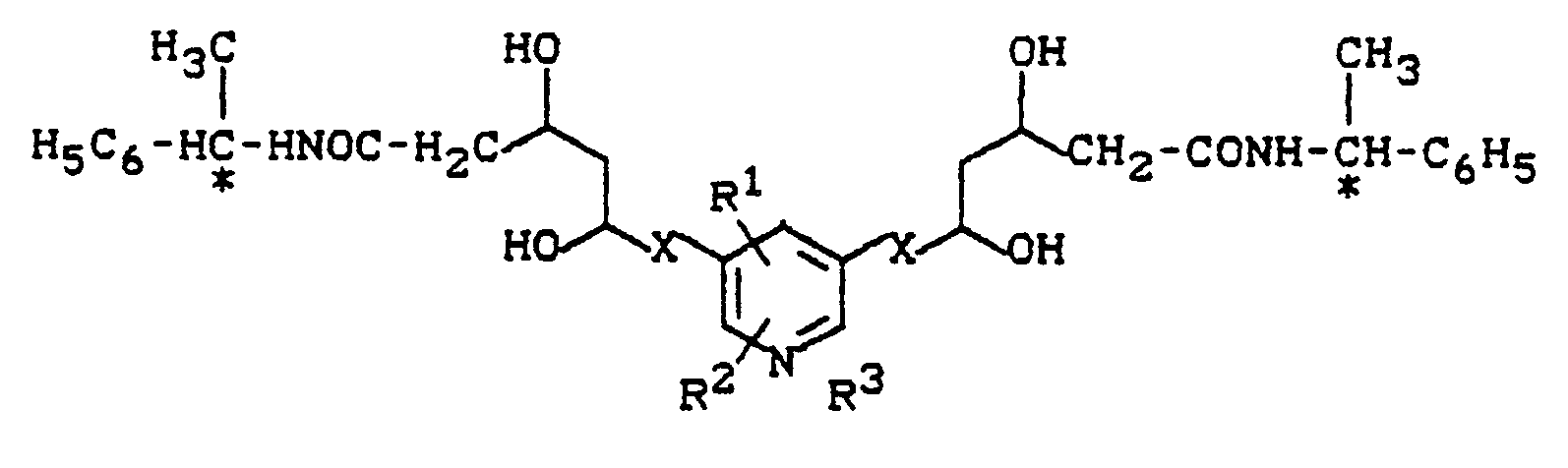
- the racemic mixture of the trans-lactones (VII) is particularly preferred here by treatment with either D - (+) - or L - (-) - a-methylbenzylamine by customary methods into the diastereomeric dihydroxyamides (Ig) transferred, which can then be separated into the individual diastereomers as usual by chromatography or crystallization.
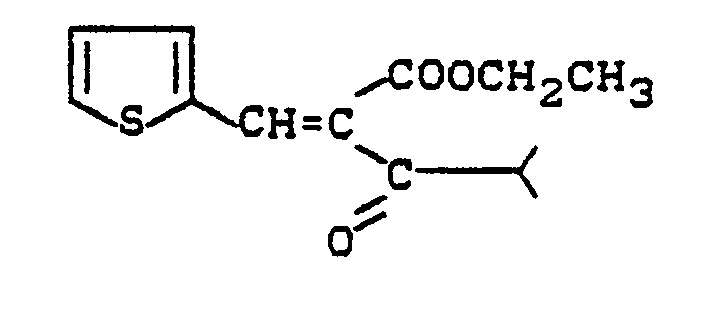
- ketones (VIII) used as starting materials are new.
- the bases here are the customary strongly basic compounds. These preferably include organolithium compounds such as N-butyllithium, sec-butyllithium, tert-butyllithium or phenyllithium, or amides such as lithium diisopropylamide, sodium amide or potassium amide, or lithium hexamethyldisilylamide, or alkali hydrides such as sodium hydride or potassium hydride. It is also possible to use mixtures of the bases mentioned. N-Butyllithium or sodium hydride or a mixture thereof is particularly preferably used.
- organic solvents which do not change under the reaction conditions are suitable as solvents.
- solvents preferably include ethers such as diethyl ether, tetrahydrofuran, dioxane or dimethoxyethane, or hydrocarbons such as benzene, toluene, xylene, cyclohexane, hexane or oil fractions. It is also possible to use mixtures of the solvents mentioned. Ethers such as diethyl ether or tetrahydrofuran are particularly preferably used.
- the reaction is generally carried out in a temperature range from -80 ° C. to + 50 ° C., preferably from -20 ° C. to + 30 ° C.
- the process is generally carried out under normal pressure, but it is also possible to carry out the process under negative pressure or under positive pressure, e.g. in a range from 0.5 to 5 bar.
- the acetoacetic ester is generally used in an amount of 1 to 2, preferably 1 to 1.5, mol, based on 1 mol of the aldehyde.
- acetoacetic esters of the formula (X) used as starting materials are known or can be prepared by known methods [Beilstein's Handbuch der organic Chemistry 111, 632; 438].
- acetoacetic esters for the process according to the invention are: methyl acetoacetate, ethyl acetoacetate, propyl acetoacetate, isopropyl acetoacetate.
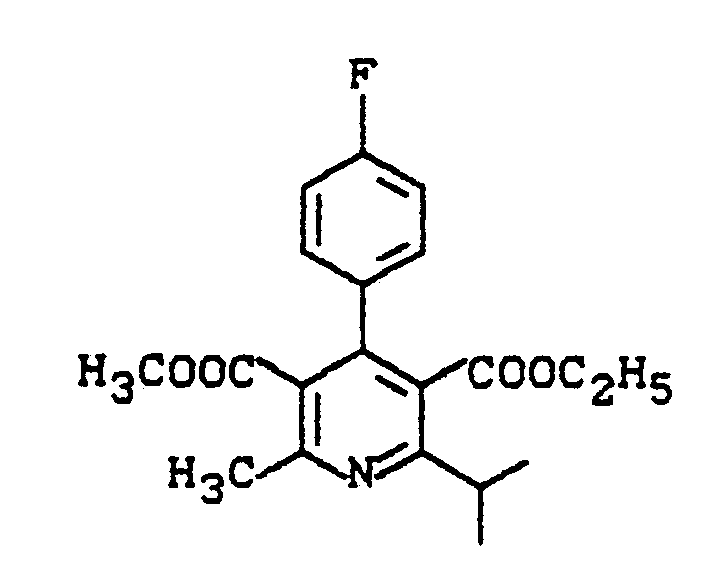
- the dihydropyridines of the general formula (X) are oxidized in suitable solvents with suitable oxidizing agents.
- the dihydropyridines are preferred in chlorinated hydrocarbons such as methylene chloride, with 2,2-dichloro-5,6-dicyan-p-benzoquinone at room temperature, or with chromium trioxide in glacial acetic acid at elevated temperatures, preferably under reflux temperature, to give the pyridines of the formula (XI) oxidized.
- the pyridines (XI) are dissolved in inert solvents such as ethers, for example diethyl ether, dioxane or tetrahydrofuran, preferably in tetrahydrofuran, with metal hydrides such as lithium aluminum hydride, sodium cyanoborohydride, diisobutyl aluminum hydride or sodium bis (2-methoxyethoxy) - dihydroaluminate, reduced in a temperature range from -80 ° C to + 40 ° C, preferably from -70 ° C to room temperature to the hydroxy compounds of the general formula (XII).
- inert solvents such as ethers, for example diethyl ether, dioxane or tetrahydrofuran, preferably in tetrahydrofuran
- metal hydrides such as lithium aluminum hydride, sodium cyanoborohydride, diisobutyl aluminum hydride or sodium bis (2-methoxyethoxy) - di
- the hydroxy compounds (XII) are prepared by known methods using oxidizing agents such as pyridinium chlorochromate, optionally in the presence of aluminum oxide, in inert solvents such as chlorinated hydrocarbons, preferably methylene chloride, at room temperature or using trifluoroacetic acid and dimethyl sulfoxide (Swern oxidation) or after other methods customary for the oxidation of hydroxymethyl compounds to aldehydes are oxidized to the aldehydes (XIII).
- oxidizing agents such as pyridinium chlorochromate
- aluminum oxide such as aluminum oxide
- inert solvents such as chlorinated hydrocarbons, preferably methylene chloride
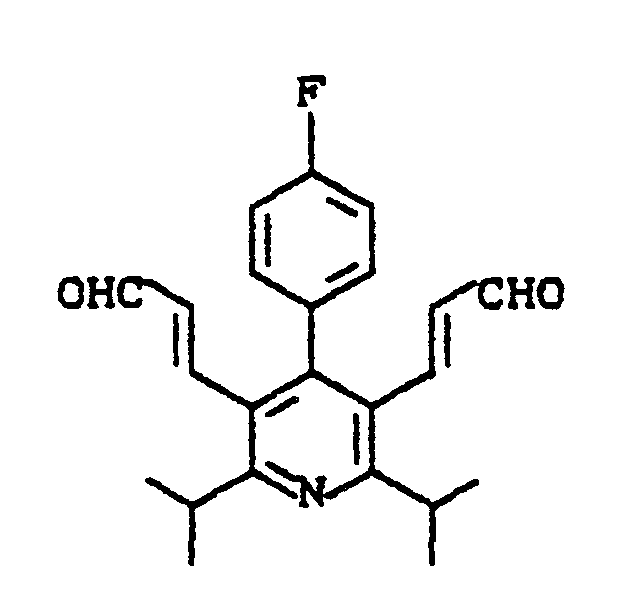
- the aldehydes (XIII) are reacted with diethyl 2- (cyclohexylamino) vinyl phosphonate in inert solvents such as ethers, preferably in tetrahydrofuran in the presence of sodium hydride, in a temperature range from -20 C to +30 ° C, preferably from -5 ° C to room temperature in the compounds (IX).
- inert solvents such as ethers, preferably in tetrahydrofuran in the presence of sodium hydride, in a temperature range from -20 C to +30 ° C, preferably from -5 ° C to room temperature in the compounds (IX).
- the dihydropyridines of the general formula (X) used as starting materials are known or can be prepared by known methods [EP-A 88 276; DE-A 28 47 236].
- the compounds of general formula (I) according to the invention are active ingredients for medicinal products.
- they are inhibitors of 3-hydroxy-3-methyl-glutaryl-coenzyme A (HGM-CoA) reductase and consequently inhibitors of cholesterol biosynthesis. They can therefore be used to treat hyperlipoproteinemia, lipoproteinemia or arteriosclerosis.
- the active compounds according to the invention also bring about a reduction in the cholesterol content in the blood.
- the new active compounds can be converted in a known manner into the customary formulations, such as tablets, dragées, pills, granules, aerosols, syrups, emulsions, suspensions and solutions, using inert, non-toxic, pharmaceutically suitable excipients or solvents.
- the therapeutically active compound should in each case be present in a concentration of about 0.5 to 98% by weight, preferably 1 to 90% by weight, of the total mixture, i.e. in amounts sufficient to achieve the dosage range indicated.
- the formulations are prepared, for example, by stretching the active ingredients with solvents and / or carriers, optionally using emulsifiers and / or dispersants, e.g. if water is used as the diluent, organic solvents can optionally be used as auxiliary solvents.
- tablets can of course also contain additives, such as sodium citrate, calcium carbonate and dicalcium phosphate, together with various additives, such as starch, preferably potato starch, gelatin and the like, in addition to the carrier substances mentioned.
- Lubricants such as magnesium stearate, sodium lauryl sulfate and talc can also be used for tableting.
- the active ingredients can be mixed with various flavor enhancers or colorants.
- solutions of the active ingredients can be used using suitable liquid carrier materials.
- Example 37 was prepared from the compound from Example 36 in analogy to the reactions from Examples 3, 27, 5, 6, 7, 8.
- Example 48 was prepared from the compound from Example 47 in analogy to the reactions from Examples 3, 27, 5, 6, 7, 8.
- Example 51 was prepared from the compound from Example 50 in analogy to the reactions from Examples 3, 27, 5, 7, 8.
- the enzyme activity determination was modified according to GC Ness et al., Archives of Biochemistry and Biophysics 197, 493-499 (1979).
- Male Ricorats (body weight 300-400 g) were treated for 11 days with altromin powder feed, to which 40 g cholestyramine / kg feed was added. After decapitation, the livers were removed from the animals and placed on ice. The livers were crushed and in the Potter-Elvejem homogenizer 3 times in 3 volumes of 0.1 m sucrose, 0.05 m KCI, 0.04 m K x Hy phosphate, 0.03 m ethylenediaminetetraacetic acid, 0.002 m dithiothreitol (SPE) Buffer pH 7.2, homogenized.
- SPE dithiothreitol
- the mixture was then centrifuged at 15,000 * g for 15 minutes and the sediment was discarded. The supernatant was sedimented at 100,000 g for 75 minutes.
- test compounds or mevinolin as reference substance
- dimethylformamide dissolved with the addition of 5 vol.% 1N NaOH and used with 10 ⁇ l in different concentrations in the enzyme test.
- the test was started after 20 minutes of pre-incubation of the compounds with the enzyme at 37 ° C.
- the test batch was 0.380 ml and contained 4 ⁇ mol glucose-6-phosphate, 1.1 mg bovine serum albumin, 2.1 ⁇ mol dithiothreitol, 0.35 ⁇ mol NADP, 1 unit glucose-6-phosphate dehydrogenase, 35 ⁇ mol K x hy-phosphate pH 7 , 2, 20 ul enzyme preparation and 56 nmol of 3-hydroxy-3-methyl-glutaryl coenzyme A (glutaryl-3- 14 C) 100 000 dpm.
- the mixture was incubated at 37 ° C. for 60 minutes and the reaction was stopped by adding 300 ⁇ l of 0.24 m HCl. After a post-incubation of 60 minutes at 37 0 C, the mixture was centrifuged and 600 .mu.l of the supernatant on a 0.7 x 4 cm with Biorex @ 5-chloride 100-200 mesh (anion exchange) column filled applied. It was distilled with 2 ml. Wash the water and add 3 ml Aquasol to the flow plus wash water and count in the LKB scintillation counter. IC 50 values were determined by plotting the percentage inhibition against the concentration of the compound in the test by intrapolation. To determine the relative inhibitory potency, the IC 50 value of the reference substance mevinolin was set to 100 and compared with the simultaneously determined IC 50 value of the test compound.
- the subchronic effect of disubstituted pyridines on blood cholesterol levels in dogs was tested in feeding experiments lasting several weeks.
- the substance to be investigated was administered once daily in a capsule to healthy beagle dogs together with the food p.o. given.
- the feed was also present during the entire trial period, i.e. Before, during and after the application period of the substance to be investigated, colestyramine (4 g / 100 g feed) was added as a bile acid sequestrant. Venous blood was drawn from the dogs twice a week and the serum cholesterol was determined enzymatically. The serum cholesterol values during the application period were compared with the serum cholesterol values before the application period (controls).
Abstract
Description
Die Erfindung betrifft disubstituierte Pyridine, Zwischenverbindungen zu ihrer Herstellung, ihre Herstellung und ihre Verwendung in Arzneimitteln.The invention relates to disubstituted pyridines, intermediates for their preparation, their preparation and their use in medicaments.
Es ist bekannt, daß aus Pilzkulturen isolierte Lactonderivate Inhibitoren der 3-Hydroxy-3-methyl-glutaryl Coenzym A Reduktase (HMG-CoA-Reduktase) sind [Mevinolin, EP-A 22 478; US 4 231 938]. Darüberhinaus sind auch bestimmte Indolderivate bzw. Pyrazolderivate Inhibitoren der HMG-CoA-Reduktase [EP-A 1 114 027; US 4 613 610].It is known that lactone derivatives isolated from fungal cultures are inhibitors of 3-hydroxy-3-methyl-glutaryl coenzyme A reductase (HMG-CoA reductase) [Mevinolin, EP-A 22 478; US 4,231,938]. In addition, certain indole derivatives or pyrazole derivatives are inhibitors of HMG-CoA reductase [EP-A 1 114 027; US 4,613,610].
Es wurden nun disubstituierte Pyridine der allgemeinen Formel (I),
- R' - Heteroaryl bedeutet, das bis zu 3-fach gleich oder verschieden durch Halogen, Alkyl, Alkoxy, Alkylthio, Alkylsulfonyl, Aryl, Aryloxy, Arylthio, Arylsulfonyl, Trifluormethyl, Trifluormethoxy, Trifluormethylthio, Alkoxycarbonyl oder durch eine Gruppe der Formel -NR4R5 substituiert sein kann, worin
- R4, RS - gleich oder verschieden sind und Alkyl, Aryl, Aralkyl, Acyl, Alkylsulfonyl oder Arylsulfonyl bedeuten, oder
- - Aryl bedeutet, das bis zu 5-fach gleich oder verschieden substituiert sein kann durch Alkyl, Alkoxy, Alkylthio, Alkylsulfonyl, Aryl, Aryloxy, Arylthio, Arylsulfonyl, Aralkyl, Aralkoxy, Aralkylthio, Aralkylsulfonyl, Halogen, Cyano, Nitro, Trifluormethyl, Trifluormethoxy, Trifluormethylthio, Alkoxycarbonyl, Sulfamoyl, Dialkylsulfamoyl, Carbamoyl, Dialkylcarbamoyl oder durch eine Gruppe der Formel -NR4R5, worin
- R4 und R5 die oben angegebene Bedeutung haben,
- R2 - Cycloalkyl bedeutet, oder
- - Alkyl bedeutet, das substituiert sein kann durch Halogen, Cyano, Alkoxy, Alkylthio, Alkylsulfonyl, Trifluormethyl, Trifluormethoxy, Trifluormethylthio, Trifluormethylsulfonyl, Alkoxycarbonyl, Acyl oder durch eine Gruppe der Formel -NR4R5, worin
- R4, Rs - gleich oder verschieden sind und Alkyl, Aryl, Aralkyl, Acyl, Alkylsulfonyl oder Arylsulfonyl bedeuten,
- oder durch Carbamoyl, Dialkylcarbamoyl, Sulfamoyl, Dialkylsulfamoyl, Heteroaryl, Aryl, Aryloxy, Arylthio, Arylsulfonyl, Aralkoxy, Aralkylthio oder Aralkylsulfonyl, wobei die Heteroaryl- und Arylreste der letztgenannten Substituenten bis zu 3-fach gleich oder verschieden durch Halogen, Cyano, Trifluormethyl, Trifluormethoxy, Alkyl, Alkoxy, Alkylthio oder Alkylsulfonyl substituiert sein können,
- R3 - Wasserstoff bedeutet, oder
- - Cycloalkyl bedeutet, oder
- - Alkyl bedeutet, das substituiert sein kann durch Halogen, Cyano, Alkoxy, Alkylthio, Alkylsulfonyl, Trifluormethyl, Trifluormethoxy, Trifluormethylthio, Trifluormethylsulfonyl, Alkoxycarbonyl, Acyl oder durch eine Gruppe der Formel -NR4.RS, worin
- R4, R5 die oben angegebene Bedeutung haben,
- oder durch Carbamoyl, Dialkylcarbamoyl, Sulfamoyl, Dialkylsulfamoyl, Heteroaryl, Aryl, Aryloxy, Arylthio, Arylsulfonyl, Aralkoxy, Aralkylthio oder Aralkylsulfonyl, wobei die Heteroaryl- und Arylreste bis zu 3-fach gleich oder verschieden durch Halogen, Cyano, Trifluormethyl, Trifluormethoxy, Alkyl, Alkoxy, Alkylthio oder Alkyisulfonyl substituiert sein können, oder
- - Heteroaryl bedeutet, das bis zu 3-fach gleich oder verschieden durch Halogen, Alkyl, Alkoxy, Alkylthio, Alkylsulfonyl, Aryl, Aryloxy, Arylthio, Arylsulfonyl, Trifluormethyl, Trifluormethoxy, Trifluormethylthio, Alkoxycarbonyl oder durch eine Gruppe der Formel -NR4R5 substituiert sein kann, worin
- R4 und R5 die oben angegebene Bedeutung haben, oder
- - Aryl bedeutet, das bis zu 5-fach gleich oder verschieden substituiert sein kann durch Alkyl, Alkoxy, Alkylthio, Alkylsulfonyl, Aryl, Aryloxy, Arylthio, Arylsulfonyl, Aralkyl, Aralkoxy, Aralkylthio, Aralkylsulfonyl, Halogen, Cyano, Nitro, Trifluormethyl, Trifluormethoxy, Trifluormethylthio, Alkoxycarbonyl, Sulfamoyl, Dialkylsulfamoyl, Carbamoyl, Dialkylcarbamoyl oder durch eine Gruppe der Formel -NR¢RS, worin
- R4 und R5 die oben angegebene Bedeutung haben,
- X - eine Gruppe der Formel -CH2-CH2- oder -CH = CH- bedeutet, und
- A - eine Gruppe der Formel
- R6 - für Wasserstoff oder Alkyl steht, und
- R7 - für Wasserstoff steht oder
- - für Alkyl, Aryl oder Aralkyl steht oder
- - für ein Kation steht, gefunden.
- R '- Heteroaryl means up to 3 times the same or different by halogen, alkyl, alkoxy, alkylthio, alkylsulfonyl, aryl, aryloxy, arylthio, arylsulfonyl, trifluoromethyl, trifluoromethoxy, trifluoromethylthio, alkoxycarbonyl or by a group of the formula -NR 4 R 5 may be substituted, wherein
- R 4 , R S - are the same or different and are alkyl, aryl, aralkyl, acyl, alkylsulfonyl or arylsulfonyl, or
- - Aryl means that up to 5-fold can be substituted identically or differently by alkyl, alkoxy, alkylthio, alkylsulfonyl, aryl, aryloxy, arylthio, arylsulfonyl, aralkyl, aralkoxy, aralkylthio, aralkylsulfonyl, halogen, cyano, nitro, trifluoromethyl, trifluoromethoxy , Trifluoromethylthio, alkoxycarbonyl, sulfamoyl, dialkylsulfamoyl, carbamoyl, dialkylcarbamoyl or by a group of the formula -NR 4 R 5 , wherein
- R 4 and R 5 have the meaning given above,
- R 2 denotes cycloalkyl, or
- - Alkyl means which can be substituted by halogen, cyano, alkoxy, alkylthio, alkylsulfonyl, trifluoromethyl, trifluoromethoxy, trifluoromethylthio, trifluoromethylsulfonyl, alkoxycarbonyl, acyl or by a group of the formula -NR 4 R 5 , in which
- R 4 , R s are the same or different and are alkyl, aryl, aralkyl, acyl, alkylsulfonyl or arylsulfonyl,
- or by carbamoyl, dialkylcarbamoyl, sulfamoyl, dialkylsulfamoyl, heteroaryl, aryl, aryloxy, arylthio, arylsulfonyl, aralkoxy, aralkylthio or aralkylsulfonyl, the heteroaryl and aryl radicals of the latter substituents being up to 3 times the same, different by tri-fluoro, identical or different by Trifluoromethoxy, alkyl, alkoxy, alkylthio or alkylsulfonyl can be substituted,
- R 3 represents hydrogen, or
- - Cycloalkyl means or
- - Alkyl means which can be substituted by halogen, cyano, alkoxy, alkylthio, alkylsulfonyl, trifluoromethyl, trifluoromethoxy, trifluoromethylthio, trifluoromethylsulfonyl, alkoxycarbonyl, acyl or by a group of the formula -NR4.RS, wherein
- R 4 , R 5 have the meaning given above,
- or by carbamoyl, dialkylcarbamoyl, sulfamoyl, dialkylsulfamoyl, heteroaryl, aryl, aryloxy, arylthio, arylsulfonyl, aralkoxy, aralkylthio or aralkylsulfonyl, wherein the heteroaryl and aryl groups of up to 3 times by identical or different halogen, cyano, trifluoromethyl, trifluoromethoxy, alkyl , Alkoxy, alkylthio or alkylsulfonyl may be substituted, or
- - Heteroaryl means up to 3 times the same or different by halogen, alkyl, alkoxy, alkylthio, alkylsulfonyl, aryl, aryloxy, arylthio, arylsulfonyl, trifluoromethyl, trifluoromethoxy, trifluoromethylthio, alkoxycarbonyl or by a group of the formula -NR 4 R 5 can be substituted wherein
- R 4 and R 5 have the meaning given above, or
- - Aryl means that up to 5-fold can be substituted identically or differently by alkyl, alkoxy, alkylthio, alkylsulfonyl, aryl, aryloxy, arylthio, arylsulfonyl, aralkyl, aralkoxy, aralkylthio, aralkylsulfonyl, halogen, cyano, nitro, trifluoromethyl, trifluoromethoxy , Trifluoromethylthio, alkoxycarbonyl, sulfamoyl, dialkylsulfamoyl, carbamoyl, dialkylcarbamoyl or by a group of the formula -NR ¢ R S , wherein
- R 4 and R 5 have the meaning given above,
- X is a group of the formula -CH 2 -CH 2 - or -CH = CH-, and
- A - a group of the formula
- R 6 - represents hydrogen or alkyl, and
- R 7 - represents hydrogen or
- - represents alkyl, aryl or aralkyl or
- - stands for a cation, found.
Überraschenderweise zeigen die erfindungsgemäßen disubstituierten Pyridine eine überlegene inhibitorische Wirkung auf die HMG-CoA Reduktase (3-Hydroxy-3-methyl-glutaryl Coenzym A Reduktase).Surprisingly, the disubstituted pyridines according to the invention show a superior inhibitory effect on the HMG-CoA reductase (3-hydroxy-3-methyl-glutaryl coenzyme A reductase).
Cycloalkyl steht im allgeinen für einen cyclischen Kohlenwasserstoffrest mit 3 bis 8 Kohlenstoffatomen. Bevorzugt ist der Cyclopropyl-, Cyclopentan- und der Cyclohexanring. Beispielsweise seien Cyclopropyl, Cyclopentyl, Cyclohexyl, Cycloheptyl und Cyclooctyl genannt.Cycloalkyl generally represents a cyclic hydrocarbon radical with 3 to 8 carbon atoms. The cyclopropyl, cyclopentane and cyclohexane rings are preferred. Examples include cyclopropyl, cyclopentyl, cyclohexyl, cycloheptyl and cyclooctyl.
Alkyl steht im allgemeinen für einen geradkettigen oder verzweigten Kohlenwasserstoffrest mit 1 bis 12 Kohlenstoffatomen. Bevorzugt wird Niederalkyl mit 1 bis etwa 6 Kohlenstoffatomen. Beispielsweise seien Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl, Pentyl, Isopentyl, Hexyl, Isohexyl, Heptyl, Isoheptyl, Octyl und Isooctyl genannt.Alkyl generally represents a straight-chain or branched hydrocarbon radical having 1 to 12 carbon atoms. Lower alkyl having 1 to about 6 carbon atoms is preferred. Examples include methyl, ethyl, propyl, isopropyl, butyl, isobutyl, pentyl, isopentyl, hexyl, isohexyl, heptyl, isoheptyl, octyl and isooctyl.
Alkoxy steht im allgemeinen für einen über ein Sauerstoffatom gebundenen geradkettigen oder verzweigten Kohlenwasserstoffrest mit 1 bis 12 Kohlenstoffatomen. Bevorzugt ist Niederalkoxy mit 1 bis etwa 6 Kohlenstoffatomen. Besonders bevorzugt ist ein Alkoxyrest mit 1 bis 4 Kohlenstoffatomen. Beispielsweise seien Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy, Pentoxy, Isopentoxy, Hexoxy, Isohexoxy, Heptoxy, Isoheptoxy, Octoxy oder Isooctoxy genannt.Alkoxy generally represents a straight-chain or branched hydrocarbon radical having 1 to 12 carbon atoms which is bonded via an oxygen atom. Lower alkoxy having 1 to about 6 carbon atoms is preferred. An alkoxy radical having 1 to 4 carbon atoms is particularly preferred. Examples include methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy, pentoxy, isopentoxy, hexoxy, isohexoxy, heptoxy, isoheptoxy, octoxy or isooctoxy.
Alkylthio steht im allgemeinen für einen über ein Schwefelatom gebundenen geradkettigen oder verzweigten Kohlenwasserstoffrest mit 1 bis 12 Kohlenstoffatomen. Bevorzugt ist Niederalkylthio mit 1 bis etwa 6 Kohlenstoffatomen. Besonders bevorzugt ist ein Alkylthiorest mit 1 bis 4 Kohlenstoffatomen. Beispielsweise seien Methylthio, Ethylthio, Propylthio, Isopropylthio, Butylthio, Isobutylthio, Pentylthio, Isopentylthio, Hexylthio, Isohexylthio, Heptylthio, Isoheptylthio, Octylthio oder Isooctylthio genannt.Alkylthio generally represents a straight-chain or branched hydrocarbon radical having 1 to 12 carbon atoms which is bonded via a sulfur atom. Lower alkylthio having 1 to about 6 carbon atoms is preferred. An alkylthio radical having 1 to 4 carbon atoms is particularly preferred. Examples include methylthio, ethylthio, propylthio, isopropylthio, butylthio, isobutylthio, pentylthio, isopentylthio, hexylthio, isohexylthio, heptylthio, isoheptylthio, octylthio or isooctylthio.
Alkylsulfonyl steht im allgemeinen für einen geradkettigen oder verzweigten Kohlenwasserstoffrest mit 1 bis 12 Kohlenstoffatomen, der über eine S02-Gruppe gebunden ist. Bevorzugt ist Niederalkylsulfonyl mit 1 bis etwa 6 Kohlenstoffatomen. Beispielsweise seien genannt: Methylsulfonyl, Ethylsulfonyl, Propylsulfonyl, Isopropylsulfonyl, Butylsulfonyl, Isobutylsulfonyl, Pentylsulfonyl, Isopentylsulfonyl, Hexylsulfonyl, Isohexylsulfonyl.Alkylsulfonyl generally represents a straight-chain or branched hydrocarbon radical having 1 to 12 carbon atoms, which is bonded via an S0 2 group. Lower alkylsulfonyl having 1 to about 6 carbon atoms is preferred. Examples include: methylsulfonyl, ethylsulfonyl, propylsulfonyl, isopropylsulfonyl, butylsulfonyl, isobutylsulfonyl, pentylsulfonyl, isopentylsulfonyl, hexylsulfonyl, isohexylsulfonyl.
Sulfamoyl (Aminosulfonyl) steht für die Gruppe -S02-NH2.Sulfamoyl (aminosulfonyl) stands for the group -S0 2 -NH2.
Aryl steht im allgemeinen für einen aromatischen Rest mit 6 bis etwa 12 Kohlenstoffatomen. Bevorzugte Arylreste sind Phenyl, Naphthyl und Biphenyl.Aryl generally represents an aromatic radical having 6 to about 12 carbon atoms. Preferred aryl radicals are phenyl, naphthyl and biphenyl.
Aryloxy steht im allgemeinen für einen aromatischen Rest mit 6 bis etwa 12 Kohlenstoffatomen, der über ein Sauerstoffatom gebunden ist. Bevorzugte Aryloxyreste sind Phenoxy oder Naphthyloxy.Aryloxy generally represents an aromatic radical having 6 to about 12 carbon atoms, which is bonded via an oxygen atom. Preferred aryloxy radicals are phenoxy or naphthyloxy.
Arylthio steht im allgemeinen für einen aromatischen Rest mit 6 bis etwa 12 Kohlenstoffatomen, der Sber ein Schwefelatom gebunden ist. Bevorzugte Arylthioreste sind Phenylthio oder Naphthylthio.Arylthio generally represents an aromatic radical having 6 to about 12 carbon atoms, to which a sulfur atom is attached. Preferred arylthio radicals are phenylthio or naphthylthio.
Arylsulfonyl steht im allgemeinen für einen aromatischen Rest mit 6 bis etwa 12 Kohlenstoffatomen, der über eine S02-Gruppe gebunden ist. Beispielsweise seien genannt: Phenylsulfonyl, Naphthylsulfonyl und Biphenylsulfonyl.Arylsulfonyl generally represents an aromatic radical having 6 to about 12 carbon atoms, which is bonded via an S0 2 group. Examples include: phenylsulfonyl, naphthylsulfonyl and biphenylsulfonyl.
Aralkyl steht im allgemeinen für einen über eine Alkylenkette gebundenen Arylrest mit 7 bis 14 Kohlenstoffatomen. Bevorzugt werden Aralkylreste mit 1 bis 6 Kohlenstoffatomen im aliphatischen Teil und 6 bis 12 Kohlenstoffatome im aromatischen Teil. Beispielsweise seien folgende Aralkylreste genannt: Benzyl, Naphthylmethyl, Phenethyl und Phenylpropyl.Aralkyl generally represents an aryl radical having 7 to 14 carbon atoms bonded via an alkylene chain. Aralkyl radicals having 1 to 6 carbon atoms in the aliphatic part and 6 to 12 carbon atoms in the aromatic part are preferred. The following aralkyl radicals may be mentioned, for example: benzyl, naphthylmethyl, phenethyl and phenylpropyl.
Aralkoxy steht im allgemeinen für einen Aralkylrest mit 7 bis 14 Kohlenstoffatomen, wobei die Alkylenkette über ein Sauerstoffatom gebunden ist. Bevorzugt werden Aralkoxyreste mit 1 bis 6 Kohlenstoffatomen im aliphatischen Teil und 6 bis 1'2 Kohlenstoffatomen im aromatischen Teil. Beispielsweise seien folgende Aralkoxyreste genannt: Benzyloxy, Naphthylmethoxy, Phenethoxy und Phenylpropoxy.Aralkoxy generally represents an aralkyl radical having 7 to 14 carbon atoms, the alkylene chain being bonded via an oxygen atom. Aralkoxy radicals having 1 to 6 carbon atoms in the aliphatic part and 6 to 1'2 carbon atoms in the aromatic part are preferred. The following aralkoxy radicals may be mentioned, for example: benzyloxy, naphthylmethoxy, phenethoxy and phenylpropoxy.
Aralkylthio steht im allgemeinen für einen Aralkylrest mit 7 bis etwa 14 Kohlenstoffatomen wobei die Alkylkette über ein Schwefelatom gebunden ist. Bevorzugt werden Aralkylthioreste mit 1 bis 6 Kohlenstoffatomen im aliphatischen Teil und 6 bis 12 Kohlenstoffatomen im aromatischen Teil. Beispielsweise seien folgende Aralkylthioreste genannt: Benzylthio, Naphthylmethylthio, Phenethylthio und Phenylpropylthio.Aralkylthio generally represents an aralkyl radical having 7 to about 14 carbon atoms, the alkyl chain being bonded via a sulfur atom. Aralkylthio radicals having 1 to 6 carbon atoms in the aliphatic part and 6 to 12 carbon atoms in the aromatic part are preferred. Examples include the following aralkylthio radicals: benzylthio, naphthylmethylthio, phenethylthio and phenylpropylthio.
Aralkylsulfonyl steht im allgemeinen für einen Aralkylrest mit 7 bis etwa 14 Kohlenstoffatomen, wobei die Alkylreste über eine S02-Kette gebunden ist. Bevorzugt werden Aralkylsulfonylreste mit 1 bis 6 Kohlenstoffatomen im aliphatischen Teil und 6 bis 12 Kohlenstoffatomen im aromatischen Teil. Beispielsweise seien folgende Aralkylsulfonylreste genannt: Benzylsulfonyl, Naphthylmethylsulfonyl, Phenethylsulfonyl und Phenylpropylsulfonyl.Aralkylsulfonyl generally represents an aralkyl radical having 7 to about 14 carbon atoms, the alkyl radicals being bonded via an SO 2 chain. Aralkylsulfonyl radicals having 1 to 6 carbon atoms in the aliphatic part and 6 to 12 carbon atoms in the aromatic part are preferred. Examples include the following aralkylsulfonyl radicals: benzylsulfonyl, naphthylmethylsulfonyl, phenethylsulfonyl and phenylpropylsulfonyl.
Alkoxycarbonyl kann beispielsweise durch die Formel
- - C II -OAlkyl 0 dargestellt werden. Alkyl steht hierbei für einen geradkettigen oder verzweigten Kohlenwasserstoffrest mit 1 bis 12 Kohlenstoffatomen. Bevorzugt wird Niederalkoxycarbonyl mit 1 bis etwa 6 Kohlenstoffatomen im Alkylteil. Insbesondere bevorzugt wird ein Alkoxycarbonyl mit 1 bis 4 Kohlenstoffatomen im Alkylteil. Beispielsweise seien die folgenden Alkoxycarbonylreste genannt: Methoxycarbonyl, Ethoxycarbonyl, Propoxycarbonyl, Isopropoxycarbonyl, Butoxycarbonyl oder Isobutoxycarbonyl.
- - C II -OAlky l 0 are shown. Alkyl here is a straight-chain or branched hydrocarbon radical having 1 to 12 carbon atoms. Lower alkoxycarbonyl having 1 to about 6 carbon atoms in the alkyl part is preferred. An alkoxycarbonyl having 1 to 4 carbon atoms in the alkyl part is particularly preferred. Examples include the following alkoxycarbonyl radicals: methoxycarbonyl, ethoxycarbonyl, propoxycarbonyl, isopropoxycarbonyl, butoxycarbonyl or isobutoxycarbonyl.
Acyl steht im allgemeinen für Phenyl oder geradkettiges oder verzweigtes Niederalkyl mit 1 bis etwa 6 Kohienstoffatomen, die über eine Carbonylgruppe gebunden sind. Bevorzugt sind Phenyl und Alkylreste mit bis zu 4 Kohlenstoffatomen. Beispielsweise seien genannt: Benzoyl, Acetyl, Ethylcarbonyl, Propylcarbonyl, Isopropylcarbonyl, Butylcarbonyl und Isobutylcarbonyl.Acyl generally represents phenyl or straight-chain or branched lower alkyl having 1 to about 6 carbon atoms which are bonded via a carbonyl group. Phenyl and alkyl radicals having up to 4 carbon atoms are preferred. Examples include: benzoyl, acetyl, ethylcarbonyl, propylcarbonyl, isopropylcarbonyl, butylcarbonyl and isobutylcarbonyl.
Halogen steht im allgemeinen für Fluor, Chlor, Brom oder lod, bevorzugt für Fluor, Chlor oder Brom. Besonders bevorzugt steht Halogen für Fluor oder Chlor.Halogen generally represents fluorine, chlorine, bromine or iodine, preferably fluorine, chlorine or bromine. Halogen is particularly preferably fluorine or chlorine.
Heteroaryl steht im allgemeinen für einen 5- bis 6-gliedrigen aromatischen Ring, der als Heteroatome Sauerstoff, Schwefel und/oder Stickstoff enthalten kann und an den weitere aromatische Ringe ankondensiert sein können. Bevorzugt sind 5- und 6-gliedrige aromatische Ringe, die einen Sauerstoff, ein Schwefel und oder bis zu 2 Stickstoffatome enthalten und die gegebenenfalls benzokondensiert sind. Als besonders bevorzugte Heteroarylreste seien genannt: Thienyl, Furyl, Pyrolyl, Pyrazolyl, Pyridyl, Pyrimidyl, Pyrazinyl, Pyridazinyl, Chinolyl, Isochinolyl, Chinazolyl, Chinoxalyl, Phthalazinyl, Cinnolyl, Thiazolyl, Benzothiazolyl, Isothiazoiyl, Oxazolyl, Benzoxazolyl, Isoxazolyl, Imidazolyl, Benzimidazolyl, Indolyl, und Isoindolyl.Heteroaryl generally represents a 5- to 6-membered aromatic ring which can contain oxygen, sulfur and / or nitrogen as heteroatoms and to which further aromatic rings can be fused. 5- and 6-membered aromatic rings are preferred which contain an oxygen, a sulfur and or up to 2 nitrogen atoms and which are optionally benzo-condensed. Particularly preferred heteroaryl residues are: thienyl, furyl, pyrolyl, pyrazolyl, pyridyl, pyrimidyl, pyridazinyl, quinolyl, isoquinolyl, quinazolyl, phthalazinyl, cinnolyl, thiazolyl, benzothiazolyl, isothiazoiyl, oxazylyl , Indolyl, and isoindolyl.
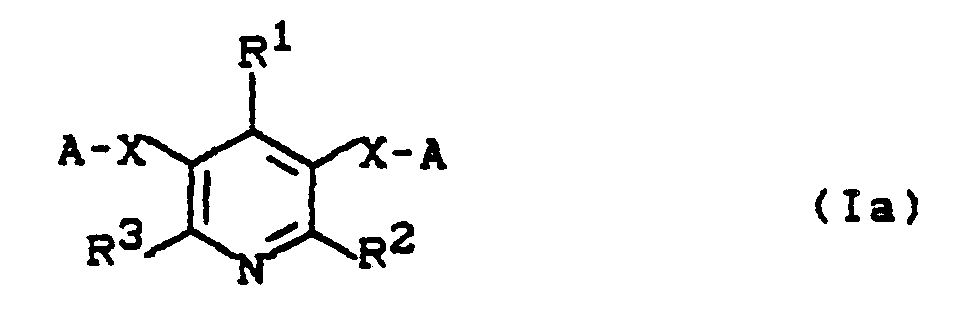
Im Rahmen der vorliegenden Erfindung entsprechen die disubstituierten Pyridine (la) der allgemeinen Formel
- R', R2, R3, X und A die oben angegebene Bedeutung haben.
- R ', R 2 , R 3 , X and A have the meaning given above.
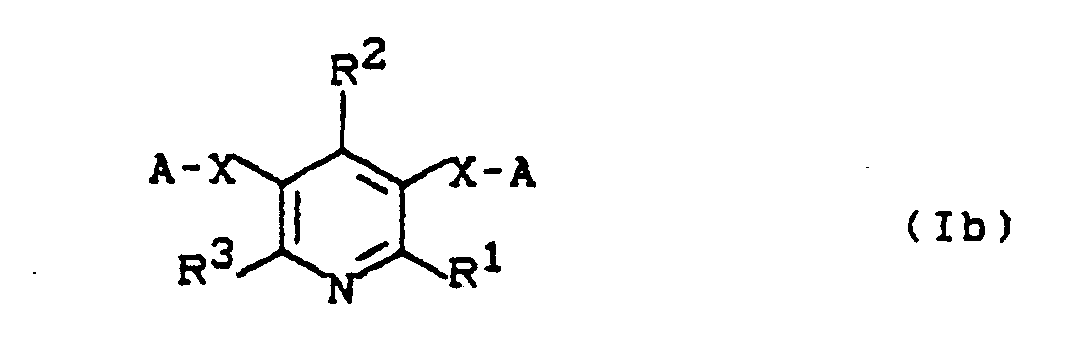
Im Rahmen der vorliegenden Erfindung entsprechen die disubstituierten Pyridine (Ib) der allgemeinen Formel
- R1, R2, R3, X und A die oben angegebene Bedeutung haben.
- R 1 , R 2 , R 3 , X and A have the meaning given above.
Im Rahmen der allgemeinen Formel (I) sind Verbindungen mit den allgemeinen Formeln (la) und (Ib) bevorzugt.In the context of the general formula (I), compounds having the general formulas (Ia) and (Ib) are preferred.
Bevorzugt sind Verbindungen der allgemeinen Formel (la) und (Ib)
- R' - Thienyl, Furyl, Thiazolyl, Isothiazolyl, Oxazolyl, Isoxazolyl, Pyridyl, Pyrimidyl, Pyrazinyl, Pyridazinyl, Indolyl, Isoindolyl, Chinolyl, Isochinolyl, Phthalazinyl, Chinoxalinyl, Chinazolinyl, Cinnolinyl, Benzothiazolyl, Benzoxazolyl oder Benzimidazolyl bedeutet, das bis zu 2-fach gleich oder verschieden substituiert sein kann durch Fluor, Chlor, Brom, Niederalkyl, Niederalkoxy, Phenyl, Phenoxy, Trifluormethyl, Trifluormethoxy oder Niederalkoxycarbonyl, oder
- - Phenyl oder Naphthyl bedeutet, das bis zu 4-fach gleich oder verschieden substituiert sein kann durch Niederalkyl, Niederalkoxy, Niederalkylthio, Niederalkylsulfonyl, Phenyl, Phenyloxy, Phenylthio, Phenylsulfonyl, Benzyl, Benzyloxy, Benzylthio, Benzylsulfonyl, Phenethyl, Phenylethoxy, Phenylethylthio, Phenylethylsulfonyl, Fluor, Chlor, Brom, Cyano, Trifluormethyl, Trifluormethoxy, Trifluormethylthio, Niederalkoxycarbonyl oder durch eine Gruppe der Formel -NR4Rs, wobei
- R4 und R5 gleich oder verschieden sind und Niederalkyl, Phenyl, Benzyl, Acetyl, Benzoyl, Phenylsulfonyl oder Niederalkylsulfonyl bedeuten,
- R2 - Cyclopropyl, Cyclopentyl oder Cyclohexyl bedeutet, oder
- - Niederalkyl bedeutet, das substituiert sein kann durch Fluor, Chlor, Brom, Cyano, Niederalkoxy, Niederalkylthio, Niederalkylsulfonyl, Phenyl, Trifluormethyl, Trifluormethoxy, Trifluormethylsulfonyl, Niederalkoxycarbonyl, Benzoyl, Niederalkylcarbonyl, durch eine Gruppe der Formel -NR"R5, worin
- R4 und R5 die oben angegebene Bedeutung haben, oder durch Pyridyl, Pyrimidyl, Pyrazinyl, Pyridazinyl, Chinolyl, Isochinolyl, Pyrrolyl, Indolyl, Thienyl, Furyl, Imidazolyl, Oxazolyl, Thiazolyl, Phenyl, Phenoxy, Phenylthio, Phenylsulfonyl, Benzyloxy, Benzylthio, Benzylsulfonyl, Phenylethoxy, Phenylethylthio oder Phenylethylsulfonyl, wobei die genannten Heteroaryl- und Arylreste bis zu 2-fach gleich oder verschieden durch Fluor, Chlor, Brom, Niederalkyl, Niederalkoxy, Trifluormethyl, oder Trifluormethoxy substituiert sein können, R3 - Wasserstoff, oder
- - Cyclopropyl, Cyclopentyl oder Cyclohexyl bedeutet, oder
- - Niederalkyl bedeutet, das substituiert sein kann durch Fluor, Chlor, Brom, Cyano, Niederalkoxy, Nie deralkylthio, Niederalkylsulfonyl, Trifluormethyl, Trifluormethoxy, Trifluormethylsulfonyl, Niederalkoxycarbonyl, Benzoyl, Niederalkylcarbonyl, durch ein Gruppe der Formel -NR4Rs, worin
- R5 und R6 die oben angegebene Bedeutung haben,
- oder durch Pyridyl, Pyrimidyl, Pyrazinyl, Pyridazinyl, Chinolyl, Isochinolyl, Pyrrolyl, Indolyl, Thienyl, Furyl, Imidazolyl, Oxazolyl, Thiazolyl, Phenyl, Phenoxy, Phenylthio, Phenylsulfonyl, Benzyloxy, Benzylthio, Benzylsulfonyl, Phenylethoxy, Phenylethylthio oder Phenylethylsulfonyl, wobei die genannten Heteroaryl-und Arylreste bis zu 2-fach gleich oder verschieden durch Fluor, Chlor, Brom, Niederalkyl, Niederalkoxy, Trifluormethyl, oder Trifluormethoxy substituiert sein können,
- - Thienyl, Furyl, Thiazolyl, Isothiazolyl, Oxazolyl, Isoxazolyl, Pyridyl, Pyrimidyl, Pyrazinyl, Pyridazinyl, Indolyl. Isoindolyl, Chinolyl, Isochinolyl, Phthalazinyl, Chinoxalinyl, Chinazolinyl, Cinnolinyl, Benzothiazolyl, Benzoxazolyl oder Benzimidazolyl bedeutet, das bis zu 2-fach gleich oder verschieden substituiert sein kann durch Fluor, Chlor, Brom, Niederalkyl, Niederalkoxy, Phenyl, Phenoxy, Trifluormethyl, Trifluormethoxy oder Niederalkoxycarbonyl, oder
- - Phenyl oder Naphthyl bedeutet, das bis zu 4-fach gleich oder verschieden substituiert sein kann durch Niederalkyl, Niederalkoxy, Niederalkylthio, Niederalkylsulfonyl, Phenyl, Phenyloxy, Phenylthio, Phenylsulfonyi, Benzyl, Benzyloxy, Benzylthio, Benzylsulfonyl, Phenethyl, Phenylethoxy, Phenylethylthio, Phenylethylsulfonyl. Fluor, Chlor, Brom, Cyano, Trifluormethyl, Trifluormethoxy, Trifluormethylthio, Niederalkoxycarbonyl oder durch eine Gruppe der Formel -NR5R6, wobei
- R5 und R6 die oben angegebene Bedeutung haben,
- X - eine Gruppe der Formel -CH = CH- bedeutet und
- A - eine Gruppe der Formel
- R6 - Wasserstoff oder Niederalkyl bedeutet, und
- R7 - Niederalkyl, Phenyl oder Benzyl bedeutet, oder - ein physiologisch verträgliches Kation bedeutet.
- R '- thienyl, furyl, thiazolyl, isothiazolyl, oxazolyl, isoxazolyl, pyridyl, pyrimidyl, pyrazinyl, pyridazinyl, indolyl, isoindolyl, quinolyl, isoquinolyl, phthalazinyl, quinoxalinyl, quinazolinyl, cinnolinyl, benzothiazolyl, benzoxazolyl or benzimidazolyl, which up to 2 may be substituted in the same or different ways by fluorine, chlorine, bromine, lower alkyl, lower alkoxy, phenyl, phenoxy, trifluoromethyl, trifluoromethoxy or lower alkoxycarbonyl, or
- - Phenyl or naphthyl, which can be substituted up to 4 times in the same or different way by lower alkyl, lower alkoxy, lower alkylthio, lower alkylsulfonyl, phenyl, phenyloxy, phenylthio, phenylsulfonyl, benzyl, benzyloxy, benzylthio, benzylsulfonyl, phenethyl, phenylethoxy, phenylethylsulfonyl, phenyl , Fluorine, chlorine, bromine, cyano, trifluoromethyl, trifluoromethoxy, trifluoromethylthio, lower alkoxycarbonyl or by a group of the formula -NR 4 R s , where
- R 4 and R 5 are identical or different and are lower alkyl, phenyl, benzyl, acetyl, benzoyl, phenylsulfonyl or lower alkylsulfonyl,
- R 2 denotes cyclopropyl, cyclopentyl or cyclohexyl, or
- - Lower alkyl means that can be substituted by fluorine, chlorine, bromine, cyano, lower alkoxy, lower alkylthio, lower alkylsulfonyl, phenyl, trifluoromethyl, trifluoromethoxy, trifluoromethylsulfonyl, lower alkoxycarbonyl, benzoyl, lower alkylcarbonyl, by a group of the formula -NR "R 5 , in which
- R 4 and R 5 have the meaning given above, or by pyridyl, pyrimidyl, pyrazinyl, pyridazinyl, quinolyl, isoquinolyl, pyrrolyl, indolyl, thienyl, furyl, imidazolyl, oxazolyl, thiazolyl, phenyl, phenoxy, phenylthio, phenylsulfonyl, benzyloxy, benzylthio , Benzylsulfonyl, phenylethoxy, phenylethylthio or phenylethylsulfonyl, where the heteroaryl and aryl radicals mentioned can be substituted up to 2 times identically or differently by fluorine, chlorine, bromine, lower alkyl, lower alkoxy, trifluoromethyl, or trifluoromethoxy, R 3 - hydrogen, or
- - Cyclopropyl, cyclopentyl or cyclohexyl, or
- - Lower alkyl means that can be substituted by fluorine, chlorine, bromine, cyano, lower alkoxy, Nie deralkylthio, lower alkylsulfonyl, trifluoromethyl, trifluoromethoxy, trifluoromethylsulfonyl, lower alkoxycarbonyl, benzoyl, lower alkylcarbonyl, by a group of the formula -NR 4 Rs, wherein
- R 5 and R 6 have the meaning given above,
- or by pyridyl, pyrimidyl, pyrazinyl, pyridazinyl, quinolyl, isoquinolyl, pyrrolyl, indolyl, thienyl, furyl, imidazolyl, oxazolyl, thiazolyl, phenyl, phenoxy, phenylthio, phenylsulfonyl, benzyloxy, benzylthio, benzylsulfonyl, phenylethysylonethyl, phenylethysulfonyl, phenyl The heteroaryl and aryl radicals mentioned can be substituted up to twice in the same or different manner by fluorine, chlorine, bromine, lower alkyl, lower alkoxy, trifluoromethyl or trifluoromethoxy,
- - thienyl, furyl, thiazolyl, isothiazolyl, oxazolyl, isoxazolyl, pyridyl, pyrimidyl, pyrazinyl, pyridazinyl, indolyl. Isoindolyl, quinolyl, isoquinolyl, phthalazinyl, quinoxalinyl, quinazolinyl, cinnolinyl, benzothiazolyl, benzoxazolyl or benzimidazolyl, which can be substituted up to 2 times by the same or different substituents by fluorine, chlorine, bromine, lower alkyl, lower alkoxy, phenyl, phenoxy, trifluoromethyl, Trifluoromethoxy or lower alkoxycarbonyl, or
- - Phenyl or naphthyl, which can be substituted up to 4 times in the same or different manner by lower alkyl, lower alkoxy, lower alkylthio, lower alkylsulfonyl, phenyl, phenyloxy, phenylthio, phenylsulfonyi, benzyl, benzyloxy, benzylthio, benzylsulfonyl, phenethyl, phenylethoxy, phenylethylsulfonyl, phenyl . Fluorine, chlorine, bromine, cyano, trifluoromethyl, trifluoromethoxy, trifluoromethylthio, lower alkoxycarbonyl or through a group of the formula -NR 5 R 6 , where
- R 5 and R 6 have the meaning given above,
- X is a group of the formula -CH = CH- and
- A - a group of the formula
- R 6 represents hydrogen or lower alkyl, and
- R 7 means lower alkyl, phenyl or benzyl, or means a physiologically compatible cation.
Besonders bevorzugt sind Verbindungen der allgemeinen Formel (la) und (Ib) in welcher
- R' - Pyridyl, Pyrimidyl, Chinolyl oder Isochinolyl bedeutet, das durch Fluor, Chlor, Methyl, Methoxy oder Trifluormethyl substituiert sein kann, oder
- - Phenyl bedeutet, das bis zu 3-fach gleich oder verschieden substituiert sein kann durch Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl, tert.Butyl, Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy, tert.Butoxy, Methylthio, Ethylthio, Propylthio, Isopropylthio, Methylsulfonyl, Ethylsulfonyl, Propylsulfonyl, Isopropylsulfonyl, Phenyl, Phenoxy, Benzyl, Benzyloxy, Fluor, Chlor, Brom, Cyano, Trifluormethyl, Trifluormethoxy, Methoxycarbonyl, Ethoxycarbonyl, Propoxycarbonyl, Isopropoxycarbonyl, Butoxycarbonyl, Isobutoxycarbonyl oder tert.Butoxycarbonyl,
- R2 - Cyclopropyl, Cyclopentyl oder Cyclohexyl bedeutet, oder
- - Methyl, Ethyl, Propyl, Isopropyl, Butyl, sec.-Butyl oder tert.Butyl bedeutet, das substituiert sein kann durch Fluor, Chlor, Brom, Cyano, Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, sec.Butoxy, tert.Butoxy, Methylthio, Ethylthio, Propylthio, Isopropylthio, Methylsulfonyl, Ethylsulfonyl, Propylsulfonyl, Isopropylsulfonyl, Trifluormethyl, Trifluormethoxy, Methoxycarbonyl, Ethoxycarbonyl, Butoxycarbonyl, Isobutoxycarbonyl, tert.-Butoxycarbonyl, Benzoyl, Acetyl, Pyridyl, Pyrimidyl, Thienyl, Furyl, Phenyl, Phenoxy, Phenylthio, Phenylsulfonyl. Benzyloxy, Benzylthio oder Benzylsulfonyl,
- R3 - Wasserstoff, Cyclopropyl, Cyclopentyl oder Cyclohexyl bedeutet, oder
- - Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl, tert.Butyl, Pentyl, Isopentyl, Hexyl oder Isohexyl bedeutet, das substituiert sein kann durch Fluor, Chlor, Brom, Cyano, Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, tsobutoxy, tert.Butoxy, Methylthio, Ethylthio, Propylthio, Isopropylthio, Butylthio, Isobutylthio, tert.Butylthio, Methyisulfonyl, Ethylsulfonyl, Propylsulfonyl, Isopropylsulfonyl, Butylsulfonyl, Isobutylsulfonyl, tert.Butylsulfonyl, Trifluormethyl, Trifluormethoxy, Methoxycarbonyl, Ethoxycarbonyl, Propoxycarbonyl, Isopropoxycarbonyl, Butoxycarbonyl, Isobutoxycarbonyl, tert.Butoxycarbonyl, Benzoyl, Acetyl, Ethylcarbonyl, oder durch eine Gruppe -NR4R5, wobei
- R4 und R5 gleich oder verschieden sind und Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl, tert.Butyl, Phenyl, Benzyl, Acetyl, Methylsulfonyl, Ethylsulfonyl, Propylsulfonyl, Isopropylsulfonyl oder Phenylsulfonyl bedeuten,
- oder durch Pyridyl, Pyrimidyl, Pyrazinyl, Pyridazinyl, Chinolyl, Isochinolyl, Thienyl, Furyl, Phenyl, Phenoxy, Phenylthio, Phenylsulfonyl, Benzyloxy, Benzylthio oder Benzylsulfonyl, wobei die genannten Heteroaryl-und Arylreste durch Fluor, Chlor, Methyl, Ethyl, Propyl, Isopropyl, Isobutyl, tert. Butyl, Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy, tert.-Butoxy, Trifluormethyl oder Trifluormethoxy substituiert sein können, oder
- - Thienyl, Furyl, Pyridyl, Pyrimidyl, Pyrazinyl, Pyridazinyl, Oxazolyl, Isooxazolyl, Imidazolyl, Pyrazolyl, Thiazolyl, Isothiazolyl, Chinolyl, Isochinolyl, Benzoxazolyl, Benzimidazolyl oder Benzthiazolyl bedeutet, wobei die genannten Reste durch Fluor, Chlor, Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl, tert.Butyl, Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy, tert.Butoxy, Phenyl, Phenoxy, Trifluormethyl, Trifluormethoxy, Methoxycarbonyl, Ethoxycarbonyl, Isopropoxycarbonyl, Propoxycarbonyl, Butoxycarbonyl, Isobutoxycarbonyl oder tert.Butoxycarbonyl substituiert sein können, oder
- - Phenyl bedeutet, das bis zu 3-fach gleich oder ver schieden durch Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl, tert.Butyl, Pentyl, Isopentyl, Hexyl, Isohexyl, Methoxy, Ethoxy, Propoxy, Isopropoxy, Butoxy, Isobutoxy, tert.-Butoxy, Methylthio, Ethylthio, Propylthio, Isopropylthio, Butylthio, Isobutylthio, tert.Butylthio, Methylsulfonyl, Ethylsulfonyl, Propylsulfonyl, Isopropylsulfonyl, Butylsulfonyl, Isobutylsulfonyl, tert.Butylsulfonyl, Phenyl, Phenoxy, Phenylthio, Phenylsulfonyl, Benzyl, Benzyloxy, Benzylthio, Benzylsulfonyl, Fluor, Chlor, Brom, Cyano, Trifluormethyl, Trifluormethoxy, Trifluormethylthio, Methoxycarbonyl, Ethoxycarbonyl, Propoxycarbonyl, Isopropoxycarbonyl, Butoxycarbonyl, Isobutoxycarbonyl, tert.Butoxycarbonyl oder durch eine Gruppe -NR4R5 substituiert sein kann, wobei
- R4- und R5 die oben angegebene Bedeutung haben, X - eine Gruppe der Formel -CH=CH- bedeutet und
- A - eine Gruppe der Formel
- R6 - Wasserstoff, Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert.Butyl bedeutet und
- R7 - Wasserstoff, Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl, tert.Butyl oder Benzyl bedeutet, oder - ein Natrium-, Kalium-, Calcium- oder Magnesium- oder Ammoniumion bedeutet.
- R 'is pyridyl, pyrimidyl, quinolyl or isoquinolyl, which can be substituted by fluorine, chlorine, methyl, methoxy or trifluoromethyl, or
- - Phenyl means that up to 3 times the same or different substitution can be substituted by methyl, ethyl, propyl, isopropyl, butyl, isobutyl, tert-butyl, methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy, tert-butoxy, methylthio , Ethylthio, propylthio, isopropylthio, methylsulfonyl, ethylsulfonyl, propylsulfonyl, isopropylsulfonyl, phenyl, phenoxy, benzyl, benzyloxy, fluorine, chlorine, bromine, cyano, trifluoromethyl, trifluoromethoxy, methoxycarbonyl, ethoxycarbonyl, propoxycarbonyl, butoxycarbonyl, butoxycarbonyl, butoxy ,
- R 2 denotes cyclopropyl, cyclopentyl or cyclohexyl, or
- - Methyl, ethyl, propyl, isopropyl, butyl, sec-butyl or tert-butyl, which can be substituted by fluorine, chlorine, bromine, cyano, methoxy, ethoxy, propoxy, isopropoxy, butoxy, sec-butoxy, tert. Butoxy, methylthio, ethylthio, propylthio, isopropylthio, methylsulfonyl, ethylsulfonyl, propylsulfonyl, isopropylsulfonyl, trifluoromethyl, trifluoromethoxy, methoxycarbonyl, ethoxycarbonyl, butoxycarbonyl, isobutoxycarbonyl, tert.-butoxycarbonyl, pyridyl, pyridyl, pyridylyl, pyridyl, pyridyl, pyridyl, pyridyl, pyridyl, pyridyl, pyridyl, pyridyl, pyridyl, pyridyl, pyridyl, pyridyl, pyridyl, pyridyl , Phenylthio, phenylsulfonyl. Benzyloxy, benzylthio or benzylsulfonyl,
- R 3 is hydrogen, cyclopropyl, cyclopentyl or cyclohexyl, or
- - Methyl, ethyl, propyl, isopropyl, butyl, isobutyl, tert-butyl, pentyl, isopentyl, hexyl or isohexyl, which can be substituted by fluorine, chlorine, bromine, cyano, methoxy, ethoxy, propoxy, isopropoxy, butoxy, tsobutoxy , tert.butoxy, methylthio, ethylthio, propylthio, isopropylthio, butylthio, isobutylthio, tert.butylthio, methylsulfonyl, ethylsulfonyl, propylsulfonyl, isopropylsulfonyl, butylsulfonyl, isobutylsulfonyl, tri-butylifoxycarbonyl, methylbutylifoxycarbonyl, methylbutylifoxycarbonyl, methylbutylifoxycarbonyl, methylbutylifoxycarbonyl , Isobutoxycarbonyl, tert.butoxycarbonyl, benzoyl, acetyl, ethylcarbonyl, or by a group -NR 4 R 5 , where
- R 4 and R 5 are the same or different and are methyl, ethyl, propyl, isopropyl, butyl, isobutyl, tert-butyl, phenyl, benzyl, acetyl, methylsulfonyl, ethylsulfonyl, propylsulfonyl, isopropylsulfonyl or phenylsulfonyl,
- or by pyridyl, pyrimidyl, pyrazinyl, pyridazinyl, quinolyl, isoquinolyl, thienyl, furyl, phenyl, phenoxy, Phenylthio, phenylsulfonyl, benzyloxy, benzylthio or benzylsulfonyl, the heteroaryl and aryl radicals mentioned being tert-substituted by fluorine, chlorine, methyl, ethyl, propyl, isopropyl, isobutyl. Butyl, methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy, tert-butoxy, trifluoromethyl or trifluoromethoxy may be substituted, or
- - Thienyl, furyl, pyridyl, pyrimidyl, pyrazinyl, pyridazinyl, oxazolyl, isooxazolyl, imidazolyl, pyrazolyl, thiazolyl, isothiazolyl, quinolyl, isoquinolyl, benzoxazolyl, benzimidazolyl or benzothiazolyl, with the radicals being methyl, eth, by fluorine , Isopropyl, butyl, isobutyl, tert-butyl, methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy, tert-butoxy, phenyl, phenoxy, trifluoromethyl, trifluoromethoxy, methoxycarbonyl, ethoxycarbonyl, isopropoxycarbonyl, propoxycarbonyl, butoxycarbonyl, isobutoxycarbonyl or tert may be substituted, or
- - Phenyl means up to 3 times the same or different by methyl, ethyl, propyl, isopropyl, butyl, isobutyl, tert-butyl, pentyl, isopentyl, hexyl, isohexyl, methoxy, ethoxy, propoxy, isopropoxy, butoxy, isobutoxy , tert-butoxy, methylthio, ethylthio, propylthio, isopropylthio, butylthio, isobutylthio, tert.Butylthio, methylsulfonyl, ethylsulfonyl, propylsulfonyl, isopropylsulfonyl, butylsulfonyl, isobutylsulfonyl, tert.Butylsulfonyl, phenyl, phenoxy, phenylthio, phenylsulphonyl, benzyl, benzyloxy, Benzylthio, benzylsulfonyl, fluorine, chlorine, bromine, cyano, trifluoromethyl, trifluoromethoxy, trifluoromethylthio, methoxycarbonyl, ethoxycarbonyl, propoxycarbonyl, isopropoxycarbonyl, butoxycarbonyl, isobutoxycarbonyl, tert.butoxycarbonyl or by a group -NR 4 R 5 , where may be substituted
- R4- and R 5 have the meaning given above, X - is a group of the formula -CH = CH- and
- A - a group of the formula
- R 6 is hydrogen, methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert-butyl and
- R 7 means hydrogen, methyl, ethyl, propyl, isopropyl, butyl, isobutyl, tert-butyl or benzyl, or - means a sodium, potassium, calcium or magnesium or ammonium ion.
Ganz besonders bevorzugt sind Verbindungen der allgemeinen Formeln (la) und (Ib) in welcher
- R' - Phenyl bedeutet, das bis zu 2-fach gleich oder verschieden durch Methyl, Ethyl, Propyl, Isopropyl, Phenoxy und/oder Fluor substituiert sein kann,
- R2 - für Cyclopropyl oder Cyclohexyl steht oder Methyl, Ethyl, Propyl, Isopropyl, Butyl, Isobutyl oder tert.Butyl bedeutet, das durch Fluor, Chlor, Methoxy, Phenyl oder Phenoxy substituiert sein kann,
- R3 - Wasserstoff, Cyclopropyl, Cyclopentyl oder Cyclohexyl oder Phenyl bedeutet, oder
- - Methyl, Ethyl, Propyl, Isopropyl, Butyl oder Benzyl bedeutet,
- X - eine Gruppe der Formel
- A - eine Gruppe der Formel
- R6 - Wasserstoff bedeutet und
- R7 - Wasserstoff, Methyl oder Ethyl bedeutet, oder - ein Natrium- oder Kaliumkation bedeutet.
- R '- phenyl which can be substituted up to two times, identically or differently, by methyl, ethyl, propyl, isopropyl, phenoxy and / or fluorine,
- R 2 - stands for cyclopropyl or cyclohexyl or means methyl, ethyl, propyl, isopropyl, butyl, isobutyl or tert-butyl, which can be substituted by fluorine, chlorine, methoxy, phenyl or phenoxy,
- R 3 is hydrogen, cyclopropyl, cyclopentyl or cyclohexyl or phenyl, or
- Means methyl, ethyl, propyl, isopropyl, butyl or benzyl,
- X - a group of the formula
- A - a group of the formula
- R 6 means hydrogen and
- R 7 means hydrogen, methyl or ethyl, or means a sodium or potassium cation.
Die erfindungsgemäßen disubstituierten Pyridine der allgemeinen Formel (I) haben mehrere asymmetrische Kohlen stoffatome und können daher in verschiedenen stereochemischen Formen existieren. Sowohl die einzelnen Isomeren als auch deren Mischungen sind Gegenstand der Erfindung.The disubstituted pyridines of the general formula (I) according to the invention have several asymmetric carbon atoms and can therefore exist in various stereochemical forms. Both the individual isomers and their mixtures are the subject of the invention.
Je nach der Bedeutung der Gruppen X bzw. der Reste A ergeben sich unterschiedliche Stereoisomere, die im folgenden näher erläutert werden sollten:
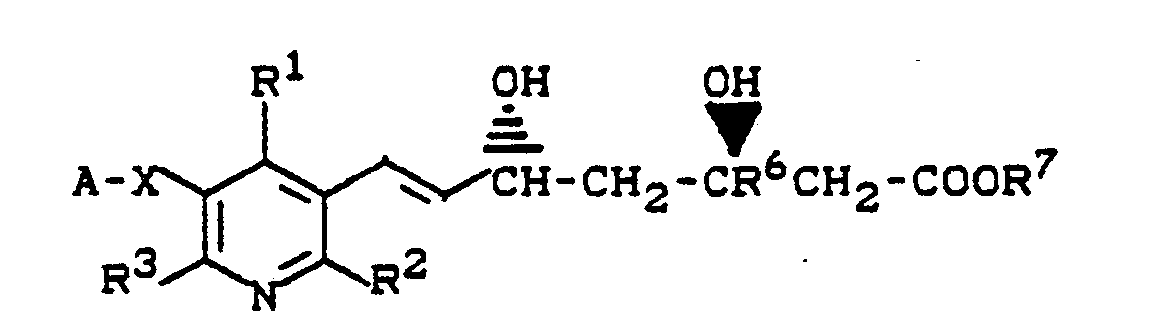
- a) Steht die Gruppe -X- für eine Gruppe der Formel -CH=CH- , so können die erfindungsgemäßen Verbindungen in zwei stereoisomeren Formen existieren, die an der Doppelbindung E-konfiguriert (II) oder Z-konfiguriert (III) sein können:
- b) Steht der Rest -A für eine Gruppe der Formel
- c) Steht der Rest -A für eine Gruppe der Formel
- a) If the group -X- stands for a group of the formula -CH = CH-, the compounds according to the invention can exist in two stereoisomeric forms which can be E-configured (II) or Z-configured (III) on the double bond:
- b) The radical -A stands for a group of the formula
- c) The radical -A stands for a group of the formula
Sowohl vom cis-Lacton aus als auch vom trans-Lacton existieren wiederum jeweils. zwei Isomere nämlich das 4R,6R-Isomere bzw. das 4S,6S-Isomere (cis-Lacton), sowie das 4R,6S-Isomere bzw. 4S,6R-Isomere (trans-Lacton). Bevorzugte Isomere sind die trans-Lactone. Besonders bevorzugt ist hierbei das 4R,6S-isomere (trans) sowie das 4R,6S-4S,6R-Racemat.Both the cis-lactone and the trans-lactone each exist. two isomers namely the 4R, 6R isomer or the 4S, 6S isomer (cis-lactone), and the 4R, 6S isomer or 4S, 6R isomer (trans-lactone). Preferred isomers are the trans lactones. The 4R, 6S isomer (trans) and the 4R, 6S-4S, 6R racemate are particularly preferred.
Beispielsweise seien die folgenden isomeren Formen der substituierten Pyridine genannt:
Darüber hinaus ergeben sich weitere Möglichkeiten der Isomerenbildung, da die erfindungsgemäßen disubstituierten Pyridine durch zwei Gruppen der Formel -X-A substituiert sind. Auch für die zweite Gruppe -X-A im Molekül gilt das oben gesagte. Es sind ebenso alle Stereoisomeren Gegenstand der Erfindung, die durch die zweite Gruppe der Formel -X-A, insbesondere im Zusammenhang mit der ersten Gruppe -X-A entstehen.In addition, there are further possibilities for isomer formation, since the disubstituted pyridines according to the invention are substituted by two groups of the formula -X-A. The same applies to the second group -X-A in the molecule. The invention also relates to all stereoisomers which arise from the second group of the formula -X-A, in particular in connection with the first group -X-A.
Außerdem wurde ein Verfahren zur Herstellung der disubstituierten Pyridine der allgemeinen Formel (I)
- R', R2, R3, X und A die oben angegebene Bedeutung haben, gefunden,
- das dadurch gekennzeichnet ist, daß man
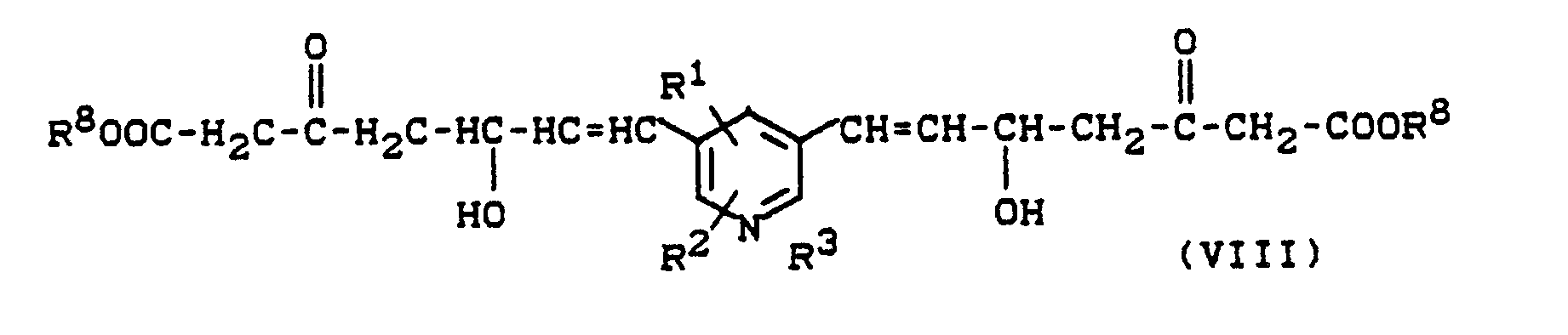
- Ketone der allgemeinen Formel (VIII)
- R1, R2 und R3 die oben angegebene Bedeutung haben, und
- R 8 - für Alkyl steht, reduziert,
- im Fall der Herstellung der Säuren die Ester verseift,
- im Fall der Herstellung der Lactone die Carbonsäuren cyclisiert,
- im Fall der Herstellung der Salze entweder die Ester oder die Lactone verseift,
- im Fall der Herstellung der Ethylenverbindungen (X = -CH2-CH2-) die Ethenverbindungen (X = -CH=CH-) nach üblichen Methoden hydriert,
- und gegebenenfalls Isomeren trennt.
- R ', R 2 , R 3 , X and A have the meaning given above, found,
- which is characterized in that one
- Ketones of the general formula (VIII)
- R 1 , R 2 and R 3 have the meaning given above, and
- R 8 - represents alkyl, reduced,
- in the case of production of the acids, the esters are saponified,
- in the case of the production of the lactones, the carboxylic acids are cyclized,
- in the case of the preparation of the salts, either the esters or the lactones are saponified,
- in the case of the production of the ethylene compounds (X = -CH 2 -CH 2 -) the ethene compounds (X = -CH = CH-) are hydrogenated by customary methods,
- and optionally separates isomers.
Das erfindungsgemäße Verfahren kann durch das folgendes Formelschema erläutert werden:
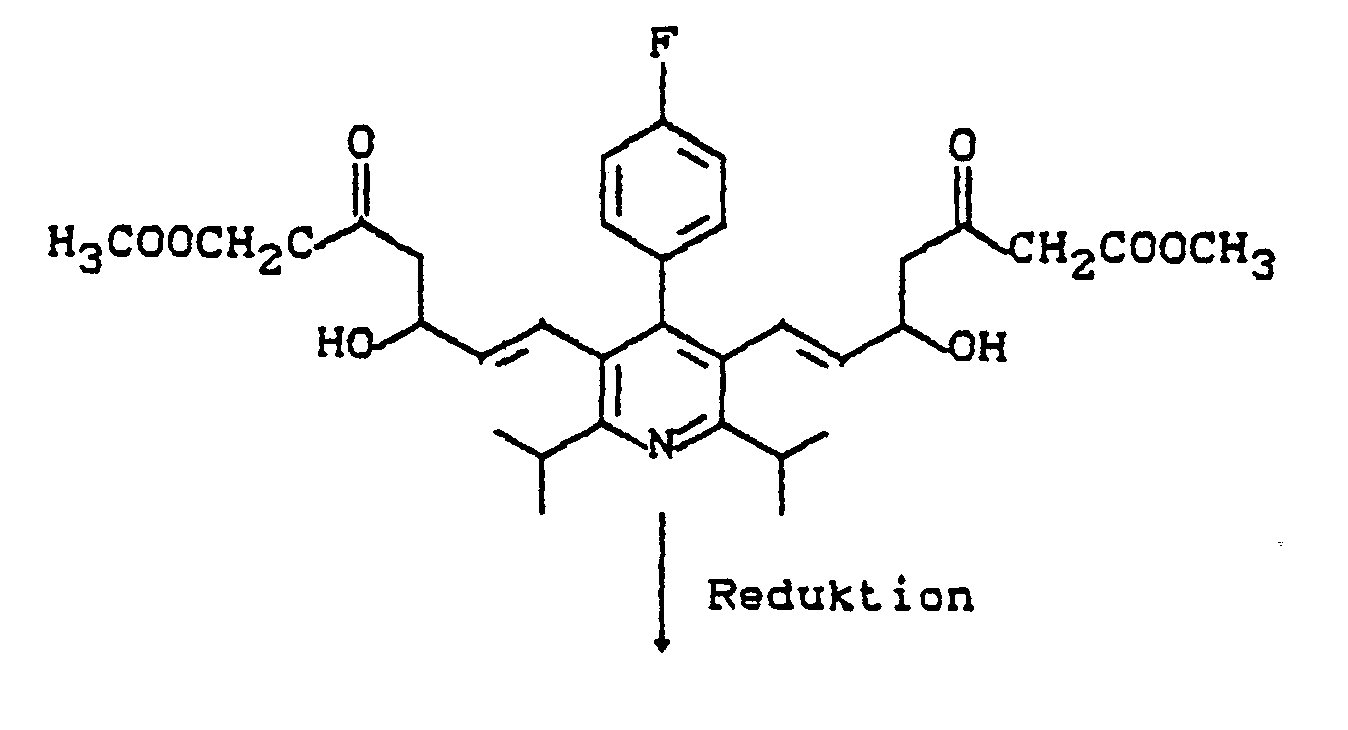
Die Reduktion kann mit den üblichen Reduktionsmitteln, bevorzugt mit solchen, die für die Reduktion von Ketonen zu Hydroxyverbindungen geeignet sind, durchgeführt werden. Besonders geeignet ist hierbei die Reduktion mit Metallhydriden oder komplexen Metallhydriden in inerten Lösemitteln, gegebenenfalls in Anwesenheit eines Trialkylborans. Bevorzugt wird die Reduktion mit komplexen Metallhydriden wie beispielsweise Lithiumboranat, Natriumboranat, Kaliumboranat, Zinkboranat, Lithium-trialkyl-hydrido-borate, Natrium-trialkyl-hydrido-boranaten, Natrium-cyano-trihydrido-borat oder Lithiumaluminiumhydrid durchgeführt. Ganz besonders bevorzugt wird die Reduktion mit Natriumborhydrid, in Anwesenheit von Triethylboran durchgeführt.The reduction can be carried out using the customary reducing agents, preferably those which are suitable for the reduction of ketones to hydroxy compounds. Reduction with metal hydrides or complex metal hydrides in inert solvents, if appropriate in the presence of a trialkylborane, is particularly suitable. The reduction is preferably carried out with complex metal hydrides such as, for example, lithium boranate, sodium boranate, potassium boranate, zinc boranate, lithium trialkyl hydridoborates, sodium trialkyl hydridoborates, sodium cyano-trihydridoborate or lithium aluminum hydride. The reduction with sodium borohydride is very particularly preferably carried out in the presence of triethylborane.
Als Lösemittel eignen sich hierbei die üblichen organischen Lösemittel, die sich unter den Reaktionsbedingungen nicht verändern. Hierzu gehören bevorzugt Ether wie beispielsweise Diethylether, Dioxan, Tetrahydrofuran oder Dimethoxyethan, oder Halogenkohlenwasserstoffe wie beispielsweise Dichlormethan, Trichlormethan, Tetrachlormethan, 1,2-Dichlorethan, oder Kohlenwasserstoffe wie beispielsweise Benzol, Toluol oder Xylol. Ebenso ist es möglich Gemische der genannten Lösemittel einzusetzen.The usual organic solvents which do not change under the reaction conditions are suitable as solvents. These preferably include ethers such as diethyl ether, dioxane, tetrahydrofuran or dimethoxyethane, or halogenated hydrocarbons such as dichloromethane, trichloromethane, carbon tetrachloride, 1,2-dichloroethane, or hydrocarbons such as benzene, toluene or xylene. It is also possible to use mixtures of the solvents mentioned.
Besonders bevorzugt wird die Reduktion der Ketongruppe zur Hydroxygruppe unter Bedingungen durchgeführt, bei denen die übrigen funktionellen Gruppen wie beispiels weise die Alkoxycarbonylgruppe nicht verändert werden. Hierzu besonders geeignet ist die Verwendung von Natriumborhydrid als Reduktionsmittel, in Anwesenheit von Triethylboran in inerten Lösemitteln wie vorzugsweise Ethern.The reduction of the ketone group to the hydroxyl group is particularly preferably carried out under conditions in which the other functional groups such as the alkoxycarbonyl group are not changed. The use of sodium borohydride as reduc is particularly suitable for this tion agent, in the presence of triethylborane in inert solvents such as preferably ethers.
Die Reduktion erfolgt im allgemeinen in einem Temperaturbereich von -80 C bis +30°C, bevorzugt von -78 C bis 0°C.The reduction is generally carried out in a temperature range from -80 ° C. to + 30 ° C., preferably from -78 ° C. to 0 ° C.
Das erfindungsgemäße Verfahren wird im allgemeinen bei Normaldruck durchgeführt. Es ist aber auch möglich, das Verfahren bei Unterdruck oder bei Überdruck durchzuführen (z.B. in einem Bereich von 0,5 bis 5 bar).The process according to the invention is generally carried out at normal pressure. However, it is also possible to carry out the process under negative pressure or under positive pressure (e.g. in a range from 0.5 to 5 bar).
Im allgemeinen wird das Reduktionsmittel in einer Menge von 1 bis 2 mol, bevorzugt von 1 bis 1,5 mol bezogen auf 1 mol der Ketoverbindung eingesetzt.In general, the reducing agent is used in an amount of 1 to 2 mol, preferably 1 to 1.5 mol, based on 1 mol of the keto compound.
Unter den oben angegebenen Reaktionsbedingungen wird im allgemeinen die Carbonylgruppe zur Hydroxygruppe reduziert, ohne daß Reduktion an der Doppelbindung zur Einfachbindung erfolgt.Under the reaction conditions given above, the carbonyl group is generally reduced to the hydroxyl group without the double bond being reduced to the single bond.
Zur Herstellung von Verbindungen der allgemeinen Formel (I), in welchen X für eine Ethylengruppierung steht, kann die Reduktion der Ketone (VIII) unter solchen Bedingungen durchgeführt werden, unter denen sowohl die Carbonylgruppe als auch die Doppelbindung reduziert wird.To prepare compounds of the general formula (I) in which X represents an ethylene grouping, the reduction of the ketones (VIII) can be carried out under conditions under which both the carbonyl group and the double bond are reduced.
Darüber hinaus ist es auch möglich, die Reduktion der Carbonylgruppe und die Reduktion der Doppelbindung in zwei getrennten Schritten durchzuführen.In addition, it is also possible to carry out the reduction of the carbonyl group and the reduction of the double bond in two separate steps.
Die Carbonsäuren im Rahmen der allgemeinen Formel (I) entsprechen der Formel (Ic)
- R1, R2, R3, R6 und X die oben angegebene Bedeutung haben.
- R 1 , R 2 , R 3 , R 6 and X have the meaning given above.
Die Carbonsäureester im Rahmen der allgemeinen Formel (I) entsprechen der Formel (Id)
- R1, R 2, R3, R6 und X die oben angegebene Bedeutung haben, und
- R8 - für Alkyl steht.
- R 1 , R 2 , R 3 , R 6 and X have the meaning given above, and
- R 8 - represents alkyl.
Die Salze der erfindungsgemäßen Verbindungen im Rahmen der allgemeinen Formel (I) entsprechen der Formel (le)
- R', R2, R3, R6 und X die oben angegebene Bedeutung haben, und
- Mn⊕ für ein Kation steht.
- R ', R 2 , R 3 , R 6 and X have the meaning given above, and
- M n ⊕ stands for a cation.
Die Lactone im Rahmen der allgemeinen Formel (I) entsprechen der Formel (If)
- R', R2, R3, R6 und X die oben angegebene Bedeutung haben.
- R ', R 2 , R 3 , R 6 and X have the meaning given above.
Zur Herstellung der erfindungsgemäßen Carbonsäuren der allgemeinen Formel (Ic) werden im allgemeinen die Carbonsäureester der allgemeinen Formel (Id) oder die Lactone der allgemeinen Formel (If) nach üblichen Methoden verseift. Die Verseifung erfolgt im allgemeinen indem man die Ester oder die Lactone in inerten Lösemitteln mit üblichen Basen behandelt, wobei im allgemeinen zunächst die Salze der allgemeinen Formel (le) entstehen, die anschließend in einem zweiten Schritt durch Behandeln mit Säure in die freien Säuren der allgemeinen Formel (Ic) überführt werden können.To prepare the carboxylic acids of the general formula (Ic) according to the invention, the carboxylic acid esters of the general formula (Id) or the lactones of the general formula (If) are in general saponified by customary methods. The saponification is generally carried out by treating the esters or the lactones in inert solvents with customary bases, the salts of the general formula (Ie) generally being formed first, which are then treated in a second step with acid in the free acids of the general Formula (Ic) can be transferred.
Als Basen eignen sich für die Verseifung die üblichen anorganischen Basen. Hierzu gehören bevorzugt Alkalihydroxide oder Erdalkalihydroxide wie beispielsweise Natriumhydroxid, Kaliumhydroxid oder Bariumhydroxid, oder Alkalicarbonate wie Natrium- oder Kaliumcarbonat oder Natriumhydrogencarbonat, oder Alkalialkoholate wie Natriumethanolat, Natriummethanolat, Kaliummethanolat, Kaliumethanolat oder Kalium- tert.butanolat. Besonders bevorzugt werden Natriumhydroxid oder Kaliumhydroxid eingesetzt.The usual inorganic bases are suitable as bases for the saponification. These preferably include alkali metal hydroxides or alkaline earth metal hydroxides such as sodium hydroxide, potassium hydroxide or barium hydroxide, or alkali metal carbonates such as sodium or potassium carbonate or sodium hydrogen carbonate, or alkali metal alcoholates such as sodium ethanolate, sodium methoxide, potassium methoxide, potassium ethoxide or potassium tert-butoxide. Sodium hydroxide or potassium hydroxide are particularly preferably used.
Als Lösemittel eignen sich für die Verseifung Wasser oder die für eine Verseifung üblichen organischen Lösemittel. Hierzu gehören bevorzugt Alkohole wie Methanol, Ethanol, Propanol, Isopropanol oder Butanol, oder Ether wie Tetrahydrofuran oder Dioxan, oder Dimethylformamid oder Dimethylsulfoxid. Besonders bevorzugt werden Alkohole wie Methanol, Ethanol, Propanol oder Isopropanol verwendet. Ebenso ist es möglich, Gemische der genannten Lösemittel einzusetzen.Suitable solvents for the saponification are water or the organic solvents customary for saponification. These preferably include alcohols such as methanol, ethanol, propanol, isopropanol or butanol, or ethers such as tetrahydrofuran or dioxane, or dimethylformamide or dimethyl sulfoxide. Alcohols such as methanol, ethanol, propanol or isopropanol are particularly preferably used. It is also possible to use mixtures of the solvents mentioned.
Die Verseifung wird im allgemeinen in einem Temperaturbereich von 0°C bis +100°C, bevorzugt von +20°C bis + 80 C durchgeführt.The saponification is generally carried out in a temperature range from 0 ° C. to + 100 ° C., preferably from + 20 ° C. to + 80 ° C.
Im allgemeinen wird die Verseifung bei Normaldruck durchgeführt. Es ist aber auch möglich, bei Unterdruck oder bei Überdruck zu arbeiten (z.B. von 0,5 bis 5 bar).The saponification is generally carried out at normal pressure. However, it is also possible to work under negative pressure or overpressure (e.g. from 0.5 to 5 bar).
Bei der Durchführung der Verseifung wird die Base im allgemeinen in einer Menge von 1 bis 3 mol, bevorzugt von 1 bis 1,5 mol bezogen auf 1 mol des Esters bzw. des Lactons eingesetzt. Besonders bevorzugt verwendet man molare.Mengen der Reaktanden.When saponification is carried out, the base is generally used in an amount of 1 to 3 mol, preferably 1 to 1.5 mol, based on 1 mol of the ester or lactone. Molar amounts of the reactants are particularly preferably used.
Bei der Durchführung der Reaktion entstehen im ersten Schritt die Salze der erfindungsgemäßen Verbindungen (le) als Zwischenprodukte, die isoliert werden können. Die erfindungsgemäßen Säuren (Ic) erhält man durch Behandeln der Salze (le) mit üblichen anorganischen Säu ren. Hierzu gehören bevorzugt Mineralsäuren wie beispielsweise Chlorwasserstoffsäure, Bromwasserstoffsäure, Schwefelsäure oder Phosphorsäure. Es hat sich bei der Herstellung der Carbonsäuren (Ic) hierbei als vorteilhaft erwiesen, die basische Reaktionsmischung der Verseifung in einem zweiten Schritt ohne Isolierung der Salze anzusäueren. Die Säuren können dann in üblicher Weise isoliert werden.When the reaction is carried out, the salts of the compounds (Ie) according to the invention are formed in the first step as intermediates which can be isolated. The acids (Ic) according to the invention are obtained by treating the salts (le) with customary inorganic acids. These preferably include mineral acids such as, for example, hydrochloric acid, hydrobromic acid, sulfuric acid or phosphoric acid. In the production of the carboxylic acids (Ic), it has proven advantageous here to acidify the basic reaction mixture of the saponification in a second step without isolating the salts. The acids can then be isolated in the usual way.
Zur Herstellung der erfindungsgemäßen Lactone der Formel (lf) werden im allgemeinen die erfindungsgemäßen Carbonsäuren (Ic) nach üblichen Methoden cyclisiert, beispielsweise durch Erhitzen der entsprechenden Säure in inerten organischen Lösemitteln, gegebenenfalls in Anwesenheit von Molsieb.To prepare the lactones of the formula (If) according to the invention, the carboxylic acids (Ic) according to the invention are generally cyclized by customary methods, for example by heating the corresponding acid in inert organic solvents, if appropriate in the presence of molecular sieve.
Als Lösemittel eignen sich hierbei Kohlenwasserstoffe wie Benzol, Toluol, Xylol, Erdölfraktionen, oder Tetralin oder Diglyme oder Triglyme. Bevorzugt werden Benzol, Toluol oder Xylol eingesetzt. Ebenso ist es möglich Gemische der genannten Lösemittel einzusetzen. Besonders bevorzugt verwendet man Kohlenwasserstoffe, insbesondere Toluol, in Anwesenheit von Molsieb.Suitable solvents here are hydrocarbons such as benzene, toluene, xylene, petroleum fractions, or tetralin or diglyme or triglyme. Benzene, toluene or xylene are preferably used. It is also possible to use mixtures of the solvents mentioned. Hydrocarbons, in particular toluene, are particularly preferably used in the presence of molecular sieve.
Die Cyclisierung wird im allgemeinen in einem Temperaturbereich von -40 °C bis + 200 °C. bevorzugt von -25 C bis +50° C durchgeführt.The cyclization is generally in a temperature range from -40 ° C to + 200 ° C. preferably carried out from -25 C to + 50 ° C.
Die Cyclisierung wird im allgemeinen bei Normaldruck durchgeführt, es ist aber auch möglich, das Verfahren bei Unterdruck oder bei Überdruck durchzuführen (z.B. in einem Bereich von 0,5 bis 5 bar).The cyclization is generally carried out at normal pressure, but it is also possible to carry out the process under reduced pressure or under elevated pressure (e.g. in a range from 0.5 to 5 bar).
Darüberhinaus wird die Cyclisierung auch in inerten organischen Lösemitteln, mit Hilfe von cyclisierenden bzw. wasserabspaltenden Agentien durchgeführt. Als wasserabspaltende Agentien werden hierbei bevorzugt Carbodiimide verwendet. Als Carbondiimide werden bevorzugt N,N'-Dicyclohexylcarbodiimid-Paratoluolsulfonat, N-Cyclohexyl-N'-[2-(N"-methylmorpholinium)ethyl]carbodiimid oder N-(3-Dimethylaminopropyl)-N'-ethylcarbodiimid-Hydrochlorid eingesetzt.In addition, the cyclization is also carried out in inert organic solvents with the aid of cyclizing or water-releasing agents. Carbodiimides are preferably used as water-releasing agents. Preferred carbondiimides are N, N'-dicyclohexylcarbodiimide paratoluenesulfonate, N-cyclohexyl-N '- [2- (N "-methylmorpholinium) ethyl] carbodiimide or N- (3-dimethylamino propyl) -N'-ethylcarbodiimide hydrochloride used.
Als Lösemittel eignen sich hierbei die üblichen organischen Lösemittel. Hierzu gehören bevorzugt Ether wie Diethylether, Tetrahydrofuran oder Dioxan, oder Chlorkohlenwasserstoffe wie Methylenchlorid, Chloroform oder Tetrachlorkohlenstoff, oder Kohlenwasserstoffe wie Benzol, Toluol, Xylol oder Erdölfraktionen. Besonders bevorzugt werden Chlorkohlenwasserstoffe wie beispielsweise Methylenchlorid, Chloroform oder Tetrachlorkohlenstoff, oder Kohlenwasserstoffe wie Benzol, Toluol, Xylol, oder Erdölfraktionen. Besonders bevorzugt werden Chlorkohlenwasserstoffe wie beispielsweise Methylenchlorid, Chloroform oder Tetrachlorkohlenstoff eingesetzt.The usual organic solvents are suitable as solvents. These preferably include ethers such as diethyl ether, tetrahydrofuran or dioxane, or chlorinated hydrocarbons such as methylene chloride, chloroform or carbon tetrachloride, or hydrocarbons such as benzene, toluene, xylene or petroleum fractions. Chlorinated hydrocarbons such as, for example, methylene chloride, chloroform or carbon tetrachloride, or hydrocarbons such as benzene, toluene, xylene, or petroleum fractions are particularly preferred. Chlorinated hydrocarbons such as methylene chloride, chloroform or carbon tetrachloride are particularly preferably used.
Die Reaktion wird im allgemeinen in einem Temperaturbereich von 0°C bis +80°C, bevorzugt von +10°C bis + 50 °C durchgeführt.The reaction is generally carried out in a temperature range from 0 ° C. to + 80 ° C., preferably from + 10 ° C. to + 50 ° C.
Bei der Durchführung der Cyclisierung hat es sich als vorteilhaft erwiesen, die Cyclisierungsmethode mit Hilfe von Carbodiimiden als dehydratisierenden Agentien einzusetzen.When carrying out the cyclization, it has proven to be advantageous to use the cyclization method with the aid of carbodiimides as dehydrating agents.
Die Trennung der Isomeren in die stereoisomer einheitlichen Bestandteile erfolgt im allgemeinen nach üblichen Methoden wie sie beispielsweise von E.L. Eliel, Stereochemistry of Carbon Compounds, McGraw Hili, 1962 beschrieben wird. Bevorzugt wird hierbei die Trennung der Isomeren auf der Stufe der racemischen Lactone. Besonders bevorzugt wird hierbei die racemische Mischung der trans-Lactone (VII) durch Behandeln entweder mit D-(+)-oder L-(-)-a-Methylbenzylamin nach üblichen Methoden in die diastereomeren Dihydroxyamide (Ig)
Die Isomerentrennung soll im folgenden Schema beispielhaft erläutert werden:
Die als Ausgangsstoffe eingesetzten Ketone (VIII) sind neu.The ketones (VIII) used as starting materials are new.
Es wurde ein Verfahren zur Herstellung der erfindungsgemäßen Ketone der allgemeinen Formel (VIII)
- R1, R2 und R3 die oben angegebene Bedeutung haben und
- R8 - für Alkyl steht,
- gefunden, das dadurch gekennzeichnet ist, daß man Aldehyde der allgemeinen Formel (IX)
- R', R2 und R3 die oben angegebene Bedeutung haben,
- in inerten Lösemitteln mit Acetessigester der allgemeinen Formel (X)
- R8 die oben angegebene Bedeutung hat,
- in Anwesenheit von Basen umsetzt.
- R 1 , R 2 and R 3 have the meaning given above and
- R 8 - represents alkyl,
- found, which is characterized in that aldehydes of the general formula (IX)
- R ', R 2 and R 3 have the meaning given above,
- in inert solvents with acetoacetic ester of the general formula (X)
- R 8 has the meaning given above,
- in the presence of bases.
Das erfindungsgemäße Verfahren kann beispielsweise durch folgendes Formelschema erläutert werden:
Als Basen kommen hierbei die üblichen stark basischen Verbindungen in Frage. Hierzu gehören bevorzugt lithium-organische Verbindungen wie beispielsweise N-Butyllithium, sec.Butyllithium, tert.Butyllithium oder Phenyllithium, oder Amide wie beispielsweise Lithiumdiisopropylamid, Natriumamid oder Kaliumamid, oder Lithiumhexamethyldisilylamid, oder Alkalihydride wie Natriumhydrid oder Kaliumhydrid. Ebenso ist es möglich, Gemische der genannten Basen einzusetzen. Besonders bevorzugt werden N-Butyllithium oder Natriumhydrid oder deren Gemisch eingesetzt.The bases here are the customary strongly basic compounds. These preferably include organolithium compounds such as N-butyllithium, sec-butyllithium, tert-butyllithium or phenyllithium, or amides such as lithium diisopropylamide, sodium amide or potassium amide, or lithium hexamethyldisilylamide, or alkali hydrides such as sodium hydride or potassium hydride. It is also possible to use mixtures of the bases mentioned. N-Butyllithium or sodium hydride or a mixture thereof is particularly preferably used.
Als Lösemittel eignen sich hierbei die üblichen organischen Lösemittel, die sich unter den Reaktionsbedingungen nicht verändern. Hierzu gehören bevorzugt Ether wie Diethylether, Tetrahydrofuran, Dioxan oder Dimethoxyethan, oder Kohlenwasserstoffe wie Benzol, Toluol, Xylol, Cyclohexan, Hexan oder Erölfraktionen. Ebenso ist es möglich, Gemische der genannten Lösemittel einzusetzen. Besonders bevorzugt werden Ether wie Diethylether oder Tetrahydrofuran verwendet.The usual organic solvents which do not change under the reaction conditions are suitable as solvents. These preferably include ethers such as diethyl ether, tetrahydrofuran, dioxane or dimethoxyethane, or hydrocarbons such as benzene, toluene, xylene, cyclohexane, hexane or oil fractions. It is also possible to use mixtures of the solvents mentioned. Ethers such as diethyl ether or tetrahydrofuran are particularly preferably used.
Die Reaktion wird im allgemeinen in einem Temperaturbereich von -80 * C bis +50°C, bevorzugt von -20 C bis + 30 C durchgeführt.The reaction is generally carried out in a temperature range from -80 ° C. to + 50 ° C., preferably from -20 ° C. to + 30 ° C.
Das Verfahren wird im allgemeinen bei Normaldruck durchgeführt, es ist aber auch möglich das Verfahren bei Unterdruck oder bei Überdruck durchzuführen, z.B. in einem Bereich von 0,5 bis 5 bar.The process is generally carried out under normal pressure, but it is also possible to carry out the process under negative pressure or under positive pressure, e.g. in a range from 0.5 to 5 bar.
Bei der Durchführung des Verfahrens wird der Acetessigester im allgemeinen in einer Menge von 1 bis 2, bevorzugt von 1 bis 1,5 mol, bezogen auf 1 mol des Aldehyds eingesetzt.When carrying out the process, the acetoacetic ester is generally used in an amount of 1 to 2, preferably 1 to 1.5, mol, based on 1 mol of the aldehyde.
Die als Ausgangsstoffe eingesetzten Acetessigester der Formel (X) sind bekannt oder können nach bekannten Methoden hergestellt werden [Beilstein's Handbuch der organischen Chemie 111, 632; 438].The acetoacetic esters of the formula (X) used as starting materials are known or can be prepared by known methods [Beilstein's Handbuch der organic Chemistry 111, 632; 438].
Als Acetessigester für das erfindungsgemäße Verfahren seien beispielsweise genannt: Acetessigsäuremethylester, Acetessigsäureethylester, Acetessigsäurepropylester, Acetessigsäureisopropylester.Examples of acetoacetic esters for the process according to the invention are: methyl acetoacetate, ethyl acetoacetate, propyl acetoacetate, isopropyl acetoacetate.
Die als Ausgangsstoffe eingesetzten Aldehyde der allgemeinen Formel (IX) sind neu.The aldehydes of the general formula (IX) used as starting materials are new.
Die Herstellung der Aldehyde kann durch das folgende Reaktionsschema beispielhaft für die Verbindungen des Typs (la) dargestellt werden:
Hierbei werden im ersten Schritt [A] die Dihydropyridine der allgemeinen Formel (X) in geeigneten Lösemitteln, mit geeigneten Oxidationsmitteln, oxidiert. Bevorzugt werden die Dihydropyridine in Chlorkohlenwasserstoffen wie beispielsweise Methylenchlorid, mit 2,2-Dichlor-5,6-dicyan-p-benzochinon bei Raumtemperatur, oder mit Chromtrioxid in Eisessig bei erhöhten Temperaturen, bevorzugt unter Rückflußtemperatur, zu den Pyridinen der Formel (XI) oxidiert. Im zweiten Schritt [B] werden die Pyridine (XI) in inerten Lösemitteln wie Ethern, beispielsweise Diethylether, Dioxan oder Tetrahydrofuran, bevorzugt in Tetrahydrofuran, mit Metallhydriden wie Lithiumaluminiumhydrid, Natriumcyano-borhydrid, Diisobutylaluminiumhydrid oder Natrium-bis-(2-methoxyethoxy)-dihydroaluminat, in einem Temperaturbereich von -80°C bis +40°C, bevorzugt von -70° C bis Raumtemperatur zu den Hydroxyverbindungen der allgemeinen Formel (XII) reduziert. Im dritten Schritt [C] werden die Hydroxyverbindungen (XII) nach bekannten Methoden mit Oxidationsmitteln wie Pyridiniumchlorochromat, gegebenenfalls in Anwesenheit von Aluminiumoxid, in inerten Lösemitteln wie Chlorkohlenwasserstoffen, bevorzugt Methylenchlorid, bei Raumtemperatur oder mit Trifluoressigsäure und Dimethylsulfoxid (Swern-Oxidation) oder aber nach anderen für die Oxidation von Hydroxymethylverbindungen zu Aldehyden üblichen Methoden zu den Aldehyden (XIII) oxidiert. Im vierten Schritt [D] werden die Aldehyde (XIII) durch Umsetzen mit Diethyl-2-(cyclohexylamino)-vinyl-phosphonat in inerten Lösemitteln wie Ethern, bevorzugt in Tetrahydrofuran in Anwesenheit von Natriumhydrid, in einem Temperaturbereich von -20 C bis +30°C, bevorzugt von -5°C bis Raumtemperatur in die Verbindungen (IX) überführt.In the first step [A], the dihydropyridines of the general formula (X) are oxidized in suitable solvents with suitable oxidizing agents. The dihydropyridines are preferred in chlorinated hydrocarbons such as methylene chloride, with 2,2-dichloro-5,6-dicyan-p-benzoquinone at room temperature, or with chromium trioxide in glacial acetic acid at elevated temperatures, preferably under reflux temperature, to give the pyridines of the formula (XI) oxidized. In the second step [B], the pyridines (XI) are dissolved in inert solvents such as ethers, for example diethyl ether, dioxane or tetrahydrofuran, preferably in tetrahydrofuran, with metal hydrides such as lithium aluminum hydride, sodium cyanoborohydride, diisobutyl aluminum hydride or sodium bis (2-methoxyethoxy) - dihydroaluminate, reduced in a temperature range from -80 ° C to + 40 ° C, preferably from -70 ° C to room temperature to the hydroxy compounds of the general formula (XII). In the third step [C], the hydroxy compounds (XII) are prepared by known methods using oxidizing agents such as pyridinium chlorochromate, optionally in the presence of aluminum oxide, in inert solvents such as chlorinated hydrocarbons, preferably methylene chloride, at room temperature or using trifluoroacetic acid and dimethyl sulfoxide (Swern oxidation) or after other methods customary for the oxidation of hydroxymethyl compounds to aldehydes are oxidized to the aldehydes (XIII). In the fourth step [D], the aldehydes (XIII) are reacted with diethyl 2- (cyclohexylamino) vinyl phosphonate in inert solvents such as ethers, preferably in tetrahydrofuran in the presence of sodium hydride, in a temperature range from -20 C to +30 ° C, preferably from -5 ° C to room temperature in the compounds (IX).
Die als Ausgangsstoffe eingesetzten Dihydropyridine der allgemeinen Formel (X) sind bekannt oder können nach bekannten Methoden hergestellt werden [EP-A 88 276; DE-A 28 47 236].The dihydropyridines of the general formula (X) used as starting materials are known or can be prepared by known methods [EP-A 88 276; DE-A 28 47 236].
Die erfindungsgemäßen Verbindungen der allgemeinen Formel (I) sind Wirkstoffe für Arzneimittel. Insbesondere sind sie Inhibitoren der 3-Hydroxy-3-methyl-glutaryl-Coenzym A (HGM-CoA) Reduktase und infolgedessen Inhibitoren der Cholesterolbiosynthese. Sie können deshalb zur Behandlung von Hyperlipoproteinämie, Lipoproteinämie oder Arteriosklerose eingesetzt werden. Die erfindungsgemäßen Wirkstoffe bewirken außerdem eine Senkung des Cholesteringehaltes im Blut.The compounds of general formula (I) according to the invention are active ingredients for medicinal products. In particular, they are inhibitors of 3-hydroxy-3-methyl-glutaryl-coenzyme A (HGM-CoA) reductase and consequently inhibitors of cholesterol biosynthesis. They can therefore be used to treat hyperlipoproteinemia, lipoproteinemia or arteriosclerosis. The active compounds according to the invention also bring about a reduction in the cholesterol content in the blood.
Die neuen Wirkstoffe können in bekannter Weise in die üblichen Formulierungen überführt werden, wie Tabletten, Dragees, Pillen, Granulate, Aerosole, Sirupe, Emulsionen, Suspensionen und Lösungen, unter Verwendung inerter, nicht toxischer, pharmazeutisch geeigneter Trägerstoffe oder Lösungsmittel. Hierbei soll die therapeutisch wirksame Verbindung jeweils in einer Konzentration von etwa 0,5 bis 98-Gew.-%, bevorzugt 1 bis 90 Gew.-%, der Gesamtmischung vorhanden sein, d.h. in Mengen, die ausreichend sind, um den angegebenen Dosierungsspielraum zu erreichen.The new active compounds can be converted in a known manner into the customary formulations, such as tablets, dragées, pills, granules, aerosols, syrups, emulsions, suspensions and solutions, using inert, non-toxic, pharmaceutically suitable excipients or solvents. Here, the therapeutically active compound should in each case be present in a concentration of about 0.5 to 98% by weight, preferably 1 to 90% by weight, of the total mixture, i.e. in amounts sufficient to achieve the dosage range indicated.
Die Formulierungen werden beispielsweise hergestellt durch Verstrecken der Wirkstoffe mit Lösungsmitteln und/oder Trägerstoffen, gegebenenfalls unter Verwendung von Emulgiermitteln und/oder Dispergiermitteln, wobei z.B. im Fall der Benutzung von Wasser als Verdünnungsmittel gegebenenfalls organische Lösungsmittel als Hilfslösungsmittel verwendet werden können.The formulations are prepared, for example, by stretching the active ingredients with solvents and / or carriers, optionally using emulsifiers and / or dispersants, e.g. if water is used as the diluent, organic solvents can optionally be used as auxiliary solvents.
Als Hilfsstoffe seien beispielsweise aufgeführt:
- Wasser, nicht-toxische organische Lösungsmittel, wie Paraffine (z.B. Erdölfraktionen), pflanzliche Öle (z.B. Erdnuß/Sesamöl), Alkohole (z.b: Ethylalkohol, Glycerin), Trägerstoffe, wie z.B. natürliche Gesteinsmehle (z.B. Kaoline, Tonerden, Talkum, Kreide), synthetische Gesteinsmehle (z.B. hochdisperse Kieselsäure, Silikate), Zucker (z.B. Rohr-, Milch- und Traubenzucker), Emulgiermittel (z.B. Polyoxyethylen-FettsäureEster, Polyoxyethylen-Fettalkohol-Ether, Alkylsulfonate und Arylsulfonate), Dispergiermittel (z.B. Lignin-Sulfitablaugen, Methylcellulose, Stärke und Polyvinylpyrrolidon) und Gleitmittel (z.B. Magnesiumstearat, Talkum, Stearinsäure und Natriumlaurylsulfat).
- Water, non-toxic organic solvents, such as paraffins (e.g. petroleum fractions), vegetable oils (e.g. peanut / sesame oil), alcohols (e.g. ethyl alcohol, glycerin), carriers, such as natural rock flour (e.g. kaolins, clays, talc, chalk), synthetic rock flour (e.g. highly disperse silica, silicates), sugar (e.g. cane, milk and dextrose), emulsifiers (e.g. polyoxyethylene fatty acid esters, polyoxyethylene fatty alcohol ethers, alkyl sulfonates and aryl sulfonates), dispersants (e.g. lignin sulfite liquor, methyl cellulose and polyvinylpyrrolidone) and lubricants (e.g. magnesium stearate, talc, stearic acid and sodium lauryl sulfate).
Die Applikation erfolgt in üblicher Weise, vorzugsweise oral, parenteral, perlingual oder intravenös. Im Falle der oralen Anwendung können Tabletten selbstverständlich außer den genannten Trägerstoffen auch Zusätze, wie Natriumcitrat, Calciumcarbonat und Dicalciumphosphat zusammen mit verschiedenen Zuschlagstoffen, wie Stärke, vorzugsweise Kartoffelstärke, Gelatine und dergleichen enthalten. Weiterhin können Gleitmittel, wie Magnesiumstearat, Natriumlaurylsulfat und Talkum zum Tablettieren mitverwendet werden. Im Falle wäßriger Suspensionen können die Wirkstoffe außer den obengenannten Hilfsstoffen mit verschiedenen Geschmacksaufbesserern oder Farbstoffen versetzt werden.The application is carried out in the usual way, preferably orally, parenterally, perlingually or intravenously. In the case of oral use, tablets can of course also contain additives, such as sodium citrate, calcium carbonate and dicalcium phosphate, together with various additives, such as starch, preferably potato starch, gelatin and the like, in addition to the carrier substances mentioned. Lubricants such as magnesium stearate, sodium lauryl sulfate and talc can also be used for tableting. In the case of aqueous suspensions, in addition to the auxiliaries mentioned above, the active ingredients can be mixed with various flavor enhancers or colorants.
Für den Fall der parenteralen Anwendung können Lösungen der Wirkstoffe unter Verwendung geeigneter flüssiger Trägermaterialien eingesetzt werden.In the case of parenteral use, solutions of the active ingredients can be used using suitable liquid carrier materials.
Im allgemeinen hat es sich als vorteilhaft erwiesen, bei intravenöser Applikation Mengen von etwa 0,001 bis 1 mg/kg, vorzugsweise etwa 0,01 bis 0,5 mg/kg Körpergewicht zur Erzielung wirksamer Ergebnisse zu verabreichen, und bei oraler Applikation beträgt die Dosierung etwa 0,01 bis 20 mg/kg, vorzugsweise 0,1 bis 10 mg/kg Körpergewicht.In general, it has proven to be advantageous to administer amounts of approximately 0.001 to 1 mg / kg, preferably approximately 0.01 to 0.5 mg / kg of body weight in the case of intravenous administration in order to achieve effective results, and the dosage is approximately in the case of oral administration 0.01 to 20 mg / kg, preferably 0.1 to 10 mg / kg body weight.
Trotzdem kann es gegebenenfalls erforderlich sein, von den genannten Mengen abzuweichen, und zwar in Abhängigkeit vom Körpergewicht bzw. der Art des Applikationsweges, vom individuellen Verhalten gegenüber dem Medikament, der Art von dessen Formulierung und dem Zeitpunkt bzw. Intervall, zu welchen die Verabreichung erfolgt. So kann es in einigen Fällen ausreichend sein, mit weniger als der vorgenannten Mindestmenge auszukommen, während in anderen Fällen die genannte obere Grenze überschritten werden muß. Im Falle der Applikation größerer Mengen kann es empfehlenswert sein, diese in mehreren Einzelgaben über den Tag zu verteilen.Nevertheless, it may be necessary to deviate from the amounts mentioned, depending on the body weight or the type of application route, on the individual behavior towards the drug, the type of its formulation and the time or interval at which the administration takes place . In some cases it may be sufficient to make do with less than the minimum quantity mentioned above, while in other cases the above-mentioned upper limit must be exceeded. In the case of application of larger quantities, it may be advisable to distribute them in several individual doses over the day.
62 g (0,5 mol) 4-Fluorbenzaldehyd und 79 g (0,5 mol) Isobutanoylessigsäureethylester werden in 300 ml trockenem Isopropanol vorgelegt und mit einem Gemisch aus 2,81 ml (28 mmol) Piperidin und 1,66 ml (29 mmol) Essigsäure in 40 ml Isopropanol versetzt. Man läßt 48 h bei Raumtemperatur rühren, engt im Vakuum ein und destilliert den Rückstand im Hochvakuum.
- Kp 0.5 mm : 127°C
- Ausbeute: 108,7 g (82,3% der Theorie)
- Kp 0.5 mm: 127 ° C
- Yield: 108.7 g (82.3% of theory)
98 g (0,371 mol) der Verbindung aus Beispiel 1 werden mit 58,3 g (0,371 mol) 3-Amino-4-methyl-pent-2-en-säure-ethylester in 300 ml Ethanol 18 Stunden unter Rückfluß gekocht. Die Mischung wird auf Raumtemperatur abgekühlt, das Lösungsmittel im Vakuum abgedampft und die nicht umgesetzten Ausgangsmaterialien werden im Hochvakuum bei 130°C abdestilliert. Den zurückbleibenden Sirup verrührt man mit n-Hexan und saugt den ausgefallenen Niederschlag ab, wäscht mit n-Hexan nach und trocknet im Exsikkator.
- Ausbeute: 35 g (23,4% der Theorie)
- 1H-NMR (CDCI3): δ = 1,1 - 1,3 (m, 18H); 4,05 - 4,25 (m, 6H); 5,0 (s, 1H); 6,13 (s, 1H); 6,88 (m, 2H); 7,2 (m, 2H).
- Yield: 35 g (23.4% of theory)
- 1 H NMR (CDCI 3 ): δ = 1.1-1.3 (m, 18H); 4.05 - 4.25 (m, 6H); 5.0 (s, 1H); 6.13 (s, 1H); 6.88 (m. 2H); 7.2 (m, 2H).
Zu einer Lösung von 6,6 g (16,4 mmol) der Verbindung aus Beispiel 2 in 200 ml Methylenchlorid p.a. gibt man 3,8 g (16,4 mmol) 2,3-Dichlor-5,6-dicyanp-benzochinon und rührt 1 h bei Raumtemperatur. Dann wird über Kieselgur abgesaugt, die Methylenchloridphase dreimal mit je 100 ml Wasser extrahiert und über Magnesiumsulfat getrocknet. Nach Einengen im Vakuum wird der Rückstand an einer Säule (100 g Kieselgel 70-230 mesh, φ 3,5 cm, mit Essigester/Petrolether (1:9), chromatographiert.
- Ausbeute: 5,8 g (87,9% der Theorie)
- 1H-NMR (CDCl3): δ = 0,98 (t, 6H); 1,41 (d, 12H); 3,1 (m, 2H); 4,11 (q, 4H); 7,04 (m, 2H); 7,25 (m, 2H).
- Yield: 5.8 g (87.9% of theory)
- 1 H NMR (CDCl 3 ): δ = 0.98 (t, 6H); 1.41 (d, 12H); 3.1 (m. 2H); 4.11 (q, 4H); 7.04 (m, 2H); 7.25 (m. 2H).
Unter Stickstoff gibt man zu einer Lösung von 4,6 g (11,4 mmol) der Verbindung aus Beispiel 3 in 100 ml trockenem Tetrahydrofuran bei -10°C bis -5°C 22,8 ml (80 mmol) einer 3,5 molaren Lösung von Natrium-bis-(2-methoxyethoxy)-dihydroaluminat in Toluol. Man rührt über Nacht bei Raumtemperatur und erwärmt anschließend 5 h auf 40° C. Nach erneutem Abkühlen auf 0°C tropft man vorsichtig 100 ml Wasser zu und extrahiert dreimal mit je 100 ml Essigester. Die vereinigten organischen Phasen werden mit gesättigter Natriumchlorid-Lösung gewaschen, über Magnesiumsulfat getrocknet und im Vakuum eingeengt. Der Rückstand wird an einer Säule (100 g Kieselgel 70-230 mesh, 0 3,5 cm, mit Essigester/Petrolether (6:4), chromatographiert.
- Ausbeute: 2,4 g (66,7% der Theorie)
- 1H-NMR (CDCl3): δ = 1,35 (d, 12H); 3,43 (m, 2H); 4,47 (d, 4H); 7,05 - 7,3 (m, 4H).
- Yield: 2.4 g (66.7% of theory)
- 1 H NMR (CDCl 3 ): δ = 1.35 (d, 12H); 3.43 (m, 2H); 4.47 (d. 4H); 7.05 - 7.3 (m, 4H).
Zu einer Lösung von 3,8 g (12 mmol) der Verbindung aus Beispiel 4 in 100 ml Methylenchlorid p.a. gibt man 10,3 g (48 mmol) Pyridiniumchlorochromat und 4,9 g (48 mmol) neutrales Aluminiumoxid und rührt 1 h bei Raumtemperatur. Man saugt über Kieselgur ab und wäscht mit 300 ml Methylenchlorid nach. Die Methylenchloridphase wird im Vakuum eingeengt und der Rückstand an einer Säule (150 g Kieselgel 70-230 mesh, φ 3,5 cm, mit Essigester/Petrolether 2:8) chromatographiert.
- Ausbeute: 3,2 g (85,3% der Theorie)
- 'H-NMR (CDCl3): δ = 1,33 (d, 12H); 3,85 (m, 2H); 7,1 -7,32 (m, 4H); 9,8 (s, 2H).
- Yield: 3.2 g (85.3% of theory)
- 'H NMR (CDCl 3 ): δ = 1.33 (d, 12H); 3.85 (m, 2H); 7.1 -7.32 (m, 4H); 9.8 (s, 2H).
Unter Stickstoff tropft man zu einer Suspension von 0,36 g (12 mmol) 80%igem Natriumhydrid in 20 ml trockenem Tetrahydrofuran bei -5 C 3,1 g (12 mmol) Diethyl-2-(cyclohexylamino)-vinylphosphonat gelöst in 20 ml trockenem Tetrahydrofuran. Nach 30 min. werden bei derselben Temperatur 1,6 g (5 mmol) der Verbindung aus Beispiel 5 in 20 ml trockenem Tetrahydrofuran zugetropft und 30 min zum Rückfluß erwärmt. Nach Abkühlen auf Raumtemperatur wird der Ansatz in 200 ml eiskaltes Wasser gegeben und dreimal mit je 100 ml Essigester extrahiert. Die vereinigten organischen Phasen werden mit gesättigter Natriumchlorid-Lösung gewaschen und über Magnesiumsulfat getrocknet. Nach Einengen im Vakuum wird der Rückstand in 50 ml Toluol aufgenommen, mit einer Lösung von 2 g (15 mmol) Oxalsäure-Dihydrat in 25 ml Wasser versetzt und 30 min zum Rückfluß erwärmt. Nach Abkühlen auf Raumtemperatur werden die Phasen getrennt, die organische Phase mit gesättigter Natriumchlorid-Lösung gewaschen, über Magnesiumsulfat getrocknet und im Vakuum eingeengt. Der Rückstand wird an einer Säule (100 g Kieselgel 70-230 mesh, 0 3,5 cm, mit EssigesteriPetrolether 2:8) chromatographiert.
- Ausbeute: 920 mg (50% der Theorie)
- 'H-NMR (CDCl3): δ = 1,33 (d, 12H); 3,33 (m, 2H); 6,03 (dd, 2H); 7,0 - 7,35 (m, 6H); 9,42 (d, 2H).
- Yield: 920 mg (50% of theory)
- 'H NMR (CDCl 3 ): δ = 1.33 (d, 12H); 3.33 (m, 2H); 6.03 (dd, 2H); 7.0 - 7.35 (m, 6H); 9.42 (d. 2H).
Unter Stickstoff tropft man zu einer Suspension von 360 mg (12 mmol) 80%igem Natriumhydrid in 30 ml trockenem Tetrahydrofuran bei -5°C 1,16 g (10 mmol) Acetessigsäuremethylester in 5 ml trockenem Tetrahyrofuran. Nach 15 min werden bei derselben Temperatur 6,2 ml (10 mmol) 15%iges Butyllithium in n-Hexan zugetropft und 15 min. nachgerührt. Anschließend werden 912 mg (2,5 mmol) der Verbindung aus Beispiel 6 gelöst in 20 ml trockenem Tetrahydrofuran zugetropft und 30 min bei -5°C nachgerührt. Die Reaktionslösung wird vorsichtig mit 3 ml 50%iger Essigsäure versetzt, mit 100 ml Wasser verdünnt und die Mischung dreimal mit je 100 ml Ether extrahiert. Die vereinigten organischen Phasen werden zweimal mit gesättigter Natriumhydrogencarbonat-Lösung und einmal mit gesättigter Natriumchlorid-Lösung gewaschen, über Magnesiumsulfat getrocknet und im Vakuum eingeengt. Der Rückstand wird an einer Säule (80 g Kieselgel 70-230 mesh, φ 3 cm, mit Essigester/Petrolether 1:1) chromatographiert.
- Ausbeute: 800 mg (53,6% der Theorie)
- 1H-NMR (CDCl3): δ = 1,25 (m, 12H); 2,47 (m, 4H); 3,25 (m, 2H); 3,42 (s, 4H); 3,73 (s, 6H); 4,5 (m, 2H); 5,25 (dd, 2H); 6,35 (dd, 2H); 7,0 (m, 4H).
- Yield: 800 mg (53.6% of theory)
- 1 H NMR (CDCl 3 ): δ = 1.25 (m, 12H); 2.47 (m, 4H); 3.25 (m. 2H); 3.42 (s, 4H); 3.73 (s, 6H); 4.5 (m. 2H); 5.25 (dd, 2H); 6.35 (dd, 2H); 7.0 (m, 4H).
Zu einer Lösung von 776 mg (1,3 mmol) der Verbindung aus Beispiel 7 in 30 ml trockenem Tetrahydrofuran gibt man bei Raumtemperatur 3,2 ml (3,2 mmol) 1 M Triethylboran-Lösung in Tetrahydrofuran, leitet während 5 min Luft durch die Lösung und kühlt auf -30 C Innentemperatur ab. Es werden 122 mg (3,2 mmol) Natriumborhydrid und langsam 2,5 ml Methanol zugegeben, 30 min bei -30 C gerührt und dann mit einem Gemisch von 10 ml 30%igem Wasserstoffperoxid und 20 ml Wasser versetzt. Die Temperatur läßt man dabei bis 0 C ansteigen und rührt noch 30 min nach. Die Mischung wird dreimal mit je 50 ml Essigester extrahiert, die vereinigten organischen Phasen je einmal mit gesättigter Natriumhydrogencarbonat-Lösung und gesättigter Natriumchlorid-Lösung gewaschen, über Magnesiumsulfat getrocknet und im Vakuum eingeengt. Der Rückstand wird an einer Säule (50 g Kieselgel 230-400 mesh, φ 2,5 cm, mit Essigester/Petrolether 1:1) chromatographiert.
- Ausbeute: 400 mg (51,4% der Theorie)
- 1H-NMR (CDCI3): δ = 12,5 (m, 12H); 1,4 (m, 4H); 2,42 (m, 4H); 3,3 (m, 2H); 3,72 (s, 6H); 4,1 (m, 2H); 4,3 (m, 2H); 5,25 (dd, 2H); 6,3 (dd, 2H); 7,0 (m, 4H).
- Yield: 400 mg (51.4% of theory)
- 1 H NMR (CDCI 3 ): δ = 12.5 (m, 12H); 1.4 (m, 4H); 2.42 (m, 4H); 3.3 (m. 2H); 3.72 (s, 6H); 4.1 (m. 2H); 4.3 (m. 2H); 5.25 (dd, 2H); 6.3 (dd, 2H); 7.0 (m, 4H).
6.9 g (0,44 mol) Isobutanoylessigsäureethylester und 46,3 g (0,44 mol) Benzaldehyd werden in 300 ml Isopropanol vorgelegt, mit einem Gemisch aus 2,5 ml (25 mmol) Piperidin und 1,5 ml (26 mmol) Essigsäure in 40 ml Isopropanol versetzt und 24 h bei Raumtemperatur gerührt. Die Mischung wird im Vakuum eingeengt und der Rückstand im Hochvakuum destilliert.
- Kp 0.5 mm : 130 °C
- Ausbeute: 60.7 g (56,2% der Theorie)
- Kp 0.5 mm: 130 ° C
- Yield: 60.7 g (56.2% of theory)
29,5 g (120 mmol) der Verbindung aus Beispiel 9 und 18,8 g (120 mmol) 3-Amino-4-methyl-pent-2-en- säureethylester werden in 150 ml Ethanol 48 Stunden unter Rückfluß gekocht. Die Mischung wird abgekühlt, im Vakuum eingeengt und der Rückstand an einer Säule (500 g Kieselgel, 70-230 mesh, φ 5 cm, mit Essigester/Pstrolether 1:9) chromatographiert.
- Ausbeute: 7,2 g (15,1% der Theorie)
- 'H-NMR (CDCl3): δ = 1,2 (m, 18 H); 4,1 (m, 4H); 4,21 (m, 2H); 5,02 (s, 1H); 6,13 (s, 1H); 7,2 (m, 5H).
- Yield: 7.2 g (15.1% of theory)
- 'H NMR (CDCl 3 ): δ = 1.2 (m, 18 H); 4.1 (m, 4H); 4.21 (m. 2H); 5.02 (s, 1H); 6.13 (s, 1H); 7.2 (m, 5H).
7,2 g (18,2 mmol) der Verbindung aus Beispiel 10 werden analog Beispiel 3 umgesetzt. Ausbeute: 6,4 g (88,8% der Theorie)7.2 g (18.2 mmol) of the compound from Example 10 are reacted analogously to Example 3. Yield: 6.4 g (88.8% of theory)
Unter Stickstoff werden zu einer Lösung von 6,4 g (16,2 mmol) der Verbindung aus Beispiel 11 in 100 ml trockenem Tetrahydrofuran bei 0°C 40,5 ml (40,5 mmol) einer 1 molaren Lösung von Lithiumaluminiumhydrid in Ether zugetropft. Man rührt über Nacht bei Raumtemperatur, erwärmt 3 h auf 50°C und kühlt erneut auf 0°C ab. Zu der Mischung tropft man vorsichtig 200 ml Wasser, saugt über Kieselgur ab und wäscht mit 250 ml Ether nach. Die organische Phase wird abgetrennt, einmal mit gesättigter Natriumchlorid-Lösung gewaschen, über Magnesiumsulfat getrocknet und im Vakuum eingeengt. Den Rückstand verrührt man mit Petrolether, saugt den Niederschlag ab und trocknet im Exsikkator.
- Ausbeute: 4 g (83,3% der Theorie)
- 1H-NMR (CDCl3): 5 = 1,3 (d, 12H); 3,5 (m, 2H); 4,3 (d, 4H); 7,35 (m, 5H).
- Yield: 4 g (83.3% of theory)
- 1 H NMR (CDCl 3 ): 5 = 1.3 (d, 12H); 3.5 (m, 2H); 4.3 (d. 4H); 7.35 (m, 5H).
4 g (13,3 mmol) der Verbindung aus Beispiel 12 werden analog Beispiel 5 umgesetzt. Ausbeute: 3,4 g (87,2% der Theorie)
- 'H-NMR (CDCl3): δ = 1,35 (d, 12H); 3,4 (m, 2H); 7,3 (m, 2H); 7,5 (m, 3H); 9,3 (s, 2H).
- 'H NMR (CDCl 3 ): δ = 1.35 (d, 12H); 3.4 (m. 2H); 7.3 (m. 2H); 7.5 (m. 3H); 9.3 (s, 2H).
3.35 g (11,4 mmol) der Verbindung aus Beispiel 13 werden analog Beispiel 6 umgesetzt. Ausbeute: 2,7 g (67,5% der Theorie)
- 'H-NMR (CDCl3): δ = 1,35 (d, 12H); 3,47 (m, 2H); 6,04 (dd, 2H); 7,0 - 7,45 (m, 7H); 9,4 (d, 2H).
- 'H NMR (CDCl 3 ): δ = 1.35 (d, 12H); 3.47 (m, 2H); 6.04 (dd, 2H); 7.0 - 7.45 (m, 7H); 9.4 (d. 2H).
2,7 g (7,8 mmol) der Verbindung aus Beispiel 14 werden analog Beispiel 7 umgesetzt. Ausbeute: 3,2 g (71,1% der Theorie)
- 1H-NMR (CDCI3): δ = 1,25 (m, 12H); 2,35 (m, 4H); 3,27 (m, 2H); 3,40 (s, 4H); 3,75 (s, 6H); 4,38 (m, 2H); 5,25 (dd, 2H); 6,37 (dd, 2H); 7,02 (m, 2H); 7,30 (m, 3H).
- 1 H NMR (CDCI 3 ): δ = 1.25 (m, 12H); 2.35 (m, 4H); 3.27 (m. 2H); 3.40 (s, 4H); 3.75 (s, 6H); 4.38 (m. 2H); 5.25 (dd, 2H); 6.37 (dd, 2H); 7.02 (m, 2H); 7.30 (m, 3H).
3,2 g (5,5 mmol) der Verbindung aus Beispiel 15 werden analog Beispiel 8 umgesetzt. Ausbeute: 2 g (62,5% der Theorie)
- 1H-NMR (CDCl3): δ = 1,25 (m, 12H); 1,3 - 1,7 (m, 4H); 2,39 (m, 4H); 3,2 - 3,4 (m, 2H); 3,71 (s, 6H); 4,02 (m, 2H); 4,27 (m, 2H); 5,3 (m, 2H); 6,32 (m, 2H); 7,0 (m, 2h); 7,25 (m, 3H).
- 1 H NMR (CDCl 3 ): δ = 1.25 (m, 12H); 1.3 - 1.7 (m, 4H); 2.39 (m, 4H); 3.2 - 3.4 (m, 2H); 3.71 (s, 6H); 4.02 (m, 2H); 4.27 (m. 2H); 5.3 (m, 2H); 6.32 (m. 2H); 7.0 (m, 2h); 7.25 (m. 3H).
62 g (0,5 mol) 4-Fluorbenzaldehyd und 53,9 ml (0,5 mol) Acetessigsäuremethylester werden in 300 ml Isopropanol vorgelegt, mit einem Gemisch aus 2,81 ml (28 mmol) Piperidin und 1,66 ml (29 mmol) Essigsäure in 40 ml Isopropanol versetzt und 48 h bei Raumtemperatur gerührt. Die Mischung wird im Vakuum eingeengt und der Rückstand im Hochvakuum destilliert.
- Kp 0,5 mm: 138°C
- Ausbeute: 50,5 g (45,5% der Theorie)
- Kp 0.5 mm: 138 ° C
- Yield: 50.5 g (45.5% of theory)
33,3 g (0,15 mol) der Verbindung aus Beispiel 17 werden mit 17,3 g (0,15 mol) 3-Aminocrotonsäuremethylester in 150 ml Ethanol 4 h unter Rückfluß gekocht. Die Mischung wird auf 0°C abgekühlt, der ausgefallene Niederschlag abgesaugt, mit wenig Petrolether nachgewaschen und im Exsikkator getrocknet. Ausbeute: 32 g (66,8% der Theorie)
- 'H-NMR (CDCl3): δ = 2,33 (s, 6H); 3,65 (s, 6H); 4,99 (s, 1H); 5,77 (s, 1H); 6,89 (m, 2H); 7,22 (m, 2H).
- 'H NMR (CDCl 3 ): δ = 2.33 (s, 6H); 3.65 (s, 6H); 4.99 (s, 1H); 5.77 (s, 1H); 6.89 (m. 2H); 7.22 (m, 2H).
32 g (0,1 mol) der Verbindung aus Beispiel 18 werden analog Beispiel 3 umgesetzt. Ausbeute: 27,2 g (87% der Theorie)
- 'H-NMR (CDCI3): δ = 2,59 (s, 6H); 3,56 (s, 6H); 7,08 (m, 2H); 7,25 (m, 2H).
- 'H NMR (CDCI 3 ): δ = 2.59 (s, 6H); 3.56 (s, 6H); 7.08 (m, 2H); 7.25 (m. 2H).
Unter Stickstoff gibt man zu einer Lösung von 7,9 g (25 mmol) der Verbindung aus Beispiel 19 in 100 ml trockenem Tetrahydrofuran bei 0°C 25 ml (87,5 mmol) einer 3,5 molaren Lösung von Natrium-bis-(2-methoxyethoxy)-dihydroaluminat in Toluol. Man rührt 6 h bei Raumtemperatur, kühlt erneut auf 0°C ab und tropft langsam 200 ml Wasser zu. Die Mischung wird dreimal mit je 150 ml Essigester extrahiert, die vereinigten organischen Phasen einmal mit gesättigter Natriumchlorid-Lösung gewaschen, über Magnesiumsulfat getrocknet und im Vakuum eingeengt. Den Rückstand verrührt man mit Ether, saugt ab und trocknet im Exsikkator.
- Ausbeute: 3,5 g (53,8% der Theorie)
- 1H-NMR (CDCl3): 5 = 2,81 (s, 6H); 4,28 (d, 4H); 7,1 (m, 2H); 7,3 (m, 2H).
- Yield: 3.5 g (53.8% of theory)
- 1 H NMR (CDCl 3 ): 5 = 2.81 (s, 6H); 4.28 (d. 4H); 7.1 (m. 2H); 7.3 (m, 2H).
3,5 g (13,4 mmol) der Verbindung aus Beispiel 20 werden analog Beispiel 5 umgesetzt. Ausbeute: 1,7 g (53% der Theorie)
- 1H-NMR (CDCI3): δ = 2,88 (s, 6H); 7,28 (m, 4H); 9,82 (s, 2H).
- 1 H NMR (CDCI 3 ): δ = 2.88 (s, 6H); 7.28 (m. 4H); 9.82 (s, 2H).
1,7 g (7 mmol) der Verbindung aus Beispiel 21 werden analog Beispiel 6 umgesetzt. Ausbeute: 1 g (47,6% der Theorie)
- 1H-NMR (CDCl3): δ = 2,7 (s, 6H); 6,15 (dd, 2H); 7,15 (m, 6H); 9,43 (d, 2H).
- 1 H NMR (CDCl 3 ): δ = 2.7 (s, 6H); 6.15 (dd, 2H); 7.15 (m. 6H); 9.43 (d. 2H).
1 g (3,2 mmol) der Verbindung aus Beispiel 22 werden analog Beispiel 7 umgesetzt. Ausbeute: 1 g (57 % der Theorie)
- 'H-NMR (CDCl3): 0 = 2,50 (m, 4H); 2,55 (s, 6H); 3,45 (s, 4H); 3,73 (s, 6H); 4,52 (m, 2H); 5,35 (dd, 2H); 6,28 (d. 2H); 7,05 (m, 4H) ppm.
- 'H NMR (CDCl 3 ): 0 = 2.50 (m, 4H); 2.55 (s, 6H); 3.45 (s, 4H); 3.73 (s, 6H); 4.52 (m. 2H); 5.35 (dd, 2H); 6.28 (d. 2H); 7.05 (m, 4H) ppm.
1 g (1,8 mmol) der Verbindung aus Beispiel 23 werden analog Beispiel 8 umgesetzt. Ausbeute: 0,7 g (69,9 % der Theorie)
- 'H-NMR (CDCl3): δ = 1,20-1,60 (m, 4H); 2,43 (m, 4H); 2,54 (s, 6H); 3,72 (s, 6H); 4,09 (m, 2H); 4,33 (m, 2H); 5,37 (dd, 2H); 6,22 (d, 2H); 7,03 (m, 4H) ppm.
- 'H NMR (CDCl 3 ): δ = 1.20-1.60 (m, 4H); 2.43 (m, 4H); 2.54 (s, 6H); 3.72 (s, 6H); 4.09 (m. 2H); 4.33 (m, 2H); 5.37 (dd, 2H); 6.22 (d. 2H); 7.03 (m, 4H) ppm.
15 g (56,8 mol) der Verbindung aus Beispiel 1 und 6,5 g (56,8 mmol) 3-Aminocrotonsäuremethylester werden in 150 ml Ethanol 20 h am Rückfluß gekocht. Die Mischung wird abgekühlt, abfiltriert und im Vakuum eingeengt. Der Rückstand wird an einer Säule (250 g Kieselgel 70-230 mesh, φ 4,5 cm, mit . Essigester/Petrolether 3:7) chromatographiert.
- Ausbeute: 13,6 g (66,3% der Theorie)
- 1H-NMR (CDCl3): δ = 1,2 (m, 9H); 2,35 (s, 3H); 3,65 (s, 3H); 4,12 (m, 3H); 4,98 (s, 1H); 5,75 (s, 1H); 6,88 (m, 2H); 7,25 (m, 2H).
- Yield: 13.6 g (66.3% of theory)
- 1 H NMR (CDCl 3 ): δ = 1.2 (m, 9H); 2.35 (s, 3H); 3.65 (s, 3H); 4.12 (m, 3H); 4.98 (s, 1H); 5.75 (s, 1H); 6.88 (m. 2H); 7.25 (m. 2H).
13,5 g (37,4 mmol) der Verbindung aus Beispiel 25 werden analog Beispiel 3 umgesetzt. Ausbeute: 9,5 g (70,9% der Theorie)
- 1H-NMR (CDCI3): δ = 0,98 (t, 3H); 1,31 (d, 6H); 2,6 (s, 3H); 3,11 (m, 1H); 3,56 (s, 3H); 4,03 (q, 2H); 7,07 (m, 2H); 7,25 (m, 2H).
- 1 H NMR (CDCI 3 ): δ = 0.98 (t, 3H); 1.31 (d, 6H); 2.6 (s. 3H); 3.11 (m, 1H); 3.56 (s. 3H); 4.03 (q, 2H); 7.07 (m, 2H); 7.25 (m. 2H).
Unter Stickstoff werden zu einer Suspension von 6 g (158 mmol) Lithiumaluminiumhydrid in 200 ml absolutem Tetrahydrofuran bei 60°C langsam 20,7 g (57,7 mmol) der Verbindung aus Beispiel 26 gelöst in 50 ml absolutem Tetrahydrofuran zugetropft. Die Mischung wird 1 h zum Rückfluß erhitzt, auf 0°C abgekühlt und vorsichtig mit 18 ml Wasser versetzt. Man gibt 6 ml 10%ige Kaliumhydroxyd-Lösung dazu, saugt vom Niederschlag ab und kocht den Rückstand zweimal mit je 250 ml Ether aus. Die vereinigten Mutterlaugen werden über Magnesiumsulfat getrocknet und im Vakuum eingeengt. Der Rückstand wird mit Petrolether verrührt, abgesaugt und im Exsikkator getrocknet.
- Ausbeute: 11,5 g (68,9% der Theorie)
- 'H-NMR (CDC13): δ = 1,3 (d, 6H); (s, 3H); 3,51 (m, 1H); 4,3 (m, 4H); 7,1 (m, 2H); 7,3 (m, 2H).
- Yield: 11.5 g (68.9% of theory)
- 'H NMR (CDC1 3 ): δ = 1.3 (d, 6H); (s, 3H); 3.51 (m, 1H); 4.3 (m. 4H); 7.1 (m. 2H); 7.3 (m, 2H).
11.5 g (40 mmol) der Verbindung aus Beispiel 27 werden analog Beispiel 5 umgesetzt. Ausbeute: 7,3 g (64% der Theorie)
- 1H-NMR (CDCl3): δ = 1,32 (d, 6H); 2,88 (s, 3H); 3,87 (m, 1H); 7,25 (m, 4H); 9,81 (d, 2H).
- 1 H NMR (CDCl 3 ): δ = 1.32 (d, 6H); 2.88 (s, 3H); 3.87 (m, 1H); 7.25 (m. 4H); 9.81 (d. 2H).
7,3 g (21,7 mmol) der Verbindung aus Beispiel 28 werden analog Beispiel 6 umgesetzt. Ausbeute: 6,35 g (86,9% der Theorie)
- 1H-NMR (CDCl3): δ = 1,32 (d, 6H); 2,7 (s, 3H); 3,34 (m, 1 H); 6,02 (dd, 1 H); 6,15 (dd, 1 H); 7,0 - 7,35 (m, 6H); 9,42 (d, 1 H); 9,43 (d, 1 H).
- 1 H NMR (CDCl 3 ): δ = 1.32 (d, 6H); 2.7 (s. 3H); 3.34 (m, 1H); 6.02 (dd, 1H); 6.15 (dd, 1H); 7.0 - 7.35 (m, 6H); 9.42 (d, 1H); 9.43 (d, 1H).
6,3 g (18,8 mol) der Verbindung aus Beispiel 29 werden analog Beispiel 7 umgesetzt. Ausbeute: 5,7 g (53,5% der Theorie)
- 1H-NMR (CDCI3): δ = 1,25 (d, 6H); 2,42 (m, 2H); 2,53 (m, 2H); 2,57 (s, 3H); 3,28 (m, 1H); 3,42 (s, 2H); 3,43 (s, 2H); 3,75 (s, 6H); 4,52 (m, 2H); 5,25 (dd, 1 H); 5,36 (dd, 1 H); 6,28 (d, 1 H); 6,37 (d, 1 H); 6,90 - 7,20 (m, 4H).
- 1 H NMR (CDCI 3 ): δ = 1.25 (d, 6H); 2.42 (m, 2H); 2.53 (m. 2H); 2.57 (s, 3H); 3.28 (m, 1H); 3.42 (s, 2H); 3.43 (s, 2H); 3.75 (s, 6H); 4.52 (m. 2H); 5.25 (dd, 1H); 5.36 (dd, 1H); 6.28 (d, 1H); 6.37 (d, 1H); 6.90 - 7.20 (m, 4H).
5,7 g (10 mmol) der Verbindung aus Beispiel 30 werden analog Beispiel 8 umgesetzt. Ausbeute: 2,9 g (50,8% der Theorie)
- 'H-NMR (CDCl3): δ = 1,25 (m, 6H); 1,2 - 1,5 (m, 4H); 2,41 (m, 4H); 2,57 (s, 3H); 3,3 (m, 1 H); 3,72 (s, 6H); 4,1 (m, 2H); 4,3 (m, 2H); 5,15 - 5,5 (m, 2H); 6,15 -6,45 (m, 2H); 7,0 (m, 4H).
- 'H NMR (CDCl 3 ): δ = 1.25 (m, 6H); 1.2 - 1.5 (m, 4H); 2.41 (m, 4H); 2.57 (s, 3H); 3.3 (m, 1H); 3.72 (s, 6H); 4.1 (m. 2H); 4.3 (m. 2H); 5.15 - 5.5 (m, 2H); 6.15 -6.45 (m, 2H); 7.0 (m, 4H).
9.5 g (73,6 mmol) 3-Amino-pent-2-en-säuremethylester und 19,4 g (73,6 mmol) der Verbindung aus Beispiel 1 werden in 200 ml n-Butanol 5 Stunden unter Rückfluß gekocht. Die Mischung wird auf Raumtemperatur abgekühlt, das Lösungsmittel im Vakuum eingeengt und der Rückstand an einer Säule (Kieselgel 70-230 mesh, mit Petrolether/Essigester 9:1) chromatographiert.
- Ausbeute: 5,3 g (19,3 % der Theorie)
- Yield: 5.3 g (19.3% of theory)
Aus der Verbindung aus Beispiel 32 wurde, in Analogie zu den Reaktionen aus den Beispielen 3, 27, 5, 6, 7, 8, das Beispiel 33 hergestellt:
- 1H-NMR (CDCl3): δ = 1,28 (m, 9H); 1,43 (M, 4H); 2,42 (m, 4H); 2,82 (q, 2H); 3,32 (m, 1 H); 3,72 (s, 6H); 4,09 (m, 2H); 4,32 (m, 2H); 5,28 (m, 2H); 6,30 (m, 2H); 7,00 (m, 4H) ppm
- 1 H NMR (CDCl 3 ): δ = 1.28 (m, 9H); 1.43 (M, 4H); 2.42 (m, 4H); 2.82 (q, 2H); 3.32 (m, 1H); 3.72 (s, 6H); 4.09 (m. 2H); 4.32 (m, 2H); 5.28 (m, 2H); 6.30 (m, 2H); 7.00 (m, 4H) ppm
5,8 g (36,8 mmol) 3-Amino-hex-2-en-säureethylester und 9,7 g (36,8 mmol) der Verbindung aus Beispiel 1 werden in 100 ml Ethanol p.A. 48 Stunden unter Rückfluß gekocht. Die Mischung wird abgekühlt, das Lösungsmittel im Vakuum eingeengt und der Rückstand an einer Säule (Kieselgel 70-230 mesh, mit Petrolether/Essigester 8:2) chromatographiert.
- Ausbeute: 2,6 g (17,7 % der Theorie).
- Yield: 2.6 g (17.7% of theory).
Aus der Verbindung aus Beispiel 34 wurde, in Analogie zu den Reaktionen aus den Beispielen 3, 27, 5, 6, 7, 8 das Beispiel 35 hergestellt.
- 'H-NMR (CDCl3): δ = 0,98 (t, 3H); 1,22 (d, 6H); 1,38 (m, 4H); 1,77 (m, 2H); 2,40 (m, 4H); 2,78 (m, 2H); 3,28 (m, 1 H); 3,70 (s, 6H); 4,05 (m, 2H); 4,28 (m, 2H); 5,25 (m, 2H); 6,28 (m, 2H); 6,95 (m, 4H) ppm.
- 'H NMR (CDCl 3 ): δ = 0.98 (t, 3H); 1.22 (d, 6H); 1.38 (m, 4H); 1.77 (m. 2H); 2.40 (m, 4H); 2.78 (m, 2H); 3.28 (m, 1H); 3.70 (s, 6H); 4.05 (m. 2H); 4.28 (m. 2H); 5.25 (m. 2H); 6.28 (m. 2H); 6.95 (m, 4H) ppm.
6.3 g (36,8 mmoi) 3-Amino-hept-2-en-säureethylester und 9,7 g (36,8 mmol) der Verbindung aus Beispiel 1 werden analog Beispiel 34 umgesetzt.
- Ausbeute: 2,5 g (16,4 % der Theorie)
- Yield: 2.5 g (16.4% of theory)
Aus der Verbindung aus Beispiel 36 wurde, in Analogie zu den Reaktionen aus den Beispielen 3, 27, 5, 6, 7, 8 das Beispiel 37 hergestellt.Example 37 was prepared from the compound from Example 36 in analogy to the reactions from Examples 3, 27, 5, 6, 7, 8.
7,4 g (36,8 mmol) 3-Amino-4-phenyl-crotonsäureethylester und 9,7 g (36,8 mmol) der Verbindung aus Beispiel 1 werden analog Beispiel 34 umgesetzt.
- Ausbeute: 2,1 g (12,6 % der Theorie).
- Yield: 2.1 g (12.6% of theory).
Aus der Verbindung aus Beispiel 38 wurde, in Analogie zu den Reaktionen aus den Beispielen 3, 27, 5, 6, 7, 8, das Beispiel 39 hergestellt.
- 1H-NMR (CDCl3): 5 = 1,10-1,50 (m, 10H); 2,40 (m, 4H); 3,32 (m, 1H); 3,72 (s, 3H); 3,73 (s, 3H); 3,98 (m, 1 H); 4,08 (m, 1 H); 4,18 (m, 1 H); 4,21 (s, 2H); 4,28 (m, 1 H); 5,13 (dd, 1 H); 5,27 (dd, 1 H); 6,25 (d, 1 H); 6,33 (d, 1 H); 6,97 (m, 4H), 7,25 (m, 5H) ppm.
- 1 H NMR (CDCl 3 ): 5 = 1.10-1.50 (m, 10H); 2.40 (m, 4H); 3.32 (m, 1H); 3.72 (s, 3H); 3.73 (s, 3H); 3.98 (m, 1H); 4.08 (m, 1H); 4.18 (m, 1H); 4.21 (s, 2H); 4.28 (m, 1H); 5.13 (dd, 1H); 5.27 (dd, 1H); 6.25 (d, 1H); 6.33 (d, 1H); 6.97 (m, 4H), 7.25 (m, 5H) ppm.
39 g (0,25 mol) Cyclopropylcarbonylessigsäureethylester und 31 g (0,25 mol) 4-Fluorbenzaldehyd werden in 150 ml trockenem Isopropanol vorgelegt und mit einem Gemisch aus 1,4 ml (14 mmol) Piperidin und 0,83 ml (14,5 mmol) Essigsäure in 20 ml Isopropanol versetzt. Man rührt 48 Stunden bei Raumtemperatur. engt im Vakuum ein und destilliert den Rückstand im Hochvakuum.
- Kp 0,5 mm: 140°C
- Ausbeute: 52,3 g (79,8 % der Theorie)
- Kp 0.5 mm: 140 ° C
- Yield: 52.3 g (79.8% of theory)
39,3 g (0,15 mol) der Verbindung aus Beispiel 40 und 23,6 g (0,15 mol) 3-Amino-4-methyl-pent-2-en- säure-ethylester werden in 150 ml Ethylenglykol über Nacht unter Rückfluß gekocht. Nach Abkühlen auf Raumtemperatur wird mehrmals mit Ether extrahiert, die vereinigten Etherphasen dreimal mit 10 %iger Salzsäure, je einmal mit Wasser und gesättigter Natriumhydrogencarbonat-Lösung gewaschen, über Magnesiumsulfat getrocknet und im Vakuum eingeengt. Den Rückstand verrührt man mit Petrolether/Ether, saugt ab und trocknet im Exsikkator. Ausbeute: 22,8 g (37,9 % der Theorie)
- 'H-NMR (CDCl3): δ = 0,65 (m, 2H); 1,03 (m, 2H); 1,15 (m, 13H); 2,78 (m, 1H); 4,15 (m, 4H); 5,03 (s, 1H); 5,72 (s, 1 H); 6,90 (m, 2H); 7,22 (m, 2H) ppm.
- 'H NMR (CDCl 3 ): δ = 0.65 (m, 2H); 1.03 (m, 2H); 1.15 (m, 13H); 2.78 (m, 1H); 4.15 (m. 4H); 5.03 (s, 1H); 5.72 (s, 1H); 6.90 (m, 2H); 7.22 (m, 2H) ppm.
Aus der Verbindung aus Beispiel 41 wurde, in Analogie zu den Reaktionen aus den Beispielen 3, 27, 5, 6, 7, 8 das Beispiel 42 hergestellt.
- 1H-NMR (CDCl3): δ = 0,90 (m, 2H); 1,20 (d, 6H); 1,10-1,60 (m, 6H); 2,25 (m, 1H); 2,43 (m, 4H); 3,25 (m, 1 H); 3,73 (s, 6H); 4,08 (m, 2H); 4,30 (m, 2H); 5,22 (dd, 1 H); 5,53 (dd, 1 H); 6,30 (m, 2H); 6,98 (m, 4H) ppm.
- 1 H NMR (CDCl 3 ): δ = 0.90 (m, 2H); 1.20 (d, 6H); 1.10-1.60 (m, 6H); 2.25 (m, 1H); 2.43 (m, 4H); 3.25 (m, 1H); 3.73 (s, 6H); 4.08 (m. 2H); 4.30 (m. 2H); 5.22 (dd, 1H); 5.53 (dd, 1H); 6.30 (m, 2H); 6.98 (m, 4H) ppm.
49,9 g (0,32 mol) Cyclopropylcarbonylessigsäureethylester in 200 ml trockenem Toluol werden mit 1,1 g p-Toluolsulfonsäure versetzt und bei Raumtemperatur unter Rühren mit Ammoniak-Gas gesättigt. Nach Stehenlassen über Nacht wird 8 Stunden am Wasserabscheider unter Rückfluß gekocht, wobei kontinuierlich Ammoniak-Gas eingeleitet wird. Man läßt über Nacht abkühlen, filtriert, engt die Toluollösung im Vakuum ein und destilliert im Hochvakuum bis 650 C vom nicht umgesetzten Ausgangsmaterial ab. Die Substanz befindet sich anschließend im Rückstand.
- Ausbeute: 11,9 g (24 % der Theorie).
- Yield: 11.9 g (24% of theory).
6,2 g (40 mmol) der Verbindung aus Beispiel 43 und 10,5 g (40 mmol) der Verbindung aus Beispiel 40 Werden in 100 ml Ethylenglykol gelöst und über Nacht am Rückfluß gekocht. Nach Abkühlen auf Raumtemperatur wird die Mischung mehrmals mit Ether extrahiert, die organische Phase je einmal mit 10 %iger Salzsäure, gesättigter Natriumbicarbonat-Lösung und Wasser gewaschen, über Magnesiumsulfat getrocknet und im Vakuum eingeengt.
- Ausbeute: 10,4 g (65,1 % der Theorie)
- 'H-NMR (CDCl3): δ = 0,60 (m, 4H); 0,95 (m, 4H); 1,23 (t, 6H); 2,72 (m, 2H); 4,12 (m, 4H); 5,02 (s, 1 H); 5,40 (s, 1 H); 6,88 (m, 2H); 7,20 (m, 2H) ppm.
- Yield: 10.4 g (65.1% of theory)
- 'H NMR (CDCl 3 ): δ = 0.60 (m, 4H); 0.95 (m, 4H); 1.23 (t, 6H); 2.72 (m, 2H); 4.12 (m, 4H); 5.02 (s, 1H); 5.40 (s, 1H); 6.88 (m. 2H); 7.20 (m, 2H) ppm.
Aus der Verbindung aus Beispiel 44 wurde, in Analogie zu den Reaktionen aus den Beispielen 3, 27, 5, 6, 7, 8, das Beispiel 45 hergestellt.
- 'H-NMR (CDCl3): δ = 0,85 (m, 4H); 1,08 (m, 4H); 1,20-1,60 (m, 4H); 2,20 (m, 2H); 2,43 (m, 4H); 3,70 (s, 6H); 4,12 (m, 2H); 4,33 (m, 2H); 5,52 (dd, 2H); 6,30 (d, 2H); 7,0 (m, 4H) ppm.
- 'H NMR (CDCl 3 ): δ = 0.85 (m, 4H); 1.08 (m, 4H); 1.20-1.60 (m, 4H); 2.20 (m, 2H); 2.43 (m, 4H); 3.70 (s, 6H); 4.12 (m, 2H); 4.33 (m, 2H); 5.52 (dd, 2H); 6.30 (d, 2H); 7.0 (m, 4H) ppm.
49 g (0,31 mol) Isobutanoylessigsäureethylester und 67 g (0,31 mol) 3-Phenoxy-4-fluorbenzaldehyd werden in 300 ml Isopropanol vorgelegt und mit einem Gemisch aus 1,81 ml (18 mmol) Piperidin und 1,067 ml (18,6 mmol) Essigsäure in 30 ml Isopropanol versetzt. Man rührt über Nacht bei Raumtemperatur, engt dann im Vakuum ein und trocknet im Hochvakuum.
- Ausbeute: 110 g (wurde ohne weitere Reinigung in Beispiel 47 eingesetzt).
- Yield: 110 g (was used in Example 47 without further purification).
30 g (84,3 mmol) der Verbindung aus Beispiel 46 und 13,2 g (84,3 mmol) 3-Amino-4-methyl-pent-2-en- säure-ethylester werden in 150 ml Ethanol über Nacht am Rückfluß gekocht. Man kühlt die Mischung auf 0 C, saugt den ausgefallenen Niederschlag ab, wäscht mit Petrolether nach und trocknet im Exsikkator. Ausbeute: 18,4 g (44,2 % der Theorie)
- 1H-NMR (CDCl3): δ = 1,05-1,25 (m, 18H); 4,05-4,2 (m, 6H); 4,95 (s, 1 H); 6,03 (s, 1 H); 6,85-7,1 (m, 6H); 7,3 (m, 2H).
- 1 H NMR (CDCl 3 ): δ = 1.05-1.25 (m, 18H); 4.05-4.2 (m, 6H); 4.95 (s, 1H); 6.03 (s, 1H); 6.85-7.1 (m, 6H); 7.3 (m, 2H).
Aus der Verbindung aus Beispiel 47 wurde, in Analogie zu den Reaktionen aus den Beispielen 3, 27, 5, 6, 7, 8, das Beispiel 48 hergestellt.Example 48 was prepared from the compound from Example 47 in analogy to the reactions from Examples 3, 27, 5, 6, 7, 8.
38.4 g (0,2 mol) Benzoylessigsäureethylester und 24,8 g (0,2 mol) 4-Fluorbenzaldehyd werden in 200 mi Toluoi gelöst, mit 3 ml Piperidin und 3,5 ml Eisessig versetzt und über Nacht am Wasserabscheider unter Rückfluß erhitzt. Nach Abkühlen auf Raumtemperatur, extrahiert man mit gesättigter Natriumhydrogencarbonat-Lösung und Wasser, trocknet die organische Phase über Magnesiumsulfat und engt im Vakuum ein. Die nicht umgesetzten Ausgangsmaterialien werden im Hochvakuum abdestilliert und man erhält 55,9 g (93 % der Theorie) Rohprodukt im Destillationsrückstand.
- 'H-NMR (CDCl3): δ = 1,15 (t, 3H); 4,21 (q, 2H); 6,85-7,95 (m, 10H) ppm.
- 'H NMR (CDCl 3 ): δ = 1.15 (t, 3H); 4.21 (q, 2H); 6.85-7.95 (m, 10H) ppm.
29,8 g (0,1 mol) der Verbindung aus Beispiel 49 und 15,7 g (0,1 mol) 3-Amino-4-methyl-pent-2-en- säure-ethylester werden in 150 ml Ethylenglykol gelöst und über Nacht am Rückfluß gekocht. Nach Einengen im Vakuum wird der Rückstand in Essigester gelöst, je einmal mit 10 %iger Salzsäure, gesättigter Natriumhydrogencarbonat- Lösung und Wasser gewaschen, über Magnesiumsulfat getrocknet und im Vakuum eingeengt. Der Rückstand wird an einer Säule (Kieselgel 70-230 mesh, mit Essigester/Petrolether 1:5) chromatographiert.
- Ausbeute: 8,6 g (19,7 % der Theorie)
- 1H-NMR (CDCl3): 5 = 0,85 (t, 3H); 1,20 (m, 9H); 3,85 (q, 2H); 4,12 (q, 2H); 4,25 (m, 1 H); 5,09 (m, 1 H); 5,93 (m, 1 H); 6,93 (m, 2H); 7,25-7,50 (m, 7H) ppm.
- Yield: 8.6 g (19.7% of theory)
- 1 H NMR (CDCl 3 ): 5 = 0.85 (t, 3H); 1.20 (m, 9H); 3.85 (q, 2H); 4.12 (q, 2H); 4.25 (m, 1H); 5.09 (m, 1H); 5.93 (m, 1H); 6.93 (m, 2H); 7.25-7.50 (m, 7H) ppm.
Aus der Verbindung aus Beispiel 50 wurde, in Analogie zu den Reaktionen aus den Beispielen 3, 27, 5, 7, 8, das Beispiel 51 hergestellt.Example 51 was prepared from the compound from Example 50 in analogy to the reactions from Examples 3, 27, 5, 7, 8.
66,9 g (0,3 mol) Cyclohexylcarbonyl-essigsäure-(2-cyanethylester) und 37,2 g (0,3 mol) 4-Fluorbenzaldehyd wurden analog Beispiel 49 umgesetzt.
- Ausbeute: 56,7 g (57,4 % der Theorie)
- Yield: 56.7 g (57.4% of theory)
32,9 g (0,1 mol) der Verbindung aus Beispiel 52 und 15,7 g (0,1 mol) 3-Amino-4-methyl-pent-2-en- säure-ethylester werden in 100 ml Ethanol gelöst und über Nacht am Rückfluß gekocht. Nach Einengen im Vakuum wird der Rückstand in Essigester gelöst, je einmal mit 10 %iger Salzsäure, gesättigter Natriumhydrogencarbonat-Lösung und Wasser gewaschen, die organische Phase über Magnesiumsulfat getrocknet und im Vakuum eingeengt. Der Rückstand wird an einer Säule (Kieselgel 70-230 mesh, mit Dichiormethan) chromatographiert.
- Ausbeute: 7,8 g (17,6 % der Theorie)
- Yield: 7.8 g (17.6% of theory)
3,53 g (7,55 mmoi) der Verbindung aus Beispiel 53 werden analog Beispiel 3 umgesetzt. Ausbeute: 2,96 g (84 % der Theorie)
- 'H-NMR (CDCl3): δ = 0,98 (t, 3H); 1,33 (m, 10H); 1,82 (m, 6H); 2,35 (t, 2H); 2,69 (m, 1 H); 3,10 (m, 1H); 4,02 (q, 2H); 4,15 (t, 2H); 7,08 (m, 2H); 7,28 (m, 2H) ppm.
- 'H NMR (CDCl 3 ): δ = 0.98 (t, 3H); 1.33 (m, 10H); 1.82 (m, 6H); 2.35 (t, 2H); 2.69 (m, 1H); 3.10 (m, 1H); 4.02 (q, 2H); 4.15 (t. 2H); 7.08 (m, 2H); 7.28 (m, 2H) ppm.
2,5 g (5,35 mmol) der Verbindung aus Beispiel 54 gelöst in 50 ml trockenem Toluol werden bei -78°C unter Stickstoffatmosphäre mit 35,7 mol (53,5 mmol) einer 1,5 molaren Lösung von Diisobutylaluminiumhydrid in Toluol versetzt, 1 Stunde bei -78 °C und über Nacht bei Raumtemperatur gerührt. Die Mischung wird unter Eiskühlung mit 20 %iger Kaliumhydroxid-Lösung versetzt und mehrmals mit Toluol extrahiert. Die organische Phase wird mit Wasser gewaschen, über Magnesiumsulfat getrocknet und im Vakuum eingeengt.
- Ausbeute: 1,64 g (86 % der Theorie)
- 1H-NMR (CDCl3): δ = 1,20-1,50 (m, 4H); 1,35 (d, 6H); 1,70-1,95 (m, 6H); 3,05 (m, 1 H); 3,43 (m, 1 H); 4,35 (s, 4H); 7,05-7,25 (m, 4H) ppm.
- Yield: 1.64 g (86% of theory)
- 1 H NMR (CDCl 3 ): δ = 1.20-1.50 (m, 4H); 1.35 (d. 6H); 1.70-1.95 (m, 6H); 3.05 (m, 1H); 3.43 (m, 1H); 4.35 (s, 4H); 7.05-7.25 (m, 4H) ppm.
Aus der Verbindung aus Beispiel 55 wurde, in Analogie zu den Reaktionen aus den Beispielen 5, 6, 7, 8, das Beispiel 56 hergestellt.
- 1H-NMR (CDCI3): δ = 1,20-1,85 (m, 20H); 2,41 (m, 4H); 2,90 (m, 1H); 3,28 (m, 1H); 3,70 (s, 6H); 4,08 (m, 2H); 4,30 (m, 2H); 5,25 (dd, 2H); 6,30 (dd, 2H); 7,0 (m, 4H) ppm.
- 1 H NMR (CDCI 3 ): δ = 1.20-1.85 (m, 20H); 2.41 (m, 4H); 2.90 (m, 1H); 3.28 (m, 1H); 3.70 (s, 6H); 4.08 (m. 2H); 4.30 (m. 2H); 5.25 (dd, 2H); 6.30 (dd, 2H); 7.0 (m, 4H) ppm.
Die Verbindung wurde analog Beipiel 1 aus Furan-2-carbaldehyd hergestellt. Ausbeute: 93 % der Theorie
- Kp 0,5 mbar; 130°C
- Kp 0.5 mbar; 130 ° C
Beispiel 58 wurde aus der Verbindung aus Beispiel 57 analog der Reaktionen der Beispiele 2, 3, 5, 6, 7, 8 und 55 hergestellt.
- Farblose Kristalle, Schmelzpunkt 106°C
- 'H-NMR (CDCI3): δ = 1,25 (m, 12H); 1,4 - 1,65 (m, 4H); 2,45 (m, 4H); 2,77 (d, 2H); 3,3 (m, 2H); 3,6 (m, 2H); 3,6 (d. 2H); 3,72 (s, 6H); 4,1 (m, 2H); 4,4 (m, 2H); 5,4 (dd, 2H); 6,12 (m, 1 H); 6,4 (m, 1 H); 6,5 (d, 2H); 7,45 (m. 1 H)
- Colorless crystals, melting point 106 ° C
- 'H NMR (CDCI 3 ): δ = 1.25 (m, 12H); 1.4 - 1.65 (m, 4H); 2.45 (m, 4H); 2.77 (d. 2H); 3.3 (m. 2H); 3.6 (m. 2H); 3.6 (i.e. 2H); 3.72 (s, 6H); 4.1 (m. 2H); 4.4 (m. 2H); 5.4 (dd, 2H); 6.12 (m, 1H); 6.4 (m, 1H); 6.5 (d. 2H); 7.45 (m. 1 h)
Beispiel 59 wurde analog Beispiel 1 aus Thiopen-2-carbaldehyd hergestellt.
- Ausbeute: 86 % der Theorie
- Kp 1,5 mbar: 145°C
- Yield: 86% of theory
- Kp 1.5 mbar: 145 ° C
Beispiel 60 wurde aus der Verbindung aus Beispiel 59 analog Beispiele 2, 3, 5, 6, 7, 8 und 27 hergestellt.
- Farblose Kristalle, Schmelzpunkt 62" C
- 1H-NMR (CDCI3): 5 = 1,25 (m, 12H); 1,35 - 1,6 (m, 4H); 2,45 (m, 4H); 2,6 (s, 2H); 3,3 (m, 2H); 3,5 (d, 2H); 3,72 (s, 6H); 4,1 (m, 2H); 4,35 (m, 2H); 5,48 (dd, 2H); 6,4 (d, 2H); 6,74 (m, 1 H); 6,98 (m, 1 H); 7,28 (m, 1 H)
- Colorless crystals, melting point 62 "C
- 1 H NMR (CDCI 3 ): 5 = 1.25 (m, 12H); 1.35 - 1.6 (m, 4H); 2.45 (m, 4H); 2.6 (s, 2H); 3.3 (m. 2H); 3.5 (d. 2H); 3.72 (s, 6H); 4.1 (m. 2H); 4.35 (m. 2H); 5.48 (dd, 2H); 6.4 (d. 2H); 6.74 (m, 1H); 6.98 (m, 1H); 7.28 (m, 1h)
583 mg (1 mmol) der Verbindung aus Beispiel 16 werden in 10 ml Tetrahydrofuran gelöst. Nach Zugabe von 20 ml 0,1 N NaOH läßt man 1 Stunde bei Raumtemperatur stehen, engt im Vakuum ein und lyophilisiert dann die wässrige Lösung.
- Ausbeute: 605 mg (96,5 % der Theorie).
- Yield: 605 mg (96.5% of theory).
Die Enzymaktivitätsbestimmung wurde modifiziert nach G.C. Ness et al., Archives of Biochemistry and Biophysics 197, 493 - 499 (1979) durchgeführt. Männliche Ricoratten (Körpergewicht 300 - 400 g) wurden 11 Tage mit Altrominpulverfutter, dem 40 g Cholestyramin/kg Futter zugesetzt war, behandelt. Nach Dekapitation wurden den Tieren die Lebern entnommen und auf Eis gegeben. Die Lebern wurden - zerkleinert und im Potter-Elvejem-Homogenisator 3 mal in 3 Volumen 0,1 m Saccharose, 0,05 m KCI, 0,04 m KxHy Phosphat, 0,03 m Ethylendiamintetraessigsäure, 0,002 m Dithiothreit (SPE)-Puffer pH 7,2, homogenisiert. Anschließend wurde 15 Minuten bei 15 000* g zentrifugiert und das Sediment verworfen. Der Überstand wurde 75 Minuten bei 100 000 g sedimentiert. Das Pellet wird in 1/4 Volumen SPE-Puffer aufgenommen, nochmals homogenisiert und anschließend erneut 60 Minuten bei 100.000 g zentrifugiert. Das Pellet wird mit der 5-fachen Menge ihres Volumes SPE-Puffer aufgenommen, homogenisiert und bei -78° C eingefroren und gelagert (= Enzymlösung).The enzyme activity determination was modified according to GC Ness et al., Archives of Biochemistry and Biophysics 197, 493-499 (1979). Male Ricorats (body weight 300-400 g) were treated for 11 days with altromin powder feed, to which 40 g cholestyramine / kg feed was added. After decapitation, the livers were removed from the animals and placed on ice. The livers were crushed and in the Potter-Elvejem homogenizer 3 times in 3 volumes of 0.1 m sucrose, 0.05 m KCI, 0.04 m K x Hy phosphate, 0.03 m ethylenediaminetetraacetic acid, 0.002 m dithiothreitol (SPE) Buffer pH 7.2, homogenized. The mixture was then centrifuged at 15,000 * g for 15 minutes and the sediment was discarded. The supernatant was sedimented at 100,000 g for 75 minutes. The pellet is taken up in 1/4 volume of SPE buffer, homogenized again and then centrifuged again at 100,000 g for 60 minutes. The pellet is taken up with 5 times its volume of SPE buffer, homogenized and frozen and stored at -78 ° C (= enzyme solution).
Zur Testung wurden die Testverbindungen (oder Mevinolin als Referenzsubstanz) in Dimethylformamid unter Zugabe von 5 Vol.-% 1 n NaOH gelöst und mit 10 µl in verschiedenen Konzentrationen in den Enzymtest eingesetzt. Der Test wurde nach 20 Minuten Vorinkubation der Verbindungen mit dem Enzym bei 37°C gestartet. Der Testansatz betrug 0,380 ml und enthielt 4 µMol Glucose-6-Phosphat, 1,1 mg Rinderserumalbumin, 2,1 µMol Dithiothreit, 0,35 µMol NADP, 1 Einheit Glucose-6-Phosphatdehydrogenase, 35 µMol KxHy-Phosphat pH 7,2, 20 µl Enzympräparation und 56 nMol 3-Hydroxy-3-methyl-glutaryl Coenzym A (Glutaryl-3-14C) 100 000 dpm.For testing, the test compounds (or mevinolin as reference substance) were in dimethylformamide dissolved with the addition of 5 vol.% 1N NaOH and used with 10 μl in different concentrations in the enzyme test. The test was started after 20 minutes of pre-incubation of the compounds with the enzyme at 37 ° C. The test batch was 0.380 ml and contained 4 μmol glucose-6-phosphate, 1.1 mg bovine serum albumin, 2.1 μmol dithiothreitol, 0.35 μmol NADP, 1 unit glucose-6-phosphate dehydrogenase, 35 μmol K x hy-phosphate pH 7 , 2, 20 ul enzyme preparation and 56 nmol of 3-hydroxy-3-methyl-glutaryl coenzyme A (glutaryl-3- 14 C) 100 000 dpm.
Man inkubierte 60 Minute bei 37° C und stoppte die Reaktion durch Zusatz von 300 ul 0,24 m HCI ab. Nach einer Nachinkubation von 60 Minuten bei 370 C wurde der Ansatz zentrifugiert und 600 µl des Überstandes auf eine 0,7 x 4 cm mit Biorex @ 5-Chlorid 100-200 mesh (Anionenaustauscher) gefüllte Säule aufgetragen. Es wurde mit 2 ml dest. Wasser nachgewaschen und Durchlauf plus Waschwasser mit 3 ml Aquasol versetzt und im LKB-Scintillationszähler gezählt. ICso-Werte wurden durch Auftrag der prozentualen Hemmung gegen die Konzentration der Verbindung im Test durch Intrapolation bestimmt. Zur Bestimmung der relativen inhibitorischen Potenz wurde der ICso-Wert der Referenzsubstanz Mevinolin als 100 gesetzt und mit dem simultan bestimmten ICso-Wert der Testverbindung verglichen.The mixture was incubated at 37 ° C. for 60 minutes and the reaction was stopped by adding 300 μl of 0.24 m HCl. After a post-incubation of 60 minutes at 37 0 C, the mixture was centrifuged and 600 .mu.l of the supernatant on a 0.7 x 4 cm with Biorex @ 5-chloride 100-200 mesh (anion exchange) column filled applied. It was distilled with 2 ml. Wash the water and add 3 ml Aquasol to the flow plus wash water and count in the LKB scintillation counter. IC 50 values were determined by plotting the percentage inhibition against the concentration of the compound in the test by intrapolation. To determine the relative inhibitory potency, the IC 50 value of the reference substance mevinolin was set to 100 and compared with the simultaneously determined IC 50 value of the test compound.
Die subchronische Wirkung der disubstituierten Pyridine auf die Blutcholesterinwerte von Hunden wurde in mehrwöchigen Fütterungsexperimenten geprüft. Dazu wurde die zu untersuchende Substanz über einen mehrwöchigen Zeitraum einmal täglich in einer Kapsel gesunden Beagle Hunden zusammen mit dem Futter p.o. gegeben. Dem Futter war außerdem während der gesamten Versuchsperiode, d.h. vor, während und nach der Applikationsperiode der zu untersuchenden Substanz Colestyramin (4 g/100 g Futter) als Gallensäuresequestrant beigemischt. Zweimal wöchentlich wurde den Hunden venöses Blut abgenommen und das Serumcholesterin enzymatisch bestimmt. Die Serumcholesterinwerte während der Applikationsperiode wurden mit den Serumcholesterinwerten vor der Applikationsperiode (Kontrollen) verglichen.The subchronic effect of disubstituted pyridines on blood cholesterol levels in dogs was tested in feeding experiments lasting several weeks. For this purpose, the substance to be investigated was administered once daily in a capsule to healthy beagle dogs together with the food p.o. given. The feed was also present during the entire trial period, i.e. Before, during and after the application period of the substance to be investigated, colestyramine (4 g / 100 g feed) was added as a bile acid sequestrant. Venous blood was drawn from the dogs twice a week and the serum cholesterol was determined enzymatically. The serum cholesterol values during the application period were compared with the serum cholesterol values before the application period (controls).
So ergab sich z.B. für das Na-Salz von Beipiel 8 (2,6-Diisopropyl-4-(4-fluorphenyl)-3,5-di-(natrium- erythro-(E)-3,5-dihydroxy-hept-6-enoat-7-yl)-pyridin) nach 2-wöchiger Applikation von täglich 8 mg/kg p.o. eine Senkung des Serumcholesterins um 22,4 %.For example, for the Na salt of example 8 (2,6-diisopropyl-4- (4-fluorophenyl) -3,5-di- (sodium erythro- (E) -3,5-dihydroxy-hept-6-enoate- 7-yl) -pyridine) after 2 weeks of application of 8 mg / kg po a 22.4% decrease in serum cholesterol.
Claims (14)
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE3801440A DE3801440A1 (en) | 1988-01-20 | 1988-01-20 | Disubstituted pyridines |
| DE3801440 | 1988-01-20 | ||
| IT8821587A IT8821587A0 (en) | 1988-07-29 | 1988-07-29 | DISSUBSTITUTED PYRIDINES. |
| IT2158788 | 1988-07-29 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| EP0325129A2 true EP0325129A2 (en) | 1989-07-26 |
| EP0325129A3 EP0325129A3 (en) | 1990-12-19 |
| EP0325129B1 EP0325129B1 (en) | 1994-09-07 |
Family
ID=25864088
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP89100249A Expired - Lifetime EP0325129B1 (en) | 1988-01-20 | 1989-01-09 | Disubstituted pyridines |
Country Status (16)
| Country | Link |
|---|---|
| US (1) | US4968689A (en) |
| EP (1) | EP0325129B1 (en) |
| JP (1) | JP2712107B2 (en) |
| KR (1) | KR890011847A (en) |
| CN (1) | CN1034716A (en) |
| AT (1) | ATE111081T1 (en) |
| AU (1) | AU614810B2 (en) |
| DE (1) | DE58908290D1 (en) |
| DK (1) | DK23289A (en) |
| ES (1) | ES2058343T3 (en) |
| FI (1) | FI92195C (en) |
| HU (1) | HU208691B (en) |
| IL (1) | IL88971A (en) |
| NO (1) | NO890046L (en) |
| NZ (1) | NZ227636A (en) |
| PT (1) | PT89478B (en) |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0411420A2 (en) * | 1989-08-03 | 1991-02-06 | Bayer Ag | Imino substituted pyridine |
| EP0416383A2 (en) * | 1989-09-06 | 1991-03-13 | Bayer Ag | Substituted aminopyridines |
| US5686433A (en) * | 1988-08-29 | 1997-11-11 | E.R. Squibb & Sons, Inc. | Quinoline and pyridine anchors for HMG-CoA reductase inhibitors |
| WO1998004528A2 (en) * | 1996-07-31 | 1998-02-05 | Bayer Corporation | Substituted pyridines and biphenyls as anti-hypercholesterinemic, anti-hyperlipoproteinemic and anti-hyperglycemic agents |
| WO2003008383A1 (en) * | 2001-07-18 | 2003-01-30 | Bayer Aktiengesellschaft | Production of enantiomer pure 3r, 5s- (+) natrium erythro- (e) 7-'4-(4-fluorophenyl)-2, 6-diisopropyl-5-methoxymethyl-pyrid-3-yl!-3, 5-dihydroxy-hept-6-e-noate |
| US6620821B2 (en) | 2000-06-15 | 2003-09-16 | Bristol-Myers Squibb Company | HMG-CoA reductase inhibitors and method |
| US6627636B2 (en) | 2000-06-15 | 2003-09-30 | Bristol-Myers Squibb Company | HMG-CoA reductase inhibitors and method |
| US6812345B2 (en) | 2000-06-15 | 2004-11-02 | Bristol-Myers Squibb Company | HMG-CoA reductase inhibitors and method |
| US7659281B2 (en) | 2006-04-25 | 2010-02-09 | Bristol-Myers Squibb Company | HMG-CoA reductase inhibitors |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3505382A1 (en) * | 1985-02-16 | 1986-08-21 | Accord-Landmaschinen Heinrich Weiste & Co Gmbh, 4770 Soest | DOUBLE DISC SPREADER |
| NO177005C (en) * | 1988-01-20 | 1995-07-05 | Bayer Ag | Analogous process for the preparation of substituted pyridines, as well as intermediates for use in the preparation |
| FI94339C (en) | 1989-07-21 | 1995-08-25 | Warner Lambert Co | Process for the preparation of pharmaceutically acceptable [R- (R *, R *)] - 2- (4-fluorophenyl) -, - dihydroxy-5- (1-methylethyl) -3-phenyl-4 - [(phenylamino) carbonyl] -1H- for the preparation of pyrrole-1-heptanoic acid and its pharmaceutically acceptable salts |
| US5183897A (en) * | 1989-08-03 | 1993-02-02 | Bayer Aktiengesellschaft | Certain intermediate imino-substituted pyridines |
| ES2193148T3 (en) * | 1993-12-10 | 2003-11-01 | Bayer Ag | 1,4-DIHYDROPIRIDINES REPLACED WITH PHENYLLUS WITH BRAIN ACTIVITY. |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4681893A (en) * | 1986-05-30 | 1987-07-21 | Warner-Lambert Company | Trans-6-[2-(3- or 4-carboxamido-substituted pyrrol-1-yl)alkyl]-4-hydroxypyran-2-one inhibitors of cholesterol synthesis |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0098690B1 (en) * | 1982-06-14 | 1987-09-09 | Takeda Chemical Industries, Ltd. | Vinyl carboxylic acid derivatives, their production and use |
| NO177005C (en) * | 1988-01-20 | 1995-07-05 | Bayer Ag | Analogous process for the preparation of substituted pyridines, as well as intermediates for use in the preparation |
-
1989
- 1989-01-05 NO NO89890046A patent/NO890046L/en unknown
- 1989-01-09 AT AT89100249T patent/ATE111081T1/en active
- 1989-01-09 ES ES89100249T patent/ES2058343T3/en not_active Expired - Lifetime
- 1989-01-09 EP EP89100249A patent/EP0325129B1/en not_active Expired - Lifetime
- 1989-01-09 DE DE58908290T patent/DE58908290D1/en not_active Expired - Fee Related
- 1989-01-17 IL IL8988971A patent/IL88971A/en unknown
- 1989-01-17 NZ NZ227636A patent/NZ227636A/en unknown
- 1989-01-17 US US07/298,453 patent/US4968689A/en not_active Expired - Fee Related
- 1989-01-18 FI FI890257A patent/FI92195C/en not_active IP Right Cessation
- 1989-01-18 PT PT89478A patent/PT89478B/en not_active IP Right Cessation
- 1989-01-19 DK DK023289A patent/DK23289A/en not_active Application Discontinuation
- 1989-01-19 JP JP1008769A patent/JP2712107B2/en not_active Expired - Lifetime
- 1989-01-19 KR KR1019890000549A patent/KR890011847A/en not_active Application Discontinuation
- 1989-01-19 AU AU28613/89A patent/AU614810B2/en not_active Ceased
- 1989-01-19 HU HU89213A patent/HU208691B/en not_active IP Right Cessation
- 1989-01-20 CN CN89100406A patent/CN1034716A/en active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4681893A (en) * | 1986-05-30 | 1987-07-21 | Warner-Lambert Company | Trans-6-[2-(3- or 4-carboxamido-substituted pyrrol-1-yl)alkyl]-4-hydroxypyran-2-one inhibitors of cholesterol synthesis |
Cited By (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5686433A (en) * | 1988-08-29 | 1997-11-11 | E.R. Squibb & Sons, Inc. | Quinoline and pyridine anchors for HMG-CoA reductase inhibitors |
| US5691322A (en) * | 1988-08-29 | 1997-11-25 | E.R. Squibb & Sons, Inc. | Quinoline and pyridine anchors for HMG-CoA reductase inhibitors |
| EP0411420A3 (en) * | 1989-08-03 | 1991-11-06 | Bayer Ag | Imino substituted pyridine |
| EP0411420A2 (en) * | 1989-08-03 | 1991-02-06 | Bayer Ag | Imino substituted pyridine |
| EP0416383A3 (en) * | 1989-09-06 | 1991-11-06 | Bayer Ag | Substituted aminopyridines |
| US5145857A (en) * | 1989-09-06 | 1992-09-08 | Bayer Aktiengesellschaft | Hmg-coa reductase-inhibiting substituted amino-pyridines |
| EP0416383A2 (en) * | 1989-09-06 | 1991-03-13 | Bayer Ag | Substituted aminopyridines |
| WO1998004528A2 (en) * | 1996-07-31 | 1998-02-05 | Bayer Corporation | Substituted pyridines and biphenyls as anti-hypercholesterinemic, anti-hyperlipoproteinemic and anti-hyperglycemic agents |
| WO1998004528A3 (en) * | 1996-07-31 | 1999-11-11 | Bayer Ag | Substituted pyridines and biphenyls as anti-hypercholesterinemic, anti-hyperlipoproteinemic and anti-hyperglycemic agents |
| US6218431B1 (en) | 1996-07-31 | 2001-04-17 | Bayer Corporation | Substituted biphenyls |
| US6620821B2 (en) | 2000-06-15 | 2003-09-16 | Bristol-Myers Squibb Company | HMG-CoA reductase inhibitors and method |
| US6627636B2 (en) | 2000-06-15 | 2003-09-30 | Bristol-Myers Squibb Company | HMG-CoA reductase inhibitors and method |
| US6812345B2 (en) | 2000-06-15 | 2004-11-02 | Bristol-Myers Squibb Company | HMG-CoA reductase inhibitors and method |
| WO2003008383A1 (en) * | 2001-07-18 | 2003-01-30 | Bayer Aktiengesellschaft | Production of enantiomer pure 3r, 5s- (+) natrium erythro- (e) 7-'4-(4-fluorophenyl)-2, 6-diisopropyl-5-methoxymethyl-pyrid-3-yl!-3, 5-dihydroxy-hept-6-e-noate |
| US7659281B2 (en) | 2006-04-25 | 2010-02-09 | Bristol-Myers Squibb Company | HMG-CoA reductase inhibitors |
Also Published As
| Publication number | Publication date |
|---|---|
| FI92195C (en) | 1994-10-10 |
| HUT50775A (en) | 1990-03-28 |
| PT89478A (en) | 1989-10-04 |
| IL88971A (en) | 1993-07-08 |
| ATE111081T1 (en) | 1994-09-15 |
| AU2861389A (en) | 1989-07-20 |
| NO890046D0 (en) | 1989-01-05 |
| AU614810B2 (en) | 1991-09-12 |
| KR890011847A (en) | 1989-08-22 |
| US4968689A (en) | 1990-11-06 |
| PT89478B (en) | 1993-12-31 |
| IL88971A0 (en) | 1989-08-15 |
| CN1034716A (en) | 1989-08-16 |
| NO890046L (en) | 1989-07-21 |
| FI92195B (en) | 1994-06-30 |
| JPH021478A (en) | 1990-01-05 |
| EP0325129A3 (en) | 1990-12-19 |
| HU208691B (en) | 1993-12-28 |
| DK23289A (en) | 1989-07-21 |
| ES2058343T3 (en) | 1994-11-01 |
| EP0325129B1 (en) | 1994-09-07 |
| FI890257A (en) | 1989-07-21 |
| DE58908290D1 (en) | 1994-10-13 |
| NZ227636A (en) | 1990-09-26 |
| DK23289D0 (en) | 1989-01-19 |
| JP2712107B2 (en) | 1998-02-10 |
| FI890257A0 (en) | 1989-01-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0373423B1 (en) | Substituted 2-pyridones and pyride-2-thiones, process for their preparation and their use in medicine | |
| EP0325130B1 (en) | Substituted pyridines | |
| EP1080086B1 (en) | Dihydropyrimidines | |
| EP0465970A1 (en) | Substituted pyrrolo-pyridines | |
| EP0325129B1 (en) | Disubstituted pyridines | |
| WO2000058302A1 (en) | Dihydropyrimidines and their use in the treatment of hepatitis b | |
| EP0287890A1 (en) | Substituted pyrroles | |
| EP0391185B1 (en) | Substituted 1,8-naphthyridines | |
| EP0317845A2 (en) | Substituted hydroxyl amines | |
| EP0330057A2 (en) | Substituted pyrimidines | |
| EP0378850B1 (en) | Substituted pyrido(2,3-d) pyrimidines | |
| EP0300278A2 (en) | Process for the preparation of 2-substituted pyrroles | |
| EP0339342A1 (en) | N-substituted N-amino pyrroles | |
| EP0416383A2 (en) | Substituted aminopyridines | |
| DE3925636A1 (en) | IMINO-SUBSTITUTED PYRIDINE | |
| EP0334014A2 (en) | Substitued imidazolinones and imidazolethiones | |
| EP0334147A1 (en) | Disubstituted pyrroles | |
| DE3905908A1 (en) | Substituted quinolines, process for their preparation, and their use in medicaments | |
| DE3909378A1 (en) | SUBSTITUTED BIPHENYLE | |
| DE3801440A1 (en) | Disubstituted pyridines | |
| EP0818447B1 (en) | 6-(Hydroxymethyl-ethyl)pyridines as HMG-CoA-reductase inhibitors | |
| DE3801406A1 (en) | Substituted pyridines | |
| EP0352575A2 (en) | Substituted annealed pyrroles | |
| DE3805884A1 (en) | Substituted imidazolinones and imidazolinethiones | |
| DE3813776A1 (en) | N-substituted N-aminopyrroles |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| 17P | Request for examination filed |
Effective date: 19890109 |
|
| AK | Designated contracting states |
Kind code of ref document: A2 Designated state(s): AT BE CH DE ES FR GB GR IT LI NL SE |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Kind code of ref document: A3 Designated state(s): AT BE CH DE ES FR GB GR IT LI NL SE |
|
| 17Q | First examination report despatched |
Effective date: 19921117 |
|
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Kind code of ref document: B1 Designated state(s): AT BE CH DE ES FR GB GR IT LI NL SE |
|
| REF | Corresponds to: |
Ref document number: 111081 Country of ref document: AT Date of ref document: 19940915 Kind code of ref document: T |
|
| REF | Corresponds to: |
Ref document number: 58908290 Country of ref document: DE Date of ref document: 19941013 |
|
| GBT | Gb: translation of ep patent filed (gb section 77(6)(a)/1977) |
Effective date: 19940920 |
|
| ITF | It: translation for a ep patent filed |
Owner name: ING. C. GREGORJ S.P.A. |
|
| REG | Reference to a national code |
Ref country code: ES Ref legal event code: FG2A Ref document number: 2058343 Country of ref document: ES Kind code of ref document: T3 |
|
| ET | Fr: translation filed | ||
| EAL | Se: european patent in force in sweden |
Ref document number: 89100249.5 |
|
| REG | Reference to a national code |
Ref country code: GR Ref legal event code: FG4A Free format text: 3014164 |
|
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |
|
| 26N | No opposition filed | ||
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: SE Payment date: 19951218 Year of fee payment: 8 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: GR Payment date: 19951221 Year of fee payment: 8 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: BE Payment date: 19960118 Year of fee payment: 8 Ref country code: AT Payment date: 19960118 Year of fee payment: 8 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: NL Payment date: 19960131 Year of fee payment: 8 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: AT Effective date: 19970109 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: SE Effective date: 19970110 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: BE Effective date: 19970131 |
|
| BERE | Be: lapsed |
Owner name: BAYER A.G. Effective date: 19970131 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GR Free format text: THE PATENT HAS BEEN ANNULLED BY A DECISION OF A NATIONAL AUTHORITY Effective date: 19970731 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NL Effective date: 19970801 |
|
| REG | Reference to a national code |
Ref country code: GR Ref legal event code: MM2A Free format text: 3014164 |
|
| NLV4 | Nl: lapsed or anulled due to non-payment of the annual fee |
Effective date: 19970801 |
|
| EUG | Se: european patent has lapsed |
Ref document number: 89100249.5 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 19981211 Year of fee payment: 11 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: GB Payment date: 19990114 Year of fee payment: 11 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: FR Payment date: 19990119 Year of fee payment: 11 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: CH Payment date: 19990121 Year of fee payment: 11 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: ES Payment date: 19990122 Year of fee payment: 11 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20000109 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: ES Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20000110 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: LI Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20000131 Ref country code: CH Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20000131 |
|
| GBPC | Gb: european patent ceased through non-payment of renewal fee |
Effective date: 20000109 |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: PL |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20000929 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20001101 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |
|
| REG | Reference to a national code |
Ref country code: ES Ref legal event code: FD2A Effective date: 20011010 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: IT Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES;WARNING: LAPSES OF ITALIAN PATENTS WITH EFFECTIVE DATE BEFORE 2007 MAY HAVE OCCURRED AT ANY TIME BEFORE 2007. THE CORRECT EFFECTIVE DATE MAY BE DIFFERENT FROM THE ONE RECORDED. Effective date: 20050109 |