CN115963149A - 用于检测微生物的电抗和电容型传感平台 - Google Patents
用于检测微生物的电抗和电容型传感平台 Download PDFInfo
- Publication number
- CN115963149A CN115963149A CN202211697198.4A CN202211697198A CN115963149A CN 115963149 A CN115963149 A CN 115963149A CN 202211697198 A CN202211697198 A CN 202211697198A CN 115963149 A CN115963149 A CN 115963149A
- Authority
- CN
- China
- Prior art keywords
- frequency
- sample
- consumable
- detection
- electrodes
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/02—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M41/00—Means for regulation, monitoring, measurement or control, e.g. flow regulation
- C12M41/30—Means for regulation, monitoring, measurement or control, e.g. flow regulation of concentration
- C12M41/36—Means for regulation, monitoring, measurement or control, e.g. flow regulation of concentration of biomass, e.g. colony counters or by turbidity measurements
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
- C12Q1/04—Determining presence or kind of microorganism; Use of selective media for testing antibiotics or bacteriocides; Compositions containing a chemical indicator therefor
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/02—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance
- G01N27/04—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance by investigating resistance
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
- G01N33/48785—Electrical and electronic details of measuring devices for physical analysis of liquid biological material not specific to a particular test method, e.g. user interface or power supply
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/02—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating impedance
- G01N27/026—Dielectric impedance spectroscopy
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
- G01N33/49—Blood
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Biochemistry (AREA)
- Analytical Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Genetics & Genomics (AREA)
- Pathology (AREA)
- General Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- Electrochemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Sustainable Development (AREA)
- Medicinal Chemistry (AREA)
- Food Science & Technology (AREA)
- Human Computer Interaction (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Toxicology (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Investigating Or Analyzing Materials By The Use Of Electric Means (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
本发明的名称是用于检测微生物的电抗和电容型传感平台。一种对微生物生长具有增加的灵敏度的系统和方法。所述系统包括信号处理电路,该信号处理电路通过两个或更多个电极连接到耗材或容器,所述电极完全刺入所述容器并与液体内容物接触。所述电路被配置以检测样品的总阻抗的组分,尤其是“异相”或虚拟电抗组分,该组分以频率依赖的方式对微生物生长具有灵敏响应。基于监测样品这些述参数的变化,所述系统检测液体基质中带电分子的组成以及微生物的数量二者的变化。这使得检出时间(TTD)减少5‑70%。所述系统和方法检测多种容器形状、体积和基质(或介质)形式中的微生物。所述电极完全浸入液体样品的连续主体之中。电极之间的距离可以被调整或调节以满足容器的需要。电压输入也能够被调整以允许容器内的内容物的恰当检测。
Description
本申请是申请日为2015年10月14日、申请号为2015800551755、题为“用于检测微生物的电抗和电容型传感平台”的专利申请的分案申请。
相关申请的交叉引用
本申请要求2014年10月14日申请的美国临时申请号62/063,602的权利,该申请的公开内容在此以引用方式被并入本文。
背景技术
本发明涉及临床样品的微生物检测领域。本发明尤其涉及实现对于生物样品中细菌存在与否的更快速的检测。
检测复制微生物(细菌、真菌、病毒)的能力在很多临床微生物应用中是一项基本的要求。在这方面,已经开发了很多用于检测微生物生长的直接和/或间接方法。
例如,间接检测方法可以评估副产物、分子、复合物或化学反应物对微生物生长/复制的影响。即,微生物的生长/复制是否导致副产物、分子、复合物或化学反应物共同和累积式的增加、减少或显著的变化。例如,可以通过荧光变化或通过弹性传感器的比色变化观察生长中的微生物群的代谢需求的变化。虽然这类检测的机制已经众所周知,但当微生物浓度达到每瓶约109集落形成单位(CFU)时即超过检测阈值。这导致许多临床相关的血液病原体的检出时间(TTD)通常在8到24小时的范围内。在一些情况下,某些微生物的检测可能需要超过72小时。
此外,用以检测溶液中活体微生物的电子检测系统已经被开发。通常,这类平台利用阻抗测量作为微生物生长的间接指示符。2013年2月14日提交的并且名称为“基于阻抗的细菌检测系统(Impendence-Based Bacterial Detection System)”的WO2013/123189中描述了一种这样的系统,其一般地与本申请相关并且在此通过引用被并入。
当微生物进行生长时,通过排出或摄入带电荷的产物(如离子、磷酸盐、硫酸盐、硝酸盐)或者产生带电荷的代谢中间产物(如乳酸)使样品中的总离子组成发生改变。微生物的生长影响介质的总电导率(或电阻率)。电导(或电阻)的这种变化通过溶液中随时间变化的总电阻抗变化来证明。通过向溶液中浸渍多个电极并测量电压(如AC或DC)和/或电流响应来测量阻抗。这些系统通常使用数据模型以使得原始阻抗数据适应理论框架从而提取与微生物生长相关的信息。
例如,一些众所周知的系统使用充满特化液体培养基(specialized broth)的10ml反应室。工业微生物样品被接种在该反应室中并孵育高达24小时。向管内供应固定频率(10kHz)的输入波形并监测阻抗。由于响应于微生物随着时间生长介质的离子组成变化,介质电导的小变化开始累积。当电导率已增加到特定的阈值之上时,微生物生长的样品测试阳性的信号被返回。但是,这类系统有一些主要的技术限制,使得它们的应用的范围主要被限制在工业微生物应用。
在这方面,电学检测系统由于其依赖微生物生长形成和积累副产物而造成生长介质的电导或电阻变化而产生技术限制。随之而来的是,对于高离子强度的介质,只有在微生物浓度达到非常高的水平时,由微生物复制产生的任何信号才能被有效标记(mask)。此外,监测高度复杂的介质(如血液)中微生物生长和检测的许多应用不能使用标准的基于阻抗的检测技术。
利用阻抗检测系统针对具有这类问题的已提出的一种解决方案是使用总阻抗的子集以增加对于测量——其指示微生物生长——的敏感性。Sengupta等人在“A micro-scale multi-frequency reactance measurement technique to detect bacterialgrowth at low bio-particle concentrations(在低生物粒子浓度下检测细菌生长的微尺度多频电抗测量技术)(Lab Chip,第6卷,第682-692页,2006)”(以下称为“Sengupta”)中使用100μL容积的微流体腔作为监测响应的腔,该响应能够指示细菌的存在。Sengupta等人指出通过提供长的(厘米级别)且非常细(小于250微米)的含有样品的管道状腔,并且在其两端处定位非常小的电极能够改善与简单的电介质电导率测量有关的感测响应。通过使用非常高的频率(从100KHz到100MHz),液体样品的电容贡献被测量。根据Sengupta,液体样品的电容对于放置在腔中的样品里的细菌的存在和/或生长引起的变化是敏感的。
然而,Sengupta指出利用针对使用电介质电导率测量来测试样品中细菌存在的微流体环境的方法,最显著的挑战是温度的波动。此外,Sengupta对每个分析时间点获取并测量了新的样品。即,Sengupta在继续测量前需要填充新的微流体腔(或者用新鲜的样品替换微流体腔内的液体样品)。由于每一份在先的样品部分被丢弃,所以每小时需要消耗约100-200μL样品,因此这一方法被认为是破坏性的。随着时间消耗掉的样品的体积将是一个非常严峻的挑战,尤其是对于生长缓慢或代谢缓慢的微生物的样品。此外,随时间获取样品必须关注固有的生物危害废物处理及灭菌。
Sengupta中所描述的技术另一缺点在于需要在微升的体积级别进行实验。这限制了这一技术在没有合适的准备或获取子样本步骤的情况下感测临床上相关的样品的使用。此外,这一技术利用来自宽频率范围(几百至几千kHz)的原始光谱数据来通过计算拟合溶液的“电容”的电路模型。因此,围绕该数据的处理存在数学上的复杂性,这可能导致每个耗材的后处理时间长达一分钟。
最后,Sengupta并没有克服所述的阻抗技术对于高离子介质(如血液)固有的不相容性。相反,Sengputa通过减少检测腔的总体积限制了总离子数量从而规避了该问题。因此,即使体积上仅有轻微的超量也会导致检测敏感性的大幅损失。
因此,需要对使用电介质测量以检测液体中微生物存在与否的方法进行改进。
发明内容
本申请描述基于阻抗的方法和系统,其使用总阻抗的子组分,即虚拟(电抗)组分,以测定介质中的总离子组成。在这方面,电抗子组分对于由于微生物生长(间接检测)造成的介质的离子组分变化以及微生物的带电的细胞量(直接检测)二者都具有极高的灵敏度。这为处理微生物的宽且多样的光谱提供了广阔的检测方法。
当前申请还描述调节方法,以允许跨度从微升级别到毫升级别范围的液体体积内的电抗检测。在这方面,在一个实施例中,系统的频率敏感度可以通过调节平行于锁定放大器检测器的电容输入级的电阻的物理值而从1kHz改变到几百kHz。这导致了针对离子组成(操作频率在1-20kHz之间)和微生物生物量(操作频率大大高于20kHz)的变化的增加的灵敏度。
根据可替代的实施方式,当前申请描述了通过使用桥式电阻器-电容器调节电路调节目标样品的频率灵敏度的方法。通过调节桥式电阻器-电容器调节电路的值,在高频光谱(远大于20kHz)下检测变得对于离子组分变化和带电微生物量变化二者均很敏感。因此,桥式电阻器-电容器调节电路可以提供更快的检出时间(TTD)。
更进一步地,调节消耗性试验内的频率响应允许在相对大的样品体积(如大于10mL)中检测微生物生长。这消除了现有技术对于恒定地子样品的需求。由于不再需要每一次采样后进行复杂的数学计算,因此通过利用处理原始电抗数据实现附加的益处。将降低的计算复杂性结合至更窄的频率范围的利用允许更快的扫描时间(由秒到分钟级别变为毫秒到秒级)。
当前申请还描述对于微生物生长具有增加的灵敏度的系统。所述系统包括信号处理电路,该信号处理电路通过完全穿过测试室并与液体内容物接触的两个或更多电极连接到测试室(即消耗性的)。所述电路被配置用来检测总阻抗的一组分,尤其是“异相”或虚拟电抗组分,所述组分以频率依赖方式对微生物生长具有敏感响应。阻抗中的电抗组分对本领域技术人员而言是公知的,并且在本文中不详细描述。在这方面,该系统可以基于监测样品中该参数的变化来检测液体基质中带电分子的组成以及微生物的数量二者的变化。这使检出时间(TTD)减少5%-70%。
由本文所述的系统和方法实现的另一优势是能够在多种消耗性形状、体积或者基质(或介质)形式下检测微生物。在这方面,电极应应当完全浸渍在连续的液体样品主体中。电极间的距离可以被调整或者调节以满足耗材的需要。更进一步地,输入电压也能被调节以便允许在耗材内对内容物进行适宜的检测。
在这方面,当前系统能够感测由于微生物细胞壁的高度带电的特性而将另外被认为是“脏(dirty)”的样品中微生物的存在与否以及其在液体基质的离子组分中的各自变化。即,当前系统可以监测有血液污染的抗微生物敏感性测试情况中微生物的生长以及其他将以其它方式破坏光学检测策略的样品的组分。
附图说明
图1图示说明装置的示例,其用于测量液体样品的电介质电容以确定其中是否存在微生物;
图2图示说明装置的另一种实施方式,其用于测量液体样品的电介质电容以确定其中是否存在微生物,由此信号发生器的测量频率被自动调节并保持在零交点频率。
图3图示说明装置的示例,其用于测量液体样品的电抗以确定其中是否存在微生物;
图4A和图4B图示说明用以测量液体样品的电抗的装置的框图;
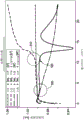
图5图示说明线形图,该线形图示出在不同频率下检测大肠杆菌(E.coli)的时间;
图6图示说明由本文描述的实施例实现的缩短的检出时间;
图7展示实验结果,该结果表明使用更高的频率可以改善检出时间;
图8图示说明线形图,该线形图示出在高频率下洛菲不动杆菌(A.lwoffii)的检出时间;
图9图示说明说明线形图,该线形图示出在高频率下藤黄微球菌(M.luteus)的检出时间。
具体实施方式
根据本文描述的示例,使用阻抗子组分测量确定微生物生长存在与否。电极的配置方式和频率可以按照本文描述进行配置,以确保即使是测试环境中离子电荷的微小变化也是可检测的,以确定微生物生长的存在与否。
阻抗是当施加电压时电路对于电流呈现的电对抗作用的度量。当在交流(AC,f>0)电路中操作时,阻抗由电阻和电抗组成。相反,在直流(DC,f=0)电路中,阻抗仅有电阻组成。因此,阻抗可以以下式表示:
Z=Zo+j*Zr(f)
其中Z=阻抗,Zo=电阻,j=√-1,Zr=电抗,且f=频率。因此,阻抗是包含两个子组分——电阻和电抗——的物质的电学特征。
电阻是电流通过电导体(如金属线、盐水溶液等)时的对抗作用。电阻是标量值并且与频率不相关。因此,电阻与给定样品中所包含的静态(非演化)带电物质(即离子、质子、氨基酸、肽、小分子等)的总数量呈现逆相关的关系。带电物质的增加导致更低的电阻,而相反地,带电物质的减少导致更高的电阻。在微生物复制(通常称作微生物生长)期间,带电颗粒的总数量将以微生物依赖的方式不断变化。例如,随着新细胞分裂,离子从介质中获得并且被参入子细胞中。因此,细胞分裂导致带电物质的数量减少。与此同时,微生物在介质中对营养物质进行代谢并且产生带电产物,该带电产物导致带电物质的数量的增加。
另一方面,电抗是电路元件对于电流或电压变化产生的对抗作用,这是由于元件的电感或电容。电抗与电阻类似,不同之处在于电抗对于操作频率是敏感的。因此,电抗与给定样品内所包含的电容性组分的总数量呈现逆相关的关系。在这方面,生物样品内的电容通过两种方式显现。第一,带电物质(通常是分子,非微生物细胞等)由于感测电压(或电势)的施加而聚集在电极界面的部位处。这是由于当电压(如,正或负)被施加到电极时具有相反极性的带电分子被吸引到电极以试图中和表面电极上的电荷。具有相反电荷的另一层分子在那些分子上产生“涂层效应(coating effect)”,导致在电极界面处几乎没有净电荷存在。这种涂层效应导致具有中和的电荷的电双层或双层电容器(如电介质双层电容器),就像绝缘体。因此,这绝缘体状的涂层导致电容效应(即绝缘体侧壁与导电介质和电极金属相连),这被称作界面电容。
当该系统在低频(小于15kHz)下运行时界面电容(Ci)最大。对于检测微生物生长,当由于微生物细胞量以及相关代谢物增加导致介质中离子组分变化时,界面电容随之变化。因此,界面电容是微生物生长的间接指示符。
对电抗产生影响的另一个生物学因素是细胞的电容。在这方面,人类和非人类细胞具有带电的外层细胞膜,随之是绝缘的膜核,且最后是高离子的内部细胞组分(如离子)。这与之前讨论的界面电容相似,并且被称为细胞电容或膜电容(Cm)。
与阻抗相反,电导率是与细菌代谢副产物(如气体,如CO2)存在与否相关的测量。在这方面,之前讨论的电容组分(以及那些随时间的变化的组分)更加直接地反应样品容器中微生物(如细菌)的存在与否。
本文所述的系统和方法检测通过使用外部频率调节电路而改变的电抗显示的界面电容(Ci)和/或细胞电容(Cm)。这导致了对于微生物生物量的增加以及由微生物相关的代谢活动而诱发的样品环境的变化二者均具有高度的检测敏感性。该外部频率调节电路与从微升到超过毫升的体积范围的多种介质体积是相容的。更进一步地,外部频率调节电路允许持续监测而不需要对于正在使用的样品进行周期性的二次采样以及更新。
图1是示出用于基于组分的电容阻抗的测量而检测微生物生长的装置的详细图示。锁定放大器被示为具有输出级210和输入级235。输出级210包括内部信号发生器,所述内部信号发生器可以用于向电介质阻抗测量腔220(未示出)的一个电极211发送正弦的RF信号。所述腔的第二电极212与所述锁定放大器的信号输入级235相连。虽然锁定放大器在图中被示出并且在本文的示例中进行了描述,但是本领域的一个普通技术人员将认识到其他测量设备,如LCR仪或者网络分析器,可以代替锁定放大器而被使用。
根据该实施方式,在所述腔220(未示出)内的样品液体直接接触两个电极并且可以通过虚框225中所示的电路图进行描述。在这方面,Ci代表金属电极和液体之间的界面电容;Ri代表金属电极和液体之间的界面电阻;Rb是液体的本体电阻;Rm是微生物的膜电阻;并且Cm是膜电容。
假定锁定放大器的输出级210的内部信号发生器具有50Ω的通常内部电阻,并且锁定放大器的输入级235具有15pF的通常电容(Cp)以及10MΩ的通常输入电阻(Rp)。
图1中示出的检测微生物生长的装置包括源匹配电阻Rs(215)和测量负载电阻Rv(216)。根据图1,源匹配电阻215和测量负载电阻216可以根据给定的电介质测量腔和液体被选定,使得测量信号的异相组分的频谱示出零交叉特征,该零交叉特征(i)依赖于Cm的值,并且(ii)在合宜低频率处被设定。在特定的实施例中,频率被设定在约100kHz的值或该值以下。这允许使用标准的锁定放大器。例如,当Rs=500Ω且Rv=500Ω时,在液体样品介质是常规的血液培养生长介质的情况下,产生在约30kHz至约100kHz的范围内的零交叉频率。这种血液培养生长介质的一个示例是购自马里兰州斯帕克斯的Becton DickinsonDiagnositics的Standard Aerobic/F介质。
根据图1,锁定放大器的输出级210的异相信号振幅与异相阻抗值成反比。换言之,在测量时异相阻抗值(如电抗值)在异相信号振幅的零交叉频率处处于其最大值。值的注意的是,改变阻抗检测腔的尺寸(由于改变样品体积、样品的高/宽比或二者),或用另一液体样品替换生长介质将很可能改变选定的Rs和Rm值。如图所示,锁定放大器输入级235提供参考电势。如所图示的参考是浮动接地。本领域普通技术人员将意识到,存在输入级能够以多种不同方式提供参考电势,而图1的参考仅是示例性说明的并且不是限制的方式。
图2图示说明用于通过使用测量频率的自动调节来测量液体样品的电介质电容和电抗以测定测试环境的离子电荷变化的装置的可替代实施方式。在这方面,相敏感信号检测器330的异相信号输出端332与电子积分器340的输入端335相连。积分器340的输出端345与压控振荡器310的频率控制输入端305相连,所述压控振荡器310与图1中所示的装置中的信号发生器作用相同。此外,Ci代表金属电极和液体之间的界面电容;Ri代表金属电极和液体之间的界面电阻;Rb是液体的本体电阻;且Cm是本体电容。此外,本体电容(Cb)可以用于检测微生物生长,该本体电容如WO 2013/123189中所述,该申请已经通过引入被并入。
在此实施例中,压控振荡器(“VCO”)310产生正弦电信号,并且该正弦电信号电偶合到与样品接触的电极311。而且,与样品接触的第二电极312电连接到相敏感信号检测器330。如前所述,相敏感信号检测器的异相输出信号与积分器340偶合。由于积分器340的输出端与VCO 310的频率控制输入端耦合,所以只有当被相敏感信号检测器测量到的异相信号振幅为零时,VCO 310的频率才被调整。久而久之,在零异相信号振幅处被调节的频率的增加表明样品内微生物生长。
在操作中,积分器340输出电压影响压控振荡器的频率。例如,如果起初频率低于60kHz,那么异相信号振幅是正的。这导致积分器输出端345处为正输出电压,并且相应地导致压控振荡器310的频率增加。频率将持续增加直到达到零交叉频率(此处异相信号振幅为零)。此时,当异相振幅变为零时,不会再有进一步的积分发生。因此,压控振荡器的频率停留在零交叉频率处,根据此实施例该零交叉频率为60.723kHz。如果起始频率过高,则实际的零交叉频率将从该过高的频率自动接近。通过记录随时间的零交叉频率可以检测细菌的存在并且检测由微生物生长导致的频率增加。
图2中所示的装置的优势在于能够以极高的精度测定零交叉频率。由于“零点信号”在相敏感信号检测器的输出端发生,所以信号发生器振幅或者相敏感信号检测器的内部增益的任何漂移都将不会影响代表系统输出信息的自动调节的零交叉频率。
转至图3,其示出利用桥式电阻器(Rp)-电容器调节电路405测量阻抗的系统400的实施方式。图3的系统包括具有内部信号发生器的锁定放大器的输出级410,一系列可变的可调节元件415(即可变电位计),包含液体样品的耗材420,桥式电阻器-电容器调节电路(如串联连接的第二可变电位计405以及开关425),以及锁定放大器的输入级435。在所示的实施例中,当开关开启时,系统在低频率下运行,而当开关关闭时,系统在较高频率下运行。
如上所述,具有内部信号发生器的锁定放大器具有50Ω的通常内部电阻。此外,锁定放大器的输入级435具有15pF的通常电容(Cis)和10MΩ的通常输入电阻(Ris)。在这方面,锁定放大器可以产生施加至液体样品的电压和频率。进一步地,本领域的普通技术人员将意识到,在不脱离本文描述的示例的范围的情况下,诸如LCR仪或者网络分析器的测量设备可以被使用。
可变桥式可调节元件(Rs)(如可变电位计)405的功能如之前描述的源匹配电阻器一样。因此,可变桥式可调节元件(Rs)405可以针对给定的耗材420(如检测腔)和液体样品被调节到一电阻(0-10,000Ω),由此,测量信号的异相组分的频谱显示出零交叉特征,该零交叉特征(i)依赖于Cm的值,并且(ii)被设置在低于100kHz的合宜低频率处。这允许使用标准的锁定放大器。
耗材420很大程度上依据设计需要选择。在此描述的实施例中,耗材是在侧面具有两条间隔约10mm到约40mm缝隙的塑料瓶或相似的塑料耗材(未示出)。每一缝隙中放置一金属电极(如用金电镀的黄铜圆柱件),并且环氧树脂(如胶水)涂布在塑料/金属界面外侧周围以将电极固定到位。重要的是,环氧树脂仅在外表面发现且不渗入含有样品的瓶的内部区域。即,环氧化合物不接触样品。
本领域普通技术人员将意识到,该耗材可以是多种几何形状的,并具有将样品无菌转移进出所述耗材的适配接口。在这方面,可以基于病人样本的类型、待测试样品的体积等因素使用不同的耗材。
金属化电极411、412可以使用任何标准的(如低成本的)金属(如铜、黄铜、钢等)制造,该金属电极具有带有施加到其上的抗腐蚀金属(如铂、金、银)的共形涂层(即厚度从亚纳米到微米)。这种抗腐蚀金属的共形涂层对于高盐生长/介质基体(如血液、尿液、痰液)的相容性是必须的。共形涂层技术的示例包括电镀、溅射和蒸发处理。这些处理方式对于本领域技术人员是熟知的并且在本文中不再详细描述。本领域普通技术人员将从常规的共形涂层技术中选择以形成本文所述的电极。
电极配置可以适用于在耗材(即测试设备)中使用的几乎任何尺寸、形状以及材料。电极(2个或更多个)可以被配置为任何已经被提供了合适尺寸特性来接收电极的耗材形式。在可替代的实施例中,该耗材可以通过在电极周围吹塑耗材而形成。在另一些示例中,电极可以通过耗材的盖子而延伸进入耗材内。这种设计不再需要直接将电极塑模或粘合在耗材的材料中。在上述实施例中,电极可以被配置以形成外界和耗材的内容物(即液体)之间的导电路径。
耗材的示例包括传统的小瓶、管式配置、微流体盒等。对于本领域技术人员而言合适的耗材是熟知的,并且在本文中不再详细描述。
用于电极的合适金属的示例包括但不限于,银、金、锌、铁、镍、铝等。更进一步地,对于电极可以使用不同的金属涂层。此外,电极间距、导线配置和电极尺寸很大程度上根据设计需要选择。电极设计与多种因素相关,该因数如介质、耗材、样品等。本领域普通技术人员将意识到,基于本文描述的示例可以使用多种配置。
在那些其中电极被放置在耗材内的实施例中的操作中,电极必须被浸入样品液体内,使得在电极之间存在导电路径。换言之,覆盖一个电极的同一液体主体也必须覆盖另一个。更进一步地,瓶子内存在的非生物性对象(如环氧树脂、树脂)必须不覆盖电极达到可以妨碍电极之间的导电路径的程度,从而造成高度可变性和不可靠的数据。
该系统被配置为接收所述耗材(如图3中示意性示出的),使得其将被电整合入系统400。根据一些实施例,可以在耗材中形成非对称特性,使得使用者能够仅在一个预定的取向上将耗材插入设备中。这将保证耗材“模块”与系统中其他组分之间的合适的相互连接。
转至图4A和图4B,示出了用于测量多种耗材中的阻抗的系统400的不同实施方式。图4A和图4B的系统包括锁定放大器的输出级410、多路器440、可变系列电阻器415、具有第一电极411和第二电极412的耗材420、搅拌器450、支架470、可变桥式电阻器405、第二多路器460、锁定放大器的输入级435和计算机500。在图4A中,开关425与可变桥式电阻器405串联。开关425和桥式电阻器405的这种关系也在图3中被图示说明。图4B是可替代的配置,其中开关425与可变桥式电阻器405并联。
根据该实施例,耗材420可以被存放在基于支架的模块化平台470中。每一个支架470可以包括能够处理多至20个耗材的多路器元件。相应地,每一个支架有至少一个专用的数字信号处理(DSP)锁定放大器模块,该模块将负责信号获取。因此,本发明设想耗材阵列和将准许从阵列中的每个耗材获取信号的开关。
多路器电路440和460可以允许计算机(如500)、信号检测板或设备来扫描多个耗材或者单一耗材的子组分。在那些实施例中,其中一个耗材具有多个腔,多个腔中的每个腔中均具有样品,多路器进行动作以“切换”检测设备/电路连接(1+输入和1+输出)至单个耗材或耗材的子组分。多路器电路将允许相对少的硬件组分来监测多个耗材。根据多路程度以及耗材配置,多路器电路可以具有多种操作变化。
在操作中,耗材的测量可以连续地进行。即,阵列中的每个耗材每次被扫描一个。每一耗材的扫描时间可以为大约几十秒。因此,每一个支架(如果完全使用)会花费约2-3分钟进行扫描。计算装置500可以每10-15分钟重复扫描活动。当阵列未被扫描时,可以通过使用搅拌器450对耗材进行搅拌以对液体进行充分混合并通气。搅拌可以通过竖直移位、环形震荡或者通过在耗材内使用搅拌棒来执行。搅拌机构(如果需要)可以具有多种设置,包括使样品混合最大化的水平震荡机构。本领域普通技术人员将意识到,根据本文描述的示例,可以使用不同的搅拌器的示例,并且因此不更详细地讨论。
可变桥式电阻器405(如桥式电阻器-电容器调节电路)可以是外部调节电路,该外部调节电路将耗材420与检测设备(即锁定放大器的输入级435)物理连接。可变桥式电阻器405可以包括一系列并联的可变电阻(数字电位计),其允许频率灵敏度的“实时的频率调节和计算”。在这方面,来自耗材的信号的频率可以在约1kHz到约200MHz之间进行调节。调节参数(即选定的频率范围以及峰与峰的电压)可以通过耗材的总体积、电极的金属化性质(如金、银或铂)、包含的液体类型等进行测定。通过在低频和高频二者处调节耗材信号,该系统能够独立地在低频下检测代谢副产物并在较高频率下检测微生物生物量。
根据一些实施方式,如图4A中所示,开关425可以与一系列可变桥式电阻器405用电线串联。在可替代示例中,如图4B所示,开关425可以与可变桥式电阻器405用电线并联。当开关打开时,系统可以在低频(即1到20kHz)下运行。如上所指示的,这将能够检测耗材中组成的变化。当开关关闭时,系统可以通过向信号发生器提供反馈而在较高频率(即远大于20kHz)下运行。如之前所讨论的,通过在较高频率下运行,系统对于液体中离子组分的变化和生物量自身的变化二者均是敏感的。由于具有在高频和低频二者下调节频率以测试的能力,该系统对于较少体积的样品可以具备更快的检出时间(TTD)。
锁定放大器的输入级435是能够从相当大的噪声环境内提取具有已知频率的信号的专用装置。更进一步地,锁定放大器可以将特别关注的信号解压成基本的子组分。例如,总阻抗的组分,尤其是“异相”电抗组分可以根据下式使用:
Z=电阻+j*电抗
总阻抗|Z|=√(电阻2+电抗2)。
在另一示例中,电容组分(即界面电容和细胞电容)对总的电抗子组分有贡献。因此,使用信号的子组分可以1)允许连续几天(如5天的方案)以特定间隔(如约10分钟)持续监测每每个耗材或者耗材中的子组分,并且2)检测带电分子组成的变化以及生物细胞或样品组分的数目。
在这方面,一旦有信号输入锁定放大器的输入级435,可以执行数据分析。根据一些实施例,数据分析分两步进行以确定微生物生长。第一步,在每一个时间点下分析原始光谱数据(即检测到的电抗信号vs频率)(如斜率、曲线下的面积、X截距、Y截距等)以得到单独的数据点。第二步,从每一个耗材或耗材的子组分获得多个数据点后,使用通用算法以确定表明微生物存在的与已知对照值有显著统计学偏差的数据点。由于对微生物生长的灵敏度加强,本文所描述的示例提供微生物生长的更快的检测时间。
在可替代实施例中,来自原始“电抗”数据的信号提取的数据值可以用来确定微生物生长与否。在这方面,提取的数据可以利用数学函数确定截距或曲线下的面积。这些数学函数的结果可以与阈值对比。因此,在阈值之上的累积变化可以用来区别包含微生物的耗材。因此,测量信号的异相组分的频谱示出零交叉特征,该零交叉特征(i)依赖于Cm值,并且(ii)在适宜低频率下进行设定。在某些实施例中,频率被设定在约100kHz或其下的值。这允许使用标准测量设备,该标准测量设备如本文描述的锁定放大器、LCR仪和/或网络分析器。
与标准光学方法相比,上述实施例改善检出时间(TTD)达5-70%。如下所述,当在与传统光学方法相比时,数据示出当在低频率调节下检测时对于大量微生物的检测能够以更快的TTD发生。更进一步地,数据表明通过使用高频调节可以进一步加强检测灵敏度,由此导致甚至更快的TTD。
在这方面,如图5中所示,在较小的聚碳酸酯管中进行实验,其包括:10mL BACTEC标准需氧介质、3mL袋装血液、17CFU(集落形成单位)的大肠杆菌(A25922),以及镀金金属电极(黄铜主体),所述电极延伸入耗材内部并浸入介质/样品混合物中。耗材中的电极与锁定放大器的其他组分相互连接。该设备的桥式电阻器被设置为187欧姆,这造成在40到80kHz频段的光谱灵敏度。
当与进行平行扫描的对照(无微生物)管进行比较时,如图6中所示,多数微生物和介质的TTD均显著改善。这样可以表明微生物的灵敏度为104-105CFU,比在约109CFU下检测微生物的当前光学检测系统的灵敏度高至少2到4个数量级。这些结果代表减少了70%的检出时间,更具体的细节将关于附图5在下面进行讨论。这些水平的检测从未被报道过,并且完全是出乎意料的。对于图示,示出大肠杆菌的频率随时间的变化(相对于对照)。在低频率下,TTD约为10小时,这加快了多达5-10%。在高频率下,TTD改善至约4小时,这几乎加快了70%。
再次参考图6,针对图6中报告的各种样品重复上述实验,其中上述实验的结果在图5中被图示说明。例如,其中3mL袋装血液和17CFU的金黄色葡萄球菌(S.aureus)(A25923)生长在7-8小时内被检测。相比于检测集落生长的标准光学检测技术在约12-14小时的时间,这表示检出时间减少42%。
图6图示说明进行不同实验的结果,这些实验包括下述条件:7mL袋装血液和17CFU大肠杆菌微生物(A25922);7mL袋装血液和17CFU金黄色葡萄球菌(A25923);7mL袋装血液和17CFU流感嗜血杆菌(H.influenzae)(A19418);7mL袋装血液和17CFU粪肠球菌(H.faecalis)(A29212);以及7mL袋装血液和17CFU念珠菌(C.glabrata)(A66032)。
因此,在7mL溶真菌的介质中大肠杆菌的生长在约8.5到9小时内被检测到,这相比于标准光学检测技术在溶真菌的介质中对于大肠杆菌的检测(10-11小时),改善TTD。金黄色葡萄球菌在溶真菌的介质中的生长在约10小时内被检测到,相比于标准光学检测技术有23%的提高。流感嗜血杆菌在溶真菌的介质中的生长在约16小时内被检测到。其TTD相比于使用标准光学检测技术对于流感嗜血杆菌的TTD(16小时)改进16%。对于溶真菌的介质中的粪肠球菌集落,其TTD为11小时,代表相对于使用标准光学检测技术11-12小时TTD的8%的改进。溶真菌的介质中的念珠菌的TTD在约17小时内被检测,这代表了使用标准光学检测技术检测念珠菌TTD(20-42小时)的45%的改进。图5和图6中还报告了在标准需氧介质中的样品相对于标准光学检测技术TTD的改善。
图7图示说明在上述较小体积中实现的检出时间的改进同样在较大体积的样品/介质中实现。具体地,在BACTEC瓶中组合40ml标准BACTEC介质和10ml血液。样品被接种有50-60CFU的大肠杆菌。在低频率下,使用本文描述的装置及方法,TTD为10.5-11小时,这加快了多达5%。在高频率下,TTD改善至9.5-10小时,这加快了多达14%。
图5图示说明不同频率下大肠杆菌的检出时间。以同样的方式准备所有的耗材,唯一的不同在于是否有微生物存在和外部电路的电参数。在这方面,用四个16mL耗材进行实验,每一耗材中准备有10mL标准需氧介质和3mL血液。两个耗材还加入大肠杆菌的17个集落形成单位(一个用于低频模式,而一个用于高频模式)。耗材的电极是30mm金电极。在实验过程中,对耗材施加500mV的峰与峰电压,并且经由每分钟120转的速率震荡来搅拌耗材。
在低频模式(如1-10kHz)下,对于含介质和血液的耗材施加的信号没有产生偏差。相比之下,对于在低频模式下加入具有大肠杆菌的耗材,频率的偏差大约10小时——如图5中所描述的在信号偏差点510处——被检测到。这代表了相对于标准光学检测技术在检出时间上5-10%的改善。对于大肠杆菌,经典的BACTED TDD为约11小时。
在高频模式(如40-80kHz)下,可变桥式电阻器(如图4A和图4B中的405)被调节至500Ω。因此,在4小时标志附近——如图5中所描述的在信号偏差点520处),检测到带有大肠杆菌的耗材中的施加的信号的偏差。这代表了相对于标准光学检测技术在检出时间上70%的改善。在之前的大肠杆菌实验中,从来没有在这些检测水平和这一时间框架下的检测被报道,是完全出乎意料的。而本发明人并不意在坚持某一特定理论,在信号偏差点520处的该早期检测特征被确信主要归因于细胞电容,或者与微生物细胞的膜电势相关的电荷。当这些细胞持续复制并产生代谢副产物时,介质的离子浓度达到临界点,在该临界点处发生第二特征,如图5中信号偏差点525处所描述的。两个信号都代表了对生长中的微生物初步鉴定可能性的独特特征。因此,目前的应用描述了通过使用高和低频检测二者来加强检测灵敏度从而产生更低的检出时间。
图8示出了在高频模式下通过测量根据时间的变化速率,对于洛菲不动杆菌(A.lowffii)的检出时间。可变桥式电阻器(如图4A和图4B中的405)被调节至200Ω。频段为50-60kHz。准备两个1mL耗材(如一个对照,而一个具有样品),其中加入0.9mL标准需氧介质和0mL血液。根据此实验,向其中一个耗材加入洛菲不动杆菌的28个集落形成单位。耗材具有两个15mm电极。在实验过程中,向耗材施加250mV的峰与峰电压,并且经由每分钟100转的速率的震荡来搅拌耗材。当施加高频率时,检测到正常频率的变化速率约11小时,如图8中信号偏差点810处所描述的。这代表了传统光学检测系统的50%的减少。对于洛菲不动杆菌,经典的BACTED TDD为约20小时。
图9代表在高频模式下检测藤黄微球菌(M.luteus)的实验结果。可变桥式电阻器(如图4A和图4B中的405)被调节至200Ω。频段为60-70kHz。准备两个1mL耗材(如一个对照,而一个具有样品),其中加入0.9mL标准需氧介质和0mL血液。向上述其中一个耗材加入藤黄微球菌的21个集落形成单位。耗材具有两个15mm电极。在实验过程中,向耗材施加250mV的峰与峰电压,并且经由每分钟100转的速率的震荡来搅拌耗材。如图9中信号偏差点910处所示的,检测到正常频率的变化速率约28-30小时,其代表了相比于传统光学检测系统的30%的减少。对于藤黄微球菌,经典的BACTED TDD为约42小时。
上述检测时间之前从未被报道过,且是完全出乎意料的。因此,目前的应用描述了对于微生物生长通过使用高和低频二者加强检测灵敏度可以产生更低的检出时间。
尽管本文参考具体实施例已经描述了本发明,但应当明确,这些实施例仅是本发明的原理和应用的图示说明。因此,应当明确可以对所示实施例做出多种修改,并且在不脱离本发明的如随附权利要求所要求保护的精神和范围的情况下,可以设想其他设置。
Claims (5)
1.一种对微生物生长敏感的系统,所述系统包括:
信号处理电路,所述信号处理电路连接到适于接收生物样品的容器;
两个或更多个电极,所述两个或更多个电极刺入所述容器并且与所述生物样品接触,
与第一电极连接的压控振荡器(“VCO”);
与第二电极连接的相敏感信号检测器;和
积分器,其配置为接收来自所述相敏感信号检测器的异相输出信号,从而将所述VCO的频率调整为第一频率,此时由所述相敏感信号检测器测量到的异相信号振幅达到零;
其中基于观察到频率增加到超过所述第一频率指示出现微生物生长。
2.根据权利要求1所述的系统,进一步包括用于调整所述频率的平行于锁定放大器的电容输入级的一个或更多个可变电阻器。
3.根据权利要求1所述的系统,进一步包括用于调整所述频率的桥式电阻器-电容器调节电路。
4.根据权利要求3所述的系统,其中所述信号处理电路在高频操作模式和低频操作模式之间可转换,其中高频在约40kHz到约80kHz的范围内,而低频在约1kHz到约10kHz的范围内。
5.根据权利要求4所述的系统,进一步包括与所述桥式电阻器串联的开关,其中当所述开关打开时,所述系统以低频模式运行,而当所述开关闭合时,所述系统以高频模式运行。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462063602P | 2014-10-14 | 2014-10-14 | |
| US62/063,602 | 2014-10-14 | ||
| PCT/US2015/055501 WO2016064635A1 (en) | 2014-10-14 | 2015-10-14 | Reactance and capacitance sensing platform for detecting microorganisms |
| CN201580055175.5A CN107110803A (zh) | 2014-10-14 | 2015-10-14 | 用于检测微生物的电抗和电容型传感平台 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201580055175.5A Division CN107110803A (zh) | 2014-10-14 | 2015-10-14 | 用于检测微生物的电抗和电容型传感平台 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN115963149A true CN115963149A (zh) | 2023-04-14 |
Family
ID=55761340
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202211697198.4A Pending CN115963149A (zh) | 2014-10-14 | 2015-10-14 | 用于检测微生物的电抗和电容型传感平台 |
| CN201580055175.5A Pending CN107110803A (zh) | 2014-10-14 | 2015-10-14 | 用于检测微生物的电抗和电容型传感平台 |
| CN201520983323.7U Active CN205538786U (zh) | 2014-10-14 | 2015-10-14 | 使用电抗和电容型传感平台对微生物生长敏感的系统 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201580055175.5A Pending CN107110803A (zh) | 2014-10-14 | 2015-10-14 | 用于检测微生物的电抗和电容型传感平台 |
| CN201520983323.7U Active CN205538786U (zh) | 2014-10-14 | 2015-10-14 | 使用电抗和电容型传感平台对微生物生长敏感的系统 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US10808217B2 (zh) |
| EP (1) | EP3207362B1 (zh) |
| JP (1) | JP6795495B2 (zh) |
| CN (3) | CN115963149A (zh) |
| AU (1) | AU2015336363B2 (zh) |
| CA (1) | CA2964310C (zh) |
| WO (1) | WO2016064635A1 (zh) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10196678B2 (en) | 2014-10-06 | 2019-02-05 | ALVEO Technologies Inc. | System and method for detection of nucleic acids |
| CN115963149A (zh) * | 2014-10-14 | 2023-04-14 | 贝克顿·迪金森公司 | 用于检测微生物的电抗和电容型传感平台 |
| US11465141B2 (en) | 2016-09-23 | 2022-10-11 | Alveo Technologies, Inc. | Methods and compositions for detecting analytes |
| CN111615628A (zh) * | 2018-01-24 | 2020-09-01 | 惠普发展公司,有限责任合伙企业 | 根据流体阻抗的流体性质确定 |
| US20190241861A1 (en) * | 2018-02-02 | 2019-08-08 | Karmel Alon Allison | Bacterial detection system |
| CN113406153B (zh) * | 2021-06-29 | 2022-06-07 | 毕玉琦 | 一种食品菌群快速检测装置 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1256756A (zh) * | 1998-02-19 | 2000-06-14 | 住友金属工业株式会社 | 阻抗检测装置和检测方法 |
| TW201226896A (en) * | 2010-12-17 | 2012-07-01 | Univ Yuanpei | Microbe or cell inspection system and method thereof |
| CN102954985A (zh) * | 2011-08-31 | 2013-03-06 | 中国科学院上海微系统与信息技术研究所 | 一种电阻抗式细菌快速检测传感器的数据分析方法 |
| WO2013123189A1 (en) * | 2012-02-15 | 2013-08-22 | Becton, Dickinson And Company | Impedence-based bacterial detection system |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000022431A1 (en) | 1998-10-09 | 2000-04-20 | Simon Feldberg | Method and apparatus for determining and evaluating bacterial populations |
| EP1162449A1 (en) * | 2000-06-06 | 2001-12-12 | Universiteit Gent | AC-based gate detection method and device for the sizing of colloidal particles, cells and bacteria in liquids |
| US6649402B2 (en) | 2001-06-22 | 2003-11-18 | Wisconsin Alumni Research Foundation | Microfabricated microbial growth assay method and apparatus |
| US6433560B1 (en) * | 2001-08-31 | 2002-08-13 | Eaton Corporation | Combined fluid condition monitor and fluid level sensor |
| WO2006048456A1 (en) * | 2004-11-05 | 2006-05-11 | Graceton Finance Sa | Method and device for the detection, measurement and analysis of biological, bioactive, bioenergetic and bioharmonic signals |
| US8318099B2 (en) | 2005-10-26 | 2012-11-27 | General Electric Company | Chemical and biological sensors, systems and methods based on radio frequency identification |
| US7923241B2 (en) | 2007-10-10 | 2011-04-12 | Corning Incorporated | Cell culture article and methods thereof |
| PL2271933T3 (pl) | 2008-05-07 | 2013-05-31 | Univ Strathclyde | System i sposób charakteryzowania komórek |
| CN101698879A (zh) | 2009-10-14 | 2010-04-28 | 电子科技大学 | 检测细菌培养基电阻抗曲线形态的药物敏感试验方法 |
| CN115963149A (zh) | 2014-10-14 | 2023-04-14 | 贝克顿·迪金森公司 | 用于检测微生物的电抗和电容型传感平台 |
| EP3523626A1 (en) * | 2016-10-07 | 2019-08-14 | Boehringer Ingelheim Vetmedica GmbH | Analysis system and method for testing a sample |
-
2015
- 2015-10-14 CN CN202211697198.4A patent/CN115963149A/zh active Pending
- 2015-10-14 CN CN201580055175.5A patent/CN107110803A/zh active Pending
- 2015-10-14 US US15/518,989 patent/US10808217B2/en active Active
- 2015-10-14 EP EP15853221.8A patent/EP3207362B1/en active Active
- 2015-10-14 WO PCT/US2015/055501 patent/WO2016064635A1/en active Application Filing
- 2015-10-14 CN CN201520983323.7U patent/CN205538786U/zh active Active
- 2015-10-14 CA CA2964310A patent/CA2964310C/en active Active
- 2015-10-14 JP JP2017518797A patent/JP6795495B2/ja active Active
- 2015-10-14 AU AU2015336363A patent/AU2015336363B2/en active Active
-
2020
- 2020-09-14 US US17/019,802 patent/US20200407677A1/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1256756A (zh) * | 1998-02-19 | 2000-06-14 | 住友金属工业株式会社 | 阻抗检测装置和检测方法 |
| TW201226896A (en) * | 2010-12-17 | 2012-07-01 | Univ Yuanpei | Microbe or cell inspection system and method thereof |
| CN102954985A (zh) * | 2011-08-31 | 2013-03-06 | 中国科学院上海微系统与信息技术研究所 | 一种电阻抗式细菌快速检测传感器的数据分析方法 |
| WO2013123189A1 (en) * | 2012-02-15 | 2013-08-22 | Becton, Dickinson And Company | Impedence-based bacterial detection system |
Also Published As
| Publication number | Publication date |
|---|---|
| US20200407677A1 (en) | 2020-12-31 |
| CA2964310C (en) | 2019-02-26 |
| EP3207362A4 (en) | 2018-05-09 |
| EP3207362A1 (en) | 2017-08-23 |
| CN107110803A (zh) | 2017-08-29 |
| US10808217B2 (en) | 2020-10-20 |
| CA2964310A1 (en) | 2016-04-28 |
| EP3207362B1 (en) | 2024-05-01 |
| WO2016064635A1 (en) | 2016-04-28 |
| JP2017532033A (ja) | 2017-11-02 |
| US20170240855A1 (en) | 2017-08-24 |
| AU2015336363A1 (en) | 2017-05-04 |
| JP6795495B2 (ja) | 2020-12-02 |
| AU2015336363B2 (en) | 2021-03-04 |
| CN205538786U (zh) | 2016-08-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20200407677A1 (en) | Reactance and capacitance sensing platform for detecting microorganisms | |
| US9400272B2 (en) | Detection method and apparatus for detecting microbial growth | |
| Richards et al. | Electronic measurement of bacterial growth | |
| Paredes et al. | Label-free interdigitated microelectrode based biosensors for bacterial biofilm growth monitoring using Petri dishes | |
| US9709516B2 (en) | Impedance-based bacterial detection system | |
| McGlennen et al. | Using electrochemical impedance spectroscopy to study biofilm growth in a 3D-printed flow cell system | |
| Canali et al. | Conductometric analysis in bio-applications: A universal impedance spectroscopy-based approach using modified electrodes | |
| EP3001193A1 (en) | System for characterisation of pure and ultrapure water | |
| Enright et al. | Fluctuation analysis of redox potential to distinguish microbial Fe (II) oxidation | |
| Buscaglia | Development of a portable impedance spectrometer | |
| Kadan-Jamal et al. | A study on the dielectric behaviour of plant cell suspensions using wideband electrical impedance spectroscopy (WB-EIS) | |
| EP4296351A1 (en) | Non-contact impedance analyzer for real-time detection of microbial growth | |
| Selvakumar et al. | Correlation of Bacteria Growth and Electrical Impedance Spectroscopy in Stored Raw Ground Water | |
| Spiller et al. | Development of an electronic microtiterplate for high throughput screening (HTS) | |
| Heijdens | Design of a mastitis indicator sensor | |
| Jalilian et al. | Impedance Properties of Biomass in Support of Practical Mensuration in Rain Gardens | |
| WO2020030926A1 (en) | Analysis of a test sample | |
| Ren et al. | A piezoelectric transducer for bacteria counts monitoring the application of piezoelectric transducer on food detection | |
| Farace et al. | Bioanalytical application of impedance analysis: Transducing in polymer-based biosensors and probes for living tissues | |
| Qu et al. | Automatically Showing Microbial Growth Kinetics with a High-Performance Microbial Growth Analyzer | |
| Al-Salami | Impedance Spectroscopic Analysis of the Interidigitated Flexible Sensor for Pseudomonas Aeruginosa Bacteria Detection |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |