CN115397441A - 新方法 - Google Patents
新方法 Download PDFInfo
- Publication number
- CN115397441A CN115397441A CN202080077678.3A CN202080077678A CN115397441A CN 115397441 A CN115397441 A CN 115397441A CN 202080077678 A CN202080077678 A CN 202080077678A CN 115397441 A CN115397441 A CN 115397441A
- Authority
- CN
- China
- Prior art keywords
- organ
- tissue
- cells
- brain
- regulatory
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000000034 method Methods 0.000 title claims abstract description 121
- 210000000056 organ Anatomy 0.000 claims abstract description 261
- 108010002350 Interleukin-2 Proteins 0.000 claims abstract description 181
- 210000003289 regulatory T cell Anatomy 0.000 claims abstract description 179
- 230000008685 targeting Effects 0.000 claims abstract description 65
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 49
- 206010061218 Inflammation Diseases 0.000 claims abstract description 46
- 230000004054 inflammatory process Effects 0.000 claims abstract description 46
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 40
- 210000003169 central nervous system Anatomy 0.000 claims abstract description 34
- 201000010099 disease Diseases 0.000 claims abstract description 31
- 210000001428 peripheral nervous system Anatomy 0.000 claims abstract description 27
- 208000035475 disorder Diseases 0.000 claims abstract description 18
- 230000001404 mediated effect Effects 0.000 claims abstract description 14
- 102000000588 Interleukin-2 Human genes 0.000 claims description 179
- 230000014509 gene expression Effects 0.000 claims description 150
- 210000004556 brain Anatomy 0.000 claims description 111
- 239000013603 viral vector Substances 0.000 claims description 80
- 241000700605 Viruses Species 0.000 claims description 51
- 208000030886 Traumatic Brain injury Diseases 0.000 claims description 35
- 230000009529 traumatic brain injury Effects 0.000 claims description 35
- 230000002276 neurotropic effect Effects 0.000 claims description 21
- 238000011282 treatment Methods 0.000 claims description 21
- 230000008499 blood brain barrier function Effects 0.000 claims description 19
- 210000001218 blood-brain barrier Anatomy 0.000 claims description 19
- 241000702421 Dependoparvovirus Species 0.000 claims description 16
- 208000036110 Neuroinflammatory disease Diseases 0.000 claims description 16
- 208000012902 Nervous system disease Diseases 0.000 claims description 13
- 208000014674 injury Diseases 0.000 claims description 13
- 108091026890 Coding region Proteins 0.000 claims description 12
- 230000003959 neuroinflammation Effects 0.000 claims description 12
- 230000004888 barrier function Effects 0.000 claims description 11
- 208000025698 brain inflammatory disease Diseases 0.000 claims description 9
- 206010014599 encephalitis Diseases 0.000 claims description 9
- 208000023275 Autoimmune disease Diseases 0.000 claims description 7
- 230000001154 acute effect Effects 0.000 claims description 6
- 201000006417 multiple sclerosis Diseases 0.000 claims description 5
- 230000008736 traumatic injury Effects 0.000 claims description 4
- 208000029028 brain injury Diseases 0.000 claims description 3
- 206010019196 Head injury Diseases 0.000 claims description 2
- 230000009692 acute damage Effects 0.000 claims description 2
- 230000005784 autoimmunity Effects 0.000 claims 1
- 238000001727 in vivo Methods 0.000 abstract description 13
- 238000004519 manufacturing process Methods 0.000 abstract description 4
- 210000001519 tissue Anatomy 0.000 description 226
- 210000004027 cell Anatomy 0.000 description 137
- 241000699670 Mus sp. Species 0.000 description 54
- 108700019146 Transgenes Proteins 0.000 description 52
- 239000004098 Tetracycline Substances 0.000 description 33
- 229960002180 tetracycline Drugs 0.000 description 33
- 108090000623 proteins and genes Proteins 0.000 description 32
- 229930101283 tetracycline Natural products 0.000 description 32
- 235000019364 tetracycline Nutrition 0.000 description 32
- 150000003522 tetracyclines Chemical class 0.000 description 32
- 102100039289 Glial fibrillary acidic protein Human genes 0.000 description 24
- 101710193519 Glial fibrillary acidic protein Proteins 0.000 description 24
- 210000005046 glial fibrillary acidic protein Anatomy 0.000 description 24
- 210000001130 astrocyte Anatomy 0.000 description 23
- 238000010361 transduction Methods 0.000 description 23
- 230000026683 transduction Effects 0.000 description 23
- 239000005090 green fluorescent protein Substances 0.000 description 19
- FFTVPQUHLQBXQZ-KVUCHLLUSA-N (4s,4as,5ar,12ar)-4,7-bis(dimethylamino)-1,10,11,12a-tetrahydroxy-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1C2=C(N(C)C)C=CC(O)=C2C(O)=C2[C@@H]1C[C@H]1[C@H](N(C)C)C(=O)C(C(N)=O)=C(O)[C@@]1(O)C2=O FFTVPQUHLQBXQZ-KVUCHLLUSA-N 0.000 description 18
- 230000001965 increasing effect Effects 0.000 description 17
- 230000001939 inductive effect Effects 0.000 description 17
- 229960004023 minocycline Drugs 0.000 description 17
- 210000001744 T-lymphocyte Anatomy 0.000 description 16
- 230000006378 damage Effects 0.000 description 16
- 108010051219 Cre recombinase Proteins 0.000 description 15
- 239000013598 vector Substances 0.000 description 15
- 241000699666 Mus <mouse, genus> Species 0.000 description 13
- 210000000653 nervous system Anatomy 0.000 description 13
- 208000006011 Stroke Diseases 0.000 description 12
- 210000002569 neuron Anatomy 0.000 description 12
- 238000012384 transportation and delivery Methods 0.000 description 12
- 108091023040 Transcription factor Proteins 0.000 description 10
- 102000040945 Transcription factor Human genes 0.000 description 10
- 230000002093 peripheral effect Effects 0.000 description 10
- 230000002829 reductive effect Effects 0.000 description 10
- 230000009885 systemic effect Effects 0.000 description 10
- 208000027418 Wounds and injury Diseases 0.000 description 9
- 230000003110 anti-inflammatory effect Effects 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 230000001419 dependent effect Effects 0.000 description 8
- 201000002491 encephalomyelitis Diseases 0.000 description 8
- 238000000684 flow cytometry Methods 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 102000007299 Amphiregulin Human genes 0.000 description 7
- 108010033760 Amphiregulin Proteins 0.000 description 7
- 102100025137 Early activation antigen CD69 Human genes 0.000 description 7
- 101000934374 Homo sapiens Early activation antigen CD69 Proteins 0.000 description 7
- 230000004913 activation Effects 0.000 description 7
- 230000001054 cortical effect Effects 0.000 description 7
- 230000001506 immunosuppresive effect Effects 0.000 description 7
- SGKRLCUYIXIAHR-AKNGSSGZSA-N (4s,4ar,5s,5ar,6r,12ar)-4-(dimethylamino)-1,5,10,11,12a-pentahydroxy-6-methyl-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1=CC=C2[C@H](C)[C@@H]([C@H](O)[C@@H]3[C@](C(O)=C(C(N)=O)C(=O)[C@H]3N(C)C)(O)C3=O)C3=C(O)C2=C1O SGKRLCUYIXIAHR-AKNGSSGZSA-N 0.000 description 6
- 206010062016 Immunosuppression Diseases 0.000 description 6
- 208000025966 Neurological disease Diseases 0.000 description 6
- 210000004369 blood Anatomy 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 229960003722 doxycycline Drugs 0.000 description 6
- 230000035755 proliferation Effects 0.000 description 6
- 210000000952 spleen Anatomy 0.000 description 6
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 230000010261 cell growth Effects 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- 230000006698 induction Effects 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 238000011002 quantification Methods 0.000 description 5
- 230000009467 reduction Effects 0.000 description 5
- 230000002441 reversible effect Effects 0.000 description 5
- 238000012385 systemic delivery Methods 0.000 description 5
- 230000001225 therapeutic effect Effects 0.000 description 5
- 208000024827 Alzheimer disease Diseases 0.000 description 4
- 102000004127 Cytokines Human genes 0.000 description 4
- 108090000695 Cytokines Proteins 0.000 description 4
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 description 4
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 description 4
- 102100027268 Interferon-stimulated gene 20 kDa protein Human genes 0.000 description 4
- NKANXQFJJICGDU-QPLCGJKRSA-N Tamoxifen Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN(C)C)=CC=1)/C1=CC=CC=C1 NKANXQFJJICGDU-QPLCGJKRSA-N 0.000 description 4
- 230000003542 behavioural effect Effects 0.000 description 4
- 230000030833 cell death Effects 0.000 description 4
- 230000003247 decreasing effect Effects 0.000 description 4
- 230000003447 ipsilateral effect Effects 0.000 description 4
- 230000003902 lesion Effects 0.000 description 4
- 239000003550 marker Substances 0.000 description 4
- 208000015122 neurodegenerative disease Diseases 0.000 description 4
- 230000003389 potentiating effect Effects 0.000 description 4
- 230000004083 survival effect Effects 0.000 description 4
- 238000011830 transgenic mouse model Methods 0.000 description 4
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 3
- 102100032912 CD44 antigen Human genes 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- 101000868273 Homo sapiens CD44 antigen Proteins 0.000 description 3
- 101000738771 Homo sapiens Receptor-type tyrosine-protein phosphatase C Proteins 0.000 description 3
- 241001529936 Murinae Species 0.000 description 3
- 102100037422 Receptor-type tyrosine-protein phosphatase C Human genes 0.000 description 3
- 239000012190 activator Substances 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 210000000133 brain stem Anatomy 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 208000010877 cognitive disease Diseases 0.000 description 3
- 230000001186 cumulative effect Effects 0.000 description 3
- 239000008121 dextrose Substances 0.000 description 3
- 231100000673 dose–response relationship Toxicity 0.000 description 3
- 210000000987 immune system Anatomy 0.000 description 3
- 239000003018 immunosuppressive agent Substances 0.000 description 3
- 208000015181 infectious disease Diseases 0.000 description 3
- 230000004968 inflammatory condition Effects 0.000 description 3
- 208000027866 inflammatory disease Diseases 0.000 description 3
- 230000004073 interleukin-2 production Effects 0.000 description 3
- 230000007774 longterm Effects 0.000 description 3
- 210000000274 microglia Anatomy 0.000 description 3
- 238000010172 mouse model Methods 0.000 description 3
- 210000001577 neostriatum Anatomy 0.000 description 3
- 230000001537 neural effect Effects 0.000 description 3
- 210000004940 nucleus Anatomy 0.000 description 3
- 239000000546 pharmaceutical excipient Substances 0.000 description 3
- 230000006798 recombination Effects 0.000 description 3
- 238000005215 recombination Methods 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 230000035939 shock Effects 0.000 description 3
- 150000003384 small molecules Chemical class 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 210000000278 spinal cord Anatomy 0.000 description 3
- 238000011144 upstream manufacturing Methods 0.000 description 3
- 230000003612 virological effect Effects 0.000 description 3
- 102000004657 Calcium-Calmodulin-Dependent Protein Kinase Type 2 Human genes 0.000 description 2
- 108010003721 Calcium-Calmodulin-Dependent Protein Kinase Type 2 Proteins 0.000 description 2
- 102000001301 EGF receptor Human genes 0.000 description 2
- 108060006698 EGF receptor Proteins 0.000 description 2
- 241000588724 Escherichia coli Species 0.000 description 2
- 101001046686 Homo sapiens Integrin alpha-M Proteins 0.000 description 2
- 101001117317 Homo sapiens Programmed cell death 1 ligand 1 Proteins 0.000 description 2
- -1 ICOS Proteins 0.000 description 2
- 102100022338 Integrin alpha-M Human genes 0.000 description 2
- 102000003814 Interleukin-10 Human genes 0.000 description 2
- 108090000174 Interleukin-10 Proteins 0.000 description 2
- 108090001090 Lectins Proteins 0.000 description 2
- 102000004856 Lectins Human genes 0.000 description 2
- 101001043827 Mus musculus Interleukin-2 Proteins 0.000 description 2
- 208000018737 Parkinson disease Diseases 0.000 description 2
- 102100024216 Programmed cell death 1 ligand 1 Human genes 0.000 description 2
- 108010091086 Recombinases Proteins 0.000 description 2
- 102000018120 Recombinases Human genes 0.000 description 2
- 235000011449 Rosa Nutrition 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 230000003321 amplification Effects 0.000 description 2
- 230000006907 apoptotic process Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 210000003710 cerebral cortex Anatomy 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000009509 cortical damage Effects 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 108010048367 enhanced green fluorescent protein Proteins 0.000 description 2
- 238000001476 gene delivery Methods 0.000 description 2
- 238000012744 immunostaining Methods 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- 230000002779 inactivation Effects 0.000 description 2
- 230000008595 infiltration Effects 0.000 description 2
- 238000001764 infiltration Methods 0.000 description 2
- 230000004941 influx Effects 0.000 description 2
- 230000010354 integration Effects 0.000 description 2
- 239000002523 lectin Substances 0.000 description 2
- 210000004698 lymphocyte Anatomy 0.000 description 2
- 238000007431 microscopic evaluation Methods 0.000 description 2
- 230000004770 neurodegeneration Effects 0.000 description 2
- 230000002314 neuroinflammatory effect Effects 0.000 description 2
- 230000000926 neurological effect Effects 0.000 description 2
- 238000003199 nucleic acid amplification method Methods 0.000 description 2
- 210000004248 oligodendroglia Anatomy 0.000 description 2
- 230000007170 pathology Effects 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 230000002035 prolonged effect Effects 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 229960001603 tamoxifen Drugs 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 238000012549 training Methods 0.000 description 2
- 238000013518 transcription Methods 0.000 description 2
- 230000035897 transcription Effects 0.000 description 2
- 210000005166 vasculature Anatomy 0.000 description 2
- 210000003462 vein Anatomy 0.000 description 2
- 108020005345 3' Untranslated Regions Proteins 0.000 description 1
- WOVKYSAHUYNSMH-RRKCRQDMSA-N 5-bromodeoxyuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(Br)=C1 WOVKYSAHUYNSMH-RRKCRQDMSA-N 0.000 description 1
- 102100023990 60S ribosomal protein L17 Human genes 0.000 description 1
- 239000013607 AAV vector Substances 0.000 description 1
- 101150053137 AIF1 gene Proteins 0.000 description 1
- 241000702423 Adeno-associated virus - 2 Species 0.000 description 1
- 108700028369 Alleles Proteins 0.000 description 1
- 102100040121 Allograft inflammatory factor 1 Human genes 0.000 description 1
- 241001156002 Anthonomus pomorum Species 0.000 description 1
- 108010063104 Apoptosis Regulatory Proteins Proteins 0.000 description 1
- 102000010565 Apoptosis Regulatory Proteins Human genes 0.000 description 1
- 208000032116 Autoimmune Experimental Encephalomyelitis Diseases 0.000 description 1
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 102000008203 CTLA-4 Antigen Human genes 0.000 description 1
- 108010021064 CTLA-4 Antigen Proteins 0.000 description 1
- 108090000835 CX3C Chemokine Receptor 1 Proteins 0.000 description 1
- 102100039196 CX3C chemokine receptor 1 Human genes 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- 101100349093 Danio rerio nrp1a gene Proteins 0.000 description 1
- 108010046276 FLP recombinase Proteins 0.000 description 1
- 101150060333 GATA3 gene Proteins 0.000 description 1
- 101150057182 GFAP gene Proteins 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 208000009329 Graft vs Host Disease Diseases 0.000 description 1
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 1
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 1
- 108010068250 Herpes Simplex Virus Protein Vmw65 Proteins 0.000 description 1
- 102100026122 High affinity immunoglobulin gamma Fc receptor I Human genes 0.000 description 1
- 101000890626 Homo sapiens Allograft inflammatory factor 1 Proteins 0.000 description 1
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 description 1
- 101000913074 Homo sapiens High affinity immunoglobulin gamma Fc receptor I Proteins 0.000 description 1
- 101001046687 Homo sapiens Integrin alpha-E Proteins 0.000 description 1
- 101000971533 Homo sapiens Killer cell lectin-like receptor subfamily G member 1 Proteins 0.000 description 1
- 101001018097 Homo sapiens L-selectin Proteins 0.000 description 1
- 101000692455 Homo sapiens Platelet-derived growth factor receptor beta Proteins 0.000 description 1
- 102100026539 Induced myeloid leukemia cell differentiation protein Mcl-1 Human genes 0.000 description 1
- 102100022341 Integrin alpha-E Human genes 0.000 description 1
- 102000013691 Interleukin-17 Human genes 0.000 description 1
- 108050003558 Interleukin-17 Proteins 0.000 description 1
- 208000032382 Ischaemic stroke Diseases 0.000 description 1
- 102100021457 Killer cell lectin-like receptor subfamily G member 1 Human genes 0.000 description 1
- 102100033467 L-selectin Human genes 0.000 description 1
- 108091026898 Leader sequence (mRNA) Proteins 0.000 description 1
- 238000000585 Mann–Whitney U test Methods 0.000 description 1
- 241000283923 Marmota monax Species 0.000 description 1
- 108700027649 Mitogen-Activated Protein Kinase 3 Proteins 0.000 description 1
- 102100024192 Mitogen-activated protein kinase 3 Human genes 0.000 description 1
- 238000012347 Morris Water Maze Methods 0.000 description 1
- 208000028389 Nerve injury Diseases 0.000 description 1
- 101150082519 PLP1 gene Proteins 0.000 description 1
- 102100026547 Platelet-derived growth factor receptor beta Human genes 0.000 description 1
- 101710089372 Programmed cell death protein 1 Proteins 0.000 description 1
- 238000003559 RNA-seq method Methods 0.000 description 1
- 238000011529 RT qPCR Methods 0.000 description 1
- 101100224604 Schizosaccharomyces pombe (strain 972 / ATCC 24843) dri1 gene Proteins 0.000 description 1
- 241000700584 Simplexvirus Species 0.000 description 1
- 206010052779 Transplant rejections Diseases 0.000 description 1
- 230000001594 aberrant effect Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 238000011861 anti-inflammatory therapy Methods 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 210000001367 artery Anatomy 0.000 description 1
- 230000003140 astrocytic effect Effects 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- BPKIGYQJPYCAOW-FFJTTWKXSA-I calcium;potassium;disodium;(2s)-2-hydroxypropanoate;dichloride;dihydroxide;hydrate Chemical compound O.[OH-].[OH-].[Na+].[Na+].[Cl-].[Cl-].[K+].[Ca+2].C[C@H](O)C([O-])=O BPKIGYQJPYCAOW-FFJTTWKXSA-I 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 210000004970 cd4 cell Anatomy 0.000 description 1
- 238000002659 cell therapy Methods 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 230000001447 compensatory effect Effects 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 238000000942 confocal micrograph Methods 0.000 description 1
- 238000004624 confocal microscopy Methods 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 210000005257 cortical tissue Anatomy 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 235000015872 dietary supplement Nutrition 0.000 description 1
- 210000003162 effector t lymphocyte Anatomy 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 208000012997 experimental autoimmune encephalomyelitis Diseases 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 208000024908 graft versus host disease Diseases 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 230000007166 healthy aging Effects 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 230000000971 hippocampal effect Effects 0.000 description 1
- 210000001320 hippocampus Anatomy 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 238000003125 immunofluorescent labeling Methods 0.000 description 1
- 229960003444 immunosuppressant agent Drugs 0.000 description 1
- 230000001861 immunosuppressant effect Effects 0.000 description 1
- 229940125721 immunosuppressive agent Drugs 0.000 description 1
- 229940124589 immunosuppressive drug Drugs 0.000 description 1
- 238000002650 immunosuppressive therapy Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000012977 invasive surgical procedure Methods 0.000 description 1
- PGHMRUGBZOYCAA-UHFFFAOYSA-N ionomycin Natural products O1C(CC(O)C(C)C(O)C(C)C=CCC(C)CC(C)C(O)=CC(=O)C(C)CC(C)CC(CCC(O)=O)C)CCC1(C)C1OC(C)(C(C)O)CC1 PGHMRUGBZOYCAA-UHFFFAOYSA-N 0.000 description 1
- PGHMRUGBZOYCAA-ADZNBVRBSA-N ionomycin Chemical compound O1[C@H](C[C@H](O)[C@H](C)[C@H](O)[C@H](C)/C=C/C[C@@H](C)C[C@@H](C)C(/O)=C/C(=O)[C@@H](C)C[C@@H](C)C[C@@H](CCC(O)=O)C)CC[C@@]1(C)[C@@H]1O[C@](C)([C@@H](C)O)CC1 PGHMRUGBZOYCAA-ADZNBVRBSA-N 0.000 description 1
- 230000013016 learning Effects 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 230000001320 lysogenic effect Effects 0.000 description 1
- 230000002101 lytic effect Effects 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 101150094281 mcl1 gene Proteins 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 238000009126 molecular therapy Methods 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 230000008764 nerve damage Effects 0.000 description 1
- 230000007171 neuropathology Effects 0.000 description 1
- 230000000324 neuroprotective effect Effects 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 230000008488 polyadenylation Effects 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 230000001124 posttranscriptional effect Effects 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- NGVDGCNFYWLIFO-UHFFFAOYSA-N pyridoxal 5'-phosphate Chemical compound CC1=NC=C(COP(O)(O)=O)C(C=O)=C1O NGVDGCNFYWLIFO-UHFFFAOYSA-N 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000001172 regenerating effect Effects 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 230000008458 response to injury Effects 0.000 description 1
- 210000002955 secretory cell Anatomy 0.000 description 1
- 238000012163 sequencing technique Methods 0.000 description 1
- 238000012174 single-cell RNA sequencing Methods 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 108700020534 tetracycline resistance-encoding transposon repressor Proteins 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 230000017423 tissue regeneration Effects 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 238000003151 transfection method Methods 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 230000000472 traumatic effect Effects 0.000 description 1
- 230000007306 turnover Effects 0.000 description 1
- 230000031836 visual learning Effects 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
- 239000002676 xenobiotic agent Substances 0.000 description 1
- 230000002034 xenobiotic effect Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/17—Lymphocytes; B-cells; T-cells; Natural killer cells; Interferon-activated or cytokine-activated lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/54—Interleukins [IL]
- C07K14/55—IL-2
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/05—Animals comprising random inserted nucleic acids (transgenic)
- A01K2217/052—Animals comprising random inserted nucleic acids (transgenic) inducing gain of function
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/20—Animal model comprising regulated expression system
- A01K2217/206—Animal model comprising tissue-specific expression system, e.g. tissue specific expression of transgene, of Cre recombinase
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/10—Mammal
- A01K2227/105—Murine
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/035—Animal model for multifactorial diseases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
- A61K48/0058—Nucleic acids adapted for tissue specific expression, e.g. having tissue specific promoters as part of a contruct
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/008—Vector systems having a special element relevant for transcription cell type or tissue specific enhancer/promoter combination
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Biophysics (AREA)
- Wood Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Virology (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Toxicology (AREA)
- Microbiology (AREA)
- Plant Pathology (AREA)
- Physics & Mathematics (AREA)
- Developmental Biology & Embryology (AREA)
- Hematology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本发明涉及在受试者的组织或器官中扩增调节性T细胞群的方法,其中所述方法包括施用IL‑2以及所述组织或器官特异性的靶向部分,并且其中所述组织或器官是中枢和/或外周神经系统。本发明还涉及根据该方法产生的调节性T细胞群以及体内所述群的产生。还提供了包含IL‑2和如本文所定义的靶向部分的药物组合物,以及治疗由炎症介导的疾病或病症的方法或用于减轻炎症的方法,所述方法包括本文定义的方法或施用如本文所定义的药物组合物。
Description
发明领域
本发明涉及在受试者的组织或器官中扩增调节性T细胞群的方法,其中所述方法包括施用IL-2以及所述组织或器官特异性的靶向部分,并且其中所述组织或器官是中枢和/或外周神经系统。本发明还涉及根据该方法产生的调节性T细胞群以及体内所述群的产生。还提供了包含IL-2和如本文所定义的靶向部分的药物组合物,以及治疗由炎症介导的疾病或病症的方法或用于减轻炎症的方法,所述方法包括本文定义的方法或施用如本文所定义的药物组合物。
发明背景
神经炎症是多种神经炎性疾病中的致病过程。由于炎症的过程是众所周知的,在多种抗炎免疫抑制药物可用的情况下,原则上神经炎症应该是易处理的问题。阻止在神经炎性疾病中使用免疫抑制剂的关键问题是:1)血脑屏障,和2)脱靶免疫抑制的问题。实质上,足以抑制神经炎症的任何剂量的免疫抑制剂必须足够高以产生广泛的外周免疫抑制,因此在患者中是不可行的。
Avles等(2017)Brain和WO 2017/060510公开了阿尔茨海默病患者海马活检中IL-2水平降低,并描述了在阿尔茨海默病转基因小鼠模型中IL-2的全身递送驱动全身和脑调节性T细胞的扩增和激活。
Dashkoff等(2016)Molecular Therapy描述和表征了在星形胶质细胞或神经元启动子的控制下表达GFP的腺相关病毒。
Rouse等(2013)Immunobiology描述了在疾病发作之前递送时,全身性IL-2治疗在改善多发性硬化症(MS)小鼠模型中的病理学方面的有效性。
因此,非常需要炎性疾病或病症的有效治疗。
发明概述
根据本发明的第一个方面,提供了一种在有需要的受试者的组织或器官中扩增调节性T细胞群的方法,其中所述方法包括施用IL-2以及所述组织或器官特异性的靶向部分,并且其中所述组织或器官是中枢和/或外周神经系统。
根据本发明的另一个方面,提供了包含IL-2以及受试者的组织或器官特异性的靶向部分的药物组合物,其中所述靶向部分对中枢和/或外周神经系统是特异性的。
根据本发明的又一个方面,提供了一种治疗由炎症介导的疾病或病症和/或用于减轻炎症的方法,其中所述方法包括如本文所定义的方法或向有需要的受试者施用如本文所定义的药物组合物。
附图简述
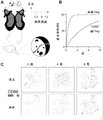
图1:调节性T细胞存在于健康小鼠脑的实质中。
A)代表性的共聚焦显微图像,其显示了位于小鼠脑实质、血管周围空间和血管内区域中使用CD4(第一列)和FoxP3(调节性T细胞的特异性标志物-第二列)免疫染色的调节性T细胞。荧光标记的凝集素用于标记脉管系统(第三列),并且细胞核用DAPI染色(第四列)。比例尺=20μm。
B)CD4+Foxp3+T细胞的实例的放大和3D重建。比例尺=10μm。
C)通过高维流式细胞术评估灌注的小鼠脑中的调节性T细胞。在健康衰老期间(第8、12、30和52周)对野生型小鼠取样。n分别为8、5、6和5。
图2:脑驻留调节性T细胞在延长的脑转运期间在原位获得驻留表型。
A)共生实验的示意图(n=12、12、18、16、14)。
B)血液和脑中CD4+Foxp3+调节性T细胞来源的最佳拟合曲线,显示了脑中的CD69+群。
C)在CD4+Foxp3-CD3+CD8-CD45+上门控的CD4+Foxp3+调节性T细胞的tSNE,建立在CD62L、CD44、CD103、CD69、CD25、PD-1、Nrp1、ICOS、KLRG1、ST2、Ki67、Helios、T-bet和CTLA4上。CD69表达以灰度显示。基于CD45.1相对于CD45.2表达来定义宿主和进入细胞(incomingcells),并在2、4和8周时间点显示。
D)CD4+Foxp3+调节性T细胞的CD69直方图。基于CD45.1相对于CD45.2表达来定义宿主和进入细胞,并在2、4和8周时间点显示。
E)处于稳态的CD4+Foxp3+调节性T细胞的群流程图。圆形区域表示群频率,针对血液和脑独立计算。小黑色圆圈表示细胞死亡。箭头末端的大小与群流动的速率成比例,如离开(向外箭头)或进入(向内箭头)。所有箭头末端的尺寸在每个图中相等地缩放,使得具有最高流动率(turnover)的群具有覆盖整个圆周的箭头(因此,这个群流动的图形表示是相同的,而与用于转运率的单位无关)。靠近每个箭头末端的数字显示相应的进入或离开速率,以事件/1000个细胞/天为单位。带有星号的数字表示具有高估计不确定性的比率。未显示两个末端速率低于0.1/1000个细胞/天的群转运。
图3:用于原理证明脑特异性调节性T细胞扩增的转基因小鼠模型。
A)Rosafl-Stop-fl IL-2等位基因含有floxed终止盒,在Cre活动后激活IL-2表达。使用CD4Cre驱动子,我们将转基因诱导的IL-2产生水平与内源性刺激诱导的IL-2减少水平进行比较。
B)和C)在该研究中测试的脑特异性启动子控制下的他莫昔芬(tamoxifen)诱导型Cre(CreERT2)的示意图:B)Plp1和C)CaMKII。
D)脑特异性IL-2产生对调节性T细胞群扩增增殖的影响。图比较了野生型、IL-2PIp1cre和IL-2aCaMKII Cre小鼠中血液和脑中的Treg(Foxp3+CD25+)扩增。
E)直方图显示CD4+细胞群中Foxp3+细胞的百分比。平均值±SEM(P值,单因素Anova)。
F)对来自野生型灌注的成年IL-2aCaMKII Cre小鼠脑的CD4 T细胞进行10×铬单细胞测序。tSNE可视化建立在组合群上的细胞簇。基于转录标志物的特征表达(底部),识别和标记幼稚CD4 T细胞、激活的CD4 T细胞和CD4+Foxp3+调节性T细胞的簇(顶部)。
G)IL-2aCaMKII Cre小鼠的常规T细胞和调节性T细胞之间所有表达的基因的倍数变化。
H)从鼠IL-2aCaMKII Cre脑纯化的CD4+T细胞中细胞因子的转录谱,通过10×单细胞管道进行分析。
I)至S)IL-2aCaMKII Cre(αCamkIIIL2)和对照小鼠的行为评估。I)在棒上的时间,300秒测试的4次重复的平均(n=23,17)。J)旷场,总移动距离和K)四角活动的时间(n=23,16)。L)筑巢评分(n=24,18)。M)进入明亮区域的明-暗测试延迟和N)在明亮区域中花费的时间(n=20,17)。O)强迫游泳实验期间不动的时间(n=24,16)。P)社交能力测试实验,以监测与陌生小鼠(S)的相互作用,与空箱(E)进行比较(n=28,18)。Q)情景获得条件化期间随时间的冻结行为(n=28,18)。平均值±SEM。R)泛化测试期间的情景辨别。平均值±SEM(n=28,18)。S)莫里斯水迷宫中的空间学习。找到隐藏站台的路径长度(n=16,8),5天和10天后以及逆向学习后的探查训练(n=28,20)。平均值±SEM。
图4:扩增的脑调节性T细胞保护免受创伤性脑损伤。
给予野生型同窝鼠和IL-2aCaMKII Cre(αCamKIIIL2)小鼠受控的皮质冲击以诱导中度创伤性脑损伤(TBI),并在TBI后15天进行检查。
A)损伤部位对脑表面的宏观损伤。
B)在同侧皮质损伤后15天,在IL-2aCaMKII Cre(αCamKIIIL2)或同窝对照小鼠的脑内捕获的代表性共聚焦图像。
C)受控皮质冲击手术后皮质组织的免疫荧光染色。GFAP(星形胶质细胞)、NeuN(神经元)、DAPI(细胞核)。比例尺=50μm。
D)损伤区域,显示为整个半球的百分比(n=3,3)。
图5:使用GFAP启动子的星形胶质细胞特异性表达。
A)GFAP启动子将TdTomato的表达限于成年小鼠脑中的星形胶质细胞,这是通过特征性细胞形态和通过星形胶质细胞特异性标志物GFAP和S100β的免疫染色来判断的。针对NeuN(神经元)、APC(少突胶质细胞)、IBA1(小胶质细胞)和PDGFRα(NG2+细胞)对切片进行复染时,未检测到脱靶表达。比例尺=20μm。数据是在来自接受GFAP-TdTomato构建体的3只独立小鼠的3个切片中观察到的代表性图像。
B)在创伤性脑损伤诱导后14天(TBI;n=5),在成年小鼠脑皮质和纹状体中的代表性染色(左)和GFAP量化表达(右),并进行量化。
图6:PHP.B-GFAP-IL2特异性扩增脑Treg并控制神经炎症。
A)从用PHP.B对照(PHP.B-GFP)或PHP.B-GFAP-IL2感染的C57BI6小鼠的脑分离的细胞的流式细胞术分析。
B)脑中的Treg(CD4+Foxp3+细胞)频率。数据显示为平均值±SEM(每组n=3)。
C)从用PHP.B对照(PHP.B-GFP)或PHP.B-GFAP-IL2感染的C57BI6小鼠的脾脏分离的细胞的流式细胞术分析。
D)脾脏中调节性T细胞的频率。数据显示为平均值±SEM(每组n=3)。
E)通过高维流式细胞术比较来自PHP.B-GFAP-GFP对照和PHP.B-GFAP-IL2处理的小鼠的血液、脾脏和灌注的小鼠脑的调节性T细胞数量。
F)通过尾静脉注射对野生型小鼠施用PHP.B-GFP对照载体或PHP.B-GFAP-IL2的109、1010或1011个载体基因组(总剂量),并在处理后14天评估灌注的脑中的常规(左)和调节性(右)T细胞的数量(每组n=3-5)。
G)用PHP.B-GFP对照或PHP.B-GFAP-IL2感染的C57BI6小鼠(109vg/小鼠)。用PHP.B感染后14天,用CFA中的MOG(35-55)免疫小鼠以诱导EAE。在EAE的第30天分离单核细胞。计算临床评分和累积临床评分的具有SEM的平均值。(n=15、14;平均值±SEM;P值,Mann-Whitney U检验)。
H)从CNS(脑和脊髓)分离细胞。顶行:显示了指示的脑浸润细胞的绝对数量或频率。底行:用PMA和离子霉素刺激源自CNS的细胞,以通过流式细胞术分析CD4或调节性T细胞中的IL-10、IL-17、GM-CSF和双调蛋白(AREG),符号描绘了单个小鼠。数据显示为平均值±SEM(每组n=6-7)。
I)与G)相同,但在诱导EAE后10天用PHP.B-GFAP-IL2或PHP.B-GFP对照处理的小鼠(由箭头指示)。发病率、每日临床评分(平均值±SEM)和累积平均临床评分(n=15、14)。
图7:PHP.B-GFAP-IL2保护免受创伤性脑损伤。
在受控皮质冲击前-14天,对小鼠以每只小鼠为PHP.B-GFAP-IL2或PHP.B对照(PHP.B-GFP)的1×109个载体基因组的1×剂量静脉注射小鼠,以诱导中度创伤性脑损伤(TBI)。在TBI后15天检查小鼠的脑。
A)在损伤部位对脑表面的宏观损伤。
B)在同侧皮质损伤后,在对照PHP.B-GFP、PHP.B-GFAP-IL2或假手术小鼠的脑内捕获的代表性共聚焦图像,显示了NeuN、BrdU和GFAP。
C)病变损失的面积、皮质和纹状体中相对Iba1表达以及皮质和纹状体中的GFAP表达的量化(同侧半球相对于对侧半球中的表达比率)。
D)在TBI后第1、7、14、35和150天,PHP.B-GFAP-GFP对照或PHP.B-GFAP-IL2处理的小鼠中病变大小的代表性MRI和基于MRI的量化(对照n=16、16、12、11、10;IL2 n=16、16、16、12、9)。
E)在探查训练期间在目标象限中花费的总时间的百分比。
F)在新型对象识别范式的第2天期间新对象与旧对象的探索时间的比率。
图8:创伤性脑损伤小鼠中PHP.B-GFAP-IL2处理后的正常外周流入。
给予在第-14天用PHP.B-GFAP-IL2或对照PHP.B-GFAP-GFP处理的小鼠受控的皮质冲击以诱导中度创伤性脑损伤(TBI),并在TBI后15天检查(n=3、4、4),对照PHP.B-GFAP-GFP组中包括一个假手术(sham)TBI。通过高维流式细胞术比较来自假手术、TBI和PHP.B-GFAP-IL2处理的TBI小鼠的TBI诱导的灌注脑。
A)小胶质细胞,在CD11b+CX3CR1+CD64+CD45mod Ly6G-细胞上门控,作为CD45+细胞的比例,或B)绝对数。
C)小胶质细胞上的MHCII表达。
D)CD4和CD8 T细胞的百分比,作为CD45+CD11b-TORβ+CD19-细胞的比例。
E)调节性T细胞(CD4+Foxp3+)的百分比,作为CD4 T细胞的比例。
F)CD25、CD44、CD69、Ki67和PDL1表达细胞的频率。
G)CD4常规T细胞群内产生双调蛋白的细胞的频率或H)CD4常规T细胞群内产生双调蛋白的细胞的平均荧光强度(MFI)。
I)CD25、CD44、CD69、Ki67和PDL1表达细胞的频率。
J)CD4常规T细胞群产生双调蛋白的细胞的频率或(K)CD4常规T细胞群内产生双调蛋白的细胞的平均表达。平均值±SEM。
图9:脑中调节性T细胞的扩增降低了中风的严重程度。
A)给予在第-14天用对照PHP.B-GFAP-GFP或PHP.B-GFAP-IL2处理的野生型小鼠(n=7、10)远端中动脉闭塞(dMCAO)中风,并在中风后15天检查宏观损伤,和B)基于TTC的损伤量化。
C)给予在第-14天用对照PHP.B-GFAP-GFP或PHP.B-GFAP-IL2处理的野生型小鼠(n=5、5)光血栓性中风,并在中风后一天检查宏观损伤,具有代表性图像和D)基于TTC的量化。
图10:用于脑特异性调节性T细胞扩增的小分子诱导系统。
通过尾静脉注射对野生型小鼠施用PHP.B-GFAP-GFP对照载体或PHP.B-GFAP-TetR-T2A-rtTA(V7/V14).TetO-IL2(PHP.GFAP/TetO-IL2)的109个载体基因组(总剂量)。每天用米诺霉素(minomycin)(50mg/kg)或PBS对照管饲小鼠(n=4-5只小鼠/组),然后在处理后14天评估脾脏或灌注脑中的Treg比例。
发明详述
根据本发明的第一个方面,提供了一种在有需要的受试者的组织或器官中扩增调节性T细胞群的方法,其中所述方法包括施用IL-2以及所述组织或器官特异性的靶向部分,并且其中所述组织或器官是中枢和/或外周神经系统。
在一个实施方案中,本文定义的方法包括扩增细胞群,如调节性T细胞群。在另外的实施方案中,所述细胞群如调节性T细胞群的扩增是在有需要的受试者的组织或器官,例如目标特定组织或器官中。
本文提及的术语“扩增(expanding)”、“扩增(expandation)”和“扩增的(expanded)”或短语“扩增调节性T细胞群”和“扩增的调节性T细胞群”包括提及比非扩增群更大的细胞群或包含比非扩增群更大数量细胞的细胞群。因此将认识到根据本文定义的方法产生的这种“扩增的”群包含比未经受IL-2的群更大数量的细胞。因此,在某些实施方案中,根据本文定义的方法产生的扩增的细胞群如扩增的调节性T细胞群与参考细胞群相比,包含更大数量的细胞。在一个实施方案中,参考细胞群可以是未经受或施用IL-2的细胞群。在一个实施方案中,根据本文定义的方法产生的扩增的细胞群,如扩增的调节性T细胞群,包含比IL-2的任何施用前的群更大数量的细胞。在另外的实施方案中,参考细胞群可以位于与根据本文定义的方法产生的扩增的细胞群不同的组织或器官中。在另外的实施方案中,根据本文定义的方法产生的扩增的细胞群如扩增的调节性T细胞群是受试者的组织或器官中扩增的群,并且与不位于所述目标组织或器官中的细胞群相比包含更大数量的细胞。在另外的实施方案中,根据本文定义的方法产生的扩增的细胞群,如扩增的调节性T细胞群,位于通过屏障(如血脑屏障)与其他组织或器官分离的组织或器官中,并且与不位于所述屏障分离的组织或器官中的细胞群相比包含更大数量的细胞。
在一个实施方案中,根据本文定义的方法产生的扩增的细胞群如扩增的调节性T细胞群包含比未经受或施用IL-2的细胞群大至少2倍、至少3倍、至少4倍、至少5倍、至少6倍、至少7倍、至少8倍、至少9倍、至少10倍、至少11倍、至少12倍、至少13倍、至少14倍或更多倍的群。在另外的实施方案中,根据本文定义的方法产生的扩增的细胞群如扩增的调节性T细胞群包含比不位于目标组织或器官中的细胞群大至少2倍、至少3倍、至少4倍、至少5倍、至少6倍、至少7倍、至少8倍、至少9倍、至少10倍、至少11倍、至少12倍、至少13倍、至少14倍或更多倍的群。在特定的实施方案中,根据本文定义的方法产生的扩增的细胞群比参考群如未经受或施用IL-2的目标组织或器官中的细胞群或不位于目标组织或器官中的细胞群大至少2倍、至少4倍、至少5倍、至少6倍、至少7倍、至少8倍、至少12倍、至少13倍或至少14倍。在一些实施方案中,根据本文定义的方法产生的扩增的细胞群如扩增的调节性T细胞群包含较大比例的构成群的子集的细胞(例如组织或器官中的T细胞总群内较大比例的调节性T细胞)。
因此,应认识到,如本文所定义的扩增的调节性T细胞群可以以依赖于施用的IL-2剂量的方式扩增。因此,在某些实施方案中,本文定义的扩增的调节性T细胞群体包含比参考群大IL-2剂量依赖性倍数的群。
在另外的实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群包含具有增加的存活率的细胞群。因此,在一个实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群包含增加的存活率。在另外的实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群包含减少的或降低的细胞死亡。在又一个实施方案中,扩增的调节性T细胞群包括增加的增殖。因此,在一个实施方案中,由于扩增的调节性T细胞群的存活率增加,根据本文定义的方法产生的扩增的调节性T细胞群大于参考群(例如,未经受或施用IL-2的调节性T细胞群或不位于目标组织或器官中的细胞群)。在另外的实施方案中,由于扩增的调节性T细胞群中减少的或降低的细胞死亡,根据本文定义的方法产生的扩增的调节性T细胞群大于参考群。在又一个实施方案中,由于增加的增殖,扩增的调节性T细胞群大于参考群。在仍另外的实施方案中,由于增加的存活率、减少/降低的细胞死亡和增加的增殖中的一种或多种的组合,根据本文定义的方法产生的扩增的调节性T细胞群大于参考群。
应认识到,本文提及根据本文定义的方法产生的“扩增的群”,如“扩增的调节性T细胞群”,还可以包括被激活的细胞群。本文提及的“扩增”可以包括根据本文定义的方法产生的细胞群如调节性T细胞群的激活。类似地,“扩增”还包括激活的调节性T细胞群的扩增,例如在施用IL-2前已经激活的群。根据本文定义的方法产生的细胞群(如调节性T细胞群)的这种激活可以独立于所述群的扩增,或者可以与所述群的扩增同时进行。因此,在一个实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群包含激活的调节性T细胞。在另外的实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群是激活的调节性T细胞群。
在替代的实施方案中,本文提及根据本文定义的方法产生的“扩增”或“扩增的群”不包括激活所述群或激活的细胞群。因此,根据这个实施方案,根据本文定义的方法产生的扩增的细胞群,如扩增的调节性T细胞群,不包含激活的表型。在另外的实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群不包含激活的调节性T细胞。因此,在又一个实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群包含尚未经受或施用IL-2的调节性T细胞群的表型,如表面表型。
调节性T细胞(也称为Treg)是调节免疫系统、维持耐受性和预防自身免疫疾病的T细胞亚群。它们通常抑制或下调效应T细胞的激活和/或增殖,并且已经显示在免疫抑制中具有效用。因此,调节性T细胞是组合多种免疫抑制和再生能力的高效能细胞,并且对使用外源调节性T细胞作为细胞疗法或使用刺激、激活或扩增内源性调节性T细胞的外源因子存在极大的兴趣。本发明的发明人已经证明了调节性T细胞存在于健康脑中(图1),尽管传统观点认为脑是与免疫系统分离的组织(例如,由于血脑屏障),并且因此可以是脑中免疫抑制治疗如抗炎治疗的有效靶标。
因此,在一个实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群包含增加的抗炎潜力。这种增加的抗炎潜力可以与非扩增的调节性T细胞群如存在于组织或器官中的非扩增的调节性T细胞群,或与存在于目标组织或器官之外的另一位置的调节性T细胞群进行比较。在一个实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群包含与目标组织或器官内的非扩增的调节性T细胞或来自目标组织或器官以外的位置的调节性T细胞类似的表型。此类表型可包括表面标志物表型、转录组表型/特征(例如基因表达特征)、基因和/或蛋白质表达谱和细胞因子表达谱。因此,在特定的实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群包含或保留非扩增的调节性T细胞群或扩增前扩增的调节性T细胞群的抗炎潜力。在另外的实施方案中,根据本文定义的方法产生的扩增的调节性T细胞群包含或保留来自目标组织或器官之外的另一位置的调节性T细胞群的抗炎潜力。
本文提及短语“在组织或器官中”是指受试者中的离散位置,如在特定组织或器官中。应认识到,这类术语不涉及其中全身性地或在目标组织或器官之外产生效果,或者其中不位于目标组织或器官中的细胞类型或细胞群受到影响(例如扩增或激活)。因此,在一个实施方案中,根据本文定义的方法产生的调节性T细胞群在特定的组织或器官中即局部受到影响(例如扩增)。在另外的实施方案中,根据本文定义的方法产生的调节性T细胞群仅在特定的组织或器官中受影响(例如扩增)。在又一个实施方案中,位于目标组织或器官之外或不在目标组织或器官中的调节性T细胞群不受影响(例如扩增)。因此,在特定的实施方案中,调节性T细胞的全身或外周群不受影响(例如扩增)。
本文定义的组织或器官包括身体或生物体的离散位置。例如,组织或器官可以包括身体的隔室,如神经系统(例如中枢或外周神经系统或脑)。在特定的实施方案中,组织或器官通过屏障如血脑屏障与其他组织或器官分离。因此,在一个实施方案中,组织或器官是中枢和/或外周神经系统。在另一个实施方案中,组织或器官是脑。
IL-2是调节性T细胞的关键群控制因子。与其他T细胞相比,调节性T细胞具有天然高的转换频率,具有快速增殖和高凋亡率。IL-2能够通过诱导抗凋亡蛋白Mcl1来提高调节性T细胞的频率,这进而降低了Bim依赖性凋亡率(Pierson等(2013),doi:https:// doi.orq/10.1038/ni.2649)。增加的IL-2水平因此可以扩大调节性T细胞群的大小(Liston和Gray(2014),doi:https://doi.org/10.1038/nri3605)。通过在多项临床前研究中扩增这种调节性T细胞群,IL-2递送已被证明是有效的抗炎剂,并且正在临床研究IL-2递送的优化。因此,在脑的情况下,对于IL-2作为抗炎介质的潜在用途,IL-2的全身性递送理论上应驱动脑中调节性T细胞数量的增加,原因在于这个群由循环中的调节性T细胞接种(seeded)(图2)。
然而,在实践中,通过提供IL-2的调节性T细胞的全身性扩增不成比例地增加了幼稚调节性T细胞群,其以低约10倍的效率水平接种脑(参见图2E)。因此,在外周中产生抗炎潜力实质性增加的全身性IL-2提供水平在脑中不产生调节性T细胞数量的显著增加。本文提供的这一发现表明了虽然IL-2具有作为脑中炎症如神经炎症的治疗剂的高潜力,但在加强脑调节性T细胞数量所需的生理范围内的全身性递送很可能诱导全身性免疫抑制。相比之下,调节性T细胞数量的脑特异性扩增或增加可以局部诱导调节性T细胞的抗炎性质,而没有全身免疫抑制的有害作用。
因此,根据本发明的某些实施方案,本文提供了在有需要的受试者的组织或器官中扩增调节性T细胞群的方法,其中组织或器官通过屏障如血脑屏障与其他组织或器官分离。因此,应认识到,本文定义的方法提供了组织或器官内调节性T细胞群的扩增,由于存在屏障如血脑屏障,这难以通过IL-2的全身性递送来实现。例如,由于所述屏障的存在,足以影响组织或器官中存在的细胞群的任何剂量的IL-2必须处于足够高的水平以产生广泛的外周或全身性作用。在使用如本文所述的IL-2在组织或器官中扩增调节性T细胞群的情况下,由于感染风险增加,所产生的广泛的外周或全身性免疫抑制对于患者来说是不可行的。
应认识到,本文提及的“施用”是指在生物体的离散位置或部位如特定的组织或器官提供IL-2或使IL-2可用。因此,这种施用将与本文先前所述的“在组织或器官中”的定义相似。因此,在一个实施方案中,IL-2的施用包括向特定组织或器官施用或在特定组织或器官中施用。在特定的实施方案中,IL-2的施用包括IL-2在特定组织或器官(例如脑或神经系统)中的表达。在一个实施方案中,施用包括在特定组织或器官(例如脑或神经系统)中编码IL-2的基因的表达。在另外的实施方案中,IL-2的表达在目标组织或器官之外如在外周中是不可检测的。在又一个实施方案中,IL-2的表达是限于目标特定组织或器官的表达。在另外的实施方案中,IL-2的表达是组织或器官特异性表达。在某些实施方案中,IL-2的施用或表达可以在多于一个目标组织或器官中进行。在一个实施方案中,IL-2的施用或表达在一个、两个或更多个相关组织或器官中(例如在脑和神经系统中或在肠道组织中)进行。在另一个实施方案中,IL-2的施用或表达是在一个、两个或更多个被认为不相关的组织或器官中进行。
此外,本文提及的“施用”和“表达”还指其中向组织或器官中的细胞群提供IL-2。在一个实施方案中,这种IL-2的提供可以包含将蛋白质或肽形式的IL-2施用于目标组织或器官或在目标组织或器官中施用,即,局部施用。在另外的实施方案中,IL-2的提供包含IL-2在目标组织或器官的细胞中的表达。因此,在特定的实施方案中,IL-2的表达包含表达IL-2的目标组织或器官的细胞如构成所述组织或器官的那些细胞(例如神经元)。在一些实施方案中,IL-2的表达包含神经元、少突胶质细胞和/或星形胶质细胞。在一个实施方案中,IL-2的表达包含星形胶质细胞。应认识到,通过星形胶质细胞的IL-2表达/在星形胶质细胞中的IL-2表达提供了若干优点:1)星形胶质细胞是跨脑广泛分布的有效的分泌细胞;2)星形胶质细胞在脊髓中有很好的代表性,提供了在脊髓中施用或表达IL-2的可能性;3)星形胶质细胞在神经炎症事件如创伤性脑损伤期间表现出时间和空间数值增加;和4)星形胶质细胞特异性启动子GFAP的表达响应损伤和疾病而上调(图5B)。在另外的实施方案中,IL-2的表达包括在构成根据本文定义的方法产生的调节性T细胞的扩增群的调节性T细胞以外的细胞中的表达。因此,在又一个实施方案中,IL-2的表达不在根据本文定义的方法产生的调节性T细胞群中。在一个实施方案中,IL-2的施用或表达包含从目标组织或器官的细胞的内源性IL-2编码基因的表达。根据这个实施方案,IL-2在组织或器官的细胞中的表达不包含外源序列的转染、转导或引入。因此,在一个实施方案中,IL-2在组织或器官的细胞中的表达包含使用仅在目标组织或器官的那些细胞中上调或“开启”编码IL-2的基因的表达的化合物的组织或器官特异性刺激。应认识到,根据这个实施方案,编码IL-2的内源性基因的表达的刺激是特异性的并且仅位于目标组织或器官。
在可替换的实施方案中,IL-2的施用或表达包含将编码IL-2的外源序列引入组织或器官的细胞中。因此,在一个实施方案中,IL-2的施用或表达包含外源序列的表达。在另外的实施方案中,IL-2的施用或表达包含转基因的表达。在又一个实施方案中,转基因包含编码IL-2的基因或元件。在特定的实施方案中,外源序列是IL-2编码序列。在另外的实施方案中,转基因包含IL-2编码序列或基因。
在一个实施方案中,编码IL-2的外源序列是包含组织或器官特异性启动子的转基因的形式。此类组织或器官特异性启动子是本领域已知的,并且包括驱动组织或器官特异性基因表达的启动子。在一个实施方案中,转基因包含组织或器官特异性启动子,其特异性地驱动目标组织或器官中的表达。在另外的实施方案中,转基因包含组织或器官特异性启动子,其不导致在目标组织或器官以外的组织或器官中表达。因此,在一个实施方案中,转基因包含驱动在神经元中特异性表达的启动子。在另外的实施方案中,转基因包含驱动在中枢和/或外周神经系统的细胞中特异性表达的启动子。在又一个实施方案中,转基因包含驱动在中枢神经系统中表达,但不驱动在外周神经系统中表达的启动子。在另一个实施方案中,转基因包含驱动在外周神经系统中表达,但不驱动在中枢神经系统中表达的启动子。在一个实施方案中,转基因包含驱动在脑中特异性表达的启动子。在特定的实施方案中,转基因包含驱动在星形胶质细胞中特异性表达的启动子。在另外的实施方案中,转基因包含GFAP启动子。在又一个实施方案中,转基因包含最小GFAP启动子。
在另外的实施方案中,IL-2的施用或表达包含转基因,所述转基因包含在外源化合物的存在下促进或诱导IL-2表达的元件。此类促进或诱导表达的元件是本领域已知的,并且包括例如四环素(Tet)诱导系统。Tet诱导系统提供转录的可逆控制并利用四环素控制的反式激活因子(tTA),其结合四环素操纵子(TetO)序列,所述四环素操纵子(TetO)序列包含在置于目标基因/编码区(及其启动子,如组织特异性启动子)上游的四环素应答元件(TRE)中。它们可以是TetOff或TetOn系统。诱导型表达的TetOff系统(也称为tTA依赖性系统)使用通过将大肠杆菌(Escherichia coli)细菌中发现的四环素阻遏物(TetR)与单纯疱疹病毒(Herpes Simplex Virus)中发现的另一种蛋白质VP16的激活结构域融合而产生的tTA蛋白。所得tTA能够在不存在四环素的情况下结合TRE内的TetO序列,并促进下游基因/编码区的表达。在四环素的存在下,tTA与TetO序列的结合被阻止,导致基因表达降低。相反,TetOn系统(也称为rtTA依赖性系统)使用反向Tet阻遏物(rTetR)来产生反向四环素控制的反式激活因子(rtTA)蛋白,其依赖于四环素的存在来促进表达。因此,rtTA仅与TRE内的TetO序列结合,并在四环素存在下促进表达。TetOn系统的具体实例包括但不限于LifeTechnologies的TetOn Advanced、TetOn 3G和T-REx系统。四环素的衍生物和类似物可以与TetOff或TetOn系统一起使用,并且包括但不限于多西环素(doxycycline)和米诺环素(minocycline)(例如米诺霉素(minomycin))。应认识到,与四环素相比,此类衍生物/类似物提供了显著的优点,如在多西环素的情况下增加的稳定性和/或在米诺环素的情况下穿过血脑屏障的能力(Chtarto等,2003,doi:https://doi.orq/10.1016/ i.neulet.2003.08.067)。因此,在某些实施方案中,编码IL-2的外源序列,如包含组织或器官特异性启动子的转基因,还包含四环素应答元件(TRE)。因此,在一个实施方案中,IL-2的施用或表达是四环素依赖性的或四环素诱导型的。在另外的实施方案中,IL-2的施用或表达包含将编码反向四环素控制的反式激活因子(rtTA)的外源序列引入组织或器官的细胞中。在一个实施方案中,编码rtTA的外源序列包含组织或器官特异性启动子,即rtTA编码序列的表达在如本文所公开的组织或器官特异性启动子的控制下。因此,在另外的实施方案中,编码rtTA的外源序列包含神经系统如中枢神经系统(例如脑)特异性启动子。在又一个实施方案中,rtTA编码序列的表达在神经系统例如中枢神经系统(例如脑)特异性启动子的控制下。在特定的实施方案中,编码rtTA的外源序列包含驱动在星形胶质细胞中特异性表达的启动子,如GFAP启动子或最小GFAP启动子。这种编码rtTA的外源序列可以是与编码IL-2的外源序列分开的序列,例如它可以与包含组织或器官特异性启动子的IL-2转基因分开。可替换地,这种编码rtTA的外源序列可以与IL-2编码序列包含在一起,例如它可以包含在相同的转基因中。因此,在一些实施方案中,IL-2的施用或表达包含TetOn系统。因此,应认识到,在一个实施方案中,IL-2的施用或表达包含施用四环素或四环素的衍生物/类似物,如多西环素或米诺环素。在特定的实施方案中,IL-2的施用或表达包含米诺环素的施用,例如米诺霉素的施用。
IL-2的四环素依赖性或四环素诱导型施用或表达的使用提供了另一控制水平,并允许IL-2的施用或表达“转换”开或关。通过允许在时间上控制的组织或器官中调节性T细胞群的扩增,将认识到这种转换在本文所述的方法中是有利的。例如,检测到/诊断出中枢和/或外周神经系统的炎症如神经炎症和/或脑部炎症)时,可以通过施用四环素或其衍生物/类似物来“开启”IL-2的表达。可替换地,IL-2的表达可以在脑部或头部急性损伤如创伤性脑损伤或中风后“开启”。然后,炎症如神经炎症不再被检测到或已经减轻时,可以通过除去四环素或其衍生物/类似物来“关闭”IL-2的表达。在认为受试者不再处于急性脑损伤如创伤性脑损伤或中风的风险之后,表达也可以被“关闭”。所述IL-2的四环素依赖性或四环素诱导型施用或表达的使用还提供了表达的剂量依赖性IL-2施用。例如,可以根据组织或器官中的炎症如神经炎症的水平和/或量来改变和/或滴定组织或器官中的IL-2施用或表达的水平和/或量。因此,检测到/诊断出中枢和/或外周神经系统的炎症如神经炎症和/或脑部炎症时,可以通过施用特定剂量的四环素或其衍生物/类似物来“开启”IL-2的表达,并且如果炎症持续存在,则可以增加所述剂量。类似地,如果在最初施用四环素或其衍生物/类似物后炎症减少,则可以减少所述剂量。
在另一个实施方案中,IL-2的施用或表达包含转基因,所述转基因包含阻止IL-2表达的元件。可以在目标组织或器官的细胞中去除和/或失活这种阻止表达的元件。在某些实施方案中,不去除或失活目标组织或器官的细胞外的细胞中防止表达的元件。因此,在一个实施方案中,在根据本文定义的方法产生的调节性T细胞群中不发生阻止表达的元件的去除或失活。在另外的实施方案中,阻止表达的元件是终止盒。在一个实施方案中,所述终止盒包含在本文定义的转基因中,并且位于编码IL-2的基因的上游。在另外的实施方案中,所述终止盒的两侧有重组酶识别的位点。这类重组酶包括Cre重组酶和Flp重组酶,并且能够分别识别和重组位点,如LoxP和FRT。所述位点的重组引起包含在它们之间的序列的去除、缺失和/或失活。因此,在一个实施方案中,终止盒两侧有LoxP重组位点。根据这个实施方案,目标组织或器官的细胞可以表达Cre重组酶,以便重组所述细胞中的重组位点。在特定的实施方案中,所述Cre重组酶的表达特异性定位于或仅定位于目标组织或器官的细胞中。Cre重组酶在目标组织或器官的细胞中的这种局部或特异性表达可以通过如本文所定义的方法使用组织或器官特异性启动子来驱动,或者可以通过本领域已知的任何其他方法来驱动。此类方法可包括Cre重组酶的组织或器官特异性递送和Cre重组酶编码序列的组织或器官特异性递送,如Cre重组酶编码mRNA或Cre重组酶编码转基因的组织或器官特异性递送。因此,在某些实施方案中,Cre重组酶的局部或特异性表达由组织或器官特异性启动子驱动。在一个实施方案中,Cre重组酶的局部或特异性表达由驱动神经元中的特异性表达的启动子来驱动。在另一个实施方案中,Cre重组酶的局部或特异性表达由驱动中枢和/或外周神经系统的细胞中的特异性表达的启动子来驱动。在又一个实施方案中,Cre重组酶的局部或特异性表达由驱动中枢神经系统中而不是外周神经系统中的表达的启动子来驱动。在另一个实施方案中,Cre重组酶的局部或特异性表达由驱动外周神经系统中而不是中枢神经系统中的表达的启动子来驱动。在一个实施方案中,Cre重组酶的局部或特异性表达由驱动脑中特异性表达的启动子来驱动。在一个具体实施方案中,Cre重组酶的局部或特异性表达由驱动星形胶质细胞中特异性表达的启动子来驱动。在另一个实施方案中,Cre重组酶的局部或特异性表达由PLP启动子来驱动。在另一个实施方案中,Cre重组酶的局部或特异性表达由CaMKIIa启动子来驱动。
应认识到,根据其中使用阻止在目标组织或器官外的细胞中表达的元件的实施方案,可不需要控制IL-2表达的组织或器官特异性启动子的存在。因此,在一个实施方案中,包含阻止在目标组织或器官的细胞外的细胞中表达的元件的转基因不包含组织或器官特异性启动子。在另一个实施方案中,包含阻止在目标组织或器官的细胞外的细胞中表达的元件的转基因还包含组织或器官特异性启动子。在这样的实施方案中,IL-2的表达将接受进一步的水平控制,以进一步确保组织或器官特异性施用或表达。
在一个实施方案中,通过转导如使用病毒或病毒载体的转导将如本文所定义的转基因引入目标组织或器官的细胞中。在特定的实施方案中,转导使用腺相关病毒。因此,在一个实施方案中,IL-2的施用包含转导,如病毒转导。在另一个实施方案中,IL-2的施用包含腺相关病毒转导。
在一个实施方案中,如本文所定义的转基因的转导利用特异性靶向或感染目标组织或器官的细胞的病毒载体。因此,在一个实施方案中,如本文所定义的转基因的转导特异性靶向或感染目标组织或器官的细胞。根据这个实施方案,应认识到,使用如本文所定义的转基因的病毒载体的转导不靶向或感染调节性T细胞群。在另外的实施方案中,如本文所定义的转基因的转导包含病毒载体,所述病毒载体能够接近目标组织或器官并且能够穿过将目标组织或器官与其他组织、器官或生物体的其余部分分开的屏障。因此,在一个实施方案中,转导包含能够特异性靶向或感染神经系统的病毒载体。在另外的实施方案中,转导包含能够靶向或感染中枢神经系统的病毒载体。在可替换的实施方案中,转导包含能够靶向或感染外周神经系统的病毒载体。在又一个实施方案中,转导包含能够靶向或感染脑的病毒载体。
在特定的实施方案中,转导包含能够穿过血脑屏障的病毒载体。在一个实施方案中,转导包含穿过血脑屏障的腺相关病毒。因此,在一个实施方案中,转导包含嗜神经病毒或病毒载体。在另一个实施方案中,病毒载体是嗜神经病毒或病毒载体。能够穿过血脑屏障的嗜神经病毒和病毒载体的实例包括但不限于AAVrh.8、AAVrh10和AAV9及其变体和衍生物(例如AAVhu68和PHP.B)。在某些实施方案中,如本文所定义的转基因包含在病毒载体,如嗜神经病毒或病毒载体和/或腺相关病毒载体中。在另外的实施方案中,转导包含腺相关病毒变体AAV9及其衍生物,如PHP.B。在又一个实施方案中,转导包含PHP.B病毒载体。在另一个实施方案中,如本文所定义的转基因包含在PHP.B病毒载体中。因此,在一个实施方案中,转导和/或病毒载体包含PHP.B-GFAP-IL2,其是包含转基因的AAV9的PHP.B衍生物,所述转基因含有IL-2编码序列和星形胶质细胞特异性启动子GFAP。病毒载体可用于将靶序列如转基因整合到宿主细胞基因组如目标组织或器官的细胞的基因组中。因此,在某些实施方案中,转导包含将如本文所定义的转基因整合到目标组织或器官的细胞的基因组中,使得实现转基因在组织或器官中的长期表达。病毒载体,如嗜神经病毒或病毒载体和腺相关病毒载体,也可用于实现稳定或长期表达,无需将靶序列整合到宿主细胞基因组中。因此,在一个实施方案中,转基因和/或靶序列稳定地维持在宿主细胞基因组外。
本文提及的“病毒”和/或“病毒载体”包括非裂解性或溶原性的病毒。应认识到,此类病毒用于实现细胞如目标组织或器官的细胞的感染,或将转基因引入细胞中而没有导致所述细胞的死亡或破坏。
从本文提供的公开内容应认识到,将特异性靶向或感染目标组织或器官的细胞的病毒或病毒载体(例如嗜神经病毒或病毒载体)和驱动在目标组织或器官的细胞中特异性表达的启动子的组合提供了卓越的特异性。这种特异性提供了所谓的“双锁”,限制了转基因靶向或感染的细胞和转基因在其中表达的细胞。因此,在一个实施方案中,如本文所定义的组织或器官特异性病毒载体和组织或器官特异性启动子的组合提供了仅目标组织或器官的那些细胞包含如本文所定义的转基因,并且仅目标组织或器官的那些细胞能够表达所述转基因。在另外的实施方案中,如本文所定义的组织或器官特异性病毒载体和组织或器官特异性启动子的组合提供了仅目标组织或器官的那些细胞包含IL-2编码基因,并且仅目标组织或器官的那些细胞能够表达所述基因。
在又一个实施方案中,如本文所定义的组织或器官特异性病毒载体和组织或器官特异性启动子与诱导元件如四环素诱导型元件的组合提供了施用诱导型元件的激活剂例如四环素、多西环素或米诺环素/米诺霉素时,仅目标组织或器官的那些细胞包含如本文所定义的转基因,并且仅目标组织或器官的那些细胞能够表达所述转基因。在一个实施方案中,如本文所定义的组织或器官特异性病毒载体和组织或器官特异性启动子与诱导型元件如四环素诱导型元件的组合提供了施用诱导型元件的激活剂例如四环素、多西环素或米诺环素/米诺霉素时,仅目标组织或器官的那些细胞包含IL-2编码基因,并且仅目标组织或器官的那些细胞能够表达所述基因。在另外的实施方案中,所述组合提供了仅目标组织或器官的那些细胞包含诱导型IL-2编码基因,并且仅目标组织或器官的那些细胞能够表达反向四环素控制的反式激活因子(rtTA),其在施用诱导型元件的激活剂例如四环素、多西环素或米诺环素/米诺霉素时引起IL-2的表达。
如本文所定义的IL-2的施用可以还包含将IL-2直接施用于目标组织或器官。直接施用的实例包括如通过颅内注射或利用合适的递送装置直接注射到目标组织或器官中。此类递送装置是本领域已知的,并且根据本公开内容,允许在治疗持续期间(例如长期地或在急性炎性疾病或病症的治疗持续期间)受控和/或持续的施用IL-2。
如本文所定义的IL-2施用的持续时间可以取决于通过本文所述方法治疗和待治疗的特定炎性病况或疾病的特征而改变。例如,IL-2的施用可以是慢性的。可替换地,IL-2的施用可以在疾病或病症的治疗如在急性炎性病况或创伤性损伤的治疗持续期间。因此,在某些实施方案中,IL-2的施用或表达的持续期间取决于待治疗的疾病或取决于病症或治疗的持续期间。在一个实施方案中,IL-2的施用或表达是急性的。
应认识到,IL-2以及组织或器官特异性的靶向部分可以组合或共同施用。因此,IL-2的施用可以包含IL-2在如本文所定义的目标组织或器官中的表达(例如组织或器官特异性表达),并且可以与受试者的组织或器官特异性的靶向部分组合。此外,IL-2的施用可以包括以蛋白质或肽形式施用IL-2,并且可以与受试者的组织或器官特异性的靶向部分组合。
本文提及的术语“靶向部分”是指提供如本文所定义的IL-2的组织或器官特异性施用或表达的任何部分。此外,应认识到,所述靶向部分用于提供如本文所定义的IL-2的局部施用或表达。
因此,在本发明的一个实施方案中,本文定义的方法包括施用受试者的组织或器官特异性的靶向部分。在另外的实施方案中,受试者的组织或器官特异性的靶向部分将IL-2定位在目标组织或器官中或定位至目标组织或器官。因此,在一个实施方案中,受试者的组织或器官特异性的靶向部分仅将IL-2定位在目标组织或器官中或定位至目标组织或器官。在另外的实施方案中,受试者的组织或器官特异性的靶向部分防止IL-2定位至目标组织或器官外的其他组织或器官,或将IL-2定位远离目标组织或器官外的组织或器官。在另一个实施方案中,靶向部分提供IL-2在目标组织或器官中的表达。因此,在一个实施方案中,受试者的组织或器官特异性的靶向部分提供仅在目标组织或器官中的IL-2的表达。本文对“在目标组织或器官中”的此类提及还包括其中所述效果在构成所述组织或器官的细胞(例如神经元和/或星形胶质细胞)中。
在一个实施方案中,受试者的组织或器官特异性的靶向部分是如本文所定义的病毒或病毒载体。在另外的实施方案中,所述病毒或病毒载体特异性地靶向或感染目标组织或器官,或特异性地靶向或感染目标组织或器官的细胞。因此,根据这个实施方案,所述目标组织或器官特异性的靶向部分是病毒或病毒载体,其不靶向或感染目标组织或器官外的其他组织或器官中的细胞,或者靶向或感染构成目标组织或器官外的其他组织或器官的细胞。还根据这个实施方案,应认识到,如本文所定义的所述组织或器官特异性的靶向部分不靶向或感染调节性T细胞群。在另外的实施方案中,如本文所定义的受试者的组织或器官特异性的靶向部分包含能够接近目标组织或器官并且能够穿过将目标组织或器官与受试者的其他组织、器官或其余部分分开的屏障的病毒或病毒载体。因此,在一个实施方案中,组织或器官特异性的靶向部分包含能够特异性地靶向或感染神经系统的病毒或病毒载体,如嗜神经病毒或病毒载体。在另外的实施方案中,组织或器官特异性的靶向部分包含能够靶向或感染中枢神经系统的病毒或病毒载体。在可替换的实施方案中,组织或器官特异性的靶向部分包含能够靶向或感染外周神经系统的病毒或病毒载体。
在特定的实施方案中,组织或器官特异性的靶向部分包含能够穿过血脑屏障的病毒或病毒载体。在一个实施方案中,组织或器官特异性的靶向部分包含穿过血脑屏障的腺相关病毒。因此,在某些实施方案中,组织或器官特异性的靶向部分包含嗜神经病毒或病毒载体。在一个实施方案中,靶向部分选自嗜神经病毒或病毒载体,如AAVrh.8、AAVrh10或AAV9以及变体和衍生物(例如AAVhu68和PHP.B)。在另外的实施方案中,组织或器官特异性的靶向部分包含腺相关病毒变体PHP.B。在某些实施方案中,如本文所定义的转基因包含在组织或器官特异性的靶向部分中,如腺相关病毒载体,其包含在如本文所定义的腺相关病毒内。在一个实施方案中,如本文所定义的转基因包含在嗜神经病毒或病毒载体,如PHP.B病毒载体中。因此,在另外的实施方案中,含有IL-2编码序列和星形胶质细胞特异性启动子、GFAP或最小GFAP的转基因包含在AAV9衍生物PHP.B病毒/病毒载体中,并且病毒/病毒载体是PHP.B-GFAP-IL2。
根据本发明的另外的方面,提供了一种用于在体内的组织或器官中扩增调节性T细胞群的方法。应认识到,本方面的实施方案为与本文先前描述的所有实施方案等同且相当。因此,在某些实施方案中,如本文所述的术语“受试者的”与“体内”同义。
在一个实施方案中,用于在体内的组织或器官中扩增调节性T细胞群的方法包括如本文所述的IL-2的施用。在另外的实施方案中,用于在体内的组织或器官中扩增调节性T细胞群的方法包括在体内施用受试者的组织或器官特异性的靶向部分。在一个实施方案中,IL-2的施用(其可包含IL-2的表达)与体内的组织或器官特异性的靶向部分组合。在另外的实施方案中,用于在体内的组织或器官中扩增调节性T细胞群的方法包括包含IL-2编码基因的病毒或病毒载体。在一个实施方案中,所述病毒或病毒载体能够靶向或感染目标组织或器官。在特定的实施方案中,所述能够靶向或感染目标组织或器官的病毒或病毒载体特异性地靶向或感染目标组织或器官的细胞。在另外的实施方案中,用于在体内的组织或器官中扩增调节性T细胞群的方法包括包含组织或器官特异性启动子的病毒或病毒载体。因此,在特定的实施方案中,用于在体内的组织或器官中扩增调节性T细胞群的方法包括施用目标组织或器官特异性的靶向部分,其中所述靶向部分是如本文所定义的穿过血脑屏障的病毒或病毒载体。在另外的实施方案中,用于在体内的组织或器官中扩增调节性T细胞群的方法包括施用目标组织或器官特异性的靶向部分,其中所述靶向部分对于神经系统如中枢和/或外周神经系统是特异性的。在又一个实施方案中,目标组织或器官特异性的靶向部分对于星形胶质细胞是特异性的。在另一个实施方案中,用于在体内的组织或器官中扩增调节性T细胞群的方法包括施用含有如本文所定义的转基因的嗜神经病毒或病毒载体,如施用PHP.B-GFAP-IL2。
根据本发明的一个方面,提供了根据本文所述的方法扩增或通过本文所述的方法获得的调节性T细胞群。因此,在一个实施方案中,提供了扩增的调节性T细胞群,其已通过施用IL-2以及所述组织或器官特异性的靶向部分在受试者的组织或器官中扩增。
药物组合物
根据本发明的一个方面,提供了包含IL-2以及受试者的组织或器官特异性的靶向部分的药物组合物,其中所述靶向部分对于中枢和/或外周神经系统是特异性的。
在一个实施方案中,药物组合物包含促进调节性T细胞群扩增的IL-2。在又一个实施方案中,药物组合物包含受试者的组织或器官特异性的靶向部分。在一个实施方案中,受试者的组织或器官特异性的靶向部分是病毒或病毒载体,其如本文所述特异性地靶向或感染组织或器官的细胞并驱动IL-2的组织或器官特异性表达。因此,根据本发明的这个方面,提供了包含组织或器官特异性病毒载体的药物组合物,所述病毒载体在受试者的所述组织或器官中扩增调节性T细胞群。在特定的实施方案中,药物组合物在受试者的目标组织或器官中特异性地或局部地扩增调节性T细胞群。
在一个实施方案中,如本文所定义的药物组合物包含能够穿过屏障的靶向部分,所述屏障将目标组织或器官与其他组织或器官或与生物体的其余部分分开。因此,在一个实施方案中,如本文所定义的药物组合物包含穿过血脑屏障的病毒或病毒载体,如腺相关病毒和/或嗜神经病毒或病毒载体。在另外的实施方案中,如本文所定义的药物组合物包含腺相关病毒变体AAV9或其衍生物,如PHP.B。在另外的实施方案中,包含在如本文所定义的药物组合物中的病毒载体包含编码IL-2的基因,如转基因。在又一个实施方案中,包含在药物组合物的病毒载体中的转基因还包含如本文所定义的组织或器官特异性启动子。
因此,在某些实施方案中,如本文所定义的药物组合物包含含有IL-2编码基因的能够靶向或感染目标组织或器官的细胞的组织或器官特异性病毒或病毒载体,其表达由组织或器官特异性启动子驱动。在一个特定的实施方案中,如本文所定义的药物组合物包含含有IL-2编码基因的病毒载体,如腺相关病毒(例如AAV9或其衍生物,如PHP.B),其特异性地靶向或感染神经元或神经系统,如脑(即嗜神经病毒或病毒载体),所述病毒载体表达由组织或器官特异性启动子驱动。在另外的实施方案中,如本文所定义的药物组合物包含腺相关病毒AAV9,其包含IL-2编码基因,其表达在神经元/星形胶质细胞中或在神经系统中由GFAP启动子或最小GFAP启动子局部驱动。在又一个实施方案中,腺相关病毒是AAV9的衍生物,如PHP.B。因此,在一个实施方案中,药物组合物包含PHP.B-GFAP-IL2。
根据一些实施方案,除了如本文所定义的组织或器官特异性病毒或病毒载体外,药物组合物还包含一种或多种药学上可接受的赋形剂。
通常,本发明的药物组合物将与药理学上合适的赋形剂或载剂一起使用。通常,这些赋形剂或载剂包括水性或醇/水性溶液、乳液或悬浮液,包括盐水和/或缓冲介质。肠胃外载体包括氯化钠溶液、林格氏(Ringer's)右旋糖、右旋糖和氯化钠以及乳酸林格氏液。如果需要将包含如本文所定义的组织或器官特异性的靶向部分的组合物保持在离散位置(例如在目标组织或器官内),合适的生理学上可接受的佐剂可以选自增稠剂,如羧甲基纤维素、聚乙烯吡咯烷酮、明胶和藻酸盐。静脉内载体包括流体和营养补充剂以及电解质补充剂,如基于林格氏右旋糖的那些。也可以存在防腐剂和其它添加剂,如抗菌剂、抗氧化剂、螯合剂和惰性气体(Mack(1982)Remington′s Pharmaceutical Sciences,第16版)。
治疗用途和方法
从本文提供的公开内容应认识到,本发明的扩增调节性T细胞群的方法、药物组合物和治疗方法将在治疗和/或改善由炎症介导的疾病或病症和/或在减轻炎症中发现特别有用。还应认识到,根据本文提供的方法和公开内容扩增的调节性T细胞群也将在治疗和/或改善由炎症介导的疾病或病症和/或在减轻炎症中发现有用。
因此,根据本发明的一个方面,提供了用于在受试者的组织或器官中扩增调节性T细胞群以用于治疗和/或改善由炎症介导的疾病或病症的方法,其中所述组织或器官是中枢和/或外周神经系统。在本发明的另一个方面,提供了用于在受试者的组织或器官中扩增调节性T细胞群以用于减轻炎症的方法,其中所述组织或器官是中枢和/或外周神经系统。在本发明的另外的方面中,提供了用于在受试者的组织或器官中扩增调节性T细胞群以用于治疗和/或改善自身免疫性疾病的方法,其中所述组织或器官是中枢和/或外周神经系统。
在本发明的另一个方面中,提供了根据本文定义的方法产生的受试者的组织或器官中扩增的调节性T细胞群,以用于治疗和/或改善由炎症介导的疾病或病症或用于减轻炎症。此类疾病或病症可以包括炎性病况、自身免疫性疾病和/或与移植相关的疾病,如移植排斥或移植物抗宿主病。在一个实施方案中,根据本文定义的方法产生的受试者的组织或器官中扩增的调节性T细胞群已经通过施用IL-2以及所述组织或器官特异性的靶向部分来扩增。在另外的实施方案中,根据本文定义的方法产生的受试者的组织或器官中扩增的调节性T细胞群已经通过如本文所定义的IL-2的组织或器官特异性表达来扩增。在另一个实施方案中,受试者的组织或器官中扩增的调节性T细胞群已经通过由诱导型元件如四环素诱导型元件促进或诱导的IL-2的组织或器官特异性表达来扩增。在又一个实施方案中,根据本文定义的方法产生的受试者的组织或器官中扩增的调节性T细胞群用于治疗和/或改善神经系统的疾病或病症。在一个实施方案中,根据本文定义的方法产生的受试者的组织或器官中扩增的调节性T细胞群用于治疗和/或改善中枢和/或外周神经系统。在又一个实施方案中,根据本文定义的方法产生的受试者的组织或器官中扩增的调节性T细胞群用于治疗和/或改善神经炎症。在某些实施方案中,根据本文定义的方法产生的受试者的组织或器官中的扩增的调节性T细胞群用于治疗和/或改善脑部炎症。因此,根据一个实施方案,如本文所定义的炎症是脑部炎症。在另外的实施方案中,脑部炎症是由于脑或头部的损伤引起的,如创伤性脑损伤或中风。在另一个实施方案中,根据本文定义的方法产生的受试者的组织或器官中的扩增的调节性T细胞群用于治疗和/或改善神经疾病或病症。因此,在一个实施方案中,脑部炎症是由于神经疾病或病症如创伤性神经疾病或病症引起的。在另一个实施方案中,根据本文定义的方法产生的受试者的组织或器官中扩增的调节性T细胞群用于治疗和/或改善认知障碍,如由神经炎症引起的认知障碍。在一个实施方案中,组织或器官中扩增的调节性T细胞群用于减轻认知障碍。在另外的实施方案中,脑部炎症是由于急性创伤性损伤、疾病或病症引起的。因此,在另外的实施方案中,神经疾病或病症是神经退行性疾病或病症以外的神经疾病或病症(即不是神经退行性疾病或病症),如阿尔茨海默病和/或帕金森病。另一个实例是自身免疫性疾病或病症和/或其中炎症是由于自身免疫疾病或病症引起的。
根据本发明另外的方面,提供了一种治疗由炎症介导的疾病或病症和/或用于减轻炎症的方法,其中所述方法包括如本文所定义的方法或向有需要的受试者施用包含IL-2以及如本文所定义的受试者的组织或器官特异性的靶向部分的药物组合物。在一个实施方案中,所述治疗方法包括向有需要的受试者施用包含如本文所定义的编码IL-2的基因的病毒或病毒载体。在一个实施方案中,如本文所定义的治疗方法包括向有需要的受试者施用病毒或病毒载体,所述病毒或病毒载体特异性地靶向或感染受疾病或病症影响的组织和器官,所述疾病和病症由炎症介导或受炎症影响。在某些实施方案中,如本文所定义的治疗方法还包括向有需要的受试者施用包含编码IL-2的基因的病毒或病毒载体,其表达由组织或器官特异性启动子驱动。在另外的实施方案中,如本文所定义的治疗方法包括向有需要的受试者施用包含编码IL-2的基因的病毒或病毒载体,其表达由组织或器官特异性启动子和诱导型元件如四环素诱导型元件驱动。在可替换的实施方案中,治疗方法包括向受试者施用包含编码IL-2的基因的病毒或病毒载体,其表达是在组织或器官特异性启动子控制下由诱导型元件如四环素诱导型元件驱动。在另外的实施方案中,如本文所定义的治疗方法包括向有需要的受试者施用包含编码IL-2的基因的嗜神经病毒,其表达由组织或器官特异性启动子驱动,如施用PHP.B-GFAP-IL2。
在某些实施方案中,所述有需要的受试者患有由炎症介导的疾病或病症。在另外的实施方案中,有需要的受试者患有炎症。在还另外的实施方案中,有需要的受试者患有自身免疫性疾病或病症。在一个实施方案中,所述疾病或病症是神经系统如中枢和/或外周神经系统的疾病或病症。在另外的实施方案中,所述疾病或病症是脑的疾病或病症。在还另外的实施方案中,所述疾病或病症是除神经退行性疾病或病症外的神经疾病或病症(即不是神经退行性疾病或病症),如阿尔茨海默病或帕金森病。在另一个实施方案中,所述炎症是神经炎症,如脑部炎症。在一个实施方案中,所述炎症是由于脑或头部损伤如创伤性脑损伤或中风引起的脑部炎症。因此,在一些实施方案中,所述炎症是由于急性创伤性损伤引起的脑部炎症。
实施例
实施例1:调节性T细胞存在于健康小鼠脑的实质中
为了研究脑(传统上认为与免疫系统分离的组织)中调节性T细胞的存在,制备来自小鼠脑实质、血管周围空间和血管内区域的组织用于共聚焦显微镜检查,以及针对CD4(T细胞的标志物)和FoxP3(调节性T细胞的特异性标志物)的免疫染色。这些组织进一步用荧光标记的凝集素染色以标记脉管系统,并用DAPI染色以识别细胞核。代表性图像显示于图1A中,并且放大倍数和3D重建显示于图1B中。图1C显示了通过流式细胞术确定的灌注的小鼠脑中调节性T细胞的数量。
从数据可以看出,通过显微镜和流式细胞术分析,可以容易地在健康小鼠的脑中识别调节性T细胞。根据所分析的小鼠的年龄,脑中可检测的调节性T细胞的数量范围为大约100个至超过2,000个细胞,大多数小鼠在脑中包含大约100-1,000个调节性T细胞。
实施例2:在延长的脑转运期间脑驻留调节性T细胞在原位获得驻留表型
进行异种共生实验以确定调节性T细胞是否从外周接种脑以及它们是否能够获得驻留样表型。使用CD45.1+和CD45.2+小鼠以及在第2、4、8和12周获取的每只小鼠的脑的样品建立异种共生对(图2A)。可以看出,可以在脑和血液中识别源自供体小鼠的CD69+和CD69-调节性T细胞(图2B)。测量源自供体小鼠的脑和血液中存在的调节性T细胞的比例(使用CD45.1或CD45.2表达确定),并确定其表型(图2C和2D)。
如数据以及从所述数据产生的群流图所证明的(图2E),调节性T细胞从外周接种脑,并且可以被检测为源自异种共生供体小鼠。脑中源自供体的调节性T细胞显示出组织驻留表型,表明这可以在脑转运期间获得。然而,数据证明了通过IL-2施用不成比例地增加的幼稚调节性T细胞群以比激活的调节性T细胞低约10倍的效率接种脑(图2E)。因此,需要在脑中特异性扩增调节性T细胞而不显著扩增外周调节性T细胞群。
实施例3:用于原理证明脑特异性调节性T细胞扩增的转基因小鼠模型
为了测试使用脑特异性IL-2递送在脑中特异性扩增调节性T细胞群的原理,开发了转基因小鼠模型。开发了Rosafl-Stop-flIL-2小鼠,其中IL-2表达在弱组成型启动子下以Cre活性开启。该系统中的表达比产生IL-2的细胞中的内源性表达每个细胞低约4倍(图3A)。因此,该系统通过改变表达的定位而不是过表达来操作。为了在脑中测试这个系统,使用两种脑特异性Cre系来诱导限制性表达,即PLP-Cre ERT(图3B)和CaMKIIa Cre ERT(图3C)。通过任一转基因的IL-2产生的激活扩增了脑中的调节性T细胞群(图3D和3E)。PLP-Cre导致外周的小幅增加,而CaMKIIa Cre不导致外周增加(图3D和3E)。因此,选择使用CaMKIIaCre驱动子用于后续实验。使用10x基因组学Chromium平台对脑CD4 T细胞进行单细胞RNA测序(RNA-seq)。来自IL-2aCaMKII Cre小鼠脑的扩增的脑调节性T细胞与来自野生型小鼠脑的(较小的)脑调节性T细胞群紧密聚集(图3F)。单细胞转录组学数据的分析揭示了IL-2aCAMKII Cre小鼠脑中的调节性T细胞表达已知标志物,如Ilr2、Gata3和Ikzf2,表明扩增对调节性T细胞群没有异常影响(图3G)。对表达的细胞因子的分析证明了来自这些扩增的调节性T细胞的仅高表达的细胞因子是Areg,一种低亲和力表皮生长因子受体(EGFR)配体,显示其参与伤口愈合和组织修复(Zaiss等(2015)doi:https://dos.org/10.1016/ i.immui.2015.01.020)(图3H)。脑调节性T细胞的扩增不导致IL-2aCamKII Cre(αCamKIIIL2)小鼠的不良行为变化(图3I-3S)。
这个数据证明了局部提供IL-2能够特异性扩增脑调节性T细胞群,而不扩增外周数量,并且扩增的调节性T细胞保留了其经典调节性T细胞表达谱。
实施例4:扩增的脑调节性T细胞保护免受创伤性脑损伤
为了确定脑特异性调节性T细胞扩增在减轻神经炎性损伤中的潜力,研究了由受控皮质冲击引起的中度创伤性脑损伤(TBI)的效果。给予IL-2aCaMKII Cre(αCaMKIIIL2)小鼠和同窝对照中度TBI并在TBI后15天检查。虽然野生型小鼠在皮质冲击部位表现出完全的皮质死亡并且没有神经元恢复的证据,但IL-2aCaMKII Cre小鼠证明了冲击部位的损伤大大减少,同侧海马体补偿性扩张,损伤大小减小并保留神经元组织(图4A-4D)。
这个数据证明了IL-2的局部递送可以产生局部抗炎环境,其能够预防神经病理学,而不增加全身调节性T细胞负荷。
实施例5:使用GFAP启动子的星形胶质细胞特异性表达
通过局部IL-2提供的功效的原理证明,开发了可用于治疗环境的递送系统。穿过血脑屏障(BBB)的腺相关病毒(AAV)是用于CNS治疗剂的快速通道施用的有力工具,因为它们允许递送编码大的生物活性分子的转基因而不需要侵入性手术程序。基于AAV的载体由于其转基因的长期表达和优异的安全性特征而成为临床试验中的首选系统。由于AAV代表了临床环境中IL-2递送至CNS的独特机会,因此使用了最近识别的AAV变体PHP.B,其已显示出能有效穿过BBB,在整个CNS中产生高水平的转导(Rincon等(2018)doi:https:// doi.org/10.1038/s41434-01B-0005-z)。这里主要关注的是IL-2在外周中的脱靶产生,因此AAV载体与GFAP启动子偶联,其仅在星形胶质细胞中产生持久和特异性的表达(图5A)。嗜神经病毒和脑特异性启动子的组合给出了对靶特异性的“双锁”,限制或消除了全身性递送后递送的靶标的外周表达。然后产生了如下携带在星形胶质细胞特异性GFAP启动子控制下的小鼠IL-2转基因(NG_06779.1)的AAV-PHP.B病毒(PHP.B-GFAP-IL2):
使用经典的三转染方法,随后使用基于qPCR的方法进行载体滴定(Rincon等(2018),doi:https://doi.org/10.1038/s41434-018-0005-z)。将小鼠IL-2编码序列与5'和3'UTR(登录号BC116845)一起克隆到源自单链AAV2的表达盒中,所述表达盒含有全长GFAP启动子(Brenner等(1994)doi:https://doi.org/10.1523/JNEURQSCI.14-03- 01030.1994)、土拨鼠肝炎转录后调控元件(WPRE)和牛生长激素聚腺苷酸化(bGH polyA)序列。通过将IL2编码序列交换为编码增强型绿色荧光蛋白(EGFP)的序列来制备对照载体。
这种治疗设计允许靶向递送在生理范围内表达的自身蛋白。WT小鼠中的PHP.B-GFAP-IL2注射成功地驱动调节性T细胞群的脑特异性扩增(图6A、6B和6E),而没有诱导外周扩增(图6C、6D和6E)。调节性T细胞群的脑特异性扩增也是PHP.B-GFAP-IL2剂量依赖性的(图6F)。
总之,这个数据提供了如本文所提供的“双锁”PHP.B介导的向脑的IL-2基因递送导致调节性T细胞的脑特异性扩增的证据。
与经典的基因治疗方法不同,其中用病毒载体进行细胞转导的效率是关键的,产生有效的分泌因子意味着即使少量的转导细胞也可以调节疾病。因此,选择PHP.B-GFAP-IL2的1×109个载体基因组的较低剂量来测试对实验性自身免疫性脑脊髓炎(EAE)(多发性硬化的金标准小鼠模型)的效果。未处理的小鼠发展为经典的EAE病理,具有严重的临床症状(图6G)和大量淋巴细胞浸润到脑中(图6H)。相比之下,PHP.B-GFAP-IL2预处理的小鼠对EAE具有抗性,疾病严重程度快速稳定和逆转(图6G),并且淋巴细胞浸润急剧减少(图6H)。潜在机制包括增加的AREG和IL-10表达(图6G)。
由于EAE的动力学适于测试治疗效果,因此在一组小鼠中诱导EAE,然后在临床表现发展后(第10天)用对照(PHP.B-GFAP-GFP)或“双锁”PHP.B-GFAP-IL2的1×109个载体基因组处理。引人注目的是,仍然观察到PHP.B-GFAP-IL2的保护作用,到第15天临床时程分开,且累积临床评分急剧降低(图6I)。
这个数据为IL-2的“双锁”基因递送到脑作为神经炎性疾病如多发性硬化的有效治疗提供了临床前证据。
实施例6:脑中调节性T细胞的扩增减少创伤性脑损伤损害
为了确定PHP.B-GFAP-IL2疗法在创伤性脑损伤期间减少进展或逆转损伤的潜力,在创伤性脑损伤之前,向小鼠施用PHP.B-GFAP-IL2或不含IL-2的对照PHP.B(PHP.B-GFAP-GFP)的1×109个载体基因组。
来自对照PHP.B处理的小鼠的脑的显微镜分析显示了在冲击部位对脑的主要表面损伤,而用PHP.B-GFAP-IL2处理显示了脑上冲击部位的大小显著减小(图7A)。组织学分析识别了撞击部位的大脑皮层的保留,其中BrdU掺入表明再生(图7B)。如组织学(图7B和7C)和MRI(图7D)所示,还观察到损伤后14天神经组织的损失减少。还在行为水平观察到神经保护作用,其中TBI后小鼠对行为测试的不良表现在PHP.B-GFAP-IL2处理的小鼠中被完全逆转(图7E和7F)。这些效果可能是通过改变局部环境介导的,观察到炎症流入的变化很小(图8)。
因此,这些数据显示IL-2的脑特异性施用和调节性T细胞扩增在创伤性脑损伤期间减少和/或逆转损伤中的效用。
实施例7:脑中调节性T细胞的扩增降低中风的严重程度
为了将上述发现扩展到第二种适应症,使用了两个独立的中风小鼠模型。在光照血栓中风(图9A和9B)和缺血性中风(图9C和9D)中,与对照(PHP.B-GFAP-GFP,均以1×109个载体基因组的剂量施用)相比,在用PHP.B-GFAP-IL2处理的小鼠中观察到严重程度的显著降低。
总之,本文提供的结果验证了“双锁”PHP.B-GFAP-IL2系统在几种独立的神经炎性疾病临床前模型中预防或治疗神经损伤而没有改变外周免疫的治疗潜力。
实施例8:用于脑特异性调节性T细胞扩增的小分子诱导系统
为了确定PHP.B-GFAP-IL2疗法的时间控制的潜力,向野生型小鼠施用PHP.B-GFAP-GFP对照载体或PHP.B-GFAP-TetR-T2A-rtTA(V7/V14).TetO-IL2(PHP.GFAP/TetO-IL2)的1×109个载体基因组(总剂量)。
PHP.B-GFAP/TetO-IL2载体包含IL-2编码基因上游的TetO序列,其与反向四环素控制的反式激活因子(rtTA)蛋白(在GFAP启动子的控制下表达)结合并在四环素如米诺环素/米诺霉素存在下促进表达。因此,每天用米诺霉素(50mg/kg)或PBS对照管饲小鼠(n=4-5只小鼠/组),并在处理后14天评估脾脏或灌注脑中Treg的比例。从图10中可以看出,向已经接受了PHP.GFAP/TetO-IL2载体的那些小鼠施用米诺霉素引起Treg在脑中的显著扩增,而在外周(脾)中没有扩增。
因此,这些数据显示了通过施用小分子由在星形胶质细胞中特异性表达的四环素诱导型元件控制的IL-2表达可用于特异性地增加脑中的调节性T细胞群,而没有增加外周中Treg的比例。
Claims (25)
1.一种在有需要的受试者的组织或器官中扩增调节性T细胞群的方法,其中所述方法包括施用IL-2以及所述组织或器官特异性的靶向部分,并且其中所述组织或器官是中枢和/或外周神经系统。
2.根据权利要求1所述的方法,其中所述组织或器官是脑。
3.根据权利要求1或权利要求2所述的方法,其中IL-2的施用包括IL-2在所述受试者的所述组织或器官中的组织或器官特异性表达。
4.根据权利要求3所述的方法,其中IL-2的组织或器官特异性表达由组织或器官特异性启动子驱动。
5.根据权利要求1至4任一项所述的方法,其中IL-2的施用或IL-2在所述组织或器官中的组织或器官特异性表达包含外源IL-2编码序列。
6.根据权利要求1至5任一项所述的方法,其中所述组织或器官特异性的靶向部分包含病毒载体。
7.根据权利要求6所述的方法,其中所述病毒载体是嗜神经病毒或病毒载体。
8.根据权利要求7所述的方法,其中嗜神经病毒或病毒载体是选自AAVrh.8、AAVrh10或AAV9及其变体和衍生物如AAVhu68和PHP.B的腺相关病毒。
9.根据权利要求8所述的方法,其中所述嗜神经病毒或病毒载体是腺相关病毒变体PHP.B。
10.根据权利要求1至9任一项所述的方法,其中所述组织或器官的特异性靶向部分或所述病毒载体穿过将所述组织或器官与所述受试者的其他组织或器官分开的屏障,如血脑屏障。
11.一种药物组合物,其包含IL-2和受试者的组织或器官特异性的靶向部分,其中所述靶向部分对于中枢和/或外周神经系统是特异性的。
12.根据权利要求11所述的药物组合物,其中所述组织或器官特异性的靶向部分包含病毒载体。
13.根据权利要求12所述的药物组合物,其中所述病毒载体是嗜神经病毒或病毒载体。
14.根据权利要求13所述的药物组合物,其中所述嗜神经病毒或病毒载体是选自AAVrh.8、AAVrh10或AAV9及其变体和衍生物如AAVhu68和PHP.B的腺相关病毒。
15.根据权利要求14所述的药物组合物,其中所述嗜神经病毒或病毒载体是腺相关病毒变体PHP.B。
16.根据权利要求11至15任一项所述的药物组合物,其中所述组织或器官特异性的靶向部分或所述病毒载体穿过将所述组织或器官与所述受试者的其他组织或器官分开的屏障,如血脑屏障。
17.根据权利要求11至16任一项所述的药物组合物,其用于治疗由炎症介导的疾病或病症和/或减轻炎症。
18.一种治疗由炎症介导的疾病或病症和/或用于减轻炎症的方法,其中所述方法包括根据权利要求1至10任一项所述的方法或向有需要的受试者施用根据权利要求11至16任一项所述的药物组合物。
19.根据权利要求17所述使用的药物组合物或根据权利要求18所述的方法,其中所述疾病或病症是神经障碍。
20.根据权利要求17所述使用的药物组合物或根据权利要求18所述的方法,其中所述疾病或病症是多发性硬化。
21.根据权利要求17所述使用的药物组合物或根据权利要求18所述的方法,其中炎症是中枢和/或外周神经系统的炎症,如神经炎症。
22.根据权利要求17或权利要求21所述使用的药物组合物或根据权利要求18或权利要求21所述的方法,其中所述炎症是脑部炎症。
23.根据权利要求17所述使用的药物组合物或根据权利要求18所述的方法,其中所述脑部炎症是由于脑或头部损伤,如创伤性脑损伤或中风引起的。
24.根据权利要求17所述使用的药物组合物或根据权利要求18所述的方法,其中所述脑部炎症是由于脑或头部的急性损伤,如急性创伤性损伤引起的。
25.根据权利要求17所述使用的药物组合物或根据权利要求18所述的方法,其中所述疾病或病症和/或炎症是自身免疫性疾病或病症和/或所述炎症是由于自身免疫引起的。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB1912863.6 | 2019-09-06 | ||
| GBGB1912863.6A GB201912863D0 (en) | 2019-09-06 | 2019-09-06 | Novel method |
| PCT/GB2020/052148 WO2021044175A1 (en) | 2019-09-06 | 2020-09-07 | Novel method |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN115397441A true CN115397441A (zh) | 2022-11-25 |
Family
ID=68241092
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202080077678.3A Pending CN115397441A (zh) | 2019-09-06 | 2020-09-07 | 新方法 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20220220180A1 (zh) |
| EP (1) | EP4025226A1 (zh) |
| JP (1) | JP2022548217A (zh) |
| KR (1) | KR20230035210A (zh) |
| CN (1) | CN115397441A (zh) |
| AU (1) | AU2020341114A1 (zh) |
| CA (1) | CA3153063A1 (zh) |
| GB (1) | GB201912863D0 (zh) |
| WO (1) | WO2021044175A1 (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB202118073D0 (en) | 2021-12-14 | 2022-01-26 | Babraham Inst | Novel method and composition comprising IL-2 and a tissue- or organ-specific targeting moiety |
| GB202202628D0 (en) | 2022-02-25 | 2022-04-13 | Babraham Inst | Novel use and method comprising IL-2 and a tissue- or organic-specific targeting moiety |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017060510A1 (en) * | 2015-10-09 | 2017-04-13 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical compositions for the treatment of alzheimer's disease |
-
2019
- 2019-09-06 GB GBGB1912863.6A patent/GB201912863D0/en not_active Ceased
-
2020
- 2020-09-07 KR KR1020227010908A patent/KR20230035210A/ko unknown
- 2020-09-07 CN CN202080077678.3A patent/CN115397441A/zh active Pending
- 2020-09-07 AU AU2020341114A patent/AU2020341114A1/en active Pending
- 2020-09-07 EP EP20771603.6A patent/EP4025226A1/en active Pending
- 2020-09-07 JP JP2022515060A patent/JP2022548217A/ja active Pending
- 2020-09-07 CA CA3153063A patent/CA3153063A1/en active Pending
- 2020-09-07 WO PCT/GB2020/052148 patent/WO2021044175A1/en unknown
-
2022
- 2022-03-04 US US17/653,554 patent/US20220220180A1/en active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017060510A1 (en) * | 2015-10-09 | 2017-04-13 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical compositions for the treatment of alzheimer's disease |
Non-Patent Citations (5)
| Title |
|---|
| FREDRIC P MANFREDSSON, AARON C RISING, RONALD J MANDEL: "AAV9: a potential blood-brain barrier buster", MOLECULAR THERAPY, vol. 17, no. 3, pages 403, XP055685538, DOI: 10.1038/mt.2009.15 * |
| HAIYUE ZHANG , YUGUO XIA , QING YE , FANG YU , WEN ZHU , PEIYING LI , ZHISHUO WEI , YUANYUAN YANG , YEJIE SHI , ANGUS W THOMSON , : "In Vivo Expansion of Regulatory T Cells with IL-2/IL-2 Antibody Complex Protects against Transient Ischemic Stroke", THE JOURNAL OF NEUROSCIENCE, vol. 38, no. 47, pages 10168 - 10179, XP055685447, DOI: 10.1523/JNEUROSCI.3411-17.2018 * |
| JODIE STEPHENSON, ERIK NUTMA, PAUL VAN DER VALK, SANDRA AMOR: "Inflammation in CNS neurodegenerative diseases", IMMUNOLOGY, vol. 154, no. 2, pages 204 - 219, XP055685535, DOI: 10.1111/imm.12922 * |
| MARK C JOHNSON, ALAINA L GARLAND, SARAH C NICOLSON, CHENGWEN LI, R JUDE SAMULSKI, BO WANG, ROLAND TISCH: "β-cell-specific IL-2 therapy increases islet Foxp3+Treg and suppresses type 1 diabetes in NOD mice", DIABETES, vol. 62, no. 11, pages 3775 - 3784, XP055685461, DOI: 10.2337/db13-0669 * |
| SUDHANSHU P RAIKWAR , RAMASAMY THANGAVEL , IULIIA DUBOVA , MOHAMMAD EJAZ AHMED , PUSHPAVATHI GOVINDHASAMY SELVAKUMAR , DURAISA: "Neuro-Immuno-Gene- and Genome-Editing-Therapy for Alzheimer\'s Disease: Are We There Yet?", JOURNAL OF ALZHEIMER\'S DISEASE, vol. 65, no. 2, pages 330 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022548217A (ja) | 2022-11-17 |
| AU2020341114A1 (en) | 2022-03-31 |
| EP4025226A1 (en) | 2022-07-13 |
| CA3153063A1 (en) | 2021-03-11 |
| KR20230035210A (ko) | 2023-03-13 |
| GB201912863D0 (en) | 2019-10-23 |
| WO2021044175A1 (en) | 2021-03-11 |
| US20220220180A1 (en) | 2022-07-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Spath et al. | Dysregulation of the cytokine GM-CSF induces spontaneous phagocyte invasion and immunopathology in the central nervous system | |
| US20220220180A1 (en) | Novel method | |
| Au et al. | Neuroinflammation, microglia and implications for retinal ganglion cell survival and axon regeneration in traumatic optic neuropathy | |
| Abdullah et al. | Targeted deletion of T‐cell S1P receptor 1 ameliorates cardiac fibrosis in streptozotocin‐induced diabetic mice | |
| US20220133910A1 (en) | Neuroprotection of neuronal soma and axon by modulating er stress/upr molecules | |
| WO2019183246A1 (en) | Compositions and methods of fas inhibition | |
| Tamura et al. | CRISPR activation rescues abnormalities in SCN2A haploinsufficiency-associated autism spectrum disorder | |
| Laird et al. | Rescue of rod synapses by induction of Cav Alpha 1F in the mature Cav1. 4 knock-out mouse retina | |
| JP6818358B2 (ja) | 神経系血管バリアーの機能回復剤及び神経系疾患治療剤 | |
| Özgür-Günes et al. | Long-term disease prevention with a gene therapy targeting oligodendrocytes in a mouse model of adrenomyeloneuropathy | |
| US20220395583A1 (en) | Compositions and methods for gene replacement | |
| Gonzalez et al. | Interleukin‐10 overexpression does not synergize with the neuroprotective action of RGD‐containing vectors after postnatal brain excitotoxicity but modulates the main inflammatory cell responses | |
| US20210214699A1 (en) | Methods and compositions for modulating myeloperoxidase (mpo) expression | |
| US9821026B2 (en) | Use of RET agonist molecules for haematopoietic stem cell expansion protocols and transplantation therapy and a RET agonist kit | |
| US20220339265A1 (en) | Modulation of ubiquitin carboxy-terminal hydrolase ligase 1 (uchl1) expression for treating neurological disease, disorders, and injuries associated with upper motor neurons | |
| US20240115737A1 (en) | Gene therapy for dopamine transporter deficiency syndrome | |
| Alvarez et al. | Treatment of monogenic and digenic dominant genetic hearing loss by CRISPR-Cas9 ribonucleoprotein delivery in vivo | |
| US20240050593A1 (en) | Compositions For and Methods of Enhancing Spinal Cord Tissue Regeneration | |
| WO2023161648A1 (en) | Novel use and method comprising il-2 and a tissue- or organ-specific targeting moiety | |
| US20210121539A1 (en) | Methods and compositions for modulating myeloperoxidase (mpo) expression | |
| Aimiuwu | Modeling Gene Therapy for Intractable Developmental and Epileptic Encephalopathy | |
| WO2023111560A1 (en) | Novel method and composition comprising il-2 and a tissue- or organ-specific targeting moiety | |
| De Winter et al. | Royal Netherlands Academy of Arts and Sciences (KNAW) | |
| Winter | Qui orna | |
| WO2023039395A1 (en) | Methods of treating neurodegenerative conditions and compositions therefor |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |