CN100445373C - 黄樟素氧化物在内皮细胞与神经干细胞培养体系中的应用 - Google Patents
黄樟素氧化物在内皮细胞与神经干细胞培养体系中的应用 Download PDFInfo
- Publication number
- CN100445373C CN100445373C CNB2006100705671A CN200610070567A CN100445373C CN 100445373 C CN100445373 C CN 100445373C CN B2006100705671 A CNB2006100705671 A CN B2006100705671A CN 200610070567 A CN200610070567 A CN 200610070567A CN 100445373 C CN100445373 C CN 100445373C
- Authority
- CN
- China
- Prior art keywords
- neural stem
- vascular endothelial
- stem cells
- endothelial cells
- cells
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- KZYXVVGEWCXONF-UHFFFAOYSA-N 5-(oxiran-2-ylmethyl)-1,3-benzodioxole Chemical compound C=1C=C2OCOC2=CC=1CC1CO1 KZYXVVGEWCXONF-UHFFFAOYSA-N 0.000 title claims abstract description 71
- 210000002569 neuron Anatomy 0.000 title abstract description 14
- 210000002889 endothelial cell Anatomy 0.000 title abstract description 12
- 238000012258 culturing Methods 0.000 title description 2
- 210000001178 neural stem cell Anatomy 0.000 claims abstract description 101
- 210000003556 vascular endothelial cell Anatomy 0.000 claims abstract description 83
- 230000006907 apoptotic process Effects 0.000 claims abstract description 41
- 238000003501 co-culture Methods 0.000 claims abstract description 26
- 238000013467 fragmentation Methods 0.000 claims abstract description 15
- 238000006062 fragmentation reaction Methods 0.000 claims abstract description 15
- 230000001939 inductive effect Effects 0.000 claims abstract description 11
- ZMQAAUBTXCXRIC-UHFFFAOYSA-N safrole Chemical compound C=CCC1=CC=C2OCOC2=C1 ZMQAAUBTXCXRIC-UHFFFAOYSA-N 0.000 claims description 12
- 230000004083 survival effect Effects 0.000 abstract description 15
- 230000001640 apoptogenic effect Effects 0.000 abstract description 12
- 230000004069 differentiation Effects 0.000 abstract description 8
- 238000000034 method Methods 0.000 abstract description 6
- 238000001727 in vivo Methods 0.000 abstract description 3
- 230000007246 mechanism Effects 0.000 abstract description 3
- 208000015122 neurodegenerative disease Diseases 0.000 abstract description 3
- 230000004770 neurodegeneration Effects 0.000 abstract description 2
- 210000004027 cell Anatomy 0.000 description 23
- 230000000694 effects Effects 0.000 description 13
- 108020004414 DNA Proteins 0.000 description 12
- 230000012010 growth Effects 0.000 description 10
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- 238000009833 condensation Methods 0.000 description 6
- 230000005494 condensation Effects 0.000 description 6
- 102000003855 L-lactate dehydrogenase Human genes 0.000 description 5
- 108700023483 L-lactate dehydrogenases Proteins 0.000 description 5
- 239000003814 drug Substances 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- HEMHJVSKTPXQMS-UHFFFAOYSA-M sodium hydroxide Inorganic materials [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 5
- 102000053171 Glial Fibrillary Acidic Human genes 0.000 description 4
- 101710193519 Glial fibrillary acidic protein Proteins 0.000 description 4
- 108091093105 Nuclear DNA Proteins 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 210000005046 glial fibrillary acidic protein Anatomy 0.000 description 4
- 239000001963 growth medium Substances 0.000 description 4
- 230000004660 morphological change Effects 0.000 description 4
- 210000004498 neuroglial cell Anatomy 0.000 description 4
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- 102000001435 Synapsin Human genes 0.000 description 3
- 108050009621 Synapsin Proteins 0.000 description 3
- 239000012531 culture fluid Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 230000007480 spreading Effects 0.000 description 3
- 210000000225 synapse Anatomy 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 102000019259 Succinate Dehydrogenase Human genes 0.000 description 2
- 108010012901 Succinate Dehydrogenase Proteins 0.000 description 2
- 210000001130 astrocyte Anatomy 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 210000004204 blood vessel Anatomy 0.000 description 2
- 230000030833 cell death Effects 0.000 description 2
- 238000010367 cloning Methods 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- -1 methylenedioxyphenyl Chemical group 0.000 description 2
- 230000017074 necrotic cell death Effects 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 238000010186 staining Methods 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- PGSPUKDWUHBDKJ-UHFFFAOYSA-N 6,7-dihydro-3h-purin-2-amine Chemical class C1NC(N)=NC2=C1NC=N2 PGSPUKDWUHBDKJ-UHFFFAOYSA-N 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 239000004593 Epoxy Chemical group 0.000 description 1
- 102100028652 Gamma-enolase Human genes 0.000 description 1
- 101710191797 Gamma-enolase Proteins 0.000 description 1
- 102000004157 Hydrolases Human genes 0.000 description 1
- 238000004566 IR spectroscopy Methods 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 102100023057 Neurofilament light polypeptide Human genes 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 102000012288 Phosphopyruvate Hydratase Human genes 0.000 description 1
- 108010022181 Phosphopyruvate Hydratase Proteins 0.000 description 1
- 102000004874 Synaptophysin Human genes 0.000 description 1
- 108090001076 Synaptophysin Proteins 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000003698 anagen phase Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 230000000711 cancerogenic effect Effects 0.000 description 1
- 231100000357 carcinogen Toxicity 0.000 description 1
- 239000003183 carcinogenic agent Substances 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 230000004528 endothelial cell apoptotic process Effects 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical class O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 210000003061 neural cell Anatomy 0.000 description 1
- 108010090677 neurofilament protein L Proteins 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 238000004626 scanning electron microscopy Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000004611 spectroscopical analysis Methods 0.000 description 1
- 210000000130 stem cell Anatomy 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 230000000946 synaptic effect Effects 0.000 description 1
- 238000012353 t test Methods 0.000 description 1
- 238000012549 training Methods 0.000 description 1
- 210000003606 umbilical vein Anatomy 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
Images
Landscapes
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
本发明公开了一种黄樟素氧化物作为诱导凋亡的工具在血管内皮细胞与神经干细胞培养体系中的应用。其中:所述黄樟素氧化物以浓度为70mg/L的量处理血管内皮细胞与神经干细胞的共培养体系,黄樟素氧化物表现为诱导血管内皮细胞凋亡,进而由凋亡的血管内皮细胞又诱导体系中的神经干细胞凋亡及DNA片段化。本发明以建立的内皮细胞与神经干细胞的共培养体系来模拟体内的微环境,以黄樟素氧化物作为诱导凋亡的工具,研究了培养体系中血管内皮细胞与神经干细胞的变化,开拓黄樟素氧化物的新用途,同时为研究体内血管内皮细胞维持神经干细胞存活及分化的机制提供方法,为今后治疗各种由于神经细胞缺失造成的神经退型性疾病提供实验基础和理论依据。
Description
技术领域
本发明涉及黄樟素氧化物的用途,尤其涉及黄樟素氧化物作为诱导凋亡的工具.在血管内皮细胞与神经干细胞培养体系中的应用。
背景技术
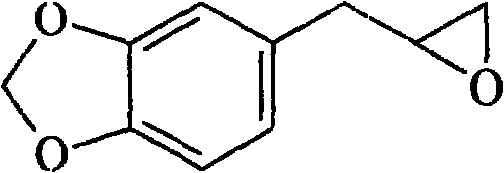
黄樟素氧化物结构式为:
分子式:C10H10O3
分子量:178,性状:浅黄色液体,沸点b.p.118℃/4mmHg,折光率n201.533。
黄樟素氧化物在40多年前已被合成出来。关于其应用的报道,始见于20世纪70年代,其用途多是将该化合物作为底物用于氧化物水解酶的光谱分析;20世纪80年代又发现黄樟素(微弱的致癌剂)在动物体内代谢时产生黄樟素氧化物。1995和1996年乔特(Qato)和根斯那(Guenthner)对黄樟素氧化物与DNA的结合性进行了研究(见《Toxicol Lett》1995,75(1-3):201-207和《Drug Metab Dispos》1996,24(9):1020-7),发现该化合物在体外能与DNA结合,并通过与DNA中的脱氧鸟核苷酸结合形成加合物,但在动物体内未检测到黄樟素氧化物与肝脏DNA之间该加合物的形成,进一步的研究证明黄樟素氧化物与DNA的结合为共价结合,除主要与鸟核苷酸结合外,它也能与DNA的其它3种碱基结合,其机制与黄樟素氧化物含有具生理活性的甲撑二氧苯基与环氧结构有关。
申请人已经发现,浓度为5~25mg/L的黄樟素氧化物能促进血管内皮细胞铺展和生长,而浓度为50~100mg/L的黄樟素氧化物则促进血管内皮细胞的脱壁和DNA片段化,最终诱导血管内皮细胞凋亡(见《Acta Pharmacologica Sinica》2002,23(4):323-326和专利号为:ZL 02110135.3的《黄樟素氧化物在血管内皮细胞生长与凋亡中的应用》专利)。
在机体内,神经干细胞并不是随意分布的,而是集中在血管附近,这就使神经干细胞与血管内皮细胞在空间上紧密相连,加强了两种细胞间的信息传递,形成了血管内皮细胞与神经干细胞组成的微环境,内皮细胞通过向微环境中释放各种细胞因子来维持神经干细胞的存活与分化。为了更好的研究内皮细胞与神经干细胞之间的相互作用,进而为治疗各种神经系统退型性疾病提供理论依据,在体外,人们通常以建立内皮细胞与神经干细胞的共培养体系来模拟体内的微环境。
与神经干细胞共培养的内皮细胞,可以维持神经干细胞存活并且诱导其分化,但是凋亡的内皮细胞对神经干细胞有何作用?经权威机构检索查新,目前国内外尚未见报道。
发明内容
针对现有技术的不足,本发明要解决的问题是以黄樟素氧化物作为诱导凋亡的工具影响血管内皮细胞与神经干细胞培养体系,研究黄樟素氧化物的影响作用以及培养体系中血管内皮细胞与神经干细胞的变化,开拓黄樟素氧化物的新用途。
本发明所述黄樟素氧化物作为诱导凋亡的工具在血管内皮细胞与神经干细胞培养体系中的应用。
其中:以浓度为70mg/L的黄樟素氧化物处理血管内皮细胞与神经干细胞的共培养体系,黄樟素氧化物表现为诱导血管内皮细胞凋亡,进而由黄樟素氧化物引起凋亡的血管内皮细胞又诱导在共培养体系中的神经干细胞凋亡及DNA片段化。
为了更好地理解本发明的实质,下面用黄樟素氧化物的药理实验及结果来说明其作为诱导凋亡的工具,在凋亡的血管内皮细胞与神经干细胞培养体系中的应用。
黄樟素氧化物的制备:将70%的间氯过氧化苯甲酸(27克,0.11摩尔)溶解在500毫升氯仿或苯中,加入黄樟素(黄樟素与间氯过氧化苯甲酸的摩尔比为1∶1.0~1∶1.5),在0-50℃搅拌2-24小时,用5%~9%碱液洗涤三次后,再水洗三次,用无水硫酸镁干燥,过滤后减压浓缩,剩余物进行减压蒸馏或用硅胶柱层析分离(展开剂为石油醚/乙酸乙酯=1∶1~3∶1,体积比),得到纯黄樟素氧化物,并经核磁共振及红外光谱验证后备用。其化学合成反应式如下:
血管内皮细胞的制备:以常规方法培养人脐静脉血管内皮细胞,选取生长状态良好的、且处于对数生长期的血管内皮细胞备用。
神经干细胞的制备:以常规方法提取培养小鼠神经干细胞,同样选取生长状态良好的,提取后6天的神经干细胞备用。
采用细胞生物学和分子生物学的方法,进行如下实验:研究黄樟素氧化物作为诱导凋亡的工具,在凋亡的血管内皮细胞与神经干细胞培养体系中的应用。
1、黄樟素氧化物对血管内皮细胞的作用
将血管内皮细胞接种于24孔板中,经黄樟素氧化物处理24小时后,光镜及荧光显微镜下直接观察血管内皮细胞形态变化。结果表明:浓度为50~100mg/L的黄樟素氧化物促进血管内皮细胞脱壁和DNA片段化,最终诱导血管内皮细胞凋亡,其最适作用浓度为70mg/L(见《Acta Pharmacologica Sinica》2002,23(4):323-326)(见附图1)。
2、黄樟素氧化物对神经干细胞的作用
(1)用MTT法检测神经干细胞琥珀酸脱氢酶的活性,以判断神经干细胞生长情况:
将神经干细胞接种于96孔培养板中,经黄樟素氧化物处理后加入5mg/ml的MTT溶液0.02ml,37℃孵箱内培养4小时,加入0.2ml三连液,37℃孵箱内培养5小时,振荡15分钟,用酶联免疫检测仪测定光密度(OD值),计算细胞相对存活率表明:处理组细胞存活率较正常对照组没有明显变化(见附图2)。
结果说明:浓度为10-100mg/L的黄樟素氧化物处理神经干细胞72小时,对神经干细胞存活没有影响,不能诱导神经干细胞死亡,细胞存活率无明显变化。
(2)倒置相差显微镜观察神经干细胞形态学变化:
以诱导血管内皮细胞凋亡用的最适作用浓度为70mg/L的黄樟素氧化物,处理神经干细胞72小时后,光镜下直接观察神经干细胞的形态学变化。
结果表明:神经干细胞形态没有发生明显变化,仍呈现克隆球状悬浮于培养液中(见附图3)。
以上实验说明,浓度为10-100mg/L黄樟素氧化物不能抑制小鼠神经干细胞生长,不诱导其凋亡。
3、黄樟素氧化物对血管内皮细胞与神经干细胞共培养体系的作用
(1)倒置相差显微镜观察血管内皮细胞与神经干细胞共培养体系中细胞形态学变化:
将神经干细胞与血管内皮细胞共培养3天后,光镜下直接观察,悬浮的神经干细胞全部贴于血管内皮细胞上,并且伸出细胞突触呈现神经元及神经胶质细胞状,克隆球与克隆球之间通过神经细胞突触形成网络状连接(见附图4)。
(2)神经细胞特异性标记物鉴定分化的神经干细胞:
激光共聚焦电子扫描显微镜观察与血管内皮细胞共培养后的神经干细胞,神经元特异性标记物NSE、NF-L及突触素呈现阳性;星形胶质细胞特异性标记物GFAP呈现阳性(见附图5)。
结果表明:共培养体系中,血管内皮细胞诱导神经干细胞分化为神经元及胶质细胞。
(3)黄樟素氧化物处理血管内皮细胞与神经干细胞的共培养体系:
将血管内皮细胞接种于24孔培养板中,培养两天后,将神经干细胞直接接种于血管内皮细胞上,以诱导血管内皮细胞凋亡用的最适作用浓度为70mg/L的黄樟素氧化物处理共培养体系。5小时后,倒置相差显微镜下观察到少量的神经干细胞伸出突触,开始分化;10小时后,血管内皮细胞凋亡,同时,已分化的神经细胞突触断裂消失,克隆球出现弥散状,克隆球的紧密结构解体,神经干细胞凋亡(见附图6)。
(4)荧光显微镜观察细胞核凝缩及核碎裂情况:
将血管内皮细胞与神经干细胞共培养,同时加入70mg/L黄樟素氧化物处理10小时,进行AO染色。血管内皮细胞大量凋亡,细胞核DNA发生大量的凝缩及碎裂。在荧光显微镜下选取神经干细胞所在的焦平面,观察神经干细胞细胞核DNA的凝缩及核碎裂情况。
结果显示:黄樟素氧化物处理血管内皮细胞与神经干细胞共培养体系后,神经干细胞核DNA发生大量的凝缩及碎裂(见附图7)。
(5)乳酸脱氢酶活性检测细胞坏死:
正常组:接触共培养血管内皮细胞和神经干细胞10小时。
实验组:70mg/L的黄樟素氧化物处理共培养体系10小时。
分别取两组细胞的培养液,用紫外分光光度计检测其乳酸脱氢酶活性,两组细胞培养液中乳酸脱氢酶活性没有明显差异,凋亡的血管内皮细胞没有引起神经干细胞坏死(见附图8注:&P>0.05vs.#)。
以上结果表明,70mg/L黄樟素氧化物处理血管内皮细胞与神经干细胞共培养体系10小时后,内皮细胞发生凋亡,继而神经干细胞发生凋亡及DNA片段化。
上述的实验数据统计学处理:
实验数据以平均值±标准误差表示,经t检验:P<0.05表示有明显差异。
归纳上述实验及其结果,可以看出:
将神经干细胞与血管内皮细胞共培养后,血管内皮细胞可以促进神经干细胞分化为神经元与神经胶质细胞。
向神经干细胞与血管内皮细胞共培养后的体系中加入浓度为70mg/L黄樟素氧化物,黄樟素氧化物表现为诱导血管内皮细胞凋亡,之后,神经干细胞也发生凋亡及DNA片段化。
前期实验已证实:浓度为10-100mg/L的黄樟素氧化物均不影响神经干细胞存活与生长,不能引起神经干细胞凋亡,因此,可以推断神经干细胞的凋亡是由于血管内皮细胞的凋亡引起的。
由此得出结论:以浓度为70mg/L的黄樟素氧化物处理血管内皮细胞与神经干细胞的共培养体系,血管内皮细胞被诱导凋亡,体系中的血管内皮细胞因凋亡不能维持神经干细胞的存活与分化,反而凋亡的血管内皮细胞诱导在共培养体系中的神经干细胞凋亡及DNA片段化。
机体内,神经干细胞总是集中于血管附近,在血管内皮细胞与神经干细胞组成的微环境中,血管内皮细胞通过释放各种细胞因子维持神经干细胞的存活,生长及分化。本发明以建立的内皮细胞与神经干细胞的共培养体系来模拟体内的微环境,以黄樟素氧化物作为诱导凋亡的工具,研究了培养体系中血管内皮细胞与神经干细胞的变化,开拓黄樟素氧化物的新用途,同时为研究体内血管内皮细胞维持神经干细胞存活及分化的机制提供方法,为今后治疗各种由于神经细胞缺失造成的神经退型性疾病提供实验基础和理论依据。
附图说明
图1是倒置相差显微镜下所示70mg/L黄樟素氧化物处理24小时后的血管内皮细胞。
其中:A为正常培养组;B为黄樟素氧化物处理组。
图2是MTT法检测细胞琥珀酸脱氢酶的活性,统计神经干细胞存活率。
图3是倒置相差显微镜下所示正常组与经70mg/L黄樟素氧化物处理72小时后的神经干细胞。
其中:A为正常培养组;B为黄樟素氧化物处理组。
图4是倒置相差显微镜下所示,血管内皮细胞诱导神经干细胞分化。
其中:A为正常单独培养的神经干细胞;B为神经干细胞与血管内皮细胞共培养0小时;C为共培养10小时;D为共培养24小时;E为共培养48小时;F为共培养72小时。
图5是分化的神经干细胞对神经细胞特异性标记物的表达。
其中:A为神经元特异性标记物-神经元特异型烯醇化酶(NSE);B为神经元特异性标记物-神经微丝蛋白(NF-L);C为神经元特异性标记物-突触素(synapsin);D为星型胶质细胞特异性标记物-胶质原纤维酸性蛋白(GFAP)。
图6是倒置相差显微镜下所示,凋亡的血管内皮细胞诱导神经干细胞凋亡。
其中:A为神经干细胞与血管内皮细胞正常共培养0小时;B为正常共培养5小时;C为正常共培养10小时;D为70mg/L黄樟素氧化物处理共培养体系0小时;E为黄樟素氧化物处理5小时;F为黄樟素氧化物处理10小时。
图7是荧光显微镜下所示正常组与70mg/L黄樟素氧化物处理共培养体系10小时后神经干细胞中核凝缩及核碎裂。
其中:A为共培养血管内皮细胞和神经干细胞10小时;B为70mg/L,黄樟素氧化物处理共培养体系10小时。
图8是乳酸脱氢酶活性检测。
其中:正常组为共培养血管内皮细胞和神经干细胞10小时:实验组为70mg/L黄樟素氧化物处理共培养体系10小时。
具体实施方式
实施例1黄樟素氧化物的合成
将含量为70%的间氯过氧化苯甲酸(27克,0.11摩尔)溶解在500毫升氯仿中,加入黄樟素(16.2克,0.10摩尔),25℃下搅拌20小时,用5%氢氧化钠水溶液洗涤三次(每次80毫升)后,再水洗三次(每次80毫升),用无水硫酸镁干燥,过滤后减压浓缩蒸出氯仿,剩余物进行减压蒸馏,b.p.118℃/4mmHg,得到纯黄樟素氧化物14克,收率为80%。
实施例2
将黄樟素氧化物配制成5mg/L、10mg/L、15mg/L、20mg/L、25mg/L、30mg/L、40mg/L、50mg/L、60mg/L、70mg/L、80mg/L、90mg/L、100mg/L等浓度,分别加入以常规方式培养的血管内皮细胞中,处理24小时,在倒置显微镜下每4小时观察一次细胞的变化,结果看到:5~25mg/L的药物浓度使血管内皮细胞贴在培养板上的能力增强,细胞铺展能力增强,生长旺盛;50~100mg/L的药物浓度处理血管内皮细胞时,随药物浓度的增加细胞不断地脱离培养板底面而漂浮于培养液中,然后细胞逐渐形成凋亡小体,即发生典型的细胞凋亡,24小时后仅有10%的细胞存活,而空白对照组此时的存活率为40%。说明黄樟素氧化物在5~25mg/L浓度时,有促进血管内皮细胞铺展和生长,抑制血管内皮细胞凋亡作用;而在50~100mg/L浓度时,有促进血管内皮细胞凋亡作用。
实施例3
将黄樟素氧化物配制成10mg/L、40mg/L、70mg/L、100mg/L浓度,分别加入以常规方式培养的神经干细胞中,处理72小时,在倒置显微镜下每12小时观察一次细胞的变化,结果看到:10~100mg/L的药物浓度均不能影响神经干细胞的生长。
将神经干细胞接种于96孔培养板中,经以上所配浓度黄樟素氧化物处理20h、44h、68h后加入5mg/ml的MTT溶液0.02ml,37℃孵箱内培养4小时,加入0.2ml三连液,37℃孵箱内培养5小时,振荡15分钟,用酶联免疫检测仪测定光密度(OD值),取各平行孔OD值的平均值,根据下式计算细胞相对存活率:存活细胞%=(实验组OD值/对照组OD值)×100%(以不含细胞的培养液为空白组调零)。
结果显示:黄樟素氧化物10-100mg/L浓度处理神经干细胞72小时,对神经干细胞存活没有影响,不能诱导神经干细胞死亡,细胞存活率无明显变化。
实施例4
将血管内皮细胞接种于24孔培养板中,培养两天后,待其形成单细胞层,将神经干细胞直接接种于血管内皮细胞上。培养3天后,光镜下直接观察。然后弃去培养液,用4%的多聚甲醛固定15分钟。用0.1M PBS清洗后,加入正常血清封闭液。弃封闭液,加一抗,弃一抗加二抗,37℃下30分钟,弃去二抗,用0.1M PBS清洗后观察。观察上述细胞是否表达NSE、NF-L、synapsin及GFAP。
结果显示:共培养体系中,血管内皮细胞可以诱导神经干细胞分化为神经元及胶质细胞。
实施例5
将血管内皮细胞接种于24孔培养板中,培养两天后,待其形成单细胞层,将神经干细胞直接接种于血管内皮细胞上,以诱导血管内皮细胞凋亡用的最适作用浓度为70mg/L的黄樟素氧化物处理共培养体系10小时,光镜下直接观察。
分别取两组细胞的培养液,用乳酸脱氢酶试剂盒检测其酶活性。
AO染色,在荧光显微镜下观察神经干细胞细胞核DNA的凝缩及核碎裂情况。
结果显示:70mg/L黄樟素氧化物诱导血管内皮细胞凋亡,凋亡的内皮细胞进而诱导神经干细胞凋亡。说明在黄樟素氧化物的作用下,体系中的血管内皮细胞因凋亡不能维持神经干细胞的存活与分化,反而诱导神经干细胞凋亡及DNA片段化。
Claims (2)
1、浓度为50~100mg/L的黄樟素氧化物作为诱导凋亡的工具在血管内皮细胞与神经干细胞培养体系中的应用。
2、如权利要求1所述的应用,其特征是:所述黄樟素氧化物以70mg/L的浓度量处理血管内皮细胞与神经干细胞的共培养体系,黄樟素氧化物表现为诱导血管内皮细胞凋亡,进而由黄樟素氧化物引起凋亡的血管内皮细胞又诱导在共培养体系中的神经干细胞凋亡及DNA片段化。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CNB2006100705671A CN100445373C (zh) | 2006-12-04 | 2006-12-04 | 黄樟素氧化物在内皮细胞与神经干细胞培养体系中的应用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CNB2006100705671A CN100445373C (zh) | 2006-12-04 | 2006-12-04 | 黄樟素氧化物在内皮细胞与神经干细胞培养体系中的应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1986782A CN1986782A (zh) | 2007-06-27 |
| CN100445373C true CN100445373C (zh) | 2008-12-24 |
Family
ID=38183726
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB2006100705671A Expired - Fee Related CN100445373C (zh) | 2006-12-04 | 2006-12-04 | 黄樟素氧化物在内皮细胞与神经干细胞培养体系中的应用 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN100445373C (zh) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1374081A (zh) * | 2002-03-26 | 2002-10-16 | 山东大学 | 黄樟素氧化物在血管内皮细胞生长与凋亡中的应用 |
| US20030203844A1 (en) * | 2001-09-19 | 2003-10-30 | Kioumars Delfani | Treatment of central nervous system disorders |
-
2006
- 2006-12-04 CN CNB2006100705671A patent/CN100445373C/zh not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030203844A1 (en) * | 2001-09-19 | 2003-10-30 | Kioumars Delfani | Treatment of central nervous system disorders |
| CN1374081A (zh) * | 2002-03-26 | 2002-10-16 | 山东大学 | 黄樟素氧化物在血管内皮细胞生长与凋亡中的应用 |
Non-Patent Citations (2)
| Title |
|---|
| Effect of safrole oxide on vascular endothelial cell growth andapoptosis induced by deprivation of fibroblast growth factor. Miao Jun-Ying et al.Acta Pharmacologica Sinica,Vol.23 No.4. 2002 |
| Effect of safrole oxide on vascular endothelial cell growth andapoptosis induced by deprivation of fibroblast growth factor. Miao Jun-Ying et al.Acta Pharmacologica Sinica,Vol.23 No.4. 2002 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1986782A (zh) | 2007-06-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2019023643A (ja) | ルテリアルの形態特性を用いた癌予防剤または抗癌剤のスクリーニング方法 | |
| Wang et al. | Environmental cadmium inhibits testicular testosterone synthesis via Parkin-dependent MFN1 degradation | |
| Jiang et al. | Pathway analysis of spermidine anti-oxidative stress and inducing autophagy in granulosa cells of Sichuan white geese | |
| CN105388294B (zh) | 线粒体三功能酶α亚基在制备AA005抑制脂质累积的药物靶标的应用 | |
| Farodoye et al. | Evidence of acrylamide-induced behavioral deficit, mitochondrial dysfunction and cell death in Drosophila melanogaster | |
| Zhao et al. | Inhibition of ROCK signaling pathway accelerates enteric neural crest cell‐based therapy after transplantation in a rat hypoganglionic model | |
| WO2024131981A1 (zh) | 粗糙凤尾蕨有效部位中单体化合物、制备方法、应用和药物 | |
| CN100445373C (zh) | 黄樟素氧化物在内皮细胞与神经干细胞培养体系中的应用 | |
| Zhuang et al. | Lipin1 ameliorates cognitive ability of diabetic encephalopathy via regulating Ca2+ transfer through mitochondria-associated endoplasmic reticulum membranes | |
| CN107115344B (zh) | 酪氨酸激酶抑制剂在制备用于预防和/或治疗纤维化疾病的药物中的用途 | |
| Mokady et al. | Small-molecule-directed endogenous regeneration of visual function in a mammalian retinal degeneration model | |
| Ko et al. | Perfluorooctanoic acid induces cardiac dysfunction in human induced pluripotent stem cell-derived cardiomyocytes | |
| Bahadur et al. | Antigiardial activity of novel triazolyl-quinolone-based chalcone derivatives: when oxygen makes the difference | |
| CN107496420A (zh) | 环匹阿尼酸类生物碱化合物的用途 | |
| US20250367238A1 (en) | Selected renal cell populations, characteristics and uses thereof | |
| Sun et al. | Polyoxyethylene tallow amine and glyphosate exert different developmental toxicities on human pluripotent stem cells-derived heart organoid model | |
| CN108398549A (zh) | 获得具有线粒体解偶联作用的药物的方法 | |
| WO2019071395A1 (zh) | 一种抗白色念珠菌的二芳基硫族化合物及其制备和应用 | |
| CN117243942A (zh) | 黄酮类衍生物cpu-008在制备胶质瘤治疗药物中的应用 | |
| CN101836993B (zh) | 2,3-二氢-3-羟甲基-6-氨基-[1,4]-苯并噁嗪在制备诱导胚胎干细胞向血管内皮细胞分化药物中的应用 | |
| Cui et al. | Naphthalene Metabolites From Long‐Term Environmental Tobacco Smoke Induce the Aging of Retinal Pigment Epithelium | |
| Chen et al. | Bilobalide activates autophagy and enhances the efficacy of bone marrow mesenchymal stem cells on spinal cord injury via upregulating FMRP to promote WNK1 mRNA decay | |
| Liu et al. | Establishment and characterization of two cell lines derived from primary cultures of Gekko japonicus cerebral cortex | |
| CN118924719B (zh) | 化合物1125-0440在制备btla抑制剂和肺癌治疗药物中的应用 | |
| Xu et al. | Preliminary Evaluation of Nanobacteria on Crystal Retention, CaSR, and Claudin‐14 Expression in HK‐2 Cells |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C17 | Cessation of patent right | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20081224 Termination date: 20111204 |