WO2004011429A1 - Novel haloalkylsulfonanilide derivatives, herbicides and usage thereof - Google Patents
Novel haloalkylsulfonanilide derivatives, herbicides and usage thereof Download PDFInfo
- Publication number
- WO2004011429A1 WO2004011429A1 PCT/JP2003/009405 JP0309405W WO2004011429A1 WO 2004011429 A1 WO2004011429 A1 WO 2004011429A1 JP 0309405 W JP0309405 W JP 0309405W WO 2004011429 A1 WO2004011429 A1 WO 2004011429A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- alkyl
- same
- factory
- different
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D249/00—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms
- C07D249/02—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D249/08—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
- C07D249/10—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D249/12—Oxygen or sulfur atoms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N41/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a sulfur atom bound to a hetero atom
- A01N41/02—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a sulfur atom bound to a hetero atom containing a sulfur-to-oxygen double bond
- A01N41/04—Sulfonic acids; Derivatives thereof
- A01N41/06—Sulfonic acid amides
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/50—1,3-Diazoles; Hydrogenated 1,3-diazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/58—1,2-Diazines; Hydrogenated 1,2-diazines
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/64—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with three nitrogen atoms as the only ring hetero atoms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/64—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with three nitrogen atoms as the only ring hetero atoms
- A01N43/647—Triazoles; Hydrogenated triazoles
- A01N43/653—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/74—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms five-membered rings with one nitrogen atom and either one oxygen atom or one sulfur atom in positions 1,3
- A01N43/78—1,3-Thiazoles; Hydrogenated 1,3-thiazoles
Definitions
- the present invention relates to a sulfonanilide derivative or a salt thereof, a herbicide containing the compound as an active ingredient, and a method for using the herbicide.
- dipheninoleether derivatives having a perfluoroalkylsulfonylamino group as a substituent have been known to be useful as herbicides or anti-inflammatory agents (for example, US Pat. No. No description or suggestion is made for skeletons other than diphenyl ether.
- perfluoroalkyl sulfonanilide derivatives having a phenoxy group, a phenylthio group, a phenylsulfonyl group or the like as substituents are useful as herbicides or anti-inflammatory agents (for example, see German Patent Application Publication No.
- a perrea derivative having a trifluoromethanesulfonylamino group as a substituent is useful as a herbicide (for example, see JP-A-60-87254). It is known that pyrazine derivatives having a trifluoromethanesulfonylamino group are useful as herbicides (see, for example, US Pat. No. 4,345,076).
- the haloalkyl sulfonanilide derivative represented by the general formula (I) of the present invention is neither described nor suggested, and the haloalkyl sulfonyl derivative represented by the general formula (I) of the present invention is not described.
- a sulfonanilide derivative having a 2-pyrimidinyloxy group at the 4-position and a herbicide containing the compound as an active ingredient are known. See Japanese Unexamined Patent Publication No. Hei 8—1931011 or Japanese Unexamined Patent Publication No. Hei 8-292911. It is described that rice has no phytotoxicity and its applicability to paddy fields, but the skeleton is different from that of the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention. There is no particular description or suggestion about this.
- sulfonanilide derivatives having a pyrimidinyloxy group at the 2-position useful as herbicides for example, International Publication No. 93Z0909 pamphlet, International Publication No.
- a sulfonanilide derivative compound useful as a herbicide having an aminomethylene group or an iminomethylene group in the bond between the 2-position of pyrimidine and the 2-position of aniline see, for example, Japanese Patent Application Laid-Open No. 2-1495677). Japanese Patent Application Laid-Open No.
- a trifluoromethanesulfonanilide derivative having a pyrimidinyl group at the 2-position and an alkoxyalkyl group at the 6-position is used for paddy fields with low toxicity to mammals. It is useful as a herbicide (for example, see Japanese Patent Application Laid-Open No. 2000-633600), and difluoromethanesulfur having a dimethoxypyrimidinylhydroxymethyl group at the 2-position.
- An anilide derivative is known as a herbicide having selectivity for rice (see, for example, JP-A-2000-44546). Both of these compounds have a dimethoxypyrimidinyl group or the like.
- haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention a nodroalkylsulfonanilide and a heterocycle are bonded via an alkylene group or the like.
- the compound having the skeleton is not described or suggested. Also, their workability as herbicides is different.
- a sulfonanilide derivative is a novel compound that has not been described in the literature. It has wide applicability to species, long-lasting effect, and excellent properties such as selectivity between crops and weeds, and has been found to be useful as a herbicide, particularly as a paddy field herbicide, and completed the present invention. Things. Disclosure of the invention
- the present invention provides a compound of the general formula (I):
- R 1 represents a halo (C Factory C 6 ) alkyl group.
- R 2 is a hydrogen atom, a (C 6 C) alkyl group, a (CC 6 ) alkoxy (CfC 6 ) alkyl group, a (-C 6 ) alkyl carbonyl group, a nodro (() alkylcarbonyl group, a phenylcarbonyl group A substituted phenylcarbonyl group having at least one substituent selected from Y (Y is shown below), (-c 6 ) alkoxycaponyl group, phenoxycarbonyl group May be the same or different, and a substituted phenyloxycarbonyl group having at least one substituent selected from ⁇ ( ⁇ is described below), (C Factory C 6 ) alkylsulfonyl group, phenol (C Factory C 6 ) represents an alkylsulfonyl group, a phenylsulfonyl group or a substituted phenylsulfonyl group which may be the same or different and has one or more substituent
- Q represents an optionally substituted heterocycle in which at least one of the constituent atoms is a nitrogen atom, and the nitrogen atom is a bonding site with A.
- A is a (Cf C 6 ) alkylene group, which may be the same or different, and is selected from a halogen atom, a hydroxyl group, a (C Factory C 6 ) alkoxy group, a (C-Cs) alkoxycarbonyl group or a cyano group 1 or more substitutions having substituent (c r c 6) alkylene group, (c 2 - c 6)
- Aruke two alkylene groups, the same or different and a halogen atom, a hydroxyl group, (C ⁇ c 6) an alkoxy group shows the - (c 6 c 2) alkenylene or (c 2 -c 6) alkynylene group (Cr) alkoxycarbonyl group or substituted with one or more location substituent selected from Shiano group.
- G is an oxygen atom, a sulfur atom, N—R 3 (where R 3 is a hydrogen atom, an alkyl group of. (C Factory C 6 ), a cyano group, a nitro group, a phenyl (C Factory C 6 ) alkyl group, the same or A substituted phenyl (C-wide C 6 ) alkyl group having at least one substituent selected from Y (Y will be described below) on the ring, a phenyl group, or the same or different; Y represents a substituted phenyl group having at least one substituent selected from the following.), N—OR 4 (wherein, is a hydrogen atom, a (C r C 6 ) alkyl group, phenyl) (c r c 6 ) alkyl group or the same or different, and Y (Y is shown below) You.
- R 5 and R 6 may be the same or different, may be a hydrogen atom, a phenyl group or the same or different, and are selected from Y (Y is shown below.) And R 5 and R 6 may be taken together to represent a (C 3 -C 6 ) alkylene group.
- n an integer of 0 or 1.
- X may be the same or different; a hydrogen atom, a halogen atom, a (C 2 C 6 ) alkyl group, a (C 2 -C 6 ) alkenyl group, a (C 2 -C 6 ) alkynyl group, a cyclo (C 3 -C 6 ) Alkyl group, Noro (C Factory C 6 ) alkyl group, cycloha (C 3 -C 6 ) alkyl group, (C Factory C 6 ) alkoxy group, halo (C Factory C 6 ) alkoxy group, (-C 6) alkylthio groups, halo (C ⁇ c 6) alkylthio groups, (C ⁇ C 6) alkylsulfinyl group, Nono port (C ⁇ c 6) alkylsulfinyl group, (c r c 6) alkylsulfonyl group, /, mouth (C factory c 6 ) alkylsulfony
- Substituted phenyl having at least one substituent selected from (Cfc 6 ) represents 1 to 4 substituents selected from an alkylaminocarbonyl group, a hydroxyl group, an amino group, a cyano group and a nitro group.
- Y may be the same or different, a halogen atom, (C t -C 6) alkyl group, (C 2 - C 6) ⁇ alkenyl group, (c 2 - C 6) alkynyl group, consequent opening (C 3 - C 6) alkyl group, halo (C ⁇ c 6) Al kill group, Shikuroha port (C 3 - C 6) alkyl groups, (C ⁇ C 6) alkoxy groups, halo (C ⁇ C 6) alkoxy groups, (C Factory C 6 ) alkylthio group, halo (-C 6 ) alkylthio group, (CFactory c 6 ) alkinolesulfinyl group, nodro (C r C 6 ) alkylsulfinyl group, (CFactory c 6 ) alkylsulfonyl group, Halo (C factory c 6 ) alkylsulfonyl group, phenyl group
- C Factory 6 Substituted phenyl having 1 to 5 substituents on the ring selected from an alkylaminocarbonyl group, a hydroxyl group, an amino group, a cyano group or a nitro group.
- Rua amino carbonyl group phenyl (C ⁇ c 6) alkyl ⁇ Mino Cal Group, which may be identical or different, halogen atom, (C ⁇ C 6) alkyl groups, (C 2 - C 6) alkenyl, (C 2 - C 6) alkynyl, cyclo (C 3 - C 6) Alkyl group, halo (C factory c 6 ) alkyl group, cycloha (C 3 -C 6 ) alkyl group, (C factory c 6 ) alkoxy group, halo (c r c 6 ) alkoxy group, (( ⁇ -C 6) alkylthio group, Bruno, mouth (C, - C B) alkylthio groups, (C -!) alkyl sulfide group, Nono b (CC 6) alkylsulfinyl group, (C ⁇ c e) an alkylsulfonyl group, Nodro (d-C 6
- Y may be the same as or different from adjacent carbon atoms on the benzene ring, and may be an oxygen atom, a sulfur atom, or a nitrogen atom (the nitrogen atom is a hydrogen atom, a (C Factory C 6 ) alkyl group, C 2 - C 6) Al Group, may be interrupted by - - (c 6 c 3) 1 to hetero atoms two of the selected from may) be substituted by an alkyl group (c 2 c 6) alkynyl group or a cycloalkyl.
- a (d-C 4 ) alkylene group may form a 5- or 6-membered ring.
- halogen atom represents a chlorine atom, a bromine atom, an iodine atom or a fluorine atom.
- the “(-C 6 ) alkylene group” is a linear or branched C 1-6 alkylene such as methylene, ethylene, propylene, trimethylene, dimethylenolethylene, tetramethylene, isoptylene, dimethylethylene, and hexamethylene.
- (C r C 6 ) alkyl group means, for example, methyl, ethyl, n-propyl, i-propyl, n-butyl, i-butyl, s-butyl, t-butyl, n-pentyl, neopentyl, n — Represents a linear or branched alkyl group having 1 to 6 carbon atoms such as hexyl.
- “(: ⁇ ) haloalkyl group” means a straight or branched alkyl group having 1 to 6 carbon atoms, which may be the same or different and may be substituted with one or more halogen atoms.
- (C 3 -C 6 ) cycloalkynole group refers to an alicyclic group having 3 to 6 carbon atoms such as cyclopropynole, cycloptynole, cyclopentynole, cyclohexynole, 2-methylcyclopentyl, and 2-methylcyclopentyl. Shows a formula alkyl group.
- (C Factory C 6 ) alkoxy group means, for example, methoxy, ethoxy, n-propoxy, isopropoxy, n-butoxy, s-butoxy, t-butoxy, n-pentinoleoxy, isopentyloxy, neopentyl A linear or branched alkoxy group having 1 to 6 carbon atoms such as oxy, n-hexyloxy and the like.
- halo (Cr) alkoxy group refers to a straight or branched alkyl group having 1 to 6 carbon atoms substituted by one or more halogen atoms, which may be the same or different.
- (C r C 6 ) alkoxycarbonyl group means, for example, methoxycarbonyl, ethoxycanoleponinole, n-propoxycanoleponinole, isopropoxycanoleboninole, n-butoxycarbonyl, t-butoxycarbonyl, etc. It represents a linear or branched alkoxy group having 1 to 6 carbon atoms.
- (C Factory C 6 ) alkylthio group means, for example, methylthio, ethylthio, n-propylthio, isopropylthio, n-butylthio, s-butylthio, t-butylthio, n-pentylthio, isopentylthio, n-hexylthio, etc. It represents a chain or branched alkylthio group having 1 to 6 carbon atoms.
- (-) Alkyl sulfier group means, for example, methylsorefininole, ethinolesnorefinole, n-propinoresorefininole, isopropinoles norefininole, n-butinoresorefininole , S-butynolesulfininole, t-butynoles norefininole, n —pentinolesnorefininole, isopentylsnorefininole, n —hexylsulfinyl and other straight or branched chain carbon atoms Represents 1 to 6 alkylsulfinyl groups.
- (C Factory C 6 ) alkylsulfonyl group means, for example, methylsulfonyl, ethynolesnorefonyl, n-propynolesulfoninole, isopropylsnolehoninole, n-butynolesnorefonyl, s-butino Straight or branched chain carbon atoms of 1 to 6 such as lesnolephonyl, t-butinoresolephoninole, n-pentinoresulfonolone, isopentylsnorefonyl, and n-hexinolesulfoninole Alkylsulfonyl groups.
- the nitrogen atom Is a 4- to 13-membered hetero ring in which the bonding position with A is a nitrogen atom and contains the nitrogen atom, and the hetero ring is 4 to 8 A condensed ring in which a benzene ring or a 4 to 7-membered hetero ring is further condensed to a membered hetero ring.
- the heterocyclic ring may include, in addition to one or more nitrogen atoms, other heteroatoms such as an oxygen atom, a sulfur atom, and a phosphorus atom.
- GG 2 may be the same or different; oxygen atom, sulfur atom, N—R 3 ′ (wherein, R 3 ′ is a hydrogen atom, (C Factory C 6 ) alkyl group, cyano group, nitro group And a phenyl (CfC 6 ) alkyl group, which may be the same or different, and have a substituted phenyl (C Factory C 6) having at least one substituent selected from ⁇ ′ (where ⁇ ′ is described below) on the ring. ) Alkyl group, phenyl group or the same or different, and ⁇ , ( ⁇ , are shown below) It represents a substituted furyl group having one or more substituents selected. ), N—OR 4 '
- R ′ 1 ′ may be a hydrogen atom, a ((C 6 C) alkyl group, a phenyl (C C 6 ) alkyl group or may be the same or different, and ⁇ ′ ( ⁇ ′ will be described later.)
- J 1 is an oxygen atom, a sulfur atom, or N—R 9 (wherein R 9 is a hydrogen atom, a (-C 6 ) alkyl group, a phenyl (C-Factory C 6 ) alkyl group, which may be the same or different; , ( ⁇ , are shown below), a substituted phenyl (C r C 6 ) alkyl group having at least one substituent selected from the following on the ring, a phenyl group, which may be the same or different, and Y ′ ( Y and are described below.)
- a substituted fuunyl group having one or more substituents selected from the group consisting of a heterocyclic group and a heterocyclic group may be the same or different.
- (Ci-Cs) alkyl group (the heterocyclic group is as defined above.), Mono (C ⁇ C 6) alkylaminocarbonyl group, the same or different and may di (Cf) alkylaminocarbonyl group, Fueniruamino A carbonyl group or a substituted or unsubstituted phenylaminocarbonyl group having at least one substituent selected from ⁇ ′ ( ⁇ ′ is shown below) which may be the same or different. Show.
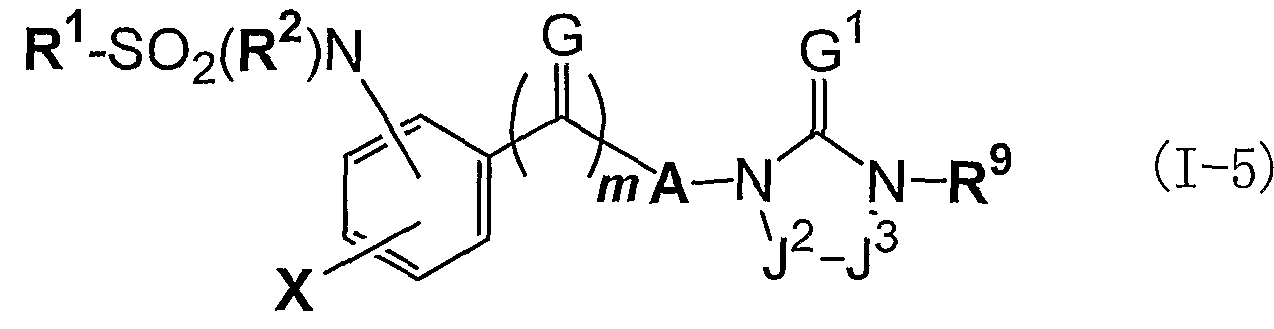
- J 2 and J 3 may be the same or different, and include an oxygen atom, a sulfur atom, N—R 9 (wherein R 9 is as defined above), R 1Q —C—R 11 (wherein R 1Q and Pi R 11 may be the same or different, a hydrogen atom, (c -!
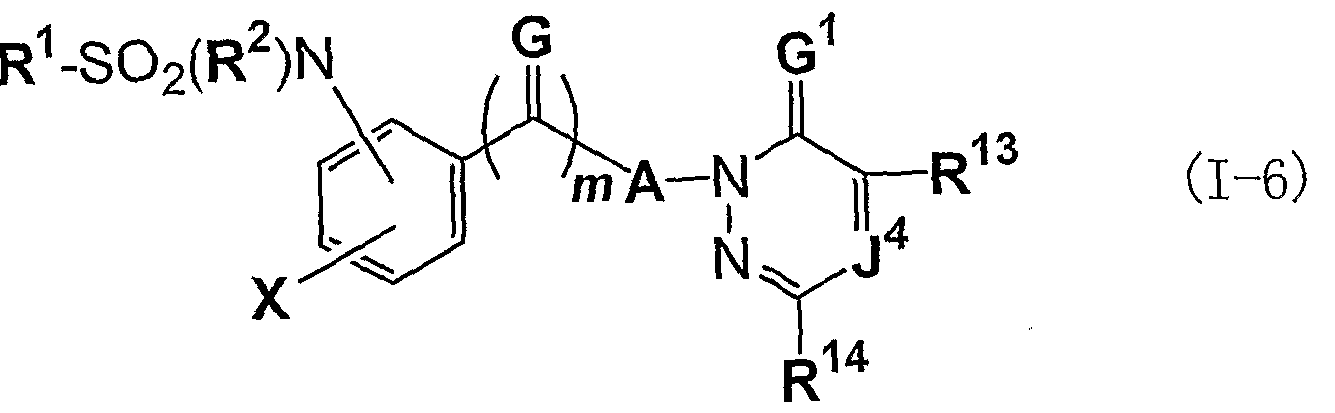
- J 4 and J 5 may be the same or different, and C—R 12 (where R 12 is a hydrogen atom, a halogen atom, a (C Factory C 6 ) alkyl group, a halo (C Factory C 6 ) alkyl group , (C Factory C 6 ) alkoxy group, Haguchi (CFactory C 6 ) alkoxy group, (Cf C 6 ) alkylthio group, Haguchi (CFactory C 6 ) alkylthio group, (CfCs) alkylsulfinyl group, nodro ( C factory c 6 ) alkylsulfinyl group, (c r c 6 ) alkynolesnorefonyl group, nodro (C factory C 6 ) anorecylsulfoninole group, phenyl (C factory c 6 ) alkyl group, same or different And a phenyl (C Factory c 6 )
- J 6 represents an oxygen atom, a sulfur atom, N_R 9 (where R 9 is the same as described above), or R 1Q —C 1 R 11 (where R ll) and R ′′ are the same as described above).
- R 9 is the same as above.
- R 13 and R w may be the same or different, and may be a hydrogen atom, a halogen atom, a (C Factory C 6 ) alkyl group, a halo (C Factory C 6 ) alkyl group, a (C Factory C 6 ) alkoxy group, a halo (C "C 6 ) alkoxy group, (C Factory C 6 ) alkylthio group, halo (C Factory C 6 ) alkylthio group, (C Factory C 6 ) alkylsulfinyl group, ⁇ ⁇ (CFactory C 6 ) alkylsulfinyl group, A C r C 6 ) alkylsulfonyl group, a halo (C Factory C 6 ) alkylsulfonyl group, a phenyl (C r C 6 ) alkyl group may be the same or different, and ⁇ ( ⁇ ) is described below.
- C Factory C 6 alkyl group, phenyl group having one or more substituents on the ring, which may be the same or different, and ⁇ ′ ( ⁇ ′ is shown below).
- a heterocyclic (C ⁇ C 6 ) alkyl group (heterocyclic group Same as above.
- R 15 and R 16 may be the same or different and represent a hydrogen atom or a (C Factory C 6 ) alkyl group.
- X ′ may be the same or different, and include a hydrogen atom, a halogen atom, a (Cfc 6 ) alkyl group, a (c 2 -c 6 ) alkenyl group, a (c 2 -g alkynyl group, a cyclo (c 3 -c 7 ) alkyl group, Nono port (c ⁇ c 6) alkyl group, Shikuroha port (c 3 - 7) alkyl group, (c ⁇ c 6) alkoxy groups, halo
- C factory c 6 anorequinoles refininole group, phenol (c r c 6 ) anore cyls norefinyl group, (c r c 6 ) anorekylsulfonyl group, phenol (C factory C 6 ) an alkylsulfonyl group, a phenyl group, the same or different, and a substituted phenyl group, a phenoxy group having one or more substituents selected from ⁇ ′ ( ⁇ ′ is described below). May be the same or different;
- C factory c 6 alkylaminocarbonyl group, same or different di ((: c 6 ) alkylaminocarbonyl group, phenylaminocarbonyl group, same or different A substituted phenylaminocarbonyl group having one or more substituents selected from the group consisting of Y ′ ( ⁇ ′ is described below), phenyl (C Factory c 6 ) alkylaminocarbinole Groups, which may be the same or different, are selected from ⁇ , ( ⁇ 'is shown below)
- substituents selected from a substituted phenyl (CfCe) alkylaminocarboxy group, a hydroxyl group, an amino group, a cyano group and a nitro group having at least one substituent on a ring.
- Y may be the same or different, and include a hydrogen atom, a halogen atom, a (c r c 6 ) alkyl group, a (c 2 -c 6 ) alkenyl group, a (c 2 -c 6 ) alkynyl group, a cyclo (c 3- c 6 ) alkyl group, phenol (c factory c 6 ) alkyl group, cycloha (c 3 -c 6 ) alkyl group, (-alkoxy group, phenol (C factory C 6 ) alkoxy group, (C r C 6 ) Alkylthio group, halo (-Ce) alkylthio group,
- the groups represented can be mentioned.
- heterocyclic group examples include a pyridyl group, a pyridine-N-oxide group, a pyrimidinyl group, a pyrazinyl group, a triazinole group, a furyl group, a tetrahydrofuryl group, a phenyl group, a tetrahydrophenyl group, a tetrahydrovinylanyl group, and a tetrahydrovinyl group.
- Examples thereof include a thiopyranyl group, an oxazolyl group, an isoxazolyl group, an oxdiazolyl group, a thiazolyl group, an isothiazolyl group, a thiadiazolyl group, an imidazolyl group, a triazolyl group, a pyrazolyl group, and a morpholinyl group.
- the salt of the haloalkylsulfonanilide derivative of the present invention may be any salt that can be used when applied as a pesticide, for example, salts with an alkali metal such as lithium salt, sodium and potassium, calcium and magnesium Salts with alkaline earths such as, salts with heavy metals such as iron, salts with inorganic metals such as salts with other metals such as aluminum and zinc, salts with organic bases such as ammonium salts, etc. These may form hydrates.
- the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention may contain one or more asymmetric carbon atoms or asymmetric centers in its structural formula, and may have two or more types.
- Optical isomers and diastereomers may exist, and the present invention includes all optical isomers and mixtures containing them in any ratio.
- the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention has two kinds of geometric isomers derived from a carbon-carbon double bond or a carbon-nitrogen double bond in its structural formula.
- the present invention encompasses all geometric isomers and mixtures containing them in any proportion.
- the heterocycle of Q is a 5-membered to 6-membered compound containing 1 to 4 nitrogen atoms, 0 to 1 oxygen atom and 0 to 1 sulfur atom. It is also preferable that the 5- or 6-membered hetero ring forms a condensed ring. Particularly preferred are Q-1, Q-2, Q-3 and the like.
- Suitable as the substituent on Q is, phenyl (C ⁇ C 6) alkyl group, a substituted phenyl (C ⁇ C 6) alkyl group, Hue group, a substituted phenyl group, pyridyl group and substitution pyridyl group is there.
- the haloalkyl as R 1 is preferably fluoromethyl, more preferably trifluoromethyl or difluoromethyl, and the substitution position is preferably the 2-position.
- R 2 is preferably a hydrogen atom.
- G and G 1 are preferably oxygen atoms.
- m is preferably 0.
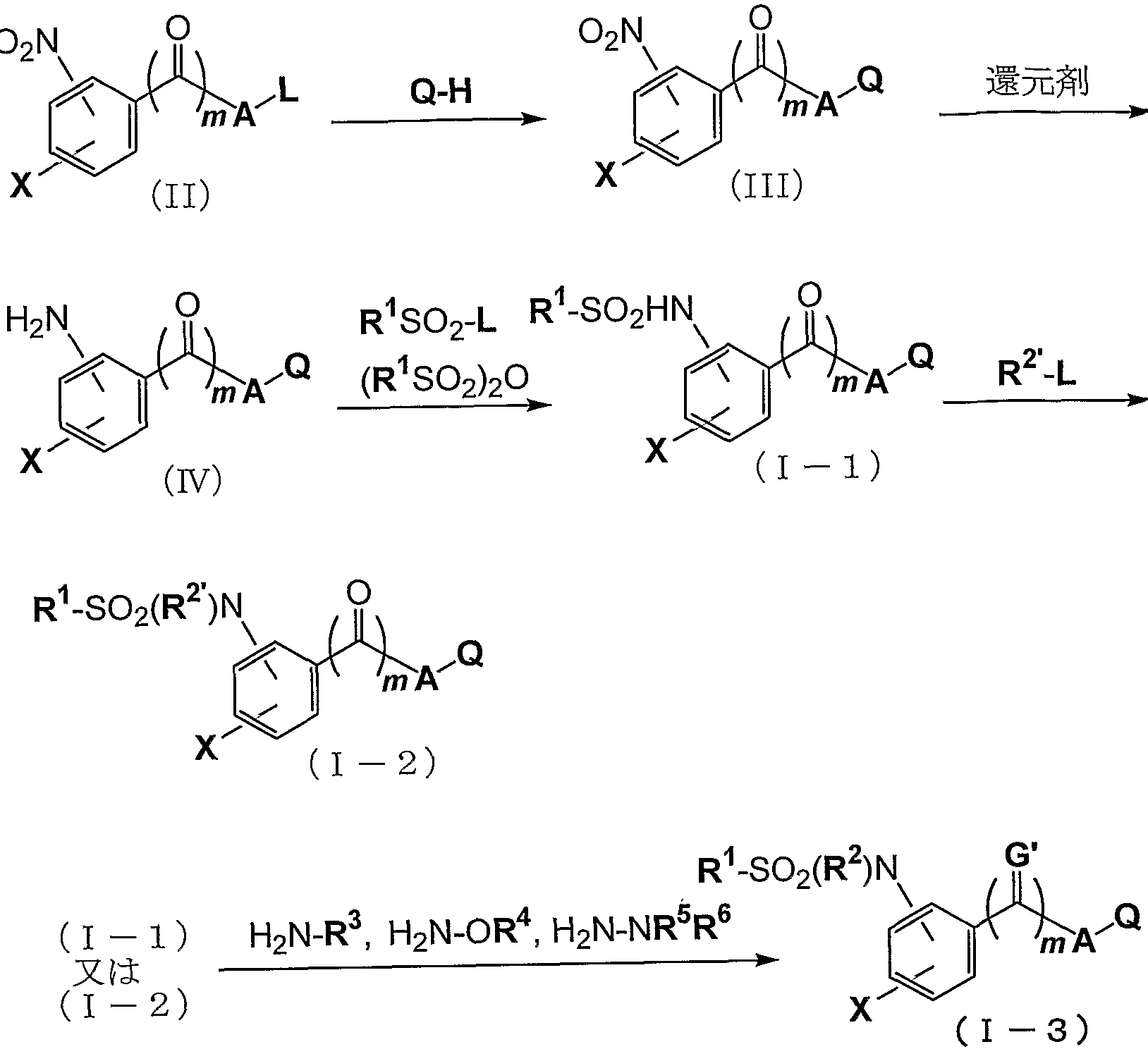
- haloalkylsulfonamide derivative represented by the general formula (I) of the present invention can be produced, for example, by the production method shown below.
- R 2 ′ is a (Cf C 6 ) alkyl group, (C 6 -C 6 ) alkyl A carbonyl group, a nitro group (C Factory C 6 ) alkyl carbonyl group, which may be the same or different, and a phenylcarbonyl group having at least one substituent selected from Y (Y is the same as described above); c 6) alkyl sulfonyl group, a halo (C ⁇ c 6) alkylsulfonyl group, or the same or different and may, Y (Y is phenylene Noresuruho radicals having 1 or more substituents selected from the same.) to the Is shown.
- L represents a leaving group such as a halogen atom.
- the compound represented by the general formula (II) is reacted with a heterocyclic compound represented by the general formula QH in the presence of a base and, if necessary, using a phase transfer catalyst in the presence or absence of an inert solvent.
- the compound represented by the general formula (III) is reacted to give a compound represented by the general formula (I) by isolating or not isolating the compound and reacting with a reducing agent or the like in the presence or absence of an inert solvent.
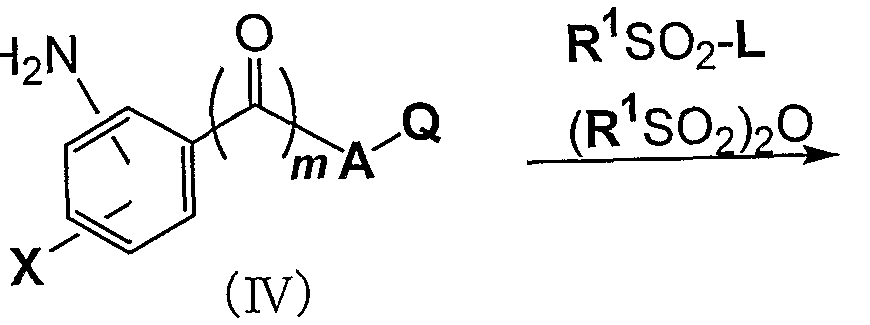
- An amino compound represented by the formula (IV) is isolated or isolated without isolation, and is prepared by the reaction of I ⁇ S 0 2 _L (in the formula, in the presence of a base, in the presence or absence of an inert solvent) R 1 and L are the same as described above.) Or (1 ⁇ 3 ⁇ 2 ) 2 R (wherein, R 1 is the same as described above.) By reacting a haloalkylsulfonyl derivative represented by the general formula ( 1 ). The compound of the present invention represented by 1-1) can be produced.
- the compound represented by the general formula (1-1) is isolated or not isolated, and the compound represented by the general formula R 2 — L (wherein, and in the presence of a base, in the presence or absence of an inert solvent)
- the compound of the present invention represented by the general formula (1-2) can be produced by reacting the compound represented by the same formula.
- the compound represented by the general formula (1-1) or (1-2) is isolated or not isolated, and in the presence or absence of an inert solvent, the compound represented by the general formula H 2 N—R 3 ( In the formula, R 3 is the same as described above.)
- the heterocyclic ring represented by Q—H is, for example, 2,3-dihydro 3H-1,2,41-triazol-3-one derivative can be prepared by the method described in WO 98-381176 or the like.
- tetrazole derivatives can be produced by the method described in J. Heterocycl. Chem., 35 (2), 405 (1998) or the like, or other heterocycles represented by Q—— are described in international patents. Publication W ⁇ 91-3470, J. Chem.
- the inert solvent that can be used in this reaction may be any solvent that does not significantly inhibit this reaction, and examples thereof include linear or cyclic ethers such as getyl ether, tetrahydrofuran, and dioxane, and benzene, toluene, and xylene.
- linear or cyclic ethers such as getyl ether, tetrahydrofuran, and dioxane, and benzene, toluene, and xylene.
- Ketones such as acetonitrile, esters such as ethyl acetate, amides such as N, N-dimethylformamide, N, N-dimethylacetamide, dimethylsulfoxide, 1,3
- inert solvents such as —dimethyl-2-imidazolinone and water. These inert solvents may be used alone or in combination of two or more. To be able to use.
- Bases that can be used in this reaction include, for example, nitrogen-containing organic bases such as triethylamine, diisopropinoletinoleamine, 1,8-diazabicyclo mouth [5.4.0] 17-indene, pyridine, sodium carbonate, and carbonic acid.
- Inorganic bases such as lime, sodium bicarbonate, sodium hydroxide, sodium hydroxide, sodium hydride, sodium metal, etc .; organic bases such as sodium acetate, sodium acetate; alcohol such as sodium methoxide and potassium t-butoxide And the like.
- the base may be used in an amount sufficient to neutralize the acid generated by the reaction, but may be used in excess.
- phase transfer catalyst examples include tetra n- 3 009405
- phase transfer catalyst examples thereof include quaternary ammonium salts such as dimethylpromide and benzyltriethylammonium bromide, and crown ethers such as 18-crown-16-ether.
- the amount of the phase transfer catalyst to be used may be appropriately selected from the range of from 0.01 to 1.5 times the mol of the compound represented by the general formula ( ⁇ ).
- each reactant may be used in an equimolar amount, but any amount of the reactant may be used in excess.
- the reaction can be carried out at a temperature of from 120 ° C. to the reflux temperature of the used inert solvent.
- the reaction time is not fixed depending on the reaction scale, the reaction temperature, etc., but is appropriately in the range of several minutes to 48 hours. Just choose.
- the target product can be produced by isolating the target product from the reaction system containing the target product by a conventional method and, if necessary, purifying the product by a recrystallization method, a distillation method, a column chromatography method or the like. Further, after the completion of the reaction, the target product can be used for the next reaction without isolation.
- inert solvent examples include alcohols such as methanol and ethanol, ethers such as tetrahydrofuran and dioxane, and water. These inert solvents may be used alone or in combination of two or more. Can be used in combination. Further, an aqueous solution of an acid used as a reducing agent described below can be used as an inert solvent as it is.
- Examples of the reducing agent that can be used in this reaction include metal monoacids and metal monoliths.
- Examples of the metal include iron, tin, and zinc, and examples of the acid include minerals such as hydrochloric acid and sulfuric acid.
- Acids, organic acids such as acetic acid and the like, tin chloride and the like, and examples of the salt include salt water ammonium and the like. It is also possible to use them in combination.
- the amount of the reducing agent used is 1 to 10 times the molar amount of the compound represented by the general formula ( ⁇ ), and the acid and salt are appropriately selected from the range of 0.05 to 10 times the molar amount. I should do it.
- the reaction temperature may be selected from the range of 0 ° C. to 150 ° C., and the reaction time is not constant depending on the reaction scale, the reaction temperature, and the like, but may be appropriately selected within the range of several minutes to 48 hours.
- the reduction can also be carried out by catalytic hydrogenation in the presence of a catalyst.
- a catalyst examples include palladium carbon, platinum, Raney nickel and the like.
- the desired product can be produced by isolating the desired product from the reaction system containing the desired product by a conventional method, and purifying the product, if necessary, by a recrystallization method, a distillation method, a column chromatography method or the like. Further, after the completion of the reaction, the target product can be used for the next reaction without isolation.
- the inert solvent that can be used in this reaction may be any solvent that does not significantly inhibit the progress of this reaction.
- examples include linear or cyclic ethers such as getyl ether, tetrahydrofuran, and dioxane; benzene, toluene, and xylene.
- Ketones such as acetonitrile, esters such as ethyl acetate, amides such as N, N-dimethylformamide, N, N-dimethylacetamide, dimethylsulfoxide, 1,3-dimethyl-2- Inert solvents such as imidazolinone can be exemplified. These inert solvents may be used alone or in combination of two or more. Can be used.
- Bases that can be used in this reaction include, for example, nitrogen-containing organic bases such as triethylamine, diisopropylethynoleamine, 1,8-diazabicycline [5.4.0] -17-indene, pyridine, sodium carbonate, carbonated lime, and the like.
- Inorganic bases such as sodium hydrogencarbonate, sodium hydroxide, hydroxylated sodium, hydrogenated sodium, metal sodium, etc .
- organic bases such as sodium acetate, sodium acetate
- alcoholate such as sodium methoxide, potassium t-butoxide, etc.
- nitrogen-containing organic bases such as pyridine can also be used as the solvent.
- the base may be used in an amount sufficient to neutralize the acid generated by the reaction, but may be used in excess.
- each reactant may be used in an equimolar amount, but any of the reactants may be used in excess.
- the reaction can be carried out at a temperature of from 120 ° C to the reflux temperature of the inert solvent used.
- the reaction time depends on the reaction scale, reaction temperature, etc. Although it is not constant, it may be appropriately selected in the range of several minutes to 48 hours.
- the desired product can be produced by isolating the desired product from the reaction system containing the desired product by a conventional method, and purifying the product, if necessary, by a recrystallization method, a distillation method, a column chromatography method or the like. Further, after the completion of the reaction, the target product can be used for the next reaction without isolation.
- This reaction can be carried out according to (1-3).
- the desired product can be produced by isolating the desired product from the reaction system containing the desired product by a conventional method, and purifying the product, if necessary, by a recrystallization method, a distillation method, a column chromatography method or the like. Further, after the completion of the reaction, the target product can be used for the next reaction without isolation.
- Any inert solvent may be used as long as it does not significantly inhibit the progress of this reaction.
- examples thereof include alcohols such as methanol, ethanol, n-propanol, and the like, and chain or cyclic ethers such as getyl ether, tetrahydrofuran, and dioxane.
- Aromatic hydrocarbons such as benzene, toluene, and xylene, and halogenated aromatic hydrocarbons such as benzene and dichlorobenzene, and these inert solvents can be used alone or individually. Two or more can be used in combination.
- Examples of the acid that can be used in this reaction include organic acids such as formic acid, acetic acid, and propionic acid, and mineral acids such as hydrochloric acid and sulfuric acid.
- each reactant may be used in an equimolar amount, but any of the reactants may be used in excess.
- the reaction can be carried out at a temperature of from 120 ° C. to the reflux temperature of the used inert solvent.
- the reaction time is not fixed depending on the reaction scale, the reaction temperature, etc., but is appropriately in the range of several minutes to 48 hours. Just choose.
- the desired product can be produced by isolating the desired product from the reaction system containing the desired product by a conventional method, and purifying the product, if necessary, by a recrystallization method, a distillation method, a column chromatography method or the like.
- R 17 is an amino group, 2-hydroxyethyla It represents a mino group or a hydrazino group.
- the compound represented by the general formula (V) as a starting material is described in, for example, J. Chem. Soc., 1 800 (1925), J. Chem. Soc., 2348 (1 926), or the like, or can be produced according to them.
- haloalkylsulfonanilide derivatives represented by the general formula (I) of the present invention are shown in Tables 1 to 13, but the present invention is not limited thereto.
- the physical properties indicate the melting point (° C) or the refractive index.
- Me represents a methyl group
- E t represents an ethyl group
- P r represents a propyl group
- Bu represents a butyl group
- P en represents a pentyl group
- H ex is a hexyl group
- Ph is a phenyl group
- Pyn is a pyridyl group
- ⁇ ym is a pyrimidyl group
- P yd is a pyridazyl group
- Ac is an acetyl group.
- substitution position indicates the substitution position of the alkylsulfonylamino group.
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Agronomy & Crop Science (AREA)
- Pest Control & Pesticides (AREA)
- Plant Pathology (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Dentistry (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
Abstract
Haloalkylsulfonanilide derivatives represented by the general formula (I) and salts thereof; herbicides containing the compounds; and usage thereof: (I) wherein R1 is halo(C1-C6)alkyl; R2 is H, C1-C6 alkyl or the like; A is C1-C6 alkylene or the like; G is OS, NR3, or the like; m is 0 or 1; X is substituted phenyl, phenoxy, or the like; and Q is an optionally substituted heterocycle having at least one ring-constituent nitrogen atom at which the heterocycle is bonded to A.
Description
明 細 書 新規なハロアルキルスルホンァニリド誘導体及び除草剤並びにその使用方法 技術分野 Description Novel Haloalkylsulfonanilide Derivatives and Herbicides and Methods of Use Thereof
スルホンァニリド誘導体又はその塩及ぴ該化合物を有効成分とする除草剤並び にその使用方法に関するものである。 The present invention relates to a sulfonanilide derivative or a salt thereof, a herbicide containing the compound as an active ingredient, and a method for using the herbicide.
背景技術 Background art
従来、 パーフルォロアルキルスルホニルァミノ基を置換基として有するジフエ 二ノレエーテル誘導体が除草剤又は抗炎症剤として有用であることが知られている (例えば、 米国特許第 3 9 0 6 0 2 4号明細書参照。 ) 力 ジフ ニルエーテル 以外の骨格についてはなんらの記载も示唆もない。 また、 フエノキシ基、 フエ二 ルチオ基、 フエニルスルホニル基等を置換基として有するパーフルォ.口アルキル スルホンァニリド誘導体が除草剤又は抗炎症剤として有用であること (例えば、 独国特許出願公開第 2 1 1 8 1 9 0 3号明細書参照。 ) が、 トリフルォロメタン スルホニルァミノ基を置換基として有するゥレア誘導体が除草剤として有用であ ること (例えば、 特開昭 6 0— 8 7 2 5 4号公報参照。 ) 力 トリフルォロメタ ンスルホニルァミノ基を有するピラジン誘導体が除草剤として有用であること (例えば、 米国特許第 4 3 4 5 0 7 6号明細書参照。 ) が知られているが、 本発 明の一般式 (I ) で表されるハロアルキルスルホンァニリ ド誘導体は記載も示唆 もされておらず、 本発明の一般式 (I ) で表されるハロアルキルスルホンァニリ ド誘導体が有するようなイネと水田雑草間の選択除草性に関する記載もない。 また、 トリフルォロメタンスルホンァニリ ド構造を有するヘテロ環誘導体が除 草剤として有用であることが知られている (例えば、 欧州特許出願公開第 0 0 1 1 6 9 3 5号明細書参照。 ) 力 トリフルォロメタンスルホンァニリ ドとヘテロ 環が直接結合した骨格であり、 本発明の一般式 (I ) のようにハロアルキルスル ホンァニリドとへテロ環がアルキレン基等を介して結合した骨格の化合物は記載 も示唆もされていない。 4位に 2—ピリミジニルォキシ基を有するスルホンァニ リ ド誘導体及び該ィヒ合物を有効成分とする除草剤が知られており (例えば、 特開
平 8— 1 9 3 0 1 1号公報又は特開平 8 - 2 9 1 1 4 6号公報参照。 ) 、 イネに 薬害がないことや水田への適用性等が記載されているが、 本発明の一般式 (I ) で表されるハロアルキルスルホンァニリ ド誘導体とは骨格が異なり、 他の骨格に ついて特段の記載も示唆もない。 Hitherto, dipheninoleether derivatives having a perfluoroalkylsulfonylamino group as a substituent have been known to be useful as herbicides or anti-inflammatory agents (for example, US Pat. No. No description or suggestion is made for skeletons other than diphenyl ether. In addition, perfluoroalkyl sulfonanilide derivatives having a phenoxy group, a phenylthio group, a phenylsulfonyl group or the like as substituents are useful as herbicides or anti-inflammatory agents (for example, see German Patent Application Publication No. However, a perrea derivative having a trifluoromethanesulfonylamino group as a substituent is useful as a herbicide (for example, see JP-A-60-87254). It is known that pyrazine derivatives having a trifluoromethanesulfonylamino group are useful as herbicides (see, for example, US Pat. No. 4,345,076). The haloalkyl sulfonanilide derivative represented by the general formula (I) of the present invention is neither described nor suggested, and the haloalkyl sulfonyl derivative represented by the general formula (I) of the present invention is not described. No description about the selected herbicidal between rice and paddy weeds such as possessed by Li de derivatives. Further, it is known that a heterocyclic derivative having a trifluoromethanesulfonanilide structure is useful as a herbicide (for example, see European Patent Application Publication No. 0,191,693). ) Force A compound having a skeleton in which trifluoromethanesulfonanilide and a heterocycle are directly bonded, and a skeleton in which a haloalkylsulfonanilide and a heterocycle are bonded via an alkylene group or the like as in the general formula (I) of the present invention. Is neither described nor suggested. A sulfonanilide derivative having a 2-pyrimidinyloxy group at the 4-position and a herbicide containing the compound as an active ingredient are known. See Japanese Unexamined Patent Publication No. Hei 8—1931011 or Japanese Unexamined Patent Publication No. Hei 8-292911. It is described that rice has no phytotoxicity and its applicability to paddy fields, but the skeleton is different from that of the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention. There is no particular description or suggestion about this.
更に、 除草剤として有用な 2位にピリミジニルォキシ基を有するスルホンァニ リ ド誘導体 (例えば、 国際公開第 9 3 Z 0 9 0 9 9号パンフレット、 国際公開第 9 6 / 4 1 7 9 9号パンフレツ ト又は特開平 2— 1 4 9 5 6 7号公報参照。 ) が、 ピリミジン 2位とァニリン 2位との結合にアミノメチレン基又はィミノメチレン 基を有する除草剤として有用なスルホンァニリド誘導体化合物 (例えば、 特開平 1 1 - 6 0 5 6 2号公報参照。 ) 、 2位にピリミジニル基を持ち、 更に 6位に アルコキシアルキル基を有するトリフルォロメタンスルホンァニリド誘導体が哺 乳動物に対する毒性の低い水田用除草剤として有用であること (例えば、 特開 2 0 0 0 - 6 3 3 6 0号公報参照。 ) 、 2位にジメトキシピリミジニルヒドロキ シメチル基を有するジフルォロメタンスルホンァニリド誘導体がイネに選択性を 有する除草剤として知られてレ、る (例えば、 特開 2 0 0 0— 4 4 5 4 6号公報参 照。 ) 力 いずれもジメトキシピリミジニル基等を有することが必須の構造的特 徴であり、 本発明の一般式 (I ) で表されるハロアルキルスルホンァニリ ド誘導 体のように、 ノヽロアルキルスルホンァニリドとヘテロ環がアルキレン基等を介し て結合した骨格の化合物は記載も示唆もされていない。 また、 除草剤としての作 用性も異なっている。 Further, sulfonanilide derivatives having a pyrimidinyloxy group at the 2-position useful as herbicides (for example, International Publication No. 93Z0909 pamphlet, International Publication No. Or a sulfonanilide derivative compound useful as a herbicide having an aminomethylene group or an iminomethylene group in the bond between the 2-position of pyrimidine and the 2-position of aniline (see, for example, Japanese Patent Application Laid-Open No. 2-1495677). Japanese Patent Application Laid-Open No. Hei 11-605056)), a trifluoromethanesulfonanilide derivative having a pyrimidinyl group at the 2-position and an alkoxyalkyl group at the 6-position is used for paddy fields with low toxicity to mammals. It is useful as a herbicide (for example, see Japanese Patent Application Laid-Open No. 2000-633600), and difluoromethanesulfur having a dimethoxypyrimidinylhydroxymethyl group at the 2-position. An anilide derivative is known as a herbicide having selectivity for rice (see, for example, JP-A-2000-44546). Both of these compounds have a dimethoxypyrimidinyl group or the like. It is an essential structural feature and, as in the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention, a nodroalkylsulfonanilide and a heterocycle are bonded via an alkylene group or the like. The compound having the skeleton is not described or suggested. Also, their workability as herbicides is different.
本発明者等は、 新規な除草剤を開発すべくスルホンァニリ ド構造を有する誘導 体の合成とその生理活性について鋭意研究を重ねた結果、 本発明の一般式 (I ) で表される新規なハロアルキルスルホンァニリド誘導体が文献未記載の新規化合 物であり、 先行技術に開示の化合物に比して顕著な除草効果、 スルホニルゥレア 系除草剤抵抗性雑草等の難防除雑草を含む多くの雑草種に対する広い適用性、 効 果の持続性、 優れた作物—雑草間の選択性等の特性を兼ね備えており、 除草剤特 に水田用除草剤として有用なことを見出し、 本発明を完成させたものである。 発明の開示 The present inventors have conducted intensive studies on the synthesis of a derivative having a sulfonanilide structure and the physiological activity thereof in order to develop a novel herbicide. As a result, a novel haloalkyl represented by the general formula (I) of the present invention was obtained. A sulfonanilide derivative is a novel compound that has not been described in the literature. It has wide applicability to species, long-lasting effect, and excellent properties such as selectivity between crops and weeds, and has been found to be useful as a herbicide, particularly as a paddy field herbicide, and completed the present invention. Things. Disclosure of the invention
{式中、 R1はハロ (C厂 C6) アルキル基を示す。 {Wherein, R 1 represents a halo (C Factory C 6 ) alkyl group.
R2は水素原子、 (C厂 C6) アルキル基、 (C C6) アルコキシ (Cf C6) アルキル 基、 ( - C6) アルキルカルポニル基、 ノヽロ (( ) アルキルカルボニル基、 フ ェニルカルボニル基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) から選 択される 1以上の置換基を有する置換フエニルカルボニル基、 ( - c6) アルコ キシカ ポニル基、 フエノキシカルボニル基、 同一又は異なっても良く、 Υ (Υ は後記に示す。 ) 力 ら選択される 1以上の置換基を有する置換フ ノキシカルボ ニル基、 (C厂 C6) アルキルスルホニル基、 ノヽロ (C厂 C6) アルキルスルホニル基、 フエニルスルホニル基又は同一若しくは異なっても良く、 Y (Yは後記に示 す。 ) から選択される 1以上の置換基を有する置換フエニルスルホニル基を示す。 R 2 is a hydrogen atom, a (C 6 C) alkyl group, a (CC 6 ) alkoxy (CfC 6 ) alkyl group, a (-C 6 ) alkyl carbonyl group, a nodro (() alkylcarbonyl group, a phenylcarbonyl group A substituted phenylcarbonyl group having at least one substituent selected from Y (Y is shown below), (-c 6 ) alkoxycaponyl group, phenoxycarbonyl group May be the same or different, and a substituted phenyloxycarbonyl group having at least one substituent selected from 力 (力 is described below), (C Factory C 6 ) alkylsulfonyl group, phenol (C Factory C 6 ) represents an alkylsulfonyl group, a phenylsulfonyl group or a substituted phenylsulfonyl group which may be the same or different and has one or more substituents selected from Y (Y is shown below).
Qは構成原子の少なくとも 1個が窒素原子であり、 かつその窒素原子が Aとの 結合部位である置換されていても良いヘテロ環を示す。 Q represents an optionally substituted heterocycle in which at least one of the constituent atoms is a nitrogen atom, and the nitrogen atom is a bonding site with A.
Aは (Cf C6) アルキレン基、 同一又は異なっても良く、 ハロゲン原子、 水酸 基、 (C厂 C6)アルコキシ基、 (C -Cs)アルコキシカルボニル基又はシァノ基から選 択される 1以上の置換基を有する置換 (cr c6) アルキレン基、 (c2- c6) ァルケ 二レン基、 同一又は異なっても良く、 ハロゲン原子、 水酸基、 (C厂 c6)アルコキ シ基、 (Cr )アルコキシカルボニル基又はシァノ基から選択される 1以上の置 換基を有する置換 (c2 - c6) アルケニレン基又は (c2-c6) アルキニレン基を示す。 A is a (Cf C 6 ) alkylene group, which may be the same or different, and is selected from a halogen atom, a hydroxyl group, a (C Factory C 6 ) alkoxy group, a (C-Cs) alkoxycarbonyl group or a cyano group 1 or more substitutions having substituent (c r c 6) alkylene group, (c 2 - c 6) Aruke two alkylene groups, the same or different and a halogen atom, a hydroxyl group, (C厂c 6) an alkoxy group, shows the - (c 6 c 2) alkenylene or (c 2 -c 6) alkynylene group (Cr) alkoxycarbonyl group or substituted with one or more location substituent selected from Shiano group.
Gは酸素原子、 硫黄原子、 N— R3 (式中、 R3は水素原子、 .(C厂 C6) アルキル 基、 シァノ基、 ニトロ基、 フエニル (C厂 C6) アルキル基、 同一又は異なっても 良く、 Y (Yは後記に示す。 ) から選択される 1以上の置換基を環上に有する置 換フヱニル (C广 C6) アルキル基、 フエニル基又は同一若しくは異なっても良く、 Y (Yは後記に示す。 ) から選択される 1以上の置換基を有する置換フエニル基 を示す。 ) 、 N— O R4 (式中、 は水素原子、 (Cr C6) アルキル基、 フエニル (crc6) アルキル基又は同一若しくは異なっても良く、 Y ( Yは後記に示
す。 ) から選択される l以上の置換基を環上に有する置換フエニル (cr c6) 了 ルキル基を示す。 ) 又は N— N R5 R6 (式中、 R5及ぴ R6は同一又は異なっても 良く、 水素原子、 フエニル基又は同一若しくは異なっても良く、 Y (Yは後記に 示す。 ) から選択される 1以上の置換基を有する置換フエ二ル基を示す。 又、 R5と R6は一緒になつて (C3-C6) アルキレン基を示すこともできる。 ) を示す。 G is an oxygen atom, a sulfur atom, N—R 3 (where R 3 is a hydrogen atom, an alkyl group of. (C Factory C 6 ), a cyano group, a nitro group, a phenyl (C Factory C 6 ) alkyl group, the same or A substituted phenyl (C-wide C 6 ) alkyl group having at least one substituent selected from Y (Y will be described below) on the ring, a phenyl group, or the same or different; Y represents a substituted phenyl group having at least one substituent selected from the following.), N—OR 4 (wherein, is a hydrogen atom, a (C r C 6 ) alkyl group, phenyl) (c r c 6 ) alkyl group or the same or different, and Y (Y is shown below) You. The l or more substituents selected from) a substituted phenyl (c r c 6) Ryo alkyl group having on the ring. Or N—NR 5 R 6 (wherein, R 5 and R 6 may be the same or different, may be a hydrogen atom, a phenyl group or the same or different, and are selected from Y (Y is shown below.) And R 5 and R 6 may be taken together to represent a (C 3 -C 6 ) alkylene group.
mは 0又は 1の整数を示す。 m represents an integer of 0 or 1.
Xは同一又は異なっても良く、 水素原子、 ハロゲン原子、 (C厂 C6)アルキル基、 (C2-C6)アルケニル基、 (C2- C6)アルキニル基、 シクロ(C3-C6)アルキル基、 ノヽロ (C厂 C6)アルキル基、 シクロハ口(C3- C6)アルキル基、 (C厂 C6)アルコキシ基、 ハロ (C厂 C6)アルコキシ基、 ( - C6)アルキルチオ基、 ハロ(C厂 c6)アルキルチオ基、 (C厂 C6)アルキルスルフィニル基、 ノヽ口(C厂 c6)アルキルスルフィニル基、 (crc6) アルキルスルホニル基、 /、口(C厂 c6)アルキルスルホニル基、 フエ二ル基、 同一 又は異なっても良く、 γ (Yは後記に示す。 ) 力 ら選択される 1以上の置換基を 有する置換フエニル基、 フエノキシ基、 同一又は異なっても良く、 Y (Yは後記 に示す。 ) 力 ら選択される 1以上の置換基を有する置換フエノキシ基、 フエニル チォ基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) から選択される 1以 上の置換基を有する置換フエ二ルチオ基、 フエニルスルフィニル基、 同一又は異 なっても良く、 Y (Yは後記に示す。 ) 力 ら選択される 1以上の置換基を有する 置換フエニルスルフィエル基、 フエニルスルホニル基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) から選択される 1以上の置換基を有する置換フエニルス ルホニル基、 (Cr C6)アルキルカルボニル基、 ノヽロ(C厂 c6)アルキルカルボニル基、 フエ二ルカルポニル基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) から 選択される 1以上の置換基を有する置換フエ二ルカルポニル基、 (C厂 c6)ァノレコ キシカルボニル基、 カルボキシル基、 モノ ( - ) アルキルアミノカルボニル 基、 同一又は異なっても良いジ (C厂 C6) アルキルァミノカルボニル基、 フエ二 ルァミノカルボニル基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) から 選択される 1以上の置換基を環上に有する置換フエニルァミノカルボニル基、 フ ェ-ル (C厂 C6) アルキルアミノカルボニル基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) から選択される 1以上の置換基を環上に有する置換フエ二
ル (Cf c6) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シァノ基又は二 トロ基から選択される 1〜4個の置換基を示す。 X may be the same or different; a hydrogen atom, a halogen atom, a (C 2 C 6 ) alkyl group, a (C 2 -C 6 ) alkenyl group, a (C 2 -C 6 ) alkynyl group, a cyclo (C 3 -C 6 ) Alkyl group, Noro (C Factory C 6 ) alkyl group, cycloha (C 3 -C 6 ) alkyl group, (C Factory C 6 ) alkoxy group, halo (C Factory C 6 ) alkoxy group, (-C 6) alkylthio groups, halo (C厂c 6) alkylthio groups, (C厂C 6) alkylsulfinyl group, Nono port (C厂c 6) alkylsulfinyl group, (c r c 6) alkylsulfonyl group, /, mouth (C factory c 6 ) alkylsulfonyl group, phenyl group, which may be the same or different, and have one or more substituents selected from γ (Y is shown below) force, substituted phenyl group, phenoxy group, Substituted phenols having one or more substituents, which may be the same or different and are selected from Y (Y is shown below) A phenylthio group, which may be the same or different, and a substituted phenylthio group having one or more substituents selected from Y (Y is shown below), a phenylsulfinyl group, the same or different A substituted phenylsulfenyl group or a phenylsulfonyl group having at least one substituent selected from the group consisting of Y (Y is shown below), and Y (Y is shown below) .) substituent Fuenirusu Ruhoniru group having one or more substituents selected from, (C r C 6) alkylcarbonyl group, Nono b (C厂c 6) alkylcarbonyl group, phenylene Rukaruponiru groups, the same or different well, Y (Y is shown later.) substituted phenylene Rukaruponiru group having one or more substituents selected from, (C厂c 6) Anoreko alkoxycarbonyl group, a carboxyl group, a mono (-) alkylamino Cal Group, the same or different and may di (C厂C 6) alkyl § amino group, phenylene Rua amino carbonyl group, the same or different and are selected from Y (Y is shown later.) 1 more substituted phenylalanine § amino group having a substituent on the ring, full E - Le (C厂C 6) alkylaminocarbonyl group, the same or different and, Y (Y is shown later. ) Substituted phenyl having at least one substituent selected from (Cfc 6 ) represents 1 to 4 substituents selected from an alkylaminocarbonyl group, a hydroxyl group, an amino group, a cyano group and a nitro group.
Yは同一又は異なっても良く、 ハロゲン原子、 (Ct-C6)アルキル基、 (C2- C6)ァ ルケニル基、 (c2- C6)アルキニル基、 シク口(C3- C6)アルキル基、 ハロ(C厂 c6)アル キル基、 シクロハ口(C3- C6)アルキル基、 (C厂 C6)アルコキシ基、 ハロ(C厂 C6)アル コキシ基、 (C厂 C6)アルキルチオ基、 ハロ( - C6)アルキルチオ基、 (C厂 c6)アルキ ノレスルフィニル基、 ノヽロ (CrC6)アルキルスルフィニル基、 (C厂 c6)アルキルスル ホニル基、 ハロ(C厂 c6)アルキルスルホニル基、 フエニル基、 同一又は異なって も良く、 ハロゲン原子、 (C厂 c6)アルキル基、 (c2- c6)アルケニル基、 (c2- c6)アル キニル基、 シク口(C3- C6)アルキル基、 ノヽロ(C厂 c6)アルキル基、 シクロハ口(c3_ C6)アルキル基、 (C厂 C6)アルコキシ基、 ハロ(C厂 c6)アルコキシ基、 (crc6)アルキ ルチオ基、 ハロ(cr C6)アルキルチオ基、 (C厂 c6)アルキルスルフィニル基、 ノヽロ (CrC6)アルキルスルフィニル基、 (C厂 C6)アルキルスルホニル基、 ハロ(C厂 c6)ァ ルキルスルホニル基、 (C厂 C6)アルキルカルボニル基、 ノ、口(Cf c6)アルキルカル ボニル基、 (CrC6)アルコキシカルボニル基、 カルボキシル基、 モノ (C厂 C6) ァ ルキルアミノカルボニル基、 同一又は異なっても良いジ (C厂 c6) アルキルアミ ノカルボ二ル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1〜 5個の置換基を有する置換フエニル基、 フエノキシ基、 同一又は異なっても良く、 ハロゲン原子、 ( - c6)アルキル基、 (c2- c6)アルケニル基、 (c2- c6)アルキニル基、 シク口(C3- C6)アルキノレ基、 ノヽロ(C厂 C6)ァノレキル基、 シクロハ口(C3- C6)ァノレキル 基、 (C厂 C6)アルコキシ基、 ハロ(C厂 C6)アルコキシ基、 (C厂 c6)アルキルチオ基、 ハロ(crc6)アルキルチオ基、 (C厂 c6)アルキルスルフィニル基、 ハロ(c! c6)アル キルスルフィニル基、 (CrC6)アルキルスルホニル基、 ノヽロ(C厂 c6)アルキノレスノレ ホニル基、 (CrC6)アルキルカルボニル基、 ハ口(c c6)アルキルカルボニル基、 (C厂 C6)アルコキシカルボニル基、 カルボキシル基、 モノ (C厂 C6) アルキルアミ ノカルボニル基、 同一又は異なっても良いジ (d-Ce) アルキルアミノカルボ二 ル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1〜 5個の置換 基を有する置換フヱノキシ基、 フエ二ルチオ基、 同一又は異なっても良く、 ハロ ゲン原子、 (C厂 c6)アルキル基、 (c2- c6)アルケニル基、 (c2- c6)アルキニル基、 シ
ク口(c3_ce)アルキル基、 ノヽ口(cr c6)アルキル基、 シクロハ口(c3- c6)アルキル基、Y may be the same or different, a halogen atom, (C t -C 6) alkyl group, (C 2 - C 6) § alkenyl group, (c 2 - C 6) alkynyl group, consequent opening (C 3 - C 6) alkyl group, halo (C厂c 6) Al kill group, Shikuroha port (C 3 - C 6) alkyl groups, (C厂C 6) alkoxy groups, halo (C厂C 6) alkoxy groups, (C Factory C 6 ) alkylthio group, halo (-C 6 ) alkylthio group, (CFactory c 6 ) alkinolesulfinyl group, nodro (C r C 6 ) alkylsulfinyl group, (CFactory c 6 ) alkylsulfonyl group, Halo (C factory c 6 ) alkylsulfonyl group, phenyl group, which may be the same or different, halogen atom, (C factory c 6 ) alkyl group, (c 2 -c 6 ) alkenyl group, (c 2 -c 6 ) Al Kiniru group, consequent opening (C 3 - C 6) alkyl group, Nono b (C厂c 6) alkyl group, Shikuroha port (c 3 _ C 6) alkyl groups, (C厂C 6) A Kokishi group, halo (C厂c 6) alkoxy groups, (c r c 6) alkyl thio groups, halo (c r C 6) alkylthio group, (C厂c 6) alkylsulfinyl group, Nono b (C r C 6 ) alkylsulfinyl groups, (C厂C 6) alkylsulfonyl groups, halo (C厂c 6) § alkylsulfonyl group, (C厂C 6) alkylcarbonyl group, Bruno, mouth (Cf c 6) alkyl Cal Boniru group, (C r C 6 ) alkoxycarbonyl group, carboxyl group, mono (C Factory C 6 ) alkylaminocarbonyl group, di (C Factory c 6 ) alkylaminocarbonyl group which may be the same or different, hydroxyl group, amino group, substituted phenyl group having from 1 to 5 substituents selected from Shiano group or a nitro group, phenoxy group, which may be identical or different, halogen atom, (- c 6) alkyl group, (c 2 - c 6) Alkenyl, (c 2 -c 6 ) alkynyl, Sik port (C 3 - C 6) Arukinore group, Nono b (C厂C 6) Anorekiru group, Shikuroha port (C 3 - C 6) Anorekiru group, (C厂C 6) alkoxy groups, halo (C厂C 6 ) Alkoxy group, (C factory c 6 ) alkylthio group, halo (c r c 6 ) alkylthio group, (C factory c 6 ) alkylsulfinyl group, halo (c! C 6 ) alkylsulfinyl group, (C r C 6) ) Alkylsulfonyl group, nodro (C Factory c 6 ) alkinoresphenolyl group, (C r C 6 ) alkyl carbonyl group, haguchi (cc 6 ) alkyl carbonyl group, (C factory C 6 ) alkoxycarbonyl group, carboxyl group, Mono (C Factory C 6 ) 1 to 5 selected from alkylaminocarbonyl groups, di (d-Ce) alkylaminocarbonyl groups, which may be the same or different, hydroxyl groups, amino groups, cyano groups or nitro groups Substituted phenoxy group, phenylthio group, May be one or different, such as a halogen atom, a (C factory c 6 ) alkyl group, a (c 2 -c 6 ) alkenyl group, a (c 2 -c 6 ) alkynyl group, (C 3 _c e ) alkyl group, ヽ (c r c 6 ) alkyl group, cycloha (c 3 -c 6 ) alkyl group,
(C厂 C6)アルコキシ基、 ハロ(C厂 C6)アルコキシ基、 (C厂 c6)アルキルチオ基、 ハロ (C厂 C6)アルキルチオ基、 (C厂 C6)アルキルスルフィニル基、 ハ口(C厂 cs)ァノレキノレ スルフィニル基、 (C厂 C6)アルキルスルホニル基、 ノヽロ (Cr c6)アルキルスルホ二 ル基、 (C厂 C6)アルキルカルボ二ル基、 ノヽロ (C厂 C6)アルキルカルボニル基、 (C厂 C6)アルコキシカルボ二ル基、 力ルポキシル基、 モノ (CfCe) アルキルアミノカ ルポ二ル基、 同一又は異なっても良いジ (C厂 c6) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1〜 5個の置換基を有 する置換フエ二ルチオ基、 フエニルスルフィニル基、 同一又は異なっても良く、 ハロゲン原子、 ( - c6)アルキル基、 (c2 - c6)アルケニル基、 (c2- c6)アルキニル基、 シク口(C3- C6)アルキル基、 ノヽ口(C厂 c6)アルキル基、 シクロハ口(c3- c6)アルキノレ 基、 (C厂 C6)アルコキシ基、 ハロ(Cf )アルコキシ基、 (C厂 c6)アルキルチオ基、 ノヽロ (CrC6)アルキルチオ基、 (C厂 C6)アルキルスルフィニル基、 ノヽロ(C厂 c6)アル キルスルフィニル基、 (CrC6)アルキルスルホニル基、 ノヽロ(C厂 c6)アルキルスル ホニル基、 (C厂 C6)アルキルカルポニル基、 ハロ(C厂 C6)アルキルカルボニル基、 (C厂 C6)アルコキシカルボニル基、 カルボキシル基、 モノ (C厂 c6) アルキルァミ ノカルポニル基、 同一又は異なっても良いジ (C厂 c6) アルキルアミノカルボ二 ル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1〜 5個の置換 基を有する置換フ ニルスルフィニル基、 フエニルスルホニル基、 同一又は異な つても良く、 ハロゲン原子、 ( -(:6)アルキル基、 (C2- C6)アルケニル基、 (C2- C6) アルキニル基、 シクロ(c3 - c6)アルキル基、 ノヽロ( - c6)アルキル基、 シクロハ口 (c3-c6)アルキル基、 (C厂 C6)アルコキシ基、 ノヽロ(C厂 C6)アルコキシ基、 (C厂 c6)ァ ルキルチオ基、 ノヽロ(C厂 C6)アルキルチオ基、 (C厂 c6)アルキルスルフィニル基、 ハロ(( )アルキルスルフィニル基、 (C厂 C6)アルキルスルホニル基、 ノヽロ(C厂 C6)アルキルスルホニル基、 (C - C6)アルキルカルボ二ル基、 ハロ(C - C6)アルキル カルボ二ル基、 (Cr C6)アルコキシカルボニル基、 カルボキシル基、 モノ (C - C6) アルキルアミノカルボニル基、 同一又は異なっても良いジ (C厂 c6) アルキル ァミノカルボニル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される(C Factory C 6 ) alkoxy group, halo (C Factory C 6 ) alkoxy group, (C Factory c 6 ) alkylthio group, halo (CFactory C 6 ) alkylthio group, (CFactory C 6 ) alkylsulfinyl group, Haguchi (C factory c s ) anolequinole sulfinyl group, (C factory C 6 ) alkyl sulfonyl group, nodro (Cr c 6 ) alkyl sulfonyl group, (C factory C 6 ) alkyl carbonyl group, nodro (C factory C 6 ) alkylcarbonyl group, (C Factory C 6 ) alkoxycarbonyl group, carbonyl group, mono (CfCe) alkylaminocarboxy group, di (C factory c 6 ) alkylamino which may be the same or different A substituted phenylthio group having 1 to 5 substituents selected from a carbonyl group, a hydroxyl group, an amino group, a cyano group or a nitro group, a phenylsulfinyl group, which may be the same or different, a halogen atom, (- c 6) alkyl group, (c 2 - c 6) alkenyl Le group, (c 2 - c 6) alkynyl group, consequent opening (C 3 - C 6) alkyl group, Nono port (C厂c 6) alkyl group, Shikuroha port (c 3 - c 6) Arukinore group, (C Factory C 6 ) alkoxy group, halo (Cf) alkoxy group, (C Factory c 6 ) alkylthio group, nodro (C r C 6 ) alkylthio group, (CFactory C 6 ) alkylsulfinyl group, nodro (CFactory c 6 ) Alkylsulfinyl group, (C r C 6 ) alkylsulfonyl group, nodro (CFactory c 6 ) alkylsulfonyl group, (CFactory C 6 ) alkylcarbonyl group, halo (CFactory C 6 ) alkylcarbonyl group , (C厂C 6) alkoxycarbonyl group, a carboxyl group, a mono (C厂c 6) Arukiruami Nokaruponiru group, the same or different and may di (C厂c 6) alkylamino carbonylation group, a hydroxyl group, an amino group, Substitution with 1 to 5 substituents selected from cyano or nitro Nils sulfinyl group, phenylpropyl sulfonyl group, the same or different connexion is good, a halogen atom, (- (- 6) alkyl, (C 2 - C 6) alkenyl, (C 2 - C 6) alkynyl, cyclo ( c 3 -c 6 ) alkyl group, nodro (-c 6 ) alkyl group, cyclohac (c 3 -c 6 ) alkyl group, (C Factory C 6 ) alkoxy group, nodro (CFactory C 6 ) alkoxy group , (C Factory c 6 ) alkylthio group, nodro (C Factory C 6 ) alkylthio group, (C Factory c 6 ) alkylsulfinyl group, halo (() alkylsulfinyl group, (CFactory C 6 ) alkylsulfonyl group, Nodro (C Factory C 6 ) alkylsulfonyl group, (C-C 6 ) alkyl carbonyl group, halo (C-C 6 ) alkyl carbonyl group, (C r C 6 ) alkoxycarbonyl group, carboxyl group, mono (C - C 6) alkylamino group may be the same or different (C厂c 6) alkyl § amino group, a hydroxyl group, an amino group, selected from Shiano group or a nitro group
1〜 5個の置換基を有する置換フエニルスルホニル基、 ( - C6)アルキルカルボ
ニル基、 ノ、口(C厂 C6)アルキルカルボニル基、 フエニルカルボニル基、 同一又は 異なっても良く、 ハロゲン原子、 (C厂 C6)アルキル基、 (C2-C6)アルケニル基、 (C2- C6)アルキニル基、 シクロ(C3 - C6)アルキル基、 ハロ(C厂 c6)アルキル基、 シクロハ 口(c3- c6)アルキル基、 (c厂 c6)アルコキシ基、 ハロ(c厂 gアルコキシ基、 (Cf c6) アルキルチオ基、 ノ、口(C,-C6)アルキルチオ基、 (CrC6)アルキルスルフィニル基、 ノヽロ(C厂 C6)アルキルスルフィニル基、 (C厂 c6)アルキルスルホニル基、 ノヽロ( - C6)アルキルスルホニル基、 (C厂 c6)アルキルカルポニル基、 ノヽロ( - c6)アルキル カルボ二ル基、 (Cf C6)アルコキシカルボニル基、 カルボキシル基、 モノ (C厂 C6) アルキルアミノカルボニル基、 同一又は異なっても良いジ (C厂 c6) アルキル ァミノカルボニル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1 〜 5個の置換基を有する置換フエ二ルカルポニル基、 (C厂 C6)アルコキシカル ボニル基、 カルボキシル基、 モノ (crc6) アルキルアミノカルボニル基、 同一 又は異なっても良いジ (Cf c6) アルキルアミノカルボニル基、 フエニルァミノ カルポニル基、 同一又は異なっても良く、 ハロゲン原子、 (c厂 gアルキル基、 (C2-C6)アルケニル基、 (C2- C6)アルキニル基、 シクロ(C3 - C6)アルキル基、 ノヽロSubstituted phenylalanine sulfonyl group having from 1 to 5 substituents, (- C 6) alkyl-carbonitrile Nyl group, H, mouth (C Factory C 6 ) alkylcarbonyl group, phenylcarbonyl group, which may be the same or different, halogen atom, (C Factory C 6 ) alkyl group, (C 2 -C 6 ) alkenyl group, (C 2 -C 6 ) alkynyl group, cyclo (C 3 -C 6 ) alkyl group, halo (C 3 c 6 ) alkyl group, cyclohalo (c 3 -c 6 ) alkyl group, (c 3 c 6 ) alkoxy Group, halo (c factory g alkoxy group, (Cf c 6 ) alkylthio group, no, mouth (C, -C 6 ) alkylthio group, (C r C 6 ) alkylsulfinyl group, nodro (C factory C 6 ) alkyl Sulfinyl group, (C factory c 6 ) alkyl sulfonyl group, nodro (-C 6 ) alkyl sulfonyl group, (C factory c 6 ) alkyl carbonyl group, noduro (-c 6 ) alkyl carbonyl group, (Cf C 6) alkoxycarbonyl group, a carboxyl group, a mono (C厂C 6) alkylaminocarbonyl group, the Or different and may di (C厂c 6) alkyl § amino group, a hydroxyl group, an amino group, a substituted phenylene Rukaruponiru group having 1 to 5 substituents selected from Shiano group or a nitro group, (C厂C 6) Arukokishikaru Boniru group, a carboxyl group, a mono (c r c 6) alkylaminocarbonyl group, the same or different and may di (Cf c 6) alkylaminocarbonyl group, Fueniruamino Karuponiru group, which may be the same or different , Halogen atom, (c-g-alkyl group, (C 2 -C 6 ) alkenyl group, (C 2 -C 6 ) alkynyl group, cyclo (C 3 -C 6 ) alkyl group, nodro
(CrCe)アルキル基、 シクロハ口(c3- c6)アルキル基、 (cr c6)アルコキシ基、 ハロ (^-(:6)アルコキシ基、 (C厂 C6)アルキルチオ基、 ノヽロ(C厂 c6)アルキルチオ基、 (CrC6)アルキルスルフィニル基、 ハロ(C厂 C6)アルキルスルフィニル基、 (C厂 c6) アルキルスルホニル基、 ノ、口(C厂 c6)アルキルスルホニル基、 (crc6)アルキル力 ルポニル基、 ハロ(CrC6)アルキルカルボニル基、 (C厂 C6)アルコキシカルボニル 基、 カルボキシル基、 モノ (C!- C6) アルキルアミノカルボニル基、 同一又は異 なっても良いジ (C厂 c6) アルキルアミノカルポニル基、 水酸基、 アミノ基、 シ ァノ基又はニトロ基から選択される 1 〜 5個の置換基を環上に有する置換フエ二 ルァミノカルボニル基、 フエニル (C厂 c6) アルキルァミノカルボニル基、 同一 又は異なっても良く、 ハロゲン原子、 (C厂 C6)アルキル基、 (C2- C6)アルケニル基、 (C2 - C6)アルキニル基、 シクロ(C3- C6)アルキル基、 ハロ(C厂 c6)アルキル基、 シク ロハ口(C3-C6)アルキル基、 (C厂 c6)アルコキシ基、 ハロ(cr c6)アルコキシ基、 ((^ - C6)アルキルチオ基、 ノ、口(C,- CB)アルキルチオ基、 (C!- )アルキルスルフィ ニル基、 ノヽロ(C C6)アルキルスルフィニル基、 (C厂 ce)アルキルスルホニル基、
ノヽロ(d - C6)アルキルスルホニル基、 (C厂 C6)アルキルカルボニル基、 ハロ(C厂 c6) アルキルカルボニル基、 (c「c6)アルコキシカルボニル基、 カルボキシル基、 モ ノ (C厂 c6) アルキルアミノカルボニル基、 同一又は異なっても良いジ (crc6) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選 択される 1 〜 5個の置換基から選択される 1以上の置換基を環上に有する置換フ ェニル (CfCe) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シァノ基又 はニトロ基から選択される 1 〜 5個の置換基を示す。 又、 Yはベンゼン環上の隣 接する炭素原子と一緒になつて、 同一又は異なっても良く、 酸素原子、 硫黄原子 又は窒素原子 (該窒素原子は水素原子、 (C厂 C6)アルキル基、 (C2- C6)アルケニル 基、 (c2- c6)アルキニル基又はシクロ(c3- c6)アルキル基によって置換されていて も良い。 ) から選択される 1乃至 2個のへテロ原子により中断されても良い(d- C4)アルキレン基により 5乃至 6員環を形成しても良い。 } (CRCE) alkyl group, Shikuroha port (c 3 - c 6) alkyl group, (c r c 6) alkoxy groups, halo (^ - (6) alkoxy groups, (C厂C 6) alkylthio group, Nono b ( C Factory c 6 ) alkylthio group, (C r C 6 ) alkyl sulfinyl group, halo (C Factory C 6 ) alkyl sulfinyl group, (C Factory c 6 ) alkyl sulfonyl group, no, mouth (C Factory c 6 ) alkyl sulfonyl Group, (c r c 6 ) alkyl force luponyl group, halo (C r C 6 ) alkylcarbonyl group, (C factory C 6 ) alkoxycarbonyl group, carboxyl group, mono (C! -C 6 ) alkylaminocarbonyl group, May be the same or different. (C Factory 6 ) Substituted phenyl having 1 to 5 substituents on the ring selected from an alkylaminocarbonyl group, a hydroxyl group, an amino group, a cyano group or a nitro group. Rua amino carbonyl group, phenyl (C厂c 6) alkyl § Mino Cal Group, which may be identical or different, halogen atom, (C厂C 6) alkyl groups, (C 2 - C 6) alkenyl, (C 2 - C 6) alkynyl, cyclo (C 3 - C 6) Alkyl group, halo (C factory c 6 ) alkyl group, cycloha (C 3 -C 6 ) alkyl group, (C factory c 6 ) alkoxy group, halo (c r c 6 ) alkoxy group, ((^ -C 6) alkylthio group, Bruno, mouth (C, - C B) alkylthio groups, (C -!) alkyl sulfide group, Nono b (CC 6) alkylsulfinyl group, (C厂c e) an alkylsulfonyl group, Nodro (d-C 6 ) alkylsulfonyl group, (C Factory C 6 ) alkylcarbonyl group, halo (C Factory c 6 ) alkylcarbonyl group, (c “c 6 ) alkoxycarbonyl group, carboxyl group, mono (C厂c 6) alkylaminocarbonyl group, the same or different and may di (c r c 6) alkylaminocarbonyl group, a hydroxyl group, an amino group, from 1 to 5 substituents selected from Shiano group or a nitro group Substituted phenyl (CfCe) having at least one selected substituent on the ring represents 1 to 5 substituents selected from an alkylaminocarbonyl group, a hydroxyl group, an amino group, a cyano group or a nitro group. And Y may be the same as or different from adjacent carbon atoms on the benzene ring, and may be an oxygen atom, a sulfur atom, or a nitrogen atom (the nitrogen atom is a hydrogen atom, a (C Factory C 6 ) alkyl group, C 2 - C 6) Al Group, may be interrupted by - - (c 6 c 3) 1 to hetero atoms two of the selected from may) be substituted by an alkyl group (c 2 c 6) alkynyl group or a cycloalkyl. A (d-C 4 ) alkylene group may form a 5- or 6-membered ring.
で表されるハロアルキルスルホンァニリ ド誘導体又はその塩類及び該化合物を含 有する除草剤並びにその使用方法に関するものである。 And a herbicide containing the compound, and a method for using the same.
発明を実施するための形態 BEST MODE FOR CARRYING OUT THE INVENTION
本発明のハロアルキルスルホンァニリ ド誘導体の一般式 (I ) 及ぴ Q— 1 〜Q 一 1 4の定義において、 「ハロゲン原子」 とは塩素原子、 臭素原子、 沃素原子又 はフッ素原子を示す。 「( - C6)アルキレン基」 はメチレン、 エチレン、 プロピ レン、 トリメチレン、 ジメチノレメチレン、 テトラメチレン、 ィソプチレン、 ジメ チルエチレン、 へキサメチレン等の直鎖又は分岐鎖状の炭素原子数 1 〜 6個のァ ノレキレン基を示し、 「(c2-c6)アルケニレン基」 又は 「(c2 - c6)アルキニレン基」 は同様に直鎖又は分岐鎖状の炭素原子数 1 〜 6個のアルケニレン基又はアルキニ レン基を示す。 「(CrC6)アルキル基」 とは、 例えばメチル、 ェチル、 n—プロ ピル、 i—プロピル、 n—ブチル、 i—ブチル、 s—プチル、 t—プチル、 n— ペンチル、 ネオペンチル、 n —へキシル等の直鎖又は分鎖状の炭素原子数 1 〜 6 個のアルキル基を示す。 「(: - )ハロアルキル基」 とは、 同一又は異なっても 良い 1以上のハロゲン原子により置換された直鎖又は分岐鎖状の炭素原子数 1 〜 6個のアルキル基を示し、 例えばトリフルォロメチル、 ジフルォロメチル、 パ一 フノレオロェチノレ、 パーフルォロイソプロピノレ、 クロロメチル、 プロモメチノレ、 1
2003/009405 In the definition of the general formula (I) and Q-1 to Q-14 of the haloalkylsulfonanilide derivative of the present invention, the "halogen atom" represents a chlorine atom, a bromine atom, an iodine atom or a fluorine atom. The “(-C 6 ) alkylene group” is a linear or branched C 1-6 alkylene such as methylene, ethylene, propylene, trimethylene, dimethylenolethylene, tetramethylene, isoptylene, dimethylethylene, and hexamethylene. indicates § Norekiren group, "(c 2 -c 6) alkenylene group" or "(c 2 - c 6) alkynylene group" is likewise linear or branched alkenylene group having 1 to 6 carbon atoms or Represents an alkynylene group. “(C r C 6 ) alkyl group” means, for example, methyl, ethyl, n-propyl, i-propyl, n-butyl, i-butyl, s-butyl, t-butyl, n-pentyl, neopentyl, n — Represents a linear or branched alkyl group having 1 to 6 carbon atoms such as hexyl. “(:−) haloalkyl group” means a straight or branched alkyl group having 1 to 6 carbon atoms, which may be the same or different and may be substituted with one or more halogen atoms. Methyl, difluoromethyl, phenololenoethyl, perfluoroisopropinole, chloromethyl, bromomethinole, 1 2003/009405
9 9
—ブロモェチル、 2 , 3—ジブロモプロピル等を示す。 「(C3- C6)シクロアルキ ノレ基」 とは、 シクロプロピノレ、 シクロプチノレ、 シクロペンチノレ、 シクロへキシノレ、 2—メチルシク口プロピル、 2—メチルシク口ペンチル等の炭素原子数 3 〜 6個 の脂環式アルキル基を示す。 —Bromoethyl, 2,3-dibromopropyl and the like. “(C 3 -C 6 ) cycloalkynole group” refers to an alicyclic group having 3 to 6 carbon atoms such as cyclopropynole, cycloptynole, cyclopentynole, cyclohexynole, 2-methylcyclopentyl, and 2-methylcyclopentyl. Shows a formula alkyl group.
「(C厂 C6)アルコキシ基」 とは、 例えばメ トキシ、 エトキシ、 n—プロポキシ、 イソプロポキシ、 n—ブトキシ、 s一ブトキシ、 t一ブトキシ、 n—ペンチノレオ キシ、 イソペンチルォキシ、 ネオペンチルォキシ、 n—へキシルォキシ等の直鎖 又は分岐鎖状の炭素原子数 1 〜 6個のアルコキシ基を示す。 「ハロ(Cr )アル コキシ基」 とは、 同一又は異なっても良レ、 1以上のハロゲン原子により置換され た直鎖又は分岐鎖状の炭素原子数 1 〜 6個のアルキル基を示し、 例えばジフルォ ロメ トキシ、 トリフルォロメ トキシ、 2, 2 , 2—トリフルォロェトキシ等を示 す。 「 (CrC6)アルコキシカルボニル基」 とは、 例えばメ トキシカルボニル、 ェ トキシカノレポ二ノレ、 n—プロポキシカノレポ二ノレ、 ィソプロポキシカノレボニノレ、 n ーブトキシカルポニル、 tーブトキシカルボニル等の直鎖又は分岐鎖状の炭素原 子数 1 〜 6個のアルコキシ力ルポ二ル基を示す。 「(C厂 C6)アルキルチオ基」 と は、 例えばメチルチオ、 ェチルチオ、 n—プロピルチオ、 イソプロピルチオ、 n ーブチルチオ、 s —プチルチオ、 t—プチルチオ、 n—ペンチルチオ、 イソペン チルチオ、 n —へキシルチオ等の直鎖又は分岐鎖状の炭素原子数 1 〜 6個のアル キルチオ基を示す。 「( - )アルキルスルフィエル基」 とは、 例えばメチルス ノレフィ二ノレ、 ェチノレスノレフィ二ノレ、 n一プロピノレスノレフィ二ノレ、 ィソプロピノレス ノレフィ二ノレ、 n—ブチノレスノレフィ二ノレ、 sーブチノレスルフィ二ノレ、 tーブチノレス ノレフィニノレ、 n—ペンチノレスノレフィ二ノレ、 ィソペンチルスノレフィ二ノレ、 n —へキ シルスルフィニル等の直鎖又は分岐鎖状の炭素原子数 1 〜 6個のアルキルスルフ ィニル基を示す。 「(C厂 C6)アルキルスルホニル基」 とは、 例えばメチルスルホ ニル、 ェチノレスノレホニル、 n—プロピノレスルホニノレ、 イソプロピルスノレホニノレ、 n—ブチノレスノレホニル、 s—ブチノレスノレホニル、 tーブチノレスノレホニノレ、 n—ぺ ンチノレスルホニノレ、 イソペンチルスノレホニル、 n—へキシノレスルホニノレ等の直鎖 又は分岐鎖状の炭素原子数 1 〜 6個のアルキルスルホ二ル基を示す。 “(C Factory C 6 ) alkoxy group” means, for example, methoxy, ethoxy, n-propoxy, isopropoxy, n-butoxy, s-butoxy, t-butoxy, n-pentinoleoxy, isopentyloxy, neopentyl A linear or branched alkoxy group having 1 to 6 carbon atoms such as oxy, n-hexyloxy and the like. The term “halo (Cr) alkoxy group” refers to a straight or branched alkyl group having 1 to 6 carbon atoms substituted by one or more halogen atoms, which may be the same or different. Difluoromethoxy, trifluoromethoxy, 2,2,2-trifluoroethoxy, etc. “(C r C 6 ) alkoxycarbonyl group” means, for example, methoxycarbonyl, ethoxycanoleponinole, n-propoxycanoleponinole, isopropoxycanoleboninole, n-butoxycarbonyl, t-butoxycarbonyl, etc. It represents a linear or branched alkoxy group having 1 to 6 carbon atoms. "(C Factory C 6 ) alkylthio group" means, for example, methylthio, ethylthio, n-propylthio, isopropylthio, n-butylthio, s-butylthio, t-butylthio, n-pentylthio, isopentylthio, n-hexylthio, etc. It represents a chain or branched alkylthio group having 1 to 6 carbon atoms. "(-) Alkyl sulfier group" means, for example, methylsorefininole, ethinolesnorefinole, n-propinoresorefininole, isopropinoles norefininole, n-butinoresorefininole , S-butynolesulfininole, t-butynoles norefininole, n —pentinolesnorefininole, isopentylsnorefininole, n —hexylsulfinyl and other straight or branched chain carbon atoms Represents 1 to 6 alkylsulfinyl groups. “(C Factory C 6 ) alkylsulfonyl group” means, for example, methylsulfonyl, ethynolesnorefonyl, n-propynolesulfoninole, isopropylsnolehoninole, n-butynolesnorefonyl, s-butino Straight or branched chain carbon atoms of 1 to 6 such as lesnolephonyl, t-butinoresolephoninole, n-pentinoresulfonolone, isopentylsnorefonyl, and n-hexinolesulfoninole Alkylsulfonyl groups.
Qの定義の 「構成原子の少なくとも 1個が窒素原子であり、 かつその窒素原子
が Aとの結合部位となるヘテロ環」 とは、 Aとの結合位置が窒素原子であってそ の窒素原子を含む 4〜1 3員へテロ環を示し、 当該へテロ環は 4〜 8員へテロ環 にさらにベンゼン環又は 4〜 7員へテロ環が縮合した縮合環を含む。 また、 へテ 口環の構成原子には 1又は複数の窒素原子の他に酸素原子、 硫黄原子、 燐原子等 他のへテロ原子を含むことができる。 Qとしては、 例えば In definition of Q, "at least one of the constituent atoms is a nitrogen atom, and the nitrogen atom Is a 4- to 13-membered hetero ring in which the bonding position with A is a nitrogen atom and contains the nitrogen atom, and the hetero ring is 4 to 8 A condensed ring in which a benzene ring or a 4 to 7-membered hetero ring is further condensed to a membered hetero ring. In addition, the heterocyclic ring may include, in addition to one or more nitrogen atoms, other heteroatoms such as an oxygen atom, a sulfur atom, and a phosphorus atom. As Q, for example
Q-1 Q-2 Q-3 Q-5 Q-1 Q-2 Q-3 Q-5
Q-6 Q-7 Q-8 Q-9 Q-6 Q-7 Q-8 Q-9
Q-10 Q-11 Q-12 Q-13 Q-14 Q-10 Q-11 Q-12 Q-13 Q-14
{式中、 G G2は同一又は異なっても良く、 酸素原子、 硫黄原子、 N— R3' (式中、 R3' は水素原子、 (C厂 C6) アルキル基、 シァノ基、 ニトロ基、 フエ二 ル (CfC6)アルキル基、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1以上の置換基を環上に有する置換フエニル (C厂 C6)アルキル基、 フエニル基又は同一若しくは異なっても良く、 Υ, (Υ, は後記に示す。 ) から
選択される 1以上の置換基を有する置換フ 二ル基を示す。 ) 、 N— O R4 '{Wherein GG 2 may be the same or different; oxygen atom, sulfur atom, N—R 3 ′ (wherein, R 3 ′ is a hydrogen atom, (C Factory C 6 ) alkyl group, cyano group, nitro group And a phenyl (CfC 6 ) alkyl group, which may be the same or different, and have a substituted phenyl (C Factory C 6) having at least one substituent selected from Υ ′ (where Υ ′ is described below) on the ring. ) Alkyl group, phenyl group or the same or different, and Υ, (Υ, are shown below) It represents a substituted furyl group having one or more substituents selected. ), N—OR 4 '
(式中、 R'1' は水素原子、 ((厂 C6) アルキル基、 フヱニル (C厂 C6)アルキル基又 は同一若しくは異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1 以上の置換基を環上に有する置換フエニル (C厂 C6)アルキル基を示す。 ) 、 N— N R5' R6' (式中、 R5 ' 及び R6' は同一又は異なっても良く、 水素原子、 フ ニル基又は同一若しくは異なっても良く、 Υ ' (Υ ' は後記に示す。 ) 力 ^選 択される 1以上の置換基を有する置換フユ二ル基を示す。 又、 R5' と R6' は一 緒になって (C3 - C6) アルキレン基を示すこともできる。 ) 又は C R7R8 (式中、 R7及び R8は同一又は異なっても良く、 水素原子、 (C厂 C6) アルキル基、 (C厂 C6) アルコキシカルボニル基、 シァノ基又はニトロ基を示す。 ) を示す。 (In the formula, R ′ 1 ′ may be a hydrogen atom, a ((C 6 C) alkyl group, a phenyl (C C 6 ) alkyl group or may be the same or different, and Υ ′ (Υ ′ will be described later.)) Represents a substituted phenyl (C Factory C 6 ) alkyl group having at least one substituent selected from the group consisting of the following:), N—NR 5 ′ R 6 ′ (wherein, R 5 ′ and R 6 ′ are the same) Or a hydrogen atom, a phenyl group, or a substituted or unsubstituted phenyl group having one or more substituents, which may be the same or different, and R 5 ′ and R 6 ′ may be taken together to represent a (C 3 -C 6 ) alkylene group, or CR 7 R 8 (wherein R 7 and R 8 are the same or It may be different, and represents a hydrogen atom, (C Factory C 6 ) alkyl group, (C Factory C 6 ) alkoxycarbonyl group, cyano group or nitro group.
J 1は酸素原子、 硫黄原子又は N— R9 (式中、 R9は水素原子、 ( - C6) アルキ ル基、 フエニル (C厂 C6) アルキル基、 同一又は異なっても良く、 Υ, (Υ, は 後記に示す。 ) から選択される 1以上の置換基を環上に有する置換フエニル (CrC6) アルキル基、 フエ二ル基、 同一又は異なっても良く、 Y ' (Y, は後 記に示す。 ) 力 ら選択される 1以上の置換基を有する置換フユニル基、 複素環基 (複素環基は請求項 2に同じ。 ) 、 同一又は異なっても良く、 Υ ' (Υ ' は後記 に示す。 ) 力 ら選択される 1以上の置換基を有する置換複素環基 (複素環基は前 記に同じ。 ) 、 複素環 (C )アルキル基 (複素環基は前記に同じ。 ) 、 同一又 は異なっても良く、 γ ' (Υ ' は後記に示す。 ) から選択される 1以上の置換基 を環上に有する置換複素環(Ci-Cs)アルキル基 (複素環基は前記に同じ。 ) 、 モ ノ (C厂 C6) アルキルアミノカルボニル基、 同一又は異なっても良いジ (Cf ) アルキルアミノカルボニル基、 フエニルァミノカルボニル基又は同一若しくは異 なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1以上の置換基を環 上に有する置換フエニルァミノカルボ二ル基を示す。 ) を示す。 J 1 is an oxygen atom, a sulfur atom, or N—R 9 (wherein R 9 is a hydrogen atom, a (-C 6 ) alkyl group, a phenyl (C-Factory C 6 ) alkyl group, which may be the same or different; , (Υ, are shown below), a substituted phenyl (C r C 6 ) alkyl group having at least one substituent selected from the following on the ring, a phenyl group, which may be the same or different, and Y ′ ( Y and are described below.) A substituted fuunyl group having one or more substituents selected from the group consisting of a heterocyclic group and a heterocyclic group (the heterocyclic group is the same as in claim 2) may be the same or different. (Υ 'is shown below.) A substituted heterocyclic group having one or more substituents selected from the group consisting of a heterocyclic group (the same applies to the above-mentioned heterocyclic group), a heterocyclic (C) alkyl group (the heterocyclic group is The same as or different from the above, and a substituted heterocyclic group having at least one substituent selected from γ ′ (Υ ′ is described below) on the ring. (Ci-Cs) alkyl group (the heterocyclic group is as defined above.), Mono (C厂C 6) alkylaminocarbonyl group, the same or different and may di (Cf) alkylaminocarbonyl group, Fueniruamino A carbonyl group or a substituted or unsubstituted phenylaminocarbonyl group having at least one substituent selected from Υ ′ (Υ ′ is shown below) which may be the same or different. Show.
J 2及び J 3は同一又は異なっても良く、 酸素原子、 硫黄原子、 N— R9 (式中、 R9は前記に同じ。 ) 、 R 1Q— C— R11 (式中、 R 1Q及ぴ R 11は同一又は異なっても 良く、 水素原子、 (c!- アルキル基、 ハロ(C厂 Cs)アルキル基、 (C厂 C6)アルコキ シ基、 ハロ(C厂 C6)アルコキシ基、 ( -(:6)アルキルチオ基、 ハロ(C厂 C6)アルキル チォ基、 (C厂 C6)アルキルスルフィニル基、 ハロ(CrC6)アルキルスルフィニル基、
(C厂 C6)アルキルスルホニル基、 ノヽロ(CrC6)アルキルスルホニル基、 フエニル(C厂 C6)アルキル基、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) 力 ^選 択される 1以上の置換基を環上に有する置換フエニル (C厂 c6)アルキル基、 フエ ニル基又は同一若しくは異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択 される 1以上の置換基を有する置換フエ二ル基を示す。 ) 、 。= 0又は。== 3を 示す。 J 2 and J 3 may be the same or different, and include an oxygen atom, a sulfur atom, N—R 9 (wherein R 9 is as defined above), R 1Q —C—R 11 (wherein R 1Q and Pi R 11 may be the same or different, a hydrogen atom, (c -! alkyl group, halo (C厂C s) alkyl group, (C厂C 6) an alkoxy group, halo (C厂C 6) alkoxy group , (- (- 6) alkylthio groups, halo (C厂C 6) alkyl Chiomoto, (C厂C 6) alkylsulfinyl groups, halo (C r C 6) alkylsulfinyl group, (C Factory C 6 ) alkylsulfonyl group, nodro (C r C 6 ) alkylsulfonyl group, phenyl (C Factory C 6 ) alkyl group, which may be the same or different, and Υ Υ (Υ 示 す is described later) A substituted phenyl (C Factory 6 ) alkyl group having one or more substituents selected on the ring, a phenyl group or the same or different, and Υ Υ (Υ 示 す is shown below) It represents a substituted phenyl group having one or more substituents selected. ),. = 0 or. == 3 is shown.
J 4及ぴ J 5は同一又は異なっても良く、 C— R12 (式中、 R12は水素原子、 ハロ ゲン原子、 (C厂 C6)アルキル基、 ハロ(C厂 C6)アルキル基、 (C厂 C6)アルコキシ基、 ハ口(C厂 C6)アルコキシ基、 (Cf C6)アルキルチオ基、 ハ口(C厂 C6)アルキルチオ基、 (CfCs)アルキルスルフィニル基、 ノヽロ(C厂 c6)アルキルスルフィニル基、 (cr c6) アルキノレスノレホニル基、 ノヽロ(C厂 C6)ァノレキルスルホ二ノレ基、 フエニル(C厂 c6)ァ ルキル基、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択され る 1以上の置換基を環上に有するフエニル(C厂 c6)アルキル基、 フエニル基、 同 一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1以上の置 換基を有する置換フヱニル基又はシァノ基を示す。 ) 又は窒素原子を示す。 J 4 and J 5 may be the same or different, and C—R 12 (where R 12 is a hydrogen atom, a halogen atom, a (C Factory C 6 ) alkyl group, a halo (C Factory C 6 ) alkyl group , (C Factory C 6 ) alkoxy group, Haguchi (CFactory C 6 ) alkoxy group, (Cf C 6 ) alkylthio group, Haguchi (CFactory C 6 ) alkylthio group, (CfCs) alkylsulfinyl group, nodro ( C factory c 6 ) alkylsulfinyl group, (c r c 6 ) alkynolesnorefonyl group, nodro (C factory C 6 ) anorecylsulfoninole group, phenyl (C factory c 6 ) alkyl group, same or different And a phenyl (C Factory c 6 ) alkyl group having at least one substituent selected from Υ ′ (Υ ′ is described below) on the ring, a phenyl group, which may be the same or different; Represents a substituted phenyl group or a cyano group having one or more substituents selected from Υ ′ (where 示 す ′ is described below), or nitrogen. Indicating the atom.
J 6は酸素原子、 硫黄原子、 N_ R9 (式中、 R9は前記に同じ。 ) 又は R1Q— C 一 R11 (式中、 Rll)及び R"は前記に同じ。 ) を示す。 J 6 represents an oxygen atom, a sulfur atom, N_R 9 (where R 9 is the same as described above), or R 1Q —C 1 R 11 (where R ll) and R ″ are the same as described above). .
R9は前記に同じ。 R 9 is the same as above.
R13及び Rwは同一又は異なっても良く水素原子、 ハロゲン原子、 (C厂 C6) 了 ルキル基、 ハロ(C厂 C6)アルキル基、 (C厂 C6)アルコキシ基、 ハロ(C「C6)アルコキ シ基、 (C厂 C6)アルキルチオ基、 ハロ(C厂 C6)アルキルチオ基、 (C厂 C6)アルキルス ルフィニル基、 ノヽ口 (C厂 C6)アルキルスルフィニル基、 (CrC6)アルキルスルホ二 ル基、 ハロ(C厂 C6)アルキルスルホニル基、 フエニル(Cr C6)アルキル基、 同一又 は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1以上の置換基 を環上に有する置換フヱニル (C厂 C6)アルキル基、 フエニル基、 同一又は異なつ ても良く、 Υ ' (Υ ' は後記に示す。 ) カ ら選択される 1以上の置換基を有する 置換フエニル基、 複素環基 (複素環基は前記に同じ。 ) 、 同一又は異なっても良 く、 Υ, (Υ ' は後記に示す。 ) から選択される 1以上の置換基を有する置換複 素環基 (複素環基は前記に同じ。 ) 、 複素環 (C厂 C6)アルキル基 (複素環基は前
記に同じ。 ) 、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択 される 1以上の置換基を環上に有する置換複素環 (C厂 c6)アルキル基 (複素環基 は前記に同じ。 ) 、 モノ ( -(]6) アルキルアミノカルボニル基、 同一又は異な つても良いジ (crc6) アルキルァミノカルボニル基、 フエニルァミノカルボ二 ル基、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1 以上の置換基を環上に有する置換フエニルァミノカルボニル基又はシァノ基を示 す。 R 13 and R w may be the same or different, and may be a hydrogen atom, a halogen atom, a (C Factory C 6 ) alkyl group, a halo (C Factory C 6 ) alkyl group, a (C Factory C 6 ) alkoxy group, a halo (C "C 6 ) alkoxy group, (C Factory C 6 ) alkylthio group, halo (C Factory C 6 ) alkylthio group, (C Factory C 6 ) alkylsulfinyl group, ヽ 口 (CFactory C 6 ) alkylsulfinyl group, A C r C 6 ) alkylsulfonyl group, a halo (C Factory C 6 ) alkylsulfonyl group, a phenyl (C r C 6 ) alkyl group may be the same or different, and Υ (Υ) is described below. ) (C Factory C 6 ) alkyl group, phenyl group having one or more substituents on the ring, which may be the same or different, and Υ ′ (Υ ′ is shown below). A substituted phenyl group having one or more substituents selected, a heterocyclic group (the heterocyclic group is as defined above), the same or Is also rather good, Upsilon, (Upsilon 'is shown later.) Substituted double heterocyclic group having one or more substituents selected from (heterocyclic group as defined above.), A heterocyclic (C 厂 C 6 ) alkyl group (heterocyclic group Same as above. ), Which may be the same or different, and a substituted heterocyclic (C Factory c 6 ) alkyl group having at least one substituent selected from Υ ′ (Υ ′ is described below) on the ring (where the heterocyclic group is the same), mono. (- (] 6) alkylaminocarbonyl group, the same or different connexion also good di (c r c 6) alkyl § amino group, phenylpropyl § amino carbonylation group, the same or different And represents a substituted phenylaminocarbonyl group or a cyano group having at least one substituent selected from Υ ′ (Υ ′ is described below) on the ring.
R15及ぴ R16は同一又は異なっても良く、 水素原子又は(C厂 C6)アルキル基を示 す。 R 15 and R 16 may be the same or different and represent a hydrogen atom or a (C Factory C 6 ) alkyl group.
X ' は同一又は異なっても良く、 水素原子、 ハロゲン原子、 (Cf c6)アルキル 基、 (c2- c6)アルケニル基、 (c2- gアルキニル基、 シクロ(c3- c7)アルキル基、 ノヽ 口(c厂 c6)アルキル基、 シクロハ口(c3- 7)アルキル基、 (c厂 c6)アルコキシ基、 ハロX ′ may be the same or different, and include a hydrogen atom, a halogen atom, a (Cfc 6 ) alkyl group, a (c 2 -c 6 ) alkenyl group, a (c 2 -g alkynyl group, a cyclo (c 3 -c 7 ) alkyl group, Nono port (c厂c 6) alkyl group, Shikuroha port (c 3 - 7) alkyl group, (c厂c 6) alkoxy groups, halo
(CrC6)アルコキシ基、 (C厂 C6)アルキルチオ基、 ハ口(C厂 c6)アルキルチオ基、(C r C 6 ) alkoxy group, (C factory C 6 ) alkylthio group, haguchi (C factory c 6 ) alkylthio group,
(C厂 c6)ァノレキノレスノレフィ二ノレ基、 ノヽ口 (crc6)ァノレキルスノレフィニル基、 (crc6) ァノレキルスルホニル基、 ノヽロ(C厂 C6)アルキルスルホ二ノレ基、 フエ二ノレ基、 同一 又は異なっても良く、 γ ' (Υ ' は後記に示す。 ) 力 ら選択される 1以上の置換 基を有する置換フエニル基、 フエノキシ基、 同一又は異なっても良く、 Υ,(C factory c 6 ) anorequinoles refininole group, phenol (c r c 6 ) anore cyls norefinyl group, (c r c 6 ) anorekylsulfonyl group, phenol (C factory C 6 ) an alkylsulfonyl group, a phenyl group, the same or different, and a substituted phenyl group, a phenoxy group having one or more substituents selected from γ ′ (Υ ′ is described below). May be the same or different;
(Υ ' は後記に示す。 ) から選択される 1以上の置換基を有する置換フヱノキシ 基、 フヱ二ルチオ基、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) か ら選択される 1以上の置換基を有する置換フエ二ルチオ基、 フエニルスルフィ二 ル基、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1 以上の置換基を有する置換フ ニルスルフィニル基、 フ ニルスルホニル基、 同 一又は異なっても良く、 γ ' (γ, は後記に示す。 ) から選択される 1以上の置 換基を有する置換フ ニルスルホニル基、 (c c6)アルキルカルボニル基、 ノヽロ (C厂 C6)アルキルカルボ二ル基、 フエニルカルボニル基、 同一又は異なっても良 く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1以上の置換基を有する置換フ ェニルカルボニル基、 (Cf )アルコキシカルボニル基、 カルボキシル基、 モノ(Υ ′ is described below.) A substituted phenoxy group having at least one substituent selected from the group consisting of phenylthio groups, which may be the same or different, and Υ ′ (Υ ′ is described later). A substituted phenylthio group or phenylsulfuryl group having one or more substituents selected, which may be the same or different, and one or more substituents selected from Υ ′ (where Υ ′ is shown below) A substituted phenylsulfinyl group, a phenylsulfonyl group, a phenylsulfonyl group which may be the same or different and has one or more substituents selected from γ ′ (γ, is shown below), (Cc 6 ) alkylcarbonyl group, nodro (C Factory C 6 ) alkylcarbonyl group, phenylcarbonyl group, which may be the same or different, and are selected from Υ ′ (Υ ′ is shown below). Substituted phenylcarbonyl group having one or more substituents (Cf) alkoxycarbonyl group, a carboxyl group, a mono
(C厂 c6) アルキルアミノカルボニル基、 同一又は異なっても良いジ ((: c6) ァ ルキルアミノカルボニル基、 フエニルァミノカルボニル基、 同一又は異なっても
良く、 Y ' (Υ ' は後記に示す。 ) 力 ら選択される 1以上の置換基を環上に有す る置換フエニルァミノカルボニル基、 フエニル (C厂 c6) アルキルアミノカルボ 二ノレ基、 同一又は異なっても良く、 Υ, (Υ ' は後記に示す。 ) から選択される(C factory c 6 ) alkylaminocarbonyl group, same or different di ((: c 6 ) alkylaminocarbonyl group, phenylaminocarbonyl group, same or different A substituted phenylaminocarbonyl group having one or more substituents selected from the group consisting of Y ′ (Υ ′ is described below), phenyl (C Factory c 6 ) alkylaminocarbinole Groups, which may be the same or different, are selected from Υ, (Υ 'is shown below)
1以上の置換基を環上に有する置換フヱニル (CfCe) アルキルアミノカルボ二 ル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1 〜 4個の置換 基を示す。 1 to 4 substituents selected from a substituted phenyl (CfCe) alkylaminocarboxy group, a hydroxyl group, an amino group, a cyano group and a nitro group having at least one substituent on a ring.
Y, は同一又は異なっても良く、 水素原子、 ハロゲン原子、 (cr c6)アルキル 基、 (c2- c6)アルケニル基、 (c2 - c6)アルキニル基、 シクロ(c3 - c6)アルキル基、 ノヽ 口(c厂 c6)アルキル基、 シクロハ口(c3 - c6)アルキル基、 ( - アルコキシ基、 ノヽ 口(C厂 C6)アルコキシ基、 (CrC6)アルキルチオ基、 ハロ( -Ce)アルキルチオ基、Y, may be the same or different, and include a hydrogen atom, a halogen atom, a (c r c 6 ) alkyl group, a (c 2 -c 6 ) alkenyl group, a (c 2 -c 6 ) alkynyl group, a cyclo (c 3- c 6 ) alkyl group, phenol (c factory c 6 ) alkyl group, cycloha (c 3 -c 6 ) alkyl group, (-alkoxy group, phenol (C factory C 6 ) alkoxy group, (C r C 6 ) Alkylthio group, halo (-Ce) alkylthio group,
(C厂 c6)アルキルスルフィニル基、 ノヽ口 (c,-c6)アルキルスルフィニル基、 (c「c6) アルキルスノレホニル基、 ノヽロ( - c6)アルキルスルホニル基、 フエニル基、 フエ ノキシ基、 (C厂 C6)アルキルカルボニル基、 ノヽロ(C厂 c6)アルキルカルボニル基、 フエニルカルボニル基、 - )アルコキシカルボニル基、 カルボキシル基、 モ ノ (CrC6) アルキルァミノカルボニル基、 ジ (C厂 C6) アルキルアミノカルボ二 ル基、 フエニルァミノカルボニル基、 水酸基、 アミノ基、 シァノ基又はニトロ基 から選択される 1 〜 5個の置換基を示す。 } で表される基を挙げることができる。 (C factory c 6 ) alkylsulfinyl group, phenol (c, -c 6 ) alkylsulfinyl group, (c “c 6 ) alkylsnolephonyl group, nodro (-c 6 ) alkylsulfonyl group, phenyl group, phenyl Nonoxy group, (C Factory C 6 ) alkylcarbonyl group, nodro (C Factory c 6 ) alkylcarbonyl group, phenylcarbonyl group,-) alkoxycarbonyl group, carboxyl group, mono (C r C 6 ) alkylamino Represents 1 to 5 substituents selected from a carbonyl group, a di (C factory C 6 ) alkylaminocarboxy group, a phenylaminocarbonyl group, a hydroxyl group, an amino group, a cyano group and a nitro group. The groups represented can be mentioned.
「複素環基」 としては、 例えばピリジル基、 ピリジン— N—ォキシド基、 ピリ ミジニル基、 ピラジニル基、 トリアジニノレ基、 フリル基、 テトラヒドロフリル基、 チェニル基、 テトラヒドロチェニル基、 テトラヒドロビラニル基、 テトラヒドロ チォピラニル基、 ォキサゾリル基、 イソキサゾリル基、 ォキサジァゾリル基、 チ ァゾリル基、 イソチアゾリル基、 チアジアゾリル基、 イミダゾリル基、 トリァゾ リル基、 ピラゾリル基、 モルホリニル基等を挙げることができる。 Examples of the “heterocyclic group” include a pyridyl group, a pyridine-N-oxide group, a pyrimidinyl group, a pyrazinyl group, a triazinole group, a furyl group, a tetrahydrofuryl group, a phenyl group, a tetrahydrophenyl group, a tetrahydrovinylanyl group, and a tetrahydrovinyl group. Examples thereof include a thiopyranyl group, an oxazolyl group, an isoxazolyl group, an oxdiazolyl group, a thiazolyl group, an isothiazolyl group, a thiadiazolyl group, an imidazolyl group, a triazolyl group, a pyrazolyl group, and a morpholinyl group.
本発明のハロアルキルスルホンァニリ ド誘導体の塩としては、 農薬として適用 するにあたり使用することができる塩であれば良く、 例えば、 リチウム塩、 ナト リウム、 カリウム等のアルカリ金属との塩類、 カルシウム、 マグネシウム等のァ ルカリ土類との塩、 鉄等の重金属との塩、 その他アルミニウム、 亜鉛等他の金属 との塩等の無機金属類との塩類、 アンモニゥム塩等の有機塩基との塩類等を挙げ ることができ、 これらは水和物を形成していても良い。
本発明の一般式 (I ) で表されるハロアルキルスルホンァニリ ド誘導体は、 そ の構造式中に 1つ又は複数個の不斉炭素原子又は不斉中心を含む場合があり、 2 種以上の光学異性体及びジァステレオマーが存在する場合もあり、 本発明は各々 の光学異性体及びそれらが任意の割合で含まれる混合物をも全て包含するもので ある。 又、 本発明の一般式 (I ) で表されるハロアルキルスルホンァニリ ド誘導 体は、 その構造式中に炭素一炭素二重結合又は炭素一窒素二重結合に由来する 2 種の幾何異性体が存在する場合もあるが、 本発明は各々の幾何異性体及びそれら が任意の割合で含まれる混合物をも全て包含するものである。 The salt of the haloalkylsulfonanilide derivative of the present invention may be any salt that can be used when applied as a pesticide, for example, salts with an alkali metal such as lithium salt, sodium and potassium, calcium and magnesium Salts with alkaline earths such as, salts with heavy metals such as iron, salts with inorganic metals such as salts with other metals such as aluminum and zinc, salts with organic bases such as ammonium salts, etc. These may form hydrates. The haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention may contain one or more asymmetric carbon atoms or asymmetric centers in its structural formula, and may have two or more types. Optical isomers and diastereomers may exist, and the present invention includes all optical isomers and mixtures containing them in any ratio. The haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention has two kinds of geometric isomers derived from a carbon-carbon double bond or a carbon-nitrogen double bond in its structural formula. However, the present invention encompasses all geometric isomers and mixtures containing them in any proportion.
本発明のハロアルキルスルホンァニリ ド誘導体の好ましい態様としては、 Qの ヘテロ環としては、 窒素原子を 1〜 4個、 酸素原子を 0乃至 1個及び硫黄原子を 0乃至 1個含む 5員乃至 6員へテ口環が良く、 当該 5員乃至 6員へテロ環が縮合 環を形成しているものも好ましい。 特に好ましいのは Q— 1、 Q— 2、 Q— 3等 である。 Q上の置換基として好適なものは、 フエニル(C厂 C6)アルキル基、 置換 フエニル(C厂 C6)アルキル基、 フエ二ル基、 置換フエニル基、 ピリジル基及び置 換ピリジル基等である。 R 1としてのハロアルキルは、 フルォロメチルが好まし く、 より好ましくはトリフルォロメチル又はジフルォロメチルが好ましく、 その 置換位置は 2位が好ましい。 R 2は水素原子が好ましい。 G及ぴ G 1は酸素原子 が好ましい。 mは 0が好ましい。 In a preferred embodiment of the haloalkylsulfonanilide derivative of the present invention, the heterocycle of Q is a 5-membered to 6-membered compound containing 1 to 4 nitrogen atoms, 0 to 1 oxygen atom and 0 to 1 sulfur atom. It is also preferable that the 5- or 6-membered hetero ring forms a condensed ring. Particularly preferred are Q-1, Q-2, Q-3 and the like. Suitable as the substituent on Q is, phenyl (C厂C 6) alkyl group, a substituted phenyl (C厂C 6) alkyl group, Hue group, a substituted phenyl group, pyridyl group and substitution pyridyl group is there. The haloalkyl as R 1 is preferably fluoromethyl, more preferably trifluoromethyl or difluoromethyl, and the substitution position is preferably the 2-position. R 2 is preferably a hydrogen atom. G and G 1 are preferably oxygen atoms. m is preferably 0.
本 ¾明の一般式 (I ) で表されるハロアルキルスルホンアミ ド誘導体は、 例え ば下記に図示する製造方法により製造することができる。 The haloalkylsulfonamide derivative represented by the general formula (I) of the present invention can be produced, for example, by the production method shown below.
製造方法 1 .
Manufacturing method 1.
(式中、 R R2、 R 3、 R 4、 R 5、 R 6、 A、 Q、 X及び mは前記に同じ。 R 2 'は (Cf C6) アルキル基、 (C -C6) アルキルカルボニル基、 ノヽロ (C厂 C6) アルキルカルボ二ル基、 同一又は異なっても良く、 Y (Yは前記に同じ。 ) から 選択される 1以上の置換基を有するフエ二ルカルポニル基、 c6) アルキル スルホニル基、 ハロ (C厂 c6) アルキルスルホニル基又は同一若しくは異なって も良く、 Y (Yは前記に同じ。 ) から選択される 1以上の置換基を有するフエ二 ノレスルホ二ル基を示す。 (Wherein, RR 2 , R 3 , R 4 , R 5 , R 6 , A, Q, X and m are the same as above. R 2 ′ is a (Cf C 6 ) alkyl group, (C 6 -C 6 ) alkyl A carbonyl group, a nitro group (C Factory C 6 ) alkyl carbonyl group, which may be the same or different, and a phenylcarbonyl group having at least one substituent selected from Y (Y is the same as described above); c 6) alkyl sulfonyl group, a halo (C厂c 6) alkylsulfonyl group, or the same or different and may, Y (Y is phenylene Noresuruho radicals having 1 or more substituents selected from the same.) to the Is shown.
は N— R3 (式中、 R3は前記に同じ。 ) 、 N—O R4 (式中、 R4は前記に 同じ。 ) 又は N— N R5R6 (式中、 R5及び R6は前記に同じ。 ) を示す。 Is N—R 3 (wherein R 3 is the same as above), N—OR 4 (where R 4 is the same as above), or N—NR 5 R 6 (wherein R 5 and R 6 Is the same as above.
Lはハロゲン原子等の脱離基を示す。 ) L represents a leaving group such as a halogen atom. )
一般式 (II) で表される化合物を塩基の存在下、 必要に応じて相関移動触媒を 用いて、 不活性溶媒の存在下又は非存在下に一般式 Q - Hで表されるヘテロ環と
反応させることにより一般式 (III) で表される化合物とし、 該化合物を単離し 又は単離せずして、 不活性溶媒の存在下又は非存在下に還元剤等を反応させるこ とにより、 一般式 (IV) で表されるァミノ化合物とし、 該化合物を単離し又は単 離せずして、 塩基の存在下、 不活性溶媒の存在下又は非存在下に I^S 02_L (式中、 R1及ぴ Lは前記に同じ。 ) あるいは (1^3〇2)2〇 (式中、 R1は前記に 同じ。 ) で表されるハロアルキルスルホニル誘導体を反応させることにより、 一 般式 (1— 1) で表される本発明化合物を製造することができる。 更に一般式 (1 -1) で表される化合物を単離し又は単離せずして、 塩基の存在下、 不活性 溶媒の存在下又は非存在下に一般式 R 2 — L (式中、 及びしは前記に同 じ。 ) で表される化合物を反応させることにより、 一般式 (1 -2) で表される 本発明化合物を製造することができる。 更に一般式 (1—1) 又は (1—2) で 表される化合物を単離し又は単離せずして、 不活性溶媒の存在下又は非存在下に —般式 H2N— R3 (式中、 R3は前記に同じ。 ) で表されるァミン誘導体、 H2N -OR4 (式中、 R4は前記に同じ。 ) で表されるォキシム誘導体又は H2N— NR ¾6 (式中、 R5及ぴ R6は前記に同じ。 ) で表されるヒ ドラジン誘導体を反応さ せることにより、 一般式 (1 _3) で表される本発明化合物を製造することがで さる。 The compound represented by the general formula (II) is reacted with a heterocyclic compound represented by the general formula QH in the presence of a base and, if necessary, using a phase transfer catalyst in the presence or absence of an inert solvent. The compound represented by the general formula (III) is reacted to give a compound represented by the general formula (I) by isolating or not isolating the compound and reacting with a reducing agent or the like in the presence or absence of an inert solvent. An amino compound represented by the formula (IV) is isolated or isolated without isolation, and is prepared by the reaction of I ^ S 0 2 _L (in the formula, in the presence of a base, in the presence or absence of an inert solvent) R 1 and L are the same as described above.) Or (1 ^ 3〇 2 ) 2 R (wherein, R 1 is the same as described above.) By reacting a haloalkylsulfonyl derivative represented by the general formula ( 1 ). The compound of the present invention represented by 1-1) can be produced. Further, the compound represented by the general formula (1-1) is isolated or not isolated, and the compound represented by the general formula R 2 — L (wherein, and in the presence of a base, in the presence or absence of an inert solvent) The compound of the present invention represented by the general formula (1-2) can be produced by reacting the compound represented by the same formula. Further, the compound represented by the general formula (1-1) or (1-2) is isolated or not isolated, and in the presence or absence of an inert solvent, the compound represented by the general formula H 2 N—R 3 ( In the formula, R 3 is the same as described above.) An amide derivative represented by the formula: H 2 N—OR 4 (wherein R 4 is the same as described above); or H 2 N—NR ¾ 6 (Wherein, R 5 and R 6 are the same as described above), whereby the compound of the present invention represented by the general formula (1_3) can be produced. .
(1-1) . 一般式 (II) →一般式 (III) (1-1). General formula (II) → General formula (III)
出発物質である一般式 (Π) の化合物は例えば、 J. Chem. Soc. , 684 (1 942) 、 Indian J. Chem. , 1 1, 609 (1 973) 、 Beilsteins Compounds of the general formula (Π) as starting materials are described, for example, in J. Chem. Soc., 684 (1942), Indian J. Chem., 11, 609 (1973), Beilsteins
Handbuch der Organischen Chemie, 7, 290等に記載の方法又はこれらに準 じて製造することができる。 Q— Hで表されるヘテロ環は例えば、 2, 3—ジヒ ドロー 3H—1, 2, 4一トリァゾールー 3—オン誘導体は WO 98— 381 7 6号公報等に記載の方法又はこれに準じて、 テトラゾール誘導体は J. Heterocycl. Chem. , 35 (2) , 405 (1998) 等に記載の方法又はこれ に準じて製造することができ、 その他の Q— Ηで表されるヘテロ環は国際特許公 開 W〇 91 - 3470号公報、 J. Chem. Soc. Perkin Trans. 1, 22, 264 4 (1973) 、 特開平 9一 100271号公報、 Liebigs Annalen der Chemie, 675, 180 (1 964) 、 J. Chem. Soc. (C), 747 1 96 7) 、 US
P 5728834号公報、 J. Heterocycl. Chem. , 22, 409 (1 985) 、 特開昭 60 _ 146879号公報、 特開平 6— 306061号公報、 特開昭 63 -41466号公報、 Doklady Akademii Nauk SSSR (Dokl. Akad. Nauk SSSR) , 1 58, 1 358 (1 964) 、 WO 98— 1 1079号公報、 Drug Research (Drug res. ) , (1) , 1 89 (1 968) 、 J. Heterocycl. Chem. , 1 5 (7) , 1 2 3 1 (1 9 78) 、 J. Chem. Soc. Perkin Trans. 2, 1 6 70 (1 979) 、 J. Am. Chem. Soc. , 80, 3908 (1958) 、 Journal fuer Praktische Chemie, 31 1, 477 (1969) 、 Chemische Berichte, 88, 1 351 (1 955) 等に記載の方法又はこれらに準じて製造することが できる。 It can be produced according to the method described in Handbuch der Organischen Chemie, 7, 290 or the like, or according to these methods. The heterocyclic ring represented by Q—H is, for example, 2,3-dihydro 3H-1,2,41-triazol-3-one derivative can be prepared by the method described in WO 98-381176 or the like. And tetrazole derivatives can be produced by the method described in J. Heterocycl. Chem., 35 (2), 405 (1998) or the like, or other heterocycles represented by Q—— are described in international patents. Publication W〇91-3470, J. Chem. Soc.Perkin Trans.1, 22, 2644 (1973), JP-A-9-1100271, Liebigs Annalen der Chemie, 675, 180 (1964), J. Chem. Soc. (C), 747 196 7), US P. 5728834, J. Heterocycl. Chem., 22, 409 (1 985), JP-A-60-146879, JP-A-6-306061, JP-A-63-41466, Doklady Akademii Nauk SSSR (Dokl. Akad. Nauk SSSR), 158, 1358 (1964), WO 98-11079, Drug Research (Drug res.), (1), 189 (1968), J. Heterocycl. Chem., 15 (7), 123 (1 78), J. Chem. Soc. Perkin Trans. 2, 1670 (1 979), J. Am. Chem. Soc., 80, 3908 (1958), Journal fuer Praktische Chemie, 311, 477 (1969), Chemische Berichte, 88, 1351 (1955) and the like, or can be produced according to them.
本反応で使用できる不活性溶媒としては、 本反応を著しく阻害しないものであ れば良く、 例えば、 ジェチルエーテル、 テトラヒ ドロフラン、 ジォキサン等の鎖 状又は環状エーテル類、 ベンゼン、 トルエン、 キシレン等の芳香族炭化水素類、 塩化メチレン、 クロ口ホルム、 四塩ィヒ炭素等のハロゲン化炭化水素類、 クロ口べ ンゼン、 ジク口口ベンゼン等のハロゲン化芳香族炭化水素類、 アセトン、 メチル ェチルケトン等のケトン類、 ァセトニトリル等の二トリル類、 酢酸ェチル等のェ ステル類、 N, N—ジメチルホルムアミ ド、 N, N—ジメチルァセトアミ ド等のァ ミ ド類、 ジメチルスルホキシド、 1 , 3—ジメチルー 2—イミダゾリノン、 水等 の不活性溶媒を例示することができ、 これらの不活性溶媒は単独で又は 2種以上 混合して使用することができる。 The inert solvent that can be used in this reaction may be any solvent that does not significantly inhibit this reaction, and examples thereof include linear or cyclic ethers such as getyl ether, tetrahydrofuran, and dioxane, and benzene, toluene, and xylene. Aromatic hydrocarbons, halogenated hydrocarbons such as methylene chloride, chloroform, tetrachloromethane, halogenated aromatic hydrocarbons such as chlorobenzene, benzene, etc., acetone, methyl ethyl ketone, etc. Ketones, nitriles such as acetonitrile, esters such as ethyl acetate, amides such as N, N-dimethylformamide, N, N-dimethylacetamide, dimethylsulfoxide, 1,3 Examples thereof include inert solvents such as —dimethyl-2-imidazolinone and water. These inert solvents may be used alone or in combination of two or more. To be able to use.
本反応で使用できる塩基としては、 例えばトリェチルァミン、 ジイソプロピノレ ェチノレアミン、 1, 8—ジァザビシク口 〔5. 4. 0〕 一 7—ゥンデセン、 ピリ ジン等の含窒素有機塩基類、 炭酸ナトリゥム、 炭酸力リゥム、 炭酸水素ナトリウ ム、 水酸化ナトリゥム、 水酸化力リゥム、 水素化ナトリゥム、 金属ナトリウム等 の無機塩基類、 酢酸ナトリゥム、 酢酸力リゥム等の有機塩基類、 ナトリゥムェト キシド、 カリウム t—ブトキシド等のアルコラ一ト類等を例示することができる。 塩基の使用量は反応により発生する酸を中和できるだけの量があれば良いが、 過 剰量使用することもできる。 Bases that can be used in this reaction include, for example, nitrogen-containing organic bases such as triethylamine, diisopropinoletinoleamine, 1,8-diazabicyclo mouth [5.4.0] 17-indene, pyridine, sodium carbonate, and carbonic acid. Inorganic bases such as lime, sodium bicarbonate, sodium hydroxide, sodium hydroxide, sodium hydride, sodium metal, etc .; organic bases such as sodium acetate, sodium acetate; alcohol such as sodium methoxide and potassium t-butoxide And the like. The base may be used in an amount sufficient to neutralize the acid generated by the reaction, but may be used in excess.
本反応で使用できる相関移動触媒としては、 例えばテトラ n -
3 009405 Examples of the phase transfer catalyst that can be used in this reaction include tetra n- 3 009405
19 19
ゥムプロミ ド、 ベンジルトリエチルアンモニゥムブロミ ド等の 4級アンモニゥム 塩、 1 8—クラウン一 6—エーテル等のクラウンエーテル類等を例示することが できる。 相関移動触媒の使用量は一般式 (Π) で表される化合物に対して 0 . 0 1倍モルから◦ . 5倍モルの範囲から適宜選択すれば良い。 Examples thereof include quaternary ammonium salts such as dimethylpromide and benzyltriethylammonium bromide, and crown ethers such as 18-crown-16-ether. The amount of the phase transfer catalyst to be used may be appropriately selected from the range of from 0.01 to 1.5 times the mol of the compound represented by the general formula (Π).
本反応は等モル反応であるので、 各反応剤を等モル使用すれば良いが、 いずれ 力の反応剤を過剰に使用することもできる。 反応温度は一 2 0 °C乃至使用する不 活性溶媒の還流温度下で行うことができ、 反応時間は反応規模、 反応温度等によ り一定しないが、 数分乃至 4 8時間の範囲で適宜選択すれば良い。 Since this reaction is an equimolar reaction, each reactant may be used in an equimolar amount, but any amount of the reactant may be used in excess. The reaction can be carried out at a temperature of from 120 ° C. to the reflux temperature of the used inert solvent.The reaction time is not fixed depending on the reaction scale, the reaction temperature, etc., but is appropriately in the range of several minutes to 48 hours. Just choose.
反応終了後、 目的物を含む反応系から常法により目的物を単離し、 必要に応じ て再結晶法、 蒸留法、 カラムクロマトグラフィ一法等で精製することにより目的 物を製造することができる。 又、 本反応終了後に目的物を単離せずに次の反応に 供することもできる。 After completion of the reaction, the target product can be produced by isolating the target product from the reaction system containing the target product by a conventional method and, if necessary, purifying the product by a recrystallization method, a distillation method, a column chromatography method or the like. Further, after the completion of the reaction, the target product can be used for the next reaction without isolation.
( 1 - 2 ) . 一般式 (III) →ー般式 (IV) (1-2). General formula (III) → General formula (IV)
本反応で使用できる不活性溶媒としては、 例えばメタノール、 ェタノール等の アルコール類、 テトラヒドロフラン、 ジォキサン等のエーテル類、 水等を例示す ることができ、 これらの不活性溶媒は単独で又は 2種以上混合して使用すること ができる。 また、 次に示す還元剤として使用する酸の水溶液をそのまま不活性溶 媒として使用することもできる。 Examples of the inert solvent that can be used in this reaction include alcohols such as methanol and ethanol, ethers such as tetrahydrofuran and dioxane, and water.These inert solvents may be used alone or in combination of two or more. Can be used in combination. Further, an aqueous solution of an acid used as a reducing agent described below can be used as an inert solvent as it is.
本反応で使用できる還元剤としては、 金属一酸、 金属一 ± 等を例示することが でき、 金属としては、 例えば鉄、 スズ、 亜鉛等を、 酸としては、 例えば塩酸、 硫 酸等の鉱酸類、 酢酸等の有機酸類、 塩化スズ等を、 塩としては、 例えば塩ィ匕アン モニゥム等を例示することができる。 また、 これらを組み合わせて使用すること も可能である。 Examples of the reducing agent that can be used in this reaction include metal monoacids and metal monoliths. Examples of the metal include iron, tin, and zinc, and examples of the acid include minerals such as hydrochloric acid and sulfuric acid. Acids, organic acids such as acetic acid and the like, tin chloride and the like, and examples of the salt include salt water ammonium and the like. It is also possible to use them in combination.
還元剤の使用量は一般式 (ΠΙ)で表される化合物に対して、 金属は 1〜1 0倍 モル、 酸および塩は 0 . 0 5〜1 0倍モルの範囲から適宜選択して使用すれば良 レ、。 反応温度は 0 °C乃至 1 5 0 °Cの範囲から選択すれば良く、 反応時間は反応規 模、 反応温度等により一定しないが、 数分乃至 4 8時間の範囲で適宜選択すれば 良い。 The amount of the reducing agent used is 1 to 10 times the molar amount of the compound represented by the general formula (ΠΙ), and the acid and salt are appropriately selected from the range of 0.05 to 10 times the molar amount. I should do it. The reaction temperature may be selected from the range of 0 ° C. to 150 ° C., and the reaction time is not constant depending on the reaction scale, the reaction temperature, and the like, but may be appropriately selected within the range of several minutes to 48 hours.
又、 還元反応は触媒の存在下、 接触水素添加法によっても行うことができ、 触
媒としては、 例えばパラジウム炭素、 白金、 ラネーニッケル等を例示することが できる。 The reduction can also be carried out by catalytic hydrogenation in the presence of a catalyst. Examples of the medium include palladium carbon, platinum, Raney nickel and the like.
反応終了後、 目的物を含む反応系から常法により目的物を単離し、 必要に応じ て再結晶法、 蒸留法、 カラムクロマトグラフィー法等で精製することにより目的 物を製造することができる。 又、 本反応終了後に目的物を単離せずに次の反応に 供することもできる。 After completion of the reaction, the desired product can be produced by isolating the desired product from the reaction system containing the desired product by a conventional method, and purifying the product, if necessary, by a recrystallization method, a distillation method, a column chromatography method or the like. Further, after the completion of the reaction, the target product can be used for the next reaction without isolation.
( 1 - 3 ) . 一般式 (IV) →—般式 ( I一 1 ) General formula (IV) → General formula (I-1)
本反応で使用できる不活性溶媒としては、 本反応の進行を著しく阻害しないも のであれば良く、 例えば、 ジェチルエーテル、 テトラヒドロフラン、 ジォキサン 等の鎖状又は環状エーテル類、 ベンゼン、 トルエン、 キシレン等の芳香族炭化水 素類、 塩化メチレン、 クロ口ホルム、 四塩ィヒ炭素等のハロゲン化炭化水素類、 ク ロロベンゼン、 ジクロロベンゼン等のハロゲン化芳香族炭化水素類、 アセトン、 メチルェチルケトン等のケトン類、 ァセトニトリル等の二トリル類、 酢酸ェチル 等のエステル類、 N, N—ジメチルホルムアミ ド、 N, N—ジメチルァセトアミ ド等のァミド類、 ジメチルスルホキシド、 1, 3―ジメチルー 2—イミダゾリノ ン等の不活性溶媒を例示することができ、 これらの不活性溶媒は単独で又は 2種 以上混合して使用することができる。 The inert solvent that can be used in this reaction may be any solvent that does not significantly inhibit the progress of this reaction.Examples include linear or cyclic ethers such as getyl ether, tetrahydrofuran, and dioxane; benzene, toluene, and xylene. Aromatic hydrocarbons, halogenated hydrocarbons such as methylene chloride, carbon form, tetrachlorocarbon, halogenated aromatic hydrocarbons such as chlorobenzene and dichlorobenzene, acetone, methylethylketone, etc. Ketones, nitriles such as acetonitrile, esters such as ethyl acetate, amides such as N, N-dimethylformamide, N, N-dimethylacetamide, dimethylsulfoxide, 1,3-dimethyl-2- Inert solvents such as imidazolinone can be exemplified.These inert solvents may be used alone or in combination of two or more. Can be used.
本反応で使用できる塩基としては、 例えばトリェチルァミン、 ジイソプロピル ェチノレアミン、 1, 8—ジァザビシク口 〔5 . 4 . 0〕 一 7—ゥンデセン、 ピリ ジン等の含窒素有機塩基類、 炭酸ナトリゥム、 炭酸力リゥム、 炭酸水素ナトリウ ム、 水酸化ナトリゥム、 水酸化力リゥム、 水素化ナトリゥム、 金属ナトリゥム等 の無機塩基類、 酢酸ナトリゥム、 酢酸力リゥム等の有機塩基類、 ナトリゥムェト キシド、 カリゥム t—ブトキシド等のアルコラ一ト類等を例示することができる。 又、 ピリジン等の含窒素有機塩基類を溶媒として使用することもできる。 塩基の 使用量は反応により発生する酸を中和できるだけの量があれば良いが、 過剰量使 用することもできる。 Bases that can be used in this reaction include, for example, nitrogen-containing organic bases such as triethylamine, diisopropylethynoleamine, 1,8-diazabicycline [5.4.0] -17-indene, pyridine, sodium carbonate, carbonated lime, and the like. Inorganic bases such as sodium hydrogencarbonate, sodium hydroxide, hydroxylated sodium, hydrogenated sodium, metal sodium, etc .; organic bases such as sodium acetate, sodium acetate; alcoholate such as sodium methoxide, potassium t-butoxide, etc. And the like. Further, nitrogen-containing organic bases such as pyridine can also be used as the solvent. The base may be used in an amount sufficient to neutralize the acid generated by the reaction, but may be used in excess.
本反応は等モル反応であるので、 各反応剤を等モル使用すれば良いが、 いずれ かの反応剤を過剰に使用することもできる。 反応温度は一 2 0 °C乃至使用する不 活性溶媒の還流温度下で行うことができ、 反応時間は反応規模、 反応温度等によ
り一定しないが、 数分乃至 4 8時間の範囲で適宜選択すれば良い。 Since this reaction is an equimolar reaction, each reactant may be used in an equimolar amount, but any of the reactants may be used in excess. The reaction can be carried out at a temperature of from 120 ° C to the reflux temperature of the inert solvent used.The reaction time depends on the reaction scale, reaction temperature, etc. Although it is not constant, it may be appropriately selected in the range of several minutes to 48 hours.
反応終了後、 目的物を含む反応系から常法により目的物を単離し、 必要に応じ て再結晶法、 蒸留法、 カラムクロマトグラフィー法等で精製することにより目的 物を製造することができる。 又、 本反応終了後に目的物を単離せずに次の反応に 供することもできる。 After completion of the reaction, the desired product can be produced by isolating the desired product from the reaction system containing the desired product by a conventional method, and purifying the product, if necessary, by a recrystallization method, a distillation method, a column chromatography method or the like. Further, after the completion of the reaction, the target product can be used for the next reaction without isolation.
( 1 - 4 ) . 一般式 (I一 1 ) →一般式 (I一 2 ) General formula (I-1) → General formula (I-1)
本反応は (1— 3 ) . に準じて行うことができる。 This reaction can be carried out according to (1-3).
反応終了後、 目的物を含む反応系から常法により目的物を単離し、 必要に応じ て再結晶法、 蒸留法、 カラムクロマトグラフィー法等で精製することにより目的 物を製造することができる。 又、 本反応終了後に目的物を単離せずに次の反応に 供することもできる。 After completion of the reaction, the desired product can be produced by isolating the desired product from the reaction system containing the desired product by a conventional method, and purifying the product, if necessary, by a recrystallization method, a distillation method, a column chromatography method or the like. Further, after the completion of the reaction, the target product can be used for the next reaction without isolation.
( 1 - 5 ) . 一般式 (1— 1 ) 又は一般式 (1一 2 ) →—般式 (I一 3 ) 本反応は、 必要に応じて触媒量の酸の存在下に反応することもできる。 (1-5). General formula (1-1) or General formula (112) → General formula (I-13) This reaction may be carried out in the presence of a catalytic amount of an acid, if necessary. it can.
不活性溶媒としては、 本反応の進行を著しく阻害しないものであれば良く、 例 えば、 メタノ一ノレ、 エタノール、 n—プロパノール等のアルコール類、 ジェチル エーテル、 テトラヒドロフラン、 ジォキサン等の鎖状又は環状エーテル類、 ベン ゼン、 トルエン、 キシレン等の芳香族炭化水素類、 クロ口ベンゼン、 ジクロロべ ンゼン等のハ口ゲン化芳香族炭化水素類を例示することができ、 これらの不活性 溶媒は単独で又は 2種以上混合して使用することができる。 Any inert solvent may be used as long as it does not significantly inhibit the progress of this reaction. Examples thereof include alcohols such as methanol, ethanol, n-propanol, and the like, and chain or cyclic ethers such as getyl ether, tetrahydrofuran, and dioxane. , Aromatic hydrocarbons such as benzene, toluene, and xylene, and halogenated aromatic hydrocarbons such as benzene and dichlorobenzene, and these inert solvents can be used alone or individually. Two or more can be used in combination.
本反応で使用できる酸としては、 例えば蟻酸、 酢酸、 プロピオン酸等の有機酸 類、 塩酸、 硫酸等の鉱酸類を例示することができる。 Examples of the acid that can be used in this reaction include organic acids such as formic acid, acetic acid, and propionic acid, and mineral acids such as hydrochloric acid and sulfuric acid.
本反応は等モル反応であるので、 各反応剤を等モル使用すれば良いが、 いずれ かの反応剤を過剰に使用することもできる。 反応温度は一 2 0 °C乃至使用する不 活性溶媒の還流温度下で行うことができ、 反応時間は反応規模、 反応温度等によ り一定しないが、 数分乃至 4 8時間の範囲で適宜選択すれば良い。 Since this reaction is an equimolar reaction, each reactant may be used in an equimolar amount, but any of the reactants may be used in excess. The reaction can be carried out at a temperature of from 120 ° C. to the reflux temperature of the used inert solvent.The reaction time is not fixed depending on the reaction scale, the reaction temperature, etc., but is appropriately in the range of several minutes to 48 hours. Just choose.
反応終了後、 目的物を含む反応系から常法により目的物を単離し、 必要に応じ て再結晶法、 蒸留法、 カラムクロマトグラフィー法等で精製することにより目的 物を製造することができる。 After completion of the reaction, the desired product can be produced by isolating the desired product from the reaction system containing the desired product by a conventional method, and purifying the product, if necessary, by a recrystallization method, a distillation method, a column chromatography method or the like.
製造方法 2 .
O N 文献記載のへテロ環〇2N, Manufacturing method 2. ON Heterocycle 文献2N ,
,R 7 製造方法等 , R 7 manufacturing method, etc.
(III) (III)
(式中、 R R2、 R2'、 R3、 R4、 R5、 R6、 A、 G 、 レ Q、 X及び mは前記 に同じ。 R17はァミノ基、 2—ヒドロキシェチルァミノ基又はヒドラジノ基を示 す。 ) (Wherein, RR 2 , R 2 ′, R 3 , R 4 , R 5 , R 6 , A, G, les Q, X and m are the same as above. R 17 is an amino group, 2-hydroxyethyla It represents a mino group or a hydrazino group.)
一般式 (V) で表されるァミン誘導体、 2—ヒドロキシェチルァミン誘導体又 はヒ ドラジン誘導体を出発物質として、 特開平 8— 1 5 1 3 64号、 Bull. Korean Chem. Soc. 2 2 ( 7 ) , 7 6 1〜 7 64 (2 0 0 1 ) 又は Synth. Commun. , 16 (2) , 163〜 1 67等に記載のへテロ環合成法又はこれに準 じて化合物 (III) を製造し、 該化合物を単離し又は単離せずして、 製造方法 1. と同じ方法で一般式 (I一 1) 〜 (1— 3) で表される本発明化合物を製造する ことができる。 Starting from an amine derivative, a 2-hydroxyethylamine derivative or a hydrazine derivative represented by the general formula (V), JP-A-8-151364, Bull. Korean Chem. Soc. 22 (7), 761 to 764 (2001) or the heterocyclic synthesis method described in Synth. Commun., 16 (2), 163-167, or a compound (III) according to the method. And the compound of the present invention represented by any of formulas (I-11) to (1-3) can be produced in the same manner as in Production method 1. .
出発物質である一般式 (V) で表される化合物は例えば、 J. Chem. Soc. , 1
800 (1925) 、 J. Chem. Soc. , 2348 (1 926) 等に記載の製造法 又はこれに準じて製造することができる。 The compound represented by the general formula (V) as a starting material is described in, for example, J. Chem. Soc., 1 800 (1925), J. Chem. Soc., 2348 (1 926), or the like, or can be produced according to them.
以下に本発明の一般式 (I) で表されるハロアルキルスルホンァニリ ド誘導体 の代表例を第 1表乃至第 1 3表に例示するが、 本発明はこれらに限定されるもの ではない。 尚、 物性は融点 (°C) 又は屈折率を示す。 Hereinafter, typical examples of the haloalkylsulfonanilide derivatives represented by the general formula (I) of the present invention are shown in Tables 1 to 13, but the present invention is not limited thereto. The physical properties indicate the melting point (° C) or the refractive index.
以下の表において、 「Me」 はメチル基を、 「E t」 はェチル基を、 「P r」 はプロピル基を、 「Bu」 はプチル基を、 「P e n」 はペンチル基を、 In the table below, “Me” represents a methyl group, “E t” represents an ethyl group, “P r” represents a propyl group, “Bu” represents a butyl group, “P en” represents a pentyl group,
「H e x」 はへキシル基を、 「Ph」 はフエニル基を、 「Pyn」 はピリジル基 を、 ΓΡ ym」 はピリミジル基を、 「P y d」 はピリダジル基を、 「Ac」 はァ セチル基を、 「n—」 はノルマルを、 「 i一」 はイソを、 「s—」 はセカンダリ 一を、 「t―」 はターシャリーを、 「c一」 は脂環式炭化水素基を示す。 “H ex” is a hexyl group, “Ph” is a phenyl group, “Pyn” is a pyridyl group, ΓΡ ym is a pyrimidyl group, “P yd” is a pyridazyl group, and “Ac” is an acetyl group. , "N-" indicates normal, "i-" indicates iso, "s-" indicates secondary, "t-" indicates tertiary, and "c-" indicates alicyclic hydrocarbon group.
「置換位置」 とはハ口アルキルスルホニルァミノ基の置換位置を示す。
“Substitution position” indicates the substitution position of the alkylsulfonylamino group.
一般式 (I一 4 ) General formula (I-I-4)
1表 (m= 0 A=一 CH2— G^0 J4=N) Table 1 (m = 0 A = one CH 2 — G ^ 0 J 4 = N)
No. 置換 物性 No. Substitution physical properties
R1 R2 X J5 R9 R 1 R 2 XJ 5 R 9
]4 [融点 (°C) ] ] 4 [Melting point (° C)]
1-1 2 3 H H CH Me 1-1 2 3 H H CH Me
1-2 2 C H H CH Et 87-88 1-2 2 C H H CH Et 87-88
1-3 2 CR 3 H H CH n— Pr 1-3 2 CR 3 H H CH n— Pr
1-4 2 3 H H CH i-Pr 1-4 2 3 H H CH i-Pr
1-5 2 3 H H CH c—Pr 1-5 2 3 H H CH c—Pr
1-6 2 CF, H H CH n-Bu 1-6 2 CF, H H CH n-Bu
1-7 2 CF, H H CH t-Bu 1-7 2 CF, H H CH t-Bu
1-8 2 CF, H H CH - CH2- Ph 130-1321-8 2 CF, HH CH-CH 2 -Ph 130-132
1-9 2 CF, H H CH - CH2 -(2- CI - Ph) 1-9 2 CF, HH CH - CH 2 - (2- CI - Ph)
1-10 2 CF, H H CH - CH2 -(3 - CI- Ph) 1-10 2 CF, HH CH-CH 2- (3-CI- Ph)
1-11 2 3 H H CH - CH2- (4-Cl-Ph) 1-11 2 3 HH CH-CH 2- (4-Cl-Ph)
1-12 2 CF, H H CH -CH2-(2, 6-Cl2-Ph) 1-12 2 CF, HH CH -CH 2- (2, 6-Cl 2 -Ph)
1-13 2 CF, H H CH -CHMe-Ph 1-13 2 CF, H H CH -CHMe-Ph
1-14 2 CF3 H H CH -CHMe-(2-Cl-Ph) 1-14 2 CF 3 HH CH -CHMe- (2-Cl-Ph)
1-15 2 CF H H CH -CHMe-(3-Cl-Ph) 1-15 2 CF H H CH -CHMe- (3-Cl-Ph)
1-16 2 CF3 H H CH -€HMe-(4-Cl-Ph) 1-16 2 CF 3 HH CH-€ HMe- (4-Cl-Ph)
1-17 2 CF3 H H CH -O e-(2, 6-Cl2-Ph) 1-17 2 CF 3 HH CH -O e- (2, 6-Cl 2 -Ph)
1-18 2 CF3 H H CH -C e2-Ph 1-18 2 CF 3 HH CH -C e 2 -Ph
1-19 2 CF 3, H H CH -C e2-(2-Cl-Ph) 1-19 2 CF 3, HH CH -C e 2- (2-Cl-Ph)
1-20 2 CF3 H H CH -tMe2-(3- ;i-Ph) 1-20 2 CF 3 HH CH -tMe 2- (3-; i-Ph)
1-21 2 CF3 H H CH -<Me2-(4-Cl-Ph) 1-21 2 CF 3 HH CH-<Me 2- (4-Cl-Ph)
1-22 2 CF3 H H CH -CMe (2, 6-Cl2~Ph) 1-22 2 CF 3 HH CH -CMe (2, 6-Cl 2 ~ Ph)
1-23 2 CF3 H H CH Ph 141-1421-23 2 CF 3 HH CH Ph 141-142
1-24 2 CF3 H H CH 2-F-Ph 1-24 2 CF 3 HH CH 2-F-Ph
1-25 2 CF3 H H CH 3-F-Ph 1-25 2 CF 3 HH CH 3-F-Ph
1-26 2 CF3 H H CH 4-F-Ph 1-26 2 CF 3 HH CH 4-F-Ph
1-27 2 CF3 H H CH 2 - CI - Ph 129-1311-27 2 CF 3 HH CH 2-CI-Ph 129-131
1-28 2 CF3 H H CH 3-Cl-Ph 133-1351-28 2 CF 3 HH CH 3-Cl-Ph 133-135
1-29 2 CF3 H H CH 4- CI Ph 171. 81-29 2 CF 3 HH CH 4- CI Ph 171.8
1-30 2 CF3 H H CH 2- Br - Ph 128-1301-30 2 CF 3 HH CH 2- Br-Ph 128-130
1-31 2 CF3 H H CH 3 - Br- Ph 1-31 2 CF 3 HH CH 3-Br- Ph
1-32 2 CF3 H H CH 4-Br-Ph 145-147
1表 (続き)1-32 2 CF 3 HH CH 4-Br-Ph 145-147 Table 1 (continued)
1 - 33 ζ CF3 H H し H -丄ー] ¾ 1-33 ζ CF 3 HH then H-丄] ¾
1-34 2 CF3 H H CH 3 - I - Ph 1-34 2 CF 3 HH CH 3-I-Ph
1-35 2 CF3 H H CH 4一 I - Ph 1-35 2 CF 3 HH CH 4 I-Ph
1-36 2 CF3 H H CH 2 - Me - Ph 51 - 531-36 2 CF 3 HH CH 2-Me-Ph 51-53
1-37 2 CF3 H H CH 3 - Me - Ph 1-37 2 CF 3 HH CH 3-Me-Ph
1-38 2 CF3 H H CH 4 - Me - Ph 154-1561-38 2 CF 3 HH CH 4-Me-Ph 154-156
1 - 39 2 CF3 H H CH 2-Et-Ph 1-39 2 CF 3 HH CH 2-Et-Ph
1-40 2 CF3 H H CH 2 - i - Pr - Ph 48 - 501-40 2 CF 3 HH CH 2-i-Pr-Ph 48-50
1-41 2 CF3 H H CH 2-OMe-Ph 140. 61-41 2 CF 3 HH CH 2-OMe-Ph 140. 6
1-42 2 CF3 H H CH 3-OMe-Ph 1-42 2 CF 3 HH CH 3-OMe-Ph
1-43 2 CF3 H H CH 4-OMe-Ph 176-1781-43 2 CF 3 HH CH 4-OMe-Ph 176-178
1-44 2 CF3 H H CH 2-SMe-Ph 125. 81-44 2 CF 3 HH CH 2-SMe-Ph 125.8
1-45 2 CF3 H H CH 3-SMe-Ph 1-45 2 CF 3 HH CH 3-SMe-Ph
1-46 2 CF3 H H CH 4-SMe-Ph 1-46 2 CF 3 HH CH 4-SMe-Ph
1-47 2 CF3 H H CH 2-SOMe-Ph 50-521-47 2 CF 3 HH CH 2-SOMe-Ph 50-52
1-48 2 CF3 H H CH 3-S0Me-Ph 1-48 2 CF 3 HH CH 3-S0Me-Ph
1-49 2 CF3 H H CH 4-SOMe-Ph 1-49 2 CF 3 HH CH 4-SOMe-Ph
1-50 2 CF3 H H CH 2-S02Me-Ph 165-167 1-50 2 CF 3 HH CH 2- S0 2 Me-Ph 165-167
1 - 51 2 CF3 H H CH 3 - S02Me - Ph 1-51 2 CF 3 HH CH 3-S0 2 Me-Ph
1-52 2 CF3 H H CH 4 - S02Me - Ph 1-52 2 CF 3 HH CH 4-S0 2 Me-Ph
1 - 53 2 CF3 H H CH 2-N02-Ph 1-53 2 CF 3 HH CH 2-N0 2 -Ph
1-54 2 CF3 H H CH 3 - N02 - Ph 1-54 2 CF 3 HH CH 3-N0 2 -Ph
1-55 2 CF3 H H CH 4 - N02— Ph 1-55 2 CF 3 HH CH 4-N0 2 — Ph
1 - 56 2 CF3 H H CH 2-CN-Ph 1-56 2 CF 3 HH CH 2-CN-Ph
1-57 2 CF3 H H CH 3 - CN- Ph 1-57 2 CF 3 HH CH 3-CN- Ph
1-58 2 CF3 H H CH 4 - CN- Ph 1-58 2 CF 3 HH CH 4-CN- Ph
1-59 2 CF3 H H CH 2 - CF3 - Ph 123-1251-59 2 CF 3 HH CH 2-CF 3 -Ph 123-125
1一 60 2 CF3 H H CH 3 - CF3 - Ph 1 1 60 2 CF 3 HH CH 3-CF 3 -Ph
1-61 2 CF3 H H CH 4 - CF3 Ph 1-61 2 CF 3 HH CH 4-CF 3 Ph
1-62 2 CF3 H H CH 2 - 0CF3 - Ph 1-62 2 CF 3 HH CH 2-0CF 3 -Ph
1-63 CF3 H H OH 3 - 0CF3— Ph 1-63 CF 3 HH OH 3-0CF 3 — Ph
1—64 Δ ο CF3 H H し i 4 - 0CF3 - Ph 1-64 Δ ο CF 3 HH then i 4-0CF 3 -Ph
1-bb ο 1-bb ο
しト 3 hi Π し i — しト3 -3 3 hi Π i i — 3 3
9 9
丄 ΌΟ 厶 PR u n U Π rし n し Γ3 ΓΠ PR PR PR PR un U Π r Π n Γ Γ 3
1-67 2 CF3 H H CH 4-SCF3-Ph 1-67 2 CF 3 HH CH 4-SCF 3 -Ph
1-68 2 CF3 H H CH 2-S0CF3-Ph 1-68 2 CF 3 HH CH 2-S0CF 3 -Ph
1-69 2 CF3 H H CH 3-SOCFg-Ph 1-69 2 CF 3 HH CH 3-SOCFg-Ph
1-70 2 CF3 H H CH 4-S0CF3-Ph 1-70 2 CF 3 HH CH 4-S0CF 3 -Ph
1 - 71 2 CF3 H H CH 2-S02CF3-Ph 1-71 2 CF 3 HH CH 2-S0 2 CF 3 -Ph
1-72 2 CF3 H H CH 3-S02CF3-Ph
1表 (続き) 1-72 2 CF 3 HH CH 3-S0 2 CF 3 -Ph Table 1 (continued)
No. 換 物性 No. Commutative properties
R1 R2 X J5 R9 R 1 R 2 XJ 5 R 9
置 [融点(c) ] -73 2 CF3 H H CH 4-S02CF3-Ph[Melting point (c)] -73 2 CF 3 HH CH 4-S0 2 CF 3 -Ph
-74 2 CF3 H H CH 2_C02H - Ph-74 2 CF 3 HH CH 2_C0 2 H-Ph
-75 2 CF3 H H CH 3 - C02H- Ph-75 2 CF 3 HH CH 3-C0 2 H- Ph
-76 2 CF3 H H CH 4-C02H-Ph-76 2 CF 3 HH CH 4-C0 2 H-Ph
-77 2 CF3 H H CH 2 - C02Me-Ph-77 2 CF 3 HH CH 2-C0 2 Me-Ph
-78 2 CF3 H H CH 3- C02Me_Ph -78 2 CF 3 HH CH 3- C0 2 Me_Ph
-79 2 CF3 H H CH 4 - C02Me_Ph-79 2 CF 3 HH CH 4-C0 2 Me_Ph
-80 2 CF3 H H CH 2 - Ph- Ph-80 2 CF 3 HH CH 2-Ph- Ph
-81 2 CF3 H H CH 4-PhO-Ph 44-46 -82 2 CF3 H H CH 2, 4- F2_Ph-81 2 CF 3 HH CH 4-PhO-Ph 44-46 -82 2 CF 3 HH CH 2, 4- F 2 _Ph
-83 2 CF3 H H CH 2, 6- F2 - Ph-83 2 CF 3 HH CH 2, 6- F 2 -Ph
-84 2 CF3 H H CH 2, 3- Cl2 - Ph 140-142 -85 2 CF3 H H CH 2, 6_C12 - Ph-84 2 CF 3 HH CH 2, 3- Cl 2 -Ph 140 -142 -85 2 CF 3 HH CH 2, 6_C1 2 -Ph
-86 2 CF3 H H CH 2, 6- Br2 - Ph-86 2 CF 3 HH CH 2, 6-Br 2 -Ph
-87 2 CF3 H H CH 2, 6- 12- Ph-87 2 CF 3 HH CH 2, 6-1 2 -Ph
-88 2 CF3 H H CH 2 - Me- 3- CI - Ph 136-137 -89 2 CF3 H H CH 2- Me- 4 - Br- Ph 174-176 -90 2 CF3 H H CH 3 - Me- 4- Br- Ph 136-138 -88 2 CF 3 HH CH 2-Me- 3- CI-Ph 136-137 -89 2 CF 3 HH CH 2- Me- 4-Br- Ph 174-176 -90 2 CF 3 HH CH 3-Me- 4 -Br- Ph 136-138
No. 換 物性 No. Commutative properties
R1 R2 X J5 R9 R 1 R 2 XJ 5 R 9
恨置 [融点 (°c) ] Grudge [melting point (° c)]
1-113 2 CF3 H H CH 6 - CF3- 2- Pyn 1-113 2 CF 3 HH CH 6 - CF 3 - 2- Pyn
1-114 2 CF3 H H CH 6-Cl-4-CF3-2-Pyn 1-114 2 CF 3 HH CH 6-Cl-4-CF 3 -2-Pyn
1-115 2 CF3 H H CH 2- Pym 1-115 2 CF 3 HH CH 2- Pym
1-116 2 CF3 H H CH 4 - Pym 1-116 2 CF 3 HH CH 4-Pym
1 - 117 2 CF3 H H CH 4, 6-Me2-2-Pym 1-117 2 CF 3 HH CH 4, 6-Me 2 -2-Pym
1-118 2 CF3 H H CH 4, 6-(CMe)2-2-Pym 1-118 2 CF 3 HH CH 4, 6- (CMe) 2 -2-Pym
1-119 2 CF3 H H CH 3- Pyd 1-119 2 CF 3 HH CH 3- Pyd
1 - 120 2 CF3 H H CH 6 - CI- 3- Pyd 1-120 2 CF 3 HH CH 6-CI-3- Pyd
1-121 2 CF3 H H CH - CO-匪 e 1-121 2 CF 3 HH CH-CO- bandit e
1-122 2 CF3 H H CH -CO-NHPh 1-122 2 CF 3 HH CH -CO-NHPh
1-123 2 CF3 H H CH - CO - NMePh 1. 5202 (28°C)1-123 2 CF 3 HH CH-CO-NMePh 1.5202 (28 ° C)
1-124 2 CF3 H H CH - CO - N (i - Pr) (2, 4· 183. 5-184. 4 1-124 2 CF 3 HH CH-CO-N (i-Pr) (2, 4
F2 - Ph) F 2 -Ph)
1-125 2 CF3 H H CH - CO- N(i - Pr) 2 1-125 2 CF 3 HH CH-CO- N (i-Pr) 2
1 - 126 2 CF3 Me H CH Ph 1-126 2 CF 3 Me H CH Ph
1-127 2 CF3 Me H CH 2-Cl-Ph 1-127 2 CF 3 Me H CH 2-Cl-Ph
1-128 2 CF3 Me H CH 3-Cl-Ph 1-128 2 CF 3 Me H CH 3-Cl-Ph
ト 129 2 CF3 Me H CH 4-Cl-Ph G 129 2 CF 3 Me H CH 4-Cl-Ph
1-130 2 CF3 Me H CH 2, 6-Cl2-Ph 1-130 2 CF 3 Me H CH 2, 6-Cl 2 -Ph
1-131 2 CF3 Me H CH 2, 6- Me2 - Ph 1-131 2 CF 3 Me H CH 2, 6-Me 2 -Ph
1-132 2 CF3 Me H CH - CH2 - Ph 1-132 2 CF 3 Me H CH-CH 2 -Ph
1-133 2 CF3 Me H CH - CMe2 - Ph 1-133 2 CF 3 Me H CH - CMe 2 - Ph
1-134 2 CF3 COMe H CH Ph 1-134 2 CF 3 COMe H CH Ph
1-135 2 CF3 COMe H CH 2- CI - Ph 1-135 2 CF 3 COMe H CH 2- CI-Ph
1-136 2 CF3 COMe H CH 3-Cl-Ph 1-136 2 CF 3 COMe H CH 3-Cl-Ph
1 - 137 2 CF3 COMe H CH 4- CI- Ph 1-137 2 CF 3 COMe H CH 4- CI- Ph
1-138 2 CF3 COMe H CH 2, 6 Cl2 - Ph 1-138 2 CF 3 COMe H CH 2, 6 Cl 2 -Ph
1-139 2 CF3 COMe H CH 2, 6-Me2- Ph 1-139 2 CF 3 COMe H CH 2, 6-Me 2 -Ph
1-140 2 CF3 COMe H CH - CH2 Ph 1-140 2 CF 3 COMe H CH-CH 2 Ph
1-141 2 CF3 COMe H CH - CMe2 - Ph 1-141 2 CF 3 COMe H CH-CMe 2 -Ph
1-142 2 CF3 C02Me H CH Ph 1-142 2 CF 3 C0 2 Me H CH Ph
1-143 2 CF3 C02Me H CH 2-Cl-Ph 1-143 2 CF 3 C0 2 Me H CH 2-Cl-Ph
1-144 2 CF3 C02Me H CH 3-Cl-Ph 1-144 2 CF 3 C0 2 Me H CH 3-Cl-Ph
1-145 2 CF3 C02Me H CH 4-Cl-Ph 1-145 2 CF 3 C0 2 Me H CH 4-Cl-Ph
1-146 2 CF3 C02 e H CH 2, 6-Cl2-Ph 1-146 2 CF 3 C0 2 e H CH 2, 6-Cl 2 -Ph
1-147 2 CF3 C02Me H CH 2, 6-Me2 - Ph 1-147 2 CF 3 C0 2 Me H CH 2, 6-Me 2 -Ph
1-148 2 CF3 C02Me H CH -CH2-Ph 1-148 2 CF 3 C0 2 Me H CH -CH 2 -Ph
1-149 2 CF3 C02Me H CH -CMe2-Ph 1-149 2 CF 3 C0 2 Me H CH -CMe 2 -Ph
1-150 2 CF3 S02CF3 H CH Ph 1-150 2 CF 3 S0 2 CF 3 H CH Ph
1-151 2 CF3 S02CF3 H CH 2-Cl-Ph
T JP2003/009405 1-151 2 CF 3 S0 2 CF 3 H CH 2-Cl-Ph T JP2003 / 009405
28 1表 (続き) 28 1 Table (continued)
No. 直 pi p2 Y T5 物性 No. Straight pi p2 Y T5 Physical properties
K λ J K K λ J K
位置 [融点 (°c) ]-152 2 CF3 S02CF3 H CH 3- CI- PhPosition [Melting point (° c)]-152 2 CF 3 S0 2 CF 3 H CH 3- CI- Ph
-153 2 CF3 S02CF3 H CH 4-Cl-Ph-153 2 CF 3 S0 2 CF 3 H CH 4-Cl-Ph
-154 2 CF3 S02CF3 H CH 2, 6-Cl2 - Ph-154 2 CF 3 S0 2 CF 3 H CH 2, 6-Cl 2 -Ph
-155 2 CF3 S02CF3 H CH 2, 6- Me2- Ph-155 2 CF 3 S0 2 CF 3 H CH 2, 6- Me 2 -Ph
-156 2 CF3 S02CF3 H CH - C - Ph-156 2 CF 3 S0 2 CF 3 H CH-C-Ph
-157 2 CF3 S02CF3 H CH - CMe2- Ph-157 2 CF 3 S0 2 CF 3 H CH-CMe 2 -Ph
-158 2 CF3 H 4 - CI CH Ph-158 2 CF 3 H 4-CI CH Ph
-159 2 CF3 H 4- CI CH 2-Cl-Ph-159 2 CF 3 H 4- CI CH 2-Cl-Ph
-160 2 CF3 H 4- CI CH 3-Cl-Ph-160 2 CF 3 H 4- CI CH 3-Cl-Ph
-161 2 CF3 H 4- CI CH 4- CI - Ph-161 2 CF 3 H 4- CI CH 4- CI-Ph
-162 2 CF3 H 4 - CI CH 2 - Me - Ph-162 2 CF 3 H 4-CI CH 2-Me-Ph
-163 2 CF3 H 4 - CI CH 2 - CF3-Ph-163 2 CF 3 H 4-CI CH 2-CF 3 -Ph
-164 2 CF3 H 4- CI CH 2, 6-Cl2 - Ph-164 2 CF 3 H 4- CI CH 2, 6-Cl 2 -Ph
-165 2 CF3 H 4 - CI CH 2, 6- Me2 - Ph 167-169-166 2 CF3 H 4 - CI CH 2- CI - 6 - F - Ph-165 2 CF 3 H 4-CI CH 2, 6-Me 2 -Ph 167-169-166 2 CF 3 H 4-CI CH 2- CI-6-F-Ph
-167 2 CF3 H 4 - CI CH 2-Cl- 6- Me- Ph-167 2 CF 3 H 4-CI CH 2-Cl- 6- Me- Ph
-168 2 CF3 H 4- CI CH - CH2 - Ph-168 2 CF 3 H 4- CI CH-CH 2 -Ph
-169 2 CF3 H 4 - CI CH - CMe2-Ph -169 2 CF 3 H 4 - CI CH - CMe 2 -Ph
-170 2 CF3 H 5-C1 CH Ph-170 2 CF 3 H 5-C1 CH Ph
-171 2 CF3 H 5 - CI CH 2- CI- Ph-171 2 CF 3 H 5-CI CH 2- CI- Ph
-172 2 CF3 H 5- CI CH 3-Cl-Ph-172 2 CF 3 H 5- CI CH 3-Cl-Ph
-173 2 CF3 H 5- CI CH 4 - CI - Ph-173 2 CF 3 H 5- CI CH 4-CI-Ph
-174 2 CF3 H 5 - CI CH 2- Me - Ph-174 2 CF 3 H 5-CI CH 2- Me-Ph
-175 2 CF3 H 5- CI CH 2- CF3-Ph-175 2 CF 3 H 5- CI CH 2- CF 3 -Ph
-176 2 CF3 H 5- CI CH 2, 6- Cl2- Ph-176 2 CF 3 H 5- CI CH 2, 6- Cl 2 -Ph
-177 2 CF3 H 5 - CI CH 2, 6 - Me2- Ph 167-169-178 2 CF3 H 5- CI CH 2-Cl- 6- F - Ph-177 2 CF 3 H 5-CI CH 2, 6-Me 2 -Ph 167-169-178 2 CF 3 H 5- CI CH 2-Cl- 6- F-Ph
-179 2 CF3 H 5- CI CH 2 - CI- 6- Me- Ph-179 2 CF 3 H 5- CI CH 2-CI- 6- Me- Ph
-180 2 CF3 H 5- CI CH - CH2 - Ph-180 2 CF 3 H 5- CI CH-CH 2 -Ph
-181 2 CF3 H 5 - CI CH _CMe2 - Ph-181 2 CF 3 H 5-CI CH _CMe 2 -Ph
-182 2 CF3 H H C - Me Me-182 2 CF 3 HHC-Me Me
-183 2 CF3 H H C - Me Et 89. 1-184 2 CF3 H H C - Me n-Pr-183 2 CF 3 HHC-Me Et 89.1-184 2 CF 3 HHC-Me n-Pr
-185 2 CF3 H H C - Me i-Pr-185 2 CF 3 HHC-Me i-Pr
-186 2 CF3 H H C - Me c-Pr-186 2 CF 3 HHC-Me c-Pr
-187 2 CF3 H H C - Me n-Bu-187 2 CF 3 HHC-Me n-Bu
-188 2 CF3 H H C-Me t-Bu-188 2 CF 3 HH C-Me t-Bu
-189 2 CF3 H H C - Me c-Hex 52-54-190 2 CF3 H H C-Me - CH2 - Ph 43-45-191 2 CF3 H H C-Me - CMe2_Ph
1表 (続き) -189 2 CF 3 HHC-Me c-Hex 52-54-190 2 CF 3 HH C-Me-CH 2 -Ph 43-45-191 2 CF 3 HH C-Me-CMe 2 _Ph Table 1 (continued)
No. 置換 v n9 物性 No. Substitution v n9 Physical properties
K Λ J K K Λ J K
1 置 [融点 (°c) ] -192 2 CF3 H H C-Me Ph 1. 5476 (23°C) -193 2 CF3 H H C - Me 2- CI - Ph 51-53 -194 2 CF3 H H C-Me 3-Cl-Ph1 position [melting point (° c)] -192 2 CF 3 HH C-Me Ph 1.5476 (23 ° C) -193 2 CF 3 HHC-Me 2- CI-Ph 51-53 -194 2 CF 3 HH C -Me 3-Cl-Ph
-195 2 CF3 H H C-Me 4-Cl-Ph-195 2 CF 3 HH C-Me 4-Cl-Ph
-196 2 CF3 H H C-Me 2- Me- Ph-196 2 CF 3 HH C-Me 2- Me- Ph
-197 2 CF3 H H C-Me 2 - CF3 - Ph-197 2 CF 3 HH C-Me 2-CF 3 -Ph
-198 2 CF3 H H C-Me 2, 6- Cl2 - Ph 186-188 -199 2 CF3 H H C-Me 2, 6 - Me2 - Ph 191-193 -200 2 CF3 H H C-Me 2-Cl-6-F-Ph-198 2 CF 3 HH C-Me 2, 6- Cl 2 -Ph 186-188 -199 2 CF 3 HH C-Me 2, 6-Me 2 -Ph 191-193 -200 2 CF 3 HH C-Me 2 -Cl-6-F-Ph
-201 2 CF3 H H C-Me 2-Cl-6-Me-Ph-201 2 CF 3 HH C-Me 2-Cl-6-Me-Ph
-202 2 CF3 H H C-Me 2-Pyn-202 2 CF 3 HH C-Me 2-Pyn
-203 2 CF3 H H C-Me 3-Pyn-203 2 CF 3 HH C-Me 3-Pyn
-204 2 CF3 H . H C-Me 4-Pyn-204 2 CF 3 H. H C-Me 4-Pyn
-205 2 CF3 H H C-Me 6-C1- 2- Pyn-205 2 CF 3 HH C-Me 6-C1- 2- Pyn
-206 2 CF3 H H C-Me 5 - CF3- 2- Pyn -206 2 CF 3 HH C-Me 5 - CF 3 - 2- Pyn
-207 2 CF3 H H C-Me 6-CF3-2-Pyn-207 2 CF 3 HH C-Me 6-CF 3 -2-Pyn
-208 2 CF3 H H C-Me 6 - - 4 - CF3- 2 - Pyn -208 2 CF 3 HH C-Me 6 - - 4 - CF 3 - 2 - Pyn
-209 2 CF3 H H C-Me 2 - Pym-209 2 CF 3 HH C-Me 2-Pym
-210 2 CF3 H H C-Me 2-Pym-210 2 CF 3 HH C-Me 2-Pym
-211 2 CF3 H H C-Me 4, 6- Me2- 2- Pym -211 2 CF 3 HH C-Me 4, 6- Me 2 - 2- Pym
-212 2 CF3 H H C-Me 4, 6- (0Me) 2-2-Pym-212 2 CF 3 HH C-Me 4, 6- (0Me) 2 -2-Pym
-213 2 CF3 H H C-Me 3-Pyd-213 2 CF 3 HH C-Me 3-Pyd
-214 2 CF3 H H C-Me 6-C1- 3- Pyd-214 2 CF 3 HH C-Me 6-C1- 3- Pyd
-215 2 CF3 H H C- CF3 Me 78. 3-84. 7 -216 2 CF3 H H C- CF3 t-Bu-215 2 CF 3 HH C- CF 3 Me 78. 3-84. 7 -216 2 CF 3 HH C- CF 3 t-Bu
-217 2 CF3 H H C-CF3 - C¾-Ph-217 2 CF 3 HH C-CF 3 -C¾-Ph
-219 2 CF3 H H C - CF3 Ph-219 2 CF 3 HHC-CF 3 Ph
-220 2 CF3 H H C - CF3 2-Cl-Ph-220 2 CF 3 HHC-CF 3 2-Cl-Ph
-221 2 CF3 H H C - CF3 3 - CI - Ph-221 2 CF 3 HHC-CF 3 3-CI-Ph
-222 2 CF3 H H C - CF3 4 - CI- Ph-222 2 CF 3 HHC-CF 3 4-CI- Ph
-223 2 CF3 H H C-CF3 2- Me - Ph-223 2 CF 3 HH C-CF 3 2- Me-Ph
-224 2 CF3 H H C-CF3 2 - CF3 - Ph -224 2 CF 3 HH C-CF 3 2 - CF 3 - Ph
-225 2 CF3 H H C- CF3 2, 6- Cl2- Ph-225 2 CF 3 HH C- CF 3 2, 6- Cl 2 -Ph
-226 2 CF3 H H C - CF3 2, 6- Me2- Ph-226 2 CF 3 HHC-CF 3 2, 6- Me 2 -Ph
-227 2 CF3 H H C- CF3 2 - CI - 6- F- Ph-227 2 CF 3 HH C- CF 3 2-CI-6- F- Ph
-228 2 CF3 H H C- CF3 2-Cl- 6- Me- Ph-228 2 CF 3 HH C- CF 3 2-Cl-6-Me- Ph
-229 2 CF3 H H c-ci Me-229 2 CF 3 HH c-ci Me
-230 2 CF3 H H c-ci t-Bu-230 2 CF 3 HH c-ci t-Bu
No. 置換 R1 R2 X 丁5 R9 物性 No. Substitution R 1 R 2 X 5 R 9 Physical properties
位置 [融点 (°c) ]-232 2 CF3 H H c-ci - CMe2 - PhPosition [Melting point (° c)]-232 2 CF 3 HH c-ci-CMe 2 -Ph
-233 2 CF3 H H C - CI Ph-233 2 CF 3 HHC-CI Ph
-234 2 CF3 H H c-ci 2 - CI - Ph-234 2 CF 3 HH c-ci 2-CI-Ph
-235 2 CF3 H H c-ci 3 - CI- Ph-235 2 CF 3 HH c-ci 3-CI- Ph
-236 2 CF3 H H C - CI 4 - CI - Ph-236 2 CF 3 HHC-CI 4-CI-Ph
-237 2 CF3 H H c-ci 2-Me-Ph 49-51-238 2 CF3 H H C - CI 2 - CF3- Ph-237 2 CF 3 HH c-ci 2-Me-Ph 49-51-238 2 CF 3 HHC-CI 2-CF 3 -Ph
-239 2 CF3 H H c-ci 2, 6- Cl2- Ph-239 2 CF 3 HH c-ci 2, 6- Cl 2 -Ph
-240 2 CF3 H H c-ci 2, 6- Me2 - Ph-240 2 CF 3 HH c-ci 2, 6- Me 2 -Ph
-241 2 CF3 H H c-ci 2 - CI- 6 - F - Ph-241 2 CF 3 HH c-ci 2-CI- 6-F-Ph
-242 2 CF3 H H C-Cl 2 - CI- 6- Me- Ph-242 2 CF 3 HH C-Cl 2-CI- 6- Me- Ph
-243 2 CF3 H H C - Br Φ Me-243 2 CF 3 HHC-Br Φ Me
-244 2 CF3 H H C - Br t-Bu-244 2 CF 3 HHC-Br t-Bu
-245 2 CF3 H H C - Br o 45-48-246 2 CF3 H H C - Br -CMe2-Ph-245 2 CF 3 HHC-Br 45-48 -246 2 CF 3 HHC-Br -CMe 2 -Ph
. a . a
-247 2 CF3 H H C - Br Ph-247 2 CF 3 HHC-Br Ph
-248 2 CF3 H H C- Br 2 - CI- Ph-248 2 CF 3 HH C- Br 2-CI- Ph
-249 2 CF3 H H C - Br 3 - CI - Ph-249 2 CF 3 HHC-Br 3-CI-Ph
-250 2 CF3 H H C- Br 4-Cl-Ph-250 2 CF 3 HH C- Br 4-Cl-Ph
-251 2 CF3 H H C-Br 2-Me-Ph 57-60-252 2 CF3 H H C - Br 2-CF3-Ph-251 2 CF 3 HH C-Br 2-Me-Ph 57-60-252 2 CF 3 HHC-Br 2-CF 3 -Ph
-253 2 CF3 H H C-Br 2, 6- Cl2- Ph-253 2 CF 3 HH C-Br 2, 6- Cl 2 -Ph
-254 2 CF3 H H C-Br 2, 6- Me2 - Ph 176-178-255 2 CF3 H H C-Br 2 - Cl-6 F - Ph-254 2 CF 3 HH C-Br 2, 6- Me 2 -Ph 176-178-255 2 CF 3 HH C-Br 2-Cl-6 F-Ph
-256 2 CF3 H H C-Br 2 - CI- 6- Me- Ph-256 2 CF 3 HH C-Br 2-CI- 6- Me- Ph
-257 2 CF3 H H C-OMe Ph NMR-1-258 2 CF3 H H C-OMe 2-Cl-Ph 48-50-259 2 CF3 H H C-OMe 3 - CI - Ph-257 2 CF 3 HH C-OMe Ph NMR-1-258 2 CF 3 HH C-OMe 2-Cl-Ph 48-50-259 2 CF 3 HH C-OMe 3-CI-Ph
-260 2 CF3 H H C-OMe 4-Cl-Ph-260 2 CF 3 HH C-OMe 4-Cl-Ph
-261 2 CF3 H H C-OMe 2, 6-Cl2-Ph-261 2 CF 3 HH C-OMe 2, 6-Cl 2 -Ph
-262 2 CF3 H H 2, 6-Me2-Ph-262 2 CF 3 HH 2, 6-Me 2 -Ph
-263 2 CF3 H H C-OMe 2-Cl-6-F-Ph-263 2 CF 3 HH C-OMe 2-Cl-6-F-Ph
-264 2 CF3 H H C-OMe 2- Cl-6 - Me - Ph-264 2 CF 3 HH C-OMe 2- Cl-6-Me-Ph
-265 2 CF3 H H C-SMe Ph 1. 5518 (23。C)-266 2 CF3 H H C SMe 2 - CI - Ph 58 - 60-267 2 CF3 H H C-SMe 3-Cl-Ph-265 2 CF 3 HH C-SMe Ph 1.555 (23.C) -266 2 CF 3 HHC SMe 2-CI-Ph 58-60 -267 2 CF 3 HH C-SMe 3-Cl-Ph
-268 2 CF3 H H C-SMe 4-Cl-Ph 121-123-269 2 CF3 H H C-SMe 2, 6 - Cl2 - Ph-268 2 CF 3 HH C-SMe 4-Cl-Ph 121-123-269 2 CF 3 HH C-SMe 2, 6-Cl 2 -Ph
-270 2 CF3 H H C-SMe 2, 6- Me2 - Ph-270 2 CF 3 HH C-SMe 2, 6-Me 2 -Ph
-271 2 CF3 H H C-SMe 2-Cl-6-F-Ph
1表 (続き) -271 2 CF 3 HH C-SMe 2-Cl-6-F-Ph Table 1 (continued)
No. 換 物性 No. Commutative properties
R1 R2 X J5 R9 R 1 R 2 XJ 5 R 9
1ϋ置 [融点( c) ]-272 2 CF3 H H C-SMe 2 - CI - 6 - Me_Ph1 position [melting point (c)]-272 2 CF 3 HH C-SMe 2-CI-6-Me_Ph
-273 2 CF3 H H C-SCHF2 Ph 49-51-274 2 CF3 H H C-SCHF2 2-Cl-Ph-273 2 CF 3 HH C-SCHF 2 Ph 49-51-274 2 CF 3 HH C-SCHF 2 2-Cl-Ph
-275 2 CF3 H H C - SCHF2 3 - CI- Ph-275 2 CF 3 HHC-SCHF 2 3-CI- Ph
-276 2 CF3 H H C-SCHF2 4-Cl-Ph-276 2 CF 3 HH C-SCHF 2 4-Cl-Ph
-277 2 CF3 H H C - SCHF2 2, 6- Cl2- Ph-277 2 CF 3 HHC-SCHF 2 2, 6- Cl 2 -Ph
-278 2 CF3 H H C - SCHF2 2, 6 - Me2 - Ph-278 2 CF 3 HHC-SCHF 2 2, 6-Me 2 -Ph
-279 2 CF3 H H C - SOMe Ph 69-71-280 2 CF3 H H C-SOMe 2 - CI- Ph-279 2 CF 3 HHC-SOMe Ph 69-71 -280 2 CF 3 HH C-SOMe 2-CI- Ph
-281 2 CF3 H H C - SOMe 3-Cl-Ph-281 2 CF 3 HHC-SOMe 3-Cl-Ph
-282 2 CF3 H H C-SOMe 4 - CI - Ph 149-150-283 2 CF3 H H C-SOMe 2, 6- Cl2- Ph-282 2 CF 3 HH C-SOMe 4-CI-Ph 149-150 -283 2 CF 3 HH C-SOMe 2, 6- Cl 2 -Ph
-284 2 CF3 H H C-SOMe 2, 6- Me2 - Ph-284 2 CF 3 HH C-SOMe 2, 6- Me 2 -Ph
-285 2 CF3 H H C-S02Me Ph 70-72-286 2 CF3 H H C-S02Me 2-Cl-Ph 154-156-287 2 CF3 H H C-S02Me 3 - CI - Ph-285 2 CF 3 HH C-S0 2 Me Ph 70-72-286 2 CF 3 HH C-S0 2 Me 2-Cl-Ph 154-156-287 2 CF 3 HH C-S0 2 Me 3-CI-Ph
-288 2 CF3 H H C-S02Me 4 - CI - Ph 141-143-289 2 CF3 H H C-S02Me 2, 6_C12 - Ph-288 2 CF 3 HH C-S0 2 Me 4-CI-Ph 141-143 -289 2 CF 3 HH C-S0 2 Me 2, 6_C1 2 -Ph
-290 2 CF3 H H C-S02Me 2, 6 - Me2 - Ph-290 2 CF 3 HH C-S0 2 Me 2, 6-Me 2 -Ph
-291 2 CF3 H H C-Ph Et 142-144-292 2 CF3 H H C-Ph Ph 159 - 160-293 2 CF3 H H C-Ph 2, 6- Cl2 - Ph-291 2 CF 3 HH C-Ph Et 142-144-292 2 CF 3 HH C-Ph Ph 159-160-293 2 CF 3 HH C-Ph 2, 6- Cl 2 -Ph
-294 2 CF3 H H C-Ph 2, 6 - Me2 - Ph-294 2 CF 3 HH C-Ph 2, 6-Me 2 -Ph
-295 3 CF3 H H CH Me-295 3 CF 3 HH CH Me
-296 3 CF3 H H CH t-Bu-296 3 CF 3 HH CH t-Bu
-297 3 CF3 H H CH - CH2 - Ph-297 3 CF 3 HH CH-CH 2 -Ph
-298 3 CF3 H H CH -CMe2-Ph-298 3 CF 3 HH CH -CMe 2 -Ph
-299 3 CF3 H H CH Ph-299 3 CF 3 HH CH Ph
-300 3 CF3 H H CH 2-Cl-Ph-300 3 CF 3 HH CH 2-Cl-Ph
-301 3 CF3 H H CH 3-Cl-Ph-301 3 CF 3 HH CH 3-Cl-Ph
-302 3 CF3 H H CH 4- CI- Ph-302 3 CF 3 HH CH 4- CI- Ph
-303 3 CF3 H H CH 2- Me- Ph-303 3 CF 3 HH CH 2- Me- Ph
-304 3 CF3 H H CH 2-CF3-Ph-304 3 CF 3 HH CH 2-CF 3 -Ph
-305 3 CF3 H H CH 2, 6- Cl2- Ph-305 3 CF 3 HH CH 2, 6- Cl 2 -Ph
-306 3 CF3 H H CH 2, 6- Me2 - Ph-306 3 CF 3 HH CH 2, 6-Me 2 -Ph
-307 3 CF3 H H CH 2 - CI - 6 - F - Ph-307 3 CF 3 HH CH 2-CI-6-F-Ph
-308 3 CF3 H H CH 2-Cl-6-Me-Ph-308 3 CF 3 HH CH 2-Cl-6-Me-Ph
-309 4 CF3 H H CH Me-309 4 CF 3 HH CH Me
-310 4 CF3 H H CH t-Bu-310 4 CF 3 HH CH t-Bu
-311 4 CF3 H H CH - CH2 - Ph
1表 (続き) -311 4 CF 3 HH CH-CH 2 -Ph Table 1 (continued)
No. 置換 物性 No. Substitution physical properties
R1 R2 X J5 R9 R 1 R 2 XJ 5 R 9
1^置 [融点 (°c) ]-312 4 CF3 H H CH - CMe2- Ph1 ^ place [melting point (° c)]-312 4 CF 3 HH CH-CMe 2 -Ph
-313 4 CF3 H H CH Ph-313 4 CF 3 HH CH Ph
-314 4 CF3 H H CH 2-Cl-Ph-314 4 CF 3 HH CH 2-Cl-Ph
-315 4 CF3 H H CH 3-Cl-Ph-315 4 CF 3 HH CH 3-Cl-Ph
-316 4 CF3 H H CH 4 - CI- Ph-316 4 CF 3 HH CH 4-CI- Ph
-317 4 CF3 H H CH 2- Me- Ph-317 4 CF 3 HH CH 2- Me- Ph
-318 4 CF3 H H CH 2-CF3-Ph-318 4 CF 3 HH CH 2-CF 3 -Ph
-319 4 CF3 H H CH 2, 6- Cl2 - Ph-319 4 CF 3 HH CH 2, 6- Cl 2 -Ph
-320 4 CF3 H H CH 2, 6- Me2 - Ph-320 4 CF 3 HH CH 2, 6- Me 2 -Ph
-321 4 CF3 H H CH 2- CI - 6- F - Ph-321 4 CF 3 HH CH 2- CI-6- F-Ph
-322 4 CF3 H H CH 2 - CI- 6-Me - Ph -322 4 CF 3 HH CH 2-CI-6-Me-Ph
4- (4-CF3-Ph) -4- (4-CF 3 -Ph)-
9 CH 136-138 9 CH 136-138
Ph Ph
2-Me-4-(4-€F3--324 2 CF3 H H CH 65-67 2-Me-4- (4- € F 3 --324 2 CF 3 HH CH 65-67
Ph) - Ph Ph)-Ph
-325 2 CF3 H 4 - CI CH 2-Pyn 46-48-326 2 CF3 H H C-Br 2, 3- Cl2- Ph 143-145 -325 2 CF 3 H 4-CI CH 2-Pyn 46-48-326 2 CF 3 HH C-Br 2, 3- Cl 2 -Ph 143-145
2 - (1-Me-n- 1. 5226 (28-327 2 CF3 H H CH 2-(1-Me-n- 1.5226 (28-327 2 CF 3 HH CH
C5HU) - Ph C)-328 2 CF3 H H CH c~Hex 114-116
C 5 H U )-Ph C) -328 2 CF 3 HH CH c ~ Hex 114-116
-般式 (1—4 ) -General formula (1-4)
(m= 0 A= X 1 2 ヽ G1=0、 丁 5=N) (m = 0 A = X 1 2 ヽ G 1 = 0, c = 5 )
置換 物性 Substitution physical properties
No. R1 R2 X J4 R9 No. R 1 R 2 XJ 4 R 9
置 [融点 ( C) j [Melting point (C) j
2-1 2 CF3 H H CH Me 2-1 2 CF 3 HH CH Me
2-2 2 CF3 H H CH Et 2-2 2 CF 3 HH CH Et
2-3 2 CF3 H H CH n-Pr 2-3 2 CF 3 HH CH n-Pr
2-4 2 CF3 H H CH i - Pr 2-4 2 CF 3 HH CH i-Pr
2-5 2 CF3 H H CH c-Pr 2-5 2 CF 3 HH CH c-Pr
2-6 2 CF3 H H CH n-Bu 2-6 2 CF 3 HH CH n-Bu
2-7 2 CF3 H H CH t-Bu 2-7 2 CF 3 HH CH t-Bu
2 ο 2 ο
2-8 CF3 H H CH - CH2 - Ph 104. 22-8 CF 3 HH CH-CH 2 -Ph 104. 2
2-9 2 CF3 H H CH _C¾- (2- CI - Ph) 49. 82-9 2 CF 3 HH CH _C¾- (2- CI-Ph) 49.8
2-10 2 CF3 H H CH - CH2- (3 - Cl_Ph) 2-10 2 CF 3 HH CH-CH 2- (3-Cl_Ph)
2-11 2 CF3 H H CH - CH2 - (4 - CI- Phノ 2-11 2 CF 3 HH CH-CH 2- (4-CI- Ph
r r
2 - 12 2 CF3 H H CH - CH2 - (2, 6- Cl2- Ph) 136. 6-138. 12-12 2 CF 3 HH CH-CH 2- (2, 6- Cl 2 -Ph) 136.6-138.1
2 - 13 2 CF3 H H CH - CHMe- Ph 2-13 2 CF 3 HH CH-CHMe- Ph
1 1
2 - 14 o CF3 H H し H —CHMe - (2—し 1- Ph) 2-14 o CF 3 HH then H —CHMe-(2—1-Ph)
Z o 1 Z o 1
-I D a o CF3 H ri し hi —し HMe—(^一し丄一 PhJ -ID ao CF 3 H ri then hi — then HMe— (^^^
-丄 t) CF3 rl し H —し HMe— 4一し丄一 hJ -丄 t) CF 3 rl then H — then HMe — 4 1 丄 1 hJ
P P
2-18 2 CF3 H H CH - CMe2 - Ph 2-18 2 CF 3 HH CH-CMe 2 -Ph
2-19 2 CF3 H H CH - CMe2- (2- CI- Ph) 2-19 2 CF 3 HH CH - CMe 2 - (2- CI- Ph)
2-20 2 CF3 H H CH CMe2- (3 - CI- Ph) 2-20 2 CF 3 HH CH CMe 2- (3-CI- Ph)
2-21 2 CF3 H H CH CMe2- (4 - -Ph) 2-21 2 CF 3 HH CH CMe 2- (4--Ph)
2-22 2 CF3 H H CH 一 CMe2— (2, 6 - Cl2— Ph) 2-22 2 CF 3 HH CH i CMe 2 — (2, 6-Cl 2 — Ph)
2-23 2 CF3 H H CH Ph 94. 22-23 2 CF 3 HH CH Ph 94.2
2-24 2 CF3 H H CH 2-F-Ph 161. 32-24 2 CF 3 HH CH 2-F-Ph 161.3
2-25 2 CF3 H H CH 3-F-Ph 2-25 2 CF 3 HH CH 3-F-Ph
2-26 2 CF3 H H CH 4-F-Ph 2-26 2 CF 3 HH CH 4-F-Ph
2-27 2 CF3 H H CH 2 - CI- Ph 187. 92-27 2 CF 3 HH CH 2-CI- Ph 187.9
2 28 2 CF3 H H CH 3 - CI- Ph 113. 2-120. 82 28 2 CF 3 HH CH 3-CI- Ph 113. 2-120. 8
2 - 29 2 CF3 H H CH 4-Cl-Ph 175. 62-29 2 CF 3 HH CH 4-Cl-Ph 175.6
2-30 2 CF3 H H CH 2 - Br- Ph 118. 32-30 2 CF 3 HH CH 2-Br- Ph 118. 3
2-31 2 CF3 H H CH 3 - Br- Ph
9 'SOS - 0 "^02 HO H H ¾3 Ζ IL-Z2-31 2 CF 3 HH CH 3-Br- Ph 9 'SOS-0 "^ 02 HO HH ¾3 Ζ IL-Z
6'9AI - 'Ζ HO H H "dD Ζ OL-Z6'9AI-'Ζ HO H H "dD Ζ OL-Z
9 ' ST-8 'Ζ 1 HO H H ¾D Ζ 69- Ζ9 'ST-8' Ζ 1 HO H H ¾D Ζ 69- Ζ
I ' AT-g - ix H3 H H ¾0 Ζ 89 - SI 'AT-g-ix H3 H H ¾0 Ζ 89-S
Z '6ZI-S "92T HD H H ¾3 Ζ L9-ZZ '6ZI-S "92T HD H H ¾3 Ζ L9-Z
9 'III H3 H H . ¾0 ζ 99-29 'III H3 H H. ¾0 ζ 99-2
9 "90S HO H H ¾0 ζ 9 "90S HO H H ¾0 ζ
9 '691— ΐ ·69ΐ ぶ 9 '691— ΐ · 69ΐ
O OHH HD H H sdつ ζ n-zO OHH HD HH s d ζ nz
I '291-9 "I9T Md-¾11— I— !~S ¾ Η3· H H つ ζ 29-ZI '291-9 "I9T Md-¾11— I—! ~ S ¾ Η3 · H H ζ 29-Z
O LO H3 H H ζ Z9-Z O LO H3 H H ζ Z9-Z
Z '6 l~ '8SI HO H H ¾D ζ 19 - 2Z '6 l ~' 8SI HO H H ¾D ζ 19-2
S '69Z-6 HO H H ¾D ζ 09-2 S '69Z-6 HO H H ¾D ζ 09-2
HD H H ζ 6 -Z HD H H ζ 6 -Z
HO H H ¾つ ζ 89-2HO H H ¾ ζ 89-2
HO H H ζ 19-Z J.JJ HO H H ¾a ζ 9 -Z HO H H ζ 19-Z J.JJ HO H H ¾a ζ 9 -Z
H3 H H ζ 99-S H3 H H ζ 99-S
HO H H ¾3 ζ f -Z — HO H H ζ HO H H ¾3 ζ f -Z — HO H H ζ
HO H H つ ζ HO H H つ
L[C [一 g HD H H ζ L [C [one g HD H H ζ
H3 H H つ ζ 09-Z —¾N - S HD H H ζ 6f-Z 一 N一 HO H H ¾3 ζ 8 S H3 H H つ 09-Z —¾N-S HD H H ζ 6f-Z one N one HO H H ¾3 ζ 8 S
H Z HO H H ζ L -Z H Z HO H H ζ L -Z
HD H H つ ζ Q -Z 一9 OS - 2 HO H H つ ζ -Z HD HH ζ Q-Z 9 OS-2 HO HH ζ -Z
HO H H ζ -Z HO H H ζ -Z
6 "9^1 - HO H . H ¾0 ζ f-Z6 "9 ^ 1-HO H. H ¾0 ζ f-Z
- 0 - ε HD H H ζ Z -Z -0-ε HD H H ζ Z -Z
OAT - 0 - s HO H H ¾つ ζ If-Z ΐ - z HO H H ζ O -Z - 3- Z HO H H ζ OAT-0-s HO H H ¾-If-Z ΐ-z HO H H ζ O -Z-3-Z HO H H ζ
6 '9εΐ - - HO H H つ ζ 88-Z 6 '9εΐ--HO H H つ ζ 88-Z
L ·χεΐ-0 Έ2ΐ - - ε HO H H つ ζ ζε-ζL · χεΐ-0 Έ2ΐ--ε HO H H ζ ζε-ζ
Z ·98ΐ HO H H ¾っ ζZ · 98ΐ HO H H
- 1 - HO H H ζ -1-HO H H ζ
- 1- ε HO H H ¾つ ζ n-z - 1 - 2 HO H H ζ εε- s -1- ε HO H H ¾-n-z-1-2 HO H H ζ εε- s
HO H H ζ HO H H ζ
¾7Ϊ) (¾7Ϊ)
6y X 6 y X
¾呦 m •O ¾ 呦 m • O
Ψ Ψ
S0l7600/C00Zdf/X3d 6ひ ΪΪ0請 OAV
2表 (続き) S0l7600 / C00Zdf / X3d 6h ΪΪ0 contract OAV Table 2 (continued)
No. w W\±. No. w W \ ±.
R1 R2 X J5 R9 R 1 R 2 XJ 5 R 9
1 LraS^?、( C)」 1 LraS ^? , (C) "
2-72 2 CF3 H H CH 3 - CI - 4 - Me - Ph 1462-72 2 CF 3 HH CH 3-CI-4-Me-Ph 146
2-73 2 CF3 H H CH 2, 3-Me2-Ph 212. 0-216. 42-73 2 CF 3 HH CH 2, 3-Me 2 -Ph 212. 0-216. 4
2-74 2 CF3 H H CH 2, 4_Me2 - Ph 2-74 2 CF 3 HH CH 2, 4_Me 2 -Ph
2-75 2 CF3 H H CH 3 - CI - 4 - Me - Ph 146. 02-75 2 CF 3 HH CH 3-CI-4-Me-Ph 146.0
2-76 2 CF3 H H CH 2, 6 - Me2- Ph 163. 7-165. 32-76 2 CF 3 HH CH 2, 6-Me 2 -Ph 163.7-165.3
2-77 2 CF3 H H CH 2, 6 - Et2 - Ph 2-77 2 CF 3 HH CH 2, 6-Et 2 -Ph
2-78 2 CF3 H H CH 2, 6- (OMe) 2 - Ph 2-78 2 CF 3 HH CH 2, 6- (OMe) 2 -Ph
2-79 2 CF3 H H CH 2 - Me - 4 - i - C3F7-Ph 91. 1-120. 62-79 2 CF 3 HH CH 2-Me-4-i-C 3 F 7 -Ph 91.
2 - 80 2 CF3 H H CH 2, 6- (CF3) 2- Ph 2-80 2 CF 3 HH CH 2, 6- (CF 3 ) 2 -Ph
2-81 2 CF3 H H CH 2- Cト 6-Me- Ph 158. 3-163. 12-81 2 CF 3 HH CH 2-C 6-Me- Ph 158.3-163.1
2-82 2 CF3 H H CH 2, 3, 5, 6— F4— Ph 157. 2-160. 22-82 2 CF 3 HH CH 2, 3, 5, 6— F 4 — Ph 157. 2-160. 2
2-83 2 CF3 H H CH 2, 3, 4, 5, 6— F5_Ph 180. 9-181. 22-83 2 CF 3 HH CH 2, 3, 4, 5, 6—F 5 _Ph 180. 9-181. 2
2-84 2 CF3 H H CH 2, 3, 4- Cl3- Ph 2-84 2 CF 3 HH CH 2, 3, 4-Cl 3 -Ph
2-85 2 CF3 H H CH 2, 4, 6-Cl3-Ph 171. 1-171. 22-85 2 CF 3 HH CH 2, 4, 6-Cl 3 -Ph 171.1-171.2
2-86 2 CF3 H H CH 2, 6- Cl2 - 4一 CF3 - Ph 124. 22-86 2 CF 3 HH CH 2, 6- Cl 2-4 CF 3 -Ph 124. 2
2-87 2 CF3 H H CH 寸 108. 1 o 2-87 2 CF 3 HH CH Dimension 108.1 o
2-88 2 CF3 H H CH 2, 6-Br2-4-F-Ph 170. 5-173. 22-88 2 CF 3 HH CH 2, 6-Br 2 -4-F-Ph 170. 5-173. 2
2-89 2 CF3 H H CH 2 - Pyn 2-89 2 CF 3 HH CH 2-Pyn
2-90 2 CF3 H H CH 3-Pyn 2-90 2 CF 3 HH CH 3-Pyn
2-91 2 CF3 H H CH 4- Pyn 2-91 2 CF 3 HH CH 4- Pyn
2-92 2 CF3 H H CH 6 - CI- 2- Pyn 64. 9-68. 62-92 2 CF 3 HH CH 6-CI- 2- Pyn 64. 9-68. 6
2-93 2 CF3 H H CH 3, 5— Cl2 - 2 - Pyn 157. 9-158. 5 2-93 2 CF 3 HH CH 3, 5- Cl 2 - 2 -. Pyn 157. 9-158 5
2-94 2 CF3 H H CH 6-Cl- 4- CF3_2- Pyn 52. 1-63. 02-94 2 CF 3 HH CH 6-Cl- 4-CF 3 _2- Pyn 52. 1-63. 0
2-95 2 CF3 H H CH 2 - Pym 2-95 2 CF 3 HH CH 2-Pym
2-96 2 CF3 H H CH 4- Pym 2-96 2 CF 3 HH CH 4- Pym
2-97 2 CF3 H H CH 4, 6- Me2 - 2- Pym 2-97 2 CF 3 HH CH 4, 6- Me 2 - 2- Pym
2-98 2 CF3 H H CH 4, 6- (OMe) 2- 2- Pym 226. 3-226. 6 2-98 2 CF 3 HH CH 4, 6- (OMe) 2 -. 2- Pym 226. 3-226 6
2 - 99 2 CF3 H H CH 3-Pyd 2-99 2 CF 3 HH CH 3-Pyd
2-100 2 CF3 H H CH 6- CI- 3 - Pyd 2-100 2 CF 3 HH CH 6- CI-3-Pyd
2-101 2 CF3 H H CH - CO -丽 e 2-101 2 CF 3 HH CH-CO-丽 e
2-102 2 CF3 H H CH - CO - NHPh 2-102 2 CF 3 HH CH-CO-NHPh
2-103 2 CF3 H H CH - CO- NMePh 2-103 2 CF 3 HH CH-CO- NMePh
2-104 2 CF3 H H CH -CO-NEt (c-Hex) 2-104 2 CF 3 HH CH -CO-NEt (c-Hex)
u u
Z -丄 Ub o u Z-丄 Ub o u
しト n Π し H -C0-N (i-Pr) 2 ト n し H H -C0-N (i-Pr) 2
2-106 2 CF3 Me H CH Ph 2-106 2 CF 3 Me H CH Ph
2-107 2 CF3 Me H CH 2-Cl-Ph 2-107 2 CF 3 Me H CH 2-Cl-Ph
2-108 2 CF3 Me H CH 2, 6- Cl2 - Ph 2-108 2 CF 3 Me H CH 2, 6- Cl 2 -Ph
2-109 2 CF3 Me H CH 2, 6- Me2_Ph 2-109 2 CF 3 Me H CH 2, 6- Me 2 _Ph
2-110 2 CF3 Me H CH -CH2-Ph 2-110 2 CF 3 Me H CH -CH 2 -Ph
2-111 2 CF3 Me H CH
表 (続き) 2-111 2 CF 3 Me H CH Table (continued)
No. 置換 物性 No. Substitution physical properties
R1 R2 X J5 R9 R 1 R 2 XJ 5 R 9
[融点 (°c) ]-112 2 CF3 COMe H CH Ph[Melting point (° c)]-112 2 CF 3 COMe H CH Ph
-113 2 CF3 COMe H CH 2 - CI - Ph-113 2 CF 3 COMe H CH 2-CI-Ph
-114 2 CF3 COMe H CH 2, 6-Cl2-Ph-114 2 CF 3 COMe H CH 2, 6-Cl 2 -Ph
-115 2 CF3 COMe H CH 2, 6 - Me2— Ph-115 2 CF 3 COMe H CH 2, 6-Me 2 — Ph
-116 2 CF3 COMe H CH - CH2 - Ph-116 2 CF 3 COMe H CH-CH 2 -Ph
-117 2 CF3 COMe H CH - CMe2 - Ph-117 2 CF 3 COMe H CH-CMe 2 -Ph
-118 2 CF3 C02Me H CH Ph-118 2 CF 3 C0 2 Me H CH Ph
-119 2 CF3 C02Me H CH 2 - CI- Ph-119 2 CF 3 C0 2 Me H CH 2-CI- Ph
-120 2 CF3 C02Me H CH 2, 6- Cl2- Ph -120 2 CF 3 C0 2 Me H CH 2, 6- Cl 2 -Ph
- 121 2 CF3 C02Me H CH 2, 6- Me2-Ph-121 2 CF 3 C0 2 Me H CH 2, 6- Me 2 -Ph
-122 2 CF3 C02Me H CH - CH2 - Ph-122 2 CF 3 C0 2 Me H CH-CH 2 -Ph
-123 2 CF3 C02Me H CH - CMe2- Ph-123 2 CF 3 C0 2 Me H CH-CMe 2 -Ph
-124 2 CF3 S02CF3 H CH Ph -124 2 CF 3 S0 2 CF 3 H CH Ph
- 125 2 CF3 S02CF3 H CH 2- CI - Ph-125 2 CF 3 S0 2 CF 3 H CH 2- CI-Ph
-126 2 CF3 S02CF3 H CH 2, 6 - Cl2- Ph-126 2 CF 3 S0 2 CF 3 H CH 2, 6-Cl 2 -Ph
127 2 CF3 S02CF3 H CH 2, 6— Me2_Ph127 2 CF 3 S0 2 CF 3 H CH 2, 6—Me 2 _Ph
-128 2 CF3 S02CF3 H CH - CH2 - Ph-128 2 CF 3 S0 2 CF 3 H CH-CH 2 -Ph
-129 2 CF3 S02CF3 H CH — CMe2 - Ph -129 2 CF 3 S0 2 CF 3 H CH — CMe 2 -Ph
- 130 2 CF3 H 5 - Me CH Ph 91. 7-106. 2-131 2 CF3 H 4- CI CH Ph-130 2 CF 3 H 5-Me CH Ph 91. 7-106. 2-131 2 CF 3 H 4- CI CH Ph
-132 2 CF3 H 4 - CI CH 2- CI- Ph-132 2 CF 3 H 4-CI CH 2- CI- Ph
-133 2 CF3 H 4- CI CH 2, 6- Cl2- Ph-133 2 CF 3 H 4- CI CH 2, 6- Cl 2 -Ph
-134 2 CF3 H 4- CI CH 2 - CI- 6 - F - Ph-134 2 CF 3 H 4- CI CH 2-CI- 6-F-Ph
-135 2 CF3 H 4 - CI CH 2, 6— Me2- Ph-135 2 CF 3 H 4-CI CH 2,6—Me 2 -Ph
-136 2 CF3 H 4-C1 CH 2-Cl-6-Me-Ph-136 2 CF 3 H 4-C1 CH 2-Cl-6-Me-Ph
-137 2 CF3 H 4- CI CH - CH2 - Ph -137 2 CF 3 H 4- CI CH-CH 2 -Ph
- 138 2 CF3 H 4- CI CH - CMe2- Ph-138 2 CF 3 H 4- CI CH-CMe 2 -Ph
-139 2 CF3 H 5 - CI CH Ph-139 2 CF 3 H 5-CI CH Ph
-140 2 CF3 H 5- CI CH 2-Cl-Ph-140 2 CF 3 H 5- CI CH 2-Cl-Ph
-141 2 CF3 H 5- CI CH 2, 6 - Cl2 - Ph-141 2 CF 3 H 5- CI CH 2, 6-Cl 2 -Ph
-142 2 CF3 H 5- CI CH 2- Cト 6 - F- Ph-142 2 CF 3 H 5- CI CH 2-C 6-F- Ph
-143 2 CF3 H 5-C1 CH 2, 6- Me2_Ph-143 2 CF 3 H 5-C1 CH 2, 6- Me 2 _Ph
-144 2 CF3 H 5-C1 CH 2- CI- 6- Me - Ph-144 2 CF 3 H 5-C1 CH 2- CI- 6- Me-Ph
-145 2 CF3 H 5- CI CH-145 2 CF 3 H 5- CI CH
-146 2 CF3 H 5- CI CH 一 CMe2- Ph-146 2 CF 3 H 5- CI CH one CMe 2 -Ph
-147 3 CF3 H H CH Me -147 3 CF 3 HH CH Me
- 148 3 CF3 H H CH -CH2-Ph-148 3 CF 3 HH CH -CH 2 -Ph
-149 3 CF3 H H CH -CMe2-Ph-149 3 CF 3 HH CH -CMe 2 -Ph
-150 3 CF3 H H CH Ph-150 3 CF 3 HH CH Ph
-151 3 CF3 H H CH 2-Cl-Ph
2表 (続き) -151 3 CF 3 HH CH 2-Cl-Ph Table 2 (continued)
No. ]ί換 R1 物性 No.] ίR 1 Physical properties
R2 X J5 R9 R 2 XJ 5 R 9
1ϋ置 [融点 (°c)]-152 3 CF3 H H CH 2 - CF3 - Ph 1 position [melting point (° c)]-152 3 CF 3 HH CH 2-CF 3 -Ph
- 153 3 CF3 H H CH 2, 6_C12- Ph-153 3 CF 3 HH CH 2, 6_C1 2 -Ph
-154 3 CF3 H H CH 2, 6-Me2-Ph-154 3 CF 3 HH CH 2, 6-Me 2 -Ph
-155 4 CF3 H H CH Me-155 4 CF 3 HH CH Me
-156 4 CF3 H H CH-156 4 CF 3 HH CH
-157 4 CF3 H H CH - CMe2 - Ph-157 4 CF 3 HH CH-CMe 2 -Ph
-158 4 CF3 H H CH Ph-158 4 CF 3 HH CH Ph
-159 4 CF3 H H CH 2 - CI- Ph-159 4 CF 3 HH CH 2-CI- Ph
-160 4 CF3 H H CH 2- CF3 - Ph-160 4 CF 3 HH CH 2- CF 3 -Ph
-161 4 CF3 H H CH 2, 6- Cl2 - Ph-161 4 CF 3 HH CH 2, 6- Cl 2 -Ph
-162 4 CF3 H H CH 2, 6- Me2- Ph-162 4 CF 3 HH CH 2, 6- Me 2 -Ph
-163 2 CHF2 H H CH t-Bu-163 2 CHF 2 HH CH t-Bu
-164 2 CHF2 H H CH - CH2 - Ph-164 2 CHF 2 HH CH-CH 2 -Ph
-165 2 CHF2 H H CH - CMe2 - Ph-165 2 CHF 2 HH CH-CMe 2 -Ph
-166 2 CHF2 H H CH Ph-166 2 CHF 2 HH CH Ph
-167 2 CHF2 H H CH 2 - CI - Ph 188. 1-168 2 CHF2 H H CH 2 - OMe-Ph-167 2 CHF 2 HH CH 2-CI-Ph 188. 1-168 2 CHF 2 HH CH 2-OMe-Ph
-169 2 CHF2 H H CH 2- CF3 - Ph 176. 7-182.-170 2 CHF2 H H CH 2 - OCF3 - Ph-169 2 CHF 2 HH CH 2- CF 3 -Ph 176. 7-182.-170 2 CHF 2 HH CH 2-OCF 3 -Ph
-171 2 CHF2 H H CH 2, 6- Cl2 - Ph-171 2 CHF 2 HH CH 2, 6- Cl 2 -Ph
-172 2 CHF2 H H CH 2, 6- Me2 - Ph-172 2 CHF 2 HH CH 2, 6-Me 2 -Ph
-173 2 CF3 H H C-Me t-Bu -173 2 CF 3 HH C-Me t-Bu
- 174 2 CF3 H H C - Me - CH2 - Ph-174 2 CF 3 HHC-Me-CH 2 -Ph
-175 2 CF3 H H C-Me - CMe2- Ph-175 2 CF 3 HH C-Me-CMe 2 -Ph
-176 2 CF3 H H C-Me Ph . 180. 6-177 2 CF3 H H C-Me 2- CI- Ph 1. 5532 (24。C)-178 2 CF3 H H C-Me 3-Cl-Ph-176 2 CF 3 HH C-Me Ph. 180. 6-177 2 CF 3 HH C-Me 2- CI- Ph 1.5532 (24.C) -178 2 CF 3 HH C-Me 3-Cl-Ph
-179 2 CF3 H H C-Me 4 - CI- Ph-179 2 CF 3 HH C-Me 4-CI- Ph
-180 2 CF3 H H C-Me 2-Me-Ph-180 2 CF 3 HH C-Me 2-Me-Ph
-181 2 CF3 H H C-Me . 2- OMe-Ph-181 2 CF 3 HH C-Me. 2- OMe-Ph
-182 2 CF3 H H C-Me 2 - CF3- Ph-182 2 CF 3 HH C-Me 2-CF 3 -Ph
-183 2 CF3 H H C-Me 2 - OCF3-Ph-183 2 CF 3 HH C-Me 2-OCF 3 -Ph
-184 2 CF3 H H C-Me 2, 6 - Cl2 - Ph 223. 5-185 2 CF3 H H C-Me 2, 4, 6 - Cl3- Ph 175. 7-186 2 CF3 H H C-Me 2, 6- Me2- Ph 161. 5-187 2 CF3 H H C-Me 2 - CI- 6- Me - Ph-184 2 CF 3 HH C-Me 2, 6-Cl 2 -Ph 223.5-185 2 CF 3 HH C-Me 2, 4, 6-Cl 3 -Ph 175.7-186 2 CF 3 HH C- Me 2, 6- Me 2 -Ph 161.5-187 2 CF 3 HH C-Me 2-CI- 6- Me-Ph
-188 2 CF3 H H C-Me 2-Pyn-188 2 CF 3 HH C-Me 2-Pyn
-189 2 CF3 H H C-Me 3-Pyn-189 2 CF 3 HH C-Me 3-Pyn
-190 2 CF3 H H C-Me 4-Pyn-190 2 CF 3 HH C-Me 4-Pyn
-191 2 CF3 H H C-Me 6 - Cl2 - Pyn
2表 (続き) -191 2 CF 3 HH C-Me 6-Cl 2 -Pyn Table 2 (continued)
No. 置換 物性 No. Substitution physical properties
R1 R2 X J5 R9 R 1 R 2 XJ 5 R 9
[融点 (°C) ]-192 2 CF3 H H C-Me 6-CF3-2-Pyn[Melting point (° C)]-192 2 CF 3 HH C-Me 6-CF 3 -2-Pyn
-193 2 CF3 H H C- Me 6 - C卜 4 - CF3 - 2 - Pyn -193 2 CF 3 HH C- Me 6 - C Bok 4 - CF 3 - 2 - Pyn
-194 2 CF3 H H C-Me 2 - Pym-194 2 CF 3 HH C-Me 2-Pym
-195 2 CF3 H H C-Me 4 - Pym-195 2 CF 3 HH C-Me 4-Pym
-196 2 CF3 H H C-Me 4, 6- Me2 - 2 - Pym -196 2 CF 3 HH C-Me 4, 6- Me 2 - 2 - Pym
-197 2 CF3 H H C-Me 4, 6 -(OMe) 2-2 - Pym-197 2 CF 3 HH C-Me 4, 6-(OMe) 2 -2-Pym
-198 2 CF3 H H C-Me 3 - Pyd-198 2 CF 3 HH C-Me 3-Pyd
-199 2 CF3 H H C-Me 6-Cl-3-Pyd-199 2 CF 3 HH C-Me 6-Cl-3-Pyd
-200 2 CF3 H H C-Me -CO-NHMe-200 2 CF 3 HH C-Me -CO-NHMe
-201 2 CF3 H H C-Me -CO-NHPh-201 2 CF 3 HH C-Me -CO-NHPh
-202 2 CF3 H H C-Me -CO-NMePh-202 2 CF 3 HH C-Me -CO-NMePh
-203 2 CF3 H H C-Me -CO-NEt (c - Hex)-203 2 CF 3 HH C-Me -CO-NEt (c-Hex)
-204 2 CF3 H H C-Me - CO - N (i - Pr) 2 -204 2 CF 3 HH C-Me-CO-N (i-Pr) 2
-205 2 CF3 Et H C-Me Ph 124. 3-206 2 CF3 H H C- CF3 t-Bu-205 2 CF 3 Et H C-Me Ph 124. 3-206 2 CF 3 HH C- CF 3 t-Bu
-207 2 CF3 H H C-CF3 - CH2- Ph-207 2 CF 3 HH C-CF 3 -CH 2 -Ph
-208 2 CF3 H H C - CF3 - CMe2 - Ph -208 2 CF 3 HHC - CF 3 - CMe 2 - Ph
-209 2 CF3 H H C-CF3 Ph 120. 3-210 2 CF3 H H C - CF3 2-Cl-Ph-209 2 CF 3 HH C-CF 3 Ph 120. 3-210 2 CF 3 HHC-CF 3 2-Cl-Ph
-211 2 CF3 H H C-CF3 2-CFg-Ph-211 2 CF 3 HH C-CF 3 2-CFg-Ph
-212 2 CF3 H H C- CF3 2 - 0CF3 - Ph-212 2 CF 3 HH C- CF 3 2-0CF 3 -Ph
-213 2 CF3 H H C- CF3 2, 6- Cl2- Ph-213 2 CF 3 HH C- CF 3 2, 6- Cl 2 -Ph
-214 2 CF3 H H C- CF3 2 - CI- 6- F- Ph -214 2 CF 3 HH C- CF 3 2 - CI- 6- F- Ph
-215 2 CF3 H H C-CF3 2, 6- Me2-Ph-215 2 CF 3 HH C-CF 3 2, 6- Me 2 -Ph
-216 2 CF3 H H C - CF3 2- CI- 6- Me - Ph-216 2 CF 3 HHC-CF 3 2- CI- 6- Me-Ph
-217 2 CF3 H H C-OMe Me-217 2 CF 3 HH C-OMe Me
-218 2 CF3 H H C-OMe t-Bu-218 2 CF 3 HH C-OMe t-Bu
-219 2 CF3 H H C-OMe - CH2- Ph-219 2 CF 3 HH C-OMe-CH 2 -Ph
-220 2 CF3 H H C-OMe - CMe2 - Ph-220 2 CF 3 HH C-OMe-CMe 2 -Ph
-221 2 CF3 H H C-OMe Ph 171. 1-222 2 CF3 H H C-OMe 2-Cl-Ph-221 2 CF 3 HH C-OMe Ph 171.1-222 2 CF 3 HH C-OMe 2-Cl-Ph
-223 2 CF3 H H C-OMe 2- CF3-Ph-223 2 CF 3 HH C-OMe 2- CF 3 -Ph
-224 2 CF3 H H C-OMe 2-0CF3 - Ph-224 2 CF 3 HH C-OMe 2-0CF 3 -Ph
-225 2 CF3 H H C-OMe 2, 6-Cl2-Ph-225 2 CF 3 HH C-OMe 2, 6-Cl 2 -Ph
-226 2 CF3 H H C-OMe 2, 6 - Me2 - Ph-226 2 CF 3 HH C-OMe 2, 6-Me 2 -Ph
-227 2 CF3 H 5- Me C-OMe Ph 176. 9-178. 3-228 2 CF3 H H C-SMe Me-227 2 CF 3 H5-Me C-OMe Ph 176. 9-178. 3-228 2 CF 3 HH C-SMe Me
-229 2 CF3 H H C - SMe t-Bu-229 2 CF 3 HHC-SMe t-Bu
-230 2 CF3 H H C-SMe - CH2_Ph-230 2 CF 3 HH C-SMe-CH 2 _Ph
-231 2 CF, H H C-SMe 一 CMe。一 Ph
第 CM 2表 (続き) -231 2 CF, HH C-SMe One CMe. One Ph Table 2 of CM (continued)
No.O 置換 物性 D C R1 R2 X J5 R9 No.O substitution physical property DCR 1 R 2 XJ 5 R 9
位置 [融点(°c) ] Position [melting point (° c)]
2-232 2 CF3 H H C-SMe Ph 2-232 2 CF 3 HH C-SMe Ph
2-233 2 CF3 H H C-SMe 2-Cl-Ph 2-233 2 CF 3 HH C-SMe 2-Cl-Ph
2-234 2 CF3 H H C-SMe 2, 6- Cl2— Ph 2-234 2 CF 3 HH C-SMe 2, 6- Cl 2 — Ph
2 - 235 2 CF3 H H C-SMe 2, 6 - Me2- Ph 2-235 2 CF 3 HH C-SMe 2, 6-Me 2 -Ph
2 CF3 H H C - CI - CH2 - Ph 2 CF 3 HHC-CI-CH 2 -Ph
2-237 2 CF3 H H C-Cl - CMe2 - Ph 2-237 2 CF 3 HH C-Cl - CMe 2 - Ph
2-238 2 CF3 H H c-ci Ph 2-238 2 CF 3 HH c-ci Ph
2-239 2 CF3 H H C-Cl 2- CI - Ph 2-239 2 CF 3 HH C-Cl 2- CI-Ph
2-240 2 CF3 H H C-Cl 2, 6 - Cl2- Ph 2-240 2 CF 3 HH C-Cl 2, 6-Cl 2 -Ph
2-241 2 CF3 H H C-Cl 2- C 6 - F- Ph 2-241 2 CF 3 HH C-Cl 2- C 6-F- Ph
2-242 2 CF3 H H C-Cl 2, 6 - Me2 - Ph 2-242 2 CF 3 HH C-Cl 2, 6-Me 2 -Ph
2-243 2 CF3 H H C-Cl 2-Cl-6-Me-Ph 2-243 2 CF 3 HH C-Cl 2-Cl-6-Me-Ph
2-244 2 CF3 H H C-Me 4-C 2- F - 5- Pr- Ph 59-61 2-244 2 CF 3 HH C-Me 4-C 2-F-5- Pr- Ph 59-61
2 CF3 H 3- CI CH 2, 4, 6 - Cl3 - Ph 129. 3-133. 12 CF 3 H 3- CI CH 2, 4, 6-Cl 3 -Ph 129.
2-246 2 CF3 H j o一 CH 2, 4, 6-Clg-Ph 106. 4-124. 22-246 2 CF 3 H jo-1 CH 2, 4, 6-Clg-Ph 106.
2-247 2 CF3 C0-i- ■Pr H CH 2, 6— Cl2 55. 6-61. 9
2-247 2 CF 3 C0-i- PrH CH 2, 6—Cl 2 55.6-61.9
一般式 ( I一 4 ) General formula (I-1 4)
3-1 2 CF3 H H Me 3-1 2 CF 3 HH Me
3-2 2 CF3 H H t-Bu 1. 4979 (27。C)3-2 2 CF 3 HH t-Bu 1.4979 (27.C)
3-3 2 CF, H H 1. 5194 (20°C)3-3 2 CF, H H 1.5194 (20 ° C)
3-4 2 CF3 H H -CH2- (2-Cl-Ph) 1. 5475 (22°C)3-4 2 CF 3 HH -CH 2- (2-Cl-Ph) 1.5475 (22 ° C)
3-5 2 CF, H H - CH2- (3 - CI- Ph) 97-983-5 2 CF, HH-CH 2- (3-CI- Ph) 97-98
3-6 2 CF3 H H - CH2 - o(4-Cト Ph) 1. 5499 (23°C)3-6 2 CF 3 HH-CH 2 -o (4-C to Ph) 1.5499 (23 ° C)
: :
3-7 2 CF3 H H -CH2 -(2,D C 6 - Cl2- Ph) 3-7 2 CF 3 HH -CH 2- (2, DC 6-Cl 2 -Ph)
3-8 2 CF3 H H -CHMe-Ph 1. 5287 (25°C)3-8 2 CF 3 HH -CHMe-Ph 1.5287 (25 ° C)
3-9 2 CF3 H H -CHMe- (2-Cl-Ph) 3-9 2 CF 3 HH -CHMe- (2-Cl-Ph)
3-10 2 CF3 H H -CHMe- (3- CI - Ph) 3-10 2 CF 3 HH -CHMe- (3- CI-Ph)
3-11 2 CF3 H H - CHMe- (4- CI Ph) 3-11 2 CF 3 HH-CHMe- (4- CI Ph)
3-12 2 CF3 H H - CHMe (2, 6 - Cl2 - Ph) 3-12 2 CF 3 HH-CHMe (2, 6-Cl 2 -Ph)
3 - 13 2 CF3 H H 1. 53 0028 (26°C)3-13 2 CF 3 HH 1.53 0028 (26 ° C)
3-14 2 CF3 H H -CMe2- (2-Cl-Ph) CO 3-14 2 CF 3 HH -CMe 2- (2-Cl-Ph) CO
3-15 2 CF3 H H - CMe2- (3- CI - Ph) o t3-15 2 CF 3 HH-CMe 2- (3- CI-Ph) ot
3-16 2 CF3 H H CMe2 -(4- Cト Ph) 3-16 2 CF 3 HH CMe 2- (4-C to Ph)
3-17 2 CF3 H H — CMe2_ (2, 6 - Cl2- Ph) 3-17 2 CF 3 HH — CMe 2 _ (2, 6-Cl 2 -Ph)
3 - 18 2 CF3 H H Ph 3-18 2 CF 3 HH Ph
3-19 2 CF3 H H 2-F-Ph 1. 5244 (21°C)3-19 2 CF 3 HH 2-F-Ph 1.5244 (21 ° C)
3-20 2 CF3 H H 3-F-Ph 3-20 2 CF 3 HH 3-F-Ph
3-21 2 CF3 H H 4-F-Ph 3-21 2 CF 3 HH 4-F-Ph
3-22 2 CF3 H H 2 - CI- Ph 105-1073-22 2 CF 3 HH 2-CI- Ph 105-107
3-23 2 CF3 H H 3-Cl-Ph 74 753-23 2 CF 3 HH 3-Cl-Ph 74 75
3-24 2 CF3 H H 4- CI- Ph 127-1283-24 2 CF 3 HH 4- CI- Ph 127-128
3-25 2 CF3 H H 2- Br- Ph 453-25 2 CF 3 HH 2- Br- Ph 45
3-26 2 CF3 H H 3 - Br - Ph 3-26 2 CF 3 HH 3-Br-Ph
3-27 2 CF3 H H 4-Br-Ph 3-27 2 CF 3 HH 4-Br-Ph
3-28 2 CF3 H H 2 - I - Ph 3-28 2 CF 3 HH 2-I-Ph
3-29 2 CF3 H H 2- Me - Ph 1. 5293 (24°C)3-29 2 CF 3 HH 2-Me-Ph 1.5293 (24 ° C)
3-30 2 CF3 H H 2-Et-Ph 3-30 2 CF 3 HH 2-Et-Ph
3-31 2 CF3 H H 2-i-Pr-Ph 3-31 2 CF 3 HH 2-i-Pr-Ph
3-32 2 CF3 H H 2-OMe-Ph 90 - 92
3表 (続き) 3-32 2 CF 3 HH 2-OMe-Ph 90-92 Table 3 (continued)
置換 D2 Y D9 物性 Substitution D2 Y D9 Physical properties
\ϋ. 1\ K Λ K \ ϋ. 1 \ K Λ K
位 [融点 (°C)、 屈折率]-33 2 CF3 H H 2-S e-PhPosition [melting point (° C), refractive index] -33 2 CF 3 HH 2-S e-Ph
-34 2 CF3 H H 2-SOMe-Ph-34 2 CF 3 HH 2-SOMe-Ph
-35 2 CF3 H H 2 - S02Me - Ph -35 2 CF 3 HH 2-S0 2 Me-Ph
- 36 2 CF3 H H 2-N02-Ph 155-37 2 CF3 H H 2-CN-Ph 1. 5443 (26°C) - 38 2 CF3 H H 2-CFj-Ph 95-97 - 39 2 CF3 H H 2 - 0CF3 - Ph-36 2 CF 3 HH 2-N0 2 -Ph 155-37 2 CF 3 HH 2-CN-Ph 1.5443 (26 ° C)-38 2 CF 3 HH 2-CFj-Ph 95-97-39 2 CF 3 HH 2-0CF 3 -Ph
-40 2 CF3 H H 2-SCF3 - Ph -40 2 CF 3 HH 2-SCF 3 -Ph
- 41 2 CF3 H H 2 - S0CF3 - Ph -41 2 CF 3 HH 2-S0CF 3 -Ph
- 42 2 CF3 H H 2-S02CF3-Ph-42 2 CF 3 HH 2-S0 2 CF 3 -Ph
-43 2 CF3 H H 2-C02Me-Ph-43 2 CF 3 HH 2-C0 2 Me-Ph
-44 2 CF3 H H 2 Ph - Ph-44 2 CF 3 HH 2 Ph-Ph
-45 2 CF3 H H 4-PhO-Ph-45 2 CF 3 HH 4-PhO-Ph
-46 2 CF3 H H 2, 6-F2-Ph 109-110-47 2 CF3 H H 2, 4- Cl2- Ph 124-48 2 CF3 H H 2, 6- Cl2-Ph 139-141-49 2 CF3 H H 3, 4- Cl2 - Ph 88-90 - 50 2 CF3 H H 3, 5- Cl2 - Ph -46 2 CF 3 HH 2,6-F 2 -Ph 109-110-47 2 CF 3 HH 2,4-Cl 2 -Ph 124-48 2 CF 3 HH 2,6-Cl 2 -Ph 139-141- 49 2 CF 3 HH 3, 4- Cl 2 -Ph 88-90-50 2 CF 3 HH 3, 5- Cl 2 -Ph
- 51 2 CF3 H H 2, 6 - Br2 - Ph -51 2 CF 3 HH 2, 6-Br 2 -Ph
- 52 2 CF3 H H 2, 6- 12- Ph-52 2 CF 3 HH 2, 6- 1 2 -Ph
-53 2 CF3 H H 2, 6 - Me2 - Ph 150-152-54 2 CF3 H H 2, 6-Et2-Ph-53 2 CF 3 HH 2, 6-Me 2 -Ph 150-152-54 2 CF 3 HH 2, 6-Et 2 -Ph
-55 2 CF3 H H 2, 6- (OMe) 2 - Ph -55 2 CF 3 HH 2, 6- (OMe) 2 -Ph
- 56 2 CF3 H H 2, 4- (CF3) 2-Ph-56 2 CF 3 HH 2, 4- (CF 3 ) 2 -Ph
-57 2 CF3 H H 2, 6- (CF3) 2-Ph-57 2 CF 3 HH 2, 6- (CF 3 ) 2 -Ph
-58 2 CF3 H H 2, 6- (0CF3) 2-Ph-58 2 CF 3 HH 2, 6- (0CF 3 ) 2 -Ph
-59 2 CF3 H H 2, 4, 6 - F3 - Ph -59 2 CF 3 HH 2, 4, 6-F 3 -Ph
- 60 2 CF3 H H 2, 3, 4- Cl3_Ph-60 2 CF 3 HH 2, 3, 4-Cl 3 _Ph
-61 2 CF3 H H 2, 4, 6-Cl3-Ph 147-149-62 2 CF3 H H 2, 6 - Cl2 - 4- CF3 - Ph -61 2 CF 3 HH 2, 4 , 6-Cl 3 -Ph 147-149-62 2 CF 3 HH 2, 6 - Cl 2 - 4- CF 3 - Ph
- 63 2 CF3 H H 2, 6 - Cl2 - 4 - 0CF3- Ph - 63 2 CF 3 HH 2, 6 - Cl 2 - 4 - 0CF 3 - Ph
-64 2 CF3 H H 2, 4, 6- e3-Ph-64 2 CF 3 HH 2, 4, 6- e 3 -Ph
-65 2 CF3 H H 2 - Pyn-65 2 CF 3 HH 2-Pyn
-66 2 CF3 H H 3 - Pyn-66 2 CF 3 HH 3-Pyn
-67 2 CF3 H H 4 Pyn-67 2 CF 3 HH 4 Pyn
-68 2 CF3 H H 6 - CI- 2- Pyn-68 2 CF 3 HH 6-CI- 2- Pyn
-69 2 CF3 H H 6 - CF3 - 2- Pyn -69 2 CF 3 HH 6 - CF 3 - 2- Pyn
- 70 2 CF3 H H 6 - CI - 4 - CF3_2 - Pyn-70 2 CF 3 HH 6-CI-4-CF 3 _2-Pyn
-71 2 CF3 H H 2-Pym-71 2 CF 3 HH 2-Pym
-72 2 CF3 H H 4-Pyra
3表 (続き) -72 2 CF 3 HH 4-Pyra Table 3 (continued)
直 ϊ¾ 物性 Direct physical properties
No. R1 R2 X R9 No. R 1 R 2 XR 9
位置 [融点 (°c)、 屈折率] Δ ο CF3 H H 4, 6— Me2— 2—Pym Position [melting point (° c), refractive index] Δ ο CF 3 HH 4, 6—Me 2 — 2—Pym
0-/ ο 0- / ο
CF3 H H 4, b— UMe り一 2 -ド ymCF 3 HH 4, b— UMe 2 1-do ym
- 0 CF3 H H 3 - Pyd -0 CF 3 HH 3-Pyd
ο ο
3 - 76 CF3 H H 6 - CI - 3 - Pyd 3-76 CF 3 HH 6-CI-3-Pyd
丁 Ding
3 - 77 CF3 H H - CO - NHMe3-77 CF 3 HH-CO-NHMe
3-79 ο CF3 H H - CO - NMePh 1. 5302 (25°C)3-79 ο CF 3 HH-CO-NMePh 1.5302 (25 ° C)
3 - 80 2 CF3 H H -CO-NEt (c-Hex) 503-80 2 CF 3 HH -CO-NEt (c-Hex) 50
3-81 2 CF3 H H - CO- N (l-Pr) 2 3-81 2 CF 3 HH-CO- N (l-Pr) 2
3 - 82 2 CF3 Me H Ph 3-82 2 CF 3 Me H Ph
3 - 83 2 CF3 Me H 2 - CI - Ph NMR-23-83 2 CF 3 Me H 2-CI-Ph NMR-2
3-84 2 CF3 Me H 2 - Me - Ph 3-84 2 CF 3 Me H 2-Me-Ph
3-85 2 CF3 Me H 2 - CF3- Ph 3-85 2 CF 3 Me H 2-CF 3 -Ph
3-86 2 CF3 Me H 2, 6 - Cl2_Ph 3-86 2 CF 3 Me H 2, 6-Cl 2 _Ph
3-87 2 CF3 Me H 2, 6 - Me2 - Ph 3-87 2 CF 3 Me H 2, 6-Me 2 -Ph
3-88 2 CF3 Me H - CH2 - Ph 3-88 2 CF 3 Me H-CH 2 -Ph
3 - 89 2 CF3 Me H -CMe2-Ph 3-89 2 CF 3 Me H -CMe 2 -Ph
3-90 2 CF3 COMe H Ph 3-90 2 CF 3 COMe H Ph
3-91 2 CF3 COMe H 2-Cl-Ph 3-91 2 CF 3 COMe H 2-Cl-Ph
3-92 2 CF3 COMe H 2, 6 - Cl2 - Ph3-92 2 CF 3 COMe H 2, 6-Cl 2 -Ph
-93 2 CF3 COMe H 2, 6- Me2- Ph-93 2 CF 3 COMe H 2, 6- Me 2 -Ph
-94 2 CF3 COMe H - CH2 - Ph -94 2 CF 3 COMe H-CH 2 -Ph
- 95 2 CF3 COMe H _CMe2 - Ph -95 2 CF 3 COMe H _CMe 2 -Ph
3-96 2 CF3 C02Me H Ph 3-96 2 CF 3 C0 2 Me H Ph
- 97 2 CF3 C02Me H 2 - CI - Ph-97 2 CF 3 C0 2 Me H 2-CI-Ph
—98 2 CF3 C02Me H 2, 6 - Cl2 - Ph —98 2 CF 3 C0 2 Me H 2, 6-Cl 2 -Ph
- 99 2 CF3 C02Me H 2, 6- Me2 - Ph -99 2 CF 3 C0 2 Me H 2, 6- Me 2 -Ph
ο ο
—100 Δ CF3 し (JJVle H - CH2 - Ph —100 Δ CF 3 (JJVle H-CH 2 -Ph
ο ο
-101 CF3 し CUde H - CMe2 - Ph-101 CF 3 CUde H-CMe 2 -Ph
-102 CF3 S02CF3 H Ph -102 CF 3 S0 2 CF 3 H Ph
- 103 2 CF3 b02CF3 H 2 - CI - Ph -103 2 CF 3 b0 2 CF 3 H 2-CI-Ph
ο on ο on
—104 CF3 02CrF3 H 2, (D—し丄2— Ph —104 CF 3 0 2 CrF 3 H 2, (D— 丄2 — Ph
L CF3 S02し F3 H Δ, b-Me2-rnL CF 3 S0 2 then F 3 H Δ, b-Me 2 -rn
-106 しト 3 H - CH2 - Ph -106 3 H-CH 2 -Ph
- 107 2 CF3 S02CF3 H -CMe2-Ph-107 2 CF 3 S0 2 CF 3 H -CMe 2 -Ph
-108 2 CF3 H 5 - Me Ph-108 2 CF 3 H 5-Me Ph
-109 2 CF3 H 5 - Me 2 - CI - Ph-109 2 CF 3 H 5-Me 2-CI-Ph
-110 2 CF3 H 5- Me 2, 6- Cl2 - Ph-110 2 CF 3 H 5-Me 2, 6- Cl 2 -Ph
-111 2 CF3 H 5 - Me 2, 6- Me2-Ph-111 2 CF 3 H 5-Me 2, 6- Me 2 -Ph
-112 2 CF3 H 5 - Me
3表 (続き) -112 2 CF 3 H 5-Me Table 3 (continued)
置換 物性 Substitution physical properties
No. /上 R1 R2 X R9 No./Top R 1 R 2 XR 9
置 [融点 (°c)、 屈折率]-113 2 CF3 H 5- Me - CMe2 - Ph[Melting point (° c), refractive index] -113 2 CF 3 H 5-Me-CMe 2 -Ph
-114 2 CF3 H 4 - CI Ph-114 2 CF 3 H 4-CI Ph
-115 2 CF3 H 4- CI 2- CI - Ph-115 2 CF 3 H 4- CI 2- CI-Ph
-116 2 CF3 H 4- CI 2, 6- Cl2 - Ph-116 2 CF 3 H 4- CI 2, 6- Cl 2 -Ph
-117 2 CF3 H 4 - CI 2, 6_Me2 - Ph-117 2 CF 3 H 4-CI 2, 6_Me 2 -Ph
-118 2 CF3 H 4-C1 - CH2- Ph-118 2 CF 3 H 4-C1-CH 2 -Ph
-119 2 CF3 H 4- CI 一 CMe2 - Ph-119 2 CF 3 H 4- CI one CMe 2 - Ph
-120 2 CF3 H 5- CI Ph-120 2 CF 3 H 5- CI Ph
-121 2 CF3 H 5-C1 2 - CI- Ph-121 2 CF 3 H 5-C1 2-CI- Ph
-122 2 CF3 H 5-C1 2, 6- Cl2— Ph-122 2 CF 3 H 5-C1 2, 6- Cl 2 — Ph
-123 2 CF3 H 5- CI 2, 6-Me2-Ph-123 2 CF 3 H 5-CI 2, 6-Me 2 -Ph
-124 2 CF3 H 5- CI - CH2 - Ph-124 2 CF 3 H 5- CI-CH 2 -Ph
-125 2 CF3 H 5- CI _CMe2 - Ph-125 2 CF 3 H 5- CI _CMe 2 -Ph
-126 3 CF3 H H Me-126 3 CF 3 HH Me
-127 3 CF3 H H t-Bu-127 3 CF 3 HH t-Bu
-128 3 CF3 H H _CH2- Ph-128 3 CF 3 HH _CH 2 -Ph
-129 3 CF3 H H - CMe2- Ph-129 3 CF 3 HH-CMe 2 -Ph
-130 3 CF3 H H Ph-130 3 CF 3 HH Ph
-131 3 CF3 H H 2- CI- Ph-131 3 CF 3 HH 2- CI- Ph
-132 3 CF3 H H 2, 6— Cl2— Ph -132 3 CF 3 HH 2, 6—Cl 2 — Ph
- 133 3 CF3 H H 2-C1-6- Me- Ph-133 3 CF 3 HH 2-C1-6- Me- Ph
-134 3 CF3 H H 2, 6-Me2-Ph-134 3 CF 3 HH 2, 6-Me 2 -Ph
-135 4 CF3 H H Me-135 4 CF 3 HH Me
-136 4 CF3 H H t-Bu-136 4 CF 3 HH t-Bu
-137 4 CF3 H H -CH2-Ph -137 4 CF 3 HH -CH 2 -Ph
- 138 4 CF3 H H -CMe2-Ph-138 4 CF 3 HH -CMe 2 -Ph
-139 4 CF3 H H Ph-139 4 CF 3 HH Ph
-140 4 CF3 H H 2- CI- Ph-140 4 CF 3 HH 2- CI- Ph
-141 4 CF3 H H 2, 6_C12— Ph-141 4 CF 3 HH 2, 6_C1 2 — Ph
-142 4 CF3 H H 2- Cト 6-Me- Ph -142 4 CF 3 HH 2-C 6-Me- Ph
- 143 4 CF3 H H 2, 6-Me2-Ph-143 4 CF 3 HH 2, 6-Me 2 -Ph
-144 2 CHF2 H H Me-144 2 CHF 2 HH Me
-145 2 CHF2 H H t-Bu-145 2 CHF 2 HH t-Bu
-146 2 CHF2 H H - CH2 - Ph-146 2 CHF 2 HH-CH 2 -Ph
-147 2 CHF2 H H -CMe2-Ph-147 2 CHF 2 HH -CMe 2 -Ph
-148 2 CHF2 H H Ph-148 2 CHF 2 HH Ph
-149 2 CHF2 H H 2-Cl-Ph-149 2 CHF 2 HH 2-Cl-Ph
-150 2 CHF2 H H 2 - CF3 - Ph-150 2 CHF 2 HH 2-CF 3 -Ph
-151 2 CHF2 H H 2- 0CF3- Ph-151 2 CHF 2 HH 2- 0CF 3 -Ph
-152 2 CHF2 H H 2, 6—Cl2— Ph
3表 (続き) -152 2 CHF 2 HH 2, 6—Cl 2 — Ph Table 3 (continued)
置換 Replace
No. R1 R2 X R9 物性 No. R 1 R 2 XR 9 Physical properties
置 [融点 (°C)、 屈折率:-153 2 CHF2 H H 2- CI- 6- F-Ph(Melting point (° C), refractive index: -153 2 CHF 2 HH 2-CI-6-F-Ph
-154 2 CHF2 H H 2- CI- 6- Me- Ph-154 2 CHF 2 HH 2- CI- 6- Me- Ph
-155 2 CHF2 H H 2, 6-Me2-Ph -155 2 CHF 2 HH 2, 6-Me 2 -Ph
- 156 2 CF3 H H c-Hex 107-157 2 CF3 H H 4 - SCF3 - Ph 1.5214 (25。C) 158 2 CF3 H H 4-OMe-Ph 130-131-159 2 CF3 H H 2-應 2 - Ph 1.5316(24°C)-160 2 CF3 H H 2-蘭 H- Ph 1.5465(24°C) 161 2 CF3 Ac H 2-NHAc-Ph 1.5241(24°C) 162 2 CF3 H H 2, 4 - F2 - Ph 112-113-163 2 CF3 H H 2-Phthalimidyl-Ph 177-180-164 2 CF3 H 6 - CI 2- CF3 - Ph 1.4936(28°C)-165 2 CF3 H 5-SMe 2- CF3 - Ph 1.5327 (21。C)-166 2 CF3 H H CH2C0-t-Bu 104-105-167 2 CF3 H H CH2C0Ph 1.5351 (23。C)-168 2 CF3 H H CH2C0(2, 4 - Cl2-Ph) 1.5494 (28。C)-169 2 CF3 H H CO匪 e2 1.5099 (25。C)-170 2 CF3 H H CHMeC02Me 1.4966(27°C)-171 2 CF3 H H CHMeC02H 1.4989 (25°C) 172 2 CF3 H H CHMeC0NH(4-Cl-Ph) 90-95-173 2 CF3 H H CMe2 -(3 - i - Pr - Ph) 1.5129(28°C)-174 2 CF3 H H CH2(2, 4- Cl2_Ph) 49 - 175 2 CF3 H H CH2(2- Me- Ph) 106-107 - 176 2 CF3 H H CH2(3 - Me- Ph) 1.5275 (23。C)-177 2 CF3 H H C¾(4 - Me - Ph) 1.5431(23°C)-178 2 CF3 H H CH2(2, 4 - Me2- Ph) 30-179 2 CF3 H H CH2(4-MeO-Ph) 1.5371(26°C)-180 2 CF3 H H CH2(4 - CF3。- Ph) 1.5077(25°C)-181 2 CF3 H H CH2(3- CF3S02NH- Ph) 161-162-182 2 CF3 H H i-Pr 1.4953(20°C) - 183 2 CF3 H H CH(Et)2 59-184 2 CF3 H H (CH2) 7-Me 1.4882(26°C)-185 2 CF3 H H CH(Me)- (C )5 - Me 1.4681 (20°C)
一般式 (I一 4 ) -156 2 CF 3 HH c-Hex 107-157 2 CF 3 HH 4-SCF 3 -Ph 1.5214 (25.C) 158 2 CF 3 HH 4-OMe-Ph 130-131-159 2 CF 3 HH 2- 2 -Ph 1.5316 (24 ° C) -160 2 CF 3 HH 2-Orchid H- Ph 1.5465 (24 ° C) 161 2 CF 3 Ac H 2-NHAc-Ph 1.5241 (24 ° C) 162 2 CF 3 HH 2 , 4-F 2 -Ph 112-113-163 2 CF 3 HH 2-Phthalimidyl-Ph 177-180-164 2 CF 3 H 6-CI 2- CF 3 -Ph 1.4936 (28 ° C) -165 2 CF 3 H 5-SMe 2- CF 3 -Ph 1.5327 (21.C) -166 2 CF 3 HH CH 2 C0-t-Bu 104-105-167 2 CF 3 HH CH 2 C0Ph 1.5351 (23.C) -168 2 CF 3 HH CH 2 C0 (2 , 4 - Cl 2 -Ph) 1.5494 (28.C) -169 2 CF 3 HH CO negation e 2 1.5099 (25.C) -170 2 CF 3 HH CHMeC0 2 Me 1.4966 (27 ° C) -171 2 CF 3 HH CHMeC0 2 H 1.4989 (25 ° C) 172 2 CF 3 HH CHMeC0NH (4-Cl-Ph) 90-95-173 2 CF 3 HH CMe 2 - (3 - i - Pr - Ph) 1.5129 (28 ° C) -174 2 CF 3 HH CH 2 (2,4-Cl 2 _Ph) 49-175 2 CF 3 HH CH 2 (2-Me-Ph) 106-107-176 2 CF 3 HH CH 2 (3-Me- Ph) 1.5275 (23.C) -177 2 CF 3 HH C¾ (4-Me-Ph) 1.5431 (23 ° C) -178 2 CF 3 HH CH 2 (2, 4-Me 2 -Ph) 30-179 2 CF 3 HH CH 2 (4-MeO-Ph) 1.5371 (26 ° C) -18 0 2 CF 3 HH CH 2 ( 4 - CF 3 .- Ph) 1.5077 (25 ° C) -181 2 CF 3 HH CH 2 (3- CF 3 S0 2 NH- Ph) 161-162-182 2 CF 3 HH i-Pr 1.4953 (20 ° C)-183 2 CF 3 HH CH (Et) 2 59-184 2 CF 3 HH (CH 2 ) 7 -Me 1.4882 (26 ° C) -185 2 CF 3 HH CH (Me) -(C) 5 -Me 1.4681 (20 ° C) General formula (I-I-4)
第 4表 (m= 0 A=-C - G^O, J'J=J5=CH) Table 4 (m = 0 A = -C-G ^ O, J ' J = J 5 = CH)
L¾"^¾L 物性 L¾ "^ ¾L Physical properties
No. R1 R2 X R9 No. R 1 R 2 XR 9
[融点 (°c) ) (Melting point (° c))
4—1 9 Me 4—1 9 Me
4.-9 9 t-Bu 4.-9 9 t-Bu
9 i H 9 i H
_ 9 H -CH - (2 - CI一 Ph) _ 9 H -CH-(2-CI-1 Ph)
¾ u 9 U n H 一 CH。—(2 6 - Cl。— Ph) ¾ u 9 U n H one CH. — (2 6-Cl. — Ph)
9 -CHMe-Ph 9 -CHMe-Ph
4.-7 9 i -CHMe- (2 - CI - Ph) 4.-7 9 i -CHMe- (2-CI-Ph)
: O 9 PR j H -CHMe- (2 6-Cl2-Ph) : O 9 PR j H -CHMe- (26-Cl 2 -Ph)
Λ-Q 9 一 CMe2 - Ph Λ-Q 9 One CMe 2 -Ph
4一 10 9 4 1 10 9
F3 H - CMe2- (2-Cl-Ph)F3 H-CMe 2- (2-Cl-Ph)
4 τ:-1 1 9 ΓΡ P 3 H — CMe2— (2, 6 - Cl2— Ph) 4 τ: -1 1 9 ΓΡ P 3 H — CMe 2 — (2, 6-Cl 2 — Ph)
4-1 9 4-1 9
ur 3 H Ph u r 3 H Ph
4一 1 ^ H H 2-F-Ph 4 1 1 ^ H H 2-F-Ph
4-14 2 01 3 H H 2- CI- Ph 117. 44-14 2 01 3 HH 2- CI- Ph 117. 4
4-1 5 2 i 3 H H 3 - CI- Ph 4-1 5 2 i 3 H H 3-CI- Ph
4-16 2 CF。 H H 4- CI- Ph 4-16 2 CF. H H 4- CI- Ph
4-17 2 3 H H 2-Br-Ph 4-17 2 3 H H 2-Br-Ph
4-19 2 CF3 H H 2- Me - Ph 4-19 2 CF 3 HH 2-Me-Ph
4-20 2 CF3 H H 2-Et-Ph 4-20 2 CF 3 HH 2-Et-Ph
4-21 2 CF3 H H 2-i-Pr-Ph 4-21 2 CF 3 HH 2-i-Pr-Ph
4-22 2 CF3 H H 2-0Me-Ph 4-22 2 CF 3 HH 2-0Me-Ph
4-23 2 CF3 H H 2-SMe-Ph 4-23 2 CF 3 HH 2-SMe-Ph
4-24 2 CF3 H H 2-S0Me-Ph 4-24 2 CF 3 HH 2-S0Me-Ph
4-25 2 CF3 H H 2-S02 e-Ph 4-25 2 CF 3 HH 2-S0 2 e-Ph
4 - 26 2 CF3 H H 2- N02 - Ph 4-26 2 CF 3 HH 2- N0 2 -Ph
4-27 2 CF3 H H 2-CN-Ph 4-27 2 CF 3 HH 2-CN-Ph
4-28 2 CF3 H H 2- CF3 - Ph 4-28 2 CF 3 HH 2- CF 3 -Ph
4-29 2 CF3 H H 2 - 0CF3- Ph 4-29 2 CF 3 HH 2-0CF 3 -Ph
4-30 2 CF3 H H 2 - SCF3 - Ph 4-30 2 CF 3 HH 2-SCF 3 -Ph
4-31 2 CF3 H H 2 - S0CF3 - Ph 4-31 2 CF 3 HH 2-S0CF 3 -Ph
4-32 2 CF3 H H 2-S02CF -Ph
表 (続き) 4-32 2 CF 3 HH 2-S0 2 CF -Ph Table (continued)
置換 物性 o. R1 R2 X R9 Substitution physical properties o.R 1 R 2 XR 9
[融点 (°c) )-33 2 CF3 H H 2 - C02Me - Ph(Melting point (° c)) -33 2 CF 3 HH 2-C0 2 Me-Ph
-34 2 CF3 H H 2-Ph-Ph-34 2 CF 3 HH 2-Ph-Ph
-35 2 CF3 H H 4-PhO-Ph-35 2 CF 3 HH 4-PhO-Ph
-36 2 CF3 H H 2, 6-F2-Ph-36 2 CF 3 HH 2, 6-F 2 -Ph
-37 2 CF3 H H 2, 3- Cl2 - Ph-37 2 CF 3 HH 2, 3-Cl 2 -Ph
-38 2 CF3 H H 2, 4- Cl2 - Ph -38 2 CF 3 HH 2, 4-Cl 2 -Ph
- 39 2 CF3 H H 2, 6 - Cl2 - Ph 182. 2-40 2 CF3 H H 2, 6- Br2 - Ph - 39 2 CF 3 HH 2, 6 - Cl 2 - Ph 182. 2-40 2 CF 3 HH 2, 6- Br 2 - Ph
-41 2 CF3 H H 2, 6 - 12- Ph -41 2 CF 3 HH 2, 6 - 1 2 - Ph
-42 2 CF3 H H 2, 6 - Me2-Ph -42 2 CF 3 HH 2, 6-Me 2 -Ph
- 43 2 CF3 H H 2, 6- Et2 - Ph-43 2 CF 3 HH 2, 6-Et 2 -Ph
-44 2 CF3 H H 2, 6- (0Me) 2- Ph-44 2 CF 3 HH 2, 6- (0Me) 2 -Ph
-45 2 CF3 H H 2, 6- (CF3) 2-Ph-45 2 CF 3 HH 2, 6- (CF 3 ) 2 -Ph
-46 2 CF3 H H 2, 6- (0CF3) 2 - Ph -46 2 CF 3 HH 2, 6- (0CF 3 ) 2 -Ph
- 47 2 CF3 H H 2, 3, 4 - Cl3-Ph-47 2 CF 3 HH 2, 3, 4-Cl 3 -Ph
-48 2 CF3 H H 2, 4, 6 - Cl3_Ph-48 2 CF 3 HH 2, 4, 6-Cl 3 _Ph
-49 2 CF3 H . H 2, 6 - Cl2-4 - CF3-Ph-49 2 CF 3 H .H 2, 6-Cl 2 -4-CF 3 -Ph
-50 2 CF3 H H 2, 6 - Cl2 - 4- 0CF3 - Ph -50 2 CF 3 HH 2, 6 - Cl 2 - 4- 0CF 3 - Ph
-51 2 CF3 H H 2, 4, 6— Me3— Ph-51 2 CF 3 HH 2, 4, 6— Me 3 — Ph
-52 2 CF3 H H 2 - Pyn-52 2 CF 3 HH 2-Pyn
-53 2 CF3 H H 3 - Pyn-53 2 CF 3 HH 3-Pyn
-54 2 CF3 H H 4 - Pyn-54 2 CF 3 HH 4-Pyn
-55 2 CF3 H H 6- CI- 2- Pyn-55 2 CF 3 HH 6- CI- 2- Pyn
-56 2 CF3 H H 6-CF3- 2- Pyn -56 2 CF 3 HH 6-CF 3 - 2- Pyn
-57 2 CF3 H H 6- CI - 4 - CF3 - 2 - Pyn -57 2 CF 3 HH 6- CI - 4 - CF 3 - 2 - Pyn
-58 2 CF3 H H 2-Pym-58 2 CF 3 HH 2-Pym
-59 2 CF3 H H 4-Pym-59 2 CF 3 HH 4-Pym
-60 2 CF3 H H 4, 6_Me2 - 2-Pym -60 2 CF 3 HH 4, 6_Me 2 - 2-Pym
-61 2 CF3 H H 4, 6- (OMe) 2-2-Pym-61 2 CF 3 HH 4, 6- (OMe) 2 -2-Pym
-62 2 CF3 H H -CO-NHMe -62 2 CF 3 HH -CO-NHMe
- 63 2 CF3 H H -CO-NHPh-63 2 CF 3 HH -CO-NHPh
-64 2 CF3 H H - CO- NMePh -64 2 CF 3 HH-CO- NMePh
- 65 2 CF3 H H -CO-NEt (c-Hex)-65 2 CF 3 HH -CO-NEt (c-Hex)
-66 2 CF3 H H - CO- N (i- Pr) 2
一般式 (I一 4) -66 2 CF 3 HH-CO- N (i- Pr) 2 General formula (I-1 4)
第 5表 (R1=CF3、 R2=H、 X=H、 J4=CH、 J5=N、 G'=0) Table 5 (R 1 = CF 3, R 2 = H, X = H, J 4 = CH, J 5 = N, G '= 0)
置換 物性 Substitution physical properties
No. m G A R9 No. m GAR 9
[融点 (°c) ] [Melting point (° c)]
5-1 2 0 0 (CH2)2 Me 5-1 2 0 0 (CH 2 ) 2 Me
5-2 2 0 0 (CH2)2 t-Bu 5-2 2 0 0 (CH 2 ) 2 t-Bu
5-3 2 0 0 (c )2 - CH2_Ph 5-3 2 0 0 (c) 2 -CH 2 _Ph
5-4 2 0 0 (CH2)2 5-4 2 0 0 (CH 2 ) 2
5-5 2 0 0 (CH2)2 r Π 5-5 2 0 0 (CH 2 ) 2 r Π
: X : X
5-6 2 0 0 (CH2)2 —し丄ー 1 1ド h 102—1055-6 2 0 0 (CH 2 ) 2 —Cool 1 1D h 102—105
5-7 2 0 0 (CH2)2 2 - Me - Ph 5-7 2 0 0 (CH 2 ) 2 2-Me-Ph
5-8 2 0 0 (CH2)2 2-OMe-Ph 5-8 2 0 0 (CH 2 ) 2 2-OMe-Ph
5-9 2 0 0 (C¾)2 2-CF3-Ph 5-9 2 0 0 (C¾) 2 2-CF 3 -Ph
5-10 2 0 0 (CH2)2 2-0CF3-Ph 5-10 2 0 0 (CH 2 ) 2 2-0CF 3 -Ph
5 - 11 2 0 0 (CH2) 2 2, 6 - Cl2 - Ph 5-11 2 0 0 (CH 2 ) 2 2, 6-Cl 2 -Ph
5 - 12 2 0 0 (CH2)2 2, 6-Me2-Ph 5-12 2 0 0 (CH 2 ) 2 2, 6-Me 2 -Ph
5-13 2 0 0 (CH2)2 2-Pyn 5-13 2 0 0 (CH 2 ) 2 2-Pyn
5-14 2 0 0 (CH2)2 3-Pyn 5-14 2 0 0 (CH 2 ) 2 3-Pyn
5-15 2 0 0 (CH2)2 4-Pyn 5-15 2 0 0 (CH 2 ) 2 4-Pyn
5-16 2 0 0 (C¾)2 4, 6 - Me2- 2-Pym 5-16 2 0 0 (C¾) 2 4, 6 - Me 2 - 2-Pym
5-17 2 0 0 (CH2)2 4, 6-(0Me) 2-2-Pym 5-17 2 0 0 (CH 2 ) 2 4, 6- (0Me) 2 -2-Pym
5-18 2 0 0 (CH2)2 3-Pyd 5-18 2 0 0 (CH 2 ) 2 3-Pyd
5-19 2 0 0 (CH2)2 -CO-匪 e 5-19 2 0 0 (CH 2 ) 2 -CO- Marauder e
5-20 2 0 0 (CH2)2 -CO-NHPh 5-20 2 0 0 (CH 2 ) 2 -CO-NHPh
5-21 2 0 0 (CH2)2 -CO-圈 ePh 5-21 2 0 0 (CH 2 ) 2 -CO-zone ePh
5-22 2 0 0 (CH2)2 -C0-NEt (c-Hex) 5-22 200 (CH 2 ) 2 -C0-NEt (c-Hex)
5-23 2 0 0 (C¾)2 -C0-N(i-Pr)2 5-23 2 0 0 (C¾) 2 -C0-N (i-Pr) 2
5-24 2 0 0 CHMe Me 5-24 2 0 0 CHMe Me
5-25 2 0 0 CHMe t-Bu 5-25 2 0 0 CHMe t-Bu
5-26 2 0 0 CHMe 5-26 2 0 0 CHMe
5 - 27 2 0 0 CHMe 5-27 2 0 0 CHMe
5-28 2 0 0 CHMe Ph 5-28 2 0 0 CHMe Ph
5 - 29 2 0 0 CHMe 2-Cl-Ph NMR-3
5表 (続き) 5-29 2 0 CHMe 2-Cl-Ph NMR-3 Table 5 (continued)
詈 ¾■ 物性 Indecent physical properties
No. m G A R9 No. m GAR 9
[融点 (。c) ] [Melting point (.c)]
5-30 2 0 0 CHMe 2-Me-Ph 5-30 200 CHMe 2-Me-Ph
5-31 2 0 0 CHMe 2-OMe-Ph 5-31 2 0 0 CHMe 2-OMe-Ph
U u し ΗΜΘ (Jし ΓΠ U u ΗΜΘ J (J ΓΠ
5-34 2 0 0 CHMe 2, 6 - Cl2 - Ph 5-34 200 CHMe 2, 6-Cl 2 -Ph
5-35 2 0 0 CHMe 2, 6- Me2 - Ph 5-35 200 CHMe 2, 6- Me 2 -Ph
5-36 2 0 0 C丽 e 2-Pyn 5-36 2 0 0 C 丽 e 2-Pyn
5-37 2 0 0 CHMe 3-Pyn 5-37 2 0 0 CHMe 3-Pyn
5-38 2 0 0 CHMe 4-Pyn 5-38 2 0 0 CHMe 4-Pyn
5-39 2 0 0 CHMe 2- Pym 5-39 2 0 0 CHMe 2- Pym
5-40 2 0 0 CHMe 4一 Pym 5-40 2 0 0 CHMe 4-1 Pym
O一 41 9 O-1 41 9
丄 u し HMS ¾, D 11ν1θ2 Δ ryin 丄 u HMS ¾, D 11ν1θ 2 Δ ryin
5-42 2 o 0 CHMe 4 6- (OMe) η-2-Pvm 5-42 2 o 0 CHMe 4 6- (OMe) η-2-Pvm
5-43 2 0 0 CHMe 3-Pyd 5-43 2 0 0 CHMe 3-Pyd
5-44 2 0 0 CHMe 6-C1- 3- Pyd 5-44 200 CHMe 6-C1- 3- Pyd
5-45 2 0 0 CH(0H) CH2 Me 5-45 2 0 0 CH (0H) CH 2 Me
5-46 2 0 0 CH(0H)CH2 t-Bu 5-46 2 0 0 CH (0H) CH 2 t-Bu
5 - 47 2 0 0 CH(0H)CH2 - CH2- Ph 5-47 2 0 0 CH (0H) CH 2 -CH 2 -Ph
5-48 2 0 0 CH(0H)CH2 - CMe2-Ph 5-48 2 0 0 CH (0H) CH 2 -CMe 2 -Ph
5-49 2 0 0 CH(OH) CH2 Ph 5-49 200 CH (OH) CH 2 Ph
5-50 2 0 0 CH(0H)CH2 2- CI- Ph NMR-45-50 2 0 0 CH (0H) CH 2 2- CI- Ph NMR-4
5-51 2 0 0 CH(0H)CH2 2, 6-Cl2-Ph 5-51 2 0 0 CH (0H) CH 2 2, 6-Cl 2 -Ph
5-52 2 0 0 CH(0H)CH2 2-C1- 6- F - Ph 5-52 2 0 0 CH (0H) CH 2 2-C1- 6- F-Ph
5 - 53 2 0 0 CH(0H)CH2 2 - CI- 6- Me - Ph 5-53 2 0 0 CH (0H) CH 2 2-CI- 6- Me-Ph
5-54 2 0 0 CH(0H)CH2 2, 6_Me2 - Ph 5-54 2 0 0 CH (0H) CH 2 2, 6_Me 2 -Ph
5-55 2 0 0 CH(0H) CH2 2- Pym 5-55 2 0 0 CH (0H) CH 2 2- Pym
5-56 2 0 0 CH(0H) CH2 4一 Pym 5-56 2 0 0 CH (0H) CH 2 4 1 Pym
5-57 2 0 0 CH(0H)CH2 4, 6 - Me2- 2 - Pym 5-57 2 0 0 CH (0H) CH 2 4, 6 - Me 2 - 2 - Pym
5-58 2 0 0 CH(0H)CH2 4, 6 - (OMe) 2 - 2 - Pym 5-58 2 0 0 CH (0H) CH 2 4, 6 - (OMe) 2 - 2 - Pym
5-59 2 1 0 CH2 Me 5-59 2 1 0 CH 2 Me
5-60 2 1 0 CH2 t-Bu 5-60 2 1 0 CH 2 t-Bu
5-61 2 1 0 C¾ 5-61 2 1 0 C¾
5-62 2 1 0 CH2 - CMe2 - Ph 5-62 2 1 0 CH 2 -CMe 2 -Ph
5-63 2 1 0 C¾ Ph 5-63 2 1 0 C¾ Ph
5-64 2 1 0 CH2 2-Cl-Ph NMR-55-64 2 10 CH 2 2-Cl-Ph NMR-5
5-65 2 1 0 CH2 2— Me - Ph
5表 (続き) 5-65 2 1 0 CH 2 2— Me-Ph Table 5 (continued)
置換 物性 Substitution physical properties
No m A R9 No m AR 9
位置 [融点 (。c) ] - 66 2 1 0 CH2 2 - OMe-PhPosition [melting point (.c)]-66 210 CH2 2 -OMe-Ph
-67 2 1 0 CH2 2- CF3- Ph -67 2 1 0 CH 2 2- CF 3 -Ph
- 68 2 1 0 CH2 2 - 0CF3- Ph-68 2 1 0 CH 2 2-0 CF 3 -Ph
-69 2 1 0 CH2 2, 6- Cl2-Ph-69 2 1 0 CH 2 2, 6- Cl 2 -Ph
-70 2 1 0 CH2 2- CI- 6- F - Ph-70 2 1 0 CH 2 2- CI- 6- F-Ph
-71 2 1 0 CH2 2 - CI- 6- Me- Ph -71 2 1 0 CH 2 2-CI- 6- Me- Ph
- 72 2 1 0 CH2 2, 6- Me2- Ph-72 2 1 0 CH 2 2, 6- Me 2 -Ph
-73 2 1 0 CH2 2-Pyn-73 2 1 0 CH 2 2-Pyn
-74 2 1 0 C¾ 3-Pyn-74 2 1 0 C¾ 3-Pyn
-75 2 1 0 CH2 4-Pyn-75 2 1 0 CH 2 4-Pyn
-76 2 1 0 CH2 2- Pym-76 2 1 0 CH 2 2- Pym
-77 2 1 0 CH2 4一 Pym-77 2 1 0 CH 2 4 1 Pym
-78 2 1 0 CH2 4, 6- Me2- 2- Pym -78 2 1 0 CH 2 4, 6- Me 2 - 2- Pym
- 79 2 1 0 CH2 4, 6- (OMe) 2- 2 - Pym - 79 2 1 0 CH 2 4 , 6- (OMe) 2 - 2 - Pym
-80 2 1 0 CH2 3-Pyd-80 2 1 0 CH 2 3-Pyd
-81 2 1 0 CH2 -CO-NHMe-81 2 1 0 CH 2 -CO-NHMe
-82 2 1 0 CH2 -CO-NHPh-82 2 1 0 CH 2 -CO-NHPh
-83 2 1 0 CH2 -C0-NH (2-Cl-Ph)-83 2 1 0 CH 2 -C0-NH (2-Cl-Ph)
-84 2 1 0 C¾ - CO- NMe2 -84 2 1 0 C¾-CO- NMe 2
- 85 2 1 0 CH2 - CO -匪 ePh -85 2 1 0 CH 2 -CO-Marauder ePh
- 86 2 1 0 CH2 -CO-NEt (c-Hex)-86 2 1 0 CH 2 -CO-NEt (c-Hex)
-87 2 1 0 CH2 -CO-N (i-Pr) 2 -87 2 1 0 CH 2 -CO-N (i-Pr) 2
-88 2 1 N- -OMe CH2 Me-88 2 1 N- -OMe CH 2 Me
-89 2 1 N - -OMe CH2 t-Bu-89 2 1 N--OMe CH 2 t-Bu
-90 2 1 N- -OMe CH2 - CH2- Ph-90 2 1 N- -OMe CH 2 -CH 2 -Ph
-91 2 1 N- -OMe CH2 -CMe2-Ph-91 2 1 N- -OMe CH 2 -CMe 2 -Ph
-92 2 1 N- -OMe C¾ Ph-92 2 1 N- -OMe C¾ Ph
-93 2 1 N- -OMe CH2 2-Cl-Ph NMR-6 - 94 2 1 N- -OMe CH2 2- Me- Ph-93 2 1 N- -OMe CH 2 2-Cl-Ph NMR-6-94 2 1 N- -OMe CH 22 2 -Me- Ph
-95 2 1 N- -OMe CH2 2 - OMe-Ph-95 2 1 N- -OMe CH 2 2-OMe-Ph
-96 2 1 N- -OMe CH2 2 - CF3 - Ph-96 2 1 N- -OMe CH 2 2-CF 3 -Ph
-97 2 1 N- -OMe CH2 2- 0CF3- Ph -97 2 1 N- -OMe CH 2 2- 0CF 3 -Ph
- 98 2 1 N - -OMe CH2 2, 6 - Cl2— Ph-98 2 1 N--OMe CH 2 2, 6-Cl 2 — Ph
-99 2 1 N- -OMe CH2 2- CI- 6 - F - Ph -99 2 1 N- -OMe CH 2 2- CI- 6-F-Ph
- 100 2 1 N- -OMe CH2 2 - CI- 6- Me- Ph
5表 (続き) -100 2 1 N- -OMe CH 2 2-CI- 6- Me- Ph Table 5 (continued)
物性 Physical properties
No. , m G A R9 No., m GAR 9
置 [融点 (°c) ]-101 2 1 N-OMe CH2 2 6 - Me2- Ph
Location mp (° c)] -101 2 1 N-OMe CH 2 2 6 - Me 2 - Ph
-般式 (I 一 5 ) -General formula (I-I-5)
(m= 0 A=一 C - G^O) (m = 0 A = one C-G ^ O)
雷換 Thunderstorm
No. R1 R2 X J2 J3 R9 No. R 1 R 2 XJ 2 J 3 R 9
1 直 1 straight
6-1 2 CF3 H H CH2 CH2 Me 6-1 2 CF 3 HH CH 2 CH 2 Me
6-2 2 CF3 H H CH2 CH2 t-Bu 6-2 2 CF 3 HH CH 2 CH 2 t-Bu
6-3 2 CF3 H H CH2 CH2 - CH2- Ph 6-3 2 CF 3 HH CH 2 CH 2 -CH 2 -Ph
6-4 2 CF3 H H C¾ CH2 -CHMe-Ph 6-4 2 CF 3 HH C¾ CH 2 -CHMe-Ph
6-5 2 CF3 H H CH2 CH2 一 CMe2— Ph 6-5 2 CF 3 HH CH 2 CH 2 CMe 2 — Ph
6-6 2 CF3 H H CH2 CH2 Ph 6-6 2 CF 3 HH CH 2 CH 2 Ph
6-7 2 CF3 H H CH2 CH2 2-F-Ph 6-7 2 CF 3 HH CH 2 CH 2 2-F-Ph
6-8 2 CF3 H H CH2 CH2 2 - CI - Ph 170. 3 6-8 2 CF 3 HH CH 2 CH 2 2 - CI - Ph 170. 3
6-9 2 CF3 H H CH2 CH2 3 - CI - Ph 161. 86-9 2 CF 3 HH CH 2 CH 2 3-CI-Ph 161.8
6-10 2 CF3 H H CH2 CH2 4 - CI - Ph 152. 6 6-10 2 CF 3 HH CH 2 CH 2 4 - CI - Ph 152. 6
6 - 11 2 CF3 H H CH2 CH2 2 - Me- Ph 6-11 2 CF 3 HH CH 2 CH 2 2-Me- Ph
6-12 2 CF3 H H CH2 CH2 2 -Pr-Ph 6-12 2 CF 3 HH CH 2 CH 2 2 -Pr-Ph
6 - 13 Z CF3 H H CH2 CH2 2 - OMe— Ph 6-13 Z CF 3 HH CH 2 CH 2 2-OMe— Ph
6 - 14 o 6-14 o
L CF3 H H CH2 C¾ 2-SMe-Ph L CF 3 HH CH 2 C¾ 2-SMe-Ph
o o
ー丄 il ー 丄 il
3 Π Π し ¾ し - UMe-rn t) o 3 Π Π ¾ ¾--UMe-rn t) o
— rn — Rn
6-18 2 CF3 H H CH2 CH2 2 - N02 Ph 6-18 2 CF 3 HH CH 2 CH 2 2-N0 2 Ph
6-19 2 CF3 H H CH2 CH2 2 - CF3- Ph 125. 86-19 2 CF 3 HH CH 2 CH 2 2-CF 3 -Ph 125. 8
6 - 20 2 CF3 H H C¾ CH2 2-0CF3-Ph 6-20 2 CF 3 HH C¾ CH 2 2-0CF 3 -Ph
6-21 2 CF3 H H CH2 C¾ 2- SCF3-Ph 6-21 2 CF 3 HH CH 2 C¾ 2- SCF 3 -Ph
6-22 2 CF3 H H CH2 CH2 2- S0CF3-Ph 6-22 2 CF 3 HH CH 2 CH 2 2- S0CF 3 -Ph
6-23 2 CF3 H H CH2 CH2 2 - S02CF3 - Ph 6-23 2 CF 3 HH CH 2 CH 2 2-S0 2 CF 3 -Ph
6-24 2 CF3 H H CH2 CH2 2 - C02Me - Ph 6-24 2 CF 3 HH CH 2 CH 2 2-C0 2 Me-Ph
6-25 2 CF3 H H CH2 CH2 2 - Ph - Ph 6-25 2 CF 3 HH CH 2 CH 2 2 - Ph - Ph
6-26 2 CF3 H H CH2 CH2 4-PhO-Ph 6-26 2 CF 3 HH CH 2 CH 2 4-PhO-Ph
6-27 2 CF3 H H CH2 C 2 6- F2 - Ph 146. 26-27 2 CF 3 HH CH 2 C 2 6- F 2 -Ph 146.2
6-28 2 CF3 H H CH2 CH2 2, 6- Cl2 - Ph 201. 26-28 2 CF 3 HH CH 2 CH 2 2, 6- Cl 2 -Ph 201. 2
6-29 2 CF3 H H CH2 CH2 2 6- Me2— Ph 200. 66-29 2 CF 3 HH CH 2 CH 2 2 6- Me 2 — Ph 200. 6
6-30 2 CF3 H H C¾ CH2 2, 6 -(CF3) 2 - Ph 6-30 2 CF 3 HH C¾ CH 2 2, 6-(CF 3 ) 2 -Ph
6-31 2 CF3 H H C¾ C¾ 2 6— (0CF3) 2 - Ph
表 (続き) 6-31 2 CF 3 HH C¾ C¾ 2 6— (0CF 3 ) 2 -Ph Table (continued)
置換 物性o. R1 R2 X J2 J3 R9 Substitution physical properties o.R 1 R 2 XJ 2 J 3 R 9
[融点 (°c) ]-32 2 CF3 H H CH2 CH2 2 - CI- 6- Me - Ph 185. 1 - 33 2 CF3 H H CH2 CH2 2, 4, 6- Cl3- Ph 144. 3 - 34 2 CF3 H H CH2 CH2 2, 6 - Cl2 - 4- CF3-PhMp (° c)] -32 2 CF 3 HH CH 2 CH 2 2 - CI- 6- Me - Ph 185. 1 - 33 2 CF 3 HH CH 2 CH 2 2, 4, 6- Cl 3 - Ph 144 . 3 - 34 2 CF 3 HH CH 2 CH 2 2, 6 - Cl 2 - 4- CF 3 -Ph
-35 2 CF3 H H CH2 CH2 2, 6_C12- 4- 0CF3- Ph -35 2 CF 3 HH CH 2 CH 2 2, 6_C1 2 - 4- 0CF 3 - Ph
-36 2 CF3 H H CH2 CH2 2, 3, 4- Me3- Ph -36 2 CF 3 HH CH 2 CH 2 2, 3, 4-Me 3 -Ph
- 37 2 CF3 H H CH2 CH2 2- Pyn -37 2 CF 3 HH CH 2 CH 2 2- Pyn
- 38 2 CF3 H H CH2 CH2 3 - Pyn -38 2 CF 3 HH CH 2 CH 2 3-Pyn
- 39 2 CF3 H H CH2 CH2 4- Pyn-39 2 CF 3 HH CH 2 CH 2 4- Pyn
-40 2 CF3 H H CH2 CH2 6-Cl-2-Pyn -40 2 CF 3 HH CH 2 CH 2 6-Cl-2-Pyn
- 41 2 CF3 H H CH2 CH2 6- CF3 - 2- Pyn - 41 2 CF 3 HH CH 2 CH 2 6- CF 3 - 2- Pyn
- 42 2 CF3 H H CH2 CH2 6- - 4- CF3 - 2- Pyn - 42 2 CF 3 HH CH 2 CH 2 6- - 4- CF 3 - 2- Pyn
-43 2 CF3 H H CH2 CH2 2-Pym-43 2 CF 3 HH CH 2 CH 2 2-Pym
-44 2 CF3 H H CH2 CH2 4-Pym -44 2 CF 3 HH CH 2 CH 2 4-Pym
- 45 2 CF3 H H CH2 CH2 4, 6- Me2- 2- Pym - 45 2 CF 3 HH CH 2 CH 2 4, 6- Me 2 - 2- Pym
-46 2 CF3 H H CH2 CH2 4, 6- (OMe) 2-2-Pym-46 2 CF 3 HH CH 2 CH 2 4, 6- (OMe) 2 -2-Pym
-47 2 CF3 H H CH2 CH2 3-Pyd-47 2 CF 3 HH CH 2 CH 2 3-Pyd
-48 2 CF3 H H CH2 CH2 6-Cl-3-Pyd -48 2 CF 3 HH CH 2 CH 2 6-Cl-3-Pyd
-49 2 CF3 H H CH2 C¾ -C0-N匪 e -49 2 CF 3 HH CH 2 C¾ -C0-N
- 50 2 CF3 H H CH2 CH2 -CO-NHPh-50 2 CF 3 HH CH 2 CH 2 -CO-NHPh
-51 2 CF3 H H CH2 CH2 -CO-NMePh -51 2 CF 3 HH CH 2 CH 2 -CO-NMePh
- 52 2 CF3 H H CH2 CH2 - C0_NEt2 -52 2 CF 3 HH CH 2 CH 2 -C0_NEt 2
- 53 2 CF3 H H CH2 CH2 -CO-NEt (c-Hex) -53 2 CF 3 HH CH 2 CH 2 -CO-NEt (c-Hex)
- 54 2 CF3 H H CH2 CH2 - CO- N (i_Pr) 2 -54 2 CF 3 HH CH 2 CH 2 -CO- N (i_Pr) 2
-55 2 CF3 H H C C=0 Me-55 2 CF 3 HHCC = 0 Me
-56 2 CF3 H H CH2 C=0 t-Bu -56 2 CF 3 HH CH 2 C = 0 t-Bu
- 57 2 CF3 H H CH2 00 -57 2 CF 3 HH CH 200
- 58 2 CF3 H H CH2 c=o -CHMe-Ph-58 2 CF 3 HH CH 2 c = o -CHMe-Ph
-59 2 CF3 H H CH2 c=o -CMe2-Ph -59 2 CF 3 HH CH 2 c = o -CMe 2 -Ph
- 60 2 CF3 H H CH2 oo Ph 1. 5561 (24°C)-61 2 CF3 H H CH2 c=o 2-F-Ph -60 2 CF 3 HH CH 2 oo Ph 1.555 (24 ° C) -61 2 CF 3 HH CH 2 c = o 2-F-Ph
- 62 2 CF3 H H CH2 c=o 2 - CI- Ph 150. 5-151. 7 - 63 2 CF3 H H C¾ oo 2-Br-Ph-62 2 CF 3 HH CH 2 c = o 2-CI- Ph 150. 5-151. 7-63 2 CF 3 HH C¾ oo 2-Br-Ph
-64 2 CF3 H H CH2 c=o 2-I-Ph-64 2 CF 3 HH CH 2 c = o 2-I-Ph
-65 2 CF3 H H C¾ c=o 2-Me-Ph-65 2 CF 3 HH C¾ c = o 2-Me-Ph
-66 2 CF3 H H CH2 c=o 2-i-Pr-Ph -66 2 CF 3 HH CH 2 c = o 2-i-Pr-Ph
- 67 2 CF3 H H CH2 oo 2- OMe- Ph-67 2 CF 3 HH CH 2 oo 2- OMe- Ph
-68 2 CF3 H H CH2 c=o 2-SMe-Ph -68 2 CF 3 HH CH 2 c = o 2-SMe-Ph
- 69 2 CF3 H H CH2 c=o 2-SOMe-Ph-69 2 CF 3 HH CH 2 c = o 2-SOMe-Ph
-70 2 CF3 H H CH2 c=o 2-S02Me-Ph -70 2 CF 3 HH CH 2 c = o 2-S0 2 Me-Ph
- 71 2 CF3 H H CH2 c=o 2-CN-Ph
6表 (続き) -71 2 CF 3 HH CH 2 c = o 2-CN-Ph Table 6 (continued)
wm 物性 wm physical properties
No. R1 R2 X J2 J3 R9 No. R 1 R 2 XJ 2 J 3 R 9
[融点 (°c) ]-72 2 CF3 H H CH2 oo 2- N02_PhMp (° c)] -72 2 CF 3 HH CH 2 oo 2- N0 2 _Ph
-73 2 CF3 H H CH2 c=o 2 - CF3 - Ph 1. 5140 (24°C)-74 2 CF3 H H C¾ c=o 2-0CF3-Ph-73 2 CF 3 HH CH 2 c = o 2-CF 3 -Ph 1.5140 (24 ° C) -74 2 CF 3 HH C¾ c = o 2-0CF 3 -Ph
-75 2 CF3 H H CH2 c=o 2 - SCF3-Ph-75 2 CF 3 HH CH 2 c = o 2-SCF 3 -Ph
-76 2 CF3 H H CH2 c=o 2- S0CF3-Ph-76 2 CF 3 HH CH 2 c = o 2- S0CF 3 -Ph
-77 2 CF3 H H CH2 c=o 2- S02CF3-Ph-77 2 CF 3 HH CH 2 c = o 2- S0 2 CF 3 -Ph
-78 2 CF3 H H CH2 c=o 2-C02Me-Ph-78 2 CF 3 HH CH 2 c = o 2-C0 2 Me-Ph
-79 2 CF3 H H CH2 c=o 2- Ph- Ph-79 2 CF 3 HH CH 2 c = o 2- Ph- Ph
-80 2 CF3 H H CH2 oo 4-PhO-Ph-80 2 CF 3 HH CH 2 oo 4-PhO-Ph
-81 2 CF3 H H CH2 c=o 2, 6-F2-Ph-81 2 CF 3 HH CH 2 c = o 2, 6-F 2 -Ph
-82 2 CF3 H H CH2 c=o 2, 6- Cl2-Ph 196. 7-198. 0-83 2 CF3 H H CH2 oo 2, 6 - Me2 - Ph 172. 9-84 2 CF3 H H CH2 c=o 2, 6 -(CF3) 2— Ph-82 2 CF 3 HH CH 2 c = o 2, 6- Cl 2 -Ph 196.7-198.0 -83 2 CF 3 HH CH 2 oo 2, 6-Me 2 -Ph 172.9 -84 2 CF 3 HH CH 2 c = o 2, 6-(CF 3 ) 2 — Ph
-85 2 CF3 H H CH2 c=o 2, 6_ (0CF3) 2 - Ph-85 2 CF 3 HH CH 2 c = o 2, 6_ (0CF 3 ) 2 -Ph
-86 2 CF3 H H CH2 c=o 2, 3, 4- Cl3- Ph-86 2 CF 3 HH CH 2 c = o 2, 3, 4- Cl 3 -Ph
-87 2 CF3 H H CH2 c=o 2, 4, 6- Cl3 - Ph-87 2 CF 3 HH CH 2 c = o 2, 4, 6- Cl 3 -Ph
-88 2 CF3 H H CH2 c=o 2, 6-Cl2-4-CF3-Ph-88 2 CF 3 HH CH 2 c = o 2, 6-Cl 2 -4-CF 3 -Ph
-89 2 CF3 H H CH2 c=o 2, 6 - Cl2 - 4 - 0CF3-Ph -89 2 CF 3 HH CH 2 c = o 2, 6 - Cl 2 - 4 - 0CF 3 -Ph
-90 2 CF3 H H CH2 c=o 2, 3, 4— Me3 Ph-90 2 CF 3 HH CH 2 c = o 2, 3, 4—Me 3 Ph
-91 2 CF3 H H CH2 c=o 2-Pyn-91 2 CF 3 HH CH 2 c = o 2-Pyn
-92 2 CF3 H H CH2 oo 3-Pyn-92 2 CF 3 HH CH 2 oo 3-Pyn
-93 2 CF3 H H CH2 c=o 4-Pyn-93 2 CF 3 HH CH 2 c = o 4-Pyn
-94 2 CF3 H H C¾ c=o 6-C1-2- Pyn-94 2 CF 3 HH C¾ c = o 6-C1-2- Pyn
-95 2 CF3 H H CH2 c=o 6-CF3-2-Pyn-95 2 CF 3 HH CH 2 c = o 6-CF 3 -2-Pyn
-96 2 CF3 H H CH2 c=o 6- - 4- CF3 - 2 Pyn -96 2 CF 3 HH CH 2 c = o 6- - 4- CF 3 - 2 Pyn
-97 2 CF3 H H CH2 c=o 2- Pym-97 2 CF 3 HH CH 2 c = o 2- Pym
-98 2 CF3 H H CH2 c=o 4 - Pym-98 2 CF 3 HH CH 2 c = o 4-Pym
-99 2 CF3 H H CH2 c=o 4, 6- Me2-2- Pym-99 2 CF 3 HH CH 2 c = o 4, 6- Me 2 -2- Pym
-100 2 CF3 H H CH2 c=o 4, 6 -(0Me) 2- 2 - Pyra -100 2 CF 3 HH CH 2 c = o 4, 6 - (0Me) 2 - 2 - Pyra
-101 2 CF3 H H CH2 c=o 3- Pyd-101 2 CF 3 HH CH 2 c = o 3- Pyd
-102 2 CF3 H H CH2 c=o 6- CI- 3- Pyd-102 2 CF 3 HH CH 2 c = o 6- CI- 3- Pyd
-103 2 CF3 H H CH2 c=o - CO-匪 e-103 2 CF 3 HH CH 2 c = o-CO-bandan e
-104 2 CF3 H H CH2 c=o -CO-NHPh-104 2 CF 3 HH CH 2 c = o -CO-NHPh
-105 2 CF3 H H CH2 oo -CO-NMePh -105 2 CF 3 HH CH 2 oo -CO-NMePh
- 106 2 CF3 H H CH2 c=o -CO-NEt (c-Hex)-106 2 CF 3 HH CH 2 c = o -CO-NEt (c-Hex)
-107 2 CF3 H H CH2 c=o - CO- N (i - Pr) 2 -107 2 CF 3 HH CH 2 c = o-CO- N (i-Pr) 2
- 108 2 CF3 H H C=0 CH2 Me-108 2 CF 3 HHC = 0 CH 2 Me
-109 2 CF3 H H C=0 CH2 t-Bu-109 2 CF 3 HHC = 0 CH 2 t-Bu
-110 2 CF3 H H C=0 CH2 _CH2 - Ph -110 2 CF 3 HHC = 0 CH 2 _CH 2 -Ph
- 111 2 CF3 H H C=0 CH2 -CHMe-Ph
第 6表 (続き)-111 2 CF 3 HHC = 0 CH 2 -CHMe-Ph Table 6 (continued)
o t o t
寸 置換 物性 Dimensions Replacement properties
No. O C R1 R2 X J2 J3 R9 No. OCR 1 R 2 XJ 2 J 3 R 9
位置 [融点 (°c) ] Position [melting point (° c)]
6-112 2 CF3 H H C=0 CH2 - CMe2 - Ph 6-112 2 CF 3 HHC = 0 CH 2 - CMe 2 - Ph
6-113 2 CF3 H H c=o CH2 Ph 96. 9一 115. 36-113 2 CF 3 HH c = o CH 2 Ph 96.
6-114 2 CF3 H H c=o c¾ 2- CI - Ph 6-114 2 CF 3 HH c = o c¾ 2- CI-Ph
6 - 115 2 CF3 H H c=o CH2 2- Me- Ph 6-115 2 CF 3 HH c = o CH 2 2- Me- Ph
6-116 2 CF3 H H oo CH2 2-OMe-Ph 6-116 2 CF 3 HH oo CH 2 2-OMe-Ph
6-117 2 CF3 H H c=o C¾ 2 - SMe-Ph 6-117 2 CF 3 HH c = o C¾ 2-SMe-Ph
6-118 2 CF3 H H c=o CH2 2-S0Me-Ph 6-118 2 CF 3 HH c = o CH 2 2-S0Me-Ph
6-119 2 CF3 H H c=o CH2 2 - S02Me - Ph 6-119 2 CF 3 HH c = o CH 2 2-S0 2 Me-Ph
6-120 2 CF3 H H c=o CH2 2-CN-Ph 6-120 2 CF 3 HH c = o CH 2 2-CN-Ph
6-121 2 CF3 H H c=o CH2 2 - N02_Ph 6-121 2 CF 3 HH c = o CH 2 2-N0 2 _Ph
6-122 2 CF3 H H c=o CH2 2- CF3- Ph 6-122 2 CF 3 HH c = o CH 2 2- CF 3 -Ph
6-123 2 CF3 H H c=o c 2- 0CF3-Ph 6-123 2 CF 3 HH c = oc 2- 0CF 3 -Ph
6-124 2 CF3 H H c=o CH2 2- SCF3- Ph 6-124 2 CF 3 HH c = o CH 2 2- SCF 3 -Ph
6-125 2 CF3 H H c=o CH2 2- S0CF3 - Ph 6-125 2 CF 3 HH c = o CH 2 2- S0CF 3 -Ph
6-126 2 CF3 H H c=o CH2 2-S02CF3-Ph 6-126 2 CF 3 HH c = o CH 2 2-S0 2 CF 3 -Ph
6-127 2 CF3 H H c=o CH2 2- C02Me - Ph 6-127 2 CF 3 HH c = o CH 2 2- C0 2 Me-Ph
6-128 2 CF3 H H oo CH2 2-Ph-Ph 6-128 2 CF 3 HH oo CH 2 2-Ph-Ph
6-129 2 CF3 H H c=o CH2 2-PhO-Ph 6-129 2 CF 3 HH c = o CH 2 2-PhO-Ph
6-130 2 CF3 H H c=o CH2 2, 6- F2- Ph 6-130 2 CF 3 HH c = o CH 2 2, 6- F 2 -Ph
6 - 131 2 CF3 H H c=o CH2 2, 6- Cl2-Ph 6-131 2 CF 3 HH c = o CH 2 2, 6- Cl 2 -Ph
6-132 2 CF3 H H c=o CH2 2, 6- Me2 - Ph 6-132 2 CF 3 HH c = o CH 2 2, 6- Me 2 -Ph
6-133 2 CF3 H H c=o CH2 2, 3, 4-Cl3-Ph 6-133 2 CF 3 HH c = o CH 2 2, 3, 4-Cl 3 -Ph
6-134 2 CF3 H H c=o CH2 2, 4, 6-Cl3-Ph 6-134 2 CF 3 HH c = o CH 2 2, 4, 6-Cl 3 -Ph
6-135 2 CF3 H H c=o CH2 2, 6- Cl2_4 - CF3-Ph 6-135 2 CF 3 HH c = o CH 2 2, 6- Cl 2 _4-CF 3 -Ph
6-136 2 CF3 H H , c=o CH2 2, 6-Cl2-4-0CF3-Ph 6-136 2 CF 3 HH, c = o CH 2 2, 6-Cl 2 -4-0CF 3 -Ph
6-137 2 CF3 H H c=o CH2 2, 3, 4-Me3-Ph 6-137 2 CF 3 HH c = o CH 2 2, 3, 4-Me 3 -Ph
6-138 2 CF3 H H oo CH2 2 - Pyn 6-138 2 CF 3 HH oo CH 2 2-Pyn
6 - 139 2 CF3 H H oo CH2 3 - Pyn 6-139 2 CF 3 HH oo CH 2 3-Pyn
6-140 2 CF3 H H c=o CH2 4-Pyn 6-140 2 CF 3 HH c = o CH 2 4-Pyn
6-141 2 CF3 H H c=o CH2 6- CI- 2- Pyn 6-141 2 CF 3 HH c = o CH 2 6- CI- 2- Pyn
6 - 142 2 CF3 H H c=o CH2 6_CF3- 2- Pyn 6 - 142 2 CF 3 HH c = o CH 2 6_CF 3 - 2- Pyn
6-143 2 CF3 H H c=o CH2 6 - CI- 4- CF3- 2- Pyn 6-143 2 CF 3 HH c = o CH 2 6 - CI- 4- CF 3 - 2- Pyn
6-144 2 CF3 H H oo CH2 2-Pym 6-144 2 CF 3 HH oo CH 2 2-Pym
6-145 2 CF3 H H c=o CH2 4-Pym 6-145 2 CF 3 HH c = o CH 2 4-Pym
6-146 2 CF3 H H c=o CH2 4, 6- Me2- 2- Pyni 6-146 2 CF 3 HH c = o CH 2 4, 6- Me 2 - 2- Pyni
6—147 2 CF3 H H c=o CH2 4, 6- (0Me) 2-2-Pym 6--147 2 CF 3 HH c = o CH 2 4, 6- (0Me) 2 -2-Pym
2 CF3 H H oo CH2 3- Pyd 2 CF 3 HH oo CH 2 3- Pyd
6-149 2 CF3 H H oo CH2 6- CI- 3 - Pyd 6-149 2 CF 3 HH oo CH 2 6- CI- 3-Pyd
6-150 2 CF3 H H c=o CH2 -CO-NHMe 6-150 2 CF 3 HH c = o CH 2 -CO-NHMe
6-151 2 CF3 H H c=o CH2 -CO-NHPh
6表 (続き) 6-151 2 CF 3 HH c = o CH 2 -CO-NHPh Table 6 (continued)
置換 物性 Substitution physical properties
No. R1 R2 X J2 J3 R9 No. R 1 R 2 XJ 2 J 3 R 9
置 [融点 (°c) ]-152 2 CF3 H H C=0 CH2 -C0-NH-2-Cl-Ph[Melting point (° c)]-152 2 CF 3 HHC = 0 CH 2 -C0-NH-2-Cl-Ph
-153 2 CF3 H H c=o CH2 -CO-NMePh-153 2 CF 3 HH c = o CH 2 -CO-NMePh
-154 2 CF3 H H oo c -CO-NE (c-Hex) ·-154 2 CF 3 HH oo c -CO-NE (c-Hex)
-155 2 CF3 H H c=o CH2 - CO- N (i - Pr) 2 -155 2 CF 3 HH c = o CH 2 -CO- N (i-Pr) 2
-156 2 CF3 H H c=o c=o Me -156 2 CF 3 HH c = oc = o Me
- 157 2 CF3 H H oo c=o t-Bu-157 2 CF 3 HH oo c = o t-Bu
-158 2 CF3 H H c=o c=o - CH2- Ph-158 2 CF 3 HH c = oc = o-CH 2 -Ph
-159 2 CF3 H H c=o oo -CHMe-Ph-159 2 CF 3 HH c = o oo -CHMe-Ph
-160 2 CF3 H H c=o oo - CMe2- Ph-160 2 CF 3 HH c = o oo-CMe 2 -Ph
-161 2 CF3 H H c=o c=o Ph -161 2 CF 3 HH c = oc = o Ph
- 162 2 CF3 H H c=o oo 2-F-Ph-162 2 CF 3 HH c = o oo 2-F-Ph
-163 2 CF3 H H c=o c=o 2 - CI - Ph-163 2 CF 3 HH c = oc = o 2-CI-Ph
-164 2 CF3 H H oo c=o 2 - Me - Ph-164 2 CF 3 HH oo c = o 2-Me-Ph
-165 2 CF3 H H c=o c=o 2-i-Pr-Ph-165 2 CF 3 HH c = oc = o 2-i-Pr-Ph
-166 2 CF3 H H oo c=o 2-OMe-Ph-166 2 CF 3 HH oo c = o 2-OMe-Ph
.-167 2 CF3 H H c=o c=o 2-SMe-Ph.-167 2 CF 3 HH c = oc = o 2-SMe-Ph
-168 2 CF3 H H c=o c=o 2-SOMe-Ph-168 2 CF 3 HH c = oc = o 2-SOMe-Ph
-169 2 CF3 H H c=o c=o 2-S02Me-Ph-169 2 CF 3 HH c = oc = o 2-S0 2 Me-Ph
-170 2 CF3 H H c=o c=o 2-CN-Ph-170 2 CF 3 HH c = oc = o 2-CN-Ph
-171 2 CF3 H H c=o c=o 2- N02 - Ph-171 2 CF 3 HH c = oc = o 2- N0 2 -Ph
-172 2 CF3 H H c=o oo 2 - CF3- Ph-172 2 CF 3 HH c = o oo 2-CF 3 -Ph
-173 2 CF3 H H c=o c=o 2 - 0CF3 - Ph-173 2 CF 3 HH c = oc = o 2-0CF 3 -Ph
-174 2 CF3 H H c=o c=o 2 - SCF3- Ph-174 2 CF 3 HH c = oc = o 2-SCF 3 -Ph
-175 2 CF3 H H c=o c=o 2-S0CF3- Ph-175 2 CF 3 HH c = oc = o 2-S0CF 3 -Ph
-176 2 CF3 H H oo c=o 2-S02CF3-Ph-176 2 CF 3 HH oo c = o 2-S0 2 CF 3 -Ph
-177 2 CF3 H H oo c=o 2- C02Me_Ph-177 2 CF 3 HH oo c = o 2- C0 2 Me_Ph
-178 2 CF3 H H oo oo 2- Ph- Ph-178 2 CF 3 HH oo oo 2- Ph- Ph
-179 2 CF3 H H c=o c=o 2-PhO-Ph-179 2 CF 3 HH c = oc = o 2-PhO-Ph
-180 2 CF3 H H c=o c=o 2, 6-F2-Ph-180 2 CF 3 HH c = oc = o 2, 6-F 2 -Ph
-181 2 CF3 H H c=o c=o 2, 6- Cl2 - Ph-181 2 CF 3 HH c = oc = o 2, 6- Cl 2 -Ph
-182 2 CF3 H H c=o c=o 2, 6_Br2- Ph-182 2 CF 3 HH c = oc = o 2, 6_Br 2 -Ph
-183 2 CF3 H H c=o c=o 2, 6-I2-Ph-183 2 CF 3 HH c = oc = o 2, 6-I 2 -Ph
-184 2 CF3 H H c=o c=o 2, 6-Me2-Ph-184 2 CF 3 HH c = oc = o 2, 6-Me 2 -Ph
-185 2 CF3 H H c=o c=o 2, 6- (0Me) 2- Ph -185 2 CF 3 HH c = oc = o 2, 6- (0Me) 2 -Ph
- 186 2 CF3 H H c=o C二 0 2, 6— (CF3) 2 - Ph-186 2 CF 3 HH c = o C2 0 2,6— (CF 3 ) 2 -Ph
-187 2 CF3 H H c=o oo 2, 6- (0CF3) 2- Ph-187 2 CF 3 HH c = o oo 2, 6- (0CF 3 ) 2 -Ph
-188 2 CF3 H H oo c=o 2, 3, 4-Cl3-Ph -188 2 CF 3 HH oo c = o 2, 3, 4-Cl 3 -Ph
- 189 2 CF3 H H c=o c=o 2, 4, 6- Cl3- Ph-189 2 CF 3 HH c = oc = o 2, 4, 6- Cl 3 -Ph
-190 2 CF3 H H c=o c=o 2, 6- Cl2 - 4- CF3 - Ph -190 2 CF 3 HH c = oc = o 2, 6- Cl 2 - 4- CF 3 - Ph
-191 2 CF3 H H oo c=o 2, 6-Cl2-4-0CF3-Ph
6表 (続き) -191 2 CF 3 HH oo c = o 2, 6-Cl 2 -4-0CF 3 -Ph Table 6 (continued)
物性 Physical properties
No. R1 R2 J2 J3 R9 No. R 1 R 2 J 2 J 3 R 9
[融点 (°C) ]-192 2 CF3 H H C=0 C=0 2, 3, 4- e3-Ph[Melting point (° C)]-192 2 CF 3 HHC = 0 C = 0 2,3,4-e 3 -Ph
-193 2 CF3 H H C=0 00 2- Pyn-193 2 CF 3 HHC = 0 00 2- Pyn
-194 2 CF3 H H C=0 C=0 3 - Pyn-194 2 CF 3 HHC = 0 C = 0 3-Pyn
-195 2 CF3 H H C=0 C=0 4— Pyn-195 2 CF 3 HHC = 0 C = 0 4— Pyn
-196 2 CF3 H H C=0 C=0 6- CI- 2 - Pyn-196 2 CF 3 HHC = 0 C = 0 6- CI- 2-Pyn
-197 2 CF3 H H C=0 C=0 6- CF3- 2- Pyn -197 2 CF 3 HHC = 0 C = 0 6- CF 3 - 2- Pyn
-198 2 CF3 H H C=0 C=0 6-Cl-4-CF3-2-Pyn-198 2 CF 3 HHC = 0 C = 0 6-Cl-4-CF 3 -2-Pyn
-199 2 CF3 H H C=0 00 2 - Pym-199 2 CF 3 HHC = 0 00 2-Pym
-200 2 CF3 H H C=0 00 4-Pym-200 2 CF 3 HHC = 0 00 4-Pym
-201 2 CF3 H H C=0 C=0 4, 6- Me2- 2- Pym -201 2 CF 3 HHC = 0 C = 0 4, 6- Me 2 - 2- Pym
-202 2 CF3 H H c=o 00 4, 6- (OMe) 2_2 - Pym -202 2 CF 3 HH c = o 00 4, 6- (OMe) 2 _2-Pym
- 203 2 CF3 H H c=o C=0 3 - Pyd-203 2 CF 3 HH c = o C = 0 3-Pyd
-204 2 CF3 H H c=o C=0 6-Cl- 3- Pyd-204 2 CF 3 HH c = o C = 0 6-Cl- 3- Pyd
-205 2 CF3 H H c=o C=0 -CO-NHMe-205 2 CF 3 HH c = o C = 0 -CO-NHMe
-206 2 CF3 H H c=o C=0 -CO-NHPh-206 2 CF 3 HH c = o C = 0 -CO-NHPh
-207 2 CF3 H H c=o C=0 - CO-匪 ePh-207 2 CF 3 HH c = o C = 0-CO-band ePh
-208 2 CF3 H H c=o C=0 -CO-NEt (c-Hex)-208 2 CF 3 HH c = o C = 0 -CO-NEt (c-Hex)
-209 2 CF3 H H c=o C=0 - CO - N (i - Pr) 2 -209 2 CF 3 HH c = o C = 0-CO-N (i-Pr) 2
-210 2 CF3 H H CH2 NH Me-210 2 CF 3 HH CH 2 NH Me
-211 2 CF3 H H C¾ NH t-Bu-211 2 CF 3 HH C¾ NH t-Bu
-212 2 CF3 H H CH2 NH - CH2 - Ph-212 2 CF 3 HH CH 2 NH-CH 2 -Ph
-213 2 CF3 H H CH2 NH -CHMe-Ph-213 2 CF 3 HH CH 2 NH -CHMe-Ph
-214 2 CF3 H H CH2 NH -CMe2-Ph-214 2 CF 3 HH CH 2 NH -CMe 2 -Ph
-215 2 CF3 H H C¾ NH Ph-215 2 CF 3 HH C¾ NH Ph
-216 2 CF3 H H CH2 NH 2-F-Ph-216 2 CF 3 HH CH 2 NH 2-F-Ph
-217 2 CF3 H H C¾ NH 2 - CI - Ph-217 2 CF 3 HH C¾ NH 2-CI-Ph
-218 2 CF3 H H C¾ NH 2- Me - Ph-218 2 CF 3 HH C¾ NH 2-Me-Ph
-219 2 CF3 H H CH2 NH 2 - i - Pr- Ph-219 2 CF 3 HH CH 2 NH 2-i-Pr- Ph
-220 2 CF3 H H C¾ NH 2-OMe-Ph-220 2 CF 3 HH C¾ NH 2-OMe-Ph
-221 2 CF3 H H CH2 NH 2-SMe-Ph-221 2 CF 3 HH CH 2 NH 2-SMe-Ph
-222 2 CF3 H H CH2 NH 2-SOMe-Ph-222 2 CF 3 HH CH 2 NH 2-SOMe-Ph
-223 2 CF3 H H C¾ NH 2- S02Me- Ph-223 2 CF 3 HH C¾ NH 2- S0 2 Me- Ph
-224 2 CF3 H H CH2 NH 2-CN-Ph-224 2 CF 3 HH CH 2 NH 2-CN-Ph
-225 2 CF3 H H CH2 NH 2- N02 - Ph-225 2 CF 3 HH CH 2 NH 2- N0 2 -Ph
-226 2 CF3 H H CH2 NH 2- CF3- Ph-226 2 CF 3 HH CH 2 NH 2- CF 3 -Ph
-227 2 CF3 H H CH2 NH 2-OCFg-Ph-227 2 CF 3 HH CH 2 NH 2-OCFg-Ph
-228 2 CF3 H H CH2 NH 2- SCF3 - Ph-228 2 CF 3 HH CH 2 NH 2- SCF 3 -Ph
-229 2 CF3 H H CH2 NH 2- S0CF3- Ph-229 2 CF 3 HH CH 2 NH 2- S0CF 3 -Ph
-230 2 CF3 H H CH2 NH 2- S02CF3 - Ph-230 2 CF 3 HH CH 2 NH 2- S0 2 CF 3 -Ph
-231 2 CF, H H CH NH 2-C0,Me-Ph
6表 (続き) -231 2 CF, HH CH NH 2-C0, Me-Ph Table 6 (continued)
W 物性 W Physical properties
No. R1 R2 X J2 J3 R9 No. R 1 R 2 XJ 2 J 3 R 9
ilLW [融点 (°c) ] ilLW [melting point (° c)]
6-232 2 CF3 H H C¾ NH 2- Ph- Ph 6-232 2 CF 3 HH C¾ NH 2- Ph- Ph
6-233 2 CF3 H H CH2 NH 2-PhO-Ph 6-233 2 CF 3 HH CH 2 NH 2-PhO-Ph
6-234 2 CF3 H H CH2 NH 2, 6-F2-Ph 6-234 2 CF 3 HH CH 2 NH 2, 6-F 2 -Ph
6 - 235 2 CF3 H H CH2 NH 2, 6-Cl2-Ph 6-235 2 CF 3 HH CH 2 NH 2, 6-Cl 2 -Ph
6-236 2 CF3 H H CH2 NH 2, 6 - Me2 - Ph 6-236 2 CF 3 HH CH 2 NH 2, 6-Me 2 -Ph
6-237 2 CF3 H H C¾ NH 2, 6- (OMe) 2 - Ph 6-237 2 CF 3 HH C¾ NH 2, 6- (OMe) 2 -Ph
6 - 261 2 CF3 H H CH2 NH - CO- N (i-Pr) 2 6-261 2 CF 3 HH CH 2 NH-CO- N (i-Pr) 2
6-262 2 CF3 H H CH2 N-Me Me 6-262 2 CF 3 HH CH 2 N-Me Me
6-263 2 CF3 H H CH2 N-Me t-Bu 6-263 2 CF 3 HH CH 2 N-Me t-Bu
6-264 2 CF3 H H CH2 N-Me - C -Ph 6-264 2 CF 3 HH CH 2 N-Me-C -Ph
6-265 2 CF3 H H CH2 N-Me -CHMe-Ph 6-265 2 CF 3 HH CH 2 N-Me -CHMe-Ph
6 - 266 2 CF3 H H CH2 N-Me - CMe2-Ph 6-266 2 CF 3 HH CH 2 N-Me-CMe 2 -Ph
2 CF3 H H CH2 N-Me Ph 2 CF 3 HH CH 2 N-Me Ph
6-268 2 CF3 H H CH2 N-Me 2-F-Ph 6-268 2 CF 3 HH CH 2 N-Me 2-F-Ph
6 - 269 2 CF3 H H CH2 N-Me 2- CI - Ph 6-269 2 CF 3 HH CH 2 N-Me 2- CI-Ph
6 - 270 2 CF3 H H CH2 N-Me 2-Me-Ph 6-270 2 CF 3 HH CH 2 N-Me 2-Me-Ph
6-271 2 CF3 H H CH2 N-Me 2-i-Pr-Ph
6表 (続き) 6-271 2 CF 3 HH CH 2 N-Me 2-i-Pr-Ph Table 6 (continued)
mm 物性 mm Physical properties
No. R1 R2 X J2 J3 R9 No. R 1 R 2 XJ 2 J 3 R 9
[融点 (°c) ]- -272 2 CF3 H H CH2 N-Me 2 - OMe- Ph[Melting point (° c)]--272 2 CF 3 HH CH 2 N-Me 2-OMe- Ph
- -273 2 CF3 H H CH2 N-Me 2-SMe-Ph--273 2 CF 3 HH CH 2 N-Me 2-SMe-Ph
- -274 2 CF3 H H CH2 N-Me 2-SOMe-Ph--274 2 CF 3 HH CH 2 N-Me 2-SOMe-Ph
- -276 2 CF3 H H CH2 N-Me 2-CN-Ph--276 2 CF 3 HH CH 2 N-Me 2-CN-Ph
- -277 2 CF3 H H C¾ N-Me 2-N02-Ph - -277 2 CF 3 HH C¾ N -Me 2-N0 2 -Ph
- -278 2 CF3 H H c¾ N-Me 2-CF3 - Ph--278 2 CF 3 HH c¾ N-Me 2-CF 3 -Ph
- -279 2 CF3 H H CH2 N-Me 2-0CF3-Ph--279 2 CF 3 HH CH 2 N-Me 2-0CF 3 -Ph
- -280 2 CF3 H H CH2 N-Me 2 - SCF3- Ph--280 2 CF 3 HH CH 2 N-Me 2-SCF 3 -Ph
- -281 2 CF3 H H CH2 N-Me 2- S0CF3 - Ph--281 2 CF 3 HH CH 2 N-Me 2- S0CF 3 -Ph
- -282 2 CF3 H H CH2 N-Me 2-S02CF3-Ph--282 2 CF 3 HH CH 2 N-Me 2-S0 2 CF 3 -Ph
- -283 2 CF3 H H CH2 N-Me 2-C02Me-Ph - -283 2 CF 3 HH CH 2 N-Me 2-C0 2 Me-Ph
- -284 2 CF3 H H CH2 N-Me 2- Ph - Ph--284 2 CF 3 HH CH 2 N-Me 2- Ph-Ph
- -285 2 CF3 H H CH2 N-Me 2-PhO-Ph--285 2 CF 3 HH CH 2 N-Me 2-PhO-Ph
- -286 2 CF3 H H CH2 N-Me 2, 6- F2- Ph--286 2 CF 3 HH CH 2 N-Me 2, 6- F 2 -Ph
- -287 2 CF3 H H CH2 N-Me 2, 6-Cl2-Ph--287 2 CF 3 HH CH 2 N-Me 2, 6-Cl 2 -Ph
- -288 2 CF3 H H CH2 N-Me 2, 6- Me2- Ph--288 2 CF 3 HH CH 2 N-Me 2, 6- Me 2 -Ph
- -289 2 CF3 H H CH2 N-Me 2, 6_ (0Me) 2- Ph--289 2 CF 3 HH CH 2 N-Me 2, 6_ (0Me) 2 -Ph
- -290 2 CF3 H H CH2 N-Me 2, 6— (CF3) 2 - Ph--290 2 CF 3 HH CH 2 N-Me 2, 6— (CF 3 ) 2 -Ph
- -291 2 CF3 H H CH2 N-Me 2, 6— (0CF3) 2- Ph--291 2 CF 3 HH CH 2 N-Me 2, 6— (0CF 3 ) 2 -Ph
- -292 2 CF3 H H CH2 N-Me 2, 3, 4一 Cl3 - Ph--292 2 CF 3 HH CH 2 N-Me 2, 3, 4-Cl 3 -Ph
- -293 2 CF3 H H CH2 N-Me 2, 4, 6- Cl3— Ph--293 2 CF 3 HH CH 2 N-Me 2, 4, 6- Cl 3 — Ph
- -294 2 CF3 H H CH2 N-Me 2, 6- Cl2- 4- CF3- Ph - -294 2 CF 3 HH CH 2 N-Me 2, 6- Cl 2 - 4- CF 3 - Ph
- -295 2 CF3 H H CH2 N-Me 2, 6 - Cl2_4 - 0CF3- Ph --295 2 CF 3 HH CH 2 N-Me 2, 6-Cl 2 _4-0CF 3 -Ph
- -296 2 CF3 H H CH2 N-Me 2, 3, 4-Me3-Ph--296 2 CF 3 HH CH 2 N-Me 2, 3, 4-Me 3 -Ph
- -297 2 · CF3 H H CH2 N-Me 2-Pyn--297 2CF 3 HH CH 2 N-Me 2-Pyn
- -298 2 CF3 H H CH2 N-Me 3-Pyn--298 2 CF 3 HH CH 2 N-Me 3-Pyn
- -299 2 CF3 H H CH2 N-Me 4-Pyn--299 2 CF 3 HH CH 2 N-Me 4-Pyn
- -300 2 CF3 H H CH2 N-Me 6- CI 2- Pyn--300 2 CF 3 HH CH 2 N-Me 6- CI 2- Pyn
- -301 2 CF3 H H CH2 N-Me 6- CF3- 2 - Pyn - -301 2 CF 3 HH CH 2 N-Me 6- CF 3 - 2 - Pyn
- -302 2 CF3 H H CH2 N-Me 6 - CI- 4- CF3- 2- Pyn - -302 2 CF 3 HH CH 2 N-Me 6 - CI- 4- CF 3 - 2- Pyn
- -303 2 CF3 H H CH2 N-Me 2- Pym--303 2 CF 3 HH CH 2 N-Me 2- Pym
- -304 2 CF3 H H CH2 N-Me 4一 Pym--304 2 CF 3 HH CH 2 N-Me 4-Pym
- -305 2 CF3 H H CH2 N-Me 4, 6 - Me2- 2- Pym - -305 2 CF 3 HH CH 2 N-Me 4, 6 - Me 2 - 2- Pym
- -306 2 CF3 H H CH2 N-Me 4, 6 -(OMe) 2- 2 - Pym - -306 2 CF 3 HH CH 2 N-Me 4, 6 - (OMe) 2 - 2 - Pym
- -307 2 CF3 H H CH2 N-Me 3 - Pyd--307 2 CF 3 HH CH 2 N-Me 3-Pyd
- -308 2 CF3 H H CH2 N-Me 6 - CI- 3- Pyd--308 2 CF 3 HH CH 2 N-Me 6-CI- 3- Pyd
- -309 2 CF3 H H CH2 N-Me -CO-NHMe--309 2 CF 3 HH CH 2 N-Me -CO-NHMe
- -310 2 CF3 H H CH2 N-Me -CO-NHPh--310 2 CF 3 HH CH 2 N-Me -CO-NHPh
- -311 2 CF3 H H CH2 N-Me -CO-NMePh
6表 (続き) --311 2 CF 3 HH CH 2 N-Me -CO-NMePh Table 6 (continued)
CO 置換 物性 CO substitution properties
No. R1 R2 X J2 J3 R9 No. R 1 R 2 XJ 2 J 3 R 9
置 [融点 ( c) ]-312 2 CF3 H H CH2 N - Me -C0-NEt2 [Melting point (c)]-312 2 CF 3 HH CH 2 N-Me -C0-NEt 2
-313 2 CF3 H H CH2 N-Me -CO-NEt (c-Hex) -313 2 CF 3 HH CH 2 N-Me -CO-NEt (c-Hex)
- 314 2 CF3 H H CH2 N - Me -C0-N (i-Pr) 2 -314 2 CF 3 HH CH 2 N-Me -C0-N (i-Pr) 2
-315 3 CF3 H H CH2 CH2 Ph-315 3 CF 3 HH CH 2 CH 2 Ph
-316 3 CF3 H H CH2 CH2 2-F-Ph-316 3 CF 3 HH CH 2 CH 2 2-F-Ph
-317 3 CF3 H H C¾ CH2 2-Cl-Ph-317 3 CF 3 HH C¾ CH 2 2-Cl-Ph
-318 3 CF3 H H CH2 CH2 2, 6-F2-Ph-318 3 CF 3 HH CH 2 CH 2 2, 6-F 2 -Ph
-319 3 CF3 H H CH2 CH2 2, 6- Cl2 - Ph -319 3 CF 3 HH CH 2 CH 2 2, 6- Cl 2 -Ph
- 320 3 CF3 H H CH2 CH2 2, 6- Me2- Ph-320 3 CF 3 HH CH 2 CH 2 2, 6- Me 2 -Ph
-321 3 CF3 H H CH2 CH2 2, 6- (CF3) 2-Ph-321 3 CF 3 HH CH 2 CH 2 2, 6- (CF 3 ) 2 -Ph
-322 3 CF3 H H CH2 CH2 2, 3, 4- Cl3- Ph-322 3 CF 3 HH CH 2 CH 2 2, 3, 4-Cl 3 -Ph
-323 3 CF3 H H CH2 CH2 2, 4, 6 - Cl3_Ph-323 3 CF 3 HH CH 2 CH 2 2,4,6-Cl 3 _Ph
-324 3 CF3 H H CH2 CH2 2, 6-Cl2-4-CF3-Ph-324 3 CF 3 HH CH 2 CH 2 2, 6-Cl 2 -4-CF 3 -Ph
-325 3 CF3 H H CH2 CH2 2, 6-Cl2-4-0CF3-Ph-325 3 CF 3 HH CH 2 CH 2 2, 6-Cl 2 -4-0CF 3 -Ph
-326 3 CF3 H H CH2 CH2 2, 3, 4 - Me3-Ph -326 3 CF 3 HH CH 2 CH 2 2, 3, 4-Me 3 -Ph
4 CF3 H H C¾ CH2 Ph4 CF 3 HH C¾ CH 2 Ph
-328 4 CF3 H H CH2 CH2 2-F-Ph-328 4 CF 3 HH CH 2 CH 2 2-F-Ph
-329 4 CF3 H H CH2 CH2 2-Cl-Ph-329 4 CF 3 HH CH 2 CH 2 2-Cl-Ph
-330 4 CF3 H H CH2 CH2 2, 6-F2-Ph-330 4 CF 3 HH CH 2 CH 2 2, 6-F 2 -Ph
-331 4 CF3 H H CH2 CH2 2, 6_C12 - Ph -331 4 CF 3 HH CH 2 CH 2 2, 6_C1 2 -Ph
- 332 4 CF3 H H CH2 CH2 2, 6- Me2- Ph-332 4 CF 3 HH CH 2 CH 2 2, 6- Me 2 -Ph
-333 4 CF3 H H CHo CH2 2, 6 -(CF3) 2— Ph-333 4 CF 3 HH CHo CH 2 2, 6-(CF 3 ) 2 — Ph
-334 4 CF3 H H CH2 CH2 2, 3, 4- Cl3- Ph-334 4 CF 3 HH CH 2 CH 2 2, 3, 4-Cl 3 -Ph
-335 4 CF3 H H CH2 CH2 2, 4, 6- Cl3- Ph-335 4 CF 3 HH CH 2 CH 2 2, 4, 6- Cl 3 -Ph
-336 4 CF3 H H CH2 CH2 2, 6-Cl2-4-CF3-Ph-336 4 CF 3 HH CH 2 CH 2 2, 6-Cl 2 -4-CF 3 -Ph
-337 4 CF3 H H C¾ CH2 2, 6- Cl2- 4 - 0CF3-Ph -337 4 CF 3 HH C¾ CH 2 2, 6- Cl 2 - 4 - 0CF 3 -Ph
-338 4 CF3 H H CH2 CH2 2, 3, 4- Me3 - Ph-338 4 CF 3 HH CH 2 CH 2 2, 3, 4-Me 3 -Ph
-339 2 CF3 H 5 - CI CH2 CH2 2- CI- Ph NMR-8-340 2 CF3 H H Me2C CH2 2, 6-Cl2-Ph 180. 3-182. 0-341 2 CF3 H H C¾ CH2 4-Br-2, 6- Me2 - Ph 200. 8 i-Pr --342 2 CF。 H CH9 CH。 4一 Br - 2, 6 - Me2 - Ph 1. 5249 (21°C) -339 2 CF 3 H 5-CI CH 2 CH 2 2- CI- Ph NMR-8 -340 2 CF 3 HH Me 2 C CH 2 2, 6-Cl 2 -Ph 180. 3-182. 0-341 2 CF 3 HH C¾ CH 2 4-Br-2, 6-Me 2 -Ph 200. 8 i-Pr --342 2 CF. H CH 9 CH. 41-Br-2, 6-Me 2 -Ph 1.5249 (21 ° C)
CO CO
-343 2 CF3 H H CH2 C¾ 4-Br-2-CF3-Ph 175. 3 c— Pr - - 344 2 CF3 H CH2 CH2 4 - Br- 2, 6 - Me2 - Ph 1. 5369 (21。C) -343 2 CF 3 HH CH 2 C¾ 4-Br-2-CF 3 -Ph 175. 3 c- Pr - - 344 2 CF 3 H CH 2 CH 2 4 - Br- 2, 6 - Me 2 - Ph 1. 5369 (21.C)
CO CO
i- Pr --345 2 CF3 H CH2 CH2 2- Cl-6- Me- Ph 1. 5241 (22°C) i- Pr --345 2 CF 3 H CH 2 CH 2 2- Cl-6- Me- Ph 1.5241 (22 ° C)
CO CO
-346 2 CF3 H H C¾ MeCH 2, 6- Cl2- Ph 166. 8-167. 7 t-Bu--347 2 CF3 H CH2 CH2 4- Br- 2, 6- Me2 - Ph 150. 5 -346 2 CF 3 HH C¾ MeCH 2, 6- Cl 2 -Ph 166.8-167.7 t-Bu --347 2 CF 3 H CH 2 CH 2 4-Br- 2, 6- Me 2 -Ph 150 . Five
CO
6表 (続き) CO Table 6 (continued)
置換 物性 Substitution physical properties
No. R1 R2 X J2 J3 R9 No. R 1 R 2 XJ 2 J 3 R 9
位置 [融点 (°c) ] Position [melting point (° c)]
6- -348 2 CF3 Ph - CO H CH2 CH2 4-Br - 2, 6- Me2 - Ph 57. 3-64. 16- -348 2 CF 3 Ph-CO H CH 2 CH 2 4-Br-2, 6- Me 2 -Ph 57.3-64. 1
6- -349 2 CF3 H H MeCH CH2 2, 6- Cl2- Ph 172. 4-173. 3 i-Pr- o- -350 2 CF3 H MeCH CH2 2, 6- Cl2- Ph 51. 7-66. 8 6- -349 2 CF 3 HH MeCH CH 2 2, 6- Cl 2 -Ph 172.4-173.3 i-Pr- o- -350 2 CF 3 H MeCH CH 2 2, 6- Cl 2 -Ph 51 . 7-66. 8
CO CO
i - Pr- i-Pr-
6- -351 2 CF, ύ H C¾ MeCH 2, 6- Cl2- Ph 1. 5375 (22°C) 6- -351 2 CF, ύ H C¾ MeCH 2, 6- Cl 2 -Ph 1.5375 (22 ° C)
CO CO
i-Pr- i-Pr-
6- -352 厶 しト 3 n し H2 し H2 一し丄—ーO 6- -352 m 3 h H 2 then H 2
rn I . iD t) ί しリ CO rn I. iD t)
6- -353 2 CF3 H H CH2 CH2 4- Br_2- Me - Ph 158. 1 i-Pr-6- -353 2 CF 3 HH CH 2 CH 2 4-Br_2- Me-Ph 158.1 i-Pr-
6- -354 2 CF, 3 H CH9 CH9 4— Br_2 - Me— Ph 1. 5371 (21°C) 6- -354 2 CF, 3 H CH 9 CH 9 4— Br_2-Me— Ph 1.5371 (21 ° C)
CO CO
6- -355 2 CF3 H H CH2 CH2 4- CI- 2- Me- Ph 158. 0-161. 9 ト Pr-6- -355 2 CF 3 HH CH 2 CH 2 4- CI- 2- Me- Ph 158.0-161.9 9 Pr-
6- -356 2 CF1 3, H CH9 CH9 4-Cl-2-Me-Ph 47. 3-60. 0 6- -356 2 CF 1 3, H CH 9 CH 9 4-Cl-2-Me-Ph 47.3-60. 0
CO CO
i - Pr - i-Pr-
6- -357 2 CF3 H CH2 CH2 2, 6- Cl2 - Ph 1. 5381 (22°C) 6- -357 2 CF 3 H CH 2 CH 2 2, 6- Cl 2 -Ph 1.5381 (22 ° C)
CO CO
6- -358 2 CF3 H H CH2 CH2 5- CI- 2_Me - Ph 167. 56- -358 2 CF 3 HH CH 2 CH 2 5- CI- 2_Me-Ph 167.5
6- -359 2 CF3 Me H C¾ CH2 2, 6- Cl2 - Ph 123-1246- -359 2 CF 3 Me H C¾ CH 2 2, 6- Cl 2 -Ph 123-124
6- -360 2 CF3 MeOCH2 H CH2 CH2 2, 6 - Cl2-Ph 1. 5403 (27°C) 6- -360 2 CF 3 MeOCH 2 H CH 2 CH 2 2, 6-Cl 2 -Ph 1.5403 (27 ° C)
2, 4, 6 2, 4, 6
6- -361 2 CF3 -Me3 - H CH2 CH2 2, 6 - Cl2- Ph NMR-9 6- -361 2 CF 3 -Me 3 -H CH 2 CH 2 2,6-Cl 2 -Ph NMR-9
Ph - CO Ph-CO
2, 6 - 2, 6-
6 - -362 2 CF3 Me2 - H CH2 CH2 2, 6-Cl2-Ph NMR-10 6--362 2 CF 3 Me 2 -H CH 2 CH 2 2,6-Cl 2 -Ph NMR-10
Ph-CO Ph-CO
6- -363 2 CF3 Ph - CO H C¾ CH2 2, 6 - Cl2- Ph 95-97 i一 6- -363 2 CF 3 Ph-CO H C¾ CH 2 2, 6-Cl 2 -Ph 95-97 i
6- -364 2 CF3 BuO- H CH2 CH2 2, 6-Cl2-Ph 1. 5232 (21。C) 6- -364 2 CF 3 BuO- H CH 2 CH 2 2, 6-Cl 2 -Ph 1.5232 (21.C)
CO CO
n一 n one
6- -365 2 CF3 BuO- H CH2 CH2 2, 6 - Cl2- Ph 1. 5335 (22°C) 6- -365 2 CF 3 BuO- H CH 2 CH 2 2, 6-Cl 2 -Ph 1.5335 (22 ° C)
CO CO
MeO- MeO-
6- -366 2 CF3 H CH2 CH2 2, 6— Cl2— Ph 126-128 6- -366 2 CF 3 H CH 2 CH 2 2, 6—Cl 2 — Ph 126-128
CO CO
EtO- EtO-
6- -367 2 CF3 H CH2 C¾ 2, 6— Cl2 - Ph 1. 5290 (21°C) 6- -367 2 CF 3 H CH 2 C¾ 2, 6— Cl 2 -Ph 1.5290 (21 ° C)
CO CO
PhO - PhO-
6- -368 2 CF3 H CH2 CH2 2, 6 - Cl2— Ph 1. 5479 (25°C) 6- -368 2 CF 3 H CH 2 CH 2 2, 6-Cl 2 — Ph 1.5479 (25 ° C)
CO CO
n-Pr- NPR-
6- -369 2 CF3 H C¾ C¾ 2, 6 - Cl2-Ph 1. 5345 (25。C) 6- -369 2 CF 3 H C¾ C¾ 2, 6-Cl 2 -Ph 1.5345 (25.C)
CO
6表 (続き) CO Table 6 (continued)
Y 2 土Y 2 Sat
IV A. Λ J T J 9 Wl IV A. Λ J T J 9 Wl
Xv Xv
位置 [融点 (。c) ] n-Bu--370 2 3 H CH。 CHo 2 6 - CI。一 Ph 1 5341 (25°C) Position [melting point (.c)] n-Bu--370 23 H CH. CHo 26-CI. One Ph 1 5341 (25 ° C)
CO CO
i-Bu--371 2 CF3 H CH2 CH2 2, 6- Cl2- Ph 127. 0-128. 0 i-Bu--371 2 CF 3 H CH 2 CH 2 2, 6- Cl 2 -Ph 127. 0-128. 0
CO CO
4-C1--372 2 CF3 H CH2 CH2 2, 6-Cl2-Ph 134-138 4-C1--372 2 CF 3 H CH 2 CH 2 2, 6-Cl 2 -Ph 134-138
Ph-CO Ph-CO
-373 2 CF3 i-Pr H CH2 CH2 2, 6 - Cl2- Ph 159-161-374 2 CF3 Et-CO H CH2 CH2 2, 6— Cl2 - Ph 1. 5370 (29。C) -373 2 CF 3 i-Pr H CH 2 CH 2 2, 6-Cl 2 -Ph 159-161-374 2 CF 3 Et-CO H CH 2 CH 2 2, 6— Cl 2 -Ph 1.5370 (29 C)
4- Me --375 2 CF3 H CH2 CH2 2, 6- Cl2-Ph 118-121 4- Me --375 2 CF 3 H CH 2 CH 2 2,6-Cl 2 -Ph 118-121
Ph- CO Ph- CO
CH2=CCH 2 = C
-376 2 CF3 H (CH2 H CH2 CH2 2, 6 - Cl2 - Ph 98-100 -376 2 CF 3 H (CH 2 H CH 2 CH 2 2, 6-Cl 2 -Ph 98-100
) 2 - CO ) 2 -CO
4一 Four
-377 2 CF3 CF3- H CH2 CH2 2, 6- Cl2- Ph 141-145 -377 2 CF 3 CF 3 -H CH 2 CH 2 2, 6- Cl 2 -Ph 141-145
Ph - CO Ph-CO
2, 4--378 2 CF3 F2- H CH2 CH2 2, 6 - Cl2 - Ph 119-122 2, 4--378 2 CF 3 F 2 -H CH 2 CH 2 2, 6-Cl 2 -Ph 119-122
Ph-CO Ph-CO
Ph--379 2 CF3 H CH2 CH2 2, 6 - Cl2 - Ph 125-128 Ph--379 2 CF 3 H CH 2 CH 2 2, 6-Cl 2 -Ph 125-128
Ph - CO Ph-CO
2- Me- - 380 2 CF3 H CH2 CH2 2, 6 - Cl2- Ph 143-146 2- Me--380 2 CF 3 H CH 2 CH 2 2, 6-Cl 2 -Ph 143-146
Ph - CO Ph-CO
-381 2 CHF2 H H CH2 C¾ 2, 6 - CI厂 Ph 176. 5-382 2 CF3 H H C=0 N-Me Ph 132-134-383 2 CF3 H H N-Ph C=0 Me 44-46
-381 2 CHF 2 HH CH 2 C¾ 2, 6-CI Factory Ph 176.5-382 2 CF 3 HHC = 0 N-Me Ph 132-134-383 2 CF 3 HH N-Ph C = 0 Me 44-46
一般式 (I一 6 ) General formula (I-I 6)
第7表 (R2=H、 R14=Hヽ m= : 0、 A= :一 C 一、 G^O) Table 7 (R 2 = H, R 14 = H ヽ m =: 0, A =: one C, G ^ O)
置換 Replace
1 Dl Y 1 Dl Y
\0. IV Λ J R13 T¾J 1土 位 \ 0. IV Λ JR 13 T¾J 1st place
7-1 2 CF3 H CH Me 7-1 2 CF 3 H CH Me
7-6 2 CF3 H CH Ph 7-6 2 CF 3 H CH Ph
7-7 2 CF3 H CH 2 - F - Ph 7-7 2 CF 3 H CH 2-F-Ph
7-8 2 CF3 H CH 2 - Cl-Ph 7-8 2 CF 3 H CH 2-Cl-Ph
7-9 2 CF3 H CH 3-Cl-Ph 7-9 2 CF 3 H CH 3-Cl-Ph
7-10 2 CF3 H CH 4 - CI - Ph 7-10 2 CF 3 H CH 4-CI-Ph
7 11 2 CF3 H CH 2 - Br Ph 7 11 2 CF 3 H CH 2-Br Ph
7-12 2 CF3 H CH 2 - 1 - Ph 7-12 2 CF 3 H CH 2-1-Ph
7-13 2 CF3 H CH 2 - Me Ph 7-13 2 CF 3 H CH 2-Me Ph
7-14 2 CF3 H CH 2-i-Pr-Ph 7-14 2 CF 3 H CH 2-i-Pr-Ph
7-15 2 CF3 H CH 2-OMe-Ph 7-15 2 CF 3 H CH 2-OMe-Ph
7-16 2 CF3 H CH 2-SMe-Ph 7-16 2 CF 3 H CH 2-SMe-Ph
7-17 2 CF3 H CH 2 - SOMe - Ph 7-17 2 CF 3 H CH 2-SOMe-Ph
7-18 2 CF3 H CH 2 - S02Me - Ph 7-18 2 CF 3 H CH 2-S0 2 Me-Ph
7-19 2 CF3 H CH 2 CN - Ph 7-19 2 CF 3 H CH 2 CN-Ph
7-20 2 CF3 H CH 2-N02-Ph 7-20 2 CF 3 H CH 2- N0 2 -Ph
7-21 2 CF3 H CH 2 - CF3 - Ph 7-21 2 CF 3 H CH 2-CF 3 -Ph
7-22 2 CF3 H CH 2 - 0CF3 - Ph 7-22 2 CF 3 H CH 2-0CF 3 -Ph
7-23 2 CF3 H CH 2 - SCF3- Ph 7-23 2 CF 3 H CH 2-SCF 3 -Ph
7-24 2 CF3 H CH 2 - S0CF3 Ph 7-24 2 CF 3 H CH 2-S0CF 3 Ph
7-25 2 CF3 H CH 2-S02CF3-Ph 7-25 2 CF 3 H CH 2-S0 2 CF 3 -Ph
7-26 2 CF3 H CH 2 - C02Me Ph 7-26 2 CF 3 H CH 2-C0 2 Me Ph
7-27 2 CF3 H CH 2-Ph-Ph 7-27 2 CF 3 H CH 2-Ph-Ph
7-28 2 CF3 H CH 2 - PhO - Ph 7-28 2 CF 3 H CH 2-PhO-Ph
7-29 2 CF3 H CH 2, 6 - F2 - Ph
7表 (続き) 7-29 2 CF 3 H CH 2, 6-F 2 -Ph Table 7 (continued)
置換 Rl3 Replacement Rl3
o. R1 X J" 物性 位置o. R 1 XJ "physical property position
-30 2 CF3 H CH 2, 6 - Cl2 - Ph-30 2 CF 3 H CH 2, 6-Cl 2 -Ph
-31 2 CF3 H CH 2, 6— Me2 - Ph-31 2 CF 3 H CH 2, 6—Me 2 -Ph
-32 2 CF3 H CH 2, 6 - (OMe) 2-Ph-32 2 CF 3 H CH 2, 6-(OMe) 2 -Ph
-33 2 CF3 H CH 2, 6— (CF3) 2 - Ph -33 2 CF 3 H CH 2,6— (CF 3 ) 2 -Ph
- 34 2 CF3 H CH 2, 6- (OCF3) 2 - Ph-34 2 CF 3 H CH 2, 6- (OCF 3 ) 2 -Ph
-35 2 CF3 H CH 2, 3, 4-Clg-Ph-35 2 CF 3 H CH 2, 3, 4-Clg-Ph
-36 2 CF3 H CH 2, 4, 6- Cl3_Ph-36 2 CF 3 H CH 2, 4, 6- Cl 3 _Ph
-37 2 CF3 H CH 2, 6- Cl2- 4 - CF3-Ph-37 2 CF 3 H CH 2, 6- Cl 2-4- CF 3 -Ph
-38 2 CF3 H CH 2, 6- Cl2 - 4— OCF3 - Ph -38 2 CF 3 H CH 2, 6- Cl 2 - 4- OCF 3 - Ph
-39 2 CF3 H CH 2, 3, 4-Me3-Ph-39 2 CF 3 H CH 2, 3, 4-Me 3 -Ph
-40 2 CF3 H CH 2 - Pyn-40 2 CF 3 H CH 2-Pyn
-41 2 CF3 H CH 3 - Pyn-41 2 CF 3 H CH 3-Pyn
-42 2 CF3 H CH 4一 Pyn-42 2 CF 3 H CH 4 1 Pyn
-43 2 CF3 H CH 6- CI- 2- Pyn-43 2 CF 3 H CH 6- CI- 2- Pyn
-44 2 CF3 H CH 6- CF3- 2- Pyn -44 2 CF 3 H CH 6- CF 3 - 2- Pyn
-45 2 CF3 H CH 6 - CI- 4- CF3- 2 - Pyn -45 2 CF 3 H CH 6 - CI- 4- CF 3 - 2 - Pyn
-46 2 CF3 H CH 2-Pym-46 2 CF 3 H CH 2-Pym
-47 2 CF3 H CH 4-Pym-47 2 CF 3 H CH 4-Pym
-48 2 CF3 H CH 4, 6-Me2-2-Pym-48 2 CF 3 H CH 4, 6-Me 2 -2-Pym
-49 2 CF3 H CH 4, 6— (OMe) 2-2-Pym-49 2 CF 3 H CH 4, 6— (OMe) 2 -2-Pym
-50 2 CF3 H CH 3-Pyd-50 2 CF 3 H CH 3-Pyd
-51 2 CF3 H CH -CO-NHMe-51 2 CF 3 H CH -CO-NHMe
-52 2 CF3 H CH -CO-匿 h-52 2 CF 3 H CH -CO-H
-53 2 CF3 H CH - CO- NMePh-53 2 CF 3 H CH-CO- NMePh
-54 2 CF3 H CH -CO- NEt -(c- Hex)-54 2 CF 3 H CH -CO- NEt-(c- Hex)
-55 2 CF3 H N Me -55 2 CF 3 HN Me
- 56 2 CF3 H N t-Bu-56 2 CF 3 HN t-Bu
-57 2 CF3 H N-57 2 CF 3 HN
-58 2 CF3 H N - CHMe- Ph-58 2 CF 3 HN-CHMe- Ph
-59 2 CF3 H N-59 2 CF 3 HN
-60 2 CF3 H N Ph 123. 8-61 2 CF3 H N 2-F-Ph-60 2 CF 3 HN Ph 123. 8-61 2 CF 3 HN 2-F-Ph
-62 2 CF3 H N 2-Cl-Ph-62 2 CF 3 HN 2-Cl-Ph
-63 2 CF3 H N 3 - CI - Ph-63 2 CF 3 HN 3-CI-Ph
-64 2 CF3 H N 4- CI - Ph-64 2 CF 3 HN 4- CI-Ph
-65 2 CF3 H N 2- Me- Ph-65 2 CF 3 HN 2- Me- Ph
-66 2 CF3 H N 2-i-Pr-Ph-66 2 CF 3 HN 2-i-Pr-Ph
-67 2 CF3 H N 2- OMe - Ph-67 2 CF 3 HN 2- OMe-Ph
-68 2 CF3 H N 2-SMe-Ph-68 2 CF 3 HN 2-SMe-Ph
-69 2 CF3 H N 2-SOMe-Ph
7表 (続き) -69 2 CF 3 HN 2-SOMe-Ph Table 7 (continued)
mm mm
No. R1 X J'1 R13 物性 置 No. R 1 X J ' 1 R 13
- 70 2 CF3 H N 2 - S02Me - Ph-70 2 CF 3 HN 2-S0 2 Me-Ph
-71 2 CF3 H N 2-CN-Ph -71 2 CF 3 HN 2-CN-Ph
- 72 2 CF3 H N 2 - N02 - Ph-72 2 CF 3 HN 2-N0 2 -Ph
-73 2 CF3 H N 2-CF3-Ph-73 2 CF 3 HN 2-CF 3 -Ph
-74 2 CF3 H N 2-0CF3-Ph-74 2 CF 3 HN 2-0CF 3 -Ph
-75 2 CF3 H N 2- SCF3 - Ph-75 2 CF 3 HN 2- SCF 3 -Ph
-76 2 CF3 H N 2-SOCFj-Ph-76 2 CF 3 HN 2-SOCFj-Ph
-77 2 CF3 H N 2- S02CF3- Ph-77 2 CF 3 HN 2- S0 2 CF 3 -Ph
-78 2 CF3 H N 2-C02Me-Ph-78 2 CF 3 HN 2-C0 2 Me-Ph
-79 2 CF3 H N 2- Ph - Ph-79 2 CF 3 HN 2- Ph-Ph
-80 2 CF3 H N 2-PhO-Ph-80 2 CF 3 HN 2-PhO-Ph
-81 2 CF3 H N 2, 6-F2-Ph-81 2 CF 3 HN 2, 6-F 2 -Ph
-82 2 CF3 H N 2, 6- Cl2-Ph-82 2 CF 3 HN 2, 6- Cl 2 -Ph
-83 2 CF3 H N 2, 6 - Me2- Ph-83 2 CF 3 HN 2, 6-Me 2 -Ph
-84 2 CF3 H N 2, 6- (OMe) 2- Ph-84 2 CF 3 HN 2, 6- (OMe) 2 -Ph
-85 2 CF3 H N 2, 6— (CF3) 2_Ph-85 2 CF 3 HN 2, 6— (CF 3 ) 2 _Ph
-86 2 CF3 H N 2, 6— (0CF3) 2— Ph-86 2 CF 3 HN 2, 6— (0CF 3 ) 2 — Ph
-87 2 CF3 H N 2, 3, 4-Cl3-Ph-87 2 CF 3 HN 2, 3, 4-Cl 3 -Ph
-88 2 CF3 H N 2, 4, 6 - Cl3- Ph-88 2 CF 3 HN 2, 4, 6-Cl 3 -Ph
-89 2 CF3 H N 2, 6 - Cl2 - 4- CF3 - Ph -89 2 CF 3 HN 2, 6 - Cl 2 - 4- CF 3 - Ph
-90 2 CF3 H N 2, 6- Cl2- 4_0CF3 - Ph -90 2 CF 3 HN 2, 6- Cl 2 - 4_0CF 3 - Ph
-91 2 CF3 H N 2, 3, 4 - Me3 - Ph-91 2 CF 3 HN 2, 3, 4-Me 3 -Ph
-92 2 CF3 H N 2-Pyn-92 2 CF 3 HN 2-Pyn
-93 2 CF3 H N 3-Pyn-93 2 CF 3 HN 3-Pyn
-94 2 CF3 H N 4-Pyn-94 2 CF 3 HN 4-Pyn
-95 2 CF3 H N 6 - CI - 2 - Pyn-95 2 CF 3 HN 6-CI-2-Pyn
-96 2 CF3 H N 6-CF3-2-Pyn-96 2 CF 3 HN 6-CF 3 -2-Pyn
-97 2 CF3 H N 6 - CI - 4 CF3- 2 - Pyn -97 2 CF 3 HN 6 - CI - 4 CF 3 - 2 - Pyn
-98 2 CF3 H N 2- Pym-98 2 CF 3 HN 2- Pym
-99 2 CF3 H N 4- Pym -99 2 CF 3 HN 4- Pym
- 100 2 CF3 H N 4, 6 - Me2 - 2 - Pym - 100 2 CF 3 HN 4, 6 - Me 2 - 2 - Pym
-101 2 CF3 H N 4, 6- (OMe) 2- 2- Pym -101 2 CF 3 HN 4, 6- (OMe) 2 - 2- Pym
-102 2 CF3 H N 3-Pyd-102 2 CF 3 HN 3-Pyd
-103 2 CF3 H N -CO-NHMe-103 2 CF 3 HN -CO-NHMe
-104 2 CF3 H N -CO-NHPh-104 2 CF 3 HN -CO-NHPh
-105 2 CF3 H N -CO-NMePh-105 2 CF 3 HN -CO-NMePh
-106 2 CF3 H N -CO-NEt (c-Hex)-106 2 CF 3 HN -CO-NEt (c-Hex)
-107 3 CF3 H N Me-107 3 CF 3 HN Me
-108 3 CF3 H N t-Bu-108 3 CF 3 HN t-Bu
-109 3 CF3 H N 一 CH2 - Ph .
第 7表 (続き) -109 3 CF 3 HN one CH 2 -Ph. Table 7 (continued)
齊撒 Scatter
No. 1 X JJ R13 物性 1 No. 1 XJ J R 13 Physical properties 1
7 Q n し f Mfci Γ 7 Q n then f Mfci Γ
Q Q
/ 丄丄丄 し u Π IN し JVJ ΓΠ / U u u Π IN J JVJ ΓΠ
7 /—1丄 1 l / 0 u Π IN ΓΠ 7 / —1 丄 1 l / 0 u Π IN ΓΠ
ο 3 Π 厶 ο 3 Π Π
71—1丄丄 1 At ο 0 71—1 丄 丄 1 At ο 0
し n し丄 i 丄丄 n IN d し丄 N n 丄 i 丄 丄 n IN d 丄
Q u Q u
/ 丄丄 し 3 n IN ·¾ し上 ΓΠ / し し3 n IN
Q Q
( 丄丄 / ^3 n IN り一 Μθ "Pk (丄 丄 / ^ 3 n IN Ri 一 θ "Pk
丄丄 u 丄 丄 u
し 3 n 1 Γ rfl Then 3 n 1 Γ rfl
u u
/ 丄丄 Q / 丄 丄 Q
し 3 n IN ujvie Γπ 3n IN ujvie Γπ
Q u M Q u M
/ 丄 し 3 n J / ο Θ / 丄 3 3 n J / ο Θ
JLZ Q JLZ Q
丄 0 しト 3 n IN UJvle rn 丄 0 Set 3 n IN UJvle rn
7 on Q 7 on Q
0 し 3 Π οϋ2Μθ rn 0 then 3 Π οϋ 2 Μθ rn
Z し IN rn Z then IN rn
0 しト 3 n IN Z—し! 0 to 3 n IN Z—to!
u u
/ 丄 ο しト 3 Π IN Z Uし! / 丄 ο Shito 3 Π IN Z U Shi!
/ 丄 { 0 しト 3 IN し 3 ril / 丄 {0 ト 3 IN 3 3 ril
丄 0 し n IN り一 Qnmし! ^ 丄 0 then n IN one Qnm! ^
ο ο
/ 丄 ο ^3 n IN 9_cn PR _DVi / 丄 ο ^ 3 n IN 9_cn PR _DVi
7 ί—1丄 Q 3H(J Mr^—O 7 ί—1 丄 Q 3H (J Mr ^ —O
し 3 π IN —Γίλ 3 π IN —Γίλ
0 M 0 M
/ 丄 丄 ο し n i\ Δ ru ΓΠ / 丄 丄 ο do n i \ Δ ru ΓΠ
7 i—1丄 Q9 7 i—1 丄 Q9
し 3 rl IN Δ rnu rn 3 rl IN Δ rnu rn
7 33 A ¾— P rnViOu— 7 33 A ¾— P rnViOu—
i 丄 し u i し then u
乙, し丄 Otsu, Shu
7 f—丄1 ^PΌ, ο Π K INf 7 f— 丄 1 ^ PΌ, ο Π K INf
^3 Ό ivie2 rfl ^ 3 Ό ivie 2 rfl
ί 丄 ύ ί ο し ム, uwieノ n w 丄 ύ ί ο ム ム, uwie no n
丄《30 0 ^3 n M Ό し Γ3ノ rii 丄 《30 0 ^ 3 n M Ό Γ 3ノ rii
上 d Q 0 し u n M Upper d Q 0 then u n M
ム υ υし ノ m M m
7-1 ΑΠ し li N Δ, 0, ¾ し丄 i ll 7-1 ΑΠ li li N Δ, 0, ¾ 丄 i ll
ί 丄 "4:丄 ο H 厶, ft Ό一门 4 丄 "4: 丄 ο H m, ft Ό 一 门
し丄 ΧΙ 丄
丄 Q NI 丄 Q NI
U し丄 ^ し^ *3 U shi ^ shi ^ * 3
丄" ¾ο Q し 9 Πし上 -4-ΠΓしΡ -Ph 丄 "¾ο Q 9 9 ΠΓ on -4-ΠΓ ΠΓ -Ph
7-144 3 CF3 H N 2 3, 4-Me3-Ph 7-144 3 CF 3 HN 23, 4-Me 3 -Ph
7-145 3 CF3 H N 2-Pyn 7-145 3 CF 3 HN 2-Pyn
7-146 3 CF3 H N 3- Pyn 7-146 3 CF 3 HN 3- Pyn
7-147 3 CF3 H N 4— Pyn 7-147 3 CF 3 HN 4— Pyn
7-148 3 CF3 H N 6 - - 2 Pyn 7-148 3 CF 3 HN 6--2 Pyn
7-149 3 CF3 H N 6- CF3_2 - Pyn
7表 (続き) 7-149 3 CF 3 HN 6- CF 3 _2-Pyn Table 7 (continued)
置 Place
No. R1 X J'1 R13 物性-150 3 CF3 H N 6-Cl-4-CF3-2-PynNo. R 1 X J ' 1 R 13 Physical properties -150 3 CF 3 HN 6-Cl-4-CF 3 -2-Pyn
-151 3 CF3 H N 2- Pym-151 3 CF 3 HN 2- Pym
-152 3 CF3 H N 4-Pym-152 3 CF 3 HN 4-Pym
-153 3 CF3 H N 4, 6_Me2 2- Pym-153 3 CF 3 HN 4, 6_Me 2 2- Pym
-154 3 CF3 H N 4, 6- (0Me) 2-2-Pym-154 3 CF 3 HN 4, 6- (0Me) 2 -2-Pym
-155 3 CF3 H N 3-Pyd-155 3 CF 3 HN 3-Pyd
-156 3 CF3 H N -CO-NHMe-156 3 CF 3 HN -CO-NHMe
-157 3 CF3 H N -CO-NHPh-157 3 CF 3 HN -CO-NHPh
-158 3 CF3 H N - CO- NMePh-158 3 CF 3 HN-CO- NMePh
-159 3 CF3 H N -CO-NEt (c-Hex)-159 3 CF 3 HN -CO-NEt (c-Hex)
-160 4 CF3 H N Me-160 4 CF 3 HN Me
-161 4 CF3 H N t-Bu-161 4 CF 3 HN t-Bu
-162 4 CF3 H N - C - Ph-162 4 CF 3 HN-C-Ph
-163 4 CF3 H N -CHMe-Ph-163 4 CF 3 HN -CHMe-Ph
-164 4 CF3 H N - CMe2- Ph-164 4 CF 3 HN-CMe 2 -Ph
-165 4 CF3 H N Ph-165 4 CF 3 HN Ph
-166 4 CF3 H N 2-F-Ph-166 4 CF 3 HN 2-F-Ph
-167 4 CF3 H N 2-Cl-Ph-167 4 CF 3 HN 2-Cl-Ph
-168 4 CF3 H N 3- CI - Ph-168 4 CF 3 HN 3- CI-Ph
-169 4 CF3 H N 4 - CI - Ph-169 4 CF 3 HN 4-CI-Ph
-170 4 CF3 H N 2- Me- Ph-170 4 CF 3 HN 2- Me- Ph
-171 4 CF3 H N 2-i-Pr-Ph-171 4 CF 3 HN 2-i-Pr-Ph
-172 4 CF3 H N 2-OMe-Ph-172 4 CF 3 HN 2-OMe-Ph
-173 4 CF3 H N 2 - SMe - Ph-173 4 CF 3 HN 2-SMe-Ph
-174 4 CF3 H N 2-SOMe-Ph-174 4 CF 3 HN 2-SOMe-Ph
-175 4 CF3 H N 2_S02Me - Ph-175 4 CF 3 HN 2_S0 2 Me-Ph
-176 4 CF3 H N 2-CN-Ph-176 4 CF 3 HN 2-CN-Ph
-177 4 CF3 H N 2 - N02 - Ph-177 4 CF 3 HN 2-N0 2 -Ph
-178 4 CF3 H N 2 - CF3 - Ph-178 4 CF 3 HN 2-CF 3 -Ph
-179 4 CF3 H N 2- OCF3- Ph-179 4 CF 3 HN 2- OCF 3 -Ph
-180 4 CF3 H N 2_SCF3 - Ph-180 4 CF 3 HN 2_SCF 3 -Ph
-181 4 CF3 H N 2- S0CF3 - Ph-181 4 CF 3 HN 2- S0CF 3 -Ph
-182 4 CF3 H N 2- S02CF3 - Ph-182 4 CF 3 HN 2- S0 2 CF 3 -Ph
-183 4 CF3 H N 2-C02Me-Ph-183 4 CF 3 HN 2-C0 2 Me-Ph
-184 4 CF3 H N 2 - Ph - Ph-184 4 CF 3 HN 2-Ph-Ph
-185 4 CF3 H N 2-PhO-Ph-185 4 CF 3 HN 2-PhO-Ph
-186 4 CF3 H N 2, 6 - F2-Ph-186 4 CF 3 HN 2, 6-F 2 -Ph
-187 4 CF3 H N 2, 6 - Cl2 - Ph-187 4 CF 3 HN 2, 6-Cl 2 -Ph
-188 4 CF3 H N 2, 6- Me2- Ph-188 4 CF 3 HN 2, 6- Me 2 -Ph
-189 4 CF3 H N 2, 6- (OMe) 2 - Ph
7表 (続き) -189 4 CF 3 HN 2, 6- (OMe) 2 -Ph Table 7 (continued)
置換 Replace
No. R1 X J1 R13 物性-190 4 o3 H N 2, 6 - (CF3) 2-Ph No. R 1 XJ 1 R 13 Physical properties -190 4 o 3 HN 2, 6-(CF 3 ) 2 -Ph
- 191 4 CF3 H N 2, 6 - (0CF3J 2- Ph-191 4 CF 3 HN 2, 6-(0CF 3 J 2- Ph
-192 4 CF3 H N 2, 3, 4 - Cl3 - Ph -192 4 CF 3 HN 2, 3, 4-Cl 3 -Ph
- 193 4 CF3 H N 2, 4, 6 - Cl3 - Ph-193 4 CF 3 HN 2, 4, 6-Cl 3 -Ph
-194 4 CF3 H N 2, 6-Cl2-4-CF3-Ph -194 4 CF 3 HN 2, 6-Cl 2 -4-CF 3 -Ph
- 195 4 CF3 H N 2, 6 Cl2 - 4 - 0CF3 - Ph - 195 4 CF 3 HN 2, 6 Cl 2 - 4 - 0CF 3 - Ph
-196 4 CF3 H N 2, 3, 4- Me3 - Ph-196 4 CF 3 HN 2, 3, 4-Me 3 -Ph
-197 4 CF3 H N 2-Pyn -197 4 CF 3 HN 2-Pyn
- 198 4 CF3 H N 3-Pyn-198 4 CF 3 HN 3-Pyn
-199 4 CF3 H N 4-Pyn-199 4 CF 3 HN 4-Pyn
-200 4 CF3 H N 6 - CI - 2 - Pyn-200 4 CF 3 HN 6-CI-2-Pyn
-201 4 CF3 H N 6-CF3-2-Pyn-201 4 CF 3 HN 6-CF 3 -2-Pyn
-202 4 CF3 H N 6-Cl-4-CF3-2-Pyn-202 4 CF 3 HN 6-Cl-4-CF 3 -2-Pyn
-203 4 CF3 H N 2-Pym-203 4 CF 3 HN 2-Pym
-204 4 CF3 H N 4-Pym -204 4 CF 3 HN 4-Pym
- 205 4 CF3 H N 4, 6-Me2-2-Pym-205 4 CF 3 HN 4, 6-Me 2 -2-Pym
-206 4 CF3 H N 4, 6- (OMe) 2 - 2_Pym -206 4 CF 3 HN 4, 6- (OMe) 2 - 2_Pym
-207 4 CF3 H N 3-Pyd-207 4 CF 3 HN 3-Pyd
-208 4 CF3 H N - CO -匪 e-208 4 CF 3 HN-CO-Marauder e
-209 4 CF3 H N - CO -匿 h-209 4 CF 3 HN-CO-Secret h
-210 4 CF3 H N - CO-丽 ePh-210 4 CF 3 HN-CO- 丽 ePh
-211 4 CF3 H N -CO-NEt (c - Hex)-211 4 CF 3 HN -CO-NEt (c-Hex)
-212 2 CHF2 H N Me-212 2 CHF 2 HN Me
-213 2 CHF2 H N t-Bu-213 2 CHF 2 HN t-Bu
-214 2 CHF2 H N - CH2- Ph-214 2 CHF 2 HN-CH 2 -Ph
-215 2 CHF2 H N -CHMe-Ph-215 2 CHF 2 HN -CHMe-Ph
-216 2 CHF2 H N-216 2 CHF 2 HN
-217 2 CHF2 H N Ph 114. 9-218 2 CHF2 H N 2- F - Ph-217 2 CHF 2 HN Ph 114. 9-218 2 CHF 2 HN 2-F-Ph
-219 2 CHF2 H N 2-Cl-Ph-219 2 CHF 2 HN 2-Cl-Ph
-220 2 CHF2 H N 3-Cl-Ph-220 2 CHF 2 HN 3-Cl-Ph
-221 2 CHF2 H N 4-Cl-Ph-221 2 CHF 2 HN 4-Cl-Ph
-222 2 CHF2 H N 2- Me- Ph-222 2 CHF 2 HN 2- Me- Ph
-223 2 CHF2 H N 2-i-Pr-Ph-223 2 CHF 2 HN 2-i-Pr-Ph
-224 2 CHF2 H N 2 - OMe - Ph-224 2 CHF 2 HN 2-OMe-Ph
-225 2 CHF2 H N 2-SMe-Ph-225 2 CHF 2 HN 2-SMe-Ph
-226 2 CHF2 H N 2-SOMe-Ph-226 2 CHF 2 HN 2-SOMe-Ph
-227 2 CHF2 H N 2- S02Me- Ph-227 2 CHF 2 HN 2- S0 2 Me- Ph
-228 2 CHF2 H N 2-CN-Ph-228 2 CHF 2 HN 2-CN-Ph
-229 2 CHF2 H N 2-N02-Ph
7表 (続き) -229 2 CHF 2 HN 2-N0 2 -Ph Table 7 (continued)
置換 Replace
X Rl3 X Rl3
No. R1 J4 物性-230 2 CHF2 H N -しト3 - iiNo. R 1 J 4 Physical properties -230 2 CHF 2 HN -Site 3 -ii
-231 2 CHF2 H N - 0しト3 -!-231 2 CHF 2 HN-0 to 3- !
-232 2 CHF2 H i - しト3 - - 233 2 CHF2 H N (JuF3 - Ph-232 2 CHF 2 H i - collected by 3 - - 233 2 CHF 2 HN (JuF 3 - Ph
-234 2 CHF2 H N 2 - S02CF3 - Ph-234 2 CHF 2 HN 2-S0 2 CF 3 -Ph
-235 2 CHF2 H N 2 C02Me - Ph-235 2 CHF 2 HN 2 C0 2 Me-Ph
-236 2 CHF2 H N 2 - Ph- Ph-236 2 CHF 2 HN 2-Ph- Ph
-237 2 CHF2 H N 2 - PhO— Ph-237 2 CHF 2 HN 2-PhO— Ph
-238 2 CHF2 H N 2, 6 - F2 - Ph-238 2 CHF 2 HN 2, 6-F 2 -Ph
-239 2 CHF2 H N 2, 6 - Cl2 - Ph-239 2 CHF 2 HN 2, 6-Cl 2 -Ph
-240 2 CHF2 H N 2, 6 - Me2 - Ph-240 2 CHF 2 HN 2, 6-Me 2 -Ph
-241 2 CHF2 H N 2, 6 - (OMe) 2- Ph-241 2 CHF 2 HN 2, 6-(OMe) 2 -Ph
-242 2 CHF2 H N 2, 6- (CF3) 2 Ph-242 2 CHF 2 HN 2, 6- (CF 3 ) 2 Ph
-243 2 CHF2 H N 2, 6 - (0CF3) 2 - Ph-243 2 CHF 2 HN 2, 6-(0CF 3 ) 2 -Ph
-244 2 CHF2 H N 2, 3, 4 - Cl3 - Ph-244 2 CHF 2 HN 2, 3, 4-Cl 3 -Ph
-245 2 CHF2 H N 2, 4, 6 - Cl3- Ph-245 2 CHF 2 HN 2, 4, 6-Cl 3 -Ph
-246 2 CHF2 H N 2, 6 - Cl2-4-CF3-Ph-246 2 CHF 2 HN 2, 6-Cl 2 -4-CF 3 -Ph
-247 2 CHF2 H N 2, 6 - Cl2 - 4 - 0CF3 - Ph -247 2 CHF 2 HN 2, 6 - Cl 2 - 4 - 0CF 3 - Ph
-248 2 CHF2 H N 2, 3, 4 - Me3- Ph-248 2 CHF 2 HN 2, 3, 4-Me 3 -Ph
-249 2 CHF2 H N 2-Pyn-249 2 CHF 2 HN 2-Pyn
-250 2 CHF2 H N 3-Pyn-250 2 CHF 2 HN 3-Pyn
-251 2 CHF2 H N 4-Pyn-251 2 CHF 2 HN 4-Pyn
-252 2 CHF2 H N 6 - CI - 2— Pyn -252 2 CHF 2 HN 6-CI-2— Pyn
- 253 2 CHF2 H N 6 - CF3 - 2- Pyn - 253 2 CHF 2 HN 6 - CF 3 - 2- Pyn
-254 2 CHF2 H N 6-Cl~4-CF -2-Pyn-254 2 CHF 2 HN 6-Cl ~ 4-CF -2-Pyn
-255 2 CHF2 H N 2 - Pym-255 2 CHF 2 HN 2-Pym
-256 2 CHF2 H N 4一 Pym-256 2 CHF 2 HN 4 1 Pym
-257 2 CHF2 H N 4, 6 - Me2 2— Pym-257 2 CHF 2 HN 4, 6-Me 2 2— Pym
-258 2 CHF2 H N 4, 6 -(OMe) 2-2- Pym-258 2 CHF 2 HN 4, 6-(OMe) 2 -2- Pym
-259 2 CHF2 H N 3-Pyd-259 2 CHF 2 HN 3-Pyd
-260 2 CHF2 H N -CO -顧 e-260 2 CHF 2 HN -CO -Customer e
-261 2 CHF2 H N - CO - NHPh-261 2 CHF 2 HN-CO-NHPh
-262 2 CHF2 H N - CO-醒 ePh-262 2 CHF 2 HN-CO-Awake ePh
Rl3Rl3
No. X J4 R9 物性 丄 Δ n u No. XJ 4 R 9 Physical properties 丄 Δ nu
し Π n Me Π Me n Me
u n u u n u
O Z Δ し Π n t-Bu O Z Δ Π n t-Bu
Q_Q Q_Q
O 0 Ζ n し n u n O 0 Ζ n then n u n
O ^ 厶 n し Π -CHMe-Ph O ^ m n Π CH -CHMe-Ph
u u
0 0 n し H n - CMe2 - Ph 0 0 n then H n-CMe 2 -Ph
O D 厶 n し u Π Ph O D m n shi u Π Ph
ru ru
o / 厶 し Π u n 2-F-Ph o / u n 2-F-Ph
o_o 0 o_o 0
o o ム u n ru o o m u n ru
し n u n 2-Cl-Ph N u n 2-Cl-Ph
0_Q 9 u n ru 0_Q 9 u n ru
し n n u 3 - CI - Ph N n u 3-CI-Ph
o_i 1 o_i 1
O 丄丄 0 r O 丄 丄 0 r
n しu n H n Z - Me -ド h n then u n H n Z-Me -do h
0_1 9 9 0_1 9 9
O 丄 ώ n し n n 2-i-Pr-Ph O 丄 ώ n then n n 2-i-Pr-Ph
Q-1 Q 9 Q-1 Q 9
O 丄 O 11 1 H 11 2-0Me-Ph O 丄 O 11 1 H 11 2-0Me-Ph
ϋ 丄 0 rw 11 2-SMe-Ph ϋ 丄 0 rw 11 2-SMe-Ph
ϋ ? H 1 H 2-SOMe-Ph ?? H 1 H 2-SOMe-Ph
ϋ 2 CH H 2-S02Me-Ph ϋ 2 CH H 2-S0 2 Me-Ph
8-17 2 H CH H 2-CN-Ph 8-17 2 H CH H 2-CN-Ph
8-18 2 H CH H 2-N02-Ph 8-18 2 H CH H 2-N0 2 -Ph
8 - 19 2 H CH H 2 - CF3 - Ph 8-19 2 H CH H 2-CF 3 -Ph
8-20 2 H CH H 2- 0CF3- Ph 8-20 2 H CH H 2- 0CF 3 -Ph
8-21 2 H CH H 2-SCF3-Ph 8-21 2 H CH H 2-SCF 3 -Ph
8-22 2 H CH H 2 - S0CF3- Ph 8-22 2 H CH H 2-S0CF 3 -Ph
8-23 2 H CH H 2-S02CF3-Ph 8-23 2 H CH H 2-S0 2 CF 3 -Ph
8-24 2 H CH H 2- C02Me- Ph 8-24 2 H CH H 2- C0 2 Me- Ph
8-25 2 H CH H 2 - Ph- Ph 8-25 2 H CH H 2-Ph- Ph
8-26 2 H CH H 2-PhO-Ph 8-26 2 H CH H 2-PhO-Ph
8-27 2 H CH H 2, 6_F2-Ph 8-27 2 H CH H 2, 6_F 2 -Ph
8-28 2 H CH H 2, 6- Cl2- Ph 8-28 2 H CH H 2, 6- Cl 2 -Ph
8-29 2 H CH H 2, 6- Me2-Ph 8-29 2 H CH H 2, 6- Me 2 -Ph
8 - 30 2 H CH H 2, 4, 6— Cl3- Ph 8-30 2 H CH H 2, 4, 6— Cl 3 -Ph
8 - 31 2 H CH H 2, 6- Cl2 - 4 - CF3 - Ph
表 (続き) o. X R13 R9 物性 置8-31 2 H CH H 2, 6- Cl 2-4- CF 3 -Ph Table (continued) o. XR 13 R 9 Physical properties
-32 2 H CH H 2, 6 - Cl2- 4 - 0CF3 - Ph -32 2 H CH H 2, 6 - Cl 2 - 4 - 0CF 3 - Ph
- 33 2 H CH H 2, 3, 4-Me3-Ph-33 2 H CH H 2, 3, 4-Me 3 -Ph
-34 2 H CH H 2- Pyn-34 2 H CH H 2- Pyn
-35 2 H CH H 3 - Pyn-35 2 H CH H 3-Pyn
-36 2 H CH H 4-Pyn-36 2 H CH H 4-Pyn
-37 2 H CH H 6-Cl-2-Pyn-37 2 H CH H 6-Cl-2-Pyn
-38 2 H CH H 6 - CF3 - 2 - Pyn-38 2 H CH H 6 - CF 3 - 2 - Pyn
-39 2 H CH H 6 - CI - 4- CF3- 2 - Pyn-39 2 H CH H 6 - CI - 4- CF 3 - 2 - Pyn
-40 2 H CH H 2-Pym-40 2 H CH H 2-Pym
-41 2 H CH H 4-Pym-41 2 H CH H 4-Pym
-42 2 H CH H 4, 6 - Me2— 2- Pym-42 2 H CH H 4, 6-Me 2 — 2- Pym
-43 2 H CH H 4, 6 - (OMe) 2-2-Pym-43 2 H CH H 4, 6-(OMe) 2 -2-Pym
-44 2 H CH H 3-Pyd-44 2 H CH H 3-Pyd
-45 2 H CH H -CO-NHMe-45 2 H CH H -CO-NHMe
-46 2 H CH H -CO-NHPh-46 2 H CH H -CO-NHPh
-47 2 H CH H - CO- O應 ePh-47 2 H CH H-CO-O ePh
-48 2 H CH H -CO-NEt (c - Hex)-48 2 H CH H -CO-NEt (c-Hex)
-49 2 H CH Me Me-49 2 H CH Me Me
-50 2 H CH Me t-Bu-50 2 H CH Me t-Bu
-51 2 H CH Me - CH2 - Ph-51 2 H CH Me-CH 2 -Ph
-52 2 H CH Me -CHMe-Ph-52 2 H CH Me -CHMe-Ph
-54 2 H CH Me Ph-54 2 H CH Me Ph
-55 2 H CH Me 2-F-Ph-55 2 H CH Me 2-F-Ph
-56 2 H CH Me 2- CI- Ph 105-106-57 2 H CH Me 3-Cl-Ph-56 2 H CH Me 2- CI- Ph 105-106-57 2 H CH Me 3-Cl-Ph
-58 2 H CH Me 4- CI- Ph-58 2 H CH Me 4- CI- Ph
-59 2 H CH Me 2 - Me- Ph-59 2 H CH Me 2-Me- Ph
-60 2 H CH Me 2-i-Pr-Ph-60 2 H CH Me 2-i-Pr-Ph
-61 2 H CH Me 2- OMe- Ph-61 2 H CH Me 2- OMe- Ph
-62 2 H CH Me 2-SMe-Ph-62 2 H CH Me 2-SMe-Ph
-63 2 H CH Me 2-SOMe-Ph-63 2 H CH Me 2-SOMe-Ph
-64 2 H CH Me 2- S02Me - Ph -64 2 H CH Me 2- S0 2 Me-Ph
- 65 2 H CH Me 2-CN-Ph-65 2 H CH Me 2-CN-Ph
-66 2 H CH Me-66 2 H CH Me
-67 2 H CH Me 2 - CF3- Ph-67 2 H CH Me 2-CF 3 -Ph
-68 2 H CH Me 2- 0CF3- Ph-68 2 H CH Me 2- 0CF 3 -Ph
-69 2 H CH Me 2 - SCF3- Ph-69 2 H CH Me 2-SCF 3 -Ph
-70 2 H CH Me 2-S0CF3-Ph-70 2 H CH Me 2-S0CF 3 -Ph
-71 2 H CH Me 2 - S02CF3 - Ph
8表 (続き) -71 2 H CH Me 2-S0 2 CF 3 -Ph Table 8 (continued)
置換 Replace
No σ. X J1 R13 R9 物性 置No σ. XJ 1 R 13 R 9
-72 2 H CH Me 2-C02Me-Ph-72 2 H CH Me 2-C0 2 Me-Ph
-73 2 H CH Me 2- Ph - Ph -73 2 H CH Me 2- Ph-Ph
-74 2 H CH Me 2-PhO-Ph -74 2 H CH Me 2-PhO-Ph
- 75 2 H CH Me 2, 6- F2_Ph-75 2 H CH Me 2, 6- F 2 _Ph
-76 2 H CH Me 2, 6 - Cl2 - Ph-76 2 H CH Me 2, 6-Cl 2 -Ph
-77 2 H CH Me 2, 6 - Me2 - Ph -77 2 H CH Me 2, 6-Me 2 -Ph
- 78 2 H CH Me 2, 4, 6 - Cl3- Ph -78 2 H CH Me 2, 4, 6-Cl 3 -Ph
- 79 2 H CH Me 2, 6 - C12_4_CF3 - Ph -79 2 H CH Me 2, 6-C1 2 _4_CF 3 -Ph
- 80 2 H CH Me 2, 6 - Cl2- 4- 0CF3- Ph - 80 2 H CH Me 2, 6 - Cl 2 - 4- 0CF 3 - Ph
- 81 2 H CH Me 2, 3, 4— Me3 - Ph-81 2 H CH Me 2, 3, 4—Me 3 -Ph
-82 2 H CH Me 2-Pyn -82 2 H CH Me 2-Pyn
- 83 2 H CH Me 3-Pyn -83 2 H CH Me 3-Pyn
-84 2 H CH Me 4-Pyn -84 2 H CH Me 4-Pyn
-85 2 H CH Me 6- Cト 2-Pyn -85 2 H CH Me 6- C G 2-Pyn
-86 2 H CH Me 6 - CF3- 2-Pyn-86 2 H CH Me 6 - CF 3 - 2-Pyn
-87 2 H CH Me 6-Cl- 。4-CF3-2-Pyn -87 2 H CH Me 6-Cl-. 4-CF 3 -2-Pyn
a a
88 2 H CH Me 2-Pym 88 2 H CH Me 2-Pym
-o -o
-89 2 H CH Me 4-Pym -89 2 H CH Me 4-Pym
- 90 2 H CH Me 4, 6- Me2- 2— Pym - 90 2 H CH Me 4, 6- Me 2 - 2- Pym
- 91 2 H CH Me 4, 6- (0Me) 2 - 2- Pym- 91 2 H CH Me 4, 6- (0Me) 2 - 2- Pym
-92 2 H CH Me 3-Pyd -92 2 H CH Me 3-Pyd
-93 2 H CH Me -CO-NHMe -93 2 H CH Me -CO-NHMe
-94 2 H CH Me -C0-NHPh -94 2 H CH Me -C0-NHPh
-95 2 H CH Me - CO-NMePh -95 2 H CH Me-CO-NMePh
- 96 2 H CH Me -C0-NEt (c-Hex) -96 2 H CH Me -C0-NEt (c-Hex)
-97 2 H N Me Me -97 2 H N Me Me
-98 2 H N Me t-Bu -98 2 H N Me t-Bu
-99 2 H N Me -99 2 H N Me
-100 2 H N Me -CHMe-Ph-100 2 H N Me -CHMe-Ph
-101 2 H N Me-101 2 H N Me
-102 2 H N Me Ph-102 2 H N Me Ph
-103 2 H N Me 2-F-Ph-103 2 H N Me 2-F-Ph
-104 2 H N Me 2 - CI- Ph-104 2 H N Me 2-CI- Ph
-105 2 H N Me 3-Cl-Ph -105 2 H N Me 3-Cl-Ph
2 H N Me 4-Cl-Ph 2 H N Me 4-Cl-Ph
-107 2 H N Me 2-Me-Ph-107 2 H N Me 2-Me-Ph
-108 2 H N Me 2-i-Pr-Ph-108 2 H N Me 2-i-Pr-Ph
-109 2 H N Me 2-OMe-Ph-109 2 H N Me 2-OMe-Ph
-110 2 H N Me 2-SMe-Ph -110 2 H N Me 2-SMe-Ph
- 111 2 H N Me 2-SOMe-Ph
8表 (続き) -111 2 HN Me 2-SOMe-Ph Table 8 (continued)
隊 ί央 隊 ί
No. X J" R13 R9 物性 d 丄丄 Z z n IN Me 2- S02Me - Ph No. XJ "R 13 R 9 properties d丄丄Z zn IN Me 2- S0 2 Me - Ph
Q Q Q Q
8 丄丄 3 z n u IN Me 2-CN-Ph 8 丄 丄 3 z n u IN Me 2-CN-Ph
Q Q
8 丄丄 4 厶 n IN Me 8 丄 丄 4 m n IN Me
8—丄丄 b o 8— 丄 丄 b o
8 丄 Z Π IN Me 2_0CF3 - Ph 8 丄 Z Π IN Me 2_0CF 3 -Ph
8 丄丄 / Δ o 8 丄 丄 / Δ o
o o o o o o
n I Me 2-SOCFg-Ph n I Me 2-SOCFg-Ph
8—丄 i ny Δ Π N Me 2_S02CF3 - Ph 8— 丄 iny Δ Π N Me 2_S0 2 CF 3 -Ph
o Π IN Me 2-C02Me- Ph o Π IN Me 2-C0 2 Me- Ph
Z H IN Me 2 - Ph-Ph Z H IN Me 2-Ph-Ph
8 -丄 Π N Me 2-PhO-Ph 8-丄 Π N Me 2-PhO-Ph
IN Me 2, 6-F2-Ph IN Me 2, 6-F 2 -Ph
8 -丄 4 厶 n IN Me 2, 6_C12 - Ph 8-丄 4 m n IN Me 2, 6_C1 2 -Ph
o o
o-l o J Me 2, 6-Me2-Ph ol o J Me 2, 6-Me 2 -Ph
8—丄 t) n Me 2, 4, 6— Cl3— Ph 8— 丄 t) n Me 2, 4, 6—Cl 3 — Ph
リ Re
~lZ / H M Me 2, 6-Cl2-4-CF3-Ph ~ lZ / HM Me 2, 6-Cl 2 -4-CF 3 -Ph
8 -丄^ o IN Me 2, 6 - Cl2 - 4- 0CF3- Ph o—丄 on 厶 n JN Me 2, 3, 4— Me3— Ph8 -丄^ o IN Me 2, 6 - Cl 2 - 4- 0CF 3 - Ph o-丄on厶n JN Me 2, 3, 4- Me 3 - Ph
8 -丄 oinU n Me 2- Pyn 8-丄 oinU n Me 2- Pyn
8—丄 3丄 Δ n IN Me 3- Pyn 8— 丄 3 丄 Δ n IN Me 3- Pyn
n IN Me 4 - Pyn n IN Me 4-Pyn
8 丄 Z n IN Me 6 - Cト 2 - Pyn 8 丄 Z n IN Me 6-C to 2-Pyn
Q Q
Z n I Me 6 - CF3- 2- Pyn Z n I Me 6 - CF 3 - 2- Pyn
Q o Q o
n IN Me 6-Cl-4-CF3-2-Pyn o u Π I Me 2 - Pym n IN Me 6-Cl-4-CF 3 -2-Pyn ou Π I Me 2-Pym
8—丄 0 厶 Π IN Me 4-Pym 8— 丄 0 Π Π IN Me 4-Pym
Q QQ Q QQ
Δ n IN Me 4, 6-Me2_2 - PymΔ n IN Me 4, 6-Me 2 _2-Pym
8 丄 Z Π I Me 4, 6- (OMe) 2-2- Pym8 丄 Z Π I Me 4, 6- (OMe) 2 -2- Pym
Q 1 Λ o u Q 1 Λ o u
o 丄 4 A U Π IN Me 3-Pyd o 丄 4 A U Π IN Me 3-Pyd
o Q— 1丄 A 11 z Π IN Me -C0-NHMe o Q— 1 丄 A 11 z Π IN Me -C0-NHMe
Q Q Q Q
o 1 z Π IN Me -CO-NHPh o 1 z Π IN Me -CO-NHPh
z Π IN Me -CO- NMePh z Π IN Me -CO- NMePh
Q_-| Q_- |
o 丄 4 Z n IN M Me -CO-NEt (c-Hex) o 丄 4 Z n IN M Me -CO-NEt (c-Hex)
8-145 4 H CH H Me 8-145 4 H CH H Me
8-146 4 H CH H t-Bu 8-146 4 H CH H t-Bu
8-147 4 . H CH H 8-147 4. H CH H
8-148 4 H CH H -CHMe-Ph 8-148 4 H CH H -CHMe-Ph
8-149 4 H CH H - CMe2- Ph 8-149 4 H CH H-CMe 2 -Ph
8-150 4 H CH H Ph 8-150 4 H CH H Ph
8-151 4 H CH H 2- CI - Ph
8表 (続き) 8-151 4 H CH H 2- CI-Ph Table 8 (continued)
MM MM
No. X J1 R13 R9 物性 置No. XJ 1 R 13 R 9 Physical properties
-152 4 Η CH Η 2— Me - Ph-152 4 Η CH Η 2— Me-Ph
-153 4 Η CH Η 3- Me - Ph-153 4 Η CH Η 3- Me-Ph
-154 4 Η CH Η 4一 Me - Ph-154 4 Η CH Η 4 ichi Me-Ph
-155 4 Η CH Η 2-OMe-Ph-155 4 Η CH Η 2-OMe-Ph
-156 4 Η CH Η 2-CN-Ph-156 4 Η CH Η 2-CN-Ph
-157 4 Η CH Η 2-N02-Ph-157 4 Η CH Η 2-N0 2 -Ph
-158 4 Η CH Η 2 - CF3 - Ph-158 4 Η CH Η 2-CF 3 -Ph
-160 4 Η CH Η 2 - C02Me - Ph-160 4 Η CH Η 2-C0 2 Me-Ph
-161 4 Η CH Η 2 - Ph- Ph-161 4 Η CH Η 2-Ph- Ph
-162 4 Η CH Η 2-PhO-Ph-162 4 Η CH Η 2-PhO-Ph
-163 4 Η CH Η 2, 6 - Cl2 - Ph-163 4 Η CH Η 2, 6-Cl 2 -Ph
-164 4 Η CH Η 2, 6- Me2_Ph-164 4 Η CH Η 2, 6- Me 2 _Ph
-165 4 Η CH Η 2, 4, 6- Cl3- Ph-165 4 Η CH Η 2, 4, 6- Cl 3 -Ph
-166 4 Η CH Η 2, 3, 4- Me3 - Ph-166 4 Η CH Η 2, 3, 4-Me 3 -Ph
-167 4 Η CH Η 2-Pyn-167 4 Η CH Η 2-Pyn
-168 4 Η CH Η 3-Pyn-168 4 Η CH Η 3-Pyn
-169 4 Η CH Η 4-Pyn-169 4 Η CH Η 4-Pyn
-170 4 Η CH Η 2- Pym-170 4 Η CH Η 2- Pym
-171 4 Η CH Η 4一 Pym-171 4 Η CH Η 4 ichi Pym
-172 4 Η CH Η 4, 6—Me2 - 2 - Pym-172 4 Η CH Η 4, 6 -Me 2 - 2 - Pym
-173 4 Η CH Η 4, 6- (0Me) 2— 2 - Pym-173 4 Η CH Η 4, 6- (0Me) 2 — 2-Pym
-174 4 Η CH Η 3-Pyd
-174 4 Η CH Η 3-Pyd
ハ 1 ハ、 C 1 c,
( -CF3, R -H m= 0、 A=— CH2_、 G -G -0) (-CF 3 , R -H m = 0, A = — CH 2 _, G -G -0)
置換 Replace
INU. Λ Y J Rl3 丄\ INU. Λ Y J Rl3 丄 \
位置 Position
9-1 2 H CH H Me 9-1 2 H CH H Me
9-2 2 H CH H t-Bu9-2 2 H CH H t-Bu
9-3 2 H CH H - CH2 - Ph9-3 2 H CH H-CH 2 -Ph
9-4 2 H CH H -CHMe-Ph9-4 2 H CH H -CHMe-Ph
9-5 2 H CH H - CMe2- Ph9-5 2 H CH H-CMe 2 -Ph
9-6 2 H CH H Ph9-6 2 H CH H Ph
9-7 2 H CH H 2-F-Ph9-7 2 H CH H 2-F-Ph
9-8 2 H CH H 2- CI- Ph9-8 2 H CH H 2- CI- Ph
9-9 2 H CH H 3 - CI- Ph -10 2 H CH H 4-Cl-Ph -11 2 H CH H 2 - Me- Ph -12 2 H CH H 2-i-Pr-Ph -13 2 H CH H 2-OMe-Ph -14 2 H CH H 2-SMe-Ph -15 2 H CH H 2-SOMe-Ph -16 2 H CH H 2-S02Me-Ph -17 2 H CH H 2-CN-Ph -18 2 H CH H 2-N02-Ph - 19 2 H CH H 2- CF3- Ph -20 2 H CH H 2-0CF3-Ph -21 2 H CH H 2-SCF3-Ph -22 2 H CH H 2- SOCF3_Ph -23 2 H CH H 2- S02CF3- Ph -24 2 H CH H 2- C02Me- Ph -25 2 H CH H 2- Ph- Ph -26 2 H CH H 2-PhO-Ph -27 2 H CH H 2, 6- F2- Ph -28 2 H CH H 2, 6—Cl2 - Ph -29 2 H CH H 2, 6 - Me2- Ph -30 2 H CH H 2, 4, 6- Cl3-Ph -31 2 H CH H 2, 6- Cl2 - 4 - CF3_Ph -32 2 H CH H 2, 6-Cl2-4-0CF3-Ph
9表 (続き) 9-9 2 H CH H 3-CI- Ph -10 2 H CH H 4-Cl-Ph -11 2 H CH H 2-Me- Ph -12 2 H CH H 2-i-Pr-Ph -13 2 H CH H 2-OMe-Ph -14 2 H CH H 2-SMe-Ph -15 2 H CH H 2-SOMe-Ph -16 2 H CH H 2-S0 2 Me-Ph -17 2 H CH H 2 -CN-Ph -18 2 H CH H 2-N0 2 -Ph-19 2 H CH H 2-CF 3 -Ph -20 2 H CH H 2-0CF 3 -Ph -21 2 H CH H 2-SCF 3 -Ph -22 2 H CH H 2- SOCF 3 _Ph -23 2 H CH H 2- S0 2 CF 3 - Ph -24 2 H CH H 2- C0 2 Me- Ph -25 2 H CH H 2- Ph- Ph -26 2 H CH H 2-PhO-Ph -27 2 H CH H 2,6-F 2 -Ph -28 2 H CH H 2,6-Cl 2 -Ph -29 2 H CH H 2, 6- Me 2 -Ph -30 2 H CH H 2, 4, 6-Cl 3 -Ph -31 2 H CH H 2, 6, 6 Cl 2-4- CF 3 _Ph -32 2 H CH H 2, 6-Cl 2 -4-0CF 3 -Ph Table 9 (continued)
置換 Replace
o. X J1 R13 R9 物性 位置o. XJ 1 R 13 R 9 Physical properties Location
-33 2 H CH H 2, 3, 4— Me3 - Ph-33 2 H CH H 2, 3, 4—Me 3 -Ph
-34 2 H CH H 2 - Pyn-34 2 H CH H 2-Pyn
-35 2 H CH H 3- Pyn -35 2 H CH H 3- Pyn
- 36 2 H CH H 4 - Pyn-36 2 H CH H 4-Pyn
-37 2 H CH H 6-C1- 2 - Pyn-37 2 H CH H 6-C1-2-Pyn
-38 2 H CH H 6 - CF3- 2 - Pyn-38 2 H CH H 6 - CF 3 - 2 - Pyn
-39 2 H CH H 6-Cl-4-CF3-2-Pyn-39 2 H CH H 6-Cl-4-CF 3 -2-Pyn
-40 2 H CH H 2- Pym -40 2 H CH H 2- Pym
- 41 2 H CH H 4 - Pym-41 2 H CH H 4-Pym
-42 2 H CH H 4, 6- Me2- 2- Pym-42 2 H CH H 4, 6- Me 2 - 2- Pym
-43 2 H CH H 4, 6- (OMe) 2 - 2- Pym-43 2 H CH H 4, 6- (OMe) 2 - 2- Pym
-44 2 H CH H 3-Pyd-44 2 H CH H 3-Pyd
-45 2 H CH H - CO -画 e-45 2 H CH H-CO -Image e
-46 2 H CH H -CO-NHPh-46 2 H CH H -CO-NHPh
-47 2 H CH H -CO-匪 ePh-47 2 H CH H -CO- Marauder ePh
-48 2 H CH H -CO-NEt (c-Hex)-48 2 H CH H -CO-NEt (c-Hex)
-49 2 H CH Me Me-49 2 H CH Me Me
-50 2 H CH Me t-Bu-50 2 H CH Me t-Bu
-51 2 H CH Me-51 2 H CH Me
-52 2 H CH Me -CHMe-Ph-52 2 H CH Me -CHMe-Ph
-53 2 H CH Me-53 2 H CH Me
-54 2 H CH Me Ph-54 2 H CH Me Ph
-55 2 H CH Me 2-F-Ph-55 2 H CH Me 2-F-Ph
-56 2 H CH Me 2 - Cl-Ph 166-167-57 2 H CH Me 3-Cl-Ph-56 2 H CH Me 2-Cl-Ph 166-167-57 2 H CH Me 3-Cl-Ph
-58 2 H CH Me 4 - CI - Ph-58 2 H CH Me 4-CI-Ph
-59 2 H CH Me 2- Me- Ph-59 2 H CH Me 2- Me- Ph
-60 2 H CH Me 2-i-Pr-Ph-60 2 H CH Me 2-i-Pr-Ph
-61 2 H CH Me 2-OMe-Ph-61 2 H CH Me 2-OMe-Ph
-62 2 H CH Me 2-SMe-Ph-62 2 H CH Me 2-SMe-Ph
-63 2 H CH Me 2-SOMe-Ph-63 2 H CH Me 2-SOMe-Ph
-64 2 H CH Me 2-S02Me-Ph-64 2 H CH Me 2-S0 2 Me-Ph
-65 2 H CH Me 2-CN-Ph-65 2 H CH Me 2-CN-Ph
-66 2 H CH Me 2- N02 - Ph-66 2 H CH Me 2- N0 2 -Ph
-67 2 H CH Me 2- CF3- Ph-67 2 H CH Me 2- CF 3 -Ph
-68 2 H CH Me 2 - 0CF3 - Ph-68 2 H CH Me 2-0CF 3 -Ph
-69 2 H CH Me 2 - SCF3 - Ph-69 2 H CH Me 2-SCF 3 -Ph
-70 2 H CH Me 2 - S0CF3 - Ph-70 2 H CH Me 2-S0CF 3 -Ph
-71 2 H CH Me 2 - S02CF3- Ph-71 2 H CH Me 2-S0 2 CF 3 -Ph
-72 2 H CH Me 2- C02Me - Ph
9表 (続き) -72 2 H CH Me 2- C0 2 Me-Ph Table 9 (continued)
置換 Replace
No. X J" R13 R9 物性 o No. XJ "R 13 R 9 Physical properties o
Δ H し H Me -rn- - 74 L H し H Me Z-rnU-rn Δ H then H Me -rn--74 L H then H Me Z-rnU-rn
—75 し H Me Z} —75 then H Me Z }
o o
-76 I H し H Me 3 b—し丄 2— -76 IH and H Me 3 b- and丄2 -
o o
- 77 H OH Me , b - Me2 -! -77 H OH Me, b-Me 2- !
- 78 Δ H CH Me , 4 b—し丄 3— -78 Δ H CH Me, 4 b— 丄3 —
- 79 2 H CH Me 6 - C丄 4 CF3— Ph-79 2 H CH Me 6-C 丄 4 CF 3 — Ph
- 81 2 H CH Me 2 3 4 - Me3 - Ph-81 2 H CH Me 2 3 4-Me 3 -Ph
-82 2 H CH Me -ryn -82 2 H CH Me -ryn
- 83 2 H CH Me 3 - Pyn -83 2 H CH Me 3-Pyn
-84 2 H CH Me 4一 Pyn -84 2 H CH Me 4 ichi Pyn
- 85 2 H CH Me 6 - CI— 2 Pyn -85 2 H CH Me 6-CI— 2 Pyn
-86 2 H CH Me 6 - CF3 - 2 - Pyn-86 2 H CH Me 6 - CF 3 - 2 - Pyn
-87 2 H CH Me 6 - CI- 4 - CF3 - 2 - Pyn-87 2 H CH Me 6 - CI- 4 - CF 3 - 2 - Pyn
-88 2 H CH Me 2-Pym -88 2 H CH Me 2-Pym
-89 2 H CH Me 4-Pym -89 2 H CH Me 4-Pym
-90 2 H CH Me 4 6— Me2 2— Pym-90 2 H CH Me 4 6— Me 2 2— Pym
-91 2 H CH Me 4, 6- (OMe) 2 - 2 - Pym-91 2 H CH Me 4, 6- (OMe) 2 - 2 - Pym
-92 2 H CH Me 3-Pyd -92 2 H CH Me 3-Pyd
- 93 2 H CH Me - CO - NHMe -93 2 H CH Me-CO-NHMe
-94 2 H CH Me 一 CO— NHPh -94 2 H CH Me one CO— NHPh
-95 2 H CH Me — CO - NMePh -95 2 H CH Me — CO-NMePh
- 96 2 H CH Me — CONEt (c-HexヽJ -96 2 H CH Me — CONEt (c-Hex ヽ J
- 97 2 H N Me Me -97 2 H N Me Me
一 98 2 H N Me t - Bu One 98 2 H N Me t-Bu
- 99 2 H N Me 一 CH2 - Ph-99 2 HN Me one CH 2 -Ph
-100 H N e 一し HMe— h -100 H Ne e HMe— h
-皿 Δ H N Me 一し Me2 - 一 o -Dish Δ HN Me One Me 2 -One o
102 H N Me rh 102 H N Me rh
一 103 H N Me o r r> One 103 H N Me o r r>
^if -_1 U H N m zi—し丄ー ^ if- _ 1 UHN m zi
丄 (Jb Z n I Me 3—し丄ー 丄 (Jb Z n I Me 3
- 106 H N Me 4_し丄ー Ph-106 H N Me 4_Shu Ph
-107 2 H N Me 2- Me - Ph-107 2 H N Me 2- Me-Ph
-108 2 H N Me 2 - i- Pr - Ph-108 2 H N Me 2-i- Pr-Ph
-109 2 H N Me 2 - OMe Ph-109 2 H N Me 2-OMe Ph
-110 2 H N Me 2-SMe-Ph-110 2 H N Me 2-SMe-Ph
-111 2 H N Me 2 - SOMe - Ph-111 2 H N Me 2-SOMe-Ph
-112 2 H N Me 2-S02Me-Ph
9表 (続き) -112 2 HN Me 2-S0 2 Me-Ph Table 9 (continued)
雷換 Thunderstorm
No. X J4 R13 R9 物性 置No. XJ 4 R 13 R 9 Physical properties
-113 2 H N Me 2 - CN - Ph-113 2 H N Me 2-CN-Ph
-114 2 H N Me 2 - N02 - Ph-114 2 HN Me 2-N0 2 -Ph
-115 2 H N Me 2 - CF3 - Ph-115 2 HN Me 2-CF 3 -Ph
-116 2 H N Me 2 - 0CF3 - Ph-116 2 HN Me 2-0CF 3 -Ph
-117 2 H N Me 2 - SCF3 - Ph-117 2 HN Me 2-SCF 3 -Ph
-118 2 H N Me 2-S0CF3-Ph-118 2 HN Me 2-S0CF 3 -Ph
-119 2 H N Me 2-S02CF3-Ph-119 2 HN Me 2-S0 2 CF 3 -Ph
-121 2 H N Me 2 - Ph - Ph-121 2 H N Me 2-Ph-Ph
-122 2 H N Me 2-PhO-Ph-122 2 H N Me 2-PhO-Ph
-123 2 H N Me 2, 6-F2-Ph-123 2 HN Me 2, 6-F 2 -Ph
-124 2 H N Me 2, 6-Cl2-Ph-124 2 HN Me 2, 6-Cl 2 -Ph
-125 2 H N Me 2, 6_Me2- Ph-125 2 HN Me 2, 6_Me 2 -Ph
-126 2 H N Me 2, 4, 6 - Cl3-Ph-126 2 HN Me 2, 4, 6-Cl 3 -Ph
-127 2 H N Me 2, 6 - Cl2 - 4 - CF3 - Ph-127 2 HN Me 2, 6-Cl 2-4- CF 3 -Ph
-128 2 H N Me 2, 6-Cl2-4-0CF3-Ph-128 2 HN Me 2, 6-Cl 2 -4-0CF 3 -Ph
-129 2 H N Me 2, 3, 4 - Me3 - Ph-129 2 HN Me 2, 3, 4-Me 3 -Ph
-130 2 H N Me 2 - Pyn -130 2 H N Me 2-Pyn
- 131 2 H N Me 3 - Pyn -131 2 H N Me 3-Pyn
- 132 2 H N Me 4-Pyn -132 2 H N Me 4-Pyn
- 133 2 H N Me 6 - CI - 2 - Pyn-133 2 H N Me 6-CI-2-Pyn
-134 2 H N Me 6 - CF3 - 2 - Pyn -134 2 HN Me 6 - CF 3 - 2 - Pyn
-135 2 H N Me 6-Cl-4-CF3-2-Pyn-135 2 HN Me 6-Cl-4-CF 3 -2-Pyn
-136 2 H N Me 2 - Pym-136 2 H N Me 2-Pym
-137 2 H N Me 4— Pym-137 2 H N Me 4— Pym
-138 2 H N Me 4, 6 - Me2 - 2 - Pym-138 2 HN Me 4, 6 - Me 2 - 2 - Pym
-139 2 H N Me 4, 6 - (0Me) 2- 2 - Pym-139 2 HN Me 4, 6 - (0Me) 2 - 2 - Pym
-140 2 H N Me 3-Pyd-140 2 H N Me 3-Pyd
-141 2 H N Me - CO - NHMe-141 2 H N Me-CO-NHMe
-142 2 H N Me - CO - NHPh-142 2 H N Me-CO-NHPh
-143 2 H N Me - CO - NMePh-143 2 H N Me-CO-NMePh
-144 2 H N Me -C0-NEt (c-Hex)-144 2 H N Me -C0-NEt (c-Hex)
-145 4 H Ch H Me-145 4 H Ch H Me
-146 4 H CH H t-Bu-146 4 H CH H t-Bu
-147 4 H CH H - C Ph-147 4 H CH H-C Ph
-148 4 H CH H -CHMe-Ph-148 4 H CH H -CHMe-Ph
-149 4 H CH H -CMe2 - Ph-149 4 H CH H -CMe 2 -Ph
-150 4 H CH H Ph-150 4 H CH H Ph
-151 4 H CH H 2 - CI - Ph -151 4 H CH H 2-CI-Ph
一 152 4 H CH H 2— Me— Ph
9表 (続き) One 152 4 H CH H 2— Me— Ph Table 9 (continued)
置換 Replace
No. X J1 R13 R9 物性-153 4 H CH H 2-OMe-PhNo. XJ 1 R 13 R 9 Physical properties -153 4 H CH H 2-OMe-Ph
-154 4 H CH H 2-CN-Ph-154 4 H CH H 2-CN-Ph
-155 4 H CH H 2-N02-Ph-155 4 H CH H 2-N0 2 -Ph
-156 4 H CH H 2- CF3 - Ph-156 4 H CH H 2- CF 3 -Ph
-157 4 H CH H 2 - 0CF3 - Ph-157 4 H CH H 2-0CF 3 -Ph
-158 4 H CH H 2-C02Me-Ph-158 4 H CH H 2-C0 2 Me-Ph
-159 4 H CH H 2 - Ph - Ph-159 4 H CH H 2-Ph-Ph
-160 4 H CH H 2-PhO-Ph-160 4 H CH H 2-PhO-Ph
-161 4 H CH H 2, 6-Cl2-Ph-161 4 H CH H 2, 6-Cl 2 -Ph
-162 4 H CH H 2, 6— Me2 - Ph-162 4 H CH H 2, 6— Me 2 -Ph
-163 4 H CH H 2, 4, 6 - Cl3- Ph-163 4 H CH H 2, 4, 6-Cl 3 -Ph
-164 4 H CH H 2, 3, 4-Me3-Ph-164 4 H CH H 2, 3, 4-Me 3 -Ph
-165 4 H CH H 2-Pyn-165 4 H CH H 2-Pyn
-166 4 H CH H 3-Pyn-166 4 H CH H 3-Pyn
-167 4 H CH H 4-Pyn-167 4 H CH H 4-Pyn
-168 4 H CH H 2-Pym-168 4 H CH H 2-Pym
-169 4 H CH H 4-Pym-169 4 H CH H 4-Pym
-170 4 H CH H 4, 6- Me2- 2- Pym-170 4 H CH H 4, 6- Me 2 - 2- Pym
-171 4 H CH H 4, 6- (0Me) 2-2- Pym-171 4 H CH H 4, 6- (0Me) 2 -2- Pym
-172 4 H CH H 3-Pyd
-172 4 H CH H 3-Pyd
一般式 (I一 9 ) General formula (I-1 9)
0表 (m= 0、 A=— CH2—) Table 0 (m = 0, A = — CH 2 —)
life: 性 life: gender
No. R1 R2 X Rl3 物 No. R 1 R 2 X Rl3
J4 J5 J 4 J 5
置 [融点 (°C)、屈折: (Melting point (° C), refraction:
10 - 1 2 CF, H H CH CH Ph 251-25210-1 2 CF, H H CH CH Ph 251-252
10 - 2 2 CF, H H N CH Ph NMR-710-22 CF, H H N CH Ph NMR-7
10-3 2 CF, H H N N Me 10-3 2 CF, H H N N Me
10-4 2 CF, H H N N t-Bu 10-4 2 CF, H H N N t-Bu
10-5 2 CF, H H N N 10-5 2 CF, H H N N
10-6 2 CF, H H N N -CHMe-Ph 10-6 2 CF, H H N N -CHMe-Ph
10 - 7 2 CF, H H N N 一 CMe2 - Ph 10-7 2 CF, HHNN one CMe 2 -Ph
10 - 8 2 CF, H H N N Ph 119-120 10-8 2 CF, H H N N Ph 119-120
10 - 9 2 CF, H H N N 2-F-Ph 10-9 2 CF, H H N N 2-F-Ph
10-10 2 CF, H H N N 3-F-Ph 10-10 2 CF, H H N N 3-F-Ph
10 - 11 2 CF3 H H N N 4-F-Ph 10-11 2 CF 3 HHNN 4-F-Ph
10-12 2 CF3 H H N N 2- CI - Ph 1. 5581 (26。C)10-12 2 CF 3 HHNN 2- CI-Ph 1.5581 (26.C)
10-13 2 CF, H H N N 3-Cl-Ph 1. 5490 (26°C)10-13 2 CF, H H N N 3-Cl-Ph 1.5490 (26 ° C)
10-17 2 CF3 H H N N 4-Me-Ph 98-9910-17 2 CF 3 HHNN 4-Me-Ph 98-99
10-18 2 CF3 H H N N 2-0Me-Ph 124-12510-18 2 CF 3 HHNN 2-0Me-Ph 124-125
10-19 2 CF3 H H N N 3-0Me-Ph 122-12310-19 2 CF 3 HHNN 3-0Me-Ph 122-123
10-20 2 CF3 H H N N 4-OMe-Ph 100-10110-20 2 CF 3 HHNN 4-OMe-Ph 100-101
10-21 2 CF3 H H N N 2-SMe-Ph 90-9110-21 2 CF 3 HHNN 2-SMe-Ph 90-91
10-22 2 CF3 H H N N 3-SMe- Ph 10-22 2 CF 3 HHNN 3-SMe- Ph
10-23 2 CF3 H H N N 4-SMe-Ph 104-10510-23 2 CF 3 HHNN 4-SMe-Ph 104-105
10-24 2 CF3 H H N N 2-SOMe-Ph 176-17810-24 2 CF 3 HHNN 2-SOMe-Ph 176-178
10-25 2 CF3 H H N N 3- S0Me-Ph 10-25 2 CF 3 HHNN 3- S0Me-Ph
10-26 2 CF3 H H N N 4-SOMe-Ph 162-16510-26 2 CF 3 HHNN 4-SOMe-Ph 162-165
10-27 2 CF3 H H N N 2-CN-Ph 10-27 2 CF 3 HHNN 2-CN-Ph
10-28 2 CF3 H H N N 2 - N02-Ph 111-11210-28 2 CF 3 HHNN 2-N0 2 -Ph 111-112
10-29 2 CF3 H H N N 2-CF3-Ph 123-12410-29 2 CF 3 HHNN 2-CF 3 -Ph 123-124
10-30 2 CF3 H H N N 2 - 0CF3- Ph 10-30 2 CF 3 HHNN 2-0CF 3 -Ph
10-31 2 CF3 H H N N 2 - SCF3-Ph 10-31 2 CF 3 HHNN 2-SCF 3 -Ph
10-32 2 CF3 H H N N 2-S0CF3-Ph
10表 (続き) 10-32 2 CF 3 HHNN 2-S0CF 3 -Ph Table 10 (continued)
No. R1 R2 X J1 J5 R13 No. R 1 R 2 XJ 1 J 5 R 13
し kJ Aヽ V ^ノ、ノ ίϋ ^^」 o u KJ A ヽ V ^ no, no ^ ^ ^ "o u
丄 U Δ u 丄 U Δ u
し Π n IN I Δ し Γ 3 ΓΙ1 Π n IN I Δ Γ Γ 3 ΓΙ1
丄 o u u 丄 o u u
し n n IN IN F十一 Ph 上. Δ Δしノ o u u Shi n n IN IN F eleven Ph. Δ Δ shi no o u u
Δ ^3 Π n IN JN , Ό Γ2 ΓΠ 丄 丄 J t Δ ^ 3 Π n IN JN, Ό Γ2 ΓΠ 丄 丄 J t
TJ "U AT TJ "U AT
丄 U όΌ Δ し n n IN IN 乙, し丄 ΓΠ 丄 U όΌ Δshi n n IN IN Otsu, Shi 丄
1 — o LI TJ NT M 1 — o LI TJ NT M
ά し Π n IN O, A£—Cし丄I 2— rxh し Π IN n IN O, A £ —C 丄 I 2— rxh
o rr LT o rr LT
丄 U ο 厶 n Π IN IN ώ, 0 し丄 2 ΓΠ 丄 U ο MU n Π IN IN ώ, 0 丄2 ΓΠ
1 1
丄 π— QQ 9 u 丄 π— QQ 9 u
U ζ) 厶 n Π IN IN ώ? 0 し丄2 丄 ί U 丄 ί丄U ζ) m n Π IN IN ώ ? 0 2丄 ί U 丄
1 ί\—Αί) LI LT 1 ί \ —Αί) LI LT
丄 U 厶 し n n IN IN し丄 Ό Γ ΓΠ 丄 U umushi n n IN IN IN Ό 丄 ΓΠ
TJ TJ
1U 4丄 し rl n IN IN 乙, Ό 1Υ1Θ2 ΓΠ 1U 4 丄 Shi rl n IN IN Otsu, Ό 1Υ1Θ 2 ΓΠ
9 u u 9 u u
ム し 3 n n I IN 厶 し丄 り Ινΐθ ΓΠ 3 nn I IN Ινΐθ ΓΠ
o IT TJ o IT TJ
ά し n n 丄 N IN D し丄 3 ΓΠά s nn 丄 N IN D s 丄3 ΓΠ
1 Α_/1 TI TT 1 Α_ / 1 TI TT
丄 (J ί3 厶 Π Π JN Δ, し丄 2 4 ULJ^ Jr l 丄 (J ί3 Π Π Π JN Δ, 丄2 4 ULJ ^ Jr l
ο TT ο TT
丄 1) D 厶 n n IN IN 厶, Ό Me3 rfi 丄 1) D nn nn IN IN rum, Ό Me 3 rfi
LI LT LI LT
Δ しト ΓΊ n IN IN z ryn Δ n IN IN z ryn
ο IT TJ ο IT TJ
Π n IN IN 0 ryn Π n IN IN 0 ryn
TJ TJ
丄1) y u 丄 1) y u
しト n n 一 N n one
IN JN 4 ryn IN JN 4 ryn
u y u y
丄 U DU ム し!^ n n IN IN 0 し丄 ryn 丄 U DU! ^ n n IN IN 0 shu ryn
1 Α_|ΓΙ θ TT rr 1 Α_ | ΓΙ θ TT rr
しト Π fl IN IN o し Ρ3 ryn Π fl IN IN o Ρ 3 ryn
LT u LT u
厶 Π n IN I MN 0 し丄 ^: し r3 Δ ryn Π n IN I MN 0 丄 ^: r r 3 Δ ryn
LI LT LI LT
丄 U 00 ά し Π n IN IN Δ rym 丄 U 00 ά Π n IN IN Δ rym
u TJ u TJ
Δ し 3 Π n IN IN t ryrn Δ 3 3 Π n IN IN t ryrn
u u u u
上り 00 厶 し Π Π IN IN t, D ΐνΐΘ2 rym 00IN IN t, D ΐνΐΘ 2 rym
IJ TJ IJ TJ
1U 00 ム し n n IN IN % D υΜΘノ ryni 1U 00 m n n IN IN% D
u y u y
丄 U ¾ し 3 Π n IN IN 0 ryo 丄 U ¾ 3 3 Π n IN IN 0 ryo
LT u LT u
丄 L/ Do ά Π n λ INΤ IN し L¾ ΐ 1丄. ¾ ΛΟy¾ΑΛ丄 f ~丄i し、 丄 L / Do ά Π n λ INΤ IN ¾ L¾ ΐ 1 丄. ¾ ΛΟy¾ΑΛ 丄 f ~ 丄 i
ο u ο u
丄 u oy し1^ Π Π u M 丄 u oy shi 1 ^ Π M u M
J JN —CしO 1 J JN —C and O 1
丄 /]θ— 1 丄 /] θ— 1
丄 IQ ο u u 丄 IQ ο u u
丄 (J DU し n n IN IN _^し0 \j— M l HnMivioe 丄 (J DU then n n IN IN _ ^ then 0 \ j— M l HnMivioe
u u u u
丄 U 0丄 ム し n n IN IN し \J lNnrn 丄 U 0 丄 n n n IN IN し \ J lNnrn
ru u ru u
丄 U ΌΔ ム n Π u 丄 U ΌΔ m n Π u
IN IN U IMVIc 11 IN IN U IMVIc 11
u u
丄 U 00 ム ^3 Π Π IN IN し U IN [2 丄 U 00 mu ^ 3 Π Π IN IN then U IN [2
u u
丄 1/ 0^: Δ し 1 Π Π u 丄 1/0 ^: Δ then 1 Π Π u
i i\ し (J し し Πΐ^Αノ i i \ shi (J shi shi ^ Πΐ ノ
丄 1/ DO ο u 丄 1 / DO ο u
し丄 Π Π I MN IN UU IN、丄 ΓΙ ) (丄 Π Π I MN IN UU IN, 丄 ΓΙ)
10— 66 2 H 5— Me N N Ph 10— 66 2 H 5— Me N N Ph
10-67 2 CF3 H 5 - Me N N 2 - CI - Ph 10-67 2 CF 3 H 5-Me NN 2-CI-Ph
10-68 2 CF3 H 5- Me N N 2 - Me Ph 10-68 2 CF 3 H 5- Me NN 2-Me Ph
10-69 2 CF3 H 5- Me N N 2-CF3-Ph 10-69 2 CF 3 H 5-Me NN 2-CF 3 -Ph
10-70 2 CF3 H 5- Me N N 2, 6- Cl2-Ph 10-70 2 CF 3 H 5-Me NN 2, 6- Cl 2 -Ph
10-71 2 CF3 H 5- Me N N 2- CI- 6- Me- Ph 10-71 2 CF 3 H 5-Me NN 2- CI- 6- Me- Ph
10-72 2 CF3 H 5 - Me N N 2, 6- Me2- Ph
0表 (続き) 10-72 2 CF 3 H 5-Me NN 2, 6- Me 2 -Ph Table 0 (continued)
置換 物性 o. R1 R2 X J'1 J5 R13 Substitution physical properties o.R 1 R 2 X J ' 1 J 5 R 13
置 [融点 (°c)、屈折率]0-73 2 CF3 H 5 - Me N N -CH2-Ph[Melting point (° c), refractive index] 0-73 2 CF 3 H 5-Me NN -CH 2 -Ph
0-74 2 CF3 H 5-Me N N - CMe2 - Ph 0-74 2 CF 3 H 5-Me NN - CMe 2 - Ph
0 - 75 2 CF3 H 4 - CI N N Ph0-75 2 CF 3 H 4-CI NN Ph
-76 2 CF3 H 4 - CI N N 2 - Cト Ph-76 2 CF 3 H 4-CI NN 2-C Ph
-77 2 CF3 H 4 - CI N N 2 - Me - Ph-77 2 CF 3 H 4-CI NN 2-Me-Ph
-78 2 CF3 H 4 - CI N N 2 - CF3 Ph-78 2 CF 3 H 4-CI NN 2-CF 3 Ph
-79 2 CF3 H 4 CI N N 2, 6-Cl2- Ph-79 2 CF 3 H 4 CI NN 2, 6-Cl 2 -Ph
-80 2 CF3 H 4 - CI N N 2-C1- 6- Me - Ph-80 2 CF 3 H 4-CI NN 2-C1-6- Me-Ph
-81 2 CF3 H 4 - CI N N 2, 6 - Me2 - Ph-81 2 CF 3 H 4-CI NN 2, 6-Me 2 -Ph
-82 2 CF3 H 4 - CI N N - CH2 - Ph-82 2 CF 3 H 4-CI NN-CH 2 -Ph
-83 2 CF3 H 4 - CI N N _CMe2 - Ph-83 2 CF 3 H 4-CI NN _CMe 2 -Ph
-84 2 CF3 H 5 - CI N N Ph-84 2 CF 3 H 5-CI NN Ph
-85 2 CP3 H 5 - CI N N 2 - CI- Ph-85 2 CP 3 H 5-CI NN 2-CI- Ph
-86 2 CF3 H 5 - CI N N 2-Me-Ph-86 2 CF 3 H 5-CI NN 2-Me-Ph
-87 2 CF3 H 5 - CI N N 2 - CF3 - Ph -87 2 CF 3 H 5-CI NN 2-CF 3 -Ph
- 88 2 CF3 H 5 - CI N N 2, 6 - Cl2 - Ph-88 2 CF 3 H 5-CI NN 2, 6-Cl 2 -Ph
-89 2 CF3 H 5 - CI N N 2- CI- 6- Me - Ph-89 2 CF 3 H 5-CI NN 2- CI- 6- Me-Ph
-90 2 CF3 H 5-C1 N N 2, 6-Me2-Ph-90 2 CF 3 H 5-C1 NN 2, 6-Me 2 -Ph
-91 2 CF3 H 5 - CI N N CH2 Ph -91 2 CF 3 H 5-CI NN CH 2 Ph
92 2 CF3 H 5- CI N N - CMe2 - Ph 92 2 CF 3 H 5- CI NN-CMe 2 -Ph
- 93 3 CF3 H H N N Me-93 3 CF 3 HHNN Me
-94 3 CF3 H H N N t-Bu-94 3 CF 3 HHNN t-Bu
-95 3 CF3 H H N N - CH2-Ph-95 3 CF 3 HHNN-CH 2 -Ph
-96 3 CF3 H H N N Ph -96 3 CF 3 HHNN Ph
- 97 3 CF3 H H N N 2-Cl-Ph-97 3 CF 3 HHNN 2-Cl-Ph
-98 3 CF3 H H N N 2- CF3-Ph-98 3 CF 3 HHNN 2- CF 3 -Ph
-99 3 CF3 H H N N 2, 6~C12-Ph-99 3 CF 3 HHNN 2, 6 ~ C1 2 -Ph
-100 3 CF3 H H N N 2- Cト 6-Me-Ph-100 3 CF 3 HHNN 2-C 6-Me-Ph
-101 3 CF3 H H N N 2, 6~Me2-Ph -101 3 CF 3 HHNN 2, 6 ~ Me 2 -Ph
- 102 4 CF3 H H N N Me-102 4 CF 3 HHNN Me
-103 4 CF3 H H N N t-Bu -103 4 CF 3 HHNN t-Bu
104 4 CF3 H H N N104 4 CF 3 HHNN
-105 4 CF3 H H N N Ph-105 4 CF 3 HHNN Ph
106 4 CF3 H H N N 2 - CI - Ph106 4 CF 3 HHNN 2-CI-Ph
-107 4 CF3 H H N N 2-CF3-Ph-107 4 CF 3 HHNN 2-CF 3 -Ph
108 4 CF3 H H N N 2, 6-Cl2-Ph108 4 CF 3 HHNN 2, 6-Cl 2 -Ph
-109 4 CF3 H H N N 2 - - 6- Me - Ph-109 4 CF 3 HHNN 2--6- Me-Ph
-110 4 CF3 H H N N 2, 6 - Me2 - Ph-110 4 CF 3 HHNN 2, 6-Me 2 -Ph
-111 2 CHF2 H H N N Me-111 2 CHF 2 HHNN Me
-112 2 CHF2 H H N N t-Bu
0表 (続き) -112 2 CHF 2 HHNN t-Bu Table 0 (continued)
物性 o. R1 R2 X J4 J5 R13 Properties o.R 1 R 2 XJ 4 J 5 R 13
置 [融点 (°c)、屈折率]-113 2 CHF2 H H N N[Melting point (° c), refractive index] -113 2 CHF 2 HHNN
-114 2 CHF2 H H N N-114 2 CHF 2 HHNN
-115 2 CHF2 H H N N Ph-115 2 CHF 2 HHNN Ph
-116 2 CHF2 H H N N 2- CI - Ph 99-100-117 2 CHF2 H H N N 2 - Me- Ph-116 2 CHF 2 HHNN 2- CI-Ph 99-100 -117 2 CHF 2 HHNN 2-Me- Ph
-118 2 CHF2 H H N N 2-0Me-Ph-118 2 CHF 2 HHNN 2-0Me-Ph
-119 2 CHF2 H H N N 2 - CF3 - Ph -119 2 CHF 2 HHNN 2-CF 3 -Ph
- 120 2 CHF2 H H N N 2 - 0CF3 - Ph-120 2 CHF 2 HHNN 2-0CF 3 -Ph
-121 2 CHF2 H H N N 2, 6- Cl2-Ph-121 2 CHF 2 HHNN 2, 6- Cl 2 -Ph
-122 2 CHF2 H H N N 2- CI- 6- F- Ph -122 2 CHF 2 HHNN 2- CI- 6- F- Ph
- 123 2 CHF2 H H N N 2 - CI 6- Me- Ph-123 2 CHF 2 HHNN 2-CI 6- Me- Ph
-124 2 CHF2 H H N N 2, 6 - Me2 - Ph -124 2 CHF 2 HHNN 2, 6-Me 2 -Ph
1 1
CD 1
CD 1
一般式 (I — 1 0 ) General formula (I — 10)
置換 物性 Substitution physical properties
No. R1 R2 X J4 J5 R13 No. R 1 R 2 XJ 4 J 5 R 13
位置 [融点 (。c) Position [melting point (.c)
11-1 2 CF, H H N N Me 11-1 2 CF, H H N N Me
11一 2 2 H H N N t-Bu 11 1 2 2 H H N N t-Bu
11-3 2 H H N N -CH,-Ph 11-3 2 H H N N -CH, -Ph
11-4 2 H H N N - CHMe-Ph 11-4 2 H H N N-CHMe-Ph
11-5 2 H H N N - CMe2 - Ph 11-5 2 HHNN-CMe 2 -Ph
11-6 2 H H N N Ph 11-6 2 H H N N Ph
11-7 2 H H N N 2- CI - Ph 141-142 11-7 2 H H N N 2- CI-Ph 141-142
11-8 2 H H N N 3 - CI - Ph 11-8 2 H H N N 3-CI-Ph
11-9 2 H H N N 4-Cl-Ph 11-9 2 H H N N 4-Cl-Ph
11-10 2 CF, i H H N N 2- Me- Ph 11-10 2 CF, i H H N N 2- Me- Ph
11-11 2 H H N N 2-OMe-Ph 156-157 11-11 2 H H N N 2-OMe-Ph 156-157
11-12 2 CF, ά H H N N 2-SMe-Ph 11-12 2 CF, ά H H N N 2-SMe-Ph
11-13 2 CF, H H N N 2-SOMe-Ph 11-13 2 CF, H H N N 2-SOMe-Ph
11-14 2 CF, H H N N 2-S02Me-Ph 11-14 2 CF, HHNN 2-S0 2 Me-Ph
11-15 2 CF3 H H N N 2-CN-Ph 11-15 2 CF 3 HHNN 2-CN-Ph
11-16 2 CF3 H H N N 2 - N02- Ph 11-16 2 CF 3 HHNN 2-N0 2 -Ph
11-17 2 CF3 H H N N 2- CF3- Ph 11-17 2 CF 3 HHNN 2- CF 3 -Ph
11-18 2 CF3 H H N N 2 - 0CF3_Ph 11-18 2 CF 3 HHNN 2-0CF 3 _Ph
11-19 2 CF3 H H N N 4-C02Et-Ph 11-19 2 CF 3 HHNN 4-C0 2 Et-Ph
11-20 2 CF3 H H N N 2- Ph- Ph 11-20 2 CF 3 HHNN 2- Ph- Ph
11-21 2 CF3 H H N N 2-PhO-Ph 11-21 2 CF 3 HHNN 2-PhO-Ph
11-22 2 CF3 H H N N 2, 6-F2-Ph 11-22 2 CF 3 HHNN 2, 6-F 2 -Ph
11-23 2 CF3 H H N N 2, 6-Cl2-Ph 163-16411-23 2 CF 3 HHNN 2, 6-Cl 2 -Ph 163-164
11-24 2 CF3 H H N N 2- CI- 6- F - Ph 11-24 2 CF 3 HHNN 2- CI- 6- F-Ph
11-25 2 CF3 H H N N 2, 6_Me2 - Ph 11-25 2 CF 3 HHNN 2, 6_Me 2 -Ph
11-26 2 CF3 H H N N 2-C1- 6- Me- Ph 11-26 2 CF 3 HHNN 2-C1- 6- Me- Ph
11-27 2 CF3 H H N N 2 6— (0Me) 2 - Ph 11-27 2 CF 3 HHNN 26-(0Me) 2 -Ph
11-28 2 CF3 H H N N 2, 6 - (CF3) 2 - Ph 11-28 2 CF 3 HHNN 2, 6-(CF 3 ) 2 -Ph
11-29 2 CF3 H H N N 2, 6- (0CF3) 2- Ph 11-29 2 CF 3 HHNN 2, 6- (0CF 3 ) 2 -Ph
11-30 2 CF3 H H N N 2, 4, 6-Cl3-Ph 11-30 2 CF 3 HHNN 2, 4, 6-Cl 3 -Ph
11-31 2 CF3 H H N N 2, 6- Cl2 4- CF3- Ph 11-31 2 CF 3 HHNN 2, 6- Cl 2 4- CF 3 -Ph
11-32 2 CF3 H H N N 2 6- Cl2_4- 0CF3 - Ph
1表 (続き) 11-32 2 CF 3 HHNN 2 6- Cl 2 _4- 0CF 3 -Ph Table 1 (continued)
物性o. mm R1 R2 X J" J5 R13 Properties o.mm R 1 R 2 XJ "J 5 R 13
位置 [融点 (。c)-33 2 CF3 H H N N 2, 4, 6- Me3_PhPosition [melting point (.c) -33 2 CF 3 HHNN 2, 4, 6- Me 3 _Ph
-34 2 CF3 H H N N 2-Pyn-34 2 CF 3 HHNN 2-Pyn
-35 2 CF3 H H N N 3-Pyn-35 2 CF 3 HHNN 3-Pyn
-36 2 CF3 H H N N 4-Pyn-36 2 CF 3 HHNN 4-Pyn
-37 2 CF3 H H N N 2-Pym-37 2 CF 3 HHNN 2-Pym
-38 2 CF3 H H N N 4-Pym-38 2 CF 3 HHNN 4-Pym
-39 2 CF3 H H N N 4, 6- Me2- 2- Pym -39 2 CF 3 HHNN 4, 6- Me 2 - 2- Pym
-40 2 CF3 H H N N 4 6- (OMe) 2-2- Pym-40 2 CF 3 HHNN 4 6- (OMe) 2 -2- Pym
-41 2 CF3 H H N N 3-Pyd-41 2 CF 3 HHNN 3-Pyd
-42 2 CF3 H H N N - C02Et-42 2 CF 3 HHNN-C0 2 Et
-43 2 CF3 H H N N -C02H-43 2 CF 3 HHNN -C0 2 H
-44 2 CF3 H H N N -CO-NHMe-44 2 CF 3 HHNN -CO-NHMe
-45 2 CF3 H H N N -CO-NHPh -45 2 CF 3 HHNN -CO-NHPh
- 46 2 CF3 H H N N - CO-匪 e2 -46 2 CF 3 HHNN-CO-Marauder e 2
-47 2 CF3 H H N N -CO-NMePh-47 2 CF 3 HHNN -CO-NMePh
-48 2 CF3 H H N N -CO-NEt (c-Hex)-48 2 CF 3 HHNN -CO-NEt (c-Hex)
-49 2 CF3 H H N N - CO- N (i - Pr) 2
-49 2 CF 3 HHNN-CO- N (i-Pr) 2
一般式 (I) General formula (I)
No. 一 No. one
Q 物性 Q physical properties
[融点 (°c) 、 屈折率] [Melting point (° c), refractive index]
第 1 3表 Table 13
No. R9 物性 No. R 9 physical properties
[融点 (°C) 、 屈折率] [Melting point (° C), refractive index]
13-1 C-SMe 2- CI- Ph 101-103 13-1 C-SMe 2- CI- Ph 101-103
13-2 CH 2-Cl-Ph 101-103 13-2 CH 2-Cl-Ph 101-103
13-3 CH 2, 6- Me2- Ph 123-125 13-3 CH 2, 6- Me 2 -Ph 123-125
13-4 CH 2 - - 6- Me - Ph 1.5488 (26°C) 第 1表から第 13表中の NMRデータを第 14表に記す。 13-4 CH 2--6- Me-Ph 1.5488 (26 ° C) Table 14 shows the NMR data in Tables 1 to 13.
第 14表 Table 14
'MR λ化合物 ¾ -匪 l CDCl TMS, δ値,) " ' MR λ compound ¾-band l CDCl TMS, δ value,) "
No. No. No. No.
ϊ 1-257 10.82 (IH, bs) , 7.62-7.26 (9H, m), 4.97 (2H, s) , 4.01 (3H, s) ϊ 1-257 10.82 (IH, bs), 7.62-7.26 (9H, m), 4.97 (2H, s), 4.01 (3H, s)
2 3 - 83 7.6-7.4 (8H, m) , 5.3 (2H, q), 3.5 (3H, s) 2 3-83 7.6-7.4 (8H, m), 5.3 (2H, q), 3.5 (3H, s)
3 5-29 10.39 (IH, s) ,"7.83 (IH, s) , 7.57-7.33 (8H, m) , 5. 62(lH,q),l.97(3H,d) 3 5-29 10.39 (IH, s), "7.83 (IH, s), 7.57-7.33 (8H, m), 5.62 (lH, q), l.97 (3H, d)
4 5-50 9.45 (IH, s) , 7.55 (IH, s) , 7.50-7.25 (8H, m) , 5.31 (IH, dd),4.60 (IH, br),4.04 (IH, dd),3.95(lH, dd) 4 5-50 9.45 (IH, s), 7.55 (IH, s), 7.50-7.25 (8H, m), 5.31 (IH, dd), 4.60 (IH, br), 4.04 (IH, dd), 3.95 ( lH, dd)
5 5-64 11.50(lH,s),8.01 (lH,dd), 7.86 (lH,d), 7,72- -7.70 (2H, m), 7.56-7. 5 5-64 11.50 (lH, s), 8.01 (lH, dd), 7.86 (lH, d), 7,72- -7.70 (2H, m), 7.56-7.
50 (2H, m) , 7.42—7.25 (3H, m) , 5.92 (2H, s) 50 (2H, m), 7.42-7.25 (3H, m), 5.92 (2H, s)
6 5 - 93 10.78 (IH, s) , 7.92 (IH, dd) , 7.68-7.65 (2H, ra) , 7.50 (IH, dd) , 7.43-7. 6 5-93 10.78 (IH, s), 7.92 (IH, dd), 7.68-7.65 (2H, ra), 7.50 (IH, dd), 7.43-7.
25 (5H, m), 5.01 (2H, s), 4.19 (3H, s) 25 (5H, m), 5.01 (2H, s), 4.19 (3H, s)
7 10-2 9.3 (IH, br) , 8.21 (IH, s) , 8.01-7.99 (2H, s) , 7. 62 (IH, d),7.45-7.39 7 10-2 9.3 (IH, br), 8.21 (IH, s), 8.01-7.99 (2H, s), 7.62 (IH, d), 7.45-7.39
(5H,m),7.26(lH, dd) , 5.34(2H, s) (5H, m), 7.26 (lH, dd), 5.34 (2H, s)
8 6-339 9.5 (IH, s) , 7.50 (IH, d) , 7.44 (IH, dd) , 7.39-7. 23(5H,m),4.49 (2H, s) 8 6-339 9.5 (IH, s), 7.50 (IH, d), 7.44 (IH, dd), 7.39-7.23 (5H, m), 4.49 (2H, s)
, 3.85 (2H, dd),3.66(2H, dd) , 3.85 (2H, dd), 3.66 (2H, dd)
9 6-361 7.57-6.92 (10H, m) , 4.58 (2H, dd) , 3.73 (2H, m) , 3. 48(2H,m),2.41(6H,s), 9 6-361 7.57-6.92 (10H, m), 4.58 (2H, dd), 3.73 (2H, m), 3.48 (2H, m), 2.41 (6H, s),
10 6-362 9.07(lH,s),8.35(lH,s),7.45— 7.13(6H,m),6.80 (2H, s),4.42 (2H, s) 10 6-362 9.07 (lH, s), 8.35 (lH, s), 7.45—7.13 (6H, m), 6.80 (2H, s), 4.42 (2H, s)
, 3.56 (4H, dd), 2.37 (6H, s) , 2.22 (3H, s)
実施例 1. , 3.56 (4H, dd), 2.37 (6H, s), 2.22 (3H, s) Example 1.
(1 -1) . 2 - (2—ニトロベンジル) 一4一フエ二ルー 2, 4—ジヒ ドロ - 3H- 1 , 2, 4—トリァゾールー 3—オンの合成 (1 -1). Synthesis of 2- (2-nitrobenzyl) -1,4-dihydro-2,4-dihydro-3H-1, 2,4-triazol-3-one
4一フエ二ルー 2, 4—ジヒ ドロー 3H— 1, 2, 4—トリァゾール一 3—ォ ン (1. 61 g、 10ミリモル) と炭酸カリウム (1. 66 g、 1 2ミリモル) を N、 N—ジメチルホルムアミ ド (35ml) に懸濁し、 ついで 2—二トロベン ジルクロリ ド (1. 80 g、 10. 5ミリモル) を加えて 50 °Cで 4時間加熱撹 拌した。 室温に冷却した後、 氷水を加え、 析出した結晶をエーテルで洗浄し 2— (2—二トロべンジノレ) - 4一フエニル一 2, 4ージヒ ドロー 3 H- 1, 2, 4 一トリァゾールー 3—オン (2. 73 g、 収率 92%) を得た。 4 1,2-dihydro-3H-1,2,4-triazole-13-one (1.61 g, 10 mmol) and potassium carbonate (1.66 g, 12 mmol) were added to N, The suspension was suspended in N-dimethylformamide (35 ml), and then 2-nitrobenzyl chloride (1.80 g, 10.5 mmol) was added, followed by heating and stirring at 50 ° C for 4 hours. After cooling to room temperature, ice water was added, and the precipitated crystals were washed with ether, and 2- (2-ditrobendinole) -4-1, phenyl-1,2,4 dihydro 3 H-1,2,4 triazole-3— Was obtained (2.73 g, yield 92%).
(1— 2) . 2— (2—ァミノベンジル) 一 4—フエ二ルー 2, 4ージヒ ドロ 一 3H— 1, 2, 4一トリァゾールー 3一オンの合成 (1-2). 2- (2-Aminobenzyl) 1-4-phenyl-2,4-dihydro-1-3H-1,2,4-triazole-3-one
2— (2—二トロベンジル) 一 4—フエ二ルー 2, 4—ジヒ ドロー 3H— 1, 2, 4—トリァゾールー 3—オン (2. 6 g、 8. 8ミ リモル) 、 塩化第一スズ 二水和物 (7. 93 g、 35ミリモル) をエタノール (30ml) と濃塩酸 (3 0m l) の混合溶媒中に加え、 6時間加熱還流した。 室温に冷却した後に、 20 %水酸化ナトリウム水溶液を加えて反応液を塩基性にし、 クロ口ホルムで抽出し た。 クロ口ホルム層を 4回水洗した後、 飽和食塩水で 1回洗浄し、 無水硫酸ナト リゥムで乾燥し溶媒を留去した。 析出した結晶をへキサンで洗浄し 2— ( 2—ァ ミノベンジル) 一 4 _フエ二ルー 2, 4—ジヒ ドロー 3 H— 1, 2, 4ートリア ゾールー 3—オン (2. 33 g、 収率 100%) を得た。 2- (2-nitrobenzyl) 1-4-phenyl 2,4-dihydro 3H-1,2,4-triazol-3-one (2.6 g, 8.8 mimol), stannous chloride The hydrate (7.93 g, 35 mmol) was added to a mixed solvent of ethanol (30 ml) and concentrated hydrochloric acid (30 ml), and the mixture was heated under reflux for 6 hours. After cooling to room temperature, a 20% aqueous sodium hydroxide solution was added to make the reaction solution basic, and the mixture was extracted with chloroform. After washing the pore-form layer four times with water, it was washed once with a saturated saline solution, dried over anhydrous sodium sulfate, and the solvent was distilled off. The precipitated crystals are washed with hexane and washed with 2- (2-aminobenzyl) -14-phenyl-2,4-dihydro 3H-1,2,4-triazol-3-one (2.33 g, yield) 100%).
(1-3) . 4一フエ二ルー 2— (2—トリフルォロメタンスルホニルァミノ ベンジル) 一 2, 4—ジヒ ドロー 3H— 1, 2, 4— トリァゾールー 3—オン (化合物 N o . 1 -23) の合成 (1-3). 4 1-2- (2-trifluoromethanesulfonylaminobenzyl) 1,2,4-dihydro 3H— 1,2,4-triazol-3-one (compound N o. 1- 23) Synthesis of
2— (2—ァミノベンジル) 一4一フエニル一 2, 4—ジヒ ドロー 3H— 1, 2, 4一トリァゾールー 3—オン (0. 30 g、 1. 1ミリモル) と トリェチル ァミン (0. 14 g、 1. 4ミリモル) をクロロホノレム (5ml) に溶解した後、 反応溶液を一 1 0°Cに冷却した。 ついでトリフルォロメタンスルホン酸無水物 (0. 39 g、 1. 4ミリモル) をクロ口ホルム 0. 5m lで希釈した溶液を 2
分で滴下した。 そのままの温度で 2時間撹拌した後, 徐々に反応温度を室温まで 上昇させながらさらに 1 0時間撹拌した。 反応終了後、 クロ口ホルムを減圧下に 留去し、 残渣をシリカゲルカラムクロマトグラフィーにて精製し、 4一フエニル -2- ( 2—トリフノレオ口メタンスルホニノレアミノベンジル) 一 2, 4一ジヒ ド 口— 3H— 1, 2, 4—トリァゾールー 3—オン (0. 36 g、 収率 79%) を 得た。 融点は 141— 142°Cであった。 2- (2-aminobenzyl) 4-phenyl-1,2,4-dihydro 3H-1,2,4-triazol-3-one (0.30 g, 1.1 mmol) and triethylamine (0.14 g, (1.4 mmol) was dissolved in chlorophonolem (5 ml), and the reaction solution was cooled to 110 ° C. Then, a solution obtained by diluting trifluoromethanesulfonic anhydride (0.39 g, 1.4 mmol) with 0.5 ml of chloroform was added. Dropped in minutes. After stirring at the same temperature for 2 hours, the mixture was further stirred for 10 hours while gradually raising the reaction temperature to room temperature. After completion of the reaction, the chloroform was distilled off under reduced pressure, and the residue was purified by silica gel column chromatography to obtain 4-phenyl-2- (2-triphnoleo methanesulfoninoleaminobenzyl) -1,2,4-dialdehyde. Mouth-3H-1,2,4-triazol-3-one (0.36 g, 79% yield) was obtained. The melting point was 141-142 ° C.
実施例 2. Example 2.
(2 - 1 ) . 2― (2—ク口 口フエ二ノレ) 一 4一 (2—二 トロべンジノレ) 一 2, 4—ジヒ ドロ一 3 H— 1, 2, 4—トリァゾールー 3—オンの合成 (2-1). 2-(2-Mouth Mouth Feninole) 1-4 (2-2 Trobenzinole) 1-2,4-Dihydro 1 3 H-1, 2, 4-Triazol-3-one Synthesis of
2— (2—クロ口フエ二ノレ) 一 2, 4ージヒ ドロ一 3H—1, 2, 4ートリア ゾールー 3—オン (1. 00 g、 5. 1ミリモル) と炭酸カリウム (0. 74 g、 5. 4ミリモル) を N、 N—ジメチルホルムアミ ド (25ml) に溶解、 懸濁し、 ついで 2—ニトロべンジノレクロリ ド (0. 88 g、 5. 1ミリモル) を加えて 5 0°Cで 2時間加熱撹拌した。 室温に冷却した後、 氷水を加え、 酢酸ェチルで抽出 した。 酢酸ェチル層を飽和食塩水で 1回洗浄した後、 無水硫酸ナトリウムで乾燥 し溶媒を留去した。 析出した結晶をへキサン一エーテル (1 : 1) 混合液で洗浄 し 2— (2—ク口口フエ二ノレ) —4一 (2—二トロべンジノレ) 一 2, 4—ジヒ ド ロー 3H— 1, 2, 4一トリァゾールー 3—オン (1. 37 g、 収率 81. 3 %) を得た。 融点は 85. 5 °Cであった。 2- (2,3-dihydropheninole) 1,2,4-dihydro-3H-1,2,4-triazol-3-one (1.00 g, 5.1 mmol) and potassium carbonate (0.74 g, 5.4 mmol) was dissolved and suspended in N, N-dimethylformamide (25 ml), and then 2-nitrobenzylinochloride (0.88 g, 5.1 mmol) was added. Heated and stirred for hours. After cooling to room temperature, ice water was added, and the mixture was extracted with ethyl acetate. The ethyl acetate layer was washed once with a saturated saline solution, dried over anhydrous sodium sulfate, and the solvent was distilled off. The precipitated crystals are washed with a mixture of hexane monoether (1: 1) and washed with 2- (2-octanol) -2,4- (2-nitrobenzene) 1,2,4-dihydro 3H — 1,2,4-Triazol-3-one (1.37 g, 81.3% yield) was obtained. The melting point was 85.5 ° C.
(2-2) . 4一 (2—ァミノベンジル) 一 2— (2—クロ口フエニル) 一 2, 4ージヒ ドロー 3H— 1, 2, 4—トリァゾールー 3—オンの合成 (2-2). Synthesis of 4- (2-aminobenzyl) -1- (2-chlorophenyl) -1,2,4-dihydro 3H-1,2,4-triazol-3-one
1— (2—クロ口フエ二ノレ) 一 2— (2—ニトロベンジル) 一 2, 4—ジヒ ド 口— 3H— 1, 2, 4ー トリアゾール— 3—オン (1. 25 g、 3. 8ミ リモ ル) 、 鉄粉末 (1 · 06 g、 18. 9ミリモル) 、 塩ィ匕アンモニゥム (0. 1 0 g、 1. 9ミ リモル) をエタノール (30m l) と水 (15ml) に溶解し、 2 時間加熱還流した。 室温に冷却した後に、 反応液を吸引ろ過し、 酉乍酸ェチルで抽 出した。 酢酸ェチル層を飽和食塩水で 1回洗浄した後、 無水硫酸ナトリゥムで乾 燥し溶媒を留去した。 析出した結晶をへキサン一エーテル (1 : 1) 混合液で洗 浄し 4一 (2—ァミノベンジル) 一2— (2—クロ口フエニル) 一 2, 4—ジヒ
ドロー 3H— 1, 2, 4—トリアゾール一 3—オン ( 0. 55 g、 収率 48. 2 %) を得た。 融点は 1 68. 6°Cであった。 1- (2-cyclohexene) 1 2- (2-nitrobenzyl) 1,2,4-dihydrogen 3H—1,2,4-triazol-3-one (1.25 g, 3. 8millimol), iron powder (1.06g, 18.9mmol), salted ammonia (0.10g, 1.9millimol) dissolved in ethanol (30ml) and water (15ml) The mixture was refluxed for 2 hours. After cooling to room temperature, the reaction solution was subjected to suction filtration and extracted with ethyl acetate. The ethyl acetate layer was washed once with a saturated saline solution, dried over anhydrous sodium sulfate, and the solvent was distilled off. The precipitated crystals were washed with a mixture of hexane monoether (1: 1) and washed with 4- (2-aminobenzyl) -12- (2-chlorophenyl) -1,2,4-diphenyl Draw 3H-1,2,4-triazol-3-one (0.55 g, 48.2% yield) was obtained. Melting point was 168.6 ° C.
(2-3) . 2 - (2—クロ口フエ二ノレ) 一 4一 (2—トリフルォロメタンス ルホニルァミノべンジル _ 2, 4—ジヒ ドロー 3 H— 1, 2, 4—トリァゾール 一 3—オン (化合物 No. 2-27) の合成 (2-3). 2-(2-Fluorinole) 1-41 (2-trifluoromethanes rufonylaminobenzyl _ 2,4-dihydro 3 H-1, 2, 4-triazole 1-3- Synthesis of ON (Compound No. 2-27)
4一 (2—ァミノベンジル) - 2 - (2—クロ口フエ二ノレ) 一 2, 4—ジヒ ド 口 - 3 H— 1 , 2 , 4— トリアゾールー 3—オン (0. 50 g、 1. 7ミ リモ ル) と トリェチルァミン (0. 18 g、 1. 8ミ リモル) をクロ口ホルム ( 20 ml) に溶解した後、 反応溶液を _ 10。Cに冷却した。 ついでトリフルォロメタ ンスルホン酸無水物 (0. 47 g、 1. 7ミ リモル) を 20分かけて滴下した。 そのままの温度で 2時間撹拌した後に、 氷を加え、 さらに 6 N塩酸を加えて反応 液を酸性にし、 酢酸ェチルで抽出した。 酢酸ェチル層を飽和食塩水で 1回洗浄し た後、 無水硫酸ナトリウムで乾燥し溶媒を留去した。 残渣をシリ力ゲル力ラムク 口マトグラフィー (へキサン:酢酸ェチル = 2 : 1) で精製して 2— (2—クロ 口フエニル) 一 4一 (2—トリフルォロメタンスルホニルァミノべンジルー 2, 4ージヒ ドロ— 3H— 1, 2, 4—トリァゾールー 3 _オン (0. 38 g、 収率 51. 7%) を得た。 融点は 187. 9°Cであった。 4- (2-Aminobenzyl)-2- (2-chloro-pheninole) 1,2,4-Dihydrid -3H-1,2,4-triazol-3-one (0.50 g, 1.7 (Millimol) and triethylamine (0.18 g, 1.8 mimol) were dissolved in chloroform (20 ml). Cooled to C. Then, trifluoromethansulfonic anhydride (0.47 g, 1.7 mmol) was added dropwise over 20 minutes. After stirring at the same temperature for 2 hours, ice was added, and the reaction solution was further acidified with 6N hydrochloric acid, and extracted with ethyl acetate. The ethyl acetate layer was washed once with a saturated saline solution, dried over anhydrous sodium sulfate, and the solvent was distilled off. The residue was purified by silica gel gel chromatography (hexane: ethyl acetate = 2: 1) to give 2- (2-chloromethylphenyl) 1-4-1 (2-trifluoromethanesulfonylaminobenziru, 2). There was obtained 4-dihydro-3H-1,2,4-triazol-3-one (0.38 g, yield 51.7%) with a melting point of 187.9 ° C.
実施例 3 · Example 3
(3-1) . 4 - (2—二トロベンジル) 一 1— (2—トリフルォロメチルフ ェニル) 一 5 (4H) —テトラゾリノンの合成 (3-1). Synthesis of 4- (2-nitrobenzyl) 1-1- (2-trifluoromethylphenyl) -5 (4H) -tetrazolinone
1— (2—トリフルォロメチルフエニル) ― 5 (4H) 一テトラゾリノン (2. 5 g、 1 1ミリモル) と炭酸カリゥム (2. 2 g、 16ミリモル) を N、 N—ジ メチルホルムアミ ド (25ml) に溶解、 懸濁し, ついで p—トルエンスルホン 酸 2—二トロべンジルエステル (3. 7 g、 1 2ミリモル) を加えて 50°Cで 2時間加熱撹拌した。 室温に冷却した後、 氷水を加え、 酢酸ェチルで抽出した。 酢酸ェチル層を飽和食塩水で 1回洗浄した後、 無水硫酸ナトリゥムで乾燥し溶媒 を留去した。 析出した結晶をへキサンで洗浄し 4一 (2—二トロベンジル) 一 1 - (2—トリフルォロメチルフエニル) - 5 (4H) —テトラゾリノン (3. 8 g、 収率 94 %) を得た。
(3-2) . 4一 (2—ァミノベンジル) 一 1— (2—トリフルォロメチルフ ェニル) 一 5 (4H) —テトラゾリノンの合成 1- (2-Trifluoromethylphenyl) -5 (4H) monotetrazolinone (2.5 g, 11 mmol) and potassium carbonate (2.2 g, 16 mmol) were added to N, N-dimethylformamid. The resulting solution was dissolved and suspended in a solution (25 ml), and p-toluenesulfonic acid 2-nitrobenzyl ester (3.7 g, 12 mmol) was added. The mixture was heated with stirring at 50 ° C for 2 hours. After cooling to room temperature, ice water was added, and the mixture was extracted with ethyl acetate. The ethyl acetate layer was washed once with a saturated saline solution, dried over anhydrous sodium sulfate, and the solvent was distilled off. The precipitated crystals were washed with hexane to obtain 41- (2-nitrobenzyl) 1-1- (2-trifluoromethylphenyl) -5 (4H) -tetrazolinone (3.8 g , yield 94%). Was. (3-2). Synthesis of 4- (2-aminobenzyl) 1-1- (2-trifluoromethylphenyl) -5 (4H) -tetrazolinone
4 - (2—二トロべンジノレ) - 1 - (2— トリフルォロメチルフヱニル) —5 (4H) ーテトラゾリノン (2. 0 g、 5ミリモル) 、 塩化第一スズ 二水和物 (4. 9 g、 22ミリモル) をエタノール (20ml) と濃塩酸 (20m l) に 溶解し、 5時間加熱還流した。 室温に冷却した後に、 10%水酸化ナトリウム水 溶液を加えて反応液を塩基性にし、 酢酸ェチルで抽出した。 酢酸ェチル層を飽和 食塩水で 1回洗浄した後、 無水硫酸ナトリウムで乾燥し溶媒を留去した。 析出し た結晶をへキサンで洗浄し 4 _ (2—ァミノベンジル) 一 1— (2—トリフルォ ロメチルフエニル) 一 5 (4H) ーテトラゾリノン (1. 3 g、 収率 70%) を 得た。 4-(2-ditrobendinole)-1-(2-trifluoromethylphenyl)-5 (4H)-tetrazolinone (2.0 g, 5 mmol), stannous chloride dihydrate (4 (9 g, 22 mmol) was dissolved in ethanol (20 ml) and concentrated hydrochloric acid (20 ml), and the mixture was heated under reflux for 5 hours. After cooling to room temperature, a 10% aqueous sodium hydroxide solution was added to make the reaction solution basic, and the mixture was extracted with ethyl acetate. The ethyl acetate layer was washed once with a saturated saline solution, dried over anhydrous sodium sulfate, and the solvent was distilled off. The precipitated crystals were washed with hexane to obtain 4_ (2-aminobenzyl) 1-1- (2-trifluoromethylphenyl) -15 (4H) -tetrazolinone (1.3 g, yield 70%).
(3-3) . 1― (2—トリフルォロメチルフエニル) 一4一 (2—トリフル ォロメタンスルホニルァミノベンジル) ― 5 (4H) 一テトラゾリノン (化合物 No. 3-38) の合成 (3-3). Synthesis of 1- (2-trifluoromethylphenyl) 1-41- (2-trifluoromethanesulfonylaminobenzyl) -5 (4H) -tetrazolinone (Compound No. 3-38)
4一 (2—ァミノべンジノレ) — 1— (2—トリフルォロメチルフエニル) 一 5 (4H) —テトラゾリノン (0. 50 g、 1. 5ミリモル) とイミダゾール (0. 26 g、 3. 8ミリモル) をクロ口ホルム (7m l) に溶解した後、 反応溶液を 一 10°Cに冷却した。 ついでトリフルォロメタンスルホン酸無水物 (0. 55 g、 1. 9ミリモル) を 20分かけて滴下した。 そのままの温度で 2時間撹拌した後 に、 氷を加え、 さらに 6 N塩酸を加えて反応液を酸性にし、 酢酸ェチルで抽出し た。 酉乍酸ェチル層を飽和食塩水で 1回洗浄した後、 無水硫酸ナトリゥムで乾燥し 溶媒を留去した。 残渣をシリカゲルカラムクロマトグラフィー (へキサン:酢酸 ェチル = 2 : 1) で精製して 1一 (2—トリフルォロメチルフエニル) 一 4— (2— トリフルォロメタンスルホニルァミノベンジル) 一 5 (4H) —テトラゾ リノン (0. 2 g、 収率 29%) を得た。 融点は 95- 97°Cであった。 4- (2-aminobenzinole) — 1— (2-trifluoromethylphenyl) -1.5 (4H) —tetrazolinone (0.50 g, 1.5 mmol) and imidazole (0.26 g, 3. (8 mmol) was dissolved in chloroform (7 ml), and the reaction solution was cooled to 110 ° C. Then, trifluoromethanesulfonic anhydride (0.55 g, 1.9 mmol) was added dropwise over 20 minutes. After stirring at the same temperature for 2 hours, ice was added, and the reaction solution was acidified by further adding 6N hydrochloric acid, and extracted with ethyl acetate. The ethyl ester layer was washed once with a saturated saline solution, dried over anhydrous sodium sulfate, and the solvent was distilled off. The residue was purified by silica gel column chromatography (hexane: ethyl acetate = 2: 1) to give 11- (2-trifluoromethylphenyl) -14- (2-trifluoromethanesulfonylaminobenzyl) -15 ( 4H) -Tetrazolinone (0.2 g, yield 29%) was obtained. Melting point was 95-97 ° C.
実施例 4. Example 4.
(4— 1) . 2 - (2, 6—ジクロ口フエニル) 一 4— 〔2— (N—イソプロピ ルカルボ二ルー N—トリフルォロメタンスルホニルァミノベンジル) 〕 一 2, 4 ージヒ ドロ _3H_1, 2, 4—トリァゾールー 3—オンの合成 (化合物 No. 2
- 247) (4-1). 2-(2,6-Dichroic phenyl) 1-4-[2-(N-isopropylcarbonyl N-trifluoromethanesulfonylaminobenzyl)]-1,2,4-dihydro_3H_1, 2 Of 1,4-triazol-3-one (Compound No. 2 -247)
2― (2, 6—ジクロ口フエ二ノレ) -4- (2—トリフルォロメタンスノレホニ ルァミノベンジル) 一 2, 4ージヒ ドロー 3H— 1, 2, 4_トリァゾールー 3 一オン (0. 30 g、 0. 6ミ リモル) と トリエチルァミン (0. 07 g、 0. 7ミ リモル) をテトラヒ ドロフラン (20m l) に溶解し, 塩化イソプチリル (0. 08 g、 0. 7ミリモル) を加えて室温で 5時間撹拌した。 反応液を氷水 に注ぎ、 酢酸ェチルで抽出した。 酢酸ェチル層を飽和食塩水で 1回洗浄した後、 無水硫酸ナトリウムで乾燥し溶媒を留去した。 濃縮物をシリカゲル力ラムクロマ トグラフィー 〔n—へキサン一酢酸ェチル (1 : 1) 〕 で精製し、 2— (2, 6 ージクロ口フエ二ノレ) —4— 〔2— (N—ィソプロピルカルボニル一 N—トリフノレ ォロメタンスノレホニルァミノべンジノレ) ] - 2, 4ージヒ ドロ一 3 H— 1, 2, 4一トリァゾールー 3—オン (0. 25 g、 収率 72. 7%) を得た。 融点は 5 5. 6— 61. 9°Cであった。 2- (2,6-dichloromouth feninole) -4- (2-trifluoromethanesnorrehonylaminobenzyl) 1,2,4-dihydro 3H—1,2,4_triazole-3-one (0.30 g, 0.6 mmol) and triethylamine (0.07 g, 0.7 mmol) were dissolved in tetrahydrofuran (20 ml), and isobutyryl chloride (0.08 g, 0.7 mmol) was added. For 5 hours. The reaction solution was poured into ice water and extracted with ethyl acetate. The ethyl acetate layer was washed once with a saturated saline solution, dried over anhydrous sodium sulfate, and the solvent was distilled off. The concentrate is purified by silica gel column chromatography [n-hexane monoacetate (1: 1)] to give 2- (2,6-dichloromethane phenyl) —4— [2— (N-isopropyl Carbonyl-1-N-trif / n-trifluoromethanes / norefonylaminobenzinole)]-2,4-dihydro-13H-1,2,4-triazol-3-one (0.25 g, 72.7% yield) was obtained. Was. Melting point was 55.6-61.9 ° C.
(4-2) . N— (2, 6—ジクロロフエ二ノレ)一 N'— [2—(N—トリフノレオロメタン スルホ二ルー N—フエニルカルボニル)アミノベンジル ]ー2—ィミダゾリジノン (化合物 No.6- 363) (4-2). N— (2,6-dichloropheninole) -1-N ′ — [2- (N-triphlonorelomethane sulfonyl N-phenylcarbonyl) aminobenzyl] -2-imidazolidinone (Compound No. .6- 363)
N— (2, 6—ジクロ口フエニル)一 Ν'— (2—トリフルォロメタンスルホニルアミ ノベンジル)一2—イミダゾリジノン (0. 30g、 0. 64ミ リモル) と トリエ チルァミン (0. 07 g、 0. 70ミリモル) をテトラヒ ドロフラン (1 5 m l) に溶角军し、 ついでべンゾィノレクロリ ド (0. 09g、 0. 64ミ リモノレ) を加えて室温で 7時間攪拌した。 その後、 水を加えて、 酢酸ェチルで抽出した。 酢酸ェチル層を飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥し溶媒を留去し た。 ついでシリカゲルカラムクロマトグラフィーにて精製し、 N—(2, 6—ジク ロロフエ二ノレ)一N,一 [2— (N—トリフノレ才ロメタンスノレホニノレ一 N—フエ二ノレ力ノレ ボニル)ァミノベンジル]— 2—イミダゾリジノン (0. 09g、 収率 24. 6 %) を得た。 融点は 95— 97 °Cであった。 N— (2,6-dichloromouth phenyl) -1-Ν (2-trifluoromethanesulfonylaminobenzyl) -1-imidazolidinone (0.30 g, 0.64 mimol) and triethylamine (0.07 g) , 0.70 mmol) was dissolved in tetrahydrofuran (15 ml), benzoinolechloride (0.09 g, 0.64 millimonole) was added, and the mixture was stirred at room temperature for 7 hours. Thereafter, water was added, and the mixture was extracted with ethyl acetate. The ethyl acetate layer was washed with saturated saline, dried over anhydrous sodium sulfate, and the solvent was distilled off. Then, the residue is purified by silica gel column chromatography, and N- (2,6-dichlorophenol) -N, 1- [2- (N-triphenylphenol-methanosulfonylone-N-phenylphenol) aminoaminobenzyl] — 2-Imidazolidinone (0.09 g, yield 24.6%) was obtained. Melting point was 95-97 ° C.
本発明の一般式 (I) で表されるハロアルキルスルホンァニリ ド誘導体又はそ の塩類を有効成分として含有する除草剤は、 例えばィヌビエ (イネ科 1年生、 水 田の害草) 、 タマガヤッリ (力ャッリグサ科 1年生草、 水田の害草) 、 マツバイ
(力ャッリグサ科多年生草、 湿地、 水路、 水田に発生、 水田の多年生害草) 、 ゥ リカヮ (ォモダカ科、 水田、 湿地、 溝に発生する多年生害草) 、 ィヌホタルイHerbicides containing the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention or a salt thereof as an active ingredient include, for example, barnyardgrass (first-year grasshopper, paddy field weed), tamagayari (power plant). Grassicaceae 1st year grass, paddy field pests) (Perennial weeds in the scrophulariaceae, swamps, waterways, paddy fields, perennial weeds in paddy fields), ゥ Lika ヮ (perennial weeds that occur in paddy fields, paddy fields, wetlands, ditch),
(力ャッリグサ科多年生草、 水田、 湿地、 溝に発生) 、 スズメノテツボウ (イネ 科越年草、 水田裏作、 低湿地に発生) 、 カラスムギ (イネ科越年草、 平地、 荒地、 畑地に発生) 、 ョモギ (キク科多年生草、 山野、 畑地に発生) 、 メヒシバ (イネ 科 1年生草、 畑、 榭園地の強害草) 、 ギシギシ (タデ科多年生草、 畑地、 道端に 発生) 、 コゴメガャッリ (力ャッリグサ科 1年生草、 畑地の害草) 、 ァオビュ(Perennial grasses of the family Rapaceae, occurring in paddy fields, swamps and ditches), Sparrow frogs (occurring in grassy annuals, paddy cultivation, lowlands), oats (occurring in grasslands, flatlands, wastelands, and fields) ), Artemisia (Asteraceae perennial grass, occurring in the mountains and fields), Meishishiba (Poaceae first grade grass, field, 榭 強 榭 強 強 、) ギ ギ ギ ギ ギ タ タ タ (Polygonaceae perennials, fieldland, on the roadside) Carrariaceae (Annual grass, Upland grass), Aobu
(ヒュ科 1年生草、 空き地、 道端、 畑地に発生) 、 ォナモミ (キク科 1年生草、 畑地の害草) 、 ィチビ (ァオイ科 1年生草、 畑地の害草) 、 シロバナヨウシュチ ヨウセンアサガオ (ナス科 1年生草、 畑地の害草) 、 ォオイヌノフグリ (ゴマノ ハグサ科越年草、 畑地の害草) 、 ヤエムダラ (ァカネ科越年草、 畑地、 榭園地の 害草) 等の水田、 畑、 樹園地、 湿地等に発生する 1年生、 越年生及び多年生雑草 を除草するのに有用である。 特に水田における雑草防除に有効であり、 スルホ二 ルゥレア系除草剤抵抗性雑草等の難防除雑草を含む多くの雑草種に対する広い適 用性、 効果の持続性、.ィネ一水田雑草間の選択性幅が広レ、ことから水田用除草剤 として優れた性能を有する。 (Herbaceous annuals, vacant lots, roadsides, upland fields), Satomi (Asteraceae annuals, upland grasses), Ichibi (Aoaceae, 1st annual grasses, upland grasses), Paddy fields, such as (Solanaceae annual grass, field grass), Ooinoufuguri (Sesame grass family, grass field grass), Yaemdara (Gallaceae, grass field, grassland grass), etc. It is useful for weeding annual, multi-year and perennial weeds that occur in fields, orchards and wetlands. It is especially effective for controlling weeds in paddy fields, and has wide applicability to many weed species including difficult-to-control weeds such as sulfonylrea herbicide-resistant weeds, long-lasting effects, and selection between rice and paddy weeds. Due to its wide range of properties, it has excellent performance as a paddy field herbicide.
本発明の一般式 (I ) で表されるハロアルキルスルホンァニリ ド誘導体又はそ の塩類を有効成分として含有する除草剤は出芽前及び出芽後にある雑草に対して 優れた除草効果を示すことから、 有用植物の植え付け予定地に予め処理するとか、 有用植物の植え付け後 (有用植物が樹園のごとく既に定植されている場合を含 む) 雑草の発生始期から生育期に処理することにより本発明除草剤の有する特徴 ある生理活性を効果的に発現させることができる。 しかし本発明の除草剤はこの ような態様においてのみ使用されねばならないというものではなく、 例えば本発 明除草剤は水田用除草剤として使用することができるばかりでなく、 一般雑草の 除草剤としても使用することができ、 例えば刈り取り跡、 休耕田畑、 畦畔、 農道、 水路、 牧草造成地、 墓地、 公園、 道路、 運動場、 建物の周辺の空き地、 開墾地、 線路端、 森林等の一般雑草の駆除のために使用することもできる。 この場合、 雑 草の発生始期までに処理するのが経済的にも最も効果的であるが、 必ずしもこれ に限定されず、 生育期にある雑草をも防除することが可能である。
本発明の一般式 (I ) で表されるハロアルキルスルホンァニリ ド誘導体又はそ の塩類を除草剤として使用する場合、 農薬製剤上の常法に従い、 使用上都合の良 い形状に製剤して使用するのが一般的である。 即ち、 本発明の一般式 (I ) で表 されるハロアルキルスルホンァニリ ド誘導体又はその塩類は、 これらを適当な不 活性担体に、 又は必要に応じて補助剤と一緒に、 適当な割合に配合して溶解、 分 離、 懸濁、 混合、 含浸、 吸着若しくは付着させ、 適宜の剤形、 例えば懸濁剤、 乳 懸濁剤、 乳剤、 液剤、 水和剤、 粒剤、 粉剤、 錠剤、 ジャンボ剤、 パック剤等に製 剤して使用すれば良い。 Since the herbicide containing the haloalkylsulfonanilide derivative represented by the general formula (I) or a salt thereof as an active ingredient of the present invention exhibits an excellent herbicidal effect on weeds before and after emergence, The herbicide of the present invention can be treated in advance from the site where the useful plant is to be planted, or after planting the useful plant (including when the useful plant has already been planted like an orchard) from the initial stage of weed development to the growing stage. A characteristic physiological activity of the agent can be effectively exhibited. However, the herbicide of the present invention does not have to be used only in such an embodiment.For example, the herbicide of the present invention can be used not only as a paddy field herbicide but also as a general weed herbicide. It can be used for general weeds such as mowing traces, fallow fields, levees, farm roads, waterways, pasture lands, cemeteries, parks, roads, playgrounds, vacant lots around buildings, reclaimed land, track ends, forests, etc. It can also be used for extermination. In this case, it is most economically effective to treat weeds until the beginning of their emergence, but it is not necessarily limited to this, and weeds in the growing season can be controlled. When the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention or a salt thereof is used as a herbicide, it is formulated into a convenient form according to a conventional method for agricultural chemicals. It is common to do. That is, the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention or a salt thereof is blended with an appropriate inert carrier or, if necessary, together with an auxiliary in an appropriate ratio. Dissolving, separating, suspending, mixing, impregnating, adsorbing or adhering to the appropriate dosage form, for example, suspension, milk suspension, emulsion, solution, wettable powder, granule, powder, tablet, jumbo It can be used by preparing it into a preparation, pack, etc.
本発明で使用できる不活性担体としては固体又は液体の何れであっても良く、 固体の担体になり得る材料としては、 例えば植物質粉末類 (例えばダイズ粉、 穀 物粉、 木粉、 樹皮粉、 鋸粉、 タバコ茎粉、 タルミ殻粉、 ふすま、 繊維素粉末、 植 物エキス抽出後の残渣等) 、 粉碎合成樹脂等の合成重合体、 粘土類 (例えばカオ リン、 ベントナイト、 酸性白土等) 、 タルク類 {例えばタルク、 ピロフィライト 等) 、 シリカ類 (例えば珪藻土、 珪砂、 雲母、 ホワイトカーボン (含水微粉珪素、 含水珪酸ともいわれる合成高分散珪酸で、 製品により珪酸カルシウムを主成分と して含むものもある。 ) } 、 活性炭、 天然鉱物質類 (例えばィォゥ粉末、 軽石、 焼成珪藻土、 ァタパルジャィトおよびゼォライト等) 、 焼成珪藻土、 レンガ粉碎 物、 フライアッシュ、 砂、 プラスチック担体等 (例えばポリエチレン、 ポリプロ ピレン、 ポリ塩ィ匕ビ二リデン等) 、 炭酸カルシウム、 燐酸カルシウム等の無機鉱 物性粉末、 硫安、 燐安、 硝安、 尿素、 塩安等の化学肥料、 堆肥等を挙げることが でき、 これらは単独で若しくは二種以上の混合物の形で使用される。 The inert carrier that can be used in the present invention may be either solid or liquid. Materials that can be solid carriers include, for example, plant powders (eg, soybean flour, cereal flour, wood flour, bark flour) , Saw powder, tobacco stem powder, flour shell powder, bran, cellulose powder, residue after extraction of plant extracts, etc.), synthetic polymers such as ground synthetic resin, clays (eg kaolin, bentonite, acid clay) , Talc (for example, talc, pyrophyllite, etc.), silica (for example, diatomaceous earth, silica sand, mica, white carbon (synthetic high-dispersion silicic acid also referred to as hydrous fine silicon powder and hydrous silicic acid, containing calcium silicate as a main component depending on the product) )}, Activated carbon, natural minerals (eg, wool powder, pumice, calcined diatomaceous earth, attapulgite and zeolite, etc.), calcined diatomaceous earth, Brick crushed material, fly ash, sand, plastic carrier (for example, polyethylene, polypropylene, polyvinyl chloride, etc.), inorganic mineral powders such as calcium carbonate and calcium phosphate, ammonium sulfate, phosphorous ammonium, ammonium nitrate, urea, Chemical fertilizers such as salt and salt, compost and the like can be mentioned, and these are used alone or in the form of a mixture of two or more.
液体の担体になり得る材料としては、 それ自体溶媒能を有するものの他、 溶媒 能を有さずとも補助剤の助けにより有効成分化合物を分散させ得ることとなるも のから選択され、 例えば代表例として次に挙げる担体を例示できるが、 これらは 単独で若しくは 2種以上の混合物の形で使用され、 例えば水、 アルコール類 (例 えばメタノール、 エタノール、 ィソプロパノール、 ブタノーノレ、 エチレングリコ ール等) 、 ケトン類 (例えばアセトン、 メチルェチノレケトン、 メチルイソブチル ケトン、 ジイソプチルケトン、 シクロへキサノン等) 、 エーテル類 (例えばェチ ノレエーテル、 ジォキサン、 セロソノレブ、 ジプロピノレエーテノレ、 テトラヒ ロフラ
ン等) 、 脂肪族炭化水素類 (例えばケロシン、 鉱油等) 、 芳香族炭化水素類 (例 えばベンゼン、 トルエン、 キシレン、 ソルベントナフサ、 アルキルナフタレン 等) 、 ハロゲン化炭化水素類 (例えばジクロロェタン、 クロ口ホルム、 四塩化炭 素等) 、 エステノレ類 (例えば酢酸ェチル、 ジイソプピルフタレート、 ジブチルフ タレート、 ジォクチルフタレート等) 、 アミ ド類 (例えばジメチルホルムアミ ド、 ジェチルホルムアミ ド、 ジメチルァセトアミ ド等) 、 二トリル類 (例えばァセト 二トリノレ等) 、 ジメチルスルホキシド類等を挙げることができる。 The material that can be a liquid carrier is selected from those having a solvent function per se and those capable of dispersing the active ingredient compound with the aid of an adjuvant even without the solvent function. Examples thereof include the following carriers, which may be used alone or in the form of a mixture of two or more types. Examples thereof include water and alcohols (eg, methanol, ethanol, isopropanol, butanol, ethylene glycol, etc.). , Ketones (for example, acetone, methyl ethyl ketone, methyl isobutyl ketone, diisobutyl ketone, cyclohexanone, etc.), ethers (for example, ethyl ether ether, dioxane, cellosonoreb, dipropinole ethereol, tetrahydrofura) ), Aliphatic hydrocarbons (eg, kerosene, mineral oil, etc.), aromatic hydrocarbons (eg, benzene, toluene, xylene, solvent naphtha, alkylnaphthalene, etc.), halogenated hydrocarbons (eg, dichloroethane, Form, carbon tetrachloride, etc.), estenoles (eg, ethyl acetate, diisopropyl phthalate, dibutyl phthalate, dioctyl phthalate, etc.), amides (eg, dimethylformamide, getylformamide, dimethylacetate) Amides), nitriles (for example, acetate ditrinole), dimethyl sulfoxides, and the like.
他の捕助剤としては次に例示する代表的な捕助剤を挙げることができ、 これら の補助剤は目的に応じて使用され、 単独で、 ある場合は二種以上の補助剤を併用 し、 又ある場合には全く補助剤を使用しないことも可能である。 有効成分化合物 の乳化、 分散、 可溶化及び Z又は湿潤の目的のために界面活性剤が使用され、 例 えばポリォキシエチレンアルキルエーテル、 ポリオキシエチレンアルキルァリ一 ルエーテル、 ポリオキシエチレン高級脂肪酸エステル、 ポリオキシエチレン樹月旨 酸エステル、 ポリオキシエチレンソルビタンモノラウレート、 ポリオキシェチレ ンソルビタンモノォレエート、 アルキルァリールスルホン酸塩、 ナフタレンスル ホン酸縮合物、 リグニンスルホン酸塩、 高級アルコール硫酸エステル等の界面活 性剤を例示することができる。 As the other scavengers, there may be mentioned the following typical scavengers, and these scaffolds are used according to the purpose, and may be used alone or in combination of two or more kinds. It is also possible, in some cases, to use no auxiliaries. Surfactants are used for the purpose of emulsifying, dispersing, solubilizing and Z or wetting the active ingredient compounds, for example polyoxyethylene alkyl ethers, polyoxyethylene alkyl aryl ethers, polyoxyethylene higher fatty acid esters , Polyoxyethylene resin acid ester, polyoxyethylene sorbitan monolaurate, polyoxyethylene sorbitan monooleate, alkylaryl sulfonate, naphthalene sulfonate condensate, lignin sulfonate, higher alcohol sulfate, etc. The following surfactants can be exemplified.
又、 有効成分化合物の分散安定化、 粘着及び/又は結合の目的のために、 次に 例示する補助剤を使用することもでき、 例えばカゼイン、 ゼラチン、 澱粉、 メチ ルセルロース、 カルボキシメチルセルロース、 アラビアゴム、 ポリビニルアルコ ール、 松根油、 糠油、 ベントナイト、 リグニンスルホン酸塩等の補助剤を使用す ることもできる。 固体製品の流動性改良のために次に挙げる補助剤を使用するこ ともでき、 例えばワックス、 ステアリン酸塩、 燐酸アルキルエステル等の補助剤 を使用できる。 懸濁性製品の解こう剤として、 例えばナフタレンスルホン酸縮合 物、 縮合憐酸塩等の補助剤を使用することもできる。 消泡剤としては、 例えばシ リコーン油等の補助剤を使用することもできる。 For the purpose of stabilizing the dispersion of the active ingredient compound, adhering and / or binding, the following auxiliary agents may be used. For example, casein, gelatin, starch, methylcellulose, carboxymethylcellulose, gum arabic Auxiliaries such as polyvinyl alcohol, pine oil, bran oil, bentonite, and lignin sulfonate can also be used. The following adjuvants can be used to improve the flowability of the solid product. For example, adjuvants such as wax, stearate, and alkyl phosphate can be used. As peptizers for suspension products, auxiliary agents such as, for example, naphthalenesulfonic acid condensates, condensed salts and the like can also be used. As an antifoaming agent, for example, an auxiliary agent such as silicone oil can be used.
有効成分化合物の配合割合は必要に応じて加減することができ特に制限されな いが、 下限はおよそ 0 . 0 0 1重量%程度〜上限は 9 0重量%程度である。 例え ば粉剤或いは粒剤とする場合の下限は 0 . 0 1重量%程度が好ましく、 より好ま
しくは 0 . 1重量%程度、 上限は 5 0重量%程度が好ましく、 より好ましくは 1 0重量%程度であり、 乳剤、 水和剤或いは顆粒水和剤等とする場合の下限は 0 . 0 1重量%程度が好ましく、 より好ましくは 0 . 1重量%程度、 上限は 9 0重量 %程度が好ましく、 より好ましくは 6 0重量%程度である。 本発明の一般式 ( I ) で表されるハロアルキルスルホンァニリド誘導体又はその塩類を有効成分 として含有する除草剤は、 各種雑草を枯殺し若しくは生育を抑制するためにその まま、 又は水等で適宜希釈し、 若しくは懸濁させた形で殺草若しくは生育抑制に 有効な量を当該雑草に、 又は当該雑草の発生若しくは成育が好ましくない場所に おいて茎葉又は土壌に適用して使用すればよい。 The compounding ratio of the active ingredient compound can be adjusted as needed and is not particularly limited, but the lower limit is about 0.001% by weight to the upper limit is about 90% by weight. For example, the lower limit for powder or granules is preferably about 0.01% by weight, more preferably. About 0.1% by weight, and the upper limit is preferably about 50% by weight, more preferably about 10% by weight, and the lower limit when using an emulsion, a wettable powder or a water-dispersible granule is 0.0. It is preferably about 1% by weight, more preferably about 0.1% by weight, and the upper limit is preferably about 90% by weight, more preferably about 60% by weight. The herbicide containing the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention or a salt thereof as an active ingredient can be used as it is to kill various weeds or suppress the growth thereof, or can be used with water or the like. It may be used by appropriately diluting or suspending it and applying it to the weed in an amount effective for weed killing or growth inhibition, or to foliage or soil in places where the generation or growth of the weed is not desirable. .
本発明の一般式 (I ) で表されるハロアルキルスルホンァニリ ド誘導体又はそ の塩類を有効成分として含有する除草剤の使用量は種々の因子、 例えば目的、 対 象雑草、 作物の生育状況、 雑草の発生傾向、 天候、 環境条件、 剤型、 施用方法、 施用場所、 施用時期等により変動するが、 有効成分化合物として 1ヘクタール当 たり 0 . l g〜1 0 k gの範囲から目的に応じて適宜選択すれば良い。 本発明の一 般式 (I ) で表されるハロアルキルスルホンァニリド誘導体又はその塩類を有効 成分として含有する除草剤を更に防除対象雑草、 防除適期の拡大のため、 或いは 薬量の低減をはかる目的で他の除草剤と混合して使用することも可能である。 以下に本発明の代表的な製剤例及び試験例を示すが、 本発明はこれらに限定さ れるものではない。 尚、 製剤例中、 部とあるのは重量部を示す。 The amount of the herbicide containing the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention or a salt thereof as an active ingredient depends on various factors, for example, the purpose, the target weed, the growing condition of the crop, It varies depending on the weed occurrence tendency, weather, environmental conditions, dosage form, method of application, place of application, time of application, etc., but as an active ingredient compound, the range of 0.1 lg to 10 kg per hectare is appropriate according to the purpose. Just choose. The herbicide containing the haloalkylsulfonanilide derivative represented by the general formula (I) of the present invention or a salt thereof as an active ingredient is further used for controlling a weed to be controlled, extending a suitable period for controlling, or reducing the amount of drug. It is also possible to use it mixed with other herbicides for the purpose. The representative preparation examples and test examples of the present invention are shown below, but the present invention is not limited to these. In the preparation examples, “parts” means “parts by weight”.
製剤例 1 . Formulation Example 1.
本発明化合物 1 0部 Compound of the present invention 10 parts
7 0部 70 copies
N—メチノレピロリ ドン 1 0部 N-methinolepyrrolidone 10 parts
ポリオキシエチレンノニルフェニルエーテルと With polyoxyethylene nonyl phenyl ether
ァノレキノレベン 1 0部 Anolequinolene 10
以上を均一に混合溶解して乳剤とする c The above are uniformly mixed and dissolved to form an emulsion c
製剤例 2 . Formulation example 2.
本発明化合物 3部 Compound of the present invention 3 parts
クレー粉末 8 2部
珪藻土粉末 1 5部 以上を均一に混合粉碎して粉剤とする。 Clay powder 8 2 parts 15 parts of diatomaceous earth powder is uniformly mixed and ground to form a powder.
製剤例 3. Formulation example 3.
本発明化合物 5部 5 parts of the compound of the present invention
ベントナイトとクレーの混合粉末 90部 90 parts mixed powder of bentonite and clay
リグニンスノレホン酸カルシウム 5部 5 parts of calcium lignin snolenate
以上を均一に混合し、 適量の水を加えて混練し、 造粒、 乾燥して粒剤とする。 製剤例 4. The above components are uniformly mixed, kneaded by adding an appropriate amount of water, granulated and dried to obtain granules. Formulation example 4.
本発明化合物 20部 Compound of the present invention 20 parts
カオリンと合成高分散珪酸 75部 Kaolin and synthetic high dispersion silicic acid 75 parts
ポリオキシエチレンノニノレフヱニノレエーテノレと With polyoxyethylene noninolefin
アルキルべンゼンスルホン酸カルシゥムとの混合物 5部 5 parts mixture with calcium alkylbenzene sulfonate
以上を均一に混合粉薛して水和剤とする。 The above is uniformly mixed to form a wettable powder.
試験例 1. 出芽前の水田雑草に対する除草効果試験 Test Example 1. Test of herbicidal effect on paddy field weeds before emergence
7 5 cm2のプラスチックポットに土壌 (埴壌土) を充填し、 水田雑草である ィヌビエ、 ィヌホタルイの種子を播種し、 ァゼナの種子を混和した土壌 7 was filled with 5 soil plastic pots cm 2 (clay loam), a paddy weed Inubie, seeds Inuhotarui were seeded and mixed seeds Azena soil
7 5 c m3で覆土した後、 水深 5 cmの状態に湛水した。 翌日に、 製剤例 1から 4に準じて調製した本発明化合物 (第 1表から第 1 3表に記載の化合物) を有効 成分とする薬剤の所定有効薬量 (gZha) を水で希釈し水面に滴下処理をした。 ついで、 温室内で育成し、 処理 2 1日後に除草効果を調査し、 無処理と比較して、 下記の基準に従って除草効果を評価した。 After covering the soil with 75 cm 3, it was flooded to a depth of 5 cm. On the next day, dilute a prescribed effective dose (gZha) of a drug containing the compound of the present invention (compounds listed in Tables 1 to 13) prepared according to Formulation Examples 1 to 4 with water, and dilute with water. Was dropped. Then, the plants were grown in a greenhouse, and after 21 days from the treatment, the herbicidal effect was investigated.
除草効果 (生育抑制程度) 及び薬害の判定基準。 Judgment criteria for herbicidal effect (growth suppression degree) and chemical injury.
4 . . . 90%〜1 00%の除草効果、 薬害。 4... 90% ~ 100% herbicidal effect, phytotoxicity.
3 . . . 70%〜8 9%の除草効果、 薬害。 3... 70% ~ 89% herbicidal effect, phytotoxicity.
2 . · · 40%〜69%の除草効果、 薬害。 2. · · 40% to 69% herbicidal effect, phytotoxicity.
1 . · . 1 %〜3 9%の除草効果、 薬害。 1. ·. 1% to 39% herbicidal effect, phytotoxicity.
0 • · · 0%の除草効果、 薬害。 0 • · · 0% herbicidal effect, phytotoxicity.
結果を第 1 5表に示す。 The results are shown in Table 15.
尚、 表中の 「Z」 は試験未実施を示す。
1 5表 “Z” in the table indicates that the test was not performed. 1 5 Table
ィメヒェ ィヌホタノレィ Imeje Inukhotanoree
1-8 1000 1 4 0 1-8 1000 1 4 0
1-23 1000 1 4 41-23 1000 1 4 4
1-27 1000 1 4 41-27 1000 1 4 4
1-28 1000 1 4 41-28 1000 1 4 4
1-29 1000 1 4 41-29 1000 1 4 4
1-30 1000 0 4 41-30 1000 0 4 4
1-32 1000 1 4 41-32 1000 1 4 4
1-36 1000 1 4 41-36 1000 1 4 4
1-38 1000 1 4 41-38 1000 1 4 4
1-40 1000 1 4 41-40 1000 1 4 4
1-41 1000 1 4 41-41 1000 1 4 4
1-43 1000 1 4 41-43 1000 1 4 4
1-44 1000 1 4 41-44 1000 1 4 4
1-47 1000 1 4 41-47 1000 1 4 4
1-50 1000 1 4 41-50 1000 1 4 4
1-59 1000 1 4 41-59 1000 1 4 4
1-81 1000 1 4 41-81 1000 1 4 4
1-84 1000 1 4 41-84 1000 1 4 4
1-88 1000 / 4 41-88 1000/4 4
1-89 1000 1 4 41-89 1000 1 4 4
1-90 1000 / 4 41-90 1000/4 4
1 - 91 1000 / 4 41-91 1000/4 4
1-92 1000 / 4 41-92 1000/4 4
1-93 1000 1 4 41-93 1000 1 4 4
1-94 1000 / 4 41-94 1000/4 4
1-95 1000 1 4 41-95 1000 1 4 4
1-102 1000 1 4 41-102 1000 1 4 4
1-103 1000 1 4 41-103 1000 1 4 4
1-107 1000 1 4 41-107 1000 1 4 4
1-108 1000 1 4 4 1-108 1000 1 4 4
ι ι
1-112 1000 I 4 4 1-112 1000 I 4 4
1 丄ー丄 I I 1 page I I
1-124 1000 1 4 41-124 1000 1 4 4
1-165 1000 1 4 41-165 1000 1 4 4
1-177 1000 1 4 41-177 1000 1 4 4
1-183 1000 1 4 01-183 1000 1 4 0
1-189 1000 1 4 11-189 1000 1 4 1
1-190 1000 1 4 11-190 1000 1 4 1
1-192 1000 4 4 4
1 5表 (続き) 1-192 1000 4 4 4 1 5 Table (continued)
ノ マ 、、" マ 2j ァ 、 + ス Αίヽクノレ Noma ,, "Ma 2j, +
^gai/na ^ gai / na
丄 丄 ο 丄 UUU 1 4 4 QQ 丄 丄 ο 丄 UUU 1 4 4 QQ
丄ー丄 8 Ί 1 1 丄 丄 8 Ί 1 1
4 4 4 4
1 1 丄ー丄 yy 丄 UUU 1 4 1 丄ー ib 丄 UUU 4 4 4 1 1 丄 ー yy 丄 UUU 1 4 1 丄 ー ib 丄 UUU 4 4 4
1 1
丄ー r / 丄 UUU 1 4 4 R r / 丄 UUU 1 4 4
1 1
1~ 4ο 丄 UUU 1 n 1 ~ 4ο 丄 UUU 1 n
I 4 o rr 1 I 4 o rr 1
lUUU 1 4 4 lUUU 1 4 4
1 1
1- 54 lUUU 1 4 4 1- 54 lUUU 1 4 4
1 1
l~Zb( lUUU 1 4 4l ~ Zb (lUUU 1 4 4
1一 258 1000 1 4 4 o * 1 1 258 1000 1 4 4 o *
1一 265 lUUU 4 4 4 1 265 lUUU 4 4 4
1 1
1UU0 1 4 4 1UU0 1 4 4
1 1
1-268 1000 1 4 4 1-268 1000 1 4 4
1 1
1-273 1000 1 4 4 1-273 1000 1 4 4
1 1
1- 79 1UU0 / 4 4 1- 79 1UU0 / 4 4
1-282 1000 1 4 4 1-282 1000 1 4 4
1 1
丄ー 285 1000 1 4 4 r r r\ 1 丄 285 1000 1 4 4 r r r \ 1
1一 28b Ιϋϋυ I 4 4 r rr 1 1 1 28b Ιϋϋυ I 4 4 r rr 1
1一 88 lUUU 1 1 1 on 1 1 88 lUUU 1 1 1 on 1
l- yi lUUU 1 4 4 l- yi lUUU 1 4 4
1 1
1- y Ιϋϋϋ 1 4 4 o rr 1 1- y Ιϋϋϋ 1 4 4 o rr 1
1~όΖ oo r\ 1 ~ όΖ oo r \
ό lUUU 1 ϋ ό lUUU 1 ϋ
rrr rrr
1 1
lUUU 1 1 lUUU 1 1
4 1 o 1 1 4 1 o 1 1
丄一 o o lUUU 4 4 o o 丄 一 o o lUUU 4 4 o o
lUUU 1 1 1 o- ny lUUU 1 4 4 lUUU 1 1 1 o-ny lUUU 1 4 4
1 1
丄 UUli 1 4 4 厶 lUUU 丄 UUli 1 4 4 m lUUU
1 1
1 t - 7 丄 A A A 1 t-7 丄 A A A
2-29 1000 4 4 4 2-29 1000 4 4 4
2-30 1000 1 4 42-30 1000 1 4 4
2-36 1000 1 4 42-36 1000 1 4 4
2-37 1000 I 4 42-37 1000 I 4 4
2-38 1000 1 4 42-38 1000 1 4 4
2—41 1000 1 4 4
1 5表 (続き) 2—41 1000 1 4 4 1 5 Table (continued)
ノ マ 、ェ No, no
荣里 ノ マ rfr Ryori Noma Rfr
小ク7ノレ Small 7
O C O C
o ^gai/ na o ^ gai / na
丄 uuu 1 1 4 4 丄 uuu 1 1 4 4
1丄 U/UΠD 1 1 1 1 1 1 丄 U / UΠD 1 1 1 1 1
Ζ b丄 丄 (J(JU 1 1 4 4 C O Ζ b 丄 丄 (J (JU 1 1 4 4 C O
丄 UUtJ 1 1 1 丄 UUtJ 1 1 1
4 1 — b4 丄 U(JU 1 1 4 1 — b4 丄 U (JU 1 1
4 4 ο c 1 4 4 ο c 1
1 1
1UUU 1 4 4 1UUU 1 4 4
1 1 1 1
- by luUU 1 4 -by luUU 1 4
1 I 4 1 1 I 4 1
O- i 1 1UUU 1 4 4O- i 1 1UUU 1 4 4
Δ- ( Δ 1UUU I 4 4 Δ- (Δ 1UUU I 4 4
1 1
-" 1UUU 1 4 4 -"1UUU 1 4 4
1 1 1 1
2-76 lUUU 1 4 4 2-76 lUUU 1 4 4
1 1
2-79 lUUU 1 1 ο 4 2-79 lUUU 1 1 ο 4
2-81 lUUU 1 4 4 2-81 lUUU 1 4 4
1 1
2-82 l 1 UUU 1 4 1 2-82 l 1 UUU 1 4 1
2-83 lUUU 1 4 4 2-83 lUUU 1 4 4
1 1
2-85 lUUU I 4 4 丄 (J(JU 1 4 4 2-85 lUUU I 4 4 丄 (J (JU 1 4 4
2-98 丄 UUU 1 1 ¾ υ 丄 UUU 丄 t t-167 ΠΠΠ 1 1 t 1 1-169 1丄 u ΠΠuΠu o 2-98 丄 UUU 1 1 ¾ 丄 丄 UUU 丄 t t-167 ΠΠΠ 1 1 t 1 1-169 1 丄 u ΠΠuΠu o
-176 1丄 Π L/ΠUΠU-176 1 丄 Π L / ΠUΠU
-177 丄 Π L/ΠUΠU 1 1-177 丄 Π L / ΠUΠU 1 1
-184 1000 1 4 4-185 1000 1 4 4-186 1000 1 4 4-205 1000 1 1 /-209 1000 4 4 4-221 1000 4 4 4-227 1000 2 4 1
第 1 5表 (続き) -184 1000 1 4 4-185 1000 1 4 4-186 1000 1 4 4-205 1000 1 1 / -209 1000 4 4 4-221 1000 4 4 4-227 1000 2 4 1 Table 15 (continued)
! 旦 ノ レ、、 ! One day,
1 喿里 ィメヒェ ィヌホグノレイ ノ す 寸 1 喿 ヒ メ 寸
寸 ^gai/ha Dimension ^ gai / ha
1000 1 4 4 1000 1 4 4
2-245 1000 1 1 42-245 1000 1 1 4
2-246 1000 1 4 42-246 1000 1 4 4
2-247 1000 1 4 4 八八八 2-247 1000 1 4 4 888
3-2 1000 1 4 4 3-2 1000 1 4 4
3-3 1000 1 4 43-3 1000 1 4 4
3-4 1000 1 4 43-4 1000 1 4 4
3-5 1000 1 4 43-5 1000 1 4 4
3-6 1000 1 4 43-6 1000 1 4 4
3-8 1000 1 4 43-8 1000 1 4 4
3 - 13 1000 1 4 43-13 1000 1 4 4
3-18 1000 / 4 43-18 1000/4 4
3-19 1000 / 4 43-19 1000/4 4
3-22 1000 4 4 43-22 1000 4 4 4
3-23 1000 1 4 43-23 1000 1 4 4
3-24 1000 1 4 43-24 1000 1 4 4
3-25 1000 1 4 43-25 1000 1 4 4
3-29 1000 1 4 43-29 1000 1 4 4
3-32 1000 1 4 43-32 1000 1 4 4
3 - 36 1000 1 4 43-36 1000 1 4 4
3 - 37 1000 1 4 43-37 1000 1 4 4
3-38 1000 1 4 43-38 1000 1 4 4
3 - 46 1000 1 4 43-46 1000 1 4 4
3 - 47 1000 1 4 43-47 1000 1 4 4
3 - 48 1000 1 4 43-48 1000 1 4 4
3-49 1000 1 1 43-49 1000 1 1 4
3 - 53 1000 1 4 43-53 1000 1 4 4
3 - 61 1000 1 1 43-61 1000 1 1 4
3 - 79 1000 1 3 43-79 1000 1 3 4
3 - 80 1000 1 4 43-80 1000 1 4 4
3-83 1000 1 1 13-83 1000 1 1 1
3-156 1000 1 4 43-156 1000 1 4 4
3-157 1000 1 1 13-157 1000 1 1 1
3-158 1000 1 4 43-158 1000 1 4 4
3-159 1000 / 4 13-159 1000/4 1
3-160 1000 1 4 13-160 1000 1 4 1
3-161 1000 1 4 43-161 1000 1 4 4
3-162 1000 1 4 43-162 1000 1 4 4
3-163 1000 1 4 43-163 1000 1 4 4
3-164 1000 1 4 4
1 5表 (続き) 3-164 1000 1 4 4 1 5 Table (continued)
里 ノ 、、ェ 1 AIヽ ノレ z| ァゼ+ ノ し ソ 丄 00 丄 UUU 1 1 ノ 、 ヽ ヽ ヽ ヽ ヽ ヽ ヽ 00 丄 UUU 1
/ 丄 Δ ο 丄 ΌΌ 丄 uuu 1 / 丄 Δ ο 丄 ΌΌ uu uuu 1
1 4 4 丄 0 丄 uuu / 0 1 4 4 丄 0 丄 uuu / 0
1 4 14
0 丄 TO ΛΠΠ 0 丄 TO ΛΠΠ
丄 UiJU 1 / 1 丄 UiJU 1/1
丄/ u 1 ΛΑΛ 1 丄 / u 1 ΛΑΛ 1
1 丄 u ύ 丄 ί丄 lUDU 1 1 丄 u ύ 丄 ί 丄 lUDU 1
I 1 1 I 1 1
Q 上 79 / Q top 79 /
1 A 1 A
i (J i (J
Q 1 7 ◦ 3_丄 ί Q Q 1 7 ◦ 3_ 丄 ί Q
ό 丄 UUU 1 4 4 d 丄 ( 丄 (JUL) 1 ό 4 ό 丄 UUU 1 4 4 d 丄 (丄 (JUL) 1 ό 4
3 丄 ί 0 1 3 丄 ί 0 1
丄 (JUL! 1 4 4 丄 (JUL! 1 4 4
3 1 3 1
丄 り 1 4 4 丄 1 4 4
1 1
3 丄 ( I 1 4 4 3 丄 (I 1 4 4
1 1
3 丄 /^ 丄 UUU 1 4 4 3 丄 / ^ 丄 UUU 1 4 4
O 1C\ 1 O 1C \ 1
丄 y lUtJU 1 1 4 ο 丄 y lUtJU 1 1 4 ο
1 4 14
Q Q Q Q
丄 uuu 1 丄 uuu 1
1 4 4 1 4 4
1 1
όー丄 8 丄 (J (J (J 1 4 4 丄 丄 8 丄 (J (J (J 1 4 4
1 1
丄 (JUL) 1 4 4 丄 (JUL) 1 4 4
Q 1 ΛΛΠ 1 Q 1 ΛΛΠ 1
1 1 4 1 1 4
3 1 ΛΛ 3 1 ΛΛ
丄 8o Λ 1 丄 8o Λ 1
1 4 4 ー 1丄 4 A 1 4 4 ー 1 丄 4 A
丄 ΙΙϋϋ 4 4 4 y 1 丄 ΙΙϋϋ 4 4 4 y 1
I 4 4 I 4 4
0 0 丄 uuu 1 0 0 丄 uuu 1
1 4 4 1 4 4
0 丄 1 丄 0 丄 1 丄
1 Q 1 Q
ϋ 丄リリリ 1 1 1 ϋ 丄 Lilyli 1 1 1
1 u o 丄リリ VJ 1 1 1 u o 丄 lily VJ 1 1
1 ooo /1 1 ooo / 1
U 1 1 tU 1 1 t
Ό 丄 U 1 Ό 丄 U 1
Ό / 丄 L UU 1 Ό / 丄 L UU 1
1 t 4 1 t 4
Ό-28 ιυυυ 1 Ό-28 ιυυυ 1
1 4 4 1 4 4
6-29 1000 1 4 46-29 1000 1 4 4
6-32 1000 1 4 46-32 1000 1 4 4
6-33 1000 1 4 46-33 1000 1 4 4
6-60 1000 4 4 46-60 1000 4 4 4
6-62 1000 1 4 46-62 1000 1 4 4
6-73 1000 1 4 4
1 5表 (続き) 6-73 1000 1 4 4 1 5 Table (continued)
ィヌビエ ィメホタノレイ 7セナ Inubiye Imhotanorei 7 Senna
(gai/ha) (gai / ha)
6-82 1000 1 4 4 6-82 1000 1 4 4
6-83 1000 1 4 4 -113 1000 4 4 4 -339 1000 1 4 4 -340 1000 1 4 4 -341 1000 1 4 4 -342 1000 1 4 4 -343 1000 1 4 4 -344 1000 1 4 4 -345 1000 1 4 4 -346 1000 1 4 4 -347 1000 1 1 1
6-83 1000 1 4 4 -113 1000 4 4 -339 1000 1 4 4 -340 1000 1 4 4 -341 1000 1 4 4 -342 1000 1 4 4 -343 1000 1 4 4 -344 1000 1 4 4- 345 1000 1 4 4 -346 1000 1 4 4 -347 1000 1 1 1
-349 1000 1 4 4 - 350 1000 1 4 4 - 351 1000 1 4 4 -349 1000 1 4 4-350 1000 1 4 4-351 1000 1 4 4
1000 / 4 4 1000/4 4
1000 1 4 4 -354 1000 1 4 4 -355 1000 1 4 4 -356 1000 1 4 4 -357 1000 1 4 4 -358 1 4 4 -359 1 1000 1 4 4 -354 1000 1 4 4 -355 1000 1 4 4 -356 1000 1 4 4 -357 1000 1 4 4 -358 1 4 4 -359 1
XtJUU 1 4 4 - 360 ι XtJUU 1 4 4-360 ι
1 4 4 -361 1 / 1 1 4 4 -361 1/1
1 1 1 -362 1 1 1 1 -362 1
1 1 -363 1 1 1 -363 1
1 1 -364 1000 1 / 1 -365 1000 I 1 1 -366 1000 1 1 1 -367 1000 1 1 1 -368 1000 1 1 1 -369 1000 1 1 1 -370 1000 1 1 1 -371 1000 1 1 1 -372 1000 / 1 1 - 373 1000 1 1 1 -374 1000 1 1 1 -375 1000 1 / 1
5表 (続き) 1 1 -364 1000 1/1 -365 1000 I 1 1 -366 1000 1 1 1 -367 1000 1 1 1 -368 1000 1 1 1 -369 1000 1 1 1 -370 1000 1 1 1 -371 1000 1 1 1 -372 1000/1 1-373 1000 1 1 1 -374 1000 1 1 1 -375 1000 1/1 Table 5 (continued)
o 薬量 ィヌビエ ィヌホタルイ ァセナ o Pharmaceutical dosage
(gai/ha) (gai / ha)
-376 1000 1 1 1-377 1000 1 1 1-378 1000 1 1 1-379 1000 1 1 1-380 1000 1 1 1-381 1000 1 1 1-382 1000 1 4 1-383 1000 1 4 0-60 1000 1 4 4-217 1000 1 4 2-56 1000 1 4 4-56 1000 1 3 4 0-1 1000 1 1 1 0-2 1000 1 4 4 0-8 1000 4 4 40 - 12 1000 4 4 40-13 1000 2 4 40-14 1000 2 4 40-15 1000 4 4 40-16 1000 4 4 40-17 1000 4 4 40 - 18 1000 4 4 40—19 1000 4 4 4 -376 1000 1 1 1-377 1000 1 1 1-378 1000 1 1 1-379 1000 1 1 1-380 1000 1 1 1-381 1000 1 1 1-382 1000 1 4 1-383 1000 1 4 0-60 1000 1 4 4-217 1000 1 4 2-56 1000 1 4 4-56 1000 1 3 4 0-1 1000 1 1 1 0-2 1000 1 4 4 0-8 1000 4 4 40-12 1000 4 4 40- 13 1000 2 4 40 -14 1000 2 4 40 -15 1000 4 4 40 -16 1000 4 4 40 -17 1000 4 4 40-18 1000 4 4 40 -19 1000 4 4 4
1UUU 4 4 40-21 Ιϋϋϋ 1 4 40-23 1000 1 4 10-24 1000 1 4 40-26 1000 1 4 10-28 1000 1 4 10-29 1000 1 4 40-34 1000 1 4 40-35 1000 1 4 40-37 1000 0 4 40-39 1000 1 4 40-40 1000 1 4 40-58 1000 1 1 10-59 1000 1 1 1-116 1000 1 4 4 1 - 7 1000 4 4 41-11 1000 1 4 4
第 1 5表 (続き) 1UUU 4 4 40-21 Ιϋϋϋ 1 4 40-23 1000 1 4 10-24 1000 1 4 40-26 1000 1 4 10-28 1000 1 4 10-29 1000 1 4 40-34 1000 1 4 40-35 1000 1 4 40-37 1000 0 4 40-39 1000 1 4 40-40 1000 1 4 40-58 1000 1 1 10-59 1000 1 1 1-116 1000 1 4 4 1-7 1000 4 4 41-11 1000 1 4 Four Table 15 (continued)
ィヌビエ ィヌホタノレイ ァゼナ Inubietinouhotanorei Azena
(gai/ha) (gai / ha)
11-23 1000 1 4 4 11-23 1000 1 4 4
12-1 1000 1 4 4 12-1 1000 1 4 4
12-4 1000 4 4 4 12-4 1000 4 4 4
12 - 7 1000 4 4 4 試験例 2 . 出芽後の水田雑草に対する除草効果試験 12-7 1000 4 4 4 Test example 2. Test on herbicidal effect on paddy field weeds after emergence
7 5 c m2のプラスチックポットに土壌 (埴壌土) を充填し、 水田雑草である ィヌビエ、 ィヌホタルイの種子を播種し、 ァゼナの種子を混和した土壌 7 5 c m3で覆土した後、 水深 5 c mの状態に湛水し、 温室内で育成した。 供試植物 がー葉期の時期に、 本発明化合物 (第 1表から第 1 3表に記載の化合物) を有効 成分とする薬剤を所定有効薬量 (g Z h a ) の薬液として処理をした。 ついで、 温室内で育成し、 処理 2 1日後に除草効果を調査し、 無処理と比較して、 試験例 1の基準に従つて除草効果を評価した。 結果を第 1 6表に示す。
7 was filled with 5 soil plastic pots cm 2 (clay loam), a paddy weed Inubie, and sown Inuhotarui, after cover soil in soil 7 5 cm 3 was mixed seeds Azena, water depth 5 cm It was submerged in water and grown in a greenhouse. During the leaf stage of the test plant, a drug containing the compound of the present invention (compounds listed in Tables 1 to 13) as an active ingredient was treated as a drug solution having a predetermined effective dose (gZha). . Then, the plants were grown in a greenhouse, and the herbicidal effect was investigated 21 days after the treatment. The results are shown in Table 16.
6表 Table 6
薬量(gai/ha) ィヌビエ ィヌホタルイ ァゼナ Dosage (gai / ha)
1-2 1000 4 4 2 1-8 1000 3 4 4 1-23 1000 4 4 4 1-27 1000 4 4 4 1-28 1000 1 4 4 1-29 1000 4 4 4 1-30 1000 4 4 4 1-32 1000 4 4 4 1-36 1000 4 4 4 1-38 1000 4 4 4 -40 1000 4 4 4 1-41 1000 4 4 4 1-43 1000 3 4 4 1-44 1000 4 4 4 1-47 1000 4 4 4 -50 1000 4 4 4 -59 1000 4 4 4 1-81 1000 0 •4 4 -84 1000 4 4 4 -88 1000 4 4 4 -89 1000 4 4 4 -90 1000 1 4 4 -91 1000 I I 4 -92 1000 4 4 4 -93 1000 4 4 4 -94 1000 4 4 4 -95 1000 4 4 4-102 1000 4 4 4-103 1000 2 4 4-107 1000 4 4 4-108 1000 4 4 4-112 1000 1 4 4-123 1000 4 I-124 1000 4 4 4-165 1000 2 4 4-177 1000 3 4 4-183 1000 4 4 4-189 1000 4 4-190 1000 4 4 4-192 1000 4 4 4-193 1000 I 4 4
6表 (続き) 1-2 1000 4 4 2 1-8 1000 3 4 4 1-23 1000 4 4 4 1-27 1000 4 4 4 1-28 1000 1 4 4 1-29 1000 4 4 4 1-30 1000 4 4 4 1 -32 1000 4 4 4 1-36 1000 4 4 4 1-38 1000 4 4 4 -40 1000 4 4 4 1-41 1000 4 4 4 1-43 1000 3 4 4 1-44 1000 4 4 4 1-47 1000 4 4 4 -50 1000 4 4 4 -59 1000 4 4 4 1-81 1000 0 • 4 4 -84 1000 4 4 4 -88 1000 4 4 4 -89 1000 4 4 4 -90 1000 1 4 4 -91 1000 II 4 -92 1000 4 4 4 -93 1000 4 4 -94 1000 4 4 4 -95 1000 4 4 4-102 1000 4 4 4-103 1000 2 4 4-107 1000 4 4 4-108 1000 4 4 4-112 1000 1 4 4-123 1000 4 I-124 1000 4 4 4-165 1000 2 4 4-177 1000 3 4 4-183 1000 4 4 4-189 1000 4 4-190 1000 4 4 4-192 1000 4 4 4-193 1000 I 4 4 Table 6 (continued)
薬量 (gai/ha) ィヌビエ ィヌホタルイ ァゼナ-198 1000 4 4 4-199 1000 4 4 4-215 1000 3 4 4-237 1000 4 4 4-245 1000 0 4 3-251 1000 4 4 4-254 1000 4 4 4-257 1000 4 4 I-258 1000 I 4 4- 265 1000 4 4 4-266 1000 4 4 4-268 1000 3 4 4-273 1000 2 4 4-279 1000 0 4 3-282 1000 0 4 4-285 1000 0 4 2-286 1000 2 4-288 1000 I /-291 1000 2 4 4-292 1000 1 4 4-323 1000 0 0 3-324 1000 0 0 4-325 1000 1 4 4-326 1000 2 4 4-327 1000 2 4 I- 328 1000 4 4 4 Dosage (gai / ha) 4 4-257 1000 4 4 I-258 1000 I 4 4-265 1000 4 4 4-266 1000 4 4 4-268 1000 3 4 4-273 1000 2 4 4-279 1000 0 4 3-282 1000 0 4 4 -285 1000 0 4 2-286 1000 2 4-288 1000 I / -291 1000 2 4 4-292 1000 1 4 4-323 1000 0 0 3-324 1000 0 0 4-325 1000 1 4 4-326 1000 2 4 4-327 1000 2 4 I- 328 1000 4 4 4
2- 8 1000 1 4 4 2-9 1000 4 4- 12 1000 0 4 4-23 1000 4 4 4-24 1000 4 4 4-27 1000 4 4 4-28 1000 1 4 4-29 1000 2 4 4-30 1000 4 4 4 - 36 1000 4 4 4-37 1000 2 4 4-38 1000 4 4 4-41 1000 2 4 4-43 1000 4 4 4-51 1000 3 4 4
1 6表 (続き) 2-8 1000 1 4 4 2-9 1000 4 4-12 1000 0 4 4-23 1000 4 4 4-24 1000 4 4 4-27 1000 4 4 4-28 1000 1 4 4-29 1000 2 4 4- 30 1000 4 4 4-36 1000 4 4 4-37 1000 2 4 4-38 1000 4 4 4-41 1000 2 4 4-43 1000 4 4 4-51 1000 3 4 4 1 6 Table (continued)
薬量(gai/ha) ィヌビエ ィヌホタルイ ァゼナ Dosage (gai / ha)
2-60 1000 1 2-60 1000 1
2-61 1000 0 4 2-61 1000 0 4
2-63 1000 4 4 2-63 1000 4 4
2-64 1000 4 2-64 1000 4
2-65 1000 4 4 4 2-66 1000 4 4 4 2-67 1000 2 4 4 2-68 1000 4 4 4 2-69 1000 1 2 4 2-70 1000 4 4 4 2-71 1000 4 4 4 2-72 1000 0 4 4 2-73 1000 4 4 I 2-76 1000 4 4 4 2-79 1000 0 4 4 2-81 1000 3 4 4 2-82 1000 1 4 I 2 - 83 1000 0 4 4 2-85 1000 4 4 4 2-86 1000 3 4 4 -87 1000 4 4 4 -88 1000 42-65 1000 4 4 4 2-66 1000 4 4 4 2-67 1000 2 4 4 2-68 1000 4 4 4 2-69 1000 1 2 4 2-70 1000 4 4 4 2-71 1000 4 4 4 2 -72 1000 0 4 4 2-73 1000 4 4 I 2-76 1000 4 4 4 2-79 1000 0 4 4 2-81 1000 3 4 4 2-82 1000 1 4 I 2-83 1000 0 4 4 2- 85 1000 4 4 4 2-86 1000 3 4 4 -87 1000 4 4 4 -88 1000 4
-92 1000 / -92 1000 /
-93 1000 4 4 -93 1000 4 4
-94 1000 1 4 4 -98 1000 1 4 2-130 1000 0 4 4-167 1000 4 4 I-169 1000 4 4-176 1000 4 4 4-177 1000 4 4 4-184 1000 4 4 4-185 1000 4 4-186 1000 4 4-205 1000 I I-209 1000 1 4 4-221 1000 4 4 4-227 1000 1 4 I-244 1000 2 4-245 1000 1 0 4-246 1000 2 4 4
6表 (続き) -94 1000 1 4 4 -98 1000 1 4 2-130 1000 0 4 4-167 1000 4 4 I-169 1000 4 4-176 1000 4 4 4-177 1000 4 4 4-184 1000 4 4 4-185 1000 4 4-186 1000 4 4-205 1000 I I-209 1000 1 4 4-221 1000 4 4 4-227 1000 1 4 I-244 1000 2 4-245 1000 1 0 4-246 1000 2 4 4 Table 6 (continued)
薬量(gai/ha) ィヌビエ ィヌホタルイ ァゼナ - 247 1000 4 4 3-2 1000 4 4 3 3-3 1000 2 4 4 3-4 1000 2 4 4 3-5 1000 0 4 3 3-6 1000 0 4 4 3-8 1000 3 4 4 Dosage (gai / ha) 3-8 1000 3 4 4
3- 13 1000 2 4 4 3-18 1000 4 4 4 3-19 1000 4 4 4 3 - 22 1000 4 4 4 3-23 1000 0 4 3-24 1000 1 4 3-25 1000 3 4 4 3-29 1000 4 4 4 3-32 1000 2 4 4 3-36 1000 I 4 4 3-37 1000 1 4 4 -38 1000 2 4 4 -46 1000 4 4 4 -47 1000 1 4 4 -48 1000 1 4 4 -49 1000 03-13 1000 2 4 4 3-18 1000 4 4 4 3-19 1000 4 4 4 3-22 1000 4 4 4 3-23 1000 0 4 3-24 1000 1 4 3-25 1000 3 4 4 3-29 1000 4 4 4 3-32 1000 2 4 4 3-36 1000 I 4 4 3-37 1000 1 4 4 -38 1000 2 4 4 -46 1000 4 4 4 -47 1000 1 4 4 -48 1000 1 4 4- 49 1000 0
-53 1000 4 4 -61 1000 0 4 4 -79 1000 0 3 4 -80 1000 2 4 4 -83 1000 -53 1000 4 4 -61 1000 0 4 4 -79 1000 0 3 4 -80 1000 2 4 4 -83 1000
-156 1000 4-156 1000 4
-157 1000 0-157 1000 0
-158 1000 4 4-158 1000 4 4
-159 1000 2 4-159 1000 2 4
-160 1000 1 4 /-161 1000 0 4 4-162 1000 4 4 4-163 1000 0 4 4-164 1000 0 4 4-165 1000 0 1 2-166 1000 4 4 4-167 1000 0 3 3-168 1000
6表 (続き) -160 1000 1 4 / -161 1000 0 4 4-162 1000 4 4 4-163 1000 0 4 4-164 1000 0 4 4-165 1000 0 1 2-166 1000 4 4 4-167 1000 0 3 3-168 1000 Table 6 (continued)
薬量(gai/ha) ィヌビエ ィヌホタルイ ァゼナ-169 1000 0 4 4-170 1000 0 0 0-171 1000 I I-172 1000 0 0-173 1000 0 4 3-174 1000 1 1 4-175 1000 4 4 4-176 1000 0 4 4-177 1000 0 2 3-178 1000 0 4 4-179 1000 0 4 3-180 1000 0 2 3-181 1000 2 4 4 - 182 1000 4 4 4-183 1000 4 4 4-184 1000 0 2 1- 185 1000 1 4 4 - 14 1000 4 4 4 - 39 1000 4 4 4 Dosage (gai / ha) -176 1000 0 4 4-177 1000 0 2 3-178 1000 0 4 4-179 1000 0 4 3-180 1000 0 2 3-181 1000 2 4 4-182 1000 4 4 4-183 1000 4 4 4-184 1000 0 2 1- 185 1000 1 4 4-14 1000 4 4 4-39 1000 4 4 4
5- 6 1000 I 4 4 -29 1000 0 4 2 -50 1000 0 2 1 -64 1000 0 4 3 - 93 1000 I5- 6 1000 I 4 4 -29 1000 0 4 2 -50 1000 0 2 1 -64 1000 0 4 3-93 1000 I
6- 8 1000 4 4 4 6-9 100Q 4 4 4 -10 1000 4 4 4-19 1000 4 4 4-27 1000 4 4 4 -28 1000 4 4 4-29 1000 4 4 4-32 1000 4 4 4-33 1000 4 4 4-60 1000 4 4 4-62 1000 4 4 4-73 1000 4 4 4-82 1000 4 4 4-83 1000 4 4 4-113 1000 4 4 4-339 1000 1 3 4-340 1000 4 4 4
6表 (続き) 6- 8 1000 4 4 4 6-9 100Q 4 4 4 -10 1000 4 4 4-19 1000 4 4 4-27 1000 4 4 4 -28 1000 4 4 4-29 1000 4 4 4-32 1000 4 4 4 -33 1000 4 4 4-60 1000 4 4 4-62 1000 4 4 4-73 1000 4 4 4-82 1000 4 4 4-83 1000 4 4 4-113 1000 4 4 4-339 1000 1 3 4-340 1000 4 4 4 Table 6 (continued)
薬量 (gai/ha) ィヌビエ ィヌホタルイ ァゼナ-341 1000 4 4 4-342 1000 4 4 4-343 1000 4 4 4-344 1000 4 4 4-345 1000 4 4 4-346 1000 4 4-347 1000 I-348 1000 4 4-349 1000 4 4-350 1000 4 4 4-351 1000 4 4 4 - 352 1000 4 4 4-353 1000 4 4 - 354 1000 4 4 4-355 1000 4 4 4 - 356 1000 4 4-357 1000 4 4-358 1000 4 4-359 1000 4 4-360 1000 4 4-361 1000 Dosage (gai / ha) 348 1000 4 4-349 1000 4 4-350 1000 4 4 4-351 1000 4 4 4-352 1000 4 4 4-353 1000 4 4-354 1000 4 4 4-355 1000 4 4 4-356 1000 4 4- 357 1000 4 4-358 1000 4 4-359 1000 4 4-360 1000 4 4-361 1000
-362 1000-362 1000
-363 1000-363 1000
-364 1000-364 1000
-365 1000-365 1000
-366 1000 I-366 1000 I
-367 1000-367 1000
-368 1000-368 1000
-369 1000 -369 1000
- 370 1000-370 1000
-371 1000-371 1000
-372 1000-372 1000
-373 1000-373 1000
-374 1000-374 1000
-375 1000-375 1000
-376 1000-376 1000
-377 1000 -377 1000
- 378 1000 I-378 1000 I
-379 1000-379 1000
-380 1000-380 1000
-381 1000
6表 (続き) -381 1000 Table 6 (continued)
薬量(gai/ha) ィヌビエ ィヌホタルイ ァゼナ-382 1000 4 4 Drug dose (gai / ha)
- 383 1000 0 4 1- 60 1000 4 4 4- 217 1000 1 4 3- 56 1000 1 4 4 - 56 1000 3 4 30-1 1000 I I I0-2 1000 0 4 40-8 1000 4 4 40-12 1000 1 4 40-13 1000 1 4 40-14 1000 0 4 40 - 15 1000 4 40-16 1000 0 4 40-17 1000 4 4 40-18 1000 2 4 40-19 1000 1 4 40-20 1000 0 4 40-21 1000 1 4 40-23 1000 1 4 40-24 1000 0 4 40-26 1000 0 4 40-28 1000 3 4 40-29 1000 2 4 40-34 1000 1 4 40-35 1000 4 4 40-37 1000 0 40-39 1000 1 4 40-40 1000 2 4 40-58 1000-383 1000 0 4 1-60 1000 4 4 4- 217 1000 1 4 3-56 1000 1 4 4-56 1000 3 4 30-1 1000 II I0-2 1000 0 4 40-8 1000 4 4 40 -12 1000 1 4 40 -13 1000 1 4 40 -14 1000 0 4 40-15 1000 4 40 -16 1000 0 4 40 -17 1000 4 4 40 -18 1000 2 4 40 -19 1000 1 4 40 -20 1000 0 4 40 -21 1000 1 4 40-23 1000 1 4 40-24 1000 0 4 40-26 1000 0 4 40-28 1000 3 4 40-29 1000 2 4 40-34 1000 1 4 40-35 1000 4 4 40-37 1000 0 40-39 1000 1 4 40-40 1000 2 4 40-58 1000
0- 59 10000- 59 1000
- 116 1000 1 41- 7 1000 2 4 41- 11 1000 0 4 41- 23 1000 4 4 42- 1 1000 0 42-4 1000 1 4 42-7 1000 2 4 4
試験例 3. 移植水稲に対する薬害試験 -116 1000 1 41-7 1000 2 4 41-11 1000 0 4 41-23 1000 4 4 42-1 1000 0 42-4 1000 1 4 42-7 1000 2 4 4 Test Example 3. Chemical damage test on transplanted rice
75 cm2のプラスチックポットに土壌 (埴壌土) を充填し、 水深 5 cniの状 態に湛水し、 2葉期のイネ (品種: 日本晴) を移植深度 1 cmで 2本移植した。 温室内で育成し、 移植 5日後に、 本発明化合物 (第 1表から第 1 3表に記載の化 合物) を有効成分とする薬剤を所定有効薬量 (gZh a) の薬液として処理をし た。 ついで、 温室内で育成し、 処理 21日後に薬害を調査し、 無処理と比較して、 試験例 1の基準に従って薬害を評価した。 結果を第 1 7表に示す。
75 was filled with soil in a plastic pot cm 2 (clay loam), and flooded to a state of depth 5 cni, 2-leaf stage rice (variety: Nipponbare) were two implanted at implantation depth 1 cm. After cultivation in a greenhouse, 5 days after transplantation, treatment with a drug containing the compound of the present invention (compounds listed in Tables 1 to 13) as the active ingredient was performed at a prescribed effective dose (gZha). did. Then, the plants were grown in a greenhouse and examined for phytotoxicity 21 days after the treatment. The results are shown in Table 17.
1 7表 1 7 Table
、 ノ , No
1丄-9 丄 リ 1丄 丄 O 丄 リ π u 1 丄 -9 丄 1 丄 丄 O 丄 π u
1丄-ム9Q Λ OOf) ο 1 丄 -m 9Q Λ OOf) ο
丄 ο 丄 ο
1丄 - Δ97 ί 丄 UUL/ A1 丄-Δ97 ί 丄 UUL / A
1丄 丄 Π L/ΠVJΠL/ 厶 丄 乙"^ π u1 丄 丄 Π L / ΠVJΠL / 丄
1丄 -' ¾π 丄 υυυ Δ 丄 乙 丄 丄 丄 ύΌ Q 1 丄-'¾π 丄 υυυ Δ 丄 乙 丄 丄 丄 ύΌ Q
丄 iJUU 丄 iJUU
1 _ ρ 1 _ ρ
丄 oo 丄 uuu z 丄—A O 丄 1 πππ 丄 丄 ^丄 丄 uuu Q o 丄 丄 IJiJ(J u 丄 ^t^i 丄 uuu 丄 丄 丄 丄 OU 丄 DUU 丄 — 丄 oo 丄 uuu z 丄 —A O 丄 1 πππ 丄 丄 ^ 丄 丄 uuu Q o 丄 丄 IJiJ (J u 丄 ^ t ^ i 丄 uuu 丄 丄 丄 OU 丄 DUU 丄 —
丄 UUU o 丄 o丄 丄 υυυ u 丄 ι υυ 丄 丄 οό 丄 υυυ 丄 丄 UUU o 丄 o 丄 丄 υυυ u 丄 ι υυ 丄 ό οό 丄 υυυ 丄
1丄 丄 UUU 丄 丄 丄 υυυ u 丄 丄 丄1 丄 丄 UUU 丄 丄 丄 υυυ u 丄 丄 丄
1 Q9 丄 υυυ Q1 Q9 丄 υυυ Q
1 1
丄 丄 υυυ π u 丄 丄 υυυ π u
丄 丄 丄 υυυ 丄 丄 丄 Π Q 丄 丄 U 丄 丄 丄 υυυ 丄 丄 丄 丄 Π Q 丄 丄 U
1丄—丄1 07 Q1 丄 — 丄 1 07 Q
1丄 丄 n υoο 1 πππ Q 丄 1—1丄1丄 ^9 1 oof] 1 丄 丄 n υoο 1 πππ Q 丄 1—1 丄 1 丄 ^ 9 1 oof]
l 1000 n l 1000 n
1-124 1000 01-124 1000 0
1-165 1000 11-165 1000 1
1-177 1000 11-177 1000 1
1-183 1000 21-183 1000 2
1-189 1000 01-189 1000 0
1-190 1000 01-190 1000 0
1-192 1000 21-192 1000 2
1-193 1000 3
1 7表 (続き) 1-193 1000 3 1 7 Table (continued)
^ ^Api. ί ^ ^ Api. Ί
a g L / /In Lノ ノ 、 a g L / / In L
1—1 no 1—1 no
丄 丄 1 A 丄 Π VJΠUΠL/丄 丄 1 A 丄 Π VJΠUΠL /
1丄 -1丄 Q!^Q y 1丄 Π *JΠ(JΠ o1 丄 -1 丄 Q! ^ Q y 1 丄 Π * JΠ (JΠ o
*J Δ 丄 丄 0 丄 υυυ n u 丄 \ 丄 UUD I) 丄 丄 uuu u * J Δ 丄 丄 0 丄 υυυ n u 丄 \ 丄 UUD I) 丄 丄 uuu u
1 1
丄 ¾丄 丄 uuu u 丄 Ζο 丄 UDU 丄 丄 ί 丄 UUU z 丄— (J 丄—Zb 丄 (JUU u 丄ー b > lUUU 丄Uu ¾ 丄 丄 uuu u 丄 Ζο 丄 UDU 丄 丄 ί 丄 UUU z 丄 — (J 丄 —Zb 丄 (JUU u 丄 ー b> lUUU 丄
Ί Ί
丄— 0 丄 (J(JU 丄 丄 丄 UUU 丄 丄 / y 丄 UUU A 丄一 1 丄一 i3 u 丄一^ (D 1U(J(J u 丄 8 lUUU 1 on 丄 — 0 丄 (J (JU 丄 丄 丄 UUU 丄 丄 / y 丄 UUU A 丄 1 1 丄 1 i3 u 丄 1 ^ (D 1U (J (Ju 丄 8 lUUU 1 on
丄 zyi 丄 UUU 丄 丄ー yz 丄 (JUL! 丄Zy zyi 丄 UUU 丄 丄 yz 丄 (JUL! 丄
1 1
丄ー d ooo lUUU u 丄一 0 4 丄 (JUL) (J 丄一 3Zb u 丄 ー d ooo lUUU u 丄 一 0 4 丄 (JUL) (J 丄 一 3Zb u
r\r\r 丄ー 丄 (JUU 丄 丄 iiZ ί 丄 UUU 丄 丄一 丄 UUU Δ r \ r \ r 丄 ー 丄 (JUU 丄 ii iiZ ί 丄 UUU 丄 丄 丄 丄 UUU Δ
Δ o υ Δ o υ
丄 DUU υ 丄 DUU υ
9-1 9-1
1 ώ o 1 ΠJΠUΠ 1 1 ώ o 1 ΠJΠUΠ 1
L 丄 L 丄
1 ΠΩΠ 11 ΠΩΠ 1
10001000
10001000
1000 01000 0
9-29 1000 19-29 1000 1
2 - 30 1000 02-30 1000 0
2-36 1000 12-36 1000 1
2-37 1000 02-37 1000 0
2-38 1000 12-38 1000 1
2-41 1000 12-41 1000 1
2-43 1000 12-43 1000 1
2 - 51 1000 1
1 7表 (続き) 2-51 1000 1 1 7 Table (continued)
量.、 /ha) イ 1ネ (Amount./ha) b
1 [)00 0リ ム ϋ丄 丄リ πリ 乙 丄 1 ΠΠΠ 1丄 ム Ό¾ 丄 1 [) 00 0 rim ϋ 丄 丄 π li 乙 1 ΠΠΠ 1 丄 丄 Ό¾ 丄
厶 1丄 ΠΠΠ 1丄 ΌΌ 1丄 ΠΠΠ 1丄 Ό ί 1 ΠΠΠ 1丄 1 丄 ΠΠΠ 1 丄 ΌΌ 1 丄 ΠΠΠ 丄 1 ΠΠΠ 1ί
1 Οο 丄 丄 1 Οο 丄 丄
1 ΠΠΠ π U ム 9—7 ( Π U 1 ΠΠΠ o 厶_7 ( 1丄 1丄 Π ι/Πι/Πυ 1 1 ΠΠΠ π U um 9—7 (Π U 1 ΠΠΠ o um_7 (1 丄 1 丄 Π ι / Πι / Πυ 1
丄 丄
Π Π
厶 { Δ VJ 厶 1 ό 丄 U ί Ό 丄 1 π uπuuπ 1 Um {Δ VJ um 1 丄 丄 U ί Ό 丄 1 π uπuuπ 1
丄 ο_70 丄 u π U 丄 ο_70 丄 u π U
1 Ο丄 丄 1 Ο 丄 丄
1 丄 丄 1 丄 丄
9 1丄 <JL/(J π U 9 1 丄 <JL / (J π U
1 πππ 1 πππ
1 1
Δ ΟΌ 丄 丄 厶 0 ί 1 ΠΠΠ 1 Δ ΟΌ 丄 0 0 0 ί 1 ΠΠΠ 1
丄 ム οο 丄 9 ム Q ΌΔ9 1 1 ム Ό 丄 m οο 丄 9 m Q ΌΔ9 1 1 m Ό
—ΟΑ 1 厶 丄 丄 —ΟΑ 1 丄
9—QQ 1丄 π υπυπυ π U9—QQ 1 丄 π υπυπυ π U
9—1丄 1丄 π υπυπυ U9—1 丄 1 丄 π υπυπυ U
2-167 1000 12-167 1000 1
2-169 1000 02-169 1000 0
2-176 1000 22-176 1000 2
2-177 1000 22-177 1000 2
2-184 1000 32-184 1000 3
2-185 1000 42-185 1000 4
9-1 丄 1 η υπυηυ9-1 丄 1 η υπυηυ
丄 (JUU U 丄 (JUU U
2-221 1000 12-221 1000 1
2-227 1000 22-227 1000 2
2-244 1000 02-244 1000 0
2-245 1000 12-245 1000 1
2-246 1000 0
1 7表 (続き) 2-246 1000 0 1 7 Table (continued)
荣里、 gai/naノ ノ Λ ヽ 丄 UtJU 丄 荣, gai / na no no 丄 ヽ t UtJU 丄
Q Q
0 Δ 丄 uuu ά 0 Δ 丄 uuu ά
丄 UlliJ u u ο 丄 UlliJ u u ο
l UUU (J ο c l UUU (J ο c
~Ό 丄 uuu (J ο ~ Ό 丄 uuu (J ο
0~0 lUUU (J 0 ~ 0 lUUU (J
lUUU u lUUU u
«3—18 ιυυυ 1 -19 Ιϋϋϋ 1 ό~ΔΔ ιυυυ u«3—18 ιυυυ 1 -19 Ιϋϋϋ 1 ό ~ ΔΔ ιυυυ u
3-23 1000 03-23 1000 0
3 - 24 1000 03-24 1000 0
3 - 32 1000 0 3-32 1000 0
3 - 36 1000 03-36 1000 0
3 - 37 1000 03-37 1000 0
3 - 38 1000 13-38 1000 1
3 - 48 1000 0 3-48 1000 0
1UUU u οο 丄 υυυ n Ό丄 w ο / y 1丄 πππ n 1UUU u οο 丄 υυυ n Ό 丄 w ο / y 1 丄 πππ n
Q-on οοο 0 u oo 丄 ΠΠΠ 1 1 丄 ΟΌ 丄 πππ Q-on οοο 0 u oo 丄 1 1 1 丄 ΟΌ 丄 πππ
丄 *_) ί 1丄 πππ o d に o 丄 * _) ί 1 丄 πππ o d to o
丄!^ U 丄 (JUU U 丄 UU(J U 丄! ^ U 丄 (JUU U 丄 UU (J U
3 丄 丄 (JUL) U _i an 3 丄 丄 (JUL) U _i an
丄 Όώ 丄 υυυ o 丄 Όώ 丄 υυυ o
3-163 1000 03-163 1000 0
3-164 1000 03-164 1000 0
3-165 1000 03-165 1000 0
3-166 1000 03-166 1000 0
3-167 1000 03-167 1000 0
3-168 1000 1
1 7表 (続き) 3-168 1000 1 1 7 Table (continued)
IK'S" i /ha ) IK'S "i / ha)
3-169 1000 3-169 1000
— 1 71 1 —"! 79 o u — 1 71 1 — "! 79 o u
1 000 1 74 1 000 1 000 1 74 1 000
f ϋ 1 000 1 丄 ί u n u f ϋ 1 000 1 ί ί u n u
Q-1 77 1 ΠΠΠ n u u ί 1 ΠΠΠ n v ί n u O 1 ΠΠΠ n u o 1 ΠΠΠ n u o 1 ΠΠΠ 1 0»3 Q-1 77 1 ΠΠΠ n u u ί 1 ΠΠΠ n v ί n u O 1 ΠΠΠ n u o 1 ΠΠΠ n u o 1 ΠΠΠ 1 0 »3
o 1 000 u oo π u o 1 000 u oo π u
4 ¾一 1丄 A 1 ΠΠΠ 1 4 1 1 A 1 1
1 ΠΠΠ o U 1丄 ΠΠΠ ο 1 ΠΠΠ o U 1 丄 ΠΠΠ ο
1 000 π 1 000 π
5-50 1 Π0Ω o5-50 1 Π0Ω o
5-64 1000 o5-64 1000 o
5-93 1000 15-93 1000 1
6-8 1000 26-8 1000 2
6-9 1000 06-9 1000 0
6 10 1000 1 \J 4 fi 7 1 ΩΠΓ) 6 10 1000 1 \ J 4 fi 7 1 ΩΠΓ)
UU UU
1 000 4 1 000 4
1 000 21 000 2
6— 33 1 ΠΩ0 3 6—33 1 ΠΩ 0 3
1 ΠΩΩ 1 ΠΩΩ
11
6 - 73 1000 6-73 1000
6-82 1000 6-82 1000
6 83 1000 6 83 1000
-113 1000 0 -339 1000 0 -340 1000 1
1 7表 (続き) -113 1000 0 -339 1000 0 -340 1000 1 1 7 Table (continued)
朵直 gai/iiaj ノ ィ · ; Honest gai / iiaj noi ;
C ΙϋϋΟ 3 C ΙϋϋΟ 3
1000 2 343 1000 4 1000 2 343 1000 4
0-344 1000 10-344 1000 1
6 - 345 1000 16-345 1000 1
6—346 1000 06—346 1000 0
6-347 1000 06-347 1000 0
6-348 1000 16-348 1000 1
6 - 349 1000 26-349 1000 2
6 - 350 1000 16-350 1000 1
6 - 351 1000 16-351 1000 1
6-352 1000 06-352 1000 0
6-353 1000 16-353 1000 1
6-354 1000 16-354 1000 1
6-355 1000 26-355 1000 2
6-356 1000 16-356 1000 1
6-357 1000 1 b iDo 6-357 1000 1 b iDo
D oy U 丄 (JUL) U D oy U 丄 (JUL) U
/ / / /
D bZ 丄 Π LlΛiJΠD 1 1 οΌό I 1D bZ 丄 Π LlΛiJΠD 1 1 οΌό I 1
Ό Ό
6-364 1000 1 6-364 1000 1
6 - 365 1000 1 八八八6-365 1000 1 888
6 - 366 1000 16-366 1000 1
6 - 367 1000 16-367 1000 1
6 - 368 1000 16-368 1000 1
6 - 369 1000 16-369 1000 1
6 - 370 1000 16-370 1000 1
6 71 1000 1 c 6-372 1000 1 6 71 1000 1 c 6 -372 1000 1
1 1
1UUU 1 -3 4 11UUU 1 -3 4 1
6-375 1000 16-375 1000 1
6-376 1000 16-376 1000 1
6-377 1000 16-377 1000 1
6 - 378 1000 16-378 1000 1
6-379 1000 16-379 1000 1
6-380 1000 16-380 1000 1
6-381 1000 1
7表 (続き) 6-381 1000 1 Table 7 (continued)
薬量 (gai/ha) イネ-382 1000 1-383 1000 0 -60 1000 1-217 1000 0 -56 1000 1 -56 1000 0 0-1 1000 1 0-2 1000 0 0-8 1000 00-12 1000 00-13 1000 00-14 1000 00-15 1000 00 - 16 1000 00 - 17 1000 00-18 1000 00-19 1000 00-20 1000 00-21 1000 00-23 1000 10 - 24 1000 00-26 1000 10-28 1000 10-29 1000 1 -34 1000 0 -35 1000 1 -37 1000 0 -39 1000 0 -40 1000 0 -58 1000 1 -59 1000 1-116 1000 01-7 1000 0 -11 1000 0 -23 1000 12-1 1000 02 - 4 1000 02-7 1000 0
試験例 4. 畑作雑草に対する茎葉処理除草効果試験 Dosage (gai / ha) Rice -382 1000 1-383 1000 0 -60 1000 1-217 1000 0 -56 1000 1 -56 1000 0 0-1 1000 1 0-2 1000 0 0-8 1000 00-12 1000 00-13 1000 00-14 1000 00-15 1000 00-16 1000 00-17 1000 00-18 1000 00-19 1000 00-20 1000 00-21 1000 00-23 1000 10-24 1000 00-26 1000 10- 28 1000 10-29 1000 1 -34 1000 0 -35 1000 1 -37 1000 0 -39 1000 0 -40 1000 0 -58 1000 1 -59 1000 1-116 1000 01-7 1000 0 -11 1000 0 -23 1000 12-1 1000 02-4 1000 02-7 1000 0 Test Example 4. Test of foliage treatment on field weeds
36 cm2のポットに土壌 (埴壌土) を充填し、 畑作雑草であるィヌビエ、 ォ ナモミの種子を播種し、 土壌約 20 cm3で覆土した後、 温室内で育成した。 供 試植物が一葉期の時期に、 製剤例 1から 4に準じて調製した本発明化合物 (第 1 表から第 1 3表に記載の化合物) を有効成分とする薬剤の所定有効薬量 (140 g/h a相当) を 1000 LZh a相当の水で希釈し、 散布処理した。 ついで、 温室内で育成し、 処理 21日後に除草効果を調査し、 無処理と比較して除草効果 の有無を評価した。 A 36 cm 2 pot was filled with soil (clay loam), seeds of upland weeds such as linubie and firgrass were sown, covered with about 20 cm 3 of soil, and grown in a greenhouse. When the test plant is in the single-leaf stage, the prescribed effective dose of the drug containing the compound of the present invention (compounds listed in Tables 1 to 13) prepared according to Formulation Examples 1 to 4 as an active ingredient (140) g / ha) was diluted with 1000 LZha of water and sprayed. Then, the plants were grown in a greenhouse, and after 21 days from the treatment, the herbicidal effect was investigated.
本発明化合物の中で、 少なくとも 1一 2、 1— 8、 1— 23、 1-27, 1 - 28、 1一 30、 1-36, 1一 40、 1一 41、 1一 44、 1—47、 1 -5 9、 1一 84、 1一 88、 1一 89、 1一 91、 1一 92、 1-93, 1一 94、 Among the compounds of the present invention, at least 1-2, 1-8, 1-23, 1-27, 1-28, 1-130, 1-36, 1-140, 1-141, 1-144, 1-- 47, 1-59, 1-184, 1-188, 1-189, 1-191, 1-192, 1-93, 1-194,
1一 95、 1— 102、 1— 103、 1— 108、 1— 165、 1一 177、 1 一 183、 1— 189、 1— 1 90、 1— 1 93 1— 199、 1— 237、 1 一 251、 1— 254、 1— 258、 1— 266 1— 279、 1— 286、 1 一 291、 1— 324、 1— 326、 1— 327 1— 328、 2— 12、 2 - 23、 2-24, 2— 27、 2— 28、 2-29 2-30, 2— 36、 2-4 1、 2— 51、 2— 61、 2— 63、 2— 64、 2— 65、 2— 66、 2-67,1-95, 1-102, 1-103, 1-108, 1-165, 1-177, 1-183, 1-189, 1-190, 1-193 1-199, 1-237, 1 1 251, 1—254, 1—258, 1—266 1—279, 1—286, 1 1—291, 1—324, 1—326, 1—327 1—328, 2—12, 2—23, 2 -24, 2—27, 2—28, 2-29 2-30, 2—36, 2-4 1, 2—51, 2—61, 2—63, 2—64, 2—65, 2—66 , 2-67,
2— 68、 2— 69、 2— 70、 2— 71、 2— 72、 2— 73、 2— 76、 2 一 79、 2— 81、 2— 82、 2— 83、 2— 85、 2— 86、 2— 87、 2— 88、 2— 93、 2— 94、 2— 130、 2— 167、 2— 169、 2-1 76. 2—177、 2— 184、 2— 185、 2— 186、 2— 209、 2— 22 1、 2— 244、 2— 245、 2— 247、 3— 2、 3_5、 3— 8、 3— 13、 3 一 18、 3— 1 9、 3— 23、 3— 24、 3— 25、 3-29, 3— 36、 3— 37、 3-38, 3— 46、 3— 47、 3— 48、 3— 53、 3— 61、 3— 8 00、、 33— - 115566、 3— 1 58、 3— 161、 3— 162、 3— 163、 3- 16 4、 3 - 166 3— 168、 3— 169、 3— 1 70、 3— 1 72、 3- 1 7 3、 3- 181 3— 1 82、 3— 183、 3— 185、 4一 39、 5— 93、 6— 8、 6-9 6— 10、 6-19. 6— 27、 6-28, 6— 29、 6-32-68, 2-69, 2-70, 2-71, 2-72, 2-73, 2-76, 2-79, 2-81, 2-82, 2-83, 2-85, 2- 86, 2-87, 2-88, 2-93, 2-94, 2-130, 2-167, 2-169, 2-1 76. 2-177, 2-184, 2-185, 2-186 , 2—209, 2—22 1, 2—244, 2—245, 2—247, 3—2, 3_5, 3—8, 3—13, 3 1-18, 3—19, 3—23, 3 — 24, 3—25, 3-29, 3—36, 3—37, 3-38, 3—46, 3—47, 3—48, 3—53, 3—61, 3—800, 33 --115566, 3-1 58, 3-161, 3-162, 3-163, 3-16 4, 3-166 3-168, 3-169, 3-1 70, 3-1 72, 3-1 7 3, 3-181 3-1-182, 3-183, 3-185, 4-39, 5-93, 6-8, 6-9 6-10, 6-19. 6-27, 6-28, 6—29, 6-3
2、 6— 33、 6— 60、 6— 62、 6— 73、 6— 82、 6-83, 6— 34
1、 6— 342、 6— 346、 6-348, 6— 349、 6— 350、 6— 35 1、 6— 352、 6— 353、 6— 354、 6— 355、 6— 356、 6— 35 7、 6— 360、 6— 362、 6— 363、 6— 364、 6— 365、 6— 36 6、 6— 367、 7— 60、 1 0-2, 10— 8、 10— 12、 10— 1 3、 1 0— 14、 10— 15、 10— 16、 10— 17、 10— 18、 10— 19、 1 0— 20、 10— 21、 10— 23、 10— 24、 10— 26、 10— 28、 1 0— 29、 10— 34、 10— 35、 10— 37、 10— 39、 10— 40、 1 0— 1 1 6、 1 1 -7, 12-1, 1 2-4, 1 2— 7は、 ィヌビエあるいはォ ナモミに除草効果を示した。
2, 6—33, 6—60, 6—62, 6—73, 6—82, 6-83, 6—34 1, 6—342, 6—346, 6-348, 6—349, 6—350, 6—35 1, 6—352, 6—353, 6—354, 6—355, 6—356, 6—35 7, 6—360, 6—362, 6—363, 6—364, 6—365, 6—36 6, 6—367, 7—60, 10-2, 10—8, 10—12, 10— 1 3, 1 0—14, 10—15, 10—16, 10—17, 10—18, 10—19, 10—20, 10—21, 10—23, 10—24, 10—26, 10 — 28, 10—29, 10—34, 10—35, 10—37, 10—39, 10—40, 1 0—1 1 6, 1 1 -7, 12-1, 1 2-4, 1 2-7 showed herbicidal effects on the moss and the fir.
Claims
1. 一般式 (I ) 1. General formula (I)
{式中、 R1はハロ (C厂 C6) アルキル基を示す。 {Wherein, R 1 represents a halo (C Factory C 6 ) alkyl group.
R2は水素原子、 (C「 C6) アルキル基、 (Cr C6) アルコキシ (C厂 C6) アルキル 基、 (C!-Cs) アルキルカルポニル基、 ノヽロ (Cf C6) アルキルカルポニル基、 フ ェニルカルボニル基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) 力 ら選 択される 1以上'の置換基を有する置換フエニルカルボニル基、 (cr c6) アルコ キシカノレポ二ノレ基、 フエノキシカルボ二ル基、 同一又は異なっても良く、 Y (Y は後記に示す。 ) から選択される 1以上の置換基を有する置換フ ノキシカルボ ニル基、 (C厂 C6) アルキルスルホニル基、 ハロ (C厂 c6) アルキルスルホニル基、 フエニルスルホニル基又は同一若しくは異なっても良く、 Y (Yは後記に示 す。 ) から選択される 1以上の置換基を有する置換フエニルスルホニル基を示す。 R 2 is a hydrogen atom, a (C “C 6 ) alkyl group, a (C r C 6 ) alkoxy (CFactory C 6 ) alkyl group, a (C! -Cs) alkyl carbonyl group, a nodro (Cf C 6 ) alkyl carbonyl group A phenylcarbonyl group, which may be the same or different and is a substituted phenylcarbonyl group having at least one substituent selected from the group consisting of Y (Y is shown below), (c r c 6 ) alcohol A substituted methoxycarbonyl group having one or more substituents, which may be the same or different, and which may be the same or different, and a (C factory C 6 ) alkyl A substituted phenyl having one or more substituents selected from a sulfonyl group, a halo (C factory c 6 ) alkylsulfonyl group, a phenylsulfonyl group or the same or different and Y (Y is shown below). Shows a sulfonyl group.
Qは構成原子の少なくとも 1個が窒素原子であり、 かつその窒素原子が Aとの 結合部位である置換されていても良レ、へテ口環を示す。 Q represents a substituted or unsubstituted heterocyclic ring in which at least one of the constituent atoms is a nitrogen atom and the nitrogen atom is a bonding site with A.
Aは ( - C6) アルキレン基、 同一又は異なっても良く、 ハロゲン原子、 水酸 基、 (C厂 C6)アルコキシ基、 (C厂 C6)アルコキシカルボニル基又はシァノ基から選 択される 1以上の置換基を有する置換 (CrC6) アルキレン基、 (C2 - C6) ァルケ 二レン基、 同一又は異なっても良く、 ハロゲン原子、 水酸基、 (Cr C6)アルコキ シ基、 (C厂 C6)アルコキシカルボニル基又はシァノ基から選択される 1以上の置 換基を有する置換 (c2- c6) アルケニレン基又は (c2- c6) アルキニレン基を示す。 A is (-C 6 ) an alkylene group, which may be the same or different, and is selected from a halogen atom, a hydroxyl group, a (C Factory C 6 ) alkoxy group, a (C Factory C 6 ) alkoxycarbonyl group or a cyano group one or more substituent (C r C 6) alkylene group having a substituent, (C 2 - C 6) Aruke two alkylene groups, which may be the same or different, a halogen atom, a hydroxyl group, (C r C 6) an alkoxy group , (C Factory C 6 ) represents a substituted (c 2 -c 6 ) alkenylene group or (c 2 -c 6 ) alkynylene group having at least one substituent selected from an alkoxycarbonyl group or a cyano group.
Gは酸素原子、 硫黄原子、 N— R3 (式中、 R3は水素原子、 ( - C6) アルキル 基、 シァノ基、 ニトロ基、 フエニル (C厂 C6) アルキル基、 同一又は異なっても 良く、 Y (Yは後記に示す。 ) から選択される 1以上の置換基を環上に有する置 換フエニル (CrC6) アルキル基、 フエニル基又は同一若しくは異なっても良く、
Y (Yは後記に示す。 ) 力 ら選択される 1以上の置換基を有する置換フ ニル基 を示す。 ) 、 Ν— O R'1 (式中、 R4は水素原子、 (C厂 C6) アルキル基、 フヱニルG is an oxygen atom, a sulfur atom, N—R 3 (where R 3 is a hydrogen atom, a (-C 6 ) alkyl group, a cyano group, a nitro group, a phenyl (C Factory C 6 ) alkyl group, the same or different And a substituted phenyl (C r C 6 ) alkyl group having at least one substituent selected from Y (Y is shown below) on the ring, a phenyl group or may be the same or different; Y (Y is shown below) represents a substituted phenyl group having at least one substituent selected from the group consisting of: ), Ν— O R ' 1 (wherein, R 4 is a hydrogen atom, (C Factory C 6 ) alkyl group, phenyl)
(CrC6) アルキル基又は同一若しくは異なっても良く、 Y ( Yは後記に示 す。 ) 力 ^選択される 1以上の置換基を環上に有する置換フエニル (C厂 C6) ァ ルキル基を示す。 ) 又は N— N R5 R6 (式中、 R5及び R6は同一又は異なっても 良く、 水素原子、 フユニル基又は同一若しくは異なっても良く、 Y (Yは後記に 示す。 ) から選択される 1以上の置換基を有する置換フエ二ル基を示す。 又、 R5と R6は一緒になつて (C3_C6) アルキレン基を示すこともできる。 ) を示す。 mは 0又は 1の整数を示す。 (C r C 6 ) alkyl group or the same or different, and Y (Y is shown below.) Force ^ Substituted phenyl having one or more selected substituents on the ring (CFactory C 6 ) Represents a alkyl group. Or N—NR 5 R 6 (wherein, R 5 and R 6 may be the same or different, may be a hydrogen atom, a fuunyl group or the same or different, and are selected from Y (Y is shown below)). And R 5 and R 6 may be taken together to represent a (C 3 _C 6 ) alkylene group. m represents an integer of 0 or 1.
Xは同一又は異なっても良く、 水素原子、 ハロゲン原子、 (cr c6)アルキル基、 (c2-c6)アルケニル基、 (c2- c6)アルキニル基、 シクロ(c3- c6)アルキル基、 ノヽロX may be the same or different, a hydrogen atom, a halogen atom, (c r c 6) alkyl group, (c 2 -c 6) alkenyl, (c 2 - c 6) alkynyl, cyclo (c 3 - c 6 ) Alkyl group, Nodro
(C厂 C6)アルキル基、 シクロハ口(C3_C6)アルキル基、 (C厂 c6)アルコキシ基、 ハロ (C厂 C6)アルコキシ基、 ( C6)アルキルチオ基、 ハロ(C厂 c6)アルキルチオ基、 (CrC6)アルキルスルフィニル基、 ノヽロ (C厂 c6)アルキルスルフィニル基、 (crc6) アルキルスルホニル基、 ノヽロ(C厂 C6)アルキルスルホニル基、 フエニル基、 同一 又は異なっても良く、 γ (Yは後記に示す。 ) から選択される 1以上の置換基を 有する置換フエニル基、 フエノキシ基、 同一又は異なっても良く、 Ύ (Yは後記 ' に示す。 ) 力 選択される 1以上の置換基を有する置換フヱノキシ基、 フエニル チォ基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) から選択される 1以 上の置換基を有する置換フエ二ルチオ基、 フエニルスルフィエル基、 同一又は異 なっても良く、 Y (Yは後記に示す。 ) 力 ら選択される 1以上の置換基を有する 置換フエニルスルフィニル基、 フヱニルスルホニル基、 同一又は異なっても良く、(C Factory C 6 ) alkyl group, cycloha (C 3 _C 6 ) alkyl group, (C Factory c 6 ) alkoxy group, halo (C Factory C 6 ) alkoxy group, (C 6 ) alkylthio group, halo (C Factory c 6 ) alkylthio group, (C r C 6 ) alkylsulfinyl group, nodro (C Factory c 6 ) alkylsulfinyl group, (c r c 6 ) alkylsulfonyl group, nodro (CFactory C 6 ) alkylsulfonyl group, A phenyl group, which may be the same or different, and a substituted phenyl group having at least one substituent selected from γ (Y is described below), a phenoxy group, which may be the same or different; ) Force A substituted phenoxy group having one or more substituents selected, a phenylthio group, which may be the same or different, and one or more substituents selected from Y (Y is shown below). Having a substituted phenylthio group, a phenylsulfiel group, the same or A substituted phenylsulfinyl group, a phenylsulfonyl group having one or more substituents selected from Y (Y is shown below), and may be the same or different;
Y (Yは後記に示す。 ) 力 ら選択される 1以上の置換基を有する置換フエニルス ルホニル基、 (Cr C6)アルキルカルボニル基、 ノヽロ(C厂 c6)アルキルカルボニル基、 フエニルカルボニル基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) から 選択される 1以上の置換基を有する置換フエ二ルカルポニル基、 (C厂 c6)アルコ キシカルボニル基、 カルボキシル基、 モノ (crc6) アルキルァミノカルボニル 基、 同一又は異なっても良いジ (C厂 c6) アルキルアミノカルボニル基、 フエ二 ルァミノカルボニル基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) から
選択される 1以上の置換基を環上に有する置換フエニルァミノカルボニル基、 フ ヱニル (cr c6) アルキルアミノカルボニル基、 同一又は異なっても良く、 Y (Yは後記に示す。 ) 力 ^選択される 1以上の置換基を環上に有する置換フ 二 ル (C厂 c6) アルキルアミノカルボ二ル基、 水酸基、 アミノ基、 シァノ基又は二 トロ基から選択される 1〜4個の置換基を示す。 Y (Y is shown below.) Substituted phenylsulfonyl group having one or more substituents selected from the group consisting of: (C r C 6 ) alkylcarbonyl group, nodro (CFactory c 6 ) alkylcarbonyl group, phenyl A carbonyl group, which may be the same or different, and a substituted phenylcarbonyl group having one or more substituents selected from Y (Y is shown below), (C Factory c 6 ) alkoxycarbonyl group, carboxyl group, Mono (c r c 6 ) alkylaminocarbonyl group, which may be the same or different di (C factory c 6 ) alkylaminocarbonyl group, phenylaminocarbonyl group, may be the same or different, and Y (Y is Shown from) Substituted phenylalanine § amino carbonyl group having one or more substituents selected on the ring, off Weniru (c r c 6) alkylaminocarbonyl group, which may be identical or different, Y (Y is shown later.) Force ^ Substituted file having one or more selected substituents on the ring (C Factory 6 ) 1-4 selected from an alkylaminocarboxy group, a hydroxyl group, an amino group, a cyano group or a nitro group Shows the substituents.
Yは同一又は異なっても良く、 ハロゲン原子、 (C厂 c6)アルキル基、 (c2- c6)ァ ルケニル基、 (c2 - c6)アルキニル基、 シク口(c3 c6)アルキル基、 ハロ( - c6)アル キル基、 シクロハ口(c3- C6)アルキル基、 (C厂 C6)アルコキシ基、 ノヽ口(C厂 c6)アル コキシ基、 (cr c6)アルキルチオ基、 ハロ(cr c6)アルキルチオ基、 (c - c6)アルキ ノレスルフィニル基、 ノヽロ(C厂 c6)アルキルスルフィエル基、 (cr c6)アルキルスル ホニル基、 ノヽロ (CfC6)アルキルスルホニル基、 フエニル基、 同一又は異なって も良く、 ハロゲン原子、 (c厂 c6)アルキル基、 (c2-c6)アルケニル基、 (c2- c6)アル キニル基、 シクロ(c3- C6)アルキル基、 ノヽロ(C厂 c6)アルキル基、 シクロハ口(c3-Y may be the same or different; a halogen atom, a (C factory c 6 ) alkyl group, a (c 2 -c 6 ) alkenyl group, a (c 2 -c 6 ) alkynyl group, a cyclic (c 3 c 6 ) alkyl group, halo (- c 6) Al kill group, Shikuroha port (c 3 - C 6) alkyl groups, (C厂C 6) alkoxy group, Nono port (C厂c 6) alkoxy groups, (c r c 6) alkylthio groups, halo (c r c 6) alkylthio group, (c - c 6) alkyl Noresurufiniru group, Nono b (C厂c 6) alkyl sulfide el group, (c r c 6) alkylsulfinyl Honiru group, Nodro (CfC 6 ) alkylsulfonyl group, phenyl group, which may be the same or different, halogen atom, (c Factory c 6 ) alkyl group, (c 2 -c 6 ) alkenyl group, (c 2 -c 6 ) al Kiniru group, cyclo (c 3 - C 6) alkyl group, Nono b (C厂c 6) alkyl group, Shikuroha port (c 3 -
C6)ァノレキル基、 (C厂 C6)アルコキシ基、 ハロ(C厂 C6)アルコキシ基、 ((^-( 6)アルキ ルチオ基、 ノヽロ (C厂 C6)アルキルチオ基、 - C6)アルキルスルフィニル基、 ノヽロ (Cr C6)アルキルスルフィニル基、 (Cr C6)アルキルスルホニル基、 ノ、口(C厂 c6)ァ ルキルスルホニル基、 (CrC6)アルキルカルボニル基、 ハ口(c!- c6)アルキル力ノレ ポニル基、 (c厂 c6)アルコキシカルボニル基、 カルボキシル基、 モノ (CrC6) ァ ルキルアミノカルボニル基、 同一又は異なっても良いジ (c「 c6) アルキルアミ ノカルボニル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1〜 5個の置換基を有する置換フヱニル基、 フヱノキシ基、 同一又は異なっても良く、 ハロゲン原子、 (C厂 c6)アルキル基、 (c2- c6)アルケニル基、 (c2- c6)アルキニル基、 シクロ(C3- C6)アルキル基、 ハ口(C厂 c6)アルキル基、 シクロハ口(c3 - c6)アルキル 基、 (Cf C6)アルコキシ基、 ハロ(C厂 c6)アルコキシ基、 ( - c6)アルキルチオ基、 ノヽロ(C厂 C6)アルキルチオ基、 (( )アルキルスルフィニル基、 ノヽロ(Ci-Ce)アル キルスルフィニル基、 (crc6)アルキルスルホニル基、 ノヽロ(crc6)アルキルスル ホニル基、 (Ci_c6)アルキルカルボニル基、 ノ、口((:厂 c6)アルキルカルポニル基、 (C! - c6)アルコキシカルボニル基、 カルボキシル基、 モノ (crc6) アルキルアミ ノカルボニル基、 同一又は異なっても良いジ (C厂 c6) アルキルアミノカルボ二
ル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1 〜 5個の置換 基を有する置換フエノキシ基、 フエ二ルチオ基、 同一又は異なっても良く、 ハロ ゲン原子、 (C厂 C6)アルキル基、 (C2- C6)アルケニル基、 (C2- C6)アルキニル基、 シ ク口(c3- C6)アルキル基、 ハロ(C厂 c6)アルキル基、 シクロハ口(c3-c6)アルキル基、 (Cr C6)アルコキシ基、 ハロ(C厂 C6)アルコキシ基、 (C厂 C6)アルキルチオ基、 ハロ (CrC6)アルキルチオ基、 (C厂 C6)アルキルスルフィニル基、 ノヽ口(C厂 c6)アルキル スルフィニル基、 (C厂 C6)アルキルスルホニル基、 ノヽロ(C厂 c6)アルキルスルホ二 ル基、 (C厂 C6)アルキルカルボニル基、 ノ、口(C厂 C6)アルキルカルボニル基、 (C厂 c6)アルコキシカルボニル基、 カルボキシル基、 モノ (C厂 c6) アルキルアミノカ ルボニル基、 同一又は異なっても良いジ ( - ) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1 〜 5個の置換基を有 する置換フエ二ルチオ基、 フエニルスルフィニル基、 同一又は異なっても良く、 ハロゲン原子、 (C厂 c6)アルキル基、 (c2- c6)アルケニル基、 (c2 - c6)アルキニル基、 シクロ(C3 - C6)アルキル基、 ハ口(C厂 c6)アルキル基、 シクロハ口(c3- c6)アルキル 基、 (C厂 C6)アルコキシ基、 ハロ(C「 C6)アルコキシ基、 (C厂 C6)アルキルチオ基、 ノヽロ(c c6)アルキルチオ基、 ( - C6)アルキルスルフィニル基、 ノヽロ(C厂 c6)アル キノレスノレフィエル基、 (CrC6)アルキルスルホニル基、 ノ、口(cr c6)アルキルスル ホニル基、 (C厂 C6)アルキルカルボニル基、 ノヽロ(C厂 c6)アルキルカルボ二ル基、 (CrC6)アルコキシカルボニル基、 カルボキシル基、 モノ (C厂 c6) アルキルァミ ノカルボニル基、 同一又は異なっても良いジ (C厂 C6) アルキルアミノカルボ二 ル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1 〜 5個の置換 基を有する置換フエニルスルフィエル基、 フエニルスルホニル基、 同一又は異な つても良く、 ハロゲン原子、 (c厂 c6)アルキル基、 (c2- c6)アルケニル基、 (c2 - c6) アルキニル基、 シク口(c3- C6)アルキル基、 ハロ(C厂 c6)アルキル基、 シクロハ口 (C3_C6)アルキル基、 (C厂 C6)アルコキシ基、 ハロ(C厂 C6)アルコキシ基、 (C厂 C6)ァ ルキルチオ基、 ハ口(C厂 C6)アルキルチオ基、 (C厂 c6)アルキルスルフィニル基、 ノヽロ(CrC6)アルキルスルフィニル基、 (C厂 C6)アルキルスルホニル基、 ノヽロ(C厂 C6)アルキルスルホニル基、 (C C6)アルキルカルボニル基、 ノヽロ(C厂 c6)アルキル カルボニル基、 (C厂 C6)アルコキシカルボニル基、 カルボキシル基、 モノ (d -
c6) アルキルアミノカルボニル基、 同一又は異なっても良いジ (c!- c6) アルキル ァミノカルボニル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択されるC 6) Anorekiru group, (C厂C 6) alkoxy groups, halo (C厂C 6) alkoxy groups, ((^ - (6) alkyl thio groups, Nono b (C厂C 6) alkylthio group, - C 6 ) alkylsulfinyl group, Nono b (C r C 6) alkylsulfinyl group, (C r C 6) alkylsulfonyl group, Bruno, mouth (C厂c 6) § alkylsulfonyl group, (C r C 6) alkylcarbonyl group (C! -C 6 ) alkyl oleponyl group, (c Factory c 6 ) alkoxycarbonyl group, carboxyl group, mono (CrC 6 ) alkylaminocarbonyl group, di (c c 6 ) a substituted phenyl group having 1 to 5 substituents selected from an alkylaminocarbonyl group, a hydroxyl group, an amino group, a cyano group or a nitro group, a phenoxy group, which may be the same or different, a halogen atom, (C厂c 6) alkyl group, (c 2 - c 6) alkenyl Le group, (c 2 - c 6) alkynyl, cyclo (C 3 - C 6) alkyl group, C port (C厂c 6) alkyl group, Shikuroha port (c 3 - c 6) alkyl group, (Cf C 6 ) alkoxy group, halo (C factory c 6 ) alkoxy group, (-c 6 ) alkylthio group, nodro (C factory C 6 ) alkylthio group, (() alkylsulfinyl group, nodro (Ci-Ce) alkyl sulfinyl group, (c r c 6) alkylsulfonyl group, Nono b (c r c 6) alkylsulfinyl Honiru group, (Ci _c 6) alkylcarbonyl group, Bruno, mouth ((:厂c 6) alkyl Cal Poni group, ( C! -C 6 ) alkoxycarbonyl group, carboxyl group, mono (c r c 6 ) alkylaminocarbonyl group, di (C factory c 6 ) alkylaminocarbon A substituted phenoxy group having 1 to 5 substituents selected from a hydroxyl group, a hydroxyl group, an amino group, a cyano group or a nitro group, a phenylthio group, which may be the same or different, a halogen atom, (C Factory C 6) alkyl, (C 2 - C 6) alkenyl, (C 2 - C 6) alkynyl group, shea click port (c 3 - C 6) alkyl groups, halo (C厂c 6) alkyl group, Shikuroha port (C 3 -c 6 ) alkyl group, (C r C 6 ) alkoxy group, halo (CFactory C 6 ) alkoxy group, (CFactory C 6 ) alkylthio group, halo (C r C 6 ) alkylthio group, (C厂C 6) alkylsulfinyl group, Nono port (C厂c 6) alkyl sulfinyl group, (C厂C 6) alkylsulfonyl group, Nono b (C厂c 6) alkyl sulfonyl group, (C厂C 6) Alkyl carbonyl group, no, mouth (C Factory c 6 ) alkyl carbonyl group, (C factory c 6 ) alkoxy carbonyl group, carbo Hexyl group, a mono (C厂c 6) alkylamino mosquitoes carbonyl group, the same or different and may di (-) alkylaminocarbonyl group, a hydroxyl group, an amino group, 1-5 selected from Shiano group or a nitro group A substituted phenylthio group having a substituent, a phenylsulfinyl group, which may be the same or different, a halogen atom, a (C factory c 6 ) alkyl group, a (c 2 -c 6 ) alkenyl group, and a (c 2 -c 6) alkynyl, cyclo (C 3 - C 6) alkyl group, C port (C厂c 6) alkyl group, Shikuroha port (c 3 - c 6) alkyl group, (C厂C 6) alkoxy groups, halo ( C “C 6 ) alkoxy group, (C Factory C 6 ) alkylthio group, nodro (cc 6 ) alkylthio group, (−C 6 ) alkylsulfinyl group, noduro (CFactory c 6 ) alkynolesnorefiel group, (C r C 6) alkylsulfonyl group, Bruno, mouth (c r c 6) Arukirusu Honiru group, (C厂C 6) alkylcarbonyl group, Nono b (C厂c 6) alkylcarbonyl alkylsulfonyl group, (C r C 6) alkoxycarbonyl group, a carboxyl group, a mono (C厂c 6) Arukiruami Bruno carbonyl group, the same or different and may di (C厂C 6) alkylamino carbonylation group, a hydroxyl group, an amino group, a substituted Hue Nils sulfide el with 1 to 5 substituents selected from Shiano group or a nitro group Group, phenylsulfonyl group, which may be the same or different, a halogen atom, a (c Factory c 6 ) alkyl group, a (c 2 -c 6 ) alkenyl group, a (c 2 -c 6 ) alkynyl group, 3 -C 6 ) alkyl group, halo (C factory c 6 ) alkyl group, cycloha (C 3 _C 6 ) alkyl group, (C factory C 6 ) alkoxy group, halo (C factory C 6 ) alkoxy group, (C厂C 6) § alkylthio group, C port (C厂C 6) alkylthio group, (C厂c 6) alkylsulfinyl group, Nono b (C r C 6) alkylsulfinyl group, (C厂C 6) alkylsulfonyl group, Nono b (C厂C 6) alkylsulfonyl group, (CC 6) alkylcarbonyl group, Noro (C Factory c 6 ) alkyl carbonyl group, (C Factory C 6 ) alkoxycarbonyl group, carboxyl group, mono (d- c 6 ) selected from alkylaminocarbonyl, same or different di (c! -c 6 ) alkylaminocarbonyl, hydroxyl, amino, cyano or nitro
:!〜 5個の置換基を有する置換フエニルスルホニル基、 (C厂 C6)アルキルカルボ ニル基、 ノヽロ(C厂 C6)アルキルカルボニル基、 フエニルカルボニル基、 同一又は 異なっても良く、 ハロゲン原子、 ( - C6)アルキル基、 (C2- C6)アルケニル基、 (C2- C6)アルキニル基、 シク口(C3- C6)アルキル基、 ハロ( -( 6)アルキル基、 シクロハ 口(C3- C6)アルキル基、 (C厂 C6)アルコキシ基、 ノヽロ(C厂 C6)アルコキシ基、 (C厂 c6) アルキルチオ基、 ハロ(C厂 C6)アルキルチオ基、 (C厂 c6)アルキルスルフィニル基、 ノ、口(C厂 C6)アルキルスルフィニル基、 (C厂 C6)アルキルスルホニル基、 ハロ(d - C6)アルキルスルホニル基、 (C厂 C6)アルキルカルボニル基、 ハロ(C厂 c6)アルキル カルボニル基、 (cr C6)アルコキシカルボニル基、 カルボキシル基、 モノ (C厂 アルキルアミノカルボニル基、 同一又は異なっても良いジ (C厂 C6) アルキル ァミノカルボ二ル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される:! Substituted phenylalanine sulfonyl group having to 5 substituents, (C厂C 6) alkylcarbonyl group, Nono b (C厂C 6) alkylcarbonyl group, phenylpropyl group, the same or different and halogen atoms, (- C 6) alkyl groups, (C 2 - C 6) alkenyl, (C 2 - C 6) alkynyl group, consequent opening (C 3 - C 6) alkyl groups, halo (- (6) alkyl group , Shikuroha port (C 3 - C 6) alkyl groups, (C厂C 6) alkoxy group, Nono b (C厂C 6) alkoxy groups, (C厂c 6) alkylthio groups, halo (C厂C 6) alkylthio Group, (CFactory c 6 ) alkylsulfinyl group, NO, mouth (CFactory C 6 ) alkylsulfinyl group, (CFactory C 6 ) alkylsulfonyl group, halo (d-C 6 ) alkylsulfonyl group, (CFactory C 6) alkylcarbonyl group, halo (C厂c 6) alkylcarbonyl group, (c r C 6) an alkoxycarbonyl Boniru group, a carboxyl group, is selected mono (C厂alkylaminocarbonyl group, the same or different and may be di (C厂C 6) alkyl Aminokarubo group, a hydroxyl group, an amino group, a Shiano group or a nitro group
:!〜 5個の置換基を有する置換フエニルカルボニル基、 (C厂 C6)アルコキシカル ポニル基、 カルボキシル基、 モノ (CfC6) アルキルアミノカルボニル基、 同一 又は異なっても良いジ (CfCs) アルキルアミノカルボニル基、 フエニルァミノ カルボ二ル基、 同一又は異なっても良く、 ハロゲン原子、 (C厂 c6)アルキル基、:! Substituted phenyl carbonyl group having 5 to 5 substituents, (C Factory C 6 ) alkoxycarbonyl group, carboxyl group, mono (CfC 6 ) alkylaminocarbonyl group, di (CfCs) which may be the same or different An alkylaminocarbonyl group, a phenylamino carbonyl group, which may be the same or different, a halogen atom, a (CFactory 6 ) alkyl group,
(c2- c6)アルケニル基、 (c2-c6)アルキニル基、 シクロ(c3- c6)アルキル基、 ハロ (Ci- アルキル基、 シクロハ口(c3-c6)アルキル基、 (CfCs)アルコキシ基、 ハロ (CrC6)アルコキシ基、 (C厂 C6)アルキルチオ基、 ノヽロ (C厂 C6)アルキルチオ基、 (C厂 C6)アルキルスルフィニル基、 ノヽ口(C厂 C6)アルキルスルフィニル基、 (C厂 c6) アルキルスルホニル基、 ノ、口(C厂 C6)アルキルスルホニル基、 (C厂 c6)アルキル力 ルボニル基、 ハロ(C厂 C6)アルキルカルボニル基、 (( c6)アルコキシカルボニル 基、 力ルポキシル基、 モノ ( - c6) アルキルアミノカルボニル基、 同一又は異 なっても良いジ (C厂 C6) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シ ァノ基又はニトロ基から選択される 1〜 5個の置換基を環上に有する置換フエ二 ルァミノカルポニル基、 フエニル (C厂 c6) アルキルアミノカルボニル基、 同一 又は異なっても良く、 ハロゲン原子、 (C厂 c6)アルキル基、 (c2- c6)アルケニル基、(c 2 - c 6) alkenyl, (c 2 -c 6) alkynyl, cyclo (c 3 - c 6) alkyl group, halo (CI- alkyl group, Shikuroha port (c 3 -c 6) alkyl group, (CfCs) alkoxy group, halo (C r C 6 ) alkoxy group, (CFactory C 6 ) alkylthio group, nodro (CFactory C 6 ) alkylthio group, (CFactory C 6 ) alkylsulfinyl group, Factory C 6 ) Alkylsulfinyl group, (C Factory c 6 ) Alkylsulfonyl group, ノ, mouth (C Factory C 6 ) Alkylsulfonyl group, (C Factory c 6 ) Alkyl force Rubonyl group, Halo (C Factory C 6 ) Alkyl carbonyl group, ((c 6) alkoxycarbonyl group, a force Rupokishiru group, mono (- c 6) alkylaminocarbonyl group, the same or may be made different di (C厂C 6) alkylaminocarbonyl group, a hydroxyl group, an amino group And 1 to 5 substituents selected from a cyano group or a nitro group Substituted phenylene Rua amino Cal Poni Le group having, phenyl (C厂c 6) alkylaminocarbonyl group, which may be identical or different, halogen atom, (C厂c 6) alkyl group, (c 2 - c 6) alkenyl group,
(c2- gアルキニル基、 シクロ(c3- c6)アルキル基、 ハロ(c「c6)アルキル基、 シク
ロハ口(C3- C6)アルキル基、 (C厂 c6)アルコキシ基、 ハロ(crc6)アルコキシ基、 (CfCs)アルキルチオ基、 ハロ( - c6)アルキルチオ基、 ( - c6)アルキルスルフィ ニル基、 ノヽロ(C厂 c6)アルキルスルフィニル基、 (cr c6)アルキルスルホニル基、 ノヽロ(C厂 C6)アルキルスルホニル基、 (CrC6)アルキルカルボニル基、 ノ、口(C厂 c6) アルキルカルボニル基、 (CrC6)アルコキシカルポニル基、 カルボキシル基、 モ ノ ( - ) アルキルアミノカルボニル基、 同一又は異なっても良いジ (C厂 C6) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選 択される 1 〜 5個の置換基から選択される 1以上の置換基を環上に有する置換フ ェニル (CrC6) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シァノ基又 はニトロ基から選択される 1 〜 5個の置換基を示す。 又、 Yはベンゼン環上の隣 接する炭素原子と一緒になつて、 同一又は異なっても良く、 酸素原子、 硫黄原子 又は窒素原子 (該窒素原子は水素原子、 (c「 c6)アルキル基、 (c2- c6)アルケニル 基、 (c2- c6)アルキニル基又はシク口(c3- c6)アルキル基によって置換されていて も良い。 ) から選択される 1乃至 2個のへテロ原子により中断されても良い(C厂 C4)アルキレン基により 5乃至 6員環を形成しても良い。 } (c 2 -g alkynyl group, cyclo (c 3 -c 6 ) alkyl group, halo (c “c 6 ) alkyl group, Loja port (C 3 - C 6) alkyl groups, (C厂c 6) alkoxy groups, halo (c r c 6) alkoxy groups, (cfcs) alkylthio groups, halo (- c 6) alkylthio group, (- c 6 ) alkyl sulfide group, Nono b (C厂c 6) alkylsulfinyl group, (c r c 6) alkylsulfonyl group, Nono b (C厂C 6) alkylsulfonyl groups, (C r C 6) alkylcarbonyl group (C Factory c 6 ) alkylcarbonyl group, (C r C 6 ) alkoxycarbonyl group, carboxyl group, mono (-) alkylaminocarbonyl group, di (C factory C 6 ) which may be the same or different Substituted phenyl having at least one substituent selected from 1 to 5 substituents selected from an alkylaminocarbonyl group, a hydroxyl group, an amino group, a cyano group, or a nitro group (C r C 6 ) Alkylaminocarbonyl group, hydroxyl group, amino group, § Roh group or represents 1 to 5 substituents selected from a nitro group. And Y may be the same as or different from an adjacent carbon atom on the benzene ring, and may be an oxygen atom, a sulfur atom, or a nitrogen atom (the nitrogen atom is a hydrogen atom, a (c “c 6 ) alkyl group, (C 2 -c 6 ) an alkenyl group, (c 2 -c 6 ) an alkynyl group or a substituted (c 3 -c 6 ) alkyl group. A 5- or 6-membered ring may be formed by an alkylene group which may be interrupted by a terrorist atom (C Factory C 4 ).
で表されるハロアルキルスルホンァニリ ド誘導体又はその塩類。 Or a salt thereof.
2. Qが、 構成原子の少なくとも 1個が窒素原子であり、 かつ窒素原子が Aと の結合部位となり、 炭素原子、 窒素原子、 酸素原子、 硫黄原子又は燐原子を構成 元素としてなる 4乃至 1 3員へテロ環又は同一若しくは異なっても良く、 ハロゲ ン原子、 (C厂 C6)アルキル基、 (C2 C6)アルケニル墓、 (C2- C6)アルキニル基、 シク 口(C3- C7)アルキル基、 ハ口( - )アルキル基、 シクロハ口(C3- C7)アルキル基、 (C厂 C6)アルコキシ基、 ハロ(C厂 C6)アルコキシ基、 ( -Ce)アルキルチオ基、 ハロ2. Q is 4 to 1 in which at least one of the constituent atoms is a nitrogen atom, and the nitrogen atom is a bonding site with A, and a carbon, nitrogen, oxygen, sulfur, or phosphorus atom is a constituent element It may be heterocyclic or the same or different to 3-membered, halogen atom, (C厂C 6) alkyl groups, (C 2 C 6) alkenyl tomb, (C 2 - C 6) alkynyl group, consequent opening (C 3 - C 7) alkyl group, C port (-) alkyl group, Shikuroha port (C 3 - C 7) alkyl group, (C厂C 6) alkoxy groups, halo (C厂C 6) alkoxy groups, (-Ce) Alkylthio group, halo
(C厂 C6)アルキルチオ基、 (C厂 C6)アルキルスルフィニル基、 ハ口(C厂 c6)アルキル スルフィニル基、 (C厂 c6)アルキルスルホニル基、 ハロ(crc6)アルキルスルホ二 ル基、 フユニル基、 同一又は異なっても良く、 Y (Yは請求項 1に同じ。 ) から 選択される 1以上の置換基を有する置換フユニル基、 フエニル (C厂 c6) アルキ ル基、 同一又は異なっても良く、 Y (Yは前記に同じ。 ) から選択される 1以上 の置換基を環上に有するフユニル (cr c6) アルキル基、 フエノキシ基、 同一又 は異なっても良く、 Y (Yは前記に同じ。 ) から選択される 1以上の置換基を有
する置換フエノキシ基、 フエ二ルチオ基、 同一又は異なっても良く、 Y (Yは前 記に同じ。 ) から選択される 1以上の置換基を有する置換フエ二ルチオ基、 フエ ニルスルフィニル基、 同一又は異なっても良く、 Y (Yは前記に同じ。 ) 力 ^選 択される 1以上の置換基を有する置換フユニルスルフィエル基、 フヱニルスルホ ニル基、 同一又は異なっても良く、 Y (Yは前記に同じ。 ) から選択される 1以 上の置換基を有する置換フヱニルスルホニル基、 (C厂 c6)アルキルカルボニル基、 ノヽロ(C^Ce)アルキルカルポニル基、 フエニルカルボニル基、 同一又は異なって も良く、 Y (Yは前記に同じ。 ) から選択される 1以上の置換基を有する置換フ ェニルカルボニル基、 (C厂 c6)アルコキシカルポニル基、 カルボキシル基、 モノ (CrC6) アルキルアミノカルボニル基、 同一又は異なっても良いジ (C厂 ce) ァ ルキルアミノカルボニル基、 フエニルァミノカルボニル基、 同一又は異なっても 良く、 Y (Yは前記に同じ。 ) から選択される 1以上の置換基を環上に有する置 換フエニノレアミノカルボ二ル基、 フエニル (C厂 c6) アルキルアミノカルボニル 基、 同一又は異なっても良く、 Y (Yは前記に同じ。 ) から選択される 1以上の 置換基を環上に有する置換フエニル (C厂 C6) アルキルァミノカルボニル基、 複 素環基 (複素環基は、 ピリジル基、 ピリジン一 N—ォキシド基、 ピリ ミジニル基、 ビラジニル基、 トリアジニル基、 フリル基、 テトラヒドロフリル基、 チェニル基、 テトラヒドロチェニル基、 テトラヒドロビラニル基、 テトラヒドロチォピラニル 基、 ォキサゾリル基、 イソキサゾリル基、 ォキサジァゾリル基、 チアゾリル基、 イソチアゾリル基、 チアジァゾリル基、 イミダゾリル基、 トリアゾリル基、 ピラ ゾリル基、 モルホリニル基から選択される複素環基を示す。 ) 、 同一又は異なつ ても良く、 Y (Yは前記に同じ。 ) から選択される 1以上の置換基を有する置換 複素環基 (複素環基は前記に同じ。 ) 、 水酸基、 アミノ基、 シァノ基又はニトロ 基から選択される 1以上の置換基で置換された構成原子の少なくとも 1個が窒素 原子であり、 かつ窒素原子が Aとの結合部位となり炭素原子、 窒素原子、 酸素原 子、 硫黄原子又は憐原子を構成元素としてなる 4乃至 1 3員へテロ環である請求 項 1記載のハロアルキルスルホンァニリ ド誘導体又はその塩類。 (C Factory C 6 ) alkylthio group, (C Factory C 6 ) alkyl sulfinyl group, haguchi (C Factory c 6 ) alkyl sulfinyl group, (C Factory c 6 ) alkyl sulfonyl group, halo (c r c 6 ) alkyl sulfo A substituted or unsubstituted fuunyl group having at least one substituent selected from the group consisting of a phenyl group, a fuunyl group and Y (Y is the same as in claim 1), and a phenyl (C Factory c 6 ) alkyl group May be the same or different, and may be a fuunyl (c r c 6 ) alkyl group having at least one substituent selected from Y (Y is the same as defined above) on the ring, a phenoxy group, the same or different. And has one or more substituents selected from Y (Y is the same as described above). Substituted phenyloxy group, phenylthio group, and the same or different, and substituted phenylthio group, phenylsulfinyl group, and the like having one or more substituents selected from Y (Y is the same as described above) Y (Y is the same as above.) Force ^ A substituted fuunylsulfiel group or a phenylsulfonyl group having at least one selected substituent, which may be the same or different, and Y (Y is The same as defined above), a substituted phenylsulfonyl group having at least one substituent selected from the group consisting of: (C Factory c 6 ) an alkylcarbonyl group, a nodro (C ^ Ce) alkylcarbonyl group, a phenylcarbonyl group, which may be identical or different, Y (Y is the same. as defined above) substituted full E alkenyl group having 1 or more substituents selected from, (C厂c 6) alkoxy Cal Poni group, a carboxyl group, a mono (C r C 6) A Kill aminocarbonyl group, the same or different and may di (C厂c e) § Le Kill aminocarbonyl group, phenylpropyl § amino carbonyl group, the same or different and, Y (Y is the same. As defined above) is selected from A substituted phenyleneaminocarbonyl group having one or more substituents on the ring, a phenyl (C Factory c 6 ) alkylaminocarbonyl group, which may be the same or different, from Y (Y is the same as defined above); Substituted phenyl having one or more substituents selected on the ring (C Factory C 6 ) Alkylaminocarbonyl group, complex ring group (heterocyclic group is pyridyl group, pyridine-N-oxide group, pyrimidinyl group , Virazinyl group, triazinyl group, furyl group, tetrahydrofuryl group, chenyl group, tetrahydrothenyl group, tetrahydroviranyl group, tetrahydrothiopyranyl group, oxa A heterocyclic group selected from the group consisting of a luyl group, an isoxazolyl group, an oxdiazolyl group, a thiazolyl group, an isothiazolyl group, a thiaziazolyl group, an imidazolyl group, a triazolyl group, a pyrazolyl group, and a morpholinyl group. A substituted heterocyclic group having one or more substituents selected from Y (Y is the same as described above) (the heterocyclic group is the same as described above), a hydroxyl group, an amino group, a cyano group or a nitro group; At least one of the constituent atoms substituted with the above substituents is a nitrogen atom, and the nitrogen atom becomes a bonding site with A, and a carbon atom, a nitrogen atom, an oxygen atom, a sulfur atom, or a pure atom is a constituent element 2. The haloalkyl sulfonanilide derivative or a salt thereof according to claim 1, which is a 4- to 13-membered hetero ring.
Q-1 Q-2 Q-1 Q-2
Q-6 Q-7 Q-8 Q-9 Q-6 Q-7 Q-8 Q-9
Q-10 Q-11 Q-12 Q-13 Q-14 Q-10 Q-11 Q-12 Q-13 Q-14
{式中、 G G2は同一又は異なっても良く、 酸素原子、 硫黄原子、 N— R3' (式中、 R3' は水素原子、 (C厂 C6) アルキル基、 シァノ基、 ニトロ基、 フエ二 ル ( - C6)アルキル基、 同一又は異なっても良く、 Υ, (Υ' は後記に示す。 ) から選択される 1以上の置換基を環上に有する置換フエニル (C厂 c6)アルキル基、 フエニル基又は同一若しくは異なっても良く、 γ, (γ' は後記に示す。 ) から 選択される 1以上の置換基を有する置換フエ二ル基を示す。 ) 、 Ν— OR4'{Wherein GG 2 may be the same or different; oxygen atom, sulfur atom, N—R 3 ′ (wherein, R 3 ′ is a hydrogen atom, (C Factory C 6 ) alkyl group, cyano group, nitro group , phenylene Le (- C 6) alkyl group, which may be identical or different, Υ, (. Υ 'is shown in the following) one or more substituted phenyl having a substituent on the ring (C厂c is selected from 6 ) represents an alkyl group, a phenyl group, or a substituted phenyl group which may be the same or different and has at least one substituent selected from γ and (γ 'is shown below.)), Ν-OR 4 '
(式中、 R は水素原子、 ( - C6) アルキル基、 フエニル ( - C6)アルキル基又 は同一若しくは異なっても良く、 Υ' (Υ' は後記に示す。 ) から選択される 1 以上の置換基を環上に有する置換フエニル (CrC6)アルキル基を示す。 ) 、 N— NR5' R6' (式中、 R5' 及ぴ R6' は同一又は異なっても良く、 水素原子、 フ
ェニル基又は同一若しくは異なっても良く、 Υ ' (Υ ' は後記に示す。 ) 力 ら選 択される 1以上の置換基を有する置換フエ二ル基を示す。 又、 R5' と R6' は一 緒になって (C3 - C6) アルキレン基を示すこともできる。 ) 又は C R7R8 (式中、 R7及ぴ R8は同一又は異なっても良く、 水素原子、 ( - C6) アルキル基、 (C厂 C6) アルコキシカルボニル基、 シァノ基又はニトロ基を示す。 ) を示す。 (In the formula, R is a hydrogen atom, a (-C 6 ) alkyl group, a phenyl (-C 6 ) alkyl group or may be the same or different, and is selected from Υ ′ (where Υ ′ is shown below.) 1 Represents a substituted phenyl (C r C 6 ) alkyl group having the above substituents on the ring.), N—NR 5 ′ R 6 ′ (where R 5 ′ and R 6 ′ may be the same or different Good, hydrogen atom, A phenyl group or a substituted phenyl group having one or more substituents, which may be the same or different and is selected from the group consisting of Υ ′ (Υ ′ is described below). R 5 ′ and R 6 ′ can be taken together to represent a (C 3 -C 6 ) alkylene group. Or CR 7 R 8 (wherein, R 7 and R 8 may be the same or different and each represents a hydrogen atom, a (-C 6 ) alkyl group, a (C Factory C 6 ) alkoxycarbonyl group, a cyano group or a nitro group. ) Is shown.
J 1は酸素原子、 硫黄原子又は N— R9 (式中、 R9は水素原子、 (C「 C6) アルキ ル基、 フエニル (C厂 C6) アルキル基、 同一又は異なっても良く、 Y ' (Y, は 後記に示す。 ) から選択される 1以上の置換基を環上に有する置換フ ニル (C厂 C6) アルキル基、 フエ二ル基、 同一又は異なっても良く、 Υ, (Υ ' は後 記に示す。 ) から選択される 1以上の置換基を有する置換フエニル基、 複素環基 (複素環基は請求項 2に同じ。 ) 、 同一又は異なっても良く、 Υ ' (Υ, は後記 に示す。 ) から選択される 1以上の置換基を有する置換複素環基 (複素環基は前 記に同じ。 ) 、 複素環(C「 C6)アルキル基 (複素環基は前記に同じ。 ) 、 同一又 は異なっても良く、 γ ' (Υ ' は後記に示す。 ) から選択される 1以上の置換基 を環上に有する置換複素環(C^Ce)アルキル基 (複素環基は前記に同じ。 ) 、 モ ノ (C厂 C6) アルキルアミノカルボニル基、 同一又は異なっても良いジ (CfCe) アルキルアミノカルポニル基、 フエニルァミノカルボニル基又は同一若しくは異 なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1以上の置換基を環 上に有する置換フエニルァミノカルボ二ル基を示す。 ) を示す。 J 1 is an oxygen atom, a sulfur atom or N—R 9 (wherein, R 9 is a hydrogen atom, a (C “C 6 ) alkyl group, a phenyl (C Factory C 6 ) alkyl group, which may be the same or different, A substituted phenyl (C Factory C 6 ) alkyl group having at least one substituent selected from Y ′ (Y, is shown below) on the ring, a phenyl group, which may be the same or different; , (Υ 'is shown below.), A substituted phenyl group having one or more substituents, a heterocyclic group (the heterocyclic group is the same as in claim 2), and may be the same or different; '(Υ, is shown below.) Substituted heterocyclic group having one or more substituents selected from the following (heterocyclic groups are the same as described above.), Heterocyclic (C “C 6 ) alkyl groups (heterocyclic The group is the same as described above.), May be the same or different, and is a substituted heterocyclic group having at least one substituent selected from γ ′ (Υ ′ is shown below) on the ring. (C ^ Ce) alkyl group (the heterocyclic group is as defined above.), Mono (C厂C 6) alkylaminocarbonyl group, the same or different and may di (CfCe) alkylamino Cal Poni group, Fueniruamino A carbonyl group or a substituted or unsubstituted phenylaminocarbonyl group having at least one substituent selected from the group consisting of Υ ′ (後 ′ is shown below) which may be the same or different. Show.
J 2及び J 3は同一又は異なっても良く、 酸素原子、 硫黄原子、 Ν— R9 (式中、 R9は前記に同じ。 ) 、 R1Q— C一 R11 (式中、 R1Q及び R 11は同一又は異なっても 良く、 水素原子、 (C「C6)アルキル基、 ハロ(C厂 C6)アルキル基、 (C厂 C6)アルコキ シ基、 ハロ(C厂 C6)アルコキシ基、 (C厂 C6)アルキルチオ基、 ハ口(C厂 C6)アルキル チォ基、 ( - C6)アルキルスルフィニル基、 ノヽロ(C厂 C6)アルキルスルフィニル基、 (CrC6)アルキルスルホニル基、 ハロ(C厂 C6)アルキルスルホニル基、 フエニル( - C6)アルキル基、 同一又は異なっても良く、 Y ' (Y, は後記に示す。 ) から選 択される 1以上の置換基を環上に有する置換フエニル(C厂 C6)アルキル基、 フエ ニル基又は同一若しくは異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択 される 1以上の置換基を有する置換フエ二ル基を示す。 ) 、 C =〇又は C = Sを
示す。 J 2 and J 3 may be the same or different; an oxygen atom, a sulfur atom, Ν—R 9 (wherein R 9 is as defined above), R 1Q —C—R 11 (wherein R 1Q and R 11 may be the same or different, a hydrogen atom, (C "C 6) alkyl groups, halo (C厂C 6) alkyl groups, (C厂C 6) an alkoxy group, halo (C厂C 6) alkoxy group, (C厂C 6) alkylthio group, C port (C厂C 6) alkyl Chiomoto, (- C 6) alkylsulfinyl group, Nono b (C厂C 6) alkylsulfinyl group, (C r C 6) alkylsulfonyl groups, halo (C厂C 6) alkylsulfonyl group, phenyl (- C 6) well alkyl groups, the same or different, Y '(. Y, is shown in the following) from one or more of which is selected A substituted phenyl (C Factory C 6 ) alkyl group having a substituent on the ring, a phenyl group or the same or different, and Υ Υ (Υ 示 す is shown below) Represents a substituted phenyl group having one or more substituents selected from:), C = or C = S Show.
J 4及び J 5は同一又は異なっても良く、 C— R12 (式中、 R12は水素原子、 ハロ ゲン原子、 (C厂 C6)アルキル基、 ハロ(C厂 C6)アルキル基、 (C厂 C6)アルコキシ基、 ハロ(cr C6)アルコキシ基、 (C - C6)アルキルチオ基、 ハロ(C厂 C6)アルキルチオ基、 (C厂 C6)アルキルスルフィニル基、 ハロ( - )アルキルスルフィニル基、 ( - ) アルキルスルホニル基、 ノヽロ(CrC6)アルキルスルホニル基、 フエニル(C厂 c6)ァ ルキル基、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択され る 1以上の置換基を環上に有するフヱニル(C厂 c6)アルキル基、 フエニル基、 同 一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1以上の置 換基を有する置換フエニル基又はシァノ基を示す。 ) 又は窒素原子を示す。 J 4 and J 5 may be the same or different, and C—R 12 (where R 12 is a hydrogen atom, a halogen atom, a (C Factory C 6 ) alkyl group, a halo (C Factory C 6 ) alkyl group, (C厂C 6) alkoxy groups, halo (c r C 6) alkoxy groups, (C - C 6) alkylthio groups, halo (C厂C 6) alkylthio group, (C厂C 6) alkylsulfinyl groups, halo ( -) Alkylsulfinyl group, (-) alkylsulfonyl group, nodro (C r C 6 ) alkylsulfonyl group, phenyl (C Factory c 6 ) alkyl group, which may be the same or different. A phenyl (C Factory 6 ) alkyl group having at least one substituent selected from the following on the ring, a phenyl group, which may be the same or different, and Υ ′ (Υ ′ is described below). Represents a substituted phenyl group or a cyano group having at least one substituent selected from the following:) or a nitrogen atom.
J 6は酸素原子、 硫黄原子、 N— R9 (式中、 R9は前記に同じ。 ) 又は R 1D— C - R11 (式中、 R1()及び R11は前記に同じ。 ) を示す。 J 6 is an oxygen atom, a sulfur atom, N—R 9 (wherein R 9 is as defined above) or R 1D —C—R 11 (where R 1 () and R 11 are as defined above) Is shown.
R9は前記に同じ。 R 9 is the same as above.
R13及び R"は同一又は異なっても良く水素原子、 ハロゲン原子、 ( - C6) ァ ルキル基、 ノヽロ(( )アルキル基、 (C厂 C6)アルコキシ基、 ハロ(C厂 C6)アルコキ シ基、 ((厂 c6)アルキルチオ基、 ハロ(c厂 c6)アルキルチオ基、 c6)アルキルス ノレフィエル基、 ノヽロ(CfC6)アルキルスルフィニル基、 (crce)アルキルスルホ二 ル基、 ノヽロ(c厂 c6)アルキルスルホニル基、 フエニル(c厂 c6)アルキル基、 同一又 は異なっても良く、 γ ' (γ ' は後記に示す。 ) から選択される 1以上の置換基 を環上に有する置換フエニル (C厂 C6)アルキル基、 フエ二ル基、 同一又は異なつ ても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1以上の置換基を有する 置換フエニル基、 複素環基 (複素環基は前記に同じ。 ) 、 同一又は異なっても良 く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1以上の置換基を有する置換複 素環基 (複素環基は前記に同じ。 ) 、 複素環 (cr c6)アルキル基 (複素環基は前 記に同じ。 ) 、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択 される 1以上の置換基を環上に有する置換複素環 (C厂 c6)アルキル基 (複素環基 は前記に同じ。 ) 、 モノ (C厂 c6) アルキルアミノカルボニル基、 同一又は異な つても良いジ (C厂 c6) アルキルアミノカルボニル基、 フエニルァミノカルボ二 ル基、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1
以上の置換基を環上に有する置換フエニルァミノカルボニル基又はシァノ基を示 す。 R 13 and R "may be the same or different and may be a hydrogen atom, a halogen atom, a (-C 6 ) alkyl group, a nodro (() alkyl group, a (C Factory C 6 ) alkoxy group, a halo (C Factory C 6 ) an alkoxy group, ((厂c 6) alkylthio groups, halo (c厂c 6) alkylthio group, c 6) Arukirusu Norefieru group, Nono b (CFC 6) alkylsulfinyl group, (c r c e) alkylsulfonyl two group, Nono b (c厂c 6) alkylsulfonyl group, phenyl (c厂c 6) alkyl group, the same or may be different, gamma 1 or more '(gamma' is shown later.) is selected from substituted phenyl (C厂C 6) alkyl group having a substituent on the ring, Hue group, which may be the same or different dates, Upsilon 1 or more of '(Upsilon' is shown later.) is selected from A substituted phenyl group having a substituent, a heterocyclic group (the heterocyclic group is the same as described above), the same or different Also rather good, Upsilon substituted double heterocyclic group '(Upsilon' is. Shown in the following) has one or more substituents selected from (heterocyclic group is as defined above.), A heterocyclic (c r c 6) An alkyl group (the heterocyclic group is the same as described above), which may be the same or different, and a substituted heterocyclic ring having at least one substituent selected from Υ ′ (Υ ′ is described below) on the ring; C factory c 6 ) alkyl group (heterocyclic group is the same as above), mono (C factory c 6 ) alkylaminocarbonyl group, di (C factory c 6 ) alkylaminocarbonyl group, which may be the same or different, phenyl An aminocarbon group, which may be the same or different, and is selected from Υ Υ (Υ 示 す is shown below) 1 It represents a substituted phenylaminocarbonyl group or a cyano group having the above substituent on the ring.
R 15及ぴ R 16は同一又は異なっても良く、 水素原子又は(C厂 gアルキル基を示 す。 R 15 and R 16 may be the same or different and represent a hydrogen atom or a (C alkyl group).
X ' は同一又は異なっても良く、 水素原子、 ハロゲン原子、 (C厂 C6)アルキル 基、 (c2 - c6)アルケニル基、 (c2- c6)アルキニル基、 シクロ(c3 - c7)アルキル基、 ノヽ 口(Cr C6)アルキル基、 シクロハ口(C3 - 7)アルキル基、 (C厂 c6)アルコキシ基、 ノヽロ (CrC6)アルコキシ基、 (C厂 C6)アルキルチオ基、. ハロ cs)アルキルチオ基、 (C厂 C6)アルキルスルフィニル基、 ノヽロ (C厂 C6)アルキルスルフィニル基、 (C厂 c6) アルキルスルホニル基、 ノ、口(C厂 c6)アルキルスルホニル基、 フヱニル基、 同一 又は異なっても良く、 γ ' (Υ ' は後記に示す。 ) 力 ^選択される 1以上の置換 基を有する置換フエニル基、 フエノキシ基、 同一又は異なっても良く、 Y 'X ′ may be the same or different; a hydrogen atom, a halogen atom, a (C Factory C 6 ) alkyl group, a (c 2 -c 6 ) alkenyl group, a (c 2 -c 6 ) alkynyl group, a cyclo (c 3- c 7) alkyl group, Nono opening (C r C 6) alkyl group, Shikuroha port (C 3 - 7) alkyl, (C厂c 6) alkoxy group, Nono b (C r C 6) alkoxy groups, (C Factory C 6 ) alkylthio group, halo c s ) alkylthio group, (CFactory C 6 ) alkylsulfinyl group, nodro (CFactory C 6 ) alkylsulfinyl group, (CFactory c 6 ) alkylsulfonyl group, no, mouth (C factory c 6 ) alkylsulfonyl group, phenyl group, which may be the same or different, and γ ′ (Υ ′ is shown below.) Force ^ substituted phenyl group having one or more substituents selected, phenoxy group, Same or different, Y '
(Υ ' は後記に示す。 ) 力 ら選択される 1以上の置換基を有する置換フエノキシ 基、 フエ二ルチオ基、 同一又は異なっても良く、 Υ, (Υ ' は後記に示す。 ) か ら選択される 1以上の置換基を有する置換フエ二ルチオ基、 フヱニルスルフィ二 ル基、 同一又は異なっても良く、 Υ ' (Υ ' は後記に示す。 ) から選択される 1 以上の置換基を有する置換フユニルスルフィエル基、 フヱニルスルホニル基、 同 一又は異なっても良く、 γ ' (γ ' は後記に示す。 ) から選択される 1以上の置 換基を有する置換フエニルスルホニル基、 (C厂 c6)アルキルカルポニル基、 ノヽロ (C厂 C6)アルキルカルボ二ル基、 フエ二ルカルポニル基、 同一又は異なっても良 く、 Υ ' (Υ ' は後記に示す。 ) 力 ら選択される 1以上の置換基を有する置換フ ェニルカルボニル基、 (C厂 c6)アルコキシカルボニル基、 カルボキシル基、 モノ (CrC6) アルキルアミノカルボニル基、 同一又は異なっても良いジ (C厂 c6) ァ ルキルアミ/カルボニル基、 フエニルァミノカルボニル基、 同一又は異なっても 良く、 Υ ' (Υ ' は後記に示す。 ) 力 ら選択される 1以上の置換基を環上に有す る置換フエニルァミノカルポニル基、 フエニル (crc6) アルキルアミノカルボ ニル基、 同一又は異なっても良く、 Υ, (Υ ' は後記に示す。 ) から選択される 1以上の置換基を環上に有する置換フヱニル (ς- c6) アルキルアミノカルボ二 ル基、 水酸基、 アミノ基、 シァノ基又はニトロ基から選択される 1〜 4個の置換
基を示す。 (Υ ′ is described below.) A substituted phenoxy group having at least one substituent selected from the group, a phenylthio group, which may be the same or different, and Υ and (Υ ′ are described later) A substituted phenylthio group or a phenylsulfinyl group having at least one selected substituent, which may be the same or different, and having at least one substituent selected from Υ ′ (Υ ′ is shown below) A substituted phenylsulfenyl group, a phenylsulfonyl group, which may be the same or different, and have a substituted phenylsulfonyl group having at least one substituent selected from γ ′ (γ ′ is shown below), (C Factory c 6 ) alkyl carbonyl group, nodro (C Factory C 6 ) alkyl carbonyl group, phenyl carponyl group, which may be the same or different. Substituted phenyl carbonyl having one or more substituents selected (C Factory c 6 ) alkoxycarbonyl group, carboxyl group, mono (C r C 6 ) alkylaminocarbonyl group, di (C Factory c 6 ) alkylamino / carbonyl group, which may be the same or different, phenyla A minocarbonyl group, which may be the same or different, and a substituted phenylaminoaminocarbonyl group having at least one substituent selected from the group consisting of Υ ′ (Υ ′ is shown below), phenyl (c r c 6 ) an alkylaminocarbonyl group, which may be the same or different, and a substituted phenyl (ς-c 6 ) having at least one substituent selected from Υ and (Υ 'shown below) on the ring 1 to 4 substituents selected from alkylaminocarbonyl, hydroxyl, amino, cyano or nitro Represents a group.
Y, は同一又は異なっても良く、 水素原子、 ハロゲン原子、 ( - c6)アルキル 基、 (c2 - c6)アルケニル基、 (c2- c6)アルキニル基、 シクロ(c3- c6)アルキル基、 ノヽ 口(cr c6)アルキル基、 シクロハ口(c3- c6)アルキル基、 (c「 c6)アルコキシ基、 ノヽ 口(C厂 C6)アルコキシ基、 ( - )アルキルチオ基、 ハロ(C厂 C6)アルキルチオ基、 (CrC6)アルキルスルフィニル基、 ノヽロ(C厂 C6)アルキルスルフィニル基、 (C!-Ce) アルキルスルホニル基、 ノヽロ c6)アルキルスルホニル基、 フヱニル基、 フエ ノキシ基、 (C厂 C6)アルキルカルボニル基、 ノヽロ(C厂 c6)アルキルカルボ二ル基、 フエニルカルボニル基、 (C厂 c6)アルコキシカルポニル基、 力ルポキシル基、 モ ノ (C厂 C6) アルキルァミノカルボニル基、 ジ (CrC6) アルキルアミノカルボ二 ル基、 フエニルァミノカルボニル基、 水酸基、 アミノ基、 シァノ基又はニトロ基 から選択される 1 〜 5個の置換基を示す。 } Y, which may be the same or different, a hydrogen atom, a halogen atom, (- c 6) alkyl group, (c 2 - c 6) alkenyl, (c 2 - c 6) alkynyl, cyclo (c 3 - c 6 ) an alkyl group, an alkyl group (c r c 6 ) alkyl group, a cycloalkyl group (c 3 -c 6 ) alkyl group, a (c “c 6 ) alkoxy group, a hydroxyl group (C Factory C 6 ) alkoxy group, ) Alkylthio group, halo (CFactory C 6 ) alkylthio group, (C r C 6 ) alkylsulfinyl group, nodro (CFactory C 6 ) alkylsulfinyl group, (C! -Ce) alkylsulfonyl group, nodro c 6 ) Alkylsulfonyl group, phenyl group, phenoxy group, (CFactory C 6 ) alkylcarbonyl group, nodro (CFactory c 6 ) alkyl carbonyl group, phenylcarbonyl group, (CFactory c 6 ) alkoxycarbonyl group force Rupokishiru group, mono (C厂C 6) alkyl § amino group, di (C r C 6 ) represents 1 to 5 substituents selected from an alkylaminocarbonyl group, a phenylaminocarbonyl group, a hydroxyl group, an amino group, a cyano group and a nitro group.}
を示す請求項 2記載のハ口アルキルスルホンァユリ ド誘導体又はその塩類。 3. A haguchialkylsulfonyluride derivative or a salt thereof according to claim 2, which shows:
4. R1がフルォロアルキノレ基を示し、 R2が水素原子を示し、 Qが
4. R 1 represents a fluoroalkynole group, R 2 represents a hydrogen atom, and Q represents
Q-1 Q-2 Q-3 Q-1 Q-2 Q-3
(式中、 G1は酸素原子を示す。 (In the formula, G 1 represents an oxygen atom.
R9はフエニル (C厂 C6)アルキル基、 同一又は異なっても良く、 水素原子、 ハロ ゲン原子、 (C厂 C6)アルキル基、 (C2- C6)アルケニル基、 (C2- C6)アルキニル基、 シ クロ(C3- C6)アルキル基、 ハロ(C厂 C6)アルキル基、 シクロハ口(C3_C6)アルキル基、R 9 may be a phenyl (C factory C 6 ) alkyl group, which may be the same or different, a hydrogen atom, a halogen atom, a (C factory C 6 ) alkyl group, a (C 2 -C 6 ) alkenyl group, a (C 2- C 6) alkynyl, cyclo (C 3 - C 6) alkyl groups, halo (C厂C 6) alkyl group, Shikuroha port (C 3 _C 6) alkyl group,
(c c6)アルコキシ基、 ハロ(c厂 gアルコキシ基、 ( - c6)アルキルチオ基、 ハロ (crc6)アルキルチオ基、 (c厂 c6)アルキルスルフィニル基、 ノヽロ (crc6)アルキル スルフィニル基、 (cr c6)アルキルスルホニル基、 ノヽロ(cr c6)アルキルスルホ二 ル基、 (Cf )アルキルカルボニル基、 ハロ(c厂 c6)アルキルカルボニル基、 (c厂 C6)アルコキシカルボ二ル基、 カルボキシル基、 モノ (C厂 C6) アルキルアミノカ
ルボニル基、 ジ (d- C6) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シ ァノ基又はニトロ基から選択される 1以上の置換基を環上に有する置換フユニル (C厂 c6)アルキル基、 フエニル基、 同一又は異なっても良く、 水素原子、 ハロゲ ン原子、 (C厂 c6)アルキル基、 (c2- c6)アルケニル基、 (c2- c6)アルキニル基、 シク 口(C3_C6)アルキル基、 ハロ(Cr C6)アルキル基、 シクロハ口(C3 - C6)アルキノレ基、 (C厂 C6)アルコキシ基、 ハロ(C厂 c6)アルコキシ基、 ( - c6)アルキルチオ基、 ハロ (C厂 C6)アルキルチオ基、 (C厂 c6)アルキルスルフィニル基、 ノヽ口( - c6)アルキノレ スルフィエル基、 (C厂 c6)アルキルスルホニル基、 ハロ(c!- c6)アルキルスルホ二 ル基、 (Cf^)アルキルカルポニル基、 ノヽロ (C厂 c6)アルキルカルポニル基、 (cr C6)アルコキシカルボニル基、 カルボキシル基、 モノ (CrC6) アルキルァミノ力 ルポニル基、 ジ (cr c6) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シ ァノ基又はニトロ基から選択される 1〜 5個の置換基を有する置換フエニル基、 ピリジル基、 同一又は異なっても良く、 ハロゲン原子、 (C厂 c6)アルキル基、 ノヽ 口(C厂 C6)アルキル基、 (C厂 C6)アルコキシ基又はハロ(C厂 c6)アルコキシ基から選 択される 1以上の置換基を有する置換ピリジル基、 ピリミジル基又は同一若しく は異なっても良く、 ハロゲン原子、 (C「 C6)アルキル基、 ハロ(C厂 c6)アルキル基、 (CfC6)アルコキシ基又はハロ(C!-Ce)アルコキシ基から選択される 1以上の置換 基を有する置換ピリミジル基を示す。 (cc 6 ) alkoxy group, halo (c factory g alkoxy group, (-c 6 ) alkylthio group, halo (c r c 6 ) alkylthio group, (c factory c 6 ) alkylsulfinyl group, nodro (c r c 6 ) alkyl sulfinyl group, (c r c 6) alkylsulfonyl group, Nono b (c r c 6) alkyl sulfonyl Le group, (Cf) alkylcarbonyl group, a halo (c厂c 6) alkylcarbonyl group, (c厂C 6 ) alkoxycarbonyl group, carboxyl group, mono (C Factory C 6 ) alkylaminoca Substituted funil (C Factory c 6 ) alkyl having at least one substituent selected from the group consisting of a rubonyl group, a di (d-C 6 ) alkylaminocarbonyl group, a hydroxyl group, an amino group, a cyano group and a nitro group. Groups, phenyl groups, which may be the same or different, a hydrogen atom, a halogen atom, a (C factory c 6 ) alkyl group, a (c 2 -c 6 ) alkenyl group, a (c 2 -c 6 ) alkynyl group, A (C 3 _C 6 ) alkyl group, a halo (C r C 6 ) alkyl group, a cycloalkyl (C 3 -C 6 ) alkynole group, a (CFactory C 6 ) alkoxy group, a halo (CFactory c 6 ) alkoxy group, (-C 6 ) alkylthio group, halo (CFactory C 6 ) alkylthio group, (CFactory c 6 ) alkylsulfinyl group, no-open (-c 6 ) alkynole sulfiel group, (CFactory c 6 ) alkylsulfonyl group, halo (C! -C 6 ) alkyl sulfonyl group, (Cf ^) alkyl carbonyl group, nodro (C Factory c 6 ) alkyl carbonyl group, (c r C 6 ) alkoxycarbonyl group, carboxyl group, mono (C r C 6 ) alkylamino group luponyl group, di (c r c 6 ) alkylaminocarbonyl group, hydroxyl group, amino group, A substituted phenyl group having 1 to 5 substituents selected from an ano group or a nitro group, a pyridyl group, which may be the same or different, a halogen atom, a (C factory c 6 ) alkyl group, C 6 ) an alkyl group, a substituted pyridyl group having one or more substituents selected from a (C factory C 6 ) alkoxy group and a halo (C factory c 6 ) alkoxy group, a pyrimidyl group, or the same or different One or more substituents selected from a halogen atom, a (C 6 C 6 ) alkyl group, a halo (C 6 c) alkyl group, a (CfC 6 ) alkoxy group or a halo (C! -Ce) alkoxy group. And a substituted pyrimidyl group.
R13はフエニル (c厂 gアルキル基、 同一又は異なっても良く、 水素原子、 ハロ ゲン原子、 ( - C6)アルキル基、 (C2- C6)アルケニル基、 (C2_C6)アルキニル基、 シ ク口(c3 - c6)アルキル基、 ハロ(crc6)アルキル基、 シクロハ口(c3 - c6)アルキル基、R 13 is phenyl (c-factor alkyl group, which may be the same or different, hydrogen atom, halogen atom, (-C 6 ) alkyl group, (C 2 -C 6 ) alkenyl group, (C 2 _C 6 ) alkynyl Group, (c 3 -c 6 ) alkyl group, halo (c r c 6 ) alkyl group, cycloha (c 3 -c 6 ) alkyl group,
(C厂 C6)アルコキシ基、 ハロ( - C6)アルコキシ基、 (C厂 c6)アルキルチオ基、 ハロ (C厂 C6)アルキルチオ基、 (C厂 C6)アルキルスルフィニル基、 ハロ (C厂 c6)アルキル スルフィニル基、 (CrC6)アルキルスルホニル基、 ノヽ口 (CrC6)アルキルスルホ二 ル基、 (Cf C6)アルキルカルポニル基、 ノヽロ(C厂 C6)アルキルカルボニル基、 (C厂 c6)アルコキシカルボニル基、 カルボキシル基、 モノ (crc6) アルキルアミノカ ルボニル基、 ジ (C厂 c6) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シ ァノ基又はニトロ基から選択される 1以上の置換基を環上に有する置換フエニル (C厂 c6)アルキル基、 フエニル基、 同一又は異なっても良く、 水素原子、 ハロゲ
ン原子、 (c厂 c6)アルキル基、 (c2- c6)アルケニル基、 (c2- c6)アルキニル基、 シク 口(c3 - c6)アルキル基、 ハロ( - c6)アルキル基、 シクロハ口(c3- c6)アルキル基、(C Factory C 6 ) alkoxy group, halo (-C 6 ) alkoxy group, (C Factory c 6 ) alkylthio group, halo (CFactory C 6 ) alkylthio group, (CFactory C 6 ) alkylsulfinyl group, halo (C C 6 ) alkyl sulfinyl group, (C r C 6 ) alkylsulfonyl group, no-open (C r C 6 ) alkylsulfonyl group, (Cf C 6 ) alkyl carbonyl group, nodro (C-factor C 6 ) alkyl carbonyl group, (C厂c 6) alkoxycarbonyl group, a carboxyl group, a mono (c r c 6) alkylamino mosquitoes carbonyl group, di (C厂c 6) alkylaminocarbonyl group, a hydroxyl group, an amino group, shea Anomoto Or a substituted phenyl having at least one substituent selected from a nitro group on a ring (C Factory c 6 ) an alkyl group, a phenyl group, which may be the same or different, a hydrogen atom, a halogeno Atom, (c factory c 6 ) alkyl group, (c 2 -c 6 ) alkenyl group, (c 2 -c 6 ) alkynyl group, cycle (c 3 -c 6 ) alkyl group, halo (-c 6 ) Alkyl group, cycloha (c 3 -c 6 ) alkyl group,
(CrC6)アルコキシ基、 ハロ( - )アルコキシ基、 (C厂 C6)アルキルチオ基、 ハロ (C厂 C6)アルキルチオ基、 (C厂 C6)アルキルスルフィニル基、 ハ口 (C厂 c6)アルキル スルフィニル基、 (CrC6)ァノレキノレスノレホニル基、 ノヽロ(C C(i)アルキルスノレホニ ル基、 ( - C6)アルキルカルボニル基、 ノヽロ(C厂 C6)アルキルカルボニル基、 (C厂 c6)アルコキシカルポニル基、 カルボキシル基、 モノ (C厂 c6) アルキルアミノカ ルポニル基、 ジ (d- c6) アルキルアミノカルボニル基、 水酸基、 アミノ基、 シ ァノ基又はニトロ基から選択される 1 〜 5個の置換基を有する置換フエニル基、 ピリジル基、 同一又は異なっても良く、 ハロゲン原子、 (c「 c6)アルキル基、 ノ、 口(C厂 C6)アルキル基、 (C厂 C6)アルコキシ基又はハロ(C厂 c6)アルコキシ基から選 択される 1以上の置換基を有する置換ピリジル基、 ピリミジル基又は同一若しく は異なっても良く、 ハロゲン原子、 (C厂 C6)アルキル基、 ハロ(C厂 c6)アルキル基、 (C「 C6)アルコキシ基又はハロ( - C6)アルコキシ基から選択される 1以上の置換 基を有する置換ピリミジル基を示す。 ) を示し、 (C r C 6 ) alkoxy group, halo (-) alkoxy group, (CFactory C 6 ) alkylthio group, halo (CFactory C 6 ) alkylthio group, (CFactory C 6 ) alkylsulfinyl group, haguchi (CFactory c 6 ) alkylsulfinyl group, (C r C 6 ) anolequinolenolesulfonyl group, nodro (CC (i ) alkylsnolephonyl group, (-C 6 ) alkylcarbonyl group, nodro (CFactory C 6) alkylcarbonyl group, (C厂c 6) alkoxy Cal Poni group, a carboxyl group, a mono (C厂c 6) alkylamino mosquitoes Ruponiru group, di (d-c 6) alkylaminocarbonyl group, a hydroxyl group, an amino group, shea substituted phenyl group having 1 to 5 substituents selected from § amino group or a nitro group, a pyridyl group, the same or different and a halogen atom, (c "c 6) alkyl group, Bruno, mouth (C Factory C 6 ) alkyl group, (C Factory C 6 ) alkoxy group or halo A substituted pyridyl group having one or more substituents selected from an (C factory c 6 ) alkoxy group, a pyrimidyl group or the same or different, a halogen atom, a (C factory C 6 ) alkyl group, a halo ( C厂c 6) alkyl group, (C "C 6) alkoxy or halo (- indicates C 6) a substituted pyrimidyl group having 1 or more substituents selected from alkoxy groups).
Aが (C厂 C6) アルキレン基又は同一若しくは異なっても良く、 ハロゲン原子、 水酸基、 (Cf C6)アルコキシ基、 (C厂 c6)アルコキシカルボニル基又はシァノ基か ら選択される 1以上の置換基を有する ( - c6) アルキレン基を示し、 A is one or more selected from a halogen atom, a hydroxyl group, a (Cf C 6 ) alkoxy group, a (C factory c 6 ) alkoxycarbonyl group or a cyano group, wherein A may be the same or different from an (C factory C 6 ) alkylene group; having substituents (- c 6) an alkylene group,
Gが酸素原子又は N— O R4 (式中、 R4は (C厂 C6) アルキル基を示す。 ) を示 し、 mが 0又は 1の整数を示し、 G represents an oxygen atom or N—OR 4 (wherein, R 4 represents a (C Factory C 6 ) alkyl group.), M represents an integer of 0 or 1,
Xが同一又は異なっても良く、 水素原子又は( - gアルキル基から選択され る 1 〜 2個の置換基を示す請求項 1記載のハロアルキルスルホンァニリ ド誘導体 又はその塩。 The haloalkylsulfonanilide derivative or a salt thereof according to claim 1, wherein X may be the same or different, and represents a hydrogen atom or one or two substituents selected from a -g alkyl group.
5. 請求項 1乃至 4いずれか 1項記載のハロアルキルスルホンァニリ ド誘導体 又はその塩類を有効成分として含有することを特徴とする除草剤。 5. A herbicide comprising the haloalkylsulfonanilide derivative according to any one of claims 1 to 4 or a salt thereof as an active ingredient.
6. 請求項 5記載の除草剤の有効量を土壌又は植物に処理することを特徴とす る除草剤の使用方法。
6. A method for using a herbicide, which comprises applying an effective amount of the herbicide according to claim 5 to soil or a plant.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2003252259A AU2003252259A1 (en) | 2002-07-26 | 2003-07-24 | Novel haloalkylsulfonanilide derivatives, herbicides and usage thereof |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002-218452 | 2002-07-26 | ||
| JP2002218452 | 2002-07-26 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2004011429A1 true WO2004011429A1 (en) | 2004-02-05 |
Family
ID=31184679
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2003/009405 WO2004011429A1 (en) | 2002-07-26 | 2003-07-24 | Novel haloalkylsulfonanilide derivatives, herbicides and usage thereof |
Country Status (3)
| Country | Link |
|---|---|
| AU (1) | AU2003252259A1 (en) |
| TW (1) | TW200404764A (en) |
| WO (1) | WO2004011429A1 (en) |
Cited By (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7312248B2 (en) * | 2004-09-23 | 2007-12-25 | Schering-Plough Animal Health Corporation | Control of parasites in animals by the use of novel trifluoromethanesulfonanilide oxime ether derivatives |
| WO2008059948A1 (en) * | 2006-11-17 | 2008-05-22 | Nihon Nohyaku Co., Ltd. | Haloalkylsulfonanilide derivative or salt thereof, herbicide comprising the derivative as active ingredient, and use of the herbicide |
| KR100890886B1 (en) * | 2005-02-24 | 2009-03-31 | 니혼노야쿠가부시키가이샤 | Novel haloalkylsulfonanilide derivative, herbicide, and method of use thereof |
| WO2010026989A1 (en) | 2008-09-02 | 2010-03-11 | 日産化学工業株式会社 | Ortho-substituted haloalkylsulfonanilide derivative and herbicide |
| JP2010509312A (en) * | 2006-11-10 | 2010-03-25 | アデックス ファーマ ソシエテ アノニム | Novel triazinedione derivatives as GABAB receptor modulators |
| WO2010119906A1 (en) * | 2009-04-14 | 2010-10-21 | 日産化学工業株式会社 | Haloalkylsulfonanilide derivative |
| WO2013039990A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040117A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040021A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2014151255A1 (en) | 2013-03-15 | 2014-09-25 | Monsanto Technology Llc | Methods and compositions for weed control |
| JP2015020950A (en) * | 2013-07-16 | 2015-02-02 | 日産化学工業株式会社 | Herbicide composition |
| WO2015097071A1 (en) | 2013-12-25 | 2015-07-02 | Syngenta Participations Ag | Herbicidal haloalkylsulphonamide derivatives |
| WO2015108982A2 (en) | 2014-01-15 | 2015-07-23 | Monsanto Technology Llc | Methods and compositions for weed control using epsps polynucleotides |
| US9121022B2 (en) | 2010-03-08 | 2015-09-01 | Monsanto Technology Llc | Method for controlling herbicide-resistant plants |
| US9416363B2 (en) | 2011-09-13 | 2016-08-16 | Monsanto Technology Llc | Methods and compositions for weed control |
| US9422558B2 (en) | 2011-09-13 | 2016-08-23 | Monsanto Technology Llc | Methods and compositions for weed control |
| US9422557B2 (en) | 2011-09-13 | 2016-08-23 | Monsanto Technology Llc | Methods and compositions for weed control |
| US9540642B2 (en) | 2013-11-04 | 2017-01-10 | The United States Of America, As Represented By The Secretary Of Agriculture | Compositions and methods for controlling arthropod parasite and pest infestations |
| US9777288B2 (en) | 2013-07-19 | 2017-10-03 | Monsanto Technology Llc | Compositions and methods for controlling leptinotarsa |
| US9850496B2 (en) | 2013-07-19 | 2017-12-26 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| WO2018135649A1 (en) | 2017-01-20 | 2018-07-26 | 北興化学工業株式会社 | Isoxazolin-5-one derivative and herbicide containing same as active ingredient |
| US10041068B2 (en) | 2013-01-01 | 2018-08-07 | A. B. Seeds Ltd. | Isolated dsRNA molecules and methods of using same for silencing target molecules of interest |
| US10240162B2 (en) | 2012-05-24 | 2019-03-26 | A.B. Seeds Ltd. | Compositions and methods for silencing gene expression |
| US10378012B2 (en) | 2014-07-29 | 2019-08-13 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| WO2020022350A1 (en) | 2018-07-24 | 2020-01-30 | 北興化学工業株式会社 | Isoxazolin-5-one derivative, and herbicide containing same as active ingredient |
| US10557138B2 (en) | 2013-12-10 | 2020-02-11 | Beeologics, Inc. | Compositions and methods for virus control in Varroa mite and bees |
| US10612019B2 (en) | 2013-03-13 | 2020-04-07 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10609930B2 (en) | 2013-03-13 | 2020-04-07 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10655136B2 (en) | 2015-06-03 | 2020-05-19 | Monsanto Technology Llc | Methods and compositions for introducing nucleic acids into plants |
| US10683505B2 (en) | 2013-01-01 | 2020-06-16 | Monsanto Technology Llc | Methods of introducing dsRNA to plant seeds for modulating gene expression |
| US10760086B2 (en) | 2011-09-13 | 2020-09-01 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10801028B2 (en) | 2009-10-14 | 2020-10-13 | Beeologics Inc. | Compositions for controlling Varroa mites in bees |
| US10806146B2 (en) | 2011-09-13 | 2020-10-20 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10808249B2 (en) | 2011-09-13 | 2020-10-20 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10829828B2 (en) | 2011-09-13 | 2020-11-10 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10883103B2 (en) | 2015-06-02 | 2021-01-05 | Monsanto Technology Llc | Compositions and methods for delivery of a polynucleotide into a plant |
| US10888579B2 (en) | 2007-11-07 | 2021-01-12 | Beeologics Inc. | Compositions for conferring tolerance to viral disease in social insects, and the use thereof |
| US10968449B2 (en) | 2015-01-22 | 2021-04-06 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US10988764B2 (en) | 2014-06-23 | 2021-04-27 | Monsanto Technology Llc | Compositions and methods for regulating gene expression via RNA interference |
| US11091770B2 (en) | 2014-04-01 | 2021-08-17 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| WO2023210623A1 (en) * | 2022-04-28 | 2023-11-02 | 株式会社エス・ディー・エス バイオテック | Haloalkyl sulfone anilide compound and herbicide containing same |
| US11807857B2 (en) | 2014-06-25 | 2023-11-07 | Monsanto Technology Llc | Methods and compositions for delivering nucleic acids to plant cells and regulating gene expression |
Citations (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1593809A (en) * | 1977-04-15 | 1981-07-22 | Ciba Geigy Ag | N-phenylsubstituted n-heterocyclic compounds their preparation and use in agents for regulating plant growth |
| JPS57130967A (en) * | 1981-02-05 | 1982-08-13 | Sumitomo Chem Co Ltd | Trifluoromethanesulfonanilide derivative, its preparation and herbicide containing said derivative as active component |
| JPS57209266A (en) * | 1981-06-16 | 1982-12-22 | Sumitomo Chem Co Ltd | Trimethanesulfanillide derivative, its preparation, and herbicide containing the same as active constituent |
| EP0253310A2 (en) * | 1986-07-11 | 1988-01-20 | E.I. Du Pont De Nemours And Company | Angiotensin II receptor blocking imidazoles |
| WO1988006580A1 (en) * | 1987-02-25 | 1988-09-07 | Schering Aktiengesellschaft | Aryl- and aryloxy-substituted tert.-alkylenamines, process for their manufacture and their use in pharmacy |
| EP0324377A2 (en) * | 1988-01-07 | 1989-07-19 | E.I. Du Pont De Nemours And Company | Angiotensin II receptor blocking imidazoles and combinations thereof with diuretics and NSaids |
| WO1992019594A1 (en) * | 1991-05-02 | 1992-11-12 | Smithkline Beecham Corporation | Pyrrolidinones |
| EP0516392A2 (en) * | 1991-05-31 | 1992-12-02 | Zeneca Limited | Naphthyridine derivatives as angiotensin II inhibitors |
| WO1993007128A1 (en) * | 1991-10-11 | 1993-04-15 | The Du Pont Merck Pharmaceutical Company | Cyclic ureas and analogues useful as retroviral protease inhibitiors |
| WO1993009099A2 (en) * | 1991-11-07 | 1993-05-13 | Agrevo Uk Limited | Sulfonamide herbicides |
| WO1993013077A1 (en) * | 1991-12-20 | 1993-07-08 | Warner-Lambert Company | Angiotensin ii receptor antagonists |
| WO1996002542A1 (en) * | 1994-07-15 | 1996-02-01 | Takeda Chemical Industries, Ltd. | Tricyclic compounds, their production and use |
| JPH08291146A (en) * | 1995-02-20 | 1996-11-05 | Sankyo Co Ltd | Herbicidal n-(substituted phenyl) sulfonamide compound |
| JPH107667A (en) * | 1996-03-22 | 1998-01-13 | Dsm Nv | Production of 1,5-benzothiazepine derivative |
| EP0822185A1 (en) * | 1996-07-31 | 1998-02-04 | Pfizer Inc. | B-3-adrenergic agonists as antidiabetic and antiobesity agents |
| JP2000247814A (en) * | 1999-03-02 | 2000-09-12 | Kumiai Chem Ind Co Ltd | Mixed herbicide composition |
| JP2000281513A (en) * | 1999-03-26 | 2000-10-10 | Kumiai Chem Ind Co Ltd | Mixed herbicidal composition |
| WO2002000656A2 (en) * | 2000-06-23 | 2002-01-03 | Lilly Icos Llc | Pirazino '1$m(1)2$m(1) :1, 6! pyrido '3,4-b! indole derivatives |
| WO2002026228A1 (en) * | 2000-09-27 | 2002-04-04 | Bristol-Myers Squibb Company | Benzimidazolone antiviral agents |
| WO2002088094A1 (en) * | 2001-04-19 | 2002-11-07 | Eisai Co., Ltd. | 2-iminoimidazole derivatives (1) |
-
2003
- 2003-07-24 AU AU2003252259A patent/AU2003252259A1/en not_active Abandoned
- 2003-07-24 WO PCT/JP2003/009405 patent/WO2004011429A1/en active Application Filing
- 2003-07-25 TW TW92120316A patent/TW200404764A/en unknown
Patent Citations (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1593809A (en) * | 1977-04-15 | 1981-07-22 | Ciba Geigy Ag | N-phenylsubstituted n-heterocyclic compounds their preparation and use in agents for regulating plant growth |
| JPS57130967A (en) * | 1981-02-05 | 1982-08-13 | Sumitomo Chem Co Ltd | Trifluoromethanesulfonanilide derivative, its preparation and herbicide containing said derivative as active component |
| JPS57209266A (en) * | 1981-06-16 | 1982-12-22 | Sumitomo Chem Co Ltd | Trimethanesulfanillide derivative, its preparation, and herbicide containing the same as active constituent |
| EP0253310A2 (en) * | 1986-07-11 | 1988-01-20 | E.I. Du Pont De Nemours And Company | Angiotensin II receptor blocking imidazoles |
| WO1988006580A1 (en) * | 1987-02-25 | 1988-09-07 | Schering Aktiengesellschaft | Aryl- and aryloxy-substituted tert.-alkylenamines, process for their manufacture and their use in pharmacy |
| EP0324377A2 (en) * | 1988-01-07 | 1989-07-19 | E.I. Du Pont De Nemours And Company | Angiotensin II receptor blocking imidazoles and combinations thereof with diuretics and NSaids |
| WO1992019594A1 (en) * | 1991-05-02 | 1992-11-12 | Smithkline Beecham Corporation | Pyrrolidinones |
| EP0516392A2 (en) * | 1991-05-31 | 1992-12-02 | Zeneca Limited | Naphthyridine derivatives as angiotensin II inhibitors |
| WO1993007128A1 (en) * | 1991-10-11 | 1993-04-15 | The Du Pont Merck Pharmaceutical Company | Cyclic ureas and analogues useful as retroviral protease inhibitiors |
| WO1993009099A2 (en) * | 1991-11-07 | 1993-05-13 | Agrevo Uk Limited | Sulfonamide herbicides |
| WO1993013077A1 (en) * | 1991-12-20 | 1993-07-08 | Warner-Lambert Company | Angiotensin ii receptor antagonists |
| WO1996002542A1 (en) * | 1994-07-15 | 1996-02-01 | Takeda Chemical Industries, Ltd. | Tricyclic compounds, their production and use |
| JPH08291146A (en) * | 1995-02-20 | 1996-11-05 | Sankyo Co Ltd | Herbicidal n-(substituted phenyl) sulfonamide compound |
| JPH107667A (en) * | 1996-03-22 | 1998-01-13 | Dsm Nv | Production of 1,5-benzothiazepine derivative |
| EP0822185A1 (en) * | 1996-07-31 | 1998-02-04 | Pfizer Inc. | B-3-adrenergic agonists as antidiabetic and antiobesity agents |
| JP2000247814A (en) * | 1999-03-02 | 2000-09-12 | Kumiai Chem Ind Co Ltd | Mixed herbicide composition |
| JP2000281513A (en) * | 1999-03-26 | 2000-10-10 | Kumiai Chem Ind Co Ltd | Mixed herbicidal composition |
| WO2002000656A2 (en) * | 2000-06-23 | 2002-01-03 | Lilly Icos Llc | Pirazino '1$m(1)2$m(1) :1, 6! pyrido '3,4-b! indole derivatives |
| WO2002026228A1 (en) * | 2000-09-27 | 2002-04-04 | Bristol-Myers Squibb Company | Benzimidazolone antiviral agents |
| WO2002088094A1 (en) * | 2001-04-19 | 2002-11-07 | Eisai Co., Ltd. | 2-iminoimidazole derivatives (1) |
Non-Patent Citations (4)
| Title |
|---|
| BULL. CHEM. SOC. JAPAN, vol. 66, no. 2, 1993, pages 432 - 436, XP002973336 * |
| EDMUNDS J.J. ET AL, J. MED. CHEM., vol. 38, no. 19, 1995, pages 3759 - 3771, XP002973334 * |
| PARTHASARATHY P.C. ET AL, EUR. J. MED. CHEM., vol. 28, no. 3, 1993, pages 195 - 199, XP002973335 * |
| RANDALL LIS ET AL, J. MED. CHEM., vol. 30, no. 4, 1987, pages 696 - 704, XP002036882 * |
Cited By (68)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7312248B2 (en) * | 2004-09-23 | 2007-12-25 | Schering-Plough Animal Health Corporation | Control of parasites in animals by the use of novel trifluoromethanesulfonanilide oxime ether derivatives |
| US7906538B2 (en) * | 2004-09-23 | 2011-03-15 | Schering-Plough Animal Health Corporation | Control of parasites in animals by the use of novel trifluoromethanesulfonanilide oxime ether derivatives |
| KR100890886B1 (en) * | 2005-02-24 | 2009-03-31 | 니혼노야쿠가부시키가이샤 | Novel haloalkylsulfonanilide derivative, herbicide, and method of use thereof |
| JP2010509312A (en) * | 2006-11-10 | 2010-03-25 | アデックス ファーマ ソシエテ アノニム | Novel triazinedione derivatives as GABAB receptor modulators |
| US8048825B2 (en) | 2006-11-17 | 2011-11-01 | Nihon Nohyaku Co., Ltd. | Haloalkylsulfonanilide derivatives or salt thereof, herbicide comprising the derivatives as active ingredient, and use of the herbicide |
| WO2008059948A1 (en) * | 2006-11-17 | 2008-05-22 | Nihon Nohyaku Co., Ltd. | Haloalkylsulfonanilide derivative or salt thereof, herbicide comprising the derivative as active ingredient, and use of the herbicide |
| JP2008143895A (en) * | 2006-11-17 | 2008-06-26 | Nippon Nohyaku Co Ltd | Haloalkylsulfonanilide derivative or salt thereof, herbicide comprising the same as effective ingredient, and use of the herbicide |
| CN101535283B (en) * | 2006-11-17 | 2011-08-17 | 日本农药株式会社 | Haloalkylsulfonanilide derivative or salt thereof, herbicide comprising the derivative as active ingredient, and use of the herbicide |
| US10888579B2 (en) | 2007-11-07 | 2021-01-12 | Beeologics Inc. | Compositions for conferring tolerance to viral disease in social insects, and the use thereof |
| JP5549592B2 (en) * | 2008-09-02 | 2014-07-16 | 日産化学工業株式会社 | Ortho-substituted haloalkylsulfonanilide derivatives and herbicides |
| KR20110056378A (en) | 2008-09-02 | 2011-05-27 | 닛산 가가쿠 고교 가부시키 가이샤 | Ortho-substituted haloalkylsulfonanilide derivative and herbicide |
| WO2010026989A1 (en) | 2008-09-02 | 2010-03-11 | 日産化学工業株式会社 | Ortho-substituted haloalkylsulfonanilide derivative and herbicide |
| EP2420493A1 (en) * | 2009-04-14 | 2012-02-22 | Nissan Chemical Industries, Ltd. | Haloalkylsulfonanilide derivative |
| EP2420493A4 (en) * | 2009-04-14 | 2012-09-05 | Nissan Chemical Ind Ltd | Haloalkylsulfonanilide derivative |
| WO2010119906A1 (en) * | 2009-04-14 | 2010-10-21 | 日産化学工業株式会社 | Haloalkylsulfonanilide derivative |
| JP5741429B2 (en) * | 2009-04-14 | 2015-07-01 | 日産化学工業株式会社 | Haloalkylsulfonanilide derivatives |
| US10801028B2 (en) | 2009-10-14 | 2020-10-13 | Beeologics Inc. | Compositions for controlling Varroa mites in bees |
| US9988634B2 (en) | 2010-03-08 | 2018-06-05 | Monsanto Technology Llc | Polynucleotide molecules for gene regulation in plants |
| US11812738B2 (en) | 2010-03-08 | 2023-11-14 | Monsanto Technology Llc | Polynucleotide molecules for gene regulation in plants |
| US9121022B2 (en) | 2010-03-08 | 2015-09-01 | Monsanto Technology Llc | Method for controlling herbicide-resistant plants |
| US10806146B2 (en) | 2011-09-13 | 2020-10-20 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10760086B2 (en) | 2011-09-13 | 2020-09-01 | Monsanto Technology Llc | Methods and compositions for weed control |
| EP3434779A1 (en) | 2011-09-13 | 2019-01-30 | Monsanto Technology LLC | Methods and compositions for weed control |
| US9416363B2 (en) | 2011-09-13 | 2016-08-16 | Monsanto Technology Llc | Methods and compositions for weed control |
| US9422558B2 (en) | 2011-09-13 | 2016-08-23 | Monsanto Technology Llc | Methods and compositions for weed control |
| US9422557B2 (en) | 2011-09-13 | 2016-08-23 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10808249B2 (en) | 2011-09-13 | 2020-10-20 | Monsanto Technology Llc | Methods and compositions for weed control |
| EP3434780A1 (en) | 2011-09-13 | 2019-01-30 | Monsanto Technology LLC | Methods and compositions for weed control |
| WO2013040021A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10829828B2 (en) | 2011-09-13 | 2020-11-10 | Monsanto Technology Llc | Methods and compositions for weed control |
| EP3296402A2 (en) | 2011-09-13 | 2018-03-21 | Monsanto Technology LLC | Methods and compositions for weed control |
| WO2013040117A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| EP3382027A2 (en) | 2011-09-13 | 2018-10-03 | Monsanto Technology LLC | Methods and compositions for weed control |
| WO2013039990A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10240161B2 (en) | 2012-05-24 | 2019-03-26 | A.B. Seeds Ltd. | Compositions and methods for silencing gene expression |
| US10240162B2 (en) | 2012-05-24 | 2019-03-26 | A.B. Seeds Ltd. | Compositions and methods for silencing gene expression |
| US10934555B2 (en) | 2012-05-24 | 2021-03-02 | Monsanto Technology Llc | Compositions and methods for silencing gene expression |
| US10041068B2 (en) | 2013-01-01 | 2018-08-07 | A. B. Seeds Ltd. | Isolated dsRNA molecules and methods of using same for silencing target molecules of interest |
| US10683505B2 (en) | 2013-01-01 | 2020-06-16 | Monsanto Technology Llc | Methods of introducing dsRNA to plant seeds for modulating gene expression |
| US10609930B2 (en) | 2013-03-13 | 2020-04-07 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10612019B2 (en) | 2013-03-13 | 2020-04-07 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10568328B2 (en) | 2013-03-15 | 2020-02-25 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2014151255A1 (en) | 2013-03-15 | 2014-09-25 | Monsanto Technology Llc | Methods and compositions for weed control |
| JP2015020950A (en) * | 2013-07-16 | 2015-02-02 | 日産化学工業株式会社 | Herbicide composition |
| US9777288B2 (en) | 2013-07-19 | 2017-10-03 | Monsanto Technology Llc | Compositions and methods for controlling leptinotarsa |
| US11377667B2 (en) | 2013-07-19 | 2022-07-05 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US10597676B2 (en) | 2013-07-19 | 2020-03-24 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US9856495B2 (en) | 2013-07-19 | 2018-01-02 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US9850496B2 (en) | 2013-07-19 | 2017-12-26 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US10927374B2 (en) | 2013-11-04 | 2021-02-23 | Monsanto Technology Llc | Compositions and methods for controlling arthropod parasite and pest infestations |
| US10100306B2 (en) | 2013-11-04 | 2018-10-16 | Monsanto Technology Llc | Compositions and methods for controlling arthropod parasite and pest infestations |
| US9540642B2 (en) | 2013-11-04 | 2017-01-10 | The United States Of America, As Represented By The Secretary Of Agriculture | Compositions and methods for controlling arthropod parasite and pest infestations |
| US10557138B2 (en) | 2013-12-10 | 2020-02-11 | Beeologics, Inc. | Compositions and methods for virus control in Varroa mite and bees |
| WO2015097071A1 (en) | 2013-12-25 | 2015-07-02 | Syngenta Participations Ag | Herbicidal haloalkylsulphonamide derivatives |
| WO2015108982A2 (en) | 2014-01-15 | 2015-07-23 | Monsanto Technology Llc | Methods and compositions for weed control using epsps polynucleotides |
| US10334848B2 (en) | 2014-01-15 | 2019-07-02 | Monsanto Technology Llc | Methods and compositions for weed control using EPSPS polynucleotides |
| US11091770B2 (en) | 2014-04-01 | 2021-08-17 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| US10988764B2 (en) | 2014-06-23 | 2021-04-27 | Monsanto Technology Llc | Compositions and methods for regulating gene expression via RNA interference |
| US11807857B2 (en) | 2014-06-25 | 2023-11-07 | Monsanto Technology Llc | Methods and compositions for delivering nucleic acids to plant cells and regulating gene expression |
| US10378012B2 (en) | 2014-07-29 | 2019-08-13 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| US11124792B2 (en) | 2014-07-29 | 2021-09-21 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| US10968449B2 (en) | 2015-01-22 | 2021-04-06 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US10883103B2 (en) | 2015-06-02 | 2021-01-05 | Monsanto Technology Llc | Compositions and methods for delivery of a polynucleotide into a plant |
| US10655136B2 (en) | 2015-06-03 | 2020-05-19 | Monsanto Technology Llc | Methods and compositions for introducing nucleic acids into plants |
| US11109593B2 (en) | 2017-01-20 | 2021-09-07 | Hokko Chemical Industry Co., Ltd. | Isoxazolin-5-one derivative and herbicide containing same as active ingredient |
| WO2018135649A1 (en) | 2017-01-20 | 2018-07-26 | 北興化学工業株式会社 | Isoxazolin-5-one derivative and herbicide containing same as active ingredient |
| WO2020022350A1 (en) | 2018-07-24 | 2020-01-30 | 北興化学工業株式会社 | Isoxazolin-5-one derivative, and herbicide containing same as active ingredient |
| WO2023210623A1 (en) * | 2022-04-28 | 2023-11-02 | 株式会社エス・ディー・エス バイオテック | Haloalkyl sulfone anilide compound and herbicide containing same |
Also Published As
| Publication number | Publication date |
|---|---|
| TW200404764A (en) | 2004-04-01 |
| AU2003252259A1 (en) | 2004-02-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2004011429A1 (en) | Novel haloalkylsulfonanilide derivatives, herbicides and usage thereof | |
| US20080274892A1 (en) | Novel Haloalkylsulfonanilide Derivative, Herbicide, and Method of Use Thereof | |
| KR100203826B1 (en) | Urasil derivatives | |
| US9556183B2 (en) | Substituted pyrazolylpyrazole derivative and use of same as herbicide | |
| CA2029027A1 (en) | Pyrimidine derivatives, their production and use | |
| US6048823A (en) | Pyridone derivatives and herbicides | |
| EP0747352A1 (en) | Cyclic nitrogenous compound and herbicide | |
| CS207657B2 (en) | Herbicide means and method of making the active substances | |
| SK7502000A3 (en) | Herbicides 3-(benzazol-4-yl)pyrimidine-dione-derivatives | |
| US5545608A (en) | Pyrazole-glycolic acid amide derivatives as herbicides | |
| JP2001302666A (en) | Azole-condensed heterocyclic anilide compound and herbicide | |
| CZ80795A3 (en) | Agent for fighting diseases of plants | |
| BG98647A (en) | Derivatives of sulphamoyltriasol and fungicides containing them as active components | |
| SK34398A3 (en) | Pyrazin-2-one derivative, method for inhibiting undesirable weeds and use of derivatives | |
| JPH11292849A (en) | Benzoylpyrazole compound and herbicide | |
| JP2004107323A (en) | New haloalkylsulfone anilide derivative, herbicide and use thereof | |
| WO1995012582A1 (en) | Novel 4,5-disubstituted pyrimidine derivative and herbicide | |
| JPH0820571A (en) | Semicarbazone derivative | |
| WO2001068613A1 (en) | Pyrimidinone derivatives and herbicides | |
| JP2002520384A (en) | Aryl vinyl ether derivatives and their use as herbicides | |
| US4790869A (en) | Sulfonamide compounds and salts thereof, herbicidal compositions containing them | |
| JPH0931069A (en) | Thiazolecarboxylic acid derivative and plant disease injury controller | |
| US6239076B1 (en) | Herbicidal 2-(5-isoxazolinyl methyloxyphenyl)-4,5,6,7-tetrahydro -2H-indazole derivatives | |
| JP2003321455A (en) | o-SUBSTITUTED BENZOYL COMPOUND AND HERBICIDE CONTAINING THE SAME AS ACTIVE INGREDIENT | |
| CA2381639A1 (en) | Substituted benzoxazoles |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): AE AG AL AM AT AU AZ BA BB BG BR BY BZ CA CH CN CO CR CU CZ DE DK DM DZ EC EE ES FI GB GD GE GH GM HR HU ID IL IN IS KE KG KR KZ LC LK LR LS LT LU LV MA MD MG MK MN MW MX MZ NI NO NZ OM PG PH PL PT RO RU SC SD SE SG SK SL SY TJ TM TN TR TT TZ UA UG US UZ VC VN YU ZA ZM ZW |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): GH GM KE LS MW MZ SD SL SZ TZ UG ZM ZW AM AZ BY KG KZ MD RU TJ TM AT BE BG CH CY CZ DE DK EE ES FI FR GB GR HU IE IT LU MC NL PT RO SE SI SK TR BF BJ CF CG CI CM GA GN GQ GW ML MR NE SN TD TG |
|
| DFPE | Request for preliminary examination filed prior to expiration of 19th month from priority date (pct application filed before 20040101) | ||
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| 122 | Ep: pct application non-entry in european phase |