KR20170029513A - 후안부 질환의 예방 또는 치료제 - Google Patents
후안부 질환의 예방 또는 치료제 Download PDFInfo
- Publication number
- KR20170029513A KR20170029513A KR1020177001365A KR20177001365A KR20170029513A KR 20170029513 A KR20170029513 A KR 20170029513A KR 1020177001365 A KR1020177001365 A KR 1020177001365A KR 20177001365 A KR20177001365 A KR 20177001365A KR 20170029513 A KR20170029513 A KR 20170029513A
- Authority
- KR
- South Korea
- Prior art keywords
- alkyl group
- lower alkyl
- formula
- hydrogen atom
- posterior segment
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/517—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with carbocyclic ring systems, e.g. quinazoline, perimidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/53—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with three nitrogens as the only ring hetero atoms, e.g. chlorazanil, melamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/0004—Screening or testing of compounds for diagnosis of disorders, assessment of conditions, e.g. renal clearance, gastric emptying, testing for diabetes, allergy, rheuma, pancreas functions
- A61K49/0008—Screening agents using (non-human) animal models or transgenic animal models or chimeric hosts, e.g. Alzheimer disease animal model, transgenic model for heart failure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
- A61K9/0051—Ocular inserts, ocular implants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/06—Ointments; Bases therefor; Other semi-solid forms, e.g. creams, sticks, gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/06—Antiglaucoma agents or miotics
-
- Y10S514/912—
Abstract
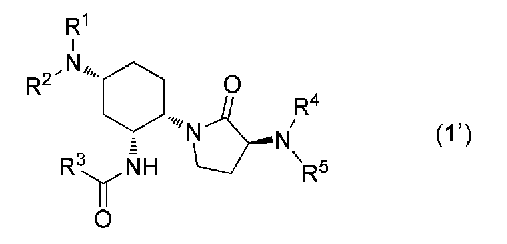
본 발명은, 하기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염(이하, 「본 화합물」이라고도 함)을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제에 관한 것이다.
Description
본 발명은 3-아미노-2-옥소피롤리딘 유도체, 특히, 하기 식 (1):
로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염(이하, 「본 화합물」이라고도 함)을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제에 관한 것이다.
후안부 질환이란, 일반적으로 유리체, 망막, 맥락막, 강막 또는 시신경에 있어서의 질환을 말하고, 이들 질환은, 신생혈관 발현과 깊이 관련되어 있다. 즉, 가령(加齡) 황반변성, 당뇨병 망막증, 당뇨병 황반부종, 망막정맥 폐색증, 포도막염 등의 후안부 질환에 있어서는 신생혈관 발현의 항진이 병태 형성 및 병태 진행의 주된 요인이며, 혈관신생을 저해하는 것이 이들 질환의 치료에 유용하다는 것이 알려져 있다(비특허문헌 1, 비특허문헌 2).
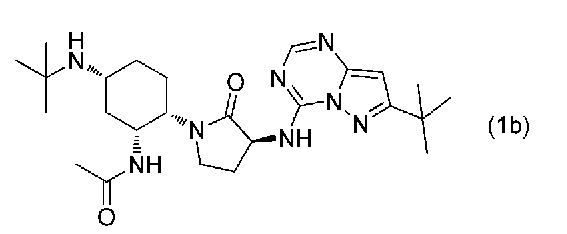
한편, 하기 식 (1b):
로 표시되는 화합물이 CCR-2 및 CCR-5 수용체 저해 활성을 갖는 것이 기재되어 있고, 상기 화합물이 염증성 질환, 알레르기성 질환, 자가면역 질환, 암 및/또는 순환기 질환의 치료에 유용하다는 것이 개시되어 있다(특허문헌 1).
그러나, 3-아미노-2-옥소피롤리딘 유도체, 특히, 하기 식 (1):
로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염(본 화합물)의 후안부 질환에 대한 예방 또는 치료 효과에 대해서 검토한 보고는 없다.
니치간카이시, 103, 923-947 (1999)
신즈세츠린쇼간카코자 제5권 「망막 유리체 질환」, p. 184-189, 232-237 (2000)
본 발명의 과제는, 3-아미노-2-옥소피롤리딘 유도체를 유효 성분으로서 함유하는 후안부 질환의 예방 또는 치료제를 제공하는 것이다.
본 발명자들은, 3-아미노-2-옥소피롤리딘 유도체를 유효 성분으로서 함유하는 후안부 질환의 예방 또는 치료제를 탐색하도록 예의 연구를 행한바, 하기 식 (1):
로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염이, 망막이나 맥락막과 같은 후안부 조직에 있어서 우수한 혈관신생 저해 작용 및 혈관 투과성 항진 억제 작용을 갖는 것을 발견하고, 본 화합물이 후안부 질환에 대하여 우수한 예방 또는 치료 효과를 갖는 것을 발견하여, 본 발명에 이르렀다.
즉, 본 발명은 이하에 관한 것이다.
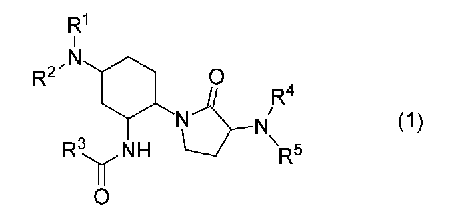
본 발명은, 하기 식 (1):
[식 (1) 중,
R1 및 R2는 동일하거나 또는 상이하고, 수소 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타내며;
R3은 수소 원자, 할로겐 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타내고;
R4는 수소 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타내며;
R5는 비치환 또는 R6으로 치환되어 있는 함질소 이환식 방향환기를 나타내고;
R6은 할로겐 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타낸다]
로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제이다.
또한, 본 발명의 다른 양태는,
상기 식 (1) 중,
R1 및 R2가 동일하거나 또는 상이하고, 수소 원자 또는 저급 알킬기를 나타내며;
R3이 수소 원자 또는 저급 알킬기를 나타내고;
R4가 수소 원자 또는 저급 알킬기를 나타내며;
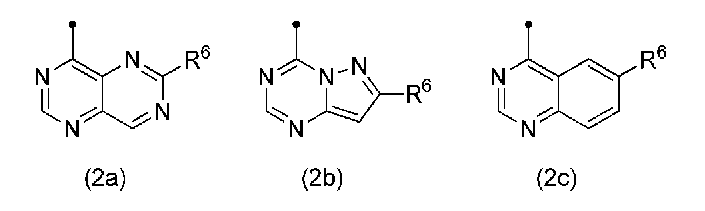
R5가 하기 식 (2a), (2b) 또는 (2c):
R6이 저급 알킬기 또는 할로겐으로 치환된 저급 알킬기를 나타내는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제이다. 여기서, 식 (2a), (2b) 또는 (2c) 중의 ·은, R5가 결합하는 질소 원자와의 결합점을 나타낸다.
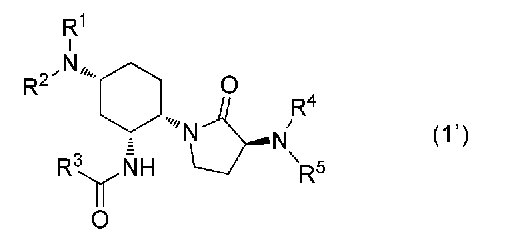
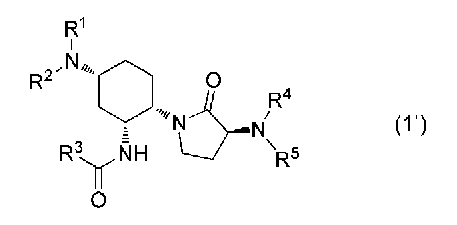
또한, 본 발명의 다른 양태는, 상기 식 (1)로 표시되는 화합물이 하기 식 (1'):
로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제이다.
또한, 본 발명의 다른 양태는,
상기 식 (1) 또는 식 (1') 중,
R1이 수소 원자를 나타내고;
R2가 tert-부틸을 나타내며;
R3이 메틸을 나타내고;
R4가 수소 원자를 나타내며;
R5가 하기 식 (2b):
R6이 tert-부틸을 나타내는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제이다. 여기서, 식 (2b) 중의 ·은, R5가 결합하는 질소 원자와의 결합점을 나타낸다.
또한, 본 발명의 다른 양태는, 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제로서, 후안부 질환이 유리체, 망막, 맥락막, 강막 또는 시신경에 있어서의 질환인, 예방 또는 치료제이다.
또한, 본 발명의 다른 양태는, 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제로서, 후안부 질환이 가령 황반변성, 당뇨병 망막증, 당뇨병 황반부종, 망막색소 변성증, 증식성 유리체 망막증, 망막동맥 폐색증, 망막정맥 폐색증, 포도막염, 레베르병, 미숙아 망막증, 망막박리, 망막색소 상피 박리, 중심성 장액성 맥락망막증, 중심성 삼출성 맥락망막증, 폴립형 맥락막 혈관증, 다발성 맥락막염, 신생혈관 황반증, 망막동맥류, 망막혈관 종상증식, 이들 질환에 기인하는 시신경장애, 녹내장에 기인하는 시신경장애 및 허혈성 시신경장애로 이루어진 군으로부터 선택되는 적어도 1종인, 예방 또는 치료제이다.
또한, 본 발명의 다른 양태는, 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제로서, 후안부 질환이 가령 황반변성, 당뇨병 망막증, 당뇨병 황반부종, 망막정맥 폐색증 및 포도막염으로 이루어진 군으로부터 선택되는 적어도 1종인, 예방 또는 치료제이다.
또한, 본 발명의 다른 양태는, 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는 맥락막 혈관신생 저해제이다.
또한, 본 발명의 다른 양태는, 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제로서, 투여 형태가 점안 투여, 유리체내 투여, 결막하 투여, 결막낭내 투여, 테논낭하 투여 또는 경구 투여인, 예방 또는 치료제, 또는 저해제이다.
또한, 본 발명의 다른 양태는, 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제로서, 제형이 점안제, 안연고, 삽입제, 첩포제, 주사제, 정제, 세립제 또는 캡슐제인, 예방 또는 치료제, 또는 저해제이다.
또한, 본 발명은 이하에 관한 것이기도 하다.
본 발명의 다른 양태는, 후안부 질환의 예방 또는 치료에 있어서의 용도를 위한 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염이다.
본 발명의 다른 양태는, 후안부 질환의 예방 또는 치료용 의약의 제조를 위한 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염의 용도이다.
본 발명의 다른 양태는, 치료 유효량의 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염 및 첨가제를 포함하는 후안부 질환의 예방 또는 치료를 위한 의약 조성물이다.
본 발명의 다른 양태는, 후안부 질환의 예방 또는 치료를 위한 방법으로서, 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염의 유효량을 투여하는 것을 포함하는 방법이다.
본 발명에 따르면, 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는 후안부 질환의 예방 또는 치료제를 제공할 수 있다.
이하에 본 발명에 대해서 상세히 설명한다.
「할로겐 원자」란 불소 원자, 염소 원자, 브롬 원자 또는 요오드 원자를 나타낸다.
「저급 알킬기」란 탄소 원자수가 1∼8개인 직쇄 또는 분지쇄의 알킬기를 나타내고, 탄소 원자수가 1∼6개인 직쇄 또는 분지쇄의 알킬기가 바람직하다. 구체예로서, 메틸, 에틸, n-프로필, n-부틸, n-펜틸, n-헥실, n-헵틸, n-옥틸, 이소프로필, 이소부틸, sec-부틸, tert-부틸, 이소펜틸 등을 들 수 있다.
「할로겐 원자로 치환된 저급 알킬기」란 1개 또는 복수개(예컨대, 2개 또는 3개)의 할로겐 원자로 치환된 저급 알킬기를 나타내고, 3개의 할로겐 원자로 치환된 저급 알킬기가 바람직하다. 구체예로서, 트리플루오로메틸 등을 들 수 있다. 또한, 할로겐 원자가 복수개 존재하는 경우, 이들 할로겐 원자는 동일하거나 또는 상이하여도 좋다.
「함질소 이환식 방향환기」란 고리 원자 중 적어도 1개는 질소 원자인 이환식의 방향환을 나타내고, 예컨대, 고리 원자가 8개, 9개 또는 10개이며, 또한 고리 원자로서 질소 원자가 1개, 2개, 3개 또는 4개 포함되는 방향환이 바람직하다. 구체예로서, 퀴놀리닐, 이소퀴놀리닐, 신놀리닐, 피라졸로[1,5-a]피리딜, 이미다조[1,2-a]피리딜, 퀴녹살리닐, 퀴나졸린, 벤조트리아졸릴, 인돌릴, 인다졸릴, 피라졸로[1,5-a][1,3,5]트리아진, 피리미도[5,4-d]피리미딘 등을 들 수 있다.
본 발명의 후안부 질환의 예방 또는 치료제에 포함되는 화합물은, 유기 합성 화학 분야에 있어서의 통상의 방법에 따라 제조할 수 있다. 예컨대, 국제 공개 2011/046916호 팜플렛 등에 기재된 방법에 따라 제조할 수 있다. 또한, 상기 화합물의 기하 이성체(시스-트랜스 이성체), 광학 이성체(에난티오머, 디아스테레오머) 또는 호변 이성체는 칼럼 크로마토그래피, HPLC 등의 통상의 방법에 따라 단리, 정제할 수도 있다.
본 발명의 후안부 질환의 예방 또는 치료제에 포함되는 화합물은, 하기 식 (1):
로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염이다.
상기 식 (1)로 표시되는 화합물에 기하 이성체(시스-트랜스 이성체), 광학 이성체(에난티오머, 디아스테레오머) 또는 호변 이성체가 존재하는 경우에는, 이들도 상기 식 (1)로 표시되는 화합물의 범위에 포함된다. 또한, 상기 식 (1)로 표시되는 화합물은, 그 기하 이성체(시스-트랜스 이성체), 광학 이성체(에난티오머, 디아스테레오머) 및 호변 이성체의 군으로부터 선택되는 1 또는 2 이상의 이성체의 혼합물이어도 좋다.
상기 식 (1) 중, R1 및 R2는 동일하거나 또는 상이하고, 수소 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타낸다.
상기 식 (1) 중, R3은 수소 원자, 할로겐 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타낸다.
상기 식 (1) 중, R4는 수소 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타낸다.
상기 식 (1) 중, R5는 비치환 또는 R6으로 치환되어 있는 함질소 이환식 방향환기를 나타낸다.
상기 식 (1) 중, R6은 할로겐 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타낸다.
각 치환기의 바람직한 예를 이하에 나타낸다.
상기 식 (1) 중, R1 및 R2는 바람직하게는 동일하거나 또는 상이하고, 수소 원자 또는 저급 알킬기이며, 보다 바람직하게는, R1이 수소 원자, R2가 저급 알킬기이고, 특히 바람직하게는, R1이 수소 원자, R2가 tert-부틸이다.
상기 식 (1) 중, R3은 바람직하게는 저급 알킬기이고, 특히 바람직하게는 메틸이다.
상기 식 (1) 중, R4는 바람직하게는 수소 원자이다.
상기 식(1) 중, R5는 바람직하게는 하기 식 (2a), (2b) 또는 (2c):
특히 바람직하게는, 하기 식 (2b):
여기서, 식 (2a), (2b) 또는 (2c) 중의 ·은, R5가 결합하는 질소 원자와의 결합점을 나타낸다.
R6은, 바람직하게는 저급 알킬기 또는 할로겐 원자로 치환된 저급 알킬기이고, 보다 바람직하게는, tert-부틸 또는 트리플루오로메틸이며, 가장 바람직하게는 tert-부틸이다.
상기 식 (1)은, 바람직하게는 하기 식 (1'):
상기 식 (1) 또는 식 (1')로 표시되는 화합물의 구체예로는, 하기 식 (1a):
로 표시되는 N-((1R,2S,5R)-2-((S)-3-((6-(tert-부틸)피리미도[5,4-d]피리미딘-4-일)아미노)-2-옥소피롤리딘-1-일)-5-(tert-부틸아미노)사이클로헥실)아세트아미드(이하, 「화합물 1a」라고도 함), 이의 에난티오머 및 디아스테레오머, 그리고 이들의 혼합물(예컨대, 라세미 혼합물, 다이아스테레오 혼합물 등)을 들 수 있다.
상기 식 (1) 또는 식 (1')로 표시되는 화합물의 구체예로는, 하기 식 (1b):
로 표시되는 N-((1R,2S,5R)-5-(tert-부틸아미노)-2-((S)-3-(7-tert-부틸피라졸로[1,5-a][1,3,5]트리아진-4-일아미노)-2-옥소피롤리딘-1-일)사이클로헥실)아세트아미드(이하, 「화합물 1b」라고도 함), 이의 에난티오머 및 디아스테레오머, 그리고 이들의 혼합물(예컨대, 라세미 혼합물, 다이아스테레오 혼합물 등)을 들 수 있다.
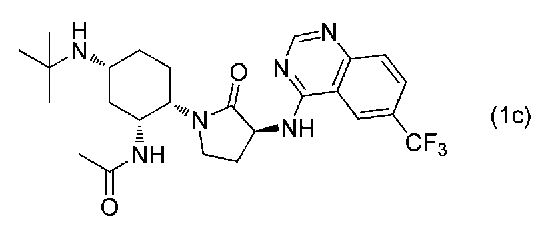
상기 식 (1) 또는 식 (1')로 표시되는 화합물의 구체예로는, 하기 식 (1c):
로 표시되는 N-((1R,2S,5R)-5-(tert-부틸아미노)-2-((S)-2-옥소-3-((6-(트리플루오로메틸)퀴나졸린-4-일)아미노)피롤리딘-1-일)사이클로헥실)아세트아미드(이하, 「화합물 1c」라고도 함), 이의 에난티오머 및 디아스테레오머, 그리고 이들의 혼합물(예컨대, 라세미 혼합물, 다이아스테레오 혼합물 등)을 들 수 있다.
상기 식 (1), (1'), (1a), (1b) 또는 (1c)로 표시되는 화합물의 「약학적으로 허용되는 염」이란, 예컨대, 무기산과의 염 또는 유기산과의 염을 들 수 있다. 무기산으로는, 예컨대, 염산, 브롬화수소산, 요오드화수소산, 질산, 황산, 인산 등을 들 수 있다. 유기산으로는, 예컨대, 아세트산, 푸마르산, 말레산, 호박산, 시트르산, 타르타르산, 아디프산, 글루콘산, 글루코헵토산, 글루쿠론산, 테레프탈산, 메탄술폰산, 젖산, 마뇨산, 1,2-에탄디술폰산, 이세티온산, 락토비온산, 올레산, 파모산, 폴리갈락투론산, 스테아르산, 탄닌산, 트리플루오로메탄술폰산, 벤젠술폰산, p-톨루엔술폰산, 황산라우릴에스테르, 황산메틸, 나프탈렌술폰산, 술포살리실산 등을 들 수 있다.
상기 식 (1), (1'), (1a), (1b) 또는 (1c)로 표시되는 화합물은, 수화물 또는 용매화물의 형태를 취하고 있어도 좋다.
상기 식 (1), (1'), (1a), (1b) 또는 (1c)로 표시되는 화합물에 결정 다형 및 결정 다형군(결정 다형 시스템)이 존재하는 경우에는, 이들 결정 다형체 및 결정 다형군(결정 다형 시스템)도 본 화합물의 범위에 포함된다. 여기서, 결정 다형군(결정 다형 시스템)이란, 이들 결정의 제조, 정출(晶出), 보존 등의 조건 및 상태(또한, 본 상태에는 제제화한 상태도 포함함)에 의해, 결정형이 여러 가지 변화되는 경우의 각 단계에 있어서의 결정형 및 그 과정 전체를 의미한다.
본 발명에 있어서, 후안부 질환이란, 유리체, 망막, 맥락막, 강막 또는 시신경에 있어서의 질환이다. 후안부 질환으로는, 가령 황반변성(삼출형 가령 황반변성, 위축형 가령 황반변성, 초기 가령 황반변성), 당뇨병 망막증, 당뇨병 황반부종, 망막색소 변성증, 증식성 유리체 망막증, 망막동맥 폐색증, 망막정맥 폐색증, 포도막염, 레베르병, 미숙아 망막증, 망막박리, 망막색소 상피 박리, 중심성 장액성 맥락망막증, 중심성 삼출성 맥락망막증, 폴립형 맥락막 혈관증, 다발성 맥락막염, 신생혈관 황반증, 망막동맥류, 망막혈관 종상증식, 이들 질환에 기인하는 시신경장애, 녹내장에 기인하는 시신경장애 및 허혈성 시신경장애로 이루어진 군으로부터 선택되는 적어도 1종인 것이 바람직하고, 가령 황반변성, 당뇨병 망막증, 당뇨병 황반부종, 망막정맥 폐색증 및 포도막염으로 이루어진 군으로부터 선택되는 적어도 1종인 것이 특히 바람직하다.
본 화합물은, 후안부 질환의 치료에 사용하는 경우, 환자에 대하여 경구적 또는 비경구적으로 투여할 수 있고, 투여 형태로는, 경구 투여, 눈에의 국소 투여(점안 투여, 결막낭내 투여, 유리체내 투여, 결막하 투여, 테논낭하 투여 등), 정맥내 투여, 경피 투여 등을 들 수 있다. 본 화합물을 눈에 국소 투여할 때에 이용되는 바람직한 제형으로는, 점안제 또는 안연고제가 이용되며, 또는, 주사제, 특히, 결막하 투여제, 테논낭 투여제 또는 유리체내 투여제가 이용된다. 본 화합물을 유효 성분으로서 함유하는 제제는, 필요에 따라, 약학적으로 허용되는 첨가제와 함께 투여에 알맞은 제형으로 제제화된다. 경구 투여에 알맞은 제형으로는, 예컨대, 정제, 캡슐제, 과립제, 산제 등을 들 수 있고, 비경구 투여에 알맞은 제형으로는, 예컨대, 주사제, 점안제, 안연고, 첩포제, 겔, 삽입제 등을 들 수 있다. 이들은 해당 분야에서 범용되고 있는 통상의 기술을 이용하여 조제할 수 있다. 또한 본 발명의 치료 효과의 지속 작용을 보다 유효하게 살리기 위해서, 안내 임플란트용 제제나 마이크로스피어 등의 DDS화된 제제로 하여도 좋다.
예컨대, 정제는, 부형제, 붕괴제, 결합제, 활택제, 코팅제, 교미제 등을 적절하게 선택하여 이용하여, 조제할 수 있다. 부형제로는, 예컨대, 젖당, 포도당, D-만니톨, 무수인산수소칼슘, 전분, 자당 등을 들 수 있다. 붕괴제로는, 예컨대, 카복시메틸셀룰로오스, 카복시메틸셀룰로오스칼슘, 크로스카멜로오스나트륨, 크로스포비돈, 전분, 부분 알파화 전분, 저치환도 하이드록시프로필셀룰로오스 등을 들 수 있다. 결합제로는, 예컨대, 하이드록시프로필셀룰로오스, 에틸셀룰로오스, 아라비아 고무, 전분, 부분 알파화 전분, 폴리비닐피롤리돈, 폴리비닐알코올 등을 들 수 있다. 활택제로는, 예컨대, 스테아르산마그네슘, 스테아르산칼슘, 탈크, 함수 이산화규소, 경화유 등을 들 수 있다. 코팅제로는, 예컨대, 정제 백당, 하이드록시프로필메틸셀룰로오스, 하이드록시프로필셀룰로오스, 메틸셀룰로오스, 에틸셀룰로오스, 폴리비닐피롤리돈 등을 들 수 있다. 교미제로는, 예컨대, 시트르산, 아스파탐, 아스코르브산, 멘톨 등을 들 수 있다.
예컨대, 주사제는 등장화제, 완충화제, 계면활성제, 증점제 등을 필요에 따라 선택하여 이용하여, 조제할 수 있다. 등장화제로는, 예컨대, 염화나트륨 등을 들 수 있다. 완충화제로는, 예컨대, 인산나트륨 등을 들 수 있다. 계면활성제로는, 예컨대, 폴리옥시에틸렌소르비탄모노올리에이트 등을 들 수 있다. 증점제로는, 예컨대, 메틸셀룰로오스 등을 들 수 있다.
예컨대, 점안제는 등장화제, 완충화제, 계면활성제, 안정화제, 방부제 등으로부터 필요에 따라 선택하여 이용하여, 조제할 수 있고, pH는 안과 제제에 허용되는 범위 내에 있으면 좋지만, 통상 4∼8의 범위 내가 바람직하다. 등장화제로는, 예컨대, 염화나트륨, 농글리세린 등을 들 수 있다. 완충화제로는, 예컨대, 인산나트륨, 아세트산나트륨 등을 들 수 있다. 계면활성제로는, 예컨대, 폴리옥시에틸렌소르비탄모노올리에이트, 스테아르산폴리옥실 40, 폴리옥시에틸렌 경화 피마자유 등을 들 수 있다. 안정화제로는, 예컨대, 시트르산나트륨, 에데트산나트륨 등을 들 수 있다. 방부제로는, 예컨대, 염화벤잘코늄, 파라벤 등을 들 수 있다.
예컨대, 안연고는 백색 바셀린, 유동 파라핀 등의 범용되는 기제를 이용하여, 조제할 수 있다.
예컨대, 삽입제는, 생체 분해성 폴리머, 예컨대, 하이드록시프로필셀룰로오스, 하이드록시프로필메틸셀룰로오스, 카복시비닐폴리머, 폴리아크릴산 등의 생체 분해성 폴리머를 본 화합물과 함께 분쇄 혼합하고, 이 분말을 압축 성형함으로써, 조제할 수 있으며, 필요에 따라, 부형제, 결합제, 안정화제, pH 조정제를 이용할 수 있다.
예컨대, 안내 임플란트용 제제는, 생체 분해성 폴리머, 예컨대, 폴리젖산, 폴리글리콜산, 젖산·글리콜산 공중합체, 하이드록시프로필셀룰로오스 등의 생체 분해성 폴리머를 이용하여, 조제할 수 있다.
본 화합물의 투여량은, 제형, 투여해야 할 환자의 증상의 경중, 연령, 체중, 안구 용적, 의사의 판단 등에 따라 적절하게 변경할 수 있지만, 경구 투여의 경우, 일반적으로는, 성인에 대하여 1일당 0.01∼10000 ㎎, 바람직하게는 0.1∼5000 ㎎, 보다 바람직하게는 0.5∼2500 ㎎을 1회 또는 수회에 나누어 투여할 수 있고, 주사제의 경우, 일반적으로는, 성인에 대하여 0.0001∼2000 ㎎을 1회 또는 수회에 나누어 투여할 수 있다. 또한, 점안제 또는 삽입제의 경우에는, 0.000001∼10%(w/v), 바람직하게는 0.00001∼1%(w/v), 보다 바람직하게는 0.0001∼0.1%(w/v)의 유효 성분 농도의 것을 1일 1회 또는 수회 투여할 수 있다. 또한, 첩포제의 경우에는, 성인에 대하여 0.0001∼2000 ㎎을 함유하는 첩포제를 첩포할 수 있고, 안내 임플란트용 제제의 경우에는, 성인에 대하여 0.0001∼2000 ㎎ 함유하는 안내 임플란트용 제제를 안내에 임플란트할 수 있다.
실시예
이하에, 약리 시험의 결과 및 제제예를 나타내지만, 이들 예는 본 발명을 보다 잘 이해하기 위한 것으로, 본 발명의 범위를 한정하는 것은 아니다.
[약리 시험 1]
레이저 유발 래트 맥락막 혈관신생 모델(Invest. Ophthalmol. Vis. Sci., 40(2), 459-466 (1999))을 이용하여, 본 화합물의 유용성을 평가하였다.
(크립톤 레이저 유발 래트 맥락막 혈관신생 모델 동물의 제작 방법)
래트에게 5%(W/V) 염산케타민 주사액 및 2% 염산자일라진 주사액의 혼합액(7:1) 1 ㎖/㎏을 근육내 투여하여 전신 마취하고, 0.5%(W/V) 트로피카미드-0.5% 염산페닐레프린 점안액을 점안하여 산동(散瞳)시킨 후, 크립톤 레이저 광응고 장치에 의해 광응고를 행하였다. 광응고는, 안저 후국부에 있어서, 굵은 망막 혈관을 피하고, 초점을 망막 심층에 맞춰 1안에 대해 8군데 산재형으로 실시하였다(응고 조건: 스폿 사이즈 100 ㎛, 출력 100 mW, 응고 시간 0.1초). 광응고 후, 안저 촬영을 행하여, 레이저 조사 부위를 확인하였다.
(시험 화합물)
본 약리 시험에서는, 본 화합물로서, 국제 공개 제2011/046916호 팜플렛에 기재된 합성 방법에 따라 합성한 상기 화합물 1b를 사용하였다.
(약물 투여 방법)
화합물 1b를 1%(W/V) 메틸셀룰로오스액(메틸셀룰로오스를 정제수에 용해시켜 조제)에 20 ㎎/㎖가 되도록 혼합하고, 100 ㎎/㎏의 용량으로 화합물 1b 함유 투여액을 광응고 수술일로부터 수술일을 포함시켜 7일간 1일 2회 경구 투여하였다. 또한, 기제 투여군에는 1%(W/V) 메틸셀룰로오스액을 동일하게 투여하였다.
(평가 방법)
광응고 후 7일째, 래트에게 5%(W/V) 염산케타민 주사액 및 2% 염산자일라진 주사액의 혼합액(7:1) 1 ㎖/㎏을 근육내 투여하여 전신 마취하고, 0.5%(W/V) 트로피카미드-0.5% 염산페닐레프린 점안액을 점안하여 산동시킨 후, 10% 플루오레세인 용액 0.1 ㎖를 음경 정맥으로부터 주입하여, 형광 안저 조영을 행하였다. 형광 안저 조영으로, 형광 누출이 확인되지 않은 스폿을 음성(혈관신생 없음), 형광 누출이 확인된 스폿을 양성으로 판단하였다. 또한, 약간의 형광 누출이 확인되는 광응고 부위는, 그것이 2군데 존재했을 때에 양성(혈관신생 있음)으로 판정하였다. 그 후, 식 1에 따라, 레이저 조사 8군데의 스폿에 대한 양성 스폿 수로부터 맥락막 혈관신생 발생률(%)을 산출하고, 식 2에 따라, 평가 약물의 억제율(%)을 산출하였다. 화합물 1b의 결과를 표 1에 나타낸다. 또한, 각 투여군의 예수는 7 또는 8이다.
[식 1]:
맥락막 혈관신생 발생률(%)=(양성 스폿 수/전체 광응고 부위 수)×100
[식 2]:
억제율(%)={(A0-AX)/A0}×100
A0: 기제 투여군의 맥락막 혈관신생 발생률
AX: 약물 투여군의 맥락막 혈관신생 발생률
표 1로부터 분명한 바와 같이, 화합물 1b가, 레이저 유발 래트 맥락막 혈관신생 모델 동물에 있어서 맥락막 혈관신생을 저해하는 것이 나타났다. 이상의 결과로부터, 본 화합물이, 후안부 질환에 대하여 우수한 예방 또는 치료 효과를 갖는 것이 나타났다.
[제제예]
제제예를 들어 본 발명의 약제를 더욱 구체적으로 설명하였으나, 본 발명은 이들 제제예에만 한정되는 것은 아니다.
처방예 1
점안제
100 ㎖ 중
본 화합물
10 ㎎
염화나트륨
900 ㎎
폴리소르베이트 80
적량
인산수소이나트륨
적량
인산이수소나트륨
적량
멸균 정제수
적량
멸균 정제수에 본 화합물 및 그 이외의 상기 성분을 첨가하고, 이들을 충분히 혼합하여 점안액을 조제한다. 본 화합물의 첨가량을 변경함으로써, 농도가 0.05%(w/v)∼1%(w/v)인 점안제를 조제할 수 있다.
처방예 2
안연고
100 g 중
본 화합물
0.3 g
유동 파라핀
10.0 g
백색 바셀린
적량
균일하게 용융된 백색 바셀린 및 유동 파라핀에, 본 화합물을 첨가하고, 이들을 충분히 혼합한 후에 서서히 냉각시킴으로써 안연고를 조제한다. 본 화합물의 첨가량을 변경함으로써, 농도가 0.05%(w/v)∼1%(w/w)인 안연고를 조제할 수 있다.
처방예 3
정제
100 ㎎ 중
본 화합물
1 ㎎
젖당
66.4 ㎎
옥수수 전분
20 ㎎
카복시메틸셀룰로오스칼슘
6 ㎎
하이드록시프로필셀룰로오스
6 ㎎
스테아르산마그네슘
0.6 ㎎
본 화합물, 젖당을 혼합기 내에서 혼합하고, 그 혼합물에 카복시메틸셀룰로오스칼슘 및 하이드록시프로필셀룰로오스를 첨가하여 조립(造粒)하고, 얻어진 과립을 건조 후 정립(整粒)하여, 그 정립 과립에 스테아르산마그네슘을 첨가하여 혼합하고, 타정기로 타정한다. 또한, 본 화합물, 카복시메틸셀룰로오스칼슘 및 하이드록시프로필셀룰로오스의 첨가량을 적절하게 변경함으로써, 100 ㎎ 중의 본 화합물의 함유량이 0.1 ㎎∼50 ㎎인 정제를 조제할 수 있다.
처방예 4
주사제 또는 유리체내 투여제
10 ㎖ 중
본 화합물
10 ㎎
염화나트륨
90 ㎎
폴리소르베이트 80
적량
멸균 정제수
적량
멸균 정제수에 본 화합물 및 그 이외의 상기 성분을 첨가하고, 충분히 혼합하여 용해 또는 현탁시켜 주사제를 조제한다. 본 화합물 및 그 이외의 상기 성분의 첨가량을 적절하게 변경함으로써, 10 ㎖ 중의 본 화합물의 함유량이 2 ㎎∼200 ㎎인 주사제를 조제할 수 있다. 이와 같이 하여 조제한 주사제는 안내 투여를 위한 주사제, 예컨대 유리체내 투여제로서 투여할 수 있다.
Claims (10)
- 하기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 후안부 질환의 예방 또는 치료제:
[식 (1) 중,
R1 및 R2는 동일하거나 또는 상이하고, 수소 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타내며;
R3은 수소 원자, 할로겐 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타내고;
R4는 수소 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타내며;
R5는 비치환 또는 R6으로 치환되어 있는 함질소 이환식 방향환기를 나타내고;
R6은 할로겐 원자, 저급 알킬기, 또는 할로겐 원자로 치환된 저급 알킬기를 나타낸다]. - 제1항 내지 제4항 중 어느 한 항에 있어서, 후안부 질환이 유리체, 망막, 맥락막, 강막 또는 시신경에 있어서의 질환인 예방 또는 치료제.
- 제1항 내지 제4항 중 어느 한 항에 있어서, 후안부 질환이 가령(加齡) 황반변성, 당뇨병 망막증, 당뇨병 황반부종, 망막색소 변성증, 증식성 유리체 망막증, 망막동맥 폐색증, 망막정맥 폐색증, 포도막염, 레베르병, 미숙아 망막증, 망막 박리, 망막색소 상피 박리, 중심성 장액성 맥락망막증, 중심성 삼출성 맥락망막증, 폴립형 맥락막 혈관증, 다발성 맥락막염, 신생혈관 황반증, 망막동맥류, 망막혈관 종상증식, 이들 질환에 기인하는 시신경장애, 녹내장에 기인하는 시신경장애 및 허혈성 시신경장애로 이루어진 군으로부터 선택되는 적어도 1종인 예방 또는 치료제.
- 제6항에 있어서, 후안부 질환이 가령 황반변성, 당뇨병 망막증, 당뇨병 황반부종, 망막정맥 폐색증 및 포도막염으로 이루어진 군으로부터 선택되는 적어도 1종인 예방 또는 치료제.
- 상기 식 (1)로 표시되는 화합물, 이의 에난티오머 또는 디아스테레오머, 또는 이의 약학적으로 허용되는 염을 유효 성분으로서 함유하는, 맥락막 혈관신생 저해제.
- 제1항 내지 제8항 중 어느 한 항에 있어서, 투여 형태가 점안 투여, 유리체내 투여, 결막하 투여, 결막낭내 투여, 테논낭하 투여 또는 경구 투여인 예방 또는 치료제, 또는 저해제.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 제형이 점안제, 안연고, 삽입제, 첩포제, 주사제, 정제, 세립제 또는 캡슐제인 예방 또는 치료제, 또는 저해제.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JPJP-P-2014-146573 | 2014-07-17 | ||
| JP2014146573 | 2014-07-17 | ||
| PCT/JP2015/070477 WO2016010130A1 (ja) | 2014-07-17 | 2015-07-17 | 後眼部疾患の予防または治療剤 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170029513A true KR20170029513A (ko) | 2017-03-15 |
Family
ID=55078616
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177001365A KR20170029513A (ko) | 2014-07-17 | 2015-07-17 | 후안부 질환의 예방 또는 치료제 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US20170202845A1 (ko) |
| EP (1) | EP3170500A4 (ko) |
| JP (1) | JP2016029037A (ko) |
| KR (1) | KR20170029513A (ko) |
| CN (1) | CN106456641A (ko) |
| BR (1) | BR112017000991A2 (ko) |
| CA (1) | CA2955862A1 (ko) |
| EA (1) | EA201790231A1 (ko) |
| MA (1) | MA40320A (ko) |
| MX (1) | MX2017000580A (ko) |
| PH (1) | PH12017500106A1 (ko) |
| SG (1) | SG11201700331RA (ko) |
| TW (1) | TW201625255A (ko) |
| WO (1) | WO2016010130A1 (ko) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011046916A1 (en) | 2009-10-13 | 2011-04-21 | Bristol-Myers Squibb Company | N-((1r,2s,5r)-5-(tert-butylamino)-2-((s)-3-(7-tert-butylpyrazolo[1,5-a][1,3,5]triazin-4-ylamino)-2-oxopyrrolidin-1-yl)cyclohexyl)acetamide, a dual modulator of chemokine receptor activity, crystalline forms and processes |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7629351B2 (en) * | 2006-07-28 | 2009-12-08 | Bristol-Myers Squibb Company | N-((1R,2S,5R)-5-(tert-butylamino)-2-((S)-2-oxo-3-(6-(trifluoromethyl)quinazolin-4-ylamino) pyrrolidin-1-yl)cyclohexyl)acetamide and other modulators of chemokine receptor activity, crystalline forms and process |
| US7687508B2 (en) * | 2006-07-28 | 2010-03-30 | Bristol-Myers Squibb Company | Cyclic derivatives as modulators of chemokine receptor activity |
| BR112013015260B1 (pt) * | 2010-12-16 | 2020-03-24 | Allergan, Inc. | Derivados de enxofre como moduladores de receptor de quimiocina, composição compreendendo o mesmo e seu uso |
| CA2821985C (en) * | 2011-01-11 | 2019-07-09 | Dimerix Bioscience Pty Ltd | Combination therapy |
| CA2902785A1 (en) * | 2013-02-28 | 2014-09-04 | Santen Pharmaceutical Co., Ltd. | Prophylactic or therapeutic agent for posterior ocular disease containing tetrahydropyranylaminocyclopentylcarbonyl-tetrahydropyridopyridine derivative as effective ingredient |
-
2015
- 2015-07-17 TW TW104123160A patent/TW201625255A/zh unknown
- 2015-07-17 CA CA2955862A patent/CA2955862A1/en not_active Abandoned
- 2015-07-17 EP EP15821760.4A patent/EP3170500A4/en not_active Withdrawn
- 2015-07-17 EA EA201790231A patent/EA201790231A1/ru unknown
- 2015-07-17 BR BR112017000991A patent/BR112017000991A2/pt not_active Application Discontinuation
- 2015-07-17 SG SG11201700331RA patent/SG11201700331RA/en unknown
- 2015-07-17 WO PCT/JP2015/070477 patent/WO2016010130A1/ja active Application Filing
- 2015-07-17 MX MX2017000580A patent/MX2017000580A/es unknown
- 2015-07-17 US US15/326,728 patent/US20170202845A1/en not_active Abandoned
- 2015-07-17 MA MA040320A patent/MA40320A/fr unknown
- 2015-07-17 KR KR1020177001365A patent/KR20170029513A/ko unknown
- 2015-07-17 CN CN201580033445.2A patent/CN106456641A/zh active Pending
- 2015-07-17 JP JP2015142550A patent/JP2016029037A/ja active Pending
-
2017
- 2017-01-17 PH PH12017500106A patent/PH12017500106A1/en unknown
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011046916A1 (en) | 2009-10-13 | 2011-04-21 | Bristol-Myers Squibb Company | N-((1r,2s,5r)-5-(tert-butylamino)-2-((s)-3-(7-tert-butylpyrazolo[1,5-a][1,3,5]triazin-4-ylamino)-2-oxopyrrolidin-1-yl)cyclohexyl)acetamide, a dual modulator of chemokine receptor activity, crystalline forms and processes |
Non-Patent Citations (2)
| Title |
|---|
| 니치간카이시, 103, 923-947 (1999) |
| 신즈세츠린쇼간카코자 제5권 「망막 유리체 질환」, p. 184-189, 232-237 (2000) |
Also Published As
| Publication number | Publication date |
|---|---|
| SG11201700331RA (en) | 2017-02-27 |
| MA40320A (fr) | 2017-05-24 |
| CN106456641A (zh) | 2017-02-22 |
| BR112017000991A2 (pt) | 2018-07-24 |
| MX2017000580A (es) | 2017-09-01 |
| JP2016029037A (ja) | 2016-03-03 |
| PH12017500106A1 (en) | 2017-05-22 |
| WO2016010130A1 (ja) | 2016-01-21 |
| US20170202845A1 (en) | 2017-07-20 |
| EP3170500A1 (en) | 2017-05-24 |
| EP3170500A4 (en) | 2018-03-14 |
| CA2955862A1 (en) | 2016-01-21 |
| EA201790231A1 (ru) | 2017-05-31 |
| TW201625255A (zh) | 2016-07-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2374336T3 (es) | Agente profiláctico o terapéutico para una enfermedad ocular posterior que comprende un agonista selectivo no ergótico del receptor d2 como principio activo. | |
| US8309612B2 (en) | Method for treating age-related macular degeneration | |
| TWI439464B (zh) | 二胺衍生物之製造方法 | |
| JPWO2002020540A1 (ja) | アデノシン誘導体及びその用途 | |
| TW200838537A (en) | Substituted quinazolines | |
| ES2354223T3 (es) | Derivados de amidina para uso en la prevención o el tratamiento de glaucoma. | |
| KR101891078B1 (ko) | 황반변성 예방 또는 치료용 약학 조성물 | |
| WO2011149012A1 (ja) | イソキノリンスルホニル誘導体を有効成分として含有する網脈絡膜変性疾患の予防または治療剤、網脈絡膜変性疾患の予防または治療方法、イソキノリンスルホニル誘導体またはその医薬的に許容される塩、ならびにその使用 | |
| KR20170029513A (ko) | 후안부 질환의 예방 또는 치료제 | |
| US9579309B2 (en) | Prophylactic or therapeutic agent for posterior ocular disease containing tetrahydropyranylaminocyclopentylcarbonyltetrahydropyridopyridine derivative as effective ingredient | |
| EP2119439A2 (en) | Angiogenesis inhibitor for treating macular degeneration | |
| US20110224200A1 (en) | Therapeutic agent for chorioretinal degenerative disease containing pyridine-3-carbaldehyde 0-(piperidin-1-yl-propyl)-oxime derivative as active ingredient | |
| JP2006188522A (ja) | 2−{3−[(e)−2−(4,6−ジメチル−ピリジン−2−イル)−ビニル]−1h−インダゾール−6−イルアミノ}−n−{4−ヒドロキシ−ブチ−2−ニル)ベンズアミドの多形型又は非晶質型 | |
| TW201605451A (zh) | 老年性黃斑部病變之預防或治療劑 | |
| JP2006348023A (ja) | アミン誘導体を有効成分として含む血管新生阻害剤 | |
| JP2009079041A (ja) | リチウム塩を有効成分として含有する後眼部疾患の治療又は予防剤 | |
| KR20150051493A (ko) | 이매티닙 또는 이의 약학적으로 허용되는 염을 유효성분으로 포함하는 혈관신생 관련 질환의 예방 또는 치료용 약학적 조성물 | |
| JP2006348024A (ja) | アミジノ誘導体を有効成分として含む神経細胞の保護剤 | |
| WO2000061148A1 (fr) | Inhibiteurs d'hypofonction optique provoquee par une lesion d'une cellule du nerf optique induite par des facteurs autres que les troubles circulatoires optiques | |
| JPWO2002048096A1 (ja) | ヒドラゾン誘導体およびその医薬用途 |