KR20140067070A - H-포스포네이트에 의한 나노입자 peg 개질 - Google Patents
H-포스포네이트에 의한 나노입자 peg 개질 Download PDFInfo
- Publication number
- KR20140067070A KR20140067070A KR1020147007934A KR20147007934A KR20140067070A KR 20140067070 A KR20140067070 A KR 20140067070A KR 1020147007934 A KR1020147007934 A KR 1020147007934A KR 20147007934 A KR20147007934 A KR 20147007934A KR 20140067070 A KR20140067070 A KR 20140067070A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- agent
- compound
- peg
- stealth
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids RP(=O)(OH)2; Thiophosphonic acids, i.e. RP(=X)(XH)2 (X = S, Se)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/548—Phosphates or phosphonates, e.g. bone-seeking
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/554—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound the modifying agent being a steroid plant sterol, glycyrrhetic acid, enoxolone or bile acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6905—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a colloid or an emulsion
- A61K47/6911—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a colloid or an emulsion the form being a liposome
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids RP(=O)(OH)2; Thiophosphonic acids, i.e. RP(=X)(XH)2 (X = S, Se)
- C07F9/40—Esters thereof
- C07F9/4071—Esters thereof the ester moiety containing a substituent or a structure which is considered as characteristic
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids RP(=O)(OH)2; Thiophosphonic acids, i.e. RP(=X)(XH)2 (X = S, Se)
- C07F9/44—Amides thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J41/00—Normal steroids containing one or more nitrogen atoms not belonging to a hetero ring
- C07J41/0033—Normal steroids containing one or more nitrogen atoms not belonging to a hetero ring not covered by C07J41/0005
- C07J41/0055—Normal steroids containing one or more nitrogen atoms not belonging to a hetero ring not covered by C07J41/0005 the 17-beta position being substituted by an uninterrupted chain of at least three carbon atoms which may or may not be branched, e.g. cholane or cholestane derivatives, optionally cyclised, e.g. 17-beta-phenyl or 17-beta-furyl derivatives
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S977/00—Nanotechnology
- Y10S977/70—Nanostructure
- Y10S977/773—Nanoparticle, i.e. structure having three dimensions of 100 nm or less
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S977/00—Nanotechnology
- Y10S977/70—Nanostructure
- Y10S977/832—Nanostructure having specified property, e.g. lattice-constant, thermal expansion coefficient
- Y10S977/835—Chemical or nuclear reactivity/stability of composition or compound forming nanomaterial
- Y10S977/836—Chemical or nuclear reactivity/stability of composition or compound forming nanomaterial having biological reactive capability
Abstract
본 발명은, 예를 들어 생체내 순환 시간 및 표적화된 전달 성능을 증가시키기 위한 나노입자의 표면 개질을 위한 개선된 방법 및 화합물을 가능하게 하는 포스포네이트 컨쥬게이트 및 포스포네이트 컨쥬게이트의 제조 방법을 제공한다.
Description
관련 출원의 상호 참조
본원은, 전체 내용이 본원에 참조로 도입되는 미국 가출원 번호 61/529,694에 대한 우선권의 이익을 청구한다.
정부 지원 연구 개발 하에 수행된 발명에 대한 권리에 관한 진술
해당 없음
컴팩트 디스크로 제출된 "서열 목록", 표 또는 컴퓨터 프로그램 목록 첨부물에 대한 참조
해당 없음
배경기술
현재, 치료제 및 진단제의 대부분은 환자에게 전신 투여된다. 불행하게도, 현행 전달 방법은, 치료제의 감소된 효능 뿐만 아니라 예를 들어 환자에서의 비-표적 부위에서의 약물 활성화로 인한 부작용을 비롯한 여러 단점을 가질 수 있다. 일부 이들 문제점을 해결하기 위한 노력에 있어, 진단제 및 치료제와 회합된 나노입자의 표적화 전달은 유망한 새로운 약물 전달 방식을 제공한다.
그러나, 특정 상황 하에, 나노입자는 환자의 면역 시스템에 의해 거부되고, 나노입자가 약물 전달에 대한 표적에 도달할 수 있기 전에 처리될 수 있다. 이들 문제를 해결하기 위해, 나노입자의 표면이 개질될 수 있다. 예를 들어, 리포솜과 같은 나노입자는 통상적으로, 생체내 성능 개선을 위해 그의 표면 상에 폴리에틸렌 글리콜 (PEG) 기를 도입하도록 개질된다. 일반적으로, 리포솜 PEG 개질을 달성하기 위해 사용되는 두가지 통상적 접근이 존재한다. 하나의 접근은, 기계적 수단, 예를 들어, 압출 하에 지질-PEG 분자를 조합하여 리포솜 제제를 형성하는 것을 포함한다. 또 다른 접근에서는, 리포솜을 예비어셈블링하고, 이어서 지질이 리포솜 이중층 내에 삽입될 수 있는 조건 하에 적절하게 배치된 PEG-지질로 처리하고, 이로써 리포솜 표면에 PEG가 부착된 리포솜을 형성할 수 있다.
표적화된 약물 전달 방법을 개발하는 데 있어 최근에 일부 진보가 있었지만, 추가의 개선에 대한 필요성이 여전히 존재한다. 예를 들어, 현행 나노입자 개질에 대한 접근은 나노입자에 적용될 수 있는 단지 제한된 수의 개질만을 제공한다. 본 발명은 이들 및 다른 필요성을 해결한다.
발명의 간단한 요약
본 발명은, 예를 들어 생체내 순환 시간 및 표적화된 전달 성능을 증가시키기 위한 나노입자의 표면 개질을 위한 개선된 방법 및 화합물을 가능하게 하는 포스포네이트 컨쥬게이트 및 포스포네이트 컨쥬게이트의 제조 방법을 제공한다.
본 발명의 하나의 측면에서, 본 발명의 포스포네이트 컨쥬게이트는 하기 화학식의 화합물을 포함할 수 있다.
상기 식에서, R1, R2, R3, R4, L1, L2, L3 및 L4는 각각 하기에서 보다 상세히 설명된다.
또 다른 측면에서, 본 발명은 하기 화학식의 화합물을 포함한다.
상기 식에서, R1, R2, R3, R4, R9, L1, L2, L3 및 L4는 하기에서 보다 상세히 설명된다.
또한 또 다른 측면에서, 본 발명은, 화학식: H2N(L1)-(R1)을 갖는 1급 아민 화합물, 화학식: O=C[(L2)-(R2)]n을 갖는 카르보닐 화합물, 및 화학식:
을 갖는 H-포스포네이트 화합물을, 화학식:
을 갖는 포스포네이트 컨쥬게이트
(여기서, 포스포네이트 컨쥬게이트, 1급 아민 화합물, 카르보닐 화합물, 및 H-포스포네이트 화합물은 하기에서 보다 상세히 설명됨)를 형성하기에 충분한 조건 하에 조합하는 것을 포함하는, 포스포네이트 컨쥬게이트의 제조 방법을 포함한다.
또한 또 다른 측면에서, 본 발명은, 화학식: HN[(L1)-(R1)](R9)을 갖는 2급 아민 화합물, 화학식: O=C[(L2)-(R2)]n을 갖는 카르보닐 화합물, 및 화학식:
을 갖는 H-포스포네이트 화합물을, 화학식:
을 갖는 포스포네이트 컨쥬게이트
(여기서, 포스포네이트 컨쥬게이트, 2급 아민 화합물, 카르보닐 화합물, 및 H-포스포네이트 화합물은 하기에서 보다 상세히 설명됨)를 형성하기에 충분한 조건 하에 조합하는 것을 포함하는, 포스포네이트 컨쥬게이트의 제조 방법을 포함한다.
본 발명의 포스포네이트 컨쥬게이트 및 그의 제조 방법은, 약물 전달 및 진단 영상 분야에 대해 수많은 독특한 측면을 제공한다. 예를 들어, 본 발명은, 표적화된 약물 전달에 사용될 수 있는 스텔스(stealth) 나노입자로의 나노입자의 변형을 용이하게 할 수 있는 화합물의 강력하고 간단한 제조 방법을 제공한다. 특정 경우에, 포스포네이트 컨쥬게이트는 나노입자 표면 상에 스텔스제의 밀도를 증가시키는 독특한 능력을 제공하고, 따라서 보다 저밀도에서는 효과적이지 않을 수 있는 다양한 스텔스제를 사용하는 데 있어 추가의 유연성을 가능하게 할 수 있다. 또한, 포스포네이트 컨쥬게이트가, 나노입자 표면 상에 스텔스제 또는 다른 성분, 예를 들어 표적화제를 제시하도록 추가의 안정성을 제공하는 방식으로 제조될 수 있다. 다른 이점들 중에서도 특히, 포스포네이트 컨쥬게이트는 양으로 대전된 및/또는 음으로 대전된 기를 도입하여 나노입자의 표면 특징의 개질을 용이하게 할 수 있다. 개질된 나노입자의 제조에 있어 유연성은, 또한, 환자에게 투여된 후 긴 생체내 반감기를 가질 수 있는 특정 치료 및/또는 진단 용도에 대해 맞춤화된(tailored) 나노입자를 가능하게 할 수 있다.
본 발명의 본질 및 이점에 대한 추가의 이해는, 명세서의 나머지 부분 및 도면을 참조함으로써 실현될 수 있다.
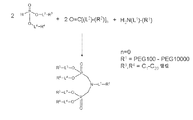
도 1은 본 발명의 포스포네이트 컨쥬게이트의 제조를 위한 합성 방법의 일례를 도시한 것이다.
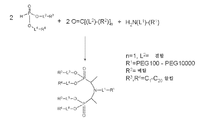
도 2는 본 발명의 포스포네이트 컨쥬게이트의 제조를 위한 합성 방법의 일례를 도시한 것이다.
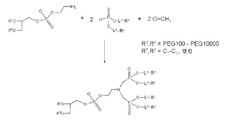
도 3은 본 발명의 포스포네이트 컨쥬게이트의 제조를 위한 합성 방법의 일례를 도시한 것이다.
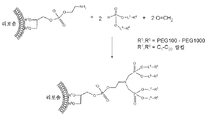
도 4는 리포솜 표면 상에서의 본 발명의 포스포네이트 컨쥬게이트의 제조를 위한 합성 방법의 일례를 도시한 것이다.
도 5는 리포솜 표면 상에서의 본 발명의 포스포네이트 컨쥬게이트의 제조를 위한 합성 방법의 일례를 도시한 것이다.
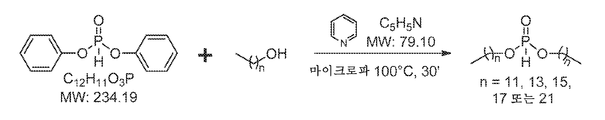
도 6은, 본 발명의 예시적 실시양태에 따른, 디페닐 포스파이트를 1-알칸올과 조합하여 디알킬 히드로겐 포스포네이트를 형성하는 일반적 반응식을 나타낸 것이다.
도 7은 본 발명의 예시적 실시양태에 따른 컨쥬게이트의 제조에 대한 일반적 반응식을 나타낸 것이다.
도 8은 본 발명의 예시적 실시양태에 따른 컨쥬게이트의 제조에 대한 또 다른 일반적 반응식을 나타낸 것이다.
도 2는 본 발명의 포스포네이트 컨쥬게이트의 제조를 위한 합성 방법의 일례를 도시한 것이다.
도 3은 본 발명의 포스포네이트 컨쥬게이트의 제조를 위한 합성 방법의 일례를 도시한 것이다.
도 4는 리포솜 표면 상에서의 본 발명의 포스포네이트 컨쥬게이트의 제조를 위한 합성 방법의 일례를 도시한 것이다.
도 5는 리포솜 표면 상에서의 본 발명의 포스포네이트 컨쥬게이트의 제조를 위한 합성 방법의 일례를 도시한 것이다.
도 6은, 본 발명의 예시적 실시양태에 따른, 디페닐 포스파이트를 1-알칸올과 조합하여 디알킬 히드로겐 포스포네이트를 형성하는 일반적 반응식을 나타낸 것이다.
도 7은 본 발명의 예시적 실시양태에 따른 컨쥬게이트의 제조에 대한 일반적 반응식을 나타낸 것이다.
도 8은 본 발명의 예시적 실시양태에 따른 컨쥬게이트의 제조에 대한 또 다른 일반적 반응식을 나타낸 것이다.
I. 정의
본원에서 사용되는 바와 같이, 용어 "알킬"은, 그 자체로 또는 또 다른 치환기의 일부로서, 달리 언급되지 않는 한, 지정된 탄소 원자수를 갖는 (즉, C10-24는 10 내지 24개의 탄소를 의미함) 직쇄 또는 분지쇄 탄화수소 라디칼을 의미한다. 일부 실시양태에서, 알킬 기는 1 내지 36개의 탄소수 범위를 가질 수 있다. 특정 실시양태에서, 알킬 기는 1 내지 10개의 탄소수 또는 1 내지 20개의 탄소수 범위를 가질 수 있다. 일부 실시양태에서, 알킬 기는 포화 또는 불포화될 수 있고, 또한 치환 또는 비-치환될 수 있다.
본원에서 사용되는 바와 같이, 용어 "치환된"은 모(parent) 분자 또는 기에 결합된 기를 지칭한다. 예를 들어, 시아노 치환기를 갖는 알킬 기는 시아노-치환된 알킬 기이다. 적합한 치환기는 할로, 시아노, 알킬, 아미노, 히드록시, 알콕시, 및 아미도를 포함하나 이에 제한되지는 않는다.
본원에서 사용되는 바와 같이, 용어 "H-포스포네이트 화합물"은 H-P(O)(OL3-R3)(OL4-R4)의 화학식을 갖는 화합물을 지칭하며, 이는 본원에서 추가로 설명된다.
본원에서 사용되는 바와 같이, 용어 "1급 아민 화합물"은, 일반적으로 화학식 H2N(L1)-(R1)을 갖는 화합물을 지칭하며, 이는 본원에서 추가로 설명된다.
본원에서 사용되는 바와 같이, 용어 "2급 아민 화합물"은, 일반적으로 화학식 HN[(L1)-(R1)](R9)를 갖는 화합물을 지칭하며, 이는 본원에서 추가로 설명된다.
본원에서 사용되는 바와 같이, 용어 "카르보닐 화합물"은, 일반적으로 화학식 O=C[(L2)-(R2)]n을 갖는 화합물을 지칭하며, 이는 본원에서 추가로 설명된다.
본원에서 사용되는 바와 같이, 용어 "표적화된 전달 조성물"은, 본 발명의 포스포네이트 컨쥬게이트에 부착된 나노입자의 조성물을 지칭하며, 이들의 세부사항은 본원에서 추가로 설명된다. 본 발명의 조성물은, 치료 조성물로서, 진단 조성물로서, 또는 치료 및 진단 조성물 둘 다로서 사용될 수 있다. 특정 실시양태에서, 조성물은, 본원에서 추가로 설명되는 바와 같이, 대상체 또는 시험 샘플 내의 특정 표적에 대해 표적화될 수 있다.
본원에서 사용되는 바와 같이, 용어 "나노입자"는 다양한 크기, 형상, 유형 및 용도를 갖는 입자를 지칭하며, 이는 본원에서 추가로 설명된다. 당업자가 인지하는 바와 같이, 나노입자의 특징, 예를 들어, 크기는, 나노입자의 유형 및/또는 용도 뿐만 아니라 당업계에 일반적으로 널리 공지되어 있는 다른 요인에 따라 달라질 수 있다. 일반적으로, 나노입자는 약 1 nm 내지 약 1000 nm의 크기 범위를 가질 수 있다. 다른 실시양태에서, 나노입자는 약 10 nm 내지 약 200 nm의 크기 범위를 가질 수 있다. 또한 다른 실시양태에서, 나노입자는 약 50 nm 내지 약 150 nm의 크기 범위를 가질 수 있다. 특정 실시양태에서, 나노입자는 신장 배설 한계 초과의 크기, 예를 들어 약 6 nm 초과의 직경을 갖는다. 다른 실시양태에서, 나노입자는 간에 의한 혈류로부터의 청소(clearance)를 피하기에 충분히 작고, 예를 들어, 1000 nm 미만의 직경을 갖는다. 나노입자는 구형, 원뿔형, 회전타원체형, 및 당업계에 일반적으로 공지되어 있는 다른 형상을 포함할 수 있다. 나노입자는 중공형 (예를 들어, 중공 내부 코어를 갖는 충실형 외부 코어)이거나 충실형이거나 또는 중공 및 충실 층 또는 다양한 충실 층을 갖는 다층형일 수 있다. 예를 들어, 나노입자는 충실 코어 영역 및 충실 외부 캡슐화 영역을 포함할 수 있고, 이들은 둘 다 가교될 수 있다. 나노입자는 지질, 중합체, 자성체 또는 금속 물질, 예컨대 실리카, 금, 산화철 등을 비롯한 각종 물질 중 하나의 물질, 또는 이들의 임의의 조합으로 구성될 수 있다. 지질은 지방, 왁스, 스테롤, 콜레스테롤, 지용성 비타민, 모노글리세리드, 디글리세리드, 인지질, 스핑고지질, 당지질, 양이온성 또는 음이온성 지질, 유도체화된 지질, 카디올리핀 등을 포함할 수 있다. 중합체는 블록 공중합체, 일반적으로 폴리(락트산), 폴리(락트-코-글리콜산), 폴리에틸렌 글리콜, 아크릴 중합체, 양이온성 중합체, 뿐만 아니라 나노입자 제조에 사용하기 위한 당업계에 공지된 다른 중합체를 포함할 수 있다. 일부 실시양태에서, 중합체는 생분해성 및/또는 생체적합성일 수 있다. 나노입자는 리포솜, 미셀, 지질단백질, 지질-코팅된 기포, 블록 공중합체 미셀, 폴리머솜, 니오솜, 양자점, 산화철 입자, 금 입자, 덴드리머, 또는 실리카 입자를 포함할 수 있다. 특정 실시양태에서, 지질 단층 또는 이중층은, 지질로 코팅될 수 있는 물질로 구성된 나노입자, 예를 들어 중합체 나노입자를 완전히 또는 부분적으로 코팅할 수 있다. 일부 실시양태에서, 리포솜은 다층 소포 (MLV), 대형 단층 소포 (LUV), 및 소형 단층 소포 (SUV)를 포함할 수 있다.
본원에서 사용되는 바와 같이, 용어 "치료제"는, 유효량으로 존재하는 경우, 치료 효과를 필요로 하는 대상체에 대해 요망되는 치료 효과를 생성하는 화합물 또는 분자를 지칭한다. 본 발명에서는, 본원에서 추가로 설명되는 바와 같이, 나노입자 및 포스포네이트 컨쥬게이트와 함께 폭넓은 범위의 치료제 및 그의 용도가 고려된다.
본원에서 사용되는 바와 같이, 용어 "진단제"는 대상체 또는 시험 샘플에서 검출될 수 있는 성분을 지칭하며, 이는 본원에서 추가로 설명된다.
본원에서 사용되는 바와 같이, 용어 "연결기"는, 컨쥬게이트의 부분들을 연결하는 포스포네이트 컨쥬게이트의 부분을 지칭한다. 예를 들어, 연결기, L3은, R3 (예를 들어, 부착 성분)을, 포스포네이트 컨쥬게이트의 인에 결합된 산소에 연결시킬 수 있다. 제조되는 포스포네이트 컨쥬게이트 및 화합물에 대해 요망되는 특성에 따라, 연결기는 표적화제와 예를 들어 나노입자에 부착될 수 있는 포스포네이트 컨쥬게이트의 다른 부분의 적절한 분리를 달성하도록 용이하게 입수가능한 단량체 성분으로부터 어셈블링될 수 있다.
본원에서 사용되는 바와 같이, 용어 "표적화제"는 표적에 대해 특이적인 분자를 지칭한다. 특정 실시양태에서, 표적화제는 표적 리간드의 소분자 모방체 (예를 들어, 펩티드 모방 리간드), 표적 리간드 (예를 들어, RGD 펩티드 함유 펩티드 또는 폴레이트 아미드), 또는 특정 표적에 대해 특이적인 항체 또는 항체 단편을 포함할 수 있다. 표적화제는, 질병의 특정 발달기와 관련될 수 있는 기관, 조직, 세포, 세포외 매트릭스 성분, 및/또는 세포내 구획에서의 표적을 비롯한 폭넓게 다양한 표적에 결합할 수 있다. 일부 실시양태에서, 표적은 암 세포, 특히 암 줄기 세포를 포함할 수 있다. 표적은 세포 표면 상의 항원, 또는 암 세포에 존재하거나 정상 조직에 비해 암 세포에 더욱 널리 퍼져있는 항원인 종양 마커를 포함할 수 있다. 특정 실시양태에서, 표적화제는 폴산 유도체, B-12 유도체, 인테그린 RGD 펩티드, RGD 모방체 (문헌 [Temming, K. et al., Drug Resistance Updates 8:381-402 (2005)]; [Liu, S., Mol. Pharm. 3(5):472-87 (2006)]), NGR 유도체, 소마토스타틴 유도체 또는 소마토스타틴 수용체에 결합하는 펩티드, 예를 들어, 옥트레오티드 및 옥트레오테이트 등을 추가로 포함할 수 있다. 일부 실시양태에서, 표적화제는 앱타머 (이는 핵산 (예를 들어, DNA 또는 RNA) 또는 펩티드로 구성되고, 특정 표적에 결합함)일 수 있다. 표적화제는 수용체 표적, 특히 종양과 관련되어 발현되는 수용체 표적에 특이적으로 또는 비-특이적으로 결합하도록 디자인될 수 있다. 수용체 표적의 예는, MUC-1, EGFR, 클라우딘(Claudin) 4, MUC-4, CXCR4, CCR7, FOL1R, 소마토스타틴 수용체 4, Erb-B2 (적혈모구 백혈병 종양유전자 동족체 2) 수용체, CD44 수용체, 및 VEGF 수용체-2 키나제를 포함하나 이에 제한되지는 않는다.
본원에서 사용되는 바와 같이, 용어 "스텔스제"는 나노입자의 표면 특성을 개질시킬 수 있는 분자를 지칭하며, 이는 본원에서 추가로 설명된다.
본원에서 사용되는 바와 같이, 용어 "4-다리 제시 성분(tetrapodal presentation component)"은 하기 화학식을 갖는 분자를 지칭한다.
상기 식에서, L5, L6, R5 및 R6은 본원에서 추가로 설명된다. 일부 실시양태에서, L5 및 L6은 각각 독립적으로 결합 및 연결기로 이루어진 군으로부터 선택되고; R5 및 R6은 각각 독립적으로 C1-C36 알킬, 표적화제, 진단제, 및 스텔스제로 이루어진 군으로부터 선택된다. 일부 실시양태에서, R5 및/또는 R6은 수소일 수 있다.
본원에서 사용되는 바와 같이, 용어 "~ 내에 내포된"은 나노입자의 표면 상에 또는 그 부근에서의 작용제의 위치를 지칭한다. 나노입자 내에 내포된 작용제는, 예를 들어, 리포솜의 이중층 멤브레인 내에 위치하거나 나노입자의 외부 중합체 쉘 내에 위치하여 그 쉘 내에 함유될 수 있다.
본원에서 사용되는 바와 같이, 용어 "캡슐화된"은, 나노입자 내부에 둘러싸이거나 완전히 함유된 작용제의 위치를 지칭한다. 리포솜의 경우, 예를 들어, 치료제 및/또는 진단제는 리포좀의 수성 내부 내에 존재하도록 캡슐화될 수 있다. 이어서, 리포솜을 불안정화시키도록 의도된 특정 조건 하에 이러한 캡슐화된 작용제의 방출이 촉발되거나 다른 방식으로 캡슐화된 작용제의 방출이 수행될 수 있다.
본원에서 사용되는 바와 같이, 용어 "~에 테더링된(tethered to)"은, 하나 이상의 성분이 공간에서 이동하는 자유를 갖도록 하나의 성분이 또 다른 성분에 부착된 것을 지칭한다. 특정 예시적 실시양태에서, 부착 성분은 나노입자를 둘러싼 용액 중에서 자유롭게 이동하도록 나노입자에 테더링될 수 있다. 일부 실시양태에서, 부착 성분은 표면으로부터 멀리 연장되면서 나노입자의 표면에 테더링될 수 있다.
본원에서 사용되는 바와 같이, 용어 "지질"은 지방, 왁스, 스테롤, 콜레스테롤, 콜레스테롤 유도체, 지용성 비타민, 모노글리세리드, 디글리세리드, C8-C36 알킬, 인지질, 스핑고지질, 당지질, 양이온성 또는 음이온성 지질, 유도체화된 지질 등을 포함할 수 있는 지질 분자를 지칭한다. 지질은 미셀, 단층, 및 이중층 멤브레인을 형성할 수 있다. 특정 실시양태에서, 지질은 리포솜으로 자체-어셈블링될 수 있다. 다른 실시양태에서, 지질은 단층 또는 이중층으로서 나노입자의 표면을 코팅할 수 있다.
본원에서 사용되는 바와 같이, 용어 "앱타머"는, 특정 표적에 특이적으로 결합하는 비-천연 올리고뉴클레오티드 (전형적으로 20 내지 200개의 뉴클레오티드)를 지칭한다. "비-천연"은 천연 뉴클레오티드 (A, T, C, G, U)의 비-천연 서열, 뿐만 아니라 비-천연 또는 변형 뉴클레오티드를 갖는 올리고뉴클레오티드를 포함한다. 예를 들어, "스피에겔머스(Spiegelmers)®"는 거울 상 핵산을 갖는 (즉, 천연 D 배열 대신에 L 키랄 배열) 앱타머이다. 앱타머는 분자내 상호작용에 의해 독특한 3차원 구조를 형성할 수 있고/거나, 예를 들어 1차 또는 2차 구조로부터 유도-적합 메커니즘에 의해 표적에 결합시 구조가 변할 수 있다. 표적에 대한 앱타머 결합은, 전형적인 상보적 핵산 하이브리드형성, 예를 들어 이중 또는 삼중 나선 형성에 의해 매개되지 않는다 (앱타머의 일부가 이러한 하이브리드형성에 참여할 수는 있지만). 예를 들어, 앱타머는 통상적으로 분자내 헤어핀 구조 및 다른 3차원 구조를 형성한다. 앱타머는 임의의 방법 또는 방법의 조합에 따라 선택될 수 있다. 기하급수적 농축에 의한 리간드의 계통 진화(Systematic Evolution of Ligands by Exponential Enrichment (셀렉스(SELEX)™), 또는 이들의 변형이 업계에서 통상적으로 사용된다. 기본적 셀렉스™ 공정은, 예를 들어 US 특허 번호 5,567,588에 기재되어 있다. 기본적 방법에 대한 다수의 변화가 또한 이용될 수 있다 (예를 들어, US 특허출원 번호 2010015041에 기재된 바와 같은 생체내 셀렉스™). 모노렉스(MONOLEX)™은, 예를 들어 문헌 [Nitsche et al. (2007) BMC Biotechnology 7:48] 및 WO02/29093에 기재된 또 다른 선택 공정이다. 종양 세포로 주입된 핵산 라이브러리를 사용한 생체내 선택 또한 가능하다 (예를 들어, 문헌 [Mi et al., (2010) Nat. Chem. Biol. 1:22] 참조). 본 발명에서 사용하기 위한 앱타머는, MUC-1, EGFR, 클라우딘 4, MUC-4, CXCR4, CCR7, FOL1R, 소마토스타틴 수용체 4, Erb-B2 (적혈모구 백혈병 종양유전자 동족체 2) 수용체, CD44 수용체, VEGF 수용체-2 키나제, 및 뉴클레올린을 포함하나 이에 제한되지는 않는 다양한 표적에 결합하도록 디자인될 수 있다.
본원에서 사용되는 바와 같이, 용어 "대상체"는 임의의 생명 단계의 임의의 포유동물, 특히 인간을 지칭한다.
본원에서 사용되는 바와 같이, 용어 "투여하다", "투여된", 또는 "투여하는"은 본 발명의 표적화된 전달 조성물의 투여 방법을 지칭한다. 본 발명의 표적화된 전달 조성물은 다양한 방식으로, 예컨대 국소, 비경구, 정맥내, 피부내, 근육내, 결장, 직장 또는 복강내 투여될 수 있다. 비경구 투여 및 정맥내 투여가 바람직한 투여 방법이다. 표적화된 전달 조성물은 또한 조성물 또는 제제의 일부로서 투여될 수 있다.
본원에서 사용되는 바와 같이, 질환, 질병, 장애, 또는 증후군을 "치료하는" 또는 이들의 "치료"라는 용어는, (i) 질병, 장애, 또는 증후군의 억제, 즉, 그의 발달 저지; 및 (ii) 질병, 장애, 또는 증후군의 경감, 즉 질병, 장애, 또는 증후군의 퇴행 유발을 포함한다. 당업계에 공지된 바와 같이, 전신 전달 대 국소 전달, 연령, 체중, 일반적 건강상태, 성별, 식습관, 투여 시간, 약물 상호작용 및 질환의 중증도에 대한 조정이 필수적일 수 있고, 이는 당업자에 의해 통상적인 실험에 의해 확인가능하다.
본원에서 사용되는 바와 같이, 용어 "제제"는 대상체로의 투여를 위한 성분들의 혼합물을 지칭한다. 예를 들어 관절내 (관절 내로), 정맥내, 근육내, 종양내, 피부내, 복강내, 및 피하 경로 투여와 같은 비경구 투여에 적합한 제제는, 산화방지제, 완충제, 정균제, 및 제제가 의도된 수용자의 혈액과 등장성이 되도록 하는 용질을 함유할 수 있는 수성 및 비-수성 등장성 멸균 주사액, 및 현탁화제, 가용화제, 증점제, 안정화제, 및 보존제를 포함할 수 있는 수성 및 비-수성 멸균 현탁액을 포함한다. 주사액 및 현탁액은 또한 멸균 분말, 과립 및 정제로부터 제조될 수 있다. 표적화된 전달 조성물의 제제는 단위-용량 또는 다중-용량 밀봉 용기, 예컨대 앰풀 및 바이알 중에 존재할 수 있다. 표적화된 전달 조성물은, 단독으로 또는 다른 적합한 성분과 조합되어, 구강 또는 비강을 통해 흡입에 의해 투여되는 에어로졸 제제를 형성할 수 있다 (즉, 이들은 "분무"될 수 있음). 에어로졸 제제는 가압 허용가능한 추진제, 예컨대 디클로로디플루오로메탄, 프로판, 질소 등 내에 배치될 수 있다. 직장 투여에 적합한 제제는, 예를 들어, 좌제 베이스와 함께 유효량의 표적화된 전달 조성물을 포함하는 좌제를 포함한다. 적합한 좌제 베이스는 천연 또는 합성 트리글리세리드 또는 파라핀 탄화수소를 포함한다. 또한, 예를 들어, 액체 트리글리세리드, 폴리에틸렌 글리콜, 및 파라핀 탄화수소를 포함한 베이스와 표적화된 전달 조성물의 조합을 함유하는 젤라틴 직장 캡슐을 사용할 수도 있다. 특정 실시양태에서, 제제는 국소 투여되거나 점안약 형태로 투여될 수 있다.
본 발명의 실시양태
II. 일반적 설명
본 발명의 포스포네이트 컨쥬게이트 및 그의 제조 방법은, 약물 전달 및 진단 영상 분야에 대해 수많은 독특한 측면을 제공한다. 예를 들어, 본 발명은, 표적화된 약물 전달에 사용될 수 있는 스텔스 나노입자로의 나노입자의 변형을 용이하게 할 수 있는 화합물의 강력하고 간단한 제조 방법을 제공한다. 특정 경우에, 포스포네이트 컨쥬게이트는 나노입자 표면 상의 스텔스제의 밀도를 증가시키는 독특한 능력을 제공하고, 따라서 보다 저밀도에서는 효과적이지 않을 수 있는 다양한 스텔스제를 사용하는 데 있어 추가의 유연성을 가능하게 할 수 있다. 또한, 포스포네이트 컨쥬게이트가, 나노입자 표면 상의 스텔스제 또는 다른 성분, 예를 들어 표적화제를 제시하도록 추가의 안정성을 제공하는 방식으로 제조될 수 있다.
또한, 포스포네이트 화합물은 다양한 방식으로 나노입자로 통합될 수 있다. 예를 들어, H-포스포네이트 화합물을 본원에 기재된 방법을 이용하여 제조하고, 이어서 이를 H-포스포네이트 화합물이 나노입자의 표면 상에 존재하도록 나노입자와 통합할 수 있다. H-포스포네이트 화합물은, 예를 들어, 나노입자 제조 전에 H-포스포네이트 화합물을 도입함으로써 나노입자와 통합될 수 있다. 다른 경우에는, 나노입자를 제조할 수 있고, H-포스포네이트 화합물을 나노입자의 표면에 부착시킴으로써 나노입자의 표면을 개질시킬 수 있다. 개질된 나노입자의 제조에 있어 유연성은, 예를 들어, 환자에게 투여된 후 긴 생체내 반감기를 가질 수 있는 특정 치료 및/또는 진단 용도에 대해 맞춤화된 나노입자를 가능하게 할 수 있다.
III. 포스포네이트 컨쥬게이트
하나의 측면에서, 본 발명의 화합물은 하기 화학식의 화합물을 포함할 수 있다.
상기 식에서, L1, L2, L3 및 L4는 각각 독립적으로 결합 및 연결기로 이루어진 군으로부터 선택되고; R1은 나노입자, 부착 성분, 표적화제, 진단제, 스텔스제, 및 4-다리 제시 성분으로 이루어진 군으로부터 선택되고; R2는 각각 독립적으로 스텔스제, C1-C10 알킬, 카르복실산 또는 에스테르, 포스폰산 또는 에스테르, 술폰산 또는 에스테르, 및 히드록시로 이루어진 군으로부터 선택되고; R3 및 R4는 각각 독립적으로 H, 나노입자, 부착 성분, 표적화제, 진단제, 및 스텔스제로 이루어진 군으로부터 선택되고, 여기서 R3 또는 R4 중 적어도 하나는 H 이외의 것이고; n은 0 내지 2의 정수이다.
또 다른 측면에서, 본 발명의 화합물은 하기 화학식의 화합물을 포함할 수 있다.
상기 식에서, L1, L2, L3 및 L4는 각각 독립적으로 결합 및 연결기로 이루어진 군으로부터 선택되고; R1은 나노입자, 부착 성분, 표적화제, 진단제 및 스텔스제로 이루어진 군으로부터 선택되고; R2는 독립적으로 스텔스제, C1-C10 알킬, 카르복실산 또는 에스테르, 포스폰산 또는 에스테르, 술폰산 또는 에스테르, 및 히드록시로 이루어진 군으로부터 선택되고; R3 및 R4는 각각 독립적으로 H, 나노입자, 부착 성분, 표적화제, 진단제, 및 스텔스제로 이루어진 군으로부터 선택되고, 여기서 R3 또는 R4 중 적어도 하나는 H 이외의 것이고; R9는 C1-C10 알킬 기이고; n은 0 내지 2의 정수이다.
나노입자
폭넓게 다양한 나노입자가 본 발명에서 사용될 수 있다. 당업자가 인지하는 바와 같이, 나노입자의 특징, 예를 들어, 크기는, 나노입자의 유형 및/또는 용도 뿐만 아니라 당업계에 일반적으로 널리 공지되어 있는 다른 요인에 따라 달라질 수 있다. 적합한 입자는 구형, 회전타원체형, 평면형, 판-형상, 관형, 입방체형, 직육면체형, 계란형, 타원형, 원통형, 원뿔형, 또는 각뿔형일 수 있다. 적합한 나노입자는 약 1 nm 내지 약 1000 nm, 약 10 nm 내지 약 200 nm, 및 약 50 nm 내지 약 150 nm의 최대 치수 (예를 들어, 직경)의 크기 범위를 가질 수 있다.
적합한 나노입자는 당업계에 일반적으로 공지되어 있는 다양한 물질로 제조될 수 있다. 일부 실시양태에서, 나노입자는 지질, 중합체, 또는 금속 물질, 예컨대 실리카, 금, 산화철 등을 비롯한 각종 물질 중 하나의 물질, 또는 이들의 임의의 조합을 포함할 수 있다. 나노입자의 예는 리포솜, 미셀, 지질단백질, 지질-코팅된 기포, 블록 공중합체 미셀, 폴리머솜, 니오솜, 산화철 입자, 금 입자, 실리카 입자, 덴드리머, 또는 양자점을 포함할 수 있으나 이에 제한되지는 않는다.
일부 실시양태에서, 나노입자는 부분적으로 또는 전체적으로 포화 또는 불포화된 지질로 구성된 리포솜이다. 적합한 지질은 지방, 왁스, 스테롤, 콜레스테롤, 콜레스테롤 유도체, 지용성 비타민, 모노글리세리드, 디글리세리드, 인지질, 스핑고지질, 당지질, 유도체화된 지질 등을 포함할 수 있으나 이에 제한되지는 않는다. 일부 실시양태에서, 적합한 지질은 양친매성, 중성, 비-양이온성, 음이온성, 양이온성, 또는 소수성 지질을 포함할 수 있다. 특정 실시양태에서, 지질은 인지질 및/또는 스핑고지질과 같은, 전형적으로 세포 막 중에 존재하는 것들을 포함할 수 있다. 적합한 인지질은 포스파티딜콜린 (PC), 포스파티드산 (PA), 포스파티딜에탄올아민 (PE), 포스파티딜글리세롤 (PG), 포스파티딜세린 (PS), 및 포스파티딜이노시톨 (PI)을 포함하나 이에 제한되지는 않는다. 적합한 스핑고지질은 스핑고신, 세라미드, 스핑고미엘린, 세레브로시드, 술파티드, 강글리오시드, 및 피토스핑고신을 포함하나 이에 제한되지는 않는다. 다른 적합한 지질은 지질 추출물, 예컨대 에그 PC, 심장 추출물, 뇌 추출물, 간 추출물, 및 소이 PC를 포함할 수 있다. 일부 실시양태에서, 소이 PC는 히드로 소이(Hydro Soy) PC (HSPC)를 포함할 수 있다. 양이온성 지질은 N,N-디올레오일-N,N-디메틸암모늄 클로라이드 (DODAC), N,N-디스테아릴-N,N-디메틸암모늄 브로마이드 (DDAB), N-(1-(2,3-디올레오일옥시)프로필)-N,N,N-트리메틸암모늄 클로라이드 (DOTAP), N-(1-(2,3-디올레일옥시)프로필)-N,N,N-트리메틸암모늄 클로라이드 (DOTMA), 및 N,N-디메틸-2,3-디올레일옥시)프로필아민 (DODMA)을 포함하나 이에 제한되지는 않는다. 비-양이온성 지질은 디미리스토일 포스파티딜 콜린 (DMPC), 디스테아로일 포스파티딜 콜린 (DSPC), 디올레오일 포스파티딜 콜린 (DOPC), 디팔미토일 포스파티딜 콜린 (DPPC), 디미리스토일 포스파티딜 글리세롤 (DMPG), 디스테아로일 포스파티딜 글리세롤 (DSPG), 디올레오일 포스파티딜 글리세롤 (DOPG), 디팔미토일 포스파티딜 글리세롤 (DPPG), 디미리스토일 포스파티딜 세린 (DMPS), 디스테아로일 포스파티딜 세린 (DSPS), 디올레오일 포스파티딜 세린 (DOPS), 디팔미토일 포스파티딜 세린 (DPPS), 디올레오일 포스파티딜 에탄올아민 (DOPE), 팔미토일올레오일포스파티딜콜린 (POPC), 팔미토일올레오일-포스파티딜에탄올아민 (POPE) 및 디올레오일-포스파티딜에탄올아민 4-(N-말레이미도메틸)-시클로헥산-1-카르복실레이트 (DOPE-mal), 디팔미토일 포스파티딜 에탄올아민 (DPPE), 디미리스토일포스포에탄올아민 (DMPE), 디스테아로일-포스파티딜-에탄올아민 (DSPE), 16-O-모노메틸 PE, 16-O-디메틸 PE, 18-1-트랜스 PE, 1-스테아로일-2-올레오일-포스파티딜에탄올아민 (SOPE), 1,2-디엘라이도일-sn-글리세로-3-포스포에탄올아민 (트랜스DOPE), 및 카디올리핀을 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, 지질은 유도체화된 지질, 예컨대 페길화된(PEGlyated) 지질을 포함할 수 있다. 유도체화된 지질은, 예를 들어, DSPE-PEG2000, 콜레스테롤-PEG2000, DSPE-폴리글리세롤, 또는 당업계에 일반적으로 널리 공지되어 있는 다른 유도체를 포함할 수 있다.
지질의 임의의 조합을 사용하여 나노입자, 예컨대 리포솜을 구성할 수 있다. 특정 실시양태에서, 리포솜의 지질 조성물은 누출률, 안정성, 입자 크기, 제타 전위, 단백질 결합, 생체내 순환, 및/또는 종양, 간, 비장 등과 같은 조직 내 축적과 같은 리포솜의 특징에 영향을 주도록 맞춤화될 수 있다. 예를 들어, DSPC 및/또는 콜레스테롤을 사용하여 리포솜으로부터의 누출을 감소시킬 수 있다. 리포솜의 표면 전하에 영향을 주도록 DSPG 및/또는 DOTAP와 같은 음의 또는 양의 지질이 포함될 수 있다. 일부 실시양태에서, 리포솜은 약 10개 이하의 유형의 지질, 또는 약 5개 이하의 유형의 지질, 또는 약 3개 이하의 유형의 지질을 포함할 수 있다. 일부 실시양태에서, 존재하는 특정 유형의 지질의 몰 퍼센트 (mol%)는 전형적으로, 나노입자, 예컨대 리포솜 중에 존재하는 총 지질의 약 0% 내지 약 10%, 약 10% 내지 약 30%, 약 30% 내지 약 50%, 약 50% 내지 약 70%, 약 70% 내지 약 90%, 약 90% 내지 100%를 이룬다. 본원에 기재된 지질은 리포솜 내에 포함될 수 있거나, 또는 지질은 본 발명의 나노입자, 예컨대 중합체 나노입자를 코팅하는 데 사용될 수 있다. 코팅은 부분적으로 또는 전체적으로 나노입자를 둘러쌀 수 있고 단층 및/또는 이중층을 포함할 수 있다.
다른 실시양태에서, 나노입자의 일부 또는 전부는 중합체, 예컨대 블록 공중합체 또는 나노입자 제조에 대해 당업계에 공지되어 있는 다른 중합체를 포함할 수 있다. 일부 실시양태에서, 중합체는 생분해성 및/또는 생체적합성일 수 있다. 적합한 중합체는 폴리에틸렌, 폴리카르보네이트, 폴리안히드라이드, 폴리히드록시산, 폴리프로필푸마레이트, 폴리카프로락톤, 폴리아미드, 폴리아세탈, 폴리에테르, 폴리에스테르, 폴리(오르토에스테르), 폴리시아노아크릴레이트, 폴리비닐 알콜, 폴리우레탄, 폴리포스파젠, 폴리아크릴레이트, 폴리메타크릴레이트, 폴리시아노아크릴레이트, 폴리우레아, 폴리스티렌, 폴리아민, 및 이들의 조합을 포함할 수 있으나 이에 제한되지는 않는다. 일부 실시양태에서, 입자의 예는 쉘 가교된 크네델(knedel)을 포함할 수 있으며, 이는 참고문헌: 미국 특허출원 번호 11/250830 (Becker et al.); [Thurmond, K.B. et al., J. Am. Chem. Soc., 119 (28) 6656 (1997)]; [Wooley, K.L., Chem. Eur. J., 3 (9): 1397-1399 (1997)]; [Wooley, K.L., J. Poly. Sci.: Part A: Polymer Chem., 38: 1397-1407 (2000)]에 추가로 설명되어 있다. 다른 실시양태에서, 적합한 입자는 폴리(락트 코-글리콜산) (PLGA)을 포함할 수 있다 (문헌 [Fu, K. et al., Pharm Res., 27:100-106 (2000)]).
또한 다른 실시양태에서, 나노입자는 부분적으로 또는 전체적으로 실리카, 금, 산화철 등의 금속 성질을 갖는 물질로 구성될 수 있다. 일부 실시양태에서, 실리카 입자는 중공형, 다공성, 및/또는 메조다공성일 수 있다 (문헌 [Slowing, I.I., et al., Adv. Drug Deliv. Rev., 60 (11):1278-1288 (2008)]). 금 입자는, 예시적 참고문헌: 문헌 [Bhattacharya, R. & Mukherjee, P., Adv. Drug Deliv. Rev., 60(11): 1289-1306 (2008)]에 제공된 바와 같이, 당업계에 일반적으로 공지되어 있다. 산화철 입자 또는 양자점이 또한 사용될 수 있고, 이들은 당업계에 널리 공지되어 있다 (문헌 [van Vlerken, L.E. & Amiji, M. M., Expert Opin. Drug Deliv., 3(2): 205-216 (2006)]). 나노입자는 또한 바이러스 입자 및 세라믹 입자를 포함하나 이에 제한되지는 않는다.
나노입자에 대한 부착
특정 실시양태에서, 부착 성분은, 부착 성분을 나노입자 상에 존재하는 반응성 기에 공유결합으로 부착시키는 데 사용될 수 있는 관능기를 포함할 수 있다. 관능기는, 예를 들어 알킬렌 또는 헤테로알킬렌 모이어티의 말단 위치와 같은, 부착 성분 상의 어디에도 위치할 수 있다. 폭넓게 다양한 관능기가 당업계에 일반적으로 공지되어 있고, 이들은 친핵성 치환 (예를 들어, 아민 및 알콜과 아실 할라이드 또는 활성 에스테르의 반응), 친전자성 치환 (예를 들어, 엔아민 반응) 및 탄소-탄소 및 탄소-헤테로원자 다중 결합에 대한 부가반응 (예를 들어, 마이클(Michael) 반응 또는 딜스-알더(Diels-Alder) 부가반응)과 같은 (이에 제한되지는 않음) 여러 부류의 반응 하에 반응할 수 있다. 이들 및 다른 유용한 반응은, 예를 들어, 문헌 [March, Advanced Organic Chemistry, 3rd Ed., John Wiley & Sons, New York, 1985]; 및 [Hermanson, Bioconjugate Techniques, Academic Press, San Diego, 1996]에서 논의되어 있다. 적합한 관능기는, 예를 들어: (a) 카르복실 기 및 그의 각종 유도체, 예컨대 N-히드록시숙신이미드 에스테르, N-히드록시벤즈트리아졸 에스테르, 산 할라이드, 아실 이미다졸, 티오에스테르, p-니트로페닐 에스테르, 알킬, 알케닐, 알키닐 및 방향족 에스테르 (이에 제한되지는 않음); (b) 에스테르, 에테르, 알데히드 등으로 전환될 수 있는 히드록실 기; (c) 할로알킬 기 (여기서, 할라이드는 이후에, 예를 들어 아민, 카르복실레이트 음이온, 티올 음이온, 탄소 음이온, 또는 알콕시드 이온 등의 친핵성 기로 치환될 수 있고, 이로써 할로겐 원자의 부위에 새로운 기의 공유결합 부착이 생김); (d) 예를 들어 말레이미도 기 등의 딜스-알더 반응에 참여할 수 있는 친디엔체 기; (e) 예를 들어 이민, 히드라존, 세미카르바존 또는 옥심 등의 카르보닐 유도체의 형성에 의해, 또는 그리냐르(Grignard) 부가반응 또는 알킬리튬 부가반응 등의 반응에 의해 후속 유도체화가 가능한 알데히드 또는 케톤 기; (f) 예를 들어 술폰아미드를 형성하는 아민과의 후속 반응을 위한 술포닐 할라이드 기; (g) 디술피드로 전환되거나 아실 할라이드와 반응할 수 있는 티올 기; (h) 예를 들어 아실화, 알킬화 또는 산화될 수 있는 아민 또는 술프히드릴 기; (i) 예를 들어 고리화부가반응, 아실화, 마이클 부가반응 등이 일어날 수 있는 알켄; 및 (j) 예를 들어 아민 및 히드록실 화합물과 반응할 수 있는 에폭시드를 포함할 수 있다. 일부 실시양태에서는, 클릭 화학에 기초한 플랫폼을 이용하여 부착 성분을 나노입자에 부착시킬 수 있다 (문헌 [Kolb, H.C., M. G. Finn and K. B. Sharpless, Angew. Chem. Int'l. Ed. 40 (11): 2004 (2001)]). 일부 실시양태에서, 부착 성분은 하나의 관능기 또는 나노입자와의 다수의 공유 결합을 형성하는 다수의 관능기를 포함할 수 있다.
표 1은 본 발명에서 사용될 수 있는 관능기의 추가의 비-제한적 대표적 목록을 제공한다.
다른 실시양태에서, 부착 성분은, 친화성 상호작용, 금속 배위, 물리적 흡착, 소수성 상호작용, 반 데르 발스 상호작용, 수소 결합 상호작용, 자기 상호작용, 정전기 상호작용, 쌍극자-쌍극자 상호작용, 항체-결합 상호작용, 상보적 DNA 사이의 하이브리드형성 상호작용 등을 포함할 수 있으나 이에 제한되지는 않는 비-공유결합 상호작용에 의해 나노입자에 부착될 수 있다. 일부 실시양태에서, 부착 성분은, 예를 들어, 나노입자 내에 도입되는 지질 또는 인지질일 수 있다. 특정 실시양태에서, 지질 또는 인지질은 나노입자의 지질 이중층 부분에 존재할 수 있고, 여기서 특정 실시양태에서 나노입자는 리포솜이다. 예를 들어, 부착 성분은, 지질 이중층의 소수성 및/또는 친수성 영역과 부분적으로 또는 전체적으로 상호작용하는 지질 또는 인지질 (예를 들어, 포화 또는 불포화될 수 있는 C8-C36 알킬)일 수 있다. 일부 실시양태에서, 부착 성분은 나노입자와의 비-공유결합 상호작용을 가능하게 하는 하나의 기를 포함할 수 있지만, 다수의 기 또한 고려된다. 예를 들어, 다수의 이온 전하를 이용하여 부착 성분과 나노입자 사이의 충분한 비-공유결합 상호작용을 생성시킬 수 있다. 대안적 실시양태에서, 부착 성분은, 다수의 지질이 리포솜의 이중층 멤브레인 또는 나노입자 상에 코팅된 이중층 또는 단층과 상호작용하도록 다수의 지질을 포함할 수 있다. 특정 실시양태에서는, 주위 용액 조건을 변화시켜 비-공유결합 상호작용을 붕괴시킴으로써 나노입자로부터 부착 성분을 탈착시킬 수 있다.
본원에서 추가로 설명되는 바와 같이, 본 발명의 화합물의 일부는 R1, R2, R3, R4, R5 및/또는 R6을 부착 성분으로서 포함할 수 있다. 일부 실시양태에서, 부착 성분은 페닐 기, 콜레스테롤, 또는 지질, 예컨대 포화 또는 불포화 C10-C24 알킬기 또는 치환된 포화 또는 불포화 C10-C24 알킬 기를 포함할 수 있다. 특정 예시적 실시양태에서, 부착 성분은 부착 성분과 지질 이중층의 회합을 용이하게 하도록 선택될 수 있다. 예를 들어, 이중 결합의 길이, 부위 및 기하구조 및/또는 알킬 기의 치환은, 예를 들어 표적화제 및/또는 스텔스제와 같은 다른 성분의 제시에 의한 리포솜의 표면 특성 개질을 가능하게 하기 위해 지질 이중층에 요망되는 도입 수준을 제공하도록 선택될 수 있다.
일부 실시양태에서, 포스포네이트 컨쥬게이트는 연결기, L1, L2, L3, L4, L5 및/또는 L6에 의해 나노입자에 직접 부착될 수 있다. 이들 실시양태에서, R1, R3, R4, 및/또는 R6은 나노입자일 수 있다. 다른 실시양태에서, R1은 부착 성분이고, 부착 성분은 인지질이다. R1이 인지질인 일부 실시양태에서, 인지질은 하기 화학식을 갖는다.
상기 식에서, R7 및 R8은 각각 독립적으로 포화 또는 불포화 C10-24 알킬 또는 알카노일 기 및 치환된 포화 또는 불포화 C10-24 알킬 또는 알카노일 기로부터 선택된다. 특정 실시양태에서, R7 및 R8은 각각 독립적으로 포화 또는 불포화 C10 -18 알킬 또는 알카노일 기 및 치환된 포화 또는 불포화 C10 -18 알킬 또는 알카노일 기로부터 선택된다. 적합한 알카노일 기는 데카노일, 운데카노일, 라우로일, 트리데카노일, 미리스토일, 펜타데카노일, 팔미토일, 헵타데카노일, 스테아로일, 노나데카노일, 아라키도일 등을 포함하나 이에 제한되지는 않는다. 당업계에 일반적으로 공지되어 있고 본원에 기재된 다른 인지질이 사용될 수도 있다.
일부 실시양태에서, 포스포네이트 컨쥬게이트는 나노입자의 표면 특징 (예를 들어, 친수성 또는 소수성 특징)을 개질시키도록 제조될 수 있다. 예를 들어, 양으로 및 음으로 대전된 기가 컨쥬게이트 내에 포함되고 나노입자에 추가로 도입될 수 있다. 특정 실시양태에서는, 산성 기가 컨쥬게이트 내에 포함되어 리포솜의 표면 상에 음전하를 도입시킬 수 있다. 본원에서 제공된 바와 같이, 본 발명의 컨쥬게이트는 표면 특징을 개질시키기 위해 사용될 수 있는 [L2-R2]n 기를 포함할 수 있다. n은 0, 1 또는 2의 정수일 수 있다. 일부 실시양태에서, L2는 결합 또는 연결기일 수 있다. R2는 스텔스제, C1-C10 알킬, 카르복실산 또는 에스테르, 포스폰산 또는 에스테르, 술폰산 또는 에스테르, 또는 히드록시를 포함할 수 있으나 이에 제한되지는 않는다.
연결기
연결기는 본 발명의 포스포네이트 컨쥬게이트의 또 다른 특징이다. 당업자는 다양한 연결기가 당업계에 공지되어 있고, 예를 들어 참고문헌 [Hermanson, G.T., Bioconjugate Techniques, 2nd Ed., Academic Press, Inc. (2008)]에서 찾아볼 수 있다는 것을 인지할 수 있다. 본 발명의 연결기를 이용하여, 화합물의 상이한 부분들 사이에 간격을 제공하는 등 화합물에 추가의 특성을 제공할 수 있다. 이러한 간격은, 예를 들어, 나노입자에 의해 발생되는 입체 장애 문제를 극복하기 위해 이용될 수 있다 (예를 들어, 나노입자로부터 일정 거리 떨어져 있는 표적화제가 표적에 결합될 수 있는 경우). 일부 실시양태에서, 연결기는 화합물의 물리적 특성을 변화시키는 데 사용될 수 있다.
일부 실시양태에서, 본 발명의 포스포네이트 컨쥬게이트는 L1, L2, L3, L4, L5 및 L6 (이들은 각각 독립적으로 연결기 또는 결합일 수 있음)을 포함한다. 특정 실시양태에서, L1, L2, L3, L4, L5 및 L6은 각각 독립적으로 친수성의 비-면역원성 수용성 연결기가 되도록 선택될 수 있다. 본 발명의 친수성의 비-면역원성 수용성 연결기는 폴리에틸렌 글리콜, 폴리프로필렌 글리콜, 폴리비닐 알콜, 폴리카르복실레이트, 폴리사카라이드, 및 덱스트란을 포함할 수 있으나 이에 제한되지는 않는다. 당업자는 연결기의 길이 및/또는 화학적 특성이 특정 용도를 위해, 예컨대 상기에서 논의된 바와 같은 간격을 고려하여 선택될 수 있음을 인지할 것이다.
다른 실시양태에서, 연결기는, 예를 들어, C1-30 알킬렌 연결기 또는 유사한 헤테로알킬렌 연결기 (탄소 사슬에 O, N 및 S로부터 선택된 1 내지 10개의 헤테로원자가 개재된 알킬렌 연결기)일 수 있다. 다르게는, 일부 실시양태에서, 연결기는 아릴 모이어티, 예컨대 페닐렌 고리 또는 헤테로아릴 대응물을 포함할 수 있다. 또한 다른 실시양태에서, 연결기는 아미도, 아미노, 케토, 및 히드록실 기로 치환된 알킬렌 또는 헤테로알킬렌 연결기를 포함할 수 있다.
스텔스제
일부 실시양태에서, 포스포네이트 컨쥬게이트는 하나 이상의 스텔스제를 포함할 수 있다. 예를 들어, 특정 실시양태에서, R1, R2, R3, R4, R5 및 R6은 독립적으로 스텔스제가 되도록 선택될 수 있다. 스텔스제는 나노입자가 서로, 또한 혈액 세포 또는 관 벽에 점착되는 것을 막을 수 있다. 특정 실시양태에서, 스텔스 나노입자, 예를 들어, 스텔스 리포솜은, 나노입자가 대상체에 투여될 때 면역원성 및/또는 반응원성을 감소시킬 수 있다. 스텔스제는 또한 대상체 내에서의 나노입자의 혈액 순환 시간을 증가시킬 수 있다. 일부 실시양태에서, 나노입자는, 예를 들어, 나노입자가 부분적으로 또는 완전히 스텔스제로 구성되도록, 또는 나노입자가 스텔스제로 코팅되도록, 스텔스제를 포함할 수 있다. 본 발명에서 사용하기 위한 스텔스제는 당업계에 일반적으로 널리 공지되어 있는 것들을 포함할 수 있다. 적합한 스텔스제는 덴드리머, 폴리알킬렌 옥시드, 폴리에틸렌 글리콜, 폴리비닐 알콜, 폴리카르복실레이트, 폴리사카라이드, 및/또는 히드록시알킬 전분을 포함할 수 있으나 이에 제한되지는 않는다. 스텔스제는, 부착 성분과 관련하여 상기에 기재된 바와 같이, 공유결합 및/또는 비-공유결합 부착을 통해 본 발명의 포스포네이트 컨쥬게이트에 부착될 수 있다.
특정 실시양태에서, 스텔스제는, 당업계에 널리 공지되어 있으며 일반적으로 에틸렌 옥시드의 올리고머 또는 중합체를 지칭하는 "폴리에틸렌 글리콜" 등의 폴리알킬렌 옥시드를 포함할 수 있다. 폴리에틸렌 글리콜 (PEG)은 선형 또는 분지형일 수 있고, 여기서 분지형 PEG 분자는 중심 코어로부터 유래된 추가의 PEG 분자를 가질 수 있고/거나 다수의 PEG 분자가 중합체 주쇄에 그래프팅될 수 있다. 당업계에서 이해되는 바와 같이, 폴리에틸렌 글리콜은, PEG의 유형을 식별하는 데 사용될 수 있는 분자량들의 분포로서 생성될 수 있다. 예를 들어, PEG500은, 당업계에 일반적으로 공지되어 있는 방법에 의해 측정시, ~500 g/mol의 평균 분자량을 갖는 PEG 분자의 분포로 식별된다. 다르게는, PEG는 하기 화학식으로 표시될 수 있다: H-[O-(CH2)2]m-OH (여기서, m은 중합체 내에 존재하는 단량체의 수임 (예를 들어, m은 1 내지 200의 범위일 수 있음)). 예를 들어, PEG100의 분포에 있어, 이는 m이 2인 PEG 중합체를 포함할 수 있다. 또 다른 예로, PEG1000은 m이 23인 PEG 분자를 포함할 수 있다. 다르게는, PEG5000은 m이 114인 PEG 분자를 포함할 수 있다.
특정 실시양태에서, PEG는 저분자량 또는 고분자량 PEG, 예를 들어, PEG100, PEG500, PEG2000, PEG3400, PEG5000, PEG10000, 또는 PEG20000을 포함할 수 있다. 일부 실시양태에서, PEG는 PEG100 내지 PEG10000, 또는 PEG1000 내지 PEG10000, 또는 PEG1000 내지 PEG5000의 범위일 수 있다. 특정 실시양태에서, 스텔스제는 PEG500, PEG1000, PEG2000, 또는 PEG5000일 수 있다. 특정 실시양태에서, PEG는 메틸 에테르, 알콜, 또는 카르복실산으로 종결될 수 있다. 특정 실시양태에서, 스텔스제는 각각 연결기와 함께 연결된 2개 이상의 PEG 분자를 포함할 수 있다. 연결기는 상기에 기재된 것들, 예를 들어 아미드 연결을 포함할 수 있다. 일부 실시양태에서는, 페길화-지질이, 나노입자를 "스텔스"로 만들기에 충분한 양으로 나노입자, 예를 들어 리포솜의 이중층 내에 존재하며, 여기서 스텔스 나노입자는 감소된 면역원성을 나타낸다.
치료제
일부 실시양태에서, 본 발명의 화합물은 치료제, 진단제, 또는 이들의 조합을 포함할 수 있다. 특정 실시양태에서, 치료제 및/또는 진단제는 본 발명의 포스포네이트 컨쥬게이트와 직접 회합될 수 있다. 예를 들어, 치료제 및/또는 진단제는 포스포네이트 컨쥬게이트에 공유결합 부착될 수 있다. 다른 실시양태에서, 치료제 및/또는 진단제는 본 발명의 포스포네이트 컨쥬게이트와 회합된 나노입자 내에, 그 위에, 또는 그 주위에 어디에도 존재할 수 있다. 일부 실시양태에서, 치료제 및/또는 진단제는 나노입자 내에 내포되거나 캡슐화되거나, 또는 그에 테더링될 수 있다. 특정 실시양태에서, 나노입자는 리포솜이고, 진단 및/또는 치료제는 리포솜 내에 캡슐화된다.
본 발명에서 사용되는 치료제는 대상체에서의 질환을 치료하도록 지향되는 임의의 작용제를 포함할 수 있다. 일반적으로, 미국 약전 (U.S.P.), 문헌 [Goodman and Gilman's The Pharmacological Basis of Therapeutics, 10th Ed., McGraw Hill, 2001]; [Katzung, Ed., Basic and Clinical Pharmacology, McGraw-Hill/Appleton & Lange, 8th ed., September 21, 2000]; [Physician's Desk Reference (Thomson Publishing; and/or The Merck Manual of Diagnosis and Therapy, 18th ed., 2006, Beers and Berkow, Eds., Merck Publishing Group]; 또는 동물의 경우, 문헌 [The Merck Veterinary Manual, 9th ed., Kahn Ed., Merck Publishing Group, 2005] (이들 모두 본원에 참조로 도입됨)에 기재된 치료제를 포함하나 이에 제한되지는 않는 당업계에 공지된 임의의 치료제가 사용될 수 있다.
치료제는 치료가 요망되는 질병의 유형에 따라 선택될 수 있다. 예를 들어, 특정 유형의 암 또는 종양, 예컨대 암종, 육종, 백혈병, 림프종, 골수종, 및 중추 신경계 암 뿐만 아니라 충실성 종양 및 혼합 종양이 동일한 또는 가능하게는 상이한 치료제의 투여에 관여될 수 있다. 특정 실시양태에서, 치료제는 대상체에서의 암 질환을 치료하거나 그에 영향을 주기 위해 전달될 수 있고, 이는 화학치료제, 예컨대 알킬화제, 항대사물질, 안트라사이클린, 알칼로이드, 토포이소머라제 억제제, 및 다른 항암제를 포함할 수 있다. 일부 실시양태에서, 치료제는 안티센스제, 마이크로RNA, siRNA 및/또는 shRNA제를 포함할 수 있다.
일부 실시양태에서, 치료제는 아바스틴, 독소루비신, 시스플라틴, 옥살리플라틴, 카르보플라틴, 5-플루오로우라실, 겜시티빈 또는 탁산, 예컨대 파클리탁셀 및 도세탁셀을 포함하나 이에 제한되지는 않는 항암제 또는 세포독성제를 포함할 수 있다. 추가의 항암제는, 20-epi-1,25 디히드록시비타민 D3,4-이포메아놀, 5-에티닐우라실, 9-디히드로탁솔, 아비라테론, 아시비신, 아클라루비신, 아코다졸 히드로클로라이드, 아크로닌, 아실풀벤, 아데시페놀, 아도젤레신, 알데스류킨, all-tk 길항제, 알트레타민, 암바무스틴, 암보마이신, 아메탄트론 아세테이트, 아미독스, 아미포스틴, 아미노글루테티미드, 아미노레불린산, 암루비신, 암사크린, 아나그렐리드, 아나스트로졸, 안드로그라폴리드, 혈관형성 억제제, 길항제 D, 길항제 G, 안타렐릭스, 안트라마이신, 항배방화 형태형성 단백질(anti-dorsalizing morphogenetic protein)-1, 항에스트로겐, 항신생물약, 안티센스 올리고뉴클레오티드, 아피디콜린 글리시네이트, 아팝토시스 유전자 조정자, 아팝토시스 조절제, 아퓨린산, ARA-CDP-DL-PTBA, 아르기닌 데아미나제, 아스파라기나제, 아스페를린, 아술라크린, 아타메스탄, 아트리무스틴, 악시나스타틴 1, 악시나스타틴 2, 악시나스타틴 3, 아자시티딘, 아자세트론, 아자톡신, 아자티로신, 아제테파, 아조토마이신, 박카틴 III 유도체, 발라놀, 바티마스타트, 벤조클로린, 벤조데파, 벤조일스타우로스포린, 베타 락탐 유도체, 베타-알레틴, 베타클라마이신 B, 베툴린산, BFGF 억제제, 비칼루타미드, 비산트렌, 비산트렌 히드로클로라이드, 비사지리디닐스페르민, 비스나피드, 비스나피드 디메실레이트, 비스트라텐 A, 비젤레신, 블레오마이신, 블레오마이신 술페이트, BRC/ABL 길항제, 브레플레이트, 브레퀴나르 나트륨, 브로피리민, 부도티탄, 부술판, 부티오닌 술폭시민, 칵티노마이신, 칼시포트리올, 칼포스틴 C, 칼루스테론, 캄포테신 유도체, 카나리폭스 IL-2, 카페시타빈, 카라세미드, 카르베티머, 카르보플라틴, 카르복사미드-아미노-트리아졸, 카르복시아미도트리아졸, 카레스트 M3, 카르무스틴, 캄 700, 카르틸라제 유래 억제제, 카루비신 히드로클로라이드, 카르젤레신, 카세인 키나제 억제제, 카스타노스페르민, 세크로핀 B, 세데핑골, 세트로렐릭스, 클로람부실, 클로린, 클로로퀴녹살린 술폰아미드, 시카프로스트, 시롤레마이신, 시스플라틴, 시스-포르피린, 클라드리빈, 클로미펜 유사체, 클로트리마졸, 콜리스마이신 A, 콜리스마이신 B, 콤브레타스타틴 A4, 콤브레타스타틴 유사체, 코나게닌, 크람베시딘 816, 크리스나톨, 크리스타톨 메실레이트, 크립토파이신 8, 크립토파이신 A 유도체, 쿠라신 A, 시클로펜탄트라퀴논, 시클로포스파미드, 시클로플라탐, 시페마이신, 시타라빈, 시타라빈 옥포스페이트, 세포용해 인자, 시토스타틴, 다카르바진, 다클릭시맙, 닥티노마이신, 다우노루비신 히드로클로라이드, 데시타빈, 데히드로디뎀님 B, 데슬로렐린, 덱시포스파미드, 덱소르마플라틴, 덱스라족산, 덱스베라파밀, 데자구아닌, 데자구아닌 메실레이트, 디아지쿠온, 디뎀닌 B, 디독스, 디에틸노르스페르민, 디히드로-5-아자시티딘, 디옥사마이신, 디페닐 스피로무스틴, 도세탁셀, 도코사놀, 돌라세트론, 독시플루리딘, 독소루비신, 독소루비신 히드로클로라이드, 드롤록시펜, 드롤록시펜 시트레이트, 드로모스타놀론 프로피오네이트, 드로나비놀, 듀아조마이신, 듀오카르마이신 SA, 에브셀렌, 에코무스틴, 에다트렉세이트, 에델포신, 에드레콜로맙, 에플로미틴, 에플로미틴 히드로클로라이드, 엘레멘, 엘사미트루신, 에미테푸르, 엔로플라틴, 엔프로메이트, 에피프로피딘, 에피루비신, 에피루비신 히드로클로라이드, 에프리스테리드, 에르불로졸, 적혈구 유전자 치료 벡터 시스템, 에소루비신 히드로클로라이드, 에스트라무스틴, 에스트라무스틴 유사체, 에스트라무스틴 포스페이트 나트륨, 에스트로겐 작동제, 에스트로겐 길항제, 에타니다졸, 에토포시드, 에토포시드 포스페이트, 에토프린, 엑세메스탄, 파드로졸, 파드로졸 히드로클로라이드, 파자라빈, 펜레티니드, 필그라스팀, 피나스테리드, 플라보피리돌, 플레젤라스틴, 플록수리딘, 플루아스테론, 플루다라빈, 플루다라빈 포스페이트, 플루오로다우노루니신 히드로클로라이드, 플루오로우라실, 플루오로시타빈, 포르페니멕스, 포르메스탄, 포스퀴돈, 포스트리에신, 포스트리에신 나트륨, 포테무스틴, 가돌리늄 텍사피린, 질산갈륨, 갈로시타빈, 가니렐릭스, 겔라티나제 억제제, 겜시타빈, 겜시타빈 히드로클로라이드, 글루타티온 억제제, 헵술팜, 헤레굴린, 헥사메틸렌 비스아세트아미드, 히드록시우레아, 하이페리신, 이반드론산, 이다루비신, 이다루비신 히드로클로라이드, 이독시펜, 이드라만톤, 이포스파미드, 일모포신, 일로마스타트, 이미다조아크리돈, 이미퀴모드, 면역자극 펩티드, 인슐린-유사 성장 인자-1 수용체 억제제, 인터페론 작동제, 인터페론 알파-2A, 인터페론 알파-2B, 인터페론 알파-N1, 인터페론 알파-N3, 인터페론 베타-IA, 인터페론 감마-IB, 인터페론, 인터류킨, 이오벤구안, 아이오도독소루비신, 이프로플라틴, 이리노테칸, 이리노테칸 히드로클로라이드, 이로플락트, 이르소글라딘, 이소벵가졸, 이소호모할리콘드린 B, 이타세트론, 자스플라키놀리드, 카할랄리드 F, 라멜라린-N 트리아세테이트, 란레오티드, 란레오티드 아세테이트, 레이나마이신, 레노그라스팀, 렌티난 술페이트, 렙톨스타틴, 레트로졸, 백혈병 억제 인자, 백혈구 알파 인터페론, 류프롤리드 아세테이트, 류프롤리드/에스트로겐/프로게스테론, 류프로렐린, 레바미솔, 리아로졸, 리아로졸 히드로클로라이드, 선형 폴리아민 유사체, 친지질성 디사카라이드 펩티드, 친지질성 백금 화합물, 리소클리나미드 7, 로바플라틴, 롬브리신, 로메트렉솔, 로메트렉솔 나트륨, 로무스틴, 로니다민, 로속산트론, 로속산트론 히드로클로라이드, 로바스타틴, 록소리빈, 루르토테칸, 루테튬 텍사피린, 리소필린, 용균 펩티드, 마이탄신, 만노스타틴 A, 마리마스타트, 마소프로콜, 마스핀, 마트릴리신 억제제, 매트릭스 메탈로프로테이나제 억제제, 마이탄신, 메클로레타민 히드로클로라이드, 메게스트롤 아세테이트, 멜렝게스트롤 아세테이트, 멜팔란, 메노가릴, 메르바론, 메르캅토퓨린, 메테렐린, 메티오니나제, 메토트렉세이트, 메토트렉세이트 나트륨, 메토클로프라미드, 메토프린, 메투레데파, 마이크로알갈 단백질 키나제 C 억제제, MIF 억제제, 미페프리스톤, 밀테포신, 미리모스팀, 미스매치 이중 가닥 RNA, 미틴도미드, 미토카신, 미토크로민, 미토길린, 미토구아존, 미톨락톨, 미토말신, 미토마이신, 미토마이신 유사체, 미토나피드, 미토스페르, 미토탄, 미토톡신 섬유아세포 성장 인자-사포린, 미톡산트론, 미톡산트론 히드로클로라이드, 모파로텐, 몰그라모스팀, 모노클로날 항체, 인간 융모성 고나도트로핀, 모노포스포릴 지질 a/미코박테륨 세포 벽 SK, 모피다몰, 다중 약물 내성 유전자 억제제, 다중 종양 억제제 1-기재의 치료제, 머스타드 항암제, 미카퍼옥시드 B, 미코박테륨 세포 벽 추출물, 미코페놀산, 미리아포론, n-아세틸디날린, 나파렐린, 나그레스팁, 날록손/펜타조신, 나파빈, 나프테르핀, 나르토그라스팀, 네다플라틴, 네모루비신, 네리드론산, 중성 엔도펩티다제, 닐루타미드, 니사마이신, 질소 산화물 조정자, 니트록시드 산화방지제, 니트룰린, 노코다졸, 노갈라마이신, n-치환된 벤즈아미드, 06-벤질구아닌, 옥트레오티드, 오키세논, 올리고뉴클레오티드, 오나프리스톤, 온단세트론, 오라신, 경구 시토킨 유도제, 오르마플라틴, 오사테론, 옥살리플라틴, 옥사우노마이신, 옥시수란, 파클리탁셀, 파클리탁셀 유사체, 파클리탁셀 유도체, 팔라우아민, 팔미토일리족신, 파미드론산, 파낙시트리올, 파노미펜, 파라박틴, 파젤립틴, 페가스파르가제, 펠데신, 펠리오마이신, 펜타무스틴, 펜토산 폴리술페이트 나트륨, 펜토스타틴, 펜트로졸, 페플로마이신 술페이트, 페르플루브론, 페르포스파미드, 페릴릴 알콜, 페나지노마이신, 페닐아세테이트, 포스파타제 억제제, 피시바닐, 필로카르핀 히드로클로라이드, 피포브로만, 피포술판, 피라루비신, 피리트렉심, 피록산트론 히드로클로라이드, 플라세틴 A, 플라세틴 B, 플라스미노겐 활성화제 억제제, 백금 착물, 백금 화합물, 백금-트리아민 착물, 플리카마이신, 플로메스탄, 포르피메르 나트륨, 포르피로마이신, 프레드니무스틴, 프로카르바진 히드로클로라이드, 프로필 비스-아크리돈, 프로스타글란딘 J2, 전립선 암종 항안드로겐, 프로테아솜 억제제, 단백질 A-기재의 면역 조정자, 단백질 키나제 C 억제제, 단백질 티로신 포스파타제 억제제, 퓨린 뉴클레오시드 포스포릴라제 억제제, 퓨로이가신, 퓨로마이신 히드로클로라이드, 퓨르퓨린, 피라조푸린, 피라졸로아크리딘, 피리독실화 헤모글로빈 폴리옥시에틸렌 컨쥬게이트, RAF 길항제, 랄티트렉세드, 라모세트론, RAS 파르네실 단백질 트랜스퍼라제 억제제, RAS 억제제, RAS-GAP 억제제, 메틸제거 레텔립틴, 레늄 RE 186 에티드로네이트, 리족신, 리보프린, 리보자임, RII 레티나미드, RNAi, 로글레티미드, 로히투킨, 로무르티드, 로퀴니멕스, 루비기논 B1, 루복실, 사핑골, 사핑골 히드로클로라이드, 사인토핀, 사르크누, 사르코피톨 A, 사르그라모스팀, SDI 1 모방체, 세무스틴, 세네센세 유래 억제제 1, 센스 올리고뉴클레오티드, 신호 전달 억제제, 신호 전달 조정자, 심트라젠, 단일 사슬 항원 결합 단백질, 시조푸란, 소부족산, 나트륨 보로캅테이트, 나트륨 페닐아세테이트, 솔베롤, 소마토메딘 결합 단백질, 소네르민, 스파르포세이트 나트륨, 스파르포스산, 스파르소마이신, 스피카마이신 D, 스피로게르마늄 히드로클로라이드, 스피로무스틴, 스피로플라틴, 스플레노펜틴, 스퐁기스타틴 1, 스쿠알라민, 줄기 세포 억제제, 줄기-세포 분할 억제제, 스티피아미드, 스트렙토니그린, 스트렙토조신, 스트로멜리신 억제제, 술피노신, 술로페누르, 초활성 혈관활성 장 펩티드 길항제, 수라디스타, 수라민, 스와인소닌, 합성 글리코사미노글리칸, 탈리소마이신, 탈리무스틴, 타목시펜 메티오디드, 타우로무스틴, 타자로텐, 테코갈란 나트륨, 테가푸르, 텔루라피릴륨, 텔로머라제 억제제, 텔록산트론 히드로클로라이드, 테모포르핀, 테모졸로미드, 테니포시드, 테록시론, 테스톨락톤, 테트라클로로데카옥시드, 테트라조민, 탈리블라스틴, 탈리도미드, 티아미프린, 티오코랄린, 티오구아닌, 티오테파, 트롬보포이에틴, 트롬보포이에틴 모방체, 티말파신, 티모포이에틴 수용체 작동제, 티모트리난, 갑상선 자극 호르몬, 티아조푸린, 틴 에틸 에티오퓨르퓨린, 티라파자민, 티타노센 디클로라이드, 토포테칸 히드로클로라이드, 톱센틴, 토레미펜, 토레미펜 시트레이트, 전분화 줄기 세포 인자, 번역 억제제, 트레스톨론 아세테이트, 트레티노인, 트리아세틸루리딘, 트리시리빈, 트리시리빈 포스페이트, 트리메트렉세이트, 트리메트렉세이트 글루쿠로네이트, 트리프토렐린, 트로피세트론, 투불로졸 히드로클로라이드, 투로스테리드, 티로신 키나제 억제제, 티르포스틴, UBC 억제제, 우베니멕스, 우라실 머스타드, 우레데파, 비뇨생식동-유래 성장 억제 인자, 우로키나제 수용체 길항제, 바프레오티드, 바리올린 B, 벨라레솔, 베라민, 베르딘, 베르테포르핀, 빈블라스틴 술페이트, 빈크리스틴 술페이트, 빈데신, 빈데신 술페이트, 비네피딘 술페이트, 빙글리시네이트 술페이트, 빈류로신 술페이트, 비노렐빈, 비노렐빈 타르트레이트, 빈로시딘 술페이트, 빈크살틴, 빈졸리딘 술페이트, 비탁신, 보로졸, 자노테론, 제니플라틴, 질라스코르브, 지노스타틴, 지노스타틴 스티말라메르, 또는 조루비신 히드로클로라이드를 포함할 수 있으나 이에 제한되지는 않는다.
일부 실시양태에서, 치료제는 2종 이상의 치료제를 투여하는 것을 포함하는 작용제의 칵테일의 일부일 수 있다. 예를 들어, 시스플라틴 및 옥살리플라틴 둘 다를 갖는 리포솜이 투여될 수 있다. 또한, 치료제는 면역 자극 애주번트, 예컨대 알루미늄 겔 또는 염 애주번트 (예를 들어, 인산알루미늄 또는 수산화알루미늄), 인산칼슘, 엔도톡신, 톨(toll)-유사 수용체 애주번트 등 전에, 그 후에, 또는 그와 함께 전달될 수 있다.
본 발명의 치료제는 또한 치료 용도에 사용하기 위한 방사성핵종을 포함할 수 있다. 예를 들어, 오제(Auger) 전자의 방사체, 예컨대 111In이 킬레이트, 예컨대 디에틸렌트리아민펜타아세트산 (DTPA) 또는 1,4,7,10-테트라아자시클로도데칸-1,4,7,10-테트라아세트산 (DOTA)과 조합되어, 치료에 사용되도록 표적화된 전달 조성물, 예컨대 리포솜 중에 포함될 수 있다. 다른 적합한 방사성핵종 및/또는 방사성핵종-킬레이트 조합은 베타 방사성핵종 (177Lu, 153Sm, 88/90Y)과 DOTA, 64Cu-TETA, 188/186Re(CO)3-IDA; 188/186Re(CO)트리아민 (시클릭 또는 선형), 188/186Re(CO)3-Enpy2, 및 188/186Re(CO)3-DTPA를 포함할 수 있으나 이에 제한되지는 않는다.
상기에 기재된 바와 같이, 본 발명에서 사용되는 치료제는, 나노입자 내에 내포되거나 캡슐화되거나, 또는 그에 테더링되는 등의 다양한 방식으로 나노입자와 회합될 수 있다. 치료제의 로딩은, 예를 들어 참고문헌 [de Villiers, M. M. et al., Eds., Nanotechnology in Drug Delivery, Springer (2009)]; [Gregoriadis, G., Ed., Liposome Technology: Entrapment of drugs and other materials into liposomes, CRC Press (2006)]에 개시된 바와 같이, 당업계에 공지된 다양한 방식으로 수행될 수 있다. 하나의 실시양태 군에서는, 1종 이상의 치료제가 리포솜 내에 로딩될 수 있다. 리포솜의 로딩은, 예를 들어, 능동 또는 수동 방식으로 수행될 수 있다. 예를 들어, 치료제는, 치료제가 리포솜 내에 캡슐화되도록, 용액 중에서의 리포솜의 자체-어셈블리 과정 동안 포함될 수 있다. 특정 실시양태에서, 치료제는 또한 리포솜 이중층 내에 또는 다층 리포솜의 다층 내에 내포될 수 있다. 대안적 실시양태에서, 치료제는 리포솜 내에 능동 로딩될 수 있다. 예를 들어, 리포솜을 전기천공법과 같은 조건에 노출시킬 수 있고, 여기서는 이중층 멤브레인이 치료제를 함유하는 용액에 대해 투과성이 되어 치료제가 리포솜의 내부 부피로 도입될 수 있다.
진단제
본 발명에서 사용되는 진단제는, 예를 들어 참고문헌 [Armstrong et al., Diagnostic Imaging, 5th Ed., Blackwell Publishing (2004)]; [Torchilin, V. P., Ed., Targeted Delivery of Imaging Agents, CRC Press (1995)]; [Vallabhajosula, S., Molecular Imaging: Radiopharmaceuticals for PET and SPECT, Springer (2009)]에 제공된 바와 같은, 당업계에 공지된 임의의 진단제를 포함할 수 있다. 특정 실시양태에서, R1, R2, R3, R4, R5 및 R6은 독립적으로 진단제가 되도록 선택될 수 있다. 진단제는, 감마-방출, 방사성, 에코발생, 광학, 형광, 흡수, 자기 또는 단층촬영 신호를 포함하나 이에 제한되지는 않는 검출가능한 신호를 제공하고/거나 향상시키는 작용제에서와 같이, 다양한 방식으로 검출될 수 있다. 진단제의 영상화 기술은 단일 광자 방출 컴퓨터 단층촬영 (SPECT), 자기 공명 영상 (MRI), 광학 영상, 양전자 방출 단층촬영 (PET), 컴퓨터 단층촬영 (CT), x-선 영상, 감마선 영상 등을 포함할 수 있으나 이에 제한되지는 않는다.
일부 실시양태에서, 진단제는, 예를 들어 금속 이온에 결합되어 다양한 진단 영상화 기술에 사용되는 킬레이터를 포함할 수 있다. 킬레이터의 예는, 에틸렌디아민테트라아세트산 (EDTA), [4-(1,4,8,11-테트라아자시클로테트라데스-1-일) 메틸]벤조산 (CPTA), 시클로헥산디아민테트라아세트산 (CDTA), 에틸렌비스(옥시에틸렌니트릴로)테트라아세트산 (EGTA), 디에틸렌트리아민펜타아세트산 (DTPA), 시트르산, 히드록시에틸 에틸렌디아민 트리아세트산 (HEDTA), 이미노디아세트산 (IDA), 트리에틸렌 테트라아민 헥사아세트산 (TTHA), 1,4,7,10-테트라아자시클로도데칸-1,4,7,10-테트라(메틸렌 포스폰산) (DOTP), 1,4,8,11-테트라아자시클로도데칸-1,4,8,11-테트라아세트산 (TETA), 1,4,7,10-테트라아자시클로도데칸-1,4,7,10-테트라아세트산 (DOTA), 및 이들의 유도체를 포함하나 이에 제한되지는 않는다.
본원에 기재된 진단제의 일부에는 방사성 동위원소가 도입될 수 있고, 이는 감마선, 양전자, 베타 및 알파 입자, 및 X-선을 방출하는 방사성핵종을 포함할 수 있다. 적합한 방사성핵종은 225Ac, 72As, 211At, 11B, 128Ba, 212Bi, 75Br, 77Br, 14C, 109Cd, 62Cu, 64Cu, 67Cu, 18F, 67Ga, 68Ga, 3H, 123I, 125I, 130I, 131I, 111In, 177Lu, 13N, 15O, 32P, 33P, 212Pb, 103Pd, 186Re, 188Re, 47Sc, 153Sm, 89Sr, 99 mTc, 88Y 및 90Y을 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, 방사능 작용제는 111In-DTPA, 99mTc(CO)3-DTPA, 99mTc(CO)3-ENPy2, 62/64/67Cu-TETA, 99mTc(CO)3-IDA, 및 99mTc(CO)3트리아민 (시클릭 또는 선형)을 포함할 수 있다. 다른 실시양태에서, 상기 작용제는 DOTA 및 111In, 177Lu, 153Sm, 88/90Y, 62/64/67Cu, 또는 67/68Ga를 갖는 그의 각종 유사체를 포함할 수 있다. 일부 실시양태에서, 리포솜은, 예를 들어, 참고문헌 [Phillips et al., Wiley Interdisciplinary Reviews: Nanomedicine and Nanobiotechnology, 1(1): 69-83 (2008)]; [Torchilin, V.P. & Weissig, V., Eds. Liposomes 2nd Ed.: Oxford Univ. Press (2003)]; [Elbayoumi, T.A. & Torchilin, V.P., Eur. J. Nucl. Med. Mol. Imaging 33:1196- (2006)]; [Mougin-Degraef, M. et al., Int'l J. Pharmaceutics 344:110-117 (2007)]에 제공된 바와 같이, DTPA-지질과 같이, 킬레이트에 부착된 지질의 도입에 의해 방사성표지될 수 있다.
다른 실시양태에서, 진단제는 형광제, 인광제, 화학발광제 등과 같은 광학 작용제를 포함할 수 있다. 수많은 작용제 (예를 들어, 염료, 프로브, 표지 또는 지시제)가 당업계에 공지되어 있고, 본 발명에서 사용될 수 있다. (예를 들어, 문헌 [Invitrogen, The Handbook-A Guide to Fluorescent Probes and Labeling Technologies, Tenth Edition (2005)] 참조). 형광제는 각종 유기 및/또는 무기 소분자 또는 각종 형광 단백질 및 이들의 유도체를 포함할 수 있다. 예를 들어, 형광제는 시아닌, 프탈로시아닌, 포르피린, 인도시아닌, 로다민, 페녹사진, 페닐크산텐, 페노티아진, 페노셀레나진, 플루오레세인, 벤조포르피린, 스쿠아레인, 디피롤로 피리미돈, 테트라센, 퀴놀린, 피라진, 코린, 크로코늄, 아크리돈, 페난트리딘, 로다민, 아크리딘, 안트라퀴논, 칼코게노피릴륨 유사체, 클로린, 나프탈로시아닌, 메틴 염료, 인돌레늄 염료, 아조 화합물, 아줄렌, 아자아줄렌, 트리페닐 메탄 염료, 인돌, 벤조인돌, 인도카르보시아닌, 벤조인도카르보시아닌, 및 4,4-디플루오로-4-보라-3a,4a-디아자-s-인다센의 일반적 구조를 갖는 보디피(BODIPY)™ 유도체, 및/또는 임의의 이들의 컨쥬게이트 및/또는 유도체를 포함할 수 있으나 이에 제한되지는 않는다. 사용가능한 다른 작용제는, 예를 들어, 플루오레세인, 플루오레세인-폴리아스파르트산 컨쥬게이트, 플루오레세인-폴리글루탐산 컨쥬게이트, 플루오레세인-폴리아르기닌 컨쥬게이트, 인도시아닌 그린, 인도시아닌-도데카아스파르트산 컨쥬게이트, 인도시아닌-폴리아스파르트산 컨쥬게이트, 이소술판 블루, 인돌 디술포네이트, 벤조인돌 디술포네이트, 비스(에틸카르복시메틸)인도시아닌, 비스(펜틸카르복시메틸)인도시아닌, 폴리히드록시인돌 술포네이트, 폴리히드록시벤조인돌 술포네이트, 경질 헤테로원자 인돌 술포네이트, 인도시아닌비스프로판산, 인도시아닌비스헥산산, 3,6-디시아노-2,5-[(N,N,N',N'-테트라키스(카르복시메틸)아미노]피라진, 3,6-[(N,N,N',N'-테트라키스(2-히드록시에틸)아미노]피라진-2,5-디카르복실산, 3,6-비스(N-아자테디노)피라진-2,5-디카르복실산, 3,6-비스(N-모르폴리노)피라진-2,5-디카르복실산, 3,6-비스(N-피페라지노)피라진-2,5-디카르복실산, 3,6-비스(N-티오모르폴리노)피라진-2,5-디카르복실산, 3,6-비스(N-티오모르폴리노)피라진-2,5-디카르복실산 S-옥시드, 2,5-디시아노-3,6-비스(N-티오모르폴리노)피라진 S,S-디옥시드, 인도카르보시아닌테트라술포네이트, 클로로인도카르보시아닌, 및 3,6-디아미노피라진-2,5-디카르복실산을 포함하나 이에 제한되지는 않는다.
당업자는, 사용되는 특정 광학 작용제는 여기에 이용되는 파장, 피부 조직 하부 깊이, 및 당업계에 일반적으로 널리 공지되어 있는 다른 요인에 따라 달라질 수 있음을 인지할 것이다. 예를 들어, 광학 작용제의 최적 흡수 또는 여기 최대는 사용되는 작용제에 따라 달라질 수 있지만, 일반적으로, 본 발명의 광학 작용제는 전자기 스펙트럼의 자외선 (UV), 가시광선 또는 적외선 (IR) 범위의 빛을 흡수하거나 그에 의해 여기될 것이다. 영상화를 위해, 근-IR에서 흡수하고 방출하는 염료 (~700 내지 900 nm, 예를 들어, 인도시아닌)이 바람직하다. 내시경 방법을 이용한 국소 시각화에서는, 가시광선 영역에서 흡수하는 임의의 염료가 적합하다.
일부 실시양태에서, 본 발명의 방법에서 사용되는 비-이온화 방사선은 약 350 nm 내지 약 1200 nm의 파장 범위일 수 있다. 하나의 예시적 실시양태에서, 형광제는 전자기 스펙트럼의 가시광선 부분의 청색 범위 (약 430 nm 내지 약 500 nm)의 파장을 갖는 빛에 의해 여기될 수 있고, 전자기 스펙트럼의 가시광선 부분의 녹색 범위 (약 520 nm 내지 약 565 nm)의 파장에서 방출한다. 예를 들어, 플루오레세인 염료는 약 488 nm의 파장을 갖는 빛으로 여기될 수 있고, 이는 약 520 nm의 방출 파장을 가질 수 있다. 또 다른 예로, 3,6-디아미노피라진-2,5-디카르복실산은 약 470 nm의 파장을 갖는 빛으로 여기될 수 있고, 약 532 nm의 파장에서 형광을 낸다. 또 다른 실시양태에서, 광학 작용제의 여기 및 방출 파장은 전자기 스펙트럼의 근-적외선 범위 내에 포함될 수 있다. 예를 들어, 인도시아닌 염료, 예컨대 인도시아닌 그린은 약 780 nm의 파장을 갖는 빛으로 여기될 수 있고, 약 830 nm의 방출 파장을 가질 수 있다.
또한 다른 실시양태에서, 진단제는 당업계에 일반적으로 널리 공지되어 있는 자기 공명 (MR) 및 x-선 콘트라스트제, 예를 들어, 아이오딘-기재의 x-선 콘트라스트제, 초상자성 산화철 (SPIO), 가돌리늄 또는 망간의 착물 등을 포함할 수 있으나 이에 제한되지는 않는다. (예를 들어, 문헌 [Armstrong et al., Diagnostic Imaging, 5th Ed., Blackwell Publishing (2004)] 참조). 일부 실시양태에서, 진단제는 자기 공명 (MR) 영상화제를 포함할 수 있다. 자기 공명 작용제의 예는 상자성 작용제, 초상자성 작용제 등을 포함하나 이에 제한되지는 않는다. 상자성 작용제의 예는 가도펜테트산, 가도테르산, 가도디아미드, 가돌리늄, 가도테리돌, 망가포디피르, 가도베르세타미드, 시트르산제2철암모늄, 가도벤산, 가도부트롤, 또는 가독세트산을 포함할 수 있으나 이에 제한되지는 않는다. 초상자성 작용제는 초상자성 산화철 및 페리스텐을 포함할 수 있으나 이에 제한되지는 않는다. 특정 실시양태에서, 진단제는, 예를 들어 참고문헌 [H.S Thomsen, R.N. Muller and R.F. Mattrey, Eds., Trends in Contrast Media, (Berlin: Springer-Verlag, 1999)]; [P. Dawson, D. Cosgrove and R. Grainger, Eds., Textbook of Contrast Media (ISIS Medical Media 1999)]; [Torchilin, V.P., Curr. Pharm. Biotech. 1:183-215 (2000)]; [Bogdanov, A.A. et al., Adv. Drug Del. Rev. 37:279-293 (1999)]; [Sachse, A. et al., Investigative Radiology 32(1):44-50 (1997)]에 제공된 바와 같은, x-선 콘트라스트제를 포함할 수 있다. x-선 콘트라스트제의 예는, 이오파미돌, 이오메프롤, 이오헥솔, 이오펜톨, 이오프로미드, 이오시미드, 이오베르솔, 이오트롤란, 이오타술, 이오딕사놀, 이오데시몰, 이오글루카미드, 이오글루니드, 이오굴라미드, 이오사르콜, 이옥실란, 이오파미론, 메트리자미드, 이오비트리돌 및 이오시메놀을 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, x-선 콘트라스트제는 이오파미돌, 이오메프롤, 이오프로미드, 이오헥솔, 이오펜톨, 이오베르솔, 이오비트리돌, 이오딕사놀, 이오트롤란 및 이오시메놀을 포함할 수 있다.
상기에 기재된 치료제와 유사하게, 진단제는, 예를 들어 나노입자 내에 내포되거나 캡슐화되거나, 또는 그에 테더링되는 것을 포함한 다양한 방식으로 나노입자와 회합될 수 있다. 유사하게, 진단제의 로딩은, 예를 들어 참고문헌 [de Villiers, M. M. et al., Eds., Nanotechnology in Drug Delivery, Springer (2009)]; [Gregoriadis, G., Ed., Liposome Technology: Entrapment of drugs and other materials into liposomes, CRC Press (2006)]에 개시된 바와 같이, 당업계에 공지된 다양한 방식으로 수행될 수 있다.
표적화제
일부 실시양태에서, 본 발명의 포스포네이트 컨쥬게이트는 또한 1종 이상의 표적화제를 포함할 수 있다. 예를 들어, 특정 실시양태에서, R1, R2, R3, R4, R5 및 R6은 독립적으로 표적화제가 되도록 선택될 수 있다. 일반적으로, 본 발명의 표적화제는, 기관, 조직, 세포, 세포외 매트릭스, 또는 세포내 영역과 회합된 표적과 같은 임의의 관심있는 표적과 회합될 수 있다. 특정 실시양태에서, 표적은 특정 질병 상태, 예컨대 암 질환과 관련될 수 있다. 다르게는, 표적화제는, 예를 들어 특정 질병 및/또는 세포, 조직, 및/또는 대상체의 특정 상태를 나타내는 표적을 가질 수 있는 하나 이상의 특정 유형의 세포를 표적화할 수 있다. 일부 실시양태에서, 표적화제는 단지 하나의 표적, 예컨대 수용체에 대해 특이적일 수 있다. 적합한 표적은 핵산, 예컨대 DNA, RNA, 또는 이들의 변형된 유도체를 포함할 수 있으나 이에 제한되지는 않는다. 적합한 표적은 또한 단백질, 예컨대 세포외 단백질, 수용체, 세포 표면 수용체, 종양-마커, 트랜스멤브레인 단백질, 효소, 또는 항체를 포함할 수 있으나 이에 제한되지는 않는다. 적합한 표적은, 예를 들어, 세포 표면 상에 존재할 수 있는, 탄수화물, 예컨대 모노사카라이드, 디사카라이드, 또는 폴리사카라이드를 포함할 수 있다. 특정 실시양태에서, 적합한 표적은 뮤신, 예컨대 MUC-1 및 MUC-4, 성장 인자 수용체, 예컨대 EGFR, 클라우딘 4, 핵소체 인단백질, 예컨대 뉴클레올린, 케모카인 수용체, 예컨대 CCR7, 수용체, 예컨대 소마토스타틴 수용체 4, Erb-B2 (적혈모구 백혈병 종양유전자 동족체 2) 수용체, CD44 수용체, 및 VEGF 수용체-2 키나제를 포함할 수 있다.
특정 실시양태에서, 표적화제는 표적 리간드의 소분자 모방체 (예를 들어, 펩티드 모방 리간드), 표적 리간드 (예를 들어, RGD 펩티드 함유 펩티드 또는 폴레이트 아미드), 또는 특정 표적에 대해 특이적인 항체 또는 항체 단편을 포함할 수 있다. 일부 실시양태에서, 표적화제는 폴산 유도체, B-12 유도체, 인테그린 RGD 펩티드, NGR 유도체, 소마토스타틴 유도체 또는 소마토스타틴 수용체에 결합하는 펩티드, 예를 들어, 옥트레오티드 및 옥트레오테이트 등을 추가로 포함할 수 있다.
본 발명의 표적화제는 또한 앱타머를 포함할 수 있다. 앱타머는 관심있는 표적과 회합되거나 그에 결합하도록 디자인될 수 있다. 앱타머는, 예를 들어, DNA, RNA, 및/또는 펩티드로 구성될 수 있고, 앱타머의 특정 측면은 당업계에 널리 공지되어 있다. (예를 들어, 문헌 [Klussman, S., Ed., The Aptamer Handbook, Wiley-VCH (2006)]; [Nissenbaum, E.T., Trends in Biotech. 26(8): 442-449 (2008)] 참조). 본 발명에서, 적합한 앱타머는 선형이거나 고리화될 수 있고, 약 150개 미만의 염기를 갖는 (즉, 약 150 mer 미만) 올리고뉴클레오티드를 포함할 수 있다. 앱타머는 길이가 약 100 내지 약 150개 염기 또는 약 80 내지 약 120개 염기의 범위일 수 있다. 특정 실시양태에서, 앱타머는 약 12 내지 약 40개 염기, 약 12 내지 약 25개 염기, 약 18 내지 약 30개 염기, 또는 약 15 내지 약 50개 염기의 범위일 수 있다. 앱타머는 질병 상태에서 존재하거나 발현되는 적합한 표적과 함께 사용하기 위해 개발될 수 있고, 이는 본원에 기재된 표적 부위를 포함하나 이에 제한되지는 않는다.
IV. 포스포네이트 컨쥬게이트 및 관련 성분의 제조 방법
포스포네이트 컨쥬게이트는 다양한 방식으로 제조될 수 있다. 하나의 측면에서, 본 발명은, 화학식: H2N(L1)-(R1)을 갖는 1급 아민 화합물, 화학식: O=C[(L2)-(R2)]n을 갖는 카르보닐 화합물, 및 화학식:
을 갖는 H-포스포네이트 화합물을, 화학식:
을 갖는 포스포네이트 컨쥬게이트
(상기 식에서, L1, L2, L3 및 L4는 각각 독립적으로 결합 및 연결기로 이루어진 군으로부터 선택되고; R1은 나노입자, 부착 성분, 표적화제, 진단제, 스텔스제, 및 4-다리 제시 성분으로 이루어진 군으로부터 선택되고; R2는 각각 독립적으로 스텔스제, C1-C10 알킬, 카르복실산 또는 에스테르, 포스폰산 또는 에스테르, 술폰산 또는 에스테르, 및 히드록시로 이루어진 군으로부터 선택되고; R3 및 R4는 각각 독립적으로 H, 부착 성분, 표적화제, 진단제, 및 스텔스제로 이루어진 군으로부터 선택되고, 여기서 R3 또는 R4 중 적어도 하나는 H 이외의 것이고; n은 0 내지 2의 정수이고, 여기서 n이 0 또는 1인 경우 카르보닐 화합물은 알데히드임)를 형성하기에 충분한 조건 하에 조합하는 것을 포함하는, 포스포네이트 컨쥬게이트의 제조 방법을 포함한다.
또 다른 측면에서, 본 발명은 포스포네이트 컨쥬게이트의 제조 방법을 포함한다. 상기 방법은, 화학식: HN[(L1)-(R1)](R9)을 갖는 2급 아민 화합물, 화학식: O=C[(L2)-(R2)]n을 갖는 카르보닐 화합물, 및 화학식:
을 갖는 H-포스포네이트 화합물을, 화학식:
을 갖는 포스포네이트 컨쥬게이트
(상기 식에서, L1, L2, L3 및 L4는 각각 독립적으로 결합 및 연결기로 이루어진 군으로부터 선택되고; R1은 나노입자, 부착 성분, 표적화제, 진단제 및 스텔스제로 이루어진 군으로부터 선택되고; R2는 독립적으로 스텔스제, C1-C10 알킬, 카르복실산 또는 에스테르, 포스폰산 또는 에스테르, 술폰산 또는 에스테르, 및 히드록시로 이루어진 군으로부터 선택되고; R3 및 R4는 각각 독립적으로 H, 부착 성분, 표적화제, 진단제, 및 스텔스제로 이루어진 군으로부터 선택되고, 여기서 R3 또는 R4 중 적어도 하나는 H 이외의 것이고; R9는 C1-C10 알킬 기로 이루어진 군으로부터 선택되고; n은 0 내지 2의 정수이고, 여기서 n이 0인 경우 카르보닐 화합물은 포름알데히드임)를 형성하기에 충분한 조건 하에 조합하는 것을 포함한다.
일반적으로, 포스포네이트 컨쥬게이트를 제조하기 위해 이용되는 반응은 H-포스포네이트 화합물, 카르보닐 화합물, 및 1급 아민 화합물 또는 2급 아민 화합물을 포함한다. 이들 화합물은 최종 포스포네이트 컨쥬게이트에 도달하기 위해 합성 동안 임의의 순서로 조합될 수 있다. 예를 들어, 일부 실시양태에서는, 1급 아민 화합물 또는 2급 아민 화합물 및 카르보닐 화합물을 조합하여 중간체 화합물을 형성한 후, H-포스포네이트 화합물과 조합하여 최종 포스포네이트 컨쥬게이트를 형성할 수 있다. 다른 실시양태에서는, H-포스포네이트 화합물을 카르보닐 화합물과 조합하여 중간체 화합물을 형성한 후, 1급 아민 화합물 또는 2급 아민 화합물과 조합하여 최종 포스포네이트 컨쥬게이트를 형성할 수 있다. 특정 실시양태에서는, 필수 화합물을 하나의 반응에서 함께 조합하여 최종 포스포네이트 컨쥬게이트를 제조할 수 있다. 특정 컨쥬게이트의 경우, H-포스포네이트 화합물, 카르보닐 화합물, 및 1급 아민 화합물의 비율은 2:2:1일 수 있다. 다른 컨쥬게이트의 경우, H-포스포네이트 화합물, 카르보닐 화합물, 및 2급 아민 화합물의 비율은 1:1:1일 수 있다. 상이한 화합물의 비율은 특정 반응 조건 및 요망되는 포스포네이트 컨쥬게이트에 따라 달라질 것이다.
본원에서 제공된 바와 같이, H-포스포네이트 화합물, 1급 또는 2급 아민 화합물, 및 카르보닐 화합물이 관여되는 반응을 이용하여, 부착 성분, 표적화제, 진단제, 치료제, 스텔스제, 또는 이들의 조합을 포함할 수 있는 매우 다양한 화합물을 제조할 수 있다. 예를 들어 도 1 및 2에 나타낸 바와 같이, 2:2:1 비율의 H-포스포네이트 화합물, 카르보닐 화합물, 및 1급 아민 화합물을 조합하여 본 발명의 포스포네이트 컨쥬게이트를 형성할 수 있다. 도 1에 나타낸 바와 같이, 포스포네이트 컨쥬게이트는 R1을 PEG100 내지 PEG10000 범위의 PEG 기로서 포함할 수 있다. R3 및 R4는 또한, 예를 들어, 리포솜의 이중층 멤브레인에 대한 부착을 용이하게 하도록 C1-C20 알킬 기로부터 선택될 수 있다. 이러한 특정 예에서, n은 0이고, 여기서 카르보닐 화합물은 포름알데히드이다. 유사하게, 도 2에 나타낸 바와 같이, 카르보닐 화합물은 n을 1로서, 또한 R2를 메틸 기로서 가질 수 있고, 이는 도 1에서의 포스포네이트 컨쥬게이트의 구조를 변화시킨다. 당업자는 본원에 개시된 범위의 포스포네이트 컨쥬게이트를 제조하기 위해 사용될 수 있는 다양한 가능한 조합을 인지할 것이다.
일부 실시양태에서, 포스포네이트 컨쥬게이트는, 예를 들어, 나노입자의 표면으로부터 연장될 수 있는 제시 어셈블리를 제공하도록 제조될 수 있다. 도 3에 나타낸 바와 같이, 지질 분자는 1급 아민 및 R7 및 R8 (이는 예를 들어, C1-C20 알킬 기일 수 있음)을 포함할 수 있다. 이러한 예에서, n은 0이고, L3 및 L4는 결합 또는 짧은 알킬렌 기 (예를 들어, C1-C6) 또는 요망되는 간격 또는 특정 용도를 위해 요망되는 다른 특징을 가능하게 하는 다른 연결기일 수 있다. 나타낸 바와 같이, 지질 분자를 H-포스포네이트 화합물 및 포름알데히드와 각각 1:2:2의 비율로 조합하여 R3 및 R4의 4-다리 어셈블리를 제시하는 포스포네이트 컨쥬게이트를 형성할 수 있다.
특정 실시양태에서는, 이들 화합물의 제조 방법을 나노입자와 조합하여 포스포네이트 컨쥬게이트의 합성을 가능하게 하면서, 출발 물질 중 하나, 예를 들어, H-포스포네이트 화합물을 나노입자에 부착시킬 수 있다. 예시적 도 4에 도시된 바와 같이, 지질 이중층 멤브레인 내의 2개의 인접한 H-포스포네이트 화합물을 2 당량의 카르보닐 화합물, O=C[(L2)-(R2)]n, 및 1 당량의 1급 아민 화합물, H2N(L1)-(R1)과 조합하여 나노입자의 표면 상의 본 발명의 포스포네이트 컨쥬게이트를 제조할 수 있다. 예를 들어, 도 4에 나타낸 바와 같이, R3 및 R4는 부착 성분, 예를 들어, 리포솜의 지질 이중층 내에 내포된 C1-C20 알킬 기일 수 있다. 이어서, 제조된 H-포스포네이트 화합물을 갖는 리포솜을, 예를 들어 스텔스제, 예컨대 PEG100 내지 PEG10000 범위의 PEG를 포함하는 1급 아민 화합물과 조합할 수 있다. 카르보닐 화합물을 포함하는 히드로포스포닐화 반응 후, 스텔스제가 리포솜의 표면 상에 나타남으로써 리포솜이 스텔스 리포솜으로 변형될 수 있다.
도 5에 도시된 바와 같이, 유사한 전략을 이용하여 나노입자의 표면으로부터 연장되는 제시 어셈블리를 제조할 수 있다. 지질 분자는 표면으로부터 연장되는 1급 아민을 포함할 수 있고, R7 및 R8은, 예를 들어, 지질 이중층 내에 내포된 C1-C20 알킬 기일 수 있다. 2 당량의 H-포스포네이트 화합물 및 포름알데히드와 조합시, 히드로포스포닐화 반응은 2개의 H-포스포네이트 화합물 사이의 브릿지를 형성할 수 있고, 또한 리포솜 표면 상에 R5 및 R6을 제시할 수 있고, 여기서 R5 및 R6은 스텔스제, 예컨대 PEG100 내지 PEG10000 범위의 PEG일 수 있다. 상기에서 보다 상세히 설명된 바와 같이, 연결기 L1, L2, 및 L3은 독립적으로, 요망되는 간격 또는 특정 용도를 위해 요망되는 다른 특징을 가능하게 하는 연결기 또는 결합으로서 선택될 수 있다. 당업자는 나노입자의 표면 상의 본 발명의 포스포네이트 컨쥬게이트를 제조하기 위해 이용될 수 있는 다양한 합성 방법을 인지할 것이다.
당업자가 인지하는 바와 같이, 본원에 기재된 합성 반응식의 출발 물질 및 중간체는 요망되는 경우 여과, 증류, 결정화, 크로마토그래피 등을 포함하나 이에 제한되지는 않는 통상의 기술을 이용하여 단리되고 정제될 수 있다. 이러한 물질은 물리적 상수 및 스펙트럼 데이터를 비롯한 통상의 수단을 이용하여 특성화될 수 있다. 달리 특정되지 않는 한, 본원에 기재된 반응은 약 -78℃ 내지 약 150℃, 또는 약 0℃ 내지 약 125℃의 반응 온도 범위에서, 또한 일부 실시양태에서는 대략 실온 (또는 주변 온도), 예를 들어, 약 20℃에서 대기압에서 불활성 분위기 하에 수행될 수 있다. 본원에 기재된 반응은 본원에 기재된 중간체 또는 최종 생성물을 제조하기 위해 이용되는 특정 반응에 따라 달라질 수 있는 다양한 용매 중에서 수행될 수 있다. 일부 실시양태에서, 반응 용매는 유기 용매, 예컨대 비양성자성 용매 (예를 들어, THF 또는 에테르)를 포함할 수 있다. 특정 실시양태에서, 반응 용매는 수성 용매일 수 있고, 추가의 완충제, 염, 첨가제 등을 포함할 수 있다. 본원에 기재된 특정 반응은, 예를 들어, 본원에 기재된 특정 화합물을 정제하기 위한 환류 조건을 포함할 수 있다.
히드로포스포닐화 반응이 나노입자 상의 본 발명의 포스포네이트 컨쥬게이트의 제조에 대한 여러 이점을 제공하지만, 다른 방법을 이용하여 화합물을 제조할 수 있다. 예를 들어, H-포스포네이트 화합물, 1급 및 2급 아민 화합물, 및 카르보닐 화합물을 함께 반응시켜 본 발명의 포스포네이트 컨쥬게이트를 형성할 수 있다. 이어서, 포스포네이트 컨쥬게이트를 나노입자에 부착시킬 수 있다. 일부 실시양태에서는, 먼저 표준 방법, 예를 들어, 압출을 이용하여 리포솜을 제조하고, 이어서 리포솜에 포스포네이트 컨쥬게이트를 부착시킴으로써, 포스포네이트 컨쥬게이트를 리포솜 내에 도입할 수 있다. 다른 실시양태에서는, 예를 들어, 포스포네이트 컨쥬게이트 및 지질 성분을 함께 건조시키고, 이어서 혼합물을 수용액 중에 재현탁시켜 이중층과 회합된 포스포네이트 컨쥬게이트를 갖는 리포솜을 형성함으로써, 리포솜의 형성 동안 포스포네이트 컨쥬게이트를 리포솜 이중층 내에 도입할 수 있다.
다른 합성 순서를 이용하여 포스포네이트 컨쥬게이트를 제조할 수 있다는 것 또한 고려된다. 예를 들어, 도 1에 나타낸 바와 같은 R1 및 L1을 포함하는 1급 아민 화합물을 R3 및 R4를 함유하지 않는 H-포스포네이트와 반응시킬 수 있다. 이러한 실시양태에서, L3 및 L4는, 예를 들어, 표적화제, 스텔스제, 또는 진단제를 포함할 수 있는, R3 및/또는 R4에 대한 결합을 위한 관능기를 포함하는 연결기일 수 있다. 따라서, R3 및/또는 R4를 L3 및 L4의 관능기와 반응시켜 최종 포스포네이트 컨쥬게이트를 제조할 수 있다. 당업자는 본 발명의 포스포네이트 컨쥬게이트를 제조하기 위한 여러 다른 가능한 합성 순서가 존재함을 인지할 것이다. 예를 들어, R3 및 R4는 동일할 수 있고, 따라서, 예를 들어, R3 및 R4가 각각 표적화제인 경우, L3 및 L4는 각각 표적화제와 반응하여 본 발명의 포스포네이트 컨쥬게이트를 제조할 수 있는 관능기를 함유할 수 있다.
나노입자
본원에서 제공된 바와 같이, 본 발명은 당업계에 일반적으로 공지되어 있는 다양한 방식에 의해 제조될 수 있는 나노입자의 용도를 포함하고, 이러한 나노입자의 제조 방법은 요망되는 특정 나노입자에 따라 달라질 수 있다. 당업계에서 이용가능한 임의의 측정 기술을 이용하여 표적화된 전달 조성물 및 나노입자의 특성을 측정할 수 있다. 예를 들어, 동적 광 산란, x-선 광전자 현미경검사, 분말 x-선 회절, 주사 전자 현미경검사 (SEM), 투과 전자 현미경검사 (TEM), 및 원자간력 현미경검사 (AFM) 등의 기술을 이용하여 나노입자 및/또는 표적화된 전달 조성물의 평균 크기 및 분산성을 측정할 수 있다.
본 발명에서 사용되는 리포솜은 당업계에 일반적으로 널리 공지되어 있는 다양한 기술을 이용하여 제조될 수 있다. (예를 들어, 문헌 [Williams, A.P., Liposomes: A Practical Approach, 2nd Edition, Oxford Univ. Press (2003)]; [Lasic, D.D., Liposomes in Gene Delivery, CRC Press LLC (1997)] 참조). 예를 들어, 리포솜은 압출, 교반, 음파파쇄, 역상 증발, 수용액 중의 자체-어셈블리, 전극-기재의 형성 기술, 미세유체 유도 형성 기술 등의 기술 (이에 제한되지는 않음)에 의해 제조될 수 있다. 특정 실시양태에서는, 방법을 이용하여, 대형 단층 소포 (LUV) 및/또는 소형 단층 소포 (SUV)를 포함할 수 있는, 다층 및/또는 단층인 리포솜을 제조할 수 있다. 용액 중에서의 리포솜의 자체-어셈블리와 유사하게, 양친매성 분자가 미셀을 형성하기에 충분한 용액 조건에서 용해시 미셀을 형성하도록, 당업계에 일반적으로 널리 공지되어 있는 기술을 이용하여 미셀을 제조할 수 있다. 또한, 당업계에 공지된 방법을 이용하여 지질-코팅된 기포 및 지질단백질을 구성할 수 있다. (예를 들어, 문헌 [Farook, U., J. R. Soc. Interface, 6(32): 271-277 (2009)]; [Lacko et al., Lipoprotein Nanoparticles as Delivery Vehicles for Anti-Cancer Agents in Nanotechnology for Cancer Therapy, CRC Press (2007)] 참조).
본 발명에서 사용될 수 있는 중합체 나노입자의 제조 방법은 당업계에 일반적으로 널리 공지되어 있다 (예를 들어, 문헌 [Sigmund, W. et al., Eds., Particulate Systems in Nano- and Biotechnologies, CRC Press LLC (2009)]; [Karnik et al., Nano Lett., 8(9): 2906-2912 (2008)] 참조). 예를 들어, 블록 공중합체가 용액 중에서 자체-어셈블링되어 폴리머솜 및/또는 블록 공중합체 미셀을 형성할 수 있도록 당업계에 공지된 합성 방법을 이용하여 블록 공중합체를 제조할 수 있다. 니오솜은 당업계에 공지되어 있고, 이는 다양한 기술 및 조성물을 이용하여 제조될 수 있다 (문헌 [Baillie A.J. et al., J. Pharm. Pharmacol., 38:502-505 (1988)]). 공-침전, 열 분해, 및 마이크로에멀젼 등의 당업계에 공지된 임의의 방법을 이용하여 자기 및/또는 금속 입자를 구성할 수 있다. (또한 문헌 [Nagarajan, R. & Hatton, T.A., Eds., Nanoparticles Synthesis, Stabilization, Passivation, and Functionalization, Oxford Univ. Press (2008)] 참조). 투르케비치(Turkevich) 방법, 브루스트(Brust) 방법, 페라우트(Perraut) 방법 또는 초음파분해(sonolysis) 등의 당업계에 일반적으로 공지되어 있는 다양한 기술을 이용하여 금 입자 및 그의 유도체를 제조할 수 있다. (또한, 문헌 [Grzelczak et al., Chem. Soc. Rev., 37: 1783-1791 (2008)] 참조). 일부 실시양태에서는, 부착 성분을 황-금 테더링 화학을 통해 부착시킬 수 있다. 콜로이드 합성 기술 등의 당업계에 공지된 임의의 방법을 이용하여 양자점 또는 반도체 나노결정을 합성할 수 있다. 일반적으로, 양자점은 셀레늄화카드뮴, 황화카드뮴, 비화인듐, 인화인듐 등을 비롯한 반도체 물질 등의 다양한 물질로 구성될 수 있다.
다른 관련 성분
본원에 기재된 바와 같이, 본 발명의 포스포네이트 컨쥬게이트는 표적화제, 스텔스제, 진단제, 치료제, 및 부착 성분 등의 성분을 포함할 수 있다. 당업자는 포스포네이트 컨쥬게이트 중에 포함된 다양한 성분의 조합을 제조하기 위해 이용될 수 있는 일반적으로 널리 공지된 표준 기술을 인지할 것이다. 예를 들어, 표적화제, 스텔스제, 진단제, 치료제는, 부착 성분에 대해 상기에 기재된 바와 같이, 공유결합 및/또는 비-공유결합 부착을 통해 본 발명의 포스포네이트 컨쥬게이트에 부착될 수 있다.
표적화제와 관련하여, 특정 실시양태에서 표적화제는 앱타머를 포함할 수 있다. 특정 표적에 대한 앱타머는, 시험관내 선택 방법, 예컨대 셀렉스™ (기하급수적 농축에 의한 리간드의 계통 진화), 또는 모노렉스™ 기술 (압타레스 아게(AptaRes AG)에서의 일회 앱타머 단리 절차), 생체내 선택 방법, 또는 이들의 조합 등 (이에 제한되지는 않음)의 당업계에 공지된 기술을 이용하여 식별될 수 있다. (예를 들어, 문헌 [Ellington, A.D. & Szostak, J.W., Nature 346(6287): 818-22]; [Bock et al., Nature 355(6360): 564-6 (1992)] 참조). 일부 실시양태에서는, 상기 언급된 방법을 이용하여, 본원에 개시된 바와 같은, 관심있는 특정 표적 부위에 결합하기 위해 사용될 수 있는 특정 DNA 또는 RNA 서열을 식별할 수 있다. 일련의 특정 앱타머가 식별되면, 앱타머를 포스포라미다이트 합성 등의 당업계에 공지된 다양한 방식으로 구성할 수 있다. 펩티드 앱타머의 경우, 다양한 식별 및 제조 기술이 이용될 수 있다 (예를 들어, 문헌 [Colas, P., J. Biol. 7:2 (2008)]; [Woodman, R. et al., J. Mol. Biol. 352(5): 1118-33 (2005)] 참조).
앱타머는 다양한 방식에 의해 H-포스포네이트 화합물, 1급 및 2급 아민 화합물, 및 카르보닐 화합물에 부착될 수 있다. 예를 들어, H-포스포네이트 화합물 및/또는 1급 또는 2급 아민 화합물 상의 연결기가 앱타머의 3' 또는 5' 말단과 반응할 수 있다. 대안적 실시양태에서, 앱타머는, 하나의 핵산을 H-포스포네이트 화합물 및 1급 또는 2급 아민 화합물 상의 연결기에 한번에 첨가함으로써 연속적으로 합성될 수 있다. 당업자는 본 발명의 포스포네이트 컨쥬게이트 내에 앱타머를 포함시키기 위해 이용될 수 있는 널리 공지된 기술을 인지할 것이다.
V. 표적화된 전달 조성물의 투여 방법
본 발명은 또한 포스포네이트 컨쥬게이트를 포함하는 표적화된 전달 조성물을 포함한다. 하나의 측면에서, 본 발명은, R3 및 R4는 각각 나노입자에 부착되는 부착 성분이고, R1은 표적화제, 진단제 및 스텔스제로부터 선택되는 것인, 본원에 기재된 포스포네이트 컨쥬게이트를 포함하는 표적화된 전달 조성물을 포함한다. 상기에서 보다 상세히 설명된 바와 같이, 부착 성분은 여러 방식으로 나노입자에 부착될 수 있고, 예를 들어, 부착 성분은 리포솜의 이중층과 회합되는 지질일 수 있다. 특정 실시양태에서, 표적화된 전달 조성물은 리포솜을 포함할 수 있고, R3 및 R4는 각각 리포솜의 이중층과 회합될 수 있고, 이는 독립적으로 지질 또는 콜레스테롤일 수 있다. 다른 실시양태에서, 포스포네이트 컨쥬게이트의 R1은 나노입자 또는 나노입자에 부착되는 부착 성분일 수 있고, R3 및 R4는 각각 표적화제, 진단제 또는 스텔스제일 수 있다.
본 발명의 표적화된 전달 조성물 및 방법은 대상체와 관련된 임의의 질병, 장애 및/또는 질환의 치료 및/또는 진단에 사용될 수 있다. 하나의 실시양태에서, 본 발명의 방법은, 암 질환을 치료하거나 진단하기에 충분한 치료제 또는 진단제를 또한 포함하며, R1, R3 및 R4 중 적어도 하나가 표적화제인, 나노입자에 부착된 본 발명의 포스포네이트 컨쥬게이트를 포함하는 표적화된 전달 조성물을 대상체에게 투여하는 것을 포함하는, 대상체에서의 암 질환의 치료 또는 진단 방법을 포함한다. 특정 실시양태에서, 암 질환은, 본 발명의 표적화된 전달 조성물의 표적화제에 의해 표적화되는 수용체를 충분히 발현하는 (예를 들어, 세포 표면 상에서 또는 혈관계 내에서) 암을 포함할 수 있다.
또 다른 실시양태에서, 본 발명의 방법은, 나노입자 및 본원에 기재된 포스포네이트 컨쥬게이트를 포함하며, 여기서 포스포네이트 컨쥬게이트 또는 나노입자는 진단제를 포함하고, R1, R3 및 R4 중 적어도 하나는 표적화제인 표적화된 전달 조성물을 대상체에게 투여하고, 상기 대상체를 영상화하여 진단제를 검출하는 것을 포함하는, 표적화된 치료 처치에 대한 대상체의 적합성을 결정하는 방법을 포함한다.
투여
일부 실시양태에서, 본 발명은 표적화된 전달 조성물 및 생리학적으로 (즉, 제약상) 허용가능한 담체를 포함할 수 있다. 본원에서 사용되는 바와 같이, 용어 "담체"는 치료제 등의 약물에 대한 희석제 또는 비히클로서 사용되는 전형적으로 불활성인 물질을 지칭한다. 상기 용어는 또한, 조성물에 응집성을 부여하는 전형적으로 불활성인 물질을 포함한다. 전형적으로, 생리학적으로 허용가능한 담체는 액체 형태로 존재한다. 액체 담체의 예는 생리 식염수, 포스페이트 완충제, 완충 생리 식염수 (135 내지 150 mM NaCl), 물, 완충수, 0.4% 식염수, 0.3% 글리신, 향상된 안정성을 제공하기 위한 당단백질 (예를 들어, 알부민, 지질단백질, 글로불린 등) 등을 포함한다. 생리학적으로 허용가능한 담체는 부분적으로, 투여되는 특정 조성물에 의해, 또한 조성물 투여에 이용되는 특정 방법에 의해 결정되기 때문에, 본 발명의 제약 조성물의 폭넓게 다양한 적합한 제제가 존재한다 (예를 들어, 문헌 [Remington: The Science and Practice of Pharmacy, 21st edition, 2005] 참조).
본 발명의 조성물은 널리 공지된 통상의 멸균 기술에 의해 멸균될 수 있거나, 또는 멸균 조건 하에 제조될 수 있다. 수용액을 사용을 위해 패키징하거나 무균 조건 하에 여과하고 동결건조시킬 수 있고, 여기서는 동결건조된 제제를 멸균 수용액과 조합한 후 투여한다. 조성물은 생리학적 조건에 가깝게 되도록 필요에 따라 제약상 허용가능한 보조 성분, 예컨대 pH 조정제 및 완충제, 긴장성 조정제, 습윤제 등, 예를 들어, 아세트산나트륨, 락트산나트륨, 염화나트륨, 염화칼륨, 염화칼슘, 소르비탄 모노라우레이트, 및 트리에탄올아민 올레에이트를 함유할 수 있다. 동결건조된 표적화된 전달 조성물에 대한 안정화제와 같이, 조성물의 안정화를 위해 당이 포함될 수도 있다.
선택된 표적화된 전달 조성물은, 단독으로 또는 다른 적합한 성분과 조합되어, 흡입에 의해 투여되는 에어로졸 제제를 형성할 수 있다 (즉, 이들은 "분무"될 수 있음). 에어로졸 제제는 가압 허용가능한 추진제, 예컨대 디클로로디플루오로메탄, 프로판, 질소 등 내에 배치될 수 있다.
직장 투여에 적합한 제제는, 예를 들어, 좌제 베이스와 함께 유효량의 패키징된 표적화된 전달 조성물을 포함하는 좌제를 포함한다. 적합한 좌제 베이스는 천연 또는 합성 트리글리세리드 또는 파라핀 탄화수소를 포함한다. 또한, 예를 들어, 액체 트리글리세리드, 폴리에틸렌 글리콜, 및 파라핀 탄화수소를 비롯한 베이스와 선택된 표적화된 전달 조성물의 조합을 함유하는 젤라틴 직장 캡슐을 사용할 수도 있다.
예를 들어 관절내 (관절 내로), 정맥내, 근육내, 종양내, 피부내, 복강내, 및 피하 경로 투여와 같은 비경구 투여에 적합한 제제는, 산화방지제, 완충제, 정균제, 및 제제가 의도된 수용자의 혈액과 등장성이 되도록 하는 용질을 함유할 수 있는 수성 및 비-수성 등장성 멸균 주사액, 및 현탁화제, 가용화제, 증점제, 안정화제, 및 보존제를 포함할 수 있는 수성 및 비-수성 멸균 현탁액을 포함한다. 주사액 및 현탁액은 또한 멸균 분말, 과립 및 정제로부터 제조될 수 있다. 본 발명의 실행에서, 조성물은, 예를 들어, 정맥내 주입, 국소, 복강내, 방광내, 또는 경막내 투여될 수 있다. 비경구 투여 및 정맥내 투여가 바람직한 투여 방법이다. 표적화된 전달 조성물의 제제는 단위-용량 또는 다중-용량 밀봉 용기, 예컨대 앰풀 및 바이알 중에 존재할 수 있다.
제약 제제는 바람직하게는 단위 투여 형태로 존재한다. 이러한 형태에서, 제제는 적절한 양의 활성 성분, 예를 들어, 표적화된 전달 조성물을 함유하는 단위 용량으로 세분된다. 단위 투여 형태는 패키징된 제제일 수 있고, 여기서 패키지는 별개의 양의 제제를 함유한다. 조성물은, 요망되는 경우, 다른 상용성 치료제를 또한 함유할 수 있다.
암 치료를 위한 치료 용도에서, 본 발명의 제약 조성물에 사용된 치료제 및/또는 진단제를 포함하는 표적화된 전달 조성물은 매일 약 0.001 mg/kg 내지 약 1000 mg/kg의 초기 투여량으로 투여될 수 있다. 약 0.01 mg/kg 내지 약 500 mg/kg, 또는 약 0.1 mg/kg 내지 약 200 mg/kg, 또는 약 1 mg/kg 내지 약 100 mg/kg, 또는 약 10 mg/kg 내지 약 50 mg/kg의 1일 용량 범위를 이용할 수 있다. 그러나, 투여량은, 환자의 요구, 치료되는 질환의 중증도, 및 사용되는 표적화된 전달 조성물에 따라 달라질 수 있다. 예를 들어, 투여량은 특정 환자에서 진단되는 암의 유형 및 단계를 고려하여 경험적으로 결정될 수 있다. 본 발명의 맥락에서, 환자에게 투여되는 용량은, 시간에 따라 환자에서 유익한 치료 반응을 제공하기에 충분하여야 한다. 용량의 크기는 또한, 특정 환자에서의 특정 표적화된 전달 조성물의 투여에 수반되는 임의의 불리한 부작용의 존재, 성질 및 정도에 의해 결정될 것이다. 특정 상황에서의 적절한 투여량의 결정은 의사의 기술 범위 내에 있다. 일반적으로, 치료는 표적화된 전달 조성물의 최적 용량 미만인 보다 소량의 투여량으로 개시된다. 그 후, 투여량이 상황에 따라 최적 효과가 달성될 때까지 작은 증분으로 증가된다. 편의상, 요망되는 경우, 1일 총 투여량을 분할하여 낮 동안 여러 부분으로 나누어 투여할 수 있다.
일부 실시양태에서, 본 발명의 표적화된 전달 조성물은 질병, 장애, 및/또는 질환의 진단에 사용될 수 있다. 일부 실시양태에서는, 표적화된 전달 조성물을 이용하여 대상체에서의 암 질환, 예컨대 폐암, 유방암, 췌장암, 전립선암, 자궁암, 난소암, 결장암, 간암, 식도암 등을 진단할 수 있다. 일부 실시양태에서, 질병 상태의 진단 방법은 표적화된 전달 조성물을 사용하여 대상체의 체내 종양을 물리적으로 검출하고/거나 위치를 찾아내는 것을 포함할 수 있다. 예를 들어, 종양은 본 발명의 표적화된 전달 조성물의 표적화제에 의해 표적화되는 수용체를 충분히 발현하는 (예를 들어, 세포 표면 상에서 또는 혈관계 내에서) 암과 관련될 수 있다. 일부 실시양태에서는, 표적화된 전달 조성물을 이용하여 암 이외의 질환, 예컨대 증식성 질환, 심혈관 질환, 위장관 질환, 비뇨생식 질환, 신경계 질환, 근골격 질환, 혈액학적 질환, 염증성 질환, 자가면역 질환, 류마티스 관절염 등을 진단할 수도 있다.
본원에 개시된 바와 같이, 본 발명의 표적화된 전달 조성물은 본질적으로 검출가능한 특성을 갖는 진단제를 포함할 수 있다. 대상체에서 진단제 검출시, 표적화된 전달 조성물, 또는 표적화된 전달 조성물이 되는 부분을 갖는 입자의 집단을 대상체에게 투여할 수 있다. 이어서, 단일 광자 방출 컴퓨터 단층촬영 (SPECT), 자기 공명 영상 (MRI), 광학 영상, 양전자 방출 단층촬영 (PET), 컴퓨터 단층촬영 (CT), x-선 영상, 감마선 영상 등과 같은 진단제의 영상화 기술을 이용하여, 대상체를 영상화할 수 있다. 본원에 기재된 임의의 영상화 기술을 다른 영상화 기술과 조합하여 이용할 수 있다. 일부 실시양태에서, 입자 내의 영상화를 위한 방사성 동위원소의 도입은 대상체에서의 표적화된 전달 조성물의 생체내 추적을 가능하게 한다. 예를 들어, 표적화된 전달 조성물의 생물학적 분배 및/또는 제거를 측정하고, 임의로 이를 이용하여 환자의 치료를 변경할 수 있다. 예를 들어, 환자의 치료 및/또는 진단을 최적화하기 위해 보다 많거나 적은 표적화된 전달 조성물이 필요할 수 있다.
표적화된 전달
특정 실시양태에서, 본 발명의 표적화된 전달 조성물은 표적화된 방식으로 대상체에게 전달되어 치료제 또는 진단제를 방출할 수 있다. 예를 들어, 표적화된 전달 조성물은 대상체에서의 표적에 전달되고, 이어서 표적화된 전달 조성물, 예컨대 나노입자 내에 내포되거나 캡슐화되거나, 또는 그에 테더링된 치료제가 표적 부근에서의 용액 조건에 기초하여 전달될 수 있다. 용액 조건, 예컨대 pH, 염 농도 등은 표적 부근의 영역으로의 단기간 또는 장기간의 시간에 걸친 치료제의 방출을 촉발할 수 있다. 다르게는, 효소가 표적화된 전달 조성물로부터 치료제 또는 진단제를 절단하여 방출을 개시할 수 있다. 일부 실시양태에서, 표적화된 전달 조성물은 엔도시토시스에 의해 세포의 내부 영역으로 전달되고, 가능하게는 이후에 세포의 내부 구획, 예컨대 리소좀에서 분해될 수 있다. 당업자는 당업계에 일반적으로 공지되어 있는 다양한 방법을 이용하여 치료제 또는 진단제의 표적화된 전달을 수행할 수 있음을 인지할 것이다.
키트
본 발명은 또한 질병 상태의 치료 및/또는 진단을 위해 대상체에게 표적화된 전달 조성물을 투여하기 위한 키트를 제공한다. 이러한 키트는 전형적으로 질병 상태, 예컨대 암 질환의 치료 및/또는 진단을 위해 필수적인 둘 이상의 구성요소를 포함한다. 구성요소는 본 발명의 표적화된 전달 조성물, 시약, 용기 및/또는 장비를 포함할 수 있다. 일부 실시양태에서, 키트 내의 용기는 사용 전에 방사성표지된 방사성약물을 포함하는 표적화된 전달 조성물을 함유할 수 있다. 키트는 표적화된 전달 조성물의 투여를 위해 필수적인 임의의 반응 성분 또는 완충제를 추가로 포함할 수 있다. 또한, 표적화된 전달 조성물은 동결건조된 형태로 존재하고, 이어서 재구성된 후 투여될 수 있다.
특정 실시양태에서, 본 발명의 키트는 환자의 질병 상태의 치료 및/또는 진단을 위해 사용되는 하나 이상의 구성요소를 포함할 수 있는 패키징 어셈블리를 포함할 수 있다. 예를 들어, 패키징 어셈블리는 본원에 기재된 바와 같은 하나 이상의 표적화된 전달 조성물을 하우징하는 용기를 포함할 수 있다. 별도의 용기가 환자에게 투여되기 전에 표적화된 전달 조성물과 혼합될 수 있는 다른 부형제 또는 작용제를 포함할 수 있다. 일부 실시양태에서, 의사는 특정 환자에게 필요한 치료 또는 진단에 따라 특정 구성요소 및/또는 패키징 어셈블리를 선택하고 매칭할 수 있다.
본원에 기재된 실시양태는 단지 예시를 목적으로 한 것이고, 이를 고려하여 다양한 변형 또는 변화가 당업자에게 시사될 것이며 이것이 본원의 사상 및 범주, 또한 첨부된 특허청구범위의 범주 내에 포함되어야 한다는 것을 이해한다. 본원에서 인용된 모든 공개문헌, 특허, 및 특허 출원은 모든 목적상 그 전문이 참조로 도입된다.
하기 제법 및 실시예는 당업자가 본 발명을 더욱 명확히 이해하고 실행할 수 있도록 하기 위해 제공된 것이다. 이들은 본 발명의 범위를 제한하는 것으로 고려되어선 안되며, 단지 본 발명을 예시하고 대표하는 것으로서 고려되어야 한다.
VI
.
실시예
출발 물질 및 이들 화합물 제조에 사용되는 시약은 일반적으로 상업적 공급원, 예컨대 알드리치 케미칼 컴파니(Aldrich Chemical Co.)로부터 입수가능하거나, 또는 과학 및 특허 문헌 및 참고문헌, 예컨대 문헌 [Fieser and Fieser's Reagents for Organic Synthesis; Wiley & Sons: New York, 1991, Volumes 1-15]; [Rodd's Chemistry of Carbon Compounds, Elsevier Science Publishers, 1989, Volumes 1-5 and Supplementals]; 및 [Organic Reactions, Wiley & Sons: New York, 1991, Volumes 1-40]에 기재된 절차에 따라 당업자에게 일반적으로 공지되어 있는 방법에 의해 제조된다. 하기 합성 반응식은 단지 본 발명의 화합물을 합성할 수 있는 일부 방법의 예이며, 이들 합성 반응식에 대한 다양한 변형이 이루어질 수 있고, 이는 본원에 포함된 개시내용을 참조하여 당업자에게 시사될 것이다.
합성 반응식의 출발 물질 및 중간체는, 요망되는 경우, 여과, 증류, 결정화, 크로마토그래피 등을 포함하나 이에 제한되지는 않는 통상의 기술을 이용하여 단리되고 정제될 수 있다. 이러한 물질은 물리적 상수 및 스펙트럼 데이터를 비롯한 통상의 수단을 이용하여 특성화될 수 있다.
실시예 1
디알킬 히드로겐 포스포네이트의 제조
일반화된 합성 절차를 이용하여 디알킬 히드로겐 포스포네이트를 제조하고, 이를 추가로 반응시켜 본 발명의 화합물의 일부를 형성할 수 있었다. 도 6에 도시된 바와 같이, 일반적 반응식은 디페닐 포스파이트와 1-알칸올을 조합하여 디알킬 히드로겐 포스포네이트를 형성하는 것이었다. 하기 디알킬 히드로겐 포스포네이트를 하기와 같이 제조하였다.
2 내지 5 mL 마이크로파 바이알 내에, 3 내지 6 mmol의 디페닐 포스파이트 및 2.1 당량의 1-알칸올을 첨가하였다. 2 당량 (부피 기준)의 무수 피리딘을 바이알 내에 시린지 주입하고, 상단을 크림핑하여 바이알을 밀봉하였다. 반응 혼합물을 100℃에서 30분 동안 바이오티지(Biotage)™ 개시제 반응기를 사용하여 마이크로파 방사선에 노출시켰다. CDCl3 중의 반응 혼합물을 31P NMR에 의해 완료에 대해 검사하였다.
반응 혼합물을 100 mL 둥근 바닥 플라스크에 옮기고, 70℃에서 회전 증발시켜 용매를 제거하였다. 조 생성물 잔사를, 헥산/에틸 아세테이트 구배를 이용하는 정상 상 실리카 겔 플래쉬 크로마토그래피에 의해 (C12 생성물) 또는 아세톤 중에서의 침전에 의해 (C14 내지 C22 생성물) 정제하였다. 각 경우에, MS 및 NMR 데이터는 목적한 생성물과 일치하였다.
실시예 2
디옥타데실 히드로겐 포스포네이트의 제조
기계적 교반기 및 열전쌍이 장착된 125 mL의 둥근 바닥 플라스크 (RBF)에 1-옥타데칸올 (25.41 g, 0.0939 mol, 2.2 eq.), 디페닐 포스파이트 (10.0 g, 0.0427 mol, 1.0 eq.), 및 피리딘 (4.053 g, 0.5124 mol, 1.2 eq)을 첨가하고, 혼합물을 75℃로 가열하였다. 2.5h 후, 31P NMR (CDCl3)에 의해 반응 완료를 검사하였다: 7.8 ppm에서의 생성물, 4.2 ppm에서의 중간체 모노-옥타데실 페닐 포스포네이트, 0.35 ppm에서의 디페닐 포스페이트. 반응에서 약 94% (적분) 생성물, 1.5% 중간체, 및 4.6%의 5.5 ppm에서의 피크가 나타났다. 혼합물을 40 내지 50℃로 냉각시키고, 약 50 mL 디클로로메탄을 물질이 고화되어 교반기를 중단시키지 않도록 서서히 첨가하였다. 혼합물을 150 mL 디클로로메탄으로 추가로 희석하고, 분별 깔때기로 옮겼다. 혼합물을 50 mL 물로 세척하고, 3 x 75 mL 3N 염산으로 추출하고, 추가로 물 및 염수 각각 75 mL로 세척하였다. 유기 층을 무수 Na2SO4로 건조시키고, 회전 증발기 (rotovap) 상에서 농축시켜 투명한 액체를 수득하였고, 이는 방치시 서서히 고화되었다.
기계적 교반기가 장착된 투명한 250 mL RBF에 100 mL 아세톤을 첨가하였다. 농축된 생성물을 플라스틱 피펫을 통해 주변 온도에서 교반 아세톤에 첨가하였고; 액체가 솜털형 백색 고체로 침전되었다. 혼합물을 1h 동안 교반한 후, 샤크스킨(Sharkskin)™ 페이퍼 층으로 덮인 와트만(Whatman)™ #4 여과지 상에서 여과하여 솜털형 백색 습윤 케이크를 수득하였다. 습윤 케이크를 주변 온도에서 밤새 진공 하에 건조시켰다. 수율: 19.11 g (76.3%). HRMS: [M + H]+ 계산치 587.5525, 실측치 587.5525; [M + Na]+ 계산치 609.5346, 실측치 609.5339. HLPC - MS: 587.25 [M + H]+, 604.17 [M + NH4]+, 609.58 [M + Na]+, 31P NMR (500 MHz, CDCl3) = 7.734 ppm. 1H 및 13C NMR은 목적한 구조와 일치하였다.
다르게는, 초기 반응이 완료된 것으로 여겨진 후에, 250 mL 증류 플라스크 내의 조 반응 혼합물을 쿠겔로(Kugelrohr) 증류 장치에 배치하고, 플라스크를 고 진공 하에 배치하고 대략 1.5시간 기간에 걸쳐 60℃로부터 120℃까지 10℃ 증분으로 쿠겔로 오븐을 점차 가온시키고 120℃에서 3시간 동안 유지함으로써 휘발성 물질을 제거하였다. 증류액 용기를 드라이 아이스/아세톤 배쓰에서 냉각시켰다. 증류 완료 후, 250 mL 증류 플라스크 내의 고온 액화 생성물을 125 mL의 타르 유리 저장 용기에 부었고, 여기서 이는 냉각됨에 따라 고화되었다. 이로부터 생성물을 백색 왁스형 고체로서 수득하였다. 분취량의 상기 고체를 CDCl3 중의 용액으로서 31P NMR 분광법으로 검사하였고, 여기서는 대략 δ 7.72에서 단일 피크가 나타났다. 생성물 중 1H 및 13C NMR에 의해 관찰가능한 유일한 불순물은 출발 1-옥타데칸올이었고, 이는 단리 생성물의 대략 15 mol%를 차지하였다.
실시예 3
디올레일 히드로겐 포스포네이트의 제조
기계적 교반기 및 열전쌍이 장착된 125 mL RBF에 올레일 알콜 (30.85 g, 0.115 mol, 2.2 eq.), 디페닐 포스파이트 (12.23 g, 0.0522 mol, 1 eq.), 및 피리딘 (4.96 g, 0.0627 mol, 1.2 eq.)을 첨가하였다. 혼합물을 3h 동안 65℃로 가열하였다. 31P NMR (CDCl3, 7.76 ppm)에 의해 반응 완료를 검사하였다. 혼합물을 <50℃로 냉각시키고, 50 mL의 디클로로메탄을 첨가하였다. 혼합물을 150 mL의 디클로로메탄으로 추가로 희석하고, 분별 깔때기로 옮겼다. 혼합물을 50 mL 물로 세척하고, 3 x 75 mL 3N 염산으로 추출하고, 추가로 물 및 염수 각각 75 mL로 세척하였다. 유기 층을 무수 Na2SO4로 건조시키고, 농축시켜 무색 오일을 수득하였다. 순수 상태(neat) 오일을 250 mL 분별 깔때기로 옮기고, 6 x 50 mL의 아세토니트릴 (ACN)로 세척하였다. 수율: 19.86 g (65.2%). 고해상 질량 분광측정법 (HRMS): [M + Na]+ 계산치 605.5033, 실측치 605.5015: 31P NMR (500 MHz, CDCl3) = 7.734 ppm. 1H 및 13C NMR은 목적한 구조와 일치하였다.
실시예 4
디콜레스테릴 히드로겐 포스포네이트의 제조
기계적 교반기 및 열전쌍이 장착된 250 mL RBF에 콜레스테롤 (44.42 g, 0.1149 mol), 디페닐 포스파이트 (12.23, 0.0522 mol), 및 피리딘 (4.957, 0.0627 mol)을 첨가하였다. 혼합물을 85 내지 90℃로 가열하였고, 이 시점에 이는 고체로부터 교반가능한 유체 덩어리가 되었다. 밤새 가열 후, 31P NMR (CDCl3)에 의해 반응 완료를 검사하였고, 이는 4.31 ppm에서 주 피크를 가졌으며, 이는 HRMS에 의해 목적 생성물인 것으로 확인되었다. 혼합물을 <50℃로 냉각시키고, 100 mL의 클로로포름을 첨가하여 고체를 용해시켰다. 혼합물을 추가로 150 mL의 클로로포름으로 희석하고, 분별 깔때기로 옮겼다. 혼합물을 50 mL 물로 세척하고, 3 x 50 mL 3N 염산으로 추출하고, 추가로 물 및 염수 각각 50 mL로 세척하였다. 유기 층을 무수 Na2SO4로 건조시키고, rotovap 상에서 농축시켜, 점성 오렌지색 오일을 수득하였다 (이는 방치시 서서히 고화됨).
기계적 교반기가 장착된 투명한 500 mL RBF에 200 mL 아세톤을 첨가하였다. 농축된 생성물을 플라스틱 피펫을 통해 주변 온도에서 교반 아세톤에 첨가하였고; 액체가 솜털형 백색 고체로 침전되었다. 혼합물을 밤새 교반한 후, 와트만™ #4 및 샤크스킨™ 페이퍼 상에서 여과하여 솜털형 회백색 분말을 수득하였다. 습윤 케이크를 주변 온도에서 밤새 진공 하에 건조시켰다. 수율은 29.69 g (69.4%)이었다. HRMS: [M + Na]+ 계산치 841.6598, 실측치 841.6599; 31P NMR (CDCl3) 4.31 ppm; 1H 및 13C NMR은 목적한 구조와 일치하였다.
실시예 5
4-다리 C
18
-PEG
1000
-OMe의 제조
테트라키스(옥타데실)(((2,5,8,11,14,17,20,23,26,29,32,35,38,41,44,47,50,53,56,59,62,65,68,71-테트라코사옥사트리헵타콘탄-73-일)아자네디일)비스(메틸렌))비스(포스포네이트) (본원에서 4-다리 C18-PEG1000-OMe로서 언급됨)
도 7은 4-다리 C18-PEG1000-OMe의 제조를 위한 일반적 반응식을 나타내고, 이는 먼저 상기 실시예 2에 기재된 바와 같이 디옥타데실 히드로겐 포스포네이트를 제조함으로써 제조되었다. 이어서, 4-다리 C18-PEG1000-OMe를 하기와 같이 제조하였다: 삼각 교반 날개가 장착된 10 mL 콘테스(Kontes) 마이크로플렉스 바이알을 디옥타데실 히드로겐 포스포네이트 (1.0 g, 1.704 mmol, 2 eq.), 파라포름알데히드 (76.7 mg, 2.56 mmol, 3 eq.), 및 단분산 PEG1000 (쿠안타 바이오디자인(Quanta Biodesign), 0.927 g, 0.852 mmol, 1 eq.)으로 충전시켰다. 캡을 단단히 돌려서 조이고, 바이알을 75℃로 가온시키고, 24 내지 72시간 동안 교반하였다. 주기적으로, 증발 광 산란 검출기 (ELSD)가 장착된 역상 (C4, 300A) HPLC를 이용하여 분석을 위해 반응을 샘플링하였다. 반응이 불완전한 것으로 여겨지면, 추가의 파라포름알데히드를 첨가하여 목적한 생성물로의 추가 전환을 보조할 수 있다. 반응이 생성물로의 충분한 전환에 도달하면, 반응물을 냉각시키고, 생성된 왁스형 고체를 정제하였다.
조 반응 물질을 음파파쇄 및 약간의 가열을 이용하여 이소프로필 알콜 중에 용해시켰다. 조 용액 (전형적으로 10 내지 15 mg/mL)을 30 mL/min의 유량으로 워터스(Waters) 컬럼 (C4, 300A, 5 ㎛, 19x150 mm) 상에서 역상 크로마토그래피에 의해 정제하였다. 사용된 용매는 아세토니트릴 (0.05% TFA) 및 물 (0.05% TFA)이었다. 이용된 구배 방법을 하기에 나타내었다.
목적한 생성물을 함유하는 분획을 진공 하에 환원시키고, 고체로 동결건조시켰다 (단리 수율: 0.334 g, 이론적 수율: 1.40 g, 퍼센트 수율: 23.8%). LC/MS: [M+H]+ = 2287.7 m/z. 증발 광 산란 검출을 이용한 HPLC 분석: 99 면적 퍼센트. 31P NMR은 목적한 구조와 일치하였다.
실시예
6
4-다리 C
18
-PEG
2000
-OMe의 제조
테트라키스(옥타데실)-(2,5,8,11,14,17,20,23,26,29,32,35,38,41,44,47,50,53,56,59,62,65,68,71,74,77,80,83,86,89,92,95,98,101,104,107,110,113,116,119,122,125,128,131,134-펜타테트라콘타옥사헥사트리아콘타헥탄-136-일 아자네디일)비스(메틸렌)비스(포스포네이트) (본원에서 4-다리 C18-PEG2000-OMe로서 언급됨)
4-다리 C18-PEG2000-OMe의 제조를 위한 합성 단계는 상기 실시예 5에 개시된 것과 유사하였다. 먼저, 실시예 2에 개시된 것과 동일한 방법에 의해 디옥타데실 히드로겐 포스포네이트를 제조하였다. 다음으로, 하기와 같이 4-다리 C18-PEG2000-OMe를 제조하였다: 삼각 교반 날개가 장착된 10 mL 콘테스 마이크로플렉스 바이알을 디옥타데실 히드로겐 포스포네이트 (0.587 g, 1.0 mmol, 2 eq.), 파라포름알데히드 (90.1 mg, 3.0 mmol, 6 eq.), 및 다분산 PEG2000 (나녹스(NANOCS)) (1.0 g, 0.50 mmol, 1 eq.)으로 충전시켰다. 캡을 단단히 돌려서 조이고, 바이알을 75℃로 가온시키고, 24 내지 72시간 동안 교반하였다. 주기적으로, 소량 샘플을 회수하고, 이소프로판올 (IPA)/물 중에 용해시키고, ELSD 검출기가 장착된 역상 (C4, 300A) 고성능 액체 크로마토그래프 (HPLC)를 이용하여 분석하였다. 반응이 불완전한 것으로 여겨지면, 추가의 파라포름알데히드를 첨가하여 목적한 생성물로의 추가 전환을 보조할 수 있다. 반응이 생성물로의 충분한 전환에 도달하면, 반응물을 냉각시키고, 생성된 왁스형 고체를 정제하였다.
조 반응 물질을 음파파쇄 및 약간의 가열을 이용하여 IPA/물 (~3 내지 5% 물) 중에 용해시켰다. 조 용액은 전형적으로 15 내지 25 mg/mL였다. C4 실리카 패킹 (5 ㎛, 300A)을 함유하는 컬럼 상의 역상 크로마토그래피에 의해 목적한 생성물을 수득하였다. 사용된 용매는 ACN (0.05% 트리플루오로아세트산 (TFA)) 및 물 (0.05% TFA)이었다. 30 mL/min의 유량으로 워터스™ 컬럼 (C4, 5 ㎛, 19x150 mm)과 함께 이용된 구배 방법을 하기에 나타내었다.
목적한 생성물을 함유하는 분획을 진공 하에 환원시키고, 동결건조에 의해 단리하였다. 단리 수율 (순수 물질): 0.335 g (20.8%). 고해상 MS: 모사 질량 스펙트럼 [M+2Na]2+ = 1628.1472; 검출 질량 스펙트럼 [M+2Na]2+ = 1628.1491. HPLC ( ELSD): 단일 피크: 체류 시간 (~7.88분) = >98 면적 퍼센트. LC/MS: [M+Na]2+ = 1616.9 m/z. 31P NMR은 목적한 구조와 일치하였다.
실시예 7
4-다리 C
14
-PEG
1000
-OMe의 제조
테트라키스(테트라데실)(((2,5,8,11,14,17,20,23,26,29,32,35,38,41,44,47,50,53,56,59,62,65,68,71-테트라코사옥사트리헵타콘탄-73-일)아자네디일)비스(메틸렌))비스(포스포네이트) (본원에서 4-다리 C14-PEG1000-OMe로서 언급됨)
절차는, 디옥타데실 히드로겐 포스포네이트 대신에 디테트라데실 히드로겐 포스포네이트를 사용하고, 하기 양을 사용한 것을 제외하고는, 실시예 5에서의 4-다리 C18-PEG1000-OMe에 대한 것과 동일하였다: 디테트라데실 히드로겐 포스포네이트 (0.404 g, 0.852 mmol, 2 eq.), 파라포름알데히드 (0.077 g, 2.56 mmol, 6 eq.), 및 단분산 PEG1000 (쿠안타 바이오디자인™) (0.464 g, 0.426 mmol, 1 eq.). 워터스™ 컬럼 (C4, 300A, 5 ㎛, 19x150 mm) 상에서의 역상 크로마토그래피 후, 목적한 생성물을 함유하는 분획을 합하고, 진공 하에 환원시키고, 반-고체로 동결건조시켰다; 단리 수율 0.496 g (56.5%). ELSD 검출을 이용한 HPLC 분석: >99 면적%. 31P NMR은 목적한 구조와 일치하였다.
실시예 8
다른 4-다리 알킬-PEG 포스포네이트 컨쥬게이트의 제조
다른 4-다리 알킬-PEG 포스포네이트 컨쥬게이트를 또한 제조할 수 있다. 실시예 1에서 일반적 반응식에 기재된 바와 같이, 디알킬 (예를 들어, C12, C16, 및 C22) 히드로겐 포스포네이트를 제조할 수 있다. 이어서, 실질적으로 실시예 6에 기재된 절차를 이용하여 C12-, C16-, 및 C22-PEG1000-OMe 포스포네이트 컨쥬게이트를 제조할 수 있다. 그러나, 1-옥타데칸올을 사용하는 것 대신에, 반응은 C12-, C16-, 및 C22-PEG1000-OMe 컨쥬게이트에 대해 1-도데칸올, 1-헥사데칸올 및 1-도코산올을 각각 포함할 수 있고, 이들 각각을 하기에 나타내었다. HRMS 및/또는 LRMS 및 31P NMR은 이들 유도체 각각의 목적한 구조와 일치하였다.
테트라키스(도데실)(((2,5,8,11,14,17,20,23,26,29,32,35,38,41,44,47,50,53,56,59,62,65,68,71-테트라코사옥사트리헵타콘탄-73-일)아자네디일)비스(메틸렌))비스(포스포네이트) (C12/PEG1000 단분산). 화학식: C99H203NO30P2, 분자량: 1949.61 g/mol.
테트라키스(헥사데실)(((2,5,8,11,14,17,20,23,26,29,32,35,38,41,44,47,50,53,56,59,62,65,68,71-테트라코사옥사트리헵타콘탄-73-일)아자네디일)비스(메틸렌))비스(포스포네이트) (C16/PEG1000 단분산). 화학식: C115H235NO30P2, 분자량: 2174.03 g/mol.
테트라키스(도코실)(((2,5,8,11,14,17,20,23,26,29,32,35,38,41,44,47,50,53,56,59,62,65,68,71-테트라코사옥사트리헵타콘탄-73-일)아자네디일)비스(메틸렌))비스(포스포네이트) (C22/PEG1000 단분산). 화학식: C139H283NO30P2, 분자량: 2510.67 g/mol.
유사하게, 다양한 길이의 PEG 분자 (예를 들어, PEG100 내지 PEG10000 또는 보다 높은 MW PEG)를 갖는 컨쥬게이트를 상기에 기재된 일부 단계에 따라 제조할 수 있다. 예를 들어, PEG1000 대신에 다분산 PEG5000을 사용한 것을 제외하고는, 실시예 6에서의 단계에 따라 4-다리 C18 포스포노-메틸 아미노-PEG5000-OMe 컨쥬게이트를 제조할 수 있다. 4-다리 C18 포스포노-메틸 아미노-PEG5000-OMe 컨쥬게이트에 대한 화학 구조는 하기와 같다:
테트라키스(옥타데실)-(2,5,8,11,14,17,20,23,26,29,32,35,38,41,44,47,50,53,56,59,62,65,68,71,74,77,80,83,86,89,92,95,98,101,104,107,110,113,116,119,122,125,128,131,134,137,140,143,146,149,152,155,158,161,164,167,170,173,176,179,182,185,188,191,194,197,200,203,206,209,212,215,218,221,224,227,230,233,236,239,242,245,248,251,254,257,260,263,266,269,272,275,278,281,284,287,290,293,296,299,302,305,308,311,314,317,320,323,326,329,332,335,338,341,344,347-헥사데카헥타옥사펜타콘타트릭탄-349-일)아자네디일)비스(메틸렌)비스(포스포네이트). 화학식: C305H615NO121P2, 정확한 질량: 6291.15, 분자량: 6295.03 g/mol.
실시예 9
디(2,5,8,11,14,17,20,23,26,29,32-운데카옥사테트라트리아콘탄-34-일) 포스포네이트
2,5,8,11,14,17,20,23,26,29,32-운데카옥사테트라트리아콘탄-34-올 (2.00 g, 3.87 mmol)을 둥근 바닥 플라스크 내에서 톨루엔 중에 용해시켰다. 용액을 공비 증류에 의해 건조시켰다. 이어서, 잔류 톨루엔을 스트리핑하였다. 이어서, 피리딘 (0.092 g, 1.16 mmol) 및 디페닐포스파이트 (0.45 g, 1.94 mmol)를 첨가하였다. 혼합물을 65℃에서 16시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 15 mL 디클로로메탄 중에 용해시키고, 30분 동안 3.0 g의 도웩스(Dowex) WBA 수지와 교반하였다. 디클로로메탄 용액을 수지 비드로부터 여과하고, 휘발성 물질을 증발시켜 황색 오일을 얻었다. 오일을 1,2,4-트리메틸벤젠 중에 용해시키고, 휘발성 물질을 감압 하에 제거하면서 페놀 부산물을 공비 제거하였다. 목적한 생성물 (1.34 g)을 오일로서 수득하였다. HRMS: 계산치: (M+2Na)/2 = 562.2842, (M+Na) = 1101.5792, 실측치: (M+2Na)/2 = 562.2818, (M+Na) = 1101.5751. 31P NMR: 9.22 ppm. 1H NMR, 13C NMR, 및 13C APT NMR은 구조와 일치하였다. 화학식: C46H95NO25P, 분자량: 1078.59 g/mol.
실시예 10
3-(((2-(비스((디(2,5,8,11,14,17,20,23,26,29,32-운데카옥사테트라트리아콘탄-34-일)포스포릴)메틸)아미노)에톡시)(히드록시)포스포릴)옥시)프로판-1,2-디일 디스테아레이트
DSPE (1,2-디스테아로일-sn-글리세로-3-포스포에탄올아민, 0.45 g, 0.60 mmol), 실시예 9에서 제조된 디(2,5,8,11,14,17,20,23,26,29,32-운데카옥사테트라트리아콘탄-34-일) 포스포네이트 (1.34 g,1.24 mmol), 파라포름알데히드 (0.054 g, 1.81 mmol의 포름알데히드), 및 디메틸포름아미드 (2.0 mL)를 섬광 바이알에 첨가하였다. 바이알을 캡핑하고, 75℃에서 24시간 동안 가열하였다. 반응 혼합물을 스트리핑하고, 메탄올 중에 용해시키고, 도웩스 WBA 수지 (1.0 g)로 처리하였다. 메탄올 용액을 수지 비드로부터 여과하고, 스트리핑하여 황색 오일을 얻었다. 오일을 15 mL의 80/20 물/이소프로필 알콜 중에 용해시키고, 물/이소프로필 알콜 용출제을 사용하여 그레이스 비닥 프로테인(Grace Vydac Protein) C-4 역상 패킹으로 로딩된 컬럼으로 크로마토그래피하였다. 목적한 분획을 동결 및 동결건조시켜 0.337 g의 표적 화합물을 백색 분말로서 수득하였다. LRMS 실측치: (M+2H)/2 = 1465, (M+2Na)/2 = 1487, (M+3H)/3 = 977. HRMS: 계산치: (M-H) 2927.7505, 실측치: (M-H) 2927.7570. 31P NMR 실측치 25.96 ppm 및 -0.21 ppm. 1H NMR, 13C NMR, 및 13C APT NMR은 구조와 일치하였다. 목적한 생성물 피크에 대한 HPLC 분석 (ELSD) 실측치 99.8 면적%. 화학식: C135H272NO58P3, 분자량: 2928.76 g/mol.
실시예
11
테트라페닐-(2-메톡시에틸아자네디일)비스(메틸렌)디포스포네이트. 화학식: C29H31NO7P2, 정확한 질량: 567.16, 분자량 567.51 g/mol.
하기 절차를 이용하여 상기 화합물을 제조하였다. 2-메톡시에틸아민 (3 g, 40 mmol; 3.44 mL)을 포름알데히드 (2.4 g; 320 mmol, H2O 중 37% 6.5 mL) 및 디메틸포름아미드 (DMF) (30 mL)와 조합하였다. 혼합물에 디페닐포스파이트 (DPP) (20.6 g, 88 mmol; 2.2 equiv.)를 서서히 첨가하였다. 짧은 초기 발열 반응 후, 혼합물을 실온에서 12시간 동안 교반하였다. HPLC에서는 완전한 반응이 나타났고, 이어서 DMF를 증발시켰다. 잔사를 에틸 아세테이트 (EA) (200 mL) 중에 용해시키고, sat. KHSO4 및 염수로 세척하였다. 층을 분리하고, 유기 층을 Na2SO4로 건조시키고, 여과하고, 휘발성 물질을 회전 증발기 상에서 진공 하에 제거하였다. 잔류 오일을 EA/헥산 혼합물 (1:4) 중에 용해시키고, 실리카 플러그로 여과하였다. 이어서, EA/헥산 혼합물 (1:1)을 사용하여 실리카에서 생성물을 용출시켰다. 용매를 증발시켜, 15.6 g (27 mmol; 69%)을 투명 오일로서 수득하였다. LC/MS: MH+=568.2 1H 및 31P NMR은 구조와 일치하였다.
실시예 12
테트라옥타데실-(2-메톡시에틸아자네디일)비스(메틸렌)디포스포네이트. 화학식: C77H159NO7P2, 정확한 질량: 1272.16, 분자량: 1273.04 g/mol.
실질적으로 실시예 11의 절차를 이용하여 상기 분자를 제조하되, 디페닐포스파이트 (DPP) 대신에 디테트라데실 히드로겐 포스포네이트를 사용하였고, 반응을 반응 바이알 (10 mL) 및 테플론 코팅된 스핀 날개를 사용하여 실시예 5에서와 같이 DMF 용매 없이 (즉, 무용매로) 진행시켰고, 실시예 5에 기재된 바와 같이 후처리 및 단리하였다.
실시예 13
3-(비스((비스(옥타데실옥시)포스포릴)메틸)아미노)프로판산. 화학식: C77H157NO8P2, 정확한 질량: 1286.14, 분자량 1287.02 g/mol.
상기 화합물을 하기와 같이 제조하였다: 디옥타데실 포스포네이트 (5.87 g, 10 mmol)를 압력 용기에서 2일 동안 교반하며 80℃에서 DMF (20 mL) 중의 β-알라닌 (0.45 g, 5 mmol) 및 포름알데히드 (물 중 37% 용액 6 mL)와 반응시켰다. 반응 혼합물을 제거하고, 휘발성 물질을 주의깊게 증발시키고, 잔사를 CHCL3 (200 mL) 중에 용해시켰다. 유기 층을 10% KHSO4 및 염수 (각각 50 ml)로 세척하였다. 유기 상을 MgSO4로 건조시키고, 여과하고 증발시켜 오일을 얻었다. 몇 시간 교반 후에 잔류 오일을 ~100 mL 아세톤과 혼합하였고, 미세 백색 침전물이 여과되었다. 수율: 5.4 g (4.2 mmol: 84%) (조 물질로서). 31P NMR 24.503 ppm. HRMS: 계산치 MH+ 1287.1384; 실측치 MH+=1287.1477.
실시예 14
2-(비스((비스(옥타데실옥시)포스포릴)메틸)아미노)아세트산. 화학식: C76H155NO8P2, 정확한 질량: 1272.12, 분자량: 1272.99 g/mol.
실시예 13과 유사하게, 디옥타데실 포스포네이트를 DMF 중의 글리신 및 포름알데히드와 반응시킴으로써 상기 화합물을 제조하였다. 생성물을 실시예 13에 나타낸 것과 유사한 방식으로 단리하였다. 구조를 31P NMR 및 HRMS로 확인하였다.
실시예 15
테트라옥타데실 (78-메틸-75-옥소-2,5,8,11,14,17,20,23,26,29,32,35,38,41,44,47,50,53,56,59,62,65,68,71-테트라코사옥사-74,78-디아자노나헵타콘탄-79-일)비스(메틸렌)디포스포네이트. 화학식: C126H256N2O31P2, 분자량: 2357.32 g/mol.
3-(비스((비스(옥타데실옥시)포스포릴)메틸)아미노)프로판산 (128 mg, 0.1 mmol)을 TBTU (O-(벤조트리아졸-1-일)-N,N,N',N'-테트라메틸우로늄 테트라플루오로보레이트) (48 mg, 0.15 mmol) 및 DIPEA (N,N-디이소프로필에틸아민) (0.175 mL)의 존재 하에 DCM (20 mL) 중의 m-dPEG24-아민 (108 mg, 0.1 mmol)과 커플링하였다. (도 8 참조). 실온에서 12시간 동안 교반한 후, 혼합물을 디클로로메탄 (DCM) (100 mL)으로 희석하고, 10% KHSO4 및 염수로 세척하였다. DCM 용액을 Na2SO4로 건조시키고, 여과하고, 용매를 증발시켜 220 mg의 투명 오일을 수득하였고 (조 물질로서), 이를 C4, 300A rphplc로 정제하고 동결건조시켜 목적한 생성물을 수득할 수 있었다. MS: M+Na+ =2,379.73이었고, 31P NMR은 구조와 일치하였다.
실시예 16
디옥타데실 (78-메틸-75-옥소-2,5,8,11,14,17,20,23,26,29,32,35,38,41,44,47,50,53,56,59,62,65,68,71-테트라코사옥사-74,78-디아자노나헵타콘탄-79-일) 포스포네이트 (C18/N-메틸 베타-알라닌/PEG1000). 화학식: C90H183N2O28P, 정확한 질량: 1771.27, 분자량: 1772.39 g/mol.
실시예 13에서 형성된 3-(비스((비스(옥타데실옥시)포스포릴)메틸)아미노)프로판산을, 실시예 15에 기재된 것과 실질적으로 동일한 반응 조건 및 정제 절차를 이용하여 TBTU의 존재 하에 m-dPEG24-아민과 반응시킴으로써 상기 화합물을 합성할 수 있다.
실시예 17
디옥타데실 (78-카르복실-75-옥소-2,5,8,11,14,17,20,23,26,29,32,35,38,41,44,47,50,53,56,59,62,65,68,71-테트라코사옥사-74,78-디아자노나헵타콘탄-79-일) 포스포네이트 (C18/N-메틸 베타-알라닌/PEG1000 카르복실레이트). 화학식: C92H185N2O30P, 정확한 질량: 1829.27, 분자량: 1830.42 g/mol.
실시예 13에서 형성된 3-(비스((비스(옥타데실옥시)포스포릴)메틸)아미노)프로판산을, 실시예 15에 기재된 것과 실질적으로 동일한 반응 조건 및 정제 절차를 이용하여 TBTU의 존재 하에 아미노-PEG24-카르복실레이트 에스테르와 반응시켜 에스테르를 얻음으로써 상기 화합물을 합성할 수 있다. 에스테르의 산으로의 가수분해는 염기성 또는 산성 조건 하에 달성될 수 있고, 생성물 카르복실레이트를 C4 역상 HPLC에 의해 단리하고, 동일 분획을 합하여 동결건조시켜 실질적으로 순수한 생성물을 수득하였다.
실시예 18
디옥타데실 158-메틸-77,155-디옥소-2,4,7,10,13,16,19,22,25,28,31,34,37,40,43,46,49,52,55,58,61,64,67,70,73,80,82,85,88,91,94,97,100,103,106,109,112,115,118,121,124,127,130,133,136,139,142,145,148,151-펜타콘타옥사-76,154,158-트리아자노나펜타콘타헥탄-159-일포스포네이트 (C18/N-메틸 베타-알라닌/PEG1000 아미드 연결된 PEG1000).
실시예 15의 생성물을 이용하고, 실질적으로 실시예 15의 커플링 절차 및 정제 절차를 이용하여 이를 아미노-PEG OMe (1000 MW)와 반응시킴으로써 상기 화합물을 제조할 수 있다.
실시예 19
2-(((비스((3S,8S,9S,10R,13R,14S,17R)-10,13-디메틸-17-((R)-6-메틸헵탄-2-일)-2,3,4,7,8,9,10,11,12,13,14,15,16,17-테트라데카히드로-1H-시클로펜타[a]페난트렌-3-일옥시)포스포릴)메틸)(메틸)아미노)아세트산 (디콜레스테롤/사르코신). 화학식: C58H98NO5P, 정확한 질량: 919.72, 분자량: 920.38 g/mol.
상기 화합물을 하기와 같이 제조하였다: 디콜레스테릴 히드로겐 포스포네이트 (5.0 g, 0.006 mol)를 75℃에서 DMF 중의 사르코신 (0.54 g, 0.006 mol) 및 포름알데히드 (2.2 g, 0.03 mol)와 불균질 혼합물로서 반응시켰다. 75℃에서 4시간 후, 목적한 디콜레스테롤포스포닐 메틸 사르코신으로의 9% 전환율을 얻었다. 포름알데히드의 또 다른 부분 (2.2 g, 0.03 mol)을 첨가하고, 반응 온도를 85℃로 증가시켰다. 85℃에서 16시간 후, 목적한 2-(((비스((3S,8S,10R,13R,17R)-10,13-디메틸-17-((R)-6-메틸헵탄-2-일)-테트라데카히드로-2,3,4,7,8,9,10,11,12,13,14,15,16,171H-시클로펜타[a]페난트렌-3-일옥시)포스포릴)메틸)(메틸)아미노)아세트산으로의 55% 전환율을 얻었고, 냉각시킴에 따라 반응 혼합물로부터 황색 고체가 침전되었다. 생성물을 여과에 의해 단리하고 (황색 고체) 31P NMR에 의해 정체를 확인하였다 (22.5 ppm). 조 2-다리(dipodal) 콜레스테롤 사르코신 (700 mg)을, 95% 클로로포름 / 5% MeOH를 사용하여 실리카 겔 (15 g) 상에서 정제하였다.
실시예 20
2-(((비스(옥타데실옥시)포스포릴)메틸)(메틸)아미노)아세트산 (C18/사르코신). 화학식: C40H82NO5P, 정확한 질량: 687.59, 분자량: 688.06 g/mol.
상기 화합물을 하기와 같이 제조하였다: 기계적 교반기 및 열전쌍이 장착된 RBF (250 mL)에, 75℃에서 N,N-디메틸포름아미드 (50 mL) 중의 디옥타데실 히드로겐 포스포네이트 (1.98 g, 0.003 mol), 사르코신 (0.30 g, 0.003 mol) 및 포름알데히드 (1.1 g, 0.013 mol)를 첨가하였다. 2시간 후, 31P NMR (24.4 ppm)에 의해 2-((비스(옥타데실옥시)포스포릴)(메틸)아미노)아세트산으로의 76% 전환율이 나타났다. 반응을 75℃에서 추가의 4시간 동안 계속하여 88.5% 전환율을 얻었다. 이 시점에 반응 혼합물을 주변 온도로 냉각시켜, 엷은 오렌지색 슬러리를 수득하였다. 물 (50 mL)을 첨가하고, 혼합물을 주변 온도에서 추가의 30분 동안 교반하였다. 여과에 의해 생성물이 엷은 오렌지색 고체로서 단리되었다. 고체를 밤새 30 내지 40℃에서 오븐에서 건조시켰다 (2.0 g). 31P NMR (24.3 ppm)에 의해 단리된 고체에 대해 2-다리 C18 사르코신의 81.3%의 최종 순도가 확인되었다. HPLC-MS (689.6 M + H +). 13C 및 1H NMR은 지정된 구조와 일치하였다.
실시예 21
3-(((비스(옥타데실옥시)포스포릴)메틸)(메틸)아미노)프로판산 (C18/N-메틸 베타-알라닌). 화학식: C41H84NO5P, 정확한 질량: 701.61, 분자량: 702.08 g/mol.
실시예 20에서와 실질적으로 동일한 절차를 이용하되, 사르코신을 메틸 베타-알라닌으로 대체하여 상기 화합물을 제조하였다. C4 역상 HPLC 정제 및 단리 후, 예상된 MS 및 31P NMR이 얻어졌다.
실시예 22
2-(((비스((Z)-옥타데스-9-에닐옥시)포스포릴)메틸)(메틸)아미노)아세트산 (C18 올레일/사르코신). 화학식: C40H78NO5P, 정확한 질량: 683.56, 분자량: 684.02 g/mol.
상기 화합물을 하기와 같이 제조하였다: 기계적 교반기 및 열전쌍이 장착된 RBF (250 mL)에, 75℃에서 N,N-디메틸포름아미드 (50 mL) 중의 디올레일 히드로겐 포스포네이트 (1.96 g, 0.003 mol), 사르코신 (0.30 g, 0.003 mol) 및 포름알데히드 (1.1 g, 0.013 mol)를 첨가하였다. 반응을 75℃에서 4시간 동안 진행시켰다. 31P NMR (~24 ppm)에서 목적한 2-((비스((Z)-옥타데스-9-에닐옥시)포스포릴)(메틸)아미노)아세트산으로의 대략 89% 전환율이 나타났다. 반응 혼합물을 밤새 주변 온도로 냉각시키고, 이어서 증발시켜 오일을 얻었다. 13C 및 1H NMR 및 LCMS로 생성물을 확인하였다.
실시예 23
2-((1-(비스(옥타데실옥시)포스포릴)-3-에톡시-3-옥소에틸)(메틸)아미노)아세트산. 화학식: C43H86NO7P, 정확한 질량: 759.61419, 분자량: 760.12 g/mol.
25 mL 둥근 바닥 플라스크 내에서, 4 mL 톨루엔 및 4 mL 디메틸 술폭시드 중의 사르코신 (0.21 g, 2.3 mmol), 디옥타데실 히드로겐 포스포네이트 (0.69 g, 1.2 mmol), 1-옥타데칸올 (0.63 g, 2.3 mmol) 및 에틸 글리옥살레이트 (0.36 g, 1.8 mmol)를 아르곤 하에 100℃에서 16h 동안 교반하였다. CDCl3 중의 반응 혼합물을 31P NMR로 검사하였고, 여기서 상당한 목적한 생성물의 존재 (24.8 ppm)가 나타났다. 반응 혼합물을 클로로포름/이소프로판올 (5% 수산화암모늄 함유)의 구배를 이용하여 정상 상 플래쉬 크로마토그래피에 의해 정제하였고, 목적한 2-((1-(비스(옥타데실옥시)포스포릴)-3-에톡시-3-옥소에틸)(메틸)아미노)아세트산을 수득하였다.
실시예 24
2-(((비스(옥타데실옥시)포스포릴)(포스포노)메틸)(메틸)아미노) 아세트산. 화학식: C40H83NO8P2, 분자량: 768.04 g/mol.
실질적으로 실시예 23의 절차에 따르되, 유사한 비율로 에틸 글리옥실레이트를 포르밀 포스폰산 (문헌 [Wagenknecht, J.H., Journal of the Electrochemical Society (1976), 123(5), 620-4], US4568432, 및 WO9850391)으로 대체하여 표제 화합물을 제조할 수 있다.
Claims (40)
- 하기 화학식의 화합물.
상기 식에서,
L1, L2, L3 및 L4는 각각 독립적으로 결합 및 연결기로 이루어진 군으로부터 선택되고;
R1은 나노입자, 부착 성분, 표적화제, 진단제, 스텔스제, 및 4-다리 제시 성분(tetrapodal presentation component)으로 이루어진 군으로부터 선택되고;
R2는 각각 독립적으로 스텔스제, C1-C10 알킬, 카르복실산 또는 에스테르, 포스폰산 또는 에스테르, 술폰산 또는 에스테르, 및 히드록시로 이루어진 군으로부터 선택되고;
R3 및 R4는 각각 독립적으로 H, 나노입자, 부착 성분, 표적화제, 진단제, 및 스텔스제로 이루어진 군으로부터 선택되고, 여기서 R3 또는 R4 중 적어도 하나는 H 이외의 것이고;
n은 0 내지 2의 정수이다. - 제1항에 있어서, L1, L2, L3, 및 L4 중 적어도 하나가 친수성의 비-면역원성 수용성 연결기인 화합물.
- 제2항에 있어서, 친수성의 비-면역원성 수용성 연결기가 폴리에틸렌 글리콜, 폴리프로필렌 글리콜, 폴리비닐 알콜, 폴리카르복실레이트, 폴리사카라이드 및 덱스트란으로 이루어진 군으로부터 선택되는, 화합물.
- 제1항에 있어서, 표적화제가 앱타머인 화합물.
- 제1항에 있어서, 진단제가 방사능 작용제, 형광제, 또는 콘트라스트제인 화합물.
- 제1항에 있어서, 스텔스제가 덴드리머, 폴리알킬렌 옥시드, 폴리비닐 알콜, 폴리카르복실레이트, 폴리사카라이드 및 히드록시알킬 전분으로 이루어진 군으로부터 선택되는, 화합물.
- 제6항에 있어서, 스텔스제가 폴리알킬렌 옥시드인 화합물.
- 제7항에 있어서, 폴리알킬렌 옥시드가 PEG100 내지 PEG10000 범위의 폴리에틸렌 글리콜 (PEG)인 화합물.
- 제6항에 있어서, 폴리알킬렌 옥시드가 PEG100, PEG500, PEG1000, PEG2000, PEG5000 및 PEG10000으로 이루어진 군으로부터 선택된 폴리에틸렌 글리콜 (PEG)인 화합물.
- 제1항에 있어서, 스텔스제가 연결기와 함께 연결된 2개 이상의 PEG 분자를 포함하는, 화합물.
- 제1항에 있어서, R3 및 R4가 각각 독립적으로 지질 및 콜레스테롤로 이루어진 군으로부터 선택되는, 화합물.
- 제1항에 있어서, R1이 스텔스제이고; R3 및 R4가 각각 부착 성분이고 독립적으로 지질 및 콜레스테롤로 이루어진 군으로부터 선택되며, 여기서 부착 성분은 나노입자에 부착되는, 화합물.
- 제13항에 있어서, 지질이 포화 또는 불포화 C10-C22 알킬인 화합물.
- 제14항에 있어서, n이 0인 화합물.
- 제1항에 있어서, R1이 부착 성분이고; R3 및 R4가 독립적으로 표적화제, 진단제 및 스텔스제로 이루어진 군으로부터 선택되는, 화합물.
- 제1항에 있어서, R1이 PEG100, PEG500, PEG1000, PEG2000, PEG5000 및 PEG10000으로 이루어진 군으로부터 선택된 스텔스제인 화합물.
- 제1항에 있어서, R1이 부착 성분이고, 부착 성분이 인지질인 화합물.
- 제1항에 있어서, R1 및 R2가 각각 스텔스제이고; R3 및 R4가 각각 독립적으로 지질 및 콜레스테롤로 이루어진 군으로부터 선택된 부착 성분이고; n이 1인 화합물.
- 화학식: H2N(L1)-(R1)을 갖는 1급 아민 화합물, 화학식: O=C[(L2)-(R2)]n을 갖는 카르보닐 화합물, 및 화학식:
을 갖는 H-포스포네이트 화합물을, 화학식:
을 갖는 포스포네이트 컨쥬게이트
(상기 식에서,
L1, L2, L3 및 L4는 각각 독립적으로 결합 및 연결기로 이루어진 군으로부터 선택되고;
R1은 나노입자, 부착 성분, 표적화제, 진단제, 스텔스제, 및 4-다리 제시 성분으로 이루어진 군으로부터 선택되고;
R2는 각각 독립적으로 스텔스제, C1-C10 알킬, 카르복실산 또는 에스테르, 포스폰산 또는 에스테르, 술폰산 또는 에스테르, 및 히드록시로 이루어진 군으로부터 선택되고;
R3 및 R4는 각각 독립적으로 H, 부착 성분, 표적화제, 진단제, 및 스텔스제로 이루어진 군으로부터 선택되고, 여기서 R3 또는 R4 중 적어도 하나는 H 이외의 것이고;
n은 0 내지 2의 정수이고, 여기서 n이 0 또는 1인 경우 카르보닐 화합물은 알데히드임)를 형성하기에 충분한 조건 하에 조합하는 것
을 포함하는, 포스포네이트 컨쥬게이트의 제조 방법. - 제21항에 있어서, 1급 아민 화합물, 카르보닐 화합물, 및 H-포스포네이트 화합물을 각각 1:2:2의 몰비로 조합하는, 방법.
- 제21항에 있어서, 1급 아민 화합물 및 카르보닐 화합물을 조합한 후, H-포스포네이트 화합물과 조합하는, 방법.
- 제21항에 있어서, H-포스포네이트 화합물 및 카르보닐 화합물을 조합한 후, 1급 아민 화합물과 조합하는, 방법.
- 제21항에 있어서, 2개의 H-포스포네이트 화합물을 리포솜의 이중층과 인접 회합시킨 후, 1급 아민 화합물 및 카르보닐 화합물과 조합하고, 여기서 R3 및 R4는 각각 독립적으로 지질 및 콜레스테롤로 이루어진 군으로부터 선택되는, 방법.
- 하기 화학식의 화합물.
상기 식에서,
L1, L2, L3 및 L4는 각각 독립적으로 결합 및 연결기로 이루어진 군으로부터 선택되고;
R1은 나노입자, 부착 성분, 표적화제, 진단제 및 스텔스제로 이루어진 군으로부터 선택되고;
R2는 독립적으로 스텔스제, C1-C10 알킬, 카르복실산 또는 에스테르, 포스폰산 또는 에스테르, 술폰산 또는 에스테르, 및 히드록시로 이루어진 군으로부터 선택되고;
R3 및 R4는 각각 독립적으로 H, 나노입자, 부착 성분, 표적화제, 진단제, 및 스텔스제로 이루어진 군으로부터 선택되고, 여기서 R3 또는 R4 중 적어도 하나는 H 이외의 것이고;
R9는 C1-C10 알킬 기이고;
n은 0 내지 2의 정수이다. - 제26항에 있어서, R3 및 R4가 각각 독립적으로 지질 및 콜레스테롤로 이루어진 군으로부터 선택되고; L3 및 L4가 각각 결합인 화합물.
- 제27항에 있어서, 지질이 포화 또는 불포화 C10-C22 알킬인 화합물.
- 제26항에 있어서, R1이 스텔스제인 화합물.
- 제29항에 있어서, 스텔스제가 PEG100, PEG500, PEG1000, PEG2000, PEG5000 및 PEG10000으로 이루어진 군으로부터 선택되는, 화합물.
- 제26항에 있어서, R9가 C1-C6 알킬이고, L1이 결합인 화합물.
- 화학식: HN[(L1)-(R1)](R5)을 갖는 2급 아민 화합물, 화학식: O=C[(L2)-(R2)]n을 갖는 카르보닐 화합물, 및 화학식:
을 갖는 H-포스포네이트 화합물을, 화학식:
을 갖는 포스포네이트 컨쥬게이트
(상기 식에서,
L1, L2, L3 및 L4는 각각 독립적으로 결합 및 연결기로 이루어진 군으로부터 선택되고;
R1은 나노입자, 부착 성분, 표적화제, 진단제 및 스텔스제로 이루어진 군으로부터 선택되고;
R2는 독립적으로 스텔스제, C1-C10 알킬, 카르복실산 또는 에스테르, 포스폰산 또는 에스테르, 술폰산 또는 에스테르, 및 히드록시로 이루어진 군으로부터 선택되고;
R3 및 R4는 각각 독립적으로 H, 부착 성분, 표적화제, 진단제, 및 스텔스제로 이루어진 군으로부터 선택되고, 여기서 R3 또는 R4 중 적어도 하나는 H 이외의 것이고;
R9는 C1-C10 알킬 기로 이루어진 군으로부터 선택되고;
n은 0 내지 2의 정수이고, 여기서 n이 0인 경우 카르보닐 화합물은 포름알데히드임)를 형성하기에 충분한 조건 하에 조합하는 것
을 포함하는, 포스포네이트 컨쥬게이트의 제조 방법. - R3 및 R4가 각각 나노입자에 부착되는 부착 성분이고, R1이 표적화제, 진단제 및 스텔스제로 이루어진 군으로부터 선택되는, 제1항 또는 제26항의 화합물을 포함하는 표적화된 전달 조성물.
- 제33항에 있어서, 나노입자가 리포솜이고, R3 및 R4가 각각 리포솜의 이중층과 회합되고 독립적으로 지질 및 콜레스테롤로 이루어진 군으로부터 선택되는, 표적화된 전달 조성물.
- R1이 나노입자 또는 나노입자에 부착되는 부착 성분이고, R3 및 R4가 각각 독립적으로 표적화제, 진단제 및 스텔스제로부터 선택되는, 제1항 또는 제26항의 화합물을 포함하는 표적화된 전달 조성물.
- 제35항에 있어서, 나노입자가 리포솜이고, R1이 리포솜의 이중층과 회합되고 독립적으로 지질 및 콜레스테롤로 이루어진 군으로부터 선택되는 표적화된 전달 조성물.
- 암 질환을 치료하거나 진단하기에 충분한 치료제 또는 진단제를 포함하며, R1, R3 및 R4 중 적어도 하나가 표적화제인, 제33항 또는 제35항의 표적화된 전달 조성물을 대상체에게 투여하는 것을 포함하는, 대상체에서의 암 질환의 치료 또는 진단 방법.
- 제37항에 있어서, 나노입자가 리포솜이고, 치료제가 리포솜 내에 캡슐화되거나 내포되거나, 또는 그에 테더링되어(tethered) 있는, 방법.
- 제38항에 있어서, 치료제가 독소루비신, 시스플라틴, 옥살리플라틴, 카르보플라틴, 5-플루오로우라실, 겜시티빈 및 탁산으로 이루어진 군으로부터 선택된 항암제인 방법.
- R1, R3 및 R4 중 적어도 하나가 표적화제이고, 나노입자가 진단제를 포함하는, 제33항 또는 제35항의 표적화된 전달 조성물을 대상체에게 투여하고, 상기 대상체를 영상화하여 진단제를 검출하는 것을 포함하는, 표적화된 치료 처치에 대한 대상체의 적합성을 결정하는 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161529694P | 2011-08-31 | 2011-08-31 | |
| US61/529,694 | 2011-08-31 | ||
| PCT/US2012/053197 WO2013033438A2 (en) | 2011-08-31 | 2012-08-30 | Nanoparticle peg modification with h-phosphonates |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20140067070A true KR20140067070A (ko) | 2014-06-03 |
Family
ID=46888663
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020147007934A KR20140067070A (ko) | 2011-08-31 | 2012-08-30 | H-포스포네이트에 의한 나노입자 peg 개질 |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US8889657B2 (ko) |
| EP (1) | EP2750712A2 (ko) |
| JP (1) | JP2014527071A (ko) |
| KR (1) | KR20140067070A (ko) |
| CN (1) | CN103930135A (ko) |
| BR (1) | BR112014004544A2 (ko) |
| CA (1) | CA2845845A1 (ko) |
| IL (1) | IL231215A0 (ko) |
| WO (1) | WO2013033438A2 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20200078962A (ko) * | 2018-12-24 | 2020-07-02 | 연세대학교 산학협력단 | 야누스 펩타이드 덴드리머 및 이의 용도 |
Families Citing this family (87)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2600901B1 (en) | 2010-08-06 | 2019-03-27 | ModernaTX, Inc. | A pharmaceutical formulation comprising engineered nucleic acids and medical use thereof |
| ES2737960T3 (es) | 2010-10-01 | 2020-01-17 | Modernatx Inc | Nucleósidos, nucleótidos y ácidos nucleicos modificados y sus usos |
| AU2012236099A1 (en) | 2011-03-31 | 2013-10-03 | Moderna Therapeutics, Inc. | Delivery and formulation of engineered nucleic acids |
| US9464124B2 (en) | 2011-09-12 | 2016-10-11 | Moderna Therapeutics, Inc. | Engineered nucleic acids and methods of use thereof |
| EP3682905B1 (en) | 2011-10-03 | 2021-12-01 | ModernaTX, Inc. | Modified nucleosides, nucleotides, and nucleic acids, and uses thereof |
| EP2791160B1 (en) | 2011-12-16 | 2022-03-02 | ModernaTX, Inc. | Modified mrna compositions |
| US9303079B2 (en) | 2012-04-02 | 2016-04-05 | Moderna Therapeutics, Inc. | Modified polynucleotides for the production of cytoplasmic and cytoskeletal proteins |
| AU2013243948A1 (en) | 2012-04-02 | 2014-10-30 | Moderna Therapeutics, Inc. | Modified polynucleotides for the production of proteins associated with human disease |
| US9283287B2 (en) | 2012-04-02 | 2016-03-15 | Moderna Therapeutics, Inc. | Modified polynucleotides for the production of nuclear proteins |
| US9572897B2 (en) | 2012-04-02 | 2017-02-21 | Modernatx, Inc. | Modified polynucleotides for the production of cytoplasmic and cytoskeletal proteins |
| EP4074834A1 (en) | 2012-11-26 | 2022-10-19 | ModernaTX, Inc. | Terminally modified rna |
| US10258698B2 (en) | 2013-03-14 | 2019-04-16 | Modernatx, Inc. | Formulation and delivery of modified nucleoside, nucleotide, and nucleic acid compositions |
| US8980864B2 (en) | 2013-03-15 | 2015-03-17 | Moderna Therapeutics, Inc. | Compositions and methods of altering cholesterol levels |
| JP6190534B2 (ja) | 2013-08-22 | 2017-08-30 | ソニー株式会社 | 水溶性蛍光染料又は有色染料及びその使用方法 |
| WO2015034925A1 (en) | 2013-09-03 | 2015-03-12 | Moderna Therapeutics, Inc. | Circular polynucleotides |
| WO2015048744A2 (en) | 2013-09-30 | 2015-04-02 | Moderna Therapeutics, Inc. | Polynucleotides encoding immune modulating polypeptides |
| CA2926218A1 (en) | 2013-10-03 | 2015-04-09 | Moderna Therapeutics, Inc. | Polynucleotides encoding low density lipoprotein receptor |
| CA2955250A1 (en) | 2014-07-16 | 2016-01-21 | Moderna Therapeutics, Inc. | Chimeric polynucleotides |
| EP3171895A1 (en) | 2014-07-23 | 2017-05-31 | Modernatx, Inc. | Modified polynucleotides for the production of intrabodies |
| PT3350157T (pt) | 2015-09-17 | 2022-03-18 | Modernatx Inc | Compostos e composições para administração intracelular de agentes terapêuticos |
| EP3364981A4 (en) | 2015-10-22 | 2019-08-07 | ModernaTX, Inc. | VACCINE AGAINST THE HUMAN CYTOMEGALOVIRUS |
| CA3002912A1 (en) | 2015-10-22 | 2017-04-27 | Modernatx, Inc. | Nucleic acid vaccines for varicella zoster virus (vzv) |
| EP3365007A4 (en) | 2015-10-22 | 2019-07-03 | ModernaTX, Inc. | VACCINE AGAINST BROAD SPECTRUM INFLUENZA VIRUS |
| SG10201914006UA (en) | 2015-10-22 | 2020-03-30 | Modernatx Inc | Respiratory syncytial virus vaccine |
| EP4011451A1 (en) | 2015-10-22 | 2022-06-15 | ModernaTX, Inc. | Metapneumovirus mrna vaccines |
| US20180303929A1 (en) | 2015-10-22 | 2018-10-25 | Moderna TX, Inc. | Herpes simplex virus vaccine |
| EP3964200A1 (en) | 2015-12-10 | 2022-03-09 | ModernaTX, Inc. | Compositions and methods for delivery of therapeutic agents |
| AU2016377681B2 (en) | 2015-12-22 | 2021-05-13 | Modernatx, Inc. | Compounds and compositions for intracellular delivery of agents |
| HRP20220525T1 (hr) | 2015-12-23 | 2022-05-27 | Modernatx, Inc. | Postupci uporabe polinukleotida koji kodiraju ligand ox40 |
| WO2017120612A1 (en) | 2016-01-10 | 2017-07-13 | Modernatx, Inc. | Therapeutic mrnas encoding anti ctla-4 antibodies |
| US11685835B2 (en) | 2016-05-11 | 2023-06-27 | Sony Corporation | Ultra bright dimeric or polymeric dyes |
| US10072032B2 (en) * | 2016-09-19 | 2018-09-11 | Afton Chemical Corporation | AminoBisPhosphonate antiwear additives |
| WO2018089540A1 (en) | 2016-11-08 | 2018-05-17 | Modernatx, Inc. | Stabilized formulations of lipid nanoparticles |
| PL3596041T3 (pl) | 2017-03-15 | 2023-03-06 | Modernatx, Inc. | Związek i kompozycje do dokomórkowego dostarczania środków terapeutycznych |
| US11969506B2 (en) | 2017-03-15 | 2024-04-30 | Modernatx, Inc. | Lipid nanoparticle formulation |
| ES2911186T3 (es) | 2017-03-15 | 2022-05-18 | Modernatx Inc | Formas cristalinas de aminolípidos |
| ES2952779T3 (es) | 2017-05-18 | 2023-11-06 | Modernatx Inc | ARN mensajero modificado que comprende elementos de ARN funcionales |
| WO2018213731A1 (en) | 2017-05-18 | 2018-11-22 | Modernatx, Inc. | Polynucleotides encoding tethered interleukin-12 (il12) polypeptides and uses thereof |
| US20200268666A1 (en) | 2017-06-14 | 2020-08-27 | Modernatx, Inc. | Polynucleotides encoding coagulation factor viii |
| US11786607B2 (en) | 2017-06-15 | 2023-10-17 | Modernatx, Inc. | RNA formulations |
| WO2019046809A1 (en) | 2017-08-31 | 2019-03-07 | Modernatx, Inc. | METHODS OF MANUFACTURING LIPID NANOPARTICLES |
| EP3691689A1 (en) * | 2017-10-05 | 2020-08-12 | Sony Corporation | Programmable dendritic drugs |
| KR20200083605A (ko) | 2017-11-16 | 2020-07-08 | 소니 주식회사 | 프로그램가능한 중합체성 약물 |
| CA3079543A1 (en) | 2017-11-22 | 2019-05-31 | Modernatx, Inc. | Polynucleotides encoding propionyl-coa carboxylase alpha and beta subunits for the treatment of propionic acidemia |
| WO2019104160A2 (en) | 2017-11-22 | 2019-05-31 | Modernatx, Inc. | Polynucleotides encoding phenylalanine hydroxylase for the treatment of phenylketonuria |
| EP3714048A1 (en) | 2017-11-22 | 2020-09-30 | Modernatx, Inc. | Polynucleotides encoding ornithine transcarbamylase for the treatment of urea cycle disorders |
| WO2019136241A1 (en) | 2018-01-05 | 2019-07-11 | Modernatx, Inc. | Polynucleotides encoding anti-chikungunya virus antibodies |
| US20190262793A1 (en) * | 2018-02-28 | 2019-08-29 | Southwest Research Institute | Polymer-Encapsulated Polyhemoglobin-Based Oxygen Carrier |
| US11874280B2 (en) | 2018-03-19 | 2024-01-16 | Sony Group Corporation | Use of divalent metals for enhancement of fluorescent signals |
| EP3773745A1 (en) | 2018-04-11 | 2021-02-17 | ModernaTX, Inc. | Messenger rna comprising functional rna elements |
| WO2019226650A1 (en) | 2018-05-23 | 2019-11-28 | Modernatx, Inc. | Delivery of dna |
| US20220184185A1 (en) | 2018-07-25 | 2022-06-16 | Modernatx, Inc. | Mrna based enzyme replacement therapy combined with a pharmacological chaperone for the treatment of lysosomal storage disorders |
| WO2020047201A1 (en) | 2018-09-02 | 2020-03-05 | Modernatx, Inc. | Polynucleotides encoding very long-chain acyl-coa dehydrogenase for the treatment of very long-chain acyl-coa dehydrogenase deficiency |
| US20220054610A1 (en) | 2018-09-12 | 2022-02-24 | University Of Florida Research Foundation, Inc. | Slow-cycling cell-rna based nanoparticle vaccine to treat cancer |
| MX2021003015A (es) | 2018-09-13 | 2021-07-15 | Modernatx Inc | Polinucleotidos que codifican glucosa-6-fosfatasa para el tratamiento de la glucogenosis. |
| WO2020056155A2 (en) | 2018-09-13 | 2020-03-19 | Modernatx, Inc. | Polynucleotides encoding branched-chain alpha-ketoacid dehydrogenase complex e1-alpha, e1-beta, and e2 subunits for the treatment of maple syrup urine disease |
| MA53615A (fr) | 2018-09-14 | 2021-07-21 | Modernatx Inc | Polynucléotides codant pour le polypeptide a1, de la famille de l'uridine diphosphate glycosyltransférase 1, pour le traitement du syndrome de crigler-najjar |
| US20220152225A1 (en) | 2018-09-27 | 2022-05-19 | Modernatx, Inc. | Polynucleotides encoding arginase 1 for the treatment of arginase deficiency |
| CA3113151A1 (en) * | 2018-10-01 | 2020-04-09 | Johannes Gutenberg-Universitat Mainz | Rna particles comprising polysarcosine |
| WO2020069718A1 (en) * | 2018-10-01 | 2020-04-09 | Johannes Gutenberg-Universität Mainz | Rna particles comprising polysarcosine |
| US20220001026A1 (en) | 2018-11-08 | 2022-01-06 | Modernatx, Inc. | Use of mrna encoding ox40l to treat cancer in human patients |
| EP3965806A1 (en) | 2019-05-08 | 2022-03-16 | Modernatx, Inc. | Polynucleotides encoding methylmalonyl-coa mutase for the treatment of methylmalonic acidemia |
| US20220226438A1 (en) | 2019-05-08 | 2022-07-21 | Astrazeneca Ab | Compositions for skin and wounds and methods of use thereof |
| WO2020263883A1 (en) | 2019-06-24 | 2020-12-30 | Modernatx, Inc. | Endonuclease-resistant messenger rna and uses thereof |
| EP3986480A1 (en) | 2019-06-24 | 2022-04-27 | ModernaTX, Inc. | Messenger rna comprising functional rna elements and uses thereof |
| AR120080A1 (es) | 2019-09-19 | 2022-02-02 | Modernatx Inc | Compuestos lipídicos de cola ramificada y composiciones para la administración intracelular de agentes terapéuticos |
| EP3861074A2 (en) | 2019-09-26 | 2021-08-11 | Sony Group Corporation | Polymeric tandem dyes with linker groups |
| US20230235298A1 (en) | 2020-06-01 | 2023-07-27 | Modernatx, Inc. | Phenylalanine hydroxylase variants and uses thereof |
| CA3181680A1 (en) | 2020-06-12 | 2021-12-16 | University Of Rochester | Encoding and expression of ace-trnas |
| WO2022104131A1 (en) | 2020-11-13 | 2022-05-19 | Modernatx, Inc. | Polynucleotides encoding cystic fibrosis transmembrane conductance regulator for the treatment of cystic fibrosis |
| US11524023B2 (en) | 2021-02-19 | 2022-12-13 | Modernatx, Inc. | Lipid nanoparticle compositions and methods of formulating the same |
| WO2022204390A1 (en) | 2021-03-24 | 2022-09-29 | Modernatx, Inc. | Lipid nanoparticles containing polynucleotides encoding phenylalanine hydroxylase and uses thereof |
| WO2022204371A1 (en) | 2021-03-24 | 2022-09-29 | Modernatx, Inc. | Lipid nanoparticles containing polynucleotides encoding glucose-6-phosphatase and uses thereof |
| WO2022204380A1 (en) | 2021-03-24 | 2022-09-29 | Modernatx, Inc. | Lipid nanoparticles containing polynucleotides encoding propionyl-coa carboxylase alpha and beta subunits and uses thereof |
| JP2024512026A (ja) | 2021-03-24 | 2024-03-18 | モデルナティエックス インコーポレイテッド | オルニチントランスカルバミラーゼ欠損症の治療を目的とした脂質ナノ粒子及びオルニチントランスカルバミラーゼをコードするポリヌクレオチド |
| WO2022204369A1 (en) | 2021-03-24 | 2022-09-29 | Modernatx, Inc. | Polynucleotides encoding methylmalonyl-coa mutase for the treatment of methylmalonic acidemia |
| WO2022266083A2 (en) | 2021-06-15 | 2022-12-22 | Modernatx, Inc. | Engineered polynucleotides for cell-type or microenvironment-specific expression |
| WO2022271776A1 (en) | 2021-06-22 | 2022-12-29 | Modernatx, Inc. | Polynucleotides encoding uridine diphosphate glycosyltransferase 1 family, polypeptide a1 for the treatment of crigler-najjar syndrome |
| WO2023056044A1 (en) | 2021-10-01 | 2023-04-06 | Modernatx, Inc. | Polynucleotides encoding relaxin for the treatment of fibrosis and/or cardiovascular disease |
| WO2023150753A1 (en) | 2022-02-07 | 2023-08-10 | University Of Rochester | Optimized sequences for enhanced trna expression or/and nonsense mutation suppression |
| WO2023161350A1 (en) | 2022-02-24 | 2023-08-31 | Io Biotech Aps | Nucleotide delivery of cancer therapy |
| WO2023177904A1 (en) | 2022-03-18 | 2023-09-21 | Modernatx, Inc. | Sterile filtration of lipid nanoparticles and filtration analysis thereof for biological applications |
| WO2023183909A2 (en) | 2022-03-25 | 2023-09-28 | Modernatx, Inc. | Polynucleotides encoding fanconi anemia, complementation group proteins for the treatment of fanconi anemia |
| WO2023196399A1 (en) | 2022-04-06 | 2023-10-12 | Modernatx, Inc. | Lipid nanoparticles and polynucleotides encoding argininosuccinate lyase for the treatment of argininosuccinic aciduria |
| WO2023215498A2 (en) | 2022-05-05 | 2023-11-09 | Modernatx, Inc. | Compositions and methods for cd28 antagonism |
| WO2024026254A1 (en) | 2022-07-26 | 2024-02-01 | Modernatx, Inc. | Engineered polynucleotides for temporal control of expression |
| WO2024044147A1 (en) | 2022-08-23 | 2024-02-29 | Modernatx, Inc. | Methods for purification of ionizable lipids |
Family Cites Families (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE514095C (de) * | 1927-07-24 | 1930-12-11 | Knoll Akt Ges Chemische Fabrik | Verfahren zur Herstellung von Estern der Sterine mit Sauerstoffsaeuren des Phosphors |
| CH336065A (de) * | 1954-03-05 | 1959-02-15 | Ciba Geigy | Verfahren zur Herstellung von neuen Stickstoff und Phosphor enthaltenden Verbindungen |
| GB1128086A (en) * | 1966-10-27 | 1968-09-25 | Pure Chem Ltd | Improvements relating to hydroxy-containing phosphonates and polyurethanes |
| US3974209A (en) * | 1971-08-04 | 1976-08-10 | Monsanto Company | Substituted tertiary amines and processes for preparing the same |
| DE3202127A1 (de) | 1982-01-23 | 1983-07-28 | Agfa-Gevaert Ag, 5090 Leverkusen | Fotografisches material mit einer durch organische farbstoffe anfaerbbaren schicht |
| US4568432A (en) | 1984-12-28 | 1986-02-04 | Monsanto Company | Process for preparing glyphosate and glyphosate derivatives |
| EP0209848A3 (en) * | 1985-07-24 | 1988-07-27 | Merck & Co. Inc. | Enzyme inhibitors |
| US5567588A (en) | 1990-06-11 | 1996-10-22 | University Research Corporation | Systematic evolution of ligands by exponential enrichment: Solution SELEX |
| DE4408729A1 (de) * | 1994-03-15 | 1995-09-21 | Hoechst Ag | Nichtcyclische Chelatbildner auf Basis von Aminodialkylphosphoroxiden zur Herstellung von Technetium- oder Rheniumkomplexen |
| US6054608A (en) | 1997-05-05 | 2000-04-25 | Monsanto Company | Method for preparing formylphosphonic acid |
| ZA989394B (en) * | 1997-10-15 | 1999-04-15 | Monsanto Co | Selective functionalization of sodium glycinate |
| JP3799435B2 (ja) * | 1998-04-13 | 2006-07-19 | 三共有機合成株式会社 | 安定化された抗菌性樹脂組成物 |
| US7833992B2 (en) * | 2001-05-18 | 2010-11-16 | Merck Sharpe & Dohme | Conjugates and compositions for cellular delivery |
| DE10049074A1 (de) | 2000-10-02 | 2002-04-18 | Andreas Kage | Verfahren zur Selektion hochaffin an ein Target bindender Nukleinsäuren |
| WO2002062398A2 (en) * | 2001-01-08 | 2002-08-15 | Neorx Corporation | Radioactively labelled conjugates of phosphonates |
| DE10259935A1 (de) * | 2002-12-20 | 2004-07-01 | Bayer Ag | Herstellung und Verwendung von in-situ-modifizierten Nanopartikeln |
| EA012240B1 (ru) * | 2003-04-03 | 2009-08-28 | Семафор Фармасьютикалз, Инк. | Пролекарства ингибиторов киназы pi-3 |
| US20040198783A1 (en) * | 2003-04-03 | 2004-10-07 | Semafore Pharmaceuticals Inc. | Targeted bone marrow protection agents |
| JP2010535701A (ja) * | 2003-04-25 | 2010-11-25 | ギリアード サイエンシーズ, インコーポレイテッド | 抗癌ホスホネートアナログ |
| DE10320071A1 (de) * | 2003-05-05 | 2004-12-02 | Basf Ag | Alkoxygruppen aufweisende Ester von Phosphor-Sauerstoff-Säuren und ihre Verwendung als Korrosionsinhibitoren |
| US7420000B2 (en) * | 2003-09-10 | 2008-09-02 | University Of Southern California | Amino phosphonate and amino bis-phosphonate derivatives |
| DE102004032781A1 (de) * | 2004-01-23 | 2005-08-11 | Mcs Micro Carrier Systems Gmbh | Bisphosphonsäurederivate |
| US20100015041A1 (en) | 2005-01-18 | 2010-01-21 | Caltagirone Gaetano T | Class of Supramolecular Drug Molecules and Methods of Identification and Use Thereof |
| CA2599673A1 (en) * | 2005-03-08 | 2006-09-14 | Reinhold Oehrlein | Metal oxide nanoparticles coated with specific n-acylaminomethylene phosphonates |
| US20120059147A1 (en) * | 2007-11-19 | 2012-03-08 | The University Of Tokyo | Method for site-selectively cleaving target nucleic acid |
| WO2010013086A1 (en) * | 2008-08-01 | 2010-02-04 | Centre National De La Recherche Scientifique | Phosphorylated dendrimers as antiinflammatory drugs |
| EP3238738B1 (en) * | 2008-11-10 | 2020-09-23 | Arbutus Biopharma Corporation | Novel lipids and compositions for the delivery of therapeutics |
| JP5381269B2 (ja) * | 2009-04-15 | 2014-01-08 | コニカミノルタ株式会社 | 光学フィルム、光学フィルムの製造方法、偏光板及び液晶表示装置 |
| WO2011097563A1 (en) | 2010-02-08 | 2011-08-11 | Board Of Regents Of The University Of Nebraska | Biomineral and metal binding liposomes, their synthesis, and methods of use thereof |
| CN102858851A (zh) * | 2010-02-18 | 2013-01-02 | 阿尔卡拉德埃纳雷斯大学 | 碳硅烷树枝状化合物及其作为抗病毒剂的用途 |
| JO3131B1 (ar) | 2010-04-27 | 2017-09-20 | Glaxosmithkline Llc | مركبات كيميائية |
| CN102093421B (zh) * | 2011-01-28 | 2014-07-02 | 北京康辰药业有限公司 | 一种含磷取代基的喹啉类化合物及其制备方法、以及含有该化合物的药物组合物及其应用 |
-
2012
- 2012-08-30 JP JP2014528610A patent/JP2014527071A/ja active Pending
- 2012-08-30 CA CA2845845A patent/CA2845845A1/en not_active Abandoned
- 2012-08-30 EP EP12762126.6A patent/EP2750712A2/en not_active Withdrawn
- 2012-08-30 CN CN201280053606.0A patent/CN103930135A/zh active Pending
- 2012-08-30 KR KR1020147007934A patent/KR20140067070A/ko not_active Application Discontinuation
- 2012-08-30 US US13/599,819 patent/US8889657B2/en not_active Expired - Fee Related
- 2012-08-30 WO PCT/US2012/053197 patent/WO2013033438A2/en active Application Filing
- 2012-08-30 BR BR112014004544A patent/BR112014004544A2/pt not_active IP Right Cessation
-
2014
- 2014-02-27 IL IL231215A patent/IL231215A0/en unknown
- 2014-10-14 US US14/513,994 patent/US20150030541A1/en not_active Abandoned
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20200078962A (ko) * | 2018-12-24 | 2020-07-02 | 연세대학교 산학협력단 | 야누스 펩타이드 덴드리머 및 이의 용도 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20130066086A1 (en) | 2013-03-14 |
| CA2845845A1 (en) | 2013-03-07 |
| CN103930135A (zh) | 2014-07-16 |
| WO2013033438A2 (en) | 2013-03-07 |
| BR112014004544A2 (pt) | 2017-04-04 |
| IL231215A0 (en) | 2014-04-30 |
| US8889657B2 (en) | 2014-11-18 |
| US20150030541A1 (en) | 2015-01-29 |
| JP2014527071A (ja) | 2014-10-09 |
| WO2013033438A3 (en) | 2013-04-25 |
| EP2750712A2 (en) | 2014-07-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20140067070A (ko) | H-포스포네이트에 의한 나노입자 peg 개질 | |
| JP5927194B2 (ja) | 治療ナノキャリアおよび/または診断ナノキャリアのターゲティングのためのアプタマーコンジュゲート | |
| Mitchell et al. | Incorporation of paramagnetic, fluorescent and PET/SPECT contrast agents into liposomes for multimodal imaging | |
| DK2501415T3 (en) | Liposomal nanoparticles of magnetic resonance imaging of tumors | |
| JP2019006815A (ja) | 修飾されたドセタキセルリポソーム製剤 | |
| KR20140096080A (ko) | Mmp-표적 치료 및/또는 진단 나노담체 | |
| KR20140069269A (ko) | 상보성 올리고뉴클레오티드 링커를 사용한 표적화된 나노입자들의 원격 조립 | |
| KR20140064917A (ko) | H-포스포네이트-엔/-인 히드로포스포닐화 반응을 이용한 표적화된 나노입자의 원격 어셈블리 | |
| US20170165382A1 (en) | Nanocarriers for cancer treatment | |
| US20160038597A9 (en) | Carrier that targets fucosylated molecule-producing cells | |
| Bofinger et al. | Drug delivery, biodistribution and anti-EGFR activity: theragnostic nanoparticles for simultaneous in vivo delivery of tyrosine kinase inhibitors and kinase activity biosensors | |
| US20140030186A1 (en) | Combined pharmaceutical preparation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |