JP2018508329A - 神経変調デバイス - Google Patents
神経変調デバイス Download PDFInfo
- Publication number
- JP2018508329A JP2018508329A JP2017562969A JP2017562969A JP2018508329A JP 2018508329 A JP2018508329 A JP 2018508329A JP 2017562969 A JP2017562969 A JP 2017562969A JP 2017562969 A JP2017562969 A JP 2017562969A JP 2018508329 A JP2018508329 A JP 2018508329A
- Authority
- JP
- Japan
- Prior art keywords
- signal
- patient
- nerve
- vagus nerve
- neural activity
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F7/00—Heating or cooling appliances for medical or therapeutic treatment of the human body
- A61F7/007—Heating or cooling appliances for medical or therapeutic treatment of the human body characterised by electric heating
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/02—Details
- A61N1/04—Electrodes
- A61N1/05—Electrodes for implantation or insertion into the body, e.g. heart electrode
- A61N1/0551—Spinal or peripheral nerve electrodes
- A61N1/0553—Paddle shaped electrodes, e.g. for laminotomy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/20—Applying electric currents by contact electrodes continuous direct currents
- A61N1/205—Applying electric currents by contact electrodes continuous direct currents for promoting a biological process
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/3601—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation of respiratory organs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/3605—Implantable neurostimulators for stimulating central or peripheral nerve system
- A61N1/36053—Implantable neurostimulators for stimulating central or peripheral nerve system adapted for vagal stimulation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/3605—Implantable neurostimulators for stimulating central or peripheral nerve system
- A61N1/3606—Implantable neurostimulators for stimulating central or peripheral nerve system adapted for a particular treatment
- A61N1/3611—Respiration control
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/3605—Implantable neurostimulators for stimulating central or peripheral nerve system
- A61N1/36128—Control systems
- A61N1/36135—Control systems using physiological parameters
- A61N1/36139—Control systems using physiological parameters with automatic adjustment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/3605—Implantable neurostimulators for stimulating central or peripheral nerve system
- A61N1/36128—Control systems
- A61N1/36146—Control systems specified by the stimulation parameters
- A61N1/36167—Timing, e.g. stimulation onset
- A61N1/36171—Frequency
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/3605—Implantable neurostimulators for stimulating central or peripheral nerve system
- A61N1/36128—Control systems
- A61N1/36146—Control systems specified by the stimulation parameters
- A61N1/36167—Timing, e.g. stimulation onset
- A61N1/36178—Burst or pulse train parameters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N5/0613—Apparatus adapted for a specific treatment
- A61N5/0622—Optical stimulation for exciting neural tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N7/00—Ultrasound therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/14—Antitussive agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F7/00—Heating or cooling appliances for medical or therapeutic treatment of the human body
- A61F7/007—Heating or cooling appliances for medical or therapeutic treatment of the human body characterised by electric heating
- A61F2007/0075—Heating or cooling appliances for medical or therapeutic treatment of the human body characterised by electric heating using a Peltier element, e.g. near the spot to be heated or cooled
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/3605—Implantable neurostimulators for stimulating central or peripheral nerve system
- A61N1/36128—Control systems
- A61N1/36189—Control systems using modulation techniques
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N2005/065—Light sources therefor
- A61N2005/0651—Diodes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N7/00—Ultrasound therapy
- A61N2007/0004—Applications of ultrasound therapy
- A61N2007/0021—Neural system treatment
- A61N2007/0026—Stimulation of nerve tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N5/067—Radiation therapy using light using laser light
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biomedical Technology (AREA)
- Radiology & Medical Imaging (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Pulmonology (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Physiology (AREA)
- Biophysics (AREA)
- Heart & Thoracic Surgery (AREA)
- Epidemiology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Cardiology (AREA)
- Pathology (AREA)
- Vascular Medicine (AREA)
- Molecular Biology (AREA)
- Mycology (AREA)
- Immunology (AREA)
- Microbiology (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Electrotherapy Devices (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Radiation-Therapy Devices (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Surgical Instruments (AREA)
Abstract
Description
迷走神経を通じた気管支収縮を研究する方法は、他の文献で詳細に記載されている(Canning他、Am J Physiol Regul Integr Comp Physiol.2002年8月;283(2):R320−30)。気道及び関連の神経を無関係な全ての組織を取り除いて解剖し、加温酸素注入Krebs緩衝液を用いて絶えず灌流される水ジャケット付き解剖皿に置く。関連する神経に傷を付けないように主幹気管支を単離する。気管支のいずれの側にもスターラップを置き、1つを記録チャンバの底部に固定し、第2のものを等尺性力変換器に取り付ける。関連の迷走神経を双極電極を用いて電気的に刺激し(0.1〜64Hz)、筋肉の収縮がもたらされる。
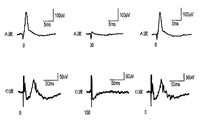
モルモットから取得した迷走神経及びヒト臓器ドナーから取得した迷走神経胸枝を周囲の組織を取り除くように解剖した。切断した迷走神経又は枝の一端を単一矩形パルスを送出する刺激器に接続された吸引電極を通して刺激した。迷走神経又は胸枝神経の他端において従来の記録吸引電極を用いて複合活動電位を記録した。得られたシグナルを増幅し(AM Systems、Model 1800)、オシロスコープ上に表示し、コンピュータ上に格納した。刺激電極と記録電極の間への神経変調電気シグナルの印加中に、複合活動電位における波の振幅は、神経変調シグナルの印加の前に記録した振幅と比較して低減した(図8、直流、及び図9、交流)。この抑制効果は、神経変調シグナルの印加を停止した時には不在である(図8及び図9)。これは、シグナルの印加が神経を不可逆に損傷しなかったことを示している。
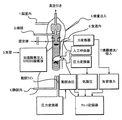
麻酔をかけたモルモットにおいて迷走神経を通じた気管支収縮を研究する方法は、他の文献で詳細に記載されており(Mazzone及びCanning、Curr Protoc Pharmacol. 2002年5月1日;第5章:ユニット5.26;Auton Neurosci.2002年8月30日;99(2):91〜101)、かつ図10に示している。モルモットにウレタン(1.5g/kg ip)を用いて麻酔をかけた。気管及び迷走神経は、頚部正中切開によって目視可能にされる。気管にカニューレ挿入し、定容量人工呼吸器(6mL/kg体重)に接続する。次いで、これらの動物をサクシニルコリン(2.5mg/kg sc)を用いて麻痺させる。心血管パラメータをモニタするために及び薬品送出のために動脈及び静脈にカニューレ挿入する。迷走神経を双極電極上に置く。気管カニューレのサイドポートに接続された圧力変換器を用いて肺膨張圧をモニタする。気管支痙攣を肺膨張圧の百分率増大として記録する。
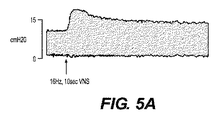
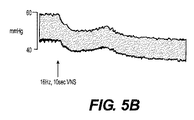
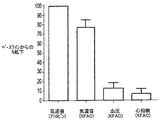
図10に示す方法を用いて、等尺性張力を測定した気管の部分(喉頭の後部にある第6及び第7の気管輪)を加温し(37℃)、酸素注入したKrebs緩衝液で灌流し、これを気管へのアトロピン(1μM)の選択的送出に用いた。副交感迷走神経の定常的に発生する緊張活動は、気道平滑筋のベースライン緊張をもたらす。左右両方の迷走神経にアトロピンを投与するか又は神経変調電気シグナル(交流20kHz、7mA)を印加すると、ベースライン気道平滑筋緊張の低下が見られる(図11)。この効果は、シグナル印加が停止されるまで維持され、停止時に、ベースライン緊張は、その治療前のレベルに向けて増大する(図11)。この抑制の大きさは、アトロピンの投与からもたらされる抑制の77±8%であった(図11及び図12)。しかし、ベースライン気道平滑緊張の抑制の開始は、アトロピンを用いた治療に続いて見られるものよりも早かった(図11)。神経変調シグナルは、心拍数又は血圧に対してごく僅かな効果しか持たなかった(図12)。
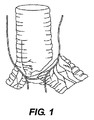
2 喉頭
3 気管
4 静脈内
5 微量注入
Claims (65)
- 患者の迷走神経の神経活動を抑制するための装置であって、
各々が前記患者の迷走神経にシグナルを印加するように構成された1又は2以上の変換器と、
前記1又は2以上の変換器に結合されて、該1又は2以上の変換器の各々によって印加される前記シグナルを該シグナルが前記迷走神経の前記神経活動を抑制して前記患者内の副交感神経性緊張反応を低減するように制御するコントローラと、
を含むことを特徴とする装置。 - 患者内の気管支収縮を治療するための装置であって、
各々が前記患者の迷走神経にシグナルを印加するように構成された1又は2以上の変換器と、
前記1又は2以上の変換器に結合されて、該1又は2以上の変換器の各々によって印加される前記シグナルを該シグナルが前記迷走神経の前記神経活動を抑制し、それによって前記患者内の副交感神経性緊張を低減して気管支収縮を軽減するように制御するコントローラと、
を含むことを特徴とする装置。 - 前記1又は2以上の変換器の各々によって印加される前記シグナルは、非破壊的シグナルであることを特徴とする請求項1又は請求項2に記載の装置。
- 前記シグナルは、前記迷走神経内の神経活動を少なくとも部分的に抑制し、任意的に該神経内の神経活動を完全に抑制することを特徴とする請求項1から請求項3のいずれか1項に記載の装置。
- 前記シグナルは、前記神経内の神経活動を少なくとも部分的に遮断し、任意的に該神経内の神経活動を完全に遮断することを特徴とする請求項4に記載の装置。
- 前記1又は2以上の変換器の各々によって印加される前記シグナルは、電気シグナル、光シグナル、超音波シグナル、機械的シグナル、及び熱シグナルから独立に選択されることを特徴とする請求項1から請求項5のいずれか1項に記載の装置。
- 前記1又は複数のシグナルは、電気シグナルであり、該シグナルを印加するように構成された前記1又は2以上の変換器は、電極であることを特徴とする請求項6に記載の装置。
- 前記シグナルは、キロヘルツ周波数の交流(AC)波形を含むことを特徴とする請求項7に記載の装置。
- 前記シグナルは、電荷均衡式直流(DC)波形を含むことを特徴とする請求項7又は請求項8に記載の装置。
- 前記シグナルは、実質的に順番に、
(i)DCランプ、及びそれに続いてプラトー及び電荷均衡を印加する段階と、
(ii)波形が印加される期間中に波形の振幅が増大する第1のAC波形を印加する段階と、
(iii)前記第1の波形よりも低い周波数及び/又は小さい振幅を有する第2のAC波形を印加する段階と、
を含む、
ことを特徴とする請求項7から請求項9のいずれか1項に記載の装置。 - 前記シグナルが1又は2以上のAC波形を含むときに、該1又は2以上のAC波形は、各々が5〜25kHz、任意的に10〜25kHz、任意的に15〜25kHz、任意的に20〜25kHzの周波数を有することを特徴とする請求項7から請求項10のいずれか1項に記載の装置。
- 前記シグナルは、1〜15V、3〜15V、5〜15V、任意的に10〜15Vの電圧を有することを特徴とする請求項7から請求項11のいずれか1項に記載の装置。
- 前記電圧は、3V、5V、10V、及び15Vから選択されることを特徴とする請求項12に記載の装置。
- 副交感神経性緊張の前記低減は、気道平滑筋緊張の低下、血中酸素飽和度の増大、血中二酸化炭素濃度の低下、呼吸数の低下、全肺気量の増加、及び努力肺活量の増加のうちの1又は2以上から選択される生理学的反応を生成することを特徴とする請求項1から請求項13のいずれか1項に記載の装置。
- 前記迷走神経内の活動電位又は活動電位のパターンが、前記シグナルの前記印加の前よりも健常者によって示されるものにより厳密に似ていることを特徴とする請求項1から請求項14のいずれか1項に記載の装置。
- 前記患者内の1又は2以上の生理学的パラメータを検出する検出器要素を更に含むことを特徴とする請求項1から請求項15のいずれか1項に記載の装置。
- 前記コントローラは、前記検出器要素に結合され、かつ前記生理学的パラメータが事前定義閾値に適合するか又はそれを超えることが検出されたときに前記1又は2以上の変換器の各々に前記シグナルを印加させることを特徴とする請求項16に記載の装置。
- 前記検出される生理学的パラメータのうちの1又は2以上が、副交感神経性緊張、ASM緊張、血中酸素飽和度、血中二酸化炭素濃度、呼吸数、全肺気量、及び努力肺活量から選択されることを特徴とする請求項16又は請求項17に記載の装置。
- 前記神経活動が変調される前記迷走神経は、迷走神経の少なくとも1つの肺枝、任意的に迷走神経の少なくとも1つの肺枝の遠心性線維であることを特徴とする請求項1から請求項18のいずれか1項に記載の装置。
- 前記1又は2以上の変換器が前記シグナルを印加する結果としての神経活動の前記変調は、実質的に永続的であることを特徴とする請求項1から請求項19のいずれか1項に記載の装置。
- 神経活動の前記変調は、一時的であることを特徴とする請求項1から請求項20のいずれか1項に記載の装置。
- 神経活動の前記変調は、是正的であることを特徴とする請求項1から請求項21のいずれか1項に記載の装置。
- 前記患者内への少なくとも部分的な埋め込みに、任意的に該患者内への完全な埋め込みに適切であることを特徴とする請求項1から請求項22のいずれか1項に記載の装置。
- 患者のCOPD又は喘息を治療する方法であって、
i.前記患者内に請求項1から請求項23のいずれか1項に記載の装置を埋め込む段階と、
ii.前記装置の少なくとも1つの変換器を前記患者の迷走神経とシグナリング接触して位置決めする段階と、
iii.前記装置を起動する段階と、
を含むことを特徴とする方法。 - 段階(ii)は、第1の変換器を前記患者の第1の迷走神経とシグナリング接触して位置決めする段階と、第2の変換器を該患者の同側又は反対側迷走神経とシグナリング接触して位置決めする段階とを更に含むことを特徴とする請求項24に記載の方法。
- 前記第1及び第2の変換器は、同じ装置の一部であることを特徴とする請求項25に記載の方法。
- 前記1又は複数の迷走神経は、各々が迷走神経の少なくとも1つの肺枝、任意的に迷走神経の該少なくとも1つの肺枝の遠心性線維であることを特徴とする請求項24から請求項26のいずれか1項に記載の方法。
- 患者のCOPD又は喘息を治療する方法であって、
前記患者の迷走神経の一部又は全部にシグナルを印加して該患者内の該神経の神経活動を変調する段階、
を含むことを特徴とする方法。 - 前記シグナルは、迷走神経の肺枝に、任意的に迷走神経の肺枝の遠心性線維に印加されることを特徴とする請求項28に記載の方法。
- 前記シグナルは、該シグナルを印加するように構成された1又は2以上の変換器を含む神経変調デバイスによって印加されることを特徴とする請求項28又は請求項29に記載の方法。
- 前記神経変調デバイスは、前記患者内に少なくとも部分的に埋め込まれ、任意的に該患者内に全体的に埋め込まれることを特徴とする請求項30に記載の方法。
- 前記病態の治療が、測定可能生理学的パラメータの改善によって示され、
前記測定可能生理学的パラメータは、副交感神経性緊張、ASM緊張、血中酸素飽和度、血中二酸化炭素濃度、呼吸数、全肺気量、努力肺活量、前記シグナルが印加される前記神経内の神経活動のプロファイルのうちの少なくとも1つである、
ことを特徴とする請求項28から請求項31のいずれか1項に記載の方法。 - 前記シグナルを印加する結果としての神経活動の前記変調は、該シグナルが印加される前記神経内の神経活動の少なくとも部分的な抑制、任意的に該シグナルが印加される該神経内の神経活動の完全な抑制であることを特徴とする請求項28から請求項32のいずれか1項に記載の方法。
- 前記シグナルを印加する結果としての神経活動の前記変調は、該シグナルが印加される前記神経内の神経活動の少なくとも部分的な遮断、任意的に神経活動の完全な遮断であることを特徴とする請求項33に記載の方法。
- 神経活動の前記変調は、実質的に永続的であることを特徴とする請求項28から請求項34のいずれか1項に記載の方法。
- 神経活動の前記変調は、一時的であることを特徴とする請求項28から請求項34のいずれか1項に記載の方法。
- 神経活動の前記変調は、是正的であることを特徴とする請求項28から請求項34のいずれか1項に記載の方法。
- 前記印加されるシグナルは、非破壊的シグナルであることを特徴とする請求項28から請求項37のいずれか1項に記載の方法。
- 前記印加されるシグナルは、電気シグナル、光シグナル、超音波シグナル、機械的シグナル、又は熱シグナルであることを特徴とする請求項28から請求項38のいずれか1項に記載の方法。
- 前記シグナルは、電気シグナルであり、かつキロヘルツ周波数の交流(AC)波形を含むことを特徴とする請求項39に記載の方法。
- 前記シグナルは、電気シグナルであり、かつ電荷均衡式直流(DC)波形を含むことを特徴とする請求項39又は請求項40に記載の方法。
- 前記シグナルは、電気シグナルであり、かつ実質的に順番に、
(i)DCランプと、それに続いてプラトー及び電荷均衡を印加する段階と、
(ii)波形が印加される期間中に波形の振幅が増大する第1のAC波形を印加する段階と、
(iii)前記第1のAC波形よりも小さい振幅及び/又は低い周波数を有する第2のAC波形を印加する段階と、
を含むことを特徴とする請求項39から請求項41のいずれか1項に記載の方法。 - 前記シグナルが1又は2以上のAC波形を含むときに、該1又は2以上のAC波形は、各々が5〜25kHz、任意的に10〜25kHz、任意的に15〜25kHz、任意的に20〜25kHzの周波数を有することを特徴とする請求項40から請求項42のいずれか1項に記載の方法。
- 前記シグナルは、1〜15V、3〜15V、5〜15V、任意的に10〜15Vの電圧を有することを特徴とする請求項41から請求項43のいずれか1項に記載の方法。
- 前記電圧は、3V、5V、10V、及び15Vから選択されることを特徴とする請求項44に記載の方法。
- 前記患者の1又は2以上の生理学的パラメータを検出する段階を更に含み、
前記シグナルは、前記検出された生理学的パラメータが事前定義閾値に適合するか又はそれを超えるときにのみ印加される、
ことを特徴とする請求項28から請求項45のいずれか1項に記載の方法。 - 1又は2以上の検出される生理学的パラメータが、副交感神経性緊張、ASM緊張、血中酸素飽和度、血中二酸化炭素濃度、呼吸数、全肺気量、及び努力肺活量から選択されることを特徴とする請求項46に記載の方法。
- 前記1又は2以上の検出された生理学的パラメータは、前記患者の神経内の活動電位又は活動電位のパターンを含み、
前記活動電位又は活動電位のパターンは、気管支収縮に関連付けられる、
ことを特徴とする請求項46又は請求項47に記載の方法。 - 前記活動電位は、前記患者の迷走神経、任意的に迷走神経の少なくとも1つの肺枝、任意的に該患者の迷走神経の少なくとも1つの肺枝の遠心性線維におけるものであることを特徴とする請求項48に記載の方法。
- 前記シグナルは、前記1又は2以上の生理学的パラメータを検出するように構成された1又は2以上の検出器を更に含む神経変調デバイスによって印加されることを特徴とする請求項28から請求項49のいずれか1項に記載の方法。
- 第1のシグナルが、前記患者の第1の迷走神経の一部又は全部に、任意的に該第1の迷走神経の少なくとも1つの肺枝に印加され、第2のシグナルが、該患者の同側又は反対側迷走神経の一部又は全部に、任意的に該同側又は反対側神経の少なくとも1つの肺枝に印加されることを特徴とする請求項28から請求項50のいずれか1項に記載の方法。
- 前記第1のシグナル及び第2のシグナルは、独立に選択されることを特徴とする請求項51に記載の方法。
- 前記第1のシグナル及び前記第2のシグナルは、同じシグナルであることを特徴とする請求項52に記載の方法。
- 前記シグナルが神経変調デバイスによって印加されるときに、各シグナルが、同じ神経変調デバイスによって印加されることを特徴とする請求項51から請求項53のいずれか1項に記載の方法。
- 前記シグナルが神経変調デバイスによって印加されるときに、各シグナルが、異なる神経変調デバイスによって印加されることを特徴とする請求項51から請求項53のいずれか1項に記載の方法。
- 前記患者に抗炎症薬を投与する段階を更に含むことを特徴とする請求項28から請求項55のいずれか1項に記載の方法。
- 前記抗炎症薬は、吸入によって投与されることを特徴とする請求項57に記載の方法。
- 前記抗炎症薬は、ステロイド、非ステロイド抗炎症薬、抗体、又はサイトカインであることを特徴とする請求項56又は請求項57に記載の方法。
- 前記ステロイドは、プロピオン酸ベクロメタゾン、ブデソニド、シクレソニド、フルニソリド、プロピオン酸フルチカゾン、モメタゾン、及びトリアムシノロンアセトニドから構成される群から選択されることを特徴とする請求項59に記載の方法。
- COPD、喘息、又は慢性咳を治療する方法に使用するための抗炎症薬であって、
前記方法は、患者の迷走神経の一部又は全部にシグナルを印加して該患者内の該神経の神経活動を変調する段階と、該患者に抗炎症薬を投与する段階とを含む、
ことを特徴とする抗炎症薬。 - 請求項60に記載の方法に使用するための抗炎症薬であって、
ステロイド、非ステロイド抗炎症薬、抗体、又はサイトカインである、
ことを特徴とする抗炎症薬。 - 請求項61に記載の方法に使用するための抗炎症薬であって、
ステロイドが、プロピオン酸ベクロメタゾン、ブデソニド、シクレソニド、フルニソリド、プロピオン酸フルチカゾン、モメタゾン、及びトリアムシノロンアセトニドから構成される群から選択される、
ことを特徴とする抗炎症薬。 - 前記患者は、哺乳類患者、任意的にヒト患者であることを特徴とする請求項1から請求項62のいずれか1項に記載の装置又は方法。
- 患者のCOPD、喘息、又は慢性咳、特にCOPD関連又は喘息関連の気管支収縮を治療する際に使用するための神経変調電気波形であって、
前記患者の迷走神経、好ましくは該迷走神経の肺枝に印加されたときに波形が該神経内の神経シグナリングを抑制するような5〜25kHzの周波数を有するAC波形である、
ことを特徴とする神経変調電気波形。 - 患者のCOPD、喘息、又は慢性咳、特にCOPD関連又は喘息関連の気管支収縮を該患者の迷走神経、好ましくは該迷走神経の肺枝、より好ましくは該迷走神経の該肺枝の遠心性線維内の神経活動を変調することによって治療するための神経変調デバイスの使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562119998P | 2015-02-24 | 2015-02-24 | |
| US62/119,998 | 2015-02-24 | ||
| PCT/US2016/019234 WO2016138066A1 (en) | 2015-02-24 | 2016-02-24 | Neuromodulation device |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2018508329A true JP2018508329A (ja) | 2018-03-29 |
| JP2018508329A5 JP2018508329A5 (ja) | 2019-04-04 |
Family
ID=56789175
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017562969A Pending JP2018508329A (ja) | 2015-02-24 | 2016-02-24 | 神経変調デバイス |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US10441787B2 (ja) |
| EP (2) | EP3261711B1 (ja) |
| JP (1) | JP2018508329A (ja) |
| KR (1) | KR20180008397A (ja) |
| CN (1) | CN107847740A (ja) |
| AU (1) | AU2016222825A1 (ja) |
| BR (1) | BR112017018068A2 (ja) |
| CA (1) | CA2977517A1 (ja) |
| ES (1) | ES2855799T3 (ja) |
| RU (1) | RU2017129539A (ja) |
| WO (1) | WO2016138066A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10029101B2 (en) | 2013-01-09 | 2018-07-24 | Mayo Foundation For Medical Education And Research | Systems for the detection and delivery of neurochemical and electrical signals for functional restoration |
| US11040197B2 (en) * | 2017-06-22 | 2021-06-22 | Mayo Foundation For Medical Education And Research | Voltammetric neurochemical detection in whole blood |
| CN109199359A (zh) * | 2018-10-15 | 2019-01-15 | 暨南大学 | 光电联合刺激系统和光电联合刺激神经纤维方法 |
| US11077314B1 (en) * | 2020-04-29 | 2021-08-03 | Multi Radiance Medical | System and method for treating patients requiring mechanical ventilation |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009515590A (ja) * | 2005-11-10 | 2009-04-16 | エレクトロコア、インコーポレイテッド | 気管支収縮の電気刺激治療 |
| US20140324129A1 (en) * | 2013-04-30 | 2014-10-30 | Case Western Reserve University | Systems and methods for temporary, incomplete, bi-directional, adjustable electrical nerve block |
| US20140371809A1 (en) * | 2005-07-28 | 2014-12-18 | Cyberonics, Inc. | Stimulating cranial nerve to treat pulmonary disorder |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7389145B2 (en) | 2001-02-20 | 2008-06-17 | Case Western Reserve University | Systems and methods for reversibly blocking nerve activity |
| US6928320B2 (en) * | 2001-05-17 | 2005-08-09 | Medtronic, Inc. | Apparatus for blocking activation of tissue or conduction of action potentials while other tissue is being therapeutically activated |
| US20060200219A1 (en) * | 2005-03-01 | 2006-09-07 | Ndi Medical, Llc | Systems and methods for differentiating and/or identifying tissue regions innervated by targeted nerves for diagnostic and/or therapeutic purposes |
| US9037247B2 (en) * | 2005-11-10 | 2015-05-19 | ElectroCore, LLC | Non-invasive treatment of bronchial constriction |
| US8874227B2 (en) * | 2009-03-20 | 2014-10-28 | ElectroCore, LLC | Devices and methods for non-invasive capacitive electrical stimulation and their use for vagus nerve stimulation on the neck of a patient |
| JP2009525805A (ja) * | 2006-02-10 | 2009-07-16 | エレクトロコア、インコーポレイテッド | 電気的変調を用いたアナフィラキシーの治療方法および治療装置 |
| US9579506B2 (en) * | 2008-01-25 | 2017-02-28 | Flint Hills Scientific, L.L.C. | Contingent cardio-protection for epilepsy patients |
| KR101719824B1 (ko) * | 2008-05-09 | 2017-04-04 | 호라이라 인코포레이티드 | 기관지나무 치료용 시스템, 어셈블리 및 방법 |
| US8918178B2 (en) | 2009-03-20 | 2014-12-23 | ElectroCore, LLC | Non-invasive vagal nerve stimulation to treat disorders |
| US9833621B2 (en) * | 2011-09-23 | 2017-12-05 | Setpoint Medical Corporation | Modulation of sirtuins by vagus nerve stimulation |
| EP3949885A1 (en) * | 2010-04-06 | 2022-02-09 | Nuvaira, Inc. | System for pulmonary treatment |
| US9358381B2 (en) * | 2011-03-10 | 2016-06-07 | ElectroCore, LLC | Non-invasive vagal nerve stimulation to treat disorders |
| WO2012159002A2 (en) * | 2011-05-19 | 2012-11-22 | Neuros Medical, Inc. | High-frequency electrical nerve block |
| US9398933B2 (en) | 2012-12-27 | 2016-07-26 | Holaira, Inc. | Methods for improving drug efficacy including a combination of drug administration and nerve modulation |
| US10413731B2 (en) * | 2014-01-17 | 2019-09-17 | Cardiac Pacemakers, Inc. | Selective nerve stimulation using presynaptic terminal depletion block |
-
2016
- 2016-02-24 RU RU2017129539A patent/RU2017129539A/ru not_active Application Discontinuation
- 2016-02-24 ES ES16756233T patent/ES2855799T3/es active Active
- 2016-02-24 CN CN201680023560.6A patent/CN107847740A/zh active Pending
- 2016-02-24 KR KR1020177026793A patent/KR20180008397A/ko unknown
- 2016-02-24 BR BR112017018068-5A patent/BR112017018068A2/pt not_active Application Discontinuation
- 2016-02-24 WO PCT/US2016/019234 patent/WO2016138066A1/en active Application Filing
- 2016-02-24 CA CA2977517A patent/CA2977517A1/en not_active Abandoned
- 2016-02-24 EP EP16756233.9A patent/EP3261711B1/en active Active
- 2016-02-24 AU AU2016222825A patent/AU2016222825A1/en not_active Abandoned
- 2016-02-24 US US15/552,475 patent/US10441787B2/en active Active
- 2016-02-24 JP JP2017562969A patent/JP2018508329A/ja active Pending
- 2016-02-24 EP EP20212912.8A patent/EP3808407A1/en not_active Withdrawn
-
2019
- 2019-09-05 US US16/562,139 patent/US20200009384A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20140371809A1 (en) * | 2005-07-28 | 2014-12-18 | Cyberonics, Inc. | Stimulating cranial nerve to treat pulmonary disorder |
| JP2009515590A (ja) * | 2005-11-10 | 2009-04-16 | エレクトロコア、インコーポレイテッド | 気管支収縮の電気刺激治療 |
| US20140324129A1 (en) * | 2013-04-30 | 2014-10-30 | Case Western Reserve University | Systems and methods for temporary, incomplete, bi-directional, adjustable electrical nerve block |
Non-Patent Citations (2)
| Title |
|---|
| KILGORE, KEVIN L., ET AL.: "Reversible Nerve Conduction Block Using Kilohertz Frequency Alternating Current", NEUROMODULATION: TECHNOLOGY AT THE NEURAL INTERFACE, vol. 17, no. 3, JPN6020041755, 2014, pages 242 - 255, XP055517592, ISSN: 0004377936, DOI: 10.1111/ner.12100 * |
| VRABEC, TINA L., ET AL.: "A Novel Waveform for No-Onset Nerve Block Combining Direct Current and Kilohertz Frequency Alternati", IN: 2013 6TH INTERNATIONAL IEEE/EMBS CONFERENCE ON NEURAL ENGINEERING (NER), JPN6020041753, 2013, pages 283 - 286, XP032538275, ISSN: 0004377935, DOI: 10.1109/NER.2013.6695927 * |
Also Published As
| Publication number | Publication date |
|---|---|
| US10441787B2 (en) | 2019-10-15 |
| KR20180008397A (ko) | 2018-01-24 |
| US20180043162A1 (en) | 2018-02-15 |
| RU2017129539A (ru) | 2019-03-25 |
| EP3261711B1 (en) | 2020-12-16 |
| CA2977517A1 (en) | 2016-09-01 |
| ES2855799T3 (es) | 2021-09-24 |
| EP3261711A1 (en) | 2018-01-03 |
| BR112017018068A2 (pt) | 2018-04-10 |
| EP3261711A4 (en) | 2019-02-20 |
| US20200009384A1 (en) | 2020-01-09 |
| CN107847740A (zh) | 2018-03-27 |
| EP3808407A1 (en) | 2021-04-21 |
| AU2016222825A1 (en) | 2017-09-07 |
| WO2016138066A1 (en) | 2016-09-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20210393949A1 (en) | Neuromodulation device | |
| US9707391B2 (en) | Method for modulation of effector organs | |
| AU2006315829B2 (en) | Electrical stimulation treatment of bronchial constriction | |
| Dicarlo et al. | Autonomic regulation therapy for the improvement of left ventricular function and heart failure symptoms: the ANTHEM-HF study | |
| US20200009384A1 (en) | Neuromodulation device | |
| JP6824889B2 (ja) | 神経調節装置 | |
| JP2018525092A (ja) | 神経調節デバイス | |
| US20240131327A1 (en) | Neuromodulation Device | |
| Benevides et al. | Optogenetic activation of the diaphragm | |
| JP2018523542A5 (ja) | ||
| JP7096167B2 (ja) | グルコース制御障害に関連する状態の治療 | |
| Ownby et al. | Cognitive training with and without transcranial direct current stimulation in older adults with HIV-related cognitive deficits: Delayed impact on mood |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190225 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190225 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200210 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200511 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201102 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210202 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20210714 |