WO2011003776A2 - Substituierte cyanobutyrate mit herbizider wirkung - Google Patents
Substituierte cyanobutyrate mit herbizider wirkung Download PDFInfo
- Publication number
- WO2011003776A2 WO2011003776A2 PCT/EP2010/059185 EP2010059185W WO2011003776A2 WO 2011003776 A2 WO2011003776 A2 WO 2011003776A2 EP 2010059185 W EP2010059185 W EP 2010059185W WO 2011003776 A2 WO2011003776 A2 WO 2011003776A2
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- formula
- alkyl
- compounds
- methyl
- haloalkyl
- Prior art date
Links
- 0 CC(C(C)=NN*)=N Chemical compound CC(C(C)=NN*)=N 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C255/00—Carboxylic acid nitriles
- C07C255/01—Carboxylic acid nitriles having cyano groups bound to acyclic carbon atoms
- C07C255/32—Carboxylic acid nitriles having cyano groups bound to acyclic carbon atoms having cyano groups bound to acyclic carbon atoms of a carbon skeleton containing at least one six-membered aromatic ring
- C07C255/41—Carboxylic acid nitriles having cyano groups bound to acyclic carbon atoms having cyano groups bound to acyclic carbon atoms of a carbon skeleton containing at least one six-membered aromatic ring the carbon skeleton being further substituted by carboxyl groups, other than cyano groups
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/34—Nitriles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/02—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms
- A01N43/24—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with two or more hetero atoms
- A01N43/26—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with two or more hetero atoms five-membered rings
- A01N43/28—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with two or more hetero atoms five-membered rings with two hetero atoms in positions 1,3
- A01N43/30—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with two or more hetero atoms five-membered rings with two hetero atoms in positions 1,3 with two oxygen atoms in positions 1,3, condensed with a carbocyclic ring
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N57/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic phosphorus compounds
- A01N57/18—Biocides, pest repellants or attractants, or plant growth regulators containing organic phosphorus compounds having phosphorus-to-carbon bonds
- A01N57/20—Biocides, pest repellants or attractants, or plant growth regulators containing organic phosphorus compounds having phosphorus-to-carbon bonds containing acyclic or cycloaliphatic radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C255/00—Carboxylic acid nitriles
- C07C255/49—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton
- C07C255/57—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton containing cyano groups and carboxyl groups, other than cyano groups, bound to the carbon skeleton
Definitions
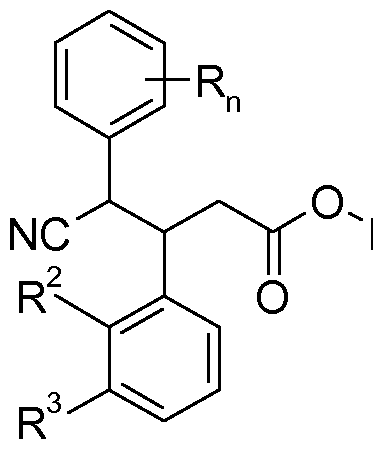
- the present invention relates to substituted cyanobutyrates of the formula I.
- R is halogen, cyano, nitro, C -C alkyl 4 -alkyl, Ci-C 4 haloalkyl, C 2 -C 6 alkenyl, C 2 -C 6 -alkyl kinyl,
- R a is hydrogen, OH, Ci-C 8 -alkyl, C 4 haloalkyl, ZC 3 -C 6 cycloalkyl, C 2 -C 8 - alkenyl, ZC 5 -C 6 cycloalkenyl, C 2 -C 8 Alkynyl, Z-Ci-C 6 alkoxy, Z-CrC 4 - haloalkoxy, ZC 3 -C 8 alkenyloxy, ZC 3 -C 8 alkynyloxy, NR 1 R ", Ci-C 6 alkyl sulfonyl, Z- (tri-C 1 -C 4 -alkyl) silyl, Z-phenyl, Z-phenoxy, Z-phenylamino and
- R 1 , R "independently of one another are hydrogen, C 1 -C 8 -alkyl, C 1 -C 4 -haloalkyl,
- R 1 and R can also together with the N-atom to which they are bonded form a 5- or 6-membered monocyclic or 9- or 10-membered bicyclic heterocycle containing 1, 2, 3 or 4 heteroatoms selected from O, N and S;
- R b independently of one another Z-CN, Z-OH, Z-NO 2 , Z-halogen, Ci-C 8 -
- R bb is C 1 -C 8 -alkyl and C 1 -C 6 -haloalkyl
- n 0, 1 or 2;
- R b can also form, together with the group R b attached to the adjacent carbon atom, a five- or six-membered saturated, partially or completely unsaturated ring which, in addition to carbon atoms, can contain 1, 2 or 3 heteroatoms selected from O, N and S. ;
- Z is a covalent bond or Ci-Cs-alkylene
- n 0, 1, 2, 3, 4 or 5;
- R 2 , R 3 independently of one another are halogen, cyano, nitro, C 1 -C 4 -alkyl, C 1 -C 4 -alkoxy,
- R 2 and R 3 may also together form a five- or six-membered saturated, partially or completely unsaturated mono- or bicyclic ring which may contain, in addition to carbon, 1, 2 or 3 heteroatoms selected from O, N and S and groups R b may be substituted;
- groups R and R 1 and their sub-substituents the carbon chains and / or the cyclic groups may be partially or completely substituted by groups R a and / or R b ,
- R 2 and R 3 are chlorine when R is hydrogen and R 1 is ethyl or allyl;
- the invention relates to processes and intermediates for the preparation of the compounds of formula I and their N-oxides, their agriculturally useful salts, agents containing them and their use as herbicides, i. for controlling harmful plants, and a method for controlling undesired plant growth, comprising allowing a herbicidally effective amount of at least one compound of formula I or an agriculturally useful salt thereof to act on plants, their seeds and / or their habitat.
- EP-A 5 341, EP-A 266 725, EP-A 270 830, JP 04/297 454, JP 04/297 455 and JP 05/058 979 disclose herbicidal cyanobutyrates, their herbicidal action, in particular at low levels
- An object of the present invention is to provide compounds having herbicidal activity.
- active ingredients should be made available which have a high herbicidal action, in particular even at low application rates, and their compatibility with crop plants for commercial exploitation is sufficient.
- the compounds according to the invention can be prepared analogously to the synthetic routes described in the cited documents by standard methods of organic chemistry, for example according to the following synthesis route:
- Phenylacetonitrile derivatives of the formula II can be reacted with cinnamate derivatives of the formula III in the sense of a Michael addition to give compounds of the formula I.
- the variables have the meaning given for formula I.
- This reaction is usually carried out at temperatures of -100 0 C to 150 0 C, preferably -78 ° C to 50 0 C, in a solvent in the presence of a base and / or a catalyst [see. J. Chem. Soc. (1945), p. 438].
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and petroleum ether, aromatic hydrocarbons such as toluene, o-, m- and p-xylene, halogenated hydrocarbons such as methylene chloride, chloroform and chlorobenzene, ethers such as diethyl ether, diisopropyl ether, tert-butyl methyl ether, dioxane , Anisole and tetrahydrofuran (THF), nitriles such as acetonitrile and propionitrile, ketones such as acetone, methyl ethyl ketone, diethyl ketone and tert-butyl methyl ketone, alcohols such as methanol, ethanol, n-propanol, isopropanol, n-butanol and tert. Butanol, and dimethyl sulfox
- Bases are generally inorganic compounds such as alkali metal and alkaline earth metal hydroxides such as lithium hydroxide, sodium hydroxide, potassium hydroxide and calcium hydroxide, alkali metal and alkaline earth metal oxides such as lithium oxide, sodium oxide, calcium oxide and magnesium oxide, alkali metal and alkaline earth metal hydrides such as lithium hydride, sodium hydride, potassium hydride and calcium hydride, Alkali metal amides such as lithium amide, sodium amide and potassium amide, alkali metal and alkaline earth metal carbonates such as lithium carbonate, potassium carbonate and calcium carbonate, and also alkali metal hydrogen carbonates such as sodium hydrogencarbonate, organometallic compounds, in particular alkali metal alkyls such as methyllithium, butyllithium and phenyllithium, alkylmagnesium halides such as methylmagnesium chloride and also alkali metal and alkaline earth metal alkoxides such as sodium methoxide, sodium ethanolate, potassium
- the bases are generally used in catalytic amounts, but they can also be used equimolar, in excess or optionally as a solvent.
- Acid catalysts include inorganic acids such as hydrofluoric acid, hydrochloric acid, hydrobromic acid, sulfuric acid and perchloric acid, Lewis acids such as boron trifluoride, aluminum trichloride, ferric chloride, tin IV chloride, titanium IV chloride, scandium III triflate and zinc -ll-chloride, and organic acids such as formic acid, acetic acid, propionic acid, oxalic acid, toluenesulfonic acid, benzenesulfonic acid,
- Camphorsulfonic acid, citric acid and trifluoroacetic acid use.
- the acids are generally used in catalytic amounts, but they can also be used equimolar, in excess or optionally as a solvent.
- the compounds of formula I can also be obtained by U-esterification of other Cyanobutyrate be obtained. This can be done by various methods, for example according to the following:
- the transesterification can be carried out in the presence of molecular sieve in an alcohol R 1 -OH, optionally in an aprotic solvent.
- This reaction is usually carried out at temperatures of 0 0 C to 180 ° C, preferably 20 0 C to 80 0 C in the presence of a Lewis or Branstedtklare or an enzyme [cf.. J. Org. Chem. 2002, 67, 431].
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and petroleum ether, aromatic hydrocarbons such as toluene, o-, m- and p-xylene, halogenated hydrocarbons such as methylene chloride, chloroform and chlorobenzene, ethers such as diethyl ether, diisopropyl ether, tert-butyl methyl ether , Dioxane, anisole and THF, nitriles such as acetonitrile and propionitrile, ketones, as well as dimethyl sulfoxide, dimethylformamide and dimethylacetamide, more preferably alcohol R 1 -OH.
- aliphatic hydrocarbons such as pentane, hexane, cyclohexane and petroleum ether
- aromatic hydrocarbons such as toluene, o-, m- and p-xylene
- transesterification may be by acid or base saponification of other cyanobutyrates (a), followed by reaction with an alcohol R 1 -OH.
- a cyanobutyrate
- These reactions are usually carried out at temperatures of from 0 C to 12O 0 C, preference example, 2O 0 C to 5O 0 C in the presence of a base, or an acid and / or a catalyst [see. J. Am. Chem. Soc. 2007, 129 (43), 13321; J. Org. Chem. 1984, 49 (22), 4287.].
- Suitable solvents are aliphatic hydrocarbons such as pentane, hexane, cyclohexane and petroleum ether, aromatic hydrocarbons such as toluene, o-, m- and p-xylene, halogenated hydrocarbons such as methylene chloride, chloroform and chlorobenzene, ethers such as diethyl ether, diisopropyl ether, tert-butyl methyl ether, dioxane , Anisole and THF, nitriles such as acetonitrile and propionitrile, ketones such as acetone, methyl ethyl ketone, diethyl ketone and tert-butyl methyl ketone, alcohols such as methanol, ethanol, n-propanol, isopropanol, n-butanol and tert-butanol, and dimethyl sulfoxide, dimethylformamide and Dimethyl
- Suitable bases are generally inorganic compounds such as alkali metal and alkaline earth metal hydroxides such as lithium hydroxide, sodium hydroxide, potassium hydroxide and calcium hydroxide, alkali metal and alkaline earth metal oxides such as lithium oxide, sodium oxide, calcium oxide and magnesium oxide, alkali metal and alkaline earth metal hydrides such as lithium hydride, sodium hydride, potassium hydride and Calcium hydride, alkali metal amides such as lithium amide, sodium amide and potassium amide, alkali metal and alkaline earth metal carbonates such as lithium carbonate, potassium carbonate and calcium carbonate and alkali metal hydrogen carbonates such as sodium bicarbonate, organometallic compounds, in particular alkali metal alkyls such as methyllithium, butyllithium and phenyllithium, Alkylmeas- siumhalogenide such as methylmagnesium chloride and alkali metal and Alkaline earth metal alkoxides such as sodium methoxide, sodium ethoxid
- acids and acidic catalysts are inorganic acids such as hydrofluoric acid, hydrochloric acid, hydrobromic acid, sulfuric acid and perchloric acid, Lewis acids such as boron trifluoride, aluminum trichloride, ferric chloride, stannic chloride, titanium IV chloride and zinc II chloride , and organic acids such as formic acid, acetic acid, propionic acid, oxalic acid, toluenesulfonic acid, benzenesulfonic acid, camphorsulfonic acid, citric acid and trifluoroacetic acid use.
- inorganic acids such as hydrofluoric acid, hydrochloric acid, hydrobromic acid, sulfuric acid and perchloric acid
- Lewis acids such as boron trifluoride, aluminum trichloride, ferric chloride, stannic chloride, titanium IV chloride and zinc II chloride
- organic acids such as formic acid, acetic acid, propionic acid, oxalic acid, tolu
- the acids are generally used in catalytic amounts, but they can also be used equimolar, in excess or optionally as a solvent.
- the starting materials required for the preparation of the compounds I are known in the literature or can be prepared according to the cited literature.
- the reaction mixtures are worked up in the usual way, e.g. by mixing with water, separation of the phases and optionally chromatographic purification of the crude products.
- the intermediate and end products are z.T. in the form of colorless or pale brownish, viscous oils, which are freed or purified under reduced pressure and at moderately elevated temperature from volatile constituents. If the intermediate and end products are obtained as solids, the purification can also be carried out by recrystallization or trituration.
- hydrocarbon chains such as alkyl, halo (gen) alkyl, alkenyl, alkynyl, and the alkyl moieties and alkenyl moieties in alkoxy, halo (gen) alkoxy, Alkylamino, dialkylamino, N-alkylsulfonylamino, alkenyloxy, alkynyloxy, alkoxyamino, alkylaminosulfonylamino, dialkylaminosulfonylamino, alkenylamino, alkynylamino, N- (alkenyl) -N- (alkyl) -amino, N- (alkynyl) -N- (alkyl) -amino, N- (alkoxy) -N- (alkyl) -amino, N- (alkenyl) -N- (alkoxy) -amino or N- (alkynyl) -N-N
- halogenated substituents preferably carry one to five identical or different halogen atoms, in particular fluorine atoms or chlorine atoms.
- halogen in each case represents fluorine, chlorine, bromine or iodine.
- Alkyl and the alkyl moieties for example, in alkoxy, alkylamino, dialkylamino, N-alkylsulfonylamino, alkylaminosulfonylamino, dialkylaminosulfonylamino, N- (alkenyl) -N- (alkyl) -amino, N- (alkynyl) -N- (alkyl) -amino, N- (Alkoxy) -N- (alkyl) -amino: saturated, straight-chain or branched hydrocarbon radicals having one or more C atoms, for example 1 to 2, 1 to 4, or 1 to 6 carbon atoms, for example C 1 -C 6 -alkyl such as methyl, ethyl, propyl, 1-methylethyl, butyl, 1-methylpropyl, 2-methylpropyl, 1, 1-dimethylethyl, pentyl, 1-methylbutyl, 2-methyl
- Haloalkyl also referred to as haloalkyl: an alkyl radical as mentioned above, the hydrogen atoms of which are partially or completely substituted by halogen atoms such as fluorine, chlorine, bromine and / or iodine, e.g.
- Cycloalkyl and the cycloalkyl moieties for example, in cycloalkoxy or cycloalkylcarbonyl: monocyclic, saturated hydrocarbon groups having three or more C atoms, e.g. 3 to 6 carbon ring members such as cyclopropyl, cyclobutyl, cyclopentyl and cyclohexyl.
- Alkenyl and alkenyl moieties for example, in alkenylamino, alkenyloxy, N- (alkenyl) -N- (alkyl) -amino, N- (alkenyl) -N- (alkoxy) -amino: monounsaturated, straight-chain or branched hydrocarbon radicals having two or more carbon atoms. Atoms, z. 2 to 4, 2 to 6 or 3 to 6 carbon atoms and a double bond in any position, e.g.
- C2-C6 alkenyl such as ethenyl, 1-propenyl, 2-propenyl, 1-methylethenyl, 1-butenyl, 2-butenyl, 3-butenyl, 1-methyl-1-propenyl, 2-methyl-1-propenyl, 1 Methyl 2-propenyl, 2-methyl-2-propenyl, 1-pentenyl, 2-pentenyl, 3-pentenyl, 4-pentenyl, 1-methyl-1-butenyl, 2-methyl-1-butenyl, 3 Methyl-1-butenyl, 1-methyl-2-butenyl, 2-methyl-2-butenyl, 3-methyl-2-butenyl, 1-methyl-3-butenyl, 2-methyl-3-butenyl, 3-methyl 3-butenyl, 1, 1-dimethyl-2-propenyl, 1, 2-dimethyl-1-propenyl, 1, 2-dimethyl-2-propenyl, 1-ethyl-1-propenyl, 1-ethyl-1
- Cycloalkenyl monocyclic, monounsaturated hydrocarbon groups having 3 to 6, preferably 5 to 6 carbon ring members, such as cyclopenten-1-yl, cyclopentene-3-yl, cyclohexen-1-yl, cyclohexen-3-yl, cyclohexen-4-yl ,
- Alkynyl and alkynyl moieties for example in alkynyloxy, alkynylamino, N- (alkynyl) -N- (alkyl) -amino or N- (alkynyl) -N- (alkoxy) -amino: straight-chain or branched hydrocarbon groups having two or more carbon atoms , z. B. 2 to 4, 2 to 6, or 3 to 6 carbon atoms and a triple bond in any position, for.
- C 2 -C 6 -alkynyl such as ethynyl, 1-propynyl, 2-propynyl, 1-butynyl, 2-butynyl, 3-butynyl, 1-methyl-2-propynyl, 1-pentynyl, 2-pentynyl, 3-pentynyl, 4-pentynyl, 1-methyl-2-butynyl, 1-methyl-3-butynyl, 2-methyl-3-butynyl, 3-methyl-1-butynyl, 1, 1-dimethyl-2-propynyl, 1-ethyl 2-propynyl, 1-hexynyl, 2-hexynyl, 3-hexynyl, 4-hexynyl, 5-hexynyl, 1-methyl-2-pentynyl, 1-methyl-3-pentynyl, 1-methyl-4-pentynyl, 2- Methyl-3-pentynyl, 2-methyl
- Alkoxy alkyl, as defined above, which is bonded via an oxygen atom: z.
- 5- or 6-membered heterocycle a cyclic group having 5 or 6 ring atoms wherein 1, 2, 3 or 4 ring atoms are heteroatoms selected from O, S and N, the cyclic group being saturated, partially unsaturated or aromatic is.
- the compounds of formula I contain two chiral centers and, depending on the substitution pattern, may contain one or more others.
- the compounds according to the invention can therefore be present as pure enantiomers or diastereomers or as enantiomer or diastereomer mixtures.
- the invention relates to both the pure enantiomers or diastereomers and mixtures thereof.
- the compounds of the formula I can also be present in the form of the N-oxides and / or their agriculturally useful salts, the type of salt generally not being important.
- the salts of those cations or the acid addition salts of those acids come into consideration whose cations, or anions, do not adversely affect the herbicidal activity of the compounds I.
- the cations used are, in particular, ions of the alkali metals, preferably lithium, sodium or potassium, the alkaline earth metals, preferably calcium or magnesium, and the transition metals, preferably manganese, copper, zinc or iron. It is likewise possible to use ammonium as cation, in which case, if desired, one to four hydrogen atoms are represented by C 1 -C 4 -alkyl, hydroxy-C 1 -C 4 -alkyl, C 1 -C 4 -alkoxy-C 1 -C 4 -alkyl, hydroxyC 1 -C 4 alkoxy-C 1 -C 4 -alkyl, phenyl or benzyl, preferably ammonium, dimethylammonium, diisopropylammonium, tetramethylammonium, tetrabutylammonium, 2- (2-hydroxyeth-1-oxy) eth-1-ylammonium, di (2-hydroxyethyl) 1-yl)
- ammonium cation is the pyridine nitrogen atom of the formula I quaternized by alkylation or arylation.
- Anions of useful acid addition salts are primarily chloride, bromide, fluoride, hydrogen sulfate, sulfate, dihydrogen phosphate, hydrogen phosphate, nitrate, bicarbonate, carbonate, hexafluorosilicate, hexafluorophosphate, benzoate and the anions of Ci-C4-alkanoic acids, preferably formate, acetate, propionate, Butyrate or trifluoroacetate.
- variables of the compounds of the formula I have the following meanings, these being considered both individually and in combination with one another in particular embodiments of the compounds of the formula I:
- the subscript n stands for a value of 0 to 3, preferably for 0 or 1, in particular for 1. In another embodiment, it stands for 0. If at least one group R is present, it stands preferably in the positions 3, 4 and / or 5, in particular 3 or 4. If the index n is 2, the groups R are preferably in positions 2.5 or 3.4.
- Embodiments of the group (s) R concern halogen, in particular chlorine or fluorine. Further embodiments of the group (s) R concern cyano or nitro, in particular cyano. Particularly preferred embodiments of the group R n include the following:
- Preferred embodiments of the group R 1 relate to hydrogen, C 1 -C 6 -alkyl, cyano-C 1 -C 4 -alkyl, C 3 -C 6 -alkynyl, C 3 -C 6 -alkynyl, C 1 -C 8 -haloalkyl, if appropriate subst.
- Particularly preferred embodiments of the group R 1 relate to hydrogen, C 1 -C 4 -alkyl, cyanomethyl, allyl, propargyl, C 1 -C 4 -haloalkyl containing preferably 1 to 3 halogen atoms, phenyl or benzyl, which aromatic groups may be partially or completely substituted.
- Particularly preferred embodiments for R 1 include the following: H, CH 3 , C 2 H 5 , CH 2 CN, CH 2 C ⁇ CH, CH 2 CH 2 F, CH 2 CHF 2 , CH 2 CF 3 , CH 2 OCH 3 ,
- Preferred embodiments of the group R 2 relate to halogen, cyano, nitro, C T C 4 - AI alkyl, Ci-C 4 alkoxy, S (O) m R bb, NR 1 R "Ci-C 4 haloalkyl, Ci- C 4 haloalkoxy
- Particularly preferred embodiments of the group R 2 include halogen, CN, NO 2 , CH 3 , CHF 2 , CF 3 , OCHF 2 , OCF 3.
- Particularly preferred embodiments of the group R 2 are selected from fluorine, chlorine, bromine and more preferably, R 2 is not chlorine.
- R 2 is fluorine
- R 2 is bromine
- R 2 is iodine.
- Preferred embodiments of the group R 3 relate to halogen, cyano, nitro, Ci-C 4 - AI alkyl, Ci-C 4 alkoxy, S (O) m R bb, NR 1 R "Ci-C 4 haloalkyl, Ci- C 4 haloalkoxy
- Particularly preferred embodiments of the group R 3 relate to halogen, CN, NO 2 , CH 3 , CHF 2 , CF 3 , OCHF 2 , OCF 3.
- Particularly preferred embodiments of the group R 3 are selected from fluorine, chlorine, bromine and iodine, more preferably R 3 is not chlorine.
- R 3 is fluorine
- R 3 is bromine
- R 3 is iodine.
- the compounds I and their agriculturally useful salts are suitable - both as mixtures of isomers and in the form of pure isomers - as herbicides. They are suitable as such or as appropriately formulated agent.
- the herbicidal compositions containing the compound I, in particular the preferred embodiments thereof control plant growth on non-crop surfaces very well, especially at high application rates. In crops such as wheat, rice, corn, soybeans and cotton, they act against weeds and grass weeds without significantly damaging the crops. This effect occurs especially at low application rates.
- the compounds I, in particular the preferred embodiments thereof, or agents containing them can be used in a further number of crop plants for the removal of undesirable plants. For example, the following cultures may be considered:
- crops also includes those that have been modified by breeding, mutagenesis or genetic engineering methods.
- Genetically engineered plants are plants whose genetic material has been altered in a manner that does not occur under natural conditions by crossing, mutations or natural recombination (i.e., rearrangement of genetic information).
- one or more genes are integrated into the genome of the plant in order to improve the properties of the plant.
- crops thus also encompasses plants which by breeding and genetic engineering measures tolerance to certain herbicide classes, such as hydroxyphenylpyruvate dioxygenase (HPPD) inhibitors, acetolactate synthase (ALS) inhibitors, such as. Sulfonylureas (EP-A 257 993, US Pat. No. 5,013,659) or imidazolinones (see, for example, US Pat. Nos. 6,222,100, WO 01/82685, WO 00/26390, WO 97/41218, US Pat.
- HPPD hydroxyphenylpyruvate dioxygenase
- ALS acetolactate synthase
- Sulfonylureas EP-A 257 993, US Pat. No. 5,013,659
- imidazolinones see, for example, US Pat. Nos. 6,222,100, WO 01/82685, WO 00/26390, WO 97/41218, US Pat.
- WO 03/13225, WO 03/14356, WO 04/16073), enolpyruvylshikimate-3-phosphate synthase (EPSPS) -inhibitors such. Glyphosate (see, for example, WO 92/00377), glutamine synthetase (GS) inhibitors such as. Glufosinate (see eg EP-A 242 236, EP-A 242 246) or oxynil herbicides (see eg US 5,559,024).
- crops eg. As Clearfield® rapeseed, which produces a tolerance to imidazolinones, z. As imazamox, have.
- crops such as soybean generated yes, cotton, corn, beets and rape, which are resistant to glyphosate or glufosinate, which under the trade names RoudupReady ® (glyphosate) and Liberty Link ® (glufosinate) can be obtained.
- crops thus also includes plants that use genetic engineering measures one or more toxins, eg. As those from the bacterial strain Bacillus ssp., Produce.
- Toxins produced by such genetically engineered plants include e.g. Insecticidal proteins of Bacillus spp., In particular B. thuringiensis such as the endotoxins CrylAb, CrylAc, CrylF, Cry1Fe2, Cry2Ab, Cry3A, Cry3Bb1, Cry9c, Cry34Ab1 or Cry35Ab1; or vegetative insecticidal proteins (VIPs) 1 eg VIP1, VIP2, VIP3, or VIP3A; insecticidal proteins of nematode-colonizing bacteria, e.g.
- RIPs Ribosome Inactivating Proteins
- Steroid metabolizing enzymes e.g. 3-hydroxysteroid oxidase, ecdysteroid IDP glycosyltransferase, cholesterol oxidase, ecdysone inhibitors or HMG-CoA reductase
- ion channel blocker e.g.
- toxins can also be produced in the plants as proteoxins, hybrid proteins, truncated or otherwise modified proteins.
- Hybrid proteins are characterized by a novel combination of different protein domains (see, for example, WO 2002/015701). Further examples of such toxins or genetically modified plants which produce these toxins are described in EP-A 374 753, WO 93/007278, WO 95/34656, EP-A 427 529, EP-A 451 878,
- the methods for producing these genetically modified plants are known in the art and z. As set forth in the publications mentioned above. Many of the aforementioned toxins confer on the plants that produce them a tolerance to pests of all taxonomic arthropod classes, in particular to beetles (Coeleropta), diptera (Diptera) and butterflies (Lepidoptera) and nematodes (Nematoda).
- Agrisure ® CB and Bt176 from Syngenta Seeds SAS, France corn varieties which produce the toxin CrylAb and the PAT enzyme
- MIR604 from Syngenta Seeds SAS, France
- MON 863 from Monsanto Europe SA, Belgium
- IPC 531 from Monsanto Europe SA, Belgium
- cottons producing a modified version of the toxin CrylAc 1507 from Pioneer Overseas Corporation, Belgium (maize varieties producing the toxin Cryl F and the PAT enzyme).
- crops thus also includes plants that produce by genetic engineering measures one or more proteins that cause increased resistance or resistance to bacterial, viral or fungal pathogens, such as.
- PR proteins pathogenesis-related proteins
- resistance proteins eg, potato varieties that produce two resistance genes against Phytophthora infestans from the Mexican wild potato Solanum bulbocastanum
- T4 lysozyme z. Potato varieties resistant to bacteria such as Erwinia amylvora by the production of this protein).
- crops thus also includes plants whose productivity has been improved by means of genetic engineering methods by z.
- yield eg biomass, grain yield, starch, oil or protein content
- tolerance to drought salt or other limiting environmental factors or resistance to pests and fungal, bacterial and viral pathogens may be increased.
- crops also includes plants whose ingredients have been modified in particular to improve the human or animal diet using genetic engineering methods by z.
- oil plants can produce health-promoting long-chain omega-3 fatty acids or monounsaturated omega-9 fatty acids (eg Nexera ® oilseed rape).
- crops also includes plants that have been modified for the improved production of raw materials by means of genetic engineering methods by z.
- the compounds of the formula I are also suitable for the defoliation and / or desiccation of plant parts, for which crop plants such as cotton, potato, oilseed rape, sunflower, soybean or field beans, in particular cotton, come into consideration.
- compositions for the desiccation and / or defoliation of plants, processes for the preparation of these agents and methods for the desiccation and / or defoliation of plants with the compounds of formula I have been found.
- Desiccants are the compounds of formula I in particular for drying the aerial parts of crop plants such as potato, rape, sunflower and soybean but also cereals. This enables a completely mechanical harvesting of these important crops. Of economic interest is also the relief of the crop, which is made possible by the time-concentrated drop or decrease in the adhesion to the tree in citrus fruits, olives or other types and varieties of pome, stone and peel fruit.
- the same mechanism that is, the promotion of the formation of release tissue between fruit or leaf and shoot part of the plants is also essential for a well controllable defoliation of crops, especially cotton.
- shortening the time interval in which the individual cotton plants ripen results in increased fiber quality after harvest.
- the compounds I or the herbicidal compositions containing them can, for example, in the form of directly sprayable aqueous solutions, powders, suspensions, even high-percentage aqueous, oily or other suspensions or dispersions, emulsions, oil dispersions, pastes, dusts, scattering agents or granules by spraying, atomizing , Dusting, scattering, pouring or treatment of the seed or mixing with the seed.
- the forms of application depend on the intended use; In any case, they should ensure the finest possible distribution of the active compounds according to the invention.
- the herbicidal compositions contain a herbicidally effective amount of at least one compound of the formula I or an agriculturally useful salt of I and auxiliaries customary for the formulation of crop protection agents.
- auxiliaries are preferred auxiliaries, solid carriers, surface-active substances (such as dispersants, protective colloids, emulsifiers, wetting agents and adhesives), organic and inorganic thickeners, bactericides, antifreeze agents, defoamers, if necessary, dyes and for seed formulations adhesives.
- surface-active substances such as dispersants, protective colloids, emulsifiers, wetting agents and adhesives
- organic and inorganic thickeners such as bactericides, antifreeze agents, defoamers, if necessary, dyes and for seed formulations adhesives.
- thickeners ie, compounds which impart modified flowability to the formulation, ie, high-level at low viscosity and low viscosity in the agitated state
- polysaccharides such as xanthan gum (Kelzan® from Kelco), Rhodopol® 23 (Rhone Poulenc) or Veegum ® (RT Vanderbilt) and organic and inorganic layer minerals such as Attaclay® (Engelhardt).
- antifoams examples include silicone emulsions (such as, for example, Silikon® SRE, Wacker or Rhodorsil® from Rhodia), long-chain alcohols, fatty acids, salts of fatty acids, organofluorine compounds and mixtures thereof.
- Bactericides may be added to stabilize the aqueous herbicidal formulation.
- bactericides are bactericides based on diclorophene and benzyl alcohol hemiformal (Proxel® from ICI or Acticide® RS from Thor Chemie and Kathon® MK from Rohm & Haas) as well as isothiazolinone derivatives such as alkylisothiazolinones and benzisothiazolinones (Acticide MBS der Fa. Thor Chemie)
- antifreeze agents are ethylene glycol, propylene glycol, urea or glycerol.
- colorants are both water-insoluble pigments and water-soluble dyes. Examples which may be mentioned under the names rhodamine B, Cl. Pigment Red 112 and Cl.
- Solvent Red 1 known dyes, and pigment blue 15: 4, pigment blue 15: 3, pigment blue 15: 2, pigment blue 15: 1, pigment blue 80, pigment yellow 1, pigment yellow 13, pigment red 1 12, pigment red 48: 1, pigment red 48: 1, pigment red 57: 1, pigment red 53: 1, pigment orange 43, pigment orange 34, pigment orange 5, pigment green 36, pigment green 7, pigment white 6, pigment brown 25, basic violet 10, basic violet 49, acid red 51, acid red 52, acid red 14, acid blue 9, acid yellow 23, basic red 10, basic red 108.
- adhesives examples include polyvinyl pyrrolidone, polyvinyl acetate, polyvinyl alcohol and Tylose.
- Suitable inert additives are, for example:
- Mineral oil fractions of medium to high boiling point such as kerosene or diesel oil, coal tar oils and oils of vegetable or animal origin, aliphatic, cyclic and aromatic hydrocarbons, e.g. Paraffin, tetrahydronaphthalene, alkylated naphthalenes or their derivatives, alkylated benzenes or their derivatives, alcohols such as methanol, ethanol, propanol, butanol, cyclohexanol, ketones such as cyclohexanone or strongly polar solvents, eg. As amines such as N-methylpyrrolidone or water.
- amines such as N-methylpyrrolidone or water.
- Solid carriers are mineral soils such as silicic acids, silica gels, silicates, talc, kaolin, limestone, lime, chalk, bolus, loess, clay, dolomite, diatomaceous earth, calcium and magnesium sulfate, magnesium oxide, ground plastics, fertilizers such as ammonium sulfate, ammonium phosphate, ammonium nitrate, Ureas and vegetable products such as cereal flour, tree bark, wood and nutshell flour, cellulose powder or other solid carriers.
- mineral soils such as silicic acids, silica gels, silicates, talc, kaolin, limestone, lime, chalk, bolus, loess, clay, dolomite, diatomaceous earth, calcium and magnesium sulfate, magnesium oxide, ground plastics, fertilizers such as ammonium sulfate, ammonium phosphate, ammonium nitrate, Ureas and vegetable products such as cereal flour, tree bark, wood and nutshell flour
- alkali alkaline earth
- ammonium salts of aromatic sulfonic acids eg lignosulfonic acids (eg Borrespers types, Borregaard), phenolsulfonic acids, naphthalenesulfonic acids (Morwet types , Akzo Nobel) and dibutylnaphthalenesulfonic acid (Nekal types, BASF SE)
- fatty acids alkyl and alkylarylsulfonates, alkyl, lauryl ether and fatty alcohol sulfates, as well as salts of sulfated hexa-, hepta- and octadecanols and of fatty alcohol glycol ethers, condensation products of sulfonated naphthalene and its derivatives with formaldehyde, condensation products of naphthalene
- Powders, dispersants and dusts may be prepared by mixing or co-grinding the active substances with a solid carrier.
- Granules e.g. Coating, impregnation and homogeneous granules can be prepared by binding the active compounds to solid carriers.
- Aqueous application forms can be prepared from emulsion concentrates, suspensions, pastes, wettable powders or water-dispersible granules by adding water.
- emulsions, pastes or oil dispersions the compounds of the formula I or Ia, as such or dissolved in an oil or solvent, can be homogenized in water by means of wetting agents, tackifiers, dispersants or emulsifiers.
- concentrates consisting of active substance, wetting, adhesion, dispersing or emulsifying agent and possibly solvent or oil, which are suitable for dilution with water.
- the concentrations of the compounds of the formula I in the ready-to-use formulations can be varied within wide limits.
- the formulations generally contain from 0.001 to 98% by weight, preferably from 0.01 to 95% by weight, of at least one active ingredient.
- the active ingredients are used in a purity of 90% to 100%, preferably 95% to 100% (according to NMR spectrum).
- the compounds I according to the invention can be formulated, for example, as follows:
- active compound 20 parts by weight are dissolved in 70 parts by weight of cyclohexanone with the addition of 10 parts by weight of a dispersant, e.g. Polyvinylpyrrolidone dissolved. Dilution in water gives a dispersion.
- a dispersant e.g. Polyvinylpyrrolidone dissolved. Dilution in water gives a dispersion.
- the active ingredient content is 20% by weight
- active compound 15 parts by weight of active compound are dissolved in 75 parts by weight of an organic solvent (for example alkylaromatics) with the addition of calcium dodecylbenzenesulfonate and castor oil ethoxylate (in each case 5 parts by weight). Dilution in water results in an emulsion.
- the formulation has 15% by weight active ingredient content.
- active compound 25 parts by weight of active compound are dissolved in 35 parts by weight of an organic solvent (for example alkylaromatics) with addition of calcium dodecylbenzenesulfonate and castor oil ethoxylate (in each case 5 parts by weight).
- organic solvent for example alkylaromatics
- calcium dodecylbenzenesulfonate and castor oil ethoxylate in each case 5 parts by weight.
- This mixture is added by means of an emulsifying machine (eg Ultraturax) in 30 parts by weight of water and a homogeneous emulsion brought. Dilution in water results in an emulsion.
- the formulation has an active ingredient content of 25% by weight.
- active compound 20 parts by weight of active compound are comminuted with the addition of 10 parts by weight dispersing and wetting agents and 70 parts by weight of water or an organic solvent in a stirred ball mill to a fine active substance suspension. Dilution in water results in a stable suspension of the active ingredient.
- the active ingredient content in the formulation is 20% by weight.
- active compound 50 parts by weight are finely ground with the addition of 50 parts by weight of dispersants and wetting agents and prepared by means of industrial equipment (for example extrusion, spray tower, fluidized bed) as water-dispersible or water-soluble granules. Dilution in water results in a stable dispersion or solution of the active ingredient.
- the formulation has an active ingredient content of 50% by weight.
- active compound 75 parts by weight of active compound are ground with the addition of 25 parts by weight of dispersing and wetting agents and silica gel in a rotor-Strator mill. Dilution in water results in a stable dispersion or solution of the active ingredient.
- the active ingredient content of the formulation is 75% by weight.
- 0.5 parts by weight of active compound are finely ground and combined with 99.5 parts by weight of carriers. Common processes are extrusion, spray drying or fluidized bed. This gives a granulate for direct application with 0.5 wt .-% active ingredient content.
- the application of the compounds I or the herbicidal compositions containing them can be carried out in the pre-emergence, postemergence or together with the seed of a crop. It is also possible, the herbicidal agents or agents in that seed of a crop plant pretreated with the herbicidal agents or active substances is applied. If the active ingredients are less compatible with certain crops, then application techniques may be employed whereby the herbicidal agents are sprayed by the sprayers so as not to hit the leaves of the sensitive crop if possible, while the active ingredients affect the leaves underneath growing undesirable plants or the uncovered floor surface (post-directed, lay-by).
- the application of the compounds of the formula I or of the herbicidal compositions can be carried out by treating seed.
- the treatment of seed comprises essentially all techniques familiar to the skilled worker (seed dressing, seed coating, seed dusting, seed soaking, seed film coating, seed multilayer coating, seed encrusting, seed dripping and seed pelleting) based on the compounds of the formula according to the invention I or funds produced therefrom.
- the herbicidal agents can be diluted or applied undiluted.
- seed includes seeds of all kinds, e.g. Grains, seeds, fruits, tubers, cuttings and similar forms.
- seed preferably describes grains and seeds here.
- Seeds of the abovementioned crops but also the seeds of transgenic or obtained by conventional breeding methods plants can be used as seeds.
- the application rates of active ingredient are 0.001 to 3.0, preferably 0.01 to 1.0 kg / ha of active substance (a. S.).
- the compounds I are usually used in amounts of 0.001 to 10 kg per 100 kg of seed.
- Safeners are chemical compounds that prevent or reduce damage to crops without significantly affecting the herbicidal activity of the compounds of formula I on undesirable plants. They can be used both before sowing (for example in seed treatments, cuttings or seedlings) as well as in the pre- or post-emergence of the crop. The safeners and the compounds of formula I can be used simultaneously or sequentially.
- Suitable safeners are, for example, (quinoline- ⁇ -oxy) acetic acids, 1-phenyl-5-haloalkyl-1H-1, 2,4-triazole-3-carboxylic acids, 1-phenyl-4,5-dihydro-5 alkyl-1H-pyrazole-3,5-dicarboxylic acids, 4,5-dihydro-5,5-diaryl-3-isoxazolecarboxylic acids, dichloroacetamides, alpha-oximinophenylacetonitriles, acetophenone oximes, 4,6-dihalo-2-phenylpyrimidines, N- [ [4- (aminocarbonyl) phenyl] sulfonyl] -2-benzoic acid amides, 1,8-naphthalic anhydride, 2-halo-4- (haloalkyl) -5-thiazolecarboxylic acids, phosphorothiolates and N-alkyl-O-phenylcarba
- the compounds of formula I can be mixed with numerous representatives of other herbicidal or growth-regulating active ingredient groups or with safeners and applied together.
- herbicides which can be used in combination with the pyridine compounds of the formula I according to the present invention are:
- Bilanaphos (bialaphos), bilanaphos-sodium, glufosinate and glufosinate-ammonium; b8) from the group of DHP synthase inhibitors: asulam;
- Y is phenyl or 5- or 6-membered heteroaryl as defined above, which may be substituted by one to three groups R aa ; R 21 , R 22 , R 23 , R 24 are H, halogen, or C 1 -C 4 -alkyl; X is O or NH; n 0 or 1.
- R 21 , R 22 , R 23 , R 24 are H, Cl, F or CH 3 ;
- R 25 is halogen, C 1 -C 4 -alkyl or C 1 -C 4 -haloalkyl;
- R 26 is C 1 -C 4 -alkyl;
- R 27 is halogen, C 1 -C 4 -alkoxy or C 1 -C 4 -haloalkoxy;
- R 28 is H, halogen, Ci-C 4 - alkyl, Ci-C 4 haloalkyl or Ci-C4-haloalkoxy;
- m is 0, 1, 2 or 3;
- Preferred compounds of the formula 2 have the following meanings:
- Particularly preferred compounds of the formula 2 are:
- auxin transport inhibitors diflufenzopyr, diflufenzopyrsodium, naptalam and naptalam sodium;
- MSMA oleic acid, oxaziclomefon, pelargonic acid, pyributicarb, quinoclamin, triaziflam, tridiphan and 6-chloro-3- (2-cyclopropyl-6-methylphenoxy) -4-pyridazinol (B-10; CAS 499223-49-3 ) and its salts and esters.
- Examples of preferred safeners C are Benoxacor, Cloquintocet, Cyometrinil, Cyprusulfamide, Dichlormid, Dicyclonon, Dietholate, Fenchlorazole, Fenclorim, Flurazole, Fluxofenim, Furilazole, Isoxadifen, Mefenpyr, Mephenate, Naphthalic Anhydride, Oxabetrinile, 4- (Dichloroacetyl ) -1-oxa-4-azaspiro [4.5] decane (B-1 1, MON4660, CAS 71526-07-3) and 2,2,5-trimethyl-3- (dichloroacetyl) -1,3-oxazolidine (B -12; R-29148, CAS 52836-31-4).
- the active compounds of groups b1) to b15) and the safeners C are known herbicides and safeners, see, for example, US Pat. B. The Compendium of Pesticide Common Names
- herbicidal active compounds are known from WO 96/26202, WO 97/411 16, WO 97/41 117, WO 97/411 18, WO 01 / 83459 and WO
- the compounds I and the compositions according to the invention may also have a plant-strengthening effect. They are therefore suitable for mobilizing plant-own defenses against infestation by undesirable microorganisms, such as harmful fungi, but also viruses and bacteria.
- plant-strengthening (resistance-inducing) substances are to be understood as meaning substances which are capable of stimulating the defense system of treated plants in such a way that they develop extensive resistance to these microorganisms during subsequent inoculation with undesired microorganisms.
- the compounds I can be used to protect plants against attack by undesired microorganisms within a certain period of time after the treatment.
- the period within which protection is provided generally extends from 1 to 28 days, preferably 1 to 14 days after treatment of the plants with the compounds I or after treatment of the seed, up to 9 months after sowing.
- the compounds I and the compositions according to the invention are also suitable for increasing crop yield.
- HPLC-MS High Performance Liquid Chromatography combined with mass spectrometry
- the culture vessels used were plastic pots with loamy sand with about 3.0% humus as substrate.
- the seeds of the test plants were sown separately by species.
- the active ingredients suspended or emulsified in water were applied directly after sowing by means of finely distributing nozzles.
- the jars were lightly rained to promote germination and growth and then covered with clear plastic hoods until the plants had grown. This cover causes a uniform germination of the test plants, if it was not affected by the active ingredients.
- test plants were grown depending on the growth form only to a height of from 3 to 15 cm and then treated with the suspended or emulsified in water agents.
- the test plants were either sown directly and grown in the same containers or they were first grown separately as seedlings and transplanted into the test containers a few days before the treatment.
- the plants were kept species-specific at temperatures of 10 - 25 ° C and 20 - 35 ° C, respectively.
- the trial period lasted for 2 to 4 weeks. During this time, the plants were cared for, and their response to each treatment was evaluated.
- the plants used in the greenhouse experiments are composed of the following species:
- the scale was rated from 0 to 100. 100 means no plants rising or completely destroying at least the above-ground parts and 0 means no damage or normal growth. A good herbicidal activity is at values of at least 70 and a very good herbicidal activity is given at values of at least 85.
- the active ingredient 1-105 showed at a rate of 0.125 kg / ha in the wake of ALOMY a good and the active ingredients I-94, I-99, 1-1 14, 1-1 19, 1-120, resp I-
- the active ingredient 1-100 showed at a rate of 0.25 kg / ha postemergence against ALOMY a good and the active ingredients I-87, I-88, I-89, 1-101, 1-102, 1-174 , I-224, I-226, I-227, and I-228 a very good herbicidal activity.
- the active compounds 1-1 18, or 1-154 showed at a rate of 0, 125 kg / ha post-emergence against POLCO a good and the active ingredients I-32, I-76, I-94, I-96, 1-105, 1-106, 1-107, 1-108, 1-109, 1-112, 1-113, 1-119, 1-120, 1-122, 1-124, 1-144, 1- 150, I-151, 1-152, 1-153, 1-155, 1-156, 1-159, 1-171, and 1-192, respectively, has a very good herbicidal activity.
- the active ingredients I-87, I-95, 1-130, 1-215, and 1-216 showed at a rate of 0.25 kg / ha post-emergence against POLCO a good and the active ingredients I-79, I -88, 1-102, 1-126, 1-143, 1-164, 1-165, 1-166, 1-167, 1-168, 1-169, 1-170, 1-172, 1-173 , I-174, 1-175, 1-178, 1-179, 1-180, 1-181, 1-196, I-205, I-206, I-207, I-208, I-209, 1 -210, I-211, 1-212, 1-213, 1-214, 1-217, 1-218, 1-219, 1-220, and 1-221 a very good herbicidal activity.
Abstract
Substituierte Cyanobutyrate der Formel (I), worin die Variablen gemäss der Beschreibung definiert sind, Verfahren und Zwischenprodukte zur Herstellung der Verbindungen der Formel (I) und deren N-Oxide, deren landwirtschaftlich brauchbaren Salze, sie enthaltende Mittel und deren Verwendung als Herbizide, sowie Verfahren zur Bekämpfung von unerwünschtem Pflanzenwuchs.
Description
Substituierte Cyanobutyrate mit herbizider Wirkung
Beschreibung
Die vorliegende Erfindung betrifft substituierte Cyanobutyrate der Formel I
worin die Variablen folgende Bedeutung haben:
R Halogen, Cyano, Nitro, Ci -C4-Al kyl, Ci-C4-Haloalkyl, C2-C6-Alkenyl, C2-C6-Al kinyl,
Z-(Tri-Ci-C4-alkyl)silyl,
R1 Wasserstoff, Z-CN, d-Cβ-Alkyl, Z-C3-C6-Cycloalkyl, d-Cβ-Haloalkyl, C3-C8-Al- kenyl, Z-C3-C6-Cycloalkenyl, C3-C8-Al kinyl, Z-(Tri-Ci-C4-alkyl)silyl, Z-C(=O)-Ra, Z-P(=O)(Ra)2, Z-Phenyl, über C oder N gebundener 3- bis 7-gliedriger mono- cyclischer oder 9- oder 10-gliedriger bicyclischer gesättigter, ungesättigter oder aromatischer Heterocyclus, enthaltend 1 , 2, 3 oder 4 Heteroatome ausgewählt aus O, N und S, der teilweise oder vollständig durch Gruppen Ra und/oder Rb substituiert sein kann,
Ra Wasserstoff, OH, Ci-C8-Al kyl, Ci-C4-Haloalkyl, Z-C3-C6-Cycloalkyl, C2-C8- Alkenyl, Z-C5-C6-Cycloalkenyl, C2-C8-Al kinyl, Z-Ci-C6-Alkoxy, Z-CrC4- Haloalkoxy, Z-C3-C8-Alkenyloxy, Z-C3-C8-Alkinyloxy, NR1R", Ci-C6-Alkyl- sulfonyl, Z-(Tri-Ci-C4-alkyl)silyl, Z-Phenyl, Z-Phenoxy, Z-Phenylamino und
5- oder 6-gliedriger monocyclischer oder 9- oder 10-gliedriger bicyclischer Heterocyclus, enthaltend 1 , 2, 3 oder 4 Heteroatome ausgewählt aus O, N und S, wobei die cyclischen Gruppen unsubstituiert oder durch 1 , 2, 3 oder 4 Gruppen Rb substituiert sind, bedeutet;
R1, R" unabhängig voneinander Wasserstoff, Ci-C8-Alkyl, Ci-C4-Haloalkyl,
C3-C8-Alkenyl, C3-C8-Al kinyl, Z-C3-C6-Cycloalkyl, Z-Ci-C8-Alkoxy, Z-Ci-C8-Haloalkoxy, Z-C(=O)-RA, wobei RA OH oder Ci-C4-Alkoxy bedeutet;
R1 und R" können auch gemeinsam mit dem N-Atom, an das sie gebun- den sind, einen 5- oder 6-gliedrigen monocyclischen oder 9- oder 10- gliedrigen bicyclischer Heterocyclus bilden, enthaltend 1 , 2, 3 oder 4 Heteroatome ausgewählt aus O, N und S;
Rb unabhängig voneinander Z-CN, Z-OH, Z-NO2, Z-Halogen, Ci-C8-
Alkyl, Ci-C4-Haloalkyl, C2-C8-Al kenyl, C2-C8-Al kinyl, Z-Ci-C8-Alkoxy, Z-Ci-C8-Haloalkoxy, Z-C3-Cio-Cycloalkyl, 0-Z-C3-Cio-Cycloalkyl,
Z-C(=O)-Ra, NR1R", Z-(Tri-Ci-C4-alkyl)silyl, Z-Phenyl und S(O)mRbb, wobei
Rbb Ci-C8-Alkyl und Ci-C6-Haloalkyl bedeutet;
m 0, 1 oder 2;
Rb kann auch gemeinsam mit der an das benachbarte C-Atom gebundene Gruppe Rb einen fünf- oder sechsgliedrigen gesättigten, teilweise oder vollständig ungesättigten Ring bilden, der neben Kohlenstoff- 1 , 2 oder 3 Heteroatome ausgewählt aus O, N und S enthalten kann;
Z eine kovalente Bindung oder Ci-Cs-Alkylen;
n 0, 1 , 2, 3, 4 oder 5;
R2, R3 unabhängig voneinander Halogen, Cyano, Nitro, Ci-C4-Alkyl, CrC4-AIkOXy,
S(O)mRbb, NR1R", Ci-C4-Halogenalkyl, Ci-C4-Halogenalkoxy;
R2 und R3 können auch gemeinsam einen fünf- oder sechsgliedrigen gesättigten, teilweise oder vollständig ungesättigten mono- oder bicyclischen Ring bilden, der ne- ben Kohlenstoff- 1 , 2 oder 3 Heteroatome ausgewählt aus O, N und S enthalten kann und durch Gruppen Rb substituiert sein kann;
wobei in Gruppen R und R1 und deren Untersubstituenten die Kohlenstoffketten und/oder die cyclischen Gruppen teilweise oder vollständig durch Gruppen Ra und/oder Rb substituiert sein können,
mit der Maßgabe, dass nicht beide R2 und R3 Chlor bedeuten, wenn R Wasserstoff und R1 Ethyl oder AIIyI bedeutet;
sowie deren N-Oxide und landwirtschaftlich geeignete Salze.
Außerdem betrifft die Erfindung Verfahren und Zwischenprodukte zur Herstellung der Verbindungen der Formel I und deren N-Oxide, deren landwirtschaftlich brauchbaren Salze, sie enthaltende Mittel und deren Verwendung als Herbizide, d.h. zur Bekämpfung von Schadpflanzen, sowie ein Verfahren zur Bekämpfung von unerwünschtem Pflanzenwuchs, bei dem man eine herbizid wirksame Menge mindestens einer Verbindung der Formel I oder eines landwirtschaftlich brauchbaren Salzes davon auf Pflanzen, deren Samen und/oder deren Lebensraum einwirken läßt.
Weitere Ausführungsformen der vorliegenden Erfindung sind den Ansprüchen, der Beschreibung und den Beispielen zu entnehmen. Es versteht sich, dass die vorstehend genannten und die nachstehend noch zu erläuternden Merkmale des erfindungsgemäßen Gegenstandes nicht nur in der jeweils angegebenen Kombination, sondern auch in anderen Kombinationen verwendbar sind, ohne den Rahmen der Erfindung zu verlassen.
Aus EP-A 5 341 , EP-A 266 725, EP-A 270 830, JP 04/297 454, JP 04/297 455 und JP 05/058 979 sind herbizide Cyanobutyrate bekannt, ihre herbizide Wirkung, insbe- sondere bei niedrigen Aufwandmengen, bzw. ihre Verträglichkeit gegenüber Kulturpflanzen bleibt jedoch verbesserungsbedürftig.
Eine Aufgabe der vorliegenden Erfindung ist die Bereitstellung von Verbindungen mit herbizider Wirkung. Insbesondere sollen Wirkstoffe zur Verfügung gestellt werden, die eine hohe herbizide Wirkung, insbesondere bereits bei niedrigen Aufwandmengen, aufweisen und deren Verträglichkeit gegenüber Kulturpflanzen für eine kommerzielle Verwertung hinreichend ist.
Diese und weitere Aufgaben werden durch die eingangs definierten Verbindungen der Formel I und durch ihre N-Oxide, sowie deren landwirtschaftlich geeigneten Salze gelöst.
Die erfindungsgemäßen Verbindungen können analog der in den zitierten Schriften beschriebenen Syntheserouten nach Standardverfahren der organischen Chemie hergestellt werden, beispielsweise nach der folgenden Syntheseroute:
Phenylacetonitrilderivate der Formel Il können mit Cinnamatderivaten der Formel III im Sinne einer Michael-Addition zu Verbindungen der Formel I umgesetzt werden. In Formeln Il und III haben die Variablen die für Formel I angegebene Bedeutung.
Diese Umsetzung erfolgt üblicherweise bei Temperaturen von -1000C bis 1500C, vorzugsweise -78°C bis 500C, in einem Lösungsmittel in Gegenwart einer Base und/oder eines Katalysators [vgl. J. Chem. Soc. (1945), S. 438].
Geeignete Lösungsmittel sind aliphatische Kohlenwasserstoffe wie Pentan, Hexan, Cyclohexan und Petrolether, aromatische Kohlenwasserstoffe wie Toluol, o-, m- und p- XyIoI, halogenierte Kohlenwasserstoffe wie Methylenchlorid, Chloroform und Chlorbenzol, Ether wie Diethylether, Diisopropylether, tert.-Butylmethylether, Dioxan, Anisol und Tetrahydrofuran (THF), Nitrile wie Acetonitril und Propionitril, Ketone wie Aceton, Me- thylethylketon, Diethylketon und tert.-Butylmethylketon, Alkohole wie Methanol, Etha- nol, n-Propanol, Isopropanol, n-Butanol und tert.-Butanol, sowie Dimethylsulfoxid, Di- methylformamid und Dimethylacetamid und Wassser, besonders bevorzugt THF und Methanol. Es können auch Gemische der genannten Lösungsmittel verwendet werden.
Als Basen kommen allgemein anorganische Verbindungen wie Alkalimetall- und Erdalkalimetallhydroxide wie Lithiumhydroxid, Natriumhydroxid, Kaliumhydroxid und CaI- ziumhydroxid, Alkalimetall- und Erdalkalimetalloxide wie Lithiumoxid, Natriumoxid, CaI- ziumoxid und Magnesiumoxid, Alkalimetall- und Erdalkalimetallhydride wie Lithiumhydrid, Natriumhydrid, Kaliumhydrid und Calziumhydrid, Alkalimetallamide wie Lithium- amid, Natriumamid und Kaliumamid, Alkalimetall- und Erdalkalimetallcarbonate wie Lithiumcarbonat, Kaliumcarbonat und Calziumcarbonat sowie Alkalimetallhydrogen- carbonate wie Natriumhydrogencarbonat, metallorganische Verbindungen, insbeson-
dere Alkalimetallalkyle wie Methyllithium, Butyllithium und Phenyllithium, Alkylmagne- siumhalogenide wie Methylmagnesiumchlorid sowie Alkalimetall- und Erdalkalimetallal- koholate wie Natriummethanolat, Natriumethanolat, Kaliumethanolat, Kalium- tert- Butanolat und Dimethoxymagnesium, außerdem organische Basen, z.B. tertiäre Amine wie Trimethylamin, Triethylamin, Tributylamin, Di-isopropylethylamin und N-Methyl- piperidin, Pyridin, substituierte Pyridine wie Collidin, Lutidin und 4-Dimethylamino- pyridin sowie bicyclische Amine in Betracht. Besonders bevorzugt werden Kalium-tert- Butanolat, Lithium bis(trimethylsilyl)amid und 7-Methyl-1 ,5,7-triazabicyclo[4.4.0]- dec-5- en.
Die Basen werden im Allgemeinen in katalytischen Mengen eingesetzt, sie können aber auch äquimolar, im Überschuß oder gegebenenfalls als Lösungsmittel verwendet werden.
Als saure Katalysatoren finden anorganische Säuren wie Fluorwasserstoffsäure, Salzsäure, Bromwasserstoffsäure, Schwefelsäure und Perchlorsäure, Lewis-Säuren wie Bortrifluorid, Aluminiumtrichlorid, Eisen-lll-chlorid, Zinn-IV-chlorid, Titan-IV-chlorid, Scandium-lll-triflat und Zink-ll-chlorid, sowie organische Säuren wie Ameisensäure, Essigsäure, Propionsäure, Oxalsäure, Toluolsulfonsäure, Benzolsulfonsäure,
Camphersulfonsäure, Zitronensäure und Trifluoressigsäure Verwendung.
Die Säuren werden im Allgemeinen in katalytischen Mengen eingesetzt, sie können aber auch äquimolar, im Überschuß oder gegebenenfalls als Lösungsmittel verwendet werden.
Alternativ können die Verbindungen der Formel I auch erhalten werden durch U- mesterung anderer Cyanobutyrate erhalten werden. Das kann nach verschiedenen Methoden erfolgen, beispielsweise nach den im Folgenden Beschriebenen:
Die Umesterung kann in Anwesenheit von Molsieb in einem Alkohol R1-OH, optional in einem aprotischen Lösungsmittel, durchgeführt werden. Diese Umsetzung erfolgt üblicherweise bei Temperaturen von 00C bis180°C, vorzugsweise 200C bis 800C in Gegenwart von einer Lewis- bzw. Branstedtsäure oder eines Enzyms [vgl. J. Org. Chem. 2002, 67, 431].
Geeignete Lösungsmittel sind aliphatische Kohlenwasserstoffe wie Pentan, Hexan, Cyclohexan und Petrolether, aromatische Kohlenwasserstoffe wie Toluol, o-, m- und p- XyIoI, halogenierte Kohlenwasserstoffe wie Methylenchlorid, Chloroform und Chlorben- zol, Ether wie Diethylether, Diisopropylether, tert.-Butylmethylether, Dioxan, Anisol und THF, Nitrile wie Acetonitril und Propionitril, Ketone, sowie Dimethylsulfoxid, Dimethyl- formamid und Dimethylacetamid, besonders bevorzugt Alkohol R1-OH. Es können auch Gemische der genannten Lösungsmittel verwendet werden. Alternativ kann die Umesterung durch saures oder basisches Verseifen anderer Cyanobutyrate (a), gefolgt von einer Umsetzung mit einem Alkohol R1-OH erfolgen. Diese Umsetzungen erfolgen üblicherweise bei Temperaturen von O0C bis 12O0C, Vorzugs-
weise 2O0C bis 5O0C in Gegenwart einer Base, bzw. einer Säure und/oder eines Katalysators [vgl. J. Am. Chem. Soc. 2007, 129 (43), 13321 ; J. Org. Chem. 1984, 49 (22), 4287.]. Geeignete Lösungsmittel sind aliphatische Kohlenwasserstoffe wie Pentan, Hexan, Cyclohexan und Petrolether, aromatische Kohlenwasserstoffe wie Toluol, o-, m- und p- XyIoI, halogenierte Kohlenwasserstoffe wie Methylenchlorid, Chloroform und Chlorbenzol, Ether wie Diethylether, Diisopropylether, tert.-Butylmethylether, Dioxan, Anisol und THF, Nitrile wie Acetonitril und Propionitril, Ketone wie Aceton, Methylethylketon, Diethylketon und tert.-Butylmethylketon, Alkohole wie Methanol, Ethanol, n-Propanol, Isopropanol, n-Butanol und tert.-Butanol, sowie Dimethylsulfoxid, Dimethylformamid und Dimethylacetamid und Wasser, besonders bevorzugt (a) Wasser, THF; (b) R1-OH. Es können auch Gemische der genannten Lösungsmittel verwendet werden.
Als Basen kommen allgemein anorganische Verbindungen wie Alkalimetall- und Er- dalkalimetallhydroxide wie Lithiumhydroxid, Natriumhydroxid, Kaliumhydroxid und CaI- ziumhydroxid, Alkalimetall- und Erdalkalimetalloxide wie Lithiumoxid, Natriumoxid, CaI- ziumoxid und Magnesiumoxid, Alkalimetall- und Erdalkalimetallhydride wie Lithiumhydrid, Natriumhydrid, Kaliumhydrid und Calziumhydrid, Alkalimetallamide wie Lithium- amid, Natriumamid und Kaliumamid, Alkalimetall- und Erdalkalimetallcarbonate wie Lithiumcarbonat, Kaliumcarbonat und Calziumcarbonat sowie Alkalimetallhydrogen- carbonate wie Natriumhydrogencarbonat, metallorganische Verbindungen, insbesondere Alkalimetallalkyle wie Methyllithium, Butyllithium und Phenyllithium, Alkylmagne- siumhalogenide wie Methylmagnesiumchlorid sowie Alkalimetall- und Erdalkalimetallal- koholate wie Natriummethanolat, Natriumethanolat, Kaliumethanolat, Kalium- tert.- Butanolat und Dimethoxymagnesium, außerdem organische Basen, z.B. tertiäre Amine wie Trimethylamin, Triethylamin, Tributylamin, Di-isopropylethylamin und N-Methyl- piperidin, Pyridin, substituierte Pyridine wie Collidin, Lutidin und 4-Dimethylamino- pyridin sowie bicyclische Amine in Betracht. Besonders bevorzugt wird Lithiumhydroxid Die Basen werden im Allgemeinen in katalytischen Mengen eingesetzt, sie können aber auch äquimolar, im Überschuß oder gegebenenfalls als Lösungsmittel verwendet werden.
Als Säuren und saure Katalysatoren finden anorganische Säuren wie Fluorwasserstoffsäure, Salzsäure, Bromwasserstoffsäure, Schwefelsäure und Perchlorsäure, Lewis-Säuren wie Bortrifluorid, Aluminiumtrichlorid, Eisen-lll-chlorid, Zinn-IV-chlorid, Titan-IV-chlorid und Zink-ll-chlorid, sowie organische Säuren wie Ameisensäure, Essigsäure, Propionsäure, Oxalsäure, Toluolsulfonsäure, Benzolsulfonsäure, Campher- sulfonsäure, Zitronensäure und Trifluoressigsäure Verwendung.
Die Säuren werden im Allgemeinen in katalytischen Mengen eingesetzt, sie können aber auch äquimolar, im Überschuß oder gegebenenfalls als Lösungsmittel verwendet werden.
Die für die Herstellung der Verbindungen I benötigten Ausgangsstoffe sind in der Literatur bekannt oder können gemäß der zitierten Literatur hergestellt werden.
Die Reaktionsgemische werden in üblicher weise aufgearbeitet, z.B. durch Mischen mit Wasser, Trennung der Phasen und gegebenenfalls chromatographische Reinigung der Rohprodukte. Die Zwischen- und Endprodukte fallen z.T. in Form farbloser oder schwach bräunlicher, zäher Öle an, die unter vermindertem Druck und bei mäßig erhöhter Temperatur von flüchtigen Anteilen befreit oder gereinigt werden. Sofern die Zwischen- und Endprodukte als Feststoffe erhalten werden, kann die Reinigung auch durch Umkristallisieren oder Digerieren erfolgen.
Sofern einzelne Verbindungen I nicht auf den voranstehend beschriebenen Wegen zugänglich sind, können sie durch Derivatisierung anderer Verbindungen I hergestellt werden.
Sofern bei der Synthese Isomerengemische anfallen, ist im Allgemeinen jedoch eine Trennung nicht unbedingt erforderlich, da sich die einzelnen Isomere teilweise während der Aufbereitung für die Anwendung oder bei der Anwendung (z.B. unter Licht-, Säureoder Baseneinwirkung) ineinander umwandeln können. Entsprechende Umwandlungen können auch nach der Anwendung, beispielsweise bei der Behandlung von Pflanzen in der behandelten Pflanze oder in der zu bekämpfenden Schadpflanze erfolgen. Die für die Substituenten der erfindungsgemäßen Verbindungen genannten organischen Molekülteile stellen Sammelbegriffe für individuelle Aufzählungen der einzelnen Gruppenmitglieder dar. Sämtliche Kohlenwasserstoffketten, wie Alkyl, Halo(gen)alkyl, Alkenyl, Alkinyl, sowie die Alkylteile und Alkenylteile in Alkoxy, Halo(gen)alkoxy, Alkyl- amino, Dialkylamino, N-Alkylsulfonylamino, Alkenyloxy, Alkinyloxy, Alkoxyamino, Alkyl- aminosulfonylamino, Dialkylaminosulfonylamino, Alkenylamino, Alkinylamino, N-(Alke- nyl)-N-(alkyl)-amino, N-(Alkinyl)-N-(alkyl)-amino, N-(Alkoxy)-N-(alkyl)-amino, N-(Alke- nyl)-N-(alkoxy)-amino oder N-(Alkinyl)-N-(alkoxy)-amino können geradkettig oder verzweigt sein.
Das Präfix Cn-Cm- gibt die jeweilige Kohlenstoffzahl der Kohlenwasserstoffeinheit an. Sofern nicht anders angegeben tragen halogenierte Substituenten vorzugsweise ein bis fünf gleiche oder verschiedene Halogenatome, insbesondere Fluoratome oder Chloratome.
Die Bedeutung Halogen steht jeweils für Fluor, Chlor, Brom oder lod.
Ferner bedeuten beispielsweise:
Alkyl sowie die Alkylteile beispielsweise in Alkoxy, Alkylamino, Dialkylamino, N-Alkylsulfonylamino, Alkylaminosulfonylamino, Dialkylaminosulfonylamino, N-(Alkenyl)-N- (alkyl)-amino, N-(Alkinyl)-N-(alkyl)-amino, N-(Alkoxy)-N-(alkyl)-amino: gesättigte, ge- radkettige oder verzweigte Kohlenwasserstoffreste mit einem oder mehr C-Atomen, z.B. 1 bis 2, 1 bis 4, oder 1 bis 6 Kohlenstoffatomen, z.B. Ci-C6-Alkyl wie Methyl, Ethyl, Propyl, 1-Methylethyl, Butyl, 1-Methylpropyl, 2-Methylpropyl, 1 ,1-Dimethylethyl, Pentyl, 1-Methylbutyl, 2-Methylbutyl, 3-Methylbutyl, 2,2-Dimethylpropyl, 1-Ethylpropyl, Hexyl, 1 ,1-Dimethylpropyl, 1 ,2-Dimethylpropyl, 1-Methylpentyl, 2-Methylpentyl, 3-Methylpen-
tyl, 4-Methylpentyl, 1 ,1-Dimethylbutyl, 1 ,2-Dimethylbutyl, 1 ,3-Dimethylbutyl, 2,2-Di- methylbutyl, 2,3-Dimethylbutyl, 3,3-Dimethylbutyl, 1-Ethylbutyl, 2-Ethylbutyl, 1 ,1 ,2-Tri- methylpropyl, 1 ,2,2-Trimethylpropyl, 1-Ethyl-1-methylpropyl, 1-Ethyl-2-methylpropyl. In einer erfindungsgemäßen Ausführungsform steht Alkyl für kleine Alkylgruppen wie d- C4-Al kyl. In einer anderen erfindungsgemäßen Ausführungsform steht Alkyl für größere Alkylgruppen wie Cs-Cβ-Alkyl.
Halogenalkyl (auch als Haloalkyl bezeichnet): einen Alkylrest wie vorstehend genannt, dessen Wasserstoffatome partiell oder vollständig durch Halogenatome wie Fluor, Chlor, Brom und/oder lod substituiert sind, z.B. Chlormethyl, Dichlormethyl, Tri- chlormethyl, Fluormethyl, Difluormethyl, Trifluormethyl, Chlorfluormethyl, Dichlorfluor- methyl, Chlordifluormethyl, 2-Fluorethyl, 2-Chlorethyl, 2-Bromethyl, 2-lodethyl, 2,2-Di- fluorethyl, 2,2,2-Trifluorethyl, 2-Chlor-2-fluorethyl, 2-Chlor-2,2-difluorethyl, 2,2-Dichlor- 2-fluorethyl, 2,2,2-Trichlorethyl, Pentafluorethyl, 2-Fluorpropyl, 3-Fluorpropyl, 2,2-Di- fluorpropyl, 2,3-Difluorpropyl, 2-Chlorpropyl, 3-Chlorpropyl, 2,3-Dichlorpropyl, 2-Brom- propyl, 3-Brompropyl, 3,3,3-Trifluorpropyl, 3,3,3-Trichlorpropyl, 2,2,3,3,3-Pentafluor- propyl, Heptafluorpropyl, 1-(Fluormethyl)-2-fluorethyl, 1-(Chlormethyl)-2-chlorethyl, 1- (Brommethyl)-2-bromethyl, 4-Fluorbutyl, 4-Chlorbutyl, 4-Brombutyl und Nonafluorbutyl.
Cycloalkyl sowie die Cycloalkylteile beispielsweise in Cycloalkoxy oder Cycloalkyl- carbonyl: monocyclische, gesättigte Kohlenwasserstoffgruppen mit drei oder mehr C- Atomen, z.B. 3 bis 6 Kohlenstoffringgliedern, wie Cyclopropyl, Cyclobutyl, Cyclopentyl und Cyclohexyl.
Alkenyl sowie Alkenylteile beispielsweise in Alkenylamino, Alkenyloxy, N-(Alkenyl)- N-(alkyl)-amino, N-(Alkenyl)-N-(alkoxy)-amino: einfach ungesättigte, geradkettige oder verzweigte Kohlenwasserstoffreste mit zwei oder mehr C-Atomen, z. B. 2 bis 4, 2 bis 6 oder 3 bis 6 Kohlenstoffatomen und einer Doppelbindung in einer beliebigen Position, z.B. C2-C6-Alkenyl wie Ethenyl, 1-Propenyl, 2-Propenyl, 1-Methylethenyl, 1-Butenyl, 2-Butenyl, 3-Butenyl, 1-Methyl-1-propenyl, 2-Methyl-1-propenyl, 1-Methyl-2-propenyl, 2-Methyl-2-propenyl, 1-Pentenyl, 2-Pentenyl, 3-Pentenyl, 4-Pentenyl, 1-Methyl-1-but- enyl, 2-Methyl-1-butenyl, 3-Methyl-1-butenyl, 1-Methyl-2-butenyl, 2-Methyl-2-butenyl, 3-Methyl-2-butenyl, 1-Methyl-3-butenyl, 2-Methyl-3-butenyl, 3-Methyl-3-butenyl, 1 ,1-Di- methyl-2-propenyl, 1 ,2-Dimethyl-1-propenyl, 1 ,2-Dimethyl-2-propenyl, 1-Ethyl-1-prop- enyl, 1-Ethyl-2-propenyl, 1-Hexenyl, 2-Hexenyl, 3-Hexenyl, 4-Hexenyl, 5-Hexenyl, 1-Methyl-1-pentenyl, 2-Methyl-1-pentenyl, 3-Methyl-1-pentenyl, 4-Methyl-1-pentenyl, 1-Methyl-2-pentenyl, 2-Methyl-2-pentenyl, 3-Methyl-2-pentenyl, 4-Methyl-2-pentenyl, 1-Methyl-3-pentenyl, 2-Methyl-3-pentenyl, 3-Methyl-3-pentenyl, 4-Methyl-3-pentenyl, 1-Methyl-4-pentenyl, 2-Methyl-4-pentenyl, 3-Methyl-4-pentenyl, 4-Methyl-4-pentenyl, 1 ,1-Dimethyl-2-butenyl, 1 ,1-Dimethyl-3-butenyl, 1 ,2-Dimethyl-1-butenyl, 1 ,2-Dimethyl- 2-butenyl, 1 ,2-Dimethyl-3-butenyl, 1 ,3-Dimethyl-1-butenyl, 1 ,3-Dimethyl-2-butenyl, 1 ,3-Dimethyl-3-butenyl, 2,2-Dimethyl-3-butenyl, 2,3-Dimethyl-1-butenyl, 2,3-Dimethyl- 2-butenyl, 2,3-Dimethyl-3-butenyl, 3,3-Dimethyl-1-butenyl, 3,3-Dimethyl-2-butenyl,
1-Ethyl-1-butenyl, 1-Ethyl-2-butenyl, 1-Ethyl-3-butenyl, 2-Ethyl-1-butenyl, 2-Ethyl-2-but-
enyl, 2-Ethyl-3-butenyl, 1 ,1 ,2-Trimethyl-2-propenyl, 1-Ethyl-1-methyl-2-propenyl, 1 -Ethyl-2-methyl-1 -propenyl, 1 -Ethyl-2-methyl-2-propenyl.
Cycloalkenyl: monocyclische, einfach ungesättigte Kohlenwasserstoffgruppen mit 3 bis 6, vorzugsweise 5 bis 6 Kohlenstoffringgliedern, wie Cyclopenten-1-yl, Cyclopen- ten-3-yl, Cyclohexen-1-yl, Cyclohexen-3-yl, Cyclohexen-4-yl.
Alkinyl sowie Alkinylteile beispielsweise in Alkinyloxy, Alkinylamino, N-(Alkinyl)-N-(al- kyl)-amino oder N-(Alkinyl)-N-(alkoxy)-amino: geradkettige oder verzweigte Kohlenwasserstoffgruppen mit zwei oder mehr C-Atomen, z. B. 2 bis 4, 2 bis 6, oder 3 bis 6 Kohlenstoffatomen und einer Dreifachbindung in beliebiger Position, z. B. C2-C6-Alkinyl wie Ethinyl, 1-Propinyl, 2-Propinyl, 1-Butinyl, 2-Butinyl, 3-Butinyl, 1-Methyl-2-propinyl, 1-Pentinyl, 2-Pentinyl, 3-Pentinyl, 4-Pentinyl, 1-Methyl-2-butinyl, 1 -Methyl-3-butinyl, 2-Methyl-3-butinyl, 3-Methyl-1 -butinyl, 1 ,1-Dimethyl-2-propinyl, 1 -Ethyl-2-propinyl, 1-Hexinyl, 2-Hexinyl, 3-Hexinyl, 4-Hexinyl, 5-Hexinyl, 1-Methyl-2-pentinyl, 1 -Methyl-3- pentinyl, 1-Methyl-4-pentinyl, 2-Methyl-3-pentinyl, 2-Methyl-4-pentinyl, 3-Methyl-1-pen- tinyl, 3-Methyl-4-pentinyl, 4-Methyl-1-pentinyl, 4-Methyl-2-pentinyl, 1 ,1-Dimethyl-2-but- inyl, 1 ,1-Dimethyl-3-butinyl, 1 ,2-Dimethyl-3-butinyl, 2,2-Dimethyl-3-butinyl, 3,3-Dime- thyl-1 -butinyl, 1-Ethyl-2-butinyl, 1 -Ethyl-3-butinyl, 2-Ethyl-3-butinyl, 1-Ethyl-1-methyl-2- propinyl.
Alkoxy: Alkyl, wie vorstehend definiert, das über ein O-Atom gebunden ist: z. B. Me- thoxy, Ethoxy, n-Propoxy, 1 -Methylethoxy, Butoxy, 1-Methylpropoxy, 2-Methylpropoxy oder 1 ,1-Dimethylethoxy, Pentoxy, 1-Methylbutoxy, 2-Methylbutoxy, 3-Methylbutoxy, 1 ,1-Dimethylpropoxy, 1 ,2-Dimethylpropoxy, 2,2-Dimethylpropoxy, 1-Ethylpropoxy, Hex- oxy, 1-Methylpentoxy, 2-Methylpentoxy, 3-Methylpentoxy, 4-Methylpentoxy, 1 , 1 -Di- methylbutoxy, 1 ,2-Dimethylbutoxy, 1 ,3-Dimethylbutoxy, 2,2-Dimethylbutoxy, 2,3-Di- methylbutoxy, 3,3-Dimethylbutoxy, 1-Ethylbutoxy, 2-Ethylbutoxy, 1 ,1 ,2-Trimethylprop- oxy, 1 ,2,2-Trimethylpropoxy, 1-Ethyl-1-methylpropoxy oder 1-Ethyl-2-methylpropoxy.
5- oder 6-gliedriger Heterocyclus: eine cyclische Gruppe, die 5 oder 6 Ringatome aufweist wobei 1 , 2, 3 oder 4 Ringatome Heteroatome sind, die ausgewählt sind aus O, S und N, wobei die cyclische Gruppe gesättigt, partiell ungesättigt oder aromatisch ist.
Die Verbindungen der Formel I enthalten zwei Chiralitätszentren und können, je nach Substitutionsmuster, ein oder mehrere weitere enthalten. Die erfindungsgemäßen Verbindungen können daher als reine Enantiomere oder Diastereomere oder als Enan- tiomeren- oder Diastereomerengemische vorliegen. Gegenstand der Erfindung sind sowohl die reinen Enantiomeren oder Diastereomeren als auch deren Gemische.
Die Verbindungen der Formel I können auch in Form der N-Oxide und/oder ihrer landwirtschaftlich brauchbaren Salze vorliegen, wobei es auf die Art des Salzes in der Regel nicht ankommt. Im Allgemeinen kommen die Salze derjenigen Kationen oder die Säureadditionssalze derjenigen Säuren in Betracht, deren Kationen, beziehungsweise Anionen, die herbizide Wirkung der Verbindungen I nicht negativ beeinträchtigen.
Es kommen als Kationen insbesondere Ionen der Alkalimetalle, vorzugsweise Lithium, Natrium oder Kalium, der Erdalkalimetalle, vorzugsweise Calcium oder Magnesium, und der Übergangsmetalle, vorzugsweise Mangan, Kupfer, Zink oder Eisen in Be- tracht. Ebenso kann als Kation Ammonium verwendet werden, wobei hier gewünsch- tenfalls ein bis vier Wasserstoffatome durch Ci-C4-AIkVl, Hydroxy-Ci-C4-alkyl, C1-C4- Alkoxy-Ci-C4-alkyl, Hydroxy-Ci-C4-alkoxy-Ci-C4-alkyl, Phenyl oder Benzyl ersetzt sein können, vorzugsweise Ammonium, Dimethylammonium, Diisopropylammonium, Tetramethylammonium, Tetrabutylammonium, 2-(2-Hydroxyeth-1 -oxy)eth-1 -ylammonium, Di(2-hydroxyeth-1-yl)ammonium, Trimethylbenzylammonium. Als Ammoniumkation kommt auch das durch Alkylierung oder Arylierung quaternisierte Pyridin-Stickstoffatom der Formel I in Frage. Des Weiteren kommen Phosphoniumionen, Sulfoniumionen, vorzugsweise Tri(Ci-C4-alkyl)sulfonium oder Sulfoxoniumionen, vorzugsweise Tri(Ci- C4-alkyl)sulfoxonium, in Betracht.
Anionen von brauchbaren Säureadditionsalzen sind in erster Linie Chlorid, Bromid, Fluorid, Hydrogensulfat, Sulfat, Dihydrogenphosphat, Hydrogenphosphat, Nitrat, Hydrogencarbonat, Carbonat, Hexafluorosilikat, Hexafluorophosphat, Benzoat sowie die Anionen von Ci-C4-Alkansäuren, vorzugsweise Formiat, Acetat, Propionat, Butyrat oder Trifluoracetat.
Die besonders bevorzugten Ausführungsformen der Zwischenprodukte in Bezug auf die Variablen entsprechen denen der Gruppen der Formel I.
In einer besonderen Ausführungsform haben die Variablen der Verbindungen der Formel I folgende Bedeutungen, wobei diese sowohl für sich allein betrachtet als auch in Kombination miteinander besondere Ausgestaltungen der Verbindungen der Formel I darstellen:
In einer Ausführungsform der Verbindungen der Formel I steht der Index n für einen Wert von 0 bis 3, bevorzugt für 0 oder 1 , insbesondere für 1. In einer weiteren Ausfüh- rung steht er für 0. Sofern mindestens eine Gruppe R vorliegt, steht sie bevorzugt in den Positionen 3, 4 und/oder 5, insbesondere 3 oder 4. Sofern der Index n den Wert 2 hat, stehen die Gruppen R bevorzugt in Positionen 2,5 oder 3,4.
Ausführungen der Gruppe(n) R betreffen Halogen, insbesondere Chlor oder Fluor. Weitere Ausführungen der Gruppe(n) R betreffen Cyano oder Nitro, insbesondere Cyano.
Besonders bevorzugte Ausführungen der Gruppe Rn umfassen die folgenden:
3-F; 3,4-F2; 3,5-F2; 3,4,5-F3; 3-F.4-CI; 4-CI; 4-F; 3-CN.
Bevorzugte Ausführungen der Gruppe R1 betreffen Wasserstoff, Ci -Ce-Al kyl, Cyano- Ci-C4-Alkyl, C3-C6-Al kenyl, C3-C6-Alkinyl, Ci-C8-Haloalkyl, ggf. subst. Z-Phenyl oder NR'R"-C-ι-C4-alkyl, wobei R1 für Wasserstoff oder Ci-C4-Alkyl und R" für Wasserstoff, Ci-C4-Alkyl oder C(=O)-RA steht. Besonders bevorzugte Ausführungen der Gruppe R1 betreffen Wasserstoff, Ci-C4-Alkyl, Cyanomethyl, AIIyI, Propargyl, Ci-C4-Haloalkyl enthaltend bevorzugt 1 bis 3 Halogenatome, Phenyl oder Benzyl, welche aromatischen Gruppen teilweise oder vollständig substituiert sein können. Besonders bevorzugte Ausführungen für R1 umfassen die folgenden: H, CH3, C2H5, CH2CN, CH2C≡ CH, CH2CH2F, CH2CHF2, CH2CF3, CH2OCH3.
Bevorzugte Ausführungen der Gruppe R2 betreffen Halogen, Cyano, Nitro, CTC4- AI kyl, Ci-C4-Alkoxy, S(O)mRbb, NR1R", Ci-C4-Halogenalkyl, Ci-C4-Halogenalkoxy. Besonders bevorzugte Ausführungen der Gruppe R2 umfassen Halogen, CN, NO2, CH3, CHF2, CF3, OCHF2, OCF3. Insbesondere bevorzugte Ausführungen der Gruppe R2 sind ausgewählt aus Fluor, Chlor, Brom und Jod. Weiter besonders bevorzugt steht R2 nicht für Chlor.
Weiter besonders bevorzugt steht R2 für Fluor.
Weiter besonders bevorzugt steht R2 für Brom.
Weiter besonders bevorzugt steht R2 für Jod.
Bevorzugte Ausführungen der Gruppe R3 betreffen Halogen, Cyano, Nitro, Ci-C4- AI kyl, Ci-C4-Alkoxy, S(O)mRbb, NR1R", Ci-C4-Halogenalkyl, Ci-C4-Halogenalkoxy. Besonders bevorzugte Ausführungen der Gruppe R3 betreffen Halogen, CN, NO2, CH3, CHF2, CF3, OCHF2, OCF3. Insbesondere bevorzugte Ausführungen der Gruppe R3 sind ausgewählt aus Fluor, Chlor, Brom und Jod. Weiter besonders bevorzugt steht R3 nicht für Chlor.
Weiter besonders bevorzugt steht R3 für Fluor.
Weiter besonders bevorzugt steht R3 für Brom.
Weiter besonders bevorzugt steht R3 für Jod.
Insbesondere bevorzugt sind folgende Kombinationen von R2 und R3:
2,3-F2; 2-F.3-CI; 2-F,3-Br; 2-F,3-CN; 2-F,3-NO2; 2-F,3-CF3; 2-F,3-OCH3; 2-CI.3-F.
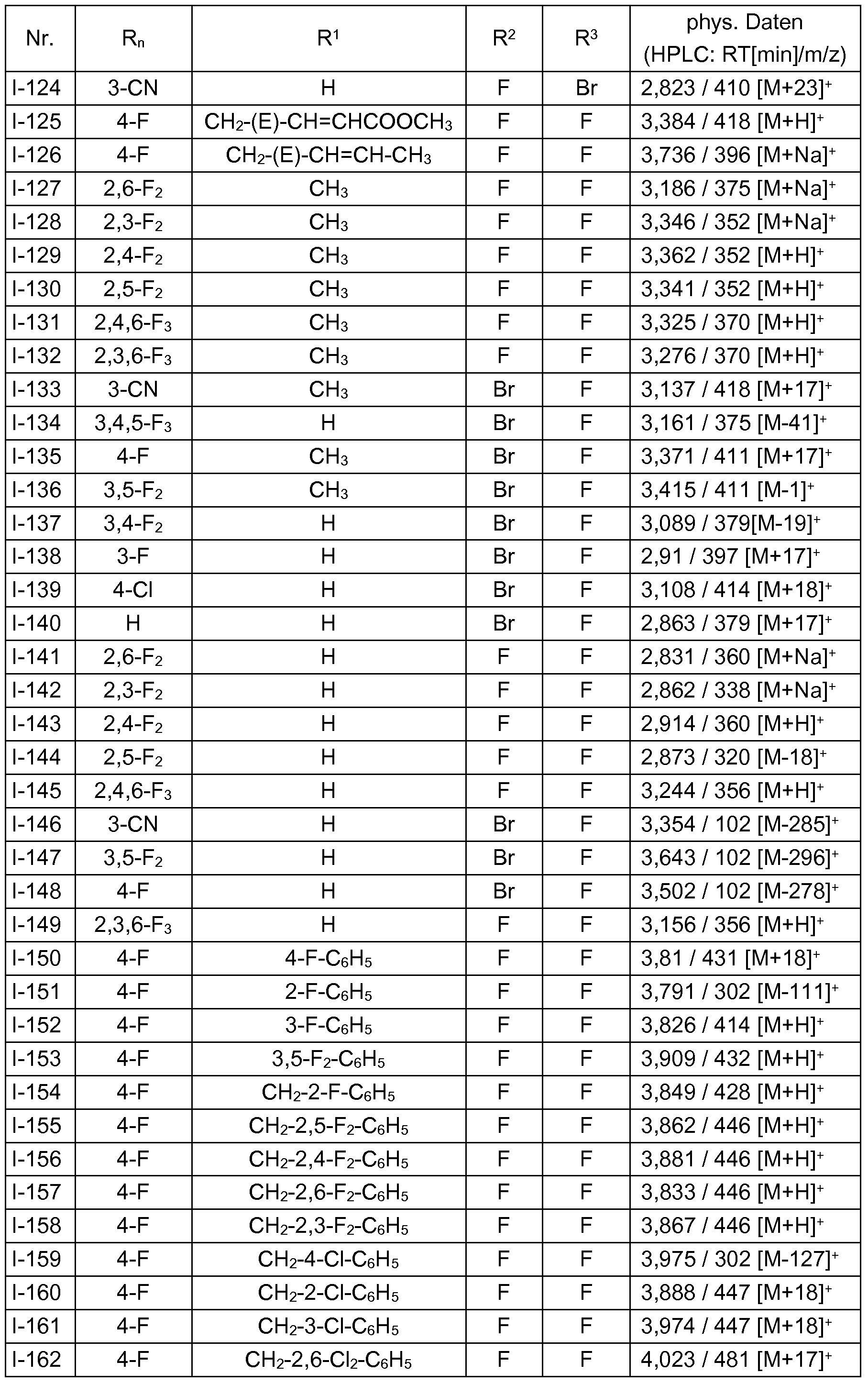
Insbesondere sind im Hinblick auf ihre Verwendung die in den folgenden Tabellen zusammengestellten Verbindungen der Formel I bevorzugt. Die in den Tabellen für einen Substituenten genannten Gruppen stellen außerdem für sich betrachtet, unab- hängig von der Kombination, in der sie genannt sind, eine besonders bevorzugte Ausgestaltung des betreffenden Substituenten dar.
Tabelle 1
Verbindungen der Formel I, in denen Rn 3-CN bedeutet und die Kombination von R1, R2 und R3 für eine Verbindung jeweils einer Zeile der Tabelle A entspricht
Tabelle 2
Verbindungen der Formel I, in denen Rn 4-CI bedeutet und die Kombination von R1, R2 und R3 für eine Verbindung jeweils einer Zeile der Tabelle A entspricht
Tabelle 3
Verbindungen der Formel I, in denen Rn 3-F bedeutet und die Kombination von R1, R2 und R3 für eine Verbindung jeweils einer Zeile der Tabelle A entspricht
Tabelle 4
Verbindungen der Formel I, in denen Rn 4-F bedeutet und die Kombination von R1, R2 und R3 für eine Verbindung jeweils einer Zeile der Tabelle A entspricht
Tabelle 5
Verbindungen der Formel I, in denen Rn 3,4-F2 bedeutet und die Kombination von R1, R2 und R3 für eine Verbindung jeweils einer Zeile der Tabelle A entspricht
Tabelle 6
Verbindungen der Formel I, in denen Rn 3,5-F2 bedeutet und die Kombination von R1, R2 und R3 für eine Verbindung jeweils einer Zeile der Tabelle A entspricht
Tabelle 7
Verbindungen der Formel I, in denen Rn 3-F,4-CI bedeutet und die Kombination von R1, R2 und R3 für eine Verbindung jeweils einer Zeile der Tabelle A entspricht
Tabelle 8
Verbindungen der Formel I, in denen Rn 3,4,5-F3 bedeutet und die Kombination von R1, R2 und R3 für eine Verbindung jeweils einer Zeile der Tabelle A entspricht
Tabelle A - Verbindungen der Formel I
Die Verbindungen I und deren landwirtschaftlich brauchbaren Salze eignen sich - sowohl als Isomerengemische als auch in Form der reinen Isomeren - als Herbizide. Sie eignen sich als solche oder als entsprechend formuliertes Mittel. Die herbiziden Mittel, die die Verbindung I, insbesondere die bevorzugten Ausgestaltungen davon, enthalten, bekämpfen Pflanzenwuchs auf Nichtkulturflächen sehr gut, besonders bei hohen Aufwandmengen. In Kulturen wie Weizen, Reis, Mais, Soja und Baumwolle wirken sie gegen Unkräuter und Schadgräser, ohne die Kulturpflanzen nennenswert zu schädigen. Dieser Effekt tritt vor allem bei niedrigen Aufwandmengen auf.
In Abhängigkeit von der jeweiligen Applikationsmethode können die Verbindungen I, insbesondere die bevorzugten Ausgestaltungen davon, bzw. sie enthaltende Mittel noch in einer weiteren Zahl von Kulturpflanzen zur Beseitigung unerwünschter Pflanzen eingesetzt werden. In Betracht kommen beispielsweise folgende Kulturen:
Allium cepa, Ananas comosus, Arachis hypogaea, Asparagus officinalis, Avena sati- va, Beta vulgaris spec. altissima, Beta vulgaris spec. rapa, Brassica napus var. napus, Brassica napus var. napobrassica, Brassica rapa var. silvestris, Brassica oleracea, Brassica nigra, Camellia sinensis, Carthamus tinctorius, Carya illinoinensis, Citrus Ii- mon, Citrus sinensis, Coffea arabica (Coffea canephora, Coffea liberica), Cucumis sa- tivus, Cynodon dactylon, Daucus carota, Elaeis guineensis, Fragaria vesca, Glycine max, Gossypium hirsutum, (Gossypium arboreum, Gossypium herbaceum, Gossypium vitifolium), Helianthus annuus, Hevea brasiliensis, Hordeum vulgäre, Humulus lupulus, Ipomoea batatas, Juglans regia, Lens culinaris, Linum usitatissimum, Lycopersicon lycopersicum, Malus spec, Manihot esculenta, Medicago sativa, Musa spec, Nicotiana tabacum (N.rustica), Olea europaea, Oryza sativa, Phaseolus lunatus, Phaseolus vulgaris, Picea abies, Pinus spec, Pistacia vera, Pisum sativum, Prunus avium, Prunus persica, Pyrus communis, Prunus armeniaca, Prunus cerasus, Prunus dulcis und prunus domestica, Ribes sylvestre, Ricinus communis, Saccharum officinarum, Seeale cereale, Sinapis alba, Solanum tuberosum, Sorghum bicolor (s. vulgäre), Theobroma cacao, Trifolium pratense, Triticum aestivum, Triticale, Triticum durum, Vicia faba, Vitis vinifera, Zea mays.
Der Begriff Kulturpflanzen schließt auch solche ein, die durch Züchtung, Mutagenese oder gentechnische Methoden verändert wurden. Gentechnisch veränderte Pflanzen sind Pflanzen, deren genetisches Material in einer Weise verändert worden ist, wie sie unter natürlichen Bedingungen durch Kreuzen, Mutationen oder natürliche Rekombination (d.h. Neuzusammenstellung der Erbinformation) nicht vorkommt. Dabei werden in der Regel ein oder mehrere Gene in das Erbgut der Pflanze integriert, um die Eigenschaften der Pflanze zu verbessern.
Der Begriff Kulturpflanzen umfasst somit auch Pflanzen, die durch züchterische und gentechnische Maßnahmen eine Toleranz gegen bestimmter Herbizidklassen, wie Hydroxyphenylpyruvat-Dioxygenase (HPPD)-Inhibitoren, Acetolactat-Synthase (ALS)- Inhibitoren, wie z. B. Sulfonylharnstoffe (EP-A 257 993, US 5,013,659) oder Imidazoli- none (siehe z. B. US 6,222,100, WO 01/82685, WO 00/26390, WO 97/41218,
WO 98/02526, WO 98/02527, WO 04/106529, WO 05/20673, WO 03/14357,
WO 03/13225, WO 03/14356, WO 04/16073), Enolpyruvylshikimat-3-Phosphat- Synthase (EPSPS)-lnhibitoren wie z. B. Glyphosat (siehe z. B. WO 92/00377), Gluta- minsynthetase (GS)-lnhibitoren wie z. B. Glufosinat (siehe z. B. EP-A 242 236, EP-A 242 246) oder Oxynil-Herbizide (siehe z. B. US 5,559,024) erworben haben.
Mit Hilfe klassischer Züchtungsmethoden (Mutagenese) wurden zahlreiche Kulturpflanzen, z. B. Clearfield®-Raps, erzeugt, die eine Toleranz gegen Imidazolinone, z. B. Imazamox, haben. Mit Hilfe gentechnischer Methoden wurden Kulturpflanzen, wie So-
ja, Baumwolle, Mais, Rüben und Raps, erzeugt, die resistent gegen Glyphosat oder Glufosinat sind, erzeugt, welche unter den Handelsnamen RoudupReady® (Glyphosat) und Liberty Link® (Glufosinat) erhältlich sind.
Der Begriff Kulturpflanzen umfasst somit auch Pflanzen, die mit Hilfe gentechnischer Maßnahmen ein oder mehrere Toxine, z. B. solche aus dem Bakterienstamm Bacillus ssp., produzieren. Toxine, die durch solche gentechnisch veränderten Pflanzen hergestellt werden, umfassen z. B. insektizide Proteine von Bacillus spp., insbesondere von B. thuringiensis, wie die Endotoxine CrylAb, CrylAc, Cryl F, Cry1 Fa2, Cry2Ab, Cry3A, Cry3Bb1 , Cry9c, Cry34Ab1 oder Cry35Ab1 ; oder vegetative insektizide Proteine (VIPs)1 Z. B. VIP1 , VIP2, VIP3, oder VIP3A; insektizide Proteine von Nematoden- kolonisierenden Bakterien, z. B. Photorhabdus spp. oder Xenorhabdus spp.; Toxine aus tierischen Organismen, z. B. Wepsen,-, Spinnen- oder Skorpionstoxine; pilzliche Toxine, z. B. aus Streptomyceten; pflanzliche Lektine, z. B. aus Erbse oder Gerste; Agglutinine; Proteinase-Inhibitoren, z. B. Trypsin-Inhibitoren, Serinprotease-Inhibitoren, Patatin, Cystatin oder Papain-Inhibitoren; Ribosomen-inaktivierende Proteine (RIPs), z. B. Ricin, Mais-RIP, Abrin, Luffin, Saporin oder Bryodin; Steroid-metabolisierende Enzyme, z. B. 3-Hydroxysteroid-Oxidase, Ecdysteroid-IDP-Glycosyl-Transferase, Cho- lesterinoxidase, Ecdyson-Inhibitoren oder HMG-CoA-Reduktase; lonenkanalblocker, z. B. Inhibitoren von Natrium- oder Calziumkanälen; Juvenilhormon-Esterase; Rezepto- ren für das diuretischen Hormon (Helicokininrezeptoren); Stilbensynthase, Bibenzyl- synthase, Chitinasen und Glucanasen. Diese Toxine können in den Pflanzen auch als Prätoxine, Hybridproteine, verkürzte oder anderweitig modfizierte Proteine produziert werden. Hybridproteine zeichnen sich durch eine neue Kombination von verschiedenen Proteindomänen aus (siehe z. B. WO 2002/015701). Weitere Besipiele für derartige Toxine oder gentechnisch veränderte Pflanzen, die diese Toxine produzieren sind in EP-A 374 753, WO 93/007278, WO 95/34656, EP-A 427 529, EP-A 451 878,
WO 03/018810 und WO 03/052073 offenbart. Die Methoden zur Herstellung dieser gentechnisch veränderten Pflanzen sind dem Fachmann bekannt und z. B. in den oben erwähnten Publikationen dargelegt. Zahlreiche der zuvor genannten Toxine verleihen den Pflanzen, die diese produzieren, eine Toleranz gegen Schädlinge aus allen taxo- nomischen Arthropodenklassen, insbesondere gegen Käfer (Coeleropta), Zweiflügler (Diptera) und Schmetterlinge (Lepidoptera) und gegen Nematoden (Nematoda).
Gentechnisch veränderte Pflanzen, die ein oder mehrere Gene, die für insektizide Toxine kodieren, produzieren sind z. B. in den oben erwähnten Publikationen be- schrieben und zum Teil kommerziell erhältlich, wie z. B. YieldGard® (Maissorten, die das Toxin CrylAb produzieren), YieldGard® Plus (Maissorten, die die Toxine CrylAb und Cry3Bb1 produzieren), Starlink® (Maissorten, die das Toxin Cry9c produzieren), Herculex® RW (Maissorten, die die Toxine Cry34Ab1 , Cry35Ab1 und das Enzym Phosphinothricin-N-Acetyltransferase [PAT] produzieren); NuCOTN® 33B (Baumwoll- Sorten, die das Toxin CrylAc produzieren), Bollgard® I (Baumwollsorten, die das Toxin CrylAc produzieren), Bollgard® Il (Baumwollsorten, die die Toxine CrylAc und
Cry2Ab2 produzieren); VIPCOT® (Baumwollsorten, die ein VIP-Toxin produzieren);
NewLeaf® (Kartoffelsorten, die das Toxin Cry3A produzieren); Bt-Xtra®, NatureGard®, KnockOut®, BiteGard®, Protecta®, Bt11 (z. B. Agrisure® CB) und Bt176 von Syngenta Seeds SAS, Frankreich, (Maissorten, die das Toxin CrylAb und das PAT-Enyzm produzieren), MIR604 von Syngenta Seeds SAS, Frankreich (Maissorten, die ein modifi- zierte Version des Toxins Cry3A produzieren, siehe hierzu WO 03/018810), MON 863 von Monsanto Europe S.A., Belgien (Maissorten, die das Toxin Cry3Bb1 produzieren), IPC 531 von Monsanto Europe S.A., Belgien (Baumwollsorten, die eine modifizierte Version des Toxins CrylAc produzieren) und 1507 von Pioneer Overseas Corporation, Belgien (Maissorten, die das Toxin Cryl F und das PAT-Enyzm produzieren).
Der Begriff Kulturpflanzen umfasst somit auch Pflanzen, die mit Hilfe gentechnischer Maßnahmen ein oder mehrere Proteine produzieren, die eine erhöhte Resistenz oder Widerstandfähigkeit gegen bakterielle, virale oder pilzliche Pathogene bewirken, wie z. B. sogenannte Pathogenesis-related-Proteine (PR-Proteine, siehe EP-A 392 225), Resistenzproteine (z. B. Kartoffelsorten, die zwei Resistenzgene gegen Phytophthora infestans aus der mexikanischen Wildkartoffel Solanum bulbocastanum produzieren) oder T4-Lysozym (z. B. Kartoffelsorten, die durch die Produktion diese Proteins resistent gegen Bakterien wie Erwinia amylvora ist).
Der Begriff Kulturpflanzen umfasst somit auch Pflanzen, deren Produktivität mit Hilfe gentechnischer Methoden verbessert wurde, indem z. B. die Ertragsfähigkeit (z. B. Biomasse, Kornertrag, Stärke-, Öl- oder Proteingehalt), die Toleranz gegenüber Trockenheit, Salz oder anderen begrenzenden Umweltfaktoren oder die Widerstandsfähigkeit gegenüber Schädlingen und pilzlichen, bakteriellen und viralen Pathogenen gesteigert wird.
Der Begriff Kulturpflanzen umfasst auch Pflanzen, deren Inhaltsstoffe insbesondere zur Verbesserung der menschlichen oder tierischen Ernährung mit Hilfe gentechnischer Methoden verändert wurden, indem z. B. Ölpflanzen gesundheitsfördernde lang- kettige Omega-3-Fettsäuren oder einfach ungesättigte Omega-9-Fettsäuren (z. B. Ne- xera®-Raps) produzieren.
Der Begriff Kulturpflanzen umfasst auch Pflanzen, die zur verbesserten Produktion von Rohstoffen mit Hilfe gentechnischer Methoden verändert wurden, indem z. B. der Amylopektin-Gehalt von Kartoffeln (Amflora®-Kartoffel) erhöht wurde.
Des Weiteren wurde gefunden, dass die Verbindungen der Formel I auch zur Defoli- ation und/oder Desikkation von Pflanzenteilen geeignet ist, wofür Kulturpflanzen wie Baumwolle, Kartoffel, Raps, Sonnenblume, Sojabohne oder Ackerbohnen, insbesonde- re Baumwolle, in Betracht kommen. Diesbezüglich wurden Mittel zur Desikkation und /oder Defoliation von Pflanzen, Verfahren zur Herstellung dieser Mittel und Verfahren zur Desikkation und/oder Defoliation von Pflanzen mit der Verbindungen der Formel I gefunden.
Als Desikkantien eignen sich die Verbindungen der Formel I insbesondere zur Aus- trocknung der oberirdischen Teile von Kulturpflanzen wie Kartoffel, Raps, Sonnenblume und Sojabohne aber auch Getreide. Damit wird ein vollständig mechanisches Be- ernten dieser wichtigen Kulturpflanzen ermöglicht.
Von wirtschaftlichem Interesse ist ferner die Ernteerleichterung, die durch das zeitlich konzentrierte Abfallen oder Vermindern der Haftfestigkeit am Baum bei Zitrusfrüchten, Oliven oder bei anderen Arten und Sorten von Kern-, Stein- und Schalenobst er- möglicht wird. Derselbe Mechanismus, d.h., die Förderung der Ausbildung von Trenngewebe zwischen Frucht- oder Blatt- und Sprossteil der Pflanzen ist auch für ein gut kontrollierbares Entblättern von Nutzpflanzen, insbesondere Baumwolle, wesentlich. Außerdem führt die Verkürzung des Zeitintervalls, in dem die einzelnen Baumwollpflanzen reif werden, zu einer erhöhten Qualität der Faser nach der Ernte.
Die Verbindungen I bzw. die sie enthaltenden herbiziden Mittel können beispielsweise in Form von direkt versprühbaren wäßrigen Lösungen, Pulvern, Suspensionen, auch hochprozentigen wäßrigen, öligen oder sonstigen Suspensionen oder Dispersionen, Emulsionen, Öldispersionen, Pasten, Stäubemitteln, Streumitteln oder Granulaten durch Versprühen, Vernebeln, Verstäuben, Verstreuen, Gießen oder Behandlung des Saatgutes bzw. Mischen mit dem Saatgut angewendet werden. Die Anwendungsformen richten sich nach den Verwendungszwecken; sie sollten in jedem Fall möglichst die feinste Verteilung der erfindungsgemäßen Wirkstoffe gewährleisten.
Die herbiziden Mittel enthalten eine herbizid wirksame Menge mindestens einer Ver- bindung der Formel I oder eines landwirtschaftlich brauchbaren Salzes von I und für die Formulierung von Pflanzenschutzmitteln übliche Hilfsstoffe.
Beispiele für die Formulierung von Pflanzenschutzmitteln übliche Hilfsmittel sind i- nerte Hilfsstoffe, feste Trägerstoffe, oberflächenaktive Stoffe (wie Dispergiermittel Schutzkolloide, Emulgatoren, Netzmittel und Haftmittel), organische und anorganische Verdicker, Bakterizide, Frostschutzmittel, Entschäumer ggf. Farbstoffe und für Saatgutformulierungen Kleber.
Beispiele für Verdicker (d.h. Verbindungen, die der Formulierung ein modifiziertes Fließverhalten verleihen, d.h. hohe Viskosität im Ruhezustand und niedrige Viskosität im bewegten Zustand) sind Polysaccharide wie Xanthan Gum (Kelzan® der Fa. Kelco), Rhodopol® 23 (Rhone Poulenc) oder Veegum® (Firma R. T. Vanderbilt) sowie organische und anorganische Schichtmineralienwie Attaclay® (Firma Engelhardt).
Beispiele für Antischaummittel sind Silikonemulsionen (wie z.Bsp. Silikon® SRE, Firma Wacker oder Rhodorsil® der Firma Rhodia ), langkettige Alkohole, Fettsäuren, Salze von Fettsäuren, fluororganische Verbindungen und deren Gemische.
Bakterizide können zur Stabilisierung der wäßrigen Herbizid-Formulierung zugesetzt werden. Beispiele für Bakterizide sind Bakterizide basierend auf Diclorophen und Ben- zylalkoholhemiformal (Proxel® der Fa. ICI oder Acticide® RS der Fa. Thor Chemie und Kathon® MK der Firma Rohm & Haas) sowie Isothiazolinonderivaten wie Alkylisothia- zolinonen und Benzisothiazolinonen (Acticide MBS der Fa. Thor Chemie)
Beispiele für Frostschutzmittel sind Ethylenglycol, Propylenglycol, Harnstoff oder Glycerin.
Beispiele für Farbmittel sind sowohl in Wasser wenig lösliche Pigmente als auch in Wasser lösliche Farbstoffe. Als Beispiele genannt seien die unter den Bezeichnungen Rhodamin B, Cl. Pigment Red 112 und Cl. Solvent Red 1 bekannten Farbstoffe, sowie pigment blue 15:4, pigment blue 15:3, pigment blue 15:2, pigment blue 15:1 , pig- ment blue 80, pigment yellow 1 , pigment yellow 13, pigment red 1 12, pigment red 48:2, pigment red 48:1 , pigment red 57:1 , pigment red 53:1 , pigment orange 43, pigment orange 34, pigment orange 5, pigment green 36, pigment green 7, pigment white 6, pigment brown 25, basic violet 10, basic violet 49, acid red 51 , acid red 52, acid red 14, acid blue 9, acid yellow 23, basic red 10, basic red 108.
Beispiele für Kleber sind Polyvinylpyrrolidon, Polyvinylacetat, Polyvinylalkohol und Tylose.
Als inerte Zusatzstoffe kommen beispielsweise in Betracht:
Mineralölfraktionen von mittlerem bis hohem Siedepunkt, wie Kerosin oder Dieselöl, ferner Kohlenteeröle sowie Öle pflanzlichen oder tierischen Ursprungs, aliphatische, cyclische und aromatische Kohlenwasserstoffe, z.B. Paraffin, Tetrahydronaphthalin, alkylierte Naphthaline oder deren Derivate, alkylierte Benzole oder deren Derivate, Alkohole wie Methanol, Ethanol, Propanol, Butanol, Cyclohexanol, Ketone wie Cycloh- exanon oder stark polare Lösungsmittel, z. B. Amine wie N-Methylpyrrolidon oder Wasser.
Feste Trägerstoffe sind Mineralerden wie Kieselsäuren, Kieselgele, Silikate, Talkum, Kaolin, Kalkstein, Kalk, Kreide, Bolus, Löß, Ton, Dolomit, Diatomeenerde, Calcium- und Magnesiumsulfat, Magnesiumoxid, gemahlene Kunststoffe, Düngemittel, wie Ammoniumsulfat, Ammoniumphosphat, Ammoniumnitrat, Harnstoffe und pflanzliche Pro- dukte wie Getreidemehl, Baumrinden-, Holz- und Nußschalenmehl, Cellulosepulver oder andere feste Trägerstoffe.
Als oberflächenaktive Stoffe (Adjuvantien, Netz-, Haft-, Dispergier- sowie Emulgiermittel) kommen die Alkali-, Erdalkali-, Ammoniumsalze von aromatischen Sulfonsäu- ren, z.B. Ligninsulfonsäuren (z.B. Borrespers-Typen, Borregaard), Phenolsulfonsäuren, Naphthalinsulfonsäuren (Morwet-Typen, Akzo Nobel) und Dibutylnaphthalinsulfonsäure (Nekal-Typen, BASF SE), sowie von Fettsäuren, Alkyl- und Alkylarylsulfonaten, Alkyl-, Laurylether- und Fettalkoholsulfaten, sowie Salze sulfatierter Hexa-, Hepta- und Octa- decanolen sowie von Fettalkoholglykolether, Kondensationsprodukte von sulfoniertem Naphthalin und seiner Derivate mit Formaldehyd, Kondensationsprodukte des Naph- thalins bzw. der Naphthalinsulfonsäuren mit Phenol und Formaldehyd, Polyoxyethylen- octylphenolether, ethoxyliertes Isooctyl-, Octyl- oder Nonylphenol, Alkylphenyl-, Tribu- tylphenylpolyglykolether, Alkylarylpolyetheralkohole, Isotridecylalkohol, Fettalkoholethy- lenoxid-Kondensate, ethoxyliertes Rizinusöl, Polyoxyethylenalkylether oder Polyoxy- propylenalkylether, Laurylalkoholpolyglykoletheracetat, Sorbitester, Lignin-Sulfitablau- gen sowie Proteine, denaturierte Proteine, Polysaccharide (z.B. Methylcellulose), hydrophob modifizierte Stärken, Polyvinylalkohol (Mowiol typen Clariant), Polycarboxylate (BASF SE, Sokalan-Typen), Polyalkoxylate, Polyvinylamin (BASF SE, Lupamin-
Typen), Polyethylenimin (BASF SE, Lupasol-Typen) , Polyvinylpyrrolidon und deren Copolymere in Betracht.
Pulver-, Streu- und Stäubemittel können durch Mischen oder gemeinsames Vermählen der wirksamen Substanzen mit einem festen Trägerstoff hergestellt werden.
Granulate, z.B. Umhüllungs-, Imprägnierungs- und Homogengranulate können durch Bindung der Wirkstoffe an feste Trägerstoffe hergestellt werden.
Wässrige Anwendungsformen können aus Emulsionskonzentraten, Suspensionen, Pasten, netzbaren Pulvern oder wasserdispergierbaren Granulaten durch Zusatz von Wasser bereitet werden. Zur Herstellung von Emulsionen, Pasten oder Öldispersionen können die Verbindungen der Formel I oder Ia als solche oder in einem Öl oder Lösungsmittel gelöst, mittels Netz-, Haft-, Dispergier- oder Emulgiermittel in Wasser homogenisiert werden. Es können aber auch aus wirksamer Substanz, Netz-, Haft-, Dispergier- oder Emulgiermittel und eventuell Lösungsmittel oder Öl bestehende Konzentrate hergestellt werden, die zur Verdünnung mit Wasser geeignet sind.
Die Konzentrationen der Verbindungen der Formel I in den anwendungsfertigen Zubereitungen können in weiten Bereichen variiert werden. Die Formulierungen enthalten im Allgemeinen 0,001 bis 98 Gew.-%, vorzugsweise 0,01 bis 95 Gew.-%, mindestens eines Wirkstoffs. Die Wirkstoffe werden dabei in einer Reinheit von 90% bis 100%, vorzugsweise 95% bis 100% (nach NMR-Spektrum) eingesetzt.
Die erfindungsgemäßen Verbindungen I können beispielsweise wie folgt formuliert werden:
1. Produkte zur Verdünnung in Wasser
A Wasserlösliche Konzentrate
10 Gew.-Teile Wirkstoff werden mit 90 Gew.-Teilen Wasser oder einem wasserlöslichen Lösungsmittel gelöst. Alternativ werden Netzmittel oder andere Hilfsmittel zugefügt. Bei der Verdünnung in Wasser löst sich der Wirkstoff. Man erhält auf diese Weise eine Formulierung mit 10 Gew.-% Wirkstoffgehalt.
B Dispergierbare Konzentrate
20 Gew.-Teile Wirkstoff werden in 70 Gew.-Teilen Cyclohexanon unter Zusatz von 10 Gew.-Teilen eines Dispergiermittels z.B. Polyvinylpyrrolidon gelöst. Bei Verdünnung in Wasser ergibt sich eine Dispersion. Der Wirkstoffgehalt beträgt 20 Gew.-%
C Emulgierbare Konzentrate
15 Gew.-Teile Wirkstoff werden in 75 Gew.-Teilen eines organisches Lösungsmittels (z.B. Alkylaromaten)-unter Zusatz von Ca-Dodecylbenzolsulfonat und Ricinusölethoxy- lat (jeweils 5 Gew.-Teile) gelöst. Bei der Verdünnung in Wasser ergibt sich eine Emulsion. Die Formulierung hat 15 Gew.-% Wirkstoffgehalt.
D Emulsionen
25 Gew.-Teile Wirkstoff werden in 35 Gew.-Teilen eines organisches Lösungsmittels (z.B. Alkylaromaten) unter Zusatz von Ca-Dodecylbenzolsulfonat und Ricinusölethoxy- lat (jeweils 5 Gew.-Teile) gelöst. Diese Mischung wird mittels einer Emulgiermaschine (z.B. Ultraturax) in 30 Gew.Teile Wasser gegeben und zu einer homogenen Emulsion
gebracht. Bei der Verdünnung in Wasser ergibt sich eine Emulsion. Die Formulierung hat einen Wirkstoffgehalt von 25 Gew.-%.
E Suspensionen
20 Gew.-Teile Wirkstoff werden unter Zusatz von 10 Gew.-Teilen Dispergier- und Netzmitteln und 70 Gew.-Teilen Wasser oder einem organischen Lösungsmittel in einer Rührwerkskugelmühle zu einer feinen Wirkstoffsuspension zerkleinert. Bei der Verdünnung in Wasser ergibt sich eine stabile Suspension des Wirkstoffs. Der Wirkstoffgehalt in der Formulierung beträgt 20 Gew.-% .
F Wasserdispergierbare und wasserlösliche Granulate
50 Gew.-Teile Wirkstoff werden unter Zusatz von 50 Gew-Teilen Dispergier- und Netzmitteln fein gemahlen und mittels technischer Geräte (z.B. Extrusion, Sprühturm, Wirbelschicht) als wasserdispergierbare oder wasserlösliche Granulate hergestellt. Bei der Verdünnung in Wasser ergibt sich eine stabile Dispersion oder Lösung des Wirkstoffs. Die Formulierung hat einen Wirkstoffgehalt von 50 Gew.-%.
G Wasserdispergierbare und wasserlösliche Pulver
75 Gew.-Teile Wirkstoff werden unter Zusatz von 25 Gew.-Teilen Dispergier- und Netzmitteln sowie Kieselsäuregel in einer Rotor-Strator Mühle vermählen. Bei der Verdünnung in Wasser ergibt sich eine stabile Dispersion oder Lösung des Wirkstoffs. Der Wirkstoffgehalt der Formulierung beträgt 75 Gew.-%.
H Gelformulierungen
In einer Kugelmühle werden 20 Gew.-Teile Wirkstoff, 10 Gew.-Teile Dispergiermittel, 1 Gew.-Teil Geliermittel und 70 Gew.-Teile Wasser oder eines organischen Lösungsmittels zu einer feinen Suspension vermählen. Bei der Verdünnung mit Wasser ergibt sich eine stabile Suspension mit 20 Gew.-% Wirkstoffgehalt.
2. Produkte für die Direktapplikation
I Stäube
5 Gew.-Teile Wirkstoff werden fein gemahlen und mit 95 Gew.-Teilen feinteiligem Kaolin innig vermischt. Man erhält dadurch ein Stäubemittel mit 5 Gew.-% Wirkstoffgehalt. J Granulate (GR, FG, GG, MG)
0,5 Gew-Teile Wirkstoff werden fein gemahlen und mit 99,5 Gewichtsteilen Trägerstoffe verbunden. Gängige Verfahren sind dabei die Extrusion, die Sprühtrocknung oder die Wirbelschicht. Man erhält dadurch ein Granulat für die Direktapplikation mit 0,5 Gew.-% Wirkstoffgehalt.
K ULV- Lösungen (UL)
10 Gew.-Teile Wirkstoff werden in 90 Gew.-Teilen eines organischen Lösungsmittels z.B. XyIoI gelöst. Dadurch erhält man ein Produkt für die Direktapplikation mit 10 Gew.- % Wirkstoffgehalt. Die Applikation der Verbindungen I oder der sie enthaltenden herbiziden Mittel kann im Vorauflauf-, im Nachauflaufverfahren oder zusammen mit dem Saatgut einer Kulturpflanze erfolgen. Es besteht auch die Möglichkeit, die herbiziden Mittel bzw. Wirkstoffe
dadurch zu applizieren, dass mit den herbiziden Mitteln bzw. Wirkstoffen vorbehandeltes Saatgut einer Kulturpflanze ausgebracht wird. Sind die Wirkstoffe für gewisse Kulturpflanzen weniger verträglich, so können Ausbringungstechniken angewandt werden, bei welchen die herbiziden Mittel mit Hilfe der Spritzgeräte so gespritzt werden, daß die Blätter der empfindlichen Kulturpflanzen nach Möglichkeit nicht getroffen werden, während die Wirkstoffe auf die Blätter darunter wachsender unerwünschter Pflanzen oder die unbedeckte Bodenfläche gelangen (post-directed, lay-by).
In einer weiteren Ausführungsform kann die Applikation der Verbindungen der For- mel I bzw. der herbiziden Mittel durch Behandlung von Saatgut erfolgen.
Die Behandlung von Saatgut umfasst im Wesentlichen alle dem Fachmann geläufigen Techniken (seed dressing, seed coating, seed dusting, seed soaking, seed film coating, seed multilayer coating, seed encrusting, seed dripping, und seed pelleting) basierend auf den erfindungsgemäßen Verbindungen der Formel I bzw. daraus herge- stellten Mitteln. Hierbei können die herbiziden Mittel verdünnt oder unverdünnt aufgetragen werden.
Der Begriff Saatgut umfasst Saatgut aller Arten, wie z.B. Körner, Samen, Früchte, Knollen, Stecklinge und ähnliche Formen. Bevorzugt beschreibt der Begriff Saatgut hier Körner und Samen.
Als Saatgut kann Saatgut der oben erwähnten Nutzpflanzen aber auch das Saatgut transgener oder durch herkömmliche Züchtungsmethoden erhaltener Pflanzen eingesetzt werden.
Die Aufwandmengen an Wirkstoff betragen je nach Bekämpfungsziel, Jahreszeit, Zielpflanzen und Wachstumsstadium 0.001 bis 3.0, vorzugsweise 0.01 bis 1.0 kg/ha aktive Substanz (a. S.). Zur Saatgutbehandlung werden die Verbindungen I üblicherweise in Mengen von 0,001 bis 10 kg pro 100 kg Saatgut eingesetzt.
Es kann auch von Vorteil sein, die Verbindungen der Formel I in Kombination mit Sa- fenern zu verwenden. Safener sind chemische Verbindungen, die Schaden an Nutzpflanzen verhindern oder reduzieren, ohne die herbizide Wirkung der Verbindungen der Formel I auf unerwünschte Pflanzen wesentlich zu beeinflussen. Sie können sowohl vor der Aussaat (beispielsweise bei Saatgutbehandlungen, bei Stecklingen oder Setzlingen) als auch im Vor- oder Nachauflauf der Nutzpflanze verwendet werden. Die Safener und die Verbindungen der Formel I können gleichzeitig oder nacheinander verwendet werden. Geeignete Safener sind beispielsweise (Chinolin-δ-oxy)essig- säuren, 1-Phenyl-5-haloalkyl-1 H-1 ,2,4-triazol-3-carbonsäuren, 1-Phenyl-4,5-dihydro-5- alkyl-1 H-pyrazol-3,5-dicarbonsäuren, 4,5-Dihydro-5,5-diaryl-3-isoxazolcarbonsäuren, Dichloroacetamide, alpha-Oximinophenylacetonitrile, Acetophenonoxime, 4,6-Dihalo-2- phenylpyrimidine, N-[[4-(Aminocarbonyl)phenyl]sulfonyl]-2-benzoesäureamide, 1 ,8- Naphthalsäureanhydrid, 2-Halo-4-(haloalkyl)-5-thiazolcarbonsäuren, Phosphorthiolate und N-Alkyl-O-phenylcarbamate sowie ihre landwirtschaftlich brauchbaren Salze, und
vorausgesetzt sie haben eine Säurefunktion, ihre landwirtschaftlich brauchbaren Derivate, wie Amide, Ester und Thioester.
Zur Verbreiterung des Wirkungsspektrums und zur Erzielung synergistischer Effekte können die Verbindungen der Formel I mit zahlreichen Vertretern anderer herbizider oder wachstumsregulierender Wirkstoffgruppen oder mit Safenern gemischt und gemeinsam ausgebracht werden. Beispielsweise kommen als Mischungspartner 1 ,2,4- Thiadiazole, 1 ,3,4-Thiadiazole, Amide, Aminophosphorsäure und deren Derivate, Ami- notriazole, Anilide, Aryloxy-/Heteroaryloxyalkansäuren und deren Derivate, Benzoesäure und deren Derivate, Benzothiadiazinone, 2-(Hetaroyl/Aroyl)-1 ,3-cyclohexandione, Heteroaryl-Aryl-Ketone, Benzylisoxazolidinone, meta-CF3-Phenylderivate, Carbamate, Chinolincarbonsäure und deren Derivate, Chloracetanilide, Cyclohexenonoximetherde- rivate, Diazine, Dichlorpropionsäure und deren Derivate, Dihydrobenzofurane, Dihydro- furan-3-one, Dinitroaniline, Dinitrophenole, Diphenylether, Dipyridyle, Halogencarbonsäuren und deren Derivate, Harnstoffe, 3-Phenyluracile, Imidazole, Imidazolinone, N- Phenyl-3,4,5,6-tetrahydrophthalimide, Oxadiazole, Oxirane, Phenole, Aryloxy- und He- teroaryloxyphenoxypropionsäureester, Phenylessigsäure und deren Derivate, 2-Phe- nylpropionsäure und deren Derivate, Pyrazole, Phenylpyrazole, Pyridazine, Pyridincar- bonsäure und deren Derivate, Pyrimidylether, Sulfonamide, Sulfonylharnstoffe, Triazi- ne, Triazinone, Triazolinone, Triazolcarboxamide, Uracile sowie Phenylpyrazoline und Isoxazoline und deren Derivate in Betracht.
Außerdem kann es von Nutzen sein, die Verbindungen I allein oder in Kombination mit anderen Herbiziden oder auch noch mit weiteren Pflanzenschutzmitteln gemischt, gemeinsam auszubringen, beispielsweise mit Mitteln zur Bekämpfung von Schädlingen oder phytopathogenen Pilzen bzw. Bakterien. Von Interesse ist ferner die Mischbarkeit mit Mineralsalzlösungen, welche zur Behebung von Ernährungs- und Spurenelementmängeln eingesetzt werden. Es können auch weitere Additve wie nicht phytotoxische Öle und Ölkonzentrate zugesetzt werden.
Beispiele für Herbizide, die in Kombination mit den Pyridinverbindungen der Formel I gemäß der vorliegenden Erfindung verwendet werden können, sind:
b1) aus der Gruppe der Lipid-Biosynthese-Inhibitoren:
Alloxydim, Alloxydim-natrium, Butroxydim, Clethodim, Clodinafop, Clodinafop-propar- gyl, Cycloxydim, Cyhalofop, Cyhalofop-butyl, Diclofop, Diclofop-methyl, Fenoxaprop, Fenoxaprop-ethyl, Fenoxaprop-P, Fenoxaprop-P-ethyl, Fluazifop, Fluazifop-butyl, FIu- azifop-P, Fluazifop-P-butyl, Haloxyfop, Haloxyfop-methyl, Haloxyfop-P, Haloxyfop-P- methyl, Metamifop, Pinoxaden, Profoxydim, Propaquizafop, Quizalofop, Quizalofop- ethyl, Quizalofop-tefuryl, Quizalofop-P, Quizalofop-P-ethyl, Quizalofop-P-tefuryl, Sethoxydim, Tepraloxydim, Tralkoxydim, Benfuresat, Butylat, Cycloat, Dalapon, Dime- piperat, EPTC, Esprocarb, Ethofumesat, Flupropanat, Molinat, Orbencarb, Pebulat, Prosulfocarb, TCA, Thiobencarb, Tiocarbazil, Triallat und Vernolat;
b2) aus der Gruppe der ALS-Inhibitoren:
Amidosulfuron, Azimsulfuron, Bensulfuron, Bensulfuron-methyl, Bispyribac, Bispyribac- natrium, Chlorimuron, Chlorimuron-ethyl, Chlorsulfuron, Cinosulfuron, Cloransulam,
Cloransulam-methyl, Cyclosulfamuron, Diclosulam, Ethametsulfuron, Ethametsulfuron- methyl, Ethoxysulfuron, Flazasulfuron, Florasulam, Flucarbazon, Flucarbazon-natrium, Flucetosulfuron, Flumetsulam, Flupyrsulfuron, Flupyrsulfuron-methyl-natrium, Foram- sulfuron, Halosulfuron, Halosulfuron-methyl, Imazamethabenz, Imazamethabenz- methyl, Imazamox, Imazapic, Imazapyr, Imazaquin, Imazethapyr, Imazosulfuron, lodo- sulfuron, lodosulfuron-methyl-natrium, Mesosulfuron, Metosulam, Metsulfuron, Metsul- furon-methyl, Nicosulfuron, Orthosulfamuron, Oxasulfuron, Penoxsulam, Primisulfuron, Primisulfuron-methyl, Propoxycarbazon, Propoxycarbazon-natrium, Prosulfuron, Pyra- zosulfuron, Pyrazosulfuron-ethyl, Pyribenzoxim, Pyrimisulfan, Pyriftalid, Pyriminobac, Pyriminobac-methyl, Pyrithiobac, Pyrithiobac-natrium, Pyroxsulam, Rimsulfuron, SuI- fometuron, Sulfometuron-methyl, Sulfosulfuron, Thiencarbazon, Thiencarbazon-methyl, Thifensulfuron, Thifensulfuron-methyl, Triasulfuron, Tribenuron, Tribenuron-methyl, Trifloxysulfuron, Triflusulfuron, Triflusulfuron-methyl und Tritosulfuron;
b3) aus der Gruppe der Photosynthese-Inhibitoren:
Ametryn, Amicarbazon, Atrazin, Bentazon, Bentazon-natrium, Bromacil, Bromofeno- xim, Bromoxynil und seine Salze und Ester, Chlorobromuron, Chloridazon, Chlorotolu- ron, Chloroxuron, Cyanazin, Desmedipham, Desmetryn, Dimefuron, Dimethametryn, Diquat, Diquat-dibromid, Diuron, Fluometuron, Hexazinon, loxynil und seine Salze und Ester, Isoproturon, Isouron, Karbutilat, Lenacil, Linuron, Metamitron, Methabenzthiazu- ron, Metobenzuron, Metoxuron, Metribuzin, Monolinuron, Neburon, Paraquat, Para- quat-dichlorid, Paraquat-dimetilsulfat, Pentanochlor, Phenmedipham, Phenmedipham- ethyl, Prometon, Prometryn, Propanil, Propazin, Pyridafol, Pyridat, Siduron, Simazin, Simetryn, Tebuthiuron, Terbacil, Terbumeton, Terbuthylazin, Terbutryn, Thidiazuron und Trietazin;
b4) aus der Gruppe der Protoporphyrinogen-IX-Oxidase-Inhibitoren:
Acifluorfen, Acifluorfen-natrium, Azafenidin, Bencarbazon, Benzfendizon, Bifenox, Bu- tafenacil, Carfentrazon, Carfentrazon-ethyl, Chlomethoxyfen, Cinidon-ethyl, Fluazolat, Flufenpyr, Flufenpyr-ethyl, Flumiclorac, Flumiclorac-pentyl, Flumioxazin, Fluoroglyco- fen, Fluoroglycofen-ethyl, Fluthiacet, Fluthiacet-methyl, Fomesafen, Halosafen, Lacto- fen, Oxadiargyl, Oxadiazon, Oxyfluorfen, Pentoxazon, Profluazol, Pyraclonil, Pyraflu- fen, Pyraflufen-ethyl, Saflufenacil, Sulfentrazon, Thidiazimin, 2-Chlor-5-[3,6-dihydro-3- methyl-2,6-dioxo-4-(trifluormethyl)-1 (2H)-pyrimidinyl]-4-fluor-N-[(isopropyl)methylsulf- amoyl]benzamid (B-1 ; CAS 372137-35-4), [3-[2-Chlor-4-fluor-5-(1-methyl-6-trifluor- methyl-2,4-dioxo-1 ,2,3,4, -tetrahydropyrimidin-3-yl)phenoxy]-2-pyridyloxy]essigsäure- ethylester (B-2; CAS 353292-31-6), N-Ethyl-3-(2,6-dichlor-4-trifluormethylphenoxy)-5- methyl-1 H-pyrazol-1-carboxamid (B-3; CAS 452098-92-9), N-Tetrahydrofurfuryl-3-(2,6- dichlor-4-trifluormethylphenoxy)-5-methyl-1 H-pyrazol-1-carboxamid (B-4; CAS 915396- 43-9), N-Ethyl-3-(2-chlor-6-fluor-4-trifluormethylphenoxy)-5-methyl-1 H-pyrazol-1 -carb- oxamid (B-5; CAS 452099-05-7) und N-Tetrahydrofurfuryl-3-(2-chlor-6-fluor-4-trifluor- methylphenoxy)-5-methyl-1 H-pyrazol-1 -carboxamid (B-6; CAS 452100-03-7);
b5) aus der Gruppe der Bleacher-Herbizide:
Aclonifen, Amitrol, Beflubutamid, Benzobicyclon, Benzofenap, Clomazon, Diflufeni- can, Fluridon, Flurochloridon, Flurtamon, Isoxaflutol, Mesotrion, Norflurazon, Picolina- fen, Pyrasulfutol, Pyrazolynat, Pyrazoxyfen, Sulcotrion, Tefuryltrion, Tembotrion, Top- ramezon, 4-Hydroxy-3-[[2-[(2-methoxyethoxy)methyl]-6-(trifluormethyl)-3-pyridyl]car- bonyl]bicyclo[3.2.1]oct-3-en-2-one (B-7; CAS 352010-68-5) und 4-(3-Trifluormethyl- phenoxy)-2-(4-trifluormethylphenyl)pyrimidin (B-8; CAS 180608-33-7);
b6) aus der Gruppe der EPSP-Synthase-lnhibitoren:
Glyphosat, Glyphosat-isopropylammonium und Glyphosat-trimesium (Sulfosat);
b7) aus der Gruppe der Glutamin-Synthase-Inhibitoren:
Bilanaphos (Bialaphos), Bilanaphos-natrium, Glufosinat und Glufosinat-ammonium; b8) aus der Gruppe der DHP-Synthase-Inhibitoren: Asulam;
b9) aus der Gruppe der Mitose-Inhibitoren:
Amiprophos, Amiprophos-methyl, Benfluralin, Butamiphos, Butralin, Carbetamid, Chlorpropham, Chlorthal, Chlorthal-dimethyl, Dinitramin, Dithiopyr, Ethalfluralin, FIu- chloralin, Oryzalin, Pendimethalin, Prodiamin, Propham, Propyzamid, Tebutam, Thia- zopyr und Trifluralin;
b10) aus der Gruppe der VLCFA-lnhibitoren:
Acetochlor, Alachlor, Anilofos, Butachlor, Cafenstrol, Dimethachlor, Dimethanamid, Dimethenamid-P, Diphenamid, Fentrazamid, Flufenacet, Mefenacet, Metazachlor, Me- tolachlor, Metolachlor-S, Naproanilid, Napropamid, Pethoxamid, Piperophos, Pretila- chlor, Propachlor, Propisochlor, Pyroxasulfon (KIH-485) und Thenylchlor;
worin die Variablen folgende Bedeutungen haben:
Y Phenyl oder 5- oder 6-gliedriges Heteroaryl wie eingangs definiert, welche durch eine bis drei Gruppen Raa substituiert sein können; R21, R22, R23, R24 H, Halogen, oder Ci-C4-Alkyl; X O oder NH; n 0 oder 1.
wobei # die Bindung zu dem Molekülgerüst bedeutet; und
R21, R22, R23, R24 H, Cl, F oder CH3; R25 Halogen, d-C4-Alkyl oder Ci-C4-Haloalkyl; R26 Ci-C4-Alkyl; R27 Halogen, Ci-C4-Alkoxy oder Ci-C4-Haloalkoxy; R28 H, Halogen, Ci-C4- Alkyl, Ci-C4-Haloalkyl oder Ci-C4-Haloalkoxy; m 0, 1 , 2 oder 3; X Sauerstoff;
n 0 oder 1.
R21 H; R22, R23 F; R24 H oder F; X Sauerstoff; n 0 oder 1.
Besonders bevorzugte Verbindungen der Formel 2 sind:
3-[5-(2,2-Difluor-ethoxy)-1-methyl-3-trifluormethyl-1 H-pyrazol-4-ylmethansulfonyl]-4- fluor-5,5-dimethyl-4,5-dihydro-isoxazol (2-1 ); 3-{[5-(2,2-Difluor-ethoxy)-1-methyl-3-tri- fluormethyl-1 H-pyrazol-4-yl]-fluor-methansulfonyl}-5,5-dimethyl-4,5-dihydro-isoxazol (2- 2); 4-(4-Fluor-5,5-dimethyl-4,5-dihydro-isoxazol-3-sulfonylmethyl)-2-methyl-5-trifluor- methyl-2H-[1 ,2,3]triazol (2-3); 4-[(5,5-Dimethyl-4,5-dihydro-isoxazol-3-sulfonyl)-fluor- methyl]-2-methyl-5-trifluormethyl-2H-[1 ,2,3]triazol (2-4); 4-(5,5-Dimethyl-4,5-dihydro- isoxazol-3-sulfonylmethyl)-2-methyl-5-trifluormethyl-2H-[1 ,2,3]triazol (2-5); 3-{[5-(2,2- Difluor-ethoxy)-1-methyl-3-trifluormethyl-1 H-pyrazol-4-yl]-difluor-methansulfonyl}-5,5- dimethyl-4,5-dihydro-isoxazol (2-6); 4-[(5,5-Dimethyl-4,5-dihydro-isoxazol-3-sulfonyl)- difluor-methyl]-2-methyl-5-trifluormethyl-2H-[1 ,2,3]triazol (2-7); 3-{[5-(2,2-Difluor- ethoxy)-1-methyl-3-trifluormethyl-1 H-pyrazol-4-yl]-difluor-methansulfonyl}-4-fluor-5,5- dimethyl-4,5-dihydro-isoxazol (2-8); 4-[Difluor-(4-fluor-5,5-dimethyl-4,5-dihydro- isoxazol-3-sulfonyl)-methyl]-2-methyl-5-trifluormethyl-2H-[1 ,2,3]triazol (2-9);
b1 1) aus der Gruppe der Cellulose-Biosynthese-Inhibitoren:
Chlorthiamid, Dichlobenil, Flupoxam und Isoxaben;
b12) aus der Gruppe der Entkoppler-Herbizide:
Dinoseb, Dinoterb und DNOC und seine Salze;
b13) aus der Gruppe der Auxin-Herbizide:
2,4-D und seine Salze und Ester, 2,4-DB und seine Salze und Ester, Aminopyralid und seine Salze wie Aminopyralid-tris(2-hydroxypropyl)ammonium und seine Ester, Benazolin, Benazolin-ethyl, Chloramben und seine Salze und Ester, Clomeprop, Clopy- ralid und seine Salze und Ester, Dicamba und seine Salze und Ester, Dichlorprop und seine Salze und Ester, Dichlorprop-P und seine Salze und Ester, Fluroxypyr, Fluroxy- pyr-butometyl, Fluroxypyr-meptyl, MCPA und seine Salze und Ester, MCPA-thioethyl, MCPB und seine Salze und Ester, Mecoprop und seine Salze und Ester, Mecoprop-P und seine Salze und Ester, Picloram und seine Salze und Ester, Quinclorac, Quinme- rac, TBA (2,3,6) und seine Salze und Ester, Triclopyr und seine Salze und Ester, und 5,6-Dichlor-2-cyclopropyl-4-pyrimidincarbonsäure (B-9; CAS 858956-08-8) und seine Salze und Ester;
b14) aus der Gruppe der Auxin-Transport-Inhibitoren: Diflufenzopyr, Diflufenzopyr- natrium, Naptalam und Naptalam-natrium;
b15) aus der Gruppe der sonstigen Herbizide: Bromobutid, Chlorflurenol, Chlor- flurenol-methyl, Cinmethylin, Cumyluron, Dalapon, Dazomet, Difenzoquat, Difenzo- quat-metilsulfate, Dimethipin, DSMA, Dymron, Endothal und seine Salze, Etobenzanid, Flamprop, Flamprop-isopropyl, Flamprop-methyl Flamprop-M-isopropyl, Flamprop-M- methyl, Flurenol, Flurenol-butyl, Flurprimidol, Fosamin, Fosamine-ammonium, Indano- fan, Maleinsäure-hydrazid, Mefluidid, Metam, Methylazid, Methylbromid, Methyl-dym-
ron, Methyljod id. MSMA, Ölsäure, Oxaziclomefon, Pelargonsäure, Pyributicarb, Quino- clamin, Triaziflam, Tridiphan und 6-Chlor-3-(2-cyclopropyl-6-methylphenoxy)-4-pyrida- zinol (B-10; CAS 499223-49-3) und seine Salze und Ester.
Beispiele für bevorzugte Safener C sind Benoxacor, Cloquintocet, Cyometrinil, Cy- prosulfamid, Dichlormid, Dicyclonon, Dietholate, Fenchlorazol, Fenclorim, Flurazol, FIu- xofenim, Furilazol, Isoxadifen, Mefenpyr, Mephenat, Naphthalsäureanhydrid, Oxabetri- nil, 4-(Dichloracetyl)-1-oxa-4-azaspiro[4.5]decan (B-1 1 ; MON4660, CAS 71526-07-3) und 2,2,5-Trimethyl-3-(dichloracetyl)-1 ,3-oxazolidin (B-12; R-29148, CAS 52836-31-4). Die Wirkstoffe der Gruppen b1 ) bis b15) und die Safener C sind bekannte Herbizide und Safener, siehe z. B. The Compendium of Pesticide Common Names
(http://www.alanwood.net/pesticides/); B. Hock, C. Fedtke, R. R. Schmidt, Herbizide, Georg Thieme Verlag, Stuttgart 1995. Weitere herbizide Wirkstoffe sind aus WO 96/26202, WO 97/411 16, WO 97/41 117, WO 97/411 18, WO 01/83459 und WO
2008/074991 sowie aus W. Krämer et al. (ed.) "Modern Crop Protection Compounds", Vol. 1 , Wiley VCH, 2007 und der darin zitierten Literatur bekannt.
Die Verbindungen I und die erfindungsgemäßen Zusammensetzungen können auch eine pflanzenstärkende Wirkung aufweisen. Sie eigenen sich daher zu Mobilisierung pflanzeneigener Abwehrkräfte gegen Befall durch unerwünschte Mikroorganismen, wie Schadpilze, aber auch Viren und Bakterien. Unter pflanzenstärkenden (resistenzinduzierenden) Stoffen sind in diesem Zusammenhang solche Substanzen zu verstehen, die in der Lage sind, das Abwehrsystem von behandelten Pflanzen so zu stimulieren, dass diese bei nachfolgender Inokulation mit unerwünschten Mikroorganismen weitgehende Resistenz gegen diese Mikroorganismen entfalten.
Die Verbindungen I können eingesetzt werden, um Pflanzen innerhalb eines gewissen Zeitraumes nach der Behandlung gegen den Befall durch unerwünschte Mikroorganismen zu schützen. Der Zeitraum, innerhalb dessen Schutz herbeigeführt wird, erstreckt sich im Allgemeinen auf 1 bis 28 Tage, vorzugsweise 1 bis 14 Tage nach der Behandlung der Pflanzen mit den Verbindungen I bzw. nach Behandlung des Saatguts, auf bis zu 9 Monate nach Aussaat.
Die Verbindungen I und die erfindungsgemäßen Zusammensetzungen eignen sich auch zur Steigerung des Ernteertrages.
Sie sind außerdem mindertoxisch und weisen eine gute Pflanzenverträglichkeit auf. Im Folgenden wird die Herstellung von Pyridinverbindungen der Formel I anhand von Beispielen erläutert ohne dabei den Gegenstand der vorliegenden Erfindung auf die gezeigten Beispiele zu begrenzen.
Synthesebeispiele
Die in den nachstehenden Synthesebeispielen wiedergegebenen Vorschriften wurden unter entsprechender Abwandlung der Ausgangsverbindungen zur Gewinnung weiterer
Verbindungen I benutzt. Die so erhaltenen Verbindungen sind in der anschließenden Tabelle mit physikalischen Angaben aufgeführt.
Die Charakterisierung der im Folgenden gezeigten Produkte erfolgte durch Bestim- mung des Schmelzpunktes, durch NMR-Spektroskopie oder anhand der durch
HPLC-MS-Spektrometrie ermittelten Massen ([m/z]) oder Retentionszeit (RT; [min.]).
[HPLC-MS = High Performance Liquid Chromatographie kombiniert mit Massen Spektrometrie; HPLC-Säule:
RP-18 Säule (Chromolith Speed ROD von Merck KgaA, Deutschland), 50*4,6 mm; Eluent: Acetonitril + 0,1 % Trifluoressigsäure (TFA)/ Wasser + 0,1 % TFA, mit einem Gradienten von 5 : 95 bis 100 : 0 in 5 Minuten bei 400C, Flussrate 1 ,8 ml/min.
MS: Quadrupol Elektrospray-Ionisation, 80 V (Positiv-Modus).] I. Herstellungsbeispiele
Beispiel 1 : Herstellung von 3-(3-Chlor-2-fluor-phenyl)-4-cyano-4-(4-fluor-phenyl)- buttersäuremethylester [I-46]
Zu einer Lösung von 52,5 mg 3-(3-Chlor-2-fluor-phenyl)-acrylsäuremethylester in THF wurden 0,33 g 4-Fluorphenylacetonitril unter Schutzgas (Ar) zugegeben. Nach 5 min wurden 0,42 ml 7-Methyl-1 ,5,7-triazabicyclo[4.4.0]dec-5-en hinzugegeben. Die
Reaktionslösung wurde 2 d bei 500C gerührt. Anschließend wurde Ethylacetat hinzugefügt und die Reaktionsmischung mit gesätt. NH4CI-Lösung gewaschen. Die organische Phase wurde getrocknet und das Lösungsmittel im Vakuum entfernt. Aus dem Rückstand wurde nach Chromatographie an Kieselgel (Cyclohexan: Ethylacetat 10:1-4:1 ) 60 mg der Titelverbindung (threo/erythro-Verhältnis 3:1 ) erhalten.
Tabelle I: Verbindungen der Formel I:
Anwendungsbeispiele
Die herbizide Wirkung der Verbindungen der Formel I ließ sich durch Gewächshaus- versuche zeigen:
Als Kulturgefäße dienten Plastiktöpfe mit lehmigem Sand mit etwa 3,0% Humus als Substrat. Die Samen der Testpflanzen wurden nach Arten getrennt eingesät. Bei Vorauflaufbehandlung wurden die in Wasser suspendierten oder emulgierten Wirkstoffe direkt nach Einsaat mittels fein verteilender Düsen aufgebracht. Die Gefäße wurden leicht beregnet, um Keimung und Wachstum zu fördern, und anschließend mit durchsichtigen Plastikhauben abgedeckt, bis die Pflanzen angewachsen waren. Diese Abdeckung bewirkt ein gleichmäßiges Keimen der Testpflanzen, sofern dies nicht durch die Wirkstoffe beeinträchtigt wurde.
Zum Zweck der Nachauflaufbehandlung wurden die Testpflanzen je nach Wuchsform erst bis zu einer Wuchshöhe von 3 bis 15 cm angezogen und dann mit den in Wasser suspendierten oder emulgierten Wirkstoffen behandelt. Die Testpflanzen wur- den dafür entweder direkt gesät und in den gleichen Gefäßen aufgezogen oder sie wurden erst als Keimpflanzen getrennt angezogen und einige Tage vor der Behandlung in die Versuchsgefäße verpflanzt.
Die Pflanzen wurden artenspezifisch bei Temperaturen von 10 - 25°C bzw. 20 - 35°C gehalten. Die Versuchsperiode erstreckte sich über 2 bis 4 Wochen. Während dieser Zeit wurden die Pflanzen gepflegt, und ihre Reaktion auf die einzelnen Behandlungen wurde ausgewertet.
Bewertet wurde nach einer Skala von O bis 100. Dabei bedeutet 100 kein Aufgang der Pflanzen bzw. völlige Zerstörung zumindest der oberirdischen Teile und 0 keine Schädigung oder normaler Wachstumsverlauf. Eine gute herbizide Aktivität ist bei Werten von wenigstens 70 und eine sehr gute herbizide Aktivität ist bei Werten von wenigstens 85 gegeben.
1 ) Der Wirkstoff 1-105 zeigte bei einer Aufwandmenge von 0,125 kg/ha im Nachauf- lauf gegen ALOMY eine gute und die Wirkstoffe I-94, I-99, 1-1 14, 1-1 19, 1-120, bzw. I-
121 eine sehr gute herbizide Wirkung.
2) Der Wirkstoff 1-100 zeigte bei einer Aufwandmenge von 0,25 kg/ha im Nachauflauf gegen ALOMY eine gute und die Wirkstoffe I-87, I-88, I-89, 1-101 , 1-102, 1-174, I-224, I- 226, I-227, bzw. I-228 eine sehr gute herbizide Wirkung.
3) Die Wirkstoffe I-32, I-94, I-96, 1-106, 1-107, 1-108, 1-109, 1-1 10, 1-1 12, 1-1 13, 1-122, 1-124, bzw. 1-192 zeigten bei einer Aufwandmenge von 0,125 kg/ha im Nachauflauf gegen AMARE eine sehr gute herbizide Wirkung.
4) Die Wirkstoffe 1-176, bzw. I-223 zeigten bei einer Aufwandmenge von 0,13 kg/ha im Nachauflauf gegen AMARE eine sehr gute herbizide Wirkung.
5) Die Wirkstoffe I-79, I-87, I-88, I-89, 1-125, 1-126, 1-173, 1-175, 1-178, 1-182, 1-183, I-
184, 1-197, I-205, I-206, I-207, I-208, I-209, 1-210, 1-211 , 1-212, 1-213, 1-214, 1-215, I- 216, 1-217, 1-218, 1-219, I-220, 1-221 , I-222, bzw. I-244 zeigten bei einer Aufwandmenge von 0,25 kg/ha im Nachauflauf gegen AMARE eine sehr gute herbizide Wirkung.
6) Die Wirkstoffe I-76, I-99, 1-100, 1-114, 1-144, 1-150, 1-151 , 1-152, 1-153, 1-154, 1-155, 1-156, 1-159, bzw. 1-171 zeigten bei einer Aufwandmenge von 0,125 kg/ha im Nachauflauf gegen AVEFA eine sehr gute herbizide Wirkung.
7) Die Wirkstoffe 1-160, bzw. 1-161 zeigten bei einer Aufwandmenge von 0,13 kg/ha im Nachauflauf gegen AVEFA eine sehr gute herbizide Wirkung.
8) Die Wirkstoffe I-95, 1-101 , 1-125, 1-130, 1-143, 1-164, 1-165, 1-166, 1-167, 1-168, I- 169, 1-170, 1-172, 1-179, 1-180, 1-181 , 1-182, 1-183, 1-184, 1-196, 1-197, I-222, I-224, I-
226, I-227, I-228, bzw. I-244 zeigten bei einer Aufwandmenge von 0,25 kg/ha im Nachauflauf gegen AVEFA eine sehr gute herbizide Wirkung.
9) Die Wirkstoffe 1-110, bzw. 1-121 zeigten bei einer Aufwandmenge von 0,125 kg/ha im Nachauflauf gegen SETVI eine sehr gute herbizide Wirkung.
10) Die Wirkstoffe 1-1 18, bzw. 1-154 zeigten bei einer Aufwandmenge von 0, 125 kg/ha im Nachauflauf gegen POLCO eine gute und die Wirkstoffe I-32, I-76, I-94, I-96,
1-105, 1-106, 1-107, 1-108, 1-109, 1-112, 1-113, 1-119, 1-120, 1-122, 1-124, 1-144, 1-150, I- 151 , 1-152, 1-153, 1-155, 1-156, 1-159, 1-171 , bzw. 1-192 eine sehr gute herbizide Wirkung.
1 1 ) Die Wirkstoffe 1-160, 1-161 , 1-176, bzw. I-223 zeigten bei einer Aufwandmenge von 0,13 kg/ha im Nachauflauf gegen POLCO eine sehr gute herbizide Wirkung.
12) Die Wirkstoffe I-87, I-95, 1-130, 1-215, bzw. 1-216 zeigten bei einer Aufwandmenge von 0,25 kg/ha im Nachauflauf gegen POLCO eine gute und die Wirkstoffe I-79, I-88, 1-102, 1-126, 1-143, 1-164, 1-165, 1-166, 1-167, 1-168, 1-169, 1-170, 1-172, 1-173, I- 174, 1-175, 1-178, 1-179, 1-180, 1-181 , 1-196, I-205, I-206, I-207, I-208, I-209, 1-210, I- 211 , 1-212, 1-213, 1-214, 1-217, 1-218, 1-219, I-220, bzw. 1-221 eine sehr gute herbizide Wirkung.
Claims
1. Cyanobutyrate der Formel I
worin die Variablen folgende Bedeutung haben
R Halogen, Cyano, Nitro, Ci-C4-Alkyl, Ci-C4-Haloalkyl, C2-C6-Alkenyl, C2-C6-
Alkinyl, Z-(Tri-Ci-C4-alkyl)silyl,
R1 Wasserstoff, Z-CN, Ci-C8-Alkyl, Z-C3-C6-Cycloalkyl, Ci-C8-Haloalkyl, C3-C8-
Alkenyl, Z-C3-C6-Cycloalkenyl, C3-C8-Al kinyl, Z-(Tri-Ci-C4-alkyl)silyl, Z-C(=O)-Ra, Z-P(=O)(Ra)2, Z-Phenyl, über C oder N gebundener 3- bis 7- gliedriger monocyclischer oder 9- oder 10-gliedriger bicyclischer gesättigter, ungesättigter oder aromatischer Heterocyclus, enthaltend 1 , 2, 3 oder 4 Heteroatome ausgewählt aus O, N und S, der teilweise oder vollständig durch Gruppen Ra und/oder Rb substituiert sein kann,
Ra Wasserstoff, OH, Ci-C8-Alkyl, Ci-C4-Haloalkyl, Z-C3-C6-Cycloalkyl,
C2-C8-Al kenyl, Z-C5-C6-Cycloalkenyl, C2-C8-Al kinyl, Z-Ci-C6-Alkoxy, Z-Ci-C4-Haloalkoxy, Z-C3-C8-Alkenyloxy, Z-C3-C8-Al kinyloxy, NR1R", C-i-Ce-Alkylsulfonyl, Z-(Tri-Ci-C4-alkyl)silyl, Z-Phenyl, Z-Phenoxy, Z-Phenylamino und 5- oder 6-gliedriger monocyclischer oder 9- oder 10-gliedriger bicyclischer Heterocyclus, enthaltend 1 , 2, 3 oder 4 Heteroatome ausgewählt aus O, N und S, wobei die cyclischen Gruppen unsubstituiert oder durch 1 , 2, 3 oder 4 Gruppen Rb substituiert sind, bedeutet;
R1, R" unabhängig voneinander Wasserstoff, Ci-C8-Alkyl, Ci-C4-HaIo- alkyl, C3-C8-Al kenyl, C3-C8-Al kinyl, Z-C3-C6-Cycloalkyl, Z-Ci-C8-
Alkoxy, Z-Ci-C8-Haloalkoxy, Z-C(=O)-RA, wobei RA OH oder d- C4-Alkoxy bedeutet;
R1 und R" können auch gemeinsam mit dem N-Atom, an das sie gebunden sind, einen 5- oder θ-gliedrigen monocyclischen oder 9- oder 10-gliedrigen bicyclischer Heterocyclus bilden, enthaltend 1 , 2, 3 oder 4 Heteroatome ausgewählt aus O, N und S;
Rb unabhängig voneinander Z-CN, Z-OH, Z-NO2, Z-Halogen, d- C8-Alkyl, Ci-C4-Haloalkyl, C2-C8-Alkenyl, C2-C8-Al kinyl, Z-Ci-C8- Alkoxy, Z-Ci-C8-Haloalkoxy, Z-C3-Cio-Cycloalkyl, 0-Z-C3-Ci0- Cycloalkyl, Z-C(=O)-Ra, NR1R", Z-(Tri-Ci-C4-alkyl)silyl, Z-Phenyl und S(O)mRbb, wobei
Rbb Ci-C8-Alkyl und d-Ce-Haloalkyl bedeutet;
m 0, 1 oder 2;
Rb kann auch gemeinsam mit der an das benachbarte C-Atom gebundene Gruppe Rb einen fünf- oder sechsgliedrigen gesättigten, teilweise oder vollständig ungesättigten Ring bilden, der neben Kohlenstoff- 1 , 2 oder 3 Heteroatome ausgewählt aus O, N und S enthalten kann;
Z eine kovalente Bindung oder Ci-Cs-Alkylen;
n 0, 1 , 2, 3, 4 oder 5;
R2, R3 unabhängig voneinander Halogen, Cyano, Nitro, Ci-C4-AIkVl, CrC4-AIkOXy,
S(O)mRbb, NR1R", Ci-C4-Halogenalkyl, Ci-C4-Halogenalkoxy;
R2 und R3 können auch gemeinsam einen fünf- oder sechsgliedrigen gesättigten, teilweise oder vollständig ungesättigten mono- oder bicyclischen Ring bilden, der neben Kohlenstoff- 1 , 2 oder 3 Heteroatome ausgewählt aus O, N und S enthalten kann und durch Gruppen Rb substituiert sein kann;
wobei in Gruppen R und R1 und deren Untersubstituenten die Kohlenstoffketten und/oder die cyclischen Gruppen teilweise oder vollständig durch Gruppen Ra und/oder Rb substituiert sein können,
mit der Maßgabe, dass nicht beide R2 und R3 Chlor bedeuten, wenn R Wasserstoff und R1 Ethyl oder AIIyI bedeutet;
sowie deren N-Oxide und landwirtschaftlich geeignete Salze.
2. Verbindungen der Formel I gemäß Anspruch 1 , worin R2 und R3 nicht gemeinsam einen Ring bilden.
3. Verbindungen der Formel I gemäß Anspruch 1 oder 2, worin R2 und R3 nicht beide Chlor bedeuten, wenn R Wasserstoff bedeutet.
4. Verbindungen der Formel I gemäß Anspruch 1 oder 2, worin R2 und R3 nicht beide Chlor bedeuten, wenn R Methyl bedeutet.
5. Verbindungen der Formel I gemäß einem der Ansprüche 1 bis 4, worin R2 und R3 nicht beide Chlor bedeuten.
6. Verbindungen der Formel I gemäß einem der Ansprüche 1 bis 5, worin R2 und R3 für 2,3-F2; 2-F.3-CI; 2-F,3-Br; 2-F,3-CN; 2-F,3-NO2; 2-F,3-CF3; 2-F,3-OCH3 oder 2-CI.3-F stehen.
7. Verbindungen der Formel I gemäß einem der Ansprüche 1 bis 6, worin R2 Fluor bedeutet.
8. Verbindungen der Formel I gemäß einem der Ansprüche 1 bis 7, worin R2 und R3 Fluor bedeuten.
9. Verbindungen der Formel I gemäß einem der Ansprüche 1 bis 8, worin R Chlor, Fluor, Cyano oder Nitro bedeutet und der Index n den Wert 1 oder 2 hat.
10. Verbindungen der Formel I gemäß einem der Ansprüche 1 bis 9, worin Rn für 3-F; 3,4-F2; 3,5-F2; 3,4,5-F3; 3-F.4-CI; 4-CI; 4-F oder 3-CN steht.
1 1. Verbindungen der Formel I gemäß einem der Ansprüche 1 bis 10, worin R Fluor bedeutet und der Index n den Wert 1 hat.
12. Verbindungen der Formel I gemäß einem der Ansprüche 1 bis 11 , worin R1 für H, CH3, C2H5, CH2CN, CH2CH2F, CH2CHF2, CH2CF3, CH2OCH3 oder CH2C≡ CH steht.
13. Verbindungen der Formel I gemäß einem der Ansprüche 1 bis 12, worin R1 für CH3 steht.
14. Mittel, enthaltend eine herbizid wirksame Menge mindestens einer Cyanobutyrat- verbindung der Formel I oder eines landwirtschaftlich geeigneten Salzes davon nach einem der Ansprüche 1 bis 13 und für die Formulierung von Pflanzenschutzmitteln übliche Hilfsmittel.
15. Verfahren zur Bekämpfung von unerwünschtem Pflanzenwuchs, dadurch gekennzeichnet, dass man eine herbizid wirksame Menge mindestens einer Cya- nobutyratverbindung der Formel I oder eines landwirtschaftlich brauchbaren Salzes davon nach einem der Ansprüche 1 bis 13 auf Pflanzen, deren Samen und/oder deren Lebensraum einwirken lässt.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP09165071 | 2009-07-09 | ||
| EP09165071.3 | 2009-07-09 | ||
| EP09180018.5 | 2009-12-18 | ||
| EP09180018 | 2009-12-18 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2011003776A2 true WO2011003776A2 (de) | 2011-01-13 |
| WO2011003776A3 WO2011003776A3 (de) | 2011-04-21 |
Family
ID=43242373
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2010/059185 WO2011003776A2 (de) | 2009-07-09 | 2010-06-29 | Substituierte cyanobutyrate mit herbizider wirkung |
Country Status (4)
| Country | Link |
|---|---|
| AR (2) | AR079401A1 (de) |
| TW (2) | TW201127284A (de) |
| UY (2) | UY32779A (de) |
| WO (1) | WO2011003776A2 (de) |
Cited By (47)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2474226A1 (de) * | 2011-01-07 | 2012-07-11 | Basf Se | Herbizid wirksame Zusammensetzung, die Cyanobutyrate umfasst |
| WO2012126765A1 (de) | 2011-03-18 | 2012-09-27 | Bayer Cropscience Ag | Substituierte (3r,4r)-4-cyan-3,4-diphenylbutanoate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| WO2012126764A1 (de) | 2011-03-18 | 2012-09-27 | Bayer Cropscience Ag | Substituierte 4-cyan-3-(2,6-difluorphenyl)-4-phenylbutanoate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| WO2013010882A2 (de) | 2011-07-15 | 2013-01-24 | Bayer Intellectual Property Gmbh | 2,3-diphenyl-valeronitrilderivate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| WO2013039990A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040021A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040033A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040116A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040005A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040117A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040057A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040049A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013064462A1 (de) | 2011-10-31 | 2013-05-10 | Bayer Intellectual Property Gmbh | Substituierte 4-cyan-3-phenyl-4-(pyridin-3-yl)butanoate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| WO2013092500A1 (de) | 2011-12-19 | 2013-06-27 | Bayer Intellectual Property Gmbh | Substituierte 4-cyan-3-phenyl-4-(pyridin-3-yl)butanoate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| WO2014151255A1 (en) | 2013-03-15 | 2014-09-25 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2014195253A1 (en) | 2013-06-07 | 2014-12-11 | Bayer Cropscience Ag | Substituted 5-hydroxy-2,3-diphenylpentanonitrile derivatives, processes for their preparation and their use as herbicides and/or plant growth regulators |
| WO2015108982A2 (en) | 2014-01-15 | 2015-07-23 | Monsanto Technology Llc | Methods and compositions for weed control using epsps polynucleotides |
| US9121022B2 (en) | 2010-03-08 | 2015-09-01 | Monsanto Technology Llc | Method for controlling herbicide-resistant plants |
| WO2016001204A1 (de) | 2014-07-04 | 2016-01-07 | Bayer Cropscience Ag | Substituierte 5-hydroxy-2-heteroaryl-3-phenylpentanonitrilderivate, verfahren zu deren herstellung und deren verwendung als herbizide und/oder pflanzenwachstumsregulatoren |
| JP2016506400A (ja) * | 2012-12-21 | 2016-03-03 | バイエル・クロップサイエンス・アクチェンゲゼルシャフト | 置換4−シアン−3−(ピリジル)−4−フェニルブタノエート類、それらを製造する方法、並びに、除草剤及び植物成長調節剤としての使用 |
| US9540642B2 (en) | 2013-11-04 | 2017-01-10 | The United States Of America, As Represented By The Secretary Of Agriculture | Compositions and methods for controlling arthropod parasite and pest infestations |
| US9777288B2 (en) | 2013-07-19 | 2017-10-03 | Monsanto Technology Llc | Compositions and methods for controlling leptinotarsa |
| US9840715B1 (en) | 2011-09-13 | 2017-12-12 | Monsanto Technology Llc | Methods and compositions for delaying senescence and improving disease tolerance and yield in plants |
| US9850496B2 (en) | 2013-07-19 | 2017-12-26 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US9920326B1 (en) | 2011-09-14 | 2018-03-20 | Monsanto Technology Llc | Methods and compositions for increasing invertase activity in plants |
| US10000767B2 (en) | 2013-01-28 | 2018-06-19 | Monsanto Technology Llc | Methods and compositions for plant pest control |
| US10041068B2 (en) | 2013-01-01 | 2018-08-07 | A. B. Seeds Ltd. | Isolated dsRNA molecules and methods of using same for silencing target molecules of interest |
| US10077451B2 (en) | 2012-10-18 | 2018-09-18 | Monsanto Technology Llc | Methods and compositions for plant pest control |
| US10172350B2 (en) | 2014-10-08 | 2019-01-08 | Bayer Cropscience Aktiengesellschaft | Substituted 5-hydroxy-2-phenyl-3-heteroaryl pentanenitrile derivatives, method for the production thereof and use thereof as herbicides and/or plant growth regulators |
| US10240161B2 (en) | 2012-05-24 | 2019-03-26 | A.B. Seeds Ltd. | Compositions and methods for silencing gene expression |
| US10378012B2 (en) | 2014-07-29 | 2019-08-13 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| US10435701B2 (en) | 2013-03-14 | 2019-10-08 | Monsanto Technology Llc | Methods and compositions for plant pest control |
| US10557138B2 (en) | 2013-12-10 | 2020-02-11 | Beeologics, Inc. | Compositions and methods for virus control in Varroa mite and bees |
| US10609930B2 (en) | 2013-03-13 | 2020-04-07 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10612019B2 (en) | 2013-03-13 | 2020-04-07 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10655136B2 (en) | 2015-06-03 | 2020-05-19 | Monsanto Technology Llc | Methods and compositions for introducing nucleic acids into plants |
| US10683505B2 (en) | 2013-01-01 | 2020-06-16 | Monsanto Technology Llc | Methods of introducing dsRNA to plant seeds for modulating gene expression |
| US10760086B2 (en) | 2011-09-13 | 2020-09-01 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10801028B2 (en) | 2009-10-14 | 2020-10-13 | Beeologics Inc. | Compositions for controlling Varroa mites in bees |
| US10806146B2 (en) | 2011-09-13 | 2020-10-20 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10829828B2 (en) | 2011-09-13 | 2020-11-10 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10883103B2 (en) | 2015-06-02 | 2021-01-05 | Monsanto Technology Llc | Compositions and methods for delivery of a polynucleotide into a plant |
| US10888579B2 (en) | 2007-11-07 | 2021-01-12 | Beeologics Inc. | Compositions for conferring tolerance to viral disease in social insects, and the use thereof |
| US10968449B2 (en) | 2015-01-22 | 2021-04-06 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US10988764B2 (en) | 2014-06-23 | 2021-04-27 | Monsanto Technology Llc | Compositions and methods for regulating gene expression via RNA interference |
| US11091770B2 (en) | 2014-04-01 | 2021-08-17 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| US11807857B2 (en) | 2014-06-25 | 2023-11-07 | Monsanto Technology Llc | Methods and compositions for delivering nucleic acids to plant cells and regulating gene expression |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113215172B (zh) * | 2021-04-29 | 2022-08-16 | 吉林农业大学 | 雄性不育基因MsJMT及其应用 |
Citations (38)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0005341A2 (de) | 1978-05-05 | 1979-11-14 | American Cyanamid Company | Polysubstituierte Butansäuren, deren Ester und Derivate verwendbar als Herbizide, diese enthaltende Zusammensetzungen und deren Verwendung |
| EP0242236A1 (de) | 1986-03-11 | 1987-10-21 | Plant Genetic Systems N.V. | Durch Gentechnologie erhaltene und gegen Glutaminsynthetase-Inhibitoren resistente Pflanzenzellen |
| EP0257993A2 (de) | 1986-08-26 | 1988-03-02 | E.I. Du Pont De Nemours And Company | Herbizid-resistante Pflanzen-Acetolactatsynthase kodierendes Nucleinsäurefragment |
| EP0266725A1 (de) | 1986-11-06 | 1988-05-11 | American Cyanamid Company | 4-Cyano-4 (Fluorophenyl)-3-(substituiertes Phenyl)-butansäuren, deren Ester und Derivate und Methode zur selektiven Kontrolle von unerwünschter Vegetation in Reiskulturen |
| EP0270830A1 (de) | 1986-11-06 | 1988-06-15 | American Cyanamid Company | Verfahren zur Regulierung des Pflanzenwachstums mit polysubstituierten Butansäuren, deren Ester und Derivate |
| EP0374753A2 (de) | 1988-12-19 | 1990-06-27 | American Cyanamid Company | Insektizide Toxine, Gene, die diese Toxine kodieren, Antikörper, die sie binden, sowie transgene Pflanzenzellen und transgene Pflanzen, die diese Toxine exprimieren |
| EP0392225A2 (de) | 1989-03-24 | 1990-10-17 | Ciba-Geigy Ag | Krankheitsresistente transgene Pflanze |
| US5013659A (en) | 1987-07-27 | 1991-05-07 | E. I. Du Pont De Nemours And Company | Nucleic acid fragment encoding herbicide resistant plant acetolactate synthase |
| EP0427529A1 (de) | 1989-11-07 | 1991-05-15 | Pioneer Hi-Bred International, Inc. | Larven abtötende Lektine und darauf beruhende Pflanzenresistenz gegen Insekten |
| EP0451878A1 (de) | 1985-01-18 | 1991-10-16 | Plant Genetic Systems, N.V. | Modifizierung von Pflanzen mittels gentechnologischer Verfahren, um Insekten zu bekämpfen oder zu kontrollieren |
| WO1992000377A1 (en) | 1990-06-25 | 1992-01-09 | Monsanto Company | Glyphosate tolerant plants |
| JPH04297454A (ja) | 1991-03-27 | 1992-10-21 | Hokko Chem Ind Co Ltd | 4−(置換フェニル)−3−(複素環)酪酸誘導体および除草剤 |
| JPH04297455A (ja) | 1991-03-27 | 1992-10-21 | Hokko Chem Ind Co Ltd | 4−複素環−3−(置換フェニル)酪酸誘導体および除草剤 |
| JPH0558979A (ja) | 1991-08-28 | 1993-03-09 | Hokko Chem Ind Co Ltd | 3,4−ジ(置換フエニル)酪酸誘導体および除草剤 |
| WO1993007278A1 (en) | 1991-10-04 | 1993-04-15 | Ciba-Geigy Ag | Synthetic dna sequence having enhanced insecticidal activity in maize |
| WO1995034656A1 (en) | 1994-06-10 | 1995-12-21 | Ciba-Geigy Ag | Novel bacillus thuringiensis genes coding toxins active against lepidopteran pests |
| WO1996026202A1 (de) | 1995-02-21 | 1996-08-29 | Degussa Aktiengesellschaft | Verfahren zur herstellung von thietanonen |
| US5559024A (en) | 1988-03-23 | 1996-09-24 | Rhone-Poulenc Agrochimie | Chimeric nitrilase-encoding gene for herbicidal resistance |
| WO1997041116A1 (fr) | 1996-04-26 | 1997-11-06 | Nippon Soda Co., Ltd. | Derives du benzene substitues par des heterocycles, et herbicides |
| WO1997041117A1 (fr) | 1996-04-26 | 1997-11-06 | Nippon Soda Co., Ltd. | Nouveaux derives du benzene substitues par des heterocycles, et herbicides |
| WO1997041118A1 (fr) | 1996-04-26 | 1997-11-06 | Nippon Soda Co., Ltd. | Derives du benzene substitues par des heterocycles, et herbicides |
| WO1997041218A1 (en) | 1996-04-29 | 1997-11-06 | Board Of Supervisors Of Louisiana State University And Agricultural And Mechanical College | Herbicide resistant rice |
| WO1998002527A1 (en) | 1996-07-17 | 1998-01-22 | Michigan State University | Imidazolinone herbicide resistant sugar beet plants |
| WO1998002526A1 (en) | 1996-07-17 | 1998-01-22 | Michigan State University | Imidazolinone herbicide resistant sugar beet plants |
| WO2000026390A2 (en) | 1998-10-29 | 2000-05-11 | American Cyanamid Company | Genes and vectors for conferring herbicide resistance in plants |
| US6222100B1 (en) | 1984-03-06 | 2001-04-24 | Mgi Pharma, Inc. | Herbicide resistance in plants |
| WO2001083459A2 (en) | 2000-05-04 | 2001-11-08 | Basf Aktiengesellschaft | Uracil substituted phenyl sulfamoyl carboxamides |
| WO2001082685A1 (en) | 2000-04-28 | 2001-11-08 | Basf Aktiengesellschaft | Use of the maize x112 mutant ahas 2 gene and imidazolinone herbicides for selection of transgenic monocots, maize, rice and wheat plants resistant to the imidazolinone herbicides |
| WO2002015701A2 (en) | 2000-08-25 | 2002-02-28 | Syngenta Participations Ag | Bacillus thuringiensis crystal protein hybrids |
| WO2003014357A1 (en) | 2001-08-09 | 2003-02-20 | University Of Saskatchewan | Wheat plants having increased resistance to imidazolinone herbicides |
| WO2003013225A2 (en) | 2001-08-09 | 2003-02-20 | Northwest Plant Breeding Company | Wheat plants having increased resistance to imidazolinone herbicides |
| WO2003014356A1 (en) | 2001-08-09 | 2003-02-20 | University Of Saskatchewan | Wheat plants having increased resistance to imidazolinone herbicides |
| WO2003018810A2 (en) | 2001-08-31 | 2003-03-06 | Syngenta Participations Ag | Modified cry3a toxins and nucleic acid sequences coding therefor |
| WO2003052073A2 (en) | 2001-12-17 | 2003-06-26 | Syngenta Participations Ag | Novel corn event |
| WO2004016073A2 (en) | 2002-07-10 | 2004-02-26 | The Department Of Agriculture, Western Australia | Wheat plants having increased resistance to imidazolinone herbicides |
| WO2004106529A2 (en) | 2003-05-28 | 2004-12-09 | Basf Aktiengesellschaft | Wheat plants having increased tolerance to imidazolinone herbicides |
| WO2005020673A1 (en) | 2003-08-29 | 2005-03-10 | Instituto Nacional De Technologia Agropecuaria | Rice plants having increased tolerance to imidazolinone herbicides |
| WO2008074991A1 (en) | 2006-12-21 | 2008-06-26 | Syngenta Limited | Novel herbicides |
-
2010
- 2010-06-29 WO PCT/EP2010/059185 patent/WO2011003776A2/de active Application Filing
- 2010-07-08 UY UY0001032779A patent/UY32779A/es unknown
- 2010-07-08 UY UY32777A patent/UY32777A/es unknown
- 2010-07-08 AR ARP100102499 patent/AR079401A1/es unknown
- 2010-07-08 AR ARP100102498 patent/AR079400A1/es unknown
- 2010-07-08 TW TW99122539A patent/TW201127284A/zh unknown
- 2010-07-08 TW TW99122541A patent/TW201105235A/zh unknown
Patent Citations (39)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0005341A2 (de) | 1978-05-05 | 1979-11-14 | American Cyanamid Company | Polysubstituierte Butansäuren, deren Ester und Derivate verwendbar als Herbizide, diese enthaltende Zusammensetzungen und deren Verwendung |
| US6222100B1 (en) | 1984-03-06 | 2001-04-24 | Mgi Pharma, Inc. | Herbicide resistance in plants |
| EP0451878A1 (de) | 1985-01-18 | 1991-10-16 | Plant Genetic Systems, N.V. | Modifizierung von Pflanzen mittels gentechnologischer Verfahren, um Insekten zu bekämpfen oder zu kontrollieren |
| EP0242236A1 (de) | 1986-03-11 | 1987-10-21 | Plant Genetic Systems N.V. | Durch Gentechnologie erhaltene und gegen Glutaminsynthetase-Inhibitoren resistente Pflanzenzellen |
| EP0242246A1 (de) | 1986-03-11 | 1987-10-21 | Plant Genetic Systems N.V. | Durch Gentechnologie erhaltene und gegen Glutaminsynthetase-Inhibitoren resistente Pflanzenzellen |
| EP0257993A2 (de) | 1986-08-26 | 1988-03-02 | E.I. Du Pont De Nemours And Company | Herbizid-resistante Pflanzen-Acetolactatsynthase kodierendes Nucleinsäurefragment |
| EP0266725A1 (de) | 1986-11-06 | 1988-05-11 | American Cyanamid Company | 4-Cyano-4 (Fluorophenyl)-3-(substituiertes Phenyl)-butansäuren, deren Ester und Derivate und Methode zur selektiven Kontrolle von unerwünschter Vegetation in Reiskulturen |
| EP0270830A1 (de) | 1986-11-06 | 1988-06-15 | American Cyanamid Company | Verfahren zur Regulierung des Pflanzenwachstums mit polysubstituierten Butansäuren, deren Ester und Derivate |
| US5013659A (en) | 1987-07-27 | 1991-05-07 | E. I. Du Pont De Nemours And Company | Nucleic acid fragment encoding herbicide resistant plant acetolactate synthase |
| US5559024A (en) | 1988-03-23 | 1996-09-24 | Rhone-Poulenc Agrochimie | Chimeric nitrilase-encoding gene for herbicidal resistance |
| EP0374753A2 (de) | 1988-12-19 | 1990-06-27 | American Cyanamid Company | Insektizide Toxine, Gene, die diese Toxine kodieren, Antikörper, die sie binden, sowie transgene Pflanzenzellen und transgene Pflanzen, die diese Toxine exprimieren |
| EP0392225A2 (de) | 1989-03-24 | 1990-10-17 | Ciba-Geigy Ag | Krankheitsresistente transgene Pflanze |
| EP0427529A1 (de) | 1989-11-07 | 1991-05-15 | Pioneer Hi-Bred International, Inc. | Larven abtötende Lektine und darauf beruhende Pflanzenresistenz gegen Insekten |
| WO1992000377A1 (en) | 1990-06-25 | 1992-01-09 | Monsanto Company | Glyphosate tolerant plants |
| JPH04297455A (ja) | 1991-03-27 | 1992-10-21 | Hokko Chem Ind Co Ltd | 4−複素環−3−(置換フェニル)酪酸誘導体および除草剤 |
| JPH04297454A (ja) | 1991-03-27 | 1992-10-21 | Hokko Chem Ind Co Ltd | 4−(置換フェニル)−3−(複素環)酪酸誘導体および除草剤 |
| JPH0558979A (ja) | 1991-08-28 | 1993-03-09 | Hokko Chem Ind Co Ltd | 3,4−ジ(置換フエニル)酪酸誘導体および除草剤 |
| WO1993007278A1 (en) | 1991-10-04 | 1993-04-15 | Ciba-Geigy Ag | Synthetic dna sequence having enhanced insecticidal activity in maize |
| WO1995034656A1 (en) | 1994-06-10 | 1995-12-21 | Ciba-Geigy Ag | Novel bacillus thuringiensis genes coding toxins active against lepidopteran pests |
| WO1996026202A1 (de) | 1995-02-21 | 1996-08-29 | Degussa Aktiengesellschaft | Verfahren zur herstellung von thietanonen |
| WO1997041116A1 (fr) | 1996-04-26 | 1997-11-06 | Nippon Soda Co., Ltd. | Derives du benzene substitues par des heterocycles, et herbicides |
| WO1997041118A1 (fr) | 1996-04-26 | 1997-11-06 | Nippon Soda Co., Ltd. | Derives du benzene substitues par des heterocycles, et herbicides |
| WO1997041117A1 (fr) | 1996-04-26 | 1997-11-06 | Nippon Soda Co., Ltd. | Nouveaux derives du benzene substitues par des heterocycles, et herbicides |
| WO1997041218A1 (en) | 1996-04-29 | 1997-11-06 | Board Of Supervisors Of Louisiana State University And Agricultural And Mechanical College | Herbicide resistant rice |
| WO1998002527A1 (en) | 1996-07-17 | 1998-01-22 | Michigan State University | Imidazolinone herbicide resistant sugar beet plants |
| WO1998002526A1 (en) | 1996-07-17 | 1998-01-22 | Michigan State University | Imidazolinone herbicide resistant sugar beet plants |
| WO2000026390A2 (en) | 1998-10-29 | 2000-05-11 | American Cyanamid Company | Genes and vectors for conferring herbicide resistance in plants |
| WO2001082685A1 (en) | 2000-04-28 | 2001-11-08 | Basf Aktiengesellschaft | Use of the maize x112 mutant ahas 2 gene and imidazolinone herbicides for selection of transgenic monocots, maize, rice and wheat plants resistant to the imidazolinone herbicides |
| WO2001083459A2 (en) | 2000-05-04 | 2001-11-08 | Basf Aktiengesellschaft | Uracil substituted phenyl sulfamoyl carboxamides |
| WO2002015701A2 (en) | 2000-08-25 | 2002-02-28 | Syngenta Participations Ag | Bacillus thuringiensis crystal protein hybrids |
| WO2003014357A1 (en) | 2001-08-09 | 2003-02-20 | University Of Saskatchewan | Wheat plants having increased resistance to imidazolinone herbicides |
| WO2003013225A2 (en) | 2001-08-09 | 2003-02-20 | Northwest Plant Breeding Company | Wheat plants having increased resistance to imidazolinone herbicides |
| WO2003014356A1 (en) | 2001-08-09 | 2003-02-20 | University Of Saskatchewan | Wheat plants having increased resistance to imidazolinone herbicides |
| WO2003018810A2 (en) | 2001-08-31 | 2003-03-06 | Syngenta Participations Ag | Modified cry3a toxins and nucleic acid sequences coding therefor |
| WO2003052073A2 (en) | 2001-12-17 | 2003-06-26 | Syngenta Participations Ag | Novel corn event |
| WO2004016073A2 (en) | 2002-07-10 | 2004-02-26 | The Department Of Agriculture, Western Australia | Wheat plants having increased resistance to imidazolinone herbicides |
| WO2004106529A2 (en) | 2003-05-28 | 2004-12-09 | Basf Aktiengesellschaft | Wheat plants having increased tolerance to imidazolinone herbicides |
| WO2005020673A1 (en) | 2003-08-29 | 2005-03-10 | Instituto Nacional De Technologia Agropecuaria | Rice plants having increased tolerance to imidazolinone herbicides |
| WO2008074991A1 (en) | 2006-12-21 | 2008-06-26 | Syngenta Limited | Novel herbicides |
Non-Patent Citations (2)
| Title |
|---|
| J. AM. CHEM. SOC., vol. 129, no. 43, 2007, pages 13321 |
| J. ORG. CHEM., vol. 49, no. 22, 1984, pages 4287 |
Cited By (82)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10888579B2 (en) | 2007-11-07 | 2021-01-12 | Beeologics Inc. | Compositions for conferring tolerance to viral disease in social insects, and the use thereof |
| US10801028B2 (en) | 2009-10-14 | 2020-10-13 | Beeologics Inc. | Compositions for controlling Varroa mites in bees |
| US9121022B2 (en) | 2010-03-08 | 2015-09-01 | Monsanto Technology Llc | Method for controlling herbicide-resistant plants |
| US11812738B2 (en) | 2010-03-08 | 2023-11-14 | Monsanto Technology Llc | Polynucleotide molecules for gene regulation in plants |
| US9988634B2 (en) | 2010-03-08 | 2018-06-05 | Monsanto Technology Llc | Polynucleotide molecules for gene regulation in plants |
| EP2474226A1 (de) * | 2011-01-07 | 2012-07-11 | Basf Se | Herbizid wirksame Zusammensetzung, die Cyanobutyrate umfasst |
| WO2012126765A1 (de) | 2011-03-18 | 2012-09-27 | Bayer Cropscience Ag | Substituierte (3r,4r)-4-cyan-3,4-diphenylbutanoate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| WO2012126764A1 (de) | 2011-03-18 | 2012-09-27 | Bayer Cropscience Ag | Substituierte 4-cyan-3-(2,6-difluorphenyl)-4-phenylbutanoate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| JP2014516920A (ja) * | 2011-03-18 | 2014-07-17 | バイエル・インテレクチユアル・プロパテイー・ゲー・エム・ベー・ハー | 置換された(3r,4r)−4−シアノ−3,4−ジフェニルブタノエート類、それらの製造方法、ならびに除草剤および植物成長調節剤としてのそれらの使用 |
| US9049863B2 (en) | 2011-03-18 | 2015-06-09 | Bayer Intellectual Property Gmbh | Substituted (3R,4R)-4-cyan-3,4-diphenylbutanoates, method for the production thereof and use thereof as herbicides and plant growth regulators |
| WO2013010882A2 (de) | 2011-07-15 | 2013-01-24 | Bayer Intellectual Property Gmbh | 2,3-diphenyl-valeronitrilderivate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| US9084425B2 (en) | 2011-07-15 | 2015-07-21 | Bayer Intellectual Property Gmbh | 2,3-diphenyl-valeronitrile derivatives, method for the production thereof and use thereof as herbicides and plant growth regulators |
| WO2013010882A3 (de) * | 2011-07-15 | 2013-04-11 | Bayer Intellectual Property Gmbh | 2,3-diphenyl-valeronitrilderivate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| CN103748075B (zh) * | 2011-07-15 | 2016-09-07 | 拜耳知识产权有限责任公司 | 2,3-二苯基戊腈衍生物、其制备方法及其作为除草剂和植物生长调节剂的用途 |
| CN103748075A (zh) * | 2011-07-15 | 2014-04-23 | 拜耳知识产权有限责任公司 | 2,3-二苯基戊腈衍生物、其制备方法及其作为除草剂和植物生长调节剂的用途 |
| EP3296402A2 (de) | 2011-09-13 | 2018-03-21 | Monsanto Technology LLC | Verfahren und zusammensetzungen zur unkrautbekämpfung |
| US9416363B2 (en) | 2011-09-13 | 2016-08-16 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013039990A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| EP3434779A1 (de) | 2011-09-13 | 2019-01-30 | Monsanto Technology LLC | Verfahren und zusammensetzungen zur unkrautbekämpfung |
| WO2013040005A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10760086B2 (en) | 2011-09-13 | 2020-09-01 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040049A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040021A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040057A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| EP3434780A1 (de) | 2011-09-13 | 2019-01-30 | Monsanto Technology LLC | Verfahren und zusammensetzungen zur unkrautbekämpfung |
| EP3382027A2 (de) | 2011-09-13 | 2018-10-03 | Monsanto Technology LLC | Verfahren und zusammensetzungen zur unkrautbekämpfung |
| WO2013040033A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10829828B2 (en) | 2011-09-13 | 2020-11-10 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040116A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| US9422557B2 (en) | 2011-09-13 | 2016-08-23 | Monsanto Technology Llc | Methods and compositions for weed control |
| US9422558B2 (en) | 2011-09-13 | 2016-08-23 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2013040117A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10808249B2 (en) | 2011-09-13 | 2020-10-20 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10435702B2 (en) | 2011-09-13 | 2019-10-08 | Monsanto Technology Llc | Methods and compositions for delaying senescence and improving disease tolerance and yield in plants |
| US10806146B2 (en) | 2011-09-13 | 2020-10-20 | Monsanto Technology Llc | Methods and compositions for weed control |
| US9840715B1 (en) | 2011-09-13 | 2017-12-12 | Monsanto Technology Llc | Methods and compositions for delaying senescence and improving disease tolerance and yield in plants |
| US10428338B2 (en) | 2011-09-14 | 2019-10-01 | Monsanto Technology Llc | Methods and compositions for increasing invertase activity in plants |
| US9920326B1 (en) | 2011-09-14 | 2018-03-20 | Monsanto Technology Llc | Methods and compositions for increasing invertase activity in plants |
| WO2013064462A1 (de) | 2011-10-31 | 2013-05-10 | Bayer Intellectual Property Gmbh | Substituierte 4-cyan-3-phenyl-4-(pyridin-3-yl)butanoate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| US8975412B2 (en) | 2011-10-31 | 2015-03-10 | Bayer Intellectual Property Gmbh | Substituted 4-cyano-3-phenyl-4-(pyridin-3-yl)butanoates, processes for preparation thereof and use thereof as herbicides and plant growth regulators |
| US9161537B2 (en) | 2011-12-19 | 2015-10-20 | Bayer Intellectual Property Gmbh | Substituted 4-cyan-3-phenyl-4-(pyridine-3-yl)butanoates, processes for preparation thereof and use thereof as herbicides and plant growth regulators |
| WO2013092500A1 (de) | 2011-12-19 | 2013-06-27 | Bayer Intellectual Property Gmbh | Substituierte 4-cyan-3-phenyl-4-(pyridin-3-yl)butanoate, verfahren zu deren herstellung und deren verwendung als herbizide und pflanzenwachstumsregulatoren |
| US10240162B2 (en) | 2012-05-24 | 2019-03-26 | A.B. Seeds Ltd. | Compositions and methods for silencing gene expression |
| US10240161B2 (en) | 2012-05-24 | 2019-03-26 | A.B. Seeds Ltd. | Compositions and methods for silencing gene expression |
| US10934555B2 (en) | 2012-05-24 | 2021-03-02 | Monsanto Technology Llc | Compositions and methods for silencing gene expression |
| US10077451B2 (en) | 2012-10-18 | 2018-09-18 | Monsanto Technology Llc | Methods and compositions for plant pest control |
| US10844398B2 (en) | 2012-10-18 | 2020-11-24 | Monsanto Technology Llc | Methods and compositions for plant pest control |
| US9661848B2 (en) | 2012-12-21 | 2017-05-30 | Bayer Cropscience Ag | Substituted 4-cyan-3-(pyridyl)-4-phenylbutanoates, method for the production thereof and uses as herbicides and plant growth regulators |
| JP2016506400A (ja) * | 2012-12-21 | 2016-03-03 | バイエル・クロップサイエンス・アクチェンゲゼルシャフト | 置換4−シアン−3−(ピリジル)−4−フェニルブタノエート類、それらを製造する方法、並びに、除草剤及び植物成長調節剤としての使用 |
| US10683505B2 (en) | 2013-01-01 | 2020-06-16 | Monsanto Technology Llc | Methods of introducing dsRNA to plant seeds for modulating gene expression |
| US10041068B2 (en) | 2013-01-01 | 2018-08-07 | A. B. Seeds Ltd. | Isolated dsRNA molecules and methods of using same for silencing target molecules of interest |
| US10000767B2 (en) | 2013-01-28 | 2018-06-19 | Monsanto Technology Llc | Methods and compositions for plant pest control |
| US10609930B2 (en) | 2013-03-13 | 2020-04-07 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10612019B2 (en) | 2013-03-13 | 2020-04-07 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10435701B2 (en) | 2013-03-14 | 2019-10-08 | Monsanto Technology Llc | Methods and compositions for plant pest control |
| WO2014151255A1 (en) | 2013-03-15 | 2014-09-25 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10568328B2 (en) | 2013-03-15 | 2020-02-25 | Monsanto Technology Llc | Methods and compositions for weed control |
| WO2014195253A1 (en) | 2013-06-07 | 2014-12-11 | Bayer Cropscience Ag | Substituted 5-hydroxy-2,3-diphenylpentanonitrile derivatives, processes for their preparation and their use as herbicides and/or plant growth regulators |
| JP2016523228A (ja) * | 2013-06-07 | 2016-08-08 | バイエル・クロップサイエンス・アクチェンゲゼルシャフト | 置換された5−ヒドロキシ−2,3−ジフェニルペンタノニトリル誘導体、それの製造方法、ならびにそれの除草剤および/または植物成長調節剤としての使用 |
| US10021877B2 (en) | 2013-06-07 | 2018-07-17 | Bayer Cropscience Aktiengesellschaft | Substituted 5-hydroxy-2,3-diphenylpentanonitrile derivatives, processes for their preparation and their use as herbicides and/or plant growth regulators |
| US9850496B2 (en) | 2013-07-19 | 2017-12-26 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US9856495B2 (en) | 2013-07-19 | 2018-01-02 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US11377667B2 (en) | 2013-07-19 | 2022-07-05 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US9777288B2 (en) | 2013-07-19 | 2017-10-03 | Monsanto Technology Llc | Compositions and methods for controlling leptinotarsa |
| US10597676B2 (en) | 2013-07-19 | 2020-03-24 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US10927374B2 (en) | 2013-11-04 | 2021-02-23 | Monsanto Technology Llc | Compositions and methods for controlling arthropod parasite and pest infestations |
| US10100306B2 (en) | 2013-11-04 | 2018-10-16 | Monsanto Technology Llc | Compositions and methods for controlling arthropod parasite and pest infestations |
| US9540642B2 (en) | 2013-11-04 | 2017-01-10 | The United States Of America, As Represented By The Secretary Of Agriculture | Compositions and methods for controlling arthropod parasite and pest infestations |
| US10557138B2 (en) | 2013-12-10 | 2020-02-11 | Beeologics, Inc. | Compositions and methods for virus control in Varroa mite and bees |
| WO2015108982A2 (en) | 2014-01-15 | 2015-07-23 | Monsanto Technology Llc | Methods and compositions for weed control using epsps polynucleotides |
| US10334848B2 (en) | 2014-01-15 | 2019-07-02 | Monsanto Technology Llc | Methods and compositions for weed control using EPSPS polynucleotides |
| US11091770B2 (en) | 2014-04-01 | 2021-08-17 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| US10988764B2 (en) | 2014-06-23 | 2021-04-27 | Monsanto Technology Llc | Compositions and methods for regulating gene expression via RNA interference |
| US11807857B2 (en) | 2014-06-25 | 2023-11-07 | Monsanto Technology Llc | Methods and compositions for delivering nucleic acids to plant cells and regulating gene expression |
| US9957248B2 (en) | 2014-07-04 | 2018-05-01 | Bayer Cropscience Aktiengesellshaft | Substituted 5-hydroxy-2-heteroaryl-3-phenylpentanonitrile derivatives, processes for their preparation and their use as herbicides and/or plant growth regulators |
| WO2016001204A1 (de) | 2014-07-04 | 2016-01-07 | Bayer Cropscience Ag | Substituierte 5-hydroxy-2-heteroaryl-3-phenylpentanonitrilderivate, verfahren zu deren herstellung und deren verwendung als herbizide und/oder pflanzenwachstumsregulatoren |
| US10378012B2 (en) | 2014-07-29 | 2019-08-13 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| US11124792B2 (en) | 2014-07-29 | 2021-09-21 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| US10172350B2 (en) | 2014-10-08 | 2019-01-08 | Bayer Cropscience Aktiengesellschaft | Substituted 5-hydroxy-2-phenyl-3-heteroaryl pentanenitrile derivatives, method for the production thereof and use thereof as herbicides and/or plant growth regulators |
| US10968449B2 (en) | 2015-01-22 | 2021-04-06 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| US10883103B2 (en) | 2015-06-02 | 2021-01-05 | Monsanto Technology Llc | Compositions and methods for delivery of a polynucleotide into a plant |
| US10655136B2 (en) | 2015-06-03 | 2020-05-19 | Monsanto Technology Llc | Methods and compositions for introducing nucleic acids into plants |
Also Published As
| Publication number | Publication date |
|---|---|
| AR079400A1 (es) | 2012-01-25 |
| TW201105235A (en) | 2011-02-16 |
| AR079401A1 (es) | 2012-01-25 |
| TW201127284A (en) | 2011-08-16 |
| WO2011003776A3 (de) | 2011-04-21 |
| UY32779A (es) | 2011-01-31 |
| UY32777A (es) | 2011-01-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2011003776A2 (de) | Substituierte cyanobutyrate mit herbizider wirkung | |
| WO2010069802A1 (de) | Heterozyklische diketon-derivate mit herbizider wirkung | |
| WO2010049270A1 (de) | Substituierte pyridine mit herbizider wirkung | |
| US9220268B2 (en) | Herbicidal benzoxazinones | |
| DE102010042864A1 (de) | Substituierte Thioamide mit herbizider Wirkung | |
| EP2325170B1 (de) | Substituierte Chinolinone mit herbizider Wirkung | |
| EP2499136B1 (de) | 3-(3,4-dihydro-2h-benzo[1,4]oxazin-6-yl)-1h-pyrimidin-2,4-dion-verbindungen als herbizide | |
| WO2011003775A2 (de) | Substituierte cyanobutyrate mit herbizider wirkung | |
| WO2011042378A1 (de) | Substituierte cyanobutyrate mit herbizider wirkung | |
| WO2011051212A1 (de) | Verwendung heteroaromatischer verbindungen als herbizide | |
| EP2437605A1 (de) | Substituierte pyridopyrazine mit herbizider wirkung | |
| WO2010066677A2 (de) | Herbizide mischungen | |
| WO2011098417A1 (en) | Substituted cyanobutyrates having herbicidal action | |
| EP2496573B1 (de) | Herbizide tetrahydrophthalimide | |
| WO2011067184A1 (de) | 3- (4, 5 -dihydroisoxazol- 5 -yl) benzoylpyrazolverbindungen und ihre mischungen mit safenern | |
| DE102011080568A1 (de) | Substituierte Cyanobutyrate mit herbizider Wirkung | |
| DE102010042867A1 (de) | Verwendung heterozyklischer Verbindungen als Herbizide |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 10726514 Country of ref document: EP Kind code of ref document: A2 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 10726514 Country of ref document: EP Kind code of ref document: A2 |