RU67722U1 - Иммуносенсор для определения симазина - Google Patents
Иммуносенсор для определения симазина Download PDFInfo
- Publication number
- RU67722U1 RU67722U1 RU2007120180/22U RU2007120180U RU67722U1 RU 67722 U1 RU67722 U1 RU 67722U1 RU 2007120180/22 U RU2007120180/22 U RU 2007120180/22U RU 2007120180 U RU2007120180 U RU 2007120180U RU 67722 U1 RU67722 U1 RU 67722U1
- Authority
- RU
- Russia
- Prior art keywords
- simazine
- determination
- bioreceptor
- immunosensor
- transistor
- Prior art date
Links
- ODCWYMIRDDJXKW-UHFFFAOYSA-N simazine Chemical compound CCNC1=NC(Cl)=NC(NCC)=N1 ODCWYMIRDDJXKW-UHFFFAOYSA-N 0.000 claims abstract description 37
- 239000012528 membrane Substances 0.000 claims abstract description 14
- 230000005669 field effect Effects 0.000 claims abstract description 7
- 229920000447 polyanionic polymer Polymers 0.000 claims abstract description 6
- 238000006243 chemical reaction Methods 0.000 claims abstract description 5
- 230000009881 electrostatic interaction Effects 0.000 claims abstract description 5
- 229920000867 polyelectrolyte Polymers 0.000 claims abstract description 5
- 108010001336 Horseradish Peroxidase Proteins 0.000 claims abstract description 4
- 239000003153 chemical reaction reagent Substances 0.000 claims abstract description 3
- 239000000575 pesticide Substances 0.000 abstract description 15
- 230000007613 environmental effect Effects 0.000 abstract description 3
- 239000000126 substance Substances 0.000 abstract description 3
- 238000004458 analytical method Methods 0.000 description 18
- 238000000034 method Methods 0.000 description 11
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- 102000013415 peroxidase activity proteins Human genes 0.000 description 7
- 108040007629 peroxidase activity proteins Proteins 0.000 description 7
- 102000004190 Enzymes Human genes 0.000 description 6
- 108090000790 Enzymes Proteins 0.000 description 6
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 6
- 229960005070 ascorbic acid Drugs 0.000 description 5
- 239000011668 ascorbic acid Substances 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 239000011541 reaction mixture Substances 0.000 description 5
- 239000000427 antigen Substances 0.000 description 4
- 235000010323 ascorbic acid Nutrition 0.000 description 4
- 238000002967 competitive immunoassay Methods 0.000 description 4
- 238000001514 detection method Methods 0.000 description 4
- 238000003018 immunoassay Methods 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 229920000193 polymethacrylate Polymers 0.000 description 4
- 230000035945 sensitivity Effects 0.000 description 4
- 239000007790 solid phase Substances 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 description 3
- 108010088160 Staphylococcal Protein A Proteins 0.000 description 3
- 102000036639 antigens Human genes 0.000 description 3
- 108091007433 antigens Proteins 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 238000011088 calibration curve Methods 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 239000002689 soil Substances 0.000 description 3
- 238000005507 spraying Methods 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000007853 buffer solution Substances 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 238000004817 gas chromatography Methods 0.000 description 2
- 230000002363 herbicidal effect Effects 0.000 description 2
- 239000004009 herbicide Substances 0.000 description 2
- 230000003100 immobilizing effect Effects 0.000 description 2
- 230000001900 immune effect Effects 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 238000004949 mass spectrometry Methods 0.000 description 2
- 239000008363 phosphate buffer Substances 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 230000008929 regeneration Effects 0.000 description 2
- 238000011069 regeneration method Methods 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 230000000007 visual effect Effects 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- RTNUTCOTGVKVBR-UHFFFAOYSA-N 4-chlorotriazine Chemical class ClC1=CC=NN=N1 RTNUTCOTGVKVBR-UHFFFAOYSA-N 0.000 description 1
- 101100139907 Arabidopsis thaliana RAR1 gene Proteins 0.000 description 1
- 240000003291 Armoracia rusticana Species 0.000 description 1
- 235000011330 Armoracia rusticana Nutrition 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 235000016623 Fragaria vesca Nutrition 0.000 description 1
- 240000009088 Fragaria x ananassa Species 0.000 description 1
- 235000011363 Fragaria x ananassa Nutrition 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 235000007688 Lycopersicon esculentum Nutrition 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 101100028790 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) PBS2 gene Proteins 0.000 description 1
- 240000003768 Solanum lycopersicum Species 0.000 description 1
- 239000005621 Terbuthylazine Substances 0.000 description 1
- 244000269722 Thea sinensis Species 0.000 description 1
- 235000021307 Triticum Nutrition 0.000 description 1
- 244000098338 Triticum aestivum Species 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 235000021028 berry Nutrition 0.000 description 1
- 229940098773 bovine serum albumin Drugs 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 238000000326 densiometry Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 239000003599 detergent Substances 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 238000002848 electrochemical method Methods 0.000 description 1
- 239000000598 endocrine disruptor Substances 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 125000000031 ethylamino group Chemical group [H]C([H])([H])C([H])([H])N([H])[*] 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 239000003673 groundwater Substances 0.000 description 1
- 230000008105 immune reaction Effects 0.000 description 1
- 230000000984 immunochemical effect Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000001471 micro-filtration Methods 0.000 description 1
- 238000004853 microextraction Methods 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 238000002414 normal-phase solid-phase extraction Methods 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- FZXISNSWEXTPMF-UHFFFAOYSA-N terbutylazine Chemical compound CCNC1=NC(Cl)=NC(NC(C)(C)C)=N1 FZXISNSWEXTPMF-UHFFFAOYSA-N 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 150000003918 triazines Chemical class 0.000 description 1
Landscapes
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
Полезная модель относится к биотехнологии и охране окружающей среды, а именно к устройствам для определения химических веществ, в частности - для определения пестицида - симазина (2-хлор-4,6-бис(этиламино)-симм-триазин).
Предложен иммуносенсор, включающий рН-чувствительный полевой транзистор, сопряженный с предварительно сформированным биорецептором, выполненным в виде мембраны, содержащей иммунные комплексы, образовавшиеся в ходе аналитической реакции между нативным и меченным пероксидазой хрена симазаном и связанными с полианионом антителами к симазину. Иммунные комплексы отделены от непрореагировавших реагентов путем добавления поликатионов за счет электростатического взаимодействия полиэлектролитов. Биорецептор укреплен на транзисторе с помощью пружинного держателя. 3 ил.
Description
Полезная модель относится к биотехнологии и охране окружающей среды, а именно к устройствам для определения химических веществ, в частности пестицида - симазина (2-хлор-4,6-бис(этиламино)-симм-триазин).
Симазин применяется для опрыскивания почвы на посевах кукурузы; в садах, ягодниках, чайных плантациях и виноградниках до всходов сорняков; для ранневесеннего опрыскивания плантаций земляники; опрыскивания посевов озимой пшеницы и ржи до появления всходов в центральных районах нечерноземной зоны. Может сохранять токсичность в почве до двух лет и проникать в грунтовые воды (Медведь, 1974).
Для определения пестицидов триазинового ряда используются такие хроматографические методы, как газовая хроматография (Navarro et al., 2000), жидкостная хроматография (Melo et al., 2005), масс-спектрометрия (Petrovic et al., 2002) и другие. Эти методы позволяют проводить качественную и количественную оценку веществ в сложных многокомпонентных матрицах при очень низких концентрациях.
К недостаткам этих методов следует отнести высокую стоимость оборудования, необходимость тщательной очистки содержащих пестицид
экстрактов, длительность анализа, зачастую недостаточную его избирательность.
Кроме того, эти методы не подходят для измерений непосредственно на месте отбора проб.
Известен иммунологический метод для определения триазинов (патент США 5573922, 1996) с помощью конкурентного иммуноанализа, в котором к пробе пестицида из образца добавляют меченный пестицид и поликлональные антитела, при этом меченный пестицид и нативный пестицид конкурируют за связывание с поликлональными антителами, которые связываются перед, во время или после иммунологической реакции
с твердой фазой (микротитрационный планшет). Твердая фаза и не связавшиеся меченные молекулы пестицида разделяют и определяют количество метки на твердой фазе. Количество метки отражает содержание пестицида в образце. Нижний предел детекции при использовании этого метода составляет 4,1 нг/л, однако время анализа - более 3-х часов.
Применение таких иммунных методов анализа позволяет проводить чувствительное и селективное определение пестицидов, но эти анализы длительны (занимают несколько часов).
Известен способ определения симазина (Yazynina et al., 1999) с использованием конкурентного иммуноанализа, в котором к пробе пестицида из образца добавляют реакционную смесь, содержащую меченный симазин, специфические антитела к нему и конъюгат стафилококкового белка А с полианионом (полиметакрилат). После инкубации эту смесь добавляют к иммобилизованному поликатиону (поли-N-этил-4-винилпиридиниум). Поликатион иммобилизован либо на поверхности микротитрационной платы, либо на мембране. После промывки в ячейки микротитрационной платы приливают субстрат фермента и с помощью денситометра определяют оптическую плотность продуктов ферментативной реакции. Если поликатион иммобилизован на мембране, после фильтрации реакционной смеси, мембрану также промывают буфером и помещают в раствор субстрата фермента для образования цветных продуктов реакции на мембране. Интенсивность окраски мембраны определяют визуально.
Благодаря высокой кооперативности электростатического взаимодействия заряженных звеньев полимеров (полианиона и поликатиона) и комплементарному их расположению процесс связывания противоионов идет с крайне высокой скоростью и в широком диапазоне условий - практически необратимо (Блинцов и др., 1995). Поэтому при добавлении реакционной смеси к иммобилизованному поликатиону происходит быстрая иммобилизация иммунных комплексов на твердой фазе, а
непрореагировавшие молекулы остаются в растворе и быстро отделяются промывкой буфером.
При этом все иммунохимические стадии анализа идут в растворе, где уровень диффузионных ограничений существенно ниже, а затем проводится быстрая стадия разделения реагентов. Тем самым значительно сокращается продолжительность анализа (с 100-120 до 20-25 мин). Высокая аффинность взаимодействия между полимерами обеспечивает вытеснение не специфически связавшихся молекул, благодаря чему снижается фоновый сигнал и уменьшается вероятность ошибочной диагностики.
Чувствительность такого анализа составляет 1 нг/мл для денситометрических измерений и 10 нг/мл для визуальных измерений.
К недостаткам этого метода стоит отнести невысокую точность анализа в случае визуальных измерений.
Известен иммуносенсор на основе ион-селективного транзистора для определения симазина (Starodub et al., 2000). В указанном устройстве поликлональные антитела к симазину прикреплены непосредственно к затвору транзистора через стрептококковый белок А. Используют 2 метода определения симазина - (1) конкурентный иммуноанализ, когда молекулы нативного (определяемого) и меченного пероксидазой симазина конкурируют за связывание с антителами на поверхности полевого транзистора, и (2) последовательное насыщение, когда антитела взаимодействуют сначала с нативным симазином в исследуемом образце, а затем с меченным ферментом - пероксидазой хрена - симазином. Концентрация связавшегося с антителами конъюгата пропорциональна начальной концентрации антигена и служит характеристикой его содержания в исследуемом образце.
Каталитическую активность связанной с симазином пероксидазы (конъюгат симазин-пероксидаза) измеряют в присутствии аскорбиновой кислоты и пероксида водорода. Предел определения симазина конкурентным иммуноанализом составляет 1,25 нг/мл, линейный диапазон 5-175 нг/мл.
Последовательное насыщение антител приводит к росту чувствительности анализа до 0,65 нг/мл. Анализ занимает около 50 мин.
Однако подготовительные процедуры (очистка поверхности транзистора, иммобилизация антител на поверхности транзистора с использованием бычьего сывороточного альбумина, глутарового альдегида, белка А и глицина) очень длительны и занимают больше 15 часов.
Задача, на решение которой направлена заявляемая полезная модель, - создание устройства для быстрого и чувствительного определения симазина, простого по конструкции и эксплуатации.
Технический результат, который может быть получен при использовании предлагаемой полезной модели, заключается в том, что иммуносенсор обеспечивает быстрое определение содержания симазина без использования сложного дорогостоящего оборудования.
Сущность полезной модели.
Предложен иммуносенсор для определения пестицида симазина, включающий рН-чувствительный полевой транзистор, сопряженный с предварительно сформированным биорецептором, выполненным в виде мембраны, содержащей иммунные комплексы, образовавшиеся в ходе аналитической реакции между нативным и меченным пероксидазой хрена симазином и антителами к симазину. Биорецептор укреплен на транзисторе с помощью пружинного держателя.
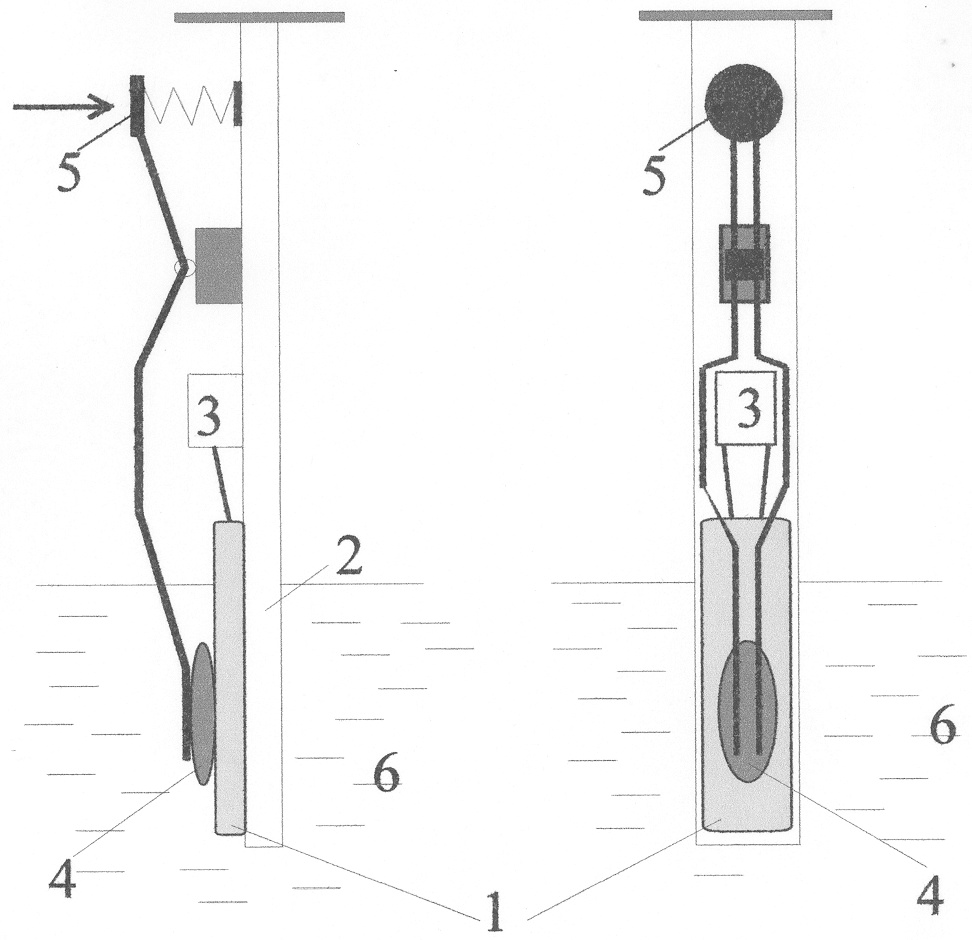
При этом рН-чувствительный полевой транзистор (1) укреплен на основании (2) и подключен в измерительную цепь через разъем (3). На затворной области транзистора находится биорецептор (4), прижатый к поверхности транзистора с помощью пружинного держателя (5). Транзистор погружен в измерительную ячейку (6) с буферным раствором (Фиг.1).
Формирование биорецептора осуществляют отдельно от транзистора по следующей схеме (Фиг.2):
1. В ячейки иммунологического планшета последовательно добавляют следующие растворы иммунореагентов в 50 мМ К-фосфатном буфере рН 7,4, содержащем 0,1 М Nad (ФБ1) и 0,05% детергента Tween-20 (ФТБ):
а) 25 мкл образца, содержащего антиген - симазин;
б) 25 мкл конъюгата симазин-пероксидаза (концентрация конъюгата 4 мкг/мл по пероксидазе), полученного, как описано в работе Yazynina et al., 1999;
в) 50 мкл специфической антисыворотки (разведение 1:500);
г) 50 мкл конъюгата белок А - полиметакрилат (20 мкг/мл), полученного, как описано в работе Yazynina et al., 1999.
Смесь инкубируют при комнатной температуре в течение 15 минут при постоянном встряхивании.
2. В специальное микрофильтрационное устройство помещают нитроцеллюлозную мембрану. В каждую ячейку устройства вносят по 50 мкл раствора поликатиона - поли-N-этил-4-винилпиридиния (40 мкг/мл, в ФБ1). После полной фильтрации раствора через мембрану добавляют по 50 мкл ФБТ для ее промывки. Затем вносят по 50 мкл реакционной смеси, которая получена в ходе выполнения пункта 1. После полной фильтрации растворов реакционной смеси мембрану промывают, добавляя в каждую ячейку 100 мкл ФБТ.
Затем устройство разбирают, извлекают мембрану с иммобилизованными на ней комплексами "поликатион - полианион - белок А - антитело -антиген", а именно - " поли-N-этил-4-винилпиридиний - полиметакрилат - стафилококковый белок А - антитело к симазину - симазин", и "поликатион - полианион - белок А - антитело - антиген - фермент", а именно - "поли-N-этил-4-винилпиридиний - полиметакрилат - стафилококковый белок А - антитело к симазину - симазин-пероксидаза хрена".
Эта мембрана и является биорецептором иммуносенсора.
Иммуносенсор работает следующим образом.
Сформированный биорецептор (4) помещают на затворную область транзистора (1), прижимают с помощью пружинного держателя (5) и погружают в измерительную ячейку (6) объемом 2 мл с буферным раствором ФБ2 (1 мМ К-фосфатный буфер, содержащий 0,015 М NaCl, pH 6,4). Затем добавляют 10 мкл аскорбиновой кислоты и 10 мкл о-фенилендиамина, регистрируют базовый уровень электрического сигнала. Реакцию фермента, размещенного в биорецепторе, инициируют добавлением 10 мкл пероксида водорода. Регистрируют максимальную скорость изменения сигнала транзистора в ходе каталитической реакции.
После анализа использованный биорецептор убирают и на затвор транзистора помещают новый биорецептор для следующего анализа.
На основании полученных данных строят калибровочную кривую (Фиг.3).
Для определения неизвестной концентрации пестицида во время проведения анализа в п.1 (а) протокола иммуноанализа добавляют 25 мкл образца с неизвестным количеством симазина, далее действуют по описанному выше протоколу. Затем по калибровочной кривой (Фиг.3), отражающей зависимость сигнала сенсора от концентрации симазина, определяют концентрацию симазина в анализируемом образце.
Принципиальными особенностями, отличающими предлагаемый иммуносенсор от известных устройств для определения симазина и позволяющими повысить чувствительность и сократить время анализа, являются:
1) Использование сменных носителей - мембран для иммобилизации иммунореагента и детектируемых иммунных комплексов - в отличие от традиционно применяемой иммобилизации непосредственно на поверхность электрода, занимающей несколько часов (Starodub et al., 2000).
Данный подход существенно повышает производительность анализа, особенно при необходимости одновременного тестирования значительного
количества образцов, так как позволяет избегать регенерации поверхности транзистора.
2) Быстрое отделение сформировавшихся в ходе аналитической реакции иммунных комплексов от непрореагировавших молекул, основанное на электростатическом взаимодействии между растворимыми линейными полиэлектролитами - носителями иммунореагентов.
Этот подход, - благодаря высокой кооперативности поливалентного электростатического взаимодействия, - значительно снижает уровень неспецифических взаимодействий и тем самым вероятность ошибочной диагностики, а также в несколько раз сокращает продолжительность анализа при использовании тех же иммунокомпонентов.
3) Применение оригинальных систем усиления каталитической активности для детекции пероксидазы, основанных на использовании специальной субстратной смеси, включающей о-фенилендиамин, аскорбиновую кислоту и пероксид водорода.
В этой смеси о-фенилендиамин играет роль электронного медиатора при трансформации аскорбиновой кислоты в гидроаскорбиновую, при этом изменяется рН раствора, что регистрируется транзистором. Это обеспечивает высокую амплитуду детектируемого сигнала, тем самым снижая порог детекции формирующихся иммунных комплексов и улучшая чувствительность иммуносенсора.
Диапазон количественного определения симазина составляет 2,6 - 333 нг/мл. Аналитическая процедура занимает 20-25 минут, а непосредственно электрохимические измерения одного образца - не более 1-2 минут. Коэффициент вариации (отношение среднеквадратичного отклонения к среднему арифметическому значению сигнала) составляет 5-11%.
На фиг.1 представлена схема иммуносенсора на основе рН-чувствительного полевого транзистора для определения симазина, а - вид сбоку, 6 - вид спереди.
На фиг.2 показана схема формирования биорецептора иммуносенсора для определения симазина.
На фиг.3 приведена калибровочная кривая иммуносенсора для определения симазина.
Таким образом, разработан иммуносенсор для определения симазина, который обеспечивает быстрое определение содержания симазина в образце без использования сложного дорогостоящего оборудования. Применение полиэлектролитов при подготовке биорецептора позволяет сократить время анализа в 4 раза по сравнению с традиционными иммуноферментными методами, а формирование биорецептора отдельно от транзистора позволяет избежать процедуры регенерации поверхности транзистора и также сокращает время анализа.
Список цитируемых источников:
1. Melo L.F., Collins C.H., Jardim I.C. High-performance liquid chromatographic determination of pesticides in tomatoes using laboratory-made NH2 and С 18 solid-phase extraction materials. // J. Chromatogr A. - 2005. V.1073, №1-2. - P. 75-81.
2. Navarro S., Oliva J., Barba A., Garcia C. Determination of simazine, terbuthylazine, and their dealkylated chlorotriazine metabolites in soil using sonication microextraction and gas chromatography. // J AOAC Int. - 2000. V.83, №5. - P. 1239-1243.
3. Petrovic M., Eljarrat E., Lopez de Alda M.J., Barcelo D. Recent advances in the mass spectrometric analysis related to endocrine disrupting compounds in aquatic environmental samples. // J. Chromatogr. A. - 2002. V.974. - P. 23-/51.
4. Starodub N.F., Dzantiev B.B., Starodub V.M., Zherdev A.V. Immunosensor for the determination of the herbicide simazine based on an ion-selective field-effect transistor. // Analytica Chimica Acta. - 2000. V.424, №1. - P. 37-43.
5. Yazynina E.V., Zherdev A.V., Dzantiev B.B., Izumrudov V.A., Gee S.J., Hanimock B.D. Immunoassay techniques for detection of the herbicide simazine based on use of oppositely charged water-soluble polyelectrolytes. // Anal. Chem. - 1999. V.71. - P. 3538-3543.
6. Блинцов А.Н., Дзантиев Б.Б., Бобкова А.Ф., Изумрудов В.А., Зезин А.Б., Атабеков И.Г. Новый метод иммуноанализа растительных вирусов, основанный на использовании интерполиэлектролитных реакций. // Доклады РАН. - 1995. Т. 345, N 2. - С.263-267.
7. Медведь Л.И. Справочник по пестицидам. // Киев: Урожай. - 1974. - 448 с.
8. Патент США №5573922, G01N 33/53, 12.11.1996.
Claims (1)
- Иммуносенсор для определения симазина, включающий рН-чувствительный полевой транзистор, с укрепленным на нем с помощью пружинного держателя предварительно сформированным биорецептором, выполненным в виде мембраны, содержащей иммунные комплексы, образовавшиеся в ходе аналитической реакции между нативным и меченным пероксидазой хрена симазаном и связанными с полианионом антителами к симазину, и отделенные от непрореагировавших реагентов путем добавления поликатионов за счет электростатического взаимодействия полиэлектролитов.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2007120180/22U RU67722U1 (ru) | 2007-05-31 | 2007-05-31 | Иммуносенсор для определения симазина |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2007120180/22U RU67722U1 (ru) | 2007-05-31 | 2007-05-31 | Иммуносенсор для определения симазина |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU67722U1 true RU67722U1 (ru) | 2007-10-27 |
Family
ID=38956271
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2007120180/22U RU67722U1 (ru) | 2007-05-31 | 2007-05-31 | Иммуносенсор для определения симазина |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU67722U1 (ru) |
-
2007
- 2007-05-31 RU RU2007120180/22U patent/RU67722U1/ru not_active IP Right Cessation
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Hayat et al. | Enzyme-linked immunosensor based on super paramagnetic nanobeads for easy and rapid detection of okadaic acid | |
| Wang et al. | A novel immunochromatographic assay based on a time-resolved chemiluminescence strategy for the multiplexed detection of ractopamine and clenbuterol | |
| Liu et al. | Construction of an impedimetric immunosensor for label-free detecting carbofuran residual in agricultural and environmental samples | |
| CN100420947C (zh) | 用单一捕获剂定量检测特异性分析物的方法及其试剂盒 | |
| ATE79679T1 (de) | Diagnostische probe. | |
| CN102841206B (zh) | 肌钙蛋白T(Troponin-T,TNT)测定试剂盒 | |
| US10078079B2 (en) | Device for detecting an analyte | |
| DE68913086D1 (de) | Qualitativer Enzymtest zur visuellen Auswertung. | |
| CN102608325A (zh) | 脂肪酸结合蛋白(fatty acid-binding proteins,H-FABP)测定试剂盒(胶乳增强免疫比浊法) | |
| Wang et al. | Luminol-reduced Au nanoparticles-based dual-signal immunochromatographic test strip for pesticide residues | |
| Höfs et al. | Electrochemical Immunomagnetic Ochratoxin A Sensing: Steps Forward in the Application of 3, 3’, 5, 5’‐Tetramethylbenzidine in Amperometric Assays | |
| Lou et al. | Direct and ultrasensitive optofluidic-based immunosensing assay of aflatoxin M1 in dairy products using organic solvent extraction | |
| US9170227B2 (en) | Multi-analyte system and method based on impedimetric measurements | |
| Siegmann-Thoss et al. | Enzyme immunosensor for diagnosis of myocardial infarction | |
| US8927219B2 (en) | Method for evaluation of quality of blood sample | |
| Campanella et al. | Reliable new immunosensor for atrazine pesticide analysis | |
| Van Emon et al. | Environmental monitoring and human exposure assessment using immunochemical techniques | |
| Meusel et al. | New ways in bioanalysis—one-way optical sensor chip for environmental analysis | |
| RU67722U1 (ru) | Иммуносенсор для определения симазина | |
| Martini et al. | Determination of traces of several pesticides in sunflower oil using organic phase immuno electrodes (OPIEs) | |
| Khattab et al. | An ELISA assay for avian serum butyrylcholinesterase: a biomarker for organophosphates | |
| CN101368946B (zh) | 丁草胺极化荧光免疫检测方法 | |
| WO2017200308A1 (ko) | 멤브레인상에서 형광 공명 에너지 전이 면역 분석법을 이용한 항원 검출방법 | |
| RU2405042C1 (ru) | Способ и набор для иммуноферментного определения функциональной активности компонента с2 комплемента человека | |
| EP1700117B1 (en) | Method and kit for pesticide analysis |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM1K | Utility model has become invalid (non-payment of fees) |
Effective date: 20150601 |