RU2770892C1 - Тест-система и способ выявления делеций длинного плеча 6 хромосомы - Google Patents
Тест-система и способ выявления делеций длинного плеча 6 хромосомы Download PDFInfo
- Publication number
- RU2770892C1 RU2770892C1 RU2021121807A RU2021121807A RU2770892C1 RU 2770892 C1 RU2770892 C1 RU 2770892C1 RU 2021121807 A RU2021121807 A RU 2021121807A RU 2021121807 A RU2021121807 A RU 2021121807A RU 2770892 C1 RU2770892 C1 RU 2770892C1
- Authority
- RU
- Russia
- Prior art keywords
- locus
- pmol
- fam
- dna
- homo sapiens
- Prior art date
Links
- 238000012217 deletion Methods 0.000 title claims abstract description 39
- 230000037430 deletion Effects 0.000 title claims abstract description 39
- 238000000034 method Methods 0.000 title claims abstract description 26
- 210000000349 chromosome Anatomy 0.000 title claims abstract description 15
- 238000012360 testing method Methods 0.000 title claims abstract description 15
- 206010028980 Neoplasm Diseases 0.000 claims abstract description 41
- 108091092878 Microsatellite Proteins 0.000 claims abstract description 36
- 238000003752 polymerase chain reaction Methods 0.000 claims abstract description 31
- 201000003444 follicular lymphoma Diseases 0.000 claims abstract description 18
- 210000001519 tissue Anatomy 0.000 claims abstract description 16
- 108700028369 Alleles Proteins 0.000 claims abstract description 12
- 238000007403 mPCR Methods 0.000 claims abstract description 7
- 230000003321 amplification Effects 0.000 claims abstract description 6
- 238000003199 nucleic acid amplification method Methods 0.000 claims abstract description 6
- 239000013068 control sample Substances 0.000 claims abstract description 5
- 210000003917 human chromosome Anatomy 0.000 claims abstract description 3
- 230000002411 adverse Effects 0.000 claims abstract 3
- 238000004458 analytical method Methods 0.000 claims description 14
- 239000000523 sample Substances 0.000 claims description 12
- 230000002068 genetic effect Effects 0.000 claims description 11
- 239000012634 fragment Substances 0.000 claims description 8
- 239000000203 mixture Substances 0.000 claims description 8
- 239000000243 solution Substances 0.000 claims description 7
- 238000001574 biopsy Methods 0.000 claims description 6
- 108091034117 Oligonucleotide Proteins 0.000 claims description 5
- 239000012188 paraffin wax Substances 0.000 claims description 5
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 claims description 4
- 238000000137 annealing Methods 0.000 claims description 4
- 210000001185 bone marrow Anatomy 0.000 claims description 4
- 239000008367 deionised water Substances 0.000 claims description 4
- 229910021641 deionized water Inorganic materials 0.000 claims description 4
- 238000004925 denaturation Methods 0.000 claims description 4
- 230000036425 denaturation Effects 0.000 claims description 4
- 210000004976 peripheral blood cell Anatomy 0.000 claims description 4
- 238000007400 DNA extraction Methods 0.000 claims description 3
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 3
- 108010006785 Taq Polymerase Proteins 0.000 claims description 3
- 238000005251 capillar electrophoresis Methods 0.000 claims description 3
- 238000002360 preparation method Methods 0.000 claims description 3
- 238000012800 visualization Methods 0.000 claims description 3
- 230000015572 biosynthetic process Effects 0.000 claims description 2
- 238000010790 dilution Methods 0.000 claims description 2
- 239000012895 dilution Substances 0.000 claims description 2
- 239000000539 dimer Substances 0.000 claims description 2
- 210000002919 epithelial cell Anatomy 0.000 claims description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 2
- 239000012807 PCR reagent Substances 0.000 claims 1
- 239000003155 DNA primer Substances 0.000 abstract description 2
- 239000003814 drug Substances 0.000 abstract description 2
- 230000000694 effects Effects 0.000 abstract description 2
- 239000000126 substance Substances 0.000 abstract 1
- 239000013615 primer Substances 0.000 description 94
- 108020004414 DNA Proteins 0.000 description 85
- 241000282414 Homo sapiens Species 0.000 description 82
- 230000002441 reversible effect Effects 0.000 description 41
- 239000002773 nucleotide Substances 0.000 description 40
- 125000003729 nucleotide group Chemical group 0.000 description 40
- 239000000047 product Substances 0.000 description 19
- 201000010099 disease Diseases 0.000 description 14
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 14
- 238000001962 electrophoresis Methods 0.000 description 11
- 238000006243 chemical reaction Methods 0.000 description 9
- 239000000463 material Substances 0.000 description 8
- 230000002559 cytogenic effect Effects 0.000 description 7
- 238000004393 prognosis Methods 0.000 description 7
- 210000004369 blood Anatomy 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 210000004027 cell Anatomy 0.000 description 6
- 238000002512 chemotherapy Methods 0.000 description 5
- 238000013507 mapping Methods 0.000 description 5
- 239000011541 reaction mixture Substances 0.000 description 5
- 102000043276 Oncogene Human genes 0.000 description 4
- 108700020796 Oncogene Proteins 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 238000003745 diagnosis Methods 0.000 description 4
- 238000002405 diagnostic procedure Methods 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- 230000035945 sensitivity Effects 0.000 description 4
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 3
- 208000028564 B-cell non-Hodgkin lymphoma Diseases 0.000 description 3
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 3
- 201000011510 cancer Diseases 0.000 description 3
- 230000002759 chromosomal effect Effects 0.000 description 3
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 3
- 230000004807 localization Effects 0.000 description 3
- 239000003550 marker Substances 0.000 description 3
- 230000000877 morphologic effect Effects 0.000 description 3
- 230000008506 pathogenesis Effects 0.000 description 3
- 238000010837 poor prognosis Methods 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 2
- 230000004075 alteration Effects 0.000 description 2
- 230000002349 favourable effect Effects 0.000 description 2
- 238000002509 fluorescent in situ hybridization Methods 0.000 description 2
- 230000004077 genetic alteration Effects 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 230000000771 oncological effect Effects 0.000 description 2
- 210000005259 peripheral blood Anatomy 0.000 description 2
- 239000011886 peripheral blood Substances 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 235000011178 triphosphate Nutrition 0.000 description 2
- 239000001226 triphosphate Substances 0.000 description 2
- UNXRWKVEANCORM-UHFFFAOYSA-N triphosphoric acid Chemical compound OP(O)(=O)OP(O)(=O)OP(O)(O)=O UNXRWKVEANCORM-UHFFFAOYSA-N 0.000 description 2
- 230000007730 Akt signaling Effects 0.000 description 1
- 101100180402 Caenorhabditis elegans jun-1 gene Proteins 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- 206010008263 Cervical dysplasia Diseases 0.000 description 1
- 206010008805 Chromosomal abnormalities Diseases 0.000 description 1
- 206010061764 Chromosomal deletion Diseases 0.000 description 1
- 208000031404 Chromosome Aberrations Diseases 0.000 description 1
- 238000007399 DNA isolation Methods 0.000 description 1
- 206010061819 Disease recurrence Diseases 0.000 description 1
- 108010009307 Forkhead Box Protein O3 Proteins 0.000 description 1
- 102100035421 Forkhead box protein O3 Human genes 0.000 description 1
- 102100038970 Histone-lysine N-methyltransferase EZH2 Human genes 0.000 description 1
- 101000882127 Homo sapiens Histone-lysine N-methyltransferase EZH2 Proteins 0.000 description 1
- 208000026350 Inborn Genetic disease Diseases 0.000 description 1
- 208000008771 Lymphadenopathy Diseases 0.000 description 1
- 102000008135 Mechanistic Target of Rapamycin Complex 1 Human genes 0.000 description 1
- 108010035196 Mechanistic Target of Rapamycin Complex 1 Proteins 0.000 description 1
- 241000582786 Monoplex Species 0.000 description 1
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 102100035593 POU domain, class 2, transcription factor 1 Human genes 0.000 description 1
- 101710084414 POU domain, class 2, transcription factor 1 Proteins 0.000 description 1
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 1
- 102100027288 Sestrin-1 Human genes 0.000 description 1
- 101710186864 Sestrin-1 Proteins 0.000 description 1
- 201000011638 T-cell childhood acute lymphocytic leukemia Diseases 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 1
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 1
- 210000001766 X chromosome Anatomy 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 239000012620 biological material Substances 0.000 description 1
- 208000007951 cervical intraepithelial neoplasia Diseases 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 230000014107 chromosome localization Effects 0.000 description 1
- 238000003200 chromosome mapping Methods 0.000 description 1
- 239000013065 commercial product Substances 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 230000002338 cryopreservative effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000003748 differential diagnosis Methods 0.000 description 1
- 230000001973 epigenetic effect Effects 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 231100000118 genetic alteration Toxicity 0.000 description 1
- 208000016361 genetic disease Diseases 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 206010024378 leukocytosis Diseases 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 208000018555 lymphatic system disease Diseases 0.000 description 1
- 208000003747 lymphoid leukemia Diseases 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 238000007479 molecular analysis Methods 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 230000009826 neoplastic cell growth Effects 0.000 description 1
- 231100000590 oncogenic Toxicity 0.000 description 1
- 230000002246 oncogenic effect Effects 0.000 description 1
- 230000008756 pathogenetic mechanism Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 201000005825 prostate adenocarcinoma Diseases 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 201000006845 reticulosarcoma Diseases 0.000 description 1
- 208000029922 reticulum cell sarcoma Diseases 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5014—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing toxicity
- G01N33/5017—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing toxicity for testing neoplastic activity
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Hematology (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Urology & Nephrology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Toxicology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pathology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biophysics (AREA)
- General Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Cell Biology (AREA)
- Tropical Medicine & Parasitology (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
Изобретение относится к набору олигонуклеотидных праймеров для специфической амплификации двадцати микросателлитных локусов длинного плеча 6 хромосомы человека (6q), который может быть использован в тест-системе для определения делеций длинного плеча 6 хромосомы (6q) методом мультиплексной полимеразной цепной реакции (ПЦР), а также в способе выявления пациентов с риском неблагоприятного течения фолликулярной лимфомы по наличию значимых делеций длинного плеча 6 хромосомы (6q) с помощью вышеупомянутой тест-системы. Наличие делеций региона 6q в случае гетерозиготного наследования на основании отсутствия пиков одного из аллелей или уменьшения интенсивности его флуоресценции по отношению к пику второго аллеля соответствующего микросателлитного локуса в опухолевой ткани при сравнении с контрольным образцом позволяет выделять группу пациентов с риском неблагоприятного течения фолликулярной лимфомы. 3 н.п. ф-лы, 6 ил., 1 табл., 4 пр.
Description
Изобретение предназначено для идентификации делеции длинного плеча 6 хромосомы (6q) как молекулярно-генетического фактора неблагоприятного прогноза В-клеточных неходжкинских лимфом (В-НХЛ), в частности фолликулярной лимфомы (ФЛ), и может быть использовано в клинической медицине на этапе первичной диагностики с целью выделения групп пациентов с риском неблагоприятного течения болезни, а также в рамках фундаментальных исследований и поиска потенциальных онкогенов.
Выделение в дебюте онкологического заболевания факторов, позволяющих идентифицировать группу пациентов с неблагоприятным прогнозом, является актуальной задачей с позиций дифференциальной диагностики и возможной персонификации терапии. Определение молекулярно-генетических маркеров является оптимальным вариантом достижения подобных задач, поскольку прямо отражает биологические особенности опухоли.
Известно, что делеции 6q прогностически неблагоприятны при ряде онкологических заболеваний. В первую очередь это касается опухолей системы крови, в частности неходжкинских В-клеточных лимфом и особенно ФЛ, однако также применимо к солидным новообразованиям. Например, ранее было показано, что общая выживаемость больных фолликулярной лимфомой с делецией 6q значительно ниже, чем пациентов без данной генетической аномалии [1]. Подобные же результаты были продемонстрированы в группе больных хроническим лимфолейкозом [2], кроме того, в случае хронического лимфолейкоза делеция 6q оказалась ассоциирована с более высокими значениями лейкоцитоза и распространенной лимфаденопатией [3]. Делеция 6q является фактором неблагоприятного прогноза и риска опухолевой трансформации и рецидива заболевания при остром Т-лимфобластном лейкозе [4-6]. В области солидной онкологии отрицательное влияние делеции 6q на течение заболевания отмечено при аденокарциноме простаты [7] и неоплазиях шейки матки [8].
В области 6q расположены гены, мутации которых обладают онкогенным потенциалом. Однако на настоящий момент точно идентифицированы только некоторые их них [9]. Варианты делеций 6q, вовлекающие различные цитогенетические регионы, обладают нозологической специфичностью [10-12] и соответственно отражают уникальность патогенетических механизмов при различных типах опухолей.
Таким образом, идентификация делеций 6q и определение локализации потерь генетического материала представляется актуальной задачей как в практическом отношении диагностики прогностически неблагоприятных вариантов ФЛ, так и с позиций фундаментальных исследований и поиска ключевых онкогенов.
Данная задача может быть решена при использовании следующих вариантов лабораторного анализа:
1) цитогенетическое исследование;
2) флуоресцентная гибридизация in situ (FISH);
3) сравнительная геномная гибридизация (CGH);
4) полимеразная цепная реакция (ПЦР).
Метод 1 отличается низкой чувствительностью и недостаточной воспроизводимостью результатов, абсолютным требованием к жизнеспособности клеток материла биоптата опухолевой ткани и способности давать достаточное количество митозов в краткосрочных культурах, что исключает возможность анализа замороженных и заключенных в парафин образцов, а также накладывает ограничения на спектр анализируемых патологий, поскольку многие типы опухолей характеризуются низкой пролиферативной способностью.
Метод 2 не применим при исследовании малоклеточных образцов и образцов с низкой сохранностью генетического материала, в частности, парафиновых блоков, а также отличается технической сложностью выполнения и длительностью проведения исследования.
Метод 3 предоставляет высокоточные результаты, максимально полно характеризующие 6q, однако отличается крайне высокой стоимостью анализа одного образца, отсутствием в большинстве практических лабораторий необходимого оборудования и реактивов.
Метод 4, заключающийся в амплификации методом ПЦР искомых последовательностей ДНК, расположенных на 6q в известной локализации, характеризуется высокой чувствительностью. Он позволяет исследовать малоклеточные образцы и архивный материал (замороженные образцы опухолевых тканей и парафиновые блоки) и отличается относительной простотой выполнения и возможностью воспроизведения методики в большинстве молекулярно-генетических лабораторий.
Таким образом, данный вариант решения поставленной задачи максимально соответствует требованиям высокой чувствительности анализа, простоты технической реализации и воспроизводимости лабораторного исследования.
Возможность поиска делеций при картировании хромосом методом ПЦР реализуется при анализе полиморфных локусов микросателлитных повторов, отличающихся высоким процентом гетерозиготности, на основании различий микросателлитного профиля в материале опухолевой ткани и нормальных клетках в качестве контроля. Сравнение проводят путем сопоставления длин амплифицированных фрагментов ДНК, соответствующих разным аллелям в парных образцах при разделении и визуализации ПЦР-продукта методами горизонтального электрофореза или капиллярного электрофореза. Последний вариант является предпочтительным, поскольку обладает большей разрешающей способностью по сравнению с электрофорезом в полиакриламидном геле.
Перечни динуклеотидных микросателлитных маркеров, которые могут быть использованы для картирования хромосом, были разработаны и представлены ранее [13, 14] и послужили основой всех последующих лабораторных систем.
Наиболее близким аналогом предлагаемого изобретения можно считать системы мультиплексных реакций ABI PRISM® Linkage Mapping Set, v2.5-HD5 и v2.5-MD10 производства компании Applied Biosystems (Thermo Fisher Scientific, USA). Указанные системы подразумевают картирование всех хромосом человека, в частности региона 6q, по микросателлитным локусам, расположенным с интервалом 5 и 10 сМ, соответственно. В качестве их недостатка можно отметить тот факт, что сочетания определяемых маркеров в мультиплексных реакциях не являются сбалансированными по хромосомным регионам, в частности последовательности 6р и 6q объединены в одних и тех же пробах. Таким образом, подробный анализ 6q может быть достигнут только при использовании полной панели коммерческого набора, что с учетом стоимости избыточных реактивов и времени на проведение дополнительных лабораторных исследований представляется нерациональным для решения поставленной задачи. Кроме того, в настоящее время данный коммерческий продукт не производится и недоступен пользователям, что является основным недостатком данного аналога.
Также в работах Merup et al. [11], Inoue et al. [15] и Starostik et al. [16] представлены другие варианты аналогов систем картирования 6q. Недостатками первого исследования являются проведение ПЦР в моноплексном режиме и анализ ПЦР-продукта методом горизонтального электрофореза, что обусловливает высокий расход биологического материла в множественных реакциях и низкое разрешение результатов, соответственно. Недостаток двух других исследований заключается в недостаточном для решения поставленной задачи покрытии 6q предлагаемыми авторами панелями микросателлитных повторов. Так, в работе Inoue et al. [15] регион 6q21, на долю которого приходится большая часть делеций при онкогематологических заболеваниях [1, 9-11], представлен только 3 микросателлитными локусами. В работе Starostik et al. [16] совершенно не отражены микросателлитные повторы центромерной области 6q.
Заявляемая группа изобретений направлена на решение задачи создания простой, доступной для реализации в большинстве молекулярно-генетических лабораторий, и информативной диагностической тест-системы и способа выявления делеций 6q при ФЛ, как маркера неблагоприятного прогноза заболевания.
Поставленная задача решена разработкой тест-системы с набором праймеров и способа выявления пациентов с риском неблагоприятного течения фолликулярной лимфомы по наличию значимых делеций 6q в образце опухолевой ткани при сравнении с нормальными клетками в качестве контрольного образца путем проведения анализа изменений 20 микросателлитных локусов ДНК методом мультиплексной ПЦР с последующим фрагментным анализом ПЦР-продуктов. Выбранные микросателлиты равномерно распределены по длине 6q от центромерной до теломерной областей с результирующим интервалом 5,7 сМ в среднем (1,7 -12,5 сМ по данным [13, 14]) и характеризуются высоким уровнем гетерозиготности 82,5% в среднем (75-91% по данным [13, 14]), что также отличает предлагаемое изобретение от известных аналогов.
Результатом исследований, произведенных авторами заявляемого изобретения, является диагностическая тест-система и способ осуществления диагностики делеций 6q с определением областей их локализации при ФЛ.
В опубликованных источниках литературы авторами не обнаружено сведений, касающихся реализованного нового решения.
Использование в клинической практике заявляемого способа позволяет достичь следующих технических результатов:
1) определение прогноза заболевания на этапе первичной диагностики путем выявления прогностически неблагоприятных генетических аномалий в опухолевой ткани, а именно делеций 6q;
2) выделение значимых в патогенезе опухоли хромосомных регионов путем идентификации областей делеции микросателлитных локусов, имеющих известные хромосомные локализации, как основы направленного поиска вовлеченных онкогенов.
Сущность предлагаемого изобретения пояснена на следующих графических материалах:
Фиг. 1 - Пул праймеров 1, относится к примеру 1 и представляет результат исследования микросателлитных локусов у здорового донора. На графике электрофореграммы по оси X отмечена длина ПЦР-продукта, п.н. По оси Y отмечена интенсивность флуоресценции меченого ПЦР-продукта.
Фиг. 2 - Пул праймеров 2, относится к примеру 1 и представляет результат исследования микросателлитных локусов у здорового донора. На графике электрофореграммы по оси X отмечена длина ПЦР-продукта, п.н. По оси Y отмечена интенсивность флуоресценции меченого ПЦР-продукта.
Фиг. 3 - Пул праймеров 3, относится к примеру 1 и представляет результат исследования микросателлитных локусов у здорового донора. На графике электрофореграммы по оси X отмечена длина ПЦР-продукта, п.н. По оси Y отмечена интенсивность флуоресценции меченого ПЦР-продукта.
Фиг. 4 - Пул праймеров 4, относится к примеру 1 и представляет результат исследования микросателлитных локусов у здорового донора. На графике электрофореграммы по оси X отмечена длина ПЦР-продукта, п.н. По оси Y отмечена интенсивность флуоресценции меченого ПЦР-продукта.
Фиг. 5 - Относится к примеру 2 и представляет результат исследования микросателлитных локусов у пациента X. На графике электрофореграммы по оси X отмечена длина ПЦР-продукта, п.н. По оси Y отмечена интенсивность флуоресценции меченого ПЦР-продукта. Стрелочками указаны локусы утраты одного из аллелей в опухолевом образце.
Фиг. 6 - Относится к примеру 3 и представляет результат исследования панели микросателлитных локусов у пациента Т. На графике электрофореграммы по оси X отмечена длина ПЦР-продукта, п.н. По оси Y отмечена интенсивность флуоресценции меченого ПЦР-продукта. Стрелочками указаны локусы утраты одного из аллелей в опухолевом образце.
Сущность группы изобретений пояснена следующими перечнями последовательностей:
SEQ ID NO: 1 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S1681;
SEQ ID NO: 2 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S1681;
SEQ ID NO: 3 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S434;
SEQ ID NO: 4 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S434;
SEQ ID NO: 5 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S403;
SEQ ID NO: 6 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S403;
SEQ ID NO: 7 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S1613;
SEQ ID NO: 8 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S1613;
SEQ ID NO: 9 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S292;
SEQ ID NO: 10 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S292;
SEQ ID NO: 11 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S460;
SEQ ID NO: 12 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S460;
SEQ ID NO: 13 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S287;
SEQ ID NO: 14 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S287;
SEQ ID NO: 15 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S300;
SEQ ID NO: 16 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S300;
SEQ ID NO: 17 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S311;
SEQ ID NO: 18 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S311;
SEQ ID NO: 19 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S447;
SEQ ID NO: 20 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S447;
SEQ ID NO: 21 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S262;
SEQ ID NO: 22 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S262;
SEQ ID NO: 23 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S441;
SEQ ID NO: 24 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S441;
SEQ ID NO: 25 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S305;
SEQ ID NO: 26 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S305;
SEQ ID NO: 27 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S446;
SEQ ID NO: 28 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S446;
SEQ ID NO: 29 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S261;
SEQ ID NO: 30 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S261;
SEQ ID NO: 31 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S1594;
SEQ ID NO: 32 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S1594;
SEQ ID NO: 33 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S1719;
SEQ ID NO: 34 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S1719;
SEQ ID NO: 35 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S415;
SEQ ID NO: 36 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S415;
SEQ ID NO: 37 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S430;
SEQ ID NO: 38 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S430;
SEQ ID NO: 39 последовательность нуклеотидов ДНК Homo sapiens, прямой праймер к локусу D6S407;
SEQ ID NO: 40 последовательность нуклеотидов ДНК Homo sapiens, обратный праймер к локусу D6S407.
Нуклеотидные последовательности праймеров к локусам D6S292 и D6S441 были заимствованы из работы Gyapay et al. [14], поскольку предоставляли оптимальный вариант амплификации искомой микросателлитной последовательности, удовлетворяющий требованиям разрабатываемой тест-системы. К остальным 18 микросателлитным локусам были подобраны оригинальные специфичные пары олигонуклеотидов, ранее не описанные в литературе.
Сущность группы изобретения заключается в следующем.
Разработана тест-система.
Состав тест-системы:
1) пары прямого и обратного праймеров к 20 динуклеотидным микросателлитным маркерам, объединенным в 4 мультиплексных пула соответственно 4 реакционным смесям
1 пул:
- локус D6S1681, расположенный в локусе 6q14 (прямой праймер SEQ ID NO: 1, 2,5 пмоль/мкл; обратный праймер SEQ ID NO: 2, меченный FAM, 2,5 пмоль/л);
- локус D6S434, расположенном в локусе 6q21 (прямой праймер SEQ ID NO: 3, 10 пмоль/мкл; обратный праймер SEQ ID NO: 4, меченный ROX, 10 пмоль/л);
- локус D6S403, расположенном в локусе 6q23 (прямой праймер SEQ ID NO: 5, 5 пмоль/мкл; обратный праймер SEQ ID NO: 6, меченный FAM, 5 пмоль/л);
- локус D6S1613, расположенном в локусе 6q16 (прямой праймер SEQ ID NO: 7, 5 пмоль/мкл; обратный праймер SEQ ID NO: 8, меченный ROX, 5 пмоль/л).
2 пул:
- локус D6S292, расположенном в локусе 6q23 (прямой праймер SEQ ID NO: 9, 5 пмоль/мкл; обратный праймер SEQ ID NO: 10, меченный FAM, 5 пмоль/л);
- локус D6S460, расположенном в локусе 6q14-15 (прямой праймер SEQ ID NO: 11, 10 пмоль/мкл; обратный праймер SEQ ID NO: 12, меченный ROX, 10 пмоль/л);
- локус D6S287, расположенном в локусе 6q22 (прямой праймер SEQ ID NO: 13, 10 пмоль/мкл; обратный праймер SEQ ID NO: 14, меченный ROX, 10 пмоль/л);
- локус D6S300, расположенном в локусе 6q 16-21 (прямой праймер SEQ ID NO: 15, 4 пмоль/мкл; обратный праймер SEQ ID NO: 16, меченный FAM, 4 пмоль/л);
- локус D6S311, расположенном в локусе 6q24-25 (прямой праймер SEQ ID NO: 17, 4 пмоль/мкл; обратный праймер SEQ ID NO: 18, меченный FAM, 4 пмоль/л).
3 пул:
- локус D6S447, расположенном в локусе 6q21 (прямой праймер SEQ ID NO: 19, 10 пмоль/мкл; обратный праймер SEQ ID NO: 20, меченный ROX, 10 пмоль/л);
- локус D6S262, расположенном в локусе 6q23 (прямой праймер SEQ ID NO: 21, 4 пмоль/мкл; обратный праймер SEQ ID NO: 22, меченный FAM, 4 пмоль/л);
- локус D6S441, расположенном в локусе 6q25 (прямой праймер SEQ ID NO: 23, 15 пмоль/мкл; обратный праймер SEQ ID NO: 24, меченный ROX, 15 пмоль/л);
- локус D6S305, расположенном в локусе 6q26 (прямой праймер SEQ ID NO: 25, 5 пмоль/мкл; обратный праймер SEQ ID NO: 26, меченный FAM, 5 пмоль/л);
- локус D6S446, расположенном в локусе 6q27 (прямой праймер SEQ ID NO: 27, 3,75 пмоль/мкл; обратный праймер SEQ ID NO: 28, меченный FAM, 3,75 пмоль/л);
- локус D6S261, расположенном в локусе 6q21-22 (прямой праймер SEQ ID NO: 29, 5 пмоль/мкл; обратный праймер SEQ ID NO: 30, меченный FAM, 5 пмоль/л).
4 пул:
- локус D6S1594, расположенном в локусе 6q21 (прямой праймер SEQ ID NO: 31, 3,75 пмоль/мкл; обратный праймер SEQ ID NO: 32, меченный FAM, 3,75 пмоль/л);
- локус D6S1719, расположенном в локусе 6q26-27 (прямой праймер SEQ ID NO: 33, 5 пмоль/мкл; обратный праймер SEQ ID NO: 34, меченный FAM, 5 пмоль/л);
- локус D6S415, расположенном в локусе 6q25.3 (прямой праймер SEQ ID NO: 35, 10 пмоль/мкл; обратный праймер SEQ ID NO: 36, меченный ROX, 10 пмоль/л);
- локус D6S430, расположенном в локусе 6q12 (прямой праймер SEQ ID NO: 37, 10 пмоль/мкл; обратный праймер SEQ ID NO: 38, меченный ROX, 10 пмоль/л);
- локус D6S407, расположенном в локусе 6q22-23 (прямой праймер SEQ ID NO: 39, 5 пмоль/мкл; обратный праймер SEQ ID NO: 40, меченный FAM, 5 пмоль/л).
Каждому пулу соответствует одна пробирка со смесью праймеров, которая подготавливается путем смешивания стоков синтезированных олигонуклеотидов в приведенных концентрациях, обеспечивающих наиболее благоприятные условия проведения ПЦР. Объем готовой смеси праймеров, необходимый для анализа одного образца - 1 мкл.
2) Реактивы для проведения мультиплексной ПЦР:
- 10х ПЦР-Буфер-Б (ООО "СИНТОЛ", Россия) в пробирках по 500 мкл из расчета 1 пробирка на 150 реакций;
- смесь dNTP (концентрация каждого дезоксинуклеотидтрифосфата 25 мМ) в пробирках по 500 мкл из расчета 1 пробирка на 150 реакций;
- 25 мМ раствор MgCl2 в пробирках по 500 мкл из расчета 1 пробирка на 300 реакций;
- Taq-полимераза 5 ед./мкл в пробирках по 1000 мкл из расчета 1 пробирка на 2000 реакций;
- деионизированная вода во флаконах по 50 мл из расчета 1 флакон на 3000 реакций.
Особенность заявляемого способа заключается в том, что определяют изменения совокупности 20 микросателлитных маркеров тест-системы. При реализации способа осуществляют анализ изменений микросателлитных локусов ДНК в образце опухолевой ткани при сравнении с контрольным образцом методом ПЦР на основании последующего анализа длин ПЦР-продуктов.
Амплификация исследуемых локусов производится в условиях 4 реакционных смесей соответственно 4 пулам праймеров методом мультиплексной ПЦР. Оптимальные сочетания специфичных пар праймеров к перечисленным микросателлитным локусам в 4 пулах, определенные на основании исключения вероятности взаимного отжига и образования димеров и с учетом лучшей визуализации отдельных ПЦР-продуктов, разделенных по длине и каналу флуоресценции, а также условия проведения ПЦР и соотношения концентраций реагентов являются оригинальной особенностью заявляемого изобретения.
Заявляемый способ осуществляется согласно описанной далее методике.
1. Подготовка материалов и компонентов
Исследуемый материал представлен образцом опухолевой ткани, в качестве которого допустимо использование следующих источников:
- фрагмент опухолевого биоптата (объемом не менее 0,5 мм3);
- срезы с парафиновых блоков (в количестве от 2 до 10 при толщине среза 10 мкм в зависимости от объема заключенного материала) с последующей депарафинизацией согласно стандартным методикам;
- клетки периферической крови или аспирата костного мозга при доказанном иными методами наличии лейкемизации или вовлечении в опухолевый процесс костного мозга (10 мл в пробирке с раствором ЭДТА).
Доля опухолевых клеток от общей клеточности образца должна быть не менее 10%, что определено чувствительностью молекулярного исследования.
В качестве отрицательного контроля используют внесение в состав реакционной смеси ПЦР деионизированный воды вместо матрицы ДНК.
В качестве парного нормального образца в параллельном исследовании целесообразно использовать клетки периферической крови того же пациента, а в случае лейкемизации - клетки буккального эпителия, что обеспечивает наличие контроля и достоверность анализа.
Фрагменты опухолевых биоптатов могут быть взяты в работу непосредственно после выполнения биопсии или после замораживания при температуре не выше минус 30°С без использования криоконсерванта.
2. Выделение ДНК из опухолевой ткани биоптатов и депарафинизированных срезов
Подготовку проводят по изложенной ранее методике [17]. Забор клеток аспирата костного мозга или периферической крови осуществляют в 10 мл пробирку с раствором ЭДТА. Выделение ДНК проводят по любой из стандартных методик.
ПЦР проводят в составе реакционной смеси путем смешивания следующих компонентов в 0,2 мл микропробирках:
- 3 мкл 10х буфера (ПЦР-Буфер-Б, ООО "СИНТОЛ", Россия);
- 3 мкл смеси dNTP (концентрация каждого дезоксинуклеотидтрифосфата 25 мМ);
- 1,5 мкл 25 мМ раствора MgCl2;
- не менее 20 нг геномной ДНК (в среднем в объеме водного раствора от 2 мкл до 5 мкл);
- 1 мкл одного из четырех пулов праймеров;
- 2,5 ед. Taq-полимеразы;
- деионизированная вода до общего объема реакционной смеси 25 мкл.
3. Постановка реакции
ПЦР проводят при следующих условиях:
- первичная денатурация 95°С 10 минут;
- 35 циклов денатурации при 95°С 40 секунд, отжига при 57°С 40 секунд, элонгации при 72°С 30 секунд;
- заключительная элонгация при 72°С 5 минут.
4. Учет результатов
Продукты амплификации в разведении 1:60-100 смешивают с формамидом в соотношении 1:3 и денатурируют при 95°С в течение 3 минут, после чего проводят фрагментный анализ на основе капиллярного электрофореза на генетическом анализаторе. Авторами заявляемого изобретения был использован генетический анализатор Нанофор-05 (ООО "СИНТОЛ", Россия).
5. Интерпретация результатов
Наличие делеции региона 6q определяют в случае гетерозиготного наследования на основании отсутствия пиков одного из аллелей или уменьшения интенсивности его флуоресценции по отношению к пику второго аллеля соответствующего микросателлитного локуса в опухолевой ткани при сравнении с контрольным образцом. Наличие делеции региона 6q у пациента с ФЛ относит его к группе высокого риска и позволяет предполагать у него неблагоприятное течение заболевания.
Сущность группы изобретений пояснена примерами конкретной реализации, которые не ограничивают объем прав.
Пример 1. Технические условия заявляемого способа были разработаны и отработаны с использованием образцов ДНК клеток периферической крови 4 здоровых доноров. В дополнительной группе из 28 здоровых доноров была доказана работоспособность и воспроизводимость разработанной диагностической тест-системы.
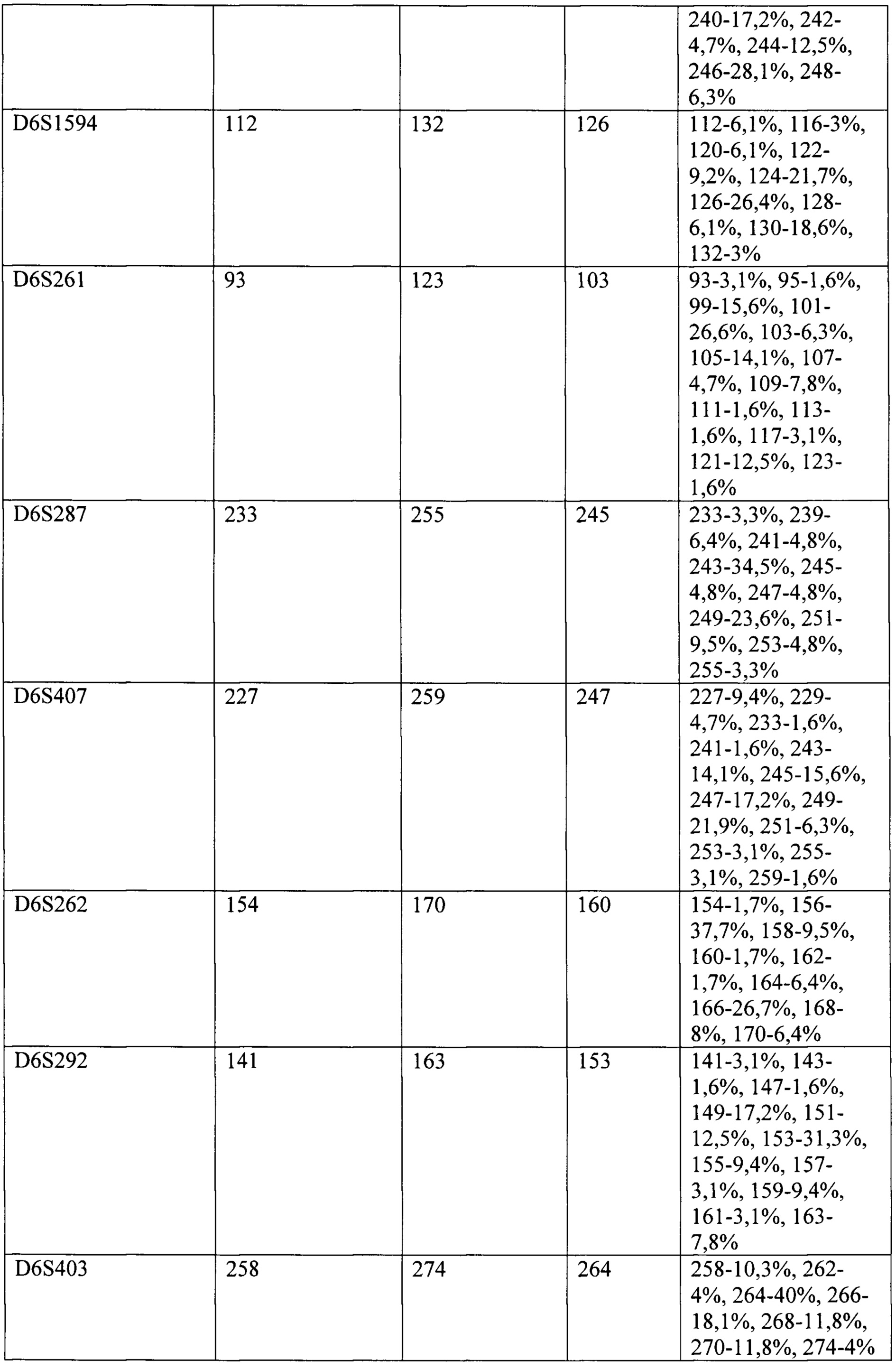
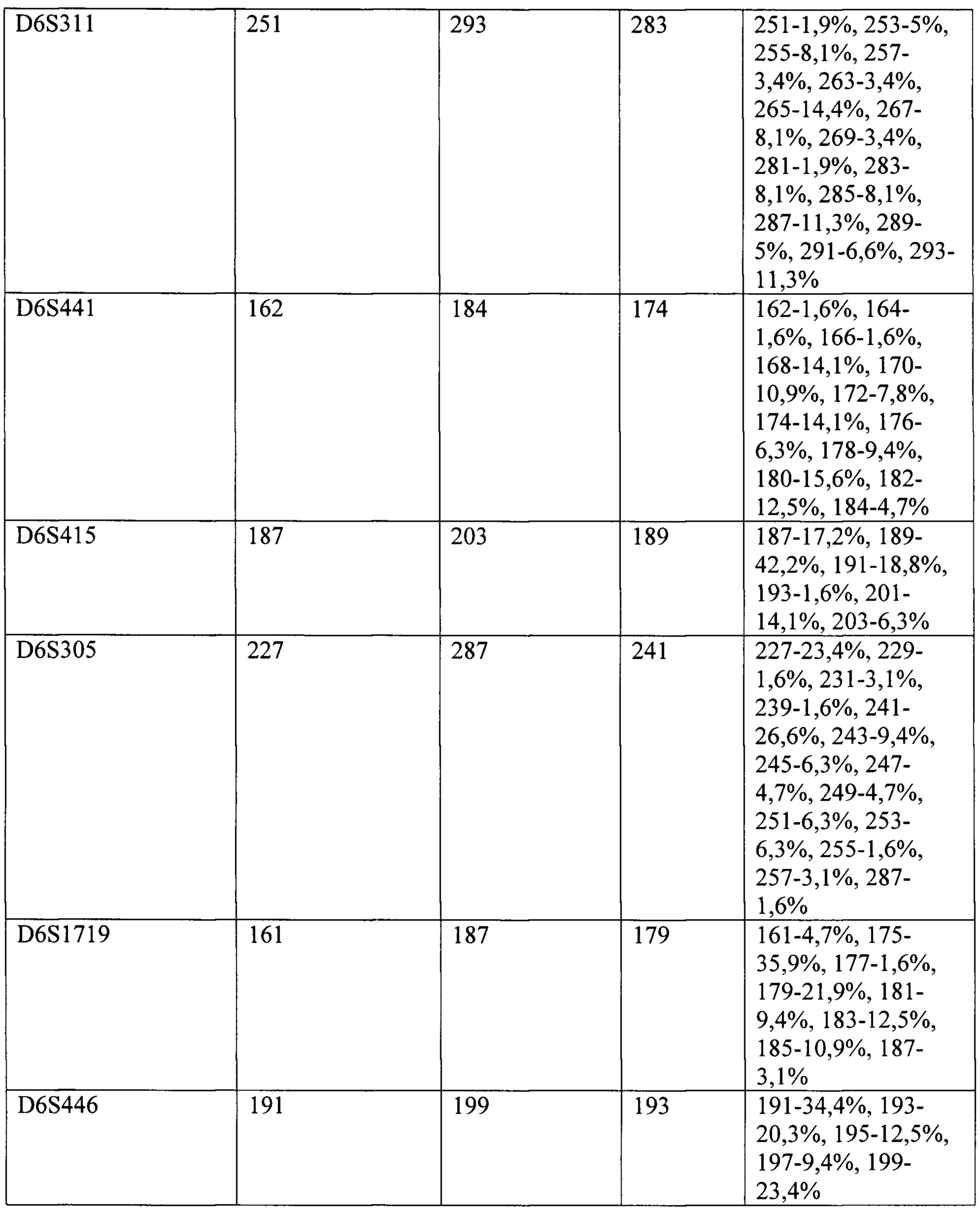
В таблице 1 представлены данные об аллельном разнообразии исследуемых микросателлитных локусов в донорской популяции.
На Фиг. 1-4 отображены электрофореграммы, полученные при анализе ДНК одного из доноров, соответственно пулам смесей праймеров и каналам флуоресценции.
Пример 2. Пациент X. Диагноз: фолликулярная лимфома 3 морфологического типа с трансформацией в крупноклеточную лимфому, 6 курсов химиотерапии 1 линии, прогрессия заболевания после окончания лечения в течение месяца, химиотерапия 2 линии, рефрактерность, смерть.
По данным стандартного цитогенетического исследования в опухоли выявлен комплексный кариотип с множественными хромосомными нарушениями: дополнительной хромосомой X, делецией короткого плеча хромосомы 1, дериватами хромосом 3, 6 и 11 (47XY,+Xdel(1)(p36),del(3)(?q23),add(6)(q26),del(6)(q26)ort(6;6)(q26;q26),add(11)(q25)[cp1]/47,XY,+X[10], idem der(3)del(3)(?q 13) [cp 12]/47,XY,+12 [1]/46,XY[6]).
На Фиг. 5 представлены результаты исследования панели микросателлитных локусов в контрольном и опухолевом образцах пациента X., а также примеры электрофореграмм отдельных локусов. По трем микросателлитным локусам (D6S292, D6S403, D6S311) в опухолевой ткани отмечена утрата одного из аллелей, что свидетельствует о наличии делеции соответствующего хромосомного региона. В данном случае протяженность делеции распространяется на цитогенетические регионы 6q23-25.
В рассмотренном примере молекулярное и цитогенетическое исследования выявили делецию 6q как фактор неблагоприятного прогноза у пациента с ФЛ с прогрессирующим течением заболевания. Проведенный анализ микросателлитного профиля подтвердил неблагоприятный прогноз течения заболевания и представил более точные данные локализации области потери генетического материала, что имеет фундаментальное значение для изучения патогенеза опухоли.
Пример 3. Пациент Т. Фолликулярная лимфома 3А морфологического типа, 6 курсов химиотерапии 1 линии, ремиссия заболевания, ранний рецидив через год после окончания лечения, химиотерапия 2 линии, вторая ремиссия.
На Фиг. 6 представлены результаты исследования панели микросателлитных локусов в контрольном и опухолевом образцах пациента Т., а также примеры электрофореграмм отдельных локусов. По тринадцати микросателлитным локусам (D6S430, D6S1681, D6S460, D6S1613, D6S434, D6S1594, D6S287, D6S407, D6S441, D6S415, D6S305, D6S1719, D6S446) в опухолевой ткани отмечена утрата одного из аллелей, что свидетельствует о наличии делеции соответствующего хромосомного региона. В приведенном случае протяженность делеции распространяется на три независимых цитогенетического региона, разделенных областями сохранения гетерозиготности: 6q12-21, 6q22-23, 6q25-27, что свидетельствует о сложном характере генетических нарушений у данного пациента. В практическом отношении у данного пациента с делецией 6q подтвердился неблагоприятный прогноз заболевания, а именно - развитие раннего рецидива.
У данного пациента отсутствовала техническая возможность проведения цитогенетического исследования материала опухоли, доступного в качестве парафиновых блоков. Таким образом, именно предложенный метод молекулярного исследования позволил расширить информацию о генетических аберрациях опухолевого клона.
Пример 4. Пациентка П. Фолликулярная морфологического типа, 6 курсов химиотерапии 1 линии, ремиссия.
У данной пациентки при исследовании микросателлитного профиля не были выявлены аберрации микросателлитных повторов, свидетельствующие о делеции 6q, что позволяло предположить благоприятный прогноз заболевания. Действительно, несмотря на наличие экстранодальных очагов поражения, что обычно сочетается с агрессивным течением ФЛ, данная пациентка находится в длительной полной ремиссии.
Таким образом, проведенные авторами исследования позволили определить набор олигонуклеотидных праймеров, разработать диагностическую тест-систему для выявления делеций области 6q при злокачественных новообразованиях и способ выявления пациентов с риском неблагоприятного течения фолликулярной лимфомы по наличию значимых делеций длинного плеча 6 хромосомы, что реализуется путем выполнения мультиплексной ПЦР с набором оригинальных олигонуклеотидных пар праймеров 20 микросателлитных локусов с последующего фрагментным анализом ПЦР-продуктов. Результаты, получаемые при осуществлении изобретения, применимы при определении характера последующего течения опухолевого заболевания на этапе первичной диагностики и могут быть полезны в дифференциации методов терапии, а также могут быть использованы для идентификации значимых в патогенезе опухолей областей хромосомных делеций, что в дальнейшем послужит основой направленного поиска вовлеченных онкогенов.
Источники информации, принятые во внимание при составлении описания к заявке на выдачу патента РФ на изобретение «Тест-система и способ выявления делеций длинного плеча 6 хромосомы»:
1. Tilly Н, Rossi A, Stamatoullas A, Lenormand В, Bigorgne С, Kimlin А, Monconduit М, Bastard С.Prognostic value of chromosomal abnormalities in follicular lymphoma. Blood. 1994 Aug 15; 84(4): 1043-9. PMID: 8049424.
2. Jarosova M, Hruba M, Oltova A, Plevova K, Kruzova L, Kriegova E, Fillerova R, Koritakova E, Doubek M, Lysak D, Prochazka V, Mraz M, Indrak K, Papajik T. Chromosome 6q deletion correlates with poor prognosis and low relative expression of FOXO3 in chronic lymphocytic leukemia patients. Am J Hematol. 2017 Oct; 92(10):E604-E607. doi: 10.1002/ajh.24852. Epub 2017 Jul 29. PMID: 28699185.
3. Stilgenbauer S, Bullinger L, Benner A, Wildenberger K, Bentz M, Dohner K, Ho AD, Lichter P, Dohner H. Incidence and clinical significance of 6q deletions in В cell chronic lymphocytic leukemia. Leukemia. 1999 Sep; 13(9):1331-4. doi: 10.1038/sj.leu.2401499. PMID: 10482982.
4. Remke M, Pfister S, Kox C, Toedt G, Becker N, Benner A, Werft W, Breit S, Liu S, Engel F, Wittmann A, Zimmermann M, Stanulla M, Schrappe M, Ludwig WD, Bartram CR, Radlwimmer B, Muckenthaler MU, Lichter P, Kulozik AE. High-resolution genomic profiling of childhood T-ALL reveals frequent copy-number alterations affecting the TGF-beta and PI3K-AKT pathways and deletions at 6q15-16.1 as a genomic marker for unfavorable early treatment response. Blood. 2009 Jul 30; 114(5):1053-62. doi: 10.1182/blood-2008-10-186536. Epub 2009 Apr 30. PMID: 19406988.
5. Gachet S, El-Chaar T, Avran D, Genesca E, Catez F, Quentin S, Delord M, Briot D, Meunier G, Hernandez L, Pla M, Smits WK, Buijs-Gladdines JG, Van Loocke W, Menschaert G, Taghon T, Van Vlierberghe P, Meijerink JP, Baruchel A, Dombret H, Clappier E, Diaz JJ, Gazin C, Sigaux F, Soulier J. Deletion 6q Drives T-cell Leukemia Progression by Ribosome Modulation. Cancer Discov. 2018 Dec; 8(12):1614-1631. doi: 10.1158/2159-8290.CD-17-0831. Epub 2018 Sep 28. PMID: 30266814.
6. Bonn BR, Rohde M, Zimmermann M, Krieger D, Oschlies I, Niggli F, Wrobel G, Attarbaschi A, Escherich G, Klapper W, Reiter A, Burkhardt B. Incidence and prognostic relevance of genetic variations in T-cell lymphoblastic lymphoma in childhood and adolescence. Blood. 2013 Apr 18; 121 (16):3153-60. doi: 10.1182/blood-2012-12-474148. Epub 2013 Feb 8. PMID: 23396305.
7. Kluth M, Jung S, Habib O, et al. Deletion lengthening at chromosomes 6q and 16q targets multiple tumor suppressor genes and is associated with an increasingly poor prognosis in prostate cancer. Oncotarget. 2017; 8(65): 108923-108935. Published 2017 Nov 11. doi:10.18632/oncotarget.22408
8. Mazurenko NN, Bliev AIu, Bidzhieva BA, Peskov DIu, Snigur NV, Savinova EB, Kiselev FL. [Loss of heterozygosity at chromosome 6 as a marker of early genetic alterations in cervical intraepithelial neoplasias and microinvasive carcinomas]. Mol Biol (Mosk). 2006 May-Jun; 40(3):436-47. Russian. PMID: 16813163.
9. Oricchio E, Katanayeva N, Donaldson MC, Sungalee S, Pasion JP, Beguelin W, Battistello E, Sanghvi VR, Jiang M, Jiang Y, Teater M, Parmigiani A, Budanov AV, Chan FC, Shah SP, Kridel R, Melnick AM, Ciriello G, Wendel HG. Genetic and epigenetic inactivation of SESTRIN1 controls mTORC1 and response to EZH2 inhibition in follicular lymphoma. Sci Transl Med. 2017 Jun 28; 9(396):eaak9969. doi: 10.1126/scitranslmed.aak9969. PMID: 28659443; PMCID: PMC5559734.
10. Offit K, Parsa NZ, Gaidano G, Filippa DA, Louie D, Pan D, Jhanwar SC, Dalla-Favera R, Chaganti RS. 6q deletions define distinct clinico-pathologic subsets of non-Hodgkin's lymphoma. Blood. 1993 Oct 1; 82(7):2157-62. PMID: 8104536.
11. Merup M, Moreno TC, Heyman M, Detlofsson R, Rasool O, Liu Y, Juliusson G, Gahrton G, Einhorn S. 6q deletions in in acute lymphoblastic leukemia and non-Hodgkin's lymphomas. Blood. 1998 May 1; 91(9):3397-400. PMID: 9558398.
12. Jackson A, Carrara P, Duke V, Sinclair P, Papaioannou M, Harrison CJ, Foroni L. Deletion of 6q16-q21 in human lymphoid malignancies: a mapping and deletion analysis. Cancer Res. 2000 Jun 1; 60(11):2775-9. PMID: 10850412.
13. Broman KW, Murray JC, Sheffield VC, White RL, Weber JL. Comprehensive human genetic maps: individual and sex-specific variation in recombination. Am J Hum Genet. 1998 Sep; 63(3):861-9. doi: 10.1086/302011. PMID: 9718341; PMCID: PMC1377399.
14. Gyapay G, Morissette J, Vignal A, Dib C, Fizames C, Millasseau P, Marc S, Bernardi G, Lathrop M, Weissenbach J. The 1993-94 human genetic linkage map. Nat Genet. 1994 Jun; 7(2 Spec No):246-339. doi: 10.1038/ng0694supp-246. PMID: 7545953.
15. Inoue M, Marx A, Zettl A, Strobel P, Muller-Hermelink HK, Starostik P. Chromosome 6 suffers frequent and multiple aberrations in thymoma. Am J Pathol. 2002 Oct; 161(4): 1507-13. doi: 10.1016/S0002-9440(10)64426-4. PMID: 12368223; PMCID: PMC 1867301.
16. Starostik P, Greiner A, Schultz A, Zettl A, Peters K, Rosenwald A, Kolve M, Genetic aberrations common in gastric high-grade large B-cell lymphoma. Blood. 2000 Feb 15; 95(4):1180-7. PMID: 10666188.
17. Sidorova JV, Biderman BV, Nikulina EE, Sudarikov AB. A simple and efficient method for DNA extraction from skin and paraffin-embedded tissues applicable to T-cell clonality assays. Exp Dermatol. 2012; 21(1):57-60. doi:10.1111/j.1600-0625.2011.01375.x
--->
Перечень последовательностей
<110> Федеральное государственное бюджетное учреждение «Национальный
медицинский исследовательский центр гематологии» Министерства
здравоохранения Российской Федерации (ФГБУ "НМИЦ гематологии" Минздрава
России)
Federal Governmental Budgetary Institution «National Research Center for
Hematology»
<120> ТЕСТ-СИСТЕМА И СПОСОБ ВЫЯВЛЕНИЯ ДЕЛЕЦИЙ ДЛИННОГО ПЛЕЧА 6 ХРОМОСОМЫ
<160> 40
<210> 1
<211> 22
<212> DNA
<213> Homo sapiens
<400> 1
ACACAGGCAT TCAAATCAGA GC
<210> 2
<211> 24
<212> DNA
<213> Homo sapiens
<400> 2
CACTCACCAC CTAAATGTTT CAGT
<210> 3
<211> 20
<212> DNA
<213> Homo sapiens
<400> 3
CAACACACAG GTAGTCCCCC
<210> 4
<211> 19
<212> DNA
<213> Homo sapiens
<400> 4
AGCTCAGGGC TTATGCCAG
<210> 5
<211> 23
<212> DNA
<213> Homo sapiens
<400> 5
TCTGAAGAAA GAGGCGTTAA CCA
<210> 6
<211> 17
<212> DNA
<213> Homo sapiens
<400> 6
CCGGCCCAAA GTCTTGT
<210> 7
<211> 23
<212> DNA
<213> Homo sapiens
<400> 7
AGGAAGACTC CACCTCATTT AAA
<210> 8
<211> 22
<212> DNA
<213> Homo sapiens
<400> 8
TCAAGATTAA GTTCCTGGCC AT
<210> 9
<211> 22
<212> DNA
<213> Homo sapiens
<400> 9
AATTCACAAG ACACAATCTC AG
<210> 10
<211> 25
<212> DNA
<213> Homo sapiens
<400> 10
AGAACTAAAG TTGCCTGTTC TTGTA
<210> 11
<211> 20
<212> DNA
<213> Homo sapiens
<400> 11
CCCAGGCTTA TAAAGGTGGC
<210> 12
<211> 20
<212> DNA
<213> Homo sapiens
<400> 12
TGGTTCTCTC ACCCTTTTGT
<210> 13
<211> 25
<212> DNA
<213> Homo sapiens
<400> 13
GCTTCTGTAA TTTTCTATAG CCTAC
<210> 14
<211> 20
<212> DNA
<213> Homo sapiens
<400> 14
GCCTTTGCCC TGAGTATTGG
<210> 15
<211> 20
<212> DNA
<213> Homo sapiens
<400> 15
TGCCTTCTTA ATGCTGCTCA
<210> 16
<211> 20
<212> DNA
<213> Homo sapiens
<400> 16
ACTTGCTTCT CTTGCCTCAA
<210> 17
<211> 20
<212> DNA
<213> Homo sapiens
<400> 17
GGCAGTGGAC ATGGAACCTT
<210> 18
<211> 20
<212> DNA
<213> Homo sapiens
<400> 18
TGGATTCAGA GCCCAGGAAG
<210> 19
<211> 20
<212> DNA
<213> Homo sapiens
<400> 19
TTCTCTCGCT CTCTCACAGC
<210> 20
<211> 20
<212> DNA
<213> Homo sapiens
<400> 20
ATTCCAGAGA GCGGGGCAAA
<210> 21
<211> 21
<212> DNA
<213> Homo sapiens
<400> 21
AGATAGCCGA ATATGCAACC A
<210> 22
<211> 23
<212> DNA
<213> Homo sapiens
<400> 22
GGACTCTCAG TTAACAAGGA GCA
<210> 23
<211> 25
<212> DNA
<213> Homo sapiens
<400> 23
AACAATATTT GGTGACTGTT AAAGG
<210> 24
<211> 25
<212> DNA
<213> Homo sapiens
<400> 24
TGGACAAATT GATTAGGAAG TAAAG
<210> 25
<211> 20
<212> DNA
<213> Homo sapiens
<400> 25
TCCTCTCCAC CAGCGTTAGA
<210> 26
<211> 20
<212> DNA
<213> Homo sapiens
<400> 26
GTTTAGATCC CAGGCCTGCA
<210> 27
<211> 20
<212> DNA
<213> Homo sapiens
<400> 27
AGGGATGTCT ACACCTACAC
<210> 28
<211> 20
<212> DNA
<213> Homo sapiens
<400> 28
GGGAGGACGT TCTGGTTTCA
<210> 29
<211> 22
<212> DNA
<213> Homo sapiens
<400> 29
TGAAACCCTG TCTCACTGCA TA
<210> 30
<211> 21
<212> DNA
<213> Homo sapiens
<400> 30
TATAGGACCA TGCCATTAGG C
<210> 31
<211> 21
<212> DNA
<213> Homo sapiens
<400> 31
GCCTGAGACT CTTCAATGCC T
<210> 32
<211> 20
<212> DNA
<213> Homo sapiens
<400> 32
AGCTTAAAGT GTAGGACGGT
<210> 33
<211> 21
<212> DNA
<213> Homo sapiens
<400> 33
GGAACTACTC CCATTCCAAC C
<210> 34
<211> 22
<212> DNA
<213> Homo sapiens
<400> 34
GAGATACAAG CAGGAGGTAG CA
<210> 35
<211> 20
<212> DNA
<213> Homo sapiens
<400> 35
TCGGCCACCA GAAGTAAAGC
<210> 36
<211> 20
<212> DNA
<213> Homo sapiens
<400> 36
GGAGGTGCAG CATCTTTCCT
<210> 37
<211> 22
<212> DNA
<213> Homo sapiens
<400> 37
CAGCATAGTT CCTTCAAGCA CA
<210> 38
<211> 21
<212> DNA
<213> Homo sapiens
<400> 38
GGCTTCCCCT TCACTTCTTC A
<210> 39
<211> 17
<212> DNA
<213> Homo sapiens
<400> 39
AAAAGTACCT CCCGCCC
<210> 40
<211> 21
<212> DNA
<213> Homo sapiens
<400> 40
GGGGACAGTT ACCTTTGGAG T
<---
Claims (53)
1. Набор олигонуклеотидных пар праймеров для специфической амплификации двадцати микросателлитных локусов длинного плеча 6 хромосомы человека (6q): D6S430, расположенный в локусе 6q12, D6S1681, расположенный в локусе 6q14, D6S460, расположенный в локусе 6q14-15, D6S1613, расположенный в локусе 6q16, D6S300, расположенный в локусе 6q16-21, D6S434, расположенный в локусе 6q21, D6S447, расположенный в локусе 6q21, D6S1594, расположенный в локусе 6q21, D6S261, расположенный в локусе 6q21-22, D6S287, расположенный в локусе 6q22, D6S407, расположенный в локусе 6q22-23, D6S262, расположенный в локусе 6q23, D6S292, расположенный в локусе 6q23, D6S403, расположенный в локусе 6q23, D6S311, расположенный в локусе 6q24-25, D6S441, расположенный в локусе 6q25, D6S415, расположенный в локусе 6q25.3, D6S305, расположенный в локусе 6q26, D6S1719, расположенный в локусе 6q26-27, D6S446, расположенный в локусе 6q27, имеющих следующие нуклеотидные последовательности SEQ ID NO: 1 - SEQ ID NO: 40:
D6S430-F: 5'-CAGCATAGTTCCTTCAAGCACA-3',
D6S430-R: 5'-ROX-GGCTTCCCCTTCACTTCTTCA-3',
D6S1681 -F: 5'-ACACAGGCATTCAAATCAGAGC-3',
D6S1681 -R: 5'-FAM-CACTCACCACCTAAATGTTTCAGT-3',
D6S434-F: 5'-CAACACACAGGTAGTCCCCC-3',
D6S434-R: 5'-ROX-AGCTCAGGGCTTATGCCAG-3',
D6S261 -F: 5'-TGAAACCCTGTCTCACTGC ATA-3',
D6S261 -R: 5'-FAM-TATAGGACCATGCCATTAGGC-3',
D6S403-F: 5'-TCTGAAGAAAGAGGCGTTAACCA-3,
D6S403-R: 5'-FAM-CCGGCCCAAAGTCTTGT-3',
D6S460-F: 5'-CCCAGGCTTATAAAGGTGGC-3',
D6S460-R: 5'-ROX-TGGTTCTCTCACCCTTTTGT-3',
D6S300-F: 5'-TGCCTTCTTAATGCTGCTCA-3',
D6S300-R: 5'-F AM- ACTTGCTTCTCTTGCCTC AA-3',
D6S1594-F: 5'-GCCTGAGACTCTTCAATGCCT-3',
D6S1594-R: 5'-FAM-AGCTTAAAGTGTAGGACGGT-3',
D6S287-F: 5'-GCTTCTGTAATTTTCTATAGCCTAC-3',
D6S287-R: 5'-ROX-GCCTTTGCCCTGAGTATTGG-3',
D6S292-F: 5'-AATTCACAAGACACAATCTCAG-3',
D6S292-R: 5'-FAM-AGAACTAAAGTTGCCTGTTCTTGTA-3,
D6S311-F: 5'-GGCAGTGGACATGGAACCTT-3',
D6S311-R: 5'-FAM-TGGATTCAGAGCCCAGGAAG-3',
D6S447-F: 5'-TTCTCTCGCTCTCTCACAGC-3',
D6S447-R: 5'-ROX-ATTCCAGAGAGCGGGGCAAA-3',
D6S262-F: 5'-AGATAGCCGAATATGCAACCA-3',
D6S262-R: 5'-FAM-GGACTCTCAGTTAACAAGGAGCA-3',
D6S441-F: 5'-AAC AATATTTGGTGACTGTTAAAGG-3',
D6S441 -R: 5'-ROX-TGGACAAATTGATTAGGAAGTAAAG-3',
D6S305-F: 5'-TCCTCTCCACCAGCGTTAGA-3',
D6S305-R: 5'-FAM-GTTTAGATCCCAGGCCTGCA-3',
D6S446-F: 5'-AGGGATGTCTACACCTACAC-3',
D6S446-R: 5'-FAM-GGGAGGACGTTCTGGTTTCA-3',
D6S415-F: 5'-TCGGCCACCAGAAGTAAAGC-3',
D6S415-R: 5'-ROX-GGAGGTGCAGCATCTTTCCT-3',
D6S1719-F: 5'-GGAACTACTCCCATTCCAACC-3',
D6S1719-R: 5'-FAM-GAGATACAAGCAGGAGGTAGCA-3,
D6S407-F: 5'-AAAAGTACCTCCCGCCC-3',
D6S407-R: 5'-FAM-GGGGACAGTTACCTTTGGAGT-3',
D6S1613-F: 5'-AGGAAGACTCCACCTCATTTAAA-3',
D6S1613-R: 5'-ROX-TCAAGATTAAGTTCCTGGCCAT-3'.
2. Тест-система для определения делеций длинного плеча 6 хромосомы (6q) методом мультиплексной полимеразной цепной реакции (ПЦР), состоящая из набора олигонуклеотидных пар праймеров по п. 1, разделенного на 4 пула-смеси праймеров, исключающих вероятность взаимного отжига и образования димеров, и с учетом лучшей визуализации отдельных ПЦР-продуктов:
1 пул - D6S1681 - 2,5 пмоль/мкл, D6S434 - 10 пмоль/мкл, D6S403 - 5 пмоль/мкл, D6S1613 - 5 пмоль/мкл;
2 пул - D6S292 - 5 пмоль/мкл, D6S460 - 10 пмоль/мкл, D6S287 - 10 пмоль/мкл, D6S300 - 4 пмоль/мкл, D6S311 - 4 пмоль/мкл;
3 пул - D6S447 - 10 пмоль/мкл, D6S262 - 4 пмоль/мкл, D6S441 - 15 пмоль/мкл, D6S305 - 5 пмоль/мкл, D6S446 - 3,75 пмоль/мкл, D6S261 - 5 пмоль/мкл;
4 пул - D6S1594 - 3,75 пмоль/мкл, D6S1719 - 5 пмоль/мкл, D6S415 - 10 пмоль/мкл, D6S430 - 10 пмоль/мкл, D6S407 - 5 пмоль/мкл;
реактивов для проведения ПЦР: 10х ПЦР-Буфер-Б, смесь dNTP по 25 мМ, 25 мМ раствор MgCl2, Taq-полимераза, деионизированная вода.
3. Способ выявления пациентов с риском неблагоприятного течения фолликулярной лимфомы по наличию значимых делеций длинного плеча 6 хромосомы (6q) с помощью тест-системы по п. 2, включающий следующие этапы: сбор и подготовка парных образцов опухоли и контрольной ткани, при этом в качестве образца опухолевой ткани допустимо использование фрагментов опухолевого биоптата, срезов с парафиновых блоков с последующей депарафинизацией, клеток периферической крови или аспирата костного мозга, в качестве парного нормального образца используют клетки периферической крови того же пациента, а в случае лейкемизации - клетки буккального эпителия; выделение ДНК, проведение мультиплексной ПЦР с помощью тест-системы по п. 2 для каждого образца при следующих условиях:
первичная денатурация 95°С 10 минут,
35 циклов денатурации при 95°С 40 секунд, отжига при 57°С 40 секунд,
элонгации при 72°С 30 секунд,
заключительная элонгация при 72°С 5 минут;
продукты амплификации в разведении 1:60-100 смешивают с формамидом в соотношении 1:3 и денатурируют при 95°С в течение 3 минут, после чего проводят фрагментный анализ на основе капиллярного электрофореза на генетическом анализаторе; интерпретацию полученных данных, при этом наличие делеции региона 6q в случае гетерозиготного наследования на основании отсутствия пиков одного из аллелей или уменьшения интенсивности его флуоресценции по отношению к пику второго аллеля соответствующего микросателлитного локуса в опухолевой ткани при сравнении с контрольным образцом позволяет выделять группу пациентов с риском неблагоприятного течения фолликулярной лимфомы.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2021121807A RU2770892C1 (ru) | 2021-07-22 | 2021-07-22 | Тест-система и способ выявления делеций длинного плеча 6 хромосомы |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2021121807A RU2770892C1 (ru) | 2021-07-22 | 2021-07-22 | Тест-система и способ выявления делеций длинного плеча 6 хромосомы |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2770892C1 true RU2770892C1 (ru) | 2022-04-25 |
Family
ID=81306254
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2021121807A RU2770892C1 (ru) | 2021-07-22 | 2021-07-22 | Тест-система и способ выявления делеций длинного плеча 6 хромосомы |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2770892C1 (ru) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2717309C2 (ru) * | 2018-08-01 | 2020-03-20 | Общество с ограниченной ответственностью "ОНКОДИАГНОСТИКА АТЛАС" | Способ определения микросателлитной нестабильности |
| US20200255913A1 (en) * | 2012-04-10 | 2020-08-13 | Vib Vzw | Novel Markers for Detecting Microsatellite Instability in Cancer and Determining Synthetic Lethality with Inhibition of the DNA Base Excision Repair Pathway |
-
2021
- 2021-07-22 RU RU2021121807A patent/RU2770892C1/ru active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20200255913A1 (en) * | 2012-04-10 | 2020-08-13 | Vib Vzw | Novel Markers for Detecting Microsatellite Instability in Cancer and Determining Synthetic Lethality with Inhibition of the DNA Base Excision Repair Pathway |
| RU2717309C2 (ru) * | 2018-08-01 | 2020-03-20 | Общество с ограниченной ответственностью "ОНКОДИАГНОСТИКА АТЛАС" | Способ определения микросателлитной нестабильности |
Non-Patent Citations (4)
| Title |
|---|
| GYAPAY G. et al., The 1993-94 Généthon human genetic linkage map, Nat Genet, 1994, Vol. 7,No 2 Spec, pp. 246-339. * |
| INOUE M. et al., Chromosome 6 suffers frequent and multiple aberrations in thymoma, Am J Pathol, 2002, Vol. 161, No. 4, pp. 1507-13. * |
| TAKEUCH S. et al., Frequent loss of heterozygosity on the long arm of chromosome 6: identification of two distinct regions of deletion in childhood acute lymphoblastic leukemia, Cancer Res, 1998, Vol. 58, No 12, pp. 2618-23. * |
| TAKEUCH S. et al., Frequent loss of heterozygosity on the long arm of chromosome 6: identification of two distinct regions of deletion in childhood acute lymphoblastic leukemia, Cancer Res, 1998, Vol. 58, No 12, pp. 2618-23. GYAPAY G. et al., The 1993-94 Généthon human genetic linkage map, Nat Genet, 1994, Vol. 7,No 2 Spec, pp. 246-339. INOUE M. et al., Chromosome 6 suffers frequent and multiple aberrations in thymoma, Am J Pathol, 2002, Vol. 161, No. 4, pp. 1507-13. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US6465177B1 (en) | Detection of loss of heterozygosity in tumor and serum of melanoma patients | |
| CA2231349C (en) | Amplifications of chromosomal region 20q13 as a prognostic indicator in breast cancer | |
| Bièche et al. | Two distinct amplified regions at 17q11–q21 involved in human primary breast cancer | |
| Choi et al. | Gene expression profiles in squamous cell cervical carcinoma using array-based comparative genomic hybridization analysis | |
| Siu et al. | Consistent patterns of allelic loss in natural killer cell lymphoma | |
| US6893820B1 (en) | Detection of methylated CpG rich sequences diagnostic for malignant cells | |
| US5925519A (en) | Genetic alterations associated with prostate cancer | |
| Maris et al. | Comprehensive analysis of chromosome 1p deletions in neuroblastoma | |
| US6794135B1 (en) | Method for detection of 5T4 RNA in plasma or serum | |
| Nakamori et al. | Genetic detection of colorectal cancer cells in circulation and lymph nodes | |
| ERILL et al. | Diagnostic utility of K-ras mutations in fine-needle aspirates of pancreatic masses | |
| Koike et al. | Frequent loss of heterozygosity in the region of the D7S523 locus in advanced ovarian cancer | |
| Brass et al. | Amplification of the genes BCHE and SLC2A2 in 40% of squamous cell carcinoma of the lung | |
| Meyers et al. | Analysis of the int-1, int-2, c-myc, and neu oncogenes in human breast carcinomas | |
| Scarisbrick et al. | Allelotyping in mycosis fungoides and Sezary syndrome: common regions of allelic loss identified on 9p, 10q, and 17p | |
| Fukumoto et al. | Association of Ki-ras with amplified DNA sequences, detected in human ovarian carcinomas by a modified in-gel renaturation assay | |
| JP2009532022A (ja) | Top2a遺伝子異常を用いた高リスク乳癌患者の予後を行う方法 | |
| Nagahata et al. | Correlation of allelic losses and clinicopathological factors in 504 primary breast cancers | |
| Emi et al. | Allelic loss at 1p34, 13q12, 17p13. 3, and 17q21. 1 correlates with poor postoperative prognosis in breast cancer | |
| RU2770892C1 (ru) | Тест-система и способ выявления делеций длинного плеча 6 хромосомы | |
| Drunat et al. | Quantification of TEL–AML1 transcript for minimal residual disease assessment in childhood acute lymphoblastic leukaemia | |
| Matsumoto et al. | Loss of heterozygosity at 3p24–p25 as a prognostic factor in breast cancer | |
| Pettus et al. | Multiple abnormalities detected by dye reversal genomic microarrays in prostate cancer: a much greater sensitivity than conventional cytogenetics | |
| Chen et al. | Technical approach for the study of the genetic evolution of breast cancer from paraffin-embedded tissue sections | |
| RU2772504C1 (ru) | Тест-система и способ выявления делеций гена SESN1 |