RU2744846C1 - Способ лечения острой печёночной недостаточности - Google Patents
Способ лечения острой печёночной недостаточности Download PDFInfo
- Publication number
- RU2744846C1 RU2744846C1 RU2020119914A RU2020119914A RU2744846C1 RU 2744846 C1 RU2744846 C1 RU 2744846C1 RU 2020119914 A RU2020119914 A RU 2020119914A RU 2020119914 A RU2020119914 A RU 2020119914A RU 2744846 C1 RU2744846 C1 RU 2744846C1
- Authority
- RU
- Russia
- Prior art keywords
- liver
- cells
- srna
- resection
- extensive
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 61
- 208000007788 Acute Liver Failure Diseases 0.000 title claims abstract description 21
- 206010000804 Acute hepatic failure Diseases 0.000 title claims abstract description 21
- 231100000836 acute liver failure Toxicity 0.000 title claims abstract description 20
- 238000011282 treatment Methods 0.000 title abstract description 26
- 210000004185 liver Anatomy 0.000 claims abstract description 142
- 241001465754 Metazoa Species 0.000 claims abstract description 37
- ZWGNFOFTMJGWBF-VZSHSMSCSA-N (2s)-2-amino-3-(1h-imidazol-5-yl)propanoic acid;(2s)-2-amino-3-(1h-indol-3-yl)propanoic acid;2-oxopentanedioic acid Chemical compound OC(=O)CCC(=O)C(O)=O.OC(=O)[C@@H](N)CC1=CN=CN1.C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 ZWGNFOFTMJGWBF-VZSHSMSCSA-N 0.000 claims abstract description 19
- 210000005228 liver tissue Anatomy 0.000 claims abstract description 19
- 238000002474 experimental method Methods 0.000 claims abstract description 17
- 238000010171 animal model Methods 0.000 claims abstract description 5
- 238000002271 resection Methods 0.000 claims description 62
- 210000001185 bone marrow Anatomy 0.000 claims description 10
- 210000005087 mononuclear cell Anatomy 0.000 claims description 8
- 230000006735 deficit Effects 0.000 claims description 6
- 230000015572 biosynthetic process Effects 0.000 claims description 3
- 230000008569 process Effects 0.000 abstract description 33
- 230000008929 regeneration Effects 0.000 abstract description 26
- 238000011069 regeneration method Methods 0.000 abstract description 26
- 241000842783 Orna Species 0.000 abstract description 24
- 230000000694 effects Effects 0.000 abstract description 18
- 230000006698 induction Effects 0.000 abstract description 15
- 210000002798 bone marrow cell Anatomy 0.000 abstract description 12
- 239000003814 drug Substances 0.000 abstract description 11
- 230000001105 regulatory effect Effects 0.000 abstract description 11
- 230000001965 increasing effect Effects 0.000 abstract description 10
- 230000007812 deficiency Effects 0.000 abstract description 4
- 239000000126 substance Substances 0.000 abstract description 3
- 108020004566 Transfer RNA Proteins 0.000 description 61
- 210000004027 cell Anatomy 0.000 description 51
- 201000000760 cerebral cavernous malformation Diseases 0.000 description 43
- 230000004900 autophagic degradation Effects 0.000 description 35
- 241000700159 Rattus Species 0.000 description 29
- 208000009304 Acute Kidney Injury Diseases 0.000 description 25
- 208000033626 Renal failure acute Diseases 0.000 description 25
- 201000011040 acute kidney failure Diseases 0.000 description 25
- 208000012998 acute renal failure Diseases 0.000 description 25
- 239000000243 solution Substances 0.000 description 25
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 21
- 238000011084 recovery Methods 0.000 description 21
- 230000000394 mitotic effect Effects 0.000 description 17
- 230000001172 regenerating effect Effects 0.000 description 17
- 210000000056 organ Anatomy 0.000 description 16
- 230000007423 decrease Effects 0.000 description 14
- 230000003044 adaptive effect Effects 0.000 description 11
- 210000003494 hepatocyte Anatomy 0.000 description 10
- 210000000130 stem cell Anatomy 0.000 description 10
- 238000003860 storage Methods 0.000 description 10
- 108700011259 MicroRNAs Proteins 0.000 description 9
- 210000005229 liver cell Anatomy 0.000 description 9
- 230000001461 cytolytic effect Effects 0.000 description 8
- 239000000284 extract Substances 0.000 description 8
- 239000000203 mixture Substances 0.000 description 8
- 239000003755 preservative agent Substances 0.000 description 8
- 230000002335 preservative effect Effects 0.000 description 8
- 102000004190 Enzymes Human genes 0.000 description 7
- 108090000790 Enzymes Proteins 0.000 description 7
- 230000004913 activation Effects 0.000 description 7
- 230000001413 cellular effect Effects 0.000 description 7
- 238000011161 development Methods 0.000 description 7
- 230000018109 developmental process Effects 0.000 description 7
- 230000002631 hypothermal effect Effects 0.000 description 7
- 238000002360 preparation method Methods 0.000 description 7
- 210000001519 tissue Anatomy 0.000 description 7
- 108010082126 Alanine transaminase Proteins 0.000 description 6
- 108010033918 Alanine-glyoxylate transaminase Proteins 0.000 description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- 230000006907 apoptotic process Effects 0.000 description 6
- 230000034994 death Effects 0.000 description 6
- 231100000517 death Toxicity 0.000 description 6
- 230000006870 function Effects 0.000 description 6
- 230000001939 inductive effect Effects 0.000 description 6
- 238000001356 surgical procedure Methods 0.000 description 6
- 230000004083 survival effect Effects 0.000 description 6
- 102100036475 Alanine aminotransferase 1 Human genes 0.000 description 5
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 5
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 5
- 206010019663 Hepatic failure Diseases 0.000 description 5
- 230000009089 cytolysis Effects 0.000 description 5
- 230000013632 homeostatic process Effects 0.000 description 5
- 238000002955 isolation Methods 0.000 description 5
- 208000007903 liver failure Diseases 0.000 description 5
- 231100000835 liver failure Toxicity 0.000 description 5
- 230000003908 liver function Effects 0.000 description 5
- 230000002062 proliferating effect Effects 0.000 description 5
- 230000008439 repair process Effects 0.000 description 5
- 230000035882 stress Effects 0.000 description 5
- 208000011580 syndromic disease Diseases 0.000 description 5
- 238000002054 transplantation Methods 0.000 description 5
- 206010057248 Cell death Diseases 0.000 description 4
- 208000010334 End Stage Liver Disease Diseases 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 206010067125 Liver injury Diseases 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 230000006978 adaptation Effects 0.000 description 4
- 230000000735 allogeneic effect Effects 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 208000011444 chronic liver failure Diseases 0.000 description 4
- 230000007774 longterm Effects 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 230000007246 mechanism Effects 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- 239000002679 microRNA Substances 0.000 description 4
- 239000012071 phase Substances 0.000 description 4
- 230000002980 postoperative effect Effects 0.000 description 4
- 238000004321 preservation Methods 0.000 description 4
- 210000002966 serum Anatomy 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- 238000001228 spectrum Methods 0.000 description 4
- 238000002560 therapeutic procedure Methods 0.000 description 4
- 239000012224 working solution Substances 0.000 description 4
- YXHLJMWYDTXDHS-IRFLANFNSA-N 7-aminoactinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=C(N)C=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 YXHLJMWYDTXDHS-IRFLANFNSA-N 0.000 description 3
- 108700012813 7-aminoactinomycin D Proteins 0.000 description 3
- 206010002091 Anaesthesia Diseases 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 206010028980 Neoplasm Diseases 0.000 description 3
- 210000000683 abdominal cavity Anatomy 0.000 description 3
- 230000001154 acute effect Effects 0.000 description 3
- 230000037005 anaesthesia Effects 0.000 description 3
- 239000008346 aqueous phase Substances 0.000 description 3
- 230000037396 body weight Effects 0.000 description 3
- 201000011510 cancer Diseases 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 238000001784 detoxification Methods 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 230000002440 hepatic effect Effects 0.000 description 3
- 230000003834 intracellular effect Effects 0.000 description 3
- 239000007928 intraperitoneal injection Substances 0.000 description 3
- 230000002427 irreversible effect Effects 0.000 description 3
- 210000003734 kidney Anatomy 0.000 description 3
- 231100000225 lethality Toxicity 0.000 description 3
- 210000004072 lung Anatomy 0.000 description 3
- 230000036210 malignancy Effects 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 230000035772 mutation Effects 0.000 description 3
- 238000010606 normalization Methods 0.000 description 3
- 238000012753 partial hepatectomy Methods 0.000 description 3
- 230000008707 rearrangement Effects 0.000 description 3
- 231100000331 toxic Toxicity 0.000 description 3
- 230000002588 toxic effect Effects 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 2
- ITPDYQOUSLNIHG-UHFFFAOYSA-N Amiodarone hydrochloride Chemical compound [Cl-].CCCCC=1OC2=CC=CC=C2C=1C(=O)C1=CC(I)=C(OCC[NH+](CC)CC)C(I)=C1 ITPDYQOUSLNIHG-UHFFFAOYSA-N 0.000 description 2
- 239000011547 Bouin solution Substances 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 2
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 2
- 229930182566 Gentamicin Natural products 0.000 description 2
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 2
- 238000012752 Hepatectomy Methods 0.000 description 2
- 206010028851 Necrosis Diseases 0.000 description 2
- 208000027418 Wounds and injury Diseases 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 229960005260 amiodarone Drugs 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 210000003484 anatomy Anatomy 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 238000010352 biotechnological method Methods 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000004271 bone marrow stromal cell Anatomy 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 238000010835 comparative analysis Methods 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- 238000012937 correction Methods 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 229960002518 gentamicin Drugs 0.000 description 2
- 230000003394 haemopoietic effect Effects 0.000 description 2
- 231100000234 hepatic damage Toxicity 0.000 description 2
- 231100000753 hepatic injury Toxicity 0.000 description 2
- 230000003284 homeostatic effect Effects 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 230000008818 liver damage Effects 0.000 description 2
- 208000019423 liver disease Diseases 0.000 description 2
- 238000012423 maintenance Methods 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- 230000017074 necrotic cell death Effects 0.000 description 2
- 108091027963 non-coding RNA Proteins 0.000 description 2
- 102000042567 non-coding RNA Human genes 0.000 description 2
- 239000012188 paraffin wax Substances 0.000 description 2
- 239000008188 pellet Substances 0.000 description 2
- 230000000149 penetrating effect Effects 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 235000018102 proteins Nutrition 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 238000012552 review Methods 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 230000035899 viability Effects 0.000 description 2
- 102100036009 5'-AMP-activated protein kinase catalytic subunit alpha-2 Human genes 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 108091007413 Extracellular RNA Proteins 0.000 description 1
- 102100039111 FAD-linked sulfhydryl oxidase ALR Human genes 0.000 description 1
- 101710188810 FAD-linked sulfhydryl oxidase ALR Proteins 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 101000783681 Homo sapiens 5'-AMP-activated protein kinase catalytic subunit alpha-2 Proteins 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 206010063897 Renal ischaemia Diseases 0.000 description 1
- 206010063837 Reperfusion injury Diseases 0.000 description 1
- 206010038669 Respiratory arrest Diseases 0.000 description 1
- 108020004459 Small interfering RNA Proteins 0.000 description 1
- 238000000692 Student's t-test Methods 0.000 description 1
- 102000013530 TOR Serine-Threonine Kinases Human genes 0.000 description 1
- 108010065917 TOR Serine-Threonine Kinases Proteins 0.000 description 1
- 108091046869 Telomeric non-coding RNA Proteins 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 230000019552 anatomical structure morphogenesis Effects 0.000 description 1
- 230000002253 anti-ischaemic effect Effects 0.000 description 1
- 230000002421 anti-septic effect Effects 0.000 description 1
- 239000012984 antibiotic solution Substances 0.000 description 1
- 229940064004 antiseptic throat preparations Drugs 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 230000001174 ascending effect Effects 0.000 description 1
- 238000004500 asepsis Methods 0.000 description 1
- 230000002886 autophagic effect Effects 0.000 description 1
- 238000002306 biochemical method Methods 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 239000000090 biomarker Substances 0.000 description 1
- 229920001222 biopolymer Polymers 0.000 description 1
- 238000009534 blood test Methods 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 210000002449 bone cell Anatomy 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- YTRQFSDWAXHJCC-UHFFFAOYSA-N chloroform;phenol Chemical compound ClC(Cl)Cl.OC1=CC=CC=C1 YTRQFSDWAXHJCC-UHFFFAOYSA-N 0.000 description 1
- 230000009693 chronic damage Effects 0.000 description 1
- 208000020832 chronic kidney disease Diseases 0.000 description 1
- 208000022831 chronic renal failure syndrome Diseases 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 230000001447 compensatory effect Effects 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000001066 destructive effect Effects 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 230000006346 energetic homeostasis Effects 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 239000012894 fetal calf serum Substances 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- 102000034356 gene-regulatory proteins Human genes 0.000 description 1
- 108091006104 gene-regulatory proteins Proteins 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 238000011134 hematopoietic stem cell transplantation Methods 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 210000002767 hepatic artery Anatomy 0.000 description 1
- 238000010562 histological examination Methods 0.000 description 1
- 239000000017 hydrogel Substances 0.000 description 1
- 230000008073 immune recognition Effects 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 230000035990 intercellular signaling Effects 0.000 description 1
- 230000016507 interphase Effects 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 238000002350 laparotomy Methods 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 208000014018 liver neoplasm Diseases 0.000 description 1
- 210000005265 lung cell Anatomy 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 230000000527 lymphocytic effect Effects 0.000 description 1
- 210000000713 mesentery Anatomy 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 108091070501 miRNA Proteins 0.000 description 1
- 230000011278 mitosis Effects 0.000 description 1
- 230000001002 morphogenetic effect Effects 0.000 description 1
- 238000011206 morphological examination Methods 0.000 description 1
- 230000001608 morphoregulatory effect Effects 0.000 description 1
- 230000036542 oxidative stress Effects 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 238000005191 phase separation Methods 0.000 description 1
- 239000002953 phosphate buffered saline Substances 0.000 description 1
- 238000005375 photometry Methods 0.000 description 1
- 229920000729 poly(L-lysine) polymer Polymers 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 230000002028 premature Effects 0.000 description 1
- 230000037452 priming Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000011514 reflex Effects 0.000 description 1
- 230000009711 regulatory function Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 230000033764 rhythmic process Effects 0.000 description 1
- 239000012266 salt solution Substances 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 210000000813 small intestine Anatomy 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 210000002536 stromal cell Anatomy 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 238000011287 therapeutic dose Methods 0.000 description 1
- AWLILQARPMWUHA-UHFFFAOYSA-M thiopental sodium Chemical compound [Na+].CCCC(C)C1(CC)C(=O)NC([S-])=NC1=O AWLILQARPMWUHA-UHFFFAOYSA-M 0.000 description 1
- 210000000689 upper leg Anatomy 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/7105—Natural ribonucleic acids, i.e. containing only riboses attached to adenine, guanine, cytosine or uracil and having 3'-5' phosphodiester links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/28—Bone marrow; Haematopoietic stem cells; Mesenchymal stem cells of any origin, e.g. adipose-derived stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- G—PHYSICS
- G09—EDUCATION; CRYPTOGRAPHY; DISPLAY; ADVERTISING; SEALS
- G09B—EDUCATIONAL OR DEMONSTRATION APPLIANCES; APPLIANCES FOR TEACHING, OR COMMUNICATING WITH, THE BLIND, DEAF OR MUTE; MODELS; PLANETARIA; GLOBES; MAPS; DIAGRAMS
- G09B23/00—Models for scientific, medical, or mathematical purposes, e.g. full-sized devices for demonstration purposes
- G09B23/28—Models for scientific, medical, or mathematical purposes, e.g. full-sized devices for demonstration purposes for medicine
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- General Physics & Mathematics (AREA)
- Cell Biology (AREA)
- Developmental Biology & Embryology (AREA)
- Physics & Mathematics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biochemistry (AREA)
- Gastroenterology & Hepatology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Educational Technology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Educational Administration (AREA)
- Business, Economics & Management (AREA)
- Pure & Applied Mathematics (AREA)
- Mathematical Physics (AREA)
- Mathematical Optimization (AREA)
- Theoretical Computer Science (AREA)
- Molecular Biology (AREA)
- Mathematical Analysis (AREA)
- Computational Mathematics (AREA)
- Algebra (AREA)
- Hematology (AREA)
- Medical Informatics (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Virology (AREA)
- Zoology (AREA)
Abstract
Изобретение относится к медицине, а именно к гепатологии, и может быть использовано для лечения острой печеночной недостаточности (ОПН) в эксперименте, после хирургической операции, в результате которой формируется критический дефицит функционирующей ткани печени. Получают несортированную фракцию мононуклеарных клеток костного мозга (ККМ) от крысы-донора и хранят в растворе «Кустодиол» при температуре 4-6°С в течение 3-18 часов. После чего из нее получают общую РНК (оРНК) и вводят однократно внутрибрюшинно интраоперационно экспериментальному животному - крысе после выполнения хирургической операции, в дозе 90-110 мкг/100 г веса животного. Способ обеспечивает возможность ускорения темпа, надежности и результативности лечения тяжелых и крайне тяжелых форм ОПН, развивающихся после хирургического иссечения критических объемов ткани печени, за счет повышения активности индукционного и регуляторного воздействия оРНК из свежевыделенных ККМ на процессы репаративной регенерации печени. 1 з.п. ф-лы, 2 ил., 4 табл.
Description
Изобретение относится к медицине, а именно, к гепатологии, и может быть использовано для профилактики и лечения острой печеночной недостаточности (ОПН).
На протяжении последних десятилетий проблема эффективного лечения печеночной недостаточности остается нерешенной проблемой, т.к. летальность, как при острой, так и при хронической печеночной недостаточности, по-прежнему, остается на высоком уровне и не имеет тенденции к снижению. По данным ВОЗ смертность от ОПН, сопровождающейся обширным некрозом паренхимы, достигает 70-90% и более [Ивашкин В.Т., Уланова И.Н. /Преждевременная смертность в Российской Федерации и пути ее снижения. Стратегия «шесть в четырех». //Российский журнал гастроэнтерологии, гепатологии, колопроктологии, 2006, №1, с. 8-14], а после часто выполняемых в клинике операций обширной резекции печени, особенно при онкологических заболеваниях печени, смертность в раннем послеоперационном периоде достигает 7% [Л.П. Котельникова, И.М. Будянская /Профилактика и лечение осложнений после резекции печени.// Вестник хирургии им. И.И. Грекова, 2012; 171(3):67-71]. Указанные обстоятельства требуют продолжения поиска эффективных и доступных методов лечения ОПН.
Настоятельная необходимость разработки более эффективных способов лечения печеночной недостаточности диктуется также неутешительными прогнозами дальнейшего повышения заболеваемости по этой нозологии во всех странах мира в ближайшие 10-20 лет [Плеханов А.Н., Товаршинов А.И. /Современные подходы к диагностике и лечению печеночной недостаточности (обзор литературы). //Бюллетень ВСНЦ, 2016, том 1, вып. 4 (110), с. 136].
К настоящему времени стало очевидным, что трансплантация печени, будучи самым эффективным методом лечения острой и хронической печеночной недостаточности из-за дефицита донорских органов не может обеспечить всех нуждающихся в ней. Рассматривая высокую летальность при ОПН, как следствие нарушения процессов регенерации в поврежденной печени, надежду на повышение эффективности восстановительного лечения печени стали связывать с регенерационной медициной, основанной на применении клеточных биотехнологий.
Были предложены методы интенсивной терапии ОПН, основанные на применении экстрактов ткани печени, полученных либо от крыс с 70% резекцией, либо от неонатальных поросят [Э.И. Гальперин, Т.Г. Дюжева, Л.В. Платонова и др. Уменьшение повреждения печени при ее обширной резекции и токсическом повреждении //Анналы хирургической гепатологии, 2008, т. 13, №1, с. 51-55]. Однако при возможном клиническом применении экстрактов из нативных тканей всегда существует потенциальная опасность заражения пациента трансмиссивными инфекциями животных, а изготовление высокоэффективного медикаментозного препарата из экстракта животных тканей предполагает идентификацию химического переносчика биологических эффектов и выделение его из тканевого экстракта, чего авторами не было предпринято.
В последние годы стал известен новый биотехнологический способ лечения ОПН после обширной резекции печени (ОРП), который основан на имплантации в организм (брыжейку тонкой кишки) клеточно-инженерных конструкций, состоящих из сокультивированных аллогенных клеток печени и мультипотентных мезенхимальных стромальных клеток костного мозга (ММСК КМ) в составе биополимерного гетерогенного коллагенсодержащего гидрогеля [М. Shagidulin, N. Onishchenko, М. Krasheninnikov et al., Transplantation liver cells and multipotent mesenchymal stromal cells for correction and treatment of hepatic failure //Medimond. International Proceedings., 2010, Р. 83-86]. Достоверно ускоренное восстановление функции печени авторы объясняют высоким регенерационным потенциалом культивированных стволовых/прогениторных клеток, выделенных из костного мозга.
Между тем, внедрение в практику регенеративной медицины клеточных технологий пока не получило единодушного одобрения из-за опасности малигнизации и генетических мутаций трансплантированных стволовых/прогениторных клеток, из-за опасности развития реакции «трансплантат против хозяина» при трансплантации гемопоэтических стволовых клеток, а также из-за быстрой гибели или быстрого снижения активности как аутологичных, так и аллогенных клеток [А.С. Lyra, М.В. Soares, L.F. da Silva et al. / Infusion of autologous bone marrow mononuclear cells through hepatic artery results in a short-term improvement of liver function in patients with chronic liver disease: a pilot randomized controlled study. //European Journal of Gastroenterology & Hepatology.- 2010. - Vol. 22(1). - Р. 33-42].
Альтернативой клинического применения биомедицинских клеточных продуктов в регенерационной медицине, включая клеточно - и тканеинженерные конструкции, могут стать технологии, основанные на применении выделенного из клеток костного мозга комплекса внутриклеточных биологически активных компонентов.
Вопрос о том, какие внутриклеточные структуры и сигнальные молекулы клеток костного мозга (ККМ) способны обеспечивать «адресный перенос регенерационной информации» к поврежденным органам долго не был предметом специальных исследований.
В последние годы, однако, появились исследования, из которых следует, что продуцентами и переносчиками регенерационной информации в межклеточной сигнальной системе выступают разнообразные по своим структурным и функциональным свойствам молекулы РНК [Н.В. Тишевская, А.Г. Бабаева, Н.М. Геворкян / Роль лимфоцитарных РНК в межклеточном информационном обмене и регуляции регенеративных процессов. // Российский Физиологический Журнал им. И.М. Сеченова. - 2016, - Т. 102. - вып. 11, С. 1280-1301; А.Г. Бабаева, Н.В. Тишевская, Н.М. Геворкян / О морфогенетических свойствах РНК лимфоидных и стволовых клеток при восстановительных процессах // Российская академия наук. - Научно-исследовательский институт морфологии человека, Москва. - 2016, 272 с].
Начиная с 2008 г. во всем мире проводятся интенсивные исследования свойств молекул малых белок некодирующих РНК - микроРНК, которые начали использовать не только в качестве биомаркеров, но и в качестве терапевтических средств регуляции восстановительных процессов при различных патологиях [D.P. Bartel / MicroRNAs: target recognition and regulatory functions // Cell.-2009. - Vol. - 136(2). - P. 215-233].
Однако, выделение какой-либо одной микро РНК с адресным эффектом для целей регенерационной терапии представляет собой сложный технологический процесс. Уже к 2015 году было идентифицировано свыше 1800 вне - и внутриклеточных микроРНК человека [S.M. Peterson, J.A. Thompson, M.L. Ufkin, P. Sthyanarayana, L. Liaw, C.B. Congdon / Common features of microRNA target prediction tools. // Frontiers in Genetics. - 2014.- Vol. - 5.- S.M. P.23], причем функция большинства из них остается неизвестной. Кроме того, вызывает сомнение возможность индукции и осуществления эффективного регенерационного процесса в поврежденных органах с помощью какой-либо одной выделенной микро РНК, так как уже показано, что в процессах регенерации принимают участие разные классы молекул РНК [I.K. Yan, X. Wang, Y.W. Asmann, H. Haga, Т. Patel / Circulating Extracellular RNA Markers of Liver Regeneration. // PLoS One.-2016.-Vol. 11(7)], в том числе разные классы белок некодирующих РНК, [J. Li, W. Jin, Y. Qin, W. Zhao, C. Chang, C. Xu / Expression Profile and Function Analysis of LncRNAs during Priming Phase of Rat Liver Regeneration/ // PLoS One.-2016, Jun 21, Vol.-11(6); F. Mottaghitalab, A. Rastegari, M. Farokhi, R. Dinarvand, H Hosseinkhani et al Prospects of siRNA applications in regenerative medicine. // International Journal of Pharmaceutics. 2017 May 30. - Vol. - 524(l-2). - P. 312-329].
В последние годы стал известен биотехнологический способ индукции восстановительных процессов в поврежденной печени с помощью общей РНК (оРНК) ММСК KM [RU 2650209, С1], который, однако, был предназначен для лечения хронической печеночной недостаточности (ХПН), когда в печени уже сформированы все признаки ее хронического повреждения. Способ обеспечивает постепенное (в течение нескольких месяцев) восстановление структуры и функции поврежденных клеток, а также восстановление гистологических характеристик ткани печени, которое достигается за счет многократного (по крайней мере, трехкратного) парентерального введения в организм оРНК, выделенной из предварительно культивированных в течение 3-4-х недель ММСК КМ здорового донора. В результате применения оРНК, выделенной из ММСК КМ, а не самих ММСК КМ, этот способ позволяет избежать развития известных опасных осложнений, связанных с применением стволовых/прогениторных клеток костного мозга (малигнизация и мутация клеток). Кроме того, предложенный способ позволяет использовать только биологически активный комплекс этих клеток, содержащий в себе все типы РНК (в том числе все типы регуляторных белок - не кодирующих микро-РНК), что позволяет осуществлять непосредственный перенос регенерационной информации клеткам хронически поврежденного органа - печени, индуцируя в них процесс эффективной репаративной регенерации.
Однако известный способ, предполагающий использование оРНК из ММСК КМ млекопитающих в качестве средства для коррекции печеночной недостаточности, не лишен недостатков, препятствующих его широкому и эффективному использованию для лечения ОПН.
Прежде всего, указанный выше известный способ относится к лечению ХПН, вызванной хроническим токсическим повреждением печени. К недостаткам относится также сложность и длительность сроков выделения и получения достаточных количеств ММСК КМ из мононуклеарной фракции клеток костного мозга, в которой эти клетки составляют не более 0,5-1,5%.
Для выделения ММСК из мононуклеарной фракции клеток костного мозга сначала проводят краткосрочное культивирование (3-4 суток), а затем путем длительного культивирования выделенных ММСК КМ в течение 3-4 недель проводят наращивание клеточной массы с применением дорогостоящих культуральных сред, что существенно повышает себестоимость получения оРНК из ММСК КМ.
Кроме того, предложенная схема использования оРНК оказалась непригодной для лечения ОПН. Применение оРНК по известной схеме обеспечивает лишь постепенную (в течение нескольких месяцев) инволюцию и устранение признаков деструкции паренхиматозных и непаренхиматозных структур ткани печени, сформировавшихся в процессе ее длительного хронического токсического повреждения. Между тем, для успешного лечения ОПН в клинике, особенно после субтотальной или обширной резекции, уже в первые часы послеоперационного периода необходимо обеспечить условия для устранения индуцированного операционным стрессом раннего и опасного ингибирования митотической и пролиферативной активности клеток в остатке печени. Более того, требуется в первые-вторые сутки достигнуть раннего и максимально ускоренного темпа наращивания дополнительных количеств здоровых клеток в остатке здоровой ткани печени для быстрого преодоления дефицита ткани печени (ее критической массы) после операции, ускоренного восстановления печеночного гомеостаза и предотвращения гибели пациента.
Известен способ коррекции ОПН в эксперименте после хирургической операции путем раннего применения оРНК из свежевыделенной несортированной мононуклеарной фракции ККМ в дозе 30 мкг/100 г веса животного, введенной внутрибрюшинно однократно через 3-5 часов после завершения моделирования обширной резекции печени [З.З. Гоникова, A.О. Никольская, Л.А. Кирсанова, М.Ю. Шагидулин, Н.А. Онищенко, B.И. Севастьянов / Сравнительный анализ эффективности стимуляции процессов регенерации печени клетками костного мозга и обшей РНК этих клеток // Вестник трансплантологии и искусственных органов, 2019, т. 21(1), С. 113-121]. Было показано, что применение оРНК из свежевыделенных мононуклеарных ККМ способствует активизации восстановительных процессов в остатке печени после ОРП, причем эффект коррекции ОПН от применения оРНК из мононуклеарных ККМ был более выраженным, чем от применения самих мононуклеарных ККМ в эквивалентной дозе, и это, как полагают, обусловлено более высокой проникающей и регуляторной способностью оРНК как химического вещества.
Между тем, анализ эффективности регуляторного воздействия оРНК из свежевыделенных ККМ на восстановительные процессы в печени при ОПН показал, что эффект от однократного применения оРНК из свежевыделенных ККМ в указанной дозе недостаточен.
Известен способ лечения ОПН [RU 2701792, С1] путем двукратного применения оРНК из свежевыделенных мононуклеарных ККМ в лечебной дозе оРНК 50-60 мкг/100 г веса животного в предоперационном периоде, а затем через 3-4 часа после операции (прототип). Обладая высокой регуляторной активностью и предотвращая развитие летальных исходов при моделировании обширной резекции печени (70-75% печени), способ-прототип не способствует предотвращению или снижению летальности при моделировании субтотальной резекции печени (85-90% печени).
Таким образом, несмотря на существующие достоинства применения оРНК из свежевыделенных мононуклеарных ККМ при ОПН по сравнению с применением свежевыделенных мононуклеарных ККМ, (отсутствие опасности возникновения мутаций и малигнизации, возможности развития реакции «трансплантат против хозяина», а также достоверно более высокая регуляторная активность) даже при двукратном применении свежевыделенной оРНК сохраняется неудовлетворенность результатами ее индукционного воздействия на процессы восстановительной регенерации в печени при моделировании тяжелых форм ОПН путем хирургического иссечения критических объемов ткани печени.
По современным представлениям недостаточная эффективность применения клеточных биотехнологий при тяжелых формах острых заболеваний печени может быть связана с возникающим в ткани печени истощением резервов активации собственных тканевых адаптационно - приспособительных механизмов, запускающих и регулирующих процесс восстановительной регенерации: например, в результате возникновения резкого дефицита печеночной ткани и возросшей функциональной нагрузки на оставшуюся ткань после обширной резекции печени при ОПН. Такое представление обосновывается тем, что индукция регенерационных процессов в печени, как и в других органах, всегда начинается с активации и использования собственных сохранившихся резервов, необходимых для защиты и выживания клеток, а именно с процессов клеточной аутофагии, развивающихся в рамках эволюционно выработанного неспецифического адаптационного синдрома клеточной системы для формирования энергетической, структурной и функциональной устойчивости клеток к действию различных стрессорных факторов внешней и внутренней среды организма [А.Д. Браун, Г.П. Мозженок / Неспецифический адаптационный синдром клеточной системы //Л., Изд. Наука, 1987].
Аутофагия представляет собой процесс прижизненной утилизации измененного метаболитами содержимого цитоплазмы клеток для поддержания их структурного и энергетического гомеостаза. В настоящее время аутофагию рассматривают даже не как процесс «запрограмированного умирания», а как процесс преимущественно «запрограммированного выживания» клеток [М.П. Потапнев / Аутофагия, апоптоз, некроз клеток и иммунное распознавание своего и чужого // Иммунология, 2014, №2, с. 95-102]. Аутофагия ингибирует развитие необратимого апоптоза клеток и играет защитную роль в условиях оксидативного стресса [Pu Т., Liao Х.Н., Sun Н. et al. / Augmenter of liver regeneration regulates autophagy in renal ischemia-reperfusion injury via the AMPK/mTOR pathway// Apoptosis, 2017 jul.; 22(7): 955-969].
В печени аутофагия служит важнейшим регулятором поддержания функциональной активности ее стволовых/прогениторных клеток, которые, как известно, являются непременными участниками запуска процессов самообновления, пролиферации и дифференцировки клеток печени при регенерации [Cheng Y., Wang В., Zhou Н., Dang S. et al. /Autophagy is required for the maintenance of liver progenitor cell functionality // Cell Physiol Biochem., 2015; 36(3): 1163-1174].
Известно также, что фармакологическая модуляция аутофагии в печени в ранние сроки после обширной (70-75%) и субтотальной (85-90%) резекции печени способна повысить выживаемость животных и эффективность регенерации оставшейся части печени [Lin C.W., Chen Y.S., Lin С.С.et al. / Amiodarone as an autophagy promoter reduces liver injury and enhances liver regeneration and survival in mice after partial hepatectomy // Sci. Rep., 2015 Oct 30; 5: 15807].
Таким образом, по нашему мнению, из-за недостаточной выраженности процессов аутофагии в печени в результате критического истощения ее индукционных резервов при тяжелом (критическом) снижении массы печени, регенерационный эффект от применения оРНК из свежевыделенных ККМ оказался недостаточным при лечении тяжелых форм ОПН.
Техническая проблема заключается в повышении активности индукционного и регуляторного воздействия оРНК из свежевыделенных ККМ на процессы репаративной регенерации печени для обеспечения ускорения темпа, надежности и результативности лечения тяжелых и крайне тяжелых форм ОПН, развивающихся после хирургического иссечения критических объемов ткани печени.
Технический результат, достигаемый при осуществлении предлагаемого изобретения заключается:
- в сокращении сроков и повышении эффективности лечения ОПН, включая предотвращение летальных исходов после обширной резекции печени (70-75% печени), а также снижение летальности при осуществлении субтотальной резекции печени (85-90% печени) путем интраоперационной индукции у оперируемого пациента раннего и более высокого темпа процессов восстановительной регенерации (индукция высокого уровня митотической и пролиферативной активности клеток в оставшейся части печени уже на вторые сутки послеоперационного периода) за счет интраоперационного применения биологически эффективной дозы активированной оРНК, полученной из ККМ, предварительно подвергнутых аутофагии, что позволяет повысить мощность и эффективность формирования регенерационного процесса в печени, всегда происходящего в рамках неспецифического адаптационного синдрома клеточной системы на воздействия стресс факторов слабой и умеренной биологической силы.
в простоте и низкой себестоимости процесса получения активированной оРНК из ККМ, предварительно подвергнутых аутофагии.
Нами предложена оригинальная «предварительная подготовка» несортированных мононуклеарных ККМ перед выделением из них оРНК. За счет хранения этих клеток при 4-6°С в ион сбалансированном водно-солевом растворе «Кустодиол» (раствор Бредшнейдера) в течение 3-18 часов происходит активация оРНК. Предлагаемый режим хранения, обеспечивая аутофагию ККМ, исключает при этом развитие необратимого апоптоза этих клеток.
Разработанная нами технология подготовки получения и применения оРНК при ОПН обеспечивает ранний и более высокий уровень митотической и пролиферативной активности в сохранившихся клетках резецированной печени, создает условия для раннего восстановления (на 7-10 сутки) исходной массы печени и тем самым позволяет предотвратить летальность после обширной резекции печени (70-75%) и снизить летальность после субтотальной резекции печени (85-90%).
В предлагаемом нами способе лечения ОПН, исходным материалом для получения активированной оРНК служит свежевыделенная фракция гемопоэтических мононуклеарных ККМ (аутологичных или аллогенных) здорового донора. В качестве донора мононуклеарных ККМ при резекции печени может выступать сам пациент, но только до резекции у него печени, так как операция обширной резекции печени (70-75%) и тем более субтотальная резекция (85-90%) сама по себе уже в ранний период (первые сутки) ингибирует регенераторные процессы, как в печени, так и в костном мозге.
В предлагаемом способе лечения ОПН, развившейся после хирургической операции резекции печени используется предварительно активированная оРНК из мононуклеарных ККМ. Активированная оРНК содержит уже готовый спектр молекул РНК тех типов и классов, которые образовались в результате аутофагии мононуклеарных ККМ в ответ на применение их гипотермической консервации (биологически допустимый стресс-фактор умеренной силы) в ион сбалансированном водно-солевом консервирующем растворе «Кустодиол», обеспечивающем при температуре 4-6°С длительную и надежную сохранность этих клеток в течение 3-18 часов. Длительная и надежная сохранность мононуклеарных ККМ обеспечивается составом консервирующего раствора и гипотермическими условиями хранения, которые воздействуют на ККМ, как адаптогены средней и слабой биологической силы, индуцирующие в самих ККМ гомеостатическую перестройку (в том числе метаболизма) через активацию процессов аутофагии в рамках развития эволюционно выработанного в клетках неспецифического адаптационного синдрома.
При введении в организм для лечения ОПН активированная оРНК в биологически эффективной дозе, полученная из ККМ, подвергнутых аутофагии, действует более ускоренно и результативно на поврежденную печень, так как реализует свой эффект на клетки печени и как адаптоген (в рамках неспецифического адаптивного синдрома), и как готовый регулятор процессов регенерации, аккумулирующий в своем составе адекватный спектр молекул РНК, необходимых для запуска процессов аутофагии и регенерации поврежденной печени. В результате активированная оРНК более ускоренно и эффективно индуцирует в клетках поврежденной печени процессы аутофагии - ранней самой важной и определяющей фазы запуска регенераторного процесса, проявляющегося более ранней активацией восстановительных и пролиферативных процессов.
Очевидно, запуск регенерационного процесса в печени осуществляют два фактора - содержащиеся в активированной оРНК многочисленные микро РНК, образовавшиеся в процессе индукции аутофагии ККМ при их гипотермическом хранении в растворе «Кустодиол», а также микро РНК ускоренно экспрессировавшиеся в клетках поврежденной печени под воздействием использования адаптогенов.
Достоинствами предлагаемого способа лечения ОПН, позволяющими обеспечить клиническую доступность метода и по существу достигнуть выраженного и надежного лечебного эффекта являются:
- раннее интраоперационное применение активированной оРНК в эффективной дозе при ОПН, вызванной обширной (70-75%) или субтотальной (85-90%) резекцией печени позволяет уже в 1-2 сутки послеоперационного периода активизировать адаптационные и восстановительные процессы в остатке печени, затормозить деструктивные процессы, обеспечить максимально раннюю регенерационную поддержку печени и, тем самым, предотвратить или достоверно снизить процент летальных исходов.
- возможность применения при необходимости повторных парентеральных введений активированной оРНК и достижения позитивного результата при использовании даже сниженных доз препарата.
- возможность обеспечить раннюю компенсаторную поддержку процессам восстановительной регенерации не только печени, но и адаптационную поддержку других органов (почки, легкие), относящихся к единой системе детоксикации организма и участвующих в поддержании печеночного гомеостаза, а также в снижении опасности возникновения летальных исходов;
- возможность проводить более эффективную регенерационную терапию различных органов и систем в организме, так как активированная оРНК, выделенная из мононуклеарной фракции ККМ здорового донора, сохраняет универсальность регуляторных свойств этих клеток и будучи биохимическим препаратом с высокой проникающей активностью, обладает более мощным регуляторным воздействием, чем неактивированная оРНК;
- возможность использования стандартного ион сбалансированного водно-солевого консервирующего раствора «Кустодиол», применяющегося в трансплантологии для сохранения (консервации) различных органов перед пересадкой делает процедуру индукции аутофагии в мононуклеарных ККМ, используемых для получения препарата активированной оРНК, доступной для широкого клинического применения.
Сущность изобретения заключается в следующем.
Для лечения ОПН в эксперименте после хирургической операции, в результате которой формируется критический дефицит функционирующей ткани печени, получают несортированную фракцию мононуклеарных клеток костного мозга от крысы-донора и хранят в растворе «Кустодиол» при температуре 4-6°С в течение 3-18 часов. Затем из нее получают общую РНК и вводят в дозе 90-110 мкг/100 г веса животного однократно внутрибрюшинно экспериментальному животному - крысе сразу после завершения хирургического моделирования ОПН путем обширной (70-75%) или субтотальной (85-90%) резекции печени, в результате которой формируется критический дефицит функционирующей ткани печени.
Хирургической операцией, в результате которой формируется критический дефицит функционирующей ткани печени может быть обширная или субтотальная резекция печени.
Таким образом, для лечения в эксперименте тяжелой формы ОПН, созданной путем хирургического иссечения больших (70-75%) и крайне больших (85-90%) объемов ткани печени, выделяют мононуклеарную фракцию ККМ от здорового животного-донора-крысы. Затем полученную фракцию несортированных мононуклеарных клеток активируют для индукции в этих клетках процессов аутофагии и адаптивной перестройки клеточного (в том числе энергетического) гомеостаза путем погружения их в охлажденный консервирующий раствор «Кустодиол» с допустимым сроком хранения в нем при температуре 4-6°С в течение от 3 до 18 часов (срок в течение которого ККМ преимущественно сохраняют жизнеспособность и в них развивается аутофагия, что контролируется по уровню появления в сохраняемых клетках необратимого апоптоза, составляющего не более 7-10% от общей массы клеток).
Затем из полученной фракции несортированных мононуклеарных ККМ, которые активированы процессом их хранения в охлажденном растворе «Кустодиол», выступающего в роли биологически допустимого адаптогена, выделяют оРНК, которая является уже активированной, т.к. содержит в своем составе новый готовый спектр образовавшихся молекул РНК, способных запустить адаптационный и регенерационный процессы в печени после применения.
Активированную оРНК вводят экспериментальному животному -крысе однократно внутрибрюшинно интраоперационно сразу после завершения хирургического моделирования ОПН путем обширной (70-75%) или субтотальной (85-90%) резекции печени в дозе 90-110 мкг/100 грамм веса животного.
Предлагаемый способ, главным компонентом которого, является получение и применение активированной оРНК, обладает более мощным лечебным воздействием на поврежденную (резецированную) печень, чем неактивированная оРНК, полученная из свежевыделенных ККМ.
Обнаруженный эффект обусловлен двумя механизмами:
- активированная оРНК, будучи экзогенным адаптогеном, оказывает адаптивное воздействие на организм пациента с острой печеночной недостаточностью, вызывает гомеостатическую перестройку метаболизма в сохранившихся клетках печени, а также в клетках других органов, индуцируя в них процессы аутофагии. За счет индукции процессов аутофагии создаются предпосылки для запуска процессов восстановительного морфогенеза (регенерации) в клетках печени, костного мозга, а также в клетках других органов (почки, легкие), участвующих в поддержании детоксикационной функции печени;
- активированная оРНК содержит дополнительно в своем составе новый готовый спектр именно тех регуляторных молекул РНК, которые образовались в процессе аутофагии мононуклеарных ККМ, более ускоренно запускающие в организме регенераторные процессы, дополнительно усиливая морфорегуляторную активность клеток печени, костного мозга, а также клеток почек и легких, участвующих в поддержании функции печени, как у экспериментального животного, так и у пациента в клинике.
Сочетанная реализация обоих механизмов при использовании активированной оРНК существенно усиливает и ускоряет восстановительный процесс в остатке резецированной печени.
Способ осуществляется следующим образом
Для лечения ОПН, развившейся после моделирования обширной и субтотальной резекции печени, применяют оРНК из активированных мононуклеарных ККМ, предварительно подвергнутых процессу аутофагии в охлажденном консервирующем растворе «Кустодиол».
В результате аутофагии в мононуклеарных ККМ происходит адаптивная структурно-функциональная перестройка, обеспечивающая повышение устойчивости этих клеток к действию стрессорных факторов. В обзоре литературы показано, что медикаментозная индукция процессов аутофагии в печени повышает эффективность регенерации печени и выживаемость мышей после частичной гепатэктомии [Lin C.W., Chen Y.S., Lin С.С.et al. / Amiodarone as an autophagy promoter reduces liver injury and enhances liver regeneration and survival in mice after partial hepatectomy // Sci. Rep., 2015 Oct 30; 5: 15807]. оРНК, полученная из этих ККМ, становится активированной, так как содержат в своем составе именно тот спектр готовых вновь образовавшихся молекул РНК, который отсутствует или недостаточен в поврежденном органе, но который при введении в организм ускоренно и более мощно адаптирует поврежденные органы (печень), индуцируя в них приспособительные (аутофагию клеток печени) и восстановительные процессы (восстановительную регенерацию).
Комплекс активированных молекул оРНК содержит все необходимые типы РНК, в том числе все типы регуляторных РНК (прежде всего микро РНК), обеспечивающих перенос «регенерационной и сигнальной информации» клеткам костного мозга и клеткам поврежденной печени пациента для ускоренной и мощной индукции восстановительных процессов в печени, а также для индукции адаптивно-приспособительных процессов в органах (почки, легкие), поддерживающих детоксикационную функцию печени.
Выполнение способа начинают с получения мононуклеарной фракции клеток из аспирата костного мозга животного. Для этого под эфирным наркозом из костномозгового канала болынеберцовых и бедренных костей крысы-донора получали ККМ путем аспирации их шприцом с иглой 18G, содержащим среду для забора (0.5 мл фосфатно-буферного раствора с 50 ЕД/мл гепарина и 0.25 мг/л гентамицина).
Суспензию ККМ центрифугировали при 1500 об/мин (350g) 5 минут, осадок клеток ресуспендировали в растворе для лизиса эритроцитов и тромбоцитов (114 мМ NH4CL, 7,5 mM KHCO3, 100 мкМ EDTA) в течение 3 минут и повторно центрифугировали. Гемолизированный супернатант удаляли отсасыванием, а клеточный осадок ресуспендировали в среде DMEM (ПанЭко, Россия), содержащей 10% телячью эмбриональную сыворотку («HyClonegold», USA), инсулин 0.4 мкМ, 0.25 мг/л гентамицина.
Выделенные клетки представляли собой мононуклеарную фракцию, преимущественно гемопоэтических ККМ, суммарный выход которых колебался от 0,8-1.5×107 клеток. Далее удаляли среду DMEM, а выделенные мононуклеарные ККМ помещали в охлажденный до 4-6°С консервирующий раствор «Кустодиол» (Др. Франц Келер Хеми ГмбХ, Германия) сроком от 3 до 18 часов, в течение которого мононуклеарные клетки сохраняют жизнеспособность, поддерживая свой гомеостаз за счет эволюционно выработанного механизма адаптивной структурно-функциональной и энергетической перестройки собственных резервов в ответ на стрессорное воздействие гипотермии и ион сбалансированного консервирующего раствора. Этот процесс структурно-функциональной и энергетической перестройки, обеспечивающий сохранение жизнеспособности ККМ, сопровождается процессом аутофагии и развитием обратимого апоптоза клеток в процессе хранения, что контролировали путем измерения и объективной оценки количества жизнеспособных клеток с помощью витального красителя 7-AAD (7 аминоактиномицин D, фирмы Beckman Coulter, США), который проникает в ядра только нежизнеспособных клеток и интерколирует в двойную спираль ДНК. Позитивно окрашенные, то есть нежизнеспособные мононуклеарные клетки при использовании 7-AAD, составляли не более 7-10% после хранения в растворе «Кустодиол» в сроках от 3 до 18 часов.
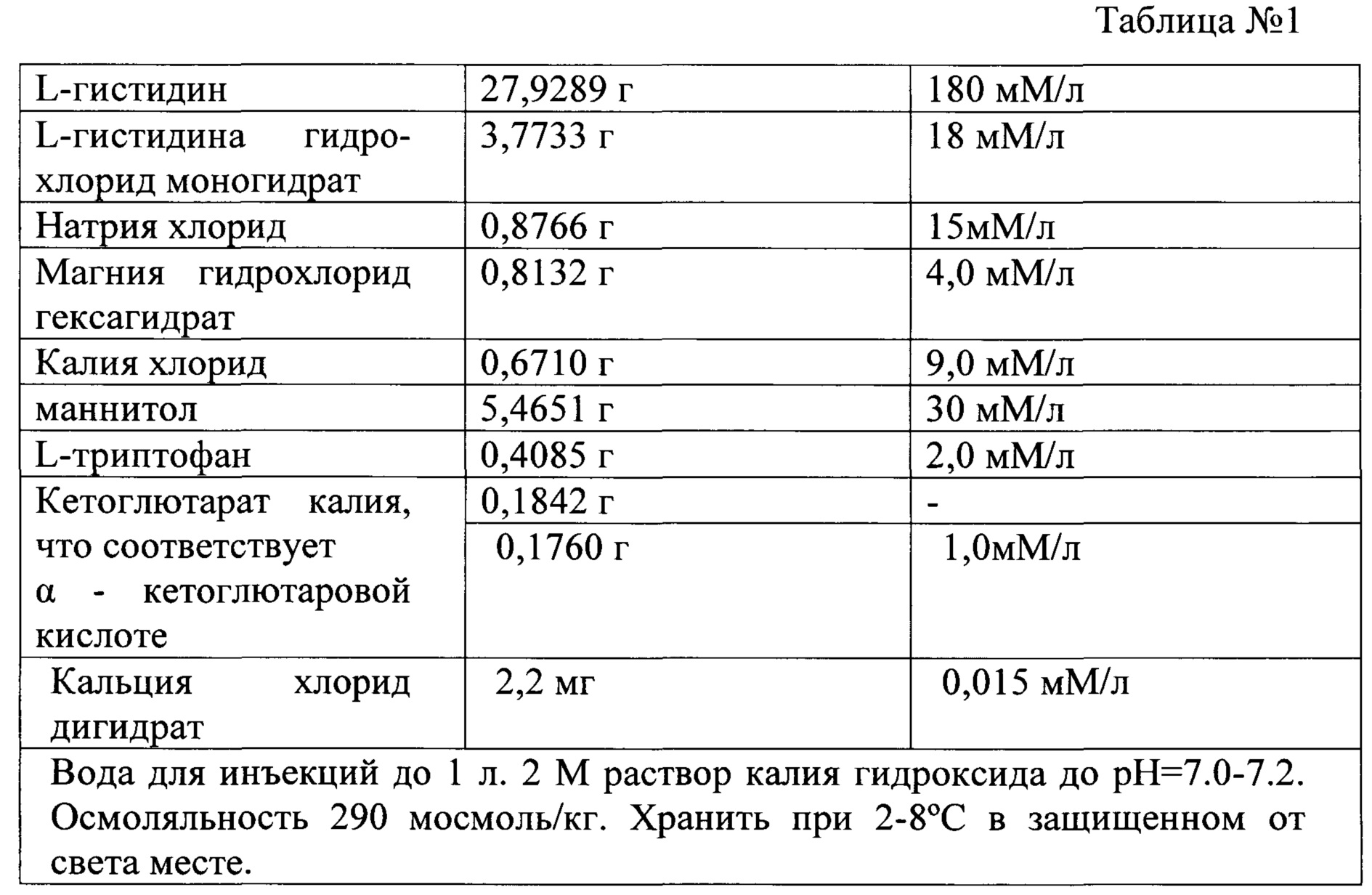
Жизнеспособность свежевыделенных мононуклеарных ККМ, то есть без холодового хранения, составляла 97-99%. Рецептура консервирующего раствора «Кустодиол», предназначенного для осуществления противоишемической защиты донорских органов при трансплантации и использованного нами для получения активированных мононуклеарных ККМ представлена в таблице №1.
Далее приступали к выделению активированной оРНК из выделенных и подвергнутых аутофагии мононуклеарных ККМ по методике «Extract RNA», разработанной фирмой «ЕВРОГЕН» (Россия).
К полученной фракции мононуклеарных клеток добавляли реагент Extract RNA из расчета 1 мл реагента на 1×106 клеток (в камере Горяева предварительно подсчитывали количество клеток), инкубировали смесь 15 минут, периодически пипетируя,) и центруфугировали при 13400 об/мин 10 минут для удаления нерастворенных фрагментов. Супернатант переносили в новую пробирку и приступали к разделению фаз. Для этого добавляли 0.2 мл хлороформа на каждый 1 мл реагента Extract RNA, инкубировали смесь в течение 5 мин при комнатной температуре, периодически встряхивая образец; затем образец центруфугировали при 13400 об/мин в течение 15 минут при комнатной температуре. В ходе центруфугирования происходило разделение смесей на три фазы: нижнюю-органическую фенол хлороформную фазу желтоватого оттенка, интерфазу белого цвета и верхнюю бесцветную водную фазу. РНК находится в верхней водной фазе, которую аккуратно собирали и переносили в чистую пробирку.
Затем приступали к непосредственному выделению оРНК. Для этого в водную фазу добавляли 0.5 мл 100% изопропанола на каждый 1 мл использованного реагента (Extract RNA). Полученную смесь инкубировали при комнатной температуре в течение 10 минут и центрифугировали при 13400 об/мин в течение 10 минут при комнатной температуре. Затем аккуратно, по стенке пробирки, добавляли 2 мл 75% этанола на каждый 1 мл изопропанола, использованного ранее. Полученный образец центрифугировали на максимальной скорости (13400 об/мин) в течение 5 минут. Удаляли этанол пипеткой и осадок, выделенной оРНК, растворяли в 1 мл воды и определяли концентрацию оРНК в 100 мкл образца на спектрофотометре при длине волны 260 нм. Из каждых 4-6 млн исходно использованных мононуклеарных клеток КМ в 1 мл определялось 380-500 мкг оРНК. Далее из этого концентрированного раствора оРНК готовили рабочие растворы оРНК, требуемой концентрации для введения в организм животного с целью лечения ОПН. Активированная оРНК, выделенная из мононуклеарных ККМ, представляет собой биотехнологический продукт высокой степени очистки, который вводят парентерально (внутрибрюшинно) и интраоперационно животным (крысы) на этапе завершения хирургического моделирования ОПН.
Рабочий раствор активированной оРНК содержал 76-100 мкг РНК/мл (к 1.0 мл концентрированного раствора оРНК добавляли 4 мл дистиллированной воды). Введение оРНК осуществляли в дозе 90-110 мкг на 100 г веса животного. У животных с моделью ОПН активированную оРНК вводили однократно интраоперационно, сразу после выполнения обширной (70-75%) или субтотальной (85-90%) резекции печени внутрибрюшинно, то есть крысе массой 300 г однократно вводят по 300±30 мкг (270-330 мкг) оРНК в виде 2,7 - 3,3 мл рабочего раствора оРНК при содержании в нем 100 мкг оРНК/мл или 3,5 - 4,3 мл рабочего раствора оРНК при содержании в нем 76 мкг оРНК/мл.
Приводим примеры осуществления предлагаемого способа лечения ОПН после обширной (70-75%) и субтотальной (85-90%) резекции печени.
Все исследования с использованием лабораторных животных проводили в строгом соответствии с законодательством Российской Федерации (в соответствии с Правилами лабораторной практики, утвержденными приказом Минздрава России №708 от 23.08.2010 г, а также стандартам ГОСТ Р ИСО 10993-2-2009 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 2. Требования к условиям содержания животных») и с соблюдением биотических принципов, утвержденных Европейской конвенцией о защите позвоночных животных, 2005 г.
Эффективность предлагаемого способа лечения ОПН, возникшей в результате снижения функционирующей массы печени до критического уровня, изучали на моделях обширной и субтотальной резекции печени у крыс.
При создании модели обширной резекции печени (резекция 70-75% общей массы печени) у крыс под внутримышечной анестезией раствором золетила из расчета 15 мг/кг с соблюдением правил асептики и антисептики вскрывали брюшную полость, выводили печень в рану и последовательно накладывали лигатуры на основания серединной, левой боковой и правой передней долей печени, после чего их резецировали.
Модель субтотальной резекции печени создавали, путем резекции (85-90% общей массы печени) за счет иссечения не только серединной, левой боковой и правой передней долей печени, но также правой задней доли печени. Под внутримышечной анестезией раствором золетила из расчета 15 мг/кг веса выполняли верхнюю срединную лапаротомию длиной 3-4 см. Срединную (40%) и левую латеральную (30%) доли печени выводили в рану, долевые сосуды перевязывали у основания, после чего доли удаляли. Далее, выделяли обе правые доли печени: переднюю и заднюю (20%), перевязывали долевые сосуды у основания и удаляли. После резекции печени в брюшную полость вводили раствор антибиотика. Лапаротомный разрез ушивали наглухо непрерывным швом. [Madrahimov N, Dirsch О, Broelsch С, Dahmen U. Marginal hepatectomy in the rat: from anatomy to surgery. //Ann Surg. 2006; - Vol. 244. - p. 89-98.]
Операцию проводили всегда в утренние часы (в период с 10 до 12 часов), когда суточный ритм митотической активности клеток печени минимален).
Всего было прооперировано 135 крыс, у 105 из которых выполняли обширную резекцию печени (n=105) и у 30 выполняли субтотальную резекцию печени (n=30).
Всех животных с обширной резекцией печени разделили на 3 группы: группа 1 (n=25, контроль с введением физ. раствора); группа 2 (n=40), группа сравнения, в которой выполняли интраоперационное однократное внутрибрюшинное введение неактивированной оРНК из свежевыделенных ККМ. Группа сравнения состояла из 2 подгрупп: А (n=20), в которой вводили оРНК в дозе 90 мкг/100 г веса животного; подгруппа Б (n=20), в которой вводили оРНК в дозе 110 мкг/100 г веса животного. Группа 3 (n=40) -опытная, в которой выполняли интраоперационное однократное внутрибрюшинное введение активированной оРНК, выделенной из мононуклеарных ККМ, активированных хранением в охлажденном консервирующем растворе «Кустодиол». Опытная группа состояла из 2 подгрупп: А (n=20), в которой оРНК выделяли из ККМ, хранившихся в растворе «Кустодиол» при температуре 4°С в течение 3 часов и вводили животному в дозе 90 мкг/100 г веса; подгруппа Б (n=20), в которой оРНК, выделяли из мононуклеарных ККМ, хранившихся в охлажденном растворе «Кустодиол» при 6°С в течение 18 часов и вводили животному в дозе 110 мкг/100 грамм веса.
Результаты 3-х групп экспериментов оценивали по летальности животных, по динамике восстановления функциональных (биохимических) показателей, гистологической структуры (по уровню митотической активности гепатоцитов) и массы резецированной печени.
Всего из 105 крыс, у которых моделировали ОПН путем обширной резекции печени, погибло 10 животных в течение 5-ти первых суток после резекции печени, (общая летальность составила 9,5%). Однако все животные, погибшие после обширной резекции, относились к 1- контрольной группе без терапии, (n=25) и внутри этой группы летальность составила 40%. У выживших животных в группах 1, 2 и 3 функциональное состояние печени исследовали в динамике параллельно с оценкой степени развития восстановительных процессов в печени в течение первых 28 суток после выполнения обширной резекции печени. Для этого животных выводили из эксперимента путем внутрибрюшинного введения раствора тиопентала натрия в дозировке, вызывающей остановку дыхания, и проводили биохимические исследования крови, а также морфологическое исследование остатка печени через 24 ч, 48 ч, 72 ч, на 5, 7,10, 14, 18, 21 и 28-е сутки после выполнения обширной резекции печени.
Биохимическими методами исследовали кровь на содержание аланин -аминотрансферазы (АлАТ), аспарагин - аминотрансферазы (АсАТ) и щелочной фосфатазы (ЩФ). Для этого у крысы забрали 28-32 мкл крови, наносили на специальные тест-полоски Reflotron™, которые сразу же устанавливали в биохимический анализатор Reflotron™, («Roche», Швейцария) (Принцип измерения - рефлексионная фотометрия, точность измерения - ±0,5%, воспроизводимость -<=0.2%, линейность: ±0,05%).
Затем вскрывали брюшную полость, эксплантировали печень и взвешивали ее. Для гистологического исследования печени извлекали фрагмент оставшейся доли печени, разрезали его на кусочки размерами 3×4×5 мм и помещали в раствор Буэна (через 24 часа раствор Буэна заменяли на 70% этанол) для фиксации. После завершения фиксации кусочки промывали в проточной воде в течение 3 ч, обезвоживали в спиртах восходящей концентрации и заливали в парафин. Парафиновые срезы толщиной 4-5 мкм наклеивали влажным способом на стекла с поли-L-лизиновым покрытием («Thermo», США). Затем препараты высушивали в течение 48 ч в термостате при 37°C, депарафинировали, регидратировали и окрашивали срезы гематоксилином и эозином. В гистологических препаратах срезов ткани печени в 30 полях зрения определяли количество митотически делящихся клеток (в %о - промилле), а так же рассчитывали митотический индекс (МИ). Достоверность различия исследуемых показателей в сравниваемых группах оценивали с помощью параметрического критерия t-Стьюдента при р<0.05.
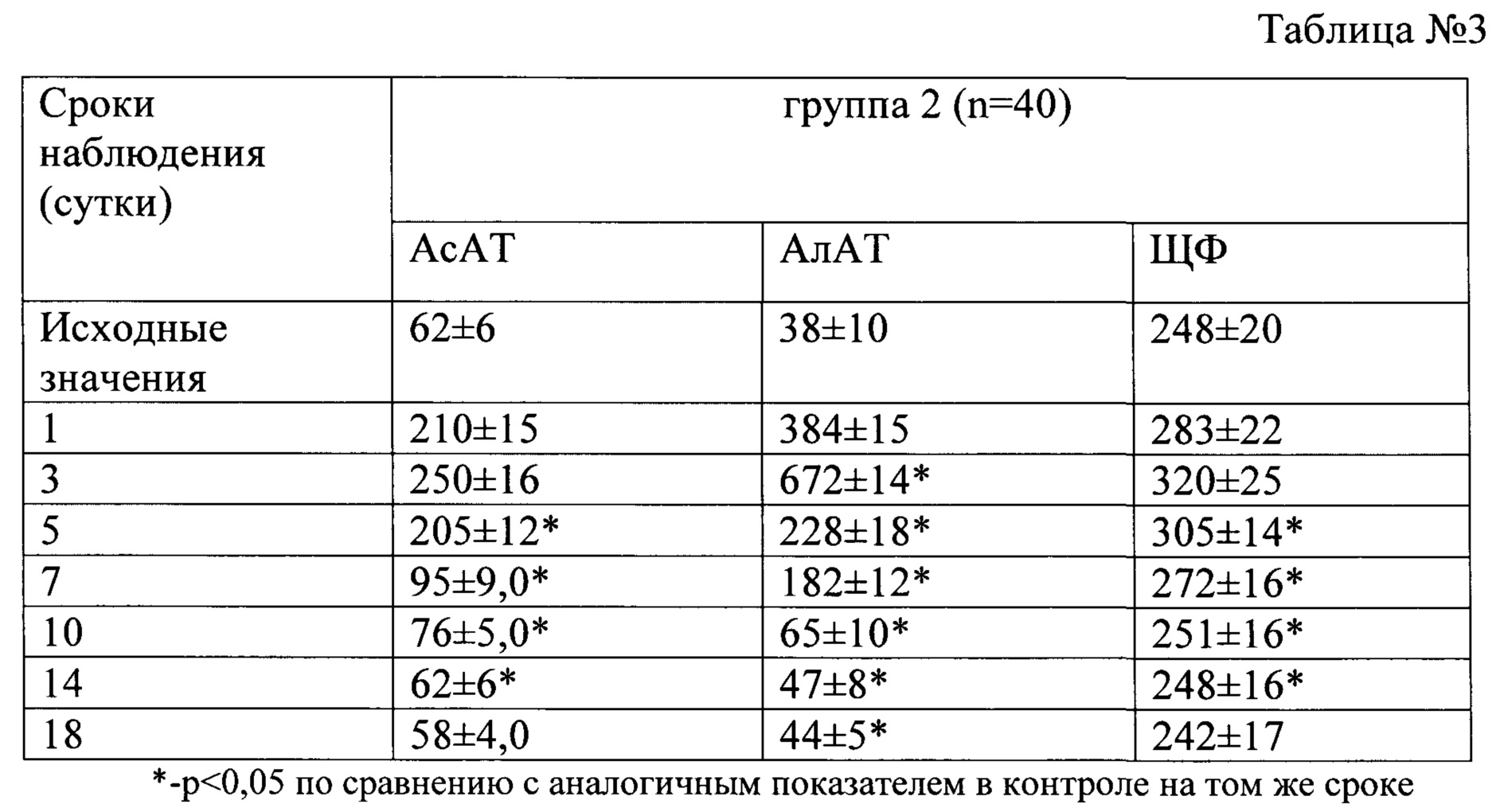
Приводим результаты сравнительного изучения эффективности применения неактивированной оРНК, выделенной из свежевыделенных ККМ, и из активированной оРНК, выделенной из ККМ после их гипотермического хранения в растворе «Кустодиол» для ускорения темпа индукции восстановительных процессов в печени в соответствии с пердлагаемым способом при ОПН после обширной (70-75%) резекции печени. Для контроля восстановления функциональных показателей печени проводили динамические исследования активности цитолитических ферментов в сыворотке крови крыс 1, 2 и 3 группы. В таблице 2, представлена динамика восстановления уровня активности цитолитических ферментов после обширной резекции печени в 1 - контрольной группе - введение физиологического раствора. В таблице 3 представлена динамика восстановления уровня активности цитолитических ферментов у крыс в группе 2, где после моделирования обширной резекции печени интраоперационно однократно внутрибрюшинно применяли неактивированную оРНК из свежевыделенных ККМ.
Так как в подгруппах А и Б у крыс 2 группы опытов, где применялись разные дозы оРНК (90 и 110 мкг/100 г веса животного), не было выявлено достоверных различий исследуемых показателей по срокам, результаты в подгруппах А и Б были объединены и составили цифровые значения исследуемых показателей в таблице 3.
В таблице 4 представлены результаты изучения динамики восстановления активности цитолитических ферментов в сыворотке крови крыс группы 3, где после моделирования обширной резекции печени интраоперационно однократно внутрибрюшинно применяли активированную оРНК в дозе 90 и 110 мкг/100 г веса животного из ККМ, подвергнутых аутофагии путем гипотермического хранения при 4-6°С в растворе «Кустодиол» в течение 3-18 часов. Так как в подгруппах А и Б у крыс группы 3, где применялись разные дозы активированной оРНК (90 и 110 мкг/100 г веса животного), выделенные из ККМ, подвергнутых разным режимам гипотермической консервации в растворе «Кустодиол» в пределах указанного диапазона значений (см. выше), не было выявлено достоверных различий уровня активности цитолитических ферментов на одних и тех же исследуемых сроках, полученные результаты были объединены и составили цифровые значения исследуемых показателей представленных в таблице 4.
Сравнительный анализ результатов, представленных в таблицах 2, 3 и 4, позволил установить, что в таблице 2 (контрольная 1 группа) показатели цитолиза (АлАТ, АсАТ и ЩФ) у выживших животных резко и неуклонно нарастали в течение первых 5 суток, затем стабилизировались и начиная с 10-14 суток возникала отчетливая тенденция их нормализации. В группе 2 (таблица №3) показатели цитолиза нарастали лишь в течение 1 и 3-х суток; к 5-м суткам намечалась отчетливая тенденция к снижению цитолитической активности. На 5-е сутки снижение цитолитической активности становилось для всех исследованных печеночных ферментов АлАТ, АсАТ и ЩФ достоверным по сравнению с контролем.
В группе 3 - опытной (таблица 4) ферменты цитолиза также нарастали в течение 1 и 2 суток, но уже на 3 сутки снижение цитолитической активности АлАТ, АсАТ в сыворотке крови становилось достоверным по сравнению с контролем (таблица 2), а на 5 сутки снижение уровня ферментов цитолиза было более выраженным и достоверным по сравнению с показателями в группе 2 (таблица 3). В результате нормализация исследуемых показателей в сыворотке крови наступала в группе 1 к 18 суткам, в группе 2 к 10-12 суткам, а в группе 3, к 6-8 суткам.
Исследование митотической активности гепатоцитов из резецированной печени позволило установить ее активацию через 48 часов во всех трех исследуемых группах (достоверные различия в митотической активности гепатоцитов печени крыс в подгруппах А и Б в группах 2 и 3 отсутствовали и поэтому результаты их подгрупп были объединены) по сравнению с исходным уровнем: исходный уровень митотической активности, оцениваемый до резекции печени по МИ, составил 0,2-0,3 промилле - %о - (1-2 митоза на 30 полей зрения), тогда как в 1 (контрольной) группе МИ через 48 час после обширной резекции печени составил 5,181%о (на 7334 клетки определялось 38 митозов), а в группе 2 с введением неактивированных оРНК из мононуклеарной фракции ККМ на этом же сроке МИ составил 21,7%о (на 9526 клеток определялось 207 митозов), т.е. во второй группе МИ был приблизительно в 4 раза выше, чем в первой контрольной группе, в 3 опытной группе МИ составил 31,8%о (10564 клеток определялось 335 митозов), то есть в группе 3 МИ был выше, чем в группе 1 более чем в 6 раз и почти в 1,5 раза выше по сравнению с группой 2. Приведенные изменения митотической активности гепатоцитов в печени крыс 1, 2 и 3 групп через 48 часов после резекции печени были установлены на основании подсчета количества митотически делящихся гепатоцитов в 30 полях зрения, однако уже в каждом поле зрения гистологических препаратов во 2, но особенно в 3 группе выявлялось существенно большее количество митотически делящихся гепатоцитов, чем в 1 - контрольной группе.
Анализируя полученные результаты, мы установили, что в группе 2 повышенный уровень митотической активности гепатоцитов сохраняется в течение 5 суток, тогда как в группе 3 повышенный уровень митотической активности снижается уже к 3 суткам после моделирования обширной резекции печени. В контроле слегка повышенный уровень митотической активности по сравнению с исходным уровнем сохраняется в сроках до 10 суток. Эти данные представлены на рис. 1, который отражает динамику сравнительного изучения митотической активности гепатоцитов (МИ) в 1, 2 и 3 группах опытов в течение 14 суток после обширной резекции печени. (*-р<0,05 по сравнению с группами 1 и 3; #-р<0,05 по сравнению с группами 2 и 3).
Достоверно более высокий уровень митотической активности гепатоцитов в группе 3 по сравнению с 1 и 2 группами на 2 сутки способствует достоверно более раннему восстановлении исходной массы печени после обширной резекции у животных группы 3.
Достоверно более высокий уровень митотической активности гепатоцитов на 2 сутки после моделирования обширной резекции печени и достоверно более резкое и раннее снижение этого показателя на 3 сутки в печени крыс группы 3 находятся в соответствии с более ранним (к 6-8 суткам) восстановлением функции печени у крыс в этой группе, так как известно, что митотически делящиеся клетки не способны одновременно эффективно выполнять свои регенераторные и тканеспецифические функции.
На рис. 2 представлена динамика восстановления массы печени после обширной резекции в 3х группах опытов: в 1 - контрольной (введение физиологического раствора), в группе 2 с интраоперационным введением неактивированной оРНК из ККМ в дозе 90 и 110 мкг/100 г веса животного и в группе 3 с интраоперационным введением активированной оРНК из ККМ в дозе 90 и ПО мкг/100 г веса животного, предварительно подвергнутых аутофагии, что соответствует их предварительной активации. (*-р<0,05 по сравнению с группами 1 и 3; #-р<0,05 по сравнению с группами 3 и 2).
Из рисунка 2 видно, что в группах 2 и 3 темп восстановления массы печени до исходных значений был выше, чем в контроле, причем в группе 3 темп восстановления массы печени до исходных значений был выше, чем в группе 2. В 1-контрольной группе восстановление массы печени происходило в более медленном темпе, особенно в первые две недели после резекции, в результате масса печени только к 18-20 суткам приближалась к исходным значениям и полностью восстанавливалась лишь на 22-24 сутки наблюдения. Нами отмечено также, что более высокий темп восстановления массы печени в группе 2 коррелировал с более высоким темпом восстановления функциональных показателей печени (АлАТ, АсАТ, ЩФ) в этой группе по сравнению с контролем.
В группе 3 восстановление массы печени до исходного уровня происходило быстрее, чем в группе 2 - к 8-10 суткам наблюдения и это соответствовало еще более раннему восстановлению функциональных показателей в группе 3 (таблицы 2-4) по сравнению с группами 1 и 2.
Подтверждением того, что процесс регенерации печени (подобно другим органам) начинается с усиления аутофагии, могут служить результаты динамического измерения массы остатка печени в опытах с применением оРНК. Из рисунка 2 видно, что, несмотря на иссечение одинаковой массы печени (70-75%) во всех 3 группах опытов в течение первых 2 суток наблюдается процесс более резкого снижения массы печени во 2 и 3-ей группах опытов, причем достоверным это снижение было в группе 3 на сроке 48 часов, по сравнению с контролем, где более резкое снижение массы остатка печени ко 2-м суткам наблюдения сменялось более резким повышением скорости восстановления массы печени с достижением исходных значений к 8-10 суткам.
В 30 опытах на крысах с субтотальной резекцией (85-90%) печени, у которых по данным литературы уровень летальности достигает 90% [Madrahimov N, Dirsch О, Broelsch С, Dahmen U. Marginal hepatectomy in the rat: from anatomy to surgery. //Ann Surg. 2006; - Vol. 244. - p. 89-98; Рудаков B.C., Астрелина T.A., Губарев K.K., Журбин A.C., Светлакова Д.С., Восканян С.Э. Влияние трансплантации аллогенных мультипотентных мезенхимальных стромальных клеток костного мозга на летальность и продолжительность жизни после обширных резекций печени: экспериментальное исследование // Клин. и эксперимент.хир. Журн. им. акад. Б.В. Петровского. 2019. Т. 7, No 2. С. 31-37], была изучена возможность снижения летальности после применения активированной оРНК. Было выполнено 2 группы опытов: 1 -контроль (n=10) - моделирование субтотальной резекции печени с введением физиологического раствора и 2 - опыт (n=20), где однократное интраоперационное внутрибрюшинное введение активированной оРНК в дозе 90 мкг/100 г (n=10) и 110 мкг/100 г веса животного (n=10) выполняли у животных с субтотальной резекцией печени. Исследование летальности крыс в течение 10 суток, показало, что в контроле летальность составила 8 крыс из 10, когда как в опытах с введением оРНК в дозе 90 мкг/100 г веса погибло 4 из 10, а с введением 110 мкг/100 г веса погибло 5 из 10, то есть активированная оРНК способствовала снижению летальности у крыс с субтотальной резекцией печени практически в 2 раза.
В совокупности полученные результаты позволяют заключить, что однократное интраоперационное введение активированной оРНК в дозе 90-110 мкг/100 грамм веса животного по предлагаемому способу лечения ОПН обеспечивает более быстрый темп нормализации показателей функции печени, исключает возникновение летальных исходов после обширной резекции и существенно снижает летальность при субтотальной резекции печени за счет индукции раннего и более высокого уровня митотической и пролиферативной активности клеток печени, позволяющей в более короткие сроки превысить критические значения массы печени и достигнуть адекватных значений функционирующей массы печени, способной обеспечить ускоренное восстановление печеночного гомеостаза в организме.
Claims (2)
1. Способ лечения острой печеночной недостаточности в эксперименте, после хирургической операции, в результате которой формируется критический дефицит функционирующей ткани печени, отличающийся тем, что получают несортированную фракцию мононуклеарных клеток костного мозга от крысы-донора и хранят в растворе «Кустодиол» при температуре 4-6°С в течение 3-18 часов, после чего из нее получают общую РНК и вводят однократно внутрибрюшинно интраоперационно экспериментальному животному - крысе после выполнения хирургической операции, в результате которой формируется критический дефицит функционирующей ткани печени, в дозе 90-110 мкг/100 г веса животного.
2. Способ по п. 1, отличающийся тем, что хирургической операцией, в результате которой формируется критический дефицит функционирующей ткани печени, является обширная или субтотальная резекция печени.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2020119914A RU2744846C1 (ru) | 2020-06-16 | 2020-06-16 | Способ лечения острой печёночной недостаточности |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2020119914A RU2744846C1 (ru) | 2020-06-16 | 2020-06-16 | Способ лечения острой печёночной недостаточности |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2744846C1 true RU2744846C1 (ru) | 2021-03-16 |
Family
ID=74874443
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2020119914A RU2744846C1 (ru) | 2020-06-16 | 2020-06-16 | Способ лечения острой печёночной недостаточности |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2744846C1 (ru) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2701792C1 (ru) * | 2018-10-30 | 2019-10-01 | Федеральное государственное бюджетное учреждение "Национальный медицинский исследовательский центр трансплантологии и искусственных органов имени академика В.И. Шумакова" Министерства здравоохранения Российской Федерации (ФГБУ "НМИЦ ТИО им. ак. В.И. Шумакова" Минздрава России) | Способ лечения острой печеночной недостаточности |
| RU2739996C1 (ru) * | 2020-06-16 | 2020-12-30 | Федеральное государственное бюджетное учреждение "Национальный медицинский исследовательский центр трансплантологии и искусственных органов имени академика В.И. Шумакова" Министерства здравоохранения Российской Федерации (ФГБУ "НМИЦ ТИО им. ак. В.И. Шумакова" Минздрава России) | Способ коррекции хронической печёночной недостаточности |
-
2020
- 2020-06-16 RU RU2020119914A patent/RU2744846C1/ru active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2701792C1 (ru) * | 2018-10-30 | 2019-10-01 | Федеральное государственное бюджетное учреждение "Национальный медицинский исследовательский центр трансплантологии и искусственных органов имени академика В.И. Шумакова" Министерства здравоохранения Российской Федерации (ФГБУ "НМИЦ ТИО им. ак. В.И. Шумакова" Минздрава России) | Способ лечения острой печеночной недостаточности |
| RU2739996C1 (ru) * | 2020-06-16 | 2020-12-30 | Федеральное государственное бюджетное учреждение "Национальный медицинский исследовательский центр трансплантологии и искусственных органов имени академика В.И. Шумакова" Министерства здравоохранения Российской Федерации (ФГБУ "НМИЦ ТИО им. ак. В.И. Шумакова" Минздрава России) | Способ коррекции хронической печёночной недостаточности |
Non-Patent Citations (5)
| Title |
|---|
| BAI H. et al. Comprehensive analysis of lncRNA-miRNA-mRNA during proliferative phase of rat liver regeneration. J Cell Physiol. 2019, 234(10), p.18897-18905. * |
| YAN I.K. et al. Circulating Extracellular RNA Markers of Liver Regeneration. PLoS One. 2016, 11(7), e0155888. * |
| ГОНИКОВА З.З. Исследование регенераторной активности общей РНК клеток костного мозга на экспериментальных моделях печеночной недостаточности. Диссер. Москва 2019, стр.1-118. * |
| ГОНИКОВА З.З. Исследование регенераторной активности общей РНК клеток костного мозга на экспериментальных моделях печеночной недостаточности. Диссер. Москва 2019, стр.1-118. РУДАКОВ В.С. Влияние мультипотентных мезенхимальных стромальных клеток на регенерацию печени после ее обширной резекции. Автореф. диссер. Москва 2017, стр.1-24. BAI H. et al. Comprehensive analysis of lncRNA-miRNA-mRNA during proliferative phase of rat liver regeneration. J Cell Physiol. 2019, 234(10), p.18897-18905. YAN I.K. et al. Circulating Extracellular RNA Markers of Liver Regeneration. PLoS One. 2016, 11(7), e0155888. * |
| РУДАКОВ В.С. Влияние мультипотентных мезенхимальных стромальных клеток на регенерацию печени после ее обширной резекции. Автореф. диссер. Москва 2017, стр.1-24. * |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2019203555B2 (en) | Compositions and methods for treating and preventing tissue injury and disease | |
| Wang et al. | Activated human umbilical cord blood platelet‐rich plasma enhances the beneficial effects of human umbilical cord mesenchymal stem cells in Chemotherapy‐induced POF rats | |
| RU2744846C1 (ru) | Способ лечения острой печёночной недостаточности | |
| RU2739996C1 (ru) | Способ коррекции хронической печёночной недостаточности | |
| RU2701792C1 (ru) | Способ лечения острой печеночной недостаточности | |
| Gokkaya et al. | Skin graft storage in platelet rich plasma (PRP) | |
| CN114599379A (zh) | 一种用于预防或治疗脓毒症的药物组合物、试剂盒及其应用和治疗方法 | |
| Alhabboubi et al. | Injection of rat mesenchymal stem cells leads to their homing and differentiation in the liver in a blunt liver trauma model | |
| BR102016022647A2 (pt) | métodos para tratar disfunção de órgão ou tecido relacionada à idade através de transbiose heterocrônica com o uso de células-tronco pluripotentes não viáveis | |
| CN119857099A (zh) | Hy-133073在制备抗肝癌中枢免疫逃逸药物中的应用 | |
| Bukulmez | Activation of Ovarian Cortex | |
| CN114209840A (zh) | 一种mif抑制剂在制备治疗骨关节炎的药物中的应用 | |
| Keck et al. | LP1: the influence of Local Anesthetics on Viability and Proliferation of Preadipocytes and Their Differentiation to Adipocytes | |
| Baumann et al. | LP20: Improving Aesthetic Outcomes in Head and Neck Reconstruction with Structural Fat Grafting | |
| Hendrickx et al. | LP15: Wound Bed Vascularization by Endothelial Cells: Differentiation Status Matters | |
| Contaldo et al. | LP18: Platelet Derived Serotonin Plays a Critical Role during Skeletal Muscle Ischemia and Reperfusion Injury | |
| Hollenbeck et al. | LP8: THE EXTENDED ABDOMINAL WALL FLAP FOR CTA | |
| Kueckelhaus et al. | LP31: Promotion of Wound Healing by Regulator Proteins of the Innate Immune System | |
| Engel et al. | LP2: Variable Vascular Carriers for Neoangiogenesis and Mutual Seeding of Bone Marrow Mesenchymal Stem Cells and Osteocytes for Advanced Osseous Tissue Engineering | |
| Tom et al. | LP6: An Analysis of Patient Quality of Life and Morbidity Due to Hand and Upper Extremity Trauma in Honduras | |
| Kuhbier et al. | LP12: Adipose-Derived Stem Cells Seeded on Three-Dimensional Scaffolds of Spider Silk | |
| Rohleder et al. | LP37: Expression of Antimicrobial Peptides in Maxillofacial Surgical Site Infections | |
| von Wild et al. | LP41: NEUROMODULATION IN FUNCTIONAL-RECONSTRUCTION THROUGH PERIPHERAL NERVE TRANSPLANTATION INTO CENTRAL NERVE SYSTEM IN SPINAL CORD INJURY IN RATS APPLYING CEREBROLYSIN | |
| Largo et al. | LP13: ACCELERATED VASCULARISATION AND IMPROVED BONE FORMATION IN CRITICAL-SIZE BONE GRAFTS BY VEGF-EXPRESSING BMSC IN A RABBIT MODEL | |
| Fabre et al. | LP25: OUTCOME AFTER REVISION OF MICROVASCULAR FREE DIEP, SIEA AND SGAP FLAP FOR AUTOLOGEOUS BREAST RECONSTRUCTION: A RETROSPECTIVE ANALYSIS |