JP2022533067A - 疾病治療用ナノ粒子複合体及びその製造方法 - Google Patents
疾病治療用ナノ粒子複合体及びその製造方法 Download PDFInfo
- Publication number
- JP2022533067A JP2022533067A JP2021567055A JP2021567055A JP2022533067A JP 2022533067 A JP2022533067 A JP 2022533067A JP 2021567055 A JP2021567055 A JP 2021567055A JP 2021567055 A JP2021567055 A JP 2021567055A JP 2022533067 A JP2022533067 A JP 2022533067A
- Authority
- JP
- Japan
- Prior art keywords
- nanoparticles
- lipid
- reactive group
- bound
- nanoparticle
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5192—Processes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/543—Lipids, e.g. triglycerides; Polyamines, e.g. spermine or spermidine
- A61K47/544—Phospholipids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6901—Conjugates being cells, cell fragments, viruses, ghosts, red blood cells or viral vectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6905—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a colloid or an emulsion
- A61K47/6919—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a colloid or an emulsion the form being a ribbon or a tubule cochleate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/0008—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'non-active' part of the composition delivered, e.g. wherein such 'non-active' part is not delivered simultaneously with the 'active' part of the composition
- A61K48/0025—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'non-active' part of the composition delivered, e.g. wherein such 'non-active' part is not delivered simultaneously with the 'active' part of the composition wherein the non-active part clearly interacts with the delivered nucleic acid
- A61K48/0033—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'non-active' part of the composition delivered, e.g. wherein such 'non-active' part is not delivered simultaneously with the 'active' part of the composition wherein the non-active part clearly interacts with the delivered nucleic acid the non-active part being non-polymeric
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/0091—Purification or manufacturing processes for gene therapy compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/5123—Organic compounds, e.g. fats, sugars
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/87—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation
- C12N15/88—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation using microencapsulation, e.g. using amphiphile liposome vesicle
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y5/00—Nanobiotechnology or nanomedicine, e.g. protein engineering or drug delivery
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Biomedical Technology (AREA)
- Epidemiology (AREA)
- Biotechnology (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- General Engineering & Computer Science (AREA)
- Nanotechnology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Optics & Photonics (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Microbiology (AREA)
- Plant Pathology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Virology (AREA)
- Manufacturing & Machinery (AREA)
- Dispersion Chemistry (AREA)
- Medical Informatics (AREA)
- Crystallography & Structural Chemistry (AREA)
- Cell Biology (AREA)
- Hematology (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
本発明は、疾病治療用ナノ粒子複合体及びその製造方法に係り、より詳細には、ナノ粒子の表面の一部分にチューブ状の脂質構造体が結合してエンドサイトーシスを引き起こすだけでなく、細胞膜を直接貫通することができ、向上した組織透過能力によりスフェロイド状の腫瘍細胞内にナノ粒子を効果的に取り込ませることができ、リピドーム形成の際に使用される第2反応基が結合しているリン脂質と第2反応基が結合していないリン脂質との比率を調節することにより、ナノ粒子の表面に十分な長さの脂質構造体を形成することができるナノ粒子複合体及びその製造方法に関する。【選択図】図16
Description
本発明は、疾病治療用ナノ粒子複合体及びその製造方法に係り、より詳細には、ナノ粒子の表面の一部分にチューブ状の脂質構造体が結合してエンドサイトーシスを引き起こすだけでなく、細胞膜を直接貫通することができ、向上した組織透過能力によりスフェロイド状の腫瘍細胞内にナノ粒子を効果的に取り込ませることができ、リピドーム形成の際に使用される第2反応基が結合したリン脂質と第2反応基が結合していないリン脂質との比率を調節することにより、ナノ粒子の表面に十分な長さの脂質構造体を形成することができるナノ粒子複合体及びその製造方法に関する。
薬物送達分野において、細胞内取り込み効率は、薬物送達効能を達成するための重要な尺度になる。このため、細胞内取り込み効率を向上させるための技術が広く開発されている。一例として、下記特許文献に記載されているように、ナノ粒子に細胞透過性ペプチドなどを化学的に結合させてナノ粒子の細胞内取り込み効率を向上させようとしている。
しかしながら、従来の細胞内取り込み効率を向上させるための技術は、十分な効果を得ることができず、結合した物質が容易に分解されて安定性に劣るという問題点がある。
本発明は、かかる問題点を解決するためになされたもので、その目的は、安定性が高く生体適合性に優れた脂質ベースの物質でナノ粒子の表面を改質することにより細胞内取り込み効率を飛躍的に向上させたナノ粒子複合体及びその製造方法を提供することにある。
本発明の他の目的は、ナノ粒子の表面の一部分にチューブ状の脂質構造体を形成することで、エンドサイトーシス(サイズ100~200nmの粒子が細胞内に取り込まれるメカニズムである)だけでなく、細胞膜を直接貫通しうるナノ粒子複合体及びその製造方法を提供することにある。
本発明の別の目的は、向上した組織透過(tissue penetration)能力によりスフェロイド状の腫瘍細胞内にナノ粒子を効果的に取り込ませることができるナノ粒子複合体及びその製造方法を提供することにある。
本発明の別の目的は、誘電体薬物を担持する或いは誘電体薬物自体からなるナノ粒子の細胞及び組織への送達効果を向上させることにより、遺伝子治療効率を高めることができるナノ粒子複合体及びその製造方法を提供することにある。
本発明の別の目的は、脂質構造体をナノ粒子に直接付着させることなく、脂質ベースのリピドーム(バブル、リポソームなど)とナノ粒子とを結合させた後、物質的な力を加えてリピドームが破砕されてナノ粒子の表面に脂質構造体が形成されるようにするTop-down方式を用いるので、容易に量産が可能なナノ粒子複合体及びその製造方法を提供することにある。
本発明の別の目的は、リピドーム形成の際に用いられる第2反応基が結合したリン脂質と第2反応基が結合していないリン脂質との比率を調節して、前記ナノ粒子の表面に十分な長さの脂質構造体を形成することができるナノ粒子複合体及びその製造方法を提供することにある。
本発明は、上記の目的を達成するために、以下の構成を持つ実施形態によって実現される。
本発明の一実施形態によれば、本発明によるナノ粒子複合体は、細胞内に取り込まれるナノ粒子と、前記ナノ粒子の外表面の一部分に複数個が自己組織化されてナノ粒子の細胞内取り込み効率を向上させる脂質ベースの脂質構造体と、を含むことを特徴とする。
本発明の他の実施形態によれば、本発明によるナノ粒子複合体において、前記ナノ粒子は、第1反応基を含み、前記脂質構造体を構成する脂質のうちの一部の脂質はナノ粒子の第1反応基と化学結合する第2反応基を含んでおり、優先的に前記第1反応基と前記第2反応基とが化学結合し、一部の脂質がナノ粒子に結合し、これを始点として残りの脂質が自己組織化によって脂質構造体を形成することを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体において、前記脂質構造体は、第2反応基が結合した脂質と、第2反応基が結合していない脂質との混合物からなるリピドームの自己組織化によって形成され、前記第2反応基が結合した脂質と第2反応基が結合していない脂質との混合比率を調節して、ナノ粒子に結合した脂質構造体の生成及び形態を制御することができることを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体において、前記第2反応基が結合した脂質と第2反応基が結合していない脂質とは1:2.33~99のモル比で混合されることを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体において、前記脂質構造体は、親水性を呈する脂質頭部が外側面に位置し、内部に疎水性を呈する脂質尾部が位置することで、全体的に長尺なチューブ形状を有することを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体において、前記ナノ粒子は50~500nmの直径を有し、前記脂質構造体は50~300nmの長さ及び3~20nmの幅を有することを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体は、従来のナノ粒子の細胞内に入り込むメカニズムであるエンドサイトーシスを引き起こすだけでなく、細胞膜を直接貫通して細胞内に取り込まれることができることを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体において、前記脂質構造体は、前記ナノ粒子のがん細胞スフェロイド細胞内取り込み効率を向上させることができることを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体において、前記ナノ粒子は、抗がん剤を含み、抗がん抵抗性を有する腫瘍細胞の死滅効率を向上させることができることを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体において、前記ナノ粒子は、誘電体薬物が担持されたナノ粒子又は誘電体薬物自体からなるナノ粒子が使用され、遺伝子治療効率を向上させることができることを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体の製造方法は、第1反応基が存在するナノ粒子を形成するナノ粒子形成ステップと、前記第1反応基と化学的に結合する第2反応基が存在する脂質ベースのマイクロサイズのリピドームを形成するリピドーム形成ステップと、前記ナノ粒子と前記リピドームとを混合して第1反応基と第2反応基とが互いに結合するようにして、前記リピドームの外面にナノ粒子が結合したリピドーム-ナノ粒子複合体を形成する脂質複合体形成ステップと、前記脂質複合体形成ステップで形成されたリピドーム-ナノ粒子複合体に機械的な力を加えてリピドームを破砕して、ナノ粒子の外表面の一部分に結合した脂質構造体を形成することにより、ナノ粒子複合体を製造する破砕形成ステップと、を含み、前記リピドーム形成ステップは、第2反応基が結合した脂質と第2反応基が結合していない脂質との混合物を用いてリピドームを形成し、前記ナノ粒子は細胞内に取り込まれ、前記脂質構造体はナノ粒子の細胞内取り込み効率を向上させることを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体の製造方法において、前記第2反応基が結合した脂質と前記第2反応基が結合していない脂質との混合比率を調節して、ナノ粒子に結合した脂質構造体の生成及び形態を制御することができることを特徴とする。
本発明の別の実施形態によれば、本発明によるナノ粒子複合体の製造方法において、前記破砕形成ステップでは、リピドーム-ナノ粒子複合体に機械的な力を加えて一定時間維持することにより、リピドームが破砕され、リピドームを成すリン脂質は再組み合わせが起こり、ナノ粒子に結合したチューブ状の脂質構造体が形成されることを特徴とする。
本発明は、まず、本実施形態によって次の効果を得ることができる。
本発明は、安定性が高く生体適合性に優れた脂質ベースの物質でナノ粒子の表面を改質することにより、細胞内取り込み効率を飛躍的に向上させることができるという効果がある。
また、本発明は、ナノ粒子の表面の一部分にチューブ状の脂質構造体が形成されることにより、エンドサイトーシス(サイズ100~200nmの粒子が細胞内に取り込まれるメカニズムである)を引き起こすだけでなく、細胞膜を直接貫通することができるようにするという効果がある。
また、本発明は、向上した組織透過(tissue penetration)能力によりスフェロイド状の腫瘍細胞内にナノ粒子を効果的に取り込ませることができるという効果がある。
また、本発明は、脂質構造体をナノ粒子に直接付着させず、脂質ベースのリピドーム(バブル、リポソームなど)とナノ粒子とを結合させた後、物質的な力を加えることにより、リピドームが破砕され、ナノ粒子の表面に脂質構造体が形成されるようにするTop-down方式を用いるので、容易に量産が可能であるという効果がある。
また、本発明は、リピドーム形成の際に用いられる第2反応基が結合したリン脂質と第2反応基が結合していないリン脂質との比率を調節して、前記ナノ粒子の表面に十分な長さの脂質構造体を形成することができるという効果がある。
以下、本発明による疾病治療用ナノ粒子複合体及びその製造方法を添付図面を参照して詳細に説明する。特別な定義がない限り、本明細書のすべての用語は、本発明の属する技術分野における通常の知識を有する技術者が理解する当該用語の一般的な意味と同一であり、もし本明細書で使用された用語の意味と衝突する場合には、本明細書で使用された定義に従う。なお、本発明の要旨を無駄に不明瞭にするおそれのある公知の機能及び構成についての詳細な説明は省略する。本明細書全体において、ある部分がある構成要素を「含む」とするとき、これは、特に反対の記載がない限り、他の構成要素を除外するのではなく、他の構成要素をさらに含むことができることを意味する。
本発明の一実施形態による疾病治療用ナノ粒子複合体を図1~図24を参照して説明すると、前記ナノ粒子複合体は、細胞内に取り込まれるナノ粒子1と、前記ナノ粒子1の外表面の一部分に結合してナノ粒子1の細胞内取り込み効率を向上させる脂質ベースの脂質構造体2などを含む。
前記ナノ粒子1は、細胞内に取り込まれる構成であり、疾病の治療などに用いられることができる。前記ナノ粒子1は、例えば薬物を担持するか、或いは疾病を治療することができる物質からなるが、細胞内に取り込まれて疾病の治療に用いられる従来の様々なナノ粒子が使用でき、例えば、疾患の治療に用いられる、アルブミンナノ粒子、核酸とアルブミンからなるナノ粒子、生分解性高分子ナノ粒子、核酸ナノ粒子、ウイルス粒子などを例示することができる。前記ナノ粒子は、例えば50~500nmの直径及び球形の形状などを有することができる。前記ナノ粒子は、脂質構造体と結合する化学反応基(以下、「第1反応基」という)を含むことができる。例えば、第1反応基としては、チオール基、アミン基、アミノ基、カルボキシ基などを含む化合物であり得る。
前記脂質構造体2は、ナノ粒子1の外表面の一部分に結合してナノ粒子1の細胞内取り込み効率を向上させる脂質ベースの構造体であって、前記脂質構造体は、例えば50~300nmの長さ及び3~20nmの幅を有することができ、前記ナノ粒子の外表面に一つ以上が結合することができる。また、前記脂質構造体は、ナノ粒子の第1反応基と化学結合する化学反応基(以下、「第2反応基」という)を含むことができる。例えば、第2反応基としてチオール基、アミン基、アミノ基、カルボキシ基などを含む化合物であってもよい。前記脂質構造体は、第2反応基が結合した脂質と、第2反応基が結合していない脂質との混合比率を調節して脂質構造体の生成及び形態(模様及び長さなど)を制御することができ、第2反応基が結合した脂質と第2反応基が結合していない脂質は、1:2.33~99のモル比で混合されることが好ましい。
前記脂質構造体は、例えば、親水性を呈する脂質頭部21が外側面に位置し、内部に疎水性を呈する脂質尾部22が位置することにより、全体的に長尺なチューブ形状を有することができ、チューブ形状の脂質構造体の一端に位置する第2反応基が前記ナノ粒子の第1反応基と化学結合してチューブ状の脂質構造体がナノ粒子1の外表面に結合する。例えば、ナノ粒子がアルブミンナノ粒子であり、前記脂質構造体にNHS(N-ヒドロキシスクシニミド)反応基を形成する場合、NHS-アミン反応によって前記ナノ粒子1と脂質構造体2とを結合させることができる。本発明は、安定性が高く生体適合性に優れた脂質ベースの物質でナノ粒子の表面を改質することにより、細胞内取り込み効率を飛躍的に向上させることができ、サイズ100~200nmのナノ粒子が細胞内に取り込まれるメカニズムはエンドサイトーシスであるが、前記ナノ粒子複合体は、ナノ粒子の表面の一部分にチューブ状の脂質構造体が結合してエンドサイトーシスを引き起こすだけでなく、細胞膜を直接貫通することができ、スフェロイド状の腫瘍細胞を効果的に摂取して生体モデルにも適用することができる。
本発明の他の実施形態によるナノ粒子複合体の製造方法を説明すると、前記ナノ粒子複合体の製造方法は、第1反応基が存在するナノ粒子を形成するナノ粒子形成ステップと、前記第1反応基と化学的に結合する第2反応基が存在する脂質ベースのマイクロサイズのリピドーム(バブル、リポソームなど)を形成するリピドーム形成ステップと、前記ナノ粒子とリピドームとを混合して第1反応基と第2反応基とが互いに結合するようにして、リピドームの外面にナノ粒子が結合したリピドーム-ナノ粒子複合体を形成する脂質複合体形成ステップと、前記脂質複合体形成ステップで形成されたリピドーム-ナノ粒子複合体に機械的な力(mechanical force)を加えることでリピドームを破砕して、ナノ粒子の外表面の一部分に結合した脂質構造体を形成する破砕形成ステップなどとを含む。
前記ナノ粒子形成ステップは、細胞内に取り込まれて疾病の治療に用いられるナノ粒子が第1反応基を含むように前記ナノ粒子を形成するステップであって、従来の様々なナノ粒子を製造する方法が使用でき、例えば、薬物を担持したアルブミンナノ粒子の場合、アルブミンにアミン基が存在して第1反応基として用いられることができ、特定のタンパク質の発現を抑制するsiRNAナノ粒子の場合、アミンが付いているヒアルロン酸をsiRNAナノ粒子にコーティングしてsiRNAナノ粒子に第1反応基を形成することができる。
前記リピドーム形成ステップは、前記第1反応基と化学的に結合する第2反応基が存在する脂質ベースのマイクロサイズのリピドーム(バブル、リポソームなど)を形成するステップであり、例えばバブルは脂質(例えば、リン脂質)で形成され、内部にガスが充填されており、前記バブルに第2反応基が位置する。内部にガスを有し、脂質からなるリポソーム状のマイクロサイズのバブルは、従来の製造方法によって製造でき、例えば、第2反応基が結合した脂質と第2反応基が結合していない脂質とを有機溶媒に一定の比率で混合して脂質フィルムを形成し、前記脂質フィルムを溶媒に溶かしてガスを注入することにより形成することができる。第2反応基が結合した脂質と第2反応基が結合していない脂質との混合比率を調節して脂質構造体の生成及び形態(模様及び長さなど)を制御することができ、第2反応基が結合した脂質と第2反応基が結合していない脂質とは、1:2.33~99のモル比で混合されることが好ましい。
前記脂質複合体形成ステップは、前記ナノ粒子とリピドームとを混合して第1反応基と第2反応基とが互いに結合するようにして、脂質の外面にナノ粒子が結合したリピドーム-ナノ粒子複合体を形成するステップである。
前記破砕形成ステップは、前記脂質複合体形成ステップで形成されたリピドーム-ナノ粒子複合体に機械的な力(mechanical force)を加えてリピドームを破砕することにより、ナノ粒子の外表面の一部分に結合した脂質構造体を形成するステップである。リピドーム-ナノ粒子複合体に超音波機器などを用いて機械的な力を加えて一定時間維持する場合、リピドームが破砕され、リピドームを成す脂質は再組み合わせが起こり、ナノ粒子に結合したチューブ状の脂質構造体が形成される。具体的には、リピドーム-ナノ粒子複合体に機械的な力を加えるとリピドームが破砕され、第2反応基を有する一部の脂質が優先的にナノ粒子に結合し(第1反応基と第2反応基とが化学結合する)、これを始点として残りの脂質が自己組織化で脂質構造体を形成する。
本発明は、脂質構造体をナノ粒子に直接付着させず、脂質ベースのリピドームとナノ粒子とを結合させた後、機械的な力を加えてリピドームが破砕され、ナノ粒子の表面に脂質構造体が形成されるようにするTop-down方式を用いるので、容易に量産が可能であるようにすることができる。
以下、実施例によって本発明をより詳細に説明する。ところが、これらの実施例は本発明をより詳細に説明するためのものに過ぎず、本発明の権利範囲はこれらの実施例に限定されるものではない。
<実施例1>アルブミンナノ粒子複合体の製造
1.アルブミンナノ粒子(NPs)の準備
アルブミン(Human serum albumin)を蒸留水に20mg/mLの濃度で溶かした後、0.2M NaOHを用いてpHを8に調節してアルブミン溶液を準備し、100%エタノールを1mL/minの速度で前記アルブミン溶液に滴定した。その後、4%のグルタルアルデヒド10μLを添加し、遮光下にエタノールを一晩蒸発させ、13200rpm、10minの条件で遠心分離を行った後、粒子化されていないアルブミンをピペットを用いて除去し、PBSで再分散して3000rpm、5minの条件で遠心分離を行った後、マイクロペレット(micropellet)を除いた上清(ナノ粒子(NPs))をピペットで得た(一方、蛍光実験を行うときには、必要による蛍光色素(dye)とナノ粒子を一晩常温で反応させた後、13200rpm、10minの条件で遠心分離を行い、反応していない蛍光色素(dye)をピペットを用いて除去した後、PBSに再分散して使用する)。
1.アルブミンナノ粒子(NPs)の準備
アルブミン(Human serum albumin)を蒸留水に20mg/mLの濃度で溶かした後、0.2M NaOHを用いてpHを8に調節してアルブミン溶液を準備し、100%エタノールを1mL/minの速度で前記アルブミン溶液に滴定した。その後、4%のグルタルアルデヒド10μLを添加し、遮光下にエタノールを一晩蒸発させ、13200rpm、10minの条件で遠心分離を行った後、粒子化されていないアルブミンをピペットを用いて除去し、PBSで再分散して3000rpm、5minの条件で遠心分離を行った後、マイクロペレット(micropellet)を除いた上清(ナノ粒子(NPs))をピペットで得た(一方、蛍光実験を行うときには、必要による蛍光色素(dye)とナノ粒子を一晩常温で反応させた後、13200rpm、10minの条件で遠心分離を行い、反応していない蛍光色素(dye)をピペットを用いて除去した後、PBSに再分散して使用する)。
2.リピドーム(リポソーム)の準備
脂質DSPC(1,2-distearoyl-sn-glycero-3-phosphocholine)及びDSPE-PEG-NHS2000(1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N-polyethylene glycol succinimidyl ester)を9.25:0.75のモル比で混合してクロロホルムに10mg/mlの濃度で溶かした後、1mg/mlとなるようにlcバイアルに100μlずつ入れ、窒素ガスを用いてクロロホルムを蒸発させた後、デシケーター(desicatcator)を用いて真空引きをしながら1時間以上乾かすことにより脂質薄膜(lipid film)を形成した。lipid film vialにauto PBSを1ml入れて脂質溶液を形成し、温度55℃以上の水に脂質溶液入りのHPLCバイアルを入れて脂質溶液の温度が55℃以上となるようにし、バスソニケーターで15秒程度ソニケーション(sonication)を行うことにより(このとき、お湯に浸す過程とソニカレーション実施過程を3回程度繰り返す)、リポソームを形成した。
脂質DSPC(1,2-distearoyl-sn-glycero-3-phosphocholine)及びDSPE-PEG-NHS2000(1,2-distearoyl-sn-glycero-3-phosphoethanolamine-N-polyethylene glycol succinimidyl ester)を9.25:0.75のモル比で混合してクロロホルムに10mg/mlの濃度で溶かした後、1mg/mlとなるようにlcバイアルに100μlずつ入れ、窒素ガスを用いてクロロホルムを蒸発させた後、デシケーター(desicatcator)を用いて真空引きをしながら1時間以上乾かすことにより脂質薄膜(lipid film)を形成した。lipid film vialにauto PBSを1ml入れて脂質溶液を形成し、温度55℃以上の水に脂質溶液入りのHPLCバイアルを入れて脂質溶液の温度が55℃以上となるようにし、バスソニケーターで15秒程度ソニケーション(sonication)を行うことにより(このとき、お湯に浸す過程とソニカレーション実施過程を3回程度繰り返す)、リポソームを形成した。
3.リピドーム(脂質を用いたバブル)の準備
実施例1の2の過程を経て得た結果物を含むバイアルに、C3F8ガスを30秒間満たし、Vial Mixerを用いて45秒間混合することにより、NHS反応基を含む脂質ベースのマイクロバブルを形成した。
実施例1の2の過程を経て得た結果物を含むバイアルに、C3F8ガスを30秒間満たし、Vial Mixerを用いて45秒間混合することにより、NHS反応基を含む脂質ベースのマイクロバブルを形成した。
4.ナノ粒子複合体(Directional LT-NPs)の形成
(1)実施例1の1で形成されたナノ粒子をリポソーム溶液(実施例1の2で形成されたリポソームがPBSに1mg/mlの濃度で混合されて形成)に入れた後、NHS-アミン反応を誘導するためにRTで2時間以上反応させた後(このとき、リポソーム-ナノ粒子複合体(Liposome-NPs)が形成される)、超音波機器を用いて2W、1MHZ、デューティ比(duty cycle)100%の条件で5分以上機械的な力(mechanical force)を加えた。その後、破砕されたリポソームが脂質構造体を十分に形成することができるように、1時間以上RTでインキュベートしてナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体(Directional LT-NPs)を形成した。
(1)実施例1の1で形成されたナノ粒子をリポソーム溶液(実施例1の2で形成されたリポソームがPBSに1mg/mlの濃度で混合されて形成)に入れた後、NHS-アミン反応を誘導するためにRTで2時間以上反応させた後(このとき、リポソーム-ナノ粒子複合体(Liposome-NPs)が形成される)、超音波機器を用いて2W、1MHZ、デューティ比(duty cycle)100%の条件で5分以上機械的な力(mechanical force)を加えた。その後、破砕されたリポソームが脂質構造体を十分に形成することができるように、1時間以上RTでインキュベートしてナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体(Directional LT-NPs)を形成した。
(2)リポソームの代わりに、実施例1の3で形成されたマイクロバブルを用いた以外は、他の条件を実施例1の4の(1)と同様にしてナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体(Directional LT-NP)を形成した。
(3)DSPCとDSPE-PEG-NHS2000の混合比率を異にするか、或いはDSPE-PEG-NHS2000の代わりにDSPE-PEGを使用した以外は、他の条件を実施例1の4の(2)と同様にして、ナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体(Directional LT-NPs)を形成した。DSPCとDSPE-PEG-NHS2000の混合比率は、それぞれ9.75:0.25、9.5:0.5、9:1、8:2、7:3とし、DSPE-PEG-NHS2000の代わりにDSPE―PEGを用いて製造されたナノ粒子複合体は、下記の図面においてNHS Xと表記した。
<実施例2>ウイルスナノ粒子複合体の製造
1.ウイルスナノ粒子の準備
ウイルスナノ粒子として、AAV2-GFP(vector Biolabs、1×1013GC/ml、20μl)粒子(AAV)を用いた。
1.ウイルスナノ粒子の準備
ウイルスナノ粒子として、AAV2-GFP(vector Biolabs、1×1013GC/ml、20μl)粒子(AAV)を用いた。
2.リピドーム(脂質を用いたバブル)の準備
脂質DSPC(1,2-distearoyl-sn-glycero-3-phosphocholine)とDSPE-PEG2k(1,2-Distearoyl-sn-glycero-3-phosphoethanolamine-N-[succinyl(polyethylene glycol)-2000])を9.5:0.5のモル比で混合した後、1mg/vialとなるようにクロロホルムに溶かし、窒素ガスを用いてクロロホルムを蒸発させた。その後、乾燥したりん脂質の濃度が1mg/mlとなるようにPBSを入れ、55℃以上のD.Wに5秒間浸漬した後、バスソニケーターを用いて30秒間乾燥したリン脂質を水溶液上に分散させた。上記の過程を3回程度繰り返し行ってリン脂質を水溶液上に完全に分散させた後、C3F8ガスをバイアルにいっぱい充填し、バイアルミキサーを用いて45秒間振とうして脂質ベースのマイクロバブルを形成した。
脂質DSPC(1,2-distearoyl-sn-glycero-3-phosphocholine)とDSPE-PEG2k(1,2-Distearoyl-sn-glycero-3-phosphoethanolamine-N-[succinyl(polyethylene glycol)-2000])を9.5:0.5のモル比で混合した後、1mg/vialとなるようにクロロホルムに溶かし、窒素ガスを用いてクロロホルムを蒸発させた。その後、乾燥したりん脂質の濃度が1mg/mlとなるようにPBSを入れ、55℃以上のD.Wに5秒間浸漬した後、バスソニケーターを用いて30秒間乾燥したリン脂質を水溶液上に分散させた。上記の過程を3回程度繰り返し行ってリン脂質を水溶液上に完全に分散させた後、C3F8ガスをバイアルにいっぱい充填し、バイアルミキサーを用いて45秒間振とうして脂質ベースのマイクロバブルを形成した。
3.ナノ粒子複合体(Directional LT-AAV)の形成
実施例2の1で準備されたウイルスナノ粒子と、実施例2の2で準備されたマイクロバブルとを混合し、3時間以上常温で反応させた後、超音波(2.0W/cm2)を用いて30秒間機械的な力を加えた。その後、破砕されたマイクロバブルが脂質構造体を十分に形成することができるように1時間以上常温で反応させ、ナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体(Directional LT-AAV)を形成した。
実施例2の1で準備されたウイルスナノ粒子と、実施例2の2で準備されたマイクロバブルとを混合し、3時間以上常温で反応させた後、超音波(2.0W/cm2)を用いて30秒間機械的な力を加えた。その後、破砕されたマイクロバブルが脂質構造体を十分に形成することができるように1時間以上常温で反応させ、ナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体(Directional LT-AAV)を形成した。
<実施例3>アルブミンとRNAからなるナノ粒子複合体の製造
1.アルブミンとRNAからなるナノ粒子(siRNA NPs)の準備
アルブミン(ヒト血清アルブミン)を0.1mM HEPES with 0.01mM EDTAに40mg/mLの濃度で溶かした後、thiol-modify VEGF siRNA duplex(5’modified)を入れ、アルブミンとsiRNAとが混合された溶液が濁るまで100%エタノールを1mL/minの速度で滴定した後、遮光下にエタノールを一晩蒸発させ、13200rpm、10minの条件で遠心分離を行った後、粒子化されていない物質をピペットを用いて除去し、PBSに再分散して3000rpm、5minの条件で遠心分離を行った後、マイクロペレットを除いた上清(siRNAとアルブミンからなるナノ粒子(siRNA NPs))をピペットで得た。前記thiol-modify VEGF siRNA duplexのセンス鎖は、5’-AUGUGAAUGCAGACCAAAGAATT-3’(配列番号:1)であり、アンチセンス鎖は、5’-thiol-UUCUUUGGUCUGCAUUCACAUTT-3’(配列番号:2)である。
1.アルブミンとRNAからなるナノ粒子(siRNA NPs)の準備
アルブミン(ヒト血清アルブミン)を0.1mM HEPES with 0.01mM EDTAに40mg/mLの濃度で溶かした後、thiol-modify VEGF siRNA duplex(5’modified)を入れ、アルブミンとsiRNAとが混合された溶液が濁るまで100%エタノールを1mL/minの速度で滴定した後、遮光下にエタノールを一晩蒸発させ、13200rpm、10minの条件で遠心分離を行った後、粒子化されていない物質をピペットを用いて除去し、PBSに再分散して3000rpm、5minの条件で遠心分離を行った後、マイクロペレットを除いた上清(siRNAとアルブミンからなるナノ粒子(siRNA NPs))をピペットで得た。前記thiol-modify VEGF siRNA duplexのセンス鎖は、5’-AUGUGAAUGCAGACCAAAGAATT-3’(配列番号:1)であり、アンチセンス鎖は、5’-thiol-UUCUUUGGUCUGCAUUCACAUTT-3’(配列番号:2)である。
2.ナノ粒子複合体(Directional siRNA LT-NPs)の形成
実施例3の1で形成されたRNAとアルブミンからなるナノ粒子をバブル溶液(実施例1の3で形成されたバブルがPBSに1mg/mlの濃度で混合されて形成)に入れた後、RTで2時間以上反応させた後、超音波機器を用いて2W、1MHZ、デューティ比100%の条件で5分以上機械的な力を加えた。その後、破砕されたバブルが脂質構造体を十分に形成することができるように、1時間以上RTでインキュベートしてsiRNAとアルブミンからなるナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体(Directional siRNA LT-NPs)を形成した。
実施例3の1で形成されたRNAとアルブミンからなるナノ粒子をバブル溶液(実施例1の3で形成されたバブルがPBSに1mg/mlの濃度で混合されて形成)に入れた後、RTで2時間以上反応させた後、超音波機器を用いて2W、1MHZ、デューティ比100%の条件で5分以上機械的な力を加えた。その後、破砕されたバブルが脂質構造体を十分に形成することができるように、1時間以上RTでインキュベートしてsiRNAとアルブミンからなるナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体(Directional siRNA LT-NPs)を形成した。
<実施例4>陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子複合体の製造
1.陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子(siRNA NPs)の準備
マウスの血管内皮増殖因子(vascular endothelial growth facter A(VEGF-A))のセンス鎖は、5’-AUGUGAAUGCAGACCAAAGAATT-3’(配列番号:1)であり、アンチセンス鎖は、5’-UUCUUUGGUCUGCAUUCA CAUTT-3’(配列番号:2)である。前記センス鎖及びアンチセンス鎖をエンコードした長い線状の一本鎖DNAを製造した。ライゲーションされた円形のDNAテンプレートをT7 RNAポリメラーゼのように37℃で20時間反応バッファー(8mM Tris-HCl、0.4mM spermidine、1.2mM MgCl2、and 2mM dithiothreitol)で培養した。生成された溶液を複数回ピペッティングし、5分間超音波処理して粒子を分解した。溶液を4℃の条件下に13,200rpmで20分間遠心分離し、上清を除去した。その後、RNase-free waterを添加して粒子を洗浄した。溶液を1分間再び超音波処理し、遠心分離した。洗浄ステップをさらに3回繰り返してRCT試薬を除去することにより、RNA-microsponge(anti-VEGF siRNA hydrogel)を得た。前記siRNA hydrogelをバスソニケーター(bath sonicator)に1分以上入れて凝集なく解砕した後、ミニセントリフュージ(mini centrifuge)で、壁面に飛び散ったものがダウン(down)される程度に数秒回した後、前記siRNA hydrogel3μlとnuclease free water12μlとを混合して第1溶液を形成し、1mg/ml bPEI1μlとnuclease free water9μlとを混合して第2溶液を形成した後、第1溶液と第2溶液を10分間常温で反応させ、1mg/ml hyaluronic acid-amineを5μlゆっくりと入れた後、10分間常温で反応させ、しかる後に、ソニケーションで凝集粒子を解砕することにより、陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子(siRNA NPs)を得た。前記陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子の製造は、本発明者の先行特許(KR10-1880790)を参照した。
1.陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子(siRNA NPs)の準備
マウスの血管内皮増殖因子(vascular endothelial growth facter A(VEGF-A))のセンス鎖は、5’-AUGUGAAUGCAGACCAAAGAATT-3’(配列番号:1)であり、アンチセンス鎖は、5’-UUCUUUGGUCUGCAUUCA CAUTT-3’(配列番号:2)である。前記センス鎖及びアンチセンス鎖をエンコードした長い線状の一本鎖DNAを製造した。ライゲーションされた円形のDNAテンプレートをT7 RNAポリメラーゼのように37℃で20時間反応バッファー(8mM Tris-HCl、0.4mM spermidine、1.2mM MgCl2、and 2mM dithiothreitol)で培養した。生成された溶液を複数回ピペッティングし、5分間超音波処理して粒子を分解した。溶液を4℃の条件下に13,200rpmで20分間遠心分離し、上清を除去した。その後、RNase-free waterを添加して粒子を洗浄した。溶液を1分間再び超音波処理し、遠心分離した。洗浄ステップをさらに3回繰り返してRCT試薬を除去することにより、RNA-microsponge(anti-VEGF siRNA hydrogel)を得た。前記siRNA hydrogelをバスソニケーター(bath sonicator)に1分以上入れて凝集なく解砕した後、ミニセントリフュージ(mini centrifuge)で、壁面に飛び散ったものがダウン(down)される程度に数秒回した後、前記siRNA hydrogel3μlとnuclease free water12μlとを混合して第1溶液を形成し、1mg/ml bPEI1μlとnuclease free water9μlとを混合して第2溶液を形成した後、第1溶液と第2溶液を10分間常温で反応させ、1mg/ml hyaluronic acid-amineを5μlゆっくりと入れた後、10分間常温で反応させ、しかる後に、ソニケーションで凝集粒子を解砕することにより、陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子(siRNA NPs)を得た。前記陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子の製造は、本発明者の先行特許(KR10-1880790)を参照した。
2.ナノ粒子複合体(Lipid-siRNA NPs(siRNA LT-NPs))の形成
実施例4の1で形成された陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子をバブル溶液(実施例1の3で形成されたバブルがPBSに1mg/mlの濃度で混合されて形成)に入れ、RTで2時間以上反応させた後、超音波機器を用いて2W、1MHZ、デューティ比100%の条件で5分以上機械的な力(mechanical force)を加えた。その後、破砕されたバブルが脂質構造体を十分に形成することができるように、1時間以上RTでインキュベートして、陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体(Lipid-siRNA NPs(siRNA LT-NPs)を形成した。
実施例4の1で形成された陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子をバブル溶液(実施例1の3で形成されたバブルがPBSに1mg/mlの濃度で混合されて形成)に入れ、RTで2時間以上反応させた後、超音波機器を用いて2W、1MHZ、デューティ比100%の条件で5分以上機械的な力(mechanical force)を加えた。その後、破砕されたバブルが脂質構造体を十分に形成することができるように、1時間以上RTでインキュベートして、陽イオン性高分子とヒアルロン酸が順次コーティングされたRNAナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体(Lipid-siRNA NPs(siRNA LT-NPs)を形成した。
<実施例5>様々な種類の脂質と官能基を用いたナノ粒子複合体の製造
1.DSPCの代わりに、DPPC(1,2-dipalmitoyl-sn-glycero-3-phosphocholine)、DOPE(1,2-dioleoyl-sn-glycero-3-phosphoethanolamine)、cis-PC(1,2-dioleoyl-sn-glycero-3-phosphocholine)を使用し、第2反応基が結合していない脂質(DSPC、DPPC、DOPE、cis-PC)と第2反応基が結合した脂質(DSPE-PEG-NHS2000)との混合比率を9.5:0.5のモル比とした以外は、他の条件を実施例1の4の(2)と同様にして、ナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体を形成した。
1.DSPCの代わりに、DPPC(1,2-dipalmitoyl-sn-glycero-3-phosphocholine)、DOPE(1,2-dioleoyl-sn-glycero-3-phosphoethanolamine)、cis-PC(1,2-dioleoyl-sn-glycero-3-phosphocholine)を使用し、第2反応基が結合していない脂質(DSPC、DPPC、DOPE、cis-PC)と第2反応基が結合した脂質(DSPE-PEG-NHS2000)との混合比率を9.5:0.5のモル比とした以外は、他の条件を実施例1の4の(2)と同様にして、ナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体を形成した。
2.DSPE-PEG-NHS2000の代わりに、DSPE-PEG2000-SH、DSPE-PEG2000-Amineを使用し、第2反応基が結合していない脂質(DSPC)と第2反応基が結合した脂質(DSPE-PEG-NHS2000、DSPE-PEG2000-SH、DSPE-PEG2000-Amine)との混合比率を9.5:0.5のモル比とした以外は、他の条件を実施例1の4の(2)と同様にして、ナノ粒子の外表面の一部分に脂質構造体が結合したナノ粒子複合体を形成した。
<実施例6>ナノ粒子複合体の特性確認
1.実施例1の1で形成したナノ粒子(NPs)と実施例1の4の(2)で形成したナノ粒子複合体(Directional LT-NPs)をTEMで測定し、その結果を図2に示した。実施例1の4の(2)で形成したナノ粒子複合体及び脂質構造体をCryo-TEMで測定し、その結果をそれぞれ図3及び図4に示した。実施例1の4の(3)で形成したナノ粒子複合体をCryo-TEMで測定し、その結果をそれぞれ図5に示した(但し、DSPCとDSPE-PEG-NHS2000との混合比率がそれぞれ9.75:0.25、9.5:0.5、9:1、8:2であるナノ粒子複合体に対してのみ測定する)。実施例2の1で準備したウイルスナノ粒子をTEMで測定し、その結果を図6に示した。実施例2の3で形成したナノ粒子複合体(Directional LT-AAV)をCryo-TEMで測定し、その結果を図7に示した。
1.実施例1の1で形成したナノ粒子(NPs)と実施例1の4の(2)で形成したナノ粒子複合体(Directional LT-NPs)をTEMで測定し、その結果を図2に示した。実施例1の4の(2)で形成したナノ粒子複合体及び脂質構造体をCryo-TEMで測定し、その結果をそれぞれ図3及び図4に示した。実施例1の4の(3)で形成したナノ粒子複合体をCryo-TEMで測定し、その結果をそれぞれ図5に示した(但し、DSPCとDSPE-PEG-NHS2000との混合比率がそれぞれ9.75:0.25、9.5:0.5、9:1、8:2であるナノ粒子複合体に対してのみ測定する)。実施例2の1で準備したウイルスナノ粒子をTEMで測定し、その結果を図6に示した。実施例2の3で形成したナノ粒子複合体(Directional LT-AAV)をCryo-TEMで測定し、その結果を図7に示した。
2.図2を参照すると、アルブミンナノ粒子の場合、表面が滑らかであることを確認することができるのに対し、アルブミンナノ粒子複合体は、脂質構造体がナノ粒子の表面に付いており、表面が滑らかでないことが分かる。また、図3を参照すると、ナノ粒子の表面にチューブ状の脂質構造体が付いていることが分かる。図4を参照すると、前記脂質構造体は、チューブ形状を有することをさらに明確にすることができる。また、図3及び図4を参照すると、前記脂質構造体が50乃至300nmの長さ及び3乃至20nmの幅を有することが分かり、前記脂質構造体はナノ粒子の外表面に一つ以上が結合できることが分かる。また、図3及び図5を参照すると、DSPCとDSPE-PEG-NHSの比率に応じて脂質構造体の形成様相が変わることを確認することができ、DSPE-PEG-NHSの量が増加するほど脂質構造体の長さが短くなり、ナノ粒子にも脂質構造体が少なく形成されることを確認することができる。図6を参照すると、ウイルスナノ粒子の場合、表面が滑らかであることを確認することができるのに対し、図7を参照すると、ウイルスナノ粒子の表面にチューブ状の脂質構造体が付いていることが分かる。
<実施例7>ナノ粒子複合体の細胞取り込み効率の評価
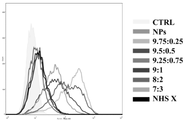
1.実施例1の1で形成したナノ粒子(NPs)と実施例1の4の(2)及び(3)で形成したナノ粒子複合体(Directional LT-NPs)に対する細胞取り込み効率を評価するために、フローサイトメトリー(Flow cytometry)を用いた分析結果を図8に示し、これを定量化した結果を表1に示し、共焦点顕微鏡を用いてイメージ化してその結果を図9に示した。フローサイトメトリーを用いた分析は、A549細胞(1×104)にAlexa 488蛍光色素(dye)が標識されたナノ粒子及びナノ粒子複合体を処理することにより行った。また、共焦点顕微鏡を用いた分析は、DAPIを用いて核が染色され且つファロイジン(Phalloidin)を用いて細胞骨格(cytoskeleton)が染色されたA549細胞(1×105)に、Cy5.5蛍光色素が標識されたナノ粒子及びナノ粒子複合体を処理することにより行った。
1.実施例1の1で形成したナノ粒子(NPs)と実施例1の4の(2)及び(3)で形成したナノ粒子複合体(Directional LT-NPs)に対する細胞取り込み効率を評価するために、フローサイトメトリー(Flow cytometry)を用いた分析結果を図8に示し、これを定量化した結果を表1に示し、共焦点顕微鏡を用いてイメージ化してその結果を図9に示した。フローサイトメトリーを用いた分析は、A549細胞(1×104)にAlexa 488蛍光色素(dye)が標識されたナノ粒子及びナノ粒子複合体を処理することにより行った。また、共焦点顕微鏡を用いた分析は、DAPIを用いて核が染色され且つファロイジン(Phalloidin)を用いて細胞骨格(cytoskeleton)が染色されたA549細胞(1×105)に、Cy5.5蛍光色素が標識されたナノ粒子及びナノ粒子複合体を処理することにより行った。
2.また、実施例1の1で形成したナノ粒子(NPs)と実施例1の4の(1)で形成したリポソーム-ナノ粒子複合体(Liposome-NPs)、ナノ粒子複合体(Directional LT-NPs)に対する細胞取り込み効率を評価するために、共焦点顕微鏡を用いてイメージ化し、その結果を図10に示す。共焦点顕微鏡を用いた分析は、DAPIを用いて核が染色されたA549細胞(1×105)に、Alexa 555蛍光色素が標識されたナノ粒子、リポソーム-ナノ粒子複合体、及びナノ粒子複合体を処理することにより行った。
3.また、実施例2の1で準備したナノ粒子(AAV)と実施例2の3で形成したナノ粒子複合体(Directional LT-AAV)に対する細胞取り込み効率を評価するために、共焦点顕微鏡を用いてイメージ化し、その結果を図11に示す。共焦点顕微鏡を用いた分析は、DAPIを用いて核が染色されたARPE19細胞(1×105)にウイルスナノ粒子及びナノ粒子複合体を処理することにより行った。
4.また、実施例4の1で準備したナノ粒子(siRNA NPs)と実施例4の2で形成したナノ粒子複合体(siRNA LT-NPs)に対する細胞取り込み効率を評価するために、共焦点顕微鏡を用いてイマージ化し、その結果を図12に示す。共焦点顕微鏡を用いた分析は、DAPIを用いて核が染色され且つFITCを用いて細胞骨格が染色されたMCF-7細胞(1×105)に、Cy3蛍光色素が標識されたナノ粒子及びナノ粒子複合体を処理することにより行った。
5.また、A549細胞(1×105)に、Alexa 647蛍光色素が標識された実施例5の1及び2で形成したナノ粒子複合体を処理した後、蛍光強度を測定し、その結果を図13及び図14に示す。図13においてDSPCと表記されたものは、DSPCが使用されて製造されたナノ粒子複合体の結果を意味し、図14においてチオールと表記されたものは、DSPE-PEG2000-SHが使用されて製造されたナノ粒子複合体の結果を意味する。
6.図8及び表1を参照すると、ナノ粒子複合体がナノ粒子に比べて著しく優れた細胞取り込み効能を示すことが分かり、DSPCとDSPE-PEG-NHS2000の比率が9:1以上であるとき、Alexa 488 positive細胞(染色されたナノ粒子を取り込んだ(uptake)細胞)の比率が対照群(control)に比べて78%以上であることを確認することができ、DSPE-PEG-NHS2000の量がこれより増加すると、細胞内の取り込み(uptake)効率が著しく低下することを確認することができるため、脂質構造体がナノ粒子の表面に十分な長さ及び形状に形成されない場合、ナノ粒子の細胞取り込み効率が低下することが分かる。また、図9を参照すると、蛍光画像を用いた実験においても、図8及び表1の結果を確認することができる。また、図10を参照すると、ナノ粒子複合体がナノ粒子やリポソーム-ナノ粒子複合体に比べて著しく優れた細胞取り込み効能を示すことを確認することができるので、ナノ粒子に脂質構造体が形成された場合、ナノ粒子にリポソームが単純に結合したものに比べて取り込み効率に優れることが分かり、脂質からなるバブルだけでなく、リポソーム又は他の脂質球状体の形でもナノ粒子複合体が形成できることが分かる。
7.また、AAV(Adeno associate Virus)は、網膜組織内に治療用遺伝子または薬物を送達するベクターとして用いられ、他のベクターに比べて良好な効率を示すが、RPE(retinal pigment epithelium)までは送達されないが、図11を参照すると、ナノ粒子複合体がナノ粒子に比べて著しく優れた取り込み効率を示すことが分かるので、脂質構造体がウイルスと細胞受容体との特異的反応を減少させることにより、ウイルストランスフェクション(transfection)率が増加し、RPE層への送達率が増加することができることが分かる。また、図12を参照すると、高分子とヒアルロン酸がコーティングされたRNAナノ粒子を用いるナノ粒子複合体もナノ粒子に比べて著しく優れた細胞取り込み効率を示すことが分かる。図13及び図14を参照すると、様々な種類の脂質と様々な官能基を用いてナノ粒子複合体を製造しても、ナノ粒子複合体がナノ粒子に比べて著しく優れた細胞取り込み効率を示すことが分かる。
<実施例8>ナノ粒子複合体が直接透過(direct penetration)で細胞内へ取り込まれることの確認
1.エンドサイトーシス阻害剤(Endocytosis Inhibitor)を処理した後のナノ粒子複合体の細胞取り込み効率の評価
(1)エンドサイトーシス阻害剤(Endocytosis Inhibitor)を処理した細胞に対して、実施例1の1で形成したナノ粒子(NPs)と実施例1の4の(2)で形成したナノ粒子複合体(Directional LT-NPs)の細胞取り込み効率を評価した。サイズ200nmのナノ粒子は、マクロピノサイトーシス(macropinocytosis)、クラスリン非依存性エンドサイトーシス(clathrin-independent endocytosis)、クラスリン依存性エンドサイトーシス(clathrin-dependent endocytosis)の合計3つのメカニズムに細胞内摂取が行われることが知られているので、これを阻害する阻害剤を選定して、まず、A549細胞(1×104)をそれぞれ又は同時に1時間処理した後、Alexa 488蛍光色素が標識されたナノ粒子及びナノ粒子複合体を3時間処理し、フローサイトメトリーを用いて測定した。測定結果に対してナノ粒子を基準に標準化(normalize)して図15に示した。マクロピノサイトーシス阻害剤(Macropinocytosis inhibitor)としては、EIPA(5-(N-Ethyl-N-isopropyl)amiloride)を選定(25μg/mlの濃度)してNa+/H+exchangeメカニズムを妨害し、クラスリン依存性エンドサイトーシス阻害剤(Clathrin-dependent endocytosis inhibitor)としては、CPZ(chlorpromazine)選定(20μg/mlの濃度)してclathrin-coated pit formationを妨害し、クラスリン非依存性エンドサイトーシス阻害剤(Clathrin-independent endocytosis inhibitor)としては、MβCD(methyl-β-cyclodextrin)を選定(3mg/mlの濃度)してcholesterol-dependent endocytic processを妨害した。また、上述のように、マクロピノサイトーシス阻害剤(Macropinocytosis inhibitor)、クラスリン依存性エンドサイトーシス阻害剤(Clathrin-dependent endocytosis inhibitor)、クラスリン非依存性エンドサイトーシス阻害剤(Clathrin-independent endocytosis inhibitor)をすべて処理したA549細胞(1×104)に、Alexa 488蛍光色素が標識された実施例1の1で形成したナノ粒子(NPs)と、実施例1の4の(2)及び(3)で形成したナノ粒子複合体(Directional LT-NPs)を導入した後、蛍光強度を測定することにより、その結果を図16に示した。
1.エンドサイトーシス阻害剤(Endocytosis Inhibitor)を処理した後のナノ粒子複合体の細胞取り込み効率の評価
(1)エンドサイトーシス阻害剤(Endocytosis Inhibitor)を処理した細胞に対して、実施例1の1で形成したナノ粒子(NPs)と実施例1の4の(2)で形成したナノ粒子複合体(Directional LT-NPs)の細胞取り込み効率を評価した。サイズ200nmのナノ粒子は、マクロピノサイトーシス(macropinocytosis)、クラスリン非依存性エンドサイトーシス(clathrin-independent endocytosis)、クラスリン依存性エンドサイトーシス(clathrin-dependent endocytosis)の合計3つのメカニズムに細胞内摂取が行われることが知られているので、これを阻害する阻害剤を選定して、まず、A549細胞(1×104)をそれぞれ又は同時に1時間処理した後、Alexa 488蛍光色素が標識されたナノ粒子及びナノ粒子複合体を3時間処理し、フローサイトメトリーを用いて測定した。測定結果に対してナノ粒子を基準に標準化(normalize)して図15に示した。マクロピノサイトーシス阻害剤(Macropinocytosis inhibitor)としては、EIPA(5-(N-Ethyl-N-isopropyl)amiloride)を選定(25μg/mlの濃度)してNa+/H+exchangeメカニズムを妨害し、クラスリン依存性エンドサイトーシス阻害剤(Clathrin-dependent endocytosis inhibitor)としては、CPZ(chlorpromazine)選定(20μg/mlの濃度)してclathrin-coated pit formationを妨害し、クラスリン非依存性エンドサイトーシス阻害剤(Clathrin-independent endocytosis inhibitor)としては、MβCD(methyl-β-cyclodextrin)を選定(3mg/mlの濃度)してcholesterol-dependent endocytic processを妨害した。また、上述のように、マクロピノサイトーシス阻害剤(Macropinocytosis inhibitor)、クラスリン依存性エンドサイトーシス阻害剤(Clathrin-dependent endocytosis inhibitor)、クラスリン非依存性エンドサイトーシス阻害剤(Clathrin-independent endocytosis inhibitor)をすべて処理したA549細胞(1×104)に、Alexa 488蛍光色素が標識された実施例1の1で形成したナノ粒子(NPs)と、実施例1の4の(2)及び(3)で形成したナノ粒子複合体(Directional LT-NPs)を導入した後、蛍光強度を測定することにより、その結果を図16に示した。
(2)図15を参照すると、ナノ粒子の場合(NPs)は、CPZ、EIPA阻害剤により細胞取り込み効能が大きく減少することを確認することができ、3種類の阻害剤(inhibitor)を全て処理してエンドサイトーシスメカニズムを全て妨害したときにナノ粒子の細胞摂取が殆ど行われないことが分かり、ナノ粒子複合体(Directional LT-NPs)の場合、ナノ粒子と比較して350%程度さらに優れた細胞取り込み効能を示すことを確認することができ、3種類の阻害剤でエンドサイトーシスメカニズムをすべて妨害したときにも、ナノ粒子よりも優れた細胞取り込み効能を示すことを観察することができる。これにより、ナノ粒子複合体は、エンドサイトーシスを引き起こすだけでなく、細胞膜を直接透過(direct penetration)を介して直接貫通することを確認することができる。また、図16を参照すると、DSPCとDSPE-PEG-NHS2000を8:2、7:3の比率で混合して製造されたナノ粒子複合体の場合は、3種類の阻害剤を全て処理すると、細胞取り込み(uptake)効能が著しく低下することが分かるのに対し、DSPCとDSPE-PEG-NHS2000を9:1以上の比率で混合して製造されたナノ粒子複合体の場合は、3種類の阻害剤をすべて処理してエンドサイトーシスメカニズムをすべて妨害したにも拘らず、細胞取り込み効能に優れることを確認することができるので、脂質構造体がナノ粒子に十分な長さと個数で形成された場合、ナノ粒子がエンドサイトーシスメカニズムではなく、トランスロケーション(translocation)などの直接透過(direct penetration)を介して細胞内に取り込まれることが分かる。
2.HAブロッキング後のナノ粒子複合体の細胞取り込み効率の評価
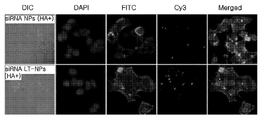
(1)実施例4の1で形成されたナノ粒子(siRNA NPs)は、最外殻がHAでコーティングされており、CD44レセプターを用いて細胞内に入るので、予めMCF-7細胞にHAを過量で処理してCD44レセプターを全てブロックした後、実施例4の1で形成したナノ粒子(siRNA NPs)と実施例4の2で形成したナノ粒子複合体(siRNA LT-NPs)を処理した後、共焦点顕微鏡を用いて分析し、その結果を図17に示す。共焦点顕微鏡を用いた分析は、DAPIを用いて核が染色され且つFITCを用いて細胞骨格が染色されたMCF-7細胞(1×105)に対してHAを過量で処理した後、Cy3蛍光色素が標識されたナノ粒子及びナノ粒子複合体を処理することにより行った。
(1)実施例4の1で形成されたナノ粒子(siRNA NPs)は、最外殻がHAでコーティングされており、CD44レセプターを用いて細胞内に入るので、予めMCF-7細胞にHAを過量で処理してCD44レセプターを全てブロックした後、実施例4の1で形成したナノ粒子(siRNA NPs)と実施例4の2で形成したナノ粒子複合体(siRNA LT-NPs)を処理した後、共焦点顕微鏡を用いて分析し、その結果を図17に示す。共焦点顕微鏡を用いた分析は、DAPIを用いて核が染色され且つFITCを用いて細胞骨格が染色されたMCF-7細胞(1×105)に対してHAを過量で処理した後、Cy3蛍光色素が標識されたナノ粒子及びナノ粒子複合体を処理することにより行った。
(2)図17を参照すると、細胞をHAでブロックしたので、ナノ粒子の場合は、低い効率で取り込まれたが、ナノ粒子複合体の場合は、CD44レセプターがブロックされたにも拘らず、細胞内の取り込み効率に優れることが分かるので、ナノ粒子複合体がエンドサイトーシスまたはレセプターバインディング(receptor binding)の他にも、直接透過(direct penetration)を介して細胞内に取り込まれることが分かる。
<実施例9>ナノ粒子複合体の抗がん剤送達体としての効能評価
1.アルブミン溶液にドキソルビシン(doxorubicin)が混合された溶液を添加して反応させた後、混合溶液が濁るまでエタノール滴定を行った以外は、実施例1の1及び実施例1の4の(2)と同様にして、ドキソルビシン含有ナノ粒子、ドキソルビシンナノ粒子複合体を形成し、抗がん抵抗性を有する乳がん細胞株MCF-7/ADRをウェルプレートにシードし、それぞれドキソルビシン(100mM、DOX)ドキソルビシン含有ナノ粒子(100mMのドキソルビシンを含む)及びドキソルビシン含有ナノ粒子複合体(100mMのドキソルビシンを含む)を含む培地をもって37℃で6時間培養した後、前記細胞株をノーマル培地(normal media)をもって48時間培養して細胞生存率(cell viability)を測定し、その結果を図18に示す。細胞生存率の測定には、MTTアッセイ及びトリパンブルー色素排除法(trypan blue dye exclusion method)を用いるが、細胞生存率は、0.4%トリパンブルー色素を有する細胞を培養し、ノイバウアー血球計(Neuauer hemocytometer)で計数することにより決定される。MTTアッセイで96ウェルプレートと1.5mg/mlのMTT試薬(3-(4,5-ジメチルチアゾール-2-イル)-2,5-ジフェニルテトラゾリウムブロミド)が使用され、15μlのMTT試薬をもって2時間培養した後、200μlのDMSOが各ウェルに追加され、Resulting culture platesは、プレートリーダー(Bio Tek Instruments、Inc、Winooski、VT、USA)によって570nmで測定した。
1.アルブミン溶液にドキソルビシン(doxorubicin)が混合された溶液を添加して反応させた後、混合溶液が濁るまでエタノール滴定を行った以外は、実施例1の1及び実施例1の4の(2)と同様にして、ドキソルビシン含有ナノ粒子、ドキソルビシンナノ粒子複合体を形成し、抗がん抵抗性を有する乳がん細胞株MCF-7/ADRをウェルプレートにシードし、それぞれドキソルビシン(100mM、DOX)ドキソルビシン含有ナノ粒子(100mMのドキソルビシンを含む)及びドキソルビシン含有ナノ粒子複合体(100mMのドキソルビシンを含む)を含む培地をもって37℃で6時間培養した後、前記細胞株をノーマル培地(normal media)をもって48時間培養して細胞生存率(cell viability)を測定し、その結果を図18に示す。細胞生存率の測定には、MTTアッセイ及びトリパンブルー色素排除法(trypan blue dye exclusion method)を用いるが、細胞生存率は、0.4%トリパンブルー色素を有する細胞を培養し、ノイバウアー血球計(Neuauer hemocytometer)で計数することにより決定される。MTTアッセイで96ウェルプレートと1.5mg/mlのMTT試薬(3-(4,5-ジメチルチアゾール-2-イル)-2,5-ジフェニルテトラゾリウムブロミド)が使用され、15μlのMTT試薬をもって2時間培養した後、200μlのDMSOが各ウェルに追加され、Resulting culture platesは、プレートリーダー(Bio Tek Instruments、Inc、Winooski、VT、USA)によって570nmで測定した。
2.図18を参照すると、同濃度のドキソルビシンを乳がん細胞に処理したとき、ナノ粒子複合体を用いる場合、一般がん細胞だけでなく、抗がん剤に対する抗がん抵抗性を有する細胞においても抗がん剤による細胞死滅効果を増加させることができることを分かる。
<実施例10>ナノ粒子複合体の誘電体薬物送達体としての評価
1.実施例3の1及び2で形成されたナノ粒子(siRNA NPs)及びナノ粒子複合体(Directional siRNA LT-NPs)に対する遺伝子サイレンシング(Gene silencing)を確認して、図19及び図20に示す。また、実施例4の1及び2で形成されたナノ粒子(siRNA NPs)及びナノ粒子複合体(siRNA LT-NPs)に対する遺伝子サイレンシング(Gene silencing)を確認して、図21及び図22に示す。遺伝子サイレンシングの確認は、MCF-7細胞(1×105)にナノ粒子、ナノ粒子複合体をそれぞれ3時間処理し、24時間培養した後にmRNAを抽出した。同様の方法で細胞に対するPCRを行った。PCR gel retardation assayにおいて、遺伝子バンド(gene bands)は、GelRed Nucleic Acid stainで染色され、Gel Doc imaging deviceによって視覚化される。図20及び図22の場合、遺伝子バンドの強度(intensity)をImageProを用いて相対的に定量化した値を示した。
1.実施例3の1及び2で形成されたナノ粒子(siRNA NPs)及びナノ粒子複合体(Directional siRNA LT-NPs)に対する遺伝子サイレンシング(Gene silencing)を確認して、図19及び図20に示す。また、実施例4の1及び2で形成されたナノ粒子(siRNA NPs)及びナノ粒子複合体(siRNA LT-NPs)に対する遺伝子サイレンシング(Gene silencing)を確認して、図21及び図22に示す。遺伝子サイレンシングの確認は、MCF-7細胞(1×105)にナノ粒子、ナノ粒子複合体をそれぞれ3時間処理し、24時間培養した後にmRNAを抽出した。同様の方法で細胞に対するPCRを行った。PCR gel retardation assayにおいて、遺伝子バンド(gene bands)は、GelRed Nucleic Acid stainで染色され、Gel Doc imaging deviceによって視覚化される。図20及び図22の場合、遺伝子バンドの強度(intensity)をImageProを用いて相対的に定量化した値を示した。
2.図19及び図20を参照すると、アルブミンとRNAからなるナノ粒子よりもナノ粒子複合体を使用したとき、一層優れた遺伝子サイレンシング(gene silencing)効率を示すことを確認することができるため、ナノ粒子複合体が誘電体薬物送達体として効果的に使用できることが分かる。また、図21及び図22を参照すると、高分子及びヒアルロン酸が順次コーティングされたRNAナノ粒子においても、上記の結果を得ることができることが分かる。
<実施例11>腫瘍細胞スフェロイド(Tumor cell spheroid)における効能評価
1.腫瘍細胞スフェロイド(Tumor cell spheroid)は、一般なadherentがん細胞とは異なり、3D cultureを用いて増殖し、このようなスフェロイド(spheroid)は、がん細胞が培地上でフロート(floating)して成長するため、集まって成長する。集まって成長した形態ががん組織のECM(Extracellular matrix)をミミック(mimic)するという研究結果があるため、脂質表面改質による組織透過(tissue penetration)の如何をin vitroで確認するためにこのモデルで実験を行った。
1.腫瘍細胞スフェロイド(Tumor cell spheroid)は、一般なadherentがん細胞とは異なり、3D cultureを用いて増殖し、このようなスフェロイド(spheroid)は、がん細胞が培地上でフロート(floating)して成長するため、集まって成長する。集まって成長した形態ががん組織のECM(Extracellular matrix)をミミック(mimic)するという研究結果があるため、脂質表面改質による組織透過(tissue penetration)の如何をin vitroで確認するためにこのモデルで実験を行った。
2.スフェロイド細胞形成
Poly(2-hydroxyethyl methacrylate)10gを1Lの100%純粋エタノール(100% pure ethanol)に添加して60℃で溶かした後、溶かしたポリ(2-ヒドロキシエチルメタクリレート)を100phi基準3.3mlだけプレート全体に均一に分散させた後、24時間乾燥させてコーティングを行い、上記で準備されたプレートにMCF7細胞をシードし、5日間維持してスフェロイドを形成した細胞を得た。
Poly(2-hydroxyethyl methacrylate)10gを1Lの100%純粋エタノール(100% pure ethanol)に添加して60℃で溶かした後、溶かしたポリ(2-ヒドロキシエチルメタクリレート)を100phi基準3.3mlだけプレート全体に均一に分散させた後、24時間乾燥させてコーティングを行い、上記で準備されたプレートにMCF7細胞をシードし、5日間維持してスフェロイドを形成した細胞を得た。
3.スフェロイド細胞へのナノ粒子複合体の処理
(1)実施例1の1で形成したナノ粒子(NPs)と実施例1の4の(2)で形成したナノ粒子複合体(Directional LT-NPs)に対するスフェロイド細胞取り込み効率を評価するために、共焦点顕微鏡を用いてイメージ化し、その結果を図23に示す。DAPIを用いて核が染色された実施例11の2で形成されたスフェロイド(Spheroid)状のMCF-7細胞(1×105)に、Alexa 555蛍光色素が標識されたナノ粒子及びナノ粒子複合体を処理した後、3時間が経過した時点で共焦点顕微鏡を用いて測定した。
(1)実施例1の1で形成したナノ粒子(NPs)と実施例1の4の(2)で形成したナノ粒子複合体(Directional LT-NPs)に対するスフェロイド細胞取り込み効率を評価するために、共焦点顕微鏡を用いてイメージ化し、その結果を図23に示す。DAPIを用いて核が染色された実施例11の2で形成されたスフェロイド(Spheroid)状のMCF-7細胞(1×105)に、Alexa 555蛍光色素が標識されたナノ粒子及びナノ粒子複合体を処理した後、3時間が経過した時点で共焦点顕微鏡を用いて測定した。
(2)また、実施例4の1で形成したナノ粒子(siRNA NPs)と実施例4の2で形成したナノ粒子複合体(Lipid siRNA NPs)に対するスフェロイド細胞取り込み効率を評価するために、共焦点顕微鏡を用いてイメージ化し、その結果を図24に示す。DAPIを用いて核が染色され且つAlexa 488を用いて細胞骨格が染色された実施例11の2で形成されたスフェロイド(Spheroid)状MCF-7細胞(1×105)に、Cy3蛍光色素が標識されたナノ粒子及びナノ粒子複合体を処理し、3時間、6時間が経過した時点で共焦点顕微鏡を用いて測定した。
(3)また、実施例4の1で形成したナノ粒子(siRNA NPs)と実施例4の2で形成したナノ粒子複合体(Lipid-siRNA NP)に対するスフェロイド(Spheroid)細胞遺伝子サイレンシング(Gene sellenging)を確認し、図25及び図26に示す。遺伝子サイレンシングの確認は、スフェロイド状MCF-7細胞(1×105)にナノ粒子、ナノ粒子複合体をそれぞれ3時間処理し、24時間培養した後にmRNAを抽出した。同様の方法で細胞に対するPCRを行った。PCR gel retardation assayにおいて、遺伝子バンドは、GelRed Nucleic Acid stainで染色され、Gel Doc imaging deviceによって視覚化される。図26は、遺伝子バンドの強度をImageProを用いて相対的に定量化した値を示した。
(4)図23乃至図26を参照すると、ナノ粒子複合体がナノ粒子に比べて細胞取り込み効率に優れることを確認することができ、これにより、単純in vitro環境だけでなく、in vivoをミミック(mimic)した環境でもナノ粒子複合体の取り込み効率に優れることを確認することができるので、ナノ粒子複合体は組織で優れた透過(penetration)効率を有することが分かる。
<実施例12>動物モデルにおけるナノ粒子複合体の細胞取り込み効率の評価
1.実施例4の1で形成したナノ粒子(siRNA NPs)と実施例4の2で形成したナノ粒子複合体(Lipid siRNA NPs)に対する動物モデルにおける細胞取り込み効率を評価するために、共焦点顕微鏡を用いてイメージ化し、その結果を図27に示す。前記動物モデル実験は、Cy5蛍光色素が標識されたナノ粒子とナノ粒子複合体をそれぞれ含む眼薬製剤5μlを準備し、前記眼薬製剤をブラウンノーウェイラット(Brown Norway Rat)の眼球に硝子体腔内注射で送達した。薬物を注入し、30日後に眼球を摘出し、4%PFAで固定した後、20%スクロースに30分間浸し、しかる後に、眼球をスクロースから取り出してO.C.Tコンパウンドに混ぜ、クリオモルド(Cryomold)にO.C.Tコンパウンドを注いで凍らせた後、眼球組織をクリオモルド(Cryomold)から分離し、cryosection機で切ってシワなく伸ばし、DAPI溶液を5分間反応させて組織の核を染色した後、共焦点顕微鏡を用いて測定した。
1.実施例4の1で形成したナノ粒子(siRNA NPs)と実施例4の2で形成したナノ粒子複合体(Lipid siRNA NPs)に対する動物モデルにおける細胞取り込み効率を評価するために、共焦点顕微鏡を用いてイメージ化し、その結果を図27に示す。前記動物モデル実験は、Cy5蛍光色素が標識されたナノ粒子とナノ粒子複合体をそれぞれ含む眼薬製剤5μlを準備し、前記眼薬製剤をブラウンノーウェイラット(Brown Norway Rat)の眼球に硝子体腔内注射で送達した。薬物を注入し、30日後に眼球を摘出し、4%PFAで固定した後、20%スクロースに30分間浸し、しかる後に、眼球をスクロースから取り出してO.C.Tコンパウンドに混ぜ、クリオモルド(Cryomold)にO.C.Tコンパウンドを注いで凍らせた後、眼球組織をクリオモルド(Cryomold)から分離し、cryosection機で切ってシワなく伸ばし、DAPI溶液を5分間反応させて組織の核を染色した後、共焦点顕微鏡を用いて測定した。
2.図27を参照すると、ナノ粒子複合体がナノ粒子よりも長い間眼球組織に滞留することが分かるため、ナノ粒子複合体は細胞取り込み効率に優れることが分かる。
以上、出願人は本発明の様々な実施例を説明したが、これらの実施例は本発明の技術的思想を実現する一実施例に過ぎず、本発明の技術的思想を実現する限り、いかなる変更例又は修正例も本発明の範囲に属するものと解釈されるべきである。
以上、出願人は本発明の様々な実施例を説明したが、これらの実施例は本発明の技術的思想を実現する一実施例に過ぎず、本発明の技術的思想を実現する限り、いかなる変更例又は修正例も本発明の範囲に属するものと解釈されるべきである。
1 ナノ粒子
2 脂質構造体
21 脂質頭部
22 脂質尾部
2 脂質構造体
21 脂質頭部
22 脂質尾部
Claims (12)
- 細胞内に取り込まれるナノ粒子と、前記ナノ粒子の外表面の一部分に結合してナノ粒子の細胞内取り込み効率を向上させる脂質ベースの脂質構造体を含み、
前記ナノ粒子は、第1反応基を含み、前記脂質構造体は、前記ナノ粒子の第1反応基と化学結合する第2反応基を含み、前記第1反応基と前記第2反応基とが化学結合することにより脂質構造体がナノ粒子に結合することを特徴とする、ナノ粒子複合体。 - 前記脂質構造体は、第2反応基が結合した脂質と、第2反応基が結合していない脂質との混合物からなるリピドームの再組み合わせによって形成され、
前記第2反応基が結合した脂質と前記第2反応基が結合していない脂質との混合比率を調節して、ナノ粒子に結合した脂質構造体の生成及び形態を制御することができることを特徴とする、請求項1に記載のナノ粒子複合体。 - 前記第2反応基が結合した脂質と前記第2反応基が結合していない脂質は1:2.33~99のモル比で使用されることを特徴とする、請求項2に記載のナノ粒子複合体。
- 前記脂質構造体は、
親水性を呈する脂質頭部が外側面に位置し、内部に疎水性を呈する脂質尾部が位置することにより、全体的に長尺なチューブ形状を有することを特徴とする、請求項1に記載のナノ粒子複合体。 - 前記ナノ粒子は50~500nmの直径を有し、前記脂質構造体は50~300nmの長さ及び3~20nmの幅を有することを特徴とする、請求項1に記載のナノ粒子複合体。
- 前記ナノ粒子複合体は、
エンドサイトーシスを引き起こすだけでなく、細胞膜を直接貫通して細胞内に取り込まれることができることを特徴とする、請求項1に記載のナノ粒子複合体。 - 前記脂質構造体は、
前記ナノ粒子のスフェロイド細胞内取り込み効率を向上させることができることを特徴とする、請求項1に記載のナノ粒子複合体。 - 前記ナノ粒子は、抗がん剤を含み、抗がん抵抗性を有する腫瘍細胞の死滅効率を向上させることができることを特徴とする、請求項1に記載のナノ粒子複合体。
- 前記ナノ粒子は、誘電体を含むか或いは遺伝体からなり、前記ナノ粒子複合体は、遺伝子治療に用いられることを特徴とする、請求項1に記載のナノ粒子複合体。
- 第1反応基が存在するナノ粒子を形成するナノ粒子形成ステップと、
前記第1反応基と化学的に結合する第2反応基が存在する脂質ベースのマイクロサイズのリピドームを形成するリピドーム形成ステップと、
前記ナノ粒子と前記リピドームとを混合して第1反応基と第2反応基とが互いに結合するようにして、リピドームの外面にナノ粒子が結合したリピドーム-ナノ粒子複合体を形成する脂質複合体形成ステップと、
前記脂質複合体形成ステップで形成されたリピドーム-ナノ粒子複合体に機械的な力を加えてリピドームを破砕して、ナノ粒子の外表面の一部分に結合した脂質構造体を形成することにより、ナノ粒子複合体を製造する破砕形成ステップと、を含み、
前記リピドーム形成ステップは、第2反応基が結合した脂質と第2反応基が結合していない脂質との混合物を用いてリピドームを形成し、
前記ナノ粒子は細胞内に取り込まれ、前記脂質構造体はナノ粒子の細胞内取り込み効率を向上させることを特徴とする、ナノ粒子複合体の製造方法。 - 前記第2反応基が結合した脂質と前記第2反応基が結合していない脂質との混合比率を調節して、ナノ粒子に結合した脂質構造体の生成及び形態を制御することができることを特徴とする、請求項10に記載のナノ粒子複合体の製造方法。
- 前記破砕形成ステップでは、リピドーム-ナノ粒子複合体に機械的な力を加えて一定時間維持することにより、リピドームが破砕され、リピドームを成すリン脂質は再組み合わせが起こり、ナノ粒子に結合したチューブ状の脂質構造体が形成されることを特徴とする、請求項10に記載のナノ粒子複合体の製造方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020190054778A KR102198900B1 (ko) | 2019-05-10 | 2019-05-10 | 질병 치료용 나노입자 복합체 및 이의 제조방법 |
| KR10-2019-0054778 | 2019-05-10 | ||
| PCT/KR2020/006109 WO2020231105A1 (ko) | 2019-05-10 | 2020-05-08 | 질병 치료용 나노입자 복합체 및 이의 제조방법 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2022533067A true JP2022533067A (ja) | 2022-07-21 |
Family
ID=73290235
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021567055A Pending JP2022533067A (ja) | 2019-05-10 | 2020-05-08 | 疾病治療用ナノ粒子複合体及びその製造方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20220347116A1 (ja) |
| EP (1) | EP3957305A4 (ja) |
| JP (1) | JP2022533067A (ja) |
| KR (1) | KR102198900B1 (ja) |
| CN (1) | CN114173768A (ja) |
| WO (1) | WO2020231105A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4014967A1 (en) | 2016-04-29 | 2022-06-22 | Icahn School of Medicine at Mount Sinai | Targeting the innate immunesystem to induce long-term tolerance and to resolve macrophage accumulation in atherosclerosis |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20150343079A1 (en) * | 2012-10-25 | 2015-12-03 | Sogang University Research Foundation | Ultrasound contrast agent with nanoparticles including drug and method for preparing the same |
| WO2017041033A1 (en) * | 2015-09-04 | 2017-03-09 | Brinker C Jeffrey | Mesoporous silica nanoparticles and supported lipid bi-layer nanoparticles for biomedical applications |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20080094473A (ko) * | 2007-04-20 | 2008-10-23 | 한국화학연구원 | 음이온성 지질나노입자 및 이의 제조방법 |
| BRPI0820302A2 (pt) * | 2007-11-09 | 2015-05-19 | Univ Northeastern | Nanopartículas semelhantes a micelas de automontagem para liberação sistêmica de gene |
| KR101085203B1 (ko) * | 2011-04-01 | 2011-11-21 | 서울대학교산학협력단 | 의약 전달용 인지질 나노입자 |
| CN102525926B (zh) * | 2011-12-27 | 2013-04-24 | 湖南师范大学 | 丙二醇胺衍生物阳离子脂质体纳米颗粒及其制备方法 |
| KR101487088B1 (ko) * | 2012-10-25 | 2015-01-27 | 서강대학교산학협력단 | 약물을 함유한 나노입자가 결합된 초음파 조영제 및 이의 제조방법 |
| KR101595795B1 (ko) * | 2014-03-19 | 2016-02-22 | (주)아이엠지티 | 약물을 함유한 나노입자가 결합된 이중-목적 pat/초음파 조영제 및 이의 제조방법 |
| US10369104B2 (en) * | 2014-04-01 | 2019-08-06 | Children's Hospital Los Angeles | Targeted polymerized nanoparticles for cancer treatment |
| KR101880790B1 (ko) | 2015-04-07 | 2018-08-16 | 서강대학교산학협력단 | 망막질병 치료를 위한 효과 지속성(Long-term) siRNA 기반 나노메디슨 및 이의 제조방법 |
| KR101837537B1 (ko) | 2015-10-02 | 2018-03-14 | 한양대학교 에리카산학협력단 | 다중 약물의 효율적 세포내 전달을 위한 다중 블럭 폴리펩타이드를 포함하는 약물전달체 및 자가조립 나노구조체 |
| US20190046446A1 (en) * | 2016-09-30 | 2019-02-14 | Eriochem Usa, Llc | Apo-e modified lipid nanoparticles for drug delivery to targeted tissues and therapeutic methods |
| EP3808344A4 (en) * | 2018-06-01 | 2022-03-30 | Sogang University Research Foundation | NANOPARTICLE COMPOSITE WITH IMPROVED ENDOCYTICAL EFFICIENCY THROUGH SURFACE MODIFICATION USING A LIPID AND MANUFACTURING PROCESSES THEREOF |
-
2019
- 2019-05-10 KR KR1020190054778A patent/KR102198900B1/ko active Active
-
2020
- 2020-05-08 CN CN202080035005.1A patent/CN114173768A/zh active Pending
- 2020-05-08 EP EP20805269.6A patent/EP3957305A4/en not_active Withdrawn
- 2020-05-08 JP JP2021567055A patent/JP2022533067A/ja active Pending
- 2020-05-08 WO PCT/KR2020/006109 patent/WO2020231105A1/ko not_active Ceased
- 2020-05-08 US US17/610,425 patent/US20220347116A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20150343079A1 (en) * | 2012-10-25 | 2015-12-03 | Sogang University Research Foundation | Ultrasound contrast agent with nanoparticles including drug and method for preparing the same |
| WO2017041033A1 (en) * | 2015-09-04 | 2017-03-09 | Brinker C Jeffrey | Mesoporous silica nanoparticles and supported lipid bi-layer nanoparticles for biomedical applications |
Non-Patent Citations (2)
| Title |
|---|
| CANCERS, vol. Vol.11,581, JPN6023003812, 24 April 2019 (2019-04-24), pages 1 - 18, ISSN: 0004984162 * |
| NANOSCALE, vol. 9, JPN6023003813, 2017, pages 15461 - 15469, ISSN: 0004984161 * |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20200130584A (ko) | 2020-11-19 |
| EP3957305A1 (en) | 2022-02-23 |
| EP3957305A4 (en) | 2023-02-08 |
| WO2020231105A1 (ko) | 2020-11-19 |
| US20220347116A1 (en) | 2022-11-03 |
| CN114173768A (zh) | 2022-03-11 |
| KR102198900B1 (ko) | 2021-01-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Boca et al. | Nanoscale delivery systems for microRNAs in cancer therapy | |
| Lohiya et al. | Carboxylated chitosan-mediated improved efficacy of mesoporous silica nanoparticle-based targeted drug delivery system for breast cancer therapy | |
| Mokhtarzadeh et al. | Applications of spherical nucleic acid nanoparticles as delivery systems | |
| Chen et al. | Smart multifunctional nanostructure for targeted cancer chemotherapy and magnetic resonance imaging | |
| Daniels et al. | Sterically stabilized siRNA: gold nanocomplexes enhance c-MYC silencing in a breast cancer cell model | |
| JP2020079287A (ja) | 核酸の送達のためのリポソーム製剤 | |
| Agarwal et al. | Intracellular delivery of polymeric nanocarriers: a matter of size, shape, charge, elasticity and surface composition | |
| Bedi et al. | Targeted delivery of siRNA into breast cancer cells via phage fusion proteins | |
| Barnaby et al. | Therapeutic applications of spherical nucleic acids | |
| Yang et al. | Inhibition of hepatic fibrosis with artificial microRNA using ultrasound and cationic liposome-bearing microbubbles | |
| Shi et al. | MnO2-gated nanoplatforms with targeted controlled drug release and contrast-enhanced MRI properties: from 2D cell culture to 3D biomimetic hydrogels | |
| KR102180631B1 (ko) | 지질을 이용한 표면 개질을 통해 세포 내 섭취 효율을 향상시킨 나노입자 복합체 및 이의 제조방법 | |
| Bellavita et al. | An overview of supramolecular platforms boosting drug delivery | |
| Ma et al. | Effect of elasticity of silica capsules on cellular uptake | |
| Awad et al. | Effect of phospholipid head group on ultrasound-triggered drug release and cellular uptake of immunoliposomes | |
| Li et al. | Antibody h-R3-dendrimer mediated siRNA has excellent endosomal escape and tumor targeted delivery ability, and represents efficient siPLK1 silencing and inhibition of cell proliferation, migration and invasion | |
| Qian et al. | Assembling defined DNA nanostructures with anticancer drugs: a metformin/DNA complex nanoplatform with a synergistic antitumor effect for KRAS-mutated lung cancer therapy | |
| Sun et al. | Multi-stimuli-responsive janus hollow polydopamine nanotubes | |
| Li et al. | Rod-shaped polypeptide nanoparticles for siRNA delivery | |
| JP2022533067A (ja) | 疾病治療用ナノ粒子複合体及びその製造方法 | |
| KR102075823B1 (ko) | 항암치료 및 유전자 치료용 나노입자를 포함하는 간동맥 화학색전술용 조성물 | |
| Lizoňová et al. | Multilobed magnetic liposomes enable remotely controlled collection, transport, and delivery of membrane-soluble cargos to vesicles and cells | |
| KR102565700B1 (ko) | 지질을 이용한 표면 개질을 통해 조직 투과성을 향상시킨 안약 제제용 나노입자 복합체 | |
| US10894020B2 (en) | Hybrid nanoparticles containing boron-doped graphene quantum dots and applications thereof | |
| Chiang et al. | From Nanoparticles to Cancer Nanomedicine: Old Problems with New Solutions. Nanomaterials 2021, 11, 1727 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20211224 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230207 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20230912 |