JP2010063433A - エタノールの製造方法 - Google Patents
エタノールの製造方法 Download PDFInfo
- Publication number
- JP2010063433A JP2010063433A JP2008235164A JP2008235164A JP2010063433A JP 2010063433 A JP2010063433 A JP 2010063433A JP 2008235164 A JP2008235164 A JP 2008235164A JP 2008235164 A JP2008235164 A JP 2008235164A JP 2010063433 A JP2010063433 A JP 2010063433A
- Authority
- JP
- Japan
- Prior art keywords
- yeast
- liquid mixture
- ethanol
- light
- plant
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 title abstract description 183
- 238000004519 manufacturing process Methods 0.000 title abstract description 61
- 241000196324 Embryophyta Species 0.000 abstract description 140
- 239000000203 mixture Substances 0.000 abstract description 110
- 240000004808 Saccharomyces cerevisiae Species 0.000 abstract description 107
- 239000007788 liquid Substances 0.000 abstract description 107
- 235000007164 Oryza sativa Nutrition 0.000 abstract description 81
- 235000009566 rice Nutrition 0.000 abstract description 81
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 abstract description 74
- 210000003763 chloroplast Anatomy 0.000 abstract description 70
- 229910002092 carbon dioxide Inorganic materials 0.000 abstract description 37
- 239000001569 carbon dioxide Substances 0.000 abstract description 37
- 238000006243 chemical reaction Methods 0.000 abstract description 33
- 238000000855 fermentation Methods 0.000 abstract description 23
- 230000004151 fermentation Effects 0.000 abstract description 23
- 229920002472 Starch Polymers 0.000 abstract description 21
- 238000000034 method Methods 0.000 abstract description 21
- 235000019698 starch Nutrition 0.000 abstract description 21
- 239000008107 starch Substances 0.000 abstract description 21
- 239000007787 solid Substances 0.000 abstract description 19
- 240000008042 Zea mays Species 0.000 abstract description 18
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 abstract description 18
- 235000002017 Zea mays subsp mays Nutrition 0.000 abstract description 18
- 235000005822 corn Nutrition 0.000 abstract description 18
- 241000195493 Cryptophyta Species 0.000 abstract description 16
- 239000001913 cellulose Substances 0.000 abstract description 7
- 229920002678 cellulose Polymers 0.000 abstract description 7
- 229920002488 Hemicellulose Polymers 0.000 abstract description 6
- 239000003795 chemical substances by application Substances 0.000 abstract description 5
- 241000894006 Bacteria Species 0.000 abstract description 4
- GXCLVBGFBYZDAG-UHFFFAOYSA-N N-[2-(1H-indol-3-yl)ethyl]-N-methylprop-2-en-1-amine Chemical compound CN(CCC1=CNC2=C1C=CC=C2)CC=C GXCLVBGFBYZDAG-UHFFFAOYSA-N 0.000 abstract description 4
- 230000003301 hydrolyzing effect Effects 0.000 abstract description 3
- 150000001720 carbohydrates Chemical class 0.000 abstract 2
- 241000195940 Bryophyta Species 0.000 abstract 1
- 240000005717 Dioscorea alata Species 0.000 abstract 1
- 235000002723 Dioscorea alata Nutrition 0.000 abstract 1
- 235000007056 Dioscorea composita Nutrition 0.000 abstract 1
- 235000009723 Dioscorea convolvulacea Nutrition 0.000 abstract 1
- 235000005362 Dioscorea floribunda Nutrition 0.000 abstract 1
- 235000004868 Dioscorea macrostachya Nutrition 0.000 abstract 1
- 235000005361 Dioscorea nummularia Nutrition 0.000 abstract 1
- 235000005360 Dioscorea spiculiflora Nutrition 0.000 abstract 1
- 240000005979 Hordeum vulgare Species 0.000 abstract 1
- 235000007340 Hordeum vulgare Nutrition 0.000 abstract 1
- 235000006350 Ipomoea batatas var. batatas Nutrition 0.000 abstract 1
- 240000007594 Oryza sativa Species 0.000 abstract 1
- 235000004879 dioscorea Nutrition 0.000 abstract 1
- 230000000694 effects Effects 0.000 abstract 1
- 230000002255 enzymatic effect Effects 0.000 abstract 1
- 235000014680 Saccharomyces cerevisiae Nutrition 0.000 description 104
- 241000209094 Oryza Species 0.000 description 80
- 230000000052 comparative effect Effects 0.000 description 74
- 230000003595 spectral effect Effects 0.000 description 48
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 34
- 238000000295 emission spectrum Methods 0.000 description 34
- 229910052760 oxygen Inorganic materials 0.000 description 34
- 239000001301 oxygen Substances 0.000 description 34
- 239000000047 product Substances 0.000 description 28
- 239000011521 glass Substances 0.000 description 21
- 238000001228 spectrum Methods 0.000 description 20
- 241000192700 Cyanobacteria Species 0.000 description 19
- 239000007789 gas Substances 0.000 description 19
- 238000005259 measurement Methods 0.000 description 16
- 241000209140 Triticum Species 0.000 description 12
- 235000021307 Triticum Nutrition 0.000 description 12
- 230000029553 photosynthesis Effects 0.000 description 12
- 238000010672 photosynthesis Methods 0.000 description 12
- 235000013312 flour Nutrition 0.000 description 8
- 230000001678 irradiating effect Effects 0.000 description 7
- 238000011084 recovery Methods 0.000 description 7
- 238000004821 distillation Methods 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 239000010902 straw Substances 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 239000004382 Amylase Substances 0.000 description 5
- 102000013142 Amylases Human genes 0.000 description 5
- 108010065511 Amylases Proteins 0.000 description 5
- 235000019418 amylase Nutrition 0.000 description 5
- 108090000790 Enzymes Proteins 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 4
- 241000736285 Sphagnum Species 0.000 description 4
- 210000000170 cell membrane Anatomy 0.000 description 4
- 229940088598 enzyme Drugs 0.000 description 4
- 235000013305 food Nutrition 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 239000002994 raw material Substances 0.000 description 4
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- 241000218916 Cycas Species 0.000 description 3
- 241000195620 Euglena Species 0.000 description 3
- 235000011201 Ginkgo Nutrition 0.000 description 3
- 244000194101 Ginkgo biloba Species 0.000 description 3
- 235000008100 Ginkgo biloba Nutrition 0.000 description 3
- 241000227166 Harrimanella hypnoides Species 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 241000592344 Spermatophyta Species 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 241001474374 Blennius Species 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 238000010533 azeotropic distillation Methods 0.000 description 2
- 238000010364 biochemical engineering Methods 0.000 description 2
- 239000006227 byproduct Substances 0.000 description 2
- 230000007062 hydrolysis Effects 0.000 description 2
- 238000006460 hydrolysis reaction Methods 0.000 description 2
- 238000010298 pulverizing process Methods 0.000 description 2
- 235000001674 Agaricus brunnescens Nutrition 0.000 description 1
- 241000195967 Anthoceros Species 0.000 description 1
- 240000006439 Aspergillus oryzae Species 0.000 description 1
- 235000002247 Aspergillus oryzae Nutrition 0.000 description 1
- 241000579185 Bucerotidae Species 0.000 description 1
- 108010073178 Glucan 1,4-alpha-Glucosidase Proteins 0.000 description 1
- 102100022624 Glucoamylase Human genes 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 235000000177 Indigofera tinctoria Nutrition 0.000 description 1
- 241000282320 Panthera leo Species 0.000 description 1
- 241000237509 Patinopecten sp. Species 0.000 description 1
- 241000985694 Polypodiopsida Species 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 241001261506 Undaria pinnatifida Species 0.000 description 1
- 102000004139 alpha-Amylases Human genes 0.000 description 1
- 108090000637 alpha-Amylases Proteins 0.000 description 1
- 229940024171 alpha-amylase Drugs 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- 235000013339 cereals Nutrition 0.000 description 1
- 239000012295 chemical reaction liquid Substances 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229940097275 indigo Drugs 0.000 description 1
- COHYTHOBJLSHDF-UHFFFAOYSA-N indigo powder Natural products N1C2=CC=CC=C2C(=O)C1=C1C(=O)C2=CC=CC=C2N1 COHYTHOBJLSHDF-UHFFFAOYSA-N 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 230000000243 photosynthetic effect Effects 0.000 description 1
- 235000020637 scallop Nutrition 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 238000001577 simple distillation Methods 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 238000005979 thermal decomposition reaction Methods 0.000 description 1
- 235000015041 whisky Nutrition 0.000 description 1
- 239000002023 wood Substances 0.000 description 1
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E50/00—Technologies for the production of fuel of non-fossil origin
- Y02E50/10—Biofuels, e.g. bio-diesel
Landscapes
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Abstract
【解決手段】糖化した固液混合物、酵母及び植物葉緑体を含む密閉された系内において発光ダイオードの光を照射することによりエタノールを生成する生成工程と該系中から生成されたエタノールを系外に回収する回収工程とを含むエタノールの製造方法であって、
前記生成工程において、
a)糖化した固液混合物を酵母により発酵させてエタノールを生成する反応、
b)a)の発酵の際に発生する二酸化炭素を、植物葉緑体と発光ダイオードの光照射により光合成させて糖とする反応、及び
c)b)で得られた糖を酵母により発酵させてエタノールを生成する反応
が並行して進行することを特徴とし、前記糖化した固液混合物は、セルロース又はヘミセルロースを熱分解又は加水分解して糖化するか或いはデンプンを含む米、麦、芋又はトウモロコシを麹、麦芽又は酵素剤を用いて糖化することにより調製されるものであり、前記植物葉緑体は、種子植物、シダ植物、藻類、コケ植物、細菌類又はこれらの混合物の植物葉緑体であり且つ前記発光ダイオードの光は、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が全波長領域に亘る発光量の70%以上となる光であるエタノールの製造方法。
【選択図】なし
Description
上記製造方法において、“微細藻培養手段1”及び“保持手段3”は、完全に独立した別工程であり、また、該2工程間には“微細藻濃縮手段2”という別工程を必要とするため、操作が煩雑であり、また、エタノールの製造方法として必ずしも効率が高いものとはいえなかった。
特に、エタノールを生成させる“保持手段3”は、暗黒かつ嫌気性雰囲気に保持する必要があるため、光照射を必要とする“微細藻培養手段1”と同一容器内で並行して行うことはできないものであった。
上記方法は、エタノール発酵の際に発生する二酸化炭素の再利用について記載するものの、該二酸化炭素を光合成によりエタノール発酵の原料である糖に変換すること、及び、該糖を上記のエタノール発酵とを同一容器内で並行して行うことに付いては何らの示唆も記載もなされていなかった。
しかし、上記方法は何れも、光合成により二酸化炭素から糖を生成する具体的な方法を記載するものではなかった。
a)糖化した固液混合物を酵母により発酵させてエタノールを生成する反応、
b)a)の発酵の際に発生する二酸化炭素を、植物葉緑体と発光ダイオードの光照射により光合成させて糖とする反応、及び
c)b)で得られた糖を酵母により発酵させてエタノールを生成する反応
が並行して進行することを見出し、またその際、特定の波長領域の光を照射することにより効率良くエタノールが製造されることを見出し、本発明を完成させた。
(1)糖化した固液混合物、酵母及び植物葉緑体を含む密閉された系内において発光ダイオードの光を照射することによりエタノールを生成する生成工程と該系中から生成されたエタノールを系外に回収する回収工程とを含むエタノールの製造方法であって、
前記生成工程において、
a)糖化した固液混合物を酵母により発酵させてエタノールを生成する反応、
b)a)の発酵の際に発生する二酸化炭素を、植物葉緑体と発光ダイオードの光照射により光合成させて糖とする反応、及び
c)b)で得られた糖を酵母により発酵させてエタノールを生成する反応
が並行して進行することを特徴とし、前記糖化した固液混合物は、セルロース又はヘミセルロースを熱分解又は加水分解して糖化するか或いはデンプンを含む米、麦、芋又はトウモロコシを麹、麦芽又は酵素剤を用いて糖化することにより調製されるものであり、前記植物葉緑体は、種子植物、シダ植物、藻類、コケ植物、細菌類又はこれらの混合物の植物葉緑体であり且つ前記発光ダイオードの光は、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が全波長領域に亘る発光量の70%以上となる光であるエタノールの製造方法、
(2)前記密閉された系内に、更なる二酸化炭素を添加する請求項1記載のエタノールの製造方法、
(3)前記回収工程が、蒸留によるものである請求項1又は2記載のエタノールの製造方法、
に関する。
加えて、光合成反応により産生された糖を原料としてエタノールが製造されるため、通常のエタノール発酵と比べると、エタノールの回収割合が高いものであり、更に、1つの容器内で3つの反応を同時に行えるため、操作が簡便で且つ効率的である、非常に優れたエタノールの製造方法である。
また、本発明の好ましい態様においては、上記反応系内に、更なる二酸化炭素が添加されるが、それにより、更に効率よくエタノールを製造することができる。
セルロース又はヘミセルロースとしては、木材等の植物体から得られるセルロース又はヘミセルロースが挙げられる。
熱分解によるセルロースの糖化は、既知の方法、例えば、特許第1400009号公報に記載の方法により行うことができる。
また、加水分解によるセルロース又はヘミセルロースの糖化は、既知の方法、例えば、特公昭61−044479号公報に記載の希硫酸を用いて加水分解する方法により行うことができる。
また、糖化した固液混合物は、デンプンを含む米、麦、芋又はトウモロコシを用い、必要に応じて外皮を取り除く工程、粉末化又は粉砕工程等を施し、これに麹、麦芽又は酵素剤を添加することにより調製することができる。
上記酵素剤としては、アミラーゼが挙げられる。
上記で調製された糖化した固液混合物は、必要に応じて滅菌工程等を行うことができる。
種子植物としては、特に限定されないが、例えば、イチョウ、稲等が好ましい。
シダ植物としては、特に限定されないが、例えば、ソテツ等が好ましい。
藻類としては、特に限定されないが、例えば、カワモズク、灰色藻、クリプト藻、ワカメ、ユーグレナ藻、クロララクニオン藻、藍藻、ユレモ等が好ましい。
コケ植物としては、特に限定されないが、例えば、ミズゴケ、クロゴケ、スギゴケ、ウロコゴケ、ゼニゴケ、ツノゴケ等が好ましい。
細菌類としては、特に限定されないが、例えば、シアノバクテリア(アオコから抽出)等が好ましい。
好ましい植物葉緑体としては、細菌類の植物葉緑体が挙げられ、また、シアノバクテリアの植物葉緑体が挙げられる。
く発酵されるように、通常、植物の細胞膜を破壊しておくことが好ましい。植物の細胞膜の破壊は、例えば、植物を粉砕することにより行われ得る。
しかし、細胞膜を破壊しなくても生成した糖が効率よく発酵される場合には、細胞膜を破壊しておく必要は無い。
ガラス容器の場合、光照射は、ガラス容器の外側から及び/又は内側から行うことができ、金属容器の場合は、容器の内側から光照射を行うことができる。
また、上記容器は、発生する気体に対応できるよう、発生した気体を一時的に収容できる伸縮可能な部位を備えていることが好ましい。
また、上記系は、攪拌可能であることが好ましい。
また、上記ガラス容器は、例えば、裏と表の両面から発光ダイオードの光照射が可能な、2枚のガラス板から構成され、該ガラス板の間に糖化した固液混合物、酵母及び植物葉緑体を含む溶液をエタノール生成反応が可能な速度で流すことによる連続反応が可能な容器でもあり得る。
a)糖化した固液混合物を酵母により発酵させてエタノールを生成する反応、
b)a)の発酵の際に発生する二酸化炭素を、植物葉緑体と発光ダイオードの光照射により光合成させて糖とする反応、及び
c)b)で得られた糖を酵母により発酵させてエタノールを生成する反応
の3つの反応が、前記密閉された系中で、並行して進行する。
生成した二酸化炭素は、植物葉緑体と発光ダイオードの光による光合成b)により、糖に変換され、またこの際、酸素が発生する。
上記糖は、エタノール発酵に使用可能な糖であれば、特に限定されず、例えば、ショ糖、ブドウ糖等が挙げられる。
上記b)で生成した糖は、酵母により発酵され(反応c))、エタノールと二酸化炭素が生成するが、生成した二酸化炭素は、再度b)の光合成、c)のアルコール発酵を経由してエタノールと酸素に変換され、このサイクルを繰り返すことにより最終的に二酸化炭素はその殆ど全てが、エタノールと酸素に変換されることとなる。
従って、系中に存在する気体中の酸素濃度を測定することによって、反応の進行状況を把握することができる。
系中に存在する気体中の酸素濃度が90%以上になるまで反応させることが好ましく、また、該濃度が95%以上になるまで反応させることがより好ましい。
上記%が70未満である場合は、エタノールの製造効率が低下する。
また、380nmよりも短い波長の光は、実質的に含まれない、即ち、発光量が5%以下、また、3%以下が好ましく、また、0%であるのが望ましい。
尚、“380ないし520nm及び620ないし780nmの波長領域の発光量の合計が全波長領域に亘る発光量の70%以上となる”とは、使用する発光ダイオードの光の発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の合計を百分率で示した値が、70%以上となることを意味する。
回収工程は、反応系中からエタノールを分離し得る方法であれば、特に限定はしないが、例えば、蒸留法、膜分離法等の既知の方法を用いることができる。
また、蒸留法でエタノールを回収する場合、蒸留操作に使用する容器は、生成工程を行った容器をそのまま使用することができ、また、別容器に反応液を移し変えて使用することもできる。
本発明の好ましい態様は、前記密閉された系内に、更なる二酸化炭素を添加するエタノールの製造方法である。
更なる二酸化炭素の添加により、エタノールの製造効率を更に向上することができる。
上記更なる二酸化炭素の添加は、例えば、反応容器に、二酸化炭素の導入管を接続したり、二酸化炭素の雰囲気下に置くこと等により達成される。
尚、二酸化炭素を添加する際、二酸化炭素が外部に流出しないように、系全体として密閉されるようにする。
蒸留法としては、要求されるエタノールの純度に応じて、単蒸留、共沸蒸留、ベンゼンを加えた共沸蒸留等の何れを選択することもできる。
食品店より購入した米粉330gにアミラーゼ6g及び水315gを加え、ミキサーで攪拌し、湯煎して70℃ないし80℃に保ち、12時間かけて米粉を糖化することにより、糖化した固液混合物(米)651gを調製した。
食品店より購入した小麦粉330gにアミラーゼ6g及び水315gを加え、ミキサーで攪拌し、湯煎して70℃ないし80℃に保ち、12時間かけて小麦粉を糖化することにより、糖化した固液混合物(小麦)651gを調製した。
食品店より購入したトウモロコシ粉330gにアミラーゼ6g及び水315gを加え、ミキサーで攪拌し、湯煎して70℃ないし80℃に保ち、12時間かけてトウモロコシ粉を糖化することにより、糖化した固液混合物(トウモロコシ)651gを調製した。
製造例1で製造した糖化した固液混合物(米)217g及び酵母3gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)220gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ11個の100mLビーカーに分け、異なる植物の粉砕物10種類を1gづつ各ビーカーに添加して攪拌した後、各溶液を透明ガラス製の容器である、100mLの注射器に注入した(実施例1ないし10)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例1)。
上記で用意した11本の注射器に白色発光ダイオード200個、赤色発光ダイオード200個、青色発光ダイオード100個及び緑色発光ダイオード100個から構成される計600個の発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、80%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表1に纏めた。
尚、表中、記号aないしjは以下の植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
a:イチョウの葉、b:ソテツの葉、c:稲の葉、d:カワモズク、e:灰色藻、f:クリプト藻、g:生ワカメ、h:ユーグレナ藻、i:クロララクニオン藻、j:藍藻
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしj)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が80%となる発光ダイオードの光を照射すると、何れの植物葉緑体を用いた場合も、3.8ないし3.9mL程度のエタノールが製造された(実施例1ないし10)が、これは、植物葉緑体を用いなかった場合(比較例1)に比して、約1.3倍の収量増であった。
製造例2で製造した糖化した固液混合物(小麦)217g及び酵母3gをミキサーで攪拌し、酵母入りの糖化した固液混合物(小麦)220gを調製した。
調製した酵母入りの糖化した固液混合物(小麦)を20gづつ11個の100mLビーカーに分け、異なる植物の粉砕物10種類を1gづつ各ビーカーに添加して攪拌した後、各溶液を透明ガラス製の容器である、100mLの注射器に注入した(実施例11ないし20)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(小麦)20gを100mLの注射器に注入した(比較例2)。
上記で用意した11本の注射器に白色発光ダイオード200個、赤色発光ダイオード200個、黄色発光ダイオード100個及び藍色発光ダイオード100個から構成される計600個の発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、77%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表2に纏めた。
尚、表中、記号aないしjは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む小麦を糖化して調製された固液混合物、酵母及び種々の植物(aないしj)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が77%となる発光ダイオードの光を照射すると、何れの植物葉緑体を用いた場合も、3.8ないし3.9mL程度のエタノールが製造された(実施例11ないし20)が、これは、植物葉緑体を用いなかった場合(比較例2)に比して、約1.3倍の収量増であった。
製造例3で製造した糖化した固液混合物(トウモロコシ)217g及び酵母3gをミキサーで攪拌し、酵母入りの糖化した固液混合物(トウモロコシ)220gを調製した。
調製した酵母入りの糖化した固液混合物(トウモロコシ)を20gづつ11個の100mLビーカーに分け、異なる植物の粉砕物10種類を1gづつ各ビーカーに添加して攪拌した後、各溶液を透明ガラス製の容器である、100mLの注射器に注入した(実施例21ないし30)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(トウモロコシ)20gを100mLの注射器に注入した(比較例3)。
上記で用意した11本の注射器に白色発光ダイオード200個、赤色発光ダイオード200個、橙色発光ダイオード100個及び紫色発光ダイオード100個から構成される計600個の発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、85%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表3に纏めた。
尚、表中、記号aないしjは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含むトウモロコシを糖化して調製された固液混合物、酵母及び種々の植物(aないしj)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が85%となる発光ダイオードの光を照射すると、何れの植物葉緑体を用いた場合も、4.3ないし4.5mL程度のエタノールが製造された(実施例21ないし30)が、これは、植物葉緑体を用いなかった場合(比較例3)に比して、約1.3倍の収量増であった。
製造例3で製造した糖化した固液混合物(トウモロコシ)217g及び酵母3gをミキサーで攪拌し、酵母入りの糖化した固液混合物(トウモロコシ)220gを調製した。
調製した酵母入りの糖化した固液混合物(トウモロコシ)を20gづつ11個の100mLビーカーに分け、異なる植物の粉砕物10種類を1gづつ各ビーカーに添加して攪拌した後、各ビーカーを密閉した箱の中に置いた。
上記実験とは別に発酵実験を行い、該発酵実験から放出される二酸化炭素を、上記密閉した箱中の各ビーカーの液面で混ざるように、各ビーカーに管を通して導入した(実施例31ないし40)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(トウモロコシ)20gが入ったビーカーを上記密閉した箱中に入れた(比較例4)。
上記の各ビーカーに白色発光ダイオード200個、赤色発光ダイオード200個、橙色発光ダイオード100個及び紫色発光ダイオード100個から構成される計600個の発光ダイオードの光(合計で36ワット/時)を24時間照射した。発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、85%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表4に纏めた。
尚、表中、記号aないしjは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含むトウモロコシを糖化して調製された固液混合物、酵母及び種々の植物(aないしj)の植物葉緑体を含む密閉された系内に、更なる二酸化炭素を添加して、38
0ないし520nm及び620ないし780nmの波長領域の発光量の合計が85%となる発光ダイオードの光を照射すると、何れの植物葉緑体を用いた場合も、5.3ないし5.6mL程度のエタノールが製造された(実施例31ないし40)が、これは、植物葉緑体を用いなかった場合(比較例4)に比して、約1.6倍の収量増であり、また、更なる二酸化炭素を添加していない実施例21ないし30に比して、約1.24倍の収量増であった。
食品店より購入した米粉530gにアミラーゼ(アルファアミラーゼとグルコアミラーゼの混合)10g及び水525gを加え、ミキサーで攪拌し、湯煎して70℃ないし80℃に保ち、12時間かけて米粉を糖化することにより、糖化した固液混合物(米)1065gを調製した。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各溶液を透明ガラス製の容器である、100mLの注射器に注入した(実施例41ないし57)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例5)。
上記で用意した18本の注射器に白色発光ダイオード600個から構成される発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、80%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表5に纏めた。
尚、表中、記号aないしqは以下の植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
a:イチョウの葉、b:ソテツの葉、c:稲の葉、d:カワモズク、e:灰色藻、f:クリプト藻、g:生ワカメ、h:ユーグレナ藻、i:クロララクニオン藻、j:藍藻、k:ミズゴケ、l:クロゴケ、m:スギゴケ、n:ウロコゴケ、o:ゼニゴケ、p:ツノゴケ、q:シアノバクテリア(アオコから抽出)
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が80%となる発光ダイオードの光を照射すると、何れの植物葉緑体を用いた場合も、3.8ないし3.9mL程度のエタノールが製造された(実施例41ないし57)が、これは、植物葉緑体を用いなかった場合(比較例5)に比して、約1.3倍の収量増であった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各
溶液を透明ガラス製の容器である、100mLの注射器に注入した(実施例58ないし74)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例6)。
上記で用意した18本の注射器に赤色発光ダイオード200個、青色発光ダイオード200個及び緑色発光ダイオード200個から構成される計600個の発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、74%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表6に纏めた。
尚、表中、記号aないしqは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が74%となる発光ダイオードの光を照射すると、何れの植物葉緑体を用いた場合も、3.8ないし3.9mL程度のエタノールが製造された(実施例58ないし74)が、これは、植物葉緑体を用いなかった場合(比較例6)に比して、約1.3倍の収量増であった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各
溶液を透明ガラス製の容器である、100mLの注射器に注入した(実施例75ないし91)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例7)。
上記で用意した18本の注射器に赤色発光ダイオード300個及び青色発光ダイオード300個から構成される計600個の発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、100%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表7に纏めた。
尚、表中、記号aないしqは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が100%となる発光ダイオードの光を照射すると、何れの植物葉緑体を用いた場合も、3.8ないし3.9mL程度のエタノールが製造された(実施例75ないし91)が、これは、植物葉緑体を用いなかった場合(比較例7)に比して、約1.3倍の収量増であった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各
溶液を透明ガラス製の容器である、100mLの注射器に注入した(比較例8ないし24)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例25)。
上記で用意した18本の注射器に青色発光ダイオード300個及び緑色発光ダイオード300個から構成される計600個の発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、60%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
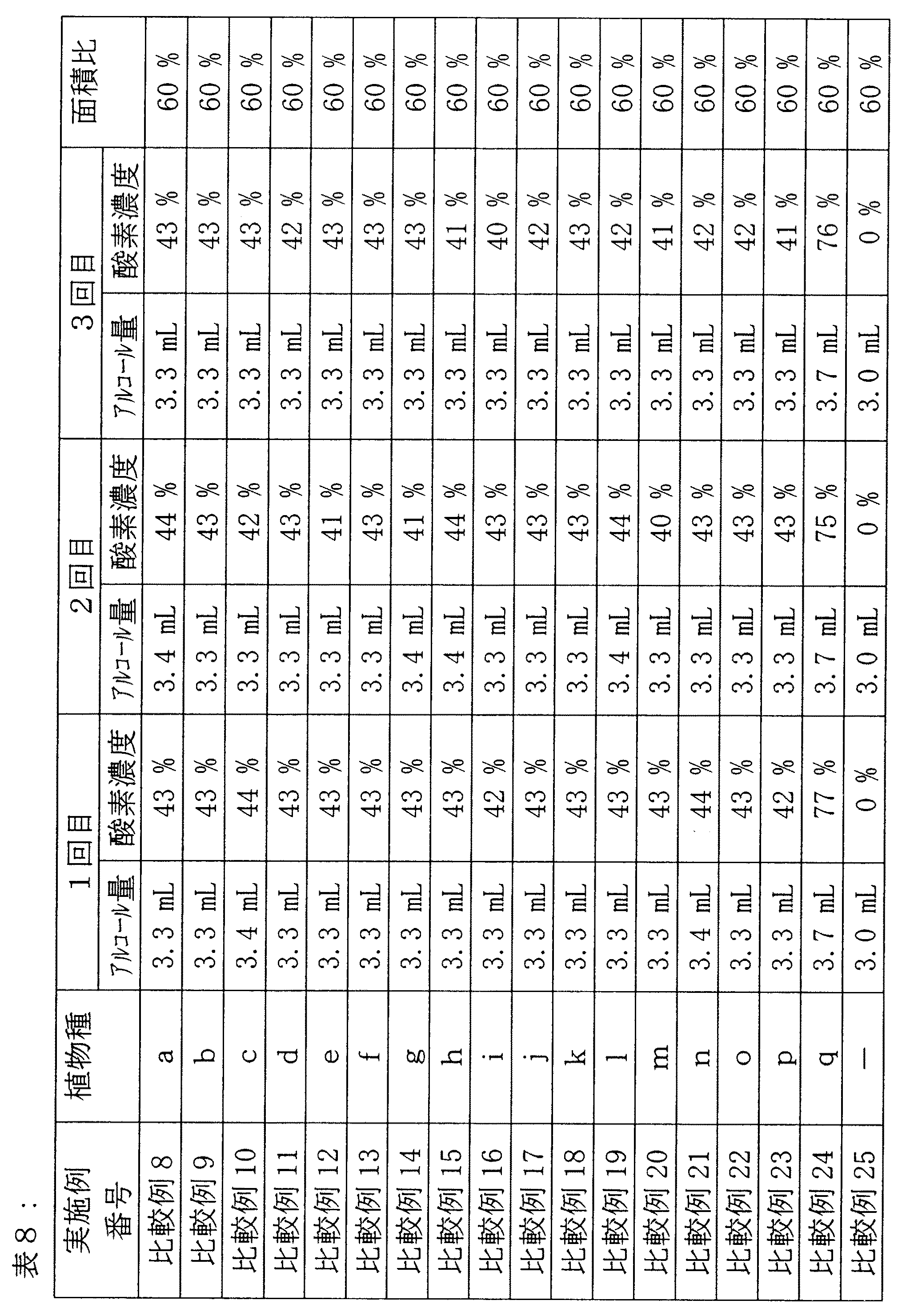
結果を表8に纏めた。
尚、表中、記号aないしqは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が60%となる発光ダイオードの光を照射すると、qのシアノバクテリアの場合(比較例24)を除き、何れの植物葉緑体を用いた場合も、3.3ないし3.4mL程度のエタノールが製造された(比較例8ないし23)が、これは、植物葉緑体を用いなかった場合(比較例25)に比して、約1.1倍程度の収量増しかなかった。qのシアノバクテリアの場合(比較例24)は、比較例25に比して、約1.23倍の収量増があった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各溶液を透明ガラス製の容器である、100mLの注射器に注入した(比較例26ないし42)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例43)。
上記で用意した18本の注射器に赤色発光ダイオード300個及び緑色発光ダイオード300個から構成される計600個の発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、60%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表9に纏めた。
尚、表中、記号aないしqは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が60%となる発光ダイオードの光を照射すると、qのシアノバクテリアの場合(比較例42)を除き、何れの植物葉緑体を用いた場合も、3.2ないし3.3mL程度のエタノールが製造された(比較例26ないし41)が、これは、植物葉緑体を用いなかった場合(比較例43)に比して、約1.1倍程度の収量増しかなかった。qのシアノバクテリアの場合(比較例42)は、比較例43に比して、約1.22倍の収量増があった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各溶液を透明ガラス製の容器である、100mLの注射器に注入した(実施例92ないし108)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例44)。
上記で用意した18本の注射器に青色発光ダイオード600個から構成される発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、100%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表10に纏めた。
尚、表中、記号aないしqは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が100%となる発光ダイオードの光を照射すると、何れの植物葉緑体を用いた場合も、3.8ないし3.9mL程度のエタノールが製造された(実施例92ないし108)が、これは、植物葉緑体を用いなかった場合(比較例44)に比して、約1.3倍の収量増であった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各
溶液を透明ガラス製の容器である、100mLの注射器に注入した(実施例109ないし125)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例45)。
上記で用意した18本の注射器に赤色発光ダイオード600個から構成される発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、100%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表11に纏めた。
尚、表中、記号aないしqは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が100%となる発光ダイオードの光を照射すると、何れの植物葉緑体を用いた場合も、3.8ないし3.9mL程度のエタノールが製造された(実施例109ないし125)が、これは、植物葉緑体を用いなかった場合(比較例45)に比して、約1.3倍の収量増であった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各
溶液を透明ガラス製の容器である、100mLの注射器に注入した(比較例46ないし62)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例63)。
上記で用意した18本の注射器に緑色発光ダイオード600個から構成される発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、20%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表12に纏めた。
尚、表中、記号aないしqは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が20%となる発光ダイオードの光を照射すると、qのシアノバクテリアの場合(比較例62)を除き、何れの植物葉緑体を用いた場合も、3.4ないし3.5mL程度のエタノールが製造された(比較例46ないし61)が、これは、植物葉緑体を用いなかった場合(比較例63)に比して、約1.15倍程度の収量増しかなかった。qのシアノバクテリアの場合(比較例62)は、比較例63に比して、約1.27倍の収量増があった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各溶液を透明ガラス製の容器である、100mLの注射器に注入した(比較例64ないし80)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例81)。
上記で用意した18本の注射器に黄色発光ダイオード600個から構成される発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、0%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表13に纏めた。
尚、表中、記号aないしqは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が0%となる発光ダイオードの光を照射すると、qのシアノバクテリアの場合(比較例80)を除き、何れの植物葉緑体を用いた場合も、3.2ないし3.4mL程度のエタノールが製造された(比較例64ないし79)が、これは、植物葉緑体を用いなかった場合(比較例81)に比して、約1.1倍程度の収量増しかなかった。qのシアノバクテリアの場合(比較例80)は、比較例81に比して、約1.22倍の収量増があった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各溶液を透明ガラス製の容器である、100mLの注射器に注入した(実施例126ないし142)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例82)。
上記で用意した18本の注射器に紫色発光ダイオード600個から構成される発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、100%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表14に纏めた。
尚、表中、記号aないしqは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が100%となる発光ダイオードの光を照射すると、qのシアノバクテリアの場合(実施例142)を除き、何れの植物葉緑体を用いた場合も、3.8ないし4.0mL程度のエタノールが製造された(実施例126ないし141)が、これは、植物葉緑体を用いなかった場合(比較例82)に比して、約1.3倍の収量増であった。qのシアノバクテリアの場合(実施例142)は、比較例82に比して約1.47倍の収量増であった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各溶液を透明ガラス製の容器である、100mLの注射器に注入した(比較例83ないし99)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gを100mLの注射器に注入した(比較例100)。
上記で用意した18本の注射器に橙色発光ダイオード600個から構成される発光ダイオードの光(合計で36ワット/時)を24時間照射した。各注射器から回収された気体の酸素濃度を酸素濃度測定器で測定した。また、発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、50%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表15に纏めた。
尚、表中、記号aないしqは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が50%となる発光ダイオードの光を照射すると、qのシアノバクテリアの場合(比較例99)を除き、何れの植物葉緑体を用いた場合も、3.4ないし3.5mL程度のエタノールが製造された(比較例83ないし98)が、これは、植物葉緑体を用いなかった場合(比較例100)に比して、約1.15倍程度の収量増しかなかった。qのシアノバクテリアの場合(比較例99)は、比較例100に比して、約1.26倍の収量増があった。
製造例4で製造した糖化した固液混合物(米)355g及び酵母5gをミキサーで攪拌し、酵母入りの糖化した固液混合物(米)360gを調製した。
調製した酵母入りの糖化した固液混合物(米)を20gづつ18個の100mLビーカーに分け、異なる植物の粉砕物17種類を1gづつ各ビーカーに添加して攪拌した後、各ビーカーを密閉した箱の中に置いた。
上記実験とは別に発酵実験を行い、該発酵実験から放出される二酸化炭素を、上記密閉した箱中の各ビーカーの液面で混ざるように、各ビーカーに管を通して導入した(実施例143ないし159)。
尚、比較として、植物の粉砕物を入れない酵母入りの糖化した固液混合物(米)20gが入ったビーカーを上記密閉した箱中に入れた(比較例101)。
上記の各ビーカーに白色発光ダイオード600個から構成される発光ダイオードの光(合計で36ワット/時)を24時間照射した。発光ダイオードの発光スペクトルを測定し、記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率を求めたところ、80%であった。
各注射器の中の溶液を蒸留し、アルコールの回収量を測定した。
測定誤差を考慮して上記操作を3回行った。
結果を表16に纏めた。
尚、表中、記号aないしjは上記で示したのと同じ植物を表わし、“面積比”は、発光スペクトルにおいて記録された全スペクトル面積に対する380ないし520nm及び620ないし780nmの波長領域のスペクトル面積の比率(%)を表わす。
デンプンを含む米を糖化して調製された固液混合物、酵母及び種々の植物(aないしq)の植物葉緑体を含む密閉された系内に、更なる二酸化炭素を添加して、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が80%となる発光ダイオードの光を照射すると、qのシアノバクテリアの場合(実施例159)を除き、何れの植物葉緑体を用いた場合も、5.5ないし5.6mL程度のエタノールが製造された(実施例143ないし158)が、これは、植物葉緑体を用いなかった場合(比較例101)に比して、約1.7倍の収量増であり、また、更なる二酸化炭素を添加していない実施例
41ないし57に比して、約1.4倍の収量増であった。また、qのシアノバクテリアの場合(実施例159)は、更なる二酸化炭素を添加していない実施例57に比して約2倍の収量増であった。
おいて有用な方法とえいる。また、本発明のエタノールの製造方法は、副生成物として酸素が得られるため、これを有効な資源として活用することもできる。
また、本発明のエタノールの製造方法は、外部からの二酸化炭素を取り込んでエタノールに変換し得るものであるため、二酸化炭素を固定化するという観点からも有用なエタノールの製造方法となり得るものである。
Claims (3)
- 糖化した固液混合物、酵母及び植物葉緑体を含む密閉された系内において発光ダイオードの光を照射することによりエタノールを生成する生成工程と該系中から生成されたエタノールを系外に回収する回収工程とを含むエタノールの製造方法であって、
前記生成工程において、
a)糖化した固液混合物を酵母により発酵させてエタノールを生成する反応、
b)a)の発酵の際に発生する二酸化炭素を、植物葉緑体と発光ダイオードの光照射により光合成させて糖とする反応、及び
c)b)で得られた糖を酵母により発酵させてエタノールを生成する反応
が並行して進行することを特徴とし、前記糖化した固液混合物は、セルロース又はヘミセルロースを熱分解又は加水分解して糖化するか或いはデンプンを含む米、麦、芋又はトウモロコシを麹、麦芽又は酵素剤を用いて糖化することにより調製されるものであり、前記植物葉緑体は、種子植物、シダ植物、藻類、コケ植物、細菌類又はこれらの混合物の植物葉緑体であり且つ前記発光ダイオードの光は、380ないし520nm及び620ないし780nmの波長領域の発光量の合計が全波長領域に亘る発光量の70%以上となる光であるエタノールの製造方法。 - 前記密閉された系内に、更なる二酸化炭素を添加する請求項1記載のエタノールの製造方法。
- 前記回収工程が、蒸留によるものである請求項1又は2記載のエタノールの製造方法。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008235164A JP4209462B1 (ja) | 2008-09-12 | 2008-09-12 | エタノールの製造方法 |
| PCT/JP2008/069523 WO2009093367A1 (ja) | 2008-01-21 | 2008-10-28 | エタノールの製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008235164A JP4209462B1 (ja) | 2008-09-12 | 2008-09-12 | エタノールの製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP4209462B1 JP4209462B1 (ja) | 2009-01-14 |
| JP2010063433A true JP2010063433A (ja) | 2010-03-25 |
Family
ID=40325706
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008235164A Expired - Fee Related JP4209462B1 (ja) | 2008-01-21 | 2008-09-12 | エタノールの製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4209462B1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9447442B2 (en) | 2008-04-28 | 2016-09-20 | Naturally Scientific Technologies Limited | Production of biofuel from tissue culture sources |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FI20235849A1 (en) * | 2023-07-28 | 2025-01-29 | Aircohol Oy | Apparatus and method for reducing carbon dioxide emissions |
-
2008
- 2008-09-12 JP JP2008235164A patent/JP4209462B1/ja not_active Expired - Fee Related
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9447442B2 (en) | 2008-04-28 | 2016-09-20 | Naturally Scientific Technologies Limited | Production of biofuel from tissue culture sources |
| US10465215B2 (en) | 2008-04-28 | 2019-11-05 | Naturally Scientific Technologies Limited | Production of biofuel from tissue culture sources |
Also Published As
| Publication number | Publication date |
|---|---|
| JP4209462B1 (ja) | 2009-01-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Pathy et al. | Biohydrogen production using algae: Potentiality, economics and challenges | |
| Shokrkar et al. | Bioethanol production from acidic and enzymatic hydrolysates of mixed microalgae culture | |
| Basak et al. | Photofermentative hydrogen production using purple non-sulfur bacteria Rhodobacter sphaeroides OU 001 in an annular photobioreactor: a case study | |
| US20080090283A1 (en) | Ethanol resistant and furfural resistant strains of E. coli FBR5 for production of ethanol from cellulosic biomass | |
| Assaf et al. | Comparative review on the production and purification of bioethanol from biomass: a focus on corn | |
| Velmozhina et al. | Production of biohydrogen from microalgae biomass after wastewater treatment and air purification from CO2 | |
| Lee et al. | Enhancement of microalgal biomass productivity through mixotrophic culture process utilizing waste soy sauce and industrial flue gas | |
| Liu et al. | Experimental study on optimization of initial pH for photo-fermentation bio-hydrogen under different enzymatic hydrolysis of chlorella vulgaris | |
| KR102229628B1 (ko) | 바이오연료 생산시스템 및 이를 이용한 바이오연료 생산방법 | |
| Show et al. | Production of biohydrogen from microalgae | |
| Benemann | Microalgae biofuels: a brief introduction | |
| JP4209462B1 (ja) | エタノールの製造方法 | |
| Sahrin et al. | Enhancing microalgal hydrogen production via photo-fermentative modelling with alimentation derived from palm kernel expeller | |
| CN102266719B (zh) | 一种工业尾气能源化系统 | |
| Palazzi et al. | Mathematical modelling and optimization of hydrogen continuous production in a fixed bed bioreactor | |
| JP2010088334A (ja) | 細胞外に澱粉を放出する藻類を用いた澱粉およびエタノールの製造方法 | |
| WO2009093367A1 (ja) | エタノールの製造方法 | |
| Sun et al. | A new hydrogen-producing strain and its characterization of hydrogen production | |
| CN100532566C (zh) | 生物质及固体有机废弃物发酵和光合耦合产氢的方法 | |
| CN102286542A (zh) | 光驱生物催化前手性羰基化合物不对称还原合成手性醇的方法 | |
| Oncel et al. | Environmental factors affecting hydrogen production from Chlamydomonas reinhardtii | |
| Nomanbhay et al. | Enhancement of bio-hydrogen production in Chlamydomonas Reinhardtii by immobilization and co-culturing | |
| Weaver | Photoconversion of organic substrates into hydrogen using photosynthetic bacteria | |
| CN107937475A (zh) | 利用斜生栅藻和菌类协同产氢的工艺 | |
| Ghimire et al. | Engineering Strategies for Enhancing Photofermentative Biohydrogen Production by Purple Nonsulfur Bacteria Using Dark Fermentation Effluents |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20081008 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20081015 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20081022 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141031 Year of fee payment: 6 |
|
| A072 | Dismissal of procedure |
Free format text: JAPANESE INTERMEDIATE CODE: A073 Effective date: 20090318 |
|
| LAPS | Cancellation because of no payment of annual fees |