JP2004122032A - 水浄化処理システム - Google Patents
水浄化処理システム Download PDFInfo
- Publication number
- JP2004122032A JP2004122032A JP2002291539A JP2002291539A JP2004122032A JP 2004122032 A JP2004122032 A JP 2004122032A JP 2002291539 A JP2002291539 A JP 2002291539A JP 2002291539 A JP2002291539 A JP 2002291539A JP 2004122032 A JP2004122032 A JP 2004122032A
- Authority
- JP
- Japan
- Prior art keywords
- water
- treated
- treatment system
- water purification
- electrolysis
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02W—CLIMATE CHANGE MITIGATION TECHNOLOGIES RELATED TO WASTEWATER TREATMENT OR WASTE MANAGEMENT
- Y02W10/00—Technologies for wastewater treatment
- Y02W10/10—Biological treatment of water, waste water, or sewage
Abstract
【課題】排水中に含まれるアンモニア態窒素の脱窒処理や難分解性有機物質の分解処理を効率良く、かつ確実に行うこと。
【解決手段】原被処理水D中のアンモニアや有機物を、少なくともハロゲン化合物を用いて電気分解処理する電気分解装置3と、前記電気分解処理で発生する次亜ハロゲン酸を還元除去するオキシダント処理装置4と、を備える水浄化処理システムで分解除去し、オキシダント処理装置4から得られる処理水を生物的に脱窒処理することができる。
【選択図】 図1
【解決手段】原被処理水D中のアンモニアや有機物を、少なくともハロゲン化合物を用いて電気分解処理する電気分解装置3と、前記電気分解処理で発生する次亜ハロゲン酸を還元除去するオキシダント処理装置4と、を備える水浄化処理システムで分解除去し、オキシダント処理装置4から得られる処理水を生物的に脱窒処理することができる。
【選択図】 図1
Description
【0001】
【発明の属する技術分野】
本発明は、水浄化処理システムに関する。より詳しくは、種々の排水又は廃水に含まれるアンモニア態窒素や有機物の処理に適する水浄化処理システムに関する。
【0002】
【従来の技術】
現在、種々の産業活動からの排水中に含まれるアンモニア態窒素や難分解性有機物質を含む有機物の処理技術の改善が強く要請されている。例えば、火力発電や原子力発電等の発電事業からの要請が高まっている。
【0003】
現在、排水中に含まれるアンモニア態窒素を除去する場合は、バクテリアを用いた「生物処理」が行われるのが一般的である。この生物処理は、数種類の独立栄養細菌からなる硝化菌群の硝化反応によってアンモニア態窒素を硝酸態窒素に転換し、その後、前記硝酸態窒素を脱窒菌の硝酸呼吸(又は異化的硝酸還元)によって窒素ガス(N2)に転換して、被処理水中から窒素を除去する過程からなる。
【0004】
そして、排水中の有機物の分解技術としては、間接電気分解方法が知られている。例えば、処理対象の排水に食塩を添加して電気分解することにより次亜塩素酸を発生させ、その次亜塩素酸の酸化力によって前記有機物を酸化分解する方法が提案されている(例えば、特許文献1参照)。また、処理対象の排水に電解質塩を添加して、電気分解により酸化マンガンを生成させ、酸素供与触媒作用により、有機物の酸化分解を促進させる間接電気分解方法が提案されている(例えば、特許文献2参照)。
【0005】
【特許文献1】
特開平10−85750号公報
【特許文献2】
特開平5−261374号公報
【0006】
【発明が解決しようとする課題】
まず、排水中のアンモニア態窒素の全てを生物処理する従来技術では、硝化菌群が、活性汚泥処理に関与する従属栄養細菌と比較して、増殖が極めて遅い(反応速度が遅い)ことから、大容量の処理水槽が必要になり、また、この処理水槽に被処理水を長時間滞留させる必要があり、更には、硝化反応で得られる大量の硝酸態窒素を、更に生物的に長時間かけて脱窒処理する必要があるので、処理効率が非常に悪いという技術的課題があった。
【0007】
また、排水中の難分解性有機物質を間接電気分解処理する従来技術では、次亜塩素酸の酸化力が充分でないため、難分解性有機物質が残存するという技術的課題があり(特許文献1の技術)、分解に長時間を要するという技術的課題があった(特許文献2の技術)。
【0008】
そこで、本発明は、排水中に含まれるアンモニア態窒素の脱窒処理や難分解性有機物質の分解処理を効率良く、かつ確実に行うことを主な目的とする。
【0009】
【課題を解決するための手段】
上記課題を解決するために、まず、本願では、被処理水中の処理対象物質を、少なくともハロゲン化合物を用いて電気分解処理する「電気分解装置」と、前記電気分解処理で発生する次亜ハロゲン酸(オキシダント)を還元除去する「オキシダント処理装置」と、を備える水浄化処理システムを提供する。
【0010】
前記水浄化処理システムでは、まず、塩素化合物、臭素化合物、ヨウ素化合物等のハロゲン化合物、特に塩素化合物、臭素化合物を用いて、被処理水中の処理対象物質を、直接電気分解処理することができる。より具体的には、ハロゲン化合物を電気分解することによって生成するオキシダントである次亜ハロゲン酸と排水中の処理対象物質とを反応させて分解したり、又は前記次亜ハロゲン酸が排水中の金属イオンを酸化することで生成する金属酸化物と処理対象物質と反応させて分解したりすることができる。
【0011】
そして、電気分解処理水中に残留する前記次亜ハロゲン酸を、還元剤(例えば、チオ硫酸ナトリウム)を用いて還元除去することができ、更には、前記オキシダント処理装置の後に、活性炭が充填された濾過装置を設け、処理水中に含まれる残留オキシダントを前記活性炭で吸着除去することができる。
【0012】
ここで、前記処理対象物質が「アンモニア(NH3)」である場合は、前記ハロゲン化合物を存在させた前記電気分解装置に前記排水を導入して通電し、該通電によって生成する前記ハロゲン化合物の加水分解生成物である次亜ハロゲン酸と排水中のアンモニアとを反応させて、前記アンモニアを窒素(N2)、水(H2O)、水素(H2)に分解することによって脱窒処理する。即ち、この脱窒処理では、排水中に含まれるアンモニア態窒素を硝酸態窒素に変換せずに、電気分解によって直接脱窒処理する。
【0013】
前記処理対象物質が「有機物」である場合は、ハロゲン化合物と金属イオンが存在する前記電気分解装置に前記排水を導入して通電し、該通電によって生成する前記次亜ハロゲン酸が前記金属イオンを酸化することにより生成する金属酸化物と排水中の有機物とを反応させて、前記有機物を分解するように工夫する。
【0014】
より具体的には、排水中のハロゲン化合物は、電気分解を受けてハロゲン分子(X2)に酸化され、このハロゲン分子は速やかに次亜ハロゲン酸イオン(XO−)に変換される。高濃度の次亜ハロゲン酸が存在することによって、前記金属イオンが酸化還元雰囲気下中に置かれて、電気分解装置の陰極上にて酸化が強力に促進され、該金属イオンが金属酸化物に効率よく変換される。このように得られる高濃度の金属酸化物の酸素供与触媒作用によって、難分解性有機物を含む有機物を、二酸化炭素(CO2)、水(H2O)、硝酸(NO3)等に酸化分解することができる。
【0015】
なお、本願において、「難分解性有機物」とは、活性汚泥処理では分解されずに残存する有機物を意味し、例えば、農薬、抗菌性物質およびその関連物質、PCB、ダオキシン類等を挙げることができる。
【0016】
ここで、「金属イオン」は、処理対象の排水中に含まれる有機物を酸化分解可能な金属酸化物となり得る金属のイオンを意味する。重金属のイオンが好ましく、より好ましくは4以上の比重を有する金属のイオン、特に好ましくは、5以上の比重を有する金属のイオンである。例えば、鉄、マンガン、クロム、銅、鉛、コバルト、ニッケル、亜鉛、チタン、モリブデン、銀、カドミウム、白金、水銀などの金属のイオンを選択でき、特に、マンガン、銅、銀、クロムのイオンが好ましい。
【0017】
次に、本発明では、前記電気分解装置に前記排水を導入して通電し、該通電によって生成する次亜ハロゲン酸と排水中のアンモニアとを反応させてアンモニアの大部分を分解し、即ち前記アンモニアを一次脱窒処理し、続いて、上記オキシダント処理装置では、処理水中に含まれている次亜臭素酸や次亜塩素酸等の次亜ハロゲン酸(オキシダント)を還元除去し、これに続いて、前記一次脱窒処理の過程で、副産物として発生する硝酸態窒素を微生物吸着性を有する担体に吸着固定された脱窒菌を接触させて脱窒する構成の生物処理装置を備える水浄化処理システムを提供する。
【0018】
前記構成の水浄化処理システムでは、電気分解によって非生物的に一次脱窒処理を行う電気分解装置と脱窒菌による二次脱窒処理を行う生物処理装置とを組み合わせることによって、排水中のアンモニアをより完全に脱窒処理できるように工夫されている。
【0019】
即ち、前記電気分解装置と前記生物処理装置の間に、オキシダント処理装置を介在させることによって、生物処理を行う前に、前記電気分解装置から送られてくる電解処理水中に存在するオキシダントである次亜ハロゲン酸を処理水から還元除去しておくようにする。これによって、生物処理装置における脱窒菌の硝酸呼吸が次亜ハロゲン酸によって阻害されなくなるので、(電気分解処理によって発生した)硝酸態窒素の生物的脱窒を効率良く行うことができる。
【0020】
前記オキシダント処理装置の後に更に、処理水中に含まれる次亜ハロゲン酸を活性炭で吸着除去する上記濾過装置を設ければ、次亜ハロゲン酸をより完全に除去できるので、生物活性の阻害をより確実に防止できる。
【0021】
なお、処理対象の排水が、火力発電所や原子力発電所の復水脱塩装置から海に放流されるブロー水や冷却排水等である場合には、アンモニア態窒素に加えてヒドラジン(N2H2)が含まれている場合がある。この場合、ヒドラジンは前記電気分解装置における電気分解によって硝酸に酸化され、この硝酸は、後続の前記生物処理装置で脱窒を受けることになる。
【0022】
ここで、前記生物処理装置で使用する前記担体に、カチオン性の水溶性ポリマーを架橋剤で不溶化することによって得られる皮膜を有する合成樹脂製発泡担体を採用することができる。
【0023】
前記水溶性ポリマーは、アミノ基を備え、該アミノ基を介して前記架橋剤によって互いに架橋することにより不溶化されたものであり、例えば、ポリエチレンイミン等のアルキレンイミンポリマー、ポリアクリルアミドおよびポリアミノ酸から選択することができる。前記合成樹脂製発泡担体は、化学的構造としてポリウレタン等のウレタン結合を有する多孔体、主成分がポリエチレンまたはポリビニルアルコールである多孔体を採用できる。前記架橋剤は、エポキシ誘導体を好適に採用できる。これらの構成を備える担体は、架橋剤で不溶化されたことによって耐久性に優れ、かつ微生物吸着能に優れた皮膜が担体内部にまで形成された構成を備える。
【0024】
更には、この担体を、二次脱窒処理槽内で撹拌等することにより流動させることによって、生物処理が進むにつれて、担体内に充満してくる窒素ガスが担体内から外部へ排出されるようなもみ運動が得られるように工夫する。これによって、長期にわたる高負荷連続運転を可能とし、連続運転中において効率の良い脱窒を継続させることを可能とする。
【0025】
ここで、本発明で採用する上記電気分解装置に配設される電極(陰極と陽極)は、直流電源に接続することも可能ではあるが、交流電源に接続することによって(以下、「交流方式」と称する)、電気分解をより高効率で行うことができるようになる。
【0026】
その結果、省エネルギーを達成でき、しかも長期安定運転が可能となる。具体的には、交流方式によれば、連続運転を行っても電極に汚れが発生し難く、また、最適周波数に制御することで電気分解の効率化を一層推進でき、更には、パルス制御による交流的動作制御を行って電極の極性を入れ変えることが可能となる等の利点が得られる。
【0027】
以上のように、本発明は、排水中のアンモニア態窒素、有機物等の分解処理を迅速かつ高効率で実施できる水浄化処理システムを発電産業界その他の関連産業界に提供するという技術的意義を有している。
【0028】
【発明の実施の形態】
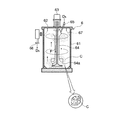
添付図面に基づいて、本発明に係る水浄化処理システムの好適な実施形態について説明する。図1は、同水浄化処理システムの要部構成並びにその付帯関連設備を簡潔に説明するための図である。
【0029】
まず、本発明に係る水浄化処理システムは、符号Dで示された原被処理水に含まれる処理対象物質を、ハロゲン化合物等を用いて電気分解処理する電気分解装置3と、前記電気分解処理で発生する次亜ハロゲン酸を還元除去するオキシダント処理装置4と、を備えている。即ち、本水浄化処理システムにおいて、前記電気分解装置3と前記オキシダント処理装置4は必須の装置である。
【0030】
原被処理水Dの例としては、工場排水、家庭排水、管理型最終処分場浸出液、下水、農村集落排水、畜舎排水、発電所等に設けられている復水脱塩装置から海に放流されるブロー水等を挙げることができ、狭く解釈されない。
【0031】
原被処理水Dを電気分解装置3に導入する前に、該原被処理水Dを一次貯留槽1に導入して一旦貯留し、この原被処理水Dが、アンモニアを分解処理するために有効な量のハロゲン化合物、あるいは有機物を酸化分解するために有効な量の金属イオン及びハロゲン化合物を含有していない場合、又はこれらを全く含有していない場合には、溶解タンクTからハロゲン化合物を含む溶液又はハロゲン化合物及び金属イオンを含む溶液を一次貯留槽1に添加する。また、原被処理水Dが上記有効量のハロゲン化合物や金属イオンを含有している場合、またはこれらが含有しているかどうかが不明の場合にも、同様にハロゲン化合物(及び金属イオン)を含む溶液を一次貯留槽1に添加してもよい。
【0032】
ハロゲン化合物は、塩素化合物、臭素化合物、ヨウ素化合物等のハロゲン化合物、特に塩素化合物、臭素化合物を用いることができる。ハロゲン化合物の被処理水中の量は、ハロゲンイオンとして換算した場合、好ましくは、1mmol/L〜1mol/L程度であり、より好ましくは、0.01mol/L〜0.3mol/Lである。金属イオンの被処理水中の量は、有機物を酸化分解可能な金属酸化物が提供される量でよいが、好ましくは、1μmol/L〜1mol/L程度であり、より好ましくは、50μmol/L〜50mmol/Lである。また、金属イオンを供給するための金属化合物は特に限定されないが、水溶性の金属塩が望ましい。
【0033】
続いて、ハロゲン化合物(及び金属イオン)が添加された被処理水D1を、前記一次貯留槽1から撹拌装置とpH測定器等を備えるpH調整槽2を通過させる。このpH調整槽2においては、pH調整剤(アルカリ剤等)を原被処理水Dに添加して、原被処理水DのpHを目的の範囲に調整する。なお、pH調整槽2では、電気分解装置3で利用できるハロゲン化合物を含んでいる海水を原被処理水Dに導入してもよい。
【0034】
pH調整槽2におけるpHは、ハロゲン分子(X2)が次亜ハロゲン酸イオン(XO−)に変換可能な範囲とし、好ましくはアルカリ側のpH7〜12の範囲、より好ましくはpH8〜10の範囲とする。被処理水D1のpHが前記範囲から外れている場合は、あるいは金属イオンやハロゲン化合物等の添加により前記被処理水D1のpHが前記範囲から外れた場合には、pH調整剤を添加して調整し、これを電解処理の対象となる被処理水D2とすることができる。
【0035】
続いて、前記pH調整槽2でpH調整された前記被処理水D2は、第1図中符号Aで示されたガス吸収塔を介して電気分解装置3に送られる。ガス吸収塔Aは、電気分解装置3における電気分解の結果発生するハロゲンガスGを被処理水D2に吸収させて前記電気分解装置3に送り込む役割を果たし(第1図中の矢印Z参照)、電気分解装置3の電解液S中には少なくともハロゲン化合物が存在するように工夫されている。
【0036】
このハロゲン化合物の存在下、被処理水D2が、電気分解装置3を構成する電気分解槽B内に配設された陽極301、陰極302間を通過する過程で、処理対象物質が分解される。
【0037】
前記処理対象物質がアンモニアである場合には、窒素、水、水素に電気分解処理(脱窒処理)される。より詳しくは、ハロゲン化合物が存在する前記電気分解槽3に被処理水D2を導入して前記電極301,302に通電し、該通電によって生成する前記ハロゲン化合物の加水分解生成物である次亜ハロゲン酸(オキシダント)と被処理水D2のアンモニアとを反応させる。これにより、前記アンモニアを窒素(N2)、水(H2O)、水素(H2)に分解して、脱窒処理する。なお、被処理水D2に含まれる場合があるヒドラジンの一部は、硝酸(NO3 +)に変換され、電気分解槽3から排出される被処理水D3中に残留する。
【0038】
処理対象物質が有機物である場合には、電気分解槽3において、該有機物を、二酸化炭素(CO2)、水(H2O)、硝酸(NO3)等に酸化分解できる。より詳しくは、ハロゲン化合物と金属イオンが存在する前記電気分解槽3に前記被処理水D2を導入して前記電極301,302に通電し、該通電によって生成する前記次亜ハロゲン酸が前記金属イオンを酸化することにより生成する金属酸化物と排水中の有機物とが反応することによって、該有機物は、二酸化炭素(CO2)、水(H2O)、硝酸(NO3)等に酸化分解される。
【0039】
次に、電気分解装置3で処理された被処理水D3は、オキシダント処理装置4に送られる。この被処理水D3中には、電気分解装置3での電気分解処理(脱窒処理又は酸化分解)の過程で発生する次亜臭素酸や次亜塩素酸等の有害な次亜ハロゲン酸(オキシダント)が含まれているので、オキシダント処理装置4において、被処理水D3中の生態系において有害な残留オキシダントを、チオ硫酸ナトリウム(Na2S2O3)等の還元剤Rで還元除去することができる。
【0040】
更に、前記オキシダント処理装置4において前記オキシダントの大部分が還元除去処理された被処理水D4を、活性炭が充填されたカラムを備える濾過装置5に導入し、被処理水D4中の残留オキシダントを活性炭で吸着除去させるように工夫することもできる。これにより、被処理水(又は最終処理水)D5から有害な残留オキシダントをより完全に除去しておくことができるので、好適である。
【0041】
以下、本発明に係る水浄化処理システムで採用可能な電気分解装置3(及びその付属装置)の第1実施形態(符号3a)の構成について説明する。図2は、同第1実施形態の構成を表す図である。
【0042】
図2に示された電気分解装置3aは、まず、吸収塔Aと、電気分解が行われる電気分解槽Bと、を備えている。電気分解槽Bの槽内に挿入された陽極301及び陰極302は、電圧、電流又は周波数等を制御する制御装置303を介して、電源304に接続されている。なお、電極301,302間の距離は被処理水の電気伝導度を考慮して、適宜決定すればよい。
【0043】
電気分解槽Bで処理された被処理水D3は、循環ポンプ305及び排水管路306を通って、後続のオキシダント処理装置4(及び濾過装置5)を経て、更には後述する二次脱窒処理を経て、河川や海等に放流され、この電気分解槽Bで処理された被処理水D3の一部は、循環管路307を通って吸収塔Aに戻される構成となっている。
【0044】
電気分解槽Bの頂部空間308は、排ガスファン309及び排ガス循環管路310を介してガス吸収塔Aに接続されている。ガス吸収塔Aには、処理対象となるアンモニア態窒素(及び有機物)を含む被処理水D2(pH調整済み)が、上記pH調整槽2から排水導入管路311を介して導入される。更に、ガス吸収塔Aからの排気gが大気に放出されるように排気管路313が設けられている。
【0045】
なお、アンモニア態窒素や有機物等の処理対象物質を含有する被処理水D2が海水系である場合、被処理水D2には塩素イオンと臭素イオン等のハロゲン化合物が元々混入されているので、このハロゲン化合物を前記処理対象物質の分解反応に利用することができる。
【0046】
電気分解槽Bからは、電気分解によって少量のCl2、Br2等のハロゲンガスGが発生し、このハロゲンガスGは、上記排ガスファン309で吸引されて吸収塔Aに送り込まれて、大量の被処理水D2に吸収され、配管312を通って電気分解槽Bに送り込まれる。
【0047】
電気分解槽Bに送られたハロゲン化合物含有の被処理水d2は、電気分解槽Bに貯留された電解液Sに存在するClイオン、Brイオン等のハロゲンイオンの存在下、陽極301と陰極302の間を通過する過程で、アンモニアについては窒素、水、水素に分解されることになる。このアンモニアの分解反応を、以下反応式に基づいて具体的に説明する。
【0048】
電気分解槽Bの電解液Sに臭素イオンを含む場合は、電気分解により、陽極301において次の化学式(1)で示される反応が起こる。
【0049】
【化1】
2Br− → Br2 + 2e−
【0050】
続いて、生じた臭素ガス(Br2)は、次化学式(2)に従って加水分解を受けて、次亜臭素酸(HOBr)を生成する。
【0051】
【化2】
Br2+H2O → HOBr + H+ + Br−
【0052】
この次亜臭素酸は、処理対象のアンモニアと次化学式(3)に従って反応する。
【0053】
【化3】
3HOBr+2NH3 → N2+3Br−+3H++3H2O
【0054】
水素イオン(H+)は、陰極302において、水素ガス(H2)に変換される。以上により、アンモニアは、窒素、水、水素に分解される。
【0055】
また、被処理水中に塩素イオンを含む場合は、電気分解により、陽極301において、次化学式(4)で示される電気分解反応が起こる。
【0056】
【化4】
2Cl− → Cl2+2e−
【0057】
生じた塩素ガス(Cl2)は、次化学式(5)、(6)からなる加水分解を受ける。
【0058】
【化5】
Cl2+H2O → HClO+H++Cl−
【0059】
【化6】
HClO ←→ H++OCl−
【0060】
続いて、塩素イオンと臭素イオンの次の交換反応(7)、(8)が起こる。
【0061】
【化7】
OCl−+Br− → OBr−+Cl−
【0062】
【化8】
OBr−+H+ ←→ HOBr
【0063】
この交換反応で生じた次亜臭素酸(HOBr)によって、次化学式(9)に従って、アンモニアが分解される。
【0064】
【化9】
3HOBr+2NH3 → N2+3Br−+3H++3H2O
【0065】
発生した水素イオン(H+)は、陰極302において、水素ガス(H2)に変換される。以上により、アンモニアは、窒素、水、水素に分解する。
【0066】
なお、電気分解槽Bで処理された被処理水は、循環ポンプ305及び排水管路306を通過し、その一部は中和槽318に送流するように構成し、その循環量のほとんどを、循環管路319を介してガス吸収塔Aに戻すように構成してもよい。なお、中和槽318には、中和剤M(例えば、NaOH)の添加装置320及びpH測定器321が設けられている。
【0067】
ここで、電源303については、電気分解槽Bの陽極301及び陰極302を、直流電源に接続した直流方式を採用してもよいし、交流電源に接続した交流方式を採用してもよい。しかしながら、交流方式であると、電気分解がより高効率で行われるので、省エネルギー化を達成でき、しかも長期安定運転が可能となる(後述の電気分解装置3bでも同様)。
【0068】
更には、陰極302を全体的に覆うように、筒体314を設け、この筒体314の頂部が、水素排気パイプ315及び水素排気ファン316を通して燃料電池317に接続されている。このような構成とすることで、電気分解槽Bの陰極302で発生する水素ガスを回収し、これを燃料電池317の水素燃料として利用しエネルギーを回収することができる(後述の電気分解装置3bでも同様)。
【0069】
そしてこの燃料電池316で発生した電力Vを、制御装置303を介して電気分解に利用することができる。燃料電池316からの排気g’は、排気管路313を通して大気に放出することができる。なお、水素燃料利用装置は、燃料電池317でなくても、例えば、水素燃焼エンジン等による発電システムの燃料として利用してもよい(後述の電気分解装置3bでも同様)。
【0070】
以下、本発明に係る水浄化処理システムにおいて採用可能な電気分解装置3(及びその付属装置)の第2実施形態(符号3b)の構成について説明する。図3は、同第2実施形態の構成を表す図である。
【0071】
図3に示された電気分解装置3bは、上記した電気分解装置3a同様に、吸収塔Aと、電気分解を行う電気分解槽Bと、を備えている。電気分解槽Bには、陽極301および陰極302を備える。陽極301には、チタンに白金を焼結したものを用い、陰極302にはチタンを用いることができる(電気分解装置3aにおいても同様)。
【0072】
この電気分解装置3bは、金属イオン添加手段およびハロゲン化合物添加手段となる、ハロゲン化合物及び金属塩の溶解タンクTが付設されており、更に該溶解タンクTには、ポンプ322、供給路323が設けられている。
【0073】
上記したpH調整槽2同様の役割を担うpH調整装置として、pHセンサー324、pH制御シークエンサー325、pH調整剤タンク326、ポンプ327および供給路328を備える。更に、ハロゲンガス循環手段として、ファン329、吸収塔Aに連結する送風路330を備える。
【0074】
ここで、原被処理水Dは、まず、一次貯留槽1に貯留される。原被処理水Dが、有機物を酸化分解するために有効な量の金属イオンおよび同有効量のハロゲン化合物を含有していない場合、又はこれらを全く含有していない場合には、溶解タンクTから、ポンプ323によりハロゲン化合物および金属イオンを含む溶液を、供給路323を介して一次貯留槽1に添加する。
【0075】
また、原被処理水Dが上記有効量のハロゲン化合物および金属イオンを含有している場合、または含有しているかどうかが不明の場合にも、同様にハロゲン化合物及び金属イオンを含む溶液を一次貯留槽1に添加してもよい。
【0076】
次に、一次貯留槽1に一旦貯留された原被処理水Dは、ポンプ331により、配管332を通じて一定量吸収塔Aに送られる。吸収塔Aに供給された原被処理水Dは、該原被処理水Dを循環させるポンプ333によって、配管334を通じて吸収塔Aを循環する。
【0077】
この原被処理水Dは、吸収塔A内を循環する過程で、電気分解槽Bからファン10によって送り込まれたハロゲンガスGを吸収する。すなわち、吸収塔A中に送り込まれたハロゲンガスGは、該吸収塔A内の充填担体を通過する際に、ポンプ333及び配管334によって充填担体の上部の散水管335から散水される原被処理水D1と混和されて吸収される。これらが連続して行われることにより、原被処理水D1中には高濃度にハロゲンガスが溶解する。
【0078】
また、原被処理水Dが吸収塔A内を循環する過程で、pH調整剤タンク326からポンプ327によって、供給路328を通じてpH調整溶液(アルカリ溶液)を原被処理水D中に添加することができる。これにより、原被処理水DのpHは既述した所定範囲に調整され、ハロゲン分子の一部が次亜ハロゲン酸に変換される。
【0079】
次に、上記のような吸収塔A内での循環の過程で、被処理水の一部d2が、原被処理水D1の供給量に応じて、吸収塔Aから配管336を通じて随時電気分解槽Bに供給される。電気分解槽Bには、電極301、302の間で連続的に通電処理がなされる。
【0080】
前記通電処理により次亜ハロゲン酸による酸化的雰囲気下に置かれた金属イオンは、陰極302において金属酸化物に変換され、これにより金属酸化物は電解液S中に高濃度に蓄積される。高濃度の金属酸化物は、その強力な酸素供給触媒作用を発揮し、通常の有機物のみならず、難生分解性有機物質をもCO2、H2O、NO3等に分解することができる。これにより、原被処理水Dは、有機物の酸化分解がなされて浄化処理される。電気分解槽Bで浄化処理された被処理水D3は、後続のオキシダント処理装置4に送られる(図3参照)。
【0081】
なお、前記通電処理により、被処理廃水中に存在するハロゲン化合物はハロゲンガスGに変換され、発生したハロゲンガスGは、ファン329により、送風路330を通じて吸収塔Aに送風される。
【0082】
以上の工程を経て、電気分解装置3bでは、ハロゲン化合物の一部循環を繰り返しながら、電気分解槽Bにおいて有機物、特に難生分解性有機物質の酸化分解を進行させることができる。なお、この際、電気分解槽Bにおいては、上記化学式(1)から(9)の反応も進行し、アンモニアの脱窒処理も同時に行うことができる。
【0083】
続いて、上記電気分解装置3a又は3bの後に配置されるオキシダント処理装置4並びに濾過装置5の詳細構成について説明する。
【0084】
まず、オキシダント処理装置4並びに濾過装置5は、電気分解装置3(3a,3b)の後処理工程を担う装置と位置づけることができる。オキシダント処理装置4は、電気分解装置3(3a,3b)での脱窒処理の際に発生する次亜塩素酸(HOCl)や次亜臭素酸(HOBr)等のオキシダントを還元除去するための貯留槽41を備える(図1参照)。この貯留槽41に添加される還元剤Rとしては、オキシダントを還元できるものであれば特に限定なく使用でき、例えば、チオ硫酸ナトリウム(Na2S2O3)を用いることができる。この場合、次化学式(10)、(11)によって、次亜塩素酸や次亜臭素酸を還元することができる。
【0085】
【化10】
4HOBr + Na2S2O3 + H2O →2NaBr + 2H2SO4 + 2HBr
【0086】
【化11】
4HOCl + Na2S2O3 + H2O →2NaCl + 2H2SO4 + 2HCl
【0087】
オキシダント処理装置4では完全に還元除去できずに、被処理水D4(第1図参照)に微量に残留しているオキシダントは、続いて配置された濾過装置5に被処理水D4を通すことによって、オキシダントを活性炭に吸着させることができる。これにより、被処理水D5(第1図参照)中から、生物活性を阻害する有害なオキシダントを完全に除去できる。
【0088】
次に、オキシダント処理に続いて、二次脱窒処理を行う場合の好適な方法について説明する。図4は、二次脱窒処理を担う生物処理装置6の好適な構成を表す図である。
【0089】
二次脱窒処理は、電気分解装置3(3a,3b)で一次脱窒処理され、更に、オキシダント処理装置4並びに濾過装置5において残留オキシダントが除去された被処理水D5に残留している硝酸態窒素を生物的に脱窒することを目的とする。
【0090】
この二次脱窒処理を担うのは、図4中符号Cで示された微生物吸着性の皮膜が形成された担体Cであり、前記皮膜に吸着固定された脱窒菌群である。即ち、脱窒菌群は、多孔体からなる担体Cの内外表面にバクテリアフィルムを形成し、被処理水D5に含まれる硝酸態窒素を次化学式(12)に従って、脱窒する。
【0091】
【化12】
2NO3 − + 6H+ → 3H2O + N2↑
【0092】
ここで、生物処理装置6の好適な実施形態の一例を図4に基づいて説明すると、所定容量の貯留槽61と、該貯留槽61上部を閉塞する蓋62に配置された撹拌モーター63と、該モーター63によって回転駆動する回転筒64と、被処理水D5の流入口65と、脱窒リアクター装置6で脱窒処理された被処理水D6の排出口66と、を備える(第3図参照)。なお、符号67は、担体Cと被処理水D6を分離するためのスクリーンである。
【0093】
貯留槽61内には、合成樹脂製の多孔体である担体C(第4図の拡大円内図参照)が多数投入されており、該担体Cの内外表面には、微生物吸着性の皮膜が形成され、この皮膜部分に脱窒菌群が確実に吸着固定される。
【0094】
この担体Cは、貯留槽61の中央に垂設された前記回転筒64の作用によって被処理水D5とともに槽内を流動し、この過程で、流動する被処理水D5中に含まれる硝酸態窒素を、効率よく脱窒する(上記化学式12参照)。
【0095】
具体的には、回転筒64の回転によって発生する遠心力で筒内部64bには強い下降流Fが生じ、この下降流Fによって担体Cは、被処理水D5とともに筒下方開口部64aから筒上部に向けて吐き出される。この下降流Fによって貯留槽61内部の被処理水D5と担体Cは、槽内を強制的に流動・撹拌されるため、被処理水D5と脱窒菌群との接触効率が高められる。
【0096】
また、生物処理装置6において担体Cを用いる上記方法によれば、担体Cに損傷を与えるような強い剪断応力を発生させることなく、該担体Cに手もみ様の振動を与えることができる。
【0097】
この振動効果によって、多孔体である担体Cの内部に(脱窒により)発生した窒素ガス(N2)を担体Cの外に追い出すことができる。この結果、担体C内部のガス充満による反応効率低下を有効に防止することができる。これにより、従来慣用の固定化濾床法と比べて、流体のチャンネリングが起きず、撹拌効率が非常に良いので、10倍近い高効率で脱窒反応を促進させることができる。
【0098】
次に、担体Cの詳細構成について説明する。生物処理装置6で使用する担体Cは、微生物吸着性に優れ、一旦吸着された微生物が容易に剥離しない性質を有する皮膜を備えるものが望ましく、特に好適には、カチオン化密度が高い物質が挙げられ、例えば、アミノ基を有する化合物が挙げられる。薄くて均一で剥がれにくく、溶出しにくい微生物吸着性物質の皮膜を形成する観点からは、水溶性ポリマーを用いることが好ましい。
【0099】
そこで、本発明では、カチオン性の水溶性ポリマーを架橋剤で不溶化することによって得られる皮膜を有する合成樹脂製の発泡担体Cを採用する。特にアミノ基を備える水溶性ポリマーは、該アミノ基を介して前記架橋剤によって互いに架橋することにより不溶化できる。例えば、水溶性ポリマーは、ポリエチレンイミン等のアルキレンイミンポリマー、ポリアクリルアミドおよびポリアミノ酸から選択することができる。
【0100】
前記架橋剤は、エポキシ誘導体、例えば、エチレングリコールジグリシジルエーテル、グリセロールジグリシジルエーテル、グリシドール、グリセロールポリグリシジルエーテル、ポリグリセロールポリグリシジルエーテル、ポリエチレングリコールジグリシジルエーテル、ポリプロピレングリコールジグリシジルエーテル、ソルビトールポリグリシジルエーテル、またはソルビタンジグリシジルエーテル等を採用できる。
【0101】
担体Cの表面上で不溶化された微生物吸着性物質からなる皮膜の厚さは、担体の物理的表面構造を維持するという観点から、100μm以下であることが好ましく、最も好ましくは、10μm以下である。
【0102】
不溶化された皮膜によりコーティングされる担体Cの基材は、合成樹脂、多糖類系のポリマー及びその誘導体、又は化学繊維を採用でき、合成樹脂製発泡担体の場合、合成樹脂は、石油、石炭、天然ガスのような化石資源由来の原料から得られた高分子であればいずれのものも使用できる。
【0103】
但し、熱可塑性樹脂の場合、不溶化工程において担体を加熱・乾燥する観点から、120℃以下で可塑性を示さない熱可塑性合成樹脂が好ましい。また、長期間使用しても加水分解を受けて徐々に崩壊しない合成樹脂が耐久性の観点から好ましい。多糖類系のポリマー(例えばセルロース)およびその誘導体は、そのままでは生物分解を受けるので、生分解性が抑制されたものを用いることが好ましい。
【0104】
担体Cを形成する合成樹脂は、化学的構造としてウレタン結合を有することを特徴とするものポリウレタンやポリエチレン又はポリビニルアルコールを主成分とするものが好適である。
【0105】
担体Cは、多孔体、起毛体、球形繊維体、またはペレット体の形態であることが望ましく、多孔体である場合、その最大粒子径は2mm〜90mm、好ましくは、5mm〜10mm、であることができる。2mm未満のものは、排水処理用担体として使用する場合、排水と担体を分離するためのスクリーン67の目を細かくする必要があり、設備費が高額になる上、他の夾雑物による目詰まりが発生しやすくなる。一方、湿潤時の最大粒子径が90mmを越えるものは、排水処理槽内で流動性が悪くなり排水処理効率が低下する。
【0106】
多孔体の多孔構造は、独立気泡内部には微生物が吸着できないため、独立気
泡型ではなく連続気泡型であるのが好ましい。連続気泡が主体であれば一部独立気泡を保有している多孔体でも利用できる。また、多孔体の孔径は0.1mm以上のものが好ましい。0.1mm未満のものは、排水処理用担体として使用する場合、担体C内部への排水の出入りが少なくなり、担体C内部に生息する脱窒菌との接触効率が著しく低下する。
【0107】
多孔体の形状は特に限定されず、立方体を含む直方体状でも、球状でも、不定形型でもよい。
【0108】
また、担体Cを製造する時に、ニーダー(練り混ぜ型撹拌混合器)を使用して薬品溶液を多孔体に十分に含浸させるため、多孔体はある程度の弾性があるのが好ましい。具体的には、反発弾性が10%以上のものが好ましい。
【0109】
以上から、好ましい合成樹脂製多孔体としてはポリウレタンフォームを挙げることができる。ポリウレタンフォームもしくはそれと類似の化学的構造を持つ合成樹脂製多孔体は、排水処理用担体として各社から数多くの種類が販売されており、セルロース製ポリエチレンイミン多孔体と比べて安価である点で有利である。
【0110】
以上説明した、電気分解装置3(3a,3b)、オキシダント処理装置4、濾過装置5、生物処理装置6を順番に配置し、その付帯設備である一次貯留槽1、pH調整槽2、ハロゲン化合物等を供給する溶解タンクT等を適宜配置すれば、図5に示すような水浄化処理システムを構築し、提供することができる。
【0111】
この水浄化処理システムは、電気分解装置3(3a,3b)による電気分解処理と生物処理装置6による脱窒処理(二次脱窒処理)を組み合わせたシステムであって、電気分解処理と生物処理の間にオキシダント処理を行うことを特徴としている。
【0112】
この図5に示された水浄化処理システムによれば、原被処理水Dに含まれるアンモニアを電気分解装置3(3a,3b)で一次脱窒し、更には、有機物を酸化分解し、オキシダントが存在しない状態で生物処理装置6において、二次脱窒処理を効率良く行うことができる。
【0113】
生物処理装置6で硝酸態窒素が脱窒処理された被処理水D6は、慣用の膜濾過ユニット7で汚泥成分Sが除去された後に、清澄な最終処理水D7として海や川に放流される。汚泥成分Sは、慣用のフィルタープレス8等の脱水処理手段によって脱水処理する(図5参照)。なお、本発明に係る水浄化処理システムでは、余剰汚泥の発生が少ないので、フィルタープレス8等の汚泥脱水処理装置は、小型のものを採用できるという利点がある。
【0114】
上記構成の水浄化処理システムによれば、pH9〜10、硝酸態窒素1000mg/L、ヒドラジン20mg/L、SS50mg/Lの性状の排水D1は、pH6〜8、全窒素10mg/L以下、SS10mg/L以下の最終処理水D7とすることができる。なお、最終処理水D7は、脱塩処理等して冷却水等として再利用してもよい。
【0115】
【発明の効果】
本発明に係る水浄化処理システムは、排水中のアンモニア態窒素の脱窒除去並びに有機物の酸化分解を迅速かつ高効率で実施できる小型の水浄化処理システムであるので、種々の産業、冷却水系等からの排水中に含まれるアンモニア態窒素や有機物の除去処理に有効に利用できる。特に、火力発電所や原子力発電所の蒸気タービンに付設される復水脱塩装置から海に放流されるブロー水中に含まれるアンモニア態窒素の脱窒処理に最適である。また、アンモニア態窒素とともに、防食剤であるヒドラジンが含まれる排水においては、アンモニア態窒素に加えてヒドラジンを脱窒処理することもできるので、産業上の利用価値が高い。
【図面の簡単な説明】
【図1】本発明に係る水浄化処理システムの要部構成並びにその付帯関連設備を簡潔に説明するための図
【図2】本発明に係る水浄化処理システムにおいて採用可能な電気分解装置(3a)及びその付属装置の第1実施形態の構成を表す図である。
【図3】本発明に係る水浄化処理システムにおいて採用可能な電気分解装置(3b)及びその付属装置)の第2実施形態の構成を表す図である。
【図4】本発明に係る水浄化処理システムに好適な生物処理装置(6)の構成を表す図
【図5】二次脱窒処理を含む水浄化処理システムの全体構成を表す図
【符号の説明】
1 一次貯留槽
2 pH調整装置
3(3a,3b) 電気分解装置
4 オキシダント処理装置
5 濾過装置
6 生物処理装置
301 陽電極
302 陰電極
A 吸収塔
B 電気分解槽
C 担体
D 原被処理水
G ハロゲンガス
R 還元剤
S 電解液
T 溶解タンク
【発明の属する技術分野】
本発明は、水浄化処理システムに関する。より詳しくは、種々の排水又は廃水に含まれるアンモニア態窒素や有機物の処理に適する水浄化処理システムに関する。
【0002】
【従来の技術】
現在、種々の産業活動からの排水中に含まれるアンモニア態窒素や難分解性有機物質を含む有機物の処理技術の改善が強く要請されている。例えば、火力発電や原子力発電等の発電事業からの要請が高まっている。
【0003】
現在、排水中に含まれるアンモニア態窒素を除去する場合は、バクテリアを用いた「生物処理」が行われるのが一般的である。この生物処理は、数種類の独立栄養細菌からなる硝化菌群の硝化反応によってアンモニア態窒素を硝酸態窒素に転換し、その後、前記硝酸態窒素を脱窒菌の硝酸呼吸(又は異化的硝酸還元)によって窒素ガス(N2)に転換して、被処理水中から窒素を除去する過程からなる。
【0004】
そして、排水中の有機物の分解技術としては、間接電気分解方法が知られている。例えば、処理対象の排水に食塩を添加して電気分解することにより次亜塩素酸を発生させ、その次亜塩素酸の酸化力によって前記有機物を酸化分解する方法が提案されている(例えば、特許文献1参照)。また、処理対象の排水に電解質塩を添加して、電気分解により酸化マンガンを生成させ、酸素供与触媒作用により、有機物の酸化分解を促進させる間接電気分解方法が提案されている(例えば、特許文献2参照)。
【0005】
【特許文献1】
特開平10−85750号公報
【特許文献2】
特開平5−261374号公報
【0006】
【発明が解決しようとする課題】
まず、排水中のアンモニア態窒素の全てを生物処理する従来技術では、硝化菌群が、活性汚泥処理に関与する従属栄養細菌と比較して、増殖が極めて遅い(反応速度が遅い)ことから、大容量の処理水槽が必要になり、また、この処理水槽に被処理水を長時間滞留させる必要があり、更には、硝化反応で得られる大量の硝酸態窒素を、更に生物的に長時間かけて脱窒処理する必要があるので、処理効率が非常に悪いという技術的課題があった。
【0007】
また、排水中の難分解性有機物質を間接電気分解処理する従来技術では、次亜塩素酸の酸化力が充分でないため、難分解性有機物質が残存するという技術的課題があり(特許文献1の技術)、分解に長時間を要するという技術的課題があった(特許文献2の技術)。
【0008】
そこで、本発明は、排水中に含まれるアンモニア態窒素の脱窒処理や難分解性有機物質の分解処理を効率良く、かつ確実に行うことを主な目的とする。
【0009】
【課題を解決するための手段】
上記課題を解決するために、まず、本願では、被処理水中の処理対象物質を、少なくともハロゲン化合物を用いて電気分解処理する「電気分解装置」と、前記電気分解処理で発生する次亜ハロゲン酸(オキシダント)を還元除去する「オキシダント処理装置」と、を備える水浄化処理システムを提供する。
【0010】
前記水浄化処理システムでは、まず、塩素化合物、臭素化合物、ヨウ素化合物等のハロゲン化合物、特に塩素化合物、臭素化合物を用いて、被処理水中の処理対象物質を、直接電気分解処理することができる。より具体的には、ハロゲン化合物を電気分解することによって生成するオキシダントである次亜ハロゲン酸と排水中の処理対象物質とを反応させて分解したり、又は前記次亜ハロゲン酸が排水中の金属イオンを酸化することで生成する金属酸化物と処理対象物質と反応させて分解したりすることができる。
【0011】
そして、電気分解処理水中に残留する前記次亜ハロゲン酸を、還元剤(例えば、チオ硫酸ナトリウム)を用いて還元除去することができ、更には、前記オキシダント処理装置の後に、活性炭が充填された濾過装置を設け、処理水中に含まれる残留オキシダントを前記活性炭で吸着除去することができる。
【0012】
ここで、前記処理対象物質が「アンモニア(NH3)」である場合は、前記ハロゲン化合物を存在させた前記電気分解装置に前記排水を導入して通電し、該通電によって生成する前記ハロゲン化合物の加水分解生成物である次亜ハロゲン酸と排水中のアンモニアとを反応させて、前記アンモニアを窒素(N2)、水(H2O)、水素(H2)に分解することによって脱窒処理する。即ち、この脱窒処理では、排水中に含まれるアンモニア態窒素を硝酸態窒素に変換せずに、電気分解によって直接脱窒処理する。
【0013】
前記処理対象物質が「有機物」である場合は、ハロゲン化合物と金属イオンが存在する前記電気分解装置に前記排水を導入して通電し、該通電によって生成する前記次亜ハロゲン酸が前記金属イオンを酸化することにより生成する金属酸化物と排水中の有機物とを反応させて、前記有機物を分解するように工夫する。
【0014】
より具体的には、排水中のハロゲン化合物は、電気分解を受けてハロゲン分子(X2)に酸化され、このハロゲン分子は速やかに次亜ハロゲン酸イオン(XO−)に変換される。高濃度の次亜ハロゲン酸が存在することによって、前記金属イオンが酸化還元雰囲気下中に置かれて、電気分解装置の陰極上にて酸化が強力に促進され、該金属イオンが金属酸化物に効率よく変換される。このように得られる高濃度の金属酸化物の酸素供与触媒作用によって、難分解性有機物を含む有機物を、二酸化炭素(CO2)、水(H2O)、硝酸(NO3)等に酸化分解することができる。
【0015】
なお、本願において、「難分解性有機物」とは、活性汚泥処理では分解されずに残存する有機物を意味し、例えば、農薬、抗菌性物質およびその関連物質、PCB、ダオキシン類等を挙げることができる。
【0016】
ここで、「金属イオン」は、処理対象の排水中に含まれる有機物を酸化分解可能な金属酸化物となり得る金属のイオンを意味する。重金属のイオンが好ましく、より好ましくは4以上の比重を有する金属のイオン、特に好ましくは、5以上の比重を有する金属のイオンである。例えば、鉄、マンガン、クロム、銅、鉛、コバルト、ニッケル、亜鉛、チタン、モリブデン、銀、カドミウム、白金、水銀などの金属のイオンを選択でき、特に、マンガン、銅、銀、クロムのイオンが好ましい。
【0017】
次に、本発明では、前記電気分解装置に前記排水を導入して通電し、該通電によって生成する次亜ハロゲン酸と排水中のアンモニアとを反応させてアンモニアの大部分を分解し、即ち前記アンモニアを一次脱窒処理し、続いて、上記オキシダント処理装置では、処理水中に含まれている次亜臭素酸や次亜塩素酸等の次亜ハロゲン酸(オキシダント)を還元除去し、これに続いて、前記一次脱窒処理の過程で、副産物として発生する硝酸態窒素を微生物吸着性を有する担体に吸着固定された脱窒菌を接触させて脱窒する構成の生物処理装置を備える水浄化処理システムを提供する。
【0018】
前記構成の水浄化処理システムでは、電気分解によって非生物的に一次脱窒処理を行う電気分解装置と脱窒菌による二次脱窒処理を行う生物処理装置とを組み合わせることによって、排水中のアンモニアをより完全に脱窒処理できるように工夫されている。
【0019】
即ち、前記電気分解装置と前記生物処理装置の間に、オキシダント処理装置を介在させることによって、生物処理を行う前に、前記電気分解装置から送られてくる電解処理水中に存在するオキシダントである次亜ハロゲン酸を処理水から還元除去しておくようにする。これによって、生物処理装置における脱窒菌の硝酸呼吸が次亜ハロゲン酸によって阻害されなくなるので、(電気分解処理によって発生した)硝酸態窒素の生物的脱窒を効率良く行うことができる。
【0020】
前記オキシダント処理装置の後に更に、処理水中に含まれる次亜ハロゲン酸を活性炭で吸着除去する上記濾過装置を設ければ、次亜ハロゲン酸をより完全に除去できるので、生物活性の阻害をより確実に防止できる。
【0021】
なお、処理対象の排水が、火力発電所や原子力発電所の復水脱塩装置から海に放流されるブロー水や冷却排水等である場合には、アンモニア態窒素に加えてヒドラジン(N2H2)が含まれている場合がある。この場合、ヒドラジンは前記電気分解装置における電気分解によって硝酸に酸化され、この硝酸は、後続の前記生物処理装置で脱窒を受けることになる。
【0022】
ここで、前記生物処理装置で使用する前記担体に、カチオン性の水溶性ポリマーを架橋剤で不溶化することによって得られる皮膜を有する合成樹脂製発泡担体を採用することができる。
【0023】
前記水溶性ポリマーは、アミノ基を備え、該アミノ基を介して前記架橋剤によって互いに架橋することにより不溶化されたものであり、例えば、ポリエチレンイミン等のアルキレンイミンポリマー、ポリアクリルアミドおよびポリアミノ酸から選択することができる。前記合成樹脂製発泡担体は、化学的構造としてポリウレタン等のウレタン結合を有する多孔体、主成分がポリエチレンまたはポリビニルアルコールである多孔体を採用できる。前記架橋剤は、エポキシ誘導体を好適に採用できる。これらの構成を備える担体は、架橋剤で不溶化されたことによって耐久性に優れ、かつ微生物吸着能に優れた皮膜が担体内部にまで形成された構成を備える。
【0024】
更には、この担体を、二次脱窒処理槽内で撹拌等することにより流動させることによって、生物処理が進むにつれて、担体内に充満してくる窒素ガスが担体内から外部へ排出されるようなもみ運動が得られるように工夫する。これによって、長期にわたる高負荷連続運転を可能とし、連続運転中において効率の良い脱窒を継続させることを可能とする。
【0025】
ここで、本発明で採用する上記電気分解装置に配設される電極(陰極と陽極)は、直流電源に接続することも可能ではあるが、交流電源に接続することによって(以下、「交流方式」と称する)、電気分解をより高効率で行うことができるようになる。
【0026】
その結果、省エネルギーを達成でき、しかも長期安定運転が可能となる。具体的には、交流方式によれば、連続運転を行っても電極に汚れが発生し難く、また、最適周波数に制御することで電気分解の効率化を一層推進でき、更には、パルス制御による交流的動作制御を行って電極の極性を入れ変えることが可能となる等の利点が得られる。
【0027】
以上のように、本発明は、排水中のアンモニア態窒素、有機物等の分解処理を迅速かつ高効率で実施できる水浄化処理システムを発電産業界その他の関連産業界に提供するという技術的意義を有している。
【0028】
【発明の実施の形態】
添付図面に基づいて、本発明に係る水浄化処理システムの好適な実施形態について説明する。図1は、同水浄化処理システムの要部構成並びにその付帯関連設備を簡潔に説明するための図である。
【0029】
まず、本発明に係る水浄化処理システムは、符号Dで示された原被処理水に含まれる処理対象物質を、ハロゲン化合物等を用いて電気分解処理する電気分解装置3と、前記電気分解処理で発生する次亜ハロゲン酸を還元除去するオキシダント処理装置4と、を備えている。即ち、本水浄化処理システムにおいて、前記電気分解装置3と前記オキシダント処理装置4は必須の装置である。
【0030】
原被処理水Dの例としては、工場排水、家庭排水、管理型最終処分場浸出液、下水、農村集落排水、畜舎排水、発電所等に設けられている復水脱塩装置から海に放流されるブロー水等を挙げることができ、狭く解釈されない。
【0031】
原被処理水Dを電気分解装置3に導入する前に、該原被処理水Dを一次貯留槽1に導入して一旦貯留し、この原被処理水Dが、アンモニアを分解処理するために有効な量のハロゲン化合物、あるいは有機物を酸化分解するために有効な量の金属イオン及びハロゲン化合物を含有していない場合、又はこれらを全く含有していない場合には、溶解タンクTからハロゲン化合物を含む溶液又はハロゲン化合物及び金属イオンを含む溶液を一次貯留槽1に添加する。また、原被処理水Dが上記有効量のハロゲン化合物や金属イオンを含有している場合、またはこれらが含有しているかどうかが不明の場合にも、同様にハロゲン化合物(及び金属イオン)を含む溶液を一次貯留槽1に添加してもよい。
【0032】
ハロゲン化合物は、塩素化合物、臭素化合物、ヨウ素化合物等のハロゲン化合物、特に塩素化合物、臭素化合物を用いることができる。ハロゲン化合物の被処理水中の量は、ハロゲンイオンとして換算した場合、好ましくは、1mmol/L〜1mol/L程度であり、より好ましくは、0.01mol/L〜0.3mol/Lである。金属イオンの被処理水中の量は、有機物を酸化分解可能な金属酸化物が提供される量でよいが、好ましくは、1μmol/L〜1mol/L程度であり、より好ましくは、50μmol/L〜50mmol/Lである。また、金属イオンを供給するための金属化合物は特に限定されないが、水溶性の金属塩が望ましい。
【0033】
続いて、ハロゲン化合物(及び金属イオン)が添加された被処理水D1を、前記一次貯留槽1から撹拌装置とpH測定器等を備えるpH調整槽2を通過させる。このpH調整槽2においては、pH調整剤(アルカリ剤等)を原被処理水Dに添加して、原被処理水DのpHを目的の範囲に調整する。なお、pH調整槽2では、電気分解装置3で利用できるハロゲン化合物を含んでいる海水を原被処理水Dに導入してもよい。
【0034】
pH調整槽2におけるpHは、ハロゲン分子(X2)が次亜ハロゲン酸イオン(XO−)に変換可能な範囲とし、好ましくはアルカリ側のpH7〜12の範囲、より好ましくはpH8〜10の範囲とする。被処理水D1のpHが前記範囲から外れている場合は、あるいは金属イオンやハロゲン化合物等の添加により前記被処理水D1のpHが前記範囲から外れた場合には、pH調整剤を添加して調整し、これを電解処理の対象となる被処理水D2とすることができる。
【0035】
続いて、前記pH調整槽2でpH調整された前記被処理水D2は、第1図中符号Aで示されたガス吸収塔を介して電気分解装置3に送られる。ガス吸収塔Aは、電気分解装置3における電気分解の結果発生するハロゲンガスGを被処理水D2に吸収させて前記電気分解装置3に送り込む役割を果たし(第1図中の矢印Z参照)、電気分解装置3の電解液S中には少なくともハロゲン化合物が存在するように工夫されている。
【0036】
このハロゲン化合物の存在下、被処理水D2が、電気分解装置3を構成する電気分解槽B内に配設された陽極301、陰極302間を通過する過程で、処理対象物質が分解される。
【0037】
前記処理対象物質がアンモニアである場合には、窒素、水、水素に電気分解処理(脱窒処理)される。より詳しくは、ハロゲン化合物が存在する前記電気分解槽3に被処理水D2を導入して前記電極301,302に通電し、該通電によって生成する前記ハロゲン化合物の加水分解生成物である次亜ハロゲン酸(オキシダント)と被処理水D2のアンモニアとを反応させる。これにより、前記アンモニアを窒素(N2)、水(H2O)、水素(H2)に分解して、脱窒処理する。なお、被処理水D2に含まれる場合があるヒドラジンの一部は、硝酸(NO3 +)に変換され、電気分解槽3から排出される被処理水D3中に残留する。
【0038】
処理対象物質が有機物である場合には、電気分解槽3において、該有機物を、二酸化炭素(CO2)、水(H2O)、硝酸(NO3)等に酸化分解できる。より詳しくは、ハロゲン化合物と金属イオンが存在する前記電気分解槽3に前記被処理水D2を導入して前記電極301,302に通電し、該通電によって生成する前記次亜ハロゲン酸が前記金属イオンを酸化することにより生成する金属酸化物と排水中の有機物とが反応することによって、該有機物は、二酸化炭素(CO2)、水(H2O)、硝酸(NO3)等に酸化分解される。
【0039】
次に、電気分解装置3で処理された被処理水D3は、オキシダント処理装置4に送られる。この被処理水D3中には、電気分解装置3での電気分解処理(脱窒処理又は酸化分解)の過程で発生する次亜臭素酸や次亜塩素酸等の有害な次亜ハロゲン酸(オキシダント)が含まれているので、オキシダント処理装置4において、被処理水D3中の生態系において有害な残留オキシダントを、チオ硫酸ナトリウム(Na2S2O3)等の還元剤Rで還元除去することができる。
【0040】
更に、前記オキシダント処理装置4において前記オキシダントの大部分が還元除去処理された被処理水D4を、活性炭が充填されたカラムを備える濾過装置5に導入し、被処理水D4中の残留オキシダントを活性炭で吸着除去させるように工夫することもできる。これにより、被処理水(又は最終処理水)D5から有害な残留オキシダントをより完全に除去しておくことができるので、好適である。
【0041】
以下、本発明に係る水浄化処理システムで採用可能な電気分解装置3(及びその付属装置)の第1実施形態(符号3a)の構成について説明する。図2は、同第1実施形態の構成を表す図である。
【0042】
図2に示された電気分解装置3aは、まず、吸収塔Aと、電気分解が行われる電気分解槽Bと、を備えている。電気分解槽Bの槽内に挿入された陽極301及び陰極302は、電圧、電流又は周波数等を制御する制御装置303を介して、電源304に接続されている。なお、電極301,302間の距離は被処理水の電気伝導度を考慮して、適宜決定すればよい。
【0043】
電気分解槽Bで処理された被処理水D3は、循環ポンプ305及び排水管路306を通って、後続のオキシダント処理装置4(及び濾過装置5)を経て、更には後述する二次脱窒処理を経て、河川や海等に放流され、この電気分解槽Bで処理された被処理水D3の一部は、循環管路307を通って吸収塔Aに戻される構成となっている。
【0044】
電気分解槽Bの頂部空間308は、排ガスファン309及び排ガス循環管路310を介してガス吸収塔Aに接続されている。ガス吸収塔Aには、処理対象となるアンモニア態窒素(及び有機物)を含む被処理水D2(pH調整済み)が、上記pH調整槽2から排水導入管路311を介して導入される。更に、ガス吸収塔Aからの排気gが大気に放出されるように排気管路313が設けられている。
【0045】
なお、アンモニア態窒素や有機物等の処理対象物質を含有する被処理水D2が海水系である場合、被処理水D2には塩素イオンと臭素イオン等のハロゲン化合物が元々混入されているので、このハロゲン化合物を前記処理対象物質の分解反応に利用することができる。
【0046】
電気分解槽Bからは、電気分解によって少量のCl2、Br2等のハロゲンガスGが発生し、このハロゲンガスGは、上記排ガスファン309で吸引されて吸収塔Aに送り込まれて、大量の被処理水D2に吸収され、配管312を通って電気分解槽Bに送り込まれる。
【0047】
電気分解槽Bに送られたハロゲン化合物含有の被処理水d2は、電気分解槽Bに貯留された電解液Sに存在するClイオン、Brイオン等のハロゲンイオンの存在下、陽極301と陰極302の間を通過する過程で、アンモニアについては窒素、水、水素に分解されることになる。このアンモニアの分解反応を、以下反応式に基づいて具体的に説明する。
【0048】
電気分解槽Bの電解液Sに臭素イオンを含む場合は、電気分解により、陽極301において次の化学式(1)で示される反応が起こる。
【0049】
【化1】
2Br− → Br2 + 2e−
【0050】
続いて、生じた臭素ガス(Br2)は、次化学式(2)に従って加水分解を受けて、次亜臭素酸(HOBr)を生成する。
【0051】
【化2】
Br2+H2O → HOBr + H+ + Br−
【0052】
この次亜臭素酸は、処理対象のアンモニアと次化学式(3)に従って反応する。
【0053】
【化3】
3HOBr+2NH3 → N2+3Br−+3H++3H2O
【0054】
水素イオン(H+)は、陰極302において、水素ガス(H2)に変換される。以上により、アンモニアは、窒素、水、水素に分解される。
【0055】
また、被処理水中に塩素イオンを含む場合は、電気分解により、陽極301において、次化学式(4)で示される電気分解反応が起こる。
【0056】
【化4】
2Cl− → Cl2+2e−
【0057】
生じた塩素ガス(Cl2)は、次化学式(5)、(6)からなる加水分解を受ける。
【0058】
【化5】
Cl2+H2O → HClO+H++Cl−
【0059】
【化6】
HClO ←→ H++OCl−
【0060】
続いて、塩素イオンと臭素イオンの次の交換反応(7)、(8)が起こる。
【0061】
【化7】
OCl−+Br− → OBr−+Cl−
【0062】
【化8】
OBr−+H+ ←→ HOBr
【0063】
この交換反応で生じた次亜臭素酸(HOBr)によって、次化学式(9)に従って、アンモニアが分解される。
【0064】
【化9】
3HOBr+2NH3 → N2+3Br−+3H++3H2O
【0065】
発生した水素イオン(H+)は、陰極302において、水素ガス(H2)に変換される。以上により、アンモニアは、窒素、水、水素に分解する。
【0066】
なお、電気分解槽Bで処理された被処理水は、循環ポンプ305及び排水管路306を通過し、その一部は中和槽318に送流するように構成し、その循環量のほとんどを、循環管路319を介してガス吸収塔Aに戻すように構成してもよい。なお、中和槽318には、中和剤M(例えば、NaOH)の添加装置320及びpH測定器321が設けられている。
【0067】
ここで、電源303については、電気分解槽Bの陽極301及び陰極302を、直流電源に接続した直流方式を採用してもよいし、交流電源に接続した交流方式を採用してもよい。しかしながら、交流方式であると、電気分解がより高効率で行われるので、省エネルギー化を達成でき、しかも長期安定運転が可能となる(後述の電気分解装置3bでも同様)。
【0068】
更には、陰極302を全体的に覆うように、筒体314を設け、この筒体314の頂部が、水素排気パイプ315及び水素排気ファン316を通して燃料電池317に接続されている。このような構成とすることで、電気分解槽Bの陰極302で発生する水素ガスを回収し、これを燃料電池317の水素燃料として利用しエネルギーを回収することができる(後述の電気分解装置3bでも同様)。
【0069】
そしてこの燃料電池316で発生した電力Vを、制御装置303を介して電気分解に利用することができる。燃料電池316からの排気g’は、排気管路313を通して大気に放出することができる。なお、水素燃料利用装置は、燃料電池317でなくても、例えば、水素燃焼エンジン等による発電システムの燃料として利用してもよい(後述の電気分解装置3bでも同様)。
【0070】
以下、本発明に係る水浄化処理システムにおいて採用可能な電気分解装置3(及びその付属装置)の第2実施形態(符号3b)の構成について説明する。図3は、同第2実施形態の構成を表す図である。
【0071】
図3に示された電気分解装置3bは、上記した電気分解装置3a同様に、吸収塔Aと、電気分解を行う電気分解槽Bと、を備えている。電気分解槽Bには、陽極301および陰極302を備える。陽極301には、チタンに白金を焼結したものを用い、陰極302にはチタンを用いることができる(電気分解装置3aにおいても同様)。
【0072】
この電気分解装置3bは、金属イオン添加手段およびハロゲン化合物添加手段となる、ハロゲン化合物及び金属塩の溶解タンクTが付設されており、更に該溶解タンクTには、ポンプ322、供給路323が設けられている。
【0073】
上記したpH調整槽2同様の役割を担うpH調整装置として、pHセンサー324、pH制御シークエンサー325、pH調整剤タンク326、ポンプ327および供給路328を備える。更に、ハロゲンガス循環手段として、ファン329、吸収塔Aに連結する送風路330を備える。
【0074】
ここで、原被処理水Dは、まず、一次貯留槽1に貯留される。原被処理水Dが、有機物を酸化分解するために有効な量の金属イオンおよび同有効量のハロゲン化合物を含有していない場合、又はこれらを全く含有していない場合には、溶解タンクTから、ポンプ323によりハロゲン化合物および金属イオンを含む溶液を、供給路323を介して一次貯留槽1に添加する。
【0075】
また、原被処理水Dが上記有効量のハロゲン化合物および金属イオンを含有している場合、または含有しているかどうかが不明の場合にも、同様にハロゲン化合物及び金属イオンを含む溶液を一次貯留槽1に添加してもよい。
【0076】
次に、一次貯留槽1に一旦貯留された原被処理水Dは、ポンプ331により、配管332を通じて一定量吸収塔Aに送られる。吸収塔Aに供給された原被処理水Dは、該原被処理水Dを循環させるポンプ333によって、配管334を通じて吸収塔Aを循環する。
【0077】
この原被処理水Dは、吸収塔A内を循環する過程で、電気分解槽Bからファン10によって送り込まれたハロゲンガスGを吸収する。すなわち、吸収塔A中に送り込まれたハロゲンガスGは、該吸収塔A内の充填担体を通過する際に、ポンプ333及び配管334によって充填担体の上部の散水管335から散水される原被処理水D1と混和されて吸収される。これらが連続して行われることにより、原被処理水D1中には高濃度にハロゲンガスが溶解する。
【0078】
また、原被処理水Dが吸収塔A内を循環する過程で、pH調整剤タンク326からポンプ327によって、供給路328を通じてpH調整溶液(アルカリ溶液)を原被処理水D中に添加することができる。これにより、原被処理水DのpHは既述した所定範囲に調整され、ハロゲン分子の一部が次亜ハロゲン酸に変換される。
【0079】
次に、上記のような吸収塔A内での循環の過程で、被処理水の一部d2が、原被処理水D1の供給量に応じて、吸収塔Aから配管336を通じて随時電気分解槽Bに供給される。電気分解槽Bには、電極301、302の間で連続的に通電処理がなされる。
【0080】
前記通電処理により次亜ハロゲン酸による酸化的雰囲気下に置かれた金属イオンは、陰極302において金属酸化物に変換され、これにより金属酸化物は電解液S中に高濃度に蓄積される。高濃度の金属酸化物は、その強力な酸素供給触媒作用を発揮し、通常の有機物のみならず、難生分解性有機物質をもCO2、H2O、NO3等に分解することができる。これにより、原被処理水Dは、有機物の酸化分解がなされて浄化処理される。電気分解槽Bで浄化処理された被処理水D3は、後続のオキシダント処理装置4に送られる(図3参照)。
【0081】
なお、前記通電処理により、被処理廃水中に存在するハロゲン化合物はハロゲンガスGに変換され、発生したハロゲンガスGは、ファン329により、送風路330を通じて吸収塔Aに送風される。
【0082】
以上の工程を経て、電気分解装置3bでは、ハロゲン化合物の一部循環を繰り返しながら、電気分解槽Bにおいて有機物、特に難生分解性有機物質の酸化分解を進行させることができる。なお、この際、電気分解槽Bにおいては、上記化学式(1)から(9)の反応も進行し、アンモニアの脱窒処理も同時に行うことができる。
【0083】
続いて、上記電気分解装置3a又は3bの後に配置されるオキシダント処理装置4並びに濾過装置5の詳細構成について説明する。
【0084】
まず、オキシダント処理装置4並びに濾過装置5は、電気分解装置3(3a,3b)の後処理工程を担う装置と位置づけることができる。オキシダント処理装置4は、電気分解装置3(3a,3b)での脱窒処理の際に発生する次亜塩素酸(HOCl)や次亜臭素酸(HOBr)等のオキシダントを還元除去するための貯留槽41を備える(図1参照)。この貯留槽41に添加される還元剤Rとしては、オキシダントを還元できるものであれば特に限定なく使用でき、例えば、チオ硫酸ナトリウム(Na2S2O3)を用いることができる。この場合、次化学式(10)、(11)によって、次亜塩素酸や次亜臭素酸を還元することができる。
【0085】
【化10】
4HOBr + Na2S2O3 + H2O →2NaBr + 2H2SO4 + 2HBr
【0086】
【化11】
4HOCl + Na2S2O3 + H2O →2NaCl + 2H2SO4 + 2HCl
【0087】
オキシダント処理装置4では完全に還元除去できずに、被処理水D4(第1図参照)に微量に残留しているオキシダントは、続いて配置された濾過装置5に被処理水D4を通すことによって、オキシダントを活性炭に吸着させることができる。これにより、被処理水D5(第1図参照)中から、生物活性を阻害する有害なオキシダントを完全に除去できる。
【0088】
次に、オキシダント処理に続いて、二次脱窒処理を行う場合の好適な方法について説明する。図4は、二次脱窒処理を担う生物処理装置6の好適な構成を表す図である。
【0089】
二次脱窒処理は、電気分解装置3(3a,3b)で一次脱窒処理され、更に、オキシダント処理装置4並びに濾過装置5において残留オキシダントが除去された被処理水D5に残留している硝酸態窒素を生物的に脱窒することを目的とする。
【0090】
この二次脱窒処理を担うのは、図4中符号Cで示された微生物吸着性の皮膜が形成された担体Cであり、前記皮膜に吸着固定された脱窒菌群である。即ち、脱窒菌群は、多孔体からなる担体Cの内外表面にバクテリアフィルムを形成し、被処理水D5に含まれる硝酸態窒素を次化学式(12)に従って、脱窒する。
【0091】
【化12】
2NO3 − + 6H+ → 3H2O + N2↑
【0092】
ここで、生物処理装置6の好適な実施形態の一例を図4に基づいて説明すると、所定容量の貯留槽61と、該貯留槽61上部を閉塞する蓋62に配置された撹拌モーター63と、該モーター63によって回転駆動する回転筒64と、被処理水D5の流入口65と、脱窒リアクター装置6で脱窒処理された被処理水D6の排出口66と、を備える(第3図参照)。なお、符号67は、担体Cと被処理水D6を分離するためのスクリーンである。
【0093】
貯留槽61内には、合成樹脂製の多孔体である担体C(第4図の拡大円内図参照)が多数投入されており、該担体Cの内外表面には、微生物吸着性の皮膜が形成され、この皮膜部分に脱窒菌群が確実に吸着固定される。
【0094】
この担体Cは、貯留槽61の中央に垂設された前記回転筒64の作用によって被処理水D5とともに槽内を流動し、この過程で、流動する被処理水D5中に含まれる硝酸態窒素を、効率よく脱窒する(上記化学式12参照)。
【0095】
具体的には、回転筒64の回転によって発生する遠心力で筒内部64bには強い下降流Fが生じ、この下降流Fによって担体Cは、被処理水D5とともに筒下方開口部64aから筒上部に向けて吐き出される。この下降流Fによって貯留槽61内部の被処理水D5と担体Cは、槽内を強制的に流動・撹拌されるため、被処理水D5と脱窒菌群との接触効率が高められる。
【0096】
また、生物処理装置6において担体Cを用いる上記方法によれば、担体Cに損傷を与えるような強い剪断応力を発生させることなく、該担体Cに手もみ様の振動を与えることができる。
【0097】
この振動効果によって、多孔体である担体Cの内部に(脱窒により)発生した窒素ガス(N2)を担体Cの外に追い出すことができる。この結果、担体C内部のガス充満による反応効率低下を有効に防止することができる。これにより、従来慣用の固定化濾床法と比べて、流体のチャンネリングが起きず、撹拌効率が非常に良いので、10倍近い高効率で脱窒反応を促進させることができる。
【0098】
次に、担体Cの詳細構成について説明する。生物処理装置6で使用する担体Cは、微生物吸着性に優れ、一旦吸着された微生物が容易に剥離しない性質を有する皮膜を備えるものが望ましく、特に好適には、カチオン化密度が高い物質が挙げられ、例えば、アミノ基を有する化合物が挙げられる。薄くて均一で剥がれにくく、溶出しにくい微生物吸着性物質の皮膜を形成する観点からは、水溶性ポリマーを用いることが好ましい。
【0099】
そこで、本発明では、カチオン性の水溶性ポリマーを架橋剤で不溶化することによって得られる皮膜を有する合成樹脂製の発泡担体Cを採用する。特にアミノ基を備える水溶性ポリマーは、該アミノ基を介して前記架橋剤によって互いに架橋することにより不溶化できる。例えば、水溶性ポリマーは、ポリエチレンイミン等のアルキレンイミンポリマー、ポリアクリルアミドおよびポリアミノ酸から選択することができる。
【0100】
前記架橋剤は、エポキシ誘導体、例えば、エチレングリコールジグリシジルエーテル、グリセロールジグリシジルエーテル、グリシドール、グリセロールポリグリシジルエーテル、ポリグリセロールポリグリシジルエーテル、ポリエチレングリコールジグリシジルエーテル、ポリプロピレングリコールジグリシジルエーテル、ソルビトールポリグリシジルエーテル、またはソルビタンジグリシジルエーテル等を採用できる。
【0101】
担体Cの表面上で不溶化された微生物吸着性物質からなる皮膜の厚さは、担体の物理的表面構造を維持するという観点から、100μm以下であることが好ましく、最も好ましくは、10μm以下である。
【0102】
不溶化された皮膜によりコーティングされる担体Cの基材は、合成樹脂、多糖類系のポリマー及びその誘導体、又は化学繊維を採用でき、合成樹脂製発泡担体の場合、合成樹脂は、石油、石炭、天然ガスのような化石資源由来の原料から得られた高分子であればいずれのものも使用できる。
【0103】
但し、熱可塑性樹脂の場合、不溶化工程において担体を加熱・乾燥する観点から、120℃以下で可塑性を示さない熱可塑性合成樹脂が好ましい。また、長期間使用しても加水分解を受けて徐々に崩壊しない合成樹脂が耐久性の観点から好ましい。多糖類系のポリマー(例えばセルロース)およびその誘導体は、そのままでは生物分解を受けるので、生分解性が抑制されたものを用いることが好ましい。
【0104】
担体Cを形成する合成樹脂は、化学的構造としてウレタン結合を有することを特徴とするものポリウレタンやポリエチレン又はポリビニルアルコールを主成分とするものが好適である。
【0105】
担体Cは、多孔体、起毛体、球形繊維体、またはペレット体の形態であることが望ましく、多孔体である場合、その最大粒子径は2mm〜90mm、好ましくは、5mm〜10mm、であることができる。2mm未満のものは、排水処理用担体として使用する場合、排水と担体を分離するためのスクリーン67の目を細かくする必要があり、設備費が高額になる上、他の夾雑物による目詰まりが発生しやすくなる。一方、湿潤時の最大粒子径が90mmを越えるものは、排水処理槽内で流動性が悪くなり排水処理効率が低下する。
【0106】
多孔体の多孔構造は、独立気泡内部には微生物が吸着できないため、独立気
泡型ではなく連続気泡型であるのが好ましい。連続気泡が主体であれば一部独立気泡を保有している多孔体でも利用できる。また、多孔体の孔径は0.1mm以上のものが好ましい。0.1mm未満のものは、排水処理用担体として使用する場合、担体C内部への排水の出入りが少なくなり、担体C内部に生息する脱窒菌との接触効率が著しく低下する。
【0107】
多孔体の形状は特に限定されず、立方体を含む直方体状でも、球状でも、不定形型でもよい。
【0108】
また、担体Cを製造する時に、ニーダー(練り混ぜ型撹拌混合器)を使用して薬品溶液を多孔体に十分に含浸させるため、多孔体はある程度の弾性があるのが好ましい。具体的には、反発弾性が10%以上のものが好ましい。
【0109】
以上から、好ましい合成樹脂製多孔体としてはポリウレタンフォームを挙げることができる。ポリウレタンフォームもしくはそれと類似の化学的構造を持つ合成樹脂製多孔体は、排水処理用担体として各社から数多くの種類が販売されており、セルロース製ポリエチレンイミン多孔体と比べて安価である点で有利である。
【0110】
以上説明した、電気分解装置3(3a,3b)、オキシダント処理装置4、濾過装置5、生物処理装置6を順番に配置し、その付帯設備である一次貯留槽1、pH調整槽2、ハロゲン化合物等を供給する溶解タンクT等を適宜配置すれば、図5に示すような水浄化処理システムを構築し、提供することができる。
【0111】
この水浄化処理システムは、電気分解装置3(3a,3b)による電気分解処理と生物処理装置6による脱窒処理(二次脱窒処理)を組み合わせたシステムであって、電気分解処理と生物処理の間にオキシダント処理を行うことを特徴としている。
【0112】
この図5に示された水浄化処理システムによれば、原被処理水Dに含まれるアンモニアを電気分解装置3(3a,3b)で一次脱窒し、更には、有機物を酸化分解し、オキシダントが存在しない状態で生物処理装置6において、二次脱窒処理を効率良く行うことができる。
【0113】
生物処理装置6で硝酸態窒素が脱窒処理された被処理水D6は、慣用の膜濾過ユニット7で汚泥成分Sが除去された後に、清澄な最終処理水D7として海や川に放流される。汚泥成分Sは、慣用のフィルタープレス8等の脱水処理手段によって脱水処理する(図5参照)。なお、本発明に係る水浄化処理システムでは、余剰汚泥の発生が少ないので、フィルタープレス8等の汚泥脱水処理装置は、小型のものを採用できるという利点がある。
【0114】
上記構成の水浄化処理システムによれば、pH9〜10、硝酸態窒素1000mg/L、ヒドラジン20mg/L、SS50mg/Lの性状の排水D1は、pH6〜8、全窒素10mg/L以下、SS10mg/L以下の最終処理水D7とすることができる。なお、最終処理水D7は、脱塩処理等して冷却水等として再利用してもよい。
【0115】
【発明の効果】
本発明に係る水浄化処理システムは、排水中のアンモニア態窒素の脱窒除去並びに有機物の酸化分解を迅速かつ高効率で実施できる小型の水浄化処理システムであるので、種々の産業、冷却水系等からの排水中に含まれるアンモニア態窒素や有機物の除去処理に有効に利用できる。特に、火力発電所や原子力発電所の蒸気タービンに付設される復水脱塩装置から海に放流されるブロー水中に含まれるアンモニア態窒素の脱窒処理に最適である。また、アンモニア態窒素とともに、防食剤であるヒドラジンが含まれる排水においては、アンモニア態窒素に加えてヒドラジンを脱窒処理することもできるので、産業上の利用価値が高い。
【図面の簡単な説明】
【図1】本発明に係る水浄化処理システムの要部構成並びにその付帯関連設備を簡潔に説明するための図
【図2】本発明に係る水浄化処理システムにおいて採用可能な電気分解装置(3a)及びその付属装置の第1実施形態の構成を表す図である。
【図3】本発明に係る水浄化処理システムにおいて採用可能な電気分解装置(3b)及びその付属装置)の第2実施形態の構成を表す図である。
【図4】本発明に係る水浄化処理システムに好適な生物処理装置(6)の構成を表す図
【図5】二次脱窒処理を含む水浄化処理システムの全体構成を表す図
【符号の説明】
1 一次貯留槽
2 pH調整装置
3(3a,3b) 電気分解装置
4 オキシダント処理装置
5 濾過装置
6 生物処理装置
301 陽電極
302 陰電極
A 吸収塔
B 電気分解槽
C 担体
D 原被処理水
G ハロゲンガス
R 還元剤
S 電解液
T 溶解タンク
Claims (10)
- 被処理水中の処理対象物質を、少なくともハロゲン化合物を用いて電気分解処理する電気分解装置と、前記電気分解処理で発生する次亜ハロゲン酸を還元除去するオキシダント処理装置と、を備える水浄化処理システム。
- 前記オキシダント処理装置の後に、被処理水中に含まれる次亜ハロゲン酸を活性炭で吸着除去する濾過装置を設けたことを特徴とする請求項1記載の水浄化処理システム。
- 前記電気分解処理は、前記電気分解装置に前記排水を導入して通電し、該通電によって生成する前記次亜ハロゲン酸と排水中のアンモニアとを反応させて、前記アンモニアを脱窒処理することを特徴とする請求項1記載の水浄化処理システム。
- 前記ハロゲン化合物に加えて金属イオンが存在する前記電気分解装置に前記排水を導入して通電し、該通電によって得られる前記次亜ハロゲン酸が前記金属イオンを酸化することにより生成する金属酸化物と排水中の有機物とを反応させて、前記有機物を分解することを特徴とする請求項3記載の水浄化処理システム。
- 前記ハロゲン化合物は、塩素化合物又は臭素化合物であることを特徴とする請求項3又は請求項4に記載の水浄化処理システム。
- 前記金属イオンは、マンガンイオン、銅イオン、亜鉛イオン、銀イオン、クロムイオンのいずれかから選択されることを特徴とする請求項4又は請求項5に記載の水浄化処理システム。
- 前記オキシダント処理装置の後に、前記電気分解処理の過程で発生する硝酸態窒素と微生物吸着性を有する担体に吸着固定された脱窒菌とを接触させて脱窒する生物処理装置を備える請求項3記載の水浄化処理システム。
- 前記担体は、カチオン性の水溶性ポリマーを架橋剤で不溶化することによって得られる皮膜を備える合成樹脂製発泡担体であることを特徴とする請求項7記載の水浄化処理システム。
- 前記担体を、前記生物処理装置を構成する槽内で流動させることを特徴とする請求項7又は請求項8記載の水浄化処理システム。
- 前記電気分解装置に配設される電極は、交流電源に接続されたことを特徴とする請求項1記載の水浄化処理システム。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002291539A JP2004122032A (ja) | 2002-10-03 | 2002-10-03 | 水浄化処理システム |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002291539A JP2004122032A (ja) | 2002-10-03 | 2002-10-03 | 水浄化処理システム |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2004122032A true JP2004122032A (ja) | 2004-04-22 |
Family
ID=32283113
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002291539A Pending JP2004122032A (ja) | 2002-10-03 | 2002-10-03 | 水浄化処理システム |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2004122032A (ja) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006314948A (ja) * | 2005-05-13 | 2006-11-24 | Sanyo Electric Co Ltd | 窒素除去システム |
| US7300592B2 (en) | 2005-08-09 | 2007-11-27 | Sanyo Electric Co., Ltd. | Water treatment device |
| JP2008080236A (ja) * | 2006-09-27 | 2008-04-10 | Kobelco Eco-Solutions Co Ltd | アンモニア性窒素含有排水の処理方法および処理装置 |
| WO2012137752A1 (ja) * | 2011-04-07 | 2012-10-11 | 国立大学法人名古屋大学 | 有機物吸着材および該有機物吸着材を含有してなる有機物吸着性担体 |
| JP2013505819A (ja) * | 2009-09-25 | 2013-02-21 | インヴェント ウムヴェルト ウント フェアファーレンシュテッヒニク アーゲー | 汚水の生物学的浄化方法及び生物学的浄化装置 |
| WO2013176032A1 (ja) * | 2012-05-25 | 2013-11-28 | 三菱重工環境・化学エンジニアリング株式会社 | アンモニア処理システム |
| CN108218053A (zh) * | 2017-12-30 | 2018-06-29 | 骆秀芳 | 生活污水的处理方法 |
| CN114806022A (zh) * | 2022-06-08 | 2022-07-29 | 中国科学院青岛生物能源与过程研究所 | 一种带正电的生物填料及其制备方法 |
-
2002
- 2002-10-03 JP JP2002291539A patent/JP2004122032A/ja active Pending
Cited By (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4596970B2 (ja) * | 2005-05-13 | 2010-12-15 | 三洋電機株式会社 | 窒素除去システム |
| JP2006314948A (ja) * | 2005-05-13 | 2006-11-24 | Sanyo Electric Co Ltd | 窒素除去システム |
| US7300592B2 (en) | 2005-08-09 | 2007-11-27 | Sanyo Electric Co., Ltd. | Water treatment device |
| JP2008080236A (ja) * | 2006-09-27 | 2008-04-10 | Kobelco Eco-Solutions Co Ltd | アンモニア性窒素含有排水の処理方法および処理装置 |
| JP2013505819A (ja) * | 2009-09-25 | 2013-02-21 | インヴェント ウムヴェルト ウント フェアファーレンシュテッヒニク アーゲー | 汚水の生物学的浄化方法及び生物学的浄化装置 |
| JPWO2012137752A1 (ja) * | 2011-04-07 | 2014-07-28 | 国立大学法人名古屋大学 | 有機物吸着材および該有機物吸着材を含有してなる有機物吸着性担体 |
| WO2012137752A1 (ja) * | 2011-04-07 | 2012-10-11 | 国立大学法人名古屋大学 | 有機物吸着材および該有機物吸着材を含有してなる有機物吸着性担体 |
| JP5952187B2 (ja) * | 2011-04-07 | 2016-07-13 | 国立大学法人名古屋大学 | 微生物吸着担体 |
| WO2013176032A1 (ja) * | 2012-05-25 | 2013-11-28 | 三菱重工環境・化学エンジニアリング株式会社 | アンモニア処理システム |
| CN104379512A (zh) * | 2012-05-25 | 2015-02-25 | 三菱重工环境·化学工程株式会社 | 氨处理系统 |
| JP2014000563A (ja) * | 2012-05-25 | 2014-01-09 | Mitsubishi Heavy Industries Environmental & Chemical Engineering Co Ltd | アンモニア処理システム |
| CN104379512B (zh) * | 2012-05-25 | 2017-06-13 | 三菱重工环境·化学工程株式会社 | 氨处理系统 |
| CN108218053A (zh) * | 2017-12-30 | 2018-06-29 | 骆秀芳 | 生活污水的处理方法 |
| CN108218053B (zh) * | 2017-12-30 | 2020-08-07 | 江西挺进环保科技有限公司 | 生活污水的处理方法 |
| CN114806022A (zh) * | 2022-06-08 | 2022-07-29 | 中国科学院青岛生物能源与过程研究所 | 一种带正电的生物填料及其制备方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Domingues et al. | Advanced oxidation processes perspective regarding swine wastewater treatment | |
| CN105585180B (zh) | 一种高效反渗透浓水处理方法 | |
| US7175765B2 (en) | Method for treating for-treatment water containing organic matter and nitrogen compound | |
| EP1477458A2 (en) | Method of treating photographic waste liquid | |
| Feijoo et al. | A review of wastewater treatment technologies for the degradation of pharmaceutically active compounds: Carbamazepine as a case study | |
| CA3107792A1 (en) | System and method for electrochemical oxidation of polyfluoroalkyl substances in water | |
| Ge et al. | Electro-activating persulfate via biochar catalytic cathode for sulfamethazine degradation: Performance and mechanism insight | |
| Zheng et al. | Integrating reactive chlorine species generation with H2 evolution in a multifunctional photoelectrochemical system for low operational carbon emissions saline sewage treatment | |
| CN110526343B (zh) | 一种电催化耦合高级氧化体系及其应用 | |
| JP2004122032A (ja) | 水浄化処理システム | |
| Mousavi et al. | Bio-electrochemical denitrification-A review | |
| JP2004202283A (ja) | 有機化合物含有水の処理方法および処理装置 | |
| CN219860737U (zh) | 一种电催化膜浓缩液的处理装置 | |
| CN204644026U (zh) | 一种采用光电化学技术去除水中氨氮的装置 | |
| JPH07100466A (ja) | 廃水の処理方法 | |
| JP2007061681A (ja) | 硝酸性窒素を含む排水の処理方法及び処理装置、並びに該排水処理用電解槽 | |
| JP2002346566A (ja) | 水処理装置および水処理方法 | |
| CN112499754B (zh) | 一种含氮废水处理系统 | |
| Ranjan et al. | Removal of Urea and Ammonia from Wastewater | |
| CN113968602A (zh) | 一种电催化去除水中硝化氮的方法 | |
| CN102730802A (zh) | 一种电催化有机物废水高级氧化方法装置及方法 | |
| JP4073699B2 (ja) | 空気中に存在する有害物質の分解方法およびそのための装置 | |
| JP4671928B2 (ja) | 排水処理方法 | |
| Yi et al. | REMOVAL OF AMMONIA NITROGEN FROM SWINE WASTERWATER BY ELECTROOXIDATION USING Ti/Mn-Ni/SnO 2-Sb-CeO 2 ANODE. | |
| JP2005224772A (ja) | 殺菌装置を備えた発酵装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050922 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20070702 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080819 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20090106 |