-
Die
Erfindung betrifft ein Verfahren zur Herstellung spezieller Oxidationsmittel,
die in Mischungen mit Vorstufen für die Herstellung leitfähiger Polymere
eine hohe Verarbeitungszeit während
der Polymerisation aufweisen, Oxidationsmittel erhältlich nach
diesem Verfahren, Mischungen enthaltend solche speziellen (retardierenden)
Oxidationsmittel und deren Verwendung zur Herstellung von Feststoffelektrolytkondensatoren
und leitfähigen
Schichten.
-
Die
Verbindungsklasse der π-konjugierten
Polymere war in den letzten Jahrzehnten Gegenstand zahlreicher Veröffentlichungen.
Sie werden auch als leitfähige
Polymere oder als synthetische Metalle bezeichnet.
-
Leitfähige Polymere
gewinnen zunehmend an wirtschaftlicher Bedeutung, da Polymere gegenüber Metallen
Vorteile bezüglich
der Verarbeitbarkeit, des Gewichts und der gezielten Einstellung
von Eigenschaften durch chemische Modifikation haben. Beispiele
für bekannte π-konjugierte
Polymere sind Polypyrrole, Polythiophene, Polyaniline, Polyacetylene,
Polyphenylene und Poly(p-phenylen-vinylene). Schichten aus leitfähigen Polymeren
werden technisch vielfältig
eingesetzt. Eine Übersicht über befindet
sich in L. Groenendaal, F. Jonas, D. Freitag, H. Pielartzik & J. R. Reynolds,
Adv. Mater. 12 (2000) 481–494.
-
Die
Herstellung leitfähiger
Polymere erfolgt chemisch oxidativ oder elektrochemisch aus Vorstufen
für die
Herstellung leitfähiger
Polymere wie z.B. gegebenenfalls substituierten Thiophenen, Pyrrolen
und Anilinen und deren jeweiligen gegebenenfalls oligomeren Derivaten.
Insbesondere die chemisch oxidative Polymerisation ist weit verbreitet,
da sie technisch einfach auf vielfältigen Substraten zu realisieren
ist. Dazu werden die Vorstufen für
die Herstellung leitfähiger
Polymere mit Hilfe eines Oxidationsmittel polymerisiert. Die Polymerisation
ist dabei so schnell, dass die Vorstufen für die Herstellung leitfähiger Polymere
und das Oxidationsmittel in der Regel nacheinander auf das Substrat
aufgebracht werden müssen.
Bei dieser sequentiellen Auftragung tritt jedoch das Problem auf,
dass stöchiometrische
Verhältnisse
zwischen den Vorstufen für
die Herstellung leitfähiger
Polymere und dem Oxidationsmittel nur sehr schwer eingestellt werden
können.
Dies hat zur Folge, dass die Reaktion zum Polymeren unvollständig ist,
die Vorstufen nur unvollständig
genutzt werden und die Qualität
der leitfähigen
Schicht und deren Leitfähigkeit
erniedrigt wird.
-
Darüber hinaus
wird durch die sequentielle Auftragung die Anzahl der notwendigen
Prozessschritte vervielfacht, so dass sequentielle Verfahren mit
deutlich höheren
Prozesskosten verbunden sind. Es besteht daher der Wunsch, Vorstufen
für die
Herstellung leitfähiger
Polymere und das Oxidationsmittel gemeinsam und in genau festgelegten
Mischungen zu verwenden.
-
Mischungen
aus Oxidationsmittel und Vorstufen für die Herstellung leitfähiger Polymere
weisen nur bei tiefen Temperaturen ausreichend niedrige Reaktionsgeschwindigkeiten
auf, um in industriell nutzbaren Verfahren eingesetzt werden zu
können.
So werden beispielsweise in
US
5 455 736 verdünnte
Mischung aus Pyrrol und Oxidationsmittel auf tiefe Temperaturen
gekühlt,
um die Polymerisation hinreichend zu verlangsamen. Der Einsatz tiefer
Temperaturen ist jedoch zum einen technisch sehr aufwendig, zum
anderen ist die Löslichkeit des
Oxidationsmittels bei tiefen Temperaturen begrenzt und die Viskosität der Lösung nimmt
mit sinkender Temperatur stark zu. Weiterhin besteht der Nachteil,
dass durch die tiefe Temperatur Feuchtigkeit aus der Umgebungsluft
in die gekühlten
Lösungen
gelangt und die Qualität
der aus diesen Lösungen
hergestellten leitfähigen
Polymeren nachteilig verändert
wird.
-
In
EP-A 339 340 wird
die chemisch oxidative Polymerisation von 3,4-disubstituierten Thiophenen
beschrieben. Bei geeigneter Wahl des Oxidationsmittels lassen sich
diese Thiophene auch in Lösung
in Gegenwart des Oxidationsmittels zu leitfähigen Schichten verarbeiten.
Die Reaktion setzt jedoch auch hier bereits nach wenigen Minuten
ein.
-
In
EP-A 615 256 wird
beschrieben, dass durch den Zusatz einer nichtflüchtigen Base wie Imidazol die Polymerisation
in Mischungen aus Oxidationsmittel und Vorstufen für die Herstellung
leitfähiger
Polymere verlangsamt werden kann. Damit lässt sich die Polymerisation
für einige
Stunden unterdrücken.
Der Zusatz verbleibt jedoch in der leitfähigen Schicht und kann sich
dort störend
auf die Funktion der Schicht auswirken.
-
In
US 6 001 281 wird die Polymerisation
dadurch verlangsamt, dass zwei Lösungsmittel
mit unterschiedlichen Siedepunkten eingesetzt werden. Das flüchtigere
Lösungsmittel
wird so gewählt,
dass es das als Oxidationsmittel eingesetzte Fe(III) schwach komplexiert
und somit die Reaktion verlangsamt. Das Lösungsmittel mit dem höheren Siedepunkt
komplexiert das Fe(III) hingegen nicht. Zur Polymerisation wird
zunächst das
flüchtigere
Siedemittel abgedampft, woraufhin die Reaktion beschleunigt abläuft. Diese
Methode hat den großen
Nachteil, dass die reaktive Lösung
stark mit einem weiteren Lösungsmittel
verdünnt
werden muss. Ferner sind die eingesetzten Lösungsmittel wie Tetrahydrofuran
industriell nicht erwünscht.
-
Es
besteht somit weiterhin Bedarf an Oxidationsmitteln, die bei technisch
einfach handhabbaren Temperaturen gemeinsam mit Vorstufen für die Herstellung
leitfähiger
Polymere angewandt werden können,
wobei die Polymerisation für
industrielle Anwendungen hinreichend lange unterdrückt wird,
ohne dass zur Verhinderung dessen aufwendige weitere Prozessschritte
durchgeführt
werden müssen.
-
Die
Aufgabe bestand daher darin, geeignete Oxidationsmittel für die chemisch
oxidative Polymerisation von Vorstufen für die Herstellung leitfähiger Polymere
aufzufinden und herzustellen, welche die Polymerisation hinreichend
lange unterdrücken
und mit denen sich leitfähige
Schichten – beispielsweise
für Feststoffelektrolytkondensatoren
oder sonstige Anwendungen – herstellen
lassen.
-
Eine
weitere Aufgabe bestand darin, solche geeigneten Oxidationsmittel
zu finden, die zudem lagerstabil sind.
-
Überraschend
wurde nun gefunden, dass Oxidationsmittel, die durch Behandlung
eines Metallsalzes einer organischen Säure oder organische Reste aufweisenden
anorganischen Säure
mit einem Ionenaustauscher hergestellt wurden, diese Anforderungen
erfüllen.
-
Gegenstand
der vorliegenden Erfindung ist daher ein Verfahren zur Herstellung
eines Oxidationsmittels für
die Herstellung leitfähiger
Polymere, dadurch gekennzeichnet, dass ein Metallsalz einer organischen Säure oder
organische Reste aufweisenden anorganischen Säure mit einem Ionenaustauscher
behandelt wird.
-
Als
Ionenaustauscher können
anorganische oder organische Ionenaustauscher verwendet werden, bevorzugt
sind jedoch organische Ionenaustauscher.
-
Anorganische
Anionenaustauscher sind beispielsweise Zeolithe, Montmorillonite,
Attapulgite, Bentonite und andere Alumosilikate, oder auch saure
Salze polyvalenter Metallionen wie Zirconiumphosphat, Titanwolframat,
Nickelhexacyanoferrat(II).
-
Organische
Anionenaustauscher sind beispielsweise Polykondensate, z.B. aus
Phenol und Formaldehyd, oder Polymerisate, z.B. durch Copolymerisation
aus Styrol, Acrylaten oder Methacrylaten und Divinylbenzol erhältlich,
die im Anschluss entsprechend funktionalisiert wurden. Es können aber
auch andere entsprechend funktionalisierte Makromoleküle, beispielsweise
solche natürlichen
Ursprungs wie Cellulosen, Dextrane und Aragosen verwendet werden.
-
Die
vorangehende Auszählung
dient der beispielhaften Erläuterung
und ist nicht als Beschränkung aufzufassen.
-
Die
Ionenaustauscher können
in den dem Fachmann bekannten Anwendungsformen, beispielsweise als
Perlform, als granulierte Form, als Pulverharze, in gemahlener Form
eingearbeitet in Gewebe oder Fasern, als Papiere, Schichten oder
sonstiger Körper,
in Form von Ionentauschermembranen, als flüssige organische Ionentauscher
oder gegebenenfalls auch als magnetische Ionentauscher, eingesetzt
werden. Die Ionenaustauscher können
makroporös,
mikroporös
oder gelförmig
sein. Bevorzugt werden makroporöse
Ionenaustauscher eingesetzt.
-
Bevorzugt
werden als Ionenaustauscher Anionenaustauscher eingesetzt. Anionenaustauscher
weisen an den Ionenaustauscher gebundene funktionelle basische Gruppen,
wie beispielsweise primäre,
sekundäre
oder tertiäre
Amingruppen bzw. quartäre
Ammoniumgruppen, auf. Je nach Art und Kombination der funktionellen
Gruppen können
die Ionentauscher in ihrer Basizität variieren. Beispielsweise
enthalten stark basische Ionenaustauscher gewöhnlich quartäre Ammoniumgruppen,
während
schwach basische Ionenaustauscher häufig die weniger basischen
primären,
sekundären
und/oder tertiären
Amingruppen tragen. Jedoch sind zwischen stark und schwach basischen
Ionenaustauschern auch beliebige Mischformen bekannt. Bevorzugt im
Sinne der Erfindung eignen sich schwach basische Anionenaustauscher.
Diese können
beispielsweise primäre,
sekundäre
und/oder tertiäre
Amingruppen gegebenenfalls zusammen mit quartären Ammoniumgruppen tragen.
Besonders bevorzugt sind solche schwach basischen Ionenaustauscher
mit überwiegend
oder ausschließlich
tertiären
Amingruppen als funktionelle Gruppen.
-
Ionenaustauscher
sowie deren Herstellung sind dem Fachmann bekannt und in der einschlägigen Fachliteratur,
wie beispielsweise in Ullmanns Encyclopädie der technischen Chemie
(Verlag Chemie, Weinheim), Band 13, 4. Auflage, S. 281-308, beschrieben.
Geeignet zur Durchführung
des erfindungsgemäßen Verfahrens
sind jedoch auch alle Ionenaustauscher, die nach neueren Methoden
herstellbar sind und die oben aufgeführten Eigenschaften besitzen.
-
Beispiele
für geeignete
Ionenaustauscher sind mit tertiären
Aminen funktionalisierte makroporöse Polymerisate aus Stryrol
und Divinylbenzol wie sie z.B. unter dem Handelnamen Lewatit® von
der Bayer AG, Leverkusen vertrieben werden.
-
Die
Ionenaustauscher können
in das erfindungsgemäße Verfahren
ohne vorherige Behandlung eingesetzt werden. Es ist aber ebenfalls
möglich,
die Ionenaustauscher vor ihrem Einsatz z.B. mit Säuren wie
z.B. Schwefelsäure
oder mit Basen wie z.B. Natron oder Kalilauge zu behandeln, beispielsweise,
um sie vor ihrer Verwendung zu regenerieren. Einer solchen Regeneration
können
die erfindungsgemäß eingesetzten
Ionenaustauscher auch dann unterzogen werden, wenn durch das erfindungsgemäße Verfahren
ihre Kapazität
soweit erschöpft
ist, d.h. sie soweit beladen sind, dass sie für die Durchführung des
erfindungsgemäßen Verfahrens
keine ausreichende Austauschfähigkeit
mehr aufweisen. Auf diese Weise können Ionenaustauscher für den Einsatz
im erfindungsgemäßen Verfahren
recycelt werden.
-
Die
Behandlung der Metallsalze mit dem Ionenaustauscher erfolgt bevorzugt
unter Anwesenheit eines Lösungsmittels
oder mehrerer verschiedener Lösungsmittel.
Die Behandlung kann kontinuierlich oder diskontinuierlich z.B. durch
Mischen, Rühren
oder Schütteln
und anschließende
Trennung erfolgen. In einer besonderen Ausführungsform wird die Behandlung
kontinuierlich durchgeführt.
Dazu wird z.B. eine Lösung
des Metallsalzes über
eine Säule,
die den Ionenaustauscher enthält
geführt.
Metallsalz, Lösungsmittel
und Ionenaustauscher können
aber auch gemeinsam in einem Behälter
zusammengeführt
werden und dort für
eine Zeit von beispielsweise einer Minute bis 72 Stunden gelagert
werden. Danach kann dann der Ionenaustauscher z.B. über einen
Filter, eine Membran oder eine Zentrifuge von Oxidationsmittel abgetrennt
werden.
-
Das
erfindungsgemäße Verfahren
kann je nach verwendetem Lösungsmittel
und Temperaturbeständigkeit
des eingesetzten Ionenaustauschers bei Temperaturen von beispielsweise –20°C bis 120°C durchgeführt werden.
Bevorzugt sind solche Temperaturen, die eine einfache und kostengünstige großtechnische Durchführung erlauben, wie
beispielsweise Temperaturen von 10 bis 40°C, besonders bevorzugt Raumtemperatur.
-
Die
Menge an zugesetzten Ionenaustauscher richtet sich nach dessen Kapazität und der
Kontaktzeit von Metallsalz und Ionenaustauscher. Sie kann gegebenenfalls
durch Vorversuche ermittelt werden. Sinnvollerweise wird die Menge
von Ionenaustauscher so gewählt,
dass die resultierenden erfindungsgemäßen Oxidationsmittel gerade
zu einer ausreichend niedrigen Polymerisationsgeschwindigkeit führen. Zu
geringe Mengen an Ionenaustauscher können zu einer Erschöpfung des
Ionenaustauschers führen,
bevor das Metallsalz hinreichend behandelt ist; eine zu kurze Kontaktzeit
kann trotz ausreichender Kapazität
des Ionenaustauschers zu einer nicht vollständigen Behandlung des Metallsalzes
führen.
Mit zu hohen Kapazitäten
und/oder langen Kontaktzeiten an Ionenaustauscher kann ein Oxidationsmittel
hergestellt werden, das die Polymerisation bei geeigneten Prozesstemperaturen
nahezu vollständig
unterdrückt.
Die geeignete Menge an zugesetzten Ionenaustauscher kann gegebenenfalls
durch Vorversuche ermittelt werden.
-
Die
eingesetzten Ionenaustauscher können
wasserhaltig oder wasserfrei sein. Insbesondere ist im Rahmen der
Erfindung unter wasserhaltig ein Wassergehalt von 1 Gew.-% und mehr
zu verstehen. In bevorzugten Ausführungsformen werden handelsübliche Ionentauscher
mit handelsüblichem
Wassergehalt von beispielsweise 30 bis 70 Gew.-% eingesetzt. Der
Wassergehalt des Ionenaustauschers kann gegebenenfalls vor der Behandlung
des Metallsalzes beispielsweise durch Spülen mit einem Lösungsmittel
oder Trocknung gesenkt werden. Dies ist besonders vorteilhaft, falls
eine Lösung
eines Oxidationsmittels mit niedrigem Wassergehalt erwünscht ist.
-
Überraschend
wurde gefunden, dass Lösungen
erfindungsgemäßer Oxidationsmittel
mit einem niedrigen Wassergehalt unter üblichen Lager- bzw. Transporbedingungen
lagerstabil sind. Unter üblichen
Lager- und Transportbedingungen sind beispielsweise Umgebungsdruck
sowie Umgebungstemperaturen bei Transport und Lagerung zu verstehen.
Insbesondere die Umgebungstemperaturen können je nach geographischer Lage
und Jahreszeit variieren und in der Regel beispielsweise bis zu
30°C betragen.
Es können
jedoch auch Temperaturen von bis zu 50°C oder höher erreicht werden.
-
In
weiteren bevorzugten Ausführungsformen
der vorliegenden Erfindung werden daher Ionenaustauscher mit einem
derart niedrigen Wassergehalt eingesetzt, dass die Lösung des
erfindungsgemäßen Oxidationsmittels
nach Behandlung mit dem Ionenaustauscher einen Wassergehalt von
0 bis 10 Gew.-%, bevorzugt von 0 bis 5 Gew.-%, besonders bevorzugt
von 0 bis 2 Gew.-% enthält,
jeweils bezogen auf das Gesamtgewicht der Lösung. Der Wassergehalt von
Ionenaustauscher mit einem hohen Wassergehalt kann dazu vor der
Behandlung des Oxidationsmittels z.B. durch stufenweises oder kontinuierliches
Spülen
mit einem wasserfreien Lösungsmittel
oder durch thermisches Trocknen oder Vakuumtrocknen reduziert werden.
Als Lösungsmittel zum
Spülen
wird bevorzugt das gleiche Lösungsmittel,
in dem das Oxidationsmittel gelöst
ist, verwendet. Es können
aber auch andere, beispielsweise kostengünstigere Lösungsmittel eingesetzt werden.
Bei Verwendung von Ionenaustauschern mit höherem Wassergehalt können die
erfindungsgemäßen Oxidationsmittel nach
der Behandlung mit dem Ionenaustauscher auch nachträglich in
ihrem Wassergehalt reduziert werden, beispielsweise durch Trocknen
und anschließendem
Lösen in
einem wasserfreien Lösungsmittel
oder durch die Verwendung von wasserentziehenden Mitteln, wie beispielsweise
Molekularsieben.
-
Solche
Lösungen
der erfindungsgemäßen Oxidationsmittel
mit niedrigem Wassergehalt erweisen sich unter üblichen Lager- und Transportbedingungen
als lagerstabil, d.h. sie zeigen während eines Zeitraumes von bis
zu mehreren Monaten keine Ausfällungen.
Lösungen
erfindungsgemäßer Oxidationsmittel
mit einem erhöhten
Wassergehalt hingegen zeigen unter gleichen Bedingungen im Laufe
der Zeit, d.h. unter Umständen schon
nach wenigen Stunden oder Tagen Ausfällungen. Letztgenannte Lösungen erfindungsgemäßer Oxidationsmittel
können
aber zur Erhöhung
der Lagerstabilität
auf Temperaturen von 10°C
oder niedriger, bevorzugt von 6°C
oder niedriger gekühlt
werden.
-
Der
Vorteil der Lösungen
der erfindungsgemäßen Oxidationsmittel
mit niedrigem Wassergehalt gegenüber
Lösungen
erfindungsgemäßer Oxidationsmittel
mit höherem
Wassergehalt liegt folglich darin, dass Transport und/oder Lagerung
keiner separaten Kühlung
bedürfen.
-
Die
Lösungen
der erfindungsgemäßen Oxidationsmittel
enthalten bevorzugt 1 bis 80 Gew.-%, besonders bevorzugt 10 bis
60 Gew.-%, ganz besonders bevorzugt 15 bis 50 Gew.-% des erfindungsgemäßen Oxidationsmittels.
-
Als
Metallsalze können
alle dem Fachmann bekannten für
die oxidative Polymerisation von Thiophenen, Anilinen oder Pyrrolen
als Oxidationsmittel geeigneten Metallsalze verwendet werden.
-
Geeignete
Metallsalze sind Metallsalze von Haupt- oder Nebengruppenmetallen,
letztere im Folgenden auch als Übergangsmetallsalze
bezeichnet, des Periodensystems der Elemente nach Mendelejew. Bevorzugt
sind Ubergangsmetallsalze. Geeignete Übergangsmetallsalze sind insbesondere
Salze einer anorganischen oder organischen Säure oder organische Reste aufweisenden
anorganischen Säure
von Übergangsmetallen,
wie z.B. von Eisen(III), Kupfer(II), Chrom(VI), Cer(IV), Mangan(IV),
Mangan(VII), Ruthenium(III) und Zink(II).
-
Bevorzugte Übergangsmetallsalze
sind solche des Eisen(III). Eisen(III)-Salze sind häufig preiswert, leicht
erhältlich
und können
leicht gehandhabt werden, wie z.B. die Eisen(III)-Salze anorganischer
Säuren,
wie beispielsweise Eisen(III)halogenide (z.B. FeCl3)
oder Eisen(III)-Salze anderer anorganischer Säuren, wie Fe(ClO4)3 oder Fe2(SO4)3, und die Eisen(III)-Salze
organischer Säuren
und organische Reste aufweisender anorganischer Säuren.
-
Als
Eisen(III)-Salze organische Reste aufweisender anorganischer Säuren seien
beispielsweise die Eisen(III)-Salze der Schwefelsäurehalbester
von C1-C20-Alkanolen,
z.B. das Eisen(III)-Salz des Laurylsulfates genannt.
-
Besonders
bevorzugte Übergangsmetallsalze
sind solche einer organischen Säure,
insbesondere Eisen(III)-Salze organischer Säuren.
-
Als
Eisen(III)-Salze organischer Säuren
seien beispielsweise genannt: die Eisen(III)-Salze von C1-C20-Alkansulfonsäuren, wie der Methan-, Ethan-,
Propan-, Butan- oder
höherer
Sulfonsäuren
wie der Dodecansulfonsäure,
von aliphatischen Perfluorsulfonsäuren, wie der Trifluormethansulfonsäure, der
Perfluorbutansulfonsäure
oder der Perfluoroctansulfonsäure,
von aliphatischen C1-C20-Carbonsäuren wie
der 2-Ethylhexylcarbonsäure, von
aliphatischen Perfluorcarbonsäuren,
wie der Trifluoressigsäure
oder der Perfluoroctansäure,
und von aromatischen, gegebenenfalls durch C1-C20-Alkylgruppen substituierten Sulfonsäuren wie
der Benzolsulfonsäure,
o-Toluolsulfonsäure, p-Toluolsulfonsäure oder
der Dodecylbenzolsulfonsäure
und von Cycloalkansulfonsäuren
wie Camphersulfonsäure.
-
Es
können
auch beliebige Gemische dieser vorgenannten Eisen(III)-Salze organischer
Säuren
eingesetzt werden.
-
Die
Verwendung der Eisen(III)-salze organischer Säuren und der organischen Reste
aufweisenden anorganischen Säuren
hat den großen
Vorteil, dass sie nicht korrosiv wirken.
-
Ganz
besonders bevorzugt als Metallsalze sind Eisen(III)-p-toluolsulfonat,
Eisen(III)-o-toluolsulfonat oder
einer Mischung aus Eisen(III)-p-toluolsulfonat und Eisen(III)-o-toluolsulfonat.
-
Weiterhin
geeignete Metallsalze sind Peroxoverbindungen wie Peroxodisulfate
(Persulfate), insbesondere Ammonium- und Alkaliperoxodisulfate,
wie Natrium- und Kaliumperoxodisulfat, oder Alkaliperborate sowie Übergangsmetalloxide,
wie z.B. Braunstein (Mangan(IV)oxid) oder Cer(IV)oxid.
-
Als
Lösungsmittel
seien vor allem folgende unter den Reaktionsbedingungen inerten
organischen Lösungsmittel
genannt: aliphatische Alkohole wie Methanol, Ethanol, i-Propanol und Butanol;
aliphatische Ketone wie Aceton und Methylethylketon; aliphatische
Carbonsäureester
wie Essigsäureethylester
und Essigsäurebutylester;
aromatische Kohlenwasserstoffe wie Toluol und Xylol; aliphatische
Kohlenwasserstoffe wie Hexan, Heptan und Cyclohexan; Chlorkohlenwasserstoffe
wie Dichlormethan und Dichlorethan; aliphatische Nitrile wie Acetonitril,
aliphatische Sulfoxide und Sulfone wie Dimethylsulfoxid und Sulfolan;
aliphatische Carbonsäureamide
wie Methylacetamid, Dimethylacetamid und Dimethylformamid; aliphatische
und araliphatische Ether wie Diethylether und Anisol. Weiterhin
kann auch Wasser oder Gemische aus Wasser mit den vorgenannten organischen
Lösungsmitteln
als Lösungsmittel
verwendet werden. Lösungsmittel
aus vorangehend aufgeführter
Auswahl, die mit dem Ionentauscher eine für das erfindungsgemäße Verfahren
nachteilige Reaktion eingehen, werden erst nach der Behandlung mit
dem Ionentauscher – entweder
nach vorheriger Entfernung des vorherigen Lösungsmittels oder zusätzlich zu
diesem – zugegeben.
-
Bevorzugt
als das oder die Lösungsmittel
werden ein oder mehrere Alkohol(e), Wasser oder eine Mischung von
einem oder mehreren Alkoholen) und Wasser eingesetzt. Besonders
bevorzugt unter den Alkoholen sind Butanol, Ethanol und Methanol.
-
Das
erfindungsgemäß hergestellte
Oxidationsmittel kann nach Behandlung mit dem Ionenaustauscher vom
Lösungsmittel
getrennt werden und gegebenenfalls im gleichen oder anderen Lösungsmittel
aus oben aufgeführter
Auswahl wieder gelöst
werden.
-
Weiterhin
Gegenstand der Erfindung sind Oxidationsmittel oder Lösungen von
Oxidationsmitteln erhältlich
durch das vorangehend beschriebene erfindungsgemäße Verfahren. Hierbei gelten
alle Vorzugsbereiche, die für
das erfindungsgemäße Verfahren
gelten, einzeln und in beliebiger Kombination auch für die nach diesem
Verfahren erhältlichen
Oxidationsmittel oder deren Lösungen.
Bevorzugt Gegenstand der Erfindung sind Oxidationsmittel oder Lösungen von
Oxidationsmitteln hergestellt durch das vorangehend beschriebene erfindungsgemäße V erfahren.
-
Im
Vergleich zu nicht mit Ionenaustauschern behandelten Oxidationsmitteln
verlangsamen bzw. verzögern
die erfindungsgemäßen Oxidationsmittel – bei gleicher
Konzentration und gleicher Reaktionstemperatur – die Polymerisation in reaktiven
Mischungen aus Vorstufen für
die Herstellung leitfähiger
Polymere und erfindungsgemäßem Oxidationsmittel.
Sie werden daher im folgenden auch retardierende Oxidationsmittel
genannt.
-
Die
Reaktionsgeschwindigkeit in den reaktiven Mischungen und somit auch
die verzögernde
bzw. verlangsamende Wirkung kann darüber hinaus gegebenenfalls durch
Verdünnung
und/oder Kühlung
weiter abgesenkt werden.
-
Ferner
lassen sich aus den erfindungsgemäßen Oxidationsmitteln gegebenenfalls
leitfähigere
Schichten als aus nicht mit Ionenaustauschern behandelten Oxidationsmitteln
herstellen.
-
Die
retardierende (verzögernde
bzw. verlangsamende) Wirkung der erfindungsgemäßen Oxidationsmittel kann beispielsweise
rein optisch auf einfache Weise beobachtet werden. Zur Bestimmung
der retardierenden Wirkung kann beispielsweise die Zeit gemessen
werden, in der für
das Auge sichtbar die ersten Polymerpartikel gebildet werden. Vorzugsweise
beträgt
die Zeit bis zur sichtbaren Bildung von Polymerpartikeln in den
reaktiven Mischungen länger
als eine Stunde, besonders bevorzugt länger als 10 Stunden und ganz
besonders bevorzugt länger
als 20 Stunden.
-
Gegenstand
der Erfindung ist daher die Verwendung der nach dem erfindungsgemäßen Verfahren
erhältlichen
Oxidationsmittel als retardierende Oxidationsmittel bei der oxidativen
Polymerisation von Vorstufen für
die Herstellung leitfähiger
Polymere.
-
Der
Begriff Polymere umfasst im Sinne der Erfindung alle Verbindungen
mit mehr als einer Wiederholungseinheit.
-
Unter
leitfähigen
Polymeren wird hier die Verbindungsklasse der π-konjugierten Polymere verstanden, die
nach Oxidation oder Reduktion eine elektrische Leitfähigkeit
besitzen. Bevorzugt werden im Sinne der Erfindung solche π-konjugierten
Polymere unter leitfähigen
Polymeren verstanden, die nach Oxidation elektrische Leitfähigkeit
besitzen. Als Beispiel seinen hier gegebenenfalls substituierte
Polythiophene, Polypyrrole und Polyaniline genannt. Bevorzugte leitfähige Polymere
im Sinne der Erfindung sind gegebenenfalls substituierte Polythiophene,
insbesondere gegebenenfalls substituierte Poly(3,4-ethylendioxythiophene).
-
Als
Vorstufen für
die Herstellung leitfähiger
Polymere, im Folgenden auch als Vorstufen bezeichnet, werden demnach
entsprechende Monomere oder deren Derivate verstanden. Es können auch
Mischungen von unterschiedlichen Vorstufen verwendet werden. Geeignete
monomere Vorstufen sind beispielsweise gegebenenfalls substituierte
Thiophene, Pyrrole oder Aniline, bevorzugt gegebenenfalls substituierte
Thiophene, besonders bevorzugt gegebenenfalls substituierte 3,4-Alkylendioxythiophene.
-
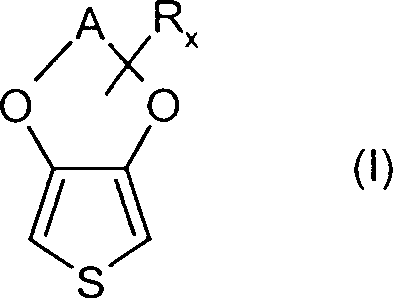
Als
substituierte 3,4-Alkylendioxythiophene seien beispielhaft die Verbindungen
der allgemeinen Formel (I) genannt,
worin
A für einen
gegebenenfalls substituierten C
1-C
5-Alkylenrest, bevorzugt für einen
gegebenenfalls substituierten C
2-C
3-Alkylenrest, steht,
R für einen
linearen oder verzweigten, gegebenenfalls substituierten C
1-C
18-Alkylrest, bevorzugt
linearen oder verzweigten, gegebenenfalls substituierten C
1-C
14-Alkylrest,
gegebenenfalls substituierten C
5-C
12-Cycloalkylrest, gegebenenfalls substituierten
C
6-C
14-Arylrest,
gegebenenfalls substituierten C
7-C
18-Aralkylrest,
gegebenenfalls substituierten C
1-C
4-Hydroxyalkylrest, bevorzugt gegebenenfalls
substituierten C
1-C
2-Hydroxyalkylrest,
oder einen Hydroxylrest steht,
x für eine ganze Zahl von 0 bis
8 steht, bevorzugt von 0 bis 6, besonders bevorzugt für 0 oder
1 steht,
wobei für
den Fall das mehrere Reste R an A gebunden sind, diese gleich oder
unterschiedlich sein können.
-
Die
allgemeine Formel (I) ist so zu verstehen, dass der Substituent
R x-mal an den Alkylenrest A gebunden sein kann.
-
Ganz
besonders bevorzugte monomere Vorstufen sind gegebenenfalls substituierte
3,4-Ethylendioxythiophene.
-
Als
substituierte 3,4-Ethylendioxythiophene seien beispielhaft die Verbindungen
der allgemeinen Formel (Ia) genannt,
worin R und x die für die allgemeine
Formel (I) genannte Bedeutung haben.
-
Unter
Derivaten dieser monomeren Vorstufen werden im Sinne der Erfindung
beispielsweise Dimere oder Trimere dieser monomeren Vorstufen verstanden.
Es sind auch höhermolekulare
Derivate, d.h. Tetramere, Pentamere etc. der monomeren Vorstufen
als Derivate möglich.
-
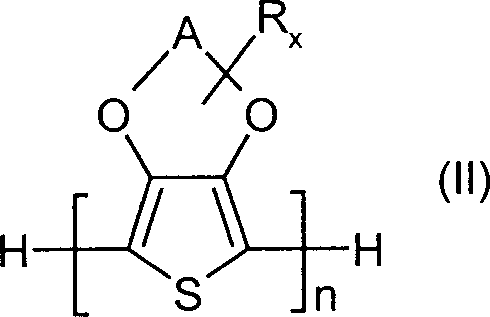
Als
Derivate substituierter 3,4-Alkylendioxythiophene seien beispielhaft
die Verbindungen der allgemeinen Formel (II) genannt,
worin
n für eine ganze
Zahl von 2 bis 20, bevorzugt 2 bis 6, besonders bevorzugt für 2 oder
3 steht,
und
A, R und x die für die allgemeine Formel (I)
genannte Bedeutung haben.
-
Die
Derivate können
sowohl aus gleichen wie unterschiedlichen Monomereinheiten aufgebaut
sein und in reiner Form sowie im Gemisch untereinander und/oder
mit den monomeren Vorstufen eingesetzt werden. Auch oxidierte oder
reduzierte Formen dieser Vorstufen sind im Sinne der Erfindung von
dem Begriff „Vorstufen" umfasst, sofern
bei ihrer Polymerisation die gleichen leitfähigen Polymeren entstehen wie
bei den vorangehend aufgeführten
Vorstufen.
-
Als
Substituenten für
die Vorstufen, insbesondere für
die Thiophene, bevorzugt für
die 3,4-Alkylendioxythiophene kommen die für die allgemeine Formel (I)
für R genannten
Reste in Frage.
-
C1-C5-Alkylenreste
A sind im Rahmen der Erfindung Methylen, Ethylen, n-Propylen, n-Butylen
oder n-Pentylen. C1-C18-Alkyl
steht im Rahmen der Erfindung für
lineare oder verzweigte C1-C18-Alkylreste
wie beispielsweise Methyl, Ethyl, n- oder iso-Propyl, n-, iso-,
sec- oder tert-Butyl, n-Pentyl, 1-Methylbutyl, 2-Methylbutyl, 3-Methylbutyl, 1-Ethylpropyl,
1,1-Dimethylpropyl, 1,2-Dimethylpropyl, 2,2-Dimethylpropyl, n-Hexyl,
n-Heptyl, n-Octyl, 2-Ethylhexyl, n-Nonyl, n-Decyl, n-Undecyl, n-Dodecyl,
n-Tridecyl, n-Tetradecyl, n-Hexadecyl oder n-Octadecyl, C5-C12-Cycloalkyl für C5-C12-Cycloalkylreste
wie beispielsweise Cyclopentyl, Cyclohexyl, Cycloheptyl, Cyclooctyl,
Cyclononyl oder Cyclodecyl, C6-C1 4-Aryl für C6-C1 4-Arylreste
wie beispielsweise Phenyl, o-, m-, p-Tolyl, 2,3-, 2,4-, 2,5-, 2,6-,
3,4-, 3,5-Xylyl, Mesityl oder Naphthyl, und C7-C18-Aralkyl für C7-C18-Aralkylreste wie beispielsweise Benzyl.
Die vorangehende Aufzählung
dient der beispielhaften Erläuterung
der Erfindung und ist nicht als abschließend zu betrachten.
-
Als
mögliche
Substituenten für
die Reste R kommen zahlreiche organische Gruppen in Frage, beispielsweise
Alkyl-, Cycloalkyl-, Aryl-, Halogen-, Hydroxyl-, Ether-, Thioether-,
Disulfid-, Sulfoxid-, Sulfonsäure-, Sulfonat-,
Amino-, Aldehyd-, Keto-, Carbonsäureester-,
Carbonat-, Carboxylat, Cyano-, Alkylsilan- und Alkoxysilangruppen
sowie Carboxylamidgruppen.
-
Verfahren
zur Herstellung der monomeren Vorstufen für die Herstellung leitfähiger Polymere
sowie deren Derivaten sind dem Fachmann bekannt und beispielsweise
in L. Groenendaal, F. Jonas, D. Freitag, H. Pielartzik & J. R. Reynolds,
Adv. Mater. 12 (2000) 481–494
und darin zitierter Literatur beschrieben.
-
Der
Vorteil des gemeinsamen Aufbringens von Oxidationsmittel und Vorstufen
für die
Herstellung leitfähiger
Polymere bei technisch einfach handhabbaren Temperatu ren liegt darin,
dass sich dadurch die Anzahl der Prozessschritte deutlich reduziert.
Außerdem
kann auf diese Weise ein definiertes stöchiometrisches Verhältnis zwischen
den Reaktionspartnern eingestellt werden. So ist es beispielsweise
möglich,
die Vorstufen zu hohen Anteilen, gegebenenfalls sogar bis nahezu
100 % in das Polymer zu überführen.
-
Weiterhin
sind die Lösungen
oder Mischungen der erfindungsgemäß erhältlichen Oxidationsmittel und den
Vorstufen in besonderem Maße
zur Erzeugung von leitfähigen
Schichten auf der Oberfläche
von porösen oder
glatten Substraten geeignet. Dadurch dass die Oxidationsmittel und
die Vorstufen in den Mischungen gleichmäßig verteilt vorliegen, entstehen
bei der Polymerisation auch homogene, d.h. dichte – im Sinne
von nicht oder wenig poröse – Polymerschichten.
Bei einer sequentiellen Auftragung von Oxidationsmittel und Vorstufen
entstehen aufgrund lokalem Über-
oder Unterschuss von Oxidationsmittel und Vorstufen, dagegen poröse Polymerschichten.
Die aus den erfindungsgemäßen Mischungen
erhältlichen
leitfähigen
Schichten zeichnen sich daher durch eine besondere Homogenität und hohe
Leitfähigkeit
aus.
-
Weiterhin
sind die erfindungsgemäßen Lösungen oder
Mischungen für
eine deutlich längere
Zeit der Verarbeitung zugänglich
als solche, die Oxidationsmittel enthalten, die nicht mit einen
Ionenaustauscher behandelt wurden. Hierdurch wird es erstmals möglich, diese
Mischungen bzw. Lösungen
in kontinuierlichen, industriellen Fertigungsprozessen einzusetzen.
-
Ebenfalls
Gegenstand der Erfindung sind Mischungen enthaltend Vorstufen für die Herstellung
leitfähiger
Polymere und ein oder mehrere erfindungsgemäße Oxidationsmittel sowie gegebenenfalls
ein oder mehrere Lösungsmittel,
dadurch gekennzeichnet, dass die Bildung von Polymeren in den Mischungen
im Vergleich zu unbehandelten Oxidationsmitteln verzögert wird.
-
Vorangehend
aufgeführte
Vorzugsbereiche, Definitionen und Beispiele für Vorstufen, erfindungsgemäße Oxidationsmittel
und Lösungsmittel
gelten hier analog.
-
Die
erfindungsgemäßen Mischungen
können
homogen oder heterogen sowie ein- oder
mehrphasig sein. Bevorzugt handelt es sich bei den erfindungsgemäßen Mischungen
um Lösungen.
-
Die
Oxidationsmittel und Vorstufen für
die Herstellung leitfähiger
Polymere können
als Feststoff und/oder Flüssigkeit
miteinander gemischt werden. Bevorzugt werden den Mischungen jedoch
ein oder mehrere Lösungsmittel
zugegeben. Als geeignete Lösungsmittel
seien vor allem die oben bereits aufgeführten Lösungsmittel genannt. Es ist
auch möglich
die Mischungen direkt auf der zu beschichtenden Oberfläche, beispielsweise
auf einer Oxidschicht eines Metalls oder auf einer Substratoberfläche, herzustellen.
Dazu werden Oxidationsmittel und Vorstufen für die Herstellung leitfähiger Polymere
nacheinander, bevorzugt in Form von Lösungen auf die zu beschichtende
Oberfläche
gegeben. Die Mischung entsteht dann durch Durchmischung der einzelnen
Lösungen
auf der zu beschichtenden Oberfläche
bzw. gegebenenfalls nach teilweisem oder vollständigem Abdampfen der Lösungsmittel
durch Diffusion an der Grenzfläche
Oxidationsmittel zu Vorstufen.
-
Die
erfindungsgemäßen Mischungen
können
Wasser enthalten. Dieses Wasser kann beispielsweise aus dem erfindungsgemäßen Oxidationsmittel
oder dessen Lösung
stammen und/oder den erfindungsgemäßen Mischungen nachträglich zugesetzt
werden. Durch den Zusatz von Wasser kann die Verzögerung der
Bildung von Polymeren in den erfindungsgemäßen Mischungen, d.h. die Topfzeit,
erhöht
werden. Eine zusätzliche
Wasserzugabe erfolgt bevorzugt bei Verwendung erfindungsgemäßer Oxidationsmittel
oder deren Lösungen
mit einem niedrigen Wassergehalt. Bevorzugt werden 1 bis 100 Gew.-%,
besonders bevorzugt 1 bis 60 Gew.-%, ganz besonders bevorzugt 1
bis 40 Gew.-% Wasser zugesetzt, bezogen auf das Gewicht des erfindungsgemäßen Oxidationsmittels.
-
Die
mit den erfindungsgemäßen Oxidationsmitteln
hergestellten leitfähigen
Polymere können
neutral oder kationisch sein, bevorzugt sind sie jedoch kationisch.
Hierbei bezieht sich „kationisch" nur auf die Ladungen,
die auf der Polymerhauptkette sitzen. Diese positiven Ladungen müssen durch
Gegenionen abgesättigt werden,
welche in den speziellen Ausführungsformen,
in denen die Wiederholungseinheiten durch anionische Gruppen wie
beispielsweise Sulfonat- oder Carboxylatgruppen substituiert sind,
an die Polymerkette kovalent gebunden sein können. Dabei können die
positiven Ladungen der Polymerhauptkette zum Teil oder vollständig durch
die kovalent gebundenen anionischen Gruppen abgesättigt werden.
Für den
Fall das mehr kovalent gebundene anionische Gruppen als positive
Ladungen vorhanden sind, kann zwar auch eine negative Gesamtladung
des Polymeren resultieren, diese werden jedoch im Rahmen der Erfindung
auch als kationische Polymere betrachtet, da die positiven Ladungen
auf der Polymerhauptkette maßgeblich
sind. Die positiven Ladungen sind im Allgemeinen in Formeln nicht
dargestellt, da ihre genaue Zahl und Position nicht einwandfrei
feststellbar sind. Die Anzahl der positiven Ladungen beträgt jedoch
mindestens 1 und höchstens
p, wobei p die Gesamtanzahl aller im Polymeren enthaltenen – gleichen
oder unterschiedlichen – Wiederholungseinheiten
ist.
-
Zur
Kompensation der positiven Ladung, soweit dies nicht bereits durch
gegebenenfalls kovalent gebundene Sulfonat- oder Carboxylat-substituierte
und somit negativ geladenen Reste erfolgt, benötigen die leitfähigen Polymere
Anionen als Gegenionen.
-
Den
Mischungen können
daher Gegenionen zugesetzt werden. Dies können monomere oder polymere
Anionen, letztere im Folgenden als Polyanionen bezeichnet, sein.
-
Als
Polyanionen dienen vorzugsweise die Anionen von polymeren Carbonsäuren, wie
Polyacrylsäuren,
Polymethacrylsäure
oder Polymaleinsäuren,
oder die Anionen von polymeren Sulfonsäuren, wie Polystyrolsulfonsäuren und
Polyvinylsulfonsäuren.
Diese Polycarbon- und -sulfonsäuren
können
auch Copolymere von Vinylcarbon- und
Vinylsulfonsäuren
mit anderen polymerisierbaren Monomeren, wie Acrylsäureestern
und Styrol, sein.
-
Besonders
bevorzugt ist das Anion der Polystyrolsulfonsäure als Gegenion.
-
Das
Molekulargewicht der die Polyanionen liefernden Polysäuren beträgt vorzugsweise
1 000 bis 2 000 000, besonders bevorzugt 2 000 bis 500 000. Die
Polysäuren
oder ihre Alkalisalze sind im Handel erhältlich, z.B. Polystyrolsulfonsäuren und
Polyacrylsäuren,
oder aber nach bekannten Verfahren herstellbar (siehe z.B. Houben
Weyl, Methoden der organischen Chemie, Bd. E 20 Makromolekulare
Stoffe, Teil 2, (1987), S. 1141 u.f.).
-
Als
monomere Anionen dienen beispielsweise solche von C1-C20-Alkansulfonsäuren, wie der Methan-, Ethan-,
Propan-, Butan- oder höherer
Sulfonsäuren
wie der Dodecansulfonsäure,
von aliphatischen Perfluorsulfonsäuren, wie der Trifluormethansulfonsäure, der
Perfluorbutansulfonsäure
oder der Perfluoroctansulfonsäure,
von aliphatischen C1-C20-Carbonsäuren wie
der 2-Ethylhexylcarbonsäure,
von aliphatischen Perfluorcarbonsäuren, wie der Trifluoressigsäure oder
der Perfluoroctansäure,
und von aromatischen, gegebenenfalls durch C1-C20-Alkylgruppen substituierten Sulfonsäuren wie
der Benzolsulfonsäure,
o-Toluolsulfonsäure,
p-Toluol-sulfonsäure oder
der Dodecylbenzolsulfonsäure
und von Cycloalkansulfonsäuren
wie Camphersulfonsäure
oder Tetrafluoroborate, Hexafluorophosphate, Perchlorate, Hexafluoroantimonate,
Hexafluoroarsenate oder Hexachloroantimonate.
-
Bevorzugt
sind die Anionen der p-Toluolsulfonsäure, Methansulfonsäure oder
Camphersulfonsäure.
-
Die
Gegenionen werden den Mischungen beispielsweise in Form ihrer Alkalisalze
oder als freie Säuren
zugegeben.
-
Bevorzugt
dienen die vorhandenen Anionen des verwendeten Oxidationsmittels
als Gegenionen, so dass eine Zugabe zusätzlicher Gegenionen nicht zwingend
erforderlich ist.
-
Den
erfindungsgemäßen Mischungen
können
außerdem
weitere Komponenten wie ein oder mehrere in organischen Lösungsmitteln
lösliche
organische Binder wie Polyvinylacetat, Polycarbonat, Polyvinylbutyrat, Polyacrylsäureester,
Polymethacrylsäureester,
Polystyrol, Polyacrylonitril, Polyvinylchlorid, Polybutadien, Polyisopren,
Polyether, Polyester, Silicone, Pyrrol/Acrylsäureester-, Vinylacetat/Acrylsäureester- und Ethylen/Vinylacetat-Copolymerisate
oder wasserlösliche
Binder wie Polyvinylalkohole, Vernetzer wie Polyurethane bzw. Polyurethandispersionen,
Polyacrylate, Polyolefindispersionen, Epoxysilane, wie 3-Glycidoxypropyltrialkoxysilan,
und Additive wie z.B. oberflächenaktive
Stoffe zugesetzt werden. Weiterhin können Alkoxysilanhydrolysate
z.B. auf Basis von Tetraethoxysilan zur Erhöhung der Kratzfestigkeit bei
Beschichtungen zugesetzt werden.
-
Für die oxidative
Polymerisation der Vorstufen für
die Herstellung leitfähiger
Polymere werden theoretisch je Mol Thiophen 2,25 Äquivalente
Oxidationsmittel benötigt
(siehe z.B. J. Polym. Sc. Part A Polymer Chemistry Vol. 26, S. 1287
(1988)). Es können
aber auch niedrigere oder höhere Äquivalente
an Oxidationsmittel eingesetzt werden.
-
Die
Mischungen enthalten vorzugsweise 1 bis 30 Gew.-% der Vorstufen
für die
Herstellung leitfähiger Polymere
und 0 bis 50 Gew.-% Bindemittel, Vernetzer und/oder Additive, beide
Gewichtsprozente bezogen auf das Gesamtgewicht der Mischung.
-
Mit
den erfindungsgemäßen Mischungen
lassen sich Elektrolytkondensatoren herstellen. Prinzipiell wird
ein Elektrolytkondensator hergestellt, indem ein oxidierbares Metall
zunächst
oxidativ, beispielsweise durch elektrochemische Oxidation, mit einem
Dielektrikum, d. h. einer Oxidschicht, überzogen wird. Auf dem Dielektrikum
wird dann mittels oxidativer Polymerisation, erfindungsgemäß mittels
einer der oben beschriebenen Mischungen, chemisch ein leitfähiges Polymer
abgeschieden, welches den Feststoffelektrolyten bildet. Ein Überzug mit
weiteren gut leitfähigen
Schichten, wie Graphit und Silber, dient der Ableitung des Stroms. Schließlich wird
der Kondensatorkörper
kontaktiert und eingekapselt.
-
Das „oxidierbare
Metall" bildet im
erfindungsgemäßen Verfahren
bevorzugt einen Anodenkörper
mit großer
Oberfläche,
z.B. in Form eines porösen
Sinterkörpers
oder einer aufgerauten Folie. Im Folgenden wird dieser auch kurz
als Anodenkörper
bezeichnet.
-
Der
Feststoffelektrolyt aus leitfähigem
Polymer wird erfindungsgemäß auf den
mit einer Oxidschicht bedeckten Anodenkörper durch oxidative Polymerisation
der oben beschriebenen Mischungen erzeugt, indem man auf die Oxidschicht
des Anodenkörpers
diese Mischungen, vorzugsweise in Form von Lösungen, ausbringt und die oxidative
Polymerisation, je nach Aktivität
des verwendeten Oxidationsmittels, gegebenenfalls durch ein Erwärmen der
Beschichtung zu Ende führt.
-
Ebenfalls
Gegenstand der vorliegenden Erfindung ist daher ein Verfahren zur
Herstellung eines Elektrolytkondensators, dadurch gekennzeichnet,
dass die erfindungsgemäßen Mischungen
gegebenenfalls in Form von Lösungen
auf eine Oxidschicht eines Metalls aufgebracht und chemisch oxidativ
bei Temperaturen von –10°C bis 250°C zu den
entsprechenden Polymeren polymerisiert werden.
-
Weiterhin
Gegenstand der vorliegenden Erfindung ist ein Verfahren zur Herstellung
eines Elektrolytkondensators, dadurch gekennzeichnet, dass Vorstufen
für die
Herstellung leitfähiger
Polymere und die erfindungsgemäß erhältlichen
Oxidationsmittel nacheinander, gegebenenfalls in Form von Lösungen,
auf eine Oxidschicht eines Metalls aufgebracht und chemisch oxidativ
bei Temperaturen von –10°C bis 250°C zu den entsprechenden
Polymeren polymerisiert werden.
-
Die
Aufbringung kann direkt oder unter Verwendung eines Haftvermittlers,
beispielsweise eines Silans, und/oder einer anderen funktionellen
Schicht auf die Oxidschicht des Anodenkörpers erfolgen.
-
Die
oxidative chemische Polymerisation der Vorstufen zur Herstellung
leitfähiger
Polymere wird je nach verwendetem Oxidationsmittel und gewünschter
Reaktionszeit im allgemeinen bei Temperaturen von –10°C bis 250°C, bevorzugt
bei Temperaturen von 0°C
bis 200°C,
vorgenommen.
-
Wie
den erfindungsgemäßen Mischungen
können
auch den Lösungen
zusätzlich
Gegenionen zugegeben werden. Geeignete Gegenionen sind die oben
für die
erfindungsgemäßen Mischungen
aufgeführten.
-
Besonders
bevorzugt zur Anwendung in den erfindungsgemäßen Elektrolytkondensatoren
sind die Anionen der monomeren Alkan- oder Cycloalkansulfonsäuren oder
aromatischen Sulfonsäuren,
da diese enthaltende Lösungen
besser geeignet sind, in das poröse
Anodenmaterial einzudringen und somit eine größere Kontaktfläche zwischen
diesem und dem Feststoffelektrolyten gebildet werden kann.
-
Außerdem können zur
Anwendung in den erfindungsgemäßen Elektrolytkondensatoren
bevorzugt als Gegenionen die gegebenenfalls vorhandenen Anionen
des verwendeten Oxidationsmittels dienen, so dass eine Zugabe zusätzlicher
Gegenionen nicht zwingend erforderlich ist.
-
Wie
die erfindungsgemäßen Mischungen
können
auch die Lösungen
zusätzlich
einen oder mehrere Binder, Vernetzer und/oder Additive enthalten.
Geeignete Binder, Vernetzer und/oder Additive sind die oben für die erfindungsgemäßen Mischungen
aufgeführten.
-
Als
Vorstufen für
die Herstellung leitfähiger
Polymere eignen sich die oben bereits aufgeführten.
-
Die
erfindungsgemäßen Mischungen
werden nach bekannten Verfahren, z.B. durch Tränkung, Gießen, Auftropfen, Spritzen,
Aufsprühen,
Aufrakeln, Bestreichen oder Bedrucken auf die Oxidschicht des Anodenkörpers aufgebracht.
-
Das
Entfernen der gegebenenfalls eingesetzten Lösungsmittel nach dem Aufbringen
der Mischungen kann durch einfaches Abdampfen bei Raumtemperatur
erfolgen. Zur Erzielung höherer
Verarbeitungsgeschwindigkeiten ist es jedoch vorteilhafter, die
Lösungsmittel
bei erhöhten
Temperaturen, z.B. bei Temperaturen von 20 bis zu 300°C, bevorzugt
40 bis zu 250°C,
zu entfernen. Eine thermische Nachbehandlung kann unmittelbar mit
dem Entfernen des Lösungsmittel
verbunden oder aber auch in zeitlichem Abstand von der Fertigstellung
der Beschichtung vorgenommen werden.
-
Die
Dauer der Wärmebehandlung
beträgt
in Abhängigkeit
von der Art des für
die Beschichtung verwendeten Polymers 5 Sekunden bis mehrere Stunden.
Für die
thermische Behandlung können
auch Temperaturprofile mit unterschiedlichen Temperaturen und Verweilzeiten
eingesetzt werden.
-
Die
Wärmebehandlung
kann z.B. in der Weise ausgeführt
werden, dass man die beschichteten Anodenkörper mit einer solchen Geschwindigkeit
durch eine auf der gewünschten
Temperatur befindliche Wärmekammer
bewegt, so dass die gewünschte
Verweilzeit bei der gewählten
Temperatur erreicht wird, oder mit einer auf der gewünschten
Temperatur befindlichen Heizplatte für die gewünschte Verweilzeit in Kontakt
bringt. Des Weiteren kann die Wärmebehandlung
beispielsweise in einem Wärmeofen
oder mehreren Wärmeöfen mit jeweils
unterschiedlichen Temperaturen erfolgen.
-
Nach
dem Entfernen der Lösungsmittel
(Trocknen) und gegebenenfalls nach der thermischen Nachbehandlung
kann es vorteilhaft sein, das überschüssige Oxidationsmittel
und Restsalze aus der Beschichtung mit einem geeigneten Lösungsmittel,
bevorzugt Wasser oder Alkoholen, auszuwaschen. Unter Restsalzen sind
hier die Salze der reduzierten Form des Oxidationsmittels und gegebenenfalls
weitere vorhandene Salze zu verstehen.
-
Je
nach Art des Anodenkörpers
kann es vorteilhaft sein, den Anodenkörper bevorzugt nach einer Waschung
weitere Male mit den Mischungen zu imprägnieren, um dickere Polymerschichten
zu erzielen.
-
Nach
der Polymerisation und bevorzugt während oder nach der Waschung
kann es vorteilhaft sein, den Oxidfilm elektrochemisch nachzubilden,
um eventuelle Fehlstellen im Oxidfilm auszubessern und dadurch den
Reststrom des fertigen Kondensators zu senken (Reformierung).
-
Bevorzugt
ist weiterhin ein Verfahren dadurch gekennzeichnet, dass es sich
bei dem oxidierbaren Metall um ein Ventilmetall oder eine Verbindung
mit vergleichbaren Eigenschaften handelt.
-
Als
Ventilmetall sind im Rahmen der Erfindung solche Metalle zu verstehen,
deren Oxidschichten den Stromfluss nicht in beide Richtungen gleichermaßen ermöglichen:
Bei anodisch angelegter Spannung sperren die Oxidschichten der Ventilmetalle
den Stromfluss, während
es bei kathodisch angelegter Spannung zu großen Strömen kommt, die die Oxidschicht
zerstören
können.
Zu den Ventilmetallen zählen
Be, Mg, Al, Ge, Si, Sn, Sb, Bi, Ti, Zr, Hf V, Nb, Ta und W sowie
eine Legierung oder Verbindung von wenigstens einem dieser Metalle
mit anderen Elementen. Die bekanntesten Vertretern der Ventilmetalle
sind Al, Ta und Nb. Verbindungen mit vergleichbaren Eigenschaften
sind solche mit metallischer Leitfähigkeit, welche oxidierbar
sind und deren Oxidschichten die vorangehend beschriebenen Eigenschaften
besitzen. Beispielsweise besitzt NbO metallische Leitfähigkeit,
wird jedoch im allgemeinen nicht als Ventilmetall betrachtet. Schichten
von oxidiertem NbO weisen jedoch die typischen Eigenschaften von
Ventilmetalloxidschichten auf, so dass NbO oder eine Legierung oder
Verbindung von NbO mit anderen Elementen typische Beispiele für solche
Verbindungen mit vergleichbaren Eigenschaften sind.
-
Demzufolge
sind unter dem Begriff „oxidierbares
Metall" nicht nur
Metalle sondern auch eine Legierung oder Verbindung eines Metalls
mit anderen Elementen gemeint, sofern sie metallische Leitfähigkeit
besitzen und oxidierbar sind.
-
Besonders
bevorzugt Gegenstand der vorliegenden Erfindung ist demgemäss ein Verfahren,
dadurch gekennzeichnet, dass es sich bei dem Ventilmetall oder der
Verbindung mit vergleichbaren Eigenschaften um Tantal, Niob, Aluminium,
Titan, Zirkonium, Hafnium, Vanadium, eine Legierung oder Verbindung
von wenigstens einem dieser Metalle mit anderen Elementen, NbO oder
eine Legierung oder Verbindung von NbO mit anderen Elementen handelt.
-
Das „oxidierbare
Metall" bildet im
erfindungsgemäßen Verfahren
bevorzugt einen Anodenkörper
mit großer
Oberfläche,
z.B. in Form eines porösen
Sinterkörpers
oder einer aufgerauten Folie.
-
Allerdings
eignen sich das erfindungsgemäße Verfahren
nicht nur zur Herstellung von Elektrolytkondensatoren, sondern ebenfalls
zur Herstellung leitfähiger
Schichten für
andere Anwendungen.
-
Erfindungsgemäß werden
die Schichten durch ein Verfahren hergestellt, welches durch oxidative
Polymerisation der erfindungsgemäßen Mischungen
die leitfähigen
Schichten liefert.
-
Ebenfalls
Gegenstand der vorliegenden Erfindung ist daher ein Verfahren zur
Herstellung elektrisch leitfähiger
Schichten, dadurch gekennzeichnet, dass die erfindungsgemäßen Mischungen,
vorzugsweise in Form von Lösungen,
auf eine Unterlage aufgebracht und auf dieser Unterlage chemisch
zu leitfähigen
Polymeren bei Temperaturen von –10°C bis 250°C, bevorzugt
bei Temperaturen von 0°C
bis 200°C,
polymerisiert werden.
-
Weiterhin
Gegenstand der vorliegenden Erfindung ist auch ein Verfahren zur
Herstellung leitfähiger Schichten,
dadurch gekennzeichnet, dass Vorstufen für die Herstellung leitfähiger Polymere
und erfindungsgemäß erhältliche
Oxidationsmittel nacheinander, gegebenenfalls in Form von Lösungen,
auf eine Unterlage aufgebracht und auf dieser Unterlage chemisch
oxidativ bei Temperaturen von –10°C bis 250°C zu den
entsprechenden leitfähigen
Polymeren polymerisiert werden.
-
Beispielhafte
und bevorzugte Reaktionsbedingungen, Molverhältnisse, Gewichtsprozentangaben,
Lösungsmittel,
Oxidationsmittel, Vorstufen für
die Herstellung leitfähiger
Polymere sowie im Zusammenhang mit diesen beschriebene Varianten
bzw. Besonderheiten bei der Durchführung der oxidativen Polymerisation
entsprechen dem vorangehend für
die Herstellung der Elektrolytkondensatoren bereits beschriebenen.
-
Für flache
Substrate bietet sich neben den für Kondensatoren geschilderten
Auftragungsmethoden insbesondere auch das Aufschleudern der Mischungen
oder Lösungen
an (Spincoating).
-
Wie
die erfindungsgemäßen Mischungen
können
auch die Lösungen
zusätzlich
einen oder mehrere Binder, Vernetzer und/oder Additive enthalten.
Geeignete Binder, Vernetzer und/oder Additive sind die oben für die erfindungsgemäßen Mischungen
aufgeführten.
-
Wie
den erfindungsgemäßen Mischungen
können
auch den Lösungen
zusätzlich
Gegenionen zugegeben werden. Geeignete Gegenionen sind die oben
für die
erfindungsgemäßen Mischungen
aufgeführten, wobei
für die
Bildung von Polymerfilmen die Polyanionen zu verbesserten Filmbildungseigenschaften
führen können und
daher bevorzugt sind.
-
Die
erfindungsgemäß hergestellten
elektrisch leitfähigen
Schichten können
nach der Polymerisation und gegebenenfalls nach Trocknung – ebenso
wie bei den Elektrolyt kondensatoren beschrieben – mit geeigneten Lösungsmitteln
gewaschen werden, um überschüssiges Oxidationsmittel
und Restsalze zu entfernen.
-
Bei
der Unterlage kann es sich beispielsweise um Glas, Dünstglas
(flexibles Glas) oder Kunststoffe handeln.
-
Besonders
geeignete Kunststoffe sind: Polycarbonate, Polyester wie z.B. PET
und PEN (Polyethylenterephthalat bzw. Polyethylennaphthenat), Copolycarbonate,
Polysulfon, Polyethersulfon, Polyimid, Polyethylen, Polypropylen
oder cyclische Polyolefine bzw. cyclische Olefincopolymere (COC),
hydrierte Styrolpolymere oder hydrierte Styrolcopolymere.
-
Geeignete
Polymerunterlagen können
beispielsweise Folien wie Polyesterfolien, PES-Folien der Firma
Sumitomo oder Polycarbonatfolien der Firma Bayer AG (Makrofol®)
sein.
-
Die
erfindungsgemäß hergestellten
leitfähigen
Schichten können
auf der Unterlage verbleiben oder von dieser abgelöst werden.
-
Die
Polythiophenschichten besitzen je nach Anwendung eine Dicke von
1 nm bis 100 μm,
bevorzugt 10 nm bis 10 μm,
besonders bevorzugt 50 nm bis 1 μm.
-
Die
erfindungsgemäß hergestellten
Schichten eignen sich hervorragend für die Verwendung als antistatische
Beschichtung, als transparente Heizung, als gegebenenfalls transparente
Elektroden, als lochinjizierende oder lochleitende Schichten in
organischen Leuchtdioden, zur Durchkontaktierung von Leiterplatten oder
als Feststoffelektrolyt in Elektrolytkondensatoren. Sie können vorteilhafterweise
transparent sein.
-
Als
antistatische Beschichtungen können
sie beispielsweise auf Filmen, Verpackungen elektronischer Bauteile,
zur Ausrüstung
von Kunststofffolien sowie zur Bildschirmbeschichtung eingesetzt
werde. Weiterhin können
sie als Kathodenmaterialien in Kondensatoren, als transparente Elektroden
z.B. in Displays, beispielsweise als Ersatz für Indium-Zinn-Oxid-Elektroden,
oder als elektrische Leiter in polymerer Elektronik verwendet werden.
Weitere Einsatzmöglichkeiten
bieten Sensoren, Batterien, Solarzellen, elektrochrome Fenster (smart windows)
und Displays sowie der Korrosionsschutz.
-
Weiterhin
Gegenstand der vorliegenden Erfindung ist die Verwendung der erfindungsgemäßen bzw. nach
dem erfindungsgemäßen Verfahren
hergestellten Oxidationsmittel sowie der erfindungsgemäßen Mischungen
zur Herstellung leitfähiger
Schichten und Elektrolytkondensatoren.
-
Die
im Folgenden aufgeführten
Beispiele sind nicht als Beschränkung
aufzufassen.
-
Beispiele
-
Beispiel 1:
-
a) Herstellung einer Lösung eines
erfindungsgemäßen Oxidationsmittels
-
In
einem Volumenmessgefäß wurden
separat zwei Volumenteile einer 40 gew.-%igen Lösung von Eisen(III)-p-toluolsulfonat
in Ethanol und ein Volumenteil des schwach basischen, makroporösen Anionenaustauschers
Lewatit® MP
62 (Bayer AG) abgemessen. Die Abmessung des festen Anionenaustauschers
erfolgte über
eine einfache Schüttung
(auf diese Weise wurden auch die Volumenteile der festen Anionentauscher
in den folgenden Beispielen abgemessen). Die abgemessenen Volumina
an ethanolischer Lösung
von Eisen(III)-p-toluolsulfonat und an Anionentauscher wurden anschließend in
einem geschlossenen Behälter
für 24
Stunden mit einem Schüttler
gemischt. Danach wurde der Anionentauscher abfiltriert.
-
b) Herstellung einer erfindungsgemäßen Mischung
aus Oxidationsmittel und Vorstufen
-
1
Gewichtsteil 3,4-Ethylendioxythiophen (BAYTRON® M,
H.C. Starck GmbH) und 20 Gewichtsteile der wie unter a) beschrieben
hergestellten Lösung
des erfindungsgemäßen Oxidationsmittels
wurden unter Rühren
gemischt und die resultierende Mischung in einem Kühlschrank
bei ca. 6°C
gelagert. In regelmäßigen Abständen wurde
ein dünner
Lösungsfilm
der erfindungsgemäßen Mischung
mit einer Lampe durchschienen und mit dem Auge auf Feststoffpartikel
untersucht. Die Zeitspanne zwischen dem Ansetzen der Mischung und
dem Zeitpunkt, zu dem die ersten Partikel sichtbar wurden, wurde
als Topfzeit definiert.
-
Es
ergab sich eine Topfzeit von 24 Stunden.
-
Beispiel 2:
-
Einer
40 gew.-%igen Lösung
von Eisen(III)-p-toluolsulfonat in Ethanol wurden analog zu Beispiel
1 verschiedene Mengen an Anionenaustauscher zugesetzt und anschließend die
Topfzeit in Mischungen mit 3,4-Ethylendioxythiophen bestimmt.
-
a) Herstellung von Lösungen erfindungsgemäßer Oxidationsmitteln
-
Dazu
wurde eine 40 gew.-%ige ethanolische Lösung von Eisen(III)-p-toluolsulfonat
im Volumenverhältnis
9:1, 3:1 und 2:1 mit dem schwach basischen, makroporösen Anionenaustauscher
Lewatit® MP
62 (Bayer AG) jeweils für
7 Stunden mit einem Schüttler
gemischt, und anschließend
wurde der Anionentauscher abfiltriert.
-
b) Herstellung von erfindungsgemäßen Mischungen
aus Oxidationsmittel und Vorstufen
-
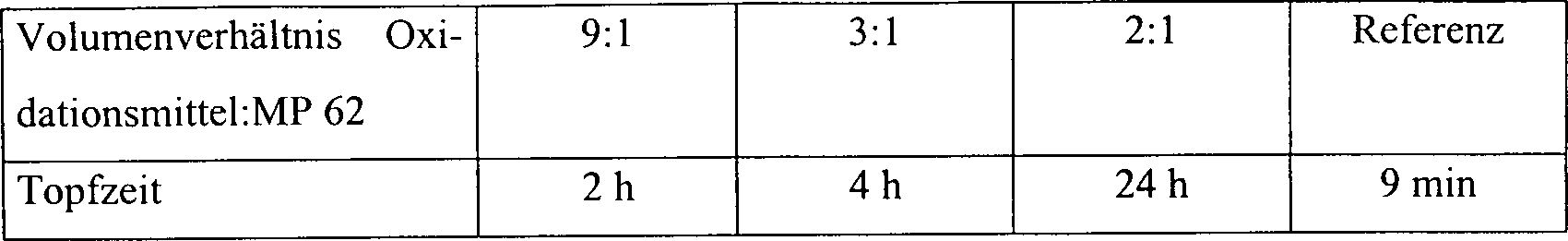
Es
wurde eine Mischung bestehend aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M, H.C.
Starck GmbH) und 20 Gewichtsteilen der wie unter a) beschrieben
hergestellten Lösungen
der erfindungsgemäßen Oxidationsmittel
hergestellt und die jeweilige Mischung in einem Kühlschrank
bei ca. 6°C
gelagert. Die Bestimmung der Topfzeit erfolgte wie in Beispiel 1.
-
c) Herstellung einer nicht-erfindungsgemäßen Vergleichsmischung
aus nicht mit einem Ionenaustauscher behandeltem Oxidationsmittel
und Vorstufen
-
Als
Vergleich wurde eine Mischung aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M, H.C.
Starck GmbH) und 20 Gewichtsteilen nicht mit einem Ionenaustauscher
behandelter 40 gew.-%iger ethanolischer Lösung von Eisen(III)-p-toluolsulfonat
hergestellt, diese bei ca. 6°C
gelagert und entsprechend dem obigen Verfahren ebenfalls untersucht
(Referenz).
-
Es
ergaben sich folgende Messwerte:
-
Die
erfindungsgemäßen Mischungen
haben eine deutlich höhere
Topfzeit als die Mischung mit nicht mit einem Ionenaustauscher behandeltem
Eisen(III)-p-toluolsulfonat.
-
Beispiel 3:
-
Zur
Bestimmung der Leitfähigkeit
von Polymerfilmen, die aus den erfindungsgemäßen Mischungen erzeugt wurden,
wurden Filme aus den Mischungen aufgeschleudert und anschließend polymerisiert.
-
a) Herstellung einer Lösung eines
erfindungsgemäßen Oxidationsmittels
-
Dazu
wurde analog zu Beispiel 1 eine 40 gew.-%ige butanolische Lösung von
Eisen(III)-p-toluolsulfonat im Volumenverhältnis 2:1 mit dem schwach basischen,
makroporösen
Anionenaustauscher Lewatit® MP 62 (Bayer AG) gemischt
und die Mischung für
64 h ruhen gelassen. Anschließend
wurde der Anionentauscher abfiltriert.
-
b) Herstellung einer erfindungsgemäßen Mischung
aus Oxidationsmittel und Vorstufen sowie einer leitfähigen Beschichtung
-
Es
wurde eine Mischung bestehend aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M, H.C.
Starck GmbH) und 20 Gewichtsteilen der wie unter a) beschrieben
hergestellten Lösung
des erfindungsgemäßen Oxidationsmittels
hergestellt und ein Teil dieser Mischung auf einen Glasobjektträger (26
mm·26 mm·1 mm)
mittels eines Spincoaters (Chemat Technology KW-4A) bei 2000 U/min
für 5 Sekunden
aufgeschleudert. Die Probe wurde 60 min bei 20°C getrocknet und anschließend 15
min in einer Glasschale mit Methanol gewaschen. Danach wurde die
Probe für
15 min bei 50°C
getrocknet und anschließend über eine Vier-Punkt-Messung
mit einem Keithley 199 Multimeter der Oberflächenwiderstand ermittelt. Die
Schichtdicke wurde mit einem Tencor Alpha Step 500 Surface Profiler
bestimmt. Aus Oberflächenwiderstand
und Schichtdicke wurde die spezifische Leitfähigkeit ermittelt. Der Rest
der Mischung wurde in einem Kühlschrank
bei ca. 6°C
gelagert und an dieser, wie in Beispiel 1 beschrieben, die Topfzeit
bestimmt.
-
c) Herstellung einer nicht-erfindungsgemäßen Vergleichsmischung
aus nicht mit einem Ionenaustauscher behandeltem Oxidationsmittel
und Vorstufen
-
Als
Vergleich wurde eine Mischung aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M, H.C.
Starck GmbH) und 20 Gewichtsteilen nicht mit einem Ionenaustauscher
behandelter 40 gew.-%iger butanolischer Lösung von Eisen(III)-p-toluolsulfonat
hergestellt, diese bei 6°C
gelagert und entsprechend den obigen Verfahren ebenfalls untersucht
(Referenz).
-
Es
ergaben sich folgende Messwerte:
-
Die
erfindungsgemäße Mischung
hat eine deutlich höhere
Topfzeit als die Mischung mit nicht mit einem Ionenaustauscher behandeltem
Oxidationsmittel. Gleichzeitig ist die Leitfähigkeit der Schicht wesentlich größer und
der Oberflächenwiderstand
wesentlich niedriger als bei der Probe, die aus der Referenzmischung hergestellt
wurde.
-
Beispiel 4:
-
Es
wurde die Topfzeit einer erfindungsgemäßen Mischung im Vergleich zu
einer Mischung aus nicht mit einem Ionenaustauscher behandeltem
Metallsalz mit Basenzusatz bestimmt.
-
a) Herstellung einer Lösung eines
erfindungsgemäßen Oxidationsmittels
-
Dazu
wurde analog zu Beispiel 1 eine 40 gew.-%ige butanolische Lösung von
Eisen(III)-p-toluolsulfonat im Volumenverhältnis 2:1 mit dem schwach basischen,
makroporösen
Anionenaustauscher Lewatit® MP 62 (Bayer AG) gemischt
und die Mischung für
64 h ruhen gelassen. Anschließend
wurde der Anionentauscher abfiltriert.
-
b) Herstellung einer erfindungsgemäßen Mischung
aus Oxidationsmittel und Vorstufen
-
Es
wurde eine Mischung, bestehend aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M,
H.C. Starck GmbH) und 20 Gewichtsteilen der wie unter a) beschrieben
hergestellten Lösung
des erfindungsgemäßen Oxidationsmittels
hergestellt. Die Mischung wurde in einem Kühlschrank bei ca. 6°C gelagert und
an dieser, wie in Beispiel 1 beschrieben, die Topfzeit bestimmt.
-
c) Herstellung einer nicht-erfindungsgemäßen Vergleichsmischung
aus nicht mit einem Ionenaustauscher behandeltem Oxidationsmittel
und Vorstufen
-
Als
Vergleich wurde eine Mischung aus einem Gewichtsteil 3,4-Ethylendioxythiophen,
(BAYTRON® M, H.C.
Starck GmbH) 20 Gewichtsteilen nicht mit einem Ionenaustauscher
behandelter 40 gew.-%iger butanolischer Lösung von Eisen(III)-p-toluolsulfonat
und 0.75 Gewichtsteilen Imidazol hergestellt, diese bei 6°C gelagert
und entsprechend den obigen Verfahren ebenfalls untersucht (Referenz).
-
Es
ergaben sich folgende Topfzeiten:
-
Aus
beiden obigen Mischungen ließen
sich durch Aufbringen der Mischung auf einer Glasplatte und Trocknen
bei 60°C
Polymerfilme herstellen. Für
Referenz-Mischungen mit größeren Zusätzen an
Imidazol ließen
sich jedoch auch bei Temperaturen von 150°C keine Polymerfilme mehr herstellen.
-
Die
erfindungsgemäße Mischung
hat eine deutlich höhere
Topfzeit als die Mischung mit nicht mit einem Ionenaustauscher behandeltem
Oxidationsmittel und Zusatz der Base Imidazol.
-
Beispiel 5:
-
Es
wurde die Topfzeit einer erfindungsgemäßen Mischung, die zwei unterschiedlich
hergestellten erfindungsgemäße Oxidationsmittel
enthält,
bestimmt.
-
a) Herstellung zweier
Lösungen
erfindungsgemäßer Oxidationsmittels
-
Dazu
wurde analog zu Beispiel 1 eine 40 gew.-%ige ethanolische Lösung von
Eisen(III)-p-toluolsulfonat im Volumenverhältnis 1:1 mit dem schwach basischen,
makroporösen
Anionenaustauscher Lewatit® MP 62 (Bayer AG) für 7 Stunden
mit einem Schüttler
gemischt, und anschließend
wurde der Anionentauscher abfiltriert (Lösung 1).
-
Eine
zweite Lösung
wurde analog hergestellt, indem eine 40 gew.-%ige ethanolische Lösung von
Eisen(III) p-toluolsulfonat im Volumenverhältnis 2:1 mit dem schwach basischen,
makroporösen
Anionenaustauscher Lewatit® MP 62 (Bayer AG) für 7 Stunden
mit einem Schüttler
gemischt, und anschließend
der Anionentauscher abfiltriert wurde (Lösung 2).
-
b) Herstellung einer erfindungsgemäßen Mischung
aus Oxidationsmittel und Vorstufen
-
Es
wurde eine erfindungsgemäße Mischung
bestehend aus einem Gewichtsteil 3,4-Ethylendioxythiophen (BAYTRON® M,
H.C. Starck GmbH), 10 Gewichtsteilen von Lösung 1 und 10 Gewichtsteilen
von Lösung 2
hergestellt und die Mischung in einem Kühlschrank bei ca. 6°C gelagert.
Die Topfzeit wurde analog zu Beispiel 1 bestimmt.
-
Es
ergab sich eine Topfzeit von 96 Stunden.
-
-
Wie
dieses Beispiel zeigt, lässt
sich die Topfzeit auch durch Mischung von unterschiedlich hergestellten
erfindungsgemäßen Oxidationsmitteln
einstellen.
-
Beispiel 6:
-
Es
wurde die Topfzeit einer erfindungsgemäßen Mischung bei einer Lagerung
bei tiefer Temperatur bestimmt.
-
a) Herstellung einer Lösung eines
erfindungsgemäßen Oxidationsmittels
-
Dazu
wurde analog zu Beispiel 1 eine 40 gew.-%ige ethanolische Lösung von
Eisen(III)-p-toluolsulfonat im Volumenverhältnis 2:1 mit dem schwach basischen,
makroporösen
Anionenaustauscher Lewatit® MP 62 (Bayer AG) für 7 Stunden
mit einem Schüttler
gemischt, und anschließend
wurde der Anionentauscher abfiltriert.
-
b) Herstellung einer erfindungsgemäßen Mischung
aus Oxidationsmittel und Vorstufen
-
Es
wurde eine Mischung, bestehend aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M,
H.C. Starck GmbH) und 20 Gewichtsteilen der wie unter a) beschrieben
hergestellten Lösung
des erfindungsgemäßen Oxidationsmittels
hergestellt und die Mischung in einem Gefrierschrank ca. –15°C gelagert. Die
Mischung blieb bei dieser Temperatur flüssig. Die Topfzeit wurde wie
in Beispiel 1 bestimmt.
-
c) Herstellung einer nicht-erfindungsgemäßen Vergleichsmischung
aus nicht mit einem Ionenaustauscher behandeltem Oxidationsmittel
und Vorstufen
-
Als
Vergleich wurde eine Mischung aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M, H.C.
Starck GmbH) und 20 Gewichtsteilen nicht mit einem Ionenaustauscher
behandelter 40 gew.-%iger ethanolischer Lösung von Eisen(III)-p-toluolsulfonat
hergestellt, diese bei –15°C gelagert
und entsprechend den obigen Verfahren ebenfalls untersucht (Referenz).
-
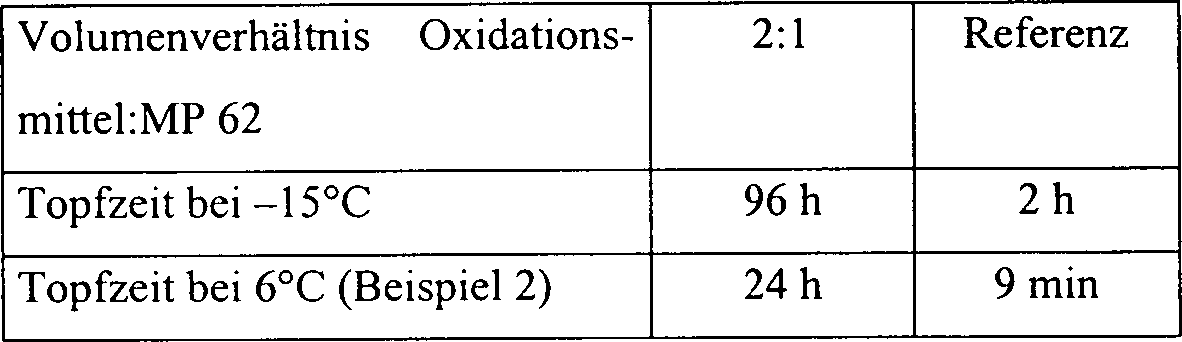
Es
ergaben sich folgende Messwerte (als Vergleich sind die entsprechenden
Topfzeiten bei einer Lagerung bei 6°C aus Beispiel 2 mit aufgeführt):
-
Wie
der Vergleich der Topfzeiten bei unterschiedlicher Lagertemperatur
zeigt, kann die Topfzeit durch Kühlung
auf tiefe Temperaturen sowohl für
die erfindungsgemäße Mischung
als auch für
die Referenz deutlich erhöht
werden. Die erfindungsgemäßen Mischungen
haben aber auch bei tiefen Temperaturen weit längere Topfzeiten als Mischungen,
die nicht mit einem Ionenaustauscher behandeltes Eisen(III)-p-toluolsulfonat
enthalten.
-
Beispiel 7:
-
Es
wurden die Topfzeiten von erfindungsgemäßen Mischungen bestimmt, die
erfindungsgemäße Oxidationsmittel
enthalten, welche mit unterschiedlichen Anionenaustauschern hergestellt
wurden.
-
a) Herstellung von Lösungen der
erfindungsgemäßen Oxidationsmittel
-
Dazu
wurde analog zu Beispiel 1 eine 40 gew.-%ige butanolische Lösung von
Eisen(III)-p-toluolsulfonat im Volumenverhältnis 2:1 mit dem schwach basischen,
makroporösen
Anionenaustauscher Lewatit® MP 62 (Bayer AG) gemischt
und die Mischung für
24 Stunden ruhen gelassen. Anschließend wurde der Anionentauscher
abfiltriert. Analog wurden erfindungsgemäße Oxidationsmittel durch Behandlung
der Eisen(III)-p-toluolsulfonat-Lösung mit dem mittelbasischen,
makroporösen
Anionenaustauscher Lewatit® MP 64 (Bayer AG) oder
dem starkbasischen, makroporösen
Anionenaustauscher Lewatit® MP 600 WS (Bayer AG)
hergestellt.
-
b) Herstellung der erfindungsgemäßen Mischungen
aus Oxidationsmittel und Vorstufen
-
Es
wurde eine Mischung, bestehend aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M,
H.C. Starck GmbH) und 20 Gewichtsteilen der wie unter a) beschrieben
hergestellten Lösung
des erfindungsgemäßen Oxidationsmittels
hergestellt und die Mischung in einem Kühlschrank bei ca. 6°C gelagert.
Die Topfzeit wurde wie in Beispiel 1 bestimmt.
-
Analog
wurden Mischungen mit den durch die gleiche Behandlung mit dem mittelbasischen,
makroporösen
Anionenaustauscher Lewatit® MP 64 (Bayer AG) oder
dem starkbasischen, makroporösen
Anionenaustauscher Lewatit® MP 600 WS (Bayer AG)
wie unter a) beschrieben hergestellten Lösungen hergestellt, bei 6°C gelagert
und die Proben ebenfalls analog untersucht.
-
c) Herstellung einer nicht-erfindungsgemäßen Vergleichsmischung
aus nicht mit einem Ionenaustauscher behandeltem Oxidationsmittel
und Vorstufen
-
Als
Vergleich wurde eine Mischung aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M, H.C.
Starck GmbH) und 20 Gewichtsteilen nicht mit einem Ionenaustauscher
behandelter 40 gew.-%iger butanolischer Lösung von Eisen(III)-p-toluolsulfonat
hergestellt, bei 6°C
gelagert und entsprechend den obigen Verfahren ebenfalls untersucht
(Referenz).
-
Es
ergaben sich folgende Messwerte:
-
Beispiel 8:
-
Es
wurde eine Lösung
eines erfindungsgemäßen Oxidationsmittel
mit niedrigem Wassergehalt und hoher Lagerstabilität hergestellt.
-
a) Herstellung einer Lösung eines
erfindungsgemäßen Oxidationsmittels
mit niedrigem Wassergehalt
-
Dazu
wurde 1 l des schwach basischen, makroporösen Anionenaustauschers Lewatit® MP
62 (Bayer AG) mit 2 l absolutem Ethanol versetzt und 6 Stunden gerührt. Anschließend wurde
das Austauscherharz über ein
Sieb abgetrennt und noch dreimal wie beschrieben konditioniert.
-
Anschließend wurde
analog zu Beispiel 1 eine 40 gew.-%ige ethanolische Lösung von
Eisen(III)-p-toluolsulfonat im Volumenverhältnis 2:1 (bezogen auf das
Volumen des Ionenaustauschers vor der Behandlung mit Ethanol) mit
dem schwach basischen, makroporösen
Anionenaustauscher Lewatit® MP 62 (Bayer AG) für 7 Stunden
mit einem Schüttler
gemischt, und anschließend
wurde der Anionentauscher abfiltriert.
-
b) Herstellung einer Lösung eines
erfindungsgemäßen Oxidationsmittel
ohne Vorbehandlung des Ionenaustauschers
-
Analog
zu Beispiel 1 wurde eine 40 gew.-%ige ethanolische Lösung von
Eisen(III)-p-toluolsulfonat
im Volumenverhältnis
2:1 mit dem schwach basischen, makroporösen Anionenaustauscher Lewatit® MP
62 (Bayer AG) für
7 Stunden mit einem Schüttler
gemischt, und anschließend
wurde der Anionentauscher abfiltriert.
-
Die
Lösung
des erfindungsgemäßen Oxidationsmittels
nach Herstellung a) hatte einen Wassergehalt von 1,1 Gew.-% bezogen
auf das Gesamtgewicht der Lösung
und die Lösung
zeigte nach drei Monaten Lagerung an Raumtemperatur (20°C) keine
Ausfällungen.
-
Die
Lösung
des erfindungsgemäßen Oxidationsmittels
nach Herstellung b) hatte einen Wassergehalt von 12,8 Gew.-% bezogen
auf das Gesamtgewicht der Lösung.
Die Lösung
zeigte bei Lagerung an Raumtemperatur nach einer Woche Ausfällungen,
bei Lagerung bei ca. 6°C
im Kühlschrank
kam es nach zwei Monaten zu Ausfällungen.
-
Beispiel 9:
-
Es
wurde die Topfzeit einer erfindungsgemäßen Mischung enthaltend ein
erfindungsgemäßes Oxidationsmittels
mit niedrigem Wassergehalt bestimmt.
-
a) Herstellung einer erfindungsgemäßen Mischung
aus Oxidationsmittel und Vorstufen
-
Es
wurde eine Mischung, bestehend aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M,
H.C. Starck GmbH) und 20 Gewichtsteilen der wie unter Beispiel 8a)
beschrieben hergestellten Lösung
des erfindungsgemäßen Oxidationsmittels
hergestellt. Die Mischung wurde in einem Kühlschrank bei ca. 6°C gelagert
und an dieser, wie in Beispiel 1 beschrieben, die Topfzeit bestimmt.
-
b) Herstellung einer erfindungsgemäßen Mischung
aus Oxidationsmittel und Vorstufen mit Wasserzusatz
-
Es
wurde eine Mischung, bestehend aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M,
H.C. Starck GmbH), 20 Gewichtsteilen der wie unter Beispiel 8a)
beschrieben hergestellten Lösung
des erfindungsgemäßen Oxidationsmittels
und 2 Teilen Wasser hergestellt. Die Mischung wurde in einem Kühlschrank
bei ca. 6°C
gelagert und an dieser, wie in Beispiel 1 beschrieben, die Topfzeit
bestimmt.
-
Die
erfindungsgemäße Mischung
aus a) hatte eine Topfzeit von 2,5 Stunden, die erfindungsgemäße Mischung
aus b) eine Topfzeit von 30 Stunden.
-
Beispiel 10:
-
Herstellung von Kondensatoren
unter Verwendung der erfindungsgemäßen Oxidationsmittel
-
Tantalpulver
mit einer spezifischen Kapazität
von 50 000 μFV/g
wurde zu Pellets gepresst und gesintert, um einen porösen, zylindrischen
Körper
mit den Abmessungen 2,5 mm Durchmesser und 1,9 mm Höhe zu bilden.
Die Pellets (Anoden) wurden in einem Phosphorsäureelektrolyten auf 30 V anodisiert.
-
Eine
40 gew.-%ige ethanolische Lösung
von Eisen(III)-p-toluolsulfonat wurde analog zu Beispiel 1 im Volumenverhältnis 2:1
mit dem schwach basischen, makroporösen Anionenaustauscher Lewatit® MP
62 (Bayer AG) für
7 Stunden mit einem Schüttler
gemischt, und anschließend
wurde der Anionentauscher abfiltriert.
-
Es
wurde eine Mischung, bestehend aus einem Gewichtsteil 3,4-Ethylendioxythiophen
(BAYTRON® M,
H.C. Starck GmbH) und 20 Gewichtsteilen der wie unter a) beschrieben
hergestellten Lösung
des erfindungsgemäßen Oxidationsmittels
hergestellt.
-
Die
erfindungsgemäße Mischung
wurde zur Imprägnierung
der Anodenpellets verwendet. Die Anodenpellets wurden in dieser
Mischung getränkt
und anschließend
für 15
min bei Zimmertemperatur, 15 min bei 50°C und 15 min bei 150°C getrocknet.
Nach der Temperaturbehandlung war die Mischung in den Pellets polymerisiert.
Anschließend
wurden die Pellets in Methanol 30 min lang gewaschen. Die beschriebene
Tränkung und
Waschung wurde noch zwei weitere Male durchgeführt. Abschließend wurden
die Pellets mit einer Graphit- und einer Silberschicht überzogen.
-
Das
gleiche Verfahren wurde mit derselben erfindungsgemäßen Mischung
an neuen Pellets durchgeführt,
nachdem die Mischung 24 Stunden alt war und während dieser Zeit bei 6°C gelagert
worden war.
-
Nachdem
die erfindungsgemäße Mischung
72 Stunden alt war und während
dieser Zeit bei 6°C
gelagert worden war, wurde diese filtriert und das Verfahren an
neuen Pellets erneut durchgeführt.
-
Die
Kondensatoren hatten folgende elektrischen Werte:
-
Die
Kapazität
wurde bei 120 Hz und der äquivalente
Serienwiderstand bei 100 kHz mittels eines LCR Meters (Agilent 4284A)
bestimmt. Es zeigen sich keine signifikanten Unterschiede in den
elektrischen Werten.