-
Die vorliegende Erfindung betrifft flüssigkristalline Medien (FK-Medien) mit negativer oder positiver dielektrischer Anisotropie enthaltend selbstausrichtende Additive, die eine homöotrope (vertikale) Ausrichtung der FK-Medien an einer Oberfläche oder den Zellwänden einer Flüssigkristallanzeige (FK-Anzeige) bewirken. Die Erfindung umfasst daher auch FK-Anzeigen mit homöotroper Ausrichtung des flüssigkristallinen Mediums (FK-Medium) ohne konventionelle Imid-Orientierungsschichten. Die FK-Medien sind optional durch eine polymerisierbare oder polymerisierte Komponente ergänzt, die zur Stabilisierung der Ausrichtung, zur Justierung des Tiltwinkels und/oder als Passivierungsschicht dient.
-
Das Prinzip der elektrisch kontrollierten Doppelbrechung, der ECB-Effekt (electrically controlled birefringence) oder auch DAP-Effekt (Deformation aufgerichteter Phasen) wurde erstmals 1971 beschrieben (
M. F. Schieckel und K. Fahrenschon, "Deformation of nematic liquid crystals with vertical orientation in electrical fields", Appl. Phys. Lett. 19 (1971), 3912). Es folgten Arbeiten von
J. F. Kahn (Appl. Phys. Lett. 20 (1972), 1193) und
G. Labrunie und J. Robert (J. Appl. Phys. 44 (1973), 4869).
-
Die Arbeiten von J. Robert und F. Clerc (SID 80 Digest Techn. Papers (1980), 30), J. Duchene (Displays 7 (1986), 3) und H. Schad (SID 82 Digest Techn. Papers (1982), 244) haben gezeigt, dass flüssigkristalline Phasen hohe Werte für das Verhältnis der elastischen Konstanten K3/K1, hohe Werte für die optische Anisotropie An und Werte für die dielektrische Anisotropie von Δε ≤ –0,5 aufweisen müssen, um für hochinformative Anzeigeelemente basierend auf dem ECB-Effekt eingesetzt werden zu können. Auf dem ECB-Effekt basierende elektrooptische Anzeigeelemente weisen eine homöotrope Randorientierung auf (VA-Technologie = Vertical Alignment).
-
Anzeigen, die den ECB-Effekt verwenden, haben sich als sogenannte VAN-(Vertically Aligned Nematic) Anzeigen beispielsweise in den Bauformen MVA-(Multi-Domain Vertical Alignment, z. B.:
Yoshide, H. et al., Vortrag 3.1: "MVA LCD for Notebook or Mobile PCs ...", SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch I, S. 6 bis 9 und
Liu, C. T. et al., Vortrag 15.1: "A 46-inch TFT-LCD HDTV Technology ...", SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch II, S. 750 bis 753), PVA-(Patterned Vertical Alignment, z. B.:
Kim, Sang Soo, Vortrag 15.4: "Super PVA Sets New State-of-the-Art for LCD-TV", SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch II, S. 760 bis 763), ASV-(Advanced Super View, z. B.:
Shigeta, Mitzuhiro und Fukuoka, Hirofumi, Vortrag 15.2: "Development of High Quality LCDTV", SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch II, S. 754 bis 757) Anzeigen, neben IPS-(In Plane Switching) (z. B.:
Yeo, S. D., Vortrag 15.3: "A LC Display for the TV Application", SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch II, S. 758 & 759) und den lange bekannten TN-(Twisted Nematic) Anzeigen, als eine der drei zur Zeit wichtigsten neueren Typen von Flüssigkristallanzeigen, insbesondere für Fernsehanwendungen, etabliert. in allgemeiner Form werden die Technologien z. B. in
Souk, Jun, SIDSeminar 2004, Seminar M-6: "Recent Advances in LCD Technology", Seminar Lecture Notes, M-6/1 bis M-6/26 und
Miller, Ian, SIDSeminar 2004, Seminar M-7: "LCD-Television", Seminar Lecture Notes, M-7/1 bis M-7/32, verglichen. Obwohl die Schaltzeiten moderner ECB-Anzeigen durch Ansteuerungsmethoden mit Übersteuerung (overdrive) bereits deutlich verbessert wurden, z. B.:
Kim, Hyeon Kyeong et al., Vortrag 9.1: "A 57-in. Wide UXGA TFT-LCD for HDTV Application", SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch I, S. 106 bis 109, ist die Erzielung von videotauglichen Schaltzeiten, insbesondere beim Schalten von Graustufen, immer noch ein nicht zufriedenstellend gelöstes Problem.
-
Mit der Erzeugung der VA-Displays mit zwei oder mehr Domänen unterschiedlicher Vorzugsrichtung ist ein beträchtlicher Aufwand verbunden. Ein Ziel dieser Erfindung ist es, die Herstellprozesse und die Anzeigevorrichtungen selbst zu vereinfachen, ohne die Vorteile der VA-Technik, wie relativ schnelle Schaltzeiten und gute Blickwinkelabhängigkeit, aufzugeben.
-
VA-Anzeigen die FK-Medien mit positiver dielektrischer Anisotropie enthalten, werden in
S. H. Lee et al. Appl. Phys. Lett. (1997), 71, 2851–2853 beschrieben. Diese Anzeigen verwenden auf eine Substratoberfläche angeordnete Interdigitalelektroden (In-plane Ansteuerelektroden-Konfiguration kammförmiger Struktur), wie sie unter anderem bei den kommerziell erhältlichen IPS-(in-plane switching) Anzeigen zum Einsatz kommen (wie z. B. in
DE 40 00 451 und
EP 0 588 568 offenbart), und weisen eine homöotrope Anordnung des Flüssigkristallmediums auf, die zu einer planaren Anordnung beim Anlegen einer elektrischen Feldes wechselt.
-
Weiterentwicklungen der oben genannten Anzeige sind zum Beispiel in
K. S. Hun et al. J. Appl. Phys. (2008), 104, 084515 (DSIPS: 'double-side inplane switching' für Verbesserungen von Treiberspannung und Transmission),
M. Jiao et al. App. Phys. Lett (2008), 92, 111101 (DFFS: 'dual fringe field switching' für verbesserte Schaltzeiten) und
Y. T. Kim et al. Jap. J. App. Phys. (2009), 48, 110205 (VAS: 'viewing angle switchable' LCD) zu finden.
-
Darüber hinaus sind VA-IPS-Anzeigen auch unter dem Namen Positiv-VA und HT-VA bekannt.
-
Bei allen solchen Anzeigen (hier nachfolgend allgemein als VA-IPS-Anzeigen bezeichnet) ist auf beiden Substratoberflächen eine Orientierungsschicht zur homöotropen Ausrichtung des FK-Mediums aufgebracht, deren Erzeugung bisher mit einem beträchtlichen Aufwand verbunden ist.
-
Ein Ziel dieser Erfindung ist es, die Herstellprozesse selbst zu vereinfachen, ohne die Vorteile der VA-Display-Technik, wie relativ schnelle Schaltzeiten, gute Blickwinkelabhängigkeit und hohen Kontrast aufzugeben.
-
Für die technische Anwendung dieser Effekte in elektrooptischen Anzeigeelementen werden FK-Phasen benötigt, die einer Vielzahl von Anforderungen genügen müssen. Besonders wichtig sind hier die chemische Beständigkeit gegenüber Feuchtigkeit, Luft, den Materialien in den Substratoberflächen und physikalischen Einflüssen wie Wärme, Strahlung im infraroten, sichtbaren und ultravioletten Bereich und elektrische Gleich- und Wechselfelder.
-
Ferner werden von technisch verwendbaren FK-Phasen eine flüssigkristalline Mesophase in einem geeigneten Temperaturbereich und eine niedrige Viskosität gefordert.
-
VA- und VA-IPS-Anzeigen sollen im Allgemeinen einen sehr hohen spezifischen Widerstand bei gleichzeitig großem Arbeitstemperaturbereich, kurze Schaltzeiten und niedrige Schwellenspannung, mit deren Hilfe verschiedene Graustufen erzeugt werden können, besitzen.
-
In den herkömmlichen VA- und VA-IPS-Displays sorgt eine Polyimidschicht auf den Substratoberflächen für die homöotrope Orientierung des Flüssigkristalls. Die Herstellung einer geeigneten Orientierungsschicht im Display erfordert einen erheblichen Aufwand. Außerdem können Wechselwirkungen der Orientierungsschicht mit dem FK-Medium den elektrischen Widerstand der Anzeige verschlechtern. Wegen solcher möglichen Wechselwirkungen reduziert sich die Zahl der geeigneten Flüssigkristallkomponenten erheblich. Daher wäre es erstrebenswert die homöotrope Ausrichtung des FK-Mediums ohne Polyimid zu erreichen.
-
Der Nachteil der häufig verwendeten Aktivmatrix-TN-Anzeigen beruht in ihrem vergleichsweise niedrigen Kontrast, der relativ hohen Blickwinkelabhängigkeit und der Schwierigkeit in diesen Anzeigen Graustufen zu erzeugen.
-
Wesentlich bessere Blickwinkelabhängigkeiten weisen VA-Displays auf und werden daher hauptsächlich für Fernseher und Monitore verwendet.
-
Eine Weiterentwicklung stellen die sogenannten PS-bzw. PSA-Anzeigen (”Polymer Sustained” bzw. ”Polymer Sustained Alignment”) dar, für die auch gelegentlich der Begriff ”Polymer Stabilized” verwendet wird. Ohne nennenswerte Einbußen sonstiger Parameter, wie insbesondere der günstigen Blickwinkelabhängigkeit des Kontrastes, zeichnen sich die PSA-Anzeigen durch die Verkürzung der Schaltzeiten aus.
-
In diesen Anzeigen wird dem FK-Medium eine geringe Menge (zum Beispiel 0,3 Gew.-%, typischerweise < 1 Gew.-%) einer oder mehrerer polymerisierbare(n) Verbindung(en) zugesetzt, welche nach Einfüllen in die FK-Zelle mit oder ohne angelegte elektrische Spannung zwischen den Elektroden in situ polymerisiert bzw. vernetzt wird, üblicherweise durch UV-Photopolymerisation. Als besonders geeignet hat sich der Zusatz von polymerisierbaren mesogenen oder flüssigkristallinen Verbindungen, auch als reaktive Mesogene oder ”RM”s bezeichnet, zur FK-Mischung erwiesen. Die PSA-Technik wird bisher hauptsächlich für FK-Medien mit negativer dielektrischer Anisotropie eingesetzt.
-
Nachfolgend wird der Begriff ”PSA”, falls nicht anders angegeben, stellvertretend für PS-Anzeigen und PSA-Anzeigen verwendet.
-
Mittlerweile wird das PSA-Prinzip in diversen klassischen FK-Anzeigen angewendet. So sind beispielsweise PSA-VA-, PSA-OCB-, PSA-IPS-, PSA-FFS- und PSA-TN-Anzeigen bekannt. Die Polymerisation der polymerisierbaren Verbindung(en) erfolgt bei PSA-VA- und PSA-OCB-Anzeigen vorzugsweise bei angelegter elektrischer Spannung, bei PSA-IPS-Anzeigen mit oder ohne angelegte elektrische Spannung. Wie man in Testzellen nachweisen kann, führt das PS(A)-Verfahren zu einem 'pretilt' in der Zelle. Bei PSA-OCB-Anzeigen beispielsweise kann man erreichen, dass die Bend-Struktur stabilisiert wird, so dass man ohne Offset-Spannung auskommt oder diese reduzieren kann. Im Falle von PSA-VA-Anzeigen wirkt sich der 'pretilt' positiv auf die Schaltzeiten aus. Für PSA-VA-Anzeigen kann ein Standard-MVA- bzw. -PVA Pixel- und Elektroden-Layout verwendet werden. Darüber hinaus kann man aber beispielsweise auch mit nur einer strukturierten Elektrodenseite und ohne 'Protrusions' auskommen, was die Herstellung wesentlich vereinfacht und gleichzeitig zu einem sehr guten Kontrast bei sehr guter Lichtdurchlässigkeit führt.
-
PSA-VA-Anzeigen sind beispielsweise in
JP 10-036847 A ,
EP 1 170 626 A2 ,
US 6,861,107 ,
US 7,169,449 ,
US 2004/0191428 A1 ,
US 2006/0066793 A1 und
US 2006/0103804 A1 beschrieben. PSA-OCB-Anzeigen sind beispielsweise in
T. -J- Chen et al., Jpn. J. Appl. Phys. 45, 2006, 2702–2704 und
S. H. Kim, L. -C- Chien, Jpn. J. Appl. Phys. 43, 2004, 7643–7647 beschrieben. PSA-IPS-Anzeigen sind zum Beispiel in
US 6,177,972 und
Appl. Phys. Lett. 1999, 75(21), 3264 beschrieben. PSA-TN-Anzeigen sind zum Beispiel in
Optics Express 2004, 12(7), 1221 beschrieben. PSA-VA-IPS Anzeigen sind zum Beispiel in
WO 2010/089092 A1 offenbart.
-
PSA-Anzeigen können ebenso wie die oben beschriebenen konventionellen FK-Anzeigen als Aktivmatrix- oder Passivmatrix-Anzeigen betrieben werden. Bei Aktivmatrix-Anzeigen erfolgt die Ansteuerung einzelner Bildpunkte üblicherweise durch integrierte, nicht-lineare aktive Elemente wie beispielsweise Transistoren (z. B. Dünnfilmtransistoren, engl. 'thin film transistor' bzw. ”TFT”), bei Passivmatrix-Anzeigen üblicherweise nach dem Multiplex-Verfahren, wobei beide Verfahren aus dem Stand der Technik bekannt sind.
-
Insbesondere für Monitor- und vor allem TV-Anwendungen ist nach wie vor die Optimierung der Schaltzeiten, wie aber auch des Kontrastes und der Luminanz (also auch Transmission) der FK-Anzeige gefragt. Hier kann das PSA-Verfahren entscheidende Vorteile bringen. Insbesondere bei PSA-VA-Anzeigen kann man ohne nennenswerte Einbußen sonstiger Parameter eine Verkürzung der Schaltzeiten erreichen, die mit einem in Testzellen messbaren 'pretilt' korrelieren.
-
Im Stand der Technik werden für PSA-VA beispielsweise polymerisierbare Verbindungen der folgenden Formel verwendet
worin P
1 und P
2 jeweils eine polymerisierbare Gruppe, üblicherweise eine Acrylat- oder Methacrylatgruppe bedeutet, wie beispielsweise in
US 7,169,449 beschrieben.
-
Der Aufwand für das Erzeugen einer Polyimidschicht, Behandlung der Schicht und Verbesserung mit Erhebungen oder Polymerschichten, ist relativ groß. Eine vereinfachende Technologie wäre daher wünschenswert, die einerseits die Produktionskosten verringert und andererseits die Bildqualität (Blickwinkelabhängigkeit, Kontrast, Schaltzeiten) zu optimieren hilft.
-
Über eine spontane horizontale bis vertikale Ausrichtung einer Flüssigkristallschicht mit Hilfe von Nanopartikeln basierend auf polyhedralen oligomeren Silsesquioxanen (nachfolgend einfach Silsesquioxane, PSS) berichtet die Druckschrift Shie-Chang Jeng et al. Optics Letters (2009), 34, 455–457. Ab einer Konzentration von ca. 1 Gew.-% wird eine nahezu homöotrope Ausrichtung beobachtet. Der 'pretilt' (engl.) ist nur durch die Konzentration beeinflussbar.
-
In der Druckschrift
US 2008/0198301 A1 wird ebenfalls PSS als Orientierungsmaterial vorgeschlagen. Man erkennt, dass die Selbstorientierung auf ITO und auf planar orientierendem Polyimid funktioniert.
-
Auf das Problem der Temperaturabhängigkeit des Schaltvorgangs und der fehlenden Passivierungsschicht wird in beiden Druckschriften nicht hingewiesen. In der Tat hat es sich gezeigt, dass der Grad der von PSS induzierten homöotropen Orientierung mit steigender Temperatur rasch abnimmt. Eine Passivierungsschicht ist darüber hinaus besonders wichtig, da die Polyimidschicht nicht nur für die Orientierung des FK-Mediums, sondern auch für eine elektrische Isolierung sorgt. Ohne Passivierungsschicht können Probleme mit der Zuverlässigkeit der Anzeige ('Reliability') wie R-DC ('Residual-DC') erscheinen.
-
Auf einem Konferenzposter zur SID 2010 (H. Y. Gim et al., P-128) wird beschrieben, dass ein phenethylsubstituiertes polyhedrales oligomeres Silsesquioxan in einer Konzentration von 10 Gew.-% in einer Anzeige ohne konventionelle Orientierungsschicht vom PSA-VA-Typ verwendet wird. Das FK-Medium mit negativer dielektrischer Anisotropie wird durch das PSS homöotrop orientiert. Die große Menge an Dotierstoff beeinflusst aber erheblich die Eigenschaften des FK-Mediums, daher ist die Anzahl an einsetzbaren Flüssigkristallkomponenten für eine derartige FK-Anzeige sehr begrenzt.
-
Langkettige Alkohole wurden bereits als Ausgangsprodukt für kovalent gebundene Ethergruppen auf Glasoberflächen verwendet (vgl.
US 4022934 A ), an denen eine vertikale Ausrichtung eines Flüssigkristalls beobachtet wurde. Die kovalente Anbindung des Alkohols an die Oberfläche erfordert eine Vorbehandlung der Substratoberfläche in einem Verarbeitungsschritt.
-
In der Druckschrift
US 3,972,589 wird über langkettige Carbonsäuren, Nitrile und Amine berichtet, die bei einer Konzentration von 1–4 Gew.-% einen Imin-Flüssigkristall (MBBA) zwischen Glassubstraten homöotrop ausrichten. Über weitere solche Additive wie Gallussäurecetylester und Lecithin wird in der Druckschrift
DE 2356889 A1 berichtet. In der Patentschrift
US 3,848,966 wir über ein Additiv der Formel Octadecyl-CH(COOH)
2 berichtet, das bei ≤ 0,5% Zugabe eine homöotrope Oberflächenausrichtung eines Flüssigkristalls induziert.
-
Auf das Problem der Stabilität der induzierten Orientierung wird in beiden Druckschriften nicht hingewiesen. In der Tat hat es sich gezeigt, dass nach Hitzebelastung der Grad der von dem Additiven induzierten homöotropen Orientierung mit steigender Temperatur rasch abnimmt.
-
Die bestehenden Ansätze um zu Displayanwendungen ohne Orientierungsschicht (Polyimidschicht etc.) zu gelangen sind daher noch nicht vollständig zufrieden stellend.
-
Ein erster Gegenstand der vorliegenden Erfindung ist ein FK-Medium enthaltend eine niedermolekulare flüssigkristalline Komponente und eine oder mehrere organische Verbindungen, die mindestens eine polare Ankergruppe und mindestens einen langkettigen unpolaren Rest mit mindestens 8 C-Atomen aufweisen. Die flüssigkristalline Komponente bzw. das FK-Medium können wahlweise eine positive oder eine negative dielektrischen Anisotropie aufweisen. Das erfindungsgemäße FK-Medium ist vorzugsweise nematisch. Das FK-Medium enthält außerdem optional eine polymerisierte oder polymerisierbare Komponente, wobei die polymerisierte Komponente erhältlich ist durch Polymerisation einer polymerisierbaren Komponente.
-
Ein weiterer Gegenstand der vorliegenden Erfindung ist ein Verfahren zur Herstellung eines FK-Mediums indem man eine niedermolekulare flüssigkristalline Komponente mit einer oder mehreren organischen Verbindungen, die mindestens eine polare Ankergruppe und mindestens einen langkettigen unpolaren Rest mit mindestens 8 C-Atomen aufweisen, mischt, optional eine oder mehrere polymerisierbare Verbindungen und optional Hilfsstoffe zugibt. Die flüssigkristalline Komponente bzw. das FK-Medium können wahlweise eine positive oder eine negative dielektrische Anisotropie aufweisen.
-
Ein weiterer Gegenstand der vorliegenden Erfindung ist eine Flüssigkristallanzeige (FK-Anzeige) enthaltend eine Flüssigkristallzelle (FK-Zelle) mit zwei Substraten und mindestens zwei Elektroden, wobei mindestens ein Substrat lichtdurchlässig ist, sowie einer zwischen den Substraten befindlichen Schicht eines Flüssigkristallmediums (FK-Mediums) enthaltend eine niedermolekulare flüssigkristalline Komponente und eine oder mehrere organische Verbindungen, wobei die organische Verbindung dadurch gekennzeichnet ist, dass sie mindestens eine polare Ankergruppe aufweist und mindestens einen langkettigen unpolaren Rest mit mindestens 8 C-Atomen aufweist, und die geeignet ist, eine homöotrope (vertikale) Ausrichtung des FK-Mediums gegenüber den Substratoberflächen herbeizuführen. Das FK-Medium der FK-Anzeige enthält außerdem optional eine polymerisierte oder polymerisierbare Komponente, wobei die polymerisierte Komponente erhältlich ist durch Polymerisation einer oder mehrerer polymerisierbarer Verbindungen zwischen den Substraten der FK-Zelle im FK-Medium, optional unter Anlegen einer elektrischen Spannung an die Elektroden der Zelle oder unter der Wirkung eines anderen elektrischen Feldes. Mit dieser Komponente lassen sich das FK-Medium und insbesondere seine Orientierung stabilisieren und gegebenenfalls ein gewünschter'pre-tilt' einstellen. Die FK-Anzeige ist bevorzugt so aufgebaut, dass sie auf mindestens einem Substrat mindestens eine oder zwei Elektroden aufweist.
-
Ein weiterer Gegenstand der Erfindung ist ein Verfahren zu Herstellung einer FK-Anzeige, vorzugsweise des PSA-VA-Typs, enthaltend eine FK-Zelle mit zwei Substraten und mindestens zwei Elektroden, wobei mindestens ein Substrat lichtdurchlässig ist, umfassend die Verfahrensschritte:
- – Befüllen der Zelle mit einem FK-Medium wie vor und nachstehend oder in den Ansprüchen beschrieben, umfassend eine organische Verbindung die geeignet ist, eine homöotrope (vertikale) Ausrichtung des FK-Mediums gegenüber den Substratoberflächen herbeizuführen, und optional:
- – Polymerisieren der optional enthaltenen polymerisierbaren Komponente, optional unter Anlegen einer Spannung an die Elektroden der Zelle oder unter der Wirkung eines elektrischen Feldes.
-
Die organische Verbindung, die mindestens eine polare Ankergruppe und mindestens einen langkettigen unpolaren Rest mit mindestens 8 C-Atomen aufweist (das Selbstorientierungsadditiv) wird im Flüssigkristall gelöst. Sie bewirkt eine homöotrope Ausrichtung des Flüssigkristalls gegenüber den Substratoberflächen (wie z. B. eine Oberfläche aus Glas oder mit ITO oder mit Polyimid beschichtetes Glas). Es scheint in Anbetracht der Untersuchungen zu dieser Erfindung so, dass die polare Ankergruppe in lockerer Wechselwirkung mit der Substratoberfläche tritt. Dadurch richten sich die organischen Verbindungen auf der Substratoberfläche aus und induzieren eine homöotrope Orientierung des Flüssigkristalls.
-
Das Selbstorientierungsadditiv wird vorzugsweise in einer Konzentration von weniger als 10 Gew.-%, besonders bevorzugt ≤ 8 Gew.-% und ganz besonders ≤ 5 Gew.-% eingesetzt. Es wird bevorzugt in einer Konzentration von mindestens 0,1 Gew.-% eingesetzt, bevorzugt mindestens 0,2 Gew.-%. Der Einsatz von 0,1 bis 2,5 Gew.-% des Selbstorientierungsadditivs führt in der Regel schon zu vollständig homöotroper Orientierung der FK-Schicht bei den üblichen Zelldicken (3 bis 4 μm).
-
Die polare Ankergruppe umfasst bevorzugt keine polymerisierbare Gruppen wie z. B. Acrylatgruppen.
-
Die polare Ankergruppe des Selbstorientierungsadditivs besteht bevorzugt aus einer Gruppe, die eine nicht-kovalente Wechselwirkung mit der Substratoberfläche aus Glas oder Metalloxiden eingeht. Geeignete Gruppen sind polare Gruppen umfassend polare Strukturelemente mit Atomen ausgewählt aus N, O, S, und P. Die Gruppen sollten gleichzeitig ausreichend stabil für den Einsatz als LC-Medium sein. Sie sollen außerdem die VHR-Werte ('voltage holding ratio') des FK-Mediums in der FK-Zelle und die Langzeitstabilität ('reliability') nur gering beeinflussen. Bevorzugt sind ein oder mehrere, bevorzugt zwei oder mehr, dieser Heteroatome in der Ankergruppe enthalten.
-
Die polare Ankergruppe besteht besonders bevorzugt aus wenigstens zwei Strukturelementen enthaltend Heteroatome ausgewählt aus (N, O), und kovalenten, verknüpfenden Strukturen zwischen den Heteroatomen und zwischen einem oder mehreren der Heteroatome und dem Rest des Moleküls der Formel I (ohne die Ankergruppe). Die polare Ankergruppe umfasst bevorzugt mindestens eine OH-Struktur oder ein N-Atom in einer primären, sekundären oder tertiären Amingruppe.
-
Die Selbstorientierungsadditive besitzen bevorzugt eine oder zwei langkettige unpolare Reste, bevorzugt einen dieser Reste. Unter den Begriff ”langkettiger unpolarer Rest” fallen bevorzugt aliphatische Kohlenwasserstoffreste, auch verzweigte, mit einer längsten Kettenlänge von mindestens 8 C-Atomen, wobei bestimmte funktionelle Gruppen in der Kette mit umfasst sind. Der Rest kann auch ungesättigt und/oder halogeniert (mit Cl, F) sein. In der langkettigen Alkylgruppe können eine oder mehrere nicht benachbarte und nicht endständige CH2-Gruppen durch -O-, -(CO)- oder eine Estergruppe ersetzt sein. Weiterhin kann eine CH2-Gruppe durch eine Cycloalkylengruppe mit 3 bis 8 C-Atomen ersetzt sein.
-
Der ”langkettige unpolare Rest” hat höchstens 30 C-Atome. Die längste Kette hat eine maximale Kettenlänge von 20 C-Atomen. Bevorzugt hat der Rest 8 bis 18 C-Atome. Bevorzugt ist der Rest eine lineare Alkylkette mit 10 bis 16 C-Atomen, wobei höchstens 5 C-Atome in Nebenketten angeschlossen sind.
-
Das Selbstorientierungsadditiv ist bevorzugt eine organische Verbindung mit einer relativen Molmasse ≥ 130 g/mol, damit die Substanzen weniger flüchtig sind. Besonders bevorzugt weist es eine relative Molmasse ≥ 150 g/mol auf, um einen noch stabileren Effekt der Selbstausrichtung zu erzielen. Als Obergrenze hat es bevorzugt eine relative Molmasse von ≤ 500 g/mol.
-
Das Selbstorientierungsadditiv hat besonders bevorzugt eine Struktur der Formel I: (R1)n-R2 wobei
R1 geradkettiges oder verzweigtes Alkyl mit 8 bis 20 C-Atomen, worin auch eine oder mehrere nicht benachbarte CH2-Gruppen durch -CH=CH-, -CF=CH-, -CH=CF- oder -C=C- ersetzt sein können, worin eine CH2-Gruppe durch eine Cycloalkylengruppe mit 3 bis 8 C-Atomen und worin auch ein oder mehrere H-Atome durch F oder Cl, ersetzt sein können,
R2 eine polare Ankergruppe, und
n 1 oder 2, bevorzugt 1,
bedeutet.
-
Der Rest R1 umfasst bevorzugt 8 bis 20 C-Atome. Besonders bevorzugt umfasst er keine Ringe und bedeutet:
R1 geradkettiges oder verzweigtes Alkyl mit 10 bis 18 C-Atomen, worin auch eine oder mehrere nicht benachbarte CH2-Gruppen durch -CH=CH-, -CF=CH-, -CH=CF-, -C≡C- oder -O-ersetzt sein können, und worin auch ein oder mehrere H-Atome durch F oder Cl, ersetzt sein können.
-
Der Rest R2 in Formel I umfasst beispielsweise Alkohole, primäre, sekundäre und tertiare Amine, Ketone, Carbonsäuren, Thiole, Ester und (Thio-)Ether, sowie Kombinationen daraus. Die Struktur kann dabei linear, verzweigt, cyclisch oder eine Kombination davon sein.
-
Die Gruppe R
2 umfasst in den vorangehenden Formeln bevorzugt eine Gruppe der Formel (A1)
-Sp-[X2-Z3-]kX1 (A1) worin
Sp eine Einfachbindung oder eine Abstandsgruppe definiert wie Sp
a wie nachstehend für Formel M definiert, bevorzugt eine Abstandsgruppe Sp''-X'' wie für Formel M unten definiert, die über die Gruppe X'' mit dem Rest R
1 verbunden ist, wobei Sp'' ganz besonders eine Einfachbindung oder ein Alkylen mit 1 bis 12 C-Atomen bedeutet,
X
1 eine Gruppe -NH
2, -NHR
11 -NR
11 2, -OR
11, -OH, -(CO)OH oder eine Gruppe der Formeln
R
0 H oder Alkyl mit 1 bis 12 C-Atomen,
X
2 jeweils unabhängig -NH-, -NR
11-, -O- oder eine Einfachbindung,
Z
3 jeweils unabhängig eine Alkylengruppe mit 1–15 C-Atomen, carbocyclische Ringe mit 5 oder 6 C-Atomen, oder Kombinationen aus einem oder mehreren Ringen und Alkylengruppen, worin jeweils Wasserstoff durch –OH, OR
11, -(CO)OH, -NH
2, -NHR
11, -NR
11 2, oder Halogen (bevorzugt F, Cl) ersetzt sein kann,
R
11 jeweils unabhängig einen halogenierten oder unsubstituierten Alkylrest mit 1 bis 15 C-Atomen, wobei in diesem Rest auch eine oder mehrere CH
2-Gruppen jeweils unabhängig voneinander durch -C≡C-, -CH=CH-, -(CO)O-, -O(CO)-, -(CO)- oder -O- so ersetzt sein können, dass O-Atome nicht direkt miteinander verknüpft sind, und wobei zwei Reste R
11 miteinander zu einem Ring verknüpft sein können, oder H, und
k 0 bis 3
bedeutet.
-
Besonders bevorzugt umfasst die Gruppe R
2 in den vorangehenden Formeln eine (N/O)-heteroatomhaltige Gruppe der Teilformel (A2)
worin
Sp, X
1, X
2 und R
11 wie oben für R
2 (Formel A1) definiert sind, und
n 1, 2 oder 3,
bedeutet.
-
Besonders bevorzugt bedeutet die Gruppe R2 genau eine Gruppe der Formeln (A1) bzw. (A2).
-
Besonders bevorzugte stickstoffhaltige Gruppen R2 sind ausgewählt aus -NH2, -NH-(CH2)n3H, -(CH2)n-NH2, -(CH2)n-NH-(CH2)n3H, -NH-(CH2)n-NH2, -NH-(CH2)n-NH-(CH2)n3H, -(CH2)n1-NH-(CH2)n2-NH2, -(CH2)n1-NH-(CH2)n2-NH-(CH2)n3H, -O-(CH2)n-NH2, -(CH2)n1-O-(CH2)n-NH2, -(CH2)n1-NH-(CH2)n2-OH, -O-(CH2)n1-NH-(CH2)n2-NH2, -O-(CH2)n1-NH-(CH2)n2-OH, -(CH2)n1-NH-(CH2)n2-NH-(CH2)n3H,
worin n, n1, n2 und n3 unabhängig 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 oder 12, insbesondere 1, 2, 3 oder 4 bedeuten. Aufgrund der besseren Löslichkeit in hochpolaren flüssigkristallinen Medien sind die Gruppen -OH und -NH2 besonders bevorzugt. Unter den sauerstoffhaltigen Funktionen in den Ankergruppen ist die OH-Gruppe aufgrund der hohen Ankerkraft bevorzugt gegenüber den Funktionen -O-, -(CO)- oder -(CO)O-. Die mehrfach mit Heteroatomen (N, O) ausgestatteten Gruppen besitzen eine besondere Stärke als Ankergruppe. Sie können in kleineren Konzentrationen eingesetzt werden.
-
Besonders bevorzugte stickstofffreie Gruppen R2 sind ausgewählt aus -OH, -(CH2)n-OH, -O-(CH2)n-OH, -[O-(CH2)n1-]n2-OH, -(CO)OH, -(CH2)n-(CO)OH, -O-(CH2)n-(CO)OH oder -[O-(CH2)n1-]n2-(CO)OH, worin n, n1 und n2 unabhängig 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 oder 12, insbesondere 1, 2, 3 oder 4 bedeuten.
-
”Halogen” steht im Zusammenhang der vorliegenden Erfindung für Fluor, Chlor, Brom beziehungsweise Iod, bevorzugt für Fluor oder Chlor.
-
Besonders bevorzugte Verbindungen der Formel I sind ausgewählt aus den folgenden beispielhaften Verbindungen, welche gleichzeitig besonders bevorzugte Gruppen R
1 und R
2 der Selbstorientierungsadditive wiedergeben:
-
In einer weiteren bevorzugten Ausführungsform der Erfindung werden organische Verbindungen mit der polaren Ankergruppe bzw. Verbindungen der Formel I verwendet, die als weitere Funktionalisierung neben dem polaren Anker eine oder mehrere polymerisierbare Gruppen aufweisen (vergleiche Gruppe Pa oder Pb unten). Bevorzugte polymerisierbare Gruppen sind Gruppen wie Acrylat-, Methacrylat-, Fluoracrylat-, Oxetan-, Vinyloxy- oder Epoxygruppe, besonders bevorzugt Acrylat und Methacrylat. Durch den Einschluss der Verbindungen der Formel I in die Polymerisation werden die Verbindungen nachhaltig immobilisiert, wodurch sie ihre Funktion beibehalten.
-
Ein Vorteil der erfindungsgemäßen FK-Anzeigen ist, dass die Anzeige ohne die übliche Polyimid-Orientierungsschicht die gewünschte homöotrope Orientierung erreicht. Dadurch vereinfacht sich die Herstellung der FK-Anzeigen erheblich. Diese Orientierung bleibt in der Regel auch bei höherer Temperatur erhalten.
-
Durch die Polymerstabilisierung wird die homöotrope Orientierung zusätzlich stabilisiert; dadurch wird eine verbesserte Temperaturstabilität des elektrooptischen Schaltens erreicht. Die homöotrope Orientierung bleibt auch bei höheren Temperaturen innerhalb des Arbeitsbereichs des Mediums (z. B. 70°C) erhalten. Auch die Langzeitstabilität der homöotropen Orientierung wird durch die polymerisierbare Komponente verbessert. Eine Temperaturbelastung jenseits des Klärpunktes über mehrere Tage führt zu keiner Veränderung der Vororientierung, auch nicht bei höheren Temperaturen. Die erfindungsgemäßen, polymerstabilisierten Anzeigen zeichnen sich durch verbesserte Schaltzeiten (Pretiltwinkel durch Polymerisation unter Anlegen von Spannung) und besseres Kontrastverhältnis (Temperaturabhängigkeit des Kontrasts) aus. Die vorzugsweise enthaltene polymerisierte Komponente kann gleichzeitig als eine Passivierungsschicht dienen, die die Zuverlässigkeit (die sog. 'reliability') des Displays erhöht, da sie die Elektrodenoberfläche von dem flüssigkristallinen Medium isoliert.
-
Die Selbstorientierungsadditive bzw. die Verbindungen der Formel I beeinflussen dank der relativ kleinen Menge die Eigenschaften der FK-Medien praktisch unerheblich. Daher kann eine breite Vielfalt an Flüssigkristall-Komponenten in der FK-Anzeige verwendet werden.
-
Die erfindungsgemäßen FK-Anzeigen besitzen daher bevorzugt keine Orientierungsschicht ('alignment layer') für homöotrope Ausrichtung auf den Oberflächen der FK-Zelle, d. h. sie sind polyimidfrei. Für den Fall, dass die FK-Anzeigen dennoch ein- oder beidseitig Orientierungsschichten aufweisen, so bestehen diese vorzugsweise aus Polyimid. Die Orientierungsschichten sind vorzugsweise nicht gerieben. Damit entfällt das bisher notwendige Reiben der Orientierungsschicht, ein besonders aufwändiger Schritt in der Herstellung. Eine ungeriebene Polyimidschicht kann dennoch als Passivierungsschicht dienen.
-
Die erfindungsgemäßen FK-Anzeigen verwenden in einer besonderen Ausführungsform ein FK-Medium mit negativer dielektrischer Anisotropie (Δε ≤ –1,5). Entsprechende flüssigkristalline Medien sind ebenfalls bevorzugt. In der Regel handelt es sich dabei um eine VA-Anzeige mit auf gegenüberliegenden Seiten der FK-Zelle angeordneten Elektroden, bevorzugt mit Elektroden, die so angeordnet sind, dass sie ein überwiegend senkrecht zur Substratoberfläche orientiertes elektrisches Feld erzeugen können. Typische verwendete Substrate sind die, die aus dem VAN-mode und PSA-VA verwendet werden (Strukturierung der Elektroden ist daher möglich).
-
Die erfindungsgemäßen FK-Anzeigen verwenden in einer besonderen Ausführungsform ein FK-Medium mit positiver dielektrischer Anisotropie (Δε ≤ 1,5). Entsprechende flüssigkristalline Medien sind ebenfalls bevorzugt. In der Regel handelt es sich dabei um eine VA-IPS-Anzeige mit auf einer Seite der FK-Zelle angeordneten Elektroden, bevorzugt mit Elektroden, die so angeordnet sind, dass sie ein überwiegend planar zur Substratoberfläche orientiertes elektrisches Feld erzeugen können, z. B. Interdigitalelektroden (In-plane Ansteuerelektroden-Konfiguration kammförmiger Struktur).
-
Die FK-Anzeigen sind in der üblichen Art und Weise mit einem oder mehreren Palarisator(en) versehen, die den Schaltvorgang des FK-Mediums sichtbar machen.
-
Die polymerisierte Komponente der FK-Zelle (Polymer) ist erhältlich durch Polymerisieren einer polymerisierbaren Komponente (Monomere). In der Regel sind die Monomere zunächst in dem FK-Medium gelöst und werden in der FK-Zelle polymerisiert, nachdem sich eine homöotrope Ausrichtung oder ein hoher Tiltwinkel des FK-Medium eingestellt hat. Zur Unterstützung der gewünschten Ausrichtung kann eine Spannung an die FK-Zelle angelegt werden. Im einfachsten Fall erübrigt sich eine solche Spannung und die gewünschte Ausrichtung stellt sich allein durch die Beschaffenheit des FK-Mediums und der Zellgeometrie ein.
-
Die geeigneten Monomere (polymerisierbare Komponente) des FK-Mediums sind solche aus dem Stand der Technik, die für PSA-VA-Anzeigen verwendet werden, insbesondere polymerisierbare Verbindungen der unten genannten Formel M und/oder der Formeln M1 bis M22. Die erfindungsgemäßen FK-Medien zur Verwendung in PSA-Anzeigen enthalten vorzugsweise < 5 Gew.-%, besonders bevorzugt < 1 Gew.-% und ganz besonders bevorzugt < 0,5 Gew.-% an polymerisierbaren Verbindungen, insbesondere polymerisierbaren Verbindungen der unten genannten Formeln. Um einen ausreichenden Effekt zu erreichen werden bevorzugt 0,2 Gew.-% oder mehr eingesetzt. Die optimale Menge ist abhängig von der Schichtdicke.
-
Geeignete Monomere der polymerisierbaren Komponente des FK-Mediums werden durch die folgende Formel M beschrieben: Pa-(Spa)s1-A2-(Z1-A1)n-(Spb)s2-Pb M worin die einzelnen Reste folgende Bedeutung besitzen:
Pa, Pb jeweils unabhängig voneinander eine polymerisierbare Gruppe,
Spa, Spb bei jedem Auftreten gleich oder verschieden eine Abstandsgruppe,
s1, s2 jeweils unabhängig voneinander 0 oder 1,
A1, A2, jeweils unabhängig voneinander einen Rest ausgewählt aus folgenden Gruppen
- a) der Gruppe bestehend aus trans-1,4-Cyclohexylen, 1,4-Cyclohexenylen und 4,4'-Bicyclohexylen, worin auch eine oder mehrere nicht benachbarte CH2-Gruppen durch -O- und/oder -S- ersetzt sein können und worin auch ein oder mehrere H-Atome durch F ersetzt sein können,
- b) der Gruppe bestehend aus 1,4-Phenylen und 1,3-Phenylen, worin auch eine oder zwei CH-Gruppen durch N ersetzt sein können und worin auch ein oder mehrere H-Atome durch L ersetzt sein können,
- c) der Gruppe bestehend aus Tetrahydropyran-2,5-diyl, 1,3-Dioxan-2,5-diyl, Tetrahydrofuran-2,5-diyl, Cyclobut-1,3-diyl, Piperidin-1,4-diyl, Thiophen-2,5-diyl und Selenophen-2,5-diyl, welche auch ein oder mehrfach durch L substituiert sein können,
- d) der Gruppe bestehend aus gesättigten, teilweise ungesättigten oder vollständig ungesättigten, und optional substituierten, polycyclischen Resten mit 5 bis 20 cyclischen C-Atomen, von denen auch eines oder mehrere durch Heteroatome ersetzt sein können, vorzugsweise ausgewählt aus der Gruppe bestehend aus Bicyclo[1.1.1]pentan-1,3-diyl, Bicyclo[2.2.2]octan-1,4-diyl, Spiro[3.3]heptan-2,6-diyl, wobei in diesen Resten auch ein oder mehrere H- Atome durch L ersetzt sein können, und/oder eine oder mehrere Doppelbindungen durch Einfachbindungen ersetzt sein können, und/oder ein oder mehrere CH-Gruppen durch N ersetzt sein können,
n 0, 1, 2 oder 3,
Z1 jeweils unabhängig voneinander -CO-O-, -O-CO-, -CH2O-, -OCH2-, -CF2O-, -OCF2-, oder -(CH2)n-, wobei n 2, 3 oder 4 ist, -O-, -CO-, -C(RcRd)-, -CH2CF2-, -CF2CF2-, oder eine Einfachbindung,
L bei jedem Auftreten gleich oder verschieden F, Cl, CN, SCN, SF5 oder geradkettiges oder verzweigtes, jeweils optional fluoriertes, Alkyl, Alkoxy, Alkylcarbonyl, Alkoxycarbonyl, Alkylcarbonyloxy oder Alkoxycarbonyloxy mit 1 bis 12 C-Atomen,
R0, R00 jeweils unabhängig voneinander H, F oder geradkettiges oder verzweigtes Alkyl mit 1 bis 12 C-Atomen, worin auch ein oder mehrere H-Atome durch F ersetzt sein können,
M -O-, -S-, -CH2-, -CHY1- oder -CY1Y2-,
Y1, und Y2 jeweils unabhängig voneinander eine der oben für R0 angegebenen Bedeutungen, Cl oder CN, und vorzugsweise H, F, Cl, CN, OCF3 oder CF3,
W1, W2 jeweils unabhängig voneinander -CH2CH2-, -CH=CH-, -CH2-O-, -O-CH2-, -C(RcRd)- oder -O-, und
Rc und Rd jeweils unabhängig voneinander H oder Alkyl mit 1 bis 6 C-Atomen, vorzugsweise H, Methyl oder Ethyl,
bedeuten.
-
Die polymerisierbare Gruppe P
a,b ist eine Gruppe, die für eine Polymerisationsreaktion, wie beispielsweise die radikalische oder ionische Kettenpolymerisation, Polyaddition oder Polykondensation, oder für eine polymeranaloge Umsetzung, beispielsweise die Addition oder Kondensation an eine Polymerhauptkette, geeignet ist Besonders bevorzugt sind Gruppen für die Kettenpolymerisation, insbesondere solche enthaltend eine C=C-Doppelbindung oder -C≡C-Dreifachbindung, sowie zur Polymerisation unter Ringöffnung geeignete Gruppen wie beispielsweise Oxetan- oder Epoxygruppen Bevorzugte Gruppen P
a,b sind ausgewählt aus der Gruppe bestehend aus
CW
1=CH-CO-NH-, CH
2=CW
1-CO-NH-, CH
3-CH=CH-O-, (CH
2=CH)
2CH-OCO-, (CH
2=CH-CH
2)
2CH-OCO-, (CH
2=CH)
2CH-O-, (CH
2=CH-CH
2)
2N-, (CH
2=CH-CH
2)
2N-CO-, HO-CW
2W
3-, HS-CW
2W
3-, HW
2N-, HO-CW
2W
3-NH-, CH
2=CW
1-CO-NH-, CH
2=CH-(COO)
k1-Phe-(O)
k2-, CH
2=CH-(CO)
k1-Phe-(O)
k2-, Phe-CH=CH-, HOOC-, OCN-, und W
4W
5W
6Si-, worin W
1 H, F, Cl, CN, CF
3, Phenyl oder Alkyl mit 1 bis 5 C-Atomen, insbesondere H, F, Cl oder CH
3 bedeutet, W
2 und W
3 jeweils unabhängig voneinander H oder Alkyl mit 1 bis 5 C-Atomen, insbesondere H, Methyl, Ethyl oder n-Propyl bedeuten, W
4, W
5 und W
6 jeweils unabhängig voneinander Cl, Oxaalkyl oder Oxacarbonylalkyl mit 1 bis 5 C-Atomen bedeuten, W
7 und W
8 jeweils unabhängig voneinander H, Cl oder Alkyl mit 1 bis 5 C-Atomen bedeuten, Phe 1,4-Phenylen bedeutet, welches optional mit einem oder mehreren, von P-Sp- verschiedenen Resten L wie oben definiert substituiert ist, k
1, k
2 und k
3 jeweils unabhängig voneinander 0 oder 1 bedeuten, k
3 vorzugsweise 1 bedeutet, und k
4 eine ganze Zahl von 1 bis 10 bedeutet.
-
Besonders bevorzugte Gruppen P
a,b sind ausgewählt aus der Gruppe bestehend aus CH
2=CW
1-CO-O-, CH
2=CW
1-CO-,
CH
2=CW
2-O-, CW
1=CH-CO-(O)
k3-, CW
1=CH-CO-NH-, CH
2=CW
1-CO-NH-, (CH
2=CH)
2CH-OCO-, (CH
2=CH-CH
2)
2CH-OCO-, (CH
2=CH)
2CH-O-, (CH
2=CH-CH
2)
2N-, (CH
2=CH-CH
2)
2N-CO-, CH
2=CW
1-CO-NH-, CH
2=CH-(COO)
k1-Phe-(O)
k2-, CH
2=CH-(CO)
k1-Phe-(O)
k2-, Phe-CH=CH- und W
4W
5W
6Si-, worin W
1 H, F, Cl, CN, CF
3, Phenyl oder Alkyl mit 1 bis 5 C-Atomen, insbesondere H, F, Cl oder CH
3 bedeutet, W
2 und W
3 jeweils unabhängig voneinander H oder Alkyl mit 1 bis 5 C-Atomen, insbesondere H, Methyl, Ethyl oder n-Propyl bedeuten, W
4, W
5 und W
6 jeweils unabhängig voneinander Cl, Oxaalkyl oder Oxacarbonylalkyl mit 1 bis 5 C-Atomen bedeuten, W
7 und W
8 jeweils unabhängig voneinander H, Cl oder Alkyl mit 1 bis 5 C-Atomen bedeuten, Phe 1,4-Phenylen bedeutet, k
1, k
2 und k
3 jeweils unabhängig voneinander 0 oder 1 bedeuten, k
3 vorzugsweise 1 bedeutet, und k
4 eine ganze Zahl von 1 bis 10 bedeutet.
-
Ganz besonders bevorzugte Gruppen P
a,b sind ausgewählt aus der Gruppe bestehend aus CH
2=CW
1-CO-O-, insbesondere CH
2=CH-CO-O-, CH
2=C(CH
3)-CO-O- und CH
2=CF-CO-O-, ferner CH
2=CH-O-,
-
Ganz besonders bevorzugte Gruppen Pa,b sind daher ausgewählt aus der Gruppe bestehend aus Acrylat-, Methacrylat-, Fluoracrylat-, ferner Vinyloxy-, Chloracrylat-, Oxetan- und Epoxygruppen, und unter diesen bevorzugt eine Acrylat- oder Methacrylatgruppe.
-
Bevorzugte Abstandsgruppen Spa , b sind ausgewählt aus der Formel Sp''-X'', so dass der Rest Pa,b-Spa/b- der Formel Pa/b-Sp''-X''- entspricht, wobei
Sp'' Alkylen mit 1 bis 20, vorzugsweise 1 bis 12 C-Atomen bedeutet, welches optional durch F, Cl, Br, I oder CN ein- oder mehrfach substituiert ist, und worin auch eine oder mehrere nicht benachbarte CH2-Gruppen jeweils unabhängig voneinander so durch -O-, -S-, -NH-, -N(R0)-, -Si(R00R000)- -CO-, -CO-O-, -O-CO-, -O-CO-O-, -S-CO-, -CO-S-, -N(R00)-CO-O-, -O-CO-N(R00)-, -N(R0 0)-CO-N(R00)-, -CH=CH- oder -C≡C- ersetzt sein können, dass O- und/oder S-Atome nicht direkt miteinander verknüpft sind,
X'' -O-, -S-, -CO-, -CO-O-, -O-CO-, -O-CO-O-, -CO-N(R00)-, -N(R00)-CO-, -N(R00)-CO-N(R00)-, -OCH2-, -CH2O-, -SCH2-, -CH2S-, -CF2O-, -OCF2-, -CF2S-, -SCF2-, -CF2CH2-, -CH2CF2-, -CF2CF2-, -CH=N-, -N=CH-, -N=N-, -CH=CR0-, -CY2=CY3-, -C≡C-, -CH=CH-CO-O-, -O-CO-CH=CH- oder eine Einfachbindung
bedeutet,
R00 und R000 jeweils unabhängig voneinander H oder Alkyl mit 1 bis 12 C-Atomen bedeuten, und
Y2 und Y3 jeweils unabhängig voneinander H, F, Cl oder CN
bedeuten.
-
X' ist vorzugsweise -O-, -S-CO-, -COO-, -OCO-, -O-COO-, -CO-NR0-, -NR0-CO-, -NR0-CO-NR0- oder eine Einfachbindung.
-
Typische Abstandsgruppen Sp'' sind beispielsweise -(CH2)p1-, -(CH2CH2O)q1-CH2CH2-, -CH2CH2-S-CH2CH2-, -CH2CH2-NH-CH2CH2- oder -(SiR00R000-O)p1-, worin p1 eine ganze Zahl von 1 bis 12 ist, q1 eine ganze Zahl von 1 bis 3 ist, und R00 und R000 die oben angegebenen Bedeutungen besitzen.
-
Besonders bevorzugte Gruppen -Sp''-X''- sind -(CH2)p1-, -(CH2)P1-O-, -(CH2)p1-O-CO-, -(CH2)p1-O-CO-O-, worin p1 und q1 die oben angegebene Bedeutung haben.
-
Besonders bevorzugte Gruppen Sp'' sind beispielsweise jeweils geradkettiges Ethylen, Propylen, Butylen, Pentylen, Hexylen, Heptylen, Octylen, Nonylen, Decylen, Undecylen, Dodecylen, Octadecylen, Ethylenoxyethylen, Methylenoxybutylen, Ethylenthioethylen, Ethylen-N-methyl-iminoethylen, 1-Methylalkylen, Ethenylen, Propenylen und Butenylen.
-
Besonders bevorzugte Monomere sind die folgenden:
worin die einzelnen Reste folgende Bedeutung besitzen:
P
1 und P
2 jeweils unabhängig voneinander eine polymerisierbare Gruppe wie für Formel I definiert, bevorzugt eine Acrylat-, Methacrylat-, Fluoracrylat-, Oxetan-, Vinyloxy- oder Epoxygruppe,
Sp
1 und Sp
2 jeweils unabhängig voneinander eine Einfachbindung oder eine Abstandsgruppe, vorzugsweise mit einer der vor- und nachstehend für Sp
a angegebenen Bedeutungen, und besonders bevorzugt -(CH
2)
p1-, -(CH
2)
p1-O-, -(CH
2)
p1-CO-O- oder -(CH
2)
p1-O-CO-O-, worin p1 eine ganze Zahl von 1 bis 12 ist, und wobei in den letztgenannten Gruppen die Verknüpfung zur benachbarten Ring über das O-Atom erfolgt, wobei auch einer oder mehrere der Reste P
1-Sp
1- und P
2-Sp
2- einen Rest R
aa bedeuten können, mit der Maßgabe dass mindestens einer der vorhandenen Reste P
1-Sp
1- und P
2-Sp
2- nicht R
aa bedeutet,
R
aa H, F, Cl, CN oder geradkettiges oder verzweigtes Alkyl mit 1 bis 25 C-Atomen, worin auch eine oder mehrere nicht benachbarte CH
2-Gruppen jeweils unabhängig voneinander durch C(RO)=C(R
00)-, -C=C-, -N(R
0)-, -O-, -S-, -CO-, -CO-O-, -O-CO-, -O-CO-O- so ersetzt sein können, dass O- und/oder S-Atome nicht direkt miteinander verknüpft sind, und worin auch ein oder mehrere H-Atome durch F, Cl, CN oder P
1-Sp
1- ersetzt sein können, besonders bevorzugt geradkettiges oder verzweigtes, optional ein- oder mehrfach fluoriertes, Alkyl, Alkoxy, Alkenyl, Alkinyl, Alkylcarbonyl, Alkoxycarbonyl, oder Alkylcarbonyloxy mit 1 bis 12 C-Atomen (wobei die Alkenyl- und Alkinylreste mindestens zwei und die verzweigten Reste mindestens drei C-Atome aufweisen),
R
0, R
00 jeweils unabhängig voneinander H oder Alkyl mit 1 bis 12 C-Atomen,
R
y und R
z jeweils unabhängig voneinander H, F, CH
3 oder CF
3,
Z
1 -O-, -CO-, -C(R
yR
z)-, oder -CF
2CF
2-,
Z
2 und Z
3 jeweils unabhängig voneinander -CO-O-, -O-CO-, -CH
2O-, -OCH
2-, -CF
2O-, -OCF
2-, oder -(CH
2)
n-, wobei n 2, 3 oder 4 ist,
L bei jedem Auftreten gleich oder verschieden F, Cl, CN, SCN, SF
5 oder geradkettiges oder verzweigtes, optional ein- oder mehrfach fluoriertes, Alkyl, Alkoxy, Alkenyl, Alkinyl, Alkylcarbonyl, Alkoxycarbonyl, Alkylcarbonyloxy oder Alkoxycarbonyloxy mit 1 bis 12 C-Atomen, vorzugsweise F,
L' und L'' jeweils unabhängig voneinander H, F oder Cl,
r 0, 1, 2, 3 oder 4,
s 0, 1, 2 oder 3,
t 0, 1 oder 2, und
x 0 oder 1.
-
Vorzugsweise enthält das FK-Medium oder die polymerisierbare Komponente eine oder mehrere Verbindungen ausgewählt aus der Gruppe bestehend aus den Formeln M1–M21, besonders bevorzugt bestehend aus den Formeln M2–M15, ganz besonders bevorzugt bestehend aus den Formeln M2, M3, M9, M14 und M15.
-
Vorzugsweise enthält das FK-Medium oder die polymerisierbare Komponente keine Verbindungen der Formel M10, worin Z2 und Z3 -(CO)O- oder -O(CO)- bedeuten.
-
Zur Herstellung von PSA-Anzeigen werden die polymerisierbaren Verbindungen im FK-Medium zwischen den Substraten der FK-Anzeige, optional unter Anlegen einer Spannung, durch in-situ-Polymerisation polymerisiert oder vernetzt (falls eine polymerisierbare Verbindung zwei oder mehr polymerisierbare Gruppen enthält). Die Polymerisation kann in einem Schritt durchgeführt werden. Es ist auch möglich, zunächst in einem ersten Schritt die Polymerisation unter Anlegen einer Spannung durchzuführen, um einen pretilt-Winkel zu erzeugen, und anschließend in einem zweiten Polymerisationsschritt ohne anliegende Spannung die im ersten Schritt nicht abreagierten Verbindungen zu polymerisieren bzw. zu vernetzen (”end curing”).
-
Geeignete und bevorzugte Polymerisationsmethoden sind beispielsweise die thermische oder Photopolymerisation, vorzugsweise Photopolymerisation, insbesondere UV-Photopolymerisation. Dabei können gegebenenfalls auch ein oder mehrere Initiatoren zugesetzt werden. Geeignete Bedingungen für die Polymerisation, sowie geeignete Arten und Mengen der Initiatoren, sind dem Fachmann bekannt und in der Literatur beschrieben. Für die radikalische Polymerisation eignen sich zum Beispiel die kommerziell erhältlichen Photoinitiatoren Irgacure651®, Irgacure184®, Irgacure907®, Irgacure369®, oder Darocure1173® (Ciba AG). Falls ein Initiator eingesetzt wird, beträgt dessen Anteil vorzugsweise 0,001 bis 5 Gew.-%, besonders bevorzugt 0,001 bis 1 Gew.-%.
-
Die polymerisierbaren Verbindungen mit aromatischen Ringen (vgl. insbesondere die Formeln M1 bis M15) eignen sich auch für die Polymerisation ohne Initiator, was erhebliche Vorteile mit sich bringt, wie beispielsweise geringere Materialkosten und insbesondere eine geringere Verunreinigung des FK-Mediums durch mögliche Restmengen des Initiators oder dessen Abbauprodukte. Die Polymerisation kann somit auch ohne Zusatz eines Initiators erfolgen. Somit enthält das FK-Medium in einer bevorzugten Ausführungsform keinen Polymerisationsinitiator.
-
Die polymerisierbare Komponente oder das FK-Medium können auch einen oder mehrere Stabilisatoren enthalten, um eine unerwünschte spontane Polymerisation der RMs, beispielsweise während der Lagerung oder des Transports, zu verhindern. Geeignete Arten und Mengen der Stabilisatoren sind dem Fachmann bekannt und in der Literatur beschrieben. Besonders geeignet sind zum Beispiel die kommerziell erhältlichen Stabilisatoren der Serie Irganox® (Ciba AG), wie beispielsweise Irganox® 1076. Falls Stabilisatoren eingesetzt werden, beträgt deren Anteil, bezogen auf die Gesamtmenge der RMs beziehungsweise der polymerisierbaren Komponente, vorzugsweise 10–10000 ppm, besonders bevorzugt 50–500 ppm.
-
Die FK-Medien zur Verwendung in den erfindungsgemäßen FK-Anzeigen enthalten, neben den oben beschriebenen Additiven und den optionalen polymerisierbaren Verbindungen (RMs) eine FK-Mischung (”Host-Mischung”) enthaltend eine oder mehr, vorzugsweise zwei oder mehr niedermolekulare (d. h. monomere bzw. unpolymerisierte) Verbindungen. Letztere sind stabil bzw. unreaktiv gegenüber einer Polymerisationsreaktion unter den zur Polymerisation der polymerisierbaren Verbindungen verwendeten Bedingungen. Prinzipiell eignet sich als Host-Mischung jede zur Verwendung in herkommlichen VA- und VA-IPS-Anzeigen geeignete dielektrisch negative oder positive FK-Mischung.
-
Geeignete FK-Mischungen sind dem Fachmann bekannt und in der Literatur beschrieben. FK-Medien für VA-Anzeigen mit negativer dielektrischer Anisotropie sind in
EP 1 378 557 A1 beschrieben.
-
-
Im Folgenden werden bevorzugte Ausführungsformen für das erfindungsgemäße flüssigkristalline Medium mit negativer dielektrischer Anisotropie angeführt:
- a) FK-Medium, welches zusätzlich eine oder mehrere Verbindungen ausgewählt aus der Gruppe der Verbindungen der Formeln A, B und C enthält, worin
R2A, R2B und R2C jeweils unabhängig voneinander H, einen unsubstituierten, einen einfach durch CN oder CF3 oder mindestens einfach durch Halogen substituierten Alkylrest mit bis zu 15 C-Atomen, wobei in diesen Resten auch eine oder mehrere CH2-Gruppen durch -O-, -S-, ,-C≡C-, -CF2O-, -OCF2-, -OC-O- oder -O-CO- so ersetzt sein können, dass O-Atome nicht direkt miteinander verknüpft sind,
L1-4 jeweils unabhängig voneinander F, Cl, CF3 oder CHF2,
Z2 und Z2' jeweils unabhängig voneinander Einfachbindung, -CH2CH2-, -CH=CH-, -CF2O-, -OCF2-, -CH2O-, -OCH2-, -COO-, -OCO-, -C2F4-, -CF=CF-, -CH=CHCH2O-,
p 1 oder 2,
q 0 oder 1, und
v 1 bis 6
bedeuten.
In den Verbindungen der Formeln A und B können Z2 gleiche oder unterschiedliche Bedeutungen haben. In den Verbindungen der Formel B können Z2 und Z2' gleiche oder verschiedene Bedeutungen aufweisen.
In den Verbindungen der Formeln A, B und C bedeuten R2A, R2B und R2C jeweils vorzugsweise Alkyl mit 1–6 C-Atomen, insbesondere CH3, C2H5, n-C3H7, n-C4H9, n-C5H11.
In den Verbindungen der Formeln A und B bedeuten L1, L2, L3 und L4 vorzugsweise L1=L2=F und L3=L4=F, ferner L1=F und L2=Cl, L1=Cl und L2=F, L3=F und L4=Cl, L3 = Cl und L4 = F. Z2 und Z2 bedeuten in den Formeln A und B vorzugsweise jeweils unabhängig voneinander eine Einfachbindung, ferner eine -C2H4-Brücke.
Sofern in der Formel B Z2 = -C2H4- ist, ist Z2' vorzugsweise eine Einfachbindung bzw. falls Z2' = -C2H4- bedeutet, ist Z2 vorzugsweise eine Einfachbindung. In den Verbindungen der Formeln A und B bedeutet (O)CvH2v+1 vorzugsweise OCvH2v+1, ferner CvH2v+1. In den Verbindungen der Formel C bedeutet (O)CvH2v+1 vorzugsweise CvH2v+1. In den Verbindungen der Formel C bedeuten L3 und L4 vorzugsweise jeweils F.
Bevorzugte Verbindungen der Formeln A, B und C werden nachfolgend genannt: worin Alkyl und Alkyl* jeweils unabhängig voneinander einen geradkettigen Alkylrest mit 1–6 C-Atomen bedeuten.
Besonders bevorzugte erfindungsgemäße Mischungen enthalten eine oder mehrere Verbindungen der Formeln A-2, A-8, A-14, A-29, A-35, B-2, B-11, B-16 und C-1.
Vorzugsweise beträgt der Anteil an Verbindungen der Formeln A und/oder B im Gesamtgemisch mindestens 20 Gew.-%.
Besonders bevorzugte erfindungsgemäße Medien enthalten mindestens eine Verbindung der Formel C-1, vorzugsweise in Mengen von > 3 Gew.-%, insbesondere > 5 Gew.-% und besonders bevorzugt von 5–25 Gew.-%.
- b) FK-Medium, welches zusätzlich eine oder mehrere Verbindungen der folgenden Formel enthält: worin die einzelnen Reste folgende Bedeutung besitzen R3 und R4 jeweils unabhängig voneinander Alkyl mit 1 bis 12 C-Atomen, worin auch eine oder zwei nicht benachbarte CH2-Gruppen durch -O-, -CH=CH-, -CO-, -O-CO- oder -CO-O- so ersetzt sein können, dass O-Atome nicht direkt miteinander verknüpft sind,
Zy -CH0CH2-, -CH=CH-, -CF2O-, -OCF2-, -CH2O-, -OCH2-, -CO-O-, -O-CO-, -C2F4-, -CF=CF-, -CH=CH-CH2O-, oder eine Einfachbindung, vorzugsweise eine Einfachbindung.
Die Verbindungen der Formel ZK sind vorzugsweise ausgewählt aus der Gruppe bestehend aus folgenden Unterformeln: worin Alkyl und Alkyl* jeweils unabhängig voneinander einen geradkettigen Alkylrest mit 1–6 C-Atomen bedeuten, und Alkenyl und Alkenyl* einen geradkettigen Alkenylrest mit 2–6 C-Atomen bedeuten. Alkenyl bedeutet vorzugsweise CH2=CH-, CH2=CHCH2CH2-, CH3-CH=CH-, CH3-CH2-CH=CH-, CH3-(CH2)2-CH=CH-, CH3-(CH2)3-CH=CH- oder CH3-CH=CH-(CH2)2-.
- c) FK-Medium, welches zusätzlich eine oder mehrere Verbindungen der folgenden Formel enthält: worin die einzelnen Reste bei jedem Auftreten gleich oder verschieden folgende Bedeutung haben:
R5 und R6 jeweils unabhängig voneinander eine der oben für R3/4 angegebenen Bedeutungen, e 1 oder 2.
Die Verbindungen der Formel DK sind vorzugsweise ausgewählt aus der Gruppe bestehend aus folgenden Unterformeln: worin Alkyl und Alkyl* jeweils unabhängig voneinander einen geradkettigen Alkylrest mit 1–6 C-Atomen, und Alkenyl und Alkenyl* jeweils unabhängig voneinander einen geradkettigen Alkenylrest mit 2–6 C-Atomen bedeuten. Alkenyl und Alkenyl* bedeuten vorzugsweise CH2=CH-, CH2=CHCH2CH2-, CH3-CH=CH-, CH3-CH2-CH=CH-, CH3-(CH2)2-CH=CH-, CH3-(CH2)3-CH=CH- oder CH3-CH=CH-(CH2)2-.
- d) FK-Medium, welches zusätzlich eine oder mehrere Verbindungen der folgenden Formel enthält: worin die einzelnen Reste folgende Bedeutung besitzen f 0 oder 1,
R1 und R2 jeweils unabhängig voneinander Alkyl mit 1 bis 12 C-Atomen, wobei auch eine oder zwei nicht benachbarte CH2-Gruppen durch -O-, -CH=CH-, -CF=CF-, -CO-, -O(CO)- oder -(CO)O- so ersetzt sein können, dass O-Atome nicht direkt miteinander verknüpft sind,
Zx und Zy jeweils unabhängig voneinander -CH2CH2-, -CH=CH-, -CF2O-, -OCF2-, -CH2O-, -OCH2-, -CO-O-, -O-CO-, -C2F4-, -CF=CF-, -CH=CH-CH2O-, oder eine Einfachbindung, vorzugsweise eine Einfachbindung,
L1 und L2 jeweils unabhängig voneinander F, Cl, OCF3, CF3, CH3, CH2F, CHF2.
Vorzugsweise bedeuten beide Reste L1 und L2F oder einer der Reste L1 und L2 F und der andere Cl.
Die Verbindungen der Formel LV sind vorzugsweise ausgewählt aus der Gruppe bestehend aus folgenden Unterformeln worin R1 die oben angegebene Bedeutung hat, Alkyl einen geradkettigen Alkylrest mit 1–6 C-Atomen, (O) ein Sauerstoffatom oder eine Einfachbindung und v eine ganze Zahl von 1 bis 6 bedeuten. R1 bedeutet vorzugsweise geradkettiges Alkyl mit 1 bis 6 C-Atomen oder geradkettiges Alkenyl mit 2 bis 6 C-Atomen, insbesondere CH3, C2H5, n-C3H7, n-C4H9, n-C5H11, CH2=CH-, CH2=CHCH2CH2-, CH3-CH=CH-, CH3-CH2-CH=CH-, CH3-(CH2)2-CH=CH-, CH3-(CH2)3-CH=CH- oder CH3-CH=CH-(CH2)2-.
- e) FK-Medium, welches zusätzlich eine oder mehrere Verbindungen ausgewählt aus der Gruppe bestehend aus folgenden Formeln enthält: worin alkyl C1-6-alkyl, Lx H oder F und X F, Cl, OCF3, OCHF2 oder OCH=CF2 bedeutet. Besonders bevorzugt sind Verbindungen der Formel G1, worin X F bedeutet.
- f) FK-Medium, welches zusätzlich eine oder mehrere Verbindungen ausgewählt aus der Gruppe bestehend aus folgenden Formeln enthält: worin R5 eine der oben für R1 angegebenen Bedeutungen besitz, alkyl C1-6-alkyl, d 0 oder 1, und z und m jeweils unabhängig voneinander eine ganze Zahl von 1 bis 6 bedeuten. R5 ist in diesen Verbindungen besonders bevorzugt C1-6-alkyl oder -alkoxy oder C2-6-alkenyl, d ist vorzugsweise 1. Vorzugsweise enthält das erfindungsgemäße FK-Medium eine oder mehrere Verbindungen der oben genannten Formeln in Mengen von ≥ 5 Gew.-%.
- g) FK-Medium, welches zusätzlich eine oder mehrere Biphenylverbindungen ausgewählt aus der Gruppe bestehend aus folgenden Formeln enthält:
worin Alkyl und Alkyl* jeweils unabhängig voneinander einen geradkettigen Alkylrest mit 1–6 C-Atomen, und Alkenyl und Alkenyl* jeweils unabhängig voneinander einen geradkettigen Alkenylrest mit 2–6 C-Atomen bedeuten. Alkenyl und Alkenyl* bedeuten vorzugsweise CH2=CH-, CH2=CHCH2CH2-, CH3-CH=CH-, CH3-CH2-CH=CH-, CH3-(CH2)2-CH=CH-, CH3-(CH2)3-CH=CH- oder CH3-CH=CH-(CH2)2-.
Der Anteil der Biphenyle der Formeln B1 bis B3 in der FK-Mischung beträgt vorzugsweise mindestens ≥ Gew.-%, insbesondere ≥ 5 Gew.-%.
Die Verbindungen der Formel B2 sind besonders bevorzugt.
Die Verbindungen der Formel B1 bis B3 sind vorzugsweise ausgewählt aus der Gruppe bestehend aus folgenden Unterformeln worin Alkyl* einen Alkylrest mit 1–6 C-Atomen bedeutet. Insbesondere bevorzugt enthält das erfindungsgemäße Medium eine oder mehrere Verbindungen der Formeln B1a und/oder B2c.
- h) FK-Medium, welches zusätzlich eine oder mehrere Terphenylverbindungen der folgenden Formel enthält: worin R5 und R6 jeweils unabhängig voneinander eine der oben für R1 angegebenen Bedeutungen besitzen und jeweils unabhängig voneinander bedeuten, worin L5 F oder Cl, vorzugsweise F, und L6 F, Cl, OCF3, CF3, CH3, CH2F oder CHF2, vorzugsweise F, bedeuten.
Die Verbindungen der Formel T sind vorzugsweise ausgewählt aus der Gruppe bestehend aus folgenden Unterformeln worin R einen geradkettigen Alkyl- oder Alkoxyrest mit 1–7 C-Atomen, R* einen geradkettigen Alkenylrest mit 2–7 C-Atomen, (O) ein Sauerstoffatom oder eine Einfachbindung, und m eine ganze Zahl von 1 bis 6 bedeutet. R* bedeutet vorzugsweise CH2=CH-, CH2=CHCH2CH2-, CH3-CH=CH-, CH3-CH2-CH=CH-, CH3-(CH2)2-CH=CH-, CH3-(CH2)3-CH=CH- oder CH3-CH=CH-(CH2)2-.
Vorzugsweise bedeutet R Methyl, Ethyl, Propyl, Butyl, Pentyl, Hexyl Methoxy, Ethoxy, Propoxy, Butoxy oder Pentoxy.
Das erfindungsgemäße FK-Medium enthält die Terphenyle der Formeln T und deren bevorzugte Unterformeln vorzugsweise in einer Menge von 0,5–30 Gew.-%, insbesondere von 1–20 Gew.-%.
Besonders bevorzugt sind Verbindungen der Formeln T1, T2, T3 und T21. In diesen Verbindungen bedeutet R vorzugsweise Alkyl, ferner Alkoxy jeweils mit 1–5 C-Atomen.
Vorzugsweise werden die Terphenyle in erfindungsgemäßen Mischungen eingesetzt, wenn der Δn-Wert der Mischung ≥ 0,1 sein soll. Bevorzugte Mischungen enthalten 2–20 Gew.-% einer oder mehrerer Terphenyl-Verbindungen der Formel T, vorzugsweise ausgewählt aus der Gruppe der Verbindungen T1 bis T22.
- i) FK-Medium, welches zusätzlich eine oder mehrere Verbindungen ausgewählt aus der Gruppe bestehend aus folgenden Formeln enthält: worin R1 und R2 die oben für Formel LY angegebenen Bedeutungen haben, und vorzugsweise jeweils unabhängig voneinander geradkettiges Alkyl mit 1 bis 6 C-Atomen oder geradkettiges Alkenyl mit 2 bis 6 C-Atomen bedeuten.
Bevorzugte Medien enthalten eine oder mehrere Verbindungen ausgewählt aus den Formeln O1, O3 und O4.
- k) FK-Medium, welches zusätzlich eine oder mehrere Verbindungen der folgenden Formel enthält: worin R9 H, CH3, C2H5 oder n-C3H7, (F) einen optionalen Fluor-substituenten und q 1, 2 oder 3 bedeutet, und R7 eine der für R1 angegebenen Bedeutungen hat, vorzugsweise in Mengen von > 3 Gew.-%, insbesondere ≥ 5 Gew.-%, und ganz besonders bevorzugt von 5–30 Gew.-%.
Besonders bevorzugte Verbindungen der Formel FI sind ausgewählt aus der Gruppe bestehend aus folgenden Unterformeln: worin R7 vorzugsweise geradkettiges Alkyl bedeutet und R9 CH3, C2H5 oder n-C3H7 bedeutet. Besonders bevorzugt sind die Verbindungen der Formel FI1, FI2 und FI3.
- m) FK-Medium, welches zusätzlich eine oder mehrere Verbindungen ausgewählt aus der Gruppe bestehend aus folgenden Formeln enthält: worin R8 die für R1 für Formel LV angegebene Bedeutung hat und Alkyl einen geradkettigen Alkylrest mit 1–6 C-Atomen bedeutet.
- n) FK-Medium, welches zusätzlich eine oder mehrere Verbindungen enthält, die eine Tetrahydronaphthyl- oder Naphthyl-Einheit aufweisen, wie z. B. die Verbindungen ausgewählt aus der Gruppe bestehend aus folgenden Formeln: worin R10 und R11 jeweils unabhängig voneinander eine der für R1 für Formel LV angegebenen Bedeutungen haben, vorzugsweise geradkettiges Alkyl oder Alkoxy mit 1 bis 6 C-Atomen oder geradkettiges Alkenyl mit 2 bis 6 C-Atomen bedeuten, und Z1 und Z2 jeweils unabhängig voneinander -C2H4-, -CH=CH-, -(CH2)4-, -(CH2)3O-, -O(CH2)3-, -CH=CH-CH2CH2-, -CH2CH2CH=CH-, -CH2O-, -OCH2-, -CO-O-, -O-CO-, -C2F4-, -CF=CF-, -CF=CH-, -CH=CF-, -CH2- oder eine Einfachbindung bedeuten.
- o) FK-Medium, welches zusätzlich eine oder mehrere eine oder mehrere Difluordibenzochromane und/oder Chromane der folgenden Formeln enthält: worin R10 und R11 jeweils unabhängig voneinander die oben für R1 in Formel LV angegebene Bedeutung aufweisen, und c 0 oder 1 bedeutet, vorzugsweise in Mengen von 3 bis 20 Gew.-%, insbesondere in Mengen von 3 bis 15 Gew.-%.
Besonders bevorzugte Verbindungen der Formeln BC und CR sind ausgewählt aus der Gruppe bestehend aus folgenden Unterformeln: worin Alkyl und Alkyl* jeweils unabhängig voneinander einen geradkettigen Alkylrest mit 1–6 C-Atomen, und Alkenyl und Alkenyl* jeweils unabhängig voneinander einen geradkettigen Alkenylrest mit 2–6 C-Atomen bedeuten. Alkenyl und Alkenyl* bedeuten vorzugsweise CH2=CH-, CH2=CHCH2CH2-, CH3-CH=CH-, CH3-CH2-CH=CH-, CH3-(CH2)2-CH=CH-, CH3-(CH2)3-CH=CH- oder CH3-CH=CH-(CH2)2-.
Ganz besonders bevorzugt sind Mischungen enthaltend eine, zwei oder drei Verbindungen der Formel BC-2.
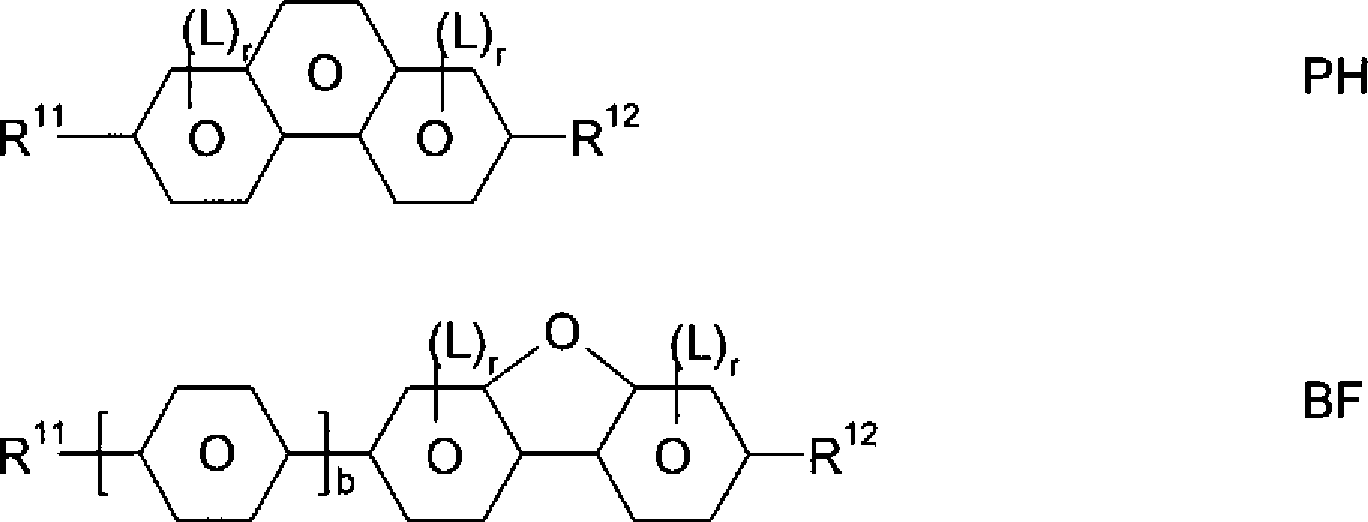
- p) FK-Medium, welches zusätzlich eine oder mehrere fluorierte Phenanthrene und/oder Dibenzofurane der folgenden Formeln enthält: worin R11 und R12 jeweils unabhängig voneinander die oben für R1 in Formel LV angegebenen Bedeutungen besitzen, b 0 oder 1, L F und r 1, 2 oder 3 bedeutet.
Besonders bevorzugte Verbindungen der Formeln PH und BF sind ausgewählt aus der Gruppe bestehend aus folgenden Unterformeln: worin R und R' jeweils unabhängig voneinander einen geradkettigen Alkyl- oder Alkoxyrest mit 1–7 C-Atomen bedeuten.
-
Die erfindungsgemäße Flüssigkristallmischung ist mit einer dielektrischen Anisotropie (Δε) von ≤ –1,5 dielektrisch negativ. Die Verbindungen der Formeln IIIA, IIIB, IIIC, LY1-LY18, Y1-Y16, T1-T24, FI, VK1-VK4, N1-N10, BC, CR, PH und BF eignen sich als dielektrisch negative Komponente. Bevorzugt sind die dielektrisch negativen Verbindungen ausgewählt aus den Formeln IIIA, IIIB und IIIC. Das FK-Medium weist vorzugsweise ein Δε von –1,5 bis –8,0, insbesondere von –2,5 bis –6,0 auf.
-
Die Werte der Doppelbrechung Δn in der Flüssigkristallmischung liegen in der Regel zwischen 0,07 und 0,16, vorzugsweise zwischen 0,08 und 0,12.
-
Die Rotationsviskosität γ1 bei 20°C vor der Polymerisation ist vorzugsweise ≤ 165 mPa·s, insbesondere ≤ 140 mPa·s.
-
Im Folgenden werden bevorzugte Ausführungsformen für das erfindungsgemäße flüssigkristalline Medium mit positiver dielektrischer Anisotropie angeführt:
- – LC-Medium, welches zusätzlich eine oder mehrere Verbindungen der Formel II und/oder III enthält: worin
Ring A 1,4-Phenylen oder trans-1,4-Cyclohexylen bedeutet,
a 0 oder 1 ist,
R3 jeweils unabhängig voneinander Alkyl mit 1 bis 9 C-Atomen oder Alkenyl mit 2 bis 9 C-Atomen bedeutet, vorzugsweise Alkenyl mit 2 bis 9 C-Atomen, und
R4 jeweils unabhängig voneinander einen unsubstituierten oder halogenierten Alkylrest mit 1 bis 12 C-Atomen, wobei auch eine oder zwei nicht benachbarte CH2-Gruppen durch -O-, -CH=CH-, -CH=CF-, -(CO)-, -O(CO)- oder -(CO)O- so ersetzt sein können, dass O-Atome nicht direkt miteinander verknüpft sind, und vorzugsweise Alkyl mit 1 bis 12 C-Atomen oder Alkenyl mit 2 bis 9 C-Atomen bedeutet.
-
Die Verbindungen der Formel II sind vorzugsweise ausgewählt aus der Gruppe bestehend aus folgenden Formeln:
worin R
3a und R
4a jeweils unabhängig voneinander H, CH
3, C
2H
5 oder C
3H
7 bedeuten, und ”alkyl” eine geradkettige Alkylgruppe mit 1 bis 8, vorzugsweise 1, 2, 3, 4 oder 5 C-Atomen bedeutet. Besonders bevorzugt sind Verbindungen der Formel IIa und IIf, insbesondere solche, worin R
3a H oder CH
3, vorzugsweise H, bedeutet, und Verbindungen der Formel IIc, insbesondere solche, worin R
3a und R
4a H, CH
3 oder C
2H
5 bedeuten.
-
Die Verbindungen der Formel III sind vorzugsweise ausgewählt aus der Gruppe bestehend aus den folgenden Formeln:
worin ”alkyl” und R
3a die oben angegebenen Bedeutungen haben und R
3a vorzugsweise H oder CH
3 bedeutet. Besonders bevorzugt sind Verbindungen der Formel IIIb;
- – LC-Medium, welches zusätzlich eine oder mehrere Verbindungen ausgewählt aus der Gruppe bestehend aus den folgenden Formeln enthält: worin
R0 einen Alkyl- oder Alkoxyrest mit 1 bis 15 C-Atomen, wobei in diesen Resten auch eine oder mehrere CH2-Gruppen jeweils unabhängig voneinander durch -C≡C-, -CF2O-, -CH=CH-, -O-, -(CO)O- oder -O(CO)- so ersetzt sein können, dass O-Atome nicht direkt miteinander verknüpft sind, und worin auch ein oder mehrere H-Atome durch Halogen ersetzt sein können,
X0 F, Cl, CN, SF5, SCN, NCS, einen halogenierten Alkylrest, halogenierten Alkenylrest, halogenierten Alkoxyrest oder halogenierten Alkenyloxyrest mit jeweils bis zu 6 C-Atomen,
Y1–6 jeweils unabhängig voneinander H oder F,
Z0 -C2H4-, -(CH2)4-, -CH=CH-, -CF=CF-, -C2F4-, -CH2CF2-, -CF2CH2-, -CH2O-, -OCH2-, -COO-, -CF2O- oder -OCF2-, in den Formeln V und VI auch eine Einfachbindung, und
b und c jeweils unabhängig voneinander 0 oder 1
bedeuten.
In den Verbindungen der Formel IV bis VIII bedeutet X0 vorzugsweise F oder OCF3, ferner OCHF2, CF3, CF2H, Cl, OCH=CF2. R0 ist vorzugsweise geradkettiges Alkyl oder Alkenyl mit jeweils bis zu 6 C-Atomen.
Die Verbindungen der Formel IV sind vorzugsweise ausgewählt aus der Gruppe bestehend aus den folgenden Formeln: worin R0 und X0 die oben angegebenen Bedeutungen haben.
Vorzugsweise bedeutet in Formel IV R0 Alkyl mit 1 bis 8 C-Atomen und X0 F, Cl, OCHF2 oder OCF3, ferner OCH=CF2. In der Verbindung der Formel IVb bedeutet R0 vorzugsweise Alkyl oder Alkenyl. In der Verbindung der Formel IVd bedeutet X0 vorzugsweise Cl, ferner F.
Die Verbindungen der Formel V sind vorzugsweise ausgewählt aus der Gruppe bestehend aus den folgenden Formeln: worin R0 und X0 die oben angegebenen Bedeutungen haben.
Vorzugsweise bedeutet R0 in Formel V Alkyl mit 1 bis 8 C-Atomen und X0 F;
- – LC-Medium, welches eine oder mehrere Verbindungen der Formel VI-1 enthält: besonders bevorzugt solche ausgewählt aus der Gruppe bestehend aus den folgenden Formeln: worin R0 und X0 die oben angegebenen Bedeutungen haben.
Vorzugsweise bedeutet R0 in Formel VI Alkyl mit 1 bis 8 C-Atomen und X0 F, ferner OCF3.
- – LC-Medium, welches eine oder mehrere Verbindungen der Formel VI-2 enthält: besonders bevorzugt solche ausgewählt aus der Gruppe bestehend aus den folgenden Formeln: worin R0 und X0 die oben angegebenen Bedeutungen haben.
Vorzugsweise bedeutet R0 in Formel VI Alkyl mit 1 bis 8 C-Atomen und X0 F;
- – LC-Medium, welches vorzugsweise eine oder mehrere Verbindungen der Formel VII, worin z0 -CF2O-, -CH2CH2 oder -(CO)O- bedeutet, enthält, besonders bevorzugt solche ausgewählt aus der Gruppe bestehend aus den folgenden Formeln: worin R0 und X0 die oben angegebenen Bedeutungen haben.
Vorzugsweise bedeutet R0 in Formel VII Alkyl mit 1 bis 8 C-Atomen und X0 F, ferner OCF3.
Die Verbindungen der Formel VIII sind vorzugsweise ausgewählt aus der Gruppe bestehend aus den folgenden Formeln: worin R0 und X0 die oben angegebenen Bedeutungen haben.
Vorzugsweise bedeutet R0 einen geradkettigen Alkylrest mit 1 bis 8 C-Atomen. X0 bedeutet vorzugsweise F.
- – LC-Medium, welches zusätzlich eine oder mehrere Verbindungen der folgenden Formel enthält: worin R0, X0, Y1 und Y2 die oben angegebene Bedeutung besitzen, und jeweils unabhängig voneinander bedeuten wobei die Ringe A und B nicht beide gleichzeitig Cyclohexylen bedeuten;
Die Verbindungen der Formel IX sind vorzugsweise ausgewählt aus der Gruppe bestehend aus den folgenden Formeln: worin R0 und X0 die oben angegebenen Bedeutungen haben.
Vorzugsweise bedeutet R0 Alkyl mit 1 bis 8 C-Atomen und X0 F. Besonders bevorzugt sind Verbindungen der Formel IXa;
- – LC-Medium, welches zusätzlich eine oder mehrere Verbindungen ausgewählt aus der Gruppe bestehend aus den folgenden Formeln enthält: worin R0, X0 und Y1-4 die oben angegebenen Bedeutungen besitzen, und jeweils unabhängig voneinander bedeuten;
Die Verbindungen der Formeln X und XI sind vorzugsweise ausgewählt aus der Gruppe bestehend aus den folgenden Formeln: worin R0 und X0 die oben angegebenen Bedeutungen haben.
Vorzugsweise bedeutet R0 Alkyl mit 1 bis 8 C-Atomen und/oder X0 F. Besonders bevorzugte Verbindungen sind solche, worin Y1 F und Y2 H oder F, vorzugsweise F, bedeuten;
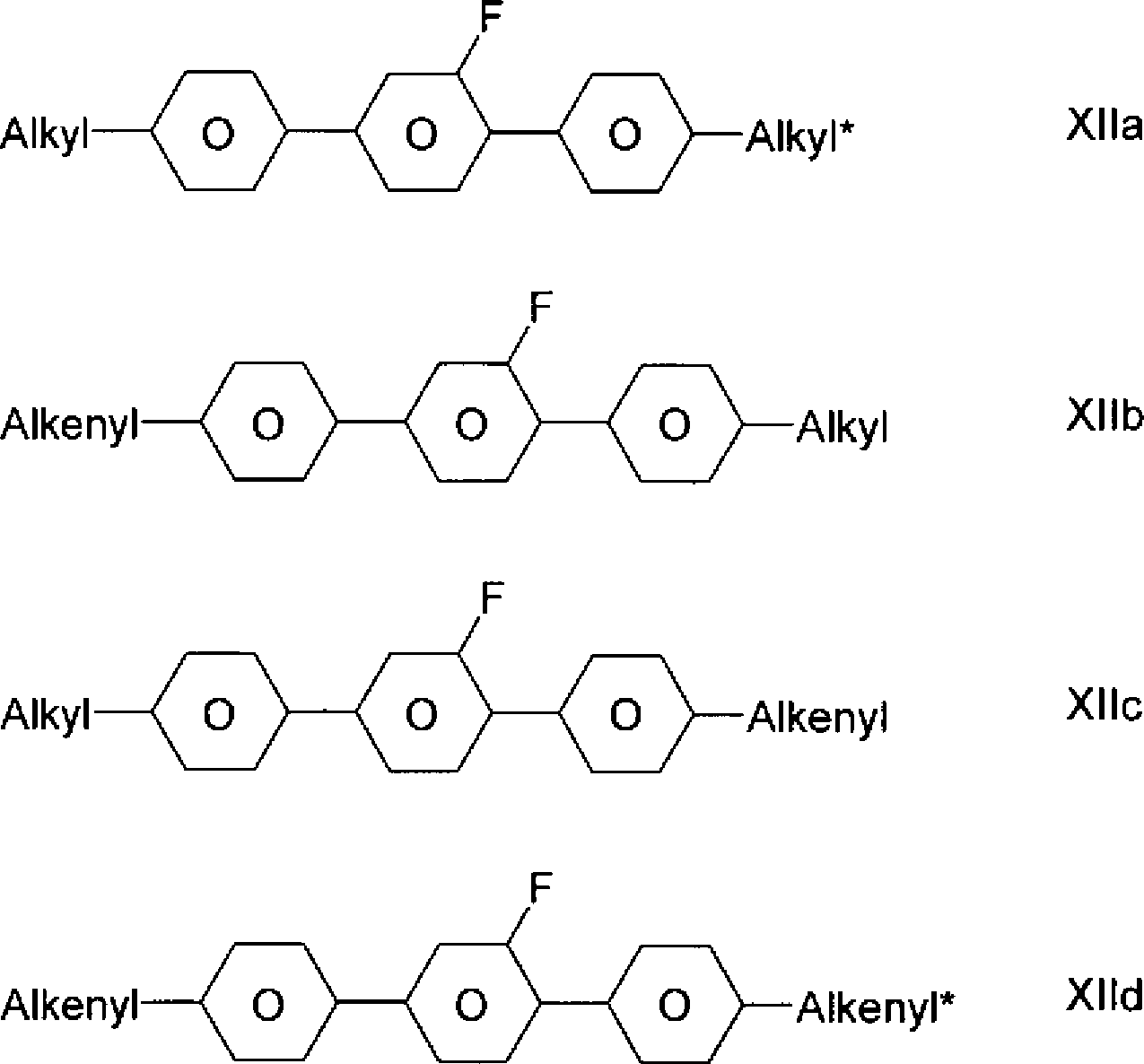
- – LC-Medium, welches zusätzlich eine oder mehrere Verbindungen der folgenden Formel XII enthält: worin R5 und R6 jeweils unabhängig voneinander n-Alkyl, Alkoxy, Oxaalkyl, Fluoralkyl oder Alkenyl mit jeweils bis zu 9 C-Atomen bedeuten, und vorzugsweise jeweils unabhängig voneinander Alkyl mit 1 bis 7 C-Atomen oder Alkenyl mit 2 bis 7 C-Atomen bedeuten. Y1 bedeutet H oder F.
Bevorzugte Verbindungen der Formel XII sind solche ausgewählt aus der Gruppe bestehend aus den folgenden Formeln: worin
Alkyl und Alkyl* jeweils unabhängig voneinander einen geradkettigen Alkylrest mit 1 bis 6 C-Atomen, und
Alkenyl und Alkenyl* jeweils unabhängig voneinander einen geradkettigen Alkenylrest mit 2 bis 6 C-Atomen
bedeuten.
Ganz besonders bevorzugt sind Verbindungen der folgenden Formel worin Alkyl die oben angegebene Bedeutung hat und R6a H oder CH3 bedeutet.
- – LC-Medium, welches zusätzlich eine oder mehrere Verbindungen ausgewählt aus der Gruppe bestehend aus den folgenden Formeln enthält: worin R0, X0, Y1 und Y2 die oben angegebenen Bedeutungen haben.
Vorzugsweise bedeutet R0 Alkyl mit 1 bis 8 C-Atomen und X0 F oder Cl;
Die Verbindungen der Formeln XIII und XIV sind vorzugsweise ausgewählt aus der Gruppe bestehend aus den folgenden Formeln: worin R0 und X0 die oben angegebenen Bedeutungen haben.
Vorzugsweise bedeutet R0 Alkyl mit 1 bis 8 C-Atomen. In den Verbindungen der Formel XIII bedeutet X0 vorzugsweise F oder Cl.
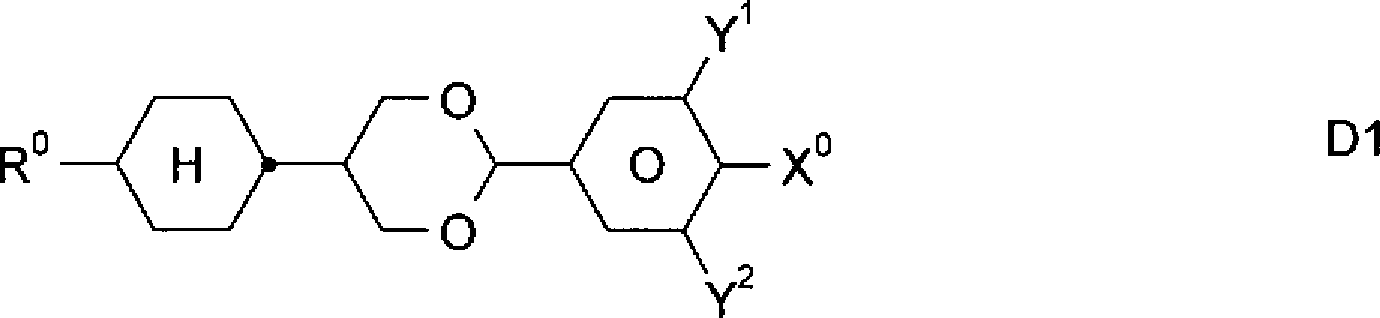
- – LC-Medium, welches zusätzlich eine oder mehrere Verbindungen der Formel D1 und/oder D2 enthält: worin Y1, Y2, R0 und X0 die oben angegebene Bedeutung besitzen.
Vorzugsweise bedeutet R0 Alkyl mit 1 bis 8 C-Atomen und X0 F. Besonders bevorzugt sind Verbindungen der folgenden Formeln: worin R0 die oben angegebenen Bedeutungen hat und vorzugsweise geradkettiges Alkyl mit 1 bis 6 C-Atomen, insbesondere C2H5, n-C3H7 oder n-C5H11 bedeutet.
- – LC-Medium, welches zusätzlich eine oder mehrere Verbindungen der folgenden Formeln enthält: worin Y1, R1 und R2 die oben angegebene Bedeutung besitzen. R1 und R2 bedeuten vorzugsweise jeweils unabhängig voneinander Alkyl mit 1 bis 8 C-Atomen. Y1 bedeutet vorzugsweise F. Bevorzugte Medien enthalten 1–15 Gew.-%, insbesondere 1–10 Gew.-% dieser Verbindungen.
- – LC-Medium, welches zusätzlich eine oder mehrere Verbindungen der folgenden Formel enthält: worin X0, Y1 und Y2 die oben angegebenen Bedeutungen besitzen und ”Alkenyl” C2-7-Alkenyl bedeutet. Besonders bevorzugt sind Verbindungen der folgenden Formel, worin R3a die oben angegebene Bedeutung hat und vorzugsweise H bedeutet;
- – LC-Medium, welches zusätzlich eine oder mehrere Vierkern-Verbindungen ausgewählt aus der Gruppe bestehend aus den Formeln XIX bis XXV enthält: worin Y1-4 , R0 und X0 jeweils unabhängig voneinander eine der oben angegebenen Bedeutungen haben. X0 ist vorzugsweise F, Cl, CF3, OCF3 oder OCHF2. R0 bedeutet vorzugsweise Alkyl, Alkoxy, Oxaalkyl, Fluoralkyl oder Alkenyl mit jeweils bis zu 8 C-Atomen.
- – LC-Medium, welches zusätzlich eine oder mehrere Verbindungen der folgenden Formel enthält: worin R0, X0 und Y1-4 die oben angegebenen Bedeutungen besitzen. Besonders bevorzugt sind Verbindungen der folgenden Formel:
- – R0 ist im Allgemeinen vorzugsweise geradkettiges Alkyl oder Alkenyl mit 2 bis 7 C-Atomen;
- – X0 ist vorzugsweise F, ferner OCF3, Cl oder CF3;
- – Das Medium enthält vorzugsweise eine oder mehrere Verbindungen ausgewählt aus der Gruppe der Verbindungen der Formel II;
- – Das Medium enthält vorzugsweise eine oder mehrere Verbindungen ausgewählt aus der Gruppe der Verbindungen der Formeln VI-2, VII-1a, VII-1b, IX, X, XI und XXVI (CF2O-verbrückte Verbindungen); der Gesamtgehalt an Verbindungen der Formeln VI-2, VII-1a, VII-1b, IX, X, XI und XXVI beträgt bevorzugt 35 Gew.-% oder mehr, besonders bevorzugt 40 Gew.-% oder mehr und ganz besonders bevorzugt 45 Gew.-% oder mehr.
- – Der Anteil an Verbindungen der Formeln II-XXVII im Gesamtgemisch beträgt vorzugsweise 20 bis 99 Gew.-%;
- – Das Medium enthält vorzugsweise 25–80 Gew.-%, besonders bevorzugt 30–70 Gew.-% an Verbindungen der Formel II und/oder III;
- – Das Medium enthält vorzugsweise 20-70 Gew.-%, besonders bevorzugt 25–60 Gew.-% an Verbindungen der Formel IIa;
- – Das Medium enthält vorzugsweise 2–25 Gew.-%, besonders bevorzugt 3–20 Gew.-% ausgewählt aus der Gruppe der Verbindungen der VI-2;
- – Das Medium enthält insgesamt 2–30 Gew.-%, besonders bevorzugt 3–20 Gew.-% an Verbindungen der Formeln XI und XXVII zusammen;
- – Das Medium enthält vorzugsweise 1–20 Gew.-%, besonders bevorzugt 2–15 Gew.-% an Verbindungen der Formel XXIV;
- – Das Medium enthält insgesamt 15–65 Gew.-%, besonders bevorzugt 30–55 Gew.-% ausgewählt aus den hochpolaren Verbindungen der Formeln VI-2, X, XI und XXV zusammen.
-
Die nematische Phase des dielektrisch negativen oder positiven FK-Mediums gemäß der Erfindung hat bevorzugt eine nematische Phasen in einem Temperaturbereich von 10°C oder weniger bis 60°C oder mehr, besonders bevorzugt von 0 oder weniger bis 70°C oder mehr.
-
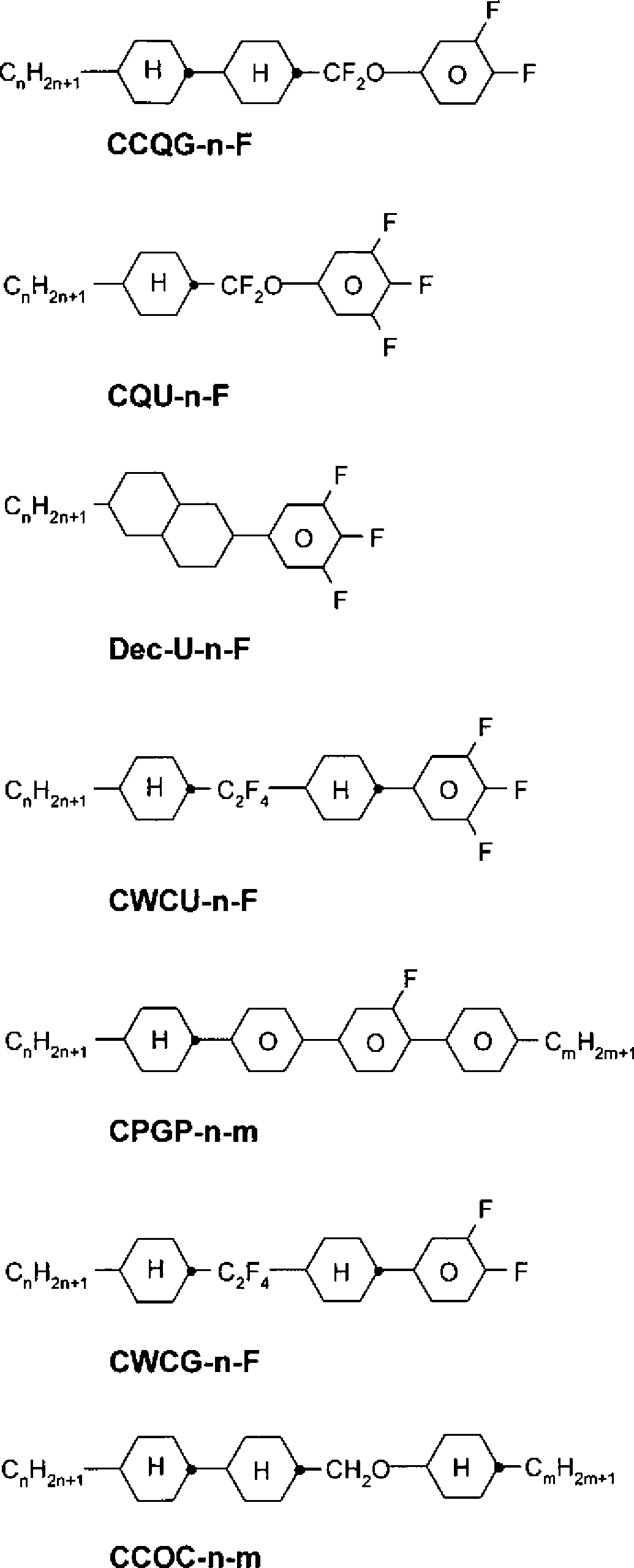
In der vorliegenden Anmeldung und in den folgenden Beispielen sind die Strukturen der Flüssigkristallverbindungen durch Akronyme angegeben, wobei die Transformation in chemische Formeln gemäß folgender Tabellen A und B erfolgt. Alle Reste C
nH
2n+1 und C
mH
2m+1 sind geradkettige Alkylreste mit n bzw. m C-Atomen; n, m, z und k sind ganze Zahlen und bedeuten vorzugsweise 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 oder 12. Die Codierung gemäß Tabelle B versteht sich von selbst. In Tabelle A ist nur das Akronym für den Grundkörper angegeben. Im Einzelfall folgt getrennt von Akronym für den Grundkörper mit einem Strich ein Code für die Substituenten R
1*, R
2*, L
1* und L
2*:
| Code für R1*, R2*, L1*, L2*, L3* | R1* | R2* | L1* | L2* |
| nm | CnH2n+1 | CmH2m+1 | H | H |
| nOm | CnH2n+1 | OCmH2m+1 | H | H |
| nO·m | OCnH2n+r | CmH2m+1 | H | H |
| n | CnH2n+1 | CN | H | H |
| nN·F | CnH2n+1 | CN | F | H |
| nN·F·F | CnH2n+1 | CN | F | F |
| nF | CnH2n+1 | F | H | H |
| nCl | CnH2n+1 | Cl | H | H |
| nOF | OCnH2n+1 | F | H | H |
| nF·F | CnH2n+1 | F | F | H |
| nF·F·F | CnH2n+1 | F | F | F |
| nOCF3 | CnH2n+1 | OCF3 | H | H |
| nOCF3·F | CnH2n+1 | OCF3 | F | H |
| n-Vm | CnH2n+1 | -CH=CH-CmH2m+1 | H | H |
| nV-Vm | CnH2n+1-CH=CH- | -CH=CH-CmH2m+1 | H | H |
-
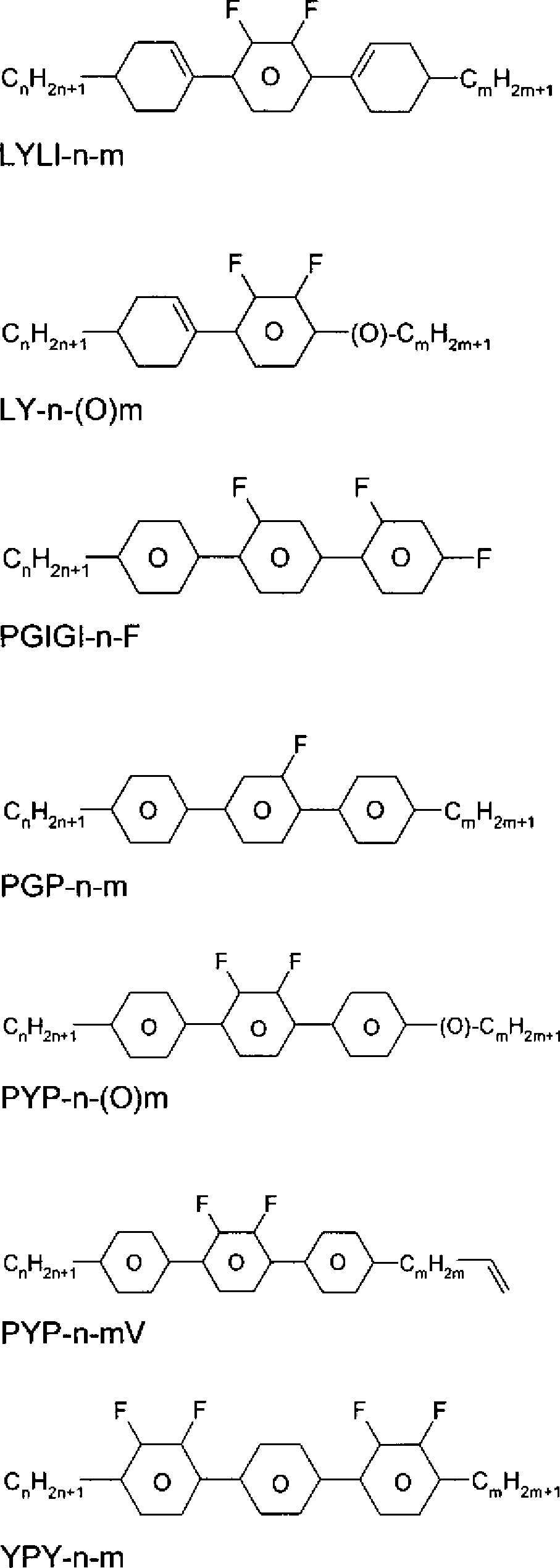
Bevorzugte Mischungskomponenten finden sich in den Tabellen A und B. Tabelle A
-
Tabelle B
-
n, m, z bedeuten unabhängig voneinander vorzugsweise 1, 2, 3, 4, 5 oder 6.
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
In einer bevorzugten Ausführungsform der vorliegenden Erfindung enthalten die erfindungsgemäßen LC-Medien eine oder mehrere Verbindungen ausgewählt aus der Gruppe bestehend aus Verbindungen der Tabelle A und B.
-
Tabelle C
-
In der Tabelle C werden mögliche chirale Dotierstoffe angegeben, die den erfindungsgemäßen FK-Medien zugesetzt werden können.
-
-
-
-
Optional enthalten die FK-Medien 0 bis 10 Gew.-%, insbesondere 0,01 bis 5 Gew.-%, besonders bevorzugt 0,1 bis 3 Gew.-% an Dotierstoffen, vorzugsweise ausgewählt aus der Gruppe bestehend aus Verbindungen der Tabelle C.
-
Tabelle D
-
In der Tabelle D werden mögliche Stabilisatoren angegeben, die den erfindungsgemaßen FK-Medien zugesetzt werden können.
(n bedeutet hier eine ganze Zahl von 1 bis 12, vorzugsweise 1, 2, 3, 4, 5, 6, 7 oder 8, endständige Methylgruppen sind nicht gezeigt).
-
-
-
-
-
-
Vorzugsweise enthalten die FK-Medien 0 bis 10 Gew.-%, insbesondere 1 ppm bis 5 Gew.-%, besonders bevorzugt 1 ppm bis 1 Gew.-% an Stabilisatoren. Vorzugsweise enthalten die FK-Medien einen oder mehrere Stabilisatoren ausgewählt aus der Gruppe bestehend aus Verbindungen der Tabelle D.
-
Tabelle E
-
In der Tabelle E sind Beispielverbindungen zusammengestellt, die in den FK-Medien gemäß der vorliegenden Erfindung vorzugsweise als polymerisierbare Verbindungen verwendet werden können.
-
-
-
-
In einer bevorzugten Ausführungsform der vorliegenden Erfindung enthalten die mesogenen Medien eine oder mehrere Verbindungen ausgewählt aus der Gruppe der Verbindungen der Tabelle E.
-
In der vorliegenden Anmeldung bedeutet der Begriff „Verbindungen”, auch geschrieben als „Verbindung(en)”, sofern nicht explizit anders angegeben, sowohl eine als auch mehrere Verbindungen. Umgekehrt schließt der Begriff ”Verbindung” generell auch mehrere Verbindungen ein, sofern dies laut Definition möglich und nicht anders angegeben ist. Gleiches gilt für die Begriffe FK-Medien und FK-Medium. Der Begriff ”Komponente” umfasst jeweils eine oder mehrere Stoffe, Verbindungen und/oder Teilchen.
-
Außerdem werden folgende Abkürzungen und Symbole verwendet:
- ne
- außerordentlicher Brechungsindex bei 20°C und 589 nm,
- no
- ordentlicher Brechungsindex bei 20°C und 589 nm,
- Δn
- optische Anisotropie bei 20°C und 589 nm,
- ε⊥
- dielektrische Permittivität senkrecht zum Direktor bei 20°C und 1 kHz,
- ε||
- dielektrische Permittivität parallel zum Direktor bei 20°C und 1 kHz,
- Δε
- dielektrische Anisotropie bei 20°C und 1 kHz,
- Kp., T(N, I)
- Klärpunkt [°C],
- γ1
- Rotationsviskosität bei 20°C [mPa·s],
- K1
- elastische Konstante, ”splay”-Deformation bei 20°C [pN],
- K2
- elastische Konstante, ”twist”-Deformation bei 20°C [pN],
- K3
- elastische Konstante, ”bend”-Deformation bei 20°C [pN].
-
Soweit nicht explizit anders vermerkt, sind in der vorliegenden Anmeldung alle Konzentrationen in Gewichtsprozent angegeben und beziehen sich auf die entsprechende Gesamtmischung, enthaltend alle festen oder flüssigkristallinen Komponenten, ohne Lösungsmittel.
-
Alle physikalischen Eigenschaften werden und wurden nach ”Merck Liquid Crystals, Physical Properties of Liquid Crystals”, Status Nov. 1997, Merck KGaA, Deutschland bestimmt und gelten für eine Temperatur von 20°C, Δn wird bei 589 nm und Δε bei 1 kHz bestimmt, sofern nicht jeweils explizit anders angegeben.
-
Die polymerisierbaren Verbindungen werden in der Anzeige bzw. Testzelle durch Bestrahlung mit UVA-Licht (üblicherweise 365 nm) einer definierten Intensität für eine vorgegebene Zeit polymerisiert, wobei optional gleichzeitig eine Spannung an die Anzeige angelegt wird (üblicherweise 5 bis 30 V Wechselstrom, 1 kHz). In den Beispielen wird, falls nicht anders angegeben, eine Quecksilberdampflampe mit 100 mW/cm2 verwendet, die Intensität wird mit einem Standard-UV-Meter (Fabrikat Ushio UNI meter) gemessen, der mit einem Bandpassfilter bei 320 nm oder 340 nm ausgerüstet ist.
-
Die folgenden Beispiele erläutern die vorliegende Erfindung, ohne sie in irgendeiner Weise beschränken zu sollen. Aus den physikalischen Eigenschaften wird dem Fachmann jedoch deutlich, welche Eigenschaften zu erzielen sind und in welchen Bereichen sie modifizierbar sind. Insbesondere ist also die Kombination der verschiedenen Eigenschaften, die vorzugsweise erreicht werden können, für den Fachmann gut definiert.
-
Weitere Kombinationen der Ausführungsformen und Varianten der Erfindung gemäß der Beschreibung ergeben sich auch aus den Ansprüchen.
-
Beispiele
-
Die eingesetzten Verbindungen, soweit nicht kommerziell erhältlich, werden nach Standard-Laborvorschriften synthetisiert. Die FK-Medien stammen von der Merck KGaA, Deutschland.
-
Die verwendeten selbstorientierenden, langkettigen Alkohole und Amine sind kommerziell erhältlich und werden ggf. vor der Verwendung gereinigt.
-
Folgende selbstorientierende Verbindungen werden in erfindungsgemäßen FK-Medien verwendet:
-
Mischungsbeispiele
-
Zur Herstellung von erfindungsgemßen FK-Medien werden die folgenden flüssigkristallinen Mischungen bestehend aus niedermolekularen Komponenten in den angegebenen prozentualen Gewichtsanteilen verwendet. Tabelle 1: Nematisches FK-Medium M1 (Δε < 0)
| CY-3-O4 | 14% | Kp. | + 80°C |
| CCY-3-O2 | 9% | Δn | 0,090 |
| CCY-3-O3 | 9% | Δε | –3,3 |
| CPY-2-O2 | 10% | ε|| | 3,4 |
| CPY-3-O2 | 10% | K3/K1 | 0,97 |
| CCY-3-1 | 8% | | |
| CCH-34 | 9% | | |
| CCH-35 | 6% | | |
| PCH-53 | 10% | | |
| CCH-301 | 6% | | |
| CCH-303 | 9% | | |
Tabelle 2: Nematisches FK-Medium M2 (Δε > 0)
| CC-4-V | 10% | Kp. | +77°C |
| CC-5-V | 13.5% | Δn | 0.113 |
| PGU-3-F | 6.5% | Δε | 19.2 |
| ACQU-2-F | 10% | ε|| | 23.8 |
| ACQU-3-F | 12% | K3/K1 | 0.97 |
| PUQU-3-F | 11% | | |
| CCP-V-1 | 12% | | |
| APUQU-2-F | 6% | | |
| APUQU-3-F | 7% | | |
| PGUQU-3-F | 8% | | |
| CPGU-3-OT | 4% | | |
-
Mischungsbeispiel 1 (a/b), ohne Polymerstabilisierung
-
Zu einem nematischen FK-Medium M1 des VA-Typs (Δε < 0) gemäß Tabelle 1 wird die Verbindung Nr. 1 (2,0 Gew.-%) zugesetzt und homogenisiert.
-
Verwendung in Testzellen ohne Vororientierungsschicht ('alignment layer'):
- a) Die entstandene Mischung wird in eine mono-Domain-Testzelle gefüllt (ohne Polyimid-Orientierungsschicht, Schichtdicke d ≈ 4,0 μm, Glass-Substrat, beidseitige ITO-Beschichtung, ohne Passivierungsschicht). Das FK-Medium weist eine spontane homöotrope (vertikale) Orientierung zu den Substratoberflächen auf. Diese Orientierung bleibt bis 70°C stabil. Im temperaturstabilen Bereich lässt sich die VA-Zelle zwischen gekreuzten Polarisatoren durch Anlegen einer Spannung zwischen 0 und 30 V reversibel schalten.
- b) Die entstandene Mischung wird in eine zwei-Domain-Testzelle gefüllt (ohne Polyimid-Orientierungsschicht, Schichtdicke d ≈ 4,0 μm, Glass-Substrat, beidseitige strukturierte ITO-Beschichtung (10 μm slit width), ohne Passivierungsschicht). Das FK-Medium weist eine spontane homöotrope (vertikale) Orientierung zu den Substratoberflächen auf. Diese Orientierung bleibt bis 40°C stabil. Im temperaturstabilen Bereich lässt sich die VA-Zelle zwischen gekreuzten Polarisatoren durch Anlegen einer Spannung zwischen 0 und 30 V reversibel schalten.
-
Mischungsbeispiel 2, ohne Polymerstabilisierung
-
Zu einem nematischen FK-Medium M2 des VA-IPS-Typs (Δε > 0) gemäß Tabelle 2 wird die Verbindung Nr. 1 (2,0 Gew.-%) zugesetzt und homogenisiert.
-
Verwendung in Testzellen ohne Vororientierungsschicht ('alignment layer'): Die entstandene Mischung wird in eine mono-Domain-Testzelle gefüllt (ohne Polyimid-Orientierungsschicht, Schichtdicke d ≈ 4,0 μm, Glass-Substrat, beidseitige ITO-Beschichtung, ohne Passivierungsschicht). Das FK-Medium weist eine spontane homöotrope (vertikale) Orientierung zu den Substratoberflächen auf.
-
Mischungsbeispiele 3–10 (a/b), ohne Polymerstabilisierung
-
Die Verbindungen Nr. 2–9 werden analog Mischungsbeispiel 1 zu einem nematischen FK-Medium M1 (Δε < 0) gemäß Tabelle 1 zugesetzt und homogenisiert Die Gewichtsanteile der Verbindungen im Medium sind in der Tabelle 3 angegeben. Das erhaltene FK-Medium wird jeweils in eine mono-Domain (a) und in eine zwei-Domain-Testzelle (b) ohne Vororientierungsschicht gefüllt. Die erhaltene Orientierung (homöotrope (vertikale) oder planar) zu den Substratoberflächen ist in Tabelle 3 angegeben. Im temperaturstabilen Bereich lassen sich die VA-Zelle (homöotrope Orientierung) zwischen gekreuzten Polarisatoren durch Anlegen einer Spannung zwischen 0 und 30 V reversibel schalten. Tabelle 3: Gewichtsanteile für Dotierung in M1 und Orientierung der erhaltenen FK-Mischung bei 20°C und 70°C.
| | a) Mono-Domain-Zelle | b) Zwei-Domain-Zelle |
| Mischungsbeispiel | Verbindung Nr. | Gewichtsanteil | Orientierung bei 20°C | Orientierung bei 70°C | Orientierung bei 20°C | Orientierung bei 70°C |
| 3 (Vergleich) | 2 | 2,0% | planar | planar | planar | planar |
| 4 | 3 | 0,6% | homöotrop | homöotrop | planar | planar |
| 5 (Vergleich) | 4 | 2,0% | homöotrop | - | planar | planar |
| 6 | 5 | 1,0% | homöotrop | homöotrop | homöotrop | homöotrop |
| 7 | 6 | 0,5% | homöotrop | Planar | homöotrop | planar |
| 8 | 7 | 0,3% | homöotrop | homöotrop | homöotrop | - |
| 9 | 8 | 0,3% | homöotrop | homöotrop | homöotrop | homöotrop |
| 10 | 9 | 2,0% | homöotrop | homöotrop | homöotrop | homöotrop |
-
Die Zellen mit homöotroper Orientierung lassen sich reversibel schalten.
-
Mischungsbeispiele 11–18
-
Die Verbindungen Nr. 2–9 werden analog Mischungsbeispiel 2 zu einem nematischen FK-Medium M2 (Δε > 0) gemäß Tabelle 1 zugesetzt und homogenisiert. Die Gewichtsanteile der Verbindungen im Medium sind in der Tabelle 4 angegeben. Das erhaltene FK-Medium wird in eine mono-Domain-Testzelle ohne Vororientierungsschicht gefüllt. Die erhaltene Orientierung (homootrope (vertikale) oder Planar) zu den Substratoberflächen ist in Tabelle 4 angegeben. Tabelle 4: Gewichtsanteile für Dotierung in M2 und Orientierung der erhaltenen FK-Mischung bei 20°C. Mono-domain Testzelle.
| Mischungsbeispiel | Verbindung Nr. | Gewichtsanteil | Orientierung bei 20°C |
| 11 (Vergleich) | 2 | 2,0% | planar |
| 12 | 3 | 0,6% | homöotrop |
| 13 (Vergleich) | 4 | 2,0% | planar |
| 14 | 5 | 1,0% | homöotrop |
| 15 | 6 | 0,5% | homöotrop |
| 16 | 7 | 0,3% | homöotrop |
| 17 | 8 | 0,3% | homöotrop |
| 18 | 9 | 2,0% | homöotrop |
-
Mischungsbeispiele 19–21 (Polymerstabilisierunq von Mischungsbeispiel 1, 4 und 6)
-
Zu einem nematischen FK-Medium M1 (Δε < 0) gemäß Tabelle 1 werden eine polymerisierbare Verbindung (RM-1, 0,5 Gew.-%) und eine selbstorientierende Verbindung gemäß Tabellen 5.a und 5.b zugesetzt und homogenisiert.
-
Verwendung in Testzellen ohne Vororientierungsschicht ('alignment layer'):
-
a) Die entstandene Mischung (Tabelle 5a) wird in eine mono-Domain-Testzelle gefüllt (ohne Polyimid-Orientierungsschicht, Schichtdicke d 4,0 μm, Glass-Substrat, beidseitige ITO-Beschichtung, ohne Passivierungsschicht). Das FK-Medium weist eine spontane homöotrope (vertikale) Orientierung zu den Substratoberflächen auf.
-
Unter Anlegen einer Spannung großer als die optische Schwellenspannung wird die Zelle 15 min mit UV-Licht der Intensität 100 mW/cm
2 bei 40°C bestrahlt. Dadurch erfolgt Polymerisation der monomeren, polymerisierbaren Verbindung. Die homöotrope Orientierung wird damit zusätzlich stabilisiert und ein 'pre-tilt' wird eingestellt. Die erhaltene PSA-VA-Zelle lässt sich bis 70°C unter Anlegen einer Spannung zwischen 0 und 30 V reversibel schalten. Die Schaltzeiten sind, im Vergleich zu den nicht polymerisierten Beispielen, verkürzt. Tabelle 5.a: Gewichtsanteile für Polymerstabilisierung in M1 und Orientierung der erhaltenen FK-Mischung bei 20°C und 70°C, vor und nach Temperaturbelastungstest bei 120°C. Mono-Domain-Zellen (a).
| | vor Belastung | nach Belastung (Anzahl Tage bei 120°C) |
| Mischungsbeispiel | Verbindung Beispiel Nr. (Gewichts.) | RM-1, Gewichtsanteil | Orientierung bei 20°C | Orientierung bei 70°C | Orientierung bei 20°C | Orientierung bei 70°C |
| 1 | 1 (2,0%) | 0% | homöotrop | homöotrop | homöotrop
(7 Tage) | planar
(7 Tage) |
| 4 | 3 (0,6%) | 0% | homöotrop | homöotrop | planar
(1 Tag) | planar
(1 Tag) |
| 6 | 5 (1,0%) | 0% | homöotrop | homöotrop | planar
(1 Tag) | planar
(1 Tag) |
| 19 | 1 (2,0%) | 0,5% | homöotrop | homöotrop | homöotrop
(7 Tage) | homöotrop
(7 Tage) |
| 20 | 3 (0,6%) | 0,5% | homöotrop | homöotrop | homöotrop
(1 Tag) | homöotrop
(1 Tag) |
| 21 | 5 (1,0%) | 0,5% | homöotrop | homöotrop | homöotrop
(1 Tag) | homöotrop
(1 Tag) |
-
Die Zellen mit homöotroper Orientierung lassen sich reversibel schalten.
- b) Die entstandene Mischung (Tabelle 5b) wird in eine zwei-Domain-Testzeile gefüllt (ohne Polyimid-Orientierungsschicht, Schichtdicke d 4,0 μm, Glass-Substrat, beidseitige strukturierte ITO-Beschichtung (10 μm slit width), ohne Passivierungsschicht). Das FK-Medium weist eine spontane homöotrope (vertikale) Orientierung zu den Substratoberflächen auf. Unter Anlegen einer Spannung größer als die optische Schwellenspannung wird die Zelle 15 min mit UV-Licht der Intensität 100 mW/cm2 bei 40°C bestrahlt. Dadurch erfolgt Polymerisation der monomeren, polymerisierbaren Verbindung. Die homöotrope Orientierung wird damit zusätzlich stabilisiert und ein 'pretilt wird eingestellt. Die erhaltene PSA-VA-Zelle lässt sich bis 70°C unter Anlegen einer Spannung zwischen 0 und 30 V reversibel schalten. Die Schaltzeiten sind, im Vergleich zu den nicht polymerisierten Beispielen, verkürzt.
-
Temperaturbelastungstest von Mischungsbeispiel 1, 6, 19–21
-
Die FK-Medien der Mischungsbeispiele 1, 6, 19-21 werden in mono- und zwei-Domain-Testzellen gefüllt. Die polymerisierbaren Verbindungen werden wie angegeben polymerisiert. Alle Zellen sind bei 120°C für die angegebene Zahl von Tagen dem Wärmebelastungstest ausgesetzt (Tabelle 5.a und 5.b). Die elektrooptischen Kurven werden vor und nach der Temperaturbelastung untersucht. Während nach Belastung ohne Polymerstabilisierung wesentliche Unterschiede in den Schaltkurven bis zum kompletten Verlust der selbst-induzierten homöotropen Orientierung beobachtet werden, bleiben die Eigenschaften der polymerstabilisierten Zellen zwischen 20°C und 70°C praktisch unverändert. Tabelle 5.b: Gewichtsanteile für Polymerstabilisierung in M1 und Orientierung der erhaltenen FK-Mischung bei 20°C und 70°C, vor und nach Temperatur Belastung beim 120°C. Zwei-Domain-Zellen (b).
| | vor Belastung | nach Belastung (Anzahl Tage bei 120°C) |
| Mischungsbeispiel | Verbindung Beispiel Nr.(Gewichts.) | RM-1, Gewichtsanteil | Orientierung bei 20°C | Orientierung bei 70°C | Orientierung bei 20°C | Orientierung bei 70°C |
| 1 | 1 (2,0%) | 0% | homöotrop | planar | planar
(1 Tag) | planar
(1 Tag) |
| 6 | 5 (1,0%) | 0% | homöotrop | homöotrop | homöotrop
(6 Tage) | planar
(6 Tage) |
| 19 | 1 (2,0%) | 0,5% | homöotrop | homöotrop | homöotrop
(1 Tag) | homöotrop
(1 Tag) |
| 21 | 5 (1,0%) | 0,5% | homöotrop | homöotrop | homöotrop
(6 Tage) | homöotrop
(6 Tage) |
-
Die Zellen mit homöotroper Orientierung lassen sich reversibel schalten.
-
ZITATE ENTHALTEN IN DER BESCHREIBUNG
-
Diese Liste der vom Anmelder aufgeführten Dokumente wurde automatisiert erzeugt und ist ausschließlich zur besseren Information des Lesers aufgenommen. Die Liste ist nicht Bestandteil der deutschen Patent- bzw. Gebrauchsmusteranmeldung. Das DPMA übernimmt keinerlei Haftung für etwaige Fehler oder Auslassungen.
-
Zitierte Patentliteratur
-
- DE 4000451 [0006]
- EP 0588568 [0006]
- JP 10-036847 A [0021]
- EP 1170626 A2 [0021]
- US 6861107 [0021]
- US 7169449 [0021, 0024]
- US 2004/0191428 A1 [0021]
- US 2006/0066793 A1 [0021]
- US 2006/0103804 A1 [0021]
- US 6177972 [0021]
- WO 2010/089092 A1 [0021]
- US 2008/0198301 A1 [0027]
- US 4022934 A [0030]
- US 3972589 [0031]
- DE 2356889 A1 [0031]
- US 3848966 [0031]
- EP 1378557 A1 [0084]
- JP 07-181439 A [0085]
- EP 0667555 [0085]
- EP 0673986 [0085]
- DE 19509410 [0085]
- DE 19528106 [0085]
- DE 19528107 [0085]
- WO 96/23851 [0085]
- WO 96/28521 [0085]
-
Zitierte Nicht-Patentliteratur
-
- M. F. Schieckel und K. Fahrenschon, ”Deformation of nematic liquid crystals with vertical orientation in electrical fields”, Appl. Phys. Lett. 19 (1971), 3912 [0002]
- J. F. Kahn (Appl. Phys. Lett. 20 (1972), 1193) [0002]
- G. Labrunie und J. Robert (J. Appl. Phys. 44 (1973), 4869) [0002]
- J. Robert und F. Clerc (SID 80 Digest Techn. Papers (1980), 30), J. Duchene (Displays 7 (1986), 3) [0003]
- H. Schad (SID 82 Digest Techn. Papers (1982), 244) [0003]
- Yoshide, H. et al., Vortrag 3.1: ”MVA LCD for Notebook or Mobile PCs ...”, SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch I, S. 6 bis 9 [0004]
- Liu, C. T. et al., Vortrag 15.1: ”A 46-inch TFT-LCD HDTV Technology ...”, SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch II, S. 750 bis 753 [0004]
- Kim, Sang Soo, Vortrag 15.4: ”Super PVA Sets New State-of-the-Art for LCD-TV”, SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch II, S. 760 bis 763 [0004]
- Shigeta, Mitzuhiro und Fukuoka, Hirofumi, Vortrag 15.2: ”Development of High Quality LCDTV”, SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch II, S. 754 bis 757 [0004]
- Yeo, S. D., Vortrag 15.3: ”A LC Display for the TV Application”, SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch II, S. 758 & 759 [0004]
- Souk, Jun, SIDSeminar 2004, Seminar M-6: ”Recent Advances in LCD Technology”, Seminar Lecture Notes, M-6/1 bis M-6/26 [0004]
- Miller, Ian, SIDSeminar 2004, Seminar M-7: ”LCD-Television”, Seminar Lecture Notes, M-7/1 bis M-7/32 [0004]
- Kim, Hyeon Kyeong et al., Vortrag 9.1: ”A 57-in. Wide UXGA TFT-LCD for HDTV Application”, SID 2004 International Symposium, Digest of Technical Papers, XXXV, Buch I, S. 106 bis 109 [0004]
- S. H. Lee et al. Appl. Phys. Lett. (1997), 71, 2851–2853 [0006]
- K. S. Hun et al. J. Appl. Phys. (2008), 104, 084515 [0007]
- M. Jiao et al. App. Phys. Lett (2008), 92, 111101 (DFFS: 'dual fringe field switching' für verbesserte Schaltzeiten) [0007]
- Y. T. Kim et al. Jap. J. App. Phys. (2009), 48, 110205 (VAS: 'viewing angle switchable' LCD) [0007]
- T. -J- Chen et al., Jpn. J. Appl. Phys. 45, 2006, 2702–2704 [0021]
- S. H. Kim, L. -C- Chien, Jpn. J. Appl. Phys. 43, 2004, 7643–7647 [0021]
- Appl. Phys. Lett. 1999, 75(21), 3264 [0021]
- Optics Express 2004, 12(7), 1221 [0021]
- Druckschrift Shie-Chang Jeng et al. Optics Letters (2009), 34, 455–457 [0026]
- H. Y. Gim et al., P-128 [0029]