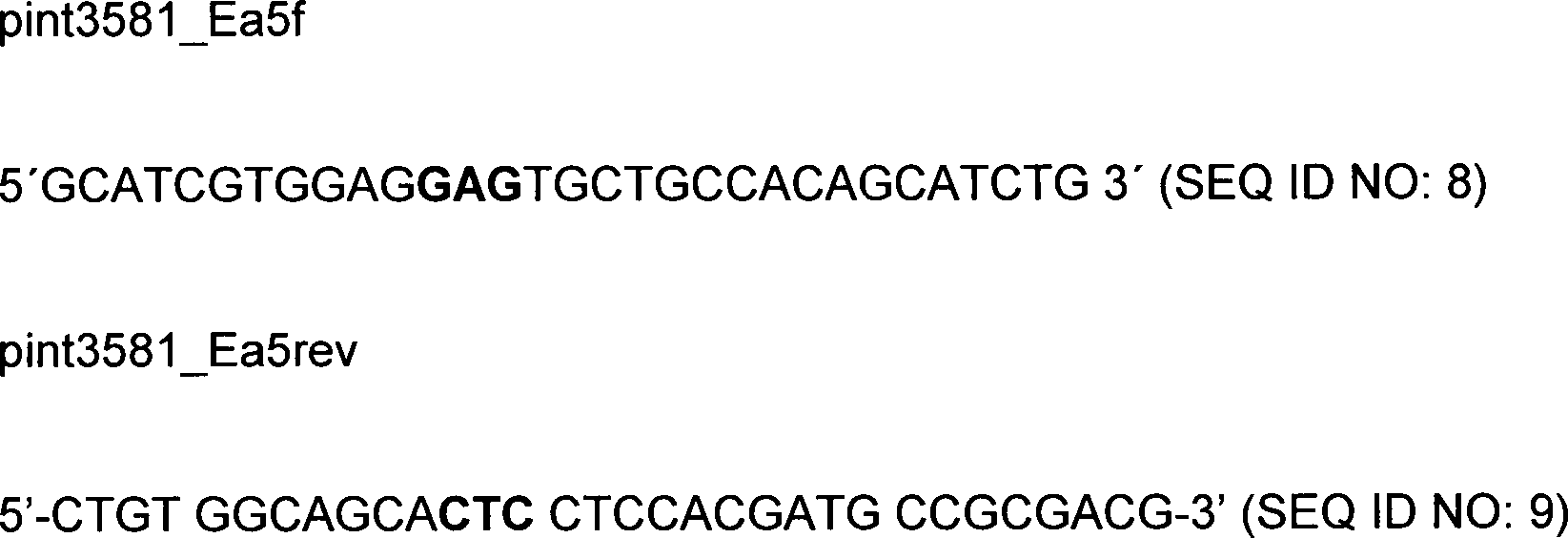-
Die
Erfindung betrifft neue Insulinanaloga mit basalem Zeit-/Wirkungsprofil,
ihre Herstellung und Verwendung.
-
Über
die letzten Jahre hat die Zahl der Erkrankungen an Diabetes in einem
geradezu epidemischen Ausmaß zugenommen. Aufgrund der Erkrankung
kann es zu einer gravierenden Verkürzung der Lebenserwartung
kommen. Menschen mit Diabetes müssen ihrem Körper
oft Insulin von außen zuführen. Es ist sinnvoll, die
Behandlung mit Insulin zu optimieren. Mittlerweile gibt es unterschiedliche
Insuline mit spezifischen pharmakologischen Eigenschaften zur Behandlung.
Praktischerweise werden die unterschiedlichen Insuline nach ihrer
Wirkdauer unterschieden in kurzwirksame Insuline, schnellwirkende
Insuline, langwirksame Insuline und Mischinsuline. Synonym verwendete
Bezeichnungen für langwirksame Insuline sind Verzögerungsinsulin,
Depotinsulin oder auch Basalinsulin. Die Wirkstoffe vieler dieser
Insulinpräparate sind sogenannte Insulinanaloga, die vom
humanen Insulin abgeleitet worden sind durch Substitution, Deletion
und/oder Addition einer oder mehrerer Aminosäuren. Die
Begriffe „Insulinanaloga” und „Insuline” werden
hier synonym verwendet.
-
Das
Konzept der intensivierten Insulintherapie versucht das Gesundheitsrisiko
abzumindern, indem eine stabile Kontrolle des Blutzuckerspiegels
durch frühe Gabe von Basalinsulinen angestrebt wird. Ein
Beispiel für ein gängiges Basalinsulin ist das
Medikament Lantus® (Wirkstoff:
Insulin Glargin = Gly(A21),Arg(B31),Arg(B32) Humaninsulin). Generell
gilt es, bei der Entwicklung neuer, verbesserter Basalinsuline die
Zahl hypoglykämischer Ereignisse zu minimieren. Ein ideales
Basalinsulin wirkt dabei sicher in jedem Patienten mindestens 24
h Stunden. Idealerweise setzt die Insulinwirkung verzögert
und mit einem möglichst flachen Zeit-/Wirkungsprofil ein,
so dass die Gefahr einer kurzfristigen Unterzuckerung deutlich minimiert ist
und die Applikation sogar ohne vorherige Einnahme von Nahrungsmitteln
erfolgen kann. Eine gute Versorgung mit Basalinsulin ist dann gegeben,
wenn die Insulinwirkung möglichst lange gleichbleibend
anhält, d. h. der Körper mit einer konstanten
Menge Insulin versorgt wird. Damit ist die Gefahr hypoglykämischer
Ereignisse gering und eine Patienten- und tagesspezifische Variabilität
minimiert. Das pharmakokinetische Profil eines idealen Basalinsulins
sollte also durch einen verzögerten Wirkeintritt und durch
eine verzögerte, d. h. lang anhaltende und gleichmäßige
Wirkung gekennzeichnet sein.
-
Jedoch
zeigt – trotz der bereits erreichten therapeutischen Vorteile – keines
der bisher beschriebenen Verzögerungsinsuline die pharmakokinetischen
Eigenschaften eines idealen Basalinsulins. Wünschenswert sind
Insuline, die ein solch flaches und lang andauerndes Zeit-/Wirkungsprofil
haben, dass die Gefahr hypoglykämischer Ereignisse und
der tagesabhängigen Varianz im Patienten weiter minimiert
ist und die Wirkdauer weiter verzögert ist, so dass unter
Umständen nicht mehr täglich Insulin verabreicht
werden muss. Dies würde eine vereinfachte Behandlung von
Diabetikern ermöglichen, insbesondere von älteren
und pflegebedürftigen Diabetikern, die sich Insulin nicht
mehr selber injizieren können und wäre somit auch
von großem volkswirtschaftlichem Nutzen. In der frühen
Phase des Diabetes Typ 2 wären solche Basalinsuline zudem
nützlich. Kliniker berichten, dass die bei vielen Menschen
vorhandene Phobie vor Spritzen sie davor zurückschrecken lässt,
rechtzeitig mit der Insulintherapie zu beginnen. Als Konsequenz
ergibt sich eine schlechte Blutzuckereinstellung, die diabetische
Spätfolgen nach sich zieht. Ein Basalinsulin, das die Anzahl
der durch Spritzen erfolgten Insulingaben vermindert, könnte
bewirken, dass Patienten leichter die Insulintherapie annehmen.
-
Kohn
et al. (Peptides 28 (2007) 935–948) beschreiben,
dass man die Optimierung der Pharmakodynamik von Insulin dadurch
erreichen kann, dass man Insulinanaloga herstellt, deren isoelektrischer
Punkt (pI) durch Addition von Lysin oder Arginin an das B-Kettenende
oder den N-Terminus der A und B-Kette in Richtung des alkalischen
Bereichs verschoben ist, verglichen mit dem isoelektrischen Punkt
von Humaninsulin (pI = 5,6), so dass die Löslichkeit unter
physiologischen Bedingungen verringert ist und sich ein verlängertes Zeit-/Wirkungsprofil
ergibt. Verbindung 18 aus Kohn et al. (Arg(A0),Gly(A21),Arg(B31),Arg(B32)
Humaninsulin (pI experimentell bestimmt = 7,3; pI berechnet = 7,58)
wird dabei als beste Verbindung im Sinne des Konzeptes dargestellt.
Das hauptsächliche Ziel bei der Gestaltung neuer Insulinanaloga
sehen Kohn et al. daher in der Addition von positiv
geladenen Aminosäuren zur Aminosäuresequenz von
Humaninsulin zwecks Erhöhung des isoelektrischen Punktes
von pI = 5,6 in den neutralen Bereich.
-
Diesem
Ziel bei der Gestaltung neuer Insulinanaloga entgegengerichtet ist
die Substitution neutraler Aminosäuren in humanem Insulin
durch saure Aminosäuren und/oder die Addition von sauren
Aminosäuren, da solch eine Substitution und/oder Additionen
den Effekt der Einführung positiv geladener Aminosäuren
zumindest teilweise aufhebt. Es wurde nun aber überraschend
gefunden, dass solche Insulinanaloga zu dem beschriebenen wünschenswerten
basalen Zeit-/Wirkungsprofil führen, die durch die Merkmale
charakterisiert sind, dass
- • das B-Kettenende
aus einem amidierten basischen Aminosäurerest wie Lysin
bzw. Argininamid besteht, und
- • der N-terminale Aminosäurerest der Insulin
A-Kette ein Lysin- oder Argininrest ist, und
- • die Aminosäureposition A8 durch einen Histidinrest
besetzt wird, und
- • die Aminosäureposition A21 durch einen Glycinrest
besetzt wird, und
- • zwei Substitutionen neutraler Aminosäuren
durch saure Aminosäuren, zwei Additionen negativ geladener Aminosäurereste
oder je eine solche Substitution und eine solche Addition jeweils
in den Positionen A5, A15, A18, B-1, B0, B1, B2, B3 und B4 erfolgt
sind.
-
Während
die ersten drei genannten Merkmale durch Einführen positiver
Ladungen bzw. der Ausschaltung negativer Ladungen tendenziell Beiträge
zu einer Erhöhung des pI-Wertes eines entsprechenden Insulinanalogs
liefern, haben die letztgenannten Substitutionen und/oder Additionen
negativ geladener Aminosäurereste den gegenteiligen Effekt
und liefern Beiträge zu einer Erniedrigung des pI-Werts. Überraschenderweise haben
gerade die beschriebenen Insulinanaloga die gewünschten
vorteilhaften Zeit-/Wirkungsprofile. Die pI-Werte dieser Verbindungen
sind niedriger als die der Verbindung 18 aus Kohn et al. (Arg(A0),Gly(A21),Arg(B319,Arg(B32)-Humaninsulin),
weisen aber nichtsdestotrotz dabei einen verzögerten Wirkeintritt
und eine längere Wirkdauer, d. h. einen extrem flachen
und lang andauernden, gleichmäßigen Wirkungsverlauf
auf. Damit wird die Gefahr von hypoglykämischen Ereignissen
deutlich minimiert. Die Verzögerung ist so deutlich, dass
sich der Effekt überraschend sogar in Modellversuchen an
Ratten nachweisen lässt, obwohl im Gegensatz dazu die verzögerte
Wirkung von Insulin Glargin in der Ratte nicht eindeutig beobachtbar ist.
In 1 ist die hypoglykämische Wirkung der
erfindungsgemäßen Verbindung YKL205 verglichen
mit der von Insulin Glargin dargestellt. Ähnliche Ergebnisse
werden im Hund erhalten (siehe 2). Damit
sind neue Basalinsuline bereitgestellt worden, die deutlich weniger
häufig appliziert werden müssen. Neben diesen
beschriebenen pharmakokinetischen Vorteilen weisen die erfindungsgemäßen
Analoga gegenüber Insulin Glargin deutlich bessere Eigenschaften
in pharmakologischer Hinsicht wie z. B. Rezeptorspezifität
und in vitro Mitogenität auf. Ferner zeigen die beanspruchten
Insuline auch in physikalisch-chemischer Hinsicht Vorteile.
-
Gegenstand
der Erfindung ist somit ein Insulinanalogon der Formel I
wobei
A0
Lys oder Arg;
A5 Asp, Gln oder Glu;
A15 Asp, Glu oder
Gln;
A18 Asp, Glu oder Asn;
B-1 Asp, Glu oder eine Aminogruppe;
B0
Asp, Glu oder eine chemische Bindung;
B1 Asp, Glu oder Phe;
B2
Asp, Glu oder Val;
B3 Asp, Glu oder Asn;
B4 Asp, Glu oder
Gln;
B29 Lys oder einer chemischen Bindung;
B30 Thr oder
einer chemischen Bindung;
B31 Arg, Lys oder einer chemischen
Bindung;
B32 Arg-Amid, Lys-Amid oder einer Aminogruppe
entspricht,
wobei zwei Aminosäurereste der Gruppe enthaltend A5, A15,
A18, B-1, B0, B1, B2, B3 und B4 gleichzeitig und unabhängig
voneinander Asp oder Glu entsprechen.
-
Insbesondere
sind Gegenstände der Erfindung Insulinanaloga wie oben
ausgeführt, bei denen unabhängig voneinander A0
Arg entspricht, oder wobei A5 Glu entspricht, oder wobei A15 Glu
entspricht, oder wobei A18 Asp entspricht, oder wobei B-1 einer
Aminogruppe entspricht, oder wobei B0 Glu entspricht, oder wobei
B1 Asp entspricht, oder wobei B2 Val entspricht, oder wobei B3 Asp
entspricht, oder wobei B4 Glu entspricht, oder wobei B29 Lys entspricht,
oder wobei B30 Thr entspricht, oder wobei B31 Arg oder Lys entspricht.
-
Besonders
bevorzugter Gegenstand der Erfindung ist ein Insulinanalogon ausgewählt
aus einer Gruppe enthaltend:
Arg(A0),His(A8),Glu(A5),Asp(A18),Gly(A21),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Asp(A18),Gly(A21),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A15),Asp(A18),Gly(A21),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A15),Asp(A18),Gly(A21),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Glu(A15),Gly(A21),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Glu(A15),Gly(A21),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Gly(A21),Asp(B3),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Gly(A21),Asp(B3),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A15),Gly(A21),Asp(B3),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A15),Gly(A21),Asp(B3),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Asp(A18),Gly(A21),Asp(B3),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Asp(A18),Gly(A21),Asp(B3),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Gly(A21),Asp(B3),Glu(B4),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Gly(A21),Asp(B3),Glu(B4),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Gly(A21),Glu(B4),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Gly(A21),Glu(B4),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A15),Gly(A21),Glu(B4),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A15),Gly(A21),Glu(B4),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Asp(A18),Gly(A21),Glu(B4),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Asp(A18),Gly(A21),Glu(B4),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Gly(A21),Glu(B0),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Gly(A21),Glu(B0),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A15),Gly(A21),Glu(B0),Arg(B31),Arg
(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A15),Gly(A21),Glu(B0),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Asp(A18),Gly(A21),Glu(B0),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Asp(A18),Gly(A21),Glu(B0),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Gly(A21),Asp(B1),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A5),Gly(A21),Asp(B1),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A15),Gly(A21),Asp(B1),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Glu(A15),Gly(A21),Asp(B1),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Asp(A18),Gly(A21),Asp(B1),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Asp(A18),Gly(A21),Asp(B1),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Gly(A21),Glu(B0),Asp(B1),Arg(B31),Arg(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Gly(A21),Glu(B0),Asp(B1),Arg(B31),Lys(B32)-NH2 Humaninsulin,
Arg(A0),His(A8),Asp(A18),Gly(A21),Asp(B3),Arg(B30),Arg(B31)-NH2 Humaninsulin,
Arg(A0),His(A8),Asp(A18),Gly(A21),Asp(B3),Arg(B30),Lys(B31)-NH2 Humaninsulin.
-
Durch
die Angabe des Begriffs ”Humaninsulin” in den
Bezeichnungen der genannten Insulinanaloga wird Bezug auf die Aminosäuresequenzen
der A- und B-Kette von Humaninsulin genommen und alle Abweichungen
(Additionen, Substitutionen, Deletionen) davon sind in einer gegebenen
Bezeichnung eines Insulinanalogons angegeben.
-
Ein
weiterer Gegenstand der Erfindung ist ein Verfahren zur Herstellung
eines Insulinanalogons wie oben genannt, insbesondere wobei ein
Vorläufer des Insulinanalogs Humaninsulin rekombinant hergestellt wird,
der Vorläufer enzymatisch zu zwei-kettigem Insulin prozessiert
wird und eine Kupplung mit Argininamid in Gegenwart eines Enzyms
mit Trypsinaktivität durchgeführt wird, und das
Insulinanalogon isoliert wird.
-
Ein
weiterer Gegenstand der Erfindung ist eine Verwendung eines Insulinanalogons
wie oben beschrieben zur Herstellung eines Medikaments zur Behandlung
von Diabetes, insbesondere von Diabetes Typ I oder Typ II. Ebenfalls
ist Gegenstand der Erfindung eine Verwendung eines Insulinanalogons
wie oben beschrieben zur Herstellung eines Medikaments zur Unterstützung
der beta-Zellregeneration
-
Ein
weiterer Gegenstand der Erfindung ist ein Arzneimittel enthaltend
ein Insulinanalogon wie oben beschrieben.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung des Insulinanalogons
wie oben beschrieben, wobei die Formulierung in wässriger
Form enthaltend das gelöste Insulinanalog vorliegt.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung des Insulinanalogons
wie oben beschrieben, wobei die Formulierung in Form von Pulver
vorliegt.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung wie oben
beschrieben, wobei das Insulinanalogon wie oben beschrieben in kristalliner
und/oder amorpher Form vorhanden ist.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung des Insulinanalogons
wie oben beschrieben, wobei die Formulierung in Form einer Suspension
vorliegt.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung des Insulinanalogons
wie oben beschrieben, wobei die Formulierung zusätzlich
ein chemisches Chaperon enthält.
-
Ein
weiterer Gegenstand der Erfindung ist eine DNA kodierend für
einen Vorläufer eines Insulinanalogons wie oben beschrieben,
oder für die A-Kette oder B-Kette eines Insulinanalogons
wie oben beschrieben.
-
Ein
weiterer Gegenstand der Erfindung ist ein Vektor enthaltend eine
DNA wie oben beschrieben.
-
Ein
weiterer Gegenstand der Erfindung ist ein Wirtsorganismus enthaltend
eine DNA wie oben beschrieben oder einen Vektor wie oben beschrieben.
-
Ein
weiterer Gegenstand der Erfindung ist ein Präproinsulinanalogon,
dadurch gekennzeichnet, dass das C-Peptid an seinem N-Terminus den
Aminosäurerest Arginin und an seinem C-Terminus zwei Argininreste oder
einen Argininrest und einen Lysinrest trägt, wobei in letzterem
Falle der Lysinrest den eigentlichen C-Terminus bildet.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung wie oben
beschrieben, bei der noch zusätzlich ein Glucagon-Like
Peptide-1 (GLP1) oder ein Analogon oder Derivat davon, oder Exendin-3
bzw. -4 oder ein Analogon oder Derivat davon, vorzugsweise Exendin-4
enthalten ist.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung wie oben
beschrieben, bei dem ein Analogon von Exendin-4 ausgewählt
wird aus einer Gruppe enthaltend
H-desPro36-Exendin-4-Lys6-NH2,
H-des(Pro36,37)-Exendin-4-Lys4-NH2 und
H-des(Pro36,37)-Exendin-4-Lys5-NH2,
oder
ein pharmakologisch tolerierbares Salz davon.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung wie oben
beschrieben, bei dem ein Analogon von Exendin-4 ausgewählt
wird aus einer Gruppe enthaltend
desPro36[Asp28]Exendin-4(1-39),
desPro36[IsoAsp28]Exendin-4(1-39),
desPro36[Met(O)14,Asp28]Exendin-4(1-39),
desPro36[Met(O)14,IsoAsp28]Exendin-4(1-39),
desPro36[Trp(O2)25,Asp28]Exendin-2(1-39),
desPro36[Trp(O2)25,IsoAsp28]Exendin-2(1-39),
desPro36[Met(O)14Trp(O2)25,Asp28]Exendin-4(1-39)
und
desPro36[Met(O)14Trp(O2)25,IsoAsp28]Exendin-4(1-39),
oder ein pharmakologisch
tolerierbares Salz davon.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung wie im vorigen
Absatz beschrieben, bei denen an die C-Termini der Analoga von Exendin-4
das Peptid-Lys6-NH2 angefügt
ist.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung wie oben
beschrieben, bei dem ein Analogon von Exendin-4 ausgewählt
wird aus einer Gruppe enthaltend
H-(Lys)6-desPro36[Asp28]Exendin-4(1-39)-Lys6-NH2
desAsp28Pro36,Pro37,Pro38Exendin-4(1-39)-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Asp28]Exendin-4(1-39)-NH2,
H-Asn-(Glu)5desPro36,Pro37,Pro38[Asp28]Exendin-4(1-39)-NH2,
desPro36,Pro37,Pro38[Asp28]Exendin-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Asp28]Exendin-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Asp28]Exendin-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36[Trp(O2)25,Asp28]Exendin-4(1-39)-Lys6-NH2,
H-desAsp28Pro36,Pro37,Pro38[Trp(O2)25]Exendin-4(1-39)-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Trp(O2)25,Asp28]Exendin-4(1-39)-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Trp(O2)25,Asp28]Exendin-4(1-39)-NH2,
desPro36,Pro37,Pro38[Trp(O2)25,Asp28]Exendin-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Trp(O2)25,Asp28]Exendin-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-desPro36Pro37Pro38[Trp(O2)25,Asp28]Exendin-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36[Met(O)14,Asp28]Exendin-4(1-39)-Lys6-NH2,
desMet(O)14Asp28Pro36,Pro37,Pro38Exendin-4(1-39)-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Met(O)14,Asp28]Exendin-4(1-39)-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Met(O)14,Asp28]Exendin-4(1-39)-NH2,
desPro36,Pro37,Pro38[Met(O)14,Asp28]Exendin-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Met(O)14,Asp28]Exendin-4(1-39)-Lys6-NH2,
H-Asn-(Glu)5desPro36,Pro37,Pro38[Met(O)14,Asp28]Exendin-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36[Met(O)14,Trp(O2)25,Asp28]Exendin-4(1-39)-Lys6-NH2,
desAsp28Pro36,Pro37,Pro38[Met(O)14,Trp(O2)25]Exendin-4(1-39)-NH2,
H-(Lys)6-desPro36Pro37,Pro38[Met(O)14,Trp(O2)25,Asp28]Exendin-4(1-39)-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Met(O)14,Asp28]Exendin-4(1-39)-NH2,
desPro36,Pro37,Pro38[Met(O)14,Trp(O2)25,Asp28]Exendin-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Met(O)14,Trp(O2)25,Asp28]Exendin-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Met(O)14,Trp(O2)25,Asp28]Exendin-4(1-39)-(Lys)6-NH2,
oder
ein pharmakologisch tolerierbares Salz davon.
-
Ein
weiterer Gegenstand der Erfindung ist eine Formulierung wie oben
beschrieben, bei dem zusätzlich Arg34,Lys26(Nε(γ-glutamyl(Nα-hexadecanoyl)))GLP-1(7-37) [liraglutide]
oder ein pharmakologisch tolerierbares Salz davon enthalten ist.
-
Dem
Fachmann ist dabei klar, dass die erfindungsgemäßen
Insuline Gegenstand einer pharmazeutischen Formulierung sein können,
die nach Applikation vorteilhaft wirkt. Dabei geht man von wässrigen
Lösungen aus. Entsprechend müssen weitere Komponenten
mischbar sein. Die Gefahr viraler tierischer Kontamination wird
dadurch minimiert, dass die Zubereitung keine Komponenten enthalten
sollte, die aus tierischen Quellen stammen. Es ist weiterhin vorteilhaft,
durch Zusatz von Konservierungsmitteln eine mikrobielle Verunreinigung
zu verhindern. Durch den Zusatz isotoner Agentien kann eine mögliche
negative Auswirkung der Formulierung auf die Physiologie der Gewebezellen
an der Applikationsstelle kompensiert werden. Stabilisierend kann
sich der Zusatz von Protamin auswirken, so dass man weitgehend salzfreien
Insulinzubereitung gelangen kann, wenn man der Formulierung Protamin
zufügt. Der Zusatz von einer phenolischen Komponente kann zu
einer Stabilisierung der Struktur des verwendeten Insulinanalogons
führen und so unter anderem den Verzögerungseffekt
beim Wirkungseintritt zusätzlich bewirken. Der Formulierung
zugesetzt können auch Substanzen sein, die die Raumstruktur
der erfindungsgemäßen Verzögerungsinsuline
stabilisieren und zu besserer thermischen Stabilität führen.
Solche chemischen Chaperone können z. B. kurze synthetische
Peptide, die auch Aminosäureanaloga enthalten können
oder z. B. vom C-Peptid des Insulin abgeleitete Peptidsequenzen umfassen.
-
Zur
Entwicklung von Depotformen können die erfindungsgemäßen
Insuline in Nanopartikel eingebunden werden. Denkbar sind auch sogenannte „Slow
release” Formuierungen, bei denen das erfindungsgemäße Verzögerungsinsulin
reversibel an polymere Träger gebunden vorliegt.
-
Die
erfindungsgemäßen Insuline können parallel
zu schnellwirksamen Insulinen wie Apidra
®,
NovoRapid
®, Humalog
® oder
sich in Entwicklung befindlichen Insulinderivaten oder Formulierungen
mit entsprechendem Zeit-/Aktionsprofil oder inhalierbarem Insulin
oder nasal oder oral applizierten Insulinen, die sich in Entwicklung
befinden, verabreicht werden. Dabei ist es dem Fachmann klar, dass
dazu auch entsprechend formulierte Mischungen aus schnellwirksamen
und erfindungsgemäßem Verzögerungsinsulin
verwendet werden können. Weiterhin können die
erfindungsgemäßen Insuinanaloga in pharmazeutischen
Zubereitungen verwendet werden, die Peptide, die durch eine dem
GLP-1 (Glucagon like Peptide-1) oder dem Exendin-4 bzw. Exendin-3
vergleichbare Aktivität beschrieben sind, enthalten. Beispiel
für solche Peptide stellen GLP-1(7-37), Exenatide (Byetta
®) oder Peptide, deren Herstellung
in den Patentanmeldungen
WO
2006/058620 ,
WO 2001/04156 ,
WO 2004/005342 und
WO 98/08871 beschrieben
sind, dar. Besonders vorteilhaft sind dabei Formulierungen, die
eine Depotformulierung dieser Peptide enthalten. Vorteilhaft besonders
in der Anfangsphase der Typ II Diabetes Erkrankung sind Therapieformen,
die parallel zu Verabreichung der erfindungsgemäßen Pharmazeutika
vorsehen, die die Insulinwirkung erhöhen, wie z. B. Metformin.
Kombinationstherapien mit Dipeptidyl Peptidase-4 Inhibitoren, die
den Spiegel an Inkretinen erhöhen, sind wie Kombinationen
mit Sulfonylharnstoffen, die die Insulinausschüttung im
Pankreas erhöhen, ebenfalls möglich. Besonders
vorteilhaft können die erfindungsgemäßen
Verzögerungsinsuline dann eingesetzt werden, wenn durch
Applikation von Differenzierungsfaktoren, die Regeneration von pankreatischen
Betazellen aus entsprechenden Stammzellen eingeleitet wird. All
diese Anwendungen sind beispielhaft für die Therapie des
Diabetes genannt und ebenfalls Gegenstand der Erfindung. Ein weiterer
Gegenstand der Erfindung ist somit die Verwendung der erfindungsgemäßen
Insuline in Kombination mit anderen Wirkstoffen zur Behandlung von
Diabetes, insbesondere Diabetes Typ I oder Typ II Diabetes.
-
Ein
weiterer Gegenstand der Erfindung ist ein Arzneimittel, das ein
erfindungsgemäßes Insulinanalogon enthält,
welches insbesondere eine wässrige Formulierung oder ein
Pulver darstellt.
-
Das
Arzneimittel ist eine pharmazeutische Zubereitung, die vorzugsweise
eine Lösung oder Suspension zu Injektionszwecken ist; sie
ist gekennzeichnet durch einen Gehalt an mindestens einem erfindungsgemäßen
Insulinanalog, und/oder mindestens einem von deren physiologisch
verträglichen Salzen in gelöster, amorpher und/oder
kristalliner – vorzugsweise in gelöster – Form.
-
Die
Zubereitung weist vorzugsweise einen pH-Wert zwischen etwa 2,5 und
8,5, insbesondere zwischen etwa 4,0 und 8,5 auf, enthält
vorzugsweise ein geeignetes Isotonisierungsmittel, ein geeignetes
Konservierungsmittel und gegebenenfalls einen geeigneten Puffer,
sowie vorzugsweise auch eine bestimmte Zinkionen-Konzentration,
in steriler wässriger Lösung. Die Gesamtheit der
Zubereitungsbestandteile außer dem Wirkstoff bildet den
Zubereitungs-Träger. Geeignete Isotonisierungsmittel sind
z. B. Glycerin, Glukose, Mannit, NaCl, Calcium- oder Magnesium-Verbindungen
wie CaCl2 etc. Durch die Wahl des Isotonisierungsmittels und/oder
Konservierungsstoffes beeinflusst man die Löslichkeit der
erfindungsgemäßen Insuline bzw. deren physiologisch
verträgliche Salze bei schwach sauren pH-Werten.
-
Geeignete
Konservierungsmittel sind z. B. Phenol, m-Cresol, Benzylalkohol
und/oder p-Hydroxybenzoesäureester.
-
Als
Puffersubstanzen, insbesondere zur Einstellung eines pH-Wertes zwischen
etwa 4,0 und 8,5 können z. B. Natriumacetat, Natriumcitrat,
Natriumphosphat etc. verwendet werden. Ansonsten sind zur Einstellung
des pH-Wertes auch physiologisch unbedenkliche verdünnte
Säuren (typischerweise HCl) bzw. Laugen (typischerweise
NaOH) geeignet.
-
Wenn
die Zubereitung einen Zinkgehalt besitzt, ist ein solcher von 1 μg/ml
bis 2 mg/ml, insbesondere von 5 μg bis 200 μg
Zink/ml bevorzugt.
-
Zwecks
Variation des Wirkstoffprofils der erfindungsgemäßen
Zubereitung kann auch unmodifiziertes Insulin, vorzugsweise Rinder-,
Schweine- oder Human-Insulin, insbesondere Humaninsulin, oder Insulinanaloga
und Derivate davon zugemischt werden. Ebenfalls können
ein oder mehrere Exendin-4 Derivate oder Peptide, die durch eine
dem GLP-1 (Glucagon like peptide-1) vergleichbare Aktivität
charakterisiert sind, zugemischt werden. Solche Arzneimittel (Zubereitungen)
sind ebenfalls Gegenstand der Erfindung.
-
Bevorzugte
Wirkstoffkonzentrationen sind solche entsprechend etwa 1–1500,
weiter bevorzugt etwa 5–1000 und insbesondere etwa 40–400
internationale Einheiten/ml.
-
Die
erfindungsgemäßen Insulinanaloga werden zunächst
als Vorstufe, die noch nicht das Amid umfasst, biotechnologisch
hergestellt. Dem Fachmann ist geläufig, das es eine Vielzahl
von Möglichkeiten zur Herstellung von Insulinen gibt. Als
Wirtszellsysteme finden dabei Bakterien, Hefen und Pflanzen bzw.
fermentativ zu kultivierende Pflanzenzellen Verwendung. Falls die
Kostenbetrachtung es erlaubt sind auch Expressionssysteme, die tierische
Zellen als Wirtssystem nutzen, denkbar. Voraussetzung dafür
ist aber eine sichere Freiheit von tierischen Viren. Somit ist klar,
dass die beispielhaft beschriebenen Expressionssysteme nur einen kleinen
Ausschnitt der für die rekombinante Herstellung von Proteinen
entwickelten Wirts/Vektorsysteme darstellen. In der Anmeldung werden
z. B. biotechnologische Verfahren, die Hefe- oder Pflanzensysteme
wie Moose, Algen oder höhere Pflanzen wie Tabak, Erbse,
Distel, Gerste, Mais oder Raps zur Grundlage haben nicht beschrieben.
Dennoch sind Wirts/Vektor Systeme sowie kodierende DNA-Sequenzen,
die die Herstellung der Zielpeptide in entsprechenden biotechnologischen
Expressionssystemen erlauben, ebenfalls Bestandteil der Erfindung.
Wirtsorganismen können also insbesondere ausgewählt
werden aus dem Pflanzenreich aus Organismen der ersten Abteilung
Schizophyta enthaltend Schizomcetes, Bakterien oder Blaualgen, Organismen
der 2. Abteilung Phycophyta V. Klasse Chlorophyceae, Organismen
der 2. Abteilung Phycophyta VII. Klasse Rhodophyceae, Organismen
der 3. Abteilung Mycophyta, Organismen der 5. Abteilung Bryophyta und
Organismen der 7. Abteilung Spermatophyta.
-
In
der Europäischen Patentanmeldung
EP-A 1 222 207 ist ein Plasmid
pINT358d beschrieben, das für ein Prä-Proinsulin
codiert, welches ein verändertes C-Peptid umfasst. Mit
Hilfe der Polymerase Kettenreaktion (PCR) ist es nun möglich,
gezielt die das Proinsulin kodierende Sequenz so zu verändern,
dass Prä-Proinsuline exprimiert werden können,
die als Vorstufen für die erfindungsgemäßen
Insulin dienen können. Entsprechende Fusionsproteine müssen
nicht notwendigerweise intrazellulär hergestellt werden.
Es ist dem Fachmann klar, dass solche Proteine auch durch bakterielle
Expression mit anschließender Sekretion in das Periplasma
und/oder in den Kulturüberstand hergestellt werden können.
Die Europäische Patentanmeldung
EP-A 1 364 029 beschreibt
dies beispielhaft. Die Proinsulinvorstufen, die zu den erfindungsgemäßen
Analoga führen, sind ebenfalls Gegenstand der Erfindung.
-
Die
so hergestellten Proinsuline können prinzipiell zu einer
Insulinanalogavorstufe umgewandelt werden, die in Position A0 Lysin
oder Arginin umfasst und am C-terminalen Ende der B-Kette Lysin
oder Arginin trägt.
-
Liegen
die erfindungsgemäßen Proinsuline nach intrazellulärer
Expression in Bakterien als Einschlusskörper oder löslich
vor, müssen diese Vorstufen durch in vitro Faltung in die
richtige Konformation gefaltet werden, bevor die Prozessierung und
biochemische Modifikation vorgenommen werden kann. Dabei erlaubt
das beschriebene Fusionsprotein eine direkte Faltung nach Denaturierung
mittels Harnstoff oder Guanidinium Hydrochlorid, Faltungsintermediate
sind dabei ebenfalls Gegenstand der Erfindung.
-
Zur
Anreicherung der einzelnen Zwischenstufen finden biochemische Methoden
insbesondere Trennverfahren Verwendung, deren zugrunde liegenden
Prinzipien publiziert und sogar Gegenstand von Lehrbüchern
sind. Dem Fachmann ist klar, dass solche Prinzipien in Folge kombiniert
werden können und so zu Verfahren führen können,
die in ihre Abfolge vorher nicht publiziert wurden. Verfahren, die
zur Reinigung der erfindungsgemäßen Analoga führen
sind somit ebenfalls Gegenstand der Erfindung.
-
Ein
weiterer Gegenstand der Erfindung ist ein Verfahren zur Herstellung
der erfindungsgemäßen Insulinanaloga, wobei ein
Vorläufer des Insulinanalogons rekombinant hergestellt
und enzymatisch zu einer 2-kettigen Insulinvorstufe umgewandelt
wird, die N-terminal zu Aminosäure 1 der A-Kette Arginin
bzw. Lysin trägt und am C-terminalen Ende der B-Kette einen
Lysin oder Argininrest aufweist, der mit Argininamid oder Lysinamid
in Gegenwart eines Enzyms mit Trypsinaktivität in das Amid
und somit in das erfindungsgemäße Verzögerungsinsulin überführt
und über ein biochemischer Reinigungsverfahren hochrein
dargestellt wird.
-
Proteine,
welche sich durch Substitution wenigstens eines natürlich
auftretenden Aminosäurerestes mit anderen Aminosäureresten
und/oder Addition und/oder Entfernen wenigstens eines Aminosäurerestes
von dem entsprechenden, ansonsten gleichen natürlich vorkommenden
Protein unterscheiden, werden als „Analoga” von
Proteinen bezeichnet. Dabei kann es sich bei den hinzugefügten
und/oder ersetzten Aminosäureresten auch um solche handeln,
die nicht natürlich vorkommen.
-
Proteine,
welche durch chemische Modifizierung bestimmter Aminosäurereste
von Ausgangsproteinen erhalten werden, bezeichnet man als „Derivate” von
Proteinen. Die chemische Modifikation kann z. B. in der Addition
einer oder mehrerer bestimmter chemischer Gruppen an eine oder mehrere
Aminosäuren bestehen.
-
Figurenlegende:
-
1:
Blutzuckersenkende Wirkung von neuen Insulinanaloga in Ratten
-
2:
Blutzuckersenkende Wirkung von neuen Insulinanaloga im Hund
-
3:
Blutzuckersenkende Wirkung von YKL205 im Hund
-
Die
folgenden Beispiele sollen den Erfindungsgedanken illustrieren,
ohne dabei beschränkend zu wirken.
-
Beispiel 1: Herstellung des Vektorderivates
pINT3580, das für Gly(A21)-Insulin und ein modifiziertes
C-Peptid, das an der C/A-Kettengrenze Arg Arg trägt, kodiert.
-
Die
Europäische Patentanmeldung
EP-A 1 222 207 beschreibt die Plasmide pINT358d,
pINT91d und die Primer-Sequenz Tir. DNA dieser Produkte findet Verwendung
in der Konstruktion des Plasmides pINT3580. Das Plasmid pINT358d
ist dabei durch eine Gensequenz charakterisiert, die für
ein modifiziertes C-Peptid mit besonderen Eigenschaften kodiert.
Drei Primersequenzen werden synthetisiert:
-
Dieser
Primer dient nach Aufarbeitung dazu in Position 21 der A-Kette der
von pINT358d kodierten Proinsulinsequenz Glycin (fett gedruckt,
unterstrichen) anstelle von Asparagin einzuführen.
-
-
Dieser
Primer dient, wie der Primer arg_cjunc_rev, zur Einführung
von Arginin anstelle von Lysin an der Insulin A-/B-Kettengrenze.
-
-
-
Das
Codon für das einzuführende Arginin ist in beiden
Primern fett gedruckt. Mit DNA des Plasmides pINT358d als Matrize
wird mit den Primerpaaren Tir/arg_cjunc_rev und arg_cjuncf/pint3580_glya21rev
entsprechend der Europäischen Patentanmeldung
EP-A 1 222 207 je eine PCR
durchgeführt. Aliquots der Produkte beider Reaktionen werden
kombiniert und zusammen mit dem Primerpaar Tir/pint3580_glya21rev
in einer dritten PCR eingesetzt. Das Produkt dieser Reaktion wird
nach gelektrophoretischer Auftrennung des Reaktionsgemisches gereinigt
und mit den Restriktionsenzymen Sal1/Nco1 nach Angaben des Herstellers
in ein und derselben Reaktion verdaut, das Reaktionsgemisch gelelektrophoretisch
aufgetrennt und das die Proinsulinsequenz kodierende DNA-Fragment
isoliert. Das Fragment wird anschließend über
eine DNA-Ligasereaktion in die Nco1/Sal1 geöffnete pINT91d
Vektor DNA insertiert.
-
Mit
dem Ligationsgemisch werden kompetente E. coli Bakterienzellen transformiert.
Das Transformationsgemisch wird auf Selektionsplatten, die 25 mg/l
Ampicillin enthalten, ausplattiert. Plasmid DNA wird von Kolonien
isoliert und mittels DNA-Sequenzanalyse charakterisiert. Richtige
Plasmide erhalten die Bezeichnung pINT3580.
-
Beispiel 2: Konstruktion des Plasmides
pINT3581 kodierend für His(A8),Gly(A21)-Präproinsulin
-
Die
Konstruktion erfolgt wie in Beispiel 1 beschrieben über
3 Polymerase Kettenreaktionen. Das Produkt der dritten Reaktion
wird nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete
pINT91d Vektor DNA insertiert. Verwendet werden die Primer Tir und
pint3580_glya21rev. Zwei weitere Primer werden synthetisiert:
-
Das
Codon, das für Histidin in Position 8 der A-Kette kodiert
ist jeweils fett herausgestellt. Die Konstruktion wird wie ins Beispiel
1 beschrieben durchgeführt. Template für PCR1
und 2 ist DNA des Plasmides pINT3580. PCR1 wird mit dem Primerpaar
Tir/pint3580_Ha8rev und PCR2 mit dem Primerpaar pint3580_Ha8f/pint3580_glya21rev
durchgeführt. In PCR3 wird mit dem Primer paar Tir/pint3580_glya21rev eingesetzt.
Template ist dabei ein Gemisch der Reaktionsprodukte von PCR1 und
PCR2. Richtige Plasmide erhalten die Bezeichnung pINT3581.
-
Beispiel 3: Konstruktion des Plasmides
pINT3582 kodierend für His(A8),Glu(A5),Gly(A21)-Präproinsulin
-
Die
Konstruktion erfolgt wie in Beispiel 1 und 2 beschrieben über
3 Polymerase Kettenreaktionen. Das Produkt der dritten Reaktion
wird nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete
pINT91d Vektor DNA insertiert. Verwendet werden die Primer Tir und
pint3580_glya21rev. Zwei weitere Primer werden synthetisiert:
-
Das
Codon, das für Glutaminsäure in Position 5 der
A-Kette kodiert, ist jeweils fett herausgestellt. Die Konstruktion
wird wie ins Beispiel 1 beschrieben durchgeführt.
-
Template
ist DNA des Plasmides pINT3581. Richtige Plasmide erhalten die Bezeichnung
pINT3582.
-
Beispiel 4: Konstruktion des Plasmides
pINT3583 kodierend für His(A8),Asp(A18),Gly(A21)-Präproinsulin
-
Die
Konstruktion erfolgt abweichend von Beispiel 1 über nur
eine Polymerase Kettenreaktionen. Das Produkt dieser Reaktion wird
nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete pINT91d
Vektor DNA insertiert. Verwendet wird der Primer Tir. Ein weiterer
Primer wird synthetisiert:
-
Das
Codon, das für Asparaginsäure in Position 18 der
A-Kette kodiert, ist fett herausgestellt. Template ist DNA des Plasmides
pINT3581. Richtige Plasmide erhalten die Bezeichnung pINT3583.
-
Beispiel 5: Konstruktion des Plasmides
pINT3584 kodierend für His(A8),Glu(A5)Asp(A18),Gly(A21)-Präproinsulin
-
Die
Konstruktion erfolgt abweichend von Beispiel 1 über nur
eine Polymerase Kettenreaktionen. Das Produkt dieser Reaktion wird
nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete pINT91d
Vektor DNA insertiert. Verwendet wird der Primer Tir. pint3580_Da18rev
(Bsp. 4). Template ist DNA des Plasmides pINT3582. Richtige Plasmide
erhalten die Bezeichnung pINT3584. Das von dem Plasmid kodierte
Prä-Proinsulin ist Vorstufe für die Verbindung
YKL205-1, die nach Amidierung mit Argininamid entsteht und die folgende
Struktur beschreibt:
Arg(A0),Glu(A5),His(A8),Asp(A18),Gly(A21),Arg(B31),Arg(B32)-NH2-Humaminsulin
-
Entsprechende
Amidierung mit Lysinamid führt zur Verbindung YKL205-1b:
Arg(A0),Glu(A5),His(A8),Asp(A18),Gly(A21),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 6: Konstruktion des Plasmides
pINT3585 kodierend für His(A8),Glu(A15),Gly(A21)-Präproinsulin
-
Die
Konstruktion erfolgt abweichend von Beispiel 1 über nur
eine Polymerase Kettenreaktionen. Das Produkt dieser Reaktion wird
nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete pINT91d
Vektor DNA insertiert. Verwendet wird der Primer Tir. Ein weiterer
Primer wird synthetisiert:
-
Das
Codon, das für Glutaminsäure in Position 15 der
A-Kette kodiert, ist fett herausgestellt. Template ist DNA des Plasmides
pINT3581. Richtige Plasmide erhalten die Bezeichnung pINT3585.
-
Beispiel 7: Konstruktion des Plasmides
pINT3586 kodierend für His(A8),Glu(A15),Asp(A18),Gly(A21)-Präproinsulin
-
Die
Konstruktion erfolgt abweichend von Beispiel 1 über nur
eine Polymerase Kettenreaktionen. Das Produkt dieser Reaktion wird
nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete pINT91d
Vektor DNA insertiert. Verwendet wird der Primer Tir. Ein weiterer
Primer wird synthetisiert:
-
Das
Codon, für Glutaminsäure in Position 15 der A-Kette
und Asparaginsäure in Position A18 der A-Kette ist jeweils
fett herausgestellt. Template ist DNA des Plasmides pINT3581. Richtige
Plasmide erhalten die Bezeichnung pINT3586. Das von dem Plasmid
kodierte Prä-Proinsulin ist Vorstufe für die Verbindung YKL205,
die nach Amidierung mit Argininamid entsteht und die folgende Struktur
beschreibt:
Arg(A0),His(A8),Glu(A15),Asp(A18),Gly(A21),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Asp(A18),Gly(A21),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 8: Konstruktion des Plasmides
pINT3587 kodierend für Glu(A5),His(A8),Glu(A15),Gly(A21)-Präproinsulin
-
Die
Konstruktion erfolgt abweichend von Beispiel 1 über nur
eine Polymerase Kettenreaktionen. Das Produkt dieser Reaktion wird
nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete pINT91d
Vektor DNA insertiert. Verwendet wird der Primer Tir und pint3580_Ea15rev
gemäß Beispiel 6. Template ist DNA des Plasmides pINT3582.
Richtige Plasmide erhalten die Bezeichnung pINT3587. Das von dem
Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-2, die nach Amidierung mit Argininamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),Glu(A5),His(A8),Glu(A15),Gly(A21),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-2b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),Glu(A5),His(A8),Glu(A15),Gly(A21),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 9: Konstruktion des Plasmides
pINT3588 kodierend für His(A8),Gly(A21),Asp(B3)-Präproinsulin
-
Die
Konstruktion erfolgt wie in Beispiel 1 und 2 beschrieben über
3 Polymerase Kettenreaktionen. Das Produkt der dritten Reaktion
wird nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete
pINT91d Vektor DNA insertiert. Verwendet werden die Primer Tir und
pint3580_glya21rev. Zwei weitere Primer werden synthetisiert:
-
Das
Codon, das für Asparaginsäure in Position 3 der
insulin B-Kette kodiert ist jeweils fett herausgestellt. Die Konstruktion
wird wie ins Beispiel 1 beschrieben durchgeführt. Template
ist DNA des Plasmides pINT3581. Richtige Plasmide erhalten die Bezeichnung
pINT3588.
-
Beispiel 10: Konstruktion des Plasmides
pINT3589 kodierend für Glu(A5),His(A8),Gly(A21),Asp(B3)-Präproinsulin
-
Führt
man die Reaktionen wie in Beispiel 9 beschrieben durch, verwendet
aber in PCR1 und PCR2 DNA des Plasmides pINT3582 als Template, so
gelangt man zu Plasmid pINT3589.
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-3, die nach Amidierung mit Argininamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),Glu(A5),His(A8),Gly(A21),Asp(B3),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-3b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),Glu(A5),His(A8),Gly(A21),Asp(B3),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 11: Konstruktion des Plasmides
pINT3590 kodierend für His(A8),Glu(A15),Gly(A21),Asp(B3)-Präproinsulin
-
Führt
man die Reaktionen wie in Beispiel 9 beschrieben durch, verwendet
aber in PCR1 und PCR2 DNA des Plasmides pINT3585 als Template, so
gelangt man zu Plasmid pINT3590. Das von dem Plasmid kodierte Prä-Proinsulin
ist Vorstufe für die Verbindung YKL205-4, die nach Amidierung
mit Argininamid entsteht und die folgende Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Gly(A21),Asp(B3),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-4b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Gly(A21),Asp(B3),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 12: Konstruktion des Plasmides
pINT3591 kodierend für His(A8),Asp(A18),Gly(A21),Asp(B3)-Präproinsulin
-
Führt
man die Reaktionen wie in Beispiel 9 beschrieben durch, verwendet
aber in PCR1 und PCR2 DNA des Plasmides pINT3586 als Template, so
gelangt man zu Plasmid pINT3591. Das von dem Plasmid kodierte Prä-Proinsulin
ist Vorstufe für die Verbindung YKL205-5, die nach Amidierung
mit Argininamid entsteht und folgende Struktur beschreibt:
Arg(A0),His(A8),Asp(A18),Gly(A21),Asp(B3),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-5b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg (A0),His(A8),Asp(A18),Gly(A21),Asp(B3),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 13: Konstruktion des Plasmides
pINT3592 kodierend für His(A8),Gly(A21),Asp(B3)-Glu(B4)-Präproinsulin
-
Die
Konstruktion erfolgt wie in Beispiel 1 und 2 beschrieben über
3 Polymerase Kettenreaktionen. Das Produkt der dritten Reaktion
wird nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete
pINT91d Vektor DNA insertiert. Verwendet werden die Primer Tir und
pint3580_glya21rev. Zwei weitere Primer werden synthetisiert:
-
Das
Codon, das für Asparaginsäure in Position 3 und
Glutaminsäure in Position 4 der Insulin B-Kette kodiert,
ist jeweils fett herausgestellt Die Konstruktion wird wie in Beispiel
1 beschrieben durchgeführt. Template ist DNA des Plasmides
pINT3581. Richtige Plasmide erhalten die Bezeichnung pINT3592. Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-6, die nach Amidierung mit Argininamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Gly(A21),Asp(B3),Glu(B4),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-6b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Gly(A21),Asp(B3),Glu(B4),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 14: Konstruktion des Plasmides
pINT3593 kodierend für His(A8),Gly(A21),Glu(B4)-Präproinsulin
-
Die
Konstruktion erfolgt wie in Beispiel 1 und 2 beschrieben über
3 Polymerase Kettenreaktionen. Das Produkt der dritten Reaktion
wird nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete
pINT91d Vektor DNA insertiert. Verwendet werden die Primer Tir und
pint3580_glya21rev. Zwei weitere Primer werden synthetisiert:
-
Das
Codon, das für Glutaminsäure in Position 4 der
Insulin B Kette kodiert, ist fett herausgestellt. Die Konstruktion
wird wie ins Beispiel 1 beschrieben durchgeführt. Template
ist DNA des Plasmides pINT3581. Richtige Plasmide erhalten die Bezeichnung
pINT3593.
-
Beispiel 15: Konstruktion des Plasmides
pINT3594 kodierend für Glu(A5),His(A8),Gly(A21),Glu(B4)-Präproinsulin.
-
Führt
man die Reaktionen wie in Beispiel 9 beschrieben durch, verwendet
aber in PCR1 und PCR2 DNA des Plasmides pINT3582 als Template, so
gelangt man zu Plasmid pINT3594.
-
Das
Proinsulin ist Vorstufe für die Verbindung YKL205-7, die
nach Amidierung mit Argininamid entsteht und die folgende Struktur
beschreibt:
Arg(A0),Glu(A5),His(A8),Gly(A21),Glu(B4),Arg(B31),Arg(B32)-NH2-Humaninsulin.
-
Das
Proinsulin ist Vorstufe für die Verbindung YKL205-7b, die
nach Amidierung mit Lysinamid entsteht und die folgende Struktur
beschreibt:
Arg(A0),Glu(A5),His(A8),Gly(A21),Glu(B4),Arg B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 16: Konstruktion des Plasmides
pINT3595 kodierend für His(A8),Glu(A15),Gly(A21),Glu(B4)-Präproinsulin.
-
Führt
man die Reaktionen wie in Beispiel 9 beschrieben durch, verwendet
aber in PCR1 und PCR2. DNA des Plasmides pINT3585 als Template,
so gelangt man zu Plasmid pINT3595. Das von dem Plasmid kodierte
Prä-Proinsulin ist Vorstufe für die Verbindung
YKL205-8, die nach Amidierung mit Argininamid entsteht und die folgende
Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Gly(A21),Glu(B4),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-8b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Gly(A21),Glu(B4),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 17: Konstruktion des Plasmides
pINT3596 kodierend für His(A8),Asp(A18),Gly(A21),Glu(B4)-Präproinsulin
-
Führt
man die Reaktionen wie in Beispiel 9 beschrieben durch, verwendet
aber in PCR1 und PCR2 DNA des Plasmides pINT3586 als Template, so
gelangt man zu Plasmid pINT3596. Das von dem Plasmid kodierte Prä-Proinsulin
ist Vorstufe für die Verbindung YKL205-9, die nach Amidierung
mit Argininamid entsteht und die folgende Struktur beschreibt:
Arg(A0),His(A8),Asp(A18),Gly(A21),Glu(B4),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-9b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Asp(A18),Gly(A21),Glu(B4),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 18: Konstruktion des Plasmides
pINT3597 kodierend für His(A8),Gly(A21),Glu(B0)-Präproinsulin
-
Die
Konstruktion erfolgt über 2 Polymerase Kettenreaktionen.
Verwendet wird der Primer pint3580_glya21rev. Zwei weitere Primer
werden synthetisiert:
-
Dabei überlappen
sich die beiden Primer partial. Pint3581_Eb0f2 enthält
eine NcoI-Erkennungssequenz. Diese ist unterstrichen dargestellt.
Das Codon, das für Glutaminsäure in Position 0
am Anfang B-Kette kodiert, ist jeweils fett herausgestellt. Template
für PCR1 ist DNA des Plasmides pINT3581.
-
PCR1
wird mit dem Primerpaar pint3581_Eb-1f2/pint3580_glya21rev. Template
für PCR2 ist das Produkt aus PCR1. PCR2 wird mit dem Primerpaar
pint3581_Eb-1f2/pint3580_glya21rev durchgeführt. Das Produkt
aus PCR2 übereckt die vollständige Präproinsulinsequenz.
Das Produkt der zweiten Reaktion wird nach Nco1/Sal1 Spaltung in
die Nco1/Sal1 geöffnete pINT91d Vektor DNA insertiert.
Richtige Plasmide erhalten die Bezeichnung pINT3597. Ersetzt man
das Codon für Glutaminsäure in Position B0 durch
das Codon von Asparaginsäure und folgt dem Beispiel, so
gelangt man zu Plasmiden, die in Position B0 anstelle von Glutaminsäure Asparaginsäure
tragen.
-
Beispiel 19: Konstruktion des Plasmides
pINT3598 kodierend für Glu(A5),His(A8),Gly(A21),Glu(B0)-Präproinsulin
-
Führt
man die Reaktionen wie in Beispiel 18 beschrieben durch, verwendet
aber in PCR1 DNA des Plasmides pINT3582 als Template, so gelangt
man zu Plasmid pINT3598. Das von dem Plasmid kodierte Prä-Proinsulin
ist Vorstufe für die Verbindung YKL205-10, die nach Amidierung
mit Argininamid entsteht und die folgende Struktur beschreibt:
Arg(A0),Glu(A5),His(A8),Gly(A21),Glu(B0),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-10b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),Glu(A5),His(A8),Gly(A21),Glu(B0),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 20: Konstruktion des Plasmides
pINT3599 kodierend für His(A8),Glu(A15),Gly(A21),Glu(B0)-Präproinsulin
-
Führt
man die Reaktionen wie in Beispiel 18 beschrieben durch, verwendet
aber in PCR1 DNA des Plasmides pINT3585 als Template, so gelangt
man zu Plasmid pINT3599. Das von dem Plasmid kodierte Prä-Proinsulin
ist Vorstufe für die Verbindung YKL205-11, die nach Amidierung
mit Argininamid entsteht und die folgende Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Gly(A21),Glu(B0),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-11b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Gly(A21),Glu(B0),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 21: Konstruktion des Plasmides
pINT3600 kodierend für His(A8),Asp(A18),Gly(A21),Glu(B0)-Präproinsulin
-
Führt
man die Reaktionen wie in Beispiel 18 beschrieben durch, verwendet
aber in PCR1 DNA des Plasmides pINT3586 als Template, so gelangt
man zu Plasmid pINT3600. Das von dem Plasmid kodierte Prä-Proinsulin
ist Vorstufe für die Verbindung YKL205-12, die nach Amidierung
mit Argininamid entsteht und die folgende Struktur beschreibt:
Arg(A0),His(A8),Asp(A18),Gly(A21),Glu(B0),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-12b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Asp(A18),Gly(A21),Glu(B0),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 22: Konstruktion des Plasmides
pINT3601 kodierend für His(A8),Gly(A21),Asp(B1)-Präproinsulin
-
Die
Konstruktion erfolgt über 2 Polymerase Kettenreaktionen.
Verwendet wird der Primer pint3580_glya21rev. Zwei weitere Primer
werden synthetisiert:
-
Dabei überlappen
sich die beiden Primer partial. Pint3581_Db-1f2 enthält
eine NcoI-Erkennungssequenz. Diese ist unterstrichen dargestellt.
Das Codon, das für Asparaginsäure in Position
1 der B-Kette kodiert, ist jeweils fett herausgestellt. Template
für PCR1 ist DNA des Plasmides pINT3581. PCR1 wird mit
dem Primerpaar pint3581_Db1f1/pint3580_glya21rev durchgeführt.
Template für PCR2 ist das Produkt aus PCR1. PCR2 wird mit
dem Primerpaar pint3581_Db1f2/pint3580_glya21rev durchgeführt.
Das Produkt aus PCR2 überdeckt die vollständige
Präproinsulinsequenz. Das Produkt der zweiten Reaktion
wird nach Nco1/Sal1 Spaltung in die Nco1/Sal1 geöffnete
pINT91d Vektor DNA insertiert. Richtige Plasmide erhalten die Bezeichnung
pINT3601.
-
Beispiel 23: Konstruktion des Plasmides
pINT3602 kodierend für Glu(A5),His(A8),Gly(A21),Asp(B1)-Präproinsulin
-
Führt
man die Reaktionen wie in Beispiel 22 beschrieben durch, verwendet
aber in PCR1 DNA des Plasmides pINT3582 als Template, so gelangt
man zu Plasmid pINT3602. Das von dem Plasmid kodierte Prä-Proinsulin
ist Vorstufe für die Verbindung YKL205-13, die nach Amidierung
mit Argininamid entsteht und die folgende Struktur beschreibt:
Arg(A0),Glu(A5),His(A8),Gly(A21),Asp(B1),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-13b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),Glu(A5),His(A8),Gly(A21),Asp(B1),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 24: Konstruktion des Plasmides
pINT3603 kodierend für His(A8),Glu(A15),Gly(A21),Asp(B1)-Präproinsulin
-
Führt
man die Reaktionen wie in Beispiel 22 beschrieben durch, verwendet
aber in PCR1 DNA des Plasmides pINT3585 als Template, so gelangt
man zu Plasmid PINT3603. Das von dem Plasmid kodierte Prä-Proinsulin
ist Vorstufe für die Verbindung YKL205-14, die nach Amidierung
mit Argininamid entsteht und die folgende Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Gly(A21),Asp(B1),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-14b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Gly(A21),Asp(B1),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 25: Konstruktion des Plasmides
pINT3604 kodierend für His(A8),Asp(A18),Gly(A21),Asp(B1)-Präproinsulin
-
Führt
man die Reaktionen wie in Beispiel 22 beschrieben durch, verwendet
aber in PCR1 DNA des Plasmides pINT3586 als Template, so gelangt
man zu Plasmid pINT3604. Das von dem Plasmid kodierte Prä-Proinsulin
ist Vorstufe für die Verbindung YKL205-15, die nach Amidierung
mit Argininamid entsteht und die folgende Struktur beschreibt:
Arg(A0),His(A8),Asp(A18),Gly(A21),Asp(B1),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-15b, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Asp(A18),Gly(A21),Asp(B1),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 26: Konstruktion des Plasmides
pINT3605 kodierend für His(A8),Gly(A21),Glu(B0),Asp(B1)-Präproinsulin
-
Die
Konstruktion erfolgt über 2 Polymerase Kettenreaktionen.
Verwendet wird der Primer pint3580_glya21rev und der in Beispiel
18 beschrieben Primer pint3581_Eb01f2. Synthetisiert wird der Primer pint3597_Db1f:
-
Das
Codon, das für Glutaminsäure in Position 0 und
das für Asparaginsäure jeweils am Anfang der B-Kette
kodiert, ist jeweils fett herausgestellt. Template für
PCR1 ist DNA des Plasmides pINT3597. PCR1 wird mit dem Primerpaar
pint3597_Db1f/pint3580_glya21rev. Template für PCR2 ist
das Produkt aus PCR1. PCR2 wird mit dem Primerpaar pint3581_Eb1f2/pint3580_glya21rev
durchgeführt. Das Produkt aus PCR2 überdeckt die
vollständige Präproinsulinsequenz. Das Produkt
der zweiten Reaktion wird nach Nco1/Sal1 Spaltung in die Nco1/Sal1
geöffnete pINT91d Vektor DNA insertiert. Richtige Plasmide
erhalten die Bezeichnung pINT3605. Das von dem Plasmid kodierte
Prä-Proinsulin ist Vorstufe für die Verbindung
YKL205-16, die nach Amidierung mit Argininamid entsteht und die
folgende Struktur beschreibt:
Arg(A0),His(A8),Gly(A21),Glu(B0),Asp(B1),Arg(B31),Arg(B32)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-16a, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Gly(A21),Glu(B0),Asp(B1),Arg(B31),Lys(B32)-NH2-Humaninsulin
-
Beispiel 27: Konstruktion des Plasmides
pINT3606 kodierend für His(A8),Glu(A15),Asp(A18),Gly(A21),desThr(B30)-Präproinsulin
-
Die
Konstruktion erfolgt wie in Beispiel 1 und 2 beschrieben über
3 Polymerase Kettenreaktionen. Verwendet werden die Primer Tir und
pint3580_glya21rev. Zwei weitere Primer werden synthetisiert:
-
Template
für PCR1 und PCR2 ist DNA des Plasmides pINT3586. PCR1
wird mit dem Primerpaar desB30f/pint3580_glya21rev und PCR2 wird
mit dem Primerpaar Tir/desB30rev Template durchgeführt.
Als Template für PCR3 wird ein äquimolares Gemisch
der Produkte aus PCR1 und PCR2 verwendet. Die Reaktion wird mit
dem Primerpaar Tir/pint3580_glya21rev durchgeführt. Das
Produkt aus PCR3 überdeckt die vollständige Präproinsulinsequenz.
Das Produkt der dritten Reaktion wird nach Nco1/Sal1 Spaltung in
die Nco1/Sal1 geöffnete pINT91d Vektor DNA insertiert.
Das von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe
für die Verbindung YKL205-17, die nach Amidierung mit Argininamid
entsteht und die folgende Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Asp(A18),Gly(A21),Arg(B30),Arg(B31)-NH2-Humaninsulin
-
Das
von dem Plasmid kodierte Prä-Proinsulin ist Vorstufe für
die Verbindung YKL205-18, die nach Amidierung mit Lysinamid entsteht
und die folgende Struktur beschreibt:
Arg(A0),His(A8),Glu(A15),Asp(A18),Gly(A21),Arg(B30),Lys(B31)-NH2-Humaninsulin
-
Beispiel 28: Expression der Proinsulinderivate
-
Die
Expression wird entsprechend Beispiel 1 der Europäischen
Patentanmeldung
EP-A
1 222 207 durchgeführt.
-
Beispiel 29: Faltung der Proinsulinderivate
-
Die
Faltung erfolgt prinzipiell nach der in
EP-A 0 668 282 beschriebenen
Methode
-
Beispiel 30: Enzymatische Prozessierung
der gefalteten Präproinsulin zu der 2-kettigen Arg(A0)-Insulinvorstufe,
deren C-terminales B-Kettenende durch Lysin oder Arginin charakterisiert
ist.
-
Die
Enzymatische Prozessierung der gefalteten Präproinsulinvorstufe
erfolgt wie z. B. in Beispiel 4 von
WO91/03550 beschrieben.
Als besonders vorteilhaft erweist sich dabei der Einsatz der in
WO 2007/031187 A1 beschriebenen
Trypsinvariante.
-
Beispiel 31: Herstellung eines Arg(A0),His(A8),Gly(A21),Arg(B31),Arg(B32)-NH2-Humaninsulins
-
Unabhängig
von der Positionierung der zusätzlichen sauren Aminosäuren
wird eine Standardreaktion wie folgt durchgeführt: 100
mg Arg(A0),Gly(A21),Arg(B31)-Insulinanalog werden in 0.95 ml Argininamidlösung (446
g/L) gelöst, 0.13 mL M Na-Acetatpuffer (pH 5.8) und 2 ml
DMF zugegeben. Die Reaktionsmischung wird auf 12°C gekühlt
und durch Zugabe von 0.094 ml Trypsin (0.075 mg, Roche Diagnostics)
gestartet. Nach 8 h wird die Reaktion durch Zugabe von TFA bis pH
2.5 gestoppt und per HPLC analysiert. Es bildet sich > 60%. Arg(A0),Gly(A21),Arg(B31),Arg(B32)-NH
2-Humaninsulin. Nach Zusatz von Trypsininhibitorlösung
erfolgt die Reinigung des amidierten Analogs in Analogie zu
US 5,656,722 .
-
Die
Herstellung der entsprechenden Lysinamid-Verbindung erfolgt analog.
Allerdings geht man von einer wässrigen Lysinamid Stammlösung
aus, die 366 g/L Lysinamid gelöst enthält.
-
Beispiel 32: Formulierung der amidierten
Indulinderivate
-
Um
die erfindungsgemäßen Insulinderivate auf ihre
biologisch, pharmakologischen und physikalisch chemischen Eigenschaften
zu testen, wurde von den Verbindungen wie folgt eine Lösung
hergestellt: Das erfindungsgemäße Insulinderivat
wurde mit einer Zielkonzentration von 240 ± 5 μM
in 1 mM Salzsäure mit 80 μg/mL Zink (als Zinkchlorid)
aufgelöst. Hierzu wurde von dem gefriergetrockneten Material
zunächst eine um etwa 30% höhere Menge als aufgrund
des Molekulargewichts und der angestrebten Konzentration benötigt eingewogen.
Danach wurde die vorliegende Konzentration mittels analytischer
HPLC bestimmt und die Lösung anschließend auf
das zur Erreichung der Zielkonzentration erforderliche Volumen 5
mM Salzsäure mit 80 μg/mL Zink aufgefüllt.
Falls erforderlich, wurde dabei der pH-Wert auf 3,5 ± 0,1
nachjustiert. Nach der endgültigen Analyse durch HPLC zur
Absicherung der Zielkonzentration von 240 ± 5 μM
wurde die fertige Lösung mittels einer Spritze mit einem
0,2 μm Filtervorsatz in ein mit einem Septum und einer
Bördelkappe verschlossenes steriles Fläschchen überführt.
Für die kurzfristige, einmalige Testung der erfindungsgemäßen
Insulinderivate wurde keine Optimierung der Formulierungen, z. B.
hinsichtlich eines Zusatzes isotonischer Agentien, Konservierungsmittel
oder Puffersubstanzen, vorgenommen.
-
Beispiel 33: Evaluierung der blutzuckersenkenden
Wirkung von neuen Insulinanaloga in der Ratte
-
Die
blutzuckersenkende Wirkung von ausgewählten neuen Insulinanaloga
wird in männlichen, gesunden, normoglykämischen
Wistarratten geprüft. Männlichen Ratten wird eine
Dosis von 9 nmol/kg eines Insulinanalogons subkutan injiziert. Unmittelbar
vor der Injektion des Insulinanalogons und in regelmäßigen
Abständen bis zu acht Stunden nach der Injektion werden
den Tieren Blutproben entnommen und darin der Blutzuckergehalt bestimmt.
Das Experiment zeigt deutlich (vgl. 1), dass
das eingesetzte erfindungsgemäße Insulinanalogon
zu einem deutlich verzögerten Wirkeintritt und einer längeren,
gleichmäßigen Wirkdauer führt.
-
Beispiel 34: Evaluierung der blutzuckersenkenden
Wirkung von neuen Insulinanaloga im Hund
-
Die
blutzuckersenkende Wirkung von ausgewählten neuen Insulinanaloga
wird in männlichen, gesunden, normoglykämischen
Beaglehunden geprüft. Männlichen Tieren wird eine
Dosis von 6 nmol/kg eines Insulinanalogons subkutan injiziert. Unmittelbar
vor der Injektion des Insulinanalogons und in regelmäßigen
Abständen bis zu achtundvierzig Stunden nach der Injektion
werden den Tieren Blutproben entnommen und darin der Blutzuckergehalt
bestimmt. Das Experiment zeigt deutlich (vgl. 2),
dass das eingesetzte erfindungsgemäße Insulinanalogon
zu einem deutlich verzögerten Wirkeintritt und einer längeren,
gleichmäßigen Wirkdauer führt.
-
Beispiel 35: Evaluierung der blutzuckersenkenden
Wirkung am Hund bei zweifach erhöhter Dosis
-
Die
blutzuckersenkende Wirkung von ausgewählten neuen Insulinanaloga
wird in männlichen, gesunden, normoglykämischen
Beaglehunden geprüft. Männlichen Tieren wird eine
Dosis von 6 nmol/kg und 12 nmol/kg eines Insulinanalogons subkutan
injiziert. Unmittelbar vor der Injektion des Insulinanalogons und
in regelmäßigen Abständen bis zu achtundvierzig
Stunden nach der Injektion werden den Tieren Blutproben entnommen
und darin der Blutzuckergehalt bestimmt. Das Experiment zeigt deutlich
(vgl. 3), dass das eingesetzte erfindungsgemäße
Insulinanalogon dosisabhängig wirkt, dass aber trotz zweifach
erhöhter Dosis der Wirkungsverlauf flach verläuft,
d. h. kein ausgeprägter Tiefpunkt (Nadir) beobachtet wird.
Daraus lässt sich ableiten, dass die erfindungsgemäßen
Insuline im Vergleich zu bekannten Verzögerungsinsulinen
zu deutlich weniger hypoglykämischen Ereignissen führen.
-
Es folgt ein
Sequenzprotokoll nach WIPO St. 25.
Dieses kann von der
amtlichen Veröffentlichungsplattform des DPMA heruntergeladen
werden.
-
ZITATE ENTHALTEN IN DER BESCHREIBUNG
-
Diese Liste
der vom Anmelder aufgeführten Dokumente wurde automatisiert
erzeugt und ist ausschließlich zur besseren Information
des Lesers aufgenommen. Die Liste ist nicht Bestandteil der deutschen
Patent- bzw. Gebrauchsmusteranmeldung. Das DPMA übernimmt
keinerlei Haftung für etwaige Fehler oder Auslassungen.
-
Zitierte Patentliteratur
-
- - WO 2006/058620 [0032]
- - WO 2001/04156 [0032]
- - WO 2004/005342 [0032]
- - WO 98/08871 [0032]
- - EP 1222207 A [0042, 0053, 0056, 0118]
- - EP 1364029 A [0042]
- - EP 0668282 A [0119]
- - WO 91/03550 [0120]
- - WO 2007/031187 A1 [0120]
- - US 5656722 [0121]
-
Zitierte Nicht-Patentliteratur
-
- - Kohn et al.
(Peptides 28 (2007) 935–948) [0005]
- - Kohn et al. [0005]
- - Kohn et al. [0005]
- - Kohn et al. [0007]